Замещенные имидазолы и их применение в качестве пестицидов
Номер патента: 15738
Опубликовано: 31.10.2011
Авторы: Довернь Жером Себастьян, Эвин Ричард Эндрю, Чабб Натан Энтони Логан, Лоре Кристель, Кокс Марк Роджер
Формула / Реферат
1. Соединение формулы (I)
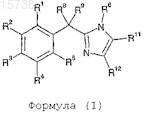
где R1, R2, R3, R4, R5независимо выбраны из группы, включающей водород, циано, галоген, C1-4алкил, С3-4 циклоалкил, C1-4алкокси, C1-4галогеналкил, C1-4галогеналкокси и SR10;
R6 выбран из группы, включающей водород, -C0-2алкилен-R7, -С1-2алкилен-OR7, -С1-2алкилен-OC(O)R7, -С1-2 алкилен-OC(O)OR7, -C0-2алкилен-C(O)OR7, -С1-2алкилен-OC(O)NHR7, -С1-2алкилен-OC(O)NR15R16 и -C0-2 алкилен-SR10;
где каждый R7, R15 и R16, если это химически возможно, независимо выбран из группы, включающей водород, C1-6алкил и C1-4алкилен(С3-6циклоалкил);
R8 обозначает C1-4алкил;
R9, R11 и R12, каждый, обозначают водород;
R10 обозначает C1-4алкил или C1-4галогеналкил,
или его фармацевтически приемлемая соль.
2. Соединение по п.1, где R1 и R2обозначают метил, a R3, R4 и R5обозначают водород.
3. Соединение по п.1 или 2, где R6 выбран из группы, состоящей из водорода, -C0-2алкилен-R7и -С1-2 алкилен-OC(O)R7.
4. Соединение по п.3, где R6 выбран из группы, включающей водород, 2,2-диметилпропионилоксиметил, пропионилоксиметил, 3-циклопентилпропионилоксиметил, 3-метилбутирилоксиметил, гептаноилоксиметил, бутирилоксиметил, пентаноилоксиметил, циклопропилметил, метил, этил, изобутоксикарбонил и изопропоксикарбонил.
5. Соединение по любому из пп.1-4, где R8 обозначает метил.
6. Соединение по п.1, выбранное из группы, включающей
2-[1-(2,3-диметилфенил)этил]-1Н-имидазол;
2-[(1S)-1-(2,3-диметилфенил)этил]-1Н-имидазол;
2-[(1R)-1-(2,3-диметилфенил)этил]-1Н-имидазол;
{2-[1-(2,3-диметилфенил)этил]-1Н-имидазол-1-ил}метилпивалат;
{2-[1-(2,3-диметилфенил)этил]-1Н-имидазол-1-ил}метилпропионат;
{2-[1-(2,3-диметилфенил)этил]-1Н-имидазол-1-ил}метил-3-метилбутаноат;
{2-[1-(2,3-диметилфенил)этил]-1Н-имидазол-1-ил}метилбутират;
{2-[1-(2,3-диметилфенил)этил]-1Н-имидазол-1-ил}метил-3-циклопентилпропаноат;
{2-[1-(2,3-диметилфенил)этил]-1Н-имидазол-1-ил}метилгептаноат;
{2-[1-(2,3-диметилфенил)этил]-1Н-имидазол-1-ил}метилпентаноат;
2-{1-[2-(трифторметил)фенил]этил}-1Н-имидазол;
2-[1-(2,5-диметилфенил)этил]-1Н-имидазол;
2-[1-(4-хлор-3-метилфенил)этил]-1Н-имидазол;
2-[1-(3,5-диметилфенил)этил]-1Н-имидазол;
1-(циклопропилметил)-2-[1-(2,3-диметилфенил)этил]-1Н-имидазол;
2-[1-(2,3-диметилфенил)этил]-1-метил-1Н-имидазол;
циклопропилметил-{2-[1-(2,3-диметилфенил)этил]-1Н-имидазол-1-ил}метилкарбонат;
{2-[1-(2,3-диметилфенил)этил]-1Н-имидазол-1-ил}метил-3-метилбутилкарбонат;
{2-[1-(2,3-диметилфенил)этил]-1Н-имидазол-1-ил}метилизопропилкарбонат;
2-[1-(2,3-диметилфенил)этил]-1-этил-1Н-имидазол;
2-[1-(2,3-диметилфенил)этил]-1-(метоксиметил)-1Н-имидазол;
изобутил-2-[1-(2,3-диметилфенил)этил]-1Н-имидазол-1-карбоксилат;
изопропил-2-[1-(2,3-диметилфенил)этил]-1Н-имидазол-1-карбоксилат и
2-[1-(3-метилфенил)этил]-1Н-имидазол,
или его фармацевтически приемлемая соль.
7. Фармацевтическая композиция, содержащая соединение формулы (I) по любому из пп.1-6 или его фармацевтически приемлемую соль, а также подходящий эксципиент или носитель.
8. Ветеринарная композиция, содержащая соединение формулы (I) по любому из пп.1-6 или его ветеринарно приемлемую соль, а также подходящий эксципиент или носитель.
9. Сельскохозяйственная композиция, содержащая соединение формулы (I) по любому из пп.1-6 или его сельскохозяйственно приемлемую соль, а также подходящий эксципиент или носитель.
10. Применение соединения формулы (I) по любому из пп.1-6 или его фармацевтически приемлемой соли в производстве противопаразитного средства для лечения человека.
11. Применение соединения формулы (I) по любому из пп.1-6 или его ветеринарно приемлемой соли в производстве противопаразитного средства для лечения животного.
12. Применение соединения формулы (I) по любому из пп.1-6 или его сельскохозяйственно приемлемой соли в производстве противопаразитного средства для обработки сельскохозяйственных культур и насекомых и борьбы с насекомыми.
13. Фармацевтическая комбинация соединения формулы (I) по любому из пп.1-6 и по меньшей мере одного другого биологически активного соединения, выбранного из инсектицидов, акарицидов, противоглистных средств, фунгицидов, нематоцидов, противопротозойных средств или бактерицидных средств.
14. Ветеринарная комбинация соединения формулы (I) по любому из пп.1-6 и по меньшей мере одного другого биологически активного соединения, выбранного из инсектицидов, акарицидов, противоглистных средств, фунгицидов, нематоцидов, противопротозойных средств или бактерицидных средств.
15. Сельскохозяйственная комбинация соединения формулы (I) по любому из пп.1-6 и по меньшей мере одного другого биологически активного соединения, выбранного из инсектицидов, акарицидов, противоглистных средств, фунгицидов, нематоцидов, противопротозойных средств, бактерицидных средств, регуляторов роста, энтомопатогенных бактерий, вирусов или грибков.
16. Способ лечения паразитарной инфекции у животного-хозяина, включающий обработку животного-хозяина эффективным количеством соединения формулы (I) по любому из пп.1-6.
17. Способ по п.16, где животное-хозяин представляет собой млекопитающее, птицу или рыбу, а паразит представляет собой насекомое или акариду.
18. Способ по п.16, где животное-хозяин представляет собой насекомое, а паразит представляет собой акариду.
19. Способ борьбы с заражением насекомыми или акаридами на участке поражения, включающий нанесение эффективного количества соединения формулы (I) по любому из пп.1-6 на указанный участок.
20. Способ по п.19, где участок поражения отличается от животного-хозяина.
Текст
Дата публикации и выдачи патента Номер заявки Изобретение относится к ряду альфа-замещенных 2-бензилзамещенных имидазольных соединений формулы (I) Чабб Натан Энтони Логан, Кокс Марк Роджер, Довернь Жером Себастьян,Эвин Ричард Эндрю, Лоре Кристель где переменные R1-R6, R8, R9 и R11 и R12 имеют значения, определенные в формуле изобретения, и их фармацевтически приемлемым солям, к композициям, содержащим такие соединения, способам их синтеза и их применению в качестве противопаразитных средств. 015738 Данное изобретение относится к имидазолам, обладающим противопаразитными свойствами. Представляющими интерес соединениями являются замещенные имидазолы, более конкретно данное изобретение относится к альфа-замещенным 2-бензилимидазолам. Существует потребность в более эффективных противопаразитных средствах для млекопитающих,включая людей и животных, в частности существует потребность в более эффективных инсектицидах и акарицидах. Кроме того, существует потребность в более эффективных продуктах для местного применения с удобным способом введения, содержащих одно или несколько таких противопаразитных средств, которые можно использовать для эффективной обработки эктопаразитов, таких как насекомые и акариды, такие как клещи и зудни. Такие продукты, в частности, можно использовать для лечения животных-компаньонов, таких как кошки, собаки и лошади, а также домашнего скота, например крупного рогатого скота. В равной степени существует потребность в средствах для борьбы с заражением паразитами животных-хозяев, отличных от млекопитающих, например насекомых, таких как пчелы, которые являются чувствительными к таким паразитам, как клещи варроа. Доступные в настоящее время соединения для инсектицидной и акарицидной обработки животныхкомпаньонов и домашнего скота не всегда обладают достаточной активностью и достаточными скоростью или длительностью действия. Большая часть лекарственных средств содержит вредные химические вещества, которые могут вызывать серьезные осложнения при слишком частом применении либо при применении в количестве, превышающем рекомендуемую дозу. Многие продукты оказывают токсичное побочное действие и являются летальными для кошек при случайном проглатывании. Они не всегда подходят для применения в виде композиций для местного или точечного нанесения, а традиционные побочные эффекты некоторых композиций для местного или точечного нанесения причиняют вред животным и их хозяевам. Людям, применяющим данные инсектицидные и акарицидные средства, советуют надевать перчатки и избегать вдыхания паров химических веществ, чтобы ограничить воздействие данных средств. Для преодоления некоторых проблем используют ошейники и этикетки для животных, однако они могут причинить вред, если животное в результате жевания ошейника или этикетки случайно проглотит соединение. Таким образом, существующие в настоящее время способы лечения имеют разные степени эффективности в зависимости от ряда факторов, включающих токсичность и способ введения. В некоторых случаях токсичность может быть связана с неселективной активностью по отношению к разным рецепторам. Кроме того, недавно было показано, что существующие в настоящее время средства становятся неэффективными при развитии у паразитов устойчивости. Настоящее изобретение направлено на преодоление одного или нескольких недостатков существующих соединений или на улучшение свойств существующих соединений. В частности, настоящее изобретение предлагает несколько новых альфа-замещенных 2-бензилимидазолов, которые обладают улучшенными свойствами. В предшествующем уровне техники, например в международной публикации патентной заявкиWO 03/092374, были раскрыты гетероциклические соединения, обладающие инсектицидной и акарицидной активностью в отношении сельскохозяйственных вредителей. В предшествующем уровне также раскрыты общие описания гетероциклических соединений, которые необязательно охватывают альфа-замещенные 2-бензилимидазолы. Например, международная публикация патентной заявки WO 2005/007188 описывает соединения общей структуры, которая необязательно охватывает альфа-замещенные 2-бензилимидазолы, для ингибирования развития яиц эктопаразитов; международная публикация патентной заявки WO 2004/103959 раскрывает соединения общей структуры, необязательно охватывающей альфа-замещенные 2-бензилимидазолы, для применения в качестве противобактериальных средств; международные публикации патентных заявок WO 01/00586 иWO 99/28300 описывают соединения общей структуры, необязательно охватывающей альфазамещенные 2-бензилимидазолы, и раскрывают их адренергическую активность; патент США 6103733 описывает соединения общей структуры, необязательно охватывающей альфа-замещенные 2-бензилимидазолы, способные повышать уровни HDL холестерина в сыворотке; как WO 2001/094318,так и FR 2681322 раскрывают аналоги бензилимидазола. Однако ни в одной из ранее опубликованных работ не приводятся примеры альфа-замещенных 2-бензилимидазолов, а также не указывается, что такие соединения можно использовать против ряда паразитов, поражающих животных-компаньонов и домашний скот, или для подавления стадий жизненного цикла ряда эктопаразитов. Таким образом, целью настоящего изобретения является преодоление одного или нескольких недостатков известных соединений или улучшение свойств известных соединений. В частности, целью настоящего изобретения является разработка некоторых новых альфа-замещенных 2-бензилзамещенных имидазолов. Другой целью является сохранение или повышение активности таких новых соединений по сравнению с противопаразитными соединениями предшествующего уровня техники. Следующей целью настоящего изобретения является разработка соединений, которые обладают аналогичным или пониженным профилем токсичности по сравнению с соединениями предшествующего уровня техники. Очередной целью является разработка соединений, которые обладают селективностью в отношении октопаминергического рецептора, известного нейромедиатора беспозвоночных, по сравнению с повсеместно распространенным адренергическим рецептором животных. Кроме того, целью данного изобретения явля-1 015738 ется уменьшение воздействия на людей и животных разрабатываемых соединений, которые можно вводить в виде форм для точечного или местного применения в небольшом объеме. Как показывают результаты анализа активности и эффективности, соединения настоящего изобретения в особенности подходят для борьбы с членистоногими. В частности, соединения настоящего изобретения обладают активностью против клещей и предотвращают их прикрепление к животному-хозяину с последующим питанием. Следующей целью настоящего изобретения является разработка соединений, обладающих высокой скоростью действия по сравнению с соединениями предшествующего уровня техники и, следовательно, повышенной эффективностью против передачи заболеваний, переносимых клещами. Кроме того, желательно, чтобы одна или несколько из таких характеристик соединений настоящего изобретения, как длительность действия, фармакокинетический профиль, безопасность, устойчивость,растворимость или другие физико-химические и композиционные свойства, такие как распространение после местного нанесения, оставались такими же, как у соединений предыдущего уровня техники, или превосходили их. Таким образом, настоящее изобретение предлагает соединение формулы (I) где R1, R2, R3, R4, R5 независимо выбраны из группы, включающей водород, циано, галоген, C1-4 алкил,С 3-4 циклоалкил, C1-4 алкокси, C1-4 галогеналкил, C1-4 галогеналкокси и SR10;R6 выбран из группы, включающей водород, -C0-2 алкилен-R7, -С 1-2 алкилен-OR7, -С 1-2 алкиленOC(O)R7, -С 1-2 алкилен-OC(O)OR7, -С 0-2 алкилен-С(О)OR7, -С 1-2 алкилен-OC(O)NHR7, -С 1-2 алкиленOC(O)NR15R16 и -C0-2 алкилен-SR10; где каждый R7, R15 и R16, если это химически возможно, независимо выбран из группы, включающей водород, C1-6 алкил и C1-4 алкилен(С 3-6 циклоалкил);R10 обозначает C1-4 алкил или C1-4 галогеналкил,или его фармацевтически приемлемую соль. В определении R1, R2, R3, R4 и R5 фраза "C1-4 алкил" относится к алкильной группе, содержащей от одного до четырех атомов углерода. В определении R1, R2, R3, R4 и R5 фраза "С 3-6 циклоалкил" относится к циклоалкильной группе, содержащей от трех до шести атомов углерода в цикле. Предпочтительно каждый из R1, R2, R3, R4 и R5 независимо выбран из водорода, галогена, такого как хлор или фтор, C1-4 алкила, такого как метил или этил, С 3-4 циклоалкила, такого как циклопропил,C1-4 алкокси, такого как метокси или этокси, C1-4 галогеналкила, такого как трифторметил или трифторэтил, C1-4 галогеналкокси, такого как трифторметокси или трифторэтокси, и SR10, a R10 выбран изC1-4 алкила, такого как метил или этил, или C1-4 галогеналкила, такого как трифторметил или трифторэтил,с образованием, например, трифторметилтио или трифторэтилтио. Более предпочтительно каждый из R1,R2, R3, R4 и R5 независимо выбран из водорода, галогена, такого как хлор, C1-4 алкила, такого как метил или этил, C1-4 алкокси, такого как метокси или этокси, и C1-4 галогеналкила, такого как трифторметил,трифторэтил. Наиболее предпочтительно каждый из R1, R2, R3, R4 и R5 независимо выбран из водорода иC1-4 алкила, такого как метил или этил. Наиболее предпочтительно два из R1, R2, R3, R4 и R5 независимо выбраны из C1-4 алкила, такого как метил или этил, предпочтительно метил, а три из R1, R2, R3, R4 и R5 обозначают Н. Еще более предпочтительно R1 и R2 выбраны из C1-4 алкила, такого как метил или этил, предпочтительно метил, a R3, R4 и R5 обозначают Н. Другие подходящие соединения представляют собой соединения, в которых по меньшей мере один из R1, R2, R3, R4 и R5 независимо выбран из C1-4 галогеналкила, такого как трифторметил или трифторэтил, предпочтительно трифторметил, а другие R1, R2, R3, R4 и R5 обозначают Н. Предпочтительно R2 обозначает C1-4 галогеналкил, такой как трифторметил или трифторэтил, предпочтительно трифторэтил, a R1, R3, R4 и R5 обозначают Н. Другие подходящие соединения представляют собой соединения, в которых по меньшей мере один из R1, R2, R3, R4 и R5 независимо выбран из C1-4 алкокси, такого как метокси или этокси, предпочтительно метокси, а другие R1, R2, R3, R4 и R5 обозначают Н. Предпочтительно R2 и R3 выбраны из C1-4 алкокси,такого как метокси или этокси, предпочтительно метокси, a R1, R4 и R5 обозначают Н.-2 015738 Другие подходящие соединения представляют собой соединения, в которых по меньшей мере один из R1, R2, R3, R4 и R5 независимо выбран из галогена, такого как хлор или фтор, а другие R1, R2, R3, R4 иR5 обозначают Н. Другие подходящие соединения представляют собой соединения, в которых по меньшей мере один из R1, R2, R3, R4 и R5 независимо выбран из галогена, такого как хлор или фтор, другие R1, R2, R3, R4 и R5 независимо выбраны из C1-4 алкила, такого как метил или этил, а остальные R1, R2, R3, R4 и R5 обозначают Н. Наиболее предпочтительными являются соединения, в которых R1 и R2 обозначают метил, a R3, R4 5 и R обозначают водород. Предпочтительно R6 выбран из группы, состоящей из водорода, -C0-2 алкилен-R7 и -С 1-2 алкиленОС(О)R7. Наиболее предпочтительными являются соединения, в которых R6 выбран из группы, включающей водород, 2,2-диметилпропионилоксиметил, пропионилоксиметил, 3-циклопентилпропионилоксиметил,3-метилбутирилоксиметил, гептаноилоксиметил, бутирилоксиметил, пентаноилоксиметил, циклопропилметил, метил, этил, изобутоксикарбонил и изопропоксикарбонил. Предпочтительно R7, R15 и R16, если это химически возможно, независимо выбраны из группы,включающей водород; C1-6 алкил, такой как метил, этил, н-пропил, изопропил, бутил, изобутил, третбутил, н-пентил, н-гексил; C1-4 алкилен(С 3-6 циклоалкил), например циклопропилметил, циклопропилэтил,циклобутилметил, циклобутилэтил, циклопентилметил, циклопентилэтил, циклогексилметил, циклогексилэтил. Более предпочтительно R7, R15 и R16, если это химически возможно, независимо выбраны из группы, включающей водород и C1-4 алкил, такой как метил, этил, пропил, изопропил, н-бутил и трет-бутил. Подходящие соединения представляют собой соединения, в которых R6 выбран из группы, включающей -С 0-2 алкилен-R7, предпочтительно в которых R6 обозначает CH2R7, где R7 выбран из группы,включающей C1-6 алкил, такой как метил, этил, н-пропил, изопропил, бутил, трет-бутил. Другая группа подходящих соединений охватывает соединения, в которых R6 выбран из группы,включающей -С 1-2 алкилен-OR7, предпочтительно где R6 обозначает CH2OR7 и где R7 выбран из группы,включающей C1-6 алкил, такой как метил, этил, н-пропил, изопропил, бутил, трет-бутил. Примеры таких замещенных групп R6 включают метоксиметил, этоксиметил, метоксиэтил, этоксиэтил, пропоксиметил,пропоксиэтил, изопропоксиэтил, бутоксиметил, втор-бутоксиоксиметил, изобутоксиметил, третбутоксиметил, бутоксиэтил, втор-бутоксиоксиэтил, изобутоксиэтил, трет-бутоксиэтил, пентилоксиметил,пентилоксиэтил, гексилоксиметил, гексилоксиэтил. Следующая группа подходящих соединений охватывает соединения, в которых R6 выбран из группы, включающей -C1-2 алкилен-OC(O)R7, предпочтительно где R6 обозначает CH2OC(O)R7 и где R7 обозначает С 1-6 алкил, такой как метил, этил, н-пропил, изопропил, бутил, трет-бутил. Примеры таких замещенных групп R6 включают ацетилоксиметил, ацетилоксиэтил, пропионилоксиметил, пропионилоксиэтил, бутирилоксиметил, бутирилоксиэтил, изобутирилоксиметил, изобутирилоксиэтил, пентаноилоксиметил, пентаноилоксиэтил, 2-метилбутирилоксиметил, 2-метилбутирилоксиэтил, 3-метилбутирилоксиметил, 3-метилбутирилкарбонилоксиэтил, 2,2-диметилпропионилоксиметил, 2,2-диметилпропионилоксиэтил гексаноилоксиметил, гексаноилоксиэтил, гептаноилоксиметил, гептаноилоксиэтил. Другие подходящие примеры соединений, в которых R6 выбран из группы, включающей-С 1-2 алкилен-OC(O)R7, предпочтительно где R6 обозначает CH2OC(O)R7, также включают соединения, в которых R7 обозначает С 1-4 алкилен(С 3-6 циклоалкил), такой как циклопропилметил, циклопропилэтил,циклобутилметил, циклобутилэтил, циклопентилметил, циклопентилэтил, циклопентилпропил, циклогексилметил и циклогексилэтил. Примеры таких замещенных групп R6 включают циклопропилацетилоксиметил, циклопропилпропионилоксиметил, циклобутилацетилоксиметил, циклобутилпропионилоксиметил, циклопентилацетилоксиметил, циклопентилпропионилоксиметил, циклопентилбутирилоксиметил, циклогексилацетилоксиметил, циклогексилпропионилоксиметил, циклопропилацетилоксиэтил, циклопропилпропионилоксиэтил, циклобутилацетилоксиэтил, циклобутилпропионилоксиэтил, циклопентилацетилоксиэтил, циклопентилпропионилоксиэтил, циклопентилбутирилоксиэтил, циклогексилацетилоксиэтил и циклогексилпропионилоксиэтил. Предпочтительно R6 обозначает 3-циклопентилпропионилоксиметил. В таких соединениях R7 предпочтительно обозначает C1-6 алкил, более предпочтительно этил или трет-бутил и наиболее предпочтительно трет-бутил. Следующая группа подходящих соединений охватывает соединения, в которых R6 выбран из группы, включающей -C1-2 алкилен-OC(O)OR7, предпочтительно где R6 обозначает СН 2 ОС(О)OR7 и где R7 обозначает C1-6 алкил, такой как метил, этил, н-пропил, изопропил, бутил, трет-бутил. Примеры таких замещенных групп R6 включают метоксикарбонилоксиметил, метоксикарбонилоксиэтил, этоксикарбонилоксиметил, этоксикарбонилоксиэтил, пропоксикарбонилоксиметил, пропоксикарбонилоксиэтил, изопропоксикарбонилоксиметил, изопропоксикарбонилоксиэтил, бутоксикарбонилоксиметил, бутоксикарбонилоксиэтил, изобутоксикарбонилоксиметил, изобутоксикарбонилоксиэтил, пентилоксикарбонилоксиметил, пентилоксикарбонилоксиэтил, 2-метилбутоксикарбонилоксиметил, 2-метилбутоксикарбонилоксиэтил, 3-метилбутоксикарбонилоксиметил, 3-метилбутоксикарбонилоксиэтил, 2,2-диметилпропокси-3 015738 карбонилоксиметил, 2,2-диметилпропоксикарбонилоксиэтил, гексилоксикарбонилоксиметил, гексилоксикарбонилоксиэтил. Следующая группа подходящих соединений охватывает соединения, в которых R6 выбран из группы, включающей -С 0-2 алкилен-C(O)OR7, предпочтительно где R6 обозначает С(О)OR7 и где R7 обозначаетC1-6 алкил, такой как метил, этил, н-пропил, изопропил, бутил, трет-бутил. Примеры таких замещенных групп R6 включают метоксикарбонил, метоксикарбонилметил, метоксикарбонилэтил, этоксикарбонил,этоксикарбонилметил, этоксикарбонилэтил, пропоксикарбонил, пропоксикарбонилметил, пропоксикарбонилэтил, изопропоксикарбонил, изопропоксикарбонилметил, изопропоксикарбонилэтил, бутоксикарбонил, бутоксикарбонилметил, бутоксикарбонилэтил, изобутоксикарбонил, изобутоксикарбонилметил,изобутоксикарбонилэтил, пентилоксикарбонил, пентилоксикарбонилметил, пентилоксикарбонилэтил,2-метилбутоксикарбонил, 2-метилбутоксикарбонилметил, 2-метилбутоксикарбонилэтил, 3-метилбутоксикарбонил,3-метилбутоксикарбонилметил,3-метилбутоксикарбонилэтил,2,2-диметилпропоксикарбонил, 2,2-диметилпропоксикарбонилметил, 2,2-диметилпропоксикарбонилэтил, гексилоксикарбонил, гексилоксикарбонилметил, гексилоксикарбонилэтил. Следующая группа подходящих соединений охватывает соединения, в которых R6 выбран из группы, включающей -C1-2 алкилен-OC(O)NHR7, предпочтительно где R6 обозначает СН 2 ОС(О)NHR7 и где R7 выбран из группы, включающей C1-6 алкил, такой как метил, этил, н-пропил, изопропил, бутил, третбутил. Предпочтительными являются соединения, в которых R6 выбран из группы, включающей водород,-C0-2 алкилен-R7 и -C1-2 алкилен-OC(O)R7, где R7 выбран из группы, включающей C1-6 алкил. Еще более предпочтительными являются соединения, в которых R6 обозначает водород.R8 предпочтительно обозначает метил. Следует понимать, что в данном описании все ссылки на формулу (I) в равной степени относятся к предпочтительным группам соединений формулы (I). Предпочтительные индивидуальные соединения данного изобретения выбраны из соединений примеров, описанных в данном документе. Более предпочтительные индивидуальные соединения данного изобретения выбраны из группы,включающей 2-[1-(2,3-диметилфенил)этил]-1 Н-имидазол; 2-[(1S)-1-(2,3-диметилфенил)этил]-1 Н-имидазол; 2-[(1R)-1-(2,3-диметилфенил)этил]-1 Н-имидазол; 2-[1-(2,3-диметилфенил)этил]-1 Н-имидазол-1-илметилпивалат; 2-[1-(2,3-диметилфенил)этил]-1 Н-имидазол-1-илметилпропионат; 2-[1-(2,3-диметилфенил)этил]-1 Н-имидазол-1-илметил-3-метилбутаноат; 2-[1-(2,3-диметилфенил)этил]-1 Н-имидазол-1-илметилбутират; 2-[1-(2,3-диметилфенил)этил]-1 Н-имидазол-1-илметил-3-циклопентилпропаноат; 2-[1-(2,3-диметилфенил)этил]-1 Н-имидазол-1-илметилгептаноат; 2-[1-(2,3-диметилфенил)этил]-1 Н-имидазол-1-илметилпентаноат; 2-1-[2-(трифторметил)фенил]этил-1 Н-имидазол; 2-[1-(2,5-диметилфенил)этил]-1 Н-имидазол; 2-[1-(4-хлор-3-метилфенил)этил]-1 Н-имидазол; 2-[1-(3,5-диметилфенил)этил]-1 Н-имидазол; 1-(циклопропилметил)-2-[1-(2,3-диметилфенил)этил]-1 Н-имидазол; 2-[1-(2,3-диметилфенил)этил]-1-метил-1 Н-имидазол; циклопропилметил-2-[1-(2,3-диметилфенил)этил]-1 Н-имидазол-1-илметилкарбонат; 2-[1-(2,3-диметилфенил)этил]-1 Н-имидазол-1-илметил-3-метилбутилкарбонат; 2-[1-(2,3-диметилфенил)этил]-1 Н-имидазол-1-илметилизопропилкарбонат; 2-[1-(2,3-диметилфенил)этил]-1-этил-1 Н-имидазол; 2-[1-(2,3-диметилфенил)этил]-1-(метоксиметил)-1 Н-имидазол; изобутил-2-[1-(2,3-диметилфенил)этил]-1 Н-имидазол-1-карбоксилат; изопропил-2-[1-(2,3-диметилфенил)этил]-1 Н-имидазол-1-карбоксилат и 2-[1-(3-метилфенил)этил]-1 Н-имидазол или их фармацевтически приемлемые соли. Еще более предпочтительными соединениями настоящего изобретения являются 2-[1-(2,3 диметилфенил)этил]-1 Н-имидазол и 2-[1-(2,3-диметилфенил)этил]-1 Н-имидазол-1-илметилпивалат или их фармацевтически приемлемые соли. Наиболее предпочтительным соединением настоящего изобретения является 2-[1-(2,3 диметилфенил)этил]-1 Н-имидазол или его фармацевтически приемлемая соль. В объем настоящего изобретения входят все стереоизомеры, такие как энантиомеры и диастереомеры, все геометрические изомеры и таутомерные формы соединений формулы (I), в том числе соединения, относящиеся к нескольким типам изомеров, а также смеси одного или нескольких изомеров. В объем настоящего изобретения также входят кислотно-аддитивные или основные соли, содержащие оптиче-4 015738 ски активный противоион, например D-лактат или L-лизин, или рацемический противоион, напримерDL-тартрат или DL-аргинин. Следует понимать, что соединения формулы (I) могут содержать один или несколько асимметричных атомов углерода, следовательно соединения данного изобретения могут существовать в виде двух или более стереоизомеров. В частности, следует понимать, что если R8 и R9 обозначают разные заместители, то существует стереоцентр, который находится на атоме углерода, к которому они присоединены на бензильном атоме углерода. Соединения, подходящие для применения в данном изобретении, включают соединения, в которых абсолютная стереохимия бензильного атома углерода представляет собой"S-конфигурацию". Другие соединения, подходящие для применения в данном изобретении, включают соединения, в которых абсолютная стереохимия бензильного атома углерода представляет собой "Rконфигурацию". Такие стереоизомеры специалист в данной области может разделить и идентифицировать с помощью известных способов. Настоящее изобретение охватывает индивидуальные стереоизомеры соединений формулы (I), а также их смеси. Предпочтительные соединения формулы (I) включают соединения формулы (IA) и соединения формулы (IB), которые обладают указанной ниже стереохимией. Следует понимать, что в данном описании все ссылки на формулу (I) в равной степени относятся к соединениям формул (IA) и (IB). Кроме того, следует понимать, что все подходящие группы и предпочтительные значения R1-R12,aR , R и n, описанные для формулы (I), в равной степени применимы к соединениям формул (IA) и (IB). В конкретном воплощении данного изобретения предпочтительные соединения представляют собой соединения формулы (IA). В конкретном воплощении данного изобретения предпочтительные соединения представляют собой соединения формулы (IB). Предпочтительные соединения настоящего изобретения включают 2-[(1S)-1-(2,3 диметилфенил)этил]-1 Н-имидазол, 2-[(1R)-1-(2,3-диметилфенил)этил]-1 Н-имидазол, 2-[(1S)-1-(2,3 диметилфенил)этил]-1 Н-имидазол-1-илметилпивалат,2-[(1R)-1-(2,3-диметилфенил)этил]-1 Нимидазол-1-илметилпивалат либо их фармацевтически приемлемые соли или пролекарства. Еще более предпочтительные соединения настоящего изобретения представляют собой 2-[(1S)-1(2,3-диметилфенил)этил]-1 Н-имидазол, 2-[(1R)-1-(2,3-диметилфенил)этил]-1 Н-имидазол либо их фармацевтически приемлемые соли или пролекарства, которые имеют указанные ниже формулы. Наиболее предпочтительным соединением является 2-[(1S)-1-(2,3-диметилфенил)этил]-1 Нимидазол. Геометрические изомеры можно разделить традиционными методами, известными специалистам в данной области, такими как хроматография и фракционированная кристаллизация. Традиционные методы получения/выделения индивидуальных энантиомеров включают хиральный синтез из подходящего оптически чистого предшественника, стереоселективный синтез из прохирального предшественника, или разделение рацемической смеси (или рацемической смеси соли или производного), например, с помощью фракционированной кристаллизации или хиральной высокоэффективной жидкостной хроматографии (ВЭЖХ). Авторы настоящего изобретения отдают предпочтение методам,описанным в "Enantiomers, Racemates и Resolutions", J. Jacques и A. Collet, опубликованной Wiley, NY,1981; и "Handbook of Chiral Chemicals", chapter 8, Eds D. Ager и М. Dekker, ISBN:0-8247-1058-4. Альтернативно, рацемическую смесь (или рацемический предшественник) можно подвергнуть взаимодействию с подходящим оптически активным соединением, например спиртом, или, если соединение формулы (I) содержит кислый или основной фрагмент, с кислотой или основанием, такими как винная кислота или 1-фенилэтиламин. Полученную диастереомерную смесь можно разделить хроматографией и/или фракционированной кристаллизацией, после чего один диастереомер или оба диастереомера можно превратить в соответствующие чистые энантиомеры с помощью способов, хорошо известных специалистам в данной области. Хиральные соединения данного изобретения (и их хиральные предшественники), обогащенные одним из энантиомеров, можно получить с помощью хроматографии, обычно ВЭЖХ, на асимметричной-5 015738 смоле с использованием мобильной фазы, состоящей из углеводорода, как правило, гептана или гексана,содержащего от 0 до 50% изопропанола, обычно от 2 до 20% и от 0 до 5% алкиламина, обычно 0,1% диэтиламина. После концентрирования элюента получают обогащенную смесь. Стереоизомерные конгломераты можно разделить с помощью традиционных методов, известных специалистам в данной области, см., например, "Stereochemistry of Organic Compounds" by E.L. Eliel(Wiley, New York, 1994). В применении к соединениям формулы (I) термин "галоген" относится к группе, включающей фтор,хлор, бром или йод. Группы алкил, алкилен, алкенил, алкинил и алкокси, содержащие определенное число атомов углерода, могут быть неразветвленными или разветвленными. Примеры алкила включают метил, этил,н-пропил, изопропил, н-бутил, изобутил, втор-бутил и т-бутил. Примеры алкокси включают метокси,этокси, н-пропокси, изопропокси, н-бутокси, изобутокси, втор-бутокси и т-бутокси. Примеры алкилена включают -СН 2-, -СН(СН 3)- и -C2H4-. Примеры циклоалкила включают циклопропил, циклобутил, циклопентил, циклогексил и циклогептил. Во избежание неясностей следует учитывать, что в данном описании все ссылки на фармацевтически приемлемые соединения включают ссылки на приемлемые для ветеринарии соединения или приемлемые для сельского хозяйства соединения. Кроме того, следует понимать, что в данном описании все ссылки на фармацевтическую активность включают ссылки на активность, используемую в ветеринарии или в сельском хозяйстве. Фармацевтически приемлемые соли соединений формулы (I) включают кислотно-аддитивные и основные соли данных соединений. Подходящие кислотно-аддитивные соли получают из кислот, образующих нетоксичные соли. Примеры включают ацетаты, аспартаты, бензоаты, безилаты, бикарбонаты/карбонаты, бисульфаты/сульфаты, бораты, камзилаты, цитраты, едизилаты, эзилаты, форматы, фумараты, глюцептаты, глюконаты, глюкуронаты, гексафторфосфаты, хибензаты, гидрохлориды/хлориды,гидробромиды/бромиды, гидроиодид/иодид, изетионаты, лактаты, малаты, малеаты, малонаты, мезилаты, метилсульфаты, нафтилаты, 2-напсилаты, никотинаты, нитраты, оротаты, оксалаты, пальмитаты, памоаты, фосфаты/гидрофосфаты/дигидрофосфаты, сахараты, стеараты, сукцинаты, тартраты, тозилаты и трифторацетаты. Подходящие основные соли получают из оснований, образующих нетоксичные соли. Примеры включают соли алюминия, аргинина, бензатина, кальция, холина, диэтиламина, диоламина,глицина, лизина, магния, меглумина, оламина, калия, натрия, трометамина и цинка. Приемлемые в фармацевтике, ветеринарии и сельском хозяйстве кислотно-аддитивные соли некоторых соединений формулы (I) также можно получить традиционным способом. Например, раствор свободного основания можно обработать соответствующей кислотой, либо непосредственно, либо в подходящем растворителе, и полученную соль можно выделить либо фильтрацией, либо упариванием реакционного растворителя при пониженном давлении. Обзор по подходящим солям можно найти в "Handbookof Pharmaceutical Salts: Properties, Selection, and Use" by Stahl и Wermuth (Wiley-VCH, Weinheim,Germany, 2002). Соединения данного изобретения могут существовать в несольватированных и сольватированных формах. Термин "сольват" в данном описании относится к молекулярному комплексу, содержащему соединение данного изобретения и одну или несколько молекул фармацевтически приемлемого растворителя, например этанола. Термин "гидрат" используют, если указанный растворитель представляет собой воду. Фармацевтически приемлемые сольваты в соответствии с данным изобретением включают сольваты, в которых кристаллизационный растворитель может представлять собой изотопно замещенный растворитель, такой как D2O, d6-ацетон, d6-DMSO. Далее и на протяжении всего описания все ссылки на соединения формулы (I) включают ссылки на их соли, сольваты и комплексы, а также на сольваты и комплексы их солей. Как указано выше, данное изобретение включает все полиморфные модификации соединений формулы (I). В объем данного изобретения входят такие комплексы, как клатраты, комплексы включения лекарственное средство-хозяин, где в отличие от вышеупомянутых сольватов лекарственное средство и хозяин присутствуют в стехиометрических или нестехиометрических количествах. Кроме того, в объем данного изобретения входят комплексы лекарственного средства, содержащие два или несколько органических и/или неорганических компонентов, которые могут присутствовать в стехиометрических или нестехиометрических количествах. Полученные комплексы могут быть ионизированными, частично ионизированными или неионизированными. Обзор по таким комплексам можно найти в J. Pharm. Sci, 64 (8), 12691288 by Haleblian (August 1975). Настоящее изобретение охватывает все фармацевтически приемлемые изотопно-меченные соединения формулы (I), в которых один или несколько атомов заменены на атомы, имеющие такой же атомный номер, но другую атомную массу, или массовое число, отличающуюся от обычно встречающейся в природе. Примерами изотопов, подходящих для включения в соединения данного изобретения, являются изотопы водорода, такие как 2 Н и 3 Н, углерода, такие как 11 С, 13 С и 14 С, хлора, такие как 36Cl, фтора, та-6 015738 кие как 18F, йода, такие как 123I и 125I, азота, такие как 13N и 15N, кислорода, такие как 15O, 17O и 18O, фосфора, такие как 32 Р, и серы, такие как 35S. В объем данного изобретения входят так называемые "пролекарства" соединений формулы (I). К ним относятся некоторые производные соединений формулы (I), которые сами по себе могут иметь низкую фармакологическую активность, или они могут быть фармакологически не активными, однако после введения в или на организм животного они превращаются в организме хозяина или паразита в соединения формулы (I), обладающие целевой активностью, например, в результате гидролитического или ферментативного расщепления. Такие производные называют "пролекарствами". Следует понимать, что некоторые соединения формулы (I) сами по себе могут функционировать как пролекарства других соединений формулы (I). Дополнительную информацию по применению пролекарств можно найти в "Prodrugs as Novel Delivery Systems, vol. 14, ACS Symposium Series (T. Higuchi и W. Stella) и "BioreversibleCarriers in Drug Design", Pergamon Press, 1987 (ed. E В Roche, American Pharmaceutical Association). В соответствии с данным изобретением пролекарства могут быть получены, например, путем замещения подходящих функциональных групп, присутствующих в соединениях формулы (I), определенными фрагментами, известными специалистам в данной области как "про-фрагменты", как описано, например, в "Design of Prodrugs" by H Bundgaard (Elsevier, 1985). Некоторые примеры пролекарств в соответствии с данным изобретением включают:(i) если соединение формулы (I) содержит карбоксильную функциональную группу (-СООН), то ее сложный эфир, полученный, например, в результате замены атома водорода на (C1-C8)алкил;(ii) если соединение формулы (I) содержит спиртовую функциональную группу (-ОН), то ее простой эфир, полученный, например, в результате замены атома водорода на (C1-С 6)алканоилоксиметил; и(iii) если соединение формулы (I) содержит первичную или вторичную аминогруппу (-NH2 или-NHR, где RH), то ее амид, полученный, например, в результате замены одного или обоих атомов водорода на (C1-С 10)алканоил. В соответствии с данным изобретением пролекарства могут быть получены, например, путем взаимодействия соединения формулы (I), где R6 обозначает Н, с определенными фрагментами, известными специалистам в данной области как "про-фрагменты", как описано, например, в "Design of Prodrugs" byEdition), 2002, 410-458, (Taylor и Francis Ltd., London); а также в приведенных в указанных документах ссылках. Примеры заместителей включают алкиламины, ариламины, амиды, мочевины, карбаматы, карбонаты, имины, енамины, имиды, сульфенамиды и сульфонамиды. Углеводородный фрагмент указанных групп может представлять собой C1-6 алкил, фенил, гетероарил, такой как пиридил, С 2-6 алкенил и С 3-8 циклоалкил; где каждая из вышеуказанных групп может иметь один или несколько необязательных заместителей, если это химически возможно, независимо выбранных из галогена; гидрокси; C1-6 алкила,C1-6 галогеналкила и C1-6 алкокси. Другие примеры замещающих групп в соответствии с приведенным выше примером и примеры пролекарств других типов можно найти в вышеуказанных ссылках. Пролекарство, введенное опытному животному, которое в соответствии с данным изобретением метаболизируется в организме хозяина, можно легко идентифицировать путем анализа жидкости организма на соединение формулы (I). Наконец, некоторые соединения формулы (I) можно непосредственно использовать как пролекарства других соединений формулы (I). В другом аспекте настоящее изобретение предлагает способы получения соединения формулы (I),или его фармацевтически, ветеринарно или сельскохозяйственно приемлемой соли, или фармацевтически, ветеринарно или сельскохозяйственно приемлемого сольвата (в том числе, гидрата), любой природы, как описано ниже. Нижеследующие способы иллюстрируют общие способы синтеза, которые можно использовать для получения соединений данного изобретения. Специалистам в данной области известно, что в процессе синтеза соединений данного изобретения чувствительные функциональные группы нужно защищать с последующим удалением защитных групп. Введение и удаление защитных групп можно осуществлять традиционными методами, например, как описано в "Protective Groups in Organic Synthesis" by T.W. Greene и P.G.M. Wuts, John WileySons Inc(1999), а также в ссылках, содержащихся в данной публикации. Так если один или несколько из R1-R12,R15 и R16 содержат реакционноспособные функциональные группы, то в процессе синтеза соединений формулы (I) может потребоваться введение дополнительных защитных групп в соответствии со стандартными методами. В описанных ниже способах предполагается, что для всех синтетических предшественников, используемых в синтезе соединений формулы (I), определения R1-R12, R15 и R16, где R1-R12, R15 и R16 имеют значения, определенные в формуле (I), необязательно включают соответствующим образом защищенные варианты R1-R12, R15 и R16. Защитные группы, подходящие для указанных функциональных групп, описаны в приведенных ниже ссылках, а применение данных защитных групп, где это необходимо, специально включено в объем способов получения соединений формулы (I) и их предшественников,описанных в настоящем изобретении. В случае применения подходящих защитных групп требуется их-7 015738 последующее удаление с получением соединений формулы (I). Удаление защитных групп можно проводить стандартными методами, включающими методы, описанные в приведенных ниже ссылках. Если R6 обозначает защитную группу, предпочтительно он представляет собой бензил, п-метоксибензил, диэтоксиметил, аллил или тритил. Соединения формулы (I) можно получить из других соединений формулы (I) с помощью стандартных методов, известных специалистам в данной области, таких как электрофильное или нуклеофильное замещение, реакции перекрестного сочетания, катализируемые органометаллическими соединениями, и взаимопревращение функциональных групп. Например, соединения формулы (I), в которых один или несколько из R1, R2, R3, R4 и R5 обозначают CO2Rc, где Rc=алкил, можно превратить в соединения формулы (I), в которых один или несколько из R1, R2, R3, R4 и R5 обозначают C(O)Rd, где Rd=NH2, путем обработки гидроксидом аммония при 85 С в течение 2 ч. Подобным образом после обработки соединений формулы (I), где один или несколько из R1, R2, R3, R4 и R5 обозначают C(O)Rd, где Rd=NH2, дегидратирующим реагентом, таким как тионилхлорид, при низкой температуре в безводном растворителе, таком как N,N-диметилформамид, получают соответствующие нитрильные соединения. Соединения формулы (I), где R8 обозначает C1-C4-алкил, R9, R11 и R12 обозначают водород, R6 обозначает водород или алкил, а R1, R2, R3, R4 и R5 имеют указанные выше значения можно синтезировать из соединений формулы (II) с помощью стандартных методов гидрирования. Например, соединения формулы (II), где Ra обозначает водород, a Rb обозначает водород или алкил, можно восстановить до соединений формулы (I) в подходящем протонном растворителе, таком как метанол или пропан-2-ол в атмосфере водорода при температуре до 60 С и повышенном давлении до 300 фунт/кв.дюйм в присутствии 10% палладия на угле или активированного 10% палладия на угле Freiborg в течение не более 72 ч. Соединения формулы (I), в которых один или несколько из R1, R2, R3, R4 и R5 необязательно обозначают галоген, а остальные R1, R2, R3, R4 и R5 имеют указанные выше значения, можно получить из соединений формулы (II), в которых один или несколько из R1, R2, R3, R4 и R5 необязательно обозначают галоген, путем гидрирования. Так соединения формулы (II) можно восстановить с получением соединений формулы (I) в атмосфере водорода при температуре до 60 С и повышенном давлении до 200 фунт/кв.дюйм в присутствии 10% палладия на угле и хелатирующего реагента, такого как бромид цинка в стандартном протонном растворителе, таком как метанол или пропан-2-ол. Альтернативно, соединения формулы (I) можно получить из соединений формулы (II) в условиях гидрирования с переносом. Например, формиат аммония, или муравьиную кислоту, или формиат аммония в присутствии муравьиной кислоты, можно использовать в качестве источника водорода in situ, который в присутствии катализатора гидрирования, такого как 10% палладий на угле, в спиртовом растворителе,таком как пропан-2-ол, в течение 2-3 ч при температуре до 80 С может обеспечивать превращение соединений формулы (II) в соединения формулы (I). Необязательно реакции с использованием муравьиной кислоты в качестве источника водорода можно проводить в отсутствие спиртовых растворителей. Стереоселективное гидрирование с получением предпочтительного стереоизомера можно проводить с использованием хиральных катализаторов в соответствии со стандартными руководствами по органической химии или предшествующими литературными данными. Например, существует много известных гомогенных и гетерогенных каталитических методов с использованием переходных металлов,таких как палладий, родий и рутений. Особенно предпочтительным катализатором является тетрафторборат бис-(норборнадиен)родия(I). Энантиочистые лиганды, используемые для проведения энантиоселективного гидрирования, описаны в литературе, иллюстративные примеры гомохиральных лигандов включают фосфоланы, такие как Duphos и его аналоги, ферроценильные лиганды, такие как Josiphos,1-[(R)-2-(дифенилфосфино)ферроценил]этилди-трет-бутилфосфин, бифенильные лиганды, такие как(+/-)-2,2'-бис-(дифенилфосфино)-1,1'-бинафталин (BINAP) и смешанные лиганды, такие как Prophos,Diamp, Bicp, Monophos. Энантиоселективное гидрирование подробно описано, например, в Y. Yamanori,T. Imamoto, Reviews on Heteroatom Chemistry, 1999, 20, 227; Т. Clark, С. Landis, Tetrahedron: Asymmetry,2004, 15, 14, 2123; H. Blaser, Topics in Catalysis, 2002, 19, 1, 3; H. Blaser et al., Synthetic Methods of organometallic and inorganic chemistry, 2002, 10, 78; Pure and Applied Chemistry, 1999, 71, 8, 1531; Pure and-8 015738 Таким образом, обогащенные одним энантиомером соединения формулы (I) можно получить из нехиральных соединений формулы (II) путем стереоселективного гидрирования. Например, соединения формулы (II), где Ra обозначает водород, a Rb обозначает водород или алкил, можно восстановить до соединения формулы (I) в подходящем протонном растворителе, таком как метанол, в атмосфере водорода при температуре окружающей среды и повышенном давлении до 60 фунт/кв.дюйм, в присутствии родиевого катализатора, такого как тетрафторборат бис-(норборнадиен)родия(I), и хирального лиганда, такого как 1-[(R)-2-(дифенилфосфино)ферроценил]этилди-трет-бутилфосфин, с получением соединения формулы (I), обогащенного одним оптическим изомером. Для повышения энантиомерной чистоты соединений формулы (I) можно использовать хиральное разделение. Например, соль кислоты можно получить энантиоселективно путем добавления энантиомерно чистой хиральной кислоты, такой как ди-п-толуоил-L-винная кислота, в подходящем протонном растворителе, таком как метанол. В данном способе один энантиомер предпочтительно образует кристаллическую соль, которую можно удалить фильтрацией, тогда как другой энантиомер остается в маточной жидкости. После раздельной обработки соли и маточной жидкости подходящим основанием, таким как гидроксид натрия (1 N), энантиомеры разделяют, получая соединения формулы (I), обогащенные разными оптическими изомерами. Альтернативно, рацемические соединения формулы (I) можно разделить методом хиральной ВЭЖХ, известным специалистам в данной области, с получением энантиомерно чистого соединения формулы (I). Соединения формулы (II), в которых R6 обозначает защитную группу, такую как бензил или замещенный бензил, например п-метоксибензил, можно подвергнуть удалению защитных групп и восстановлению в условиях гидрирования с получением соединений формулы (I), в которых R6 обозначает водород. Кроме того, соединения формулы (I) можно получить путем образования имидазольного цикла, а также с помощью других способов синтеза, описанных в учебниках и в литературе. В одном иллюстративном примере данные соединения получают из соответствующим образом замещенных фенилацетонитрильных реагентов, например такое соединение, как 2-(2,3-диметилфенил)пропаннитрил можно подвергнуть взаимодействию с соответствующим образом замещенным этилендиамином, таким как соль птолуолсульфоновой кислоты и этилендиамина, при повышенной температуре в интервале 140-180 С с получением соединения формулы (I), где R1, R2 и R8 обозначают метил, a R3, R4, R5, R6 и R9, R11 и R12 обозначают водород. В другом примере имидазольный цикл получают путем взаимодействия подходящим образом 2 замещенных 2-арил-1,1-дибромэтенов и соответствующим образом замещенного этилендиамина при комнатной температуре с получением промежуточного 2-замещенного 2-арилметилимидазолина. Промежуточный 2-замещенный 2-арилметилимидазолин можно превратить в соединение формулы (I) с помощью стандартных способов окисления, таких как окисление Сверна. Соединения формулы (II) можно получить с помощью реакции Виттига путем взаимодействия соединения формулы (X) с илидом фосфора, полученного из соли соответствующего алкилфосфония. Например, обработка галогенида метилтрифенилфосфония сильным основанием в подходящем растворителе с последующим добавлением (X) дает соединение формулы (II), где и Ra, и Rb обозначают водород. Предпочтительно основной реагент представляет собой раствор н-бутиллития в гексане, растворитель представляет собой эфир или тетрагидрофуран, а температура реакции находится в интервале от комнатной до приблизительно 35 С. Соединения формулы (II) можно превратить в другие соединения формулы (II) путем взаимопревращения функциональных групп. Например, если один или несколько из R1, R2, R3, R4 и R5 обозначают бром или йод, a R6 защищен подходящей защитной группой, такой как бензил, можно использовать катализируемые палладием реакции сочетания, такие как реакции сочетания Стилла, Хека и Сузуки. Например, путем обработки такого органогалогенида соединения формулы (II) подходящей бороновой кислотой, такой как алкил- или арилбороновая кислота, в инертном растворителе, таком как толуол, в присутствии подходящего основания, такого как фосфат калия, подходящего фосфинового лиганда, такого как трициклогексилфосфин, и ацетата палладия в инертной атмосфере при повышенной температуре до 120 С в течение не более 18 ч, получают соответствующее алкилированное или арилированное соединение формулы (II). Аналогично, соединения формулы (II), где один или несколько из R1, R2, R3, R4 и R5 обозначают бром или йод, a R6 защищен подходящей защитной группой, такой как бензил, можно подвергнуть реакции трансметилирования в присутствии палладиевого катализатора, такого как хлорид [1,1-9 015738 бис-(дифенилфосфино)ферроцен]палладия(II), и затем реакции перекрестного сочетания с подходящим бороновым ангидридом, таким как триалкилбороксин, в инертной атмосфере, в присутствии слабого основания, такого как карбонат натрия, и подходящего инертного растворителя, такого как диоксан и вода,при повышенной температуре до 120 С. Альтернативно, соединения формулы (II), где один или несколько из R1, R2, R3, R4 и R5 обозначают бром или йод, a R6 защищен подходящей защитной группой, такой как бензил, можно подвергнуть реакции нуклеофильного замещения. Например, нитрильные соединения можно получить путем обработки такого галогенового соединения формулы (II) в полярном растворителе, таком как N,N-диметилацетамид, источником цианида, таким как цианид меди, при температуре до 150 С в течение 3 дней, с получением соответствующего соединения формулы (II), где один или несколько из R1, R2, R3, R4 и R5 обозначают циано, a R6 защищен подходящей защитной группой, такой как бензил. Нитрильные соединения формулы (II) также можно получить из соответствующих галогеновых соединений формулы (II) путем обработки источником цианида, таким как цианид натрия, в присутствии подходящего трансметаллирующего реагента, такого как бромид никеля, в полярном растворителе, таком как N-метилпирролидинон, при нагревании в микроволновой печи при 150 Вт до 150 С в течение 5 мин. Нитрильные соединения формулы (II) также можно получить из соответствующего галогенового соединения формулы (II) путем взаимодействия с подходящим источником цианида, таким как гексацианоферрат калия, трансметаллирующим реагентом, таким как иодид меди, солью, такой как иодид калия, и координирующим реагентом, таким как диметилэтилендиамин, в полярном растворителе, таком как N-метилпирролидинон, в инертной атмосфере при повышенной температуре до 140 С в течение не более 60 ч. Соединения формулы (II) можно получить из соединений формулы (III), используя стандартные условия дегидратации, необязательно R6 может представлять собой подходящую защитную группу, такую как бензил или замещенный бензил. Дегидратацию можно проводить в кислых условиях. Например, соединения формулы (III) можно обработать неорганической кислотой, такой как хлористо-водородная кислота (4-6 н.) или концентрированная серная кислота, в течение не более 72 ч, необязательно в органическом смешиваемом растворителе, таком как ацетонитрил, необязательно при повышенной температуре до 60 С. Альтернативно, дегидратацию можно проводить путем нагревания соединения формулы (III) при температуре кипения с органической кислотой, такой как трифторуксусная кислота или п-толуолсульфоновая кислота, в апротонном растворителе, таком как толуол. Дегидратацию соединений формулы (III) также можно осуществить с помощью реагента Итона, как правило, перемешивая при комнатной температуре в течение нескольких часов в отсутствие растворителя, или в полярном растворителе, таком как метанол. Дегидратацию также можно проводить путем обработки соединения формулы (III) тионилхлоридом в полярном растворителе,таком как ацетонитрил. Соединения формулы (III) можно использовать для непосредственного получения соединений формулы (I) путем обработки катализатором Перлмана в подходящем протонном растворителе, таком как метанол, в атмосфере водорода, если R6 представляет собой бензильную защитную группу, после удаления защитной группы получают соединение формулы (I), в котором R6 обозначает водород. Альтернативно, соединения формулы (III), в которых R6 обозначает защитную группу, такую как бензил, можно подвергнуть удалению защитных групп, дегидратации и восстановлению одновременно с гидрированием в кислых условиях. Например, после обработки соединений формулы (III) источником водорода, таким как формиат аммония, в присутствии кислоты, такой как муравьиная кислота, и 10% палладия на угле,необязательно в течение не более 72 ч, получают соединения формулы (I), в которых R6 обозначает водород. Соединения формулы (II) можно получить из соединений формулы (III) с помощью способов дегидрогалогенирования, известных специалистам в данной области, например, путем стандартного хлорирования с последующим дегидрохлорированием. Альтернативно, соединения формулы (II) можно получить с помощью реакций перекрестного сочетания, катализируемых переходными металлами, используя описанные в литературе способы. Для проведения данных реакций иногда нужно защитить основной имидазол, R6 необязательно может включать подходящую защитную группу, такую как диэтоксиметил. Так подходящим образом защищенные органоцинкаты, такие как соединения формулы (V), где X представляет собой галоген, например хлор или бром, можно подвергнуть реакции сочетания с подходящим образом замещенными стиролами, такими как соединения формулы (IV), где Y представляет собой группу, подходящую для трансметаллирования,такую как OTf, Cl, Br или I, в присутствии палладиевого катализатора, такого как Pd(PPh3)3.- 10015738 После стандартного удаления защитных групп с соединений формулы (II), в которых R6 обозначает подходящую защитную группу, получают соединения формулы (II), в которых R6 обозначает водород. Например, если R6 представляет собой диэтоксиметил, обработка органической кислотой, такой как трифторуксусная кислота, или неорганической кислотой, такой как хлористо-водородная кислота, дает соединение (II), в котором R6 представляет собой водород. Подобным образом, удаление защитных групп с соединений формулы (II), где R6 представляет собой бензильную защитную группу, можно легко провести путем гидрирования. Соединения формулы (III), где R6 обозначает защитную группу, можно получить путем 1,2 присоединения подходящим образом защищенного органометаллического соединения (VI) к соответствующему кетону (VII), если это допустимо с точки зрения химии, например, если R1, R2, R3, R4 и R5 независимо выбраны из алкила и хлора, a Ra и Rb представляют собой алкил. Например, соединение (VI) можно подвергнуть взаимодействию с кетоном (VII) в апротонном растворителе, таком как тетрагидрофуран, при температуре, обычно варьирующей от -80 до 0 С, с получением соединения формулы (III), с которого при желании можно легко удалить защитные группы и получить соединение формулы (III), в котором R6 обозначает Н. Альтернативную реакцию с органометаллическим соединением можно использовать для получения соединения формулы (III), в котором R6 обозначает подходящую защитную группу, такую как бензил, в данном способе органометаллическое соединение формулы (VIII), где X может обозначать галоген, например хлор или бром, добавляют к кетону формулы (IX), где R6 обозначает защитную группу. Подобным образом, соединения формулы (III), где R6 необязательно обозначает подходящую защитную группу, такую как бензил, также можно получить путем добавления органометаллического соединения к защищенному кетону (X), подходящие органометаллические реагенты включают реактивы Гриньяра и органолитиевые реагенты. Например, реактив Гриньяра, такой как хлорид метилмагния, добавляют к раствору соединения (X) в безводном апротонном растворителе, таком как тетрагидрофуран,толуол или диэтиловый эфир, при -10-0 С в течение не более 4 ч, получая соединение формулы (III), в котором Ra и Rb обозначают Н. Защитные группы с соединений формулы (III), в которых R6 обозначает защитную группу, такую как бензил, можно удалить в стандартных условиях гидрирования, таких как 10% палладий на угле в протонном растворителе при повышенных давлении и температуре, с получением незащищенного соединения формулы (III), где R6 обозначает водород. После постадийного удаления защитных групп с соединений формулы (III) и последующей дегидратации с получением соединений формулы (II), при необходимости, можно провести стереоселективное восстановление соединений формулы (II) с получением соединений формулы (I).- 11015738 Соединения формул (IV), (V), (VI), (VII), (VIII) и (IX) можно легко получить с помощью описанных в литературе способов или их модификаций, которые могут легко осуществить специалисты в данной области. Например, соединения формулы (V) можно получить путем перемешивания 1-защищенного имидазола с н-бутиллитием при пониженной температуре, обычно от -60 до -20 С, с последующим добавлением хлорида цинка и нагреванием до комнатной температуры. Например, соединение (VI) можно получить in situ путем обработки защищенного имидазольного реагента органолитиевым реагентом, таким как н-бутиллитий, в апротонном растворителе, таком как тетрагидрофуран, при пониженной температуре, обычно варьирующей от -80 до 0 С. Подходящие защитные группы включают диэтоксиметил. Например, соединения формулы (IX) можно синтезировать путем ацилирования подходящим образом замещенного имидазола хлорангидридами кислот. Так, нагревание в течение нескольких часов подходящего хлорангидрида с 1-защищенным имидазолом в присутствии слабого основания, такого как триэтиламин, дает соединение формулы (IX). Соединения формулы (VII) можно получить разными способами. В некоторых способах используются простые предшественники, как подробно описано ниже. Соединения формулы (VII) можно получить путем добавления хелатирующего реагента, такого какFe(acac)3, и реактива Гриньяра, такого как бромид метилмагния, к подходящим образом замещенному хлорангидриду (XI) при пониженной температуре, обычно при -20 С, в подходящем апротонном растворителе. Хлорангидриды (XI) можно получить путем взаимодействия соответствующей бензойной кислоты (XII) с тионилхлоридом или оксалилхлоридом при повышенной температуре, обычно при 100 С, в течение нескольких часов. Соединения формулы (VII) также можно получить путем взаимодействия ангидрида кислоты, такого как уксусный ангидрид, с фенильным реактивом Гриньяра (XIII) в апротонном растворителе. Альтернативно, вместо ангидридов кислот можно использовать амиды или хлорангидриды. Соединения формулы (XIII) можно получить in situ путем взаимодействия подходящего бромбензольного производного с магниевой стружкой в безводном апротонном растворителе, таком как тетрагидрофуран. Подобным образом соединения формулы (VII) можно получить путем взаимодействия реактива Гриньяра, например бромида метилмагния, с амидом, например подходящим образом замещенного бензоилморфолина (XIV), при кипении с обратным холодильником в подходящем растворителе, таком как тетрагидрофуран. Соединения формулы (VII) также можно получить путем взаимодействия подходящей бензойной кислоты (XII) с органолитиевым реагентом, например метиллитием, при пониженной температуре в безводном апротонном растворителе, таком как тетрагидрофуран. Соединения формулы (VII) можно получить путем ацилирования по Фриделю-Крафтсу фенильных фрагментов, содержащих подходящие функциональные группы. Например, содержащий функциональные группы фенильный реагент можно подвергнуть взаимодействию с кислотой Льюиса, такой как хлорид алюминия, в присутствии подходящего ацилирующего реагента, такого как ацетилхлорид, в апротонном растворителе, таком как дихлорметан, при комнатной температуре в течение периода времени не более 18 ч, с получением целевого соединения формулы (VII).- 12015738 Альтернативно соединения формулы (VII) можно получить с помощью двустадийного способа из подходящим образом замещенного галогенбензола, предпочтительно бром- или иодбензола. Например,бромбензольное соединение можно подвергнуть трансметаллированию с использованием органометаллического реагента, такого как н-бутиллитий, в безводном, неполярном растворителе, таком как тетрагидрофуран, при низкой температуре до -80 С, с последующим электрофильным гашением альдегидом с получением соответствующего вторичного спирта, который можно окислить в стандартных условиях,например с использованием периодинана Десса-Мартина, с получением соединения формулы (VII), гдеRa выбран из Н, С 1-4 алкила или С 0-4 алкиленфенила, а Rb - С 1-4 алкил или С 0-4 алкиленфенил. Соединения формулы (VII) также можно получить из соответствующего арилиодида и бороновых кислот с использованием химии палладия в атмосфере монооксида углерода. Так нагревание арилиодидов с монооксидом углерода, метилбороновой кислотой и тетракистрифенилфосфином палладия дает соединения формулы (VII), в которых Ra и Rb обозначают Н. Соединения формулы (VII) можно подвергнуть стандартным химическим реакциям и реакциям взаимопревращения функциональных групп, известных специалистам в данной области, с получением других соединений формулы (VII). Так соединения формулы (VII) можно хлорировать с помощью стандартных реагентов, таких как Selectafluor и хлорид натрия. Кроме того, подходящим образом замещенные галогенсодержащие соединения формулы (VII) можно подвергнуть катализируемым палладием стандартным реакциям перекрестного сочетания, таким как реакции Сузуки, Стилла, Хека, с получением ряда стандартных продуктов. Например, бром- или иодсодержащие соединения формулы (VII) можно алкилировать и арилировать с помощью реакций сочетания Сузуки путем обработки органоборана, например триэтилборана, в присутствии хлорида [1,1-бис-(дифенилфосфино)ферроцен]палладия(II) и карбоната калия в апротонном растворителе, таком как N,N-диметилформамид, с получением алкил- или арилзамещенных соединений формулы (VII). Соединения формулы (X) можно получить путем взаимодействия хлорангидридов формулы (XI) с имидазолами формулы (XV), где R6 обозначает подходящую защитную группу, в подходящем апротонном растворителе, таком как толуол или ацетонитрил, в присутствии слабого основания, такого как триэтиламин, при температуре, варьирующей от -10 до 130 С. Хлорангидриды формулы (XI), содержащие подходящие функциональные группы, можно синтезировать из соответствующей кислоты путем обработки тионилхлоридом при 80 С в течение 1 ч. Альтернативно, хлорангидриды можно синтезировать из карбоновых кислот путем обработки оксалилхлоридом в апротонном растворителе, таком как толуол, при комнатной температуре в течение периода времени не более 4 ч. Кислоты, содержащие подходящие функциональные группы, можно получить с помощью описанных в литературе стандартных методов, доступных специалистам в данной области, например, заместители можно ввести посредством электрофильного или нуклеофильного замещения, или реакций перекрестного сочетания, или взаимопревращения функциональных групп. Соединения формулы (X) также можно синтезировать путем окисления соединений формулы (XVI) с использованием подходящих окисляющих реагентов, где R6 обозначает водород или подходящую защитную группу. Такое окисление можно проводить, например, с использованием условий Десса-Мартина. Например, соединение формулы (X) можно получить путем перемешивания соответствующего соединения формулы (XVI) при комнатной температуре с периодинаном Десса-Мартина в подходящем полярном растворителе, таком как дихлорметан. Соединения формулы (XVI) можно получить путем 1,2-присоединения соответствующим образом защищенного органометаллического соединения к подходящему альдегиду. Так взаимодействие органолитиевого соединения формулы (VI) и соответствующего альдегида формулы (XVII) в безводном, апротонном растворителе, таком как тетрагидрофуран, при температуре, варьирующей от -80 до 0 С, дает соединения формулы (XVI). Следует понимать, что предшественники соединений формулы (I) и сами соединения формулы (I) можно подвергать взаимопревращению функциональных групп с получением альтернативных соединений формулы (I). Например, соединения формулы (I), в которых R6 обозначает водород, можно подвергнуть взаимодействию с алкилирующими реагентами формул L-C0-2 алкилен-R7, L-С 1-2 алкилен-OR7,- 13015738NHC(O)NR R , L-C1-2 алкилен-NR C(O)NR R , L-С 1-2 алкилен-С(О)NR15R16, L-C1-2 алкилен-OC(O)NHR7,L-С 1-2 алкилен-ОС(O)NR15R16, с получением соединений, в которых R6 обозначает -C0-2 алкилен-HR7,-C1-2 алкилен-OR7, -С 1-2 алкилен-С(О)R7, -С 1-2 алкилен-OC(O)R7, -C1-2 алкилен-OC(O)OR7, -С 1-2 алкиленС(О)OR7, -С 1-2 алкилен-N(H)C(O)R7, -C1-2 алкилен-N(R7)C(O)R7, -C1-2 алкилен-С(О)NHR7, -C1-2 алкиленNHC(O)NR15R16, -C1-2 алкилен-NR7C(О)NR15R16, -C1-2 алкилен-C(O)NR15R16, -С 1-2 алкилен-ОС(О)NHR7,-C1-2 алкилен-OC(O)NR15R16. L обозначает подходящую уходящую группу, такую как Cl, Br, I или сульфонат, такой как трифторметансульфонат. Например, соединения формулы (I), в которых R6 обозначает водород, можно подвергнуть взаимодействию с алкилирующими реагентами в присутствии слабого основания, такого как карбонат цезия, карбонат калия, триэтиламин или диизопропилэтиламин, в апротонном растворителе, таком как ацетон, 1-метил-2-пирролидинон, дихлорметан, тетрагидрофуран, ацетонитрил или N,N-диметилформамид, необязательно в присутствии соли, такой как иодид натрия. Как правило, реакция алкилирования протекает не более 72 ч при комнатной температуре, реакционную смесь необязательно нагревают при температуре кипения или в микроволновой печи при 200 Вт в течение не более 1 ч. Алкилирующие реагенты формулы Cl-СН 2 ОС(О)R7 можно получить путем взаимодействия хлорангидрида ClC(O)R7 с параформальдегидом в присутствии кислоты Льюиса, такой как хлорид цинка, при температуре до 80 С в течение 2-3 ч. В условиях алкилирования такие реагенты дают соединения формулы (I), в которых R6 обозначает CH2OC(O)R7. Алкилирующие реагенты формулы L-CH2OC(О)OR7 можно получить путем взаимодействия спирта 7HOR с хлорметилхлорформатом в апротонном растворителе, таком как дихлорметан, при температуре,варьирующей от 0 С до комнатной. В условиях алкилирования такие реагенты дают соединения формулы (I), в которых R6 обозначает CH2OC(O)OR7. Алкилирующие реагенты формулы L-CH2OC(О)NHR7 можно получить путем взаимодействия ами 7 на R NH2 с хлорметилхлорформатом в апротонном растворителе, таком как дихлорметан, при температуре, варьирующей от -10 С до комнатной. В условиях алкилирования такие реагенты дают соединения формулы (I), в которых R6 обозначает СН 2 ОС(О)NHR7. Алкилирующие реагенты формулы L-CH2OC(О)NR15R16 можно получить путем взаимодействия амина R15R16NH с хлорметилхлорформатом в апротонном растворителе, таком как дихлорметан, необязательно в присутствии слабого основания, такого как диизопропилэтиламин, при температуре, варьирующей от 0 С до комнатной. В условиях алкилирования такие реагенты дают соединения формулы (I),в которых R6 обозначает CH2OC(O)NR15R16. Соединения формулы (I), в которых R6 обозначает водород, можно подвергнуть взаимодействию с ацилирующими реагентами формул ClC(O)R7, О[ОС(О)R7]2, ClC(O)OR7, ClC(O)NHR7, ClC(O)NR15R16, с получением соединений, в которых R6 обозначает -C(O)R7, -OC(O)R7, -C(O)OR7, -C(O)NHR7,-C(O)NR15R16. Например, соединения формулы (I), в которых R6 обозначает водород, можно подвергнуть взаимодействию с ацилирующими реагентами в присутствии слабого основания, такого как триэтиламин или пиридин, в апротонном растворителе, таком как дихлорметан, тетрагидрофуран или ацетонитрил,при температуре, варьирующей от комнатной до 100 С, в течение периода времени от 1 до 36 ч. Ацилирующий реагент ClC(O)OR7 можно получить in situ. Так соединение формулы (I), в которых 6R обозначает водород, можно подвергнуть взаимодействию с фосгеном или дифосгеном в безводном растворителе, таком как дихлорметан или ацетонитрил, в присутствии слабого основания, такого как пиридин, в присутствии спирта R7OH при температуре окружающей среды с получением соединения формулы (I), в котором R6 обозначает С(О)OR7. Соединения формулы (I), в которых R6 обозначает водород, можно подвергнуть взаимодействию с фосфорилирующим реагентом формулы Cl-Р(=O)[N(R7)2(R7)2] с получением соединения формулы (I), в котором R6 обозначает Р(=O)[N(R7)2(R7)2], например взаимодействию с соответствующим бис(диалкиламино)фосфорилхлоридом, таким как бис-(диметиламино)фосфорилхлорид, в апротонном растворителе, таком как дихлорметан. Соединения формулы (I), в которых R6 обозначает водород, можно подвергнуть взаимодействию с силилирующим реагентом формулы Cl-Si(R7) с получением соединения формулы (I), в котором R6 обозначает Si(R7)3, например взаимодействию с соответствующим алкилсиланом или арилсиланом, таким как хлортриметилсилан, в апротонном растворителе, таком как дихлорметан или тетрагидрофуран. Соединения формулы (I), в которых R6 обозначает водород, можно подвергнуть взаимодействию с сульфонирующим реагентом формулы Cl-S(=O)2R10 с получением соединения формулы (I), в котором R6 обозначает S(=O)2R10, например взаимодействию с соответствующим сульфонилхлоридом, таким как метансульфонилхлорид, в апротонном растворителе, таком как дихлорметан, необязательно в присутствии слабого основания, такого как триэтиламин. Соединения формулы (I), в которых R6 обозначает водород, можно подвергнуть взаимодействию с цианогенбромидом в апротонном растворителе, таком как дихлорметан, необязательно в присутствии слабого основания, такого как диизопропилэтиламин, с получением соединения формулы (I), в которомR6 обозначает CN. Соединения формулы (III) можно алкилировать с получением соединений формулы (I), в которыхR9 обозначает С 1-С 4 алкокси. Так обработка соединений формулы (III) сильным основанием, таким как гидрид натрия, в апротонном растворителе, таком как тетрагидрофуран, с последующим добавлением алкилирующего реагента дает соединения формулы (I), в которых R9 обозначает С 1-С 4 алкокси. Соединения формулы (II) можно циклопропилировать с получением соединений формулы (I), в которых R8 и R9 вместе образуют циклопропильный фрагмент. Соединения формулы (II) можно подвергнуть взаимодействию с карбеноидным соединением, CRdRe. Например, если Rd=Re=F, реакционноспособные соединения, такие как триметилсилил дифтор(фторсульфонил)ацетат (TFDA), можно подвергнуть взаимодействию с соединением формулы (II), необязательно в неполярном растворителе, при повышенной температуре, в присутствии фторида натрия, с получением, после удаления защитных групп,продукта формулы (I), где циклопропильный фрагмент замещен фтором. Другие конкретные способы включают обработку хлороформом в присутствии основания, предпочтительно в условиях межфазного катализа, термолиз подходящего органометаллического предшественника, такого как арилтрифторметильное, трихлорметильное или фенил(трифторметильное) соединение ртути, или обработку диазоалканом в присутствии переходного металла в качестве катализатора, и обработку диазоалканом в отсутствие переходного металла в качестве катализатора, с последующим термолизом промежуточного пиразолина, или получение из илида серы. Кроме того, специалисты в данной области могут осуществлять модификации описанных способов,или использовать альтернативные способы, которые позволяют получать соединения формулы (I). Специалистам в данной области также известно, что в некоторых из описанных способов порядок стадий синтеза может варьировать и зависит, в числе прочего, от таких факторов, как природа других функциональных групп, присутствующих в конкретном субстрате, доступность ключевых промежуточных соединений, и используемая стратегия защитных групп (в случае необходимости). Очевидно, что такие факторы оказывают влияние на выбор реагента, используемого в указанных стадиях синтеза. Специалисты в данной области могут получить соединения данного изобретения с помощью способов, отличных от описанных в данном документе, путем адаптации описанных в данном документе способов и/или адаптации способов, известных, например, в области, к которой относится данное изобретение, или с помощью способов, описанных в стандартных руководствах, таких как "ComprehensiveOrganic Transformations - A Guide to Functional Group Transformations", R.C. Larock, Wiley-VCH (1999 или более поздние издания). Следует понимать, что способы синтетических превращений, упомянутые в данном описании, являются только иллюстративными и для эффективной сборки целевых соединений их можно использовать в разной последовательности. На основании накопленного опыта опытный химик может выбрать последовательность реакций, наиболее эффективную для синтеза заданного целевого соединения. Другие примеры замещающих групп в соответствии с приведенными выше примерами и примерами пролекарств других типов можно найти в вышеуказанных ссылках. Настоящее изобретение также относится к промежуточным соединениям формулы (LX), приведенной ниже где R1-R12, Ra, Rb и n имеют значения, определенные выше для формулы (I), или к их фармацевтически приемлемым солям или пролекарствам. В формуле (LX) подходящие R1 и R2 выбраны из C1-4 алкила, a R3,R4 и R5 обозначают водород. Настоящее изобретение также относится к промежуточным соединениям формулы (LXV), приведенной ниже где R1-R12, Ra, Rb и n имеют значения, определенные выше для формулы (I), и где Pg обозначает химическую защитную группу, или к их фармацевтически приемлемым солям или пролекарствам. В формуле- 15015738 Настоящее изобретение также относится к промежуточным соединениям формулы (LXX), приведенной ниже где R1-R12, Ra, Rb и n имеют значения, определенные выше для формулы (I), и где Pg обозначает химическую защитную группу, или к их фармацевтически приемлемым солям или пролекарствам. В формуле(LXX) подходящие R1 и R2 выбраны из C1-4 алкила, a R3, R4 и R5 обозначают водород. Следует понимать, что в данном описании все ссылки на формулу (I) в равной степени относятся к соединениям указанных выше формул (LX), (LXV) и (LXX). Кроме того, следует понимать, что все подходящие группы и предпочтительные значения R1-R12,aR , R и n, описанные для формулы (I), в равной степени применимы к соединениям указанных выше формул (LX), (LXV) и (LXX). Наконец, некоторые соединения формулы (I) можно использовать в качестве промежуточных соединений для получения других соединений формулы (I). Специалистам в данной области следует понимать, что Pg в вышеприведенных формулах (LX),(LXV) и (LXX) может включать широкий диапазон возможных защитных групп и что выбор конкретной группы зависит от получаемого конечного соединения и может быть легко осуществлен рядовым специалистом. Предпочтительные защитные группы включают бензил, параметоксибензил, аллил, тритил или 1,1-диэтоксиметил, предпочтительно бензил. Данное изобретение также относится к фармацевтической композиции, содержащей соединение формулы (I), или его фармацевтически приемлемую соль, или фармацевтически приемлемый сольват любой природы, наряду с фармацевтически приемлемым разбавителем или носителем, который может быть адаптирован для орального, парентерального или местного введения. Фармацевтические композиции, подходящие для доставки соединений настоящего изобретения, а также способы их получения хорошо известны специалистам в данной области. Такие композиции и способы их получения можно найти, например, в "Remington's Pharmaceutical Sciences", 19th Edition (MackPublishing Company, 1995). Соединения данного изобретения, предназначенные для фармацевтического применения, можно вводить в виде кристаллических или аморфных продуктов. Их можно получить, например, в виде твердых свечей, порошков или пленок, с помощью таких способов, как осаждение, кристаллизация, сушка из замороженного состояния, или сушка распылением, или сушка выпариванием. Для этой цели можно использовать микроволновую или высокочастотную сушку. Способы введения данных соединений включают оральное введение в виде капсул, болюсов, таблеток, порошков, пастилок, жвачек, лекарственных форм, состоящих из множества частиц, или наночастиц,гелей, твердых растворов, пленок, спреев или жидких композиций. Жидкие формы включают суспензии,растворы, сиропы, кисели и эликсиры. Такие композиции, пригодные для использования в качестве наполнителей мягких или твердых капсул, обычно содержат носитель, например воду, этанол, полиэтиленгликоль, пропиленгликоль, метилцеллюлозу или подходящее масло, а также одно или несколько эмульгирующих средств и/или суспендирующих средств. Жидкие композиции также можно получить путем восстановления твердого вещества, например, из саше. Кисели для орального применения обычно получают путем растворения или суспендирования активного ингредиента в подходящей среде. Соединения настоящего изобретения можно вводить отдельно, или в сочетании с одним или несколькими другими соединениями данного изобретения, или в сочетании с одним или несколькими другими лекарственными средствами (или с любой их комбинацией). Соединения можно вводить отдельно или в составе композиции, подходящей для конкретного предполагаемого применения, конкретных видов хозяев-млекопитающих, подлежащих лечению, и присутствующих паразитов. Как правило, их вводят в составе композиции в сочетании с одним или несколькими фармацевтически приемлемыми эксципиентами. Термин "эксципиент" в данном описании относится к любому ингредиенту, отличному от соединения (соединений) данного изобретения. Выбор эксципиента в значительной степени зависит от таких факторов, как конкретный способ введения, влияние эксципиента на растворимость и стабильность,а также от вида дозированной формы. Так, композиции для орального введения можно получить путем смешивания активного ингредиента с подходящим тонкоизмельченным разбавителем, и/или дезинтегрирующим средством, и/или связующим средством, и/или лубрикантом и т.п. Другие возможные ингредиенты включают антиоксиданты,красители, ароматизаторы, консерванты, а также средства, маскирующие вкус лекарственного средства.- 16015738 В оральных дозированных формах в зависимости от дозы масса лекарственного средства может составлять от 1 до 80% от массы дозированной формы, предпочтительно от 5 до 60% от массы дозированной формы. Примеры дезинтегрирующих средств включают гликолят крахмала натрия, карбоксиметилцеллюлозу натрия, карбоксиметилцеллюлозу кальция, кроскармелозу натрия, кросповидон, поливинилпирролидон, метилцеллюлозу, микрокристаллическую целлюлозу, низший алкилзамещенную гидроксипропилцеллюлозу, крахмал, желатинизированный крахмал и альгинат натрия. Как правило, масса дезинтегрирующего средства составляет от 1 до 25%, предпочтительно от 5 до 20% от массы дозированной формы. Связующие средства обычно используют для придания таблеточной композиции эффекта сцепления. Подходящие связующие средства включают микрокристаллическую целлюлозу, желатин, сахара,полиэтиленгликоль, природные и синтетические камеди, поливинилпирролидон, желатинизированный крахмал, гидроксипропилцеллюлозу и гидроксипропилметилцеллюлозу. Примеры разбавителей включают лактозу (моногидрат, высушенный распылением моногидрат, безводную лактозу и т.п.), маннит,ксилит, декстрозу, сахарозу, сорбит, микрокристаллическую целлюлозу, крахмал и дигидрат фосфата двухосновного кальция. Кроме того, оральные композиции могут необязательно содержать поверхностно-активные средства, такие как лаурилсульфат натрия и полисорбат 80, и средства, обеспечивающие скольжение, такие как диоксид кремния и тальк. Масса поверхностно-активных средств, если они присутствуют, может составлять от 0,2 до 5% от массы таблетки, а масса средств, обеспечивающих скольжение, может составлять от 0,2 до 1% от массы таблетки. Лубриканты включают стеарат магния, стеарат кальция, стеарат цинка, стеарилфумарат натрия, а также смеси стеарата магния с лаурилсульфатом натрия. Масса лубрикантов обычно составляет от 0,25 до 10%, предпочтительно от 0,5 до 3% от массы таблетки. Типичные таблетки содержат примерно до 80% лекарственного средства, приблизительно от 10 до 90 мас.% связующего средства, приблизительно от 0 до 85 мас.% разбавителя, приблизительно от 2 до 10 мас.% дезинтегрирующего средства и приблизительно от 0,25 до 10 мас.% лубриканта. Композиции таблеток описаны в "Pharmaceutical Dosage Forms: Tablets", vol. 1, by H. Lieberman andL. Lachman, Marcel Dekker, N.Y., 1980 (ISBN 0-8247-6918-X). Соединения можно вводить местно на кожу или на слизистую оболочку, то есть наружно или чрескожно. Это предпочтительный способ введения и желательно разрабатывать активные соединения, подходящие конкретно для таких композиций. Типичные композиции для данного способа введения включают композиции для обрызгивания, композиции для точечного нанесения, дезинфицирующие растворы,спреи, муссы, шампуни, порошковые композиции, гели, гидрогели, лосьоны, растворы, кремы, мази, порошки для присыпки, повязки, пенки, пленки, кожные пластыри, облатки, имплантаты, тампоны, волокна, бандажы и микроэмульсии. Также можно использовать липосомы. Типичные носители включают спирт, воду, минеральное масло, вазелиновое масло, белый вазелин, глицерин, полиэтиленгликоль и пропиленгликоль. В состав композиций могут входить средства, усиливающие проникновение, см., например, J. Pharm. Sci., 88 (10), 955-958, Finnin and Morgan (October 1999). Композиции для обрызгивания или для точечного нанесения можно получить путем растворения активного ингредиента в приемлемом жидком носителе, таком как бутилдигол, жидкий парафин или нелетучий сложный эфир, необязательно с добавлением летучего компонента, такого как пропан-2-ол. Альтернативно, композиции для обрызгивания или для точечного нанесения можно получить в виде капсул, оставляющих остаток активного средства на поверхности животного, что обеспечивает повышенные постоянство и продолжительность действия соединений формулы (I), например, они могут обладать повышенной устойчивостью к действию влаги. В композиции настоящего изобретения можно добавить средства, повышающие устойчивость таких композиций на поверхности животного, которому их вводят, например, для повышения устойчивости композиций на шерсти животного. В частности, предпочтительно включать такие средства в состав композиций, применяющихся для разбрызгивания или точечного нанесения. Примерами таких средств являются акриловые сополимеры, в особенности, фторированные акриловые сополимеры. Особенно подходящим реагентом является Foraperle (Redline Products Inc, Texas, USA). Чтобы минимизировать случайное оральное воздействие, в состав некоторых композиций для местного применения вводят добавки, придающие неприятный вкус. Композиции для инъекций можно получить в виде стерильных растворов, которые могут содержать и другие вещества, например соли или глюкозу, в количестве, достаточном для того, чтобы сделать раствор изотоническим по отношению к крови. Приемлемые жидкие носители включают растительные масла, такие как кунжутное масло, глицериды, такие как триацетин, сложные эфиры, такие как бензилбензоат, изопропилмиристат и производные пропиленгликоля и жирных кислот, а также органические растворители, такие как пирролидин-2-он и глицеринформаль. Данные композиции получают путем растворения или суспендирования активного ингредиента в жидком носителе, так, чтобы конечная композиция содержала от 0,01 до 10% по массе активного ингредиента.- 17015738 Альтернативно, соединения можно вводить парентерально или путем инъекции непосредственно в кровоток, мышцу или внутренний орган. Подходящие способы парентерального введения включают внутривенное, внутриартериальное, внутрибрюшинное, интратекальный, внутрижелудочковое, внутриуретральное, надчревное, внутричерепное, внутримышечное и подкожное введение. Подходящие способы парентерального введения включают введение посредством шприца с иглой (в том числе, с микроиглой), шприца без иглы и инфузии. Парентеральные композиции обычно представляют собой водные растворы, которые могут содержать эксципиенты, такие как соли, углеводы и забуферивающие средства(предпочтительно до pH от 3 до 9), однако для отдельных применений они могут быть получены в виде стерильного неводного раствора или порошкообразной высушенной формы, предназначенной для применения в сочетании с подходящей средой, такой как стерильная, не содержащая пирогенов вода. Парентеральные композиции можно получить в стерильных условиях, например путем лиофилизации, с помощью стандартных методов фармацевтической химии, хорошо известных специалистам в данной области. Растворимость соединений формулы (I), используемых для получения парентеральных растворов,можно повысить путем включения в состав композиций средств, повышающих растворимость. Такие композиции получают традиционным способом в соответствии со стандартной медицинской или ветеринарной практикой. Данные композиции варьируют в соответствии с массой содержащегося в ней активного соединения в зависимости от вида подлежащего лечению животного-хозяина, тяжести и типа инфекции и массы тела хозяина. При парентеральном, местном и оральном введении доза активного ингредиента обычно находится в интервале от 0,01 до 100 мг на кг массы тела животного. Предпочтительно доза находится в интервале от 0,1 до 10 мг на 1 кг. Композиции могут обеспечивать быстрое и/или модифицированное контролируемое высвобождение. Композиции с контролируемым высвобождением включают композиции с модифицированным высвобождением, в том числе, с отсроченным, замедленным, пульсирующим, контролируемым, направленным или программируемым высвобождением. Композиции с модифицированным высвобождением, подходящие для целей данного изобретения, описаны в патенте США 6106864. Другие технологии подходящего высвобождения, такие как применение высокоэнергетических дисперсий, а также осмотических и покрытых частиц, подробно описаны в Verma et al., Pharmaceutical Technology On-line, 25(2), 1-14(2001). Применение жевательной резинки для достижения контролируемого высвобождения описано вWO 00/35298. Альтернативно, композиции на основе соединений данного изобретения можно получать в твердом виде, полутвердом виде или в виде тиксотропной жидкости для введения в виде имплантируемого депо, обеспечивающего модифицированное высвобождение активного соединения. Примеры таких композиций включают стенты, покрытые лекарственным средством, и микросферы PGLA. В качестве альтернативы, соединения можно вводить отличному от человека животному вместе с кормом путем смешивания полученной концентрированной пищевой добавки или предварительно приготовленной смеси с обычной пищей животного. Все вышеуказанные водные дисперсии, или эмульсии, или смеси для распыления, можно наносить,например, на сельскохозяйственные культуры с помощью любых подходящих способов в основном путем распыления, с нормой расхода, которая обычно составляет приблизительно от 100 до 1200 л распыляемой смеси на гектар, однако она может быть выше или ниже (например, низкий или ультранизкий объем), в зависимости от необходимости или метода применения. Соединения или композиции в соответствии с данным изобретением можно наносить на растения, в частности на корни или листья, содержащие вредителей, подлежащих устранению. Другой способ применения соединений или композиций данного изобретения заключается во внесении их с поливной водой, другими словами, при добавлении композиции, содержащей активный ингредиент, к поливной воде. Орошение можно производить разбрызгиванием, как в случае лиственных пестицидов, или его можно производить непосредственно на землю или под землей, в случае почвенных или системных пестицидов. Концентрированные суспензии, которые можно наносить, например, путем распыления, получают в виде стабильного жидкого продукта с отсутствием оседания (тонкое диспергирование), который обычно содержит приблизительно от 10 до 75% по массе активного ингредиента, приблизительно от 0,5 до 30% поверхностно-активных веществ, приблизительно от 0,1 до 10% тиксотропных веществ, приблизительно от 0 до 30% подходящих добавок, таких как пеногасители, ингибиторы коррозии, стабилизаторы, смачивающие средства, связующие средства и в качестве носителя - воду или органическую жидкость, в которых активный ингредиент растворяется плохо или не растворяется. В носителе могут быть растворены некоторые органические твердые вещества или неорганические соли, предотвращающие оседание ингредиентов или замерзание воды. Смачиваемые порошки (или порошки для распыления) обычно содержит приблизительно от 10 до 80% по массе активного ингредиента, приблизительно от 20 до 90% твердого носителя, приблизительно от 0 до 5% увлажняющего средства, приблизительно от 3 до 10% диспергирующего средства и, при необходимости, приблизительно от 0 до 80% одного или нескольких стабилизаторов и/или других добавок,таких как смачивающие средства, способствующие проникновению, адгезивные средства, средства, предотвращиющие спекаемость, красители и т.п. Чтобы получить такие смачиваемые порошки, активный- 18015738 ингредиент (активные ингредиенты) тщательно смешивают в подходящем блендере с дополнительными веществами, которыми может быть пропитан пористый фильтр, и перемалывают с помощью мельницы или другой подходящей машины для измельчения. Полученные смачиваемые порошки обладают улучшенной смачиваемостью и способностью к суспендированию. Суспензии данных порошков в воде с желательной концентрацией можно эффективно использовать, в особенности, для нанесения на листья растений."Диспергируемые в воде гранулы (WG)" (гранулы, которые легко диспергируются в воде) представляют собой композиции, близкие к композицям смачиваемых порошков. Их можно получить путем гранулирования композиций смачиваемых порошков либо влажным способом (после приведения в контакт тонкоизмельченного активного ингредиента с инертным наполнителем и небольшим количеством воды, например от 1 до 20% по массе, или с водным раствором диспергирующего средства или связующего средства, смесь сушат и просеивают), либо сухим способом (после приведения в контакт смесь перемалывают и просеивают). В зависимости от способа нанесения, или природы композиции, или способа ее применения, количество и концентрация наносимых композиций могут варьировать. В общем композиции для подавления таких вредителей, как членистоногие, растительные нематоды, гельминты или простейшие, обычно содержат приблизительно от 0,00001 до 95%, более конкретно приблизительно от 0,0005 до 50% по массе одного или нескольких соединений формулы (I), или их пестицидно приемлемых солей, или суммарных активных ингредиентов (другими словами, соединения формулы (I), или его пестицидно приемлемой соли, вместе с другими веществами, токсичными для членистоногих или растительных нематод, противоглистными средствами, противококцидными средствами, синергически действующими лекарственными средствами, следовыми элементами или стабилизаторами). Выбор конкретной композиции и наносимое количество, обеспечивающее желательный эффект (эффекты), осуществляется фермером, животноводом, врачом или ветеринаром, оператором по борьбе с вредителями или другим специалистом в данной области. С целью улучшения растворимости, скорости растворения, маскирования вкуса, биодоступности и/или стабильности при применении в любом из вышеуказанных способов введения соединения данного изобретения могут быть объединены с растворимыми макромолекулярными соединениями, такими как циклодекстрин и его подходящие производные, или полиэтиленгликольсодержащие полимеры. Например, комплексы лекарственное средство-циклодекстрин обычно используются в большинстве дозированных форм и способов введения. Можно использовать как комплексы включения, так и другие комплексы. В качестве альтернативы непосредственному образованию комплекса с лекарственным средством, циклодекстрин можно использовать в качестве вспомогательного средства, т.е. в качестве носителя, разбавителя или солюбилизатора. Чаще всего с этой целью используются альфа-, бета- и гаммациклодекстрины, примеры которых можно найти в международных патентных заявках WO 91/11172,WO 94/02518 и WO 98/55148. Соединения данного изобретения также можно смешать с одним или несколькими биологически активными соединениями или средствами, включающими инсектициды, акарициды, противоглистные средства, фунгициды, нематоциды, противопротозойные средства, бактерицидные средства, регуляторы роста, энтомопатогенные бактерии, вирусы или грибки, с получением многокомпонентного пестицида,обладающего еще более широким спектром фармацевтического, ветеринарного или сельскохозяйственного применения. Так, настоящее изобретение также относится к композиции, содержащей биологически эффективное количество соединений данного изобретения и эффективное количество по меньшей мере одного другого биологически активного соединения или средства, а также одно или несколько поверхностно-активных веществ, твердый разбавитель или жидкий разбавитель. Конкретные другие активные соединения включают соединения, описанные в международной патентной заявке WO 2005/090313 на с. 39-44. Иногда желательно вводить комбинацию активного соединения, например, для лечения конкретного заболевания или состояния соответственно в объем настоящего изобретения входит комбинация двух или более фармацевтических композиций, по меньшей мере одна из которых содержит соединение данного изобретения, объединенных в наборе, подходящем для совместного введения композиций. Таким образом, набор данного изобретения содержит две или более отдельных фармацевтических композиций, по меньшей мере одна из которых содержит соединение формулы (I) в соответствии с данным изобретением, а также средства для раздельного хранения указанных композиций, такие как контейнер, разделенная на отсеки бутыль, или разделенный на отсеки пакет из фольги. Примером такого набора является обычная блистерная упаковка, используемая для хранения таблеток, капсул и т.п. Набор данного изобретения в особенности подходит для введения разных дозированных форм, например оральных и парентеральных, для введения отдельных композиций с разными дозировочными интервалами, или для титрования композиций друг против друга. В соответствии с техническими требованиями набор обычно содержит инструкции по введению и, кроме того, он может быть снабжен памяткой.- 19015738 Соединения данного изобретения, т.е. соединения формулы (I), обладают паразитицидной активностью у людей, животных, насекомых и растений. В особенности они подходят для обработки эктопаразитов. Данное изобретение также относится к соединению формулы (I), или его фармацевтически приемлемой соли, или его фармацевтически приемлемому сольвату любой природы, а также к фармацевтической композиции, содержащей любое из вышеупомянутых веществ, для применения в качестве лекарственного средства. Другой аспект данного изобретения относится к применению соединения формулы (I), или его фармацевтически приемлемой соли, или его фармацевтически приемлемого сольвата любой природы, в производстве лекарственного средства для лечения паразитарной инфекции. В одном воплощении данное изобретение можно использовать в производстве лекарственного средства для лечения паразитарной инфекции у людей. В одном воплощении данное изобретение можно использовать в производстве лекарственного средства для лечения паразитарной инфекции у животных. В одном воплощении данное изобретение можно использовать в производстве лекарственного средства для лечения паразитарной инфекции у насекомых. В одном воплощении данное изобретение можно использовать в производстве лекарственного средства для лечения паразитарной инфекции растений. Следующий аспект данного изобретения относится к способу лечения паразитарной инфекции у млекопитающего, который включает обработку указанного млекопитающего эффективным количеством соединения формулы (I), или его фармацевтически приемлемой солью, или его фармацевтически приемлемым сольватом любой природы, или фармацевтической композицией, содержащей любое из вышеуказанных веществ. Следующий аспект данного изобретения относится к способу профилактики паразитарной инфекции у млекопитающего, который включает обработку указанного млекопитающего эффективным количеством соединения формулы (I), или его фармацевтически приемлемой солью, или его фармацевтически приемлемым сольватом любой природы, или фармацевтической композицией, содержащей любое из вышеуказанных веществ. В следующем аспекте данное изобретение также относится к способу борьбы с переносом заболевания у млекопитающего, который включает обработку указанного млекопитающего эффективным количеством соединения формулы (I), или его фармацевтически приемлемой солью, или его фармацевтически приемлемым сольватом любой природы, или фармацевтической композицией, содержащей любое из вышеуказанных веществ. В соответствии с другим аспектом настоящего изобретения предлагается способ борьбы с такими вредителями, как членистоногие, растительные нематоды или гельминты, на некотором участке, который включает обработку данного участка (например, путем нанесения или введения) эффективным количеством соединения общей формулы (I), или его пестицидно приемлемой соли. Во избежание неясностей следует указать, что термин "обработка" в данном описании относится к лечению, ослаблению симптомов и профилактике, термин "борьба" (с паразитами и/или вредителей и др.) включает уничтожение, отталкивание, удаление, ограничение дееспособности, отпугивание, ликвидацию, уменьшение, минимизацию, истребление. Соединения данного изобретения можно использовать для борьбы с членистоногими вредителями. В частности, их можно использовать в областях ветеринарии, животноводства и здравоохранения против членистоногих, которые являются внутренними или внешними паразитами позвоночных, особенно теплокровных позвоночных, включая человека и домашних животных, таких как собаки, кошки, крупный рогатый скот, овцы, козы, лошади, свиньи, домашняя птица и рыбы, например Acarina, таких как зудниpharaonis). Кроме того, соединения настоящего изобретения можно использовать для подавления вредителей растений, населяющих почву вредителей и других вредителей, присутствующих в окружающей среде. В особенности, настоящее изобретение можно использовать для борьбы с членистоногими вредителями у млекопитающих, в частности у людей и животных. Предпочтительно данное изобретение можно использовать для борьбы с членистоногими вредителями у таких животных, как домашний скот, например рогатый скот, овцы, козы, лошади, свиньи, и животные-компаньоны, такие как собаки и кошки.- 20015738 Соединения данного изобретения предпочтительно можно использовать для борьбы с членистоногими, наносящими вред человеку и домашним животным, или распространяющимися у людей и домашних животных, или действующими как переносчики заболеваний у людей и домашних животных, например, указанных выше, и более предпочтительно для подавления зудней, клещей, вшей, блох, мошек и власоедов, вредных и переносящих миаз мух. В особенности их можно использовать для борьбы с членистоногими, которые паразитируют в коже, или на коже, или питаются кровью животного, путем орального, парентерального, чрескожного или местного введения. Соединения данного изобретения можно использовать для обработки паразитов и подавления стадий их жизненного цикла, включающих яйца, куколки, личинки, неполовозрелые особи и зрелые особи. В соответствии с другим аспектом настоящее изобретение предлагает способ борьбы с членистоногими вредителями насекомых, который включает обработку насекомого эффективным количеством соединения общей формулы (I) или его пестицидно приемлемой соли. Соединения настоящего изобретения также можно использовать для лечения инфекций, вызываемых клещами, в особенности клещами варроа. В частности, соединения настоящего изобретения можно использовать для лечения инфекции клещей варроа у пчел. В соответствии с другим аспектом настоящее изобретение предлагает способ борьбы с членистоногими вредителями растений, который включает обработку растения эффективным количеством соединения общей формулы (I) или его пестицидно приемлемой соли. Соединения данного изобретения также можно использовать для борьбы с членистоногими вредителями растений. Активное соединение обычно наносят на участок, в котором нужно подавить инфекцию членистоногих, при норме расхода приблизительно от 0,005 до 25 кг активного соединения на гектар (га) обрабатываемого участка, предпочтительно от 0,02 до 2 кг/га. В идеальных условиях, в зависимости от вида вредителя, подлежащего уничтожению,достаточная защита может достигаться при более низких дозах. С другой стороны, неблагоприятные погодные условия и другие факторы могут потребовать увеличения концентрации активного ингредиента. Для нанесения на листву можно использовать норму расхода от 0,01 до 1 кг/га. Предпочтительно участок представляет собой поверхность растения или почву вокруг обрабатываемого растения. В соответствии с другим аспектом настоящее изобретение предлагает способ защиты лесоматериалов, который включает обработку лесоматериалов эффективным количеством соединения общей формулы (I) или его пестицидно приемлемой соли. Соединения настоящего изобретения также можно использовать для защиты лесоматериалов (стоящих, срубленных, распиленных, хранящихся или конструкционных) от воздействия пилильщиков, жуков-вредителей или термитов. Их можно использовать для защиты продуктов, таких как зерно, фрукты, орехи, пряности и табак, хранящихся в целом виде, в размолотом виде, или в составе продуктов, от воздействия моли, жуков-вредителей и клещей. С помощью соединений настоящего изобретения также можно защищать такие животные продукты, как кожа, волосы,шерсть и перья, хранящиеся в естественном или обработанном виде (например, в виде ковров или текстильных изделий), от воздействия моли и жуков-вредителей; кроме того, от воздействия жуковвредителей, клещей и мух можно защищать хранящиеся мясо и рыбу. Твердые или жидкие композиции для местного нанесения на лесоматериалы, хранящиеся продукты или предметы домашнего обихода обычно содержат приблизительно от 0,00005 до 90%, более предпочтительно приблизительно от 0,001 до 10% по массе одного или нескольких соединений формулы (I) или их пестицидно приемлемых солей. Жидкие композиции данного изобретения помимо обычного сельскохозяйственного применения можно использовать, например, для обработки подложек или участков, инфицированных членистоногими, или подверженных заражению членистоногими (или другими вредителями, подавляемыми соединениями данного изобретения), включающих помещения, открытые или закрытые хранилища, или производственные помещения, контейнеры или оборудование, или стоячую или водопроводную воду. Настоящее изобретение также относится к способу чистки животных, имеющих хорошее состояние здоровья, включающему нанесение на животное соединения формулы (I) или его ветеринарно приемлемой соли. Целью такой чистки является уменьшение или устранение заражения людей паразитами, присутствующими на животном, а также улучшение окружающей среды, в которой живут люди. Биологическую активность соединений тестируют с помощью одного или нескольких описанных ниже способов тестирования.In vitro анализ на активность против зудней. Нанесение октопаминовых агонистов вызывает у акарид, например зудней, различные изменения в поведении по сравнению с необработанными контрольными зуднями. Обработанные зудни приходят в возбужденное состояние и начинают непрерывно двигаться, что препятствует их прикреплению и питанию на животном-хозяине, на которое наносят соединение. При нормальном поведении зудни приходят в состояние покоя после удаления всех других внешних стимулов. Возбуждение и движение можно измерить in vitro в лаборатории, чтобы предсказать эффективность и активность соединений in vivo. Анализ проводят, используя голодных Rhipicephalus sanguineus (коричневый собачий зудень) и предварительно покрытые стеклянные флаконы с площадью внутренней поверхности 34,5 см 2. Каждое соединение тестируют с 2 повторами. Соединение (345 мкг) растворяют в изопропиловом спирте (500 мкл) и вносят в каждый флакон.- 21015738 Флаконы помещают в поворотном роллере в вытяжной шкаф на 2 ч и оставляют, чтобы изопропиловый спирт испарился с получением концентрации соединения в каждом флаконе 10 мкг/см 2. В каждый предварительно покрытый флакон добавляют пять R.sanguineus (самцов и самок), после чего флаконы закрывают плотной пробкой из хлопковой ваты. Затем флаконы держат неподвижными на стеллаже при комнатной температуре. Наблюдение и регистрацию активности осуществляют через 24, 48 и 72 ч после добавления зудней во флаконы. Значение ED100 определяют как самую низкую дозу, при которой все пять зудней двигаются по кругу внутри флакона. Октопаминовая активность. Специалист в данной области может определить агонистическую активность соединений против рецепторов октопамина насекомых, экспрессирующихся в клетках СНО путем адаптации способов, описанных в В. Maqueira, H. Chatwin, P.D. Evans, J. Neurochemistry, 2005, 94, 2, 547. Активность соединения определяют по увеличению уровня цАМФ с помощью разных методов, известных специалистам в данной области, и выражают в виде %Vmax (Vmax=максимальный октопаминовый ответ) и ЕС 50. Адренергическая активность. 2-Адренергическую активность соединений определяют с помощью описанных в литературе методов, подвергнутых простой адаптации, которую может выполнить любой специалист в данной области. Подходящие методы включают описанные в J.J. Meana, F. Barturen, J.A. Garcia-Sevilla, Journal of Neurochemistry, 1989, 1210; и D.J. Loftus, J.M. Stolk, D.С. U'Pritchard, Life Sciences, 1984, 35, 610. Примеры Нижеследующие примеры иллюстрируют способы получения соединений формулы (I). В нижеследующих примерах структуры изображают следующим образом: Если не указано иначе, клинообразные и прерывистые линии отражают абсолютную стереохимию конкретного хирального центра, волнистые линии показывают, что абсолютная стереохимия неизвестна,однако соединение представляет собой индивидуальный стереоизомер по данному хиральному центру. Прямые линии, исходящие от хирального центра, показывают, что стереоизомеры не разделены и имеет место смесь стереоизомеров. Если источник простого предшественника не указан, такое соединение может быть получено от коммерческих поставщиков или с помощью известных из литературы способов. Ниже приведен список коммерческих поставщиков таких соединений:JRD Fluorochemicals Ltd., Unit 11, Mole Business Park, Leatherhead, Surrey, KT22 7BA, UK. Используемые инструменты. В приведенных ниже экспериментах спектры ядерного магнитного резонанса получают с помощью спектрометров Varian Inova 300, Varian Inova 400, Varian Mercury 400, Varian Unityplus 400, Bruker AC 300 мГц, Bruker AM 250 мГц или Varian T60 мГц, наблюдаемые химические сдвиги согласуются с предполагаемыми структурами. Химические сдвиги ЯМР выражают в м.д. по отношению к тетраметилсилану. Масс-спектры получают на масс-пектрометрах Finnigan ThermoQuest Aqa, Waters micromass ZQ,Bruker APEX II FT-MS или Hewlett Packard система ЖХ-МС, модель 5971. Рассчитанные и наблюдаемые ионы относят к изотопному составу с наименьшей массой. ВЭЖХ - это краткое обозначение высокоэффективной жидкостной хроматографии. Результаты аналитической ВЭЖХ получают с помощью системы ВЭЖХ НР 1100. Результаты препаративной ВЭЖХ получают с помощью системы препаративной ВЭЖХ- 22015738 Данные микроанализа CHN получают с помощью приборов Exeter Analytical CE 440 в аналитическом центре Уорика (University of Warwick Science Park, Barclays Venture Centre, Sir William Lyons Road,Coventry, CV4 7EZ). Данные оптического вращения получают с помощью поляриметра Perkin Elmer 341 в аналитическом центре Уорика (University of Warwick Science Park, Barclays Venture Centre, Sir William Lyons Road,Coventry, CV4 7EZ). Пример 1. 2-[1-(2,3-Диметилфенил)этил]-1 Н-имидазол Раствор соединения, полученного по способу 194 (11,0 г, 38,1 ммоль), и гидроксида палладия(II)(1,10 г, 7,83 ммоль) в метаноле (100 мл) нагревают до 60 С при давлении 300 фунт/кв.дюйм в атмосфере водорода в течение 18 ч. Затем реакционную смесь фильтруют и концентрируют в вакууме, после чего остаток перекристаллизовывают из горячего ацетонитрила (50 мл), получая указанное в заголовке соединение (3,27 г). Экспериментальное значение МН+ 201,3; ожидаемое значение 201,1. 1H-ЯМР (CD3OD): 1,50-1,55 (3 Н), 2,15-2,20 (3 Н), 2,20-2,25 (3 Н), 4,40-4,50 (1 Н), 6,80-6,85 (1 Н), 6,906,92 (2 Н), 6,95-7,00 (2 Н). Действие на Rhipicephalus (Rhip). ED100 мкг/см 2=0,1. Альтернативный синтез. Раствор соединения, полученного по способу 1 (72 мг, 0,36 ммоль), в метаноле (5 мл) гидрируют при давлении 100 фунт/кв.дюйм и 60 С с использованием палладия (10 мас.% на угле, 10 мг) в течение ночи. Смесь фильтруют, после чего фильтрат концентрируют в вакууме. Остаток растворяют в метаноле(1 мл) и диэтиламине (2-3 капли, 1 мл) и очищают методом автоматизированной препаративной жидкостной хроматографии (система Gilson, колонка 150 мм 30 мм LUNA C18(2), 10 мкм, 40 мл/мин), используя градиент ацетонитрил:вода [от 30:70 до 98:2]. Соответствующие фракции концентрируют в вакууме, получая указанное в заголовке соединение (26 мг). Экспериментальное значение МН+ 201,2; ожидаемое значение 201,1. 1H-ЯМР (d6-ДМСО): 1,65-1,72 (3 Н), 2,13-2,18 (3 Н), 2,24-2,31 (3 Н), 4,43-4,52 (1 Н), 6,89-6,92 (2 Н),7,00-7,03 (1 Н), 7,03-7,11 (2 Н). Альтернативный синтез. К смеси соединения, полученного по способу 1 (1,0 г, 3,26 ммоль), и формиата аммония (1,0 г,15,9 ммоль) в муравьиной кислоте (20 мл) добавляют палладий (10 мас.% на угле, 1,0 г). Реакционную смесь нагревают при 100 С в течение 72 ч, фильтруют и концентрируют в вакууме. Остаток перетирают со смесью метанол:этилацетат [1:9], получая указанное в заголовке соединение (200 мг). Экспериментальное значение МН+ 201,3; ожидаемое значение 201,1. 1 Н-ЯМР (CD3OD): 1,65-1,70 (3 Н), 2,20-2,25 (3 Н), 2,25-2,30 (3 Н), 4,80-4,90 (1 Н), 6,80-6,85 (1 Н), 7,007,10 (2 Н), 7,35-7,40 (2 Н). Альтернативный синтез. Смесь неочищенного соединения, полученного по способу 13 (500 мг, 2,3 ммоль), и палладия(10 мас.% на угле, 223 мг) в муравьиной кислоте (10 мл) нагревают при кипении с обратным холодильником в течение 36 ч. Реакционную смесь фильтруют, после чего фильтрат концентрируют в вакууме и получают указанное в заголовке соединение в неочищенном виде. Экспериментальное значение МН+ 201,3; ожидаемое значение 201,1. Пример 2. 2-1-[2-Метил-3-(трифторметил)фенил]этил-1 Н-имидазол Смесь соединения, полученного по способу 148 (2,0 г, 5,8 ммоль), и палладия (10 мас.% на угле,500 мг) в метаноле (25 мл) нагревают при 60 С в атмосфере водорода (150 фунт/кв.дюйм) в течение 24 ч. Смесь фильтруют через Arbocel, после чего фильтрат концентрируют в вакууме. Остаток очищают флэш-хроматографией (на оксиде кремния), элюируя метанолом. Соответствующие фракции объединяют и концентрируют, получая указанное в заголовке соединение (11 мг). 1 К раствору соединения, полученного по способу 167 (50 мг, 0,17 ммоль), в 2-пропаноле (2 мл) добавляют формиат аммония (105 мг, 1,67 ммоль) и палладий (10 мас.% на угле, 36 мг). Реакционную смесь нагревают при 80 С, в атмосфере азота в течение 2 ч и затем охлаждают. Смесь фильтруют черезArbocel и промывают 2-пропанолом, после чего фильтрат концентрируют в вакууме. Остаток растворяют в смеси ацетонитрил:вода (9:1, 4 мл) и очищают методом автоматизированной препаративной жидкостной хроматографии (система Gilson, колонка 150 мм 30 мм LUNA С 18(2) 10 мкм, 40 мл/мин), используя градиент ацетонитрил:вода [30:70 (20 мин) до 95:5 (21 мин)]. Соответствующие фракции объединяют и концентрируют, получая указанное в заголовке соединение (8 мг). Экспериментальное значение МН+ 212,1; ожидаемое значение 212,1. 1 К раствору соединения, полученного по способу 142 (100 мг, 0,32 ммоль), в 2-пропаноле (4 мл) добавляют формиат аммония (406 мг, 6,44 ммоль) и палладий (10 мас.% на угле, 137 мг). Реакционную смесь нагревают при 80 С в атмосфере азота в течение 18 ч и затем охлаждают. Смесь фильтруют черезArbocel, промывают 2-пропанолом и фильтрат концентрируют в вакууме. Остаток растворяют в смеси ацетонитрил:вода (9:1, 4 мл) и очищают методом автоматизированной препаративной жидкостной хроматографии (система Gilson, колонка 100 мм 30 мм LUNA С 18(2) 5 мкм, 40 мл/мин), используя градиент ацетонитрил:вода [от 40:60 (20 мин) до 95:5 (25 мин)]. Соответствующие фракции объединяют и концентрируют, получая указанное в заголовке соединение (8 мг). Экспериментальное значение МН+ 313,4; ожидаемое значение 313,2. 1 Н-ЯМР (d6-ацетон): 1,58-1,61 (3 Н), 4,25-4,31 (1 Н), 4,99-5,03 (1 Н), 5,10-5,14 (1 Н), 6,80-6,82 (1 Н),6,94-6,98 (3 Н), 7,00-7,02 (1 Н), 7,20-7,25 (3 Н), 7,38-7,41 (4 Н). Действие на Rhip. ED100 мкг/см 21. Подобным способом получают К раствору соединения, полученного по способу 136 (720 мг, 2,3 ммоль), в 2-пропаноле (20 мл) добавляют формиат аммония (1,0 г, 20 ммоль) и палладий (10 мас.% на угле, 300 мг). Реакционную смесь нагревают при 80 С в атмосфере азота в течение 72 ч и затем охлаждают. Смесь фильтруют черезArbocel и промывают 2-пропанолом, после чего фильтрат концентрируют в вакууме. Остаток растворяют в ацетонитриле (2 мл) и диэтиламине (2-3 капли) и очищают методом автоматизированной препаративной жидкостной хроматографии (система Gilson, 150 мм 50 мм LUNA С 18(2) АХ 5 мкм колонка, 40 мл/мин), используя градиент ацетонитрил:вода [от 40:60 (15 мин) до 95:5(15,5 мин)]. Соответствующие фракции объединяют и концентрируют, получая указанное в заголовке соединение (74 мг). Экспериментальное значение МН+ 229,3; ожидаемое значение 229,2. 1 Н-ЯМР (d6-ацетон): 0,95-1,00 (3 Н), 1,51-1,60 (5 Н), 2,13-2,15 (3 Н), 2,58-2,61 (2 Н), 4,47-4,52 (1 Н),6,85-6,90 (2 Н), 6,96-7,00 (3 Н). Действие на Rhip. ED100 мкг/см 210. Пример 16. 2-1-[2-(Трифторметил)фенил]этил-1 Н-имидазол Смесь соединения, полученного по способу 51 (212 мг, 0,88 ммоль), и палладия (10 мас.% на угле,500 мг) в метаноле (10 мл) нагревают при 60 С в атмосфере водорода (150 фунт/кв.дюйм) в течение 60 ч. Смесь фильтруют через Arbocel и фильтрат концентрируют в вакууме. Остаток растворяют в метаноле (2 мл) и диэтиламине (2-3 капли) и очищают методом автоматизированной препаративной жидкостной хроматографии (система Gilson, колонка 150 мм 50 мм LUNAC18(2), 10 мкм, 40 мл/мин), используя градиент ацетонитрил:вода [от 35:65 до 95:5]. Соответствующие фракции концентрируют в вакууме, получая указанное в заголовке соединение (58 мг). Экспериментальное значение МН+ 241,3; ожидаемое значение 241,1. 1 Смесь соединения, полученного по способу 64 (150 мг, 0,52 ммоль), и палладия (10 мас.% на угле,15 мг) в 2-пропаноле (5 мл) нагревают при 60 С в атмосфере водорода (200 фунт/кв.дюйм) в течение 18 ч. Смесь фильтруют через Arbocel, после чего фильтрат концентрируют в вакууме. Остаток растворяют в ацетонитриле (1,22 мл) и диэтиламине (2-3 капли) и очищают методом автоматизированной препаративной жидкостной хроматографии (система Gilson, колонка 150 мм 50 мм(21 мин)]. Соответствующие фракции объединяют и концентрируют, получая указанное в заголовке соединение (30 мг). Экспериментальное значение МН+ 215,4; ожидаемое значение 215,2. 1 Н-ЯМР (CD3OD): 1,57-1,60 (3 Н), 2,15-2,19 (6 Н), 2,20-2,22 (3 Н), 4,35-4,39 (1 Н), 6,80-6,82 (1 Н), 6,876,90 (3 Н). Действие на Rhip. ED100 мкг/см 21. Пример 33. 2-[1-(2,3-Диметилфенил)пропил]-1 Н-имидазол Смесь соединения, полученного по способу 47 (255 мг, 1,2 ммоль) и палладия (10 мас.% на угле, 50 мг) в 2-пропаноле (50 мл) нагревают при 40 С в атмосфере водорода (200 фунт/кв.дюйм) в течение 18 ч. Смесь фильтруют через Arbocel, после чего фильтрат концентрируют в вакууме. Остаток перекристаллизовывают из теплого диэтилового эфира (5 мл) и твердое вещество перетирают с дополнительной порцией диэтилового эфира (5 мл), получая указанное в заголовке соединение (175 мг). Экспериментальное значение МН+ 215,3; ожидаемое значение 215,2. 1 Смесь соединения, полученного по способу 67 (1,51 г, 6,8 ммоль), и гидроксид палладия (20 мас.%Pd на угле, 500 мг) в 2-пропаноле (100 мл) нагревают при 50 С в атмосфере водорода (200 фунт/кв.дюйм) в течение 18 ч. Смесь фильтруют через Arbocel, после чего фильтрат концентрируют в вакууме. Остаток растворяют в ацетонитриле (1 мл) и диэтиламине (2-3 капли) и очищают методом автоматизированной препаративной жидкостной хроматографии (система Gilson, колонка 100 мм 30 мм(15,5 мин)]. Соответствующие фракции объединяют и концентрируют, получая указанное в заголовке соединение (21 мг). Экспериментальное значение МН+ 221,3; ожидаемое значение 221,1. 1 Н-ЯМР (d6-ДМСО): 1,49-1,53 (3 Н), 2,34-2,37 (3 Н), 4,58-4,62 (1 Н), 6,79-6,81 (1 Н), 6,95-7,00 (2 Н),7,10-7,13 (1 Н), 7,18-7,20 (1 Н). Действие на Rhip. ED100 мкг/см 2=0,1. Подобным способом получают
МПК / Метки
МПК: C07D 233/54, C07D 405/12, A01P 7/02, A61P 33/00, C07D 417/04, A01P 7/04, A01N 43/50, C07D 403/12, C07D 417/12, C07D 413/12, C07D 401/12, A61K 31/4174
Метки: пестицидов, применение, замещенные, имидазолы, качестве
Код ссылки
<a href="https://eas.patents.su/30-15738-zameshhennye-imidazoly-i-ih-primenenie-v-kachestve-pesticidov.html" rel="bookmark" title="База патентов Евразийского Союза">Замещенные имидазолы и их применение в качестве пестицидов</a>
Предыдущий патент: Новые производные дигидропсевдоэритромицина
Следующий патент: Защитная крышка с предохранительным кольцом и индикацией вскрытия
Случайный патент: Машина для независящего от рядков скашивания кукурузы и иных подобных стеблевых культур












