Новые амидозамещённые гидрокси-6-фенилфенантридины
Номер патента: 12451
Опубликовано: 30.10.2009
Авторы: Феннеманн Маттиас, Беккерс Томас, Баер Томас, Дулльвебер Франк, Гиммних Петра, Майер Томас
Формула / Реферат
1. Соединения формулы I
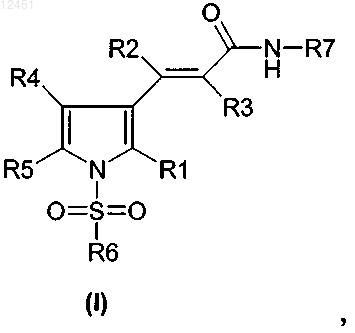
где R1 обозначает водород, С1-С4алкил, галоген или С1-С4алкоксигруппу,
R2 обозначает водород или С1-С4алкил,
R3 обозначает водород или С1-С4алкил,
R4 обозначает водород, С1-С4алкил, галоген или С1-С4алкоксигруппу,
R5 обозначает водород, С1-С4алкил, галоген или С1-С4алкоксигруппу,
R6 обозначает -T1-Q1, где
Т1 обозначает связь или С1-С4алкилен,
Q1 обозначает Ar1, Aa1, Hh1 или Ah1, где
Ar1 обозначает фенил или R61- и/или R62-замещенный фенил, где
R61 обозначает С1-С4алкил или -T2-N(R611)R612, где либо
Т2 обозначает связь и
R611 обозначает водород, С1-С4алкил, гидроксиС2-С4алкил, С1-С4алкоксиС2-С4алкил, фенилС1-С4алкил или Har1-С1-С4алкил, где
Har1 необязательно замещен R6111 и/или R6112 и обозначает моноциклическое или конденсированное бициклическое 5-10-членное ненасыщенное гетероароматическое кольцо, включающее от одного до трех гетероатомов, каждый из которых выбран из группы, состоящей из азота, кислорода и серы, где
R6111 обозначает галоген или С1-С4алкил,
R6112 обозначает С1-С4алкил, и
R612 обозначает водород, С1-С4алкил, С1-С4алкоксиС2-С4алкил или гидроксиС2-С4алкил,
или R611 и R612 вместе с атомом азота, к которому они присоединены, образуют гетероциклическое кольцо Het1, где
Het1 обозначает морфолиногруппу, тиоморфолиногруппу, S-оксотиоморфолиногруппу, S,S-диоксотиоморфолиногруппу, пиперидиногруппу, пирролидиногруппу, пиперазиногруппу или 4N-(C1-С4 алкил)пиперазиногруппу, либо
Т2 обозначает С1-С4алкилен или С2-С4алкилен с включенным в цепь атомом кислорода, и
R611 обозначает водород, С1-С4алкил, гидроксиС2-С4алкил, С1-С4алкокси-С2-С4алкил, фенилС1-С4алкил или Har1-С1-С4алкил, где
Har1 необязательно замещен R6111 и/или R6112 и обозначает моноциклическое или конденсированное бициклическое 5-10-членное ненасыщенное гетероароматическое кольцо, включающее от одного до трех гетероатомов, каждый из которых выбран из группы, состоящей из азота, кислорода и серы, где
R6111 обозначает галоген или С1-С4алкил,
R6112 обозначает С1-С4алкил и
R612 обозначает водород, С1-С4алкил, С1-С4алкоксиС2-С4алкил или гидроксиС2-С4алкил, или
R611 и R612 вместе с атомом азота, к которому они присоединены, образуют гетероциклическое кольцо Het1, где
Het1 обозначает морфолиногруппу, тиоморфолиногруппу, S-оксотиоморфолиногруппу, S,S-диоксотиоморфолиногруппу, пиперидиногруппу, пирролидиногруппу, пиперазиногруппу, 4N-(C1-С4алкил)пиперазиногруппу, имидазологруппу, пиррологруппу или пиразологруппу,
R62 обозначает С1-С4алкил, С1-С4алкоксигруппу, галоген, цианогруппу, С1-С4алкоксиС1-С4алкил, С1-С4алкилкарбониламиногруппу или С1-С4алкилсульфониламиногруппу,
Aa1 обозначает бисарильный радикал, состоящий из двух арильных групп, которые независимо выбраны из группы, включающей фенил и нафтил, и которые связаны между собой простой связью,
Hh1 обозначает бисгетероарильный радикал, состоящий из двух гетероарильных групп, которые независимо выбраны из группы, состоящей из моноциклических 5- или 6-членных гетероарильных радикалов, включающих один или два гетероатома, каждый из которых выбран из группы, состоящей из азота, кислорода и серы, и которые связаны между собой простой связью,
Ah1 обозначает гетероариларильный радикал или арилгетероарильный радикал, состоящий из гетероарильной группы, выбранной из группы, состоящей из моноциклических 5- или 6-членных гетероарильных радикалов, включающих один или два гетероатома, каждый из которых выбран из группы, состоящей из азота, кислорода и серы, и арильной группы, выбраннной из группы, состоящей из фенила и нафтила, при этом названные гетероарильная и арильная группы связаны между собой простой связью,
R7 обозначает гидроксил или Cyc1, где
Cyc1 обозначает кольцевую систему формулы Ia
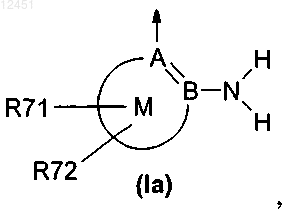
где
А обозначает С (углерод),
В обозначает C (углерод),
R71 обозначает водород, галоген, С1-С4алкил или С1-С4алкоксигруппу,
R72 обозначает водород, галоген, С1-С4алкил или С1-С4алкоксигруппу,
М с включенными А и В обозначает или кольцо Ar2, или кольцо Har2, где
Ar2 обозначает бензольное кольцо,
Har2 обозначает моноциклическое 5- или 6-членное ненасыщенное гетероароматическое кольцо, включающее от одного до трех гетероатомов, каждый из которых выбран из группы, состоящей из азота, кислорода и серы,
и соли этих соединений.
2. Соединения формулы I по п.1, где
R1 обозначает водород, С1-С4алкил, галоген или С1-С4алкоксигруппу,
R2 обозначает водород или С1-С4алкил,
R3 обозначает водород или С1-С4алкил,
R4 обозначает водород, С1-С4алкил, галоген или С1-С4алкоксигруппу,
R5 обозначает водород, С1-С4алкил, галоген или С1-С4алкоксигруппу,
R6 обозначает -T1-Q1, где
Т1 обозначает связь или С1-С4алкилен,
Q1 обозначает Ar1, Aa1, Hh1 или Ah1, где
Ar1 обозначает фенил или R61- и/или R62-замещенный фенил, где
R61 обозначает С1-С4алкил или -T2-N(R611)R612, где
Т2 обозначает связь, С1-С4алкилен или С2-С4алкилен с включенным в цепь атомом кислорода,
R611 обозначает водород, С1-С4алкил, гидроксиС2-С4алкил, C1-С4алкоксиС2-С4алкил, фенилС1-С4алкил или Har1-С1-С4алкил, где
Har1 необязательно замещен R6111 и/или R6112 и обозначает моноциклическое или конденсированное бициклическое 5-10-членное ненасыщенное гетероароматическое кольцо, включающее от одного до трех гетероатомов, каждый из которых выбран из группы, состоящей из азота, кислорода и серы, где
R6111 обозначает галоген или С1-С4алкил,
R6112 обозначает С1-С4алкил, и
R612 обозначает водород, С1-С4алкил, С1-С4алкоксиС2-С4алкил или гидроксиС2-С4алкил,
R62 обозначает С1-С4алкил, С1-С4алкоксигруппу, галоген, цианогруппу, С1-С4алкоксиС1-С4алкил, С1-С4алкилкарбониламиногруппу или С1-С4алкилсульфониламиногруппу,
Aa1 обозначает бисарильный радикал, состоящий из двух арильных групп, которые независимо выбраны из группы, состоящей из фенила и нафтила, и которые связаны между собой простой связью,
Hh1 обозначает бисгетероарильный радикал, состоящий из двух гетероарильных групп, которые независимо выбраны из группы, состоящей из моноциклических 5- шыш 6-членных гетероарильных радикалов, включающих один или два гетероатома, каждый из которых выбран из группы, состоящей из азота, кислорода и серы и которые связаны между собой простой связью,
Ah1 обозначает гетероариларильный радикал или арилгетероарильный радикал, состоящий из гетероарильной группы, выбранной из группы, состоящей из моноциклических 5- или 6-членных гетероарильных радикалов, включающих один или два гетероатома, каждый из которых выбран из группы, состоящей из азота, кислорода и серы, и арильной группы, выбраннной из группы, состоящей из фенила и нафтила, при этом названные гетероарильная и арильная группы связаны между собой простой связью,
R7 обозначает гидроксил или Cyc1, где
Cyc1 обозначает кольцевую систему формулы Ia
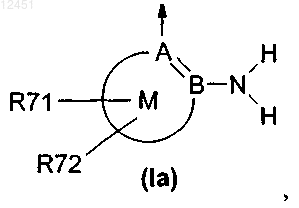
в которой
А обозначает С (углерод),
В обозначает С (углерод),
R71 обозначает водород, галоген, С1-С4алкил или С1-С4алкоксигруппу,
R72 обозначает водород, галоген, С1-С4алкил или С1-С4алкоксигруппу,
М с включенными А и В обозначает или кольцо Ar2, или кольцо Har2, где
Ar2 обозначает бензольное кольцо,
Har2 обозначает моноциклическое 5- или 6-членное ненасыщенное гетероароматическое кольцо, включающее от одного до трех гетероатомов, каждый из которых выбран из группы, состоящей из азота, кислорода и серы,
и соли этих соединений.
3. Соединения формулы I по п.1, где
R1 обозначает водород или C1-С4алкил,
R2 обозначает водород или С1-С4алкил,
R3 обозначает водород или С1-С4алкил,
R4 обозначает водород или С1-С4алкил,
R5 обозначает водород или С1-С4алкил,
R6 обозначает -T1-Q1, где
Т1 обозначает связь или С1-С4алкилен,
Q1 обозначает Ar1, Aa1, Hh1 или Ah1, где
Ar1 обозначает фенил или R61-замещенный фенил, где
R61 обозначает С1-С4алкил или -T2-N(R611)R612, где либо
Т2 обозначает связь,
R611 обозначает водород, С1-С4алкил,фенилС1-С4алкил или Har1-C1-С4алкил, где
Har1 обозначает или
моноциклическое 5-членное ненасыщенное гетероароматическое кольцо, включающее один, два или три гетероатома, каждый из которых выбран из группы, состоящей из азота, кислорода и серы, или
моноциклическое 6-членное ненасыщенное гетероароматическое кольцо, включающее один или два атома азота, или
конденсированное бициклическое 9-членное ненасыщенное гетероароматическое кольцо, включающее один, два или три гетероатома, каждый из которых выбран из группы, состоящей из азота, кислорода и серы, или
конденсированное бициклическое 10-членное ненасыщенное гетероароматическое кольцо, включающее один или два гетероатома, каждый из которых выбран из группы, состоящей из азота, кислорода и серы, и
R612 обозначает водород, С1-С4алкил или гидроксиС2-С4алкил,
или R611 и R612 вместе с атомом азота, к которому они присоединены, образуют гетероциклическое кольцо Het1, где
Het1 обозначает морфолиногруппу; либо
Т2 обозначает С1-С4алкилен,
R611 обозначает водород, С1-С4алкил, фенилС1-С4алкил или Har1-C1-С4алкил, где
Har1 обозначает или
моноциклическое 5-членное ненасыщенное гетероароматическое кольцо, включающее один, два или три гетероатома, каждый из которых выбран из группы, состоящей из азота, кислорода и серы, или
моноциклическое 6-членное ненасыщенное гетероароматическое кольцо, включающее один или два атома азота, или
конденсированное бициклическое 9-членное ненасыщенное гетероароматическое кольцо, включающее один, два или три гетероатома, каждый из которых выбран из группы, состоящей из азота, кислорода и серы, или
конденсированное бициклическое 10-членное ненасыщенное гетероароматическое кольцо, включающее один или два гетероатома, каждый из которых выбран из группы, состоящей из азота, кислорода и серы, и
R612 обозначает водород, С1-С4алкил или гидроксиС2-С4алкил, или
R611 и R612 вместе с атомом азота, к которому они присоединены, образуют гетероциклическое кольцо Het1, где
Het1 обозначает морфолиногруппу,
Aa1 обозначает бифенильный радикал,
Hh1 обозначает бипиридил, пиразолилпиридинил, имидазолилпиридинил или пиридинилтиофенил,
Ah1 обозначает пиридинилфенил, пиразолилфенил или имидазолилфенил,
R7 обозначает гидроксил или 2-аминофенил,
и соли этих соединений.
4. Соединения формулы I по п.1, где
R1 обозначает водород,
R2 обозначает водород,
R3 обозначает водород,
R4 обозначает водород,
R5 обозначает водород,
R6 обозначает -T1-Q1, Aa1, Hh1 или Ah1, где
Т1 обозначает связь или С1-С2алкилен,
Q1 обозначает Ar1, где
Ar1 обозначает фенил или R61-замещенный фенил, где
R61 обозначает С1-С4алкил или -T2-N(R611)R612, где либо
Т2 обозначает связь,
R611 обозначает водород, С1-С4алкил, фенилС1-С2алкил или Har1-C1-С2алкил, где
Har1 обозначает пиридинил, бензимидазолил, бензоксазолил, бензофуранил, бензотиофенил или индолил, и
R612 обозначает водород, С1-С4алкил или гидроксиС2-С3алкил,
или R611 и R612 вместе с атомом азота, к которому они присоединены, образуют гетероциклическое кольцо Het1, где
Het1 обозначает морфолиногруппу; либо
Т2 обозначает С1-С2алкилен,
R611 обозначает водород, С1-С4алкил, фенилС1-С2алкил или Har1-C1-С2алкил, где
Har1 обозначает пиридинил, бензимидазолил, бензоксазолил, бензофуранил, бензотиофенил или индолил, и
R612 обозначает водород, С1-С4алкил или гидроксиС2-С3алкил, или
R611 и R612 вместе с атомом азота, к которому они присоединены, образуют гетероциклическое кольцо Het1, где
Het1 обозначает морфолиногруппу,
Aa1 обозначает бифенильный радикал,
Hh1 обозначает бипиридил, пиразолилпиридинил, имидазолилпиридинил или пиридинилтиофенил,
Ah1 обозначает пиридинилфенил, пиразолилфенил или имидазолилфенил,
R7 обозначает гидроксил или 2-аминофенил,
и соли этих соединений.
5. Соединения формулы I по п.1, где
R1 обозначает водород,
R2 обозначает водород,
R3 обозначает водород,
R4 обозначает водород,
R5 обозначает водород,
R6 обозначает -T1-Q1, Aa1, Hh1, Ah1 или бензил, где
Т1 обозначает связь,
Q1 обозначает Ar1, где
Ar1 обозначает фенил или R61-замещенный фенил, где
R61 обозначает С1-С4алкил или -T2-N(R611)R612, где либо
Т2 обозначает связь,
R611 обозначает С1-С4алкил, и
R612 обозначает С1-С4алкил, либо
Т2 обозначает С1-С2алкилен,
R611 обозначает водород, C1-С4алкил, фенилС1-С2алкил или Har1-C1-С2алкил, где
Har1 обозначает пиридинил или индолил, и
R612 обозначает водород, С1-С4алкил или гидроксиС2-С3алкил, или
R611 и R612 вместе с атомом азота, к которому они присоединены, образуют гетероциклическое кольцо Het1, где
Het1 обозначает морфолиногруппу,
Aa1 обозначает 1,1'-бифен-4-ил или 1,1'-бифен-3-ил,
Hh1 обозначает пиридинилтиофенил,
Ah1 обозначает 3-(пиридинил)фенил, 3-(пиразолил)фенил, 4-(пиридинил)фенил или 4-(пиразолил)фенил,
R7 обозначает гидроксил или 2-аминофенил,
и соли этих соединений.
6. Соединения формулы I по п.1, где
R1 обозначает водород,
R2 обозначает водород,
R3 обозначает водород,
R4 обозначает водород,
R5 обозначает водород,
R6 обозначает -T1-Q1, Aa1, Hh1, Ah1 или бензил, где
Т1 обозначает связь,
Q1 обозначает Ar1, где
Ar1 обозначает фенил, 3-(R61)фенил или 4-(R61)фенил, где
R61 обозначает метил или -T2-N(R611)R612, где либо
Т2 обозначает связь,
R611 обозначает метил и
R612 обозначает метил, либо
Т2 обозначает метилен,
R611 обозначает водород, метил, изобутил, бензил, Har1-метил или 2-(Har1)этил, где
Har1 обозначает пиридинил или индолил, и
R612 обозначает водород, метил или 2-гидроксиэтил,
или R611 и R612 вместе с атомом азота, к которому они присоединены, образуют гетероциклическое кольцо Het1, где
Het1 обозначает морфолиногруппу,
Aa1 обозначает 1,1'-бифен-4-ил или 1,1'-бифен-3-ил,
Hh1 обозначает пиридинилтиофенильный радикал,
Ah1 обозначает 3-(пиридинил)фенил, 3-(пиразолил)фенил, 4-(пиридинил)фенил или 4-(пиразолил) фенил,
R7 обозначает гидроксил или 2-аминофенил,
и соли этих соединений.
7. Соединения формулы I по п.1, где
R1 обозначает водород,
R2 обозначает водород,
R3 обозначает водород,
R4 обозначает водород,
R5 обозначает водород,
R6 обозначает -T1-Q1, Aa1, Hh1, Ah1 или бензил, где
Т1 обозначает связь, Q1 обозначает Ar1, где
Ar1 обозначает фенил, 3-(R61)фенил или 4-(R61)фенил, где
R61 обозначает метил или -T2-N(R611)R612, где либо
Т2 обозначает связь,
R611 обозначает метил и
R612 обозначает метил, либо
Т2 обозначает метилен,
R611 обозначает водород, метил, изобутил, бензил, Har1-метил или 2-(Har1)этил, где
Har1 обозначает пиридин-3-ил, пиридин-4-ил, индол-2-ил, индол-3-ил или индол-5-ил, и
R612 обозначает водород, метил или 2-гидроксиэтил,
или R611 и R612 вместе с атомом азота, к которому они присоединены, образуют гетероциклическое кольцо Het1, где
Het1 обозначает морфолиногруппу,
Aa1 обозначает 1,1'-бифен-4-ил или 1,1'-бифен-3-ил,
Hh1 обозначает 5-(пиридин-2-ил)тиофен-2-ил,
Ah1 обозначает 3-(пиридин-3-ил)фенил, 3-(пиридин-4-ил)фенил, 3-(пиразол-1-ил)фенил, 3-(1Н-пиразол-4-ил)фенил, 4-(пиридин-3-ил)фенил, 4-(пиридин-4-ил)фенил, 4-(пиразол-1-ил)фенил или 4-(1Н-пиразол-4-ил)фенил,
R7 обозначает гидроксил или 2-аминофенил,
и соли этих соединений.
8. Соединения формулы I по п.1, где
R1 обозначает водород,
R2 обозначает водород,
R3 обозначает водород,
R4 обозначает водород,
R5 обозначает водород,
R6 обозначает -T1-Q1, Aa1, Hh1, Ah1 или бензил, где
Т1 обозначает связь,
Q1 обозначает Ar1, где
Ar1 обозначает фенил, 3-(R61)фенил или 4-(R61)фенил, где
R61 обозначает метил или -T2-N(R611)R612, где либо
Т2 обозначает связь,
R611 обозначает метил и
R612 обозначает метил, либо
Т2 обозначает метилен,
R611 обозначает водород, изобутил, бензил, Har1-метил или 2-(Har1)этил, где
Har1 обозначает пиридин-3-ил, пиридин-4-ил, индол-2-ил, индол-3-ил или индол-5-ил и
R612 обозначает водород, либо
Т2 обозначает метилен,
R611 обозначает метил или 2-(Har1)этил, где
Har1 обозначает индол-2-ил и
R612 обозначает метил, либо
Т2 обозначает метилен,
R611 обозначает 2-(Har1)этил, где
Har1 обозначает индол-2-ил и
R612 обозначает 2-гидроксиэтил, либо
Т2 обозначает метилен и
R611 и R612 вместе с атомом азота, к которому они присоединены, образуют гетероциклическое кольцо Het1, где
Het1 обозначает морфолиногруппу,
Aa1 обозначает 1,1'-бифен-4-ил или 1,1'-бифен-3-ил,
Hh1 обозначает 5-(пиридин-2-ил)тиофен-2-ил,
Ah1 обозначает 3-(пиридин-3-ил)фенил, 3-(пиридин-4-ил)фенил, 3-(пиразол-1-ил)фенил, 3-(1Н-пиразол-4-ил)фенил, 4-(пиридин-3-ил)фенил, 4-(пиридин-4-ил)фенил, 4-(пиразол-1-ил)фенил или 4-(1Н-пиразол-4-ил)фенил,
R7 обозначает гидроксил,
и соли этих соединений.
9. Соединения формулы I, где
R1 обозначает водород,
R2 обозначает водород,
R3 обозначает водород,
R4 обозначает водород,
R5 обозначает водород,
R6 обозначает -T1-Q1, Aa1, Hh1, Ah1 или бензил, где
Т1 обозначает связь,
Q1 обозначает Ar1, где
Ar1 обозначает фенил, 3-(R61)фенил или 4-(R61)фенил, где
R61 обозначает метил или -T2-N(R611)R612, где либо
Т2 обозначает связь,
R611 обозначает метил и
R612 обозначает метил, либо
Т2 обозначает метилен,
R611 обозначает водород, изобутил, бензил, Har1-метил или 2-(Har1)этил, где
Har1 обозначает пиридин-3-ил, пиридин-4-ил, индол-3-ил или индол-5-ил и
R612 обозначает водород, либо
Т2 обозначает метилен,
R611 обозначает метил или 2-(Har1)этил, где
Har1 обозначает индол-2-ил и
R612 обозначает метил, либо
Т2 обозначает метилен,
R611 обозначает 2-(Har1)этил, где
Har1 обозначает индол-2-ил и
R612 обозначает 2-гидроксиэтил, либо
Т2 обозначает метилен, и
R611 и R612 вместе с атомом азота, к которому они присоединены, образуют гетероциклическое кольцо Het1, где
Het1 обозначает морфолиногруппу,
Aa1 обозначает 1,1'-бифен-4-ил или 1,1'-бифен-3-ил,
Hh1 обозначает 5-(пиридин-2-ил)тиофен-2-ил,
Ah1 обозначает 3-(пиридин-3-ил)фенил, 3-(пиридин-4-ил)фенил, 3-(пиразол-1-ил)фенил, 3-(1Н-пиразол-4-ил)фенил, 4-(пиридин-3-ил)фенил, 4-(пиридин-4-ил)фенил, 4-(пиразол-1-ил)фенил или 4-(1Н-пиразол-4-ил)фенил,
R7 обозначает 2-аминофенил,
и соли этих соединений.
10. Соединения формулы I по п.1, где
R1 обозначает водород,
R2 обозначает водород,
R3 обозначает водород,
R4 обозначает водород,
R5 обозначает водород,
R6 обозначает -T1-Q1 или бифенил, где
Т1 обозначает связь или C1-С2алкилен,
Q1 обозначает Ar1, где
Ar1 обозначает фенил или R61-замещенный фенил, где
R61 обозначает С1-С4алкил или -T2-N(R611)R612, где
Т2 обозначает связь или С1-С2алкилен,
R611 обозначает водород, С1-С4алкил или Har1-С1-С2алкил, где
Har1 обозначает бензимидазолил или индолил,
R612 обозначает С1-С4алкил,
R7 обозначает гидроксил или 2-аминофенил,
и соли этих соединений.
11. Соединения формулы I по п.1, где
R1 обозначает водород,
R2 обозначает водород,
R3 обозначает водород,
R4 обозначает водород,
R5 обозначает водород,
R6 обозначает -T1-Q1, бифенил или бензил, где
Т1 обозначает связь,
Q1 обозначает Ar1, где
Ar1 обозначает R61-замещенный фенил, где
R61 обозначает метил, диметиламиногруппу или -T2-N(R611)R612, где
Т2 обозначает метилен,
R611 обозначает метил или 2-(индол-2-ил)этил,
R612 обозначает метил,
R7 обозначает гидроксил или 2-аминофенил,
и соли этих соединений.
12. Соединение формулы I по п.1, выбранное из группы:
1) (Е)-N-гидрокси-3-[1-(толуол-4-сульфонил)-1Н-пиррол-3-ил]акриламид;
2) N-гидрокси-3-(1-фенилметансульфонил-1Н-пиррол-3-ил)акриламид;
3) (Е)-3-[1-(бифенил-4-сульфонил)-1H-пиррол-3-ил]-N-гидроксиакриламид;
4) (Е)-3-[1-(4-диметиламинбензолсульфонил)-1Н-пиррол-3-ил]-N-гидроксиакриламид;
5) (Е)-N-(2-аминофенил)-3-[1-(толуол-4-сульфонил)-1Н-пиррол-3-ил]акриламид;
6) (Е)-N-(2-аминофенил)-3-(1-фенилметансульфонил-1Н-пиррол-3-ил)акриламид;
7) (Е)-N-(2-аминофенил)-3-[1-(бифенил-4-сульфонил)-1H-пиррол-3-ил]акриламид;
8) (Е)-N-(2-аминофенил)-3-[1-(4-диметиламинбензолсульфонил)-1Н-пиррол-3-ил]акриламид;
9) (Е)-N-гидрокси-3-(1-[4-(([2-(1H-индол-2-ил)этил]метиламино)метил)бензолсульфонил]-1Н-пиррол-3-ил)акриламид;
10) (Е)-3-[1-(4-диметиламинометилбензолсульфонил)-1H-пиррол-3-ил]-N-гидроксиакриламид;
11) (Е)-N-гидрокси-3-[1-(4-{[(пиридин-3-илметил)амино]метил}бензолсульфонил)-1Н-пиррол-3-ил]акриламид;
12) (Е)-N-гидрокси-3-[1-(4-{[(1Н-индол-3-илметил)амино]метил}бензолсульфонил)-1Н-пиррол-3-ил]акриламид;
13) (Е)-3-{1-[4-(бензиламинометил)бензолсульфонил]-1Н-пиррол-3-ил}-N-гидроксиакриламид;
14) (Е)-N-гидрокси-3-{1-[4-(изобутиламинометил)бензолсульфонил]-1Н-пиррол-3-ил}акриламид;
15) (Е)-N-гидрокси-3-[1-(4-{[(1H-индол-5-илметил)амино]метил}бензолсульфонил)-1Н-пиррол-3-ил]акриламид;
16) (Е)-N-гидрокси-3-[1-(4-{[(пиридин-4-илметил)амино]метил}бензолсульфонил)-1Н-пиррол-3-ил]акриламид;
17) (Е)-3-[1-(4-аминометилбензолсульфонил)-1H-пиррол-3-ил]-N-гидроксиакриламид;
18) (Е)-N-гидрокси-3-[1-(4-пиридин-4-илбензолсульфонил)-1H-пиррол-3-ил]акриламид;
19) (Е)-N-гидрокси-3-{1-[4-(1Н-пиразол-4-ил)бензолсульфонил]-1Н-пиррол-3-ил}акриламид;
20) (Е)-N-(2-аминофенил)-3-[1-(4-пиридин-4-илбензолсульфонил)-1H-пиррол-3-ил]акриламид;
21) (Е)-N-(2-аминофенил)-3-[1-(4-пиридин-3-илбензолсульфонил)-1H-пиррол-3-ил]акриламид;
22) (Е)-N-(2-аминофенил)-3-{1-[4-(1Н-пиразол-4-ил)бензолсульфонил]-1Н-пиррол-3-ил}акриламид;
23) (Е)-3-[1-(бифенил-3-сульфонил)-1Н-пиррол-3-ил]-N-гидроксиакриламид;
24) (Е)-N-гидрокси-3-[1-(5-пиридин-2-илтиофен-2-сульфонил)-1Н-пиррол-3-ил]акриламид;
25) (Е)-N-гидрокси-3-[1-(4-пиразол-1-илбензолсульфонил)-1Н-пиррол-3-ил]акриламид;
26) (Е)-N-(2-аминофенил)-3-[1-(5-пиридин-2-илтиофен-2-сульфонил)-1Н-пиррол-3-ил]акриламид;
27) (Е)-N-гидрокси-3-[1-(4-морфолин-4-илметилбензолсульфонил)-1H-пиррол-3-ил]акриламид;
28) (Е)-N-гидрокси-3-{1-[4-({(2-гидроксиэтил)-[2-(1Н-индол-2-ил)этил]амино}метил)бензолсульфонил]-1Н-пиррол-3-ил}акриламид;
29) (Е)-N-гидрокси-3-[1-(3-пиридин-4-илбензолсульфонил)-1Н-пиррол-3-ил]акриламид;
30) (Е)-N-(2-аминофенил)-3-[1-(3-пиридин-4-илбензолсульфонил)-1Н-пиррол-3-ил]акриламид;
31) (Е)-N-(2-аминофенил)-3-[1-(3-пиридин-3-илбензолсульфонил)-1Н-пиррол-3-ил]акриламид,
или его соль.
13. Фармацевтическая композиция, обладающая ингибирующим действием в отношении гистондеацетилазы, включающая одно или более соединений формулы I по п.1 вместе со стандартными фармацевтическими наполнителями и/или носителями.
14. Применение соединений формулы I по п.1 для получения фармацевтических композиций для лечения болезней, отвечающих на ингибирование или чувствительных к ингибированию активности гистондеацетилазы.
15. Применение соединений формулы I по п.1 для получения фармацевтических композиций для лечения доброкачественной и/или злокачественной неоплазии, такой, например, как рак.
16. Применение соединений формулы I по п.1 для получения фармацевтических композиций для лечения болезней, отличных от злокачественной неоплазии, таких, например, как заболевания суставов и остеопатологические состояния, системная красная волчанка, ревматоидный артрит, клеточная пролиферация гладкой мускулатуры, включая сосудистые пролиферативные заболевания, атеросклероз и рестеноз, или воспалительные состояния.
17. Способ лечения у пациента болезней, отвечающих на ингибирование или чувствительных к ингибированию активности гистондеацетилазы, включающий введение названному пациенту терапевтически эффективного и толерантного количества соединения формулы I по п.1.
18. Способ лечения доброкачественной и/или злокачественной неоплазии, такой, например, как рак, у пациента, включающий введение названному пациенту терапевтически эффективного и толерантного количества соединения формулы I по п.1, необязательно совместно, последовательно или раздельно с одним или более других терапевтических агентов.
19. Способ лечения незлокачественных болезней, таких, например, как заболевания суставов и остеопатологические состояния, системная красная волчанка, ревматоидный артрит, клеточная пролиферация гладкой мускулатуры, включая сосудистые пролиферативные заболевания, атеросклероз и рестеноз, или воспалительные состояния у пациента, включающий введение названному пациенту терапевтически эффективного и толерантного количества соединения формулы I по п.1, необязательно совместно, последовательно или раздельно с одним или более других терапевтических агентов.
Текст
012451 Область применения изобретения Изобретение относится к новым производным N-сульфонилпиррола, которые используются в фармацевтической индустрии для производства фармацевтических композиций. Известные технические предпосылки Регуляция транскрипции в клетках представляет собой сложный биологический процесс. Одним из основных ее принципов является регуляция посредством посттрансляционной модификации гистоновых белков, а именно, гистоновых белков H2 А/В, Н 3 и H4, образующих октамерный гистоновый ядерный комплекс. Эти комплексные N-концевые модификации, образующиеся при лизиновых остатках посредством ацетилирования или метилирования, а при сериновых остатках - посредством фосфорилирования,составляют часть так называемого гистонового кода (StrahlEllis, Nature 403, 41-45, 2000). В простой модели ацетилирование положительно заряженных лизиновых остатков увеличивает сродство к отрицательно заряженной ДНК, которая благодаря этому становится доступной для входа факторов транскрипции. Гистоновое ацетилирование и деацетилирование катализируется гистонацетилтрансферазамиal. Nature Cancer Rev. 1, 194-202, 2001). Противоположной точки зрения придерживаются относительноHATs, которые ассоциируются с транскрипционно активными комплексами. В настоящее время описаны три различных класса HDACs, а именно, класс 1 (HDAC 1-3, 8) с молекулярной массой 42-55 кДа, главным образом, локализованный в ядре, и чувствительный в отношении ингибирования посредством трихостатина A (TSA), класс II (HDAC 4-7, 9, 10) с молекулярной массой 120-130 кДа и TSAвосприимчивостью, и класс III (Sir2 гомологи), который полностью отличен от предыдущих благодаря своей NAD+-зависимости и TSA-невосприимчивости (Ruijter et al. Biochem. J. 370, 737-749, 2003; Khochbin et al. Curr. Opin. Gen. Dev. 11, 162-166, 2001; Verdin et; al. Trends Gen. 19, 286-293, 2003). HDAC 11 с молекулярной массой 39 кДа недавно клонирован и является гомологичным по отношению к членам семейства классов I и II (Gao et al. J. Biol. Chem. 277, 25748-25755, 2002). HATs и HDACs существуют в больших комплексах вместе с фактором транскрипции и платформенными белками (Fischle et al. MolCell 9, 45-47, 2002). Неожиданно оказалось, что только около 2% всех генов регулируются посредством гистонацетилирования (von Lint et al. Gene Expression 5, 245-253, 1996). Новые исследования, проведенные с SAHA (субероиланилид гидроксамовой кислоты) в клетках мультиплетной миеломы, показали, что эти транскрипционные изменения могут быть сгруппированы в различных функциональных генетических классах, важных, например, для регуляции апоптоза или пролиферации (Mitsiades et al. Proc. Natl.Acad. Sci. 101, pp. 540, 2004). Существуют субстраты, отличающиеся от гистоновых белков. Для HDACs они включают транскрипционные факторы, подобные р 53 и TFII Е, или шапероны, подобные Hsp90 (JohnstoneLicht, Cancer Cell 4, 13-18, 2003). Поэтому правильным названием для HDACs может быть лизин-специфичные протеиндеацетилазы. Исходя из этих данных, ингибиторы HDACs воздействуют не только на структуру хроматина и генную транскрипцию, но также и на белковую функцию и стабильность посредством регулирования ацетилирования белка в общем. Эта функция HDACs в ацетилировании белка может быть также важной для понимания немедленной генной репрессии при обработке посредством HDIs (von Lintet al. Gene Expression 5, 245-253, 1996). В этом отношении белки, включаемые в онкогенную трансформацию и злокачественный рост клеток, имеют особое значение. Различные публикации отмечают важность гистонацетилирования в развитии рака (обзор Kramer et(ii) отклоняющийся от нормы рекрутмент HDAC1 активности вследствие транскрипционных факторов при остром промиелоцитарном лейкозе (APL) посредством рецепторагенного слияния PMLретиноевой кислоты (Не et al. Nat. Genet. 18, 126-135, 1998);(iii) отклоняющийся от нормы рекрутмент HDAC активности вследствие сверхэкспрессирующегоBCL6 белка в не-Ходжкинской лимфоме (Dhordain et al. Nuceic Acid. Res. 26, 4645-4651, 1998) и, наконец,(iv) отклоняющийся от нормы рекрутмент HDAC активности вследствие образования AML-ETO гибридного белка при остром миелолейкозе (AML М 2 подтип; Wang et al. Proc. Natl. Acad. Sci. USA 95,10860-10865, 1998). В этом AML подтипе рекрутмент HDAC1 активности является причиной, приводящей к генному сайленсингу, блокированию дифференцировки и онкогенной трансформации;(v) HDAC1 нокаутированного гена мыши показал, что HDAC1 основательно функционирует при пролиферации эмбриональных стволовых клеток посредством регрессирующих циклинзависимых ингибиторов киназы p21wafl и p27kipl (Lagger et al. Embo J. 21, 2672-2681, 2002). Поскольку р 21wafl индуцируется с помощью HDIs во многих линиях раковых клеток, HDAC1 может быть также решающим компонентом в пролиферации раковых клеток. Первичная siPHK, возникающая в экспериментах с нокдауном ге-1 012451 нов в HeLa клетках, подтверждает эту гипотезу (Glaser et al. 310, 529-536, 2003);(vi) HDAC2 сверхэкспрессирует при карциноме толстой кишки при активации wnt/-катенин/TCF пути передачи сигнала посредством потери белка при функциональном аденоматозном полипозе coli(APC) белка, как было сообщено недавно Zhu et al. (Cancer Cell 5, 455-463, 2004). На молекулярном уровне обзор опубликованных данных по различным HDAC ингибиторам, подобным трихостатину A(TSA), показал, что многие релевантные к раку гены могут положительно (up) или отрицательно (down) регулироваться. Они включают р 21CIP1, циклин Е, трансформирующий фактор роста(TGF), р 53 илиvon Hippel-Lindau (VHL) гены-супрессоры опухоли, которые являются положительно регулируемыми, в то время как Bcl-XL, bcl2, гипоксия-индуцируемый фактор (HIF)1, васкулярный эндотелиальный фактор роста (VEGF) и циклин A/D являются отрицательно регулируемыми посредством HDAC ингибирования (обзор Kramer et al. Trends Endocrin. Metabol. 12, 294-300, 2001). HDAC ингибиторы задерживают клетки при G1 и G2/M внутри клеточного цикла и инактивируют клетки S-фазы, как показано на примере депсипеитида (Sandor et al., British J. Cancer 83, 817-825, 2000). HDAC ингибиторные соединения индуцируют р 53 и caspase3/8 независимый апоптоз и проявляют широкую антиопухолевую активность. Описана также антиангиогенная активность, которая может быть отнесена к отрицательной регуляцииVEGF и HIF1. В целом, HDAC ингибирование воздействует на опухолевые клетки на различных молекулярных уровнях и направлено на многочисленные клеточные белки. Интересным оказалась найденная способность HDAC ингибиторов инициировать клеточную дифференцировку, и эта фармакологическая активность может способствовать также их противораковой активности. Недавно, например, было показано, что субероиланилид гидроксамовой кислоты (SAHA) индуцирует дифференцировку клеточных линий рака молочной железы, например, посредством ресинтеза мембранного глобулярного белка молочного жира (MFMG), молочного жирового глобулярного белка и липида (Munster et al. Cancer Res. 61, 8492, 2001). Можно отметить возрастающий рациональный подход к совместному действию HDAC ингибиторов и химиотерапии, а также с избирательно направленными против рака лекарствами. Например, совместное действие было обнаружено для SAHA с киназа/cdk ингибитором флавопиридолом (Alemenara et al.Leukemia 16, 1331-1343, 2002), для LAQ-824 с bcr-abl киназа ингибитором гливек в CML клетках (Nimmanapalli et al. Cancer Res. 63, 5126-5135, 2003) и для SAHA и трихостатина A (TSA) с этопозидом(VP16), цисплатина и доксорубицина (Kim et al. Cancer Res. 63, 7291-7300, 2003) и LBH589 с hsp90 ингибитором 17-аллиламино-деметокси-гелдамицином (17-AAG; George et al. Blood online, Oct.28, 2004). Было показано также, что HDAC ингибирование вызывает реэкспрессию рецепторов эстрогена или андрогена в раковых клетках грудной железы и простаты с потенциальным возвращением этих опухолей к антигормональной терапии (Yang et al. Cancer Res. 60, 6890-6894, 2000; Nakayama et al. Lab. Invest. 80,1789-1796, 2000). В литературе описаны HDAC ингибиторы различных классов химических соединений, из которых наибольшее значение представляют четыре класса, а именно: (i) аналоги гидроксамовых кислот, (ii) аналоги бензамида, (iii) циклические пептиды/пептолиды и (iv) аналоги жирных кислот. Недавно опубликован исчерпывающий обзор HDAC ингибиторов (Miller et al. J Med Chem 46, 5097-5116, 2003). Относительно специфичности ингибиторов гистондеацетилазы имеется ограниченное число публикаций. В общем, большинство HDI на основе гидроксаматов не специфичны в отношении класса I и II HDAC ферментов. Например, TSA ингибирует HDACs 1, 3, 4, 6 и 10 с величиной IC50 около 20 нМ, в то время, какHDAC8 ингибируется с IC50 0,49 мкМ (Tatamiya et al., AACR Annual Meeting 2004, Abstract 2451). Но существуют исключения, подобные экспериментальному HDI тубацину, селективному по отношению к классу II фермента HDAC 6 (Haggarty et al. Proc. Natl. Acad. Sci. USA 100, 4389-4394, 2003). Кроме того,появляются данные о селективности бензамидных HDIs относительно класса I. MS-275 ингибирует классAnnual Meeting 2004, Abstract 2451). Пока не ясно, действительно ли специфичность в отношенииHDAC класса I или II ферментов или определенного единственного изофермента является лучшей в смысле терапевтической эффективности и индексирования. Продолжаются клинические исследования рака с использованием таких HDAC ингибиторов, как:(Berlex-Schering), NVP LBH-589 (Novartis), PXD-101 (Topotarget/Curagen), MGCD0103 (methylgene Inc.) и пивалоилоксиметилбутират / Pivanex (Titan Pharmaceuticals). Эти исследования послужили первым доказательством клинической эффективности и в последнее время вышли вперед благодаря получению частичных или полных ответов при использовании FK228/депсипептида у пациентов с периферической Тклеточной лимфомой (Plekarz et al. Blood, 98, 2865-2868, 2001). В последних публикациях также показана возможность применения HDAC ингибиторов в лечении болезней, отличных от рака. Эти болезни включают системную красную волчанку (Mishra et al. J Clinal. Mol. Therapy 8, 707-717, 2003; Nishida et al. ArthritisRheumatology 50, 3365-3376, 2004), воспали-2 012451 тельные болезни (Leoni et al. Proc. Natl. Acad. Sci. USA 99, 2995-3000, 2002) и нейродегенеративные болезни, подобные болезни Хантингтона (Steffan et al. Nature 413, 739-743, 2001, Hockly et al. Proc. Natl.Acad. Sci. USA 100(4):2041-6, 2003). Противораковая химиотерапия основана на концепции предпочтительного уничтожения раковых клеток с неконтролируемой пролиферацией и пропорционального высокого содержания клеток в митозе. Стандартные лекарства противораковой химиотерапии в конце концов убивают раковые клетки благодаря стимуляции запрограммированной клеточной смерти (апоптоза) посредством направленного действия на основные клеточные процессы и молекулы, а именно на: РНК/ДНК (алкилирующие и карбамилирующие агенты, аналоги платины и ингибиторы топоизомеразы), метаболизм (лекарства этого класса называются антиметаболитами), а также митотический веретенообразный аппарат (ингибиторы стабилизации и дестабилизации трубочек). Ингибиторы гистондеацетилазы (HDIs) составляют новый класс противораковых лекарств с активностью, индуцирующую дифференцировку и апоптоз. Посредством целенаправленного действия на гистондеацетилазу, HDIs оказывают воздействие на гистон (белок) ацетилирование и структуру хроматина, включая комплекс транскрипционного репрограммирования, иллюстрируемого реактивацией опухолевых супрессорных генов и репрессией онкогенов. Помимо воздействия на ацетилирование N-концевых лизиновых остатков в ядерных гистоновых белках, существуют негистоновые мишени, важные для биологии раковых клеток, подобные хитшоковому белку 90 (Hsp90) или р 53 опухолевому супрессорному белку. Медицинское применение HDIs не ограничивается раковой терапией, поскольку обнаружена их эффективность на моделях воспалительных заболеваний, ревматоидного артрита и нейродегенеративных болезней. Известный уровень техники Бензоил или ацетилзамещенные пирролилпропенамиды описаны в публикациях в качестве HDAC ингибиторов, где ацильная группа находится в положении 2 или 3 пиррольного кольца. (Mai etal., JournalMed.Chem. 2004, Vol. 47, No. 5, 1098-1109). Далее в патенте US 4960787 описаны производные пирролилзамещенных гидроксамовых кислот в качестве ингибиторов липоксигеназы или в патенте US 6432999 в качестве ингибиторов циклооксигеназы. Различные соединения, которые, как отмечено, являются HDAC ингибиторами, приведены в WO 01/38322; Journal Med. Chem. 2003, Vol. 46, No. 24, 5097-5116; Journal Med. Chem. 2003, Vol. 46, No. 4,512-524; Journal Med. Chem. 2003, Vol. 46, No. 5, 820-830; и в Current Opinion Drug Discovery 2002, Vol. 5,487-499. Однако остается необходимость в разработке новых, достаточно толерантных и более эффективных ингибиторов HDACs. Описание изобретения Было найдено, что производные N-сульфонилпиррола, более подробно описанные ниже, существенно отличаются от известных из уровня техники соединений и являются эффективными ингибиторами гистондеацетилазы и обладают неожиданными и особенно перспективными свойствами. Изобретение относится, таким образом, в первом аспекте (аспект 1) к соединениям формулы I где R1 обозначает водород, С 1-С 4 алкил, галоген или С 1-С 4 алкоксигруппу,R2 обозначает водород или С 1-С 4 алкил,R3 обозначает водород или С 1-С 4 алкил,R4 обозначает водород, С 1-С 4 алкил, галоген или С 1-С 4 алкоксигруппу,R5 обозначает водород, С 1-С 4 алкил, галоген или С 1-С 4 алкоксигруппу,R6 обозначает -T1-Q1, где Т 1 обозначает связь или С 1-С 4 алкилен,Q1 обозначает Ar1, Aa1, Hh1 или Ah1, гдеAr1 обозначает фенил или R61- и/или R62-замещенный фенил, гдеHar1 необязательно замещен R6111 и/или R6112, и обозначает моноциклическое или конденсированное бициклическое 5-10-членное ненасыщенное гетероароматическое кольцо, включающее от одного до трех гетероатомов, каждый из которых выбран из группы, состоящей из азота, кислорода и серы, вR6111 обозначает галоген или С 1-С 4 алкил,R6112 обозначает С 1-С 4 алкил, иR612 обозначает водород, С 1-С 4 алкил, С 1-С 4 алкоксиС 2-С 4 алкил или гидроксиС 2-С 4 алкил, илиR611 и R612 вместе с атомом азота, к которому они присоединены, образуют гетероциклическое кольцо Het1, гдеHar1 не обязательно замещен R6111 и/или R6112, и обозначает моноциклическое или конденсированное бициклическое 5-10-членное ненасыщенное гетероароматическое кольцо, включающее от одного до трех гетероатомов, каждый из которых выбран из группы, состоящей из азота, кислорода и серы, гдеR6111 обозначает галоген или С 1-С 4 алкил,R6112 обозначает С 1-С 4 алкил, иR612 обозначает водород, С 1-С 4 алкил, С 1-С 4 алкоксиС 2-С 4 алкил или гидроксиС 2-С 4 алкил, илиR611 и R612 вместе с атомом азота, к которому они присоединены, образуют гетероциклическое кольцо Het1, гдеHet1 обозначает морфолиногруппу, тиоморфолиногруппу, S-оксотиоморфолиногруппу, S,S-диоксотиоморфолиногруппу, пиперидиногруппу, пирролидиногруппу, пиперазиногруппу, 4N-(C1-С 4 алкил)пиперазиногруппу, имидазологруппу, пиррологруппу или пиразологруппу,R62 обозначает С 1-С 4 алкил, С 1-С 4 алкоксигруппу, галоген, цианогруппу, С 1-С 4 алкоксиС 1-С 4 алкил,С 1-С 4 алкилкарбониламиногруппу или С 1-С 4 алкилсульфониламиногруппу,Aa1 обозначает бисарильный радикал, состоящий из двух арильных групп, которые независимо выбраны из группы, состоящей из фенила и нафтила, и которые связаны между собой простой связью,Hh1 обозначает бисгетероарильный радикал, состоящий из двух гетероарильных групп, которые независимо выбраны из группы, состоящей из моноциклических 5- или 6-членных гетероарильных радикалов, включающих один или два гетероатома, каждый из которых выбран из группы, состоящей из азота,кислорода и серы, и которые связаны между собой простой связью,Ah1 обозначает гетероариларильный или арилгетероарильный радикалы, включающие гетероарильную группу, выбранную из группы, состоящей из моноциклических 5- или 6-членных гетероарильных радикалов, включающих один или два гетероатома, каждый из которых выбран из группы, состоящей из азота, кислорода и серы, и арильная группа выбрана из группы, состоящей из фенила и нафтила,при этом названные гетероарильная и арильная группы связаны между собой простой связью,R7 обозначает гидроксил или Cycl, гдеCycl обозначает кольцевую систему формулы Ia в которой А обозначает С (углерод),В обозначает С (углерод),R71 обозначает водород, галоген, С 1-С 4 алкил или С 1-С 4 алкоксигруппу,R72 обозначает водород, галоген, С 1-С 4 алкил или С 1-С 4 алкоксигруппу,М с включенными А и В обозначает или кольцо Ar2, либо кольцо Har2, где Аr2 обозначает бензольное кольцо,Наr2 обозначает моноциклическое 5- или 6-членное ненасыщенное гетероароматическое кольцо,включающее от одного до трех гетероатомов, каждый из которых выбран из группы, состоящей из азота,кислорода и серы,и солям этих соединений. Изобретение относится во втором аспекте (аспект 2) к соединениям формулы I, гдеR1 обозначает водород, С 1-С 4 алкил, галоген или С 1-С 4 алкоксигруппу,R2 обозначает водород или С 1-С 4 алкил,R3 обозначает водород или С 1-С 4 алкил,R4 обозначает водород, С 1-С 4 алкил, галоген или С 1-С 4 алкоксигруппу,R5 обозначает водород, С 1-С 4 алкил, галоген или С 1-С 4 алкоксигруппу,R6 обозначает -T1-Q1, где-4 012451 Т 1 обозначает связь или С 1-С 4 алкилен,Q1 обозначает Ar1, Aa1, Hh1 или Ah1, гдеAr1 обозначает фенил или R61- и/или R62-замещенный фенил, гдеHar1 необязательно замещен R6111 и/или R6112, и обозначает моноциклическое или конденсированное бициклическое 5-10-членное ненасыщенное гетероароматическое кольцо, включающее от одного до трех гетероатомов, каждый из которых выбран из группы, состоящей из азота, кислорода и серы, гдеR6111 обозначает галоген или С 1-С 4 алкил,R6112 обозначает С 1-С 4 алкил, иR612 обозначает водород, С 1-С 4 алкил, С 1-С 4 алкоксиС 2-С 4 алкил или гидроксиС 2-С 4 алкил,R62 обозначает С 1-С 4 алкил, С 1-С 4 алкоксигруппу, галоген, цианогруппу, C1-С 4 алкоксиС 1-С 4 алкил,С 1-С 4 алкилкарбониламиногруппу или С 1-С 4 алкилсульфониламиногруппу,Aa1 обозначает бисарильный радикал, состоящий из двух арильных групп, которые независимо выбраны из группы, состоящей из фенила и нафтила, и которые связаны между собой простой связью,Hh1 обозначает бисгетероарильный радикал, состоящий из двух гетероарильных групп, которые независимо выбраны из группы, состоящей из моноциклических 5- или 6-членных гетероарильных радикалов, включающих один или два гетероатома, каждый из которых выбран из группы, состоящей из азота,кислорода и серы, и которые связаны между собой простой связью,Ah1 обозначает гетероариларильный или арилгетероарильный радикалы, включающие гетероарильную группу, выбранную из группы, состоящей из моноциклических 5- или 6-членных гетероарильных радикалов, включающих один или два гетероатома, каждый из которых выбран из группы, состоящей из азота, кислорода и серы, и арильная группа выбрана из группы, состоящей из фенила и нафтила,при этом названные гетероарильная и арильная группы связаны между собой простой связью,R7 обозначает гидроксил или Cyc1, гдеCyc1 обозначает кольцевую систему формулы Ia в которой А обозначает С (углерод),В обозначает С (углерод),R71 обозначает водород, галоген, С 1-С 4 алкил или С 1-С 4 алкоксигруппу,R72 обозначает водород, галоген, С 1-С 4 алкил или С 1-С 4 алкоксигруппу,М с включенными А и В обозначает или кольцо Ar2, либо кольцо Har2, гдеAr2 обозначает бензольное кольцо,Har2 обозначает моноциклическое 5- или 6-членное ненасыщенное гетероароматическое кольцо,включающее от одного до трех гетероатомов, каждый из которых выбран из группы, состоящей из азота,кислорода и серы,и солям этих соединений. С 1-С 4 алкил представляет собой линейный или разветвленный алкильный радикал, содержащий от 1 до 4 атомов углерода. В качестве примеров могут быть отмечены бутильный, изобутильный, вторбутильный, трет-бутильный, пропильный, изопропильный и, предпочтительно, этильный и метильный радикалы. С 2-С 4 алкил представляет собой линейный или разветвленный алкильный радикал, содержащий от 2 до 4 атомов углерода. В качестве примеров могут быть отмечены бутильный, изобутильный, вторбутильный, трет-бутильный, пропильный, изопропильный и, предпочтительно, этильный и пропильный радикалы. С 1-С 4 алкилен представляет собой разветвленный или, прежде всего, линейный алкиленовый радикал, содержащий от 1 до 4 атомов углерода. В качестве примеров могут быть названы метиленовый(-СН 2-), этиленовый (-СН 2-СН 2-), триметиленовый (-СН 2-СН 2-СН 2-) и тетраметиленовый (-СН 2-СН 2-СН 2 СН 2-) радикалы. С 2-С 4 алкилен, включающий атом кислорода, представляет собой линейный алкиленовый радикал,имеющий от 1 до 4 атомов углерода, и соответственно включающий в цепь кислородный атом, например, такой, как [-СН 2-СН 2-О-СН 2-СН 2-] радикал. С 1-С 4 алкоксигруппа представляет собой радикал, который кроме атома кислорода содержит линейный или разветвленный алкильный радикал, содержащий от 1 до 4 атомов углерода. Примерами могут-5 012451 служить бутоксирадикал, изобутоксирадикал, втор-бутоксирадикал, трет-бутоксирадикал, пропоксирадикал, изопропоксирадикал и, предпочтительно, этоксирадикал и метоксирадикал. С 1-С 4 алкоксиС 1-С 4 алкил представляет собой один из упомянутых выше С 1-С 4 алкильных радикалов,замещенных одним из названных выше С 1-С 4 алкоксирадикалов. Примерами могут служить метоксиметильный, метоксиэтильный и изопропоксиэтильный радикалы, в частности, 2-метоксиэтильный и 2 изопропоксиэтильный радикалы. С 1-С 4 алкоксиС 2-С 4 алкил представляет собой один из упомянутых выше С 2-С 4 алкильных радикалов,замещенных одним из названных выше С 1-С 4 алкоксирадикалов. Примерами могут служить метоксиэтильный, этоксиэтильный и изопропоксиэтильный радикалы, в частности, 2-метоксиэтильный, 2 этоксиэтильный и 2-изопропоксиэтильный радикалы. ГидроксиС 2-С 4 алкил представляет собой один из упомянутых выше С 2-С 4 алкильных радикалов, замещенных гидроксирадикалом. Примерами могут служить 2-гидроксиэтильный или 3-гидроксипропильный радикалы. Фенил C1-С 4 алкил представляет собой один из упомянутых выше С 1-С 4 алкильных радикалов, замещенных фенильным радикалом. Примерами могут служить бензильный и фенэтильный радикалы. Галоген в рамках изобретения обозначает бром, в особенности, хлор и фтор.C1-С 4 алкилкарбонил представляет собой радикал, содержащий кроме карбонильной группы один из упомянутых выше С 1-С 4 алкильных радикалов. Примером может служить ацетильный радикал. С 1-С 4 алкилкарбониламиногруппа представляет собой аминорадикал, замещенный одним из упомянутых выше С 1-С 4 алкилкарбонильных радикалов. Примером может служить ацетамидорадикалAa1 обозначает бисарильный радикал, состоящий из двух арильных групп, которые независимо выбраны из группы, состоящей из фенила и нафтила, и которые связаны между собой простой связью. Aa1 может включать, не ограничивая при этом, например, 1,1-бифенил-4-ил или 1,1-бифенил-3-ил.Hh1 обозначает бисгетероарильный радикал, состоящий из двух гетероарильных групп, которые независимо выбраны из группы, состоящей из моноциклических 5- или 6-членных гетероарильных радикалов, включающих один или два гетероатома, каждый из которых выбран из группы, состоящей из азота,кислорода и серы, и которые связаны между собой простой связью.Hh1 может включать, не ограничивая при этом, битиофенил, бипиридил, пиразолилпиридинил (в частности, пиразол-1-илпиридинил), имидазолилпиридинил (в частности, имидазол-1-илпиридинил) или пиридинилтиофенил, например, 5-(пиридин-2-ил)тиофен-2-ил радикал. Более конкретно примеры Hh1 радикалов могут включать пиридинилтиофенил, например, 5(пиридин-2-ил)тиофен-2-ил.Ah1 обозначает гетероариларильный или арилгетероарильный радикалы, включающие гетероарильную группу, выбранную из группы, состоящей из моноциклических 5- или 6-членных гетероарильных радикалов, включающих один или два гетероатома, каждый из которых выбран из группы, состоящей из азота, кислорода и серы, и арильная группа выбрана из группы, состоящей из фенила и нафтила,при этом названные гетероарильная и арильная группы связаны между собой простой связью.Ah1 радикал может быть присоединен к исходной молекулярной группе либо через названный гетероарильный, либо через названный арильный фрагменты. Особые варианты Ah1 радикалов относятся к гетероарилфенильным радикалам, например, 3(гетероарил)фенильному или 4-(гетероарил)фенильному радикалу.Ah1 может включать, не ограничивая при этом, фенилтиофенильный или фенилпиридильнй радикалы. Альтернативно, Ah1 может включать, не ограничивая при этом, фуранилфенильный, пиразолилфенильный (например, пиразол-1-илфенил или 1 Н-пиразол-4-илфенил), имидазолилфенильный (например,имидазол-1-илфенил) или пиридинилфенильный радикалы. Конкретно, примеры Ah1 радикалов могут включать 3-(пиразолил)фенил, 4-(пиразолил)фенил, 4(пиридинил)фенил или 3-(пиридинил)фенил. Более конкретно, примеры Ah1 радикалов могут включать 3-(пиразол-1-ил)фенил, 4-(пиразол-1-ил) фенил, 4-(пиридин-4-ил)фенил, 3-(пиридин-4-ил)фенил, 4-(пиридин-3-ил)фенил, 3-(пиридин-3-ил)фенил,3-(1 Н-пиразол-4-ил)фенил или 4-(1 Н-пиразол-4-ил)фенил. Установлено, что каждый из радикалов Hh1 и Ah1 связан с фрагментом Т 1 предпочтительно через углеродный атом кольца.Har1 не обязательно замещен R6111 и/или R6112, и обозначает моноциклический или конденсированный бициклический 5-10-членный ненасыщенный (гетероароматический) гетероарильный радикал,включающий от одного до трех гетероатомов, каждый из которых выбран из группы, состоящей из азота,кислорода и серы. Конкретно, следует упомянуть конденсированные, в частности, конденсированные с бензолом, бициклические 9- или 10-членные гетероарильные радикалы, включающие от одного до трех,-6 012451 особенно, один или два гетероатома, каждый из которых выбран из группы, состоящей из азота, кислорода и серы. Примеры Har1 включают, не ограничивая, тиофенил, фуранил, пирролил, оксазолил, изоксазолил, пиразолил, имидазолил, тиазолил, изотиазолил, триазолил, оксадиазолил, тиадиазолил, пиридинил, пиримидинил, пиразинил или пиридазинил; и, в частности, их стабильные бензоконденсированные производные такие, как бензотиофенил, бензофуран, индолил, бензоксазолил, бензотиазолил, индазолил, бензимидазолил, бензизоксазолил, бензизотиазолил, бензофуразонил, хинолинил, изохинолинил,хиназолинил, хиноксалинил, фталазинил или циннолинил; и пуринил, индолизинил, нафтиридинил или птеридинил. Конкретно, примеры Har1 радикалов могут включать пиридинил, бензимидазолил, бензоксазолил,бензофуранил, бензотиофенил и индолил, такие как, например, пиридин-2-ил, пиридин-3-ил, пиридин-4 ил, бензимидазол-2-ил, бензоксазол-2-ил, бензофуран-2-ил, бензофуран-3-ил, бензотиофен-2-ил, бензотиофен-3-ил, индол-2-ил, индол-3-ил или индол-5-ил. Конкретнее, примером Har1 радикала может быть индолил такой, как, например, индол-2-ил, индол-3-ил или индол-5-ил. Еще конкретнее, примером Har1 радикала может быть пиридинил такой, как, например, пиридин-2 ил, пиридин-3-ил или пиридин-4-ил. В качестве дополнительных примеров Har1 могут быть отмечены R6111- и/или R6112-замещенные производные упомянутых выше в качестве примеров Har1 радикалов. Наr1-С 1-С 4 алкил означает один из упомянутых выше С 1-С 4 алкильных радикалов, таких как метил,этил или пропил, замещенных упомянутыми выше Har1 радикалами такими, как, например, имидазолил,бензимидазолил, индолил или пирролил и подобными или их замещенными производными. В качестве примеров могут быть отмечены, без ограничения, пиридинилметил (например, пиридин-3-илметил),имидазолилметил, пирролилметил, 2-имидазолилметил (например, 2-имидазол-5-илэтил), 2-пиридинилэтил, 3-(бензофуран-2-ил)пропил, 3-(бензимидазол-2-ил)пропил, 2-индолилэтил (например, 2-индол-2 илэтил или 2-индол-3-илэтил), индолилметил (например, индол-2-илметил, индол-3-илметил или индол 5-илметил), 2-бензимидазолилэтил (например, 2-бензимидазол-2-илэтил), бензимидазолилметил (например, бензимидазол-2-илметил), и им подобные. Конкретно, примеры Har1-C1-С 4 алкильных радикалов могут включать пиридинилметил (например,пиридин-3-илметил или пиридин-4-илметил), 2-пиридинилэтил (например, 2-пиридин-3-илэтил), индолилметил (например, индол-2-илметил, индол-3-илметил или индол-5-илметил) или 2-индолилэтил (например, 2-индолил-2-илэтил или 2-индолил-3-илэтил). Более конкретно, примеры Har1-С 1-С 4 алкильных радикалов могут включать пиридин-3-илметил,пиридин-4-илметил, 2-пиридин-3-илэтил, индол-2-илметил, индол-3-илметил, индол-5-илметил, 2 индолил-2-илэтил или 2-индолил-3-илэтил. В радикале Har1-С 1-С 4 алкил, как было установлено, фрагмент Har1 связан с Har1-С 1-С 4 алкилом через кольцевой углеродный атом. Один вариант таких Har1-С 1-С 4 алкильных радикалов, в которых Har1 фрагмент обозначает конденсированное бициклическое кольцо, содержащее бензольное кольцо, относится к таким радикалам, в которых, Har1 фрагмент предпочтительно связан с С 1-С 4 алкильным фрагментом через углеродный атом кольца, включающего один или более гетероатомов. Другой вариант таких Har1-С 1-С 4 алкильных радикалов, в которых Har1 фрагмент обозначает конденсированное бициклическое кольцо, содержащее бензольное кольцо, относится к таким радикалам, в которых, Har1 фрагмент предпочтительно связан с С 1-С 4 алкильным фрагментом через углеродный атом бензольного кольца.Har2 обозначает моноциклическое 5- или 6-членное ненасыщенное гетероароматическое кольцо,включающее от одного до трех гетероатомов, каждый из которых выбран из группы, состоящей из азота,кислорода и серы. Har2 может включать, не ограничивая, тиофен, оксазол, изооксазол, тиазол, изотиазол,имидазол, пиразол, триазол, тиадиазол, оксадиазол, пиридин, пиримидин, пиразин или пиридазин. Конкретно, примером Har2 радикала может быть пиридин.Cyc1 обозначает циклическую систему формулы Ia, которая соединена с атомом азота карбоксамидной группы через фрагмент A. Cyc1 может включать, не ограничивая, 2-аминофенил, замещенныйR71 и/или R72. Нафтил, один или как часть другой группы, включает нафталин-1-ил и нафталин-2-ил. Согласно настоящему изобретению, следует понимать, что когда две структурные части соединений по настоящему изобретению связаны через составную часть, обозначенную, как связь, тогда две названные части непосредственно присоединены друг к другу через простую связь. В общем, если не указано иначе, гетероциклические группы, упомянутые в данном описании, относятся ко всем их возможным изомерным формам. Гетероциклические группы, упомянутые в данном описании, если не указано иначе, относятся, в частности, ко всем их возможным изомерам положения. Таким образом, например, термин пиридил или пиридинил, отдельно или как часть другой группы,включает пиридин-2-ил, пиридин-3-ил и пиридин-4-ил. Составные части, которые необязательно заме-7 012451 щены, как установлено в описании, могут быть замещены, если не указано иначе, в любом возможном положении. Карбоциклические группы, отдельно или в составе других групп, как отмечено в данном описании,могут быть замещены рассмотренными заместителями или исходными молекулярными группами, если не указано иначе, при любом способном к замещению углеродном кольцевом атоме. Гетероциклические группы, отдельно или в составе других групп, как отмечено в данном описании,могут быть замещены рассмотренными заместителями или исходными молекулярными группами, если не указано иначе, в любом возможном положении таком, например, как любой способный к замещению кольцевой углеродный атом или кольцевой атом азота. Кольца, содержащие способные к кватернизации кольцевые атомы азота (-N=) иминного типа, могут быть предпочтительно не кватернизированы по этим кольцевым атомам азота иминного типа с помощью названных заместителей или исходных молекулярных групп. Предполагается, что любой гетероатом или гетероцикл с ненасыщенными валентностями, упомянутый в данном описании, имеет атом(ы) водорода в соответствии с валентностями. Если любая переменная величина встречается более одного раза в любой составной части, каждое определение является независимым. Подходящими солями соединений формулы 1 - в зависимости от замещения - являются, в частности, все кислотно-аддитивные соли или все соли с основаниями. Особенно следует отметить фармакологически приемлемые соли неорганических и органических кислот и оснований, обычно применяемые в фармации. Подходящими являются водонерастворимые и, особенно водорастворимые кислотноаддитивные соли с такими кислотами, как, например, хлористо-водородная кислота, бромисто-водородная кислота, фосфорная кислота, азотная кислота, серная кислота, уксусная кислота, лимонная кислота,D-глюконовая кислота, бензойная кислота, 2-(4-гидроксибензоил)бензойная кислота, масляная кислота,сульфосалициловая кислота, малеиновая кислота, лауроновая кислота, яблочная кислота, фумаровая кислота, янтарная кислота, щавелевая кислота, винная кислота, эмбоновая кислота, стеариновая кислота,толуолсульфоновая кислота, метансульфоновая кислота или 3-гидрокси-2-нафтойная кислота, причем,при получении солей кислоты используются в эквимолярном соотношении или различных соотношениях в зависимости от того, является кислота моно- или полиосновной кислотой, и от требуемой соли. С другой стороны, соли с основаниями - в зависимости от замещения - также являются подходящими. В качестве примеров солей с основаниями отмечаются соли лития, натрия, калия, кальция, алюминия, магния, титана, аммония, меглуминовые (meglumine) или гуанидиновые соли, причем основания при получении соли также используются в эквимолярном или различных соотношениях. Фармакологически неприемлемые соли, которые могут быть получены, например, в качестве продуктов реакций при получении соединений по изобретению в промышленном масштабе, могут быть превращены в фармакологически приемлемые соли с помощью методов, известных специалистам в данной области техники. Специалистам в данной области техники известно, что соединения по изобретению, а также и их соли могут, например, при выделении в кристаллической форме, содержать различные количества растворителей. Изобретение поэтому включает в свой объем также все сольваты и, в частности, все гидраты соединений формулы 1, а также все сольваты и, в частности, все гидраты солей соединений формулы 1 Заместители R61 и R62 соединений формулы I могут быть присоединены в о-, м- или п-положение по отношению к положению присоединения фенильного кольца к Т 1, при этом предпочтительным является присоединение в м- или, в частности, в п-положение. В другом варианте, Ar1 обозначает фенил, который монозамещен R61, при этом предпочтительным является присоединение R61 в м- или п-положение относительно положения присоединения фенильного кольца к Т 1. В еще одном варианте, Ar1 обозначает фенил, который монозамещен R61, при этом предпочтительным является присоединение R61 в п-положение относительно положения присоединения фенильного кольца к Т 1. Тем не менее в еще одном варианте, Ar1 обозначает фенил, который монозамещен R61, при этом предпочтительным является присоединение R61 в м-положение относительно положения присоединения фенильного кольца к Т 1. Соединения согласно аспекту 1 по настоящему изобретению, более заслуживающие внимание, являются соединениями формулы I, гдеR1 обозначает водород или С 1-С 4 алкил,R2 обозначает водород или С 1-С 4 алкил,R3 обозначает водород или С 1-С 4 алкил,R4 обозначает водород или С 1-С 4 алкил,R5 обозначает водород или С 1-С 4 алкил,R6 обозначает -T1-Q1, где Т 1 обозначает связь или С 1-С 4 алкилен,Q1 обозначает Ar1, Aa1, Hh1 или Ah1, гдеHar1 обозначает или моноциклическое 5-членное ненасыщенное гетероароматическое кольцо, включающее один, два или три гетероатома, каждый из которых выбран из группы, включающей азот, кислород и серу, или моноциклическое 6-членное ненасыщенное гетероароматическое кольцо, включающее один или два атома азота, или конденсированное бициклическое 9-членное ненасыщенное гетероароматическое кольцо, включающее один, два или три гетероатома, каждый из которых выбран из группы, включающей азот, кислород и серу, или конденсированное бициклическое 10-членное ненасыщенное гетероароматическое кольцо, включающее один или два гетероатома, каждый из которых выбран из группы, включающей азот, кислород и серу, иR612 обозначает водород, С 1-С 4 алкил или гидроксиС 2-С 4 алкил,или R611 и R612 вместе с атомом азота, к которому они присоединены, образуют гетероциклическое кольцо Het1, гдеHar1 обозначает или моноциклическое 5-членное ненасыщенное гетероароматическое кольцо, включающее один, два или три гетероатома, каждый из которых выбран из группы, включающей азот, кислород и серу, или моноциклическое 6-членное ненасыщенное гетероароматическое кольцо, включающее один или два атома азота, или конденсированное бициклическое 9-членное ненасыщенное гетероароматическое кольцо, включающее один, два или три гетероатома, каждый из которых выбран из группы, включающей азот, кислород и серу, или конденсированное бициклическое 10-членное ненасыщенное гетероароматическое кольцо, включающее один или два гетероатома, каждый из которых выбран из группы, включающей азот, кислород и серу, иR612 обозначает водород, С 1-С 4 алкил или гидроксиС 2-С 4 алкил, илиR611 и R612 вместе с атомом азота, к которому они присоединены, образуют гетероциклическое кольцо Het1, гдеHet1 обозначает морфолиногруппу,Aa1 обозначает бифенильный радикал,Hh1 обозначает бипиридил, пиразолилпиридинил, имидазолилпиридинил или пиридинилтиофенил радикалы,Ah1 обозначает пиридинилфенил, пиразолилфенил или имидазолилфенил радикалы,R7 обозначает гидроксил или 2-аминофенил,и соли этих соединений. Соединения согласно аспекту 2 по настоящему изобретению, заслуживающие большего внимания,являются соединениями формулы I, гдеR1 обозначает водород или С 1-С 4 алкил,R2 обозначает водород или С 1-С 4 алкил,R3 обозначает водород или С 1-С 4 алкил,R4 обозначает водород или С 1-С 4 алкил,R5 обозначает водород или С 1-С 4 алкил,R6 обозначает -T1-Q1, где Т 1 обозначает связь или С 1-С 4 алкилен,Q1 обозначает Ar1 или Aa1, гдеR61 обозначает С 1-С 4 алкил, или -T2-N(R611)R612, где Т 2 обозначает связь или С 1-С 4 алкилен,R611 обозначает водород, С 1-С 4 алкил или Har1-С 1-С 4 алкил, где Har1 обозначает имидазолил, бензимидазолил, индолил или пирролил,R612 обозначает водород или С 1-С 4 алкил,Aa1 обозначает бифенильный радикал, R7 обозначает гидроксил или 2-аминофенил, и соли этих соединений. Соединения согласно аспекту 1 по настоящему изобретению, заслуживающие особого внимания,-9 012451 являются соединениями формулы I, гдеR1 обозначает водород,R2 обозначает водород,R3 обозначает водород,R4 обозначает водород,R5 обозначает водород,R6 обозначает -T1-Q1, Aa1, Hh1 или Ah1, где Т 1 обозначает связь или C1-С 2 алкилен,Q1 обозначает Ar1, гдеR612 обозначает водород, С 1-С 4 алкил или гидроксиС 2-С 3 алкил, или или R611 и R612 вместе с атомом азота, к которому они присоединены, образуют гетероциклическое кольцо Het1, гдеR612 обозначает водород, С 1-С 4 алкил или гидроксиС 2-С 3 алкил,или R611 и R612 вместе с атомом азота, к которому они присоединены, образуют гетероциклическое кольцо Het1, гдеHet1 обозначает морфолиногруппу,Aa1 обозначает бифенильный радикал,Hh1 обозначает бипиридил, пиразолилпиридинил, имидазолилпиридинил или пиридинилтиофенил радикалы,Ah1 обозначает пиридинилфенил, пиразолилфенил или имидазолилфенил радикалы,R7 обозначает гидроксил или 2-аминофенил,и соли этих соединений. Соединения согласно аспекту 2 по настоящему изобретению, заслуживающие особого внимания,являются соединениями формулы I, гдеR1 обозначает водород,R2 обозначает водород,R3 обозначает водород,R4 обозначает водород,R5 обозначает водород,R6 обозначает -T1-Q1 или бифенил, где Т 1 обозначает связь или С 1-С 2 алкилен,Q1 обозначает Ar1, гдеR61 обозначает С 1-С 4 алкил или -T2-N(R611)R612, где Т 2 обозначает связь или С 1-С 2 алкилен,R611 обозначает водород, С 1-С 4 алкил или Har1-C1-С 2 алкил, гдеHar1 обозначает бензимидазолил или индолил,R612 обозначает С 1-С 4 алкил,R7 обозначает гидроксил или 2-аминофенил,и соли этих соединений. Соединения согласно аспекту 1 по настоящему изобретению, заслуживающие наибольшего внимания, являются соединениями формулы I, гдеHar1 обозначает пиридинил или индолил иR612 обозначает водород, С 1-С 4 алкил или гидроксиС 2-С 3 алкил,или R611 и R612 вместе с атомом азота, к которому они присоединены, образуют гетероциклическое кольцо Het1, гдеHet1 обозначает морфолиногруппу,Aa1 обозначает 1,1'-бифен-4-ил или 1,1'-бифен-3-ил,Hh1 обозначает пиридинилтиофенил радикал,Ah1 обозначает 3-(пиридинил)фенил, 3-(пиразолил)фенил, 4-(пиридинил)фенил или 4-(пиразолил) фенил радикалы,R7 обозначает гидроксил или 2-аминофенил,и соли этих соединений. Соединения согласно аспекту 2 по настоящему изобретению, заслуживающие наибольшего внимания, являются соединения формулы I, гдеR61 обозначает метил, диметиламиногруппу или -T2-N(R611)R612, где Т 2 обозначает метилен,R611 обозначает метил или 2-(индол-2-ил)этил,R612 обозначает метил,R7 обозначает гидроксил или 2-аминофенил,и соли этих соединений. Из соединений согласно аспекту 1 по настоящему изобретению следует отметить такие соединения формулы I, гдеR61 обозначает метил или -T2-N(R611)R612, где либо Т 2 обозначает связь,R611 обозначает метил иHar1 обозначает пиридинил или индолил иR612 обозначает водород, метил или 2-гидроксиэтил,или R611 и R612 вместе с атомом азота, к которому они присоединены, образуют гетероциклическое кольцо Het1, гдеHet1 обозначает морфолиногруппу,Aa1 обозначает 1,1'-бифен-4-ил или 1,1'-бифен-3-ил,Hh1 обозначает пиридинилтиофенильный радикал,Ah1 обозначает 3-(пиридинил)фенил, 3-(пиразолил)фенил, 4-(пиридинил)фенил или 4-(пиразолил) фенил радикалы,R7 обозначает гидроксил или 2-аминофенил,и соли этих соединений.- 11012451 Более выделяемыми соединениями формулы I согласно аспекту 1 по настоящему изобретению являются соединения, гдеR61 обозначает метил или -T2-N(R611)R612, где либоR611 и R612 вместе с атомом азота, к которому они присоединены, образуют гетероциклическое кольцо Het1, гдеHet1 обозначает морфолиногруппу,Aa1 обозначает 1,1'-бифен-4-ил или 1,1'-бифен-3-ил,Hh1 обозначает 5-(пиридин-2-ил)тиофен-2-ил,Ah1 обозначает 3-(пиридин-3-ил)фенил, 3-(пиридин-4-ил)фенил, 3-(пиразол-1-ил)фенил, 3-(1 Нпиразол-4-ил)фенил, 4-(пиридин-3-ил)фенил, 4-(пиридин-4-ил)фенил, 4-(пиразол-1-ил)фенил или 4-(1 Нпиразол-4-ил)фенил,R7 обозначает гидроксил или 2-аминофенил,и соли этих соединений. Соединениями формулы I согласно аспекту 1 по настоящему изобретению, которые следует особо выделить, являются соединения, гдеR61 обозначает метил или -T2-N(R611)R612, где либо Т 2 обозначает связь,R611 обозначает метил иR612 обозначает водород, либо Т 2 обозначает метилен,R611 обозначает метил или 2-(Har1)этил, гдеR611 и R612 вместе с атомом азота, к которому они присоединены, образуют гетероциклическое кольцо Het1, гдеAh1 обозначает 3-(пиридин-3-ил)фенил, 3-(пиридин-4-ил)фенил, 3-(пиразол-1-ил)фенил, 3-(1 Нпиразол-4-ил)фенил, 4-(пиридин-3-ил)фенил, 4-(пиридин-4-ил)фенил, 4-(пиразол-1-ил)фенил или 4-(1 Нпиразол-4-ил)фенил,R7 обозначает гидроксил,и соли этих соединений. Дополнительно, соединениями формулы I согласно аспекту 1 по настоящему изобретению, которые следует особо выделить, являются соединения, гдеR61 обозначает метил или -T2-N(R611)R612, где либо Т 2 обозначает связь,R611 обозначает метил иR612 обозначает водород, либо Т 2 обозначает метилен,R611 обозначает метил или 2-(Har1)этил, гдеR611 и R612 вместе с атомом азота, к которому они присоединены, образуют гетероциклическое кольцо Het1, гдеHet1 обозначает морфолиногруппу,Aa1 обозначает 1,1'-бифен-4-ил или 1,1'-бифен-3-ил,Hh1 обозначает 5-(пиридин-2-ил)тиофен-2-ил,Ah1 обозначает 3-(пиридин-3-ил)фенил, 3-(пиридин-4-ил)фенил, 3-(пиразол-1-ил)фенил, 3-(1 Нпиразол-4-ил)фенил, 4-(пиридин-3-ил)фенил, 4-(пиридин-4-ил)фенил, 4-(пиразол-1-ил)фенил или 4-(1 Нпиразол-4-ил)фенил,R7 обозначает 2-аминофенил,и соли этих соединений. Особенный интерес среди соединений по настоящему изобретению представляют соединения по этому изобретению, которые включают в себя, в объеме настоящего изобретения, одну или, если возможно, комбинацию большего числа следующих вариантов. Один вариант соединений по настоящему изобретению относится к таким соединениям формулы I,где R1, R2, R3, R4 и R5 все обозначают водород. Следующий вариант соединений по настоящему изобретению относится к таким соединениям формулы I, где R7 обозначает гидроксил. Следующий вариант соединений по настоящему изобретению относится к таким соединениям формулы I, где R7 обозначает Cyc1, при этом в подварианте Cyc1 обозначает 2-фенил. Следующий вариант соединений по настоящему изобретению относится к таким соединениям формулы I, где R7 обозначает 2-аминофенил. Следующий вариант соединений по настоящему изобретению относится к таким соединениям формулы I, где R6 обозначает Aa1. Следующий вариант соединений по настоящему изобретению относится к таким соединениям формулы I, где R6 обозначает Ar1 или -СН 2-Ar1. Следующий вариант соединений по настоящему изобретению относится к таким соединениям формулы I, где Ar1 обозначает R61-замещенный фенил. Следующий вариант соединений по настоящему изобретению относится к таким соединениям формулы I, где Ar1 обозначает фенил, монозамещенный R61 в м-положении относительно места связывания- 13012451 фенильного кольца с Т 1. Следующий вариант соединений по настоящему изобретению относится к таким соединениям формулы I, где Ar1 обозначает фенил, монозамещенный R61 в п-положении относительно места связывания фенильного кольца с Т 1. Следующий вариант соединений по настоящему изобретению относится к таким соединениям формулы I, где R6 обозначает Hh1. Следующий вариант соединений по настоящему изобретению относится к таким соединениям формулы I, где R6 обозначает Ah1. Следующий вариант соединений по настоящему изобретению относится к таким соединениям формулы I, где Т 2 обозначает связь. Следующий вариант соединений по настоящему изобретению относится к таким соединениям формулы I, где Т 2 обозначает С 1-С 4 алкилен такой, как, например, метилен. Следующий вариант соединений по настоящему изобретению относится к таким соединениям формулы I, гдеR61 обозначает -T2-N(R611)R612, где Т 2 обозначает связь. Следующий вариант соединений по настоящему изобретению относится к таким соединениям формулы I, гдеR61 обозначает -T2-N(R611)R612, где Т 2 обозначает С 1-С 4 алкилен такой, как, например, метилен. Следующий вариант соединений по настоящему изобретению относится к таким соединениям формулы I, гдеR1, R2, R3, R4 и R5 все обозначают водород иAr1 обозначает любое соединение, выбранное из группы, включающей 3-метилфенил, 4 метилфенил, 3-диметиламинофенил, 4-диметиламинофенил, 3-аминометилфенил, 4-аминометилфенил,3-(морфолин-4-илметил)фенил, 4-(морфолин-4-илметил)фенил, 3-(N-бензиламинометил)фенил, 3-(Nизобутиламинометил)фенил, 4-(N-бензиламинометил)фенил, 4-(N-изобутиламинометил)фенил, 3-[N(пиридинилметил)аминометил]фенил, 3-[N-(индолилметил)аминометил]фенил, 4-[N-(пиридинилметил) аминометил]фенил, 4-[N-(индолилметил)аминометил]фенил, 3-(N,N-диметиламинометил)фенил, 4-(N,Nдиметиламинометил)фенил, 3-[N,N-(2-индолилэтил)метиламинометил]фенил, 4-[N,N-(2-индолилэтил) метиламинометил]фенил, 3-[N,N-(2-индолилэтил)-(2-гидроксиэтил)аминометил]фенил и 4-[N,N-(2 индолилэтил)-(2-гидроксиэтил)аминометил]фенил. Следующий вариант соединений по настоящему изобретению относится к таким соединениям формулы I, гдеR1, R2, R3, R4 и R5 все обозначают водород иAr1 обозначает бифенильный радикал. Следующий вариант соединений по настоящему изобретению относится к таким соединениям формулы I, гдеR1, R2, R3, R4 и R5 все обозначают водород иHa1 обозначает пиридинилтиофенильный радикал. Следующий вариант соединений по настоящему изобретению относится к таким соединениям формулы I, гдеR1, R2, R3, R4 и R5 все обозначают водород иAr1 обозначает 3-(пиразолил)фенил, 4-(пиразолил)фенил, 4-(пиридинил)фенил или 3-(пиридинил) фенил. Следующий вариант соединений по настоящему изобретению относится к таким соединениям формулы I, где R1, R2, R3, R4 и R5 все обозначают водород и R7 обозначает гидроксил. Следующий вариант соединений по настоящему изобретению относится к таким соединениям формулы I, где R1, R2, R3, R4 и R5 все обозначают водород и R7 обозначает Cyc1. Следующий вариант соединений по настоящему изобретению относится к таким соединениям формулы I, где R1, R2, R3, R4 и R5 все обозначают водород и R7 обозначает 2-аминофенил. Следующий вариант соединений по настоящему изобретению относится к таким соединениям формулы I, где R1, R2, R3, R4 и R5 все обозначают водород и R7 обозначает аминопиридил. Следующий вариант соединений по настоящему изобретению относится к таким соединениям фор- 14012451 мулы I, гдеR1, R2, R3, R4 и R5 все обозначают водород иAr1 обозначает любое соединение, выбранное из группы, включающей 3-метилфенил, 4 метилфенил, 3-диметиламинофенил, 4-диметиламинофенил, 3-аминометилфенил, 4-аминометилфенил,3-(морфолин-4-илметил)фенил, 4-(морфолин-4-илметил)фенил, 3-(N-бензиламинометил)фенил, 3-(Nизобутиламинометил)фенил, 4-(N-бензиламинометил)фенил, 4-(N-изобутиламинометил)фенил, 3-[N(пиридин-3-илметил)аминометил]фенил, 3-[N-(пиридин-4-илметил)аминометил]фенил, 3-[N-(индол-5 илметил)аминометил]фенил, 3-[N-(индол-3-илметил)аминометил]фенил, 4-[N-(пиридин-3-илметил)аминометил]фенил, 4-[N-(пиридин-4-илметил)аминометил]фенил 4-N-(индол-5-илметил)аминометил]фенил,4-[N-(индол-3-илметил)аминометил]фенил, 3-(N,N-диметиламинометил)фенил, 4-(N,N-диметиламинометил)фенил, 3-[N,N-(2-индол-2-илэтил)метиламинометил]фенил, 4-[N,N-(2-индол-2-илэтил)метиламинометил]фенил, 3-N,N-[2-(индол-2-ил)этил]-(2-гидроксиэтил)аминометилфенил и 4-N,N-[2-(индол-2 ил)этил]-(2-гидроксиэтил)аминометилфенил,R7 обозначает гидроксил,и их солям. Другой особый вариант соединений по настоящему изобретению относится к таким соединениям формулы I, гдеAa1 обозначает 1,1'-бифен-4-ил или 1,1'-бифен-3-ил,R7 обозначает гидроксил,и их солям. Другой особый вариант соединений по настоящему изобретению относится к таким соединениям формулы I, гдеR7 обозначает гидроксил,и их солям. Другой особый вариант соединений по настоящему изобретению относится к таким соединениям формулы I, гдеAh1 обозначает 3-(пиразол-1-ил)фенил, 4-(пиразол-1-ил)фенил, 4-(пиридин-4-ил)фенил, 3(пиридин-4-ил)фенил, 4-(пиридин-3-ил)фенил, 3-(пиридин-3-ил)фенил, 3-(1 Н-пиразол-4-ил)фенил или 4(1 Н-пиразол-4-ил)фенил,R7 обозначает гидроксил,и их солям. Другой особый вариант соединений по настоящему изобретению относится к таким соединениям формулы I, гдеR1, R2, R3, R4 и R5 все обозначают водород иAr1 обозначает любое соединение, выбранное из группы, включающей 3-метилфенил, 4 метилфенил, 3-диметиламинофенил, 4-диметиламинофенил, 3-аминометилфенил, 4-аминометилфенил,3-(морфолин-4-илметил)фенил, 4-(морфолин-4-илметил)фенил, 3-(N-бензиламинометил)фенил, 3-(Nизобутиламинометил)фенил, 4-(N-бензиламинометил)фенил, 4-(N-изобутиламинометил)фенил, 3-[N(пиридин-3-илметил)аминометил]фенил, 3-[N-(пиридин-4-илметил)аминометил]фенил, 3-[N-(индол-5 илметил)аминометил]фенил, 3-[N-(индол-3-илметил)аминометил]фенил, 4-[N-(пиридин-3-илметил)аминометил]фенил, 4-[N-(пиридин-4-илметил)аминометил]фенил, 4-[N-(индол-5-илметил)аминометил]фенил, 4-[N-(индол-3-илметил)аминометил]фенил, 3-(N,N-диметиламинометил)фенил, 4-(N,N-диметиламинометил)фенил, 3-N,N-[2-(индол-2-ил)этил]метиламинометилфенил, 4-N,N-[2-(индол-2-ил)этил] метиламинометилфенил, 3-N,N-[2-(индол-2-ил)этил]-(2-гидроксиэтил)аминометилфенил и 4-N,N-[2(индол-2-ил)этил]-(2-гидроксиэтил)аминометилфенил,R7 обозначает 2-аминофенил,и их солям. Другой особый вариант соединений по настоящему изобретению относится к таким соединениям формулы I, гдеAa1 обозначает 1,1'-бифен-4-ил или 1,1'-бифен-3-ил,R7 обозначает 2-аминофенил,- 15012451 и их солям. Другой особый вариант соединений по настоящему изобретению относится к таким соединениям формулы I, гдеR7 обозначает 2-аминофенил,и их солям. Другой особый вариант соединений по настоящему изобретению относится к таким соединениям формулы I, гдеAh1 обозначает 3-(пиразол-1-ил)фенил, 4-(пиразол-1-ил)фенил, 4-(пиридин-4-ил)фенил, 3-(пиридин-4-ил)фенил, 4-(пиридин-3-ил)фенил, 3-(пиридин-3-ил)фенил, 3-(1 Н-пиразол-4-ил)фенил или 4-(1 Нпиразол-4-ил)фенил,R7 обозначает 2-аминофенил,и их солям. Примерные соединения по настоящему изобретению могут включать любое соединение, выбранное из: 1. (E)-N-гидрокси-3-[1-(толуол-4-сульфонил)-1-Н-пиррол-3-ил]акриламид. 2. N-Гидрокси-3-(1-фенилметансульфонил-1 Н-пиррол-3-ил)акриламид. 3. (Е)-3-[1-(Бифенил-4-сульфонил)-1H-пиррол-3-ил]-N-гидроксиакриламид. 4. (Е)-3-[1-(4-Диметиламинбензолсульфонил)-1 Н-пиррол-3-ил]-N-гидроксиакриламид. 5. (Е)-N-(2-Аминофенил)-3-[1-(толуол-4-сульфонил)-1 Н-пиррол-3-ил]акриламид. 6. (Е)-N-(2-Аминофенил)-3-(1-фенилметансульфонил-1 Н-пиррол-3-ил)акриламид. 7. (Е)-N-(2-Аминофенил)-3-[1-(бифенил-4-сульфонил)-1H-пиррол-3-ил]акриламид. 8. (Е)-N-(2-Аминофенил)-3-[1-(4-диметиламинбензолсульфонил)-1 Н-пиррол-3-ил]акриламид. 9. (Е)-N-Гидрокси-3-(1-[4-[2-(1 Н-индол-2-ил)этил]метиламино)метил)бензолсульфонил]-1 Н-пиррол-3-ил)акриламид. 10. (Е)-3-[1-(4-Диметиламинометилбензолсульфонил)-1H-пиррол-3-ил]-N-гидроксиакриламид. 11.(Е)-N-Гидрокси-3-[1-(4-[(пиридин-3-илметил)амино]метилбензолсульфонил)-1 Н-пиррол-3 ил]акриламид. 12. (Е)-N-Гидрокси-3-[1-(4-[(1H-индол-3-илметил)амино]метилбензолсульфонил)-1 Н-пиррол-3 ил]акриламид. 13. (Е)-3-1-[4-(Бензиламинометил)бензолсульфонил]-1 Н-пиррол-3-ил-N-гидроксиакриламид. 14. (Е)-N-Гидрокси-3-1-[4-(изобутиламинометил)бензолсульфонил]-1 Н-пиррол-3-илакриламид. 15. (Е)-N-Гидрокси-3-[1-(4-[(1H-индол-5-илметил)амино]метилбензолсульфонил)-1 Н-пиррол-3 ил]акриламид 16. (Е)-N-Гидрокси-3-[1-(4-[(пиридин-4-илметил)амино]метилбензолсульфонил)-1 Н-пиррол-3-ил] акриламид. 17. (Е)-3-[1-(4-Аминометилбензолсульфонил)-1 Н-пиррол-3-ил]-N-гидроксиакриламид. 18. (Е)-N-Гидрокси-3-[1-(4-пиридин-4-ил-бензолсульфонил)-1 Н-пиррол-3-ил]акриламид. 19. (Е)-N-Гидрокси-3-1-[4-(1 Н-пиразол-4-ил)бензолсульфонил]-1 Н-пиррол-3-илакриламид. 20. (Е)-N-(2-Аминофенил)-3-[1-(4-пиридин-4-ил-бензолсульфонил)-1 Н-пиррол-3-ил]акриламид. 21. (Е)-N-(2-Аминофенил)-3-[1-(4-пиридин-3-ил-бензолсульфонил)-1 Н-пиррол-3-ил]акриламид. 22. (Е)-N-(2-Аминофенил)-3-1-[4-(1 Н-пиразол-4-ил)бензолсульфонил]-1H-пиррол-3-илакриламид. 23. (Е)-3-[1-(Бифенил-3-сульфонил)-1H-пиррол-3-ил]-N-гидроксиакриламид. 24. (Е)-N-Гидрокси-3-[1-(5-пиридин-2-илтиофен-2-сульфонил)-1 Н-пиррол-3-ил]акриламид. 25. (Е)-N-Гидрокси-3-[1-(4-пиразол-1-ил-бензолсульфонил)-1 Н-пиррол-3-ил]акриламид. 26. (Е)-N-(2-Аминофенил)-3-[1-(5-пиридин-2-илтиофен-2-сульфонил)-1H-пиррол-3-ил]акриламид. 27. (Е)-N-Гидрокси-3-[1-(4-морфолин-4-илметилбензолсульфонил)-1H-пиррол-3-ил]акриламид. 28. (Е)-N-Гидрокси-3-1-[4-2-гидроксиэтил)-[2-(1H-индол-2-ил)этил]аминометил)бензолсульфонил]-1H-пиррол-3-илакриламид. 29. (Е)-N-Гидрокси-3-[1-(3-пиридин-4-илбензолсульфонил)-1H-пиррол-3-ил]акриламид. 30. (Е)-N-(2-Аминофенил)-3-[1-(3-пиридин-4-илбензолсульфонил)-1H-пиррол-3-ил]акриламид. 31. (Е)-N-(2-Аминофенил)-3-[1-(3-пиридин-3-илбензолсульфонил)-1 Н-пиррол-3-ил]акриламид. 32. (Е)-N-Гидрокси-3-1-[3-(1H-пиразол-4-ил)бензолсульфонил]-1 Н-пиррол-3-илакриламид. 33. (Е)-N-(2-Аминофенил)-3-1-[3-(1 Н-пиразол-4-ил)бензолсульфонил]-1 Н-пиррол-3-илакриламид и его соль. Соединения по настоящему изобретению могут быть получены, например, согласно приведенным ниже схемам и согласно реакционным стадиям, охарактеризованным следующим образом или, в частности, способами, описанными в следующих примерах, или с использованием аналогичных методов и пу- 16012451 тей синтеза, известных специалистам в данной области техники. В реакционной схеме 1 углеродная цепь соединений формулы V, в которой R1, R2, R4 и R5 имеют значения, отмеченные выше, удлиняется, например, посредством реакции конденсации (с производным малоновой кислоты) или с помощью реакций Виттига или Жюлиа или, в частности, в случае, когда R2 обозначает водород, с помощью реакции Хорнера-Вадсворта-Эммонса (с диалкиловым эфиром (алкоксикарбонил)фосфоновой кислоты) для получения соединений формулы IV, в которой R1, R2, R3,R4 и R5 имеют значения, приведенные выше, и PG1 означает соответствующую временную защитную группу для карбоксильной группы, например, трет-бутильную или одну из тех хорошо известных специалистам защитных групп, которые представлены в Protective Groups in Organic Synthesis by T. Greene и Р. Wuts (John WileySons, Inc. 1999, 3rd Ed.) или в "Protecting Groups (Thieme Foundations Organic Соединения формулы V, в которой R1, R2, R4 и R5 имеют значения, указанные выше, известны или могут быть получены методами, известными специалистам из области техники, или могут быть получены, как описано в следующих примерах для случая, когда R2 обозначает водород, из соединений формулы VI. Соединения формулы VI известны, или доступны с помощью известных методов, или могут быть получены, как описано в следующих примерах. Соединения формулы IV, в которой R1, R2, R3, R4 и R5 имеют значения, указанные выше, и PG1 обозначает названную соответствующую защитную группу, могут вступать в реакцию с соединениями формулы R6-SO2-X, в которой R6 имеет значения, указанные выше, и X обозначает соответствующую уходящую группу такую, как, например, хлор, давая соответствующее соединение формулы III. На следующей реакционной стадии защитная группа PG1 соединений формулы III может быть удалена методом, описанным в следующих примерах или известным из уровня техники, с получением соединений формулы II. Соединения формулы R6-SO2-X известны или могут быть получены известным способом. Соединения формулы II, в которой R1, R2, R3, R4, R5 и R6 имеют значения, указанные выше, могут быть введены в реакцию конденсации с соединениями формулы H2N-O-PG2, в которой PG2 обозначает соответствующую, защищающую кислород группу такую, как, например, соответствующая силильная или тетрагидропиран-2-ильная защитная группа или IIa, в которой PG3 обозначает соответствующую, защищающую азот группу такую, как, например, трет-бутилоксикарбонильная защитная группа, посредством реакции с реагентами, образующими амидную связь, необязательно в присутствии конденсирующих добавок, известных специалистам в данной области техники. В качества примеров реагентов, образующих амидную связь, известных специалистам в данной области техники, могут быть названы, например, карбодиимиды (например,дициклогексилкарбодиимид, или, предпочтительно, гидрохлорид 1-этил-3-(3-диметиламидопропил)карбодиимида) производные азодикарбоновой кислоты (например, диэтилазодикарбоксилат), соли урония [например, О-(бензотриазол-1-ил)-N,N,N',N'-тетраметилуронийтетрафторборат или О-(бензотриазолуроний-1-ил)- 17012451N,N,N',N'-тетраметилуронийгексафторфосфат] и N,N'-карбонилдиимидазол. Альтернативно, соединения формулы II могут быть превращены в активную форму перед реакцией конденсации получением из них галоидангидрида или ангидрида кислоты, необязательно в процессе реакции, без выделения галоидангидрида или ангидрида кислоты. Соединения формулы H2N-O-PG2 или IIa известны или могут быть получены известными из уровня техники методами. Удаление защитных групп PG2 или PG3 может быть осуществлено методами, известными специалистам в данной области техники, или описанными в следующих примерах с получением соединений формулы I, в которой R1, R2, R3, R4, R5, R6 и R7 имеют значения, указанные выше. Соединения формулы I, в которой Т 2 обозначает С 1-С 4 алкилен, в частности, метилен, могут быть получены в соответствии с приведенными ниже реакционными схемами 2-5, и охарактеризованы далее,или в соответствии с описанием, приведенным в примерах, или аналогично, или подобно им. Как показано в реакционной схеме 2 соединения формулы VII, в которой Т 2 обозначает С 1 С 4 алкилен, в частности, метилен, и Y1 обозначает соответствующую уходящую группу такую, как йод,хлор или, прежде всего, бром, и PG4 обозначает соответствующую временную защитную группу для карбоксильной группы, например, трет-бутильную, могут вступать в реакцию с соединениями формулыHN(R611)R612, образуя в известной из уровня техники реакции нуклеофильного замещения соответствующие аминосоединения, у которых удаляется PG4 защитная группа с образованием соответствующих свободных кислот формулы VIII, которые могут быть введены в реакцию конденсации с соединениями формулы H2N-O-PG2 или IIa, как описано выше, давая после удаления PG2 и PG3, соответствующие соединения формулы Ia. Реакционная схема 2 Альтернативно, как показано в реакционной схеме 3, соединения формулы VII, в которой Т 2 обозначает С 1-С 4 алкилен, в частности, метилен, и Y1 обозначает соответствующую уходящую группу такую, как йод, хлор или, прежде всего, бром, и PG4 обозначает соответствующую временную защитную группу для карбоксильной группы, например, трет-бутильную, могут вступать в реакцию с временно защищенным амином (первичным или, прежде всего, вторичным) таким, как, например, фталимид, образуя в известной из уровня техники реакции нуклеофильного замещения соответствующие аминосоединения, у которых удаляется PG4 защитная группа с образованием соответствующих свободных кислот формулы IX, которые могут быть введены в реакцию конденсации с соединениями формулы H2N-O-PG2 или IIa, как описано выше, давая соответствующие соединения формулы X. Реакционная схема 3- 18012451 Аминофрагмент соединений формулы X может быть освобожден от защитной группы известным из уровня техники способом с образованием соответствующих соединений формулы XI, так например, при использовании фталимидной защитной группы она может быть удалена обычным, известным специалистам в области техники методом, например, добавлением гидразина. Соединения формулы XI могут быть освобождены от защитной группы с образованием соответствующих соединений формулы Iб. Альтернативно, как показано на реакционной схеме 4, соединения формулы XI могут быть введены в реакцию с соединениями формулы R611-Y1 и/или R612-Y2, в которых R611 и R612 имеют значения,приведенные выше, и отличны от водорода, a Y1 и Y2 являются соответствующими уходящими группами такими, как например, хлор, бром, йод или сульфонат (например, трифлат), образуя в известной из уровня техники реакции нуклеофильного замещения соответствующие соединения формул XII или XII. Соединения формул XII или XII' освобождаются от защитных групп, давая соединения формул Iв или Iг, соответственно. Реакционная схема 4 Ещ один альтернативный путь представлен на схеме 5, по которой соединения формулы XI могут быть введены с альдегидами или кетонами в реакцию восстановительного аминирования, так, например,соединения формулы XI могут реагировать с бензальдегидом, или соединениями формул С 1-С 3 алкилСНО или Har1-CHO, в которых Har1 обозначен выше, образуя в известной из уровня техники реакции восстановительного аминирования соответствующие соединения формулы XIII. Соединения формулы XIII освобождаются от защиты, образуя соответствующие соединения формулы Iд. Реакционная схема 5 Соединения формулы VII могут быть получены в соответствии со схемой 1 и описаны выше. Представленные выше соединения формул HN(R611)R612, R611-Y1, R612-Y2, C1-С 3 алкил-СНО или Har1-CHO известны или могут быть получены в соответствии с известными из уровня техники методами.- 19012451 Соединения формулы I, в которой R6 обозначает Aa1 или Ah1, могут быть получены в соответствии с приведенной ниже реакционной схемой 6, и охарактеризованы далее, или в соответствии с описанием в приведенных далее примерах, или аналогично, или подобно им. Реакционная схема 6 Как показано на реакционной схеме 6, соединения формулы XIV, в которой Y3 обозначает соответствующую уходящую группу как, например, йод или бром, и PG5 обозначает соответствующую временную защитную группу для карбоксильной группы, например, трет-бутильную, могут вступать в реакцию с бороновыми кислотами формулы R/-В(ОН)2, в которой R/ обозначает концевой арильный или гетероарильный фрагмент вышеназванных Aa1 или Ha1 радикалов, или со сложными эфирами бороновых кислот (например, пинаконовые сложные эфиры), образуя по известной из уровня техники реакции Сузуки соответствующие С-С-конденсированные соединения, образующие после удаления PG5 соответствующие свободные кислоты формулы XV, которые могут быть введены в реакцию конденсации с соединениями формулы H2N-O-PG2 или IIa, описанными выше, давая после удаления PG2 и PG3 соответствующие соединения формулы Ie. Альтернативно, как показано на реакционной схеме 7, соединения формулы XIV, в которой Y3 обозначает соответствующую уходящую группу как, например, йод или бром, и PG5 обозначает соответствующую временную защитную группу для карбоксильной группы, например, трет-бутильную, могут быть освобождены от защитной группы PG5, а свободная карбоновая кислота может быть затем введена в реакцию конденсации с соединениями формулы H2N-O-PG2 или IIa, как описано выше, с образованием соединений формулы XVI. Соединения формулы XVI могут вступать в реакцию с бороновыми кислотами формулы R/-В(ОН)2, в которой R/ обозначает концевой арильный или гетероарильный фрагмент вышеназванных Aa1 или Ha1 радикалов, или со сложными эфирами бороновых кислот (например, пинаконовые сложные эфиры), образуя по известной из уровня техники реакции Сузуки соответствующие С-Сконденсированные соединения, образующие после удаления PG5 соответствующие свободные кислоты формулы XV, которые могут быть введены в реакцию конденсации с соединениями формулы H2N-OPG2 или IIa, описанными выше, давая после удаления PG2 и PG3 соответствующие соединения формулы Реакция Сузуки проводится обычным способом, известным специалистам в данной области техники, или по методикам, описанным в следующих примерах, или аналогично или подобно им. Соединения формулы XIV могут быть получены в соответствии с синтетической схемой 1, описанной выше. Упомянутые выше соединения формулы R/-В(ОН)2 известны или могут быть получены согласно известным из уровня техники методам. Упомянутые выше реакции целесообразно проводить аналогично методам, известным специалистам в данной области техники, или как описано в следующих примерах. Кроме того, специалистам в данной области техники известно, что, если существует некоторое число реакционных центров в исходном или промежуточном соединении, может возникнуть необходимость временно заблокировать один или более реакционных центров защитными группами, чтобы позволить реакции проходить конкретно при нужном реакционном центре. Детальное описание использования- 20012451 большого числа предложенных защитных групп можно найти, например, в "Protective Groups in OrganicFoundations Organic Chemistry Series N Group" by P. Kocienski (Thieme Medical Publishers, 2000. Выделение и очистка соединений по настоящему изобретению осуществляется общеизвестными методами, например отгонкой растворителя в вакууме и перекристаллизацией образовавшегося остатка из подходящего растворителя, или одним из стандартных методов, таким как, например, колоночная хроматография на соответствующем носителе. Необязательно соединения формулы I могут быть превращены в их соли или необязательно соли соединений формулы I могут быть превращены в свободные соединения. Соли получают растворением свободного соединения в подходящем растворителе (например, эфире, таком как диэтиловый эфир, тетрагидрофуран или диоксан, хлорированном углеводороде, таком как метиленхлорид или хлороформ, или низкомолекулярном алифатическом спирте, таком как этанол или изопропанол), который содержит нужную кислоту или основание или к которому нужная кислота или основание затем присоединяются. Соли получают фильтрованием, переосаждением осадителем или выпариванием растворителя. Полученные соли могут быть посредством подщелачивания или подкисления превращены в свободные соединения, которые, в свою очередь, могут быть превращены в соли. Таким путем фармакологически неприемлемые соли могут быть превращены в фармакологически приемлемые соли. Соответственно, превращения, упоминаемые в настоящем изобретении, могут осуществляться аналогично или подобно методам, известным специалистам в данной области техники. Специалисту в данной области техники благодаря его/ее профессиональным знаниям или на основе синтетических схем, показанных и представленных в описании данного изобретения, известно, как найти другие возможные синтетические пути для соединений формулы I. Все эти другие возможные синтетические схемы также входят в объем настоящего изобретения. При детальном описании изобретения объем настоящего изобретения не лимитируется только этими описанными характеристиками или вариантами. Специалистам в данной области техники также должно быть очевидным, что модификации, аналоги, варианты, выводы, гомологизации и адаптации к описанному изобретению могут быть сделаны на основе знаний известного уровня техники, особенно на основе раскрытия (например, явного, подразумеваемого или присущего раскрытия) настоящего изобретения, не выходя за рамки сущности и объема настоящего изобретения, определяемого формулой изобретения. Следующие примеры иллюстрируют изобретение, не ограничивая его объем. Аналогично, дополнительные соединения формулы I, получение которых подробно не описано, могут быть получены аналогичным методом или методом, известным специалисту в данной области техники с использованием обычных методик. Любые или все соединения, отмеченные как конечные продукты в следующих примерах, а также их соли, являются предпочтительным объектом по настоящему изобретению. В примерах МС обозначает масс-спектры, М обозначает молекулярный ион, ТСП обозначает ионизацию термораспылением, ЭСИ обозначает ионизацию электрораспылением, ЭИ обозначает электронную ионизацию, ч обозначает часы, мин обозначает минуты. Другие аббревиатуры, используемые в данном описании, имеют значения, обычно известные сами по себе специалистам в области техники. Примеры Конечные продукты 1. (Е)-N-Гидрокси-3-[1-(толуол-4-сульфонил)-1-Н-пиррол-3-ил]акриламид. 0,231 г (Е)-3-[1-(толуол-4-сульфонил)-1H-пиррол-3-ил]акриловой кислоты (соединение А 1) растворяют в 8 мл дихлорметана при комнатной температуре. Затем добавляют 50 мкл N,N-диметилформамида(ДМФ) и по каплям 0,275 г хлорангидрида щавелевой кислоты, растворенной в 2 мл дихлорметана, и перемешивают в течение 1,5 ч. К раствору добавляют 0,439 г О-(триметилсилил)гидроксиламина и перемешивают в течение 15 мин. Затем добавляют 20 мл водного раствора хлористо-водородной кислоты (1 молярный раствор) и экстрагируют этилацетатом. Объединенную органическую фазу высушивают над сульфатом натрия, отфильтровывают и выпаривают в вакууме. Сырой продукт очищают с помощью ускоренной хроматографии на силикагеле, используя градиент дихлорметана и метанола в соотношении от 98:2 до 6:4, получая 0,050 г названного в заголовке соединения в виде белого твердого вещества. МС (ТСП): 307,0 (МН+, 100%). ЯМР (ДМСО-d6): 2,37 (s, 3 Н); 6,12 (d, J = 15,9 Гц, 1 Н); 6,54 (m, 1H); 7,25 (m, J = 16,1 Гц, 2H); 7,42(соединение А 2) растворяют в 50 мл раствора метанол/вода (3/2). Затем добавляют 0,102 г катионообменной смолы IR15 и перемешивают смесь в течение 91 ч при комнатной температуре. Смесь отфильтровывают, фильтрат выпаривают, а остаток кристаллизуют из метанола, получая 0,144 г названного в(m, J = 17 Гц, 5 Н); 8,90 (s, обмен., 1 Н); 10,60 (s, обмен., 1 Н) 3. (Е)-3-[1-(Бифенил-4-сульфонил)-1 Н-пиррол-3-ил]-N-гидроксиакриламид. Метод, используемый для получения этого соединения, аналогичен методу, описанному для соединения 2. Исходные вещества: (Е)-3-(1-(бифенил-4-сульфонил)-1H-пиррол-3-ил)-N-(тетрагидропиран-2 илокси)акриламид (соединение A3) (0,150 г), метанол/вода в соотношении 3:2 (50 мл), смола IR15 (0,300 г). Реакционные условия: КТ, 34 ч. Выход: 0,041 г в виде бледно-серых кристаллов. МС (ЭСИ): 381,1 (MH+-CH3NO2, 100%). ЯМР (ДМСО-d6): 6,14 (d, J = 15,8 Гц, 1 Н); 6,58 (m, 1H); 7,31 (d, J = 15,7 Гц, 1H); 7,43 (т, J = 6,9 Гц,4 Н); 7,70 (m, J =6,6 Гц, 3 Н); 7,91 (d, J = 8,0 Гц, 2 Н); 8,02 (d, J = 8,1 Гц, 2 Н); 8,92 (s, обмен., 1 Н); 10,60 (s,обмен., 1H). 4. (Е)-3-[1-(4-Диметиламинобензолсульфонил)-1H-пиррол-3-ил]-N-гидроксиакриламид. Метод, используемый для получения этого соединения, аналогичен методу, описанному для соединения 2. Исходные вещества:(m, J1= 8,6 Гц, J2 = 17,7 Гц, 3 Н); 8,89 (расширен., обмен., 1 Н), 10,59 (расширен., обмен., 1 Н). 5. (Е)-N-(2-Аминофенил)-3-[1-(толуол-4-сульфонил)-1 Н-пиррол-3-ил]акриламид. 0,116 г трет-бутилового эфира (2-(Е)-3-[1-(толуол-4-сульфонил)-1-Н-пиррол-3-ил]алланоиламино фенил)карбаминовой кислоты (соединение А 5) растворяют в 20 мл дихлорметана при КТ, добавляют 2 мл трифторуксусной кислоты (ТФК) и перемешивают раствор в течение 93 ч. Растворитель выпаривают без досушивания и к остатку добавляют 25 мл воды. Водную фазу экстрагируют посредством отсасывания с этилацетатом. Вслед за этим объединенные органические фазы высушивают над сульфатом натрия и фильтруют. Фильтрат выпаривают в вакууме. Затем остаток кристаллизуют из метанола, получая 0,050 г названного в заголовке соединения в виде белых кристаллов. МС (ЭСИ): 382,0 (МН+, 100%). 1 ЯМР (ДМСО-d6): 2,38 (s, 3 Н); 4,48 (s, обмен 2 Н); 6,55 (m, 3H); 6,71 (m, 1H); 6,90 (m, 1 Н); 7,40 (m,J = 8,1 Гц, 5 Н); 7,70 (m, 1 Н); 7,89 (d, J = 8,3 Гц, 2 Н); 9,20 (s, обмен., 1 Н). 6. (Е)-N-(2-Аминофенил)-3-(1-фенилметансульфонил-1 Н-пиррол-3-ил)акриламид. Метод, используемый для получения этого соединения, аналогичен методу, описанному для соединения 5, за исключением того, что продукт очищают с помощью ускоренной хроматографии на силикагеле, используя градиент дихлорметан/метанол в соотношении от 99:1 до 95:5. Исходные вещества: трет-бутиловый эфир 2-(Е)-3-[1-(фенилметансульфонил-1-Н-пиррол-3-ил) алланоиламино]фенилкарбаминовой кислоты (соединение А 6) (0,146 г), CH2Cl2 (20 мл), ТФК (2 мл). Реакционные условия: КТ, 65 ч. Выход: 0,037 г в виде белых кристаллов. МС (ЭСИ): 382,0 (МН+). 1 ЯМР (ДМСО-d6): 4,90 (s, 2 Н); 5,01 (s, обмен., 1 Н); 6,58 (m, J = 5,7 Гц, 3 Н); 6,74 (m, J = 6,7 Гц, 2 Н); 6,90 (m, 1H); 7,01 (m, 1H); 7,11 (m, J = 5,6, 2 Н); 7,34 (m, J1 = 5,7 Гц, J2 = 6,7 Гц, 5 Н); 9,25 (s, обмен., 1 Н). 7. (Е)-N-(2-Аминофенил)-3-[1-(бифенил-4-сульфонил)-1 Н-пиррол-3-ил]акриламид. Метод, используемый для получения этого соединения, аналогичен методу, описанному для соединения 5. Исходные вещества: трет-бутиловый эфир (2-(Е)-3-[1-(бифенил-4-сульфонил)-1H-пиррол-3-ил]алланоиламинофенил)карбаминовой кислоты (соединение А 7) (0,460 ммоля), CH2Cl2 (50 мл), ТФК (5 мл). Реакционные условия: КТ, 18 ч. Выход: 0,061 г в виде белых кристаллов. МС (ЭСИ): 444,0 (МН+). 1 ЯМР (ДМСО-d6): 4,90 (расширен., обмен., 2 Н); 6,58 (m, J1 = 51,4 Гц, J2 = 7,5 Гц, 3 Н); 6,71 (m, J1 = 1,4 Гц, J2 = 6,6 Гц, 1 Н); 6,90 (m, J1 = 1,4 Гц, J2 = 6,6 Гц, 1H); 7,40 (m, J1 = 7,5 Гц, J2 = 7,7 Гц, 6 Н); 7,78 (m, J= 7,7 Гц, 3 Н); 7,95 (d, J = 8,6 Гц, 2 Н); 8,08 (d, J = 8,8 Гц, 2 Н); 9,23 (s, обмен., 1 Н). 8. (Е)-N-(2-Аминофенил)-3-[1-(4-диметиламинобензолсульфонил)-1 Н-пиррол-3-ил]акриламид. Метод, используемый для получения этого соединения, аналогичен методу, описанному для соединения 5, за исключением того, что продукт очищают кристаллизацией из этилацетата. Исходные вещества: трет-бутиловый эфир (2-(Е)-3-[1-(4-диметиламинобензолсульфонил)-1 Нпиррол-3-ил]алланоиламинофенил)карбаминовой кислоты (соединение А 8) (0,141 г), CH2Cl2 (10 мл),- 22012451 ТФК (1 мл). Реакционные условия: КТ, 20 ч. Выход: 0,109 г в виде светло-красных кристаллов. МС (ЭСИ): 411,0 (МН+, 100%). 1 ЯМР (ДMCO-d6): 3,00 (s, 6 Н); 3,97 (s, обмен., 2 Н); 6,79 (m, J = 15,4 Гц, 2 Н); 6,79 (d, J = 9,2 Гц, 2 Н); 7,04 (m, J1 = 2,7 Гц, J2 = 8,7 Гц, J3= 15,5 Гц, 3 Н); 7,40 (m, J1 = 15,6 Гц, J2 = 8,6 Гц, 3 Н) 7,70 (m, J, = 2,9 Гц,J2 = 9,2 Гц, 3 Н) 9,74 (s, обмен., 1 Н). 9. (Е)-N-Гидрокси-3-(1-[4-[2-(1H-индол-2-ил)гидроксиэтил]метиламино)метил)бензолсульфонил]1 Н-пиррол-3-ил)акриламид. 81 мг (Е)-3-(1-[4-([2-(1 Н-индол-2-ил)гидроксиэтил]метиламино)бензолсульфонил]-1 Н-пиррол-3 ил)-N-(тетрагидропиран-2-илокси)акриламида (соединение А 9) растворяют в 5 мл метанола. После добавления 15 мл 0,1-нормального раствора хлористо-водородной кислоты смесь перемешивают в течение 21 ч. Затем реакционную смесь выпаривают. Остаток промывают этилацетатом и высушивают в вакууме при -50 С. Выход: 55 мг в виде бледно-желтого твердого вещества 10. (Е)-3-[1-(4-Диметиламинометилбензолсульфонил)-1 Н-пиррол-3-ил]-N-гидроксиакриламид. Метод, используемый для получения этого соединения, аналогичен методу, описанному для соединения 9. Исходное вещество:(Е)-3-[1-(4-диметиламинометилбензолсульфонил)-1 Н-пиррол-3-ил]-N(тетрагидропиран-2-илокси)акриламид (соединение А 10). 11. (E)-N-Гидрокси-3-[1-(4-[(пиридин-3-илметил)амино]метилбензолсульфонил)-1 Н-пиррол-3-ил] акриламид. Получают исходя из соединения A11 методом, аналогичным методу, описанному для соединения 9. Сырой продукт очищают до степени, пригодной для биологического тестирования. МН+ = 413,0 12. (Е)-N-Гидрокси-3-[1-(4-[(1 Н-индол-3-илметил)амино]метилбензолсульфонил)-1 Н-пиррол-3 ил]акриламид. Получают исходя из соединения А 12, методом, аналогичным методу, описанному для соединения 9. Сырой продукт очищают до степени, пригодной для биологического тестирования. МН+ = 449,0. 13. (Е)-3-1-[4-(Бензиламинометил)бензолсульфонил]-1H-пиррол-3-ил-N-гидроксиакриламид. Получают исходя из соединения А 13 методом, аналогичным методу, описанному для соединения 9. МН+ = 412,1 14. (Е)-N-Гидрокси-3-1-[4-(изобутиламинометил)бензолсульфонил]-1H-пиррол-3-илакриламид. Получают исходя из соединения А 14 методом, аналогичным методу, описанному для соединения 9. МН+ = 378,1 15. (Е)-N-Гидрокси-3-[1-(4-[(1 Н-индол-5-илметил)амино]метилбензолсульфонил)-1H-пиррол-3 ил]акриламид. Получают исходя из соединения А 15 методом, аналогичным методу, описанному для соединения 9. МН- = 449,1. 16. (E)-N-Гидрокси-3-[1-(4-[(пиридин-4-илметил)амино]метилбензолсульфонил)-1 Н-пиррол-3-ил] акриламид. Получают, исходя из соединение А 16 методом, аналогичным методу, описанному для соединения 9. МН+ = 413,1. 17. (Е)-3-[1-(4-Аминометилбензолсульфонил)-1 Н-пиррол-3-ил]-N-гидроксиакриламид. Получают исходя из соединения В 6 методом, аналогичным методу, описанному для соединения 9. Сырой продукт очищают промыванием метанолом. Получают твердое вещество с 69%-ным выходом. Т. пл.: 227,0-228,6 С. 18. (Е)-N-Гидрокси-3-[1-(4-пиридин-4-илбензолсульфонил)-1 Н-пиррол-3-ил]акриламид/ Получают исходя из соединения А 17 методом, аналогичным методу, описанному для соединения 9. Реакционную смесь частично выпаривают, а образовавшуюся суспензию фильтруют. Продукт выделяют в виде бесцветного твердого вещества. Т. пл: 219,3-221,4 С. 19. (E)-N-Гидрокси-3-1-[4-(1H-пиразол-4-ил)бензолсульфонил]-1H-пиррол-3-илакриламид. Получают исходя из соединения А 18 методом, аналогичным методу, описанному для соединения 9. Т. пл.: 203,8-211,9 С. 20. (Е)-N-(2-Аминофенил)-3-[1-(4-пиридин-4-илбензолсульфонил)-1 Н-пиррол-3-ил]акриламид. Получают исходя из соединения А 19 методом, аналогичным методу, описанному для соединения 21. Т. пл.: 244,2-246,5 С/ 21. (Е)-N-(2-Аминофенил)-3-[1-(4-пиридин-3-илбензолсульфонил)-1 Н-пиррол-3-ил]акриламид. Соединение получают обработкой трет-бутилового эфира (2-(Е)-3-[1-(4-пиридин-3-илбензосуль- 23012451 фонил)-1H-пиррол-3-ил]алланоиламинофенил)карбаминовой кислоты (соединение А 20) в диоксане хлористым водородом. После окончания реакции продукт выпадает в осадок из реакционной смеси. Т. пл.: 199,7-202,3 С. 22. (Е)-N-(2-Аминофенил)-3-1-[4-(1H-пиразол-4-ил)бензолсульфонил]-1H-пиррол-3-ил)акриламид. Получают исходя из соединения А 21 методом, аналогичным методу, описанному для соединения 21. Т. пл.: 232,3-240,9 С. 23. (Е)-3-[1-(Бифенил-3-сульфонил)-1 Н-пиррол-3-ил]-N-гидроксиакриламид. Получают исходя из соединения А 22 методом, аналогичным методу, описанному для соединения 9. Т. пл.: 114-159,4 С, образует спекшийся агломерат при 83 С. 24. (Е)-N-Гидрокси-3-[1-(5-пиридин-2-илтиофен-2-сульфонил)-1H-пиррол-3-ил]акриламид. Получают исходя из соединения А 23 методом, аналогичным методу, описанному для соединения 9. Продукт кристаллизуется из реакционной смеси. Т. пл.: 181,3-182 С. 25. (Е)-N-Гидрокси-3-[1-(4-пиразол-1-илбензолсульфонил)-1 Н-пиррол-3-ил]акриламид. Получают исходя из соединения А 24 методом, аналогичным методу, описанному для соединения 9. Сырой продукт очищают посредством промывки дихлорметаном. Т. пл.: 160,7-166,6 С. 26. (Е)-N-(2-Аминофенил)-3-[1-(5-пиридин-2-илтиофен-2-сульфонил)-1 Н-пиррол-3 -ил]акриламид. Получают исходя из соединения А 25 методом, аналогичным методу, описанному для соединения 21. Вещество очищают, промывая сырой продукт этилацетатом. Т. пл.: 171,3-174,7 С. 27. (Е)-N-Гидрокси-3-[1-(4-морфолин-4-илметилбензолсульфонил)-1 Н-пиррол-3-ил]акриламид. Получают исходя из соединения А 26 методом, аналогичным методу, описанному для соединения 9. Названное в заголовке соединение выделяют с помощью вымораживания. Т. пл.: 168-170 С. 28. (Е)-N-Гидрокси-3-1-[4-2-гидроксиэтил)-[2-(1 Н-индол-2-ил)этил]аминометил)бензолсульфонил]-1 Н-пиррол-3-илакриламид. Получают исходя из соединения А 27 методом, аналогичным методу, описанному для соединения 9. Реакционную смесь выпаривают и названное в заголовке соединение выделяют в виде масла. МН+ = 509,1. Исходя из соединения Г 6 могут быть получены синтетическими методами, аналогичными методам получения соединений примеров 18-22, следующие соединения. 29. (Е)-N-Гидрокси-3-[1-(3-пиридин-4-илбензолсульфонил)-1 Н-пиррол-3-ил]акриламид. 30. (Е)-N-(2-Аминофенил)-3-[1-(3-пиридин-4-илбензолсульфонил)-1H-пиррол-3-ил]акриламид. 31. (Е)-N-(2-Аминофенил)-3-[1-(3-пиридин-3-илбензолсульфонил)-1H-пиррол-3-ил]акриламид. 32. (Е)-N-Гидрокси-3-1-[3-(1 Н-пиразол-4-ил)бензолсульфонил]-1 Н-пиррол-3-илакриламид. 33. (Е)-N-(2-Аминофенил)-3-1-[3-(1 Н-пиразол-4-ил)бензолсульфонил]-1 Н-пиррол-3-илакриламид. Исходные соединения А 1. (Е)-3-[1-(Толуол-4-сульфонил)-1 Н-пиррол-3-ил]акриловая кислота. 1,60 г трет-бутилового эфира (Е)-3-[1-(толуол-4-сульфонил)-1 Н-пиррол-3-ил]акриловой кислоты(соединение В 1) растворяют в 70 мл дихлорметана при комнатной температуре. Затем добавляют 7 мл трифторуксусной кислоты (ТФК) и перемешивают в течение 4 ч. Растворитель выпаривают без досушивания и добавляют к остатку 30 мл воды. Водную фазу экстрагируют этилацетатом. Затем органическую фазу высушивают над сульфатом натрия. Фильтрат выпаривают и высушивают в вакууме, получая 0,951 г названного в заголовке соединения в виде сероватого твердого вещества. МС (ТСП): 290,0 (М-Н+, 100%). ЯМР (ДМСО-d6): 2,36 (s, 3 Н); 6,20 (d, J = 15,9 Гц, 1 Н); 6,74 (m, J = 3,1 Гц, 1H); 7,41 (m, J1 = 3,1 Гц,J2 = 8,2 Гц, J3 = 16,1 Гц, 4 Н); 7,78 (m, 1H), 7,87 (d, J = 8,4 Гц, 2H); 11,80 (расширен., обмен., 1 Н). А 2. (Е)-3-(1-Фенилметансульфонил-1 Н-пиррол-3-ил)-N-(тетрагидропиран-2-илокси)акриламид. 0,295 г (Е)-3-(1-фенилметансульфонил-1H-пиррол-3-ил)акриловой кислоты (соединение Б 1), 0,152 гN-гидроксибензотриазолгидрата (HOBtH2O) и 561 мкл триэтиламина растворяют в 20 мл N,Nдиметилформамида (ДМФ) при комнатной температуре. Вслед за этим добавляют 0,601 г гидрохлоридаN-(3-диметиламинопропил)-N'-этилкарбодиимида (EDCHCl) и перемешивают в течение 1 ч при комнатной температуре. Затем добавляют 0,152 г О-(тетрагидро-2 Н-пиран-2-ил)гидроксиламина и перемешивают в течение 2 ч. ДМФ выпаривают в высоком вакууме. К остатку добавляют воду и смесь экстрагируют этилацетатом. Органическую фазу высушивают над сульфатом натрия, фильтруют и выпаривают в вакууме. Сырой продукт очищают с помощью ускоренной хроматографии на силикагеле с использованием градиента дихлорметан/метанол в соотношении от 99:1 до 98:2, получая 0,189 г названного в заголовке соединения в виде сероватого твердого вещества. МС (ЭСИ): 390,9 (МН+, 100%).A3. (Е)-3-(1-(Бифенил-4-сульфонил)-1 Н-пиррол-3-ил)-N-(тетрагидропиран-2-илокси)акриламид. Метод, используемый для получения этого соединения, аналогичен методу описанному для соединения А 2, за исключением того, что продукт очищают кристаллизацией из воды и метанола. Исходные вещества: (Е)-3-[1-(бифенил-4-сульфонил)-1H-пиррол-3-ил]акриловая кислота (соединение Б 2) (0,300 г), HOBtH2O (0,130 г), триэтиламин (668 мкл), ДМФ (20 мл), EDCHCl (0,508 г), О(тетрагидро-2 Н-пиранил)гидроксиламин (0,089 г). Реакционные условия: комнатная температура, 1 ч; комнатная температура, 18 ч. Выход: 0,345 г в виде сероватого твердого вещества. МС (ЭСИ): 452,8 (МН+); 369,0 (МН+ -С 5 Н 9 О, 100%). ЯМР (ДМСО-d6): 1,61 (m, 6); 3,50 (m, 1 Н); 3,92 (m, 1H); 4,87 (m, 1H); 6,21 (d, J = 14,7 Гц, 1H); 6,60(Е)-3-[1-(4-Диметиламинобензолсульфонил)-1 Н-пиррол-3-ил]-N-(тетрагидропиран-2-илокси) акриламид. Метод, используемый для получения этого соединения, аналогичен методу, описанному для соединения А 2, за исключением того, что продукт очищают с помощью ускоренной хроматографии на силикагеле с использованием градиента дихлорметан/метанол в соотношении от 99:1 до 98:2. Исходные вещества: (Е)-3-[1-(4-диметиламинобензолсульфонил)-1H-пиррол-3-ил]акриловая кислота (соединение Б 3) (0,150 г), HOBtН 2 О (0,072 г), триэтиламин (259 мкл), ДМФ (10 мл), EDCHCl (0,269 г), О-(тетрагидро-2 Н-пиран-2-ил)гидроксиламин (0,049 г). Реакционные условия: комнатная температура, 1 ч; комнатная температура, 17 ч. Выход: 0,187 г в виде красноватого твердого вещества. МС (ЭСИ): 419,2 (МН+); 336,0 (МН+ -С 5 Н 9 О, 100%). 1 Н-ЯМР (ДМСО-d6): 1,61 (m, 6); 3,02 (s, 6 Н); 3,50 (m, 1 Н); 3,92 (m, 1H); 4,85 (m, 1H); 6,19 (m, 1H); 6,50 (m, 1H); 6,75 (m, J = 9,2 Гц, 2 Н); 7,31 (m, 2 Н); 7,64 (m, J = 9,2 Гц, 3 Н); 11,01 (расширен., обмен., 1 Н). А 5. трет-Бутиловый эфир (2-(Е)-3-[1-(толуол-4-сульфонил)-1-Н-пиррол-3-ил]алланоиламинофенил)карбаминовой кислоты. Метод, используемый для получения этого соединения, аналогичен методу, описанному для соединения А 2 за исключением того, что продукт очищают с помощью ускоренной хроматографии на силикагеле с использованием градиента дихлорметан/метанол в соотношении от 99:1 до 98:1. Исходные вещества: (Е)-3-[1-(толуол-4-сульфонил)-1 Н-пиррол-3-ил]акриловая кислота (соединение А 1) (0,400 г), HOBtH2O (0,285 г), триэтиламин (652 мкл), ДМФ (25 мл), EDCHCl (0,698 г), N-BOC-1,2 фенилендиамин (0,286 г). Реакционные условия: комнатная температура, 1 ч; комнатная температура, 2 ч. Выход: 0,609 г в виде сероватого твердого вещества. МС (ЭСИ): 481,7 (МН+, 100%). 1 Н-ЯМР (ДМСО-d6): 1,40 (m, 9H); 2,39 (s, 3 Н); 6,61 (m, J1= 1,7 Гц, J2 = 2,2 Гц, J3 = 5,0 Гц, 2 Н); 7,09(m, J1 = 1,8 Гц, J2 = 2,3 Гц, 2 Н); 7,37 (m, J1 = 2,0 Гц, J2 = 5,0 Гц, J3 = 8,0 Гц, 4 Н); 7,64 (m, 1H); 7,88 (d, J = 8,4 Гц, 2 Н); 8,41 (s, обмен., 1 Н); 9,57 (s, обмен., 1H). А 6. трет-Бутиловый эфир 2- (Е)-3-[1-(фенилметансульфонил-1-Н-пиррол-3-ил)алланоиламино] фенилкарбаминовой кислоты. Метод, используемый для получения этого соединения, аналогичен методу, описанному для соединения А 2 за исключением того, что продукт очищают с помощью ускоренной хроматографии на силикагеле с использованием градиента дихлорметан/метанол в соотношении от 99:1 до 95:5. Исходные вещества: (Е)-3-(1-фенилметансульфонил-1 Н-пиррол-3-ил)акриловая кислота (соединение В 1) (0,180 г), HOBtH2O (0,090 г), триэтиламин (295 мкл), ДМФ (10 мл), EDCHCl (0,315 г), N-BOC1,2-фенилендимин (0,081 г). Реакционные условия: комнатная температура, 1 ч; комнатная температура,17 ч. Выход: 0,218 г в виде сероватого твердого вещества. МС (ЭСИ): 504,0 (MNa+, 100%); 481,8 (МН+). 1H-ЯМР (ДМСО-d6): 1,42 (m, 9H); 5,04 (s,2H); 6,56 (m, J1 = 2,2 Гц, J2 = 10,2 Гц, 2 Н); 7,14 (m, J, = 2,2 Гц, J2 = 5,5 Гц, J3 = 10,1 Гц, 4 Н); 7,36 (m, J1 = 5,5 Гц, J2 = 7,2 Гц, 4 Н); 7,52 (m, J1 = 2,2 Гц, J2 = 7,2 Гц, 2 Н); 8,49 (s, обмен., 1 Н); 9,67 (s, обмен., 1 Н). А 7. трет-Бутиловый эфир (2-(Е)-3-[1-(бифенил-4-сульфонил)-1 Н-пиррол-3-ил]алланоиламино фенил)карбаминовой кислоты. Метод, используемый для получения этого соединение, аналогичен методу, описанному для соединение А 2 за исключением того, что продукт очищают с помощью ускоренной хроматографии на силикагеле с использованием градиента толуол/этилацетат в соотношении от 99:1 до 9:1. Исходные вещества: (Е)-3-[1-(бифенил-4-сульфонил)-1H-пиррол-3-ил)]акриловая кислота (соедине- 25012451 ние Б 2) (0,300 г), HOBtH2O (0,130 г), триэтиламин (668 мкл), ДМФ (20 мл), EDCHCl (0,508 г), N-BOC1,2-фенилендиамин (0,176 г). Реакционные условия: комнатная температура, 1 ч; комнатная температура,17 ч. Выход: 0,285 в виде сероватого твердого вещества. МС (ЭСИ): 543,8 (МН+); 487,9 (МН+ -С 4 Н 8); 336,1 (МН+ -C11H14N2O2, 100%). 1 Н-ЯМР (ДМСО-d6): 1,47 (m, 9 Н); 6,50 (m, J = 5,4 Гц, 1 Н); 6,64 (m, J = 7,7 Гц, 2H); 7,10 (m, J1 = 5,4 Гц, J2 = 7,7 Гц, 3 Н); 7,51 (m, J1=J2=J3= 3,6 Гц, 5H); 7,73 (m, 2 Н); 7,81 (m, 1 Н); 7,96 (d, J = 8,6 Гц, 2 Н); 8,08(d, J = 8,6 Гц, 2 Н); 8,41 (s, обмен., 1H); 8,59 (s, обмен., 1H). А 8. трет-Бутиловый эфир (2-(Е)-3-[1-(4-диметиламинобензолсульфонил)-1 Н-пиррол-3-ил]алланоиламинофенил)карбаминовой кислоты. Метод, используемый для получения этого соединения, аналогичен методу, описанному для соединения А 2, за исключением того, что продукт очищают кристаллизацией из этилацетата. Исходные вещества: (Е)-3-[1-(4-диметиламинобензолсульфонил)-1H-пиррол-3-ил)]акриловая кислота (соединение Б 3) (0,150 г), HOBtН 2 О (0,072 г), триэтиламин (259 мкл), ДМФ (10 мл), EDCHCl(0,269 г), N-BOC-1,2-фенилендиамин (0,049 г). Реакционные условия: комнатная температура, 1 ч; комнатная температура, 21 ч. Выход: 0,142 г красноватого твердого вещества. МС (ЭСИ): 510,9 (МН+, 100%). ЯМР (ДМСО-d6): 1,42 (m, 9 Н); 3,00 (s, 6 Н); 6,51 (m, 2 Н) 6,79 (d, J = 9,2 Гц, 2 Н); 7,09 (m, J = 5,5 Гц,2 Н); 7,36 (m, 2 Н); 7,50 (m, J = 5,5 Гц, 2 Н); 7,70 (m, J = 9,2 Гц, 2 Н); 8,41 (s, обмен., 1 Н); 9,55 (s, обмен.,1 Н). А 9. (Е)-3-(1-[4-([2-(1 Н-Индол-2-ил)этил]метиламино)бензолсульфонил]-1H-пиррол-3-ил)-N-(тетрагидропиран-2-илокси)акриламид. 825 мг (Е)-3-(1-[4-([2-(1H-индол-2-ил)этил]метиламино)бензолсульфонил]-1 Н-пиррол-3-ил)акриловой кислоты (соединение Б 4), 165 мг HOBtH2O и 1,24 мл триэтиламина растворяют в 70 мл ДМФ при комнатной температуре. Вслед за этим добавляют 726 мг EDCHCl и перемешивают в течение 1 ч. Затем добавляют 140 мг О-(тетрагидро-2 Н-пиран-2-ил)гидроксиламина и перемешивают в течение 18 ч. ДМФ выпаривают в высоком вакууме. К остатку прибавляют воду и экстрагируют этилацетатом. Органическую фазу высушивают над сульфатом натрия и выпаривают в вакууме. Сырой продукт очищают с помощью ускоренной хроматографии на силикагеле с использованием градиента дихлорметан/метанол в соотношении от 98:2 до 9:1. Выход: 289 мг красноватого твердого вещества. А 10.(Е)-3-[1-(4-Диметиламинометилбензолсульфонил)-1 Н-пиррол-3-ил]-N-(тетрагидропиран-2 илокси)акриламид. Метод, используемый для получения названного в заголовке соединения, аналогичен методу, описанному для получения соединения А 9. Исходные вещества: (Е)-3-[1-(4-диметиламинометилбензолсульфонил)-1H-пирролил]акриловая кислота (соединение Б 5) (1,78 г), HOBtH2O (366 мг), триэтиламин (2,1 мл), ДМФ (80 мл), EDCHCl (1,54 г),О-(тетрагидро-2 Н-пиран-2-ил)гидроксиламин (306 мг). Реакционные условия: комнатная температура, 1 ч; комнатная температура, 48 ч. Выход: 835 мг желтоватого твердого вещества.A11. (Е)-3-[1-(4-[(Пиридин-3-илметил)амино]метилбензолсульфонил)-1H-пиррол-3-ил]-N-(тетрагидропиран-2-илокси)акриламид. Смесь соединения Б 6, триацетоксиборгидрида натрия, метанола и 3-пиридинкарбоксальдегида перемешивают при комнатной температуре в течение ночи. Реакционную смесь выпаривают и распределяют между дихлорметаном и водой. Сырой продукт очищают с помощью ускоренной хроматографии на силикагеле, получая почти бесцветное масло. Исходя из соединения Б 6 и соответствующего альдегида могут быть получены соединения А 12-А 16 аналогично получению соединения A11. А 12. (Е)-3-[1-(4-[(1H-Индол-3-илметил)амино]метилбензолсульфонил)-1 Н-пиррол-3-ил]-N-(тетрагидропиран-2-илокси)акриламид. А 13. (Е)-3-1-[4-(Бензиламинометил)бензолсульфонил]-1 Н-пиррол-3-ил-N-(тетрагидропиран-2-илокси)акриламид. А 14. (Е)-3-1-[4-(Изобутиламинометил)бензолсульфонил]-1 Н-пиррол-3-ил-N-(тетрагидропиран-2 илокси)акриламид. А 15. (Е)-3-[1-(4-[(1 Н-Индол-5-илметил)амино]метилбензолсульфонил)-1 Н-пиррол-3-ил]-N-(тетрагидропиран-2-илокси)акриламид. А 16. (Е)-3-[1-(4-[(Пиридин-4-илметил)амино]метилбензолсульфонил)-1 Н-пиррол-3-ил]-N-(тетрагидропиран-2-илокси)акриламид. А 17.- 26012451 Исходя из соединение Б 7, названное в заголовке соединение может быть получено аналогично получению соединения А 2. А 18. (Е)-3-1-[4-(1H-Пиразол-4-ил)фенилсульфонил]-1H-пиррол-3-ил-N-(тетрагидропиран-2-илокси)акриламид. Исходя из соединения Б 8, названное в заголовке соединение может быть получено аналогично получению соединения А 2. А 19. трет-Бутиловый эфир [2-Е)-3-1-[4-пиридин-4-ил-бензолсульфонил]-1 Н-пиррол-3-илалланоиламино)фенил]карбаминовой кислоты. Исходя из соединение Б 7, названное в заголовке соединение может быть получено аналогично получению соединения А 5. А 20. трет-Бутиловый эфир [2-Е)-3-1-[4-пиридин-3-ил-бензолсульфонил]-1 Н-пиррол-3-илалланоиламино)фенил]карбаминовой кислоты. Исходя из соединение Б 9, названное в заголовке соединение может быть получено аналогично получению соединения А 5. А 21. трет-Бутиловый эфир [2-Е)-3-1-[4-(1 Н-пиразол-4-ил)бензолсульфонил]-1 Н-пиррол-3-ил алланоиламино)фенил]карбаминовой кислоты. Исходя из соединение Б 8, названное в заголовке соединение может быть получено аналогично получению соединения А 5. А 22. (Е)-3-(1-(Бифенил-3-сульфонил)-1 Н-пиррол-3-ил)-N-(тетрагидропиран-2-илокси)акриламид. Исходя из соединение Б 10, названное в заголовке соединение может быть получено аналогично получению соединения А 2. А 23. (Е)-3-(1-(5-Пиридин-2-илтиофен-2-сульфонил)-1H-пиррол-3-ил)-N-(тетрагидропиран-2-илокси)акриламид. Исходя из соединение Б 11, названное в заголовке соединение может быть получено аналогично получению соединения А 2. А 24.(Е)-3-(1-(4-Пиразол-1-илбензолсульфонил)-1 Н-пиррол-3-ил)-N-(тетрагидропиран-2-илокси) акриламид Исходя из соединения Б 12, названное в заголовке соединение может быть получено аналогично получению соединения А 2. А 25. трет-Бутиловый эфир (2-(Е)-3-[1-(5-пиридин-2-илтиофен-2-ил-сульфонил)-1 Н-пиррол-3-ил] алланоиламинофенил)карбаминовой кислоты. Исходя из соединение Б 11, названное в заголовке соединение может быть получено аналогично получению соединения А 5. А 26. (Е)-3-1-[4-(Морфолин-4-илметил)бензолсульфонил]-1 Н-пиррол-3-ил-N-(тетрагидропиран-2 илокси)акриламид. Исходя из соединения Б 13, названное в заголовке соединение может быть получено аналогично получению соединения А 2. А 27. (E)-3-1-[4-([2-Гидроксиэтил]-[2-(1 Н-индол-3-ил)этил]аминометил)бензолсульфонил]-1 Нпиррол-3-ил-N-(тетрагидропиран-2-илокси)акриламид.(Е)-3-1-[4-([2-(трет-Бутилдиметилсиланилокси)этил]-[2-(1 Н-индол-3-ил)этил]аминометил)бензолсульфонил]-1H-пиррол-3-ил-N-(тетрагидропиран-2-илокси)акриламид (соединение Б 14) (120 мг,0,169 ммоля) растворяют в ТГФ (20 мл). Затем добавляют тетрабутиламмонийфторид (203 мкл, 1 молярный раствор в ТГФ) и триэтиламин (47 мкл, 0,338 ммоля) и смесь перемешивают в течение 17 ч. После добавления воды (50 мл) и экстракции этилацетатом органическую фазу высушивают над сульфатом натрия, фильтруют и выпаривают. Сырой продукт очищают с помощью ускоренной хроматографии на силикагеле, используя элюент дихлорметан-метанол. Б 1. (Е)-3-(1-Фенилметансульфонил-1 Н-пиррол-3-ил)акриловая кислота. Метод, используемый для получения этого соединения, аналогичен методу, описанному для получения соединения А 1 за исключением того, что продукт выделяют кристаллизацией из смеси ацетона(m, J = 5,3, 1H); 7,10 (m, J= 1,6 Гц, 2H); 7,31 (m, 7,41, m, J1 = 1,6 Гц, J2 = 1,9 Гц, J3= 3,4 Гц, J4 = 5,3 Гц, J5 = 16,1 Гц, 4 Н). Б 2. (Е)-3-[1-(Бифенил-4-сульфонил)-1 Н-пиррол-3-ил]акриловая кислота. Метод, используемый для получения этого соединения, аналогичен методу, описанному для получения соединения А 1. Исходные вещества: трет-бутиловый эфир (Е)-3-[1-(бифенил-4-сульфонил)-1H-пиррол-3-ил)акри- 27012451 ловой кислоты (соединение В 3) (1,05 г), CH2Cl2 (100 мл), ТФК (10 мл). Реакционные условия: комнатная температура, 21 ч. Выход: 0,710 г в виде светло-желтого твердого вещества. МС (ЭСИ): 728,7 (2MNa+, 100%); 354,1 (МН+). 1 Н-ЯМР (ДМСО-d6): 6,29 (d, J= 16,0 Гц, 1H); 6,81 (m, J1= 1,2 Гц, J2 = 1,8 Гц, J3 = 3,0 Гц, 1 Н); 7,49 (m,J1 = 3 Гц, J2 = 7,7 Гц, J0 = 16,0 Гц, 5 Н); 7,75 (m, J1 =1,3 Гц, J2= 1,8 Гц, J3 = 7,7 Гц, 2H); 7,85 (s, 1 Н); 7,95 (d, J= 8,6 Гц, 2H); 8,09 (d, J = 8,6 Гц, 2H); 12,17 (расширен., обмен., 1H). Б 3. (Е)-3-[1-(4-Диметиламинобензолсульфонил)-1 Н-пиррол-3-ил]акриловая кислота. Метод, используемый для получения этого соединения, аналогичен методу, описанному для получения соединения А 1. Исходные вещества: трет-бутиловый эфир (Е)-3-[1-(4-диметиламинобензолсульфонил)-1H-пиррол 3-ил)акриловой кислоты (соединение В 4) (0,801 г), CH2Cl2 (100 мл), ТФК (10 мл). Реакционные условия: комнатная температура, 16 ч. Выход: 0,550 г в виде красноватого твердого вещества. МС (ЭСИ): 662,7 (2MNa+, 100%); 321,0 (МН+). 1(Е)-3-(1-[4-([2-(1 Н-индол-2-ил)этил]метиламино)бензолсульфонил]-1Hпиррол-3-ил)акриловой кислоты (1,01 г) (соединение В 5) растворяют в 100 мл дихлорметана и перемешивают в течение 5 мин, потом добавляют 10 мл ТФК и смесь перемешивают в течение 19 ч. Раствор выпаривают в вакууме, затем добавляют к остатку толуол (небольшое количество для очистки ТФК соли) и выпаривают в вакууме. Выход: 1,32 г в виде светло-коричневого твердого вещества. Б 5. (E)-3-[1-(4-Диметиламинометилбензолсульфонил)-1 Н-пиррол-ил]акриловая кислота. Метод, используемый для получения этого соединения, аналогичен методу, описанному для получения соединения Б 4. Исходные вещества: трет-бутиловый эфир (Е)-3-[1-(4-диметиламинометилбензолсульфонил)-1 Нпиррол-ил]акриловой кислоты (соединение В 6) (2,13 г), ТФК (10 мл); 24 ч. Выход: 3,21 г (соль с 3 ТФК) в виде светло-коричневого твердого вещества. Б 6. (Е)-3-[1-(4-Аминометилбензолсульфонил)-1 Н-пиррол-3-ил]-N-(тетрагидропиран-2-илокси)акриламид. К смеси 1 г соединения В 7 и 50 мл этанола добавляют 0,57 мл гидразингидрата (80%-ного). Смесь нагревают с обратным холодильником в течение 2,5 ч. После этого смесь охлаждают до комнатной температуры и образовавшуюся суспензию белого цвета отфильтровывают. Продукт очищают с помощью ускоренной хроматографии на силикагеле. Б 7. (Е)-3-[1-(4-Пиридин-4-илфенилсульфонил)-1H-пиррол-3-ил]акриловая кислота. Исходя из соединения В 8, названное в заголовке соединение может быть получено аналогично получению соединения А 1. Б 8. (Е)-3-1-[4-(1 Н-Пиразол-4-ил)фенилсульфонил]-1 Н-пиррол-3-илакриловая кислота. Исходя из соединения В 9, названное в заголовке соединение может быть получено аналогично получению соединения А 1. Б 9. (Е)-3-[1-(4-Пиридин-3-илфенилсульфонил)-1 Н-пиррол-3-ил]акриловая кислота. Исходя из соединения В 10, названное в заголовке соединение может быть получено аналогично получению соединения А 1. Б 10. (Е)-3-(1-(Бифенил-3-сульфонил)-1 Н-пиррол-3-ил)акриловая кислота. Исходя из соединения В 11, названное в заголовке соединение может быть получено аналогично получению соединения А 1. Б 11. (Е)-3-(1-(5-Пиридин-2-илтиофен-2-сульфонил)-1 Н-пиррол-3-ил)акриловая кислота. Исходя из соединения B12, названное в заголовке соединение может быть получено аналогично получению соединения А 1. Б 12. (Е)-3-(1-(4-Пиразол-1-илбензолсульфонил)-1 Н-пиррол-3-ил)акриловая кислота. Исходя из соединения В 13, названное в заголовке соединение может быть получено аналогично получению соединения А 1. Б 13. (Е)-3-1-[4-(Морфолин-4-илметил)бензолсульфонил]-1 Н-пиррол-3-илакриловая кислота. Исходя из соединения В 14, названное в заголовке соединение может быть получено аналогично получению соединения А 1. Б 14. (Е)-3-1-[4-([2-(трет-Бутилдиметилсиланилокси)этил]-[2-(1 Н-индол-3-ил)этил]аминометил) бензолсульфонил]-1H-пиррол-3-ил-N-(тетрагидропиран-2-илокси)акриламид.(171 мг, 1,16 ммоля) и триэтиламин (2 мл) растворяют в ДМФ (100 мл) при комнатной температуре. После добавления EDCHCl (786 мг, 3,48 ммолей) смесь перемешивают в течение 1,5 ч. Затем добавляют О(тетрагидро-2 Н-пиран-2-ил)гидроксиламин (136 мг, 1,16 ммоля) и перемешивают в течение 17 ч. После выпаривания и добавления 200 мл воды смесь экстрагируют этилацетатом. Органическую фазу высушивают над сульфатом натрия, затем фильтруют и выпаривают. Сырой продукт очищают с помощью ускоренной хроматографии на силикагеле, используя элюент дихлорметан-метанол.-30 С, затем добавляют к суспензии 1,01 г трет-бутилового эфира (Е)-3-(1 Н-пиррол-3-ил)акриловой кислоты (соединение Г 1), медленно нагревают до комнатной температуры и перемешивают в течение 30 мин. Вслед за этим снова охлаждают до -30 С, добавляют 1,19 г п-толуолсульфонилхлорида и перемешивают в течение 2,5 ч. Суспензию медленно нагревают до комнатной температуры и добавляют 40 мл насыщенного водного раствора хлористого натрия. Смесь экстрагируют этилацетатом, объединенные органические фазы высушивают над сульфатом натрия (Na2SO4), отфильтровывают и выпаривают в вакууме. Сырой продукт очищают с помощью ускоренной хроматографии на силикагеле с использованием градиента гексан/этилацетатом в соотношении от 9:1 до 1:1, получая 1,60 г названного в заголовке соединения в виде бледно-желтого твердого вещества. МС (ЭСИ): 347,6 (МН+); 291,9 (МН+ -С 4 Н 9, 100%). 1B2. трет-Бутиловый эфир (Е)-3-(1-фенилметансульфонил-1H-пиррол-3-ил)акриловой кислоты. Метод, используемый для получения этого соединения, аналогичен методу, описанному для соединения B1 за исключением того, что продукт очищают с помощью ускоренной хроматографии на силикагеле, используя градиент гексан/этилацетат в соотношении от 8:1 до 5:1. Исходные вещества: гидрид натрия 60%-ный (0,240 г), трет-бутиловый эфир (Е)-3-(1H-пиррол-3 ил)акриловой кислоты (соединение Г 1 ) (1,01 г), -толуолсульфонилхлорид (1,19 г). Реакционные условия: -30 С, 30 мин; 30 С, 2,5 ч. Выход: 1,45 г в виде светло-желтого твердого вещества. МС (ТСП): 346,3 (М-Н+, 100%). 1 Н-ЯМР (ДМСО-d6): 1,47 (s, 9 Н); 5,00 (s, 2 Н); 6,21 (d, J= 15,8 Гц, 1H); 6,72 (m, J1 =1,8 Гц, J2 = 3,3 Гц, 1H); 6,98 (m, J = 5,3, 1 Н); 7,09 (m, J1 = 2,1 Гц, J2 = 7,8 Гц, 2 Н); 7,31 (m, J1 = 1,9 Гц, J2= 3,5 Гц, J3 = 5,4 Гц, J4 = 7,7 Гц, J5 = 15,7 Гц, 5 Н).B3. трет-Бутиловый эфир (Е)-3-[1-(бифенил-4-сульфонил)-1 Н-пиррол-3-ил]акриловой кислоты. Метод, используемый для получения этого соединения, аналогичен методу, описанному для соединения В 1, за исключением того, что продукт очищают с помощью ускоренной хроматографии на силикагеле с использованием градиента петролейный эфир/диэтиловый эфир в соотношении от 7:1 до 1:1. Исходные вещества: гидрид натрия 60%-ный (0,207 г), трет-бутиловый эфир (Е)-3-(1 Н-пиррол-3 ил)акриловой кислоты (соединение Г 1) (0,531 г), 4-бифенилсульфонилхлорид (0,834 г). Реакционные условия: -30 С, 10 мин; 30 С, 30 мин. Выход: 1,05 г в виде светло-желтого твердого вещества. МС (ЭСИ): 354,0 (МН+ -С 4 Н 9, 100%). 1B4. трет-Бутиловый эфир (Е)-3-[1-(4-диметиламинобензолсульфонил)-1H-пиррол-3-ил]акриловой кислоты. Метод, используемый для получения этого соединения, аналогичен методу, описанному для соединения В 1, за исключением того, что продукт очищают с помощью ускоренной хроматографии на силикагеле с использованием градиента петролейный эфир/диэтиловый эфир в соотношении от 7:1 до 1:1. Исходные вещества: гидрид натрия 60%-ный (0,031 г), трет-бутиловый эфир (Е)-3-(1H-пиррол-3 ил)акриловой кислоты (соединение Г 1) (0,100 г), 4-диметиламинобензолсульфонилхлорид (0,145 г). Реакционные условия: 30 С, 45 мин; -30 С, 2,5 ч. Выход: 0,160 г в виде красноватого твердого вещества. МС (ЭСИ): 376,8 (МН+); 321,0 (МН+ -С 4 Н 9, 100%). 1 Н-ЯМР (ДМСО-d6): 1,42 (s, 9H); 3,00 (s, 6 Н); 6,19 (d, J = 15,8 Гц, 1H); 6,72 (m, J = 9,2 Гц, 3 Н); 7,25B5. трет-Бутиловый эфир (Е)-3-(1-[4-([2-(1H-индол-2-ил)этил]метиламино)бензолсульфонил]-1 Нпиррол-3-ил)акриловой кислоты. 1,50 г трет-Бутилового эфира (Е)-3-[1-(4-бромметилбензолсульфонил)-1H-пиррол-3-ил]акриловой кислоты (соединение Г 2) растворяют в 70 мл этанола при комнатной температуре. Затем добавляют 0,486 мл триэтиламина и 696 мг -метилтриптамина и перемешивают в течение 21 ч. Раствор выпарива- 29012451 ют в вакууме, а сырой продукт очищают с помощью ускоренной хроматографии на силикагеле с использованием градиента гексан/этилацетат в соотношении от 5:1 до 2:1. Выход: 1,08 г в виде светло-желтого твердого вещества.B6. трет-Бутиловый эфир (Е)-3-[1-(4-диметиламинометилбензолсульфонил)-1H-пирролил]акриловой кислоты. Метод, используемый для получения этого соединения, аналогичен методу, описанному для соединения В 5, за исключением того, что продукт кристаллизуют из этанола. Исходные вещества: трет-бутиловый эфир (Е)-3-[1-(4-бромметилбензолсульфонил)-1H-пиррол-3 ил]акриловой кислоты (соединение Г 2) (3,94 г), этанол (150 мл), диметиламин (1,89 г). Выход: 2,19 г в виде светло-желтого твердого вещества.(Е)-3-1-[4-(1,3-Диоксо-1,3-дигидроизоиндол-2-илметил)бензолсульфонил]-1H-пиррол-3-ил акриловая кислота. Исходя из соединения Г 3 используют для получения этого соединения метод, аналогичный методу,описанному для соединения Б 4. Названное в заголовке соединение очищают промыванием толуолом. Исходя из трет-бутилового эфира (Е)-3-[1-(4-бромбензолсульфонил)-1 Н-пиррол-3-ил]акриловой кислоты (соединение Г 4) и соответствующего производного бороновой кислоты, следующие соединения В 8 и В 9 могут быть получены аналогично методу получения соединения В 10.B10. трет-Бутиловый эфир (Е)-3-[1-(4-пиридин-3-илфенилсульфонил)-1 Н-пиррол-3-ил]акриловой кислоты. 0,18 г трет-бутилового эфира (Е)-3-[1-(4-бромбензолсульфонил)-1 Н-пиррол-3-ил]акриловой кислоты (соединение Г 4) и 62 мг 3-пиридилбороновой кислоты растворяют в 10 мл DME. Добавляют каталитическое количество бис-(трифенилфосфинпалладий(II)хлорида и 0,6 мл водного раствора карбоната натрия и смесь нагревают с обратным холодильником в течение ночи. Названное в заголовке соединение выделяют хроматографически.B11. трет-Бутиловый эфир (Е)-3-[1-(бифенил-3-сульфонил)-1 Н-пиррол-3-ил]акриловой кислоты. Исходя из трет-бутилового эфира (Е)-3-(1 Н-пиррол-3-ил)акриловой кислоты (соединение Г 1) и известного из уровня техники 3-бифенилсульфонилхлорида, названное в заголовке соединение может быть получено аналогично или подобно методу, описанному для получения соединения В 1.B12. трет-Бутиловый эфир (Е)-3-[1-(5-пиридин-2-илтиофен-2-сульфонил)-1 Н-пиррол-3-ил]акриловой кислоты. Исходя из трет-бутилового эфира (Е)-3-(1 Н-пиррол-3-ил)акриловой кислоты (соединение Г 1) и известного из уровня техники 5-пиридин-2-илтиофен-2-сульфонилхлорида, названное в заголовке соединение может быть получено аналогично или подобно методу, описанному для получения соединения В 1.B13. трет-Бутиловый эфир (Е)-3-[1-(4-пиразол-1-илбензолсульфонил)-1 Н-пиррол-3-ил]акриловой кислоты. Исходя из трет-бутилового эфира (Е)-3-(1H-пиррол-3-ил)акриловой кислоты (соединение Г 1) и известного из уровня техники 4-пиразол-1-илбензолсульфонилхлорида, названное в заголовке соединение может быть получено аналогично или подобно методу, описанному для получения соединения В 1.B14. трет-Бутиловый эфир (Е)-3-1-[4-(морфолин-4-илметил)бензолсульфонил]-1 Н-пиррол-3-ил акриловой кислоты. Исходя из соединение Г 2 и морфолина, названное в заголовке соединение может быть получено аналогично методу, описанному для получения соединения В 5.B15. (Е)-3-1-[4-([2-(трет-Бутилдиметилсиланилокси)этил]-[2-(1 Н-индол-3-ил)этил]аминометил) бензолсульфонил]-1 Н-пиррол-3-илакриловая кислота. трет-Бутиловый эфир (E)-3-3-[4-([2-(трет-бутилдиметилсиланилокси)этил]-[2-(1H-индол-3-ил) этил]аминометил)бензолсульфонил]-1 Н-пиррол-3 -илакриловой кислоты (соединение Г 5) растворяют в дихлорметане (50 мл). Затем добавляют ТФК и смесь перемешивают в течение 26 ч. После выпаривания остаток промывают толуолом. Г 1. трет-Бутиловый эфир (Е)-3-(1 Н-пиррол-3-ил)акриловой кислоты. 5,29 г гидрида натрия (60%-ный раствор) суспендируют в 100 мл тетрагидрофурана в атмосфере азота при -30 С. К суспензии добавляют 27,81 г трет-бутилдифосфонацетата, медленно нагревают до комнатной температуры и перемешивают в течение 30 мин. Затем смесь снова охлаждают до -30 С, добавляют 5,24 г 1 Н-пиррол-3-карбальдегида (соединение Д 1) и перемешивают при -30 С в течение 30 мин. Суспензию медленно нагревают до комнатной температуры и добавляют 200 мл водного раствора аммиака, затем экстрагируют этилацетатом. Объединенные органические фазы высушивают над Na2SO4,фильтруют и выпаривают в вакууме. Сырой продукт очищают с помощью ускоренной хроматографии на силикагеле с использованием градиента н-гексан/этилацетат в соотношении от 2:1 до 1:1, получая 9,68 г названного в заголовке соединения в виде светло-желтого твердого вещества.
МПК / Метки
МПК: C07D 401/12, A61K 31/4025, C07D 409/12, C07D 403/12, C07D 207/48, A61P 35/00, A61K 31/40
Метки: новые, амидозамещённые, гидрокси-6-фенилфенантридины
Код ссылки
<a href="https://eas.patents.su/30-12451-novye-amidozameshhyonnye-gidroksi-6-fenilfenantridiny.html" rel="bookmark" title="База патентов Евразийского Союза">Новые амидозамещённые гидрокси-6-фенилфенантридины</a>
Предыдущий патент: Способ производства сульфата целлюлозы с улучшенными характеристиками
Следующий патент: Ингибиторы взаимодействия между mdm2 и р53
Случайный патент: Монокристаллический пластинчатый сульфат бария в косметических композициях