Применение с-мет-модуляторов в комбинированной терапии рака
Номер патента: 24563
Опубликовано: 30.09.2016
Авторы: Афтаб Дана Т., Вейцман Аарон, Холланд Джеймс, Мюллер Томас
Формула / Реферат
1. Применение соединения, имеющего структуру
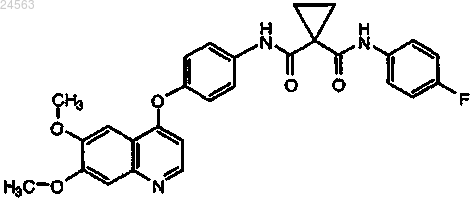
или его фармацевтически приемлемой соли в комбинации с темозоломидом и лучевой терапией (RT) для лечения рака, который выбран из астроцитомы, глиобластомы, гигантоклеточной глиобластомы, глиосаркомы и глиобластомы с олигодендроглиальными компонентами.
2. Применение по п.1, где соединение представлено следующей структурой:
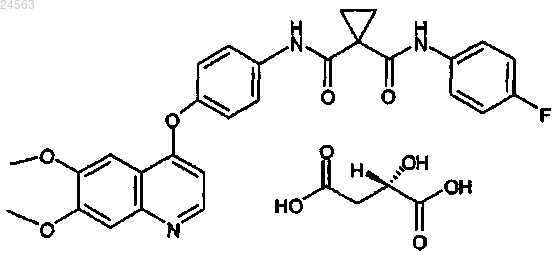
3. Применение по п.1, где соединение или его фармацевтически приемлемую соль вводят в составе фармацевтической композиции, содержащей фармацевтически приемлемый носитель, эксципиент или разбавитель.
4. Применение по п.1, где одновременная фаза равна 6-7 неделям по продолжительности, фаза покоя равна приблизительно 4 неделям по продолжительности и фаза поддержания имеет продолжительность, достаточную для замедления роста рака.
5. Применение по п.1, где TMZ вводят пациенту в дозах 5-180 мг один раз в день во время одновременной фазы; RT вводят пациенту во время одновременной фазы с использованием 1,8-2 Gy на фракцию, один раз в день в течение 5 дней в неделю для общей дозы до 60 Gy; соединение формулы I вводят пациенту в дозах 25-125 мг один раз в день во время фазы поддержания и TMZ вводят пациенту в дозах 5-180 мг в течение 5 последовательных дней и повторяют каждые 28 дней, пока рост рака не замедлится.
Текст
В изобретении описано применение соединения, имеющего структуру или его фармацевтически приемлемой соли в комбинации с темозоломидоми и лучевой терапией(RT) для лечения рака, который выбран из астроцитомы, глиобластомы, гигантоклеточной глиобластомы, глиосаркомы и глиобластомы с олигодендроглиальными компонентами. Область техники, к которой относится изобретение Это изобретение относится к способам применения с-Met-модуляторов и, конкретно, c-Metмодуляторов в комбинации с другими противораковыми агентами и/или облучением, которые могут быть применимы для модуляции различных клеточных активностей и для лечения различных заболеваний, описанных в этом описании. Уровень техники Традиционно, существенные улучшения в лечении рака ассоциируются с идентификацией терапевтических агентов, действующих посредством новых механизмов. Одним механизмом, который может быть использован в лечении рака, является модулирование активности протеинкиназы, так как трансдукция сигнала через активацию протеинкиназы является ответственной за многие характеристики опухолевых клеток. Трансдукция сигнала протеинкиназой особенно уместна в случае, например, щитовидной железы, рака желудка, головы и шеи, легкого, молочной железы, предстательной железы и колоректальных раков, а также в росте и пролиферации опухолевых клеток головного мозга. Протеинкиназы могут быть классифицированы как протеинкиназы рецепторного типа или нерецепторного типа. Тирозинкиназы рецепторного типа включают в себя большое число трансмембранных рецепторов с различной биологической активностью. В отношении подробного обсуждения тирозинкиназ и их лигандов см. Plowman et al., DNP 7(6): 334-339, 1994. Поскольку протеинкиназы и их лиганды играют критическую роль в различных клеточных активностях, нарушение регуляции ферментативной активности протеинкиназы может приводить к измененным клеточным активностям, таким как неконтролируемый рост клеток, ассоциированный с раком. Кроме онкологических показаний, измененная передача сигнала киназой принимает участие в многочисленных других патологических заболеваниях, например иммунологических нарушениях, сердечно-сосудистых заболеваниях, воспалительных заболеваниях и дегенеративных заболеваниях. Таким образом, протеинкиназы являются привлекательными мишенями для обнаружения лекарственных средств с малыми молекулами. Особенно привлекательные мишени для модуляции малых молекул в отношении антиангиогенной и антипролиферативной активности включают в себя тирозинкиназы рецепторного типа Ret, c-Met и VEGFR2. Киназа c-Met является членом-прототипом подсемейства гетеродимерных рецепторных тирозинкиназ (RTK), которые включают в себя Met, Ron и Sea. Эндогенным лигандом для c-Met является фактор роста гепатоцитов (HGF), сильнодействующий индуктор ангиогенеза. Связывание HGF с c-Met индуцирует активацию этого рецептора посредством автофосфорилирования, приводя к увеличению рецепторзависимой передачи сигнала, который стимулирует рост и инвазию клеток. Было показано, что антиHGF-антитела или антагонисты HGF ингибируют метастазирование опухолей in vivo (см. Maulik et al.CytokineGrowth Factor Reviews 2002, 13, 41-59). Сверхэкспрессия c-Met, VEGFR2 и/или Ret была продемонстрирована на большом разнообразии типов опухолей, включающих в себя рак молочной железы,ободочной кишки, рак почки, легкого, плоскоклеточный миелоидный лейкоз, гемангиомы, меланомы,астроцитомы и глиобластомы. Белок Ret является трансмембранным рецептором с тирозинкиназной активностью. Ret является мутированным в большинстве семейных форм медуллярного рака щитовидной железы. Эти мутации активируют киназную функцию Ret и превращают его в онкогенный продукт. Ингибирование трансдукции сигналов EGF, VEGF и эфрина будет предотвращать пролиферацию и ангиогенез клеток, два ключевых клеточных процесса, необходимых для роста и выживания опухоли(Matter A. Drug Disc. Technol. 2001, 6, 1005-1024). Киназа KDR (как называют рецепторную тирозинкиназу с киназным доменом-инсертом) и flt-4 (fms-подобная тирозинкиназа-4), обе являются рецепторами эндотелиального фактора роста сосудов (VEGF). Ингибирование передачи сигналов EGF, VEGF и эфрина будет предотвращать пролиферацию и ангиогенез клеток, два ключевых клеточных процесса, необходимые для роста и выживания опухоли (Matter A. Drug Disc. Technol. 2001, 6, 1005-1024). Рецепторы EGF и VEGF являются желаемыми мишенями для ингибирования малых молекул. Глиобластома является наиболее агрессивной формой первичной опухоли головного мозга с встречаемостью 2,3 на 100000 субъектов в год в Соединенных Штатах. Медианное время выживания после установления диагноза равно 12-15 месяцам с существующим стандартом ухода, включающего в себя хирургию с последующей лучевой терапией. Сообщалось, что поражение пути МЕТ потенцирует реакцию GBM на гамма-облучение (Lal et al., 2005). Сообщалось также, что экспрессия МЕТ коррелирует сGBM-опухолями высокой стадии (Hirose et al., 1998) и экспрессия HGF и МЕТ коррелирует со злокачественностью (Koochekpour et al., 1995; Abounader et al., 2001, Uchinokura et al., 2006). Сообщалось также,что глиома, произведенная фактором стволовых клеток, индуцирует ангиогенез в головном мозге. SCF иVEGF могут играть дополняющие роли в сильной ангиогенной реакции в GBM (Sun et al., 2006). Таким образом, соединения с малыми молекулами, которые специфически ингибируют, регулируют и/или модулируют трансдукцию сигналов киназ, в частности, включающих в себя Ret, c-Met иVEGFR2, описанных выше, являются особенно предпочтительными в качестве средства для лечения или предотвращения состояний, ассоциированных с патологической пролиферацией клеток и ангиогенезом. Одной такой малой молекулой является N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамид, который имеет химическую структуруWO 2005/030140 описывает синтез N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамида (примеры 25, 37, 38 и 48) и также описывает терапевтическую активность этой молекулы для ингибирования, регулирования и/или модулирования трансдукции сигналов киназами (Assays, Table 4, entry 289). Было измерено, что соединение (I) имеет величину IC50 cMet 1,3-наномолярную (нМ) и величину IC50 Ret 5,2 наномолярную (нМ). Таким образом, желательным является обнаружение новых применений соединений для лечения заболеваний с использованием новых комбинированных терапий. Сущность изобретения Раздел сущности изобретения суммирует только некоторые аспекты этого изобретения и не предназначен для ограничения. Эти аспекты и другие аспекты и варианты осуществления описаны более подробно ниже. Все ссылки, цитируемые в этом описании, включены в качестве ссылки в полном объеме. В случае противоречия между точно выраженным раскрытием описания этого изобретения и ссылками,включенными посредством ссылки, главным будет точно выраженное раскрытие описания изобретения. Один аспект этого раскрытия изобретения относится к способам лечения заболеваний, определенных в подробном данном описании ниже. Эти способы лечения включают в себя введение соединения формулы I, где соединение формулы I является таким, как определено в подробном описании настоящего изобретения, пациенту, нуждающемуся в лечении, в комбинации или с темозоломидом (TMZ), и/или с лучевой терапией (RT). Подробное описание изобретения Аспект (I) этого раскрытия изобретения относится к применению соединения, имеющего структуру или его фармацевтически приемлемой соли в комбинации с темозоломидоми и лучевой терапией(RT) для лечения рака, который выбран из астроцитомы, глиобластомы, гигантоклеточной глиобластомы, глиосаркомы и глиобластомы с олигодендроглиальными компонентами. В других вариантах осуществления аспекта (I) этого описания соединение формулы I или его фармацевтически приемлемая соль вводятся в составе фармацевтической композиции, которая дополнительно содержит фармацевтически приемлемый носитель, эксципиент или разбавитель. В других вариантах осуществления аспекта (I) соединение формулы I в любом из вышеуказанных вариантов осуществления является следующим соединением: Соединение формулы (I) включает в себя как указанные соединения, так и индивидуальные изомеры и смеси изомеров. В каждом случае соединение формулы (I) включает в себя фармацевтически приемлемые соли, гидраты и/или сольваты указанных соединений и любые индивидуальные изомеры или смесь их изомеров. Аббревиатуры и определения. Следующие аббревиатуры и термины имеют указанные значения во всем тексте: При изображении или описании химических структур, если совершенно точно не указывается другое, предполагается, что все атомы углерода имеют водородное замещение для конформации валентности четыре. Например, в структуре левой стороны схемы, приведенной ниже, имеются девять атомов водорода. Эти девять атомов водорода изображены в правой структуре. Иногда конкретный атом в структуре описывается текстовой формулой как имеющей водород или атомы водорода в качестве замещения (точно определенный водород), например СН 2 СН 2-. Среднему квалифицированному в данной области специалисту понятно, что вышеуказанные описательные способы являются обычными в областях химии для обеспечения краткости и простоты описания сложных в противном случае комплексов. то, если не указано другое, заместитель "R" может находиться на любом атоме этой кольцевой системы при предположении вытеснения изображенного, предполагаемого или точно определенного атома водорода из одного из атомов кольца, пока образуется стабильная структура. Если группа "R" изображена как плавающая на системе конденсированных колец, как, например, в формулах то, если не указано другое, заместитель "R" может находиться на любом атоме этой системы конденсированных колец при предположении вытеснения изображенного водорода (например, -NH- в формуле выше), предполагаемого водорода (например, как в формуле, приведенной выше, где эти атомы водорода не показаны, но понятно, что они присутствуют), или точно определенного водорода (например, где в формуле выше "Z" обозначает =СН-) из одного из атомов кольца, пока образуется стабильная структура. В изображенном примере группа "R" может находиться либо на 5-членном, либо на 6 членном кольце этой конденсированной системы колец. В формулах, изображенных выше, могут быть более чем одна группа R (Ry), где у обозначает целое число 1 или более. Когда у является, например, 2,то эти две группы "R" могут находиться на любых двух атомах системы колец, опять при предположении, что каждая вытесняет изображенный, предполагаемый или точно определенный водород на этом кольце. Когда группа "R" изображена как существующая на системе кольца, содержащей насыщенные атомы углерода, как, например, в формуле где в этом примере "у" может быть больше чем 1 при предположении, что каждая вытесняет изображенный, предполагаемый или точно определенный водород на этом кольце; то, если не указано другое, где полученная структура является стабильной, две группы "R" могут находиться на одном и том же углероде. Простым примером является пример, когда R является метильной группой; может существовать сдвоенный диметил на углероде изображенного кольца ("кольцевой" углерод). В другом примере две группы R на одном и том же углероде с включением этого углерода могут образовать кольцо с созданием таким образом структуры спироциклического кольца ("спироциклильной группы") с изображенным кольцом, например, в виде формулы"Выход" для каждой из описанных в данном описании реакций выражается в виде процента теоретического выхода."Раком" называют клеточно-пролиферативные состояния заболевания, включающие в себя, но не ограничивающиеся ими: сердечные: саркому (ангиосаркому, фибросаркому, рабдомиосаркому, липосаркому), миксому, рабдомиому, фиброму, липому и тератому; легочные: бронхогенную карциному (плоскоклеточную карциному, карциному недифференцированных малых клеток, недифференцированных больших клеток, аденокарциному), альвеолярную (бронхиолярную) карциному, бронхиальную аденому,саркому, лимфому, хондроматозную ханлартому, мезотелиому; желудочно-кишечные: пищевода (плоскоклеточную карциному, аденокарциному, лейомиосаркому, лимфому), желудка (карциному, лимфому,лейомиосаркому), поджелудочной железы (проточную аденокарциному, инсулиному, глюкагоному, гастриному, карциноидные опухоли, випому), тонкой кишки (аденокарциному, лимфому, карциноидные опухоли, саркому Капоши, лейомиому, гемангиому, липому, нефрофиброму, фиброму), толстой кишки(астроцитому, медуллобластому, глиому, эпендиому, герминому [пинеалому], глиобластому мультиформную, олигодендроглиому, шванному, ретинобластому, врожденные опухоли), нейрофиброму спинного мозга, менингиому, глиому, саркому); гинекологические: матки (эндометриальную карциному),шейки матки (рак шейки матки, предопухолевую дисплазию шейки матки), яичников (рак яичника [серозную цистаденокарциному, муцинозную цистаденокарциному, неклассифицированную карциному],опухоли гранулеза-оболочечных клеток, опухоли клеток Сертоли-Лейдига, дисгерминому, злокачественную иератому), вульвы (плоскоклеточный рак, интраэпителиальный рак, аденокарциному, фибросаркому, меланому, влагалища (прозрачно-клеточную карциному, плоскоклеточный рак, ботриоидную саркому (эмбриональную рабдомиосаркому), фаллопиевых труб (карциному); гематологические: крови (миелоидный лейкоз [острый и хронический], острый лимфобластный лейкоз, хронический лимфоцитарный лейкоз, миелопролиферативные заболевания, множественную миелому, миелодиспластический син-4 024563 дром), болезнь Ходжкина, неходжкинскую лимфому [злокачественную лимфому]; кожи: злокачественную меланому, баазально-клеточную карциному, плоскоклеточную карциному, саркому Капоши, диспластические родимые пятна, липому, ангиому, дерматофиброму, келоиды, псориаз; надпочечников: нейробластому; и рак молочной железы. Таким образом, термин "раковая клетка", описанная здесь,включает в себя клетку, пораженную любым из идентифицированных выше состояний."Терапия гормонами" или "гормональная терапия" включает в себя, например, лечение одним или несколькими из следующих лекарственных средств: стероидами (например, дексаметазоном), финастеридом, тамоксифеном и ингибитором ароматазы."Пациент" для целей данного изобретения включает в себя людей и других животных, в частности млекопитающих, и другие организмы. Таким образом, эти способы применимы как к терапии человека,так и к ветеринарным применениям. В другом варианте осуществления этим пациентом является млекопитающее и в другом варианте осуществления этим пациентом является человек. Фармацевтически приемлемая соль соединения обозначает соль, которая является фармацевтически приемлемой солью и которая имеет желаемую фармакологическую активность исходного соединения. Понятно, что эти фармацевтически приемлемые соли являются нетоксичными. Дополнительная информация о подходящих фармацевтически приемлемых солях может быть найдена в Remington's Pharmaceutical Sciences, 17th ed., Mack Publishing Company, Easton, PA, 1985, который включен в данное описание посредством ссылки или в руководстве S.М. Berge, et al., "Pharmaceutical Salts," J. Pharm. Sci, 1977; 66:119, которое включено в данное описание посредством ссылки. Примеры фармацевтически приемлемых кислотно-аддитивных солей включают в себя соли, образованные неорганическими кислотами, такими как хлористо-водородная кислота, бромисто-водородная кислота, азотная кислота, фосфорная кислота и т.п.; а также органическими кислотами, такими как уксусная кислота, трифторуксусная кислота, пропионовая кислота, гексановая кислота, циклопентанпропионовая кислота, гликолевая кислота, пировиноградная кислота, молочная кислота, щавелевая кислота,малеиновая кислота, малоновая кислота, янтарная кислота, фумаровая кислота, винная кислота, лимонная кислота, бензойная кислота, коричная кислота, 3-(4-гидроксибензоил)бензойная кислота, миндальная кислота, метансульфоновая кислота, этансульфоновая кислота, 1,2-этандисульфоновая кислота, 2 гидроксиэтансульфоновая кислота, бензолсульфоновая кислота, 4-хлорбензолсульфоновая кислота, 2 нафталинсульфоновая кислота, 4-толуолсульфоновая кислота, камфорсульфоновая кислота, глюкогептоновая кислота, 4,4'-метиленбис-(3-гидрокси-2-ен-1-карбоновая кислота), 3-фенилпропионовая кислота,триметилуксусная кислота, трет-бутилуксусная кислота, лаурилсерная кислота, глюконовая кислота,глутаминовая кислота, гидроксинафтойная кислота, салициловая кислота, стеариновая кислота, муконовая кислота, п-толуолсульфоновая кислота и салициловая кислота и т.п. Примеры фармацевтически приемлемых основно-аддитивных солей включают в себя соли, образованные, когда кислотный протон в исходном соединении заменен ионом металла, таким как натрий, калий, литий, соли аммония, кальция, магния, железа, цинка, меди, марганца, алюминия и т.п. Конкретными солями являются соли аммония, калия, натрия, кальция и магния. Соли, полученные из фармацевтически приемлемых органических нетоксичных оснований, включают в себя, но не ограничиваются ими,соли первичного, вторичного и третичного аминов, замещенных аминов, включающих в себя встречающиеся в природе амины, циклические амины и катионообменные смолы. Примеры органических оснований включают в себя изопропиламин, триметиламин, диэтиламин, триэтиламин, трипропиламин,этаноламин, 2-диметиламиноэтанол, 2-диэтиламиноэтанол, дициклогексиламин, лизин, аргинин,гистидин, кофеин, прокаин, гидрабамин, холин, бетаин, этилендиамин, глюкозамин, метилглюкамин,теобромин, пурины, пиперазин, пиперидин, N-этилпиперидин, трометамин, N-метилглюкамин, полиаминные смолы и т.п. Примерами органических оснований являются изопропиламин, диэтиламин, этаноламин, триметиламин, дициклогексиламин, холин и кофеин."Пролекарство" относится к соединениям, которые превращаются (обычно быстро) in vivo с образованием исходного соединения вышеописанных формул, например гидролизом в крови. Обычные примеры включают в себя, но не ограничиваются ими, сложноэфирные и амидные формы соединения, имеющего активную форму, несущую группу карбоновой кислоты. Примеры фармацевтически приемлемых сложных эфиров соединений настоящего изобретения включают в себя, но не ограничиваются ими, алкиловые эфиры (например, с приблизительно одним, приблизительно шестью атомами углерода), где алкильная группа является прямой или разветвленной цепью. Приемлемые сложные эфиры включают в себя также циклоалкиловые и арилалкиловые сложные эфиры, такие как, но не ограничивающиеся ими,бензил. Примеры фармацевтически приемлемых амидов настоящего изобретения включают, но ими не ограничиваются, первичные амиды и вторичные и третичные алкиламиды (например, с приблизительно одним, приблизительно шестью атомами углерода). Амиды и сложные эфиры соединений этого изобретения могут быть получены в соответствии с общепринятыми способами. Подробное обсуждение пролекарств обеспечено в Т. Higuchi and V. Stella, "Pro-drugs as Novel Delivery Systems," Vol 14 of the A.C.S.Association and Pergamon Press, 1987, которые включены в настоящее описание посредством ссылки для всех целей."Таксан (таксаны)" включает в себя, например, один или более из следующих веществ: паклитаксел"Терапевтически эффективным количеством" является количество соединения этого изобретения,которое при введении пациенту ослабляет симптом этого заболевания. Предполагается, что терапевтически эффективное количество включает в себя количество соединения, одного или в комбинации с другими активными ингредиентами, эффективными для модуляции Ret, c-Met и/или VEGFR2 или эффективными для лечения или предотвращения рака. Количество соединения этого изобретения, которое составляет "терапевтически эффективное количество", будет варьироваться в зависимости от конкретного соединения, патологического состояния и его тяжести, возраста подлежащего лечению пациента и т. д. Терапевтически эффективное количество может быть определено рутинным образом специалистом в данной области с учетом знаний и в соответствии с этим описанием."Ингибитор топоизомеразы" включает в себя, например, один или несколько из следующих веществ: амсакрина, камптотецина, этопозида, фосфата этопозида, экзатекана, иринотекана, луртотекана и тенипозида и топотекана."Лечение" или "терапия" заболевания, нарушения или синдрома включает в себя в данном контексте (i) предотвращение появления этого заболевания, нарушения или синдрома у человека, т.е. развития клинических симптомов этого заболевания, нарушения или синдрома у животного, которое может быть подвергнутым или предрасположенным к этому заболеванию, нарушению или синдрому, но еще не испытывающим или не проявляющим симптомов этого заболевания, нарушения или синдрома; (ii) ингибирование заболевания, нарушения или синдрома, т.е. задержку его развития; и (iii) ослабление заболевания, нарушения или синдрома, т.е. вызывание регрессии этого заболевания, нарушения или синдрома. Как известно в данной области, могут быть необходимы корректирования в отношении системной против локализованной доставки, возраста, массы тела, общего здоровья, пола, рациона, времени введения,взаимодействия лекарственных средств и тяжести состояния, и они будут определяться рутинным экспериментированием специалистом с обычной квалификацией в данной области. Дополнительные варианты осуществления изобретения. В другом варианте осуществления терапия для пациентов с GB предусматривает (1) "одновременную фазу", за которой следует (2) "фаза покоя", за которой следует (3) "фаза поддержания". За одновременной фазой следует (2) "фаза покоя", которая может находиться в диапазоне приблизительно 2 недели - приблизительно 8 недель по длительности. Предполагается, что фаза покоя позволяет восстановиться от задержанной токсичности в случае ее присутствия. В другом варианте осуществления фаза покоя может находиться в диапазоне приблизительно 3 недели - приблизительно 6 недель по длительности. В другом варианте осуществления фаза покоя длится приблизительно 4 недели. За фазой покоя следует (3) "фаза поддержания", во время которой пациенты получают фармацевтически активные ингредиенты в течение приблизительно двенадцати 28-дневных циклов, но эти циклы могут варьироваться от приблизительно шести до приблизительно 24 28-дневных циклов. В разных вариантах осуществления пациенты получают различные количества соединения формулы I в разных временных точках в соответствии с фазой TMZ и лучевой терапией. Одновременная фаза. Во время одновременной (согласованной) фазы соединение формулы I в одном варианте осуществления может вводиться пациенту одновременно с RT и TMZ в течение 3-12, или 4-10, или 6-7 недель. В другом варианте осуществления для пациентов, имеющих мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, соединение формулы I будет вводиться пациенту одновременно с RT в течение 6-7 недель в одновременной фазе. Эта одновременная фаза будет находиться в диапазоне от приблизительно 3 до приблизительно 12 недель по длительности. В другом варианте осуществления эта одновременная фаза находится в диапазоне от приблизительно 4 недель до приблизительно 10 недель по длительности. В другом варианте осуществления одновременная фаза находится в диапазоне от приблизительно 6 недель до приблизительно 8 недель по длительности. В другом варианте осуществления одновременная фаза находится в диапазоне от приблизительно 6 недель до приблизительно 7 недель по длительности. Во время этой одновременной фазы активные фармацевтические ингредиенты предоставляются с (RT). В другом варианте осуществления активными фармацевтическими ингредиентами в одновременной фазе являются TMZ и соединение формулы I. В другом варианте осуществления активным фармацевтическим ингредиентом в одновременной фазе является TMZ при условии, что соединение формулы I является по меньшей мере одним из активных фармацевтических ингредиентов в фазе поддержания. В другом варианте осуществления активным фармацевтическим ингредиентом в одновременной фазе является соединение формулы I. Фаза покоя. Во время фазы покоя ни RT, ни соединения формулы I, ни TMZ не вводят пациенту. Фаза покоя может длиться от приблизительно 2 недель до приблизительно 12 недель. В другом варианте осуществления фаза покоя может находиться в диапазоне от приблизительно 3 недель до приблизительно 6 недель по длительности. В другом варианте осуществления диапазон фазы покоя составляет приблизительно 4 недели по длительности. Фаза поддержания. В одном варианте фазы поддержания соединение формулы I вводят пациенту. В другом варианте фазы поддержания пациенту вводят как темозоломид, так и соединение формулы I. В другом варианте фазы поддержания как темозоломид, так и соединение формулы I вводят пациенту в течение периода времени в диапазоне от приблизительно 4 месяцев до приблизительно 10 месяцев. В другом варианте фазы поддержания как темозоломид, так и соединение формулы I вводят пациенту в течение приблизительно 4 месяцев. В другом варианте фазы поддержания как темозоломид, так и соединение формулы I вводят этому пациенту в течение приблизительно 5 месяцев. В другом варианте фазы поддержания как темозоломид, так и соединение формулы I вводят пациенту в течение приблизительно 6 месяцев. В другом варианте фазы поддержания как темозоломид, так и соединение формулы I вводят пациенту в течение приблизительно 7 месяцев. В другом варианте фазы поддержания как темозоломид, так и соединение формулы I вводят пациенту в течение приблизительно 8 месяцев. В другом варианте фазы поддержания как темозоломид, так и соединение формулы I вводят пациенту в течение приблизительно 9 месяцев. В другом варианте фазы поддержания как темозоломид, так и соединение формулы I вводят пациенту в течение приблизительно 10 месяцев. В другом варианте фазы поддержания соединение формулы I вводят пациенту в течение периода времени в диапазоне от приблизительно 4 месяцев до приблизительно 10 месяцев. В другом варианте фазы поддержания соединение формулы I вводят в течение приблизительно 4 месяцев. В другом варианте фазы поддержания соединение формулы I вводят в течение приблизительно 5 месяцев. В другом варианте фазы поддержания соединение формулы I вводят в течение приблизительно 6 месяцев. В другом варианте фазы поддержания соединение формулы I вводят в течение приблизительно 7 месяцев. В другом варианте фазы поддержания соединение формулы I вводят в течение приблизительно 8 месяцев. В другом варианте фазы поддержания соединение формулы I вводят в течение приблизительно 9 месяцев. В другом варианте фазы поддержания соединение формулы I вводят в течение приблизительно 10 месяцев. Во время фазы поддержания соединение формулы I может вводиться один раз в день в виде единственного перорального агента в виде доз 10-200 мг (которые могут находиться в капсулах или таблетках). В другом варианте фазы поддержания соединение формулы I может вводиться один раз в день в качестве единственного перорального агента в дозе 25-125 мг или дозе 25-100 мг (которые могут находиться в капсуле или таблетке). Во время фазы поддержания TMZ также может вводиться в течение 5 последовательных дней, и введение может повторяться каждые 28 дней. TMZ во время фазы поддержания может вводиться пациенту в виде доз 5-300 мг (которые могут находиться в капсулах или таблетках). Для целей настоящего описания изобретения для всех примеров, которые описаны здесь, которые ссылаются на соединение формулы I или темозоломид в дозовых количествах в миллиграммах (мг), это должно пониматься как мг рассматриваемого соединения, и это дозовое количество может вводиться в любой форме, в том числе в форме таблетки и капсулы. Примеры форм капсулы или таблетки, которые находятся в скобках после дозовых количеств, являются неограничивающими примерами того, каким образом эти дозы могут вводиться, и предполагается, что эти примеры не являются ограничивающими. Например, в приведенном выше варианте TMZ может вводиться в других способах наряду с капсулами или таблетками, которые, как имеется в виду, являются только неограничивающими примерами того,каким образом может быть введено это дозовое количество. В неограничивающих примерах во всех вышеуказанных вариантах (включающих в себя одновременную фазу и фазу поддержания) соединение формулы I может вводиться в дозах 5, 10, 15, 20, 25, 30,35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100, 105, 110 , 115, 120, 125, 130, 135, 140, 145, 150, 155,160, 165, 170, 175, 180, 185, 190, 195 и 200 мг (которые могут находиться в капсулах или таблетках). В неограничивающих примерах во всех вышеуказанных вариантах (включающих в себя одновременную фазу и фазу поддержания) TMZ может вводиться в дозах 5, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55,60, 65, 70, 75, 80, 85, 90, 95, 100, 105, 110, 115, 120, 125, 130, 135, 140, 145, 150, 155, 160, 165, 170, 175,180, 185, 190, 195, 200, 205, 210, 215, 220, 225, 230, 235, 240, 245, 250, 255, 260, 265, 260, 275, 280, 285,290, 295 и 300 мг (которые могут находиться в капсулах или таблетках). В другом варианте осуществления аспекта (I) или аспекта (II) настоящего описания одновременная фаза предусматривает введение облучения и соединения формулы I пациенту; фаза покоя предусматривает отсутствие введения соединения яформулы I или облучения пациенту; и фаза поддержания предусматривает введение соединения формулы I пациенту. В одном подварианте этого варианта одновременная фаза может иметь продолжительность приблизительно 7-8 недель, фаза покояможет иметь продолжительность приблизительно 4 недели, и фаза поддержания имеет продолжительность, достаточную для замедления роста рака. В другом подварианте этого варианта соединение формулы I вводят пациенту в дозах 25-100 мг или дозах 25-125 мг (которые могут находиться в капсулах или таблетках) один раз в день во время одновременной фазы; TMZ вводят пациенту в дозах 5-180 мг (которые могут находиться в капсулах или таблетках) один раз в день во время одновременной фазы; RT вводят пациенту во время одновременной фазы с использованием 1,8-2 Gy (Грей) на фракцию один раз в день в течение 5 дней в неделю для получения общей дозы до 60 Gy; соединение формулы I вводят пациенту в дозах 25-100 мг или дозах 25-125 мг (которые могут находиться в капсулах или таблетках) один раз в день во время фазы поддержания; и TMZ вводят пациенту в дозах 5-180 мг (которые могут находиться в капсулах или таблетках) в течение 5 последовательных дней и повторяют введение каждые 28 дней, пока рост рака не уменьшится. В других вариантах осуществления любого из вариантов аспекта (I) и аспекта (II) соединением формулы I является следующее соединение: или его фармацевтическая соль. В другом варианте осуществления соединением формулы I является форма (L)-малатной соли N-(4[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамида,имеющая следующую структуру: Общее введение. В одном аспекте изобретение обеспечивает фармацевтические композиции, содержащие соединение формулы I, описанной выше, и фармацевтически приемлемый носитель, эксципиент или разбавитель. В некоторых других вариантах осуществления способом введения является пероральный способ. Введение соединения формулы I или его фармацевтически приемлемых солей в чистом виде или в виде подходящей фармацевтической композиции может проводиться посредством любого из общепринятых способов введения или агентов для обслуживания подобных применений. Так, введение может быть, например, пероральным, назальным, парентеральным (внутривенным, внутримышечным или подкожным), местным, чрескожным, внутривлагалищным, внутрипузырным, интрацистернальным или ректальным, в форме твердого, полутвердого вещества, лиофилизированного порошка или жидких лекарственных форм, таких как, например, таблетки, суппозитории, пилюли, мягкие и твердые желатиновые формы (которые могут быть в капсулах или таблетках), порошки, растворы, суспензии или аэрозоли или т.п., особенно, в единичных дозированных формах, подходящих для простого введения точных доз. Композиции будут включать в себя общепринятые фармацевтические носитель или эксципиент и соединение формулы I в качестве активного агента и, кроме того, могут включать в себя носители и адъюванты и т. п. Адъюванты включают в себя консервирующие, увлажняющие, суспендирующие, подслащивающие,ароматизирующие, отдушивающие, эмульгирующие и диспергирующие агенты. Предотвращение действия микроорганизмов может обеспечиваться различными антибактериальными и противогрибковыми агентами, например парабенами, хлорбутанолом, фенолом, сорбиновой кислотой и т.п. Может быть также желательным включение изотонических агентов, например сахаров, хлорида натрия и т.п. Пролонгированная абсорбция инъекционной фармацевтической формы может быть получена с использованием задерживающих абсорбцию агентов, например моностеарата алюминия и желатина. Если желательно, фармацевтическая композиция соединения формулы I может также содержать минорные количества вспомогательных веществ, таких как увлажняющие или эмульгирующие агенты,рН буферящие агенты, антиоксиданты и т.п., такие как, например, лимонная кислота, монолаурат сорбитана, олеат триэтаноламина, бутилированный гидрокситолуол и т.д. Выбор готовой формы зависит от различных факторов, таких как способ введения лекарственного средства (например, для перорального введения, препараты в форме таблеток, пилюль или капсул) и биодоступность лекарственного средства. Недавно были разработаны фармацевтические композиции специально для лекарственных средств, которые обнаруживают слабую биодоступность, на основе принципа, что биодоступность может быть увеличена увеличением площади поверхности, т.е. уменьшения размера частиц. Например, патент США 4107288 описывает фармацевтический препарат, имеющий частицы в диапазоне размеров от 10 до 1000 нм, в которых этот активный материал поддерживается на сшитом матриксе макромолекул. Патент США 5145684 описывает получение фармацевтического препарата, в котором лекарственное вещество распыляют на наночастицы (средний размер частиц 400 нм) в присутствии модификатора поверхности и затем диспергируют в жидкой среде с получением фармацевтического препарата, который проявляет удивительно высокую биодоступность. Композиции, подходящие для парентеральной инъекции, могут содержать физиологически приемлемые стерильные водные или неводные растворы, дисперсии, суспензии или эмульсии и стерильные порошки для воссоздания в стерильные инъекционные растворы или дисперсии. Примеры подходящих водных или неводных носителей, разбавителей, растворителей или наполнителей включают в себя воду,этанол, полиолы (пропиленгликоль, полиэтиленгликоль, глицерин и т. п.), их подходящие смеси, растительные масла (такие как оливковое масло) и инъецируемые органические сложные эфиры, такие как этилолеат. Должная текучесть может поддерживаться, например, применением покрытия, такого как лецитин, поддержанием требуемого размера частиц в случае дисперсий и применением поверхностноактивных веществ. Одним конкретным способом введения является пероральный, использующий удобную схему дневных доз, которая может корректироваться в соответствии со степенью тяжести подлежащего лечению патологического состояния. Твердые лекарственные формы для перорального введения включают в себя капсулы, таблетки, пилюли, порошки и гранулы. В таких твердых лекарственных формах активное соединение смешано по меньшей мере с одним инертным общепринятым эксципиентом (или носителем), таким как цитрат натрия или дикальцийфосфат, или (а) наполнителями или разбавителями, такими как, например, крахмалы,лактоза, сахароза, глюкоза, маннит и кремниевая кислота, (b) связывающими веществами, такими как,например, производные целлюлозы, крахмал, альгинаты, желатин, поливинилпирролидон, сахароза и аравийская камедь, (с) увлажнителями, такими как, например, глицерин, (d) дезинтегрирующими агентами, такими как, например, агар-агар, карбонат кальция, крахмал картофеля или тапиоки, альгиновая кислота, натрий-кроскармеллоза, комплексные силикаты и карбонат натрия, (е) ретардантами растворов,такими как, например, парафин, (f) ускорителями абсорбции, такими как, например, соединения четвертичного аммония, (g) увлажняющими агентами, такими как, например, цетиловый спирт и моностеарат глицерина, стеарат магния и т. п., (h) адсорбентами, такими как, например, каолин и бентонит, и (i) смазывающими веществами, такими как, например, тальк, стеарат кальция, стеарат магния, твердые полиэтиленгликоли, лаурилсульфат натрия или их смеси. В случае капсул, таблеток и пилюль лекарственные формы могут также содержать буферные агенты. Твердые лекарственные формы, описанные выше, могут быть приготовлены с покрытиями и оболочками, такими как энтеросолюбильные покрытия, и другими, хорошо известными в данной области. Они могут содержать успокаивающие агенты и могут также быть такой композицией, что они высвобождают активное соединение или активные соединения в определенной части кишечного тракта задержанным образом. Примерами используемых композиций, которые могут быть использованы, являются полимерные вещества и воски. Активные соединения могут находиться также в микроинкапсулированной форме, если необходимо, с одним или несколькими вышеуказанными эксципиентами. Жидкие лекарственные формы для перорального введения включают в себя фармацевтически приемлемые эмульсии, растворы, суспензии, сиропы и эликсиры. Такие лекарственные формы готовят, например, растворением, диспергированием и т. д. соединения формулы I или его фармацевтически приемлемой соли и необязательных фармацевтических адъювантов в носителе, таком как, например, вода, солевой раствор, водная декстроза, глицерин, этанол и т. п.; солюбилизирующих агентах и эмульгаторах,таких как, например, этиловый спирт, изопропиловый спирт, этилкарбонат, этилацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, 1,3-бутиленгликоль, диметилформамид; маслах, в частности хлопковом масле, арахисовом масле, масле зародышей кукурузы, оливковом масле, касторовом масле и кунжутном масле, глицерине, тетрагидрофурфуриловом спирте, полиэтиленгликолях и эфирах жирной кислоты сорбитана; или смесях этих веществ и т.п. с образованием таким образом раствора или суспензии. Суспензии наряду с активными соединениями могут содержать суспендирующие агенты, такие как,например, этоксилированные изостеариловые спирты, полиоксиэтиленсорбитол и сложные эфиры сорбитана, микрокристаллическую целлюлозу, метагидроксид алюминия, бентонит, агар-агар и трагакант или смесь этих веществ и т. п. Композициями для ректального введения являются, например, суппозитории, которые могут быть приготовлены смешиванием соединения формулы I, например, с подходящими нераздражающими эксципиентами или носителями, такими как какао-масло, полиэтиленгликоль или воск для суппозиториев,которые являются твердыми при обычной температуре, но жидкими при температуре тела и, следовательно, плавятся в подходящей полости тела и высвобождают находящийся в них активный компонент. Лекарственные формы для местного введения соединения формулы I включают в себя мази, порошки, спреи и ингаляционные средства. Этот активный компонент смешивают при стерильных условиях с физиологически приемлемым носителем и любыми консервантами, буферами или пропеллентами,которые могут потребоваться. Офтальмические препараты, глазные мази, порошки и растворы рассматриваются также как находящиеся в объеме этого описания изобретения. Для диспергирования соединения формулы I в аэрозольной форме могут быть использованы сжатые газы. Инертными газами, подходящими для этой цели, являются азот, диоксид углерода и т.д. Обычно в зависимости от предполагаемого способа введения фармацевтические композиции будут содержать приблизительно 1 мас.% - приблизительно 99 мас.% соединения (соединений) формулы I или его фармацевтически приемлемой соли и 99 мас.% - 1 мас.% подходящего фармацевтического эксципи-9 024563 ента. В одном примере композиция будет иметь приблизительно 5 мас.% - приблизительно 75 мас.% соединения (соединений) формулы I или его фармацевтически приемлемой соли, причем остальная часть является подходящими фармацевтическими эксципиентами. Современные способы приготовления таких лекарственных форм известны или будут очевидными квалифицированным в данной области специалистам; например, см. Remington's Pharmaceutical Sciences,18th Ed. (Mack Publishing Company, Easton, Pa., 1990). Композиция, подлежащая введению, будет в любом случае содержать терапевтически эффективное количество соединения формулы I или его фармацевтически приемлемой соли для лечения патологического состояния в соответствии с принципами этого описания. Соединения настоящего описания, или их фармацевтически приемлемые соли, или сольваты вводят в терапевтически эффективном количестве, которое будет варьироваться в зависимости от различных факторов, включающих в себя активность конкретно используемого соединения, метаболическую стабильность и продолжительность действия этого соединения, возраст, массу тела, общее здоровье, пол,рацион, способ и время введения, скорость экскреции, комбинацию лекарственных средств, тяжесть конкретных патологических состояний и хозяина, подвергающегося терапии. Соединение формулы I может вводиться пациенту при уровнях доз в диапазоне приблизительно 0,1 - приблизительно 1000 мг в день. Для здорового взрослого человека, имеющего массу тела около 70 кг, примерной дозой является доза в диапазоне приблизительно 0,01 - приблизительно 100 мг/кг массы тела в день. Однако, конкретная доза может варьироваться. Например, доза может зависеть от ряда факторов, включающих в себя требования пациента, тяжесть подлежащего лечению состояния и фармакологическую активность используемого соединения. Определение оптимальных доз для конкретного пациента хорошо известно квалифицированному специалисту в данной области. При приготовлении в виде фиксированной дозы такие комбинированные продукты используют соединение формулы I в пределах вышеописанного диапазона доз и другие фармацевтически активные агенты в пределах одобренного для них диапазона доз. Соединения формулы I могут альтернативно использоваться последовательно с известным фармацевтически приемлемым агентом (известными фармацевтически приемлемыми агентами), когда комбинированная форма является неприемлемой. Общий синтез. Соединения этого изобретения могут быть получены синтетическими процедурами, описанными ниже. Эти процедуры являются только иллюстрацией некоторых способов, при помощи которых могут быть синтезированы соединения формулы I, и могут быть произведены различные модификации этих процедур. Исходные материалы и промежуточные продукты реакции могут быть выделены и очищены,если желательно, с использованием общепринятых способов, включающих в себя, но не ограничивающихся ими, фильтрование, дистилляцию, кристаллизацию, хроматографию и т.п. Такие материалы могут быть охарактеризованы с использованием общепринятых средств, включающих в себя физические константы и спектральные данные. Это описание дополнительно иллюстрируется следующими примерами, которые не должны рассматриваться как ограничивающие это описание в идее или объеме в отношении специфических процедур, описанных в них. Примеры Пример 1 А. ПолучениеN-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамида и его (L)-малатной соли. Синтетический способ,который был использован для получения Приведенный выше процесс описан более подробно ниже. Получение 4-хлор-6,7-диметоксихинолина. Реактор загружали последовательно 6,7-диметоксихинолин-4-олом (10,0 кг) и ацетонитрилом (64,0 л). Полученную смесь нагревали до приблизительно 65 С и добавляли оксихлорид фосфора (POCl3 50,0 кг). После добавления POCl3 температуру этой реакционной смеси повышали до приблизительно 80 С. Реакцию считали завершенной (приблизительно 9,0 ч), когда оставалось 2% исходного материала (согласно анализу высокоэффективной жидкостной хроматографией [HPLC] в процессе). Эту реакционную смесь охлаждали до приблизительно 10 С и затем гасили с использованием охлажденного раствора дихлорметана (ДХМ, 238,0 кг), 30% NH4OH (135,0 кг) и льда (440,0 кг). Полученную смесь нагревали до приблизительно 14 С, и фазы разделяли. Органическую фазу промывали водой (40,0 кг) и концентрировали вакуумной перегонкой с удалением растворителя (приблизительно 190,0 кг). В этой загрузке добавляли метил-трет-бутиловый эфир (МТВЕ, 50,0 кг), и смесь охлаждали до приблизительно 10 С с кристаллизацией продукта в этот период времени. Твердые вещества извлекали центрифугированием, промывали н-гептаном (20,0 кг) и сушили при приблизительно 40 С с получением указанного в заголовке соединения (8,0 кг). Получение 6,7-диметил-4-(4-нитрофенокси)хинолина. Реактор последовательно загружали 4-хлор-6,7-диметоксихинолином (8,0 кг), 4-нитрофенолом (7,0 кг), 4-диметиламинопиридином (0,9 кг) и 2,6-лутидином (40,0 кг). Содержимое реактора нагревали до приблизительно 147 С. Когда реакция заканчивалась (5% остающегося исходного материала, как определено посредством ВЖХ-анализа в процессе, приблизительно 20 ч), содержимому реактора давали остыть до приблизительно 25 С. Добавляли метанол (26,0 кг) с последующим добавлением карбоната калия (3,0 кг), растворенного в воде (50,0 кг). Содержимое реактора перемешивали в течение приблизительно 2 ч. Полученный твердый осадок отфильтровывали, промывали водой (67,0 кг) и сушили при 25 С в течение приблизительно 12 ч с получением указанного в заголовке соединения (4,0 кг). Получение 4-(6,7-диметоксихинолин-4-илокси)фениламина. Раствор, содержащий формиат калия (5,0 кг), муравьиную кислоту (3,0 кг) и воду (16,0 кг), добавляли к смеси 6,7-диметокси-4-(4-нитрофенокси) хинолина (4,0 кг), 10% палладия на угле (на 50% увлажненный водой, 0,4 кг) в тетрагидрофуране (40,0 кг), которая была нагрета до приблизительно 60 С. Добавление проводили таким образом, что температура реакционной смеси оставалась приблизительно 60 С. Когда реакцию считали законченной, как определено с использованием ВЖХ-анализа в процессе(2% остающегося исходного материала, обычно 15 ч), содержимое реактора фильтровали. Фильтрат концентрировали вакуумной перегонкой при приблизительно 35 С до половины его исходного объема,что приводило к осаждению этого продукта. Продукт извлекали фильтрованием, промывали водой (12,0 кг) и сушили в вакууме при приблизительно 50 С с получением указанного в заголовке соединения (3,0 кг). Получение 1-(4-фторфенилкарбамоил)циклопропанкарбоновой кислоты. Триэтиламин (8,0 кг) добавляли к охлажденному (приблизительно 4 С) раствору коммерчески доступной циклопропан-1,1-дикарбоновой кислоты (21, 10,0 кг) в ТГФ (63,0 кг) при такой скорости, что температура загрузки не превышала 10 С. Раствор перемешивали в течение приблизительно 30 мин и затем добавляли тионилхлорид (9,0 кг) с поддержанием температуры загрузки ниже 10 С. Когда добавление заканчивалось, добавляли раствор 4-фторанилина (9,0 кг) в ТГФ (25,0 кг) при такой скорости, что температура этой загрузки не превышала 10 С. Смесь перемешивали в течение приблизительно 4 ч и затем разбавляли изопропилацетатом (87,0 кг). Этот раствор промывали последовательно водным гидроксидом натрия (2,0 кг, растворенных в 50,0 л воды), водой (40,0 л) и водным хлоридом натрия (10,0 кг,растворенных в 40,0 л воды). Органический слой концентрировали вакуумной перегонкой с последующим добавлением гептана, что приводило к осаждению твердого вещества. Это твердое вещество извлекали центрифугированием и затем сушили при приблизительно 35 С в вакууме с получением указанного в заголовке соединения (10,0 кг). Получение 1-(4-фторфенилкарбамоил)циклопропанкарбонилхлорида. Оксалилхлорид (1,0 кг) добавляли к раствору 1-(4-фторфенилкарбамоил)циклопропанкарбоновой кислоты (2,0 кг) в смеси ТГФ (11 кг) и N,N-диметилформамида (ДМФ; 0,02 кг) при такой скорости, что температура загрузки не превышала 30 С. Этот раствор использовали в следующей стадии без дополнительной обработки. ПолучениеN-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан 1,1-дикарбоксамида. Раствор из предыдущей стадии,содержащий 1-(4-фторфенилкарбамоил)циклопропанкарбонилхлорид, добавляли к смеси 4-(6,7-диметоксихинолин-4-илокси)фениламина (3,0 кг) и карбоната калия (4,0 кг) в ТГФ (27,0 кг) и воде (13,0 кг) при такой скорости, что температура загрузки не превышала 30 С. Когда реакция заканчивалась (обычно за 10 мин), добавляли воду (74,0 кг). Смесь перемешивали при 15-30 С в течение приблизительно 10 ч, что приводило к осаждению этого продукта. Про- 11024563 дукт извлекали фильтрованием, промывали предварительно приготовленным раствором ТГФ (11,0 кг) и водой (24,0 кг) и сушили при приблизительно 65 С в вакууме в течение приблизительно 12 ч с получением указанного в заголовке соединения (свободного основания, 5,0 кг). 1N-4(-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамида. Раствор L-яблочной кислоты (2,0 кг) в воде (2,0 кг) добавляли к раствору свободного основания [4(6,7-диметоксихинолин-4-илокси)фенил]амид-(4-фторфенил)амида циклопропан-1,1-дикарбоновой кислоты (1-5, 5,0 кг) в этаноле, поддерживая температуру загрузки при приблизительно 25 С. Затем добавляли уголь (0,5 кг) и тиол-диоксид кремния (0,1 кг), и полученную смесь нагревали до температуры приблизительно 78 С и в этот момент добавляли воду (6,0 кг). Затем реакционную смесь фильтровали с последующим добавлением изопропанола (38,0 кг) и давали ей остыть до приблизительно 25 С. Продукт извлекали фильтрованием, промывали изопропанолом (20,0 кг) и сушили при приблизительно 65 С с получением указанного в заголовке соединения (5,0 кг). Пример 1 В. ПолучениеN-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамида и его (L)-малатной соли. Другой синтетический способ, который использовали для получения N-(4-[6,7 бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамида и его (L)малатной соли, изображен на фиг. 2 Фиг. 2 Получение 4-хлор-6,7-диметоксихинолина. Реактор загружали последовательно 6,7-диметоксихинолин-4-олом (47,0 кг) и ацетонитрилом (318,8 кг). Полученную смесь нагревали до приблизительно 60 С и добавляли оксихлорид фосфора (POCl3,130,6 кг). После добавления POCl3 температуру этой реакционной смеси повышали до приблизительно 77 С. Реакцию считали завершенной (приблизительно 13 ч), когда оставалось 3% исходного материала(согласно анализу высокоэффективной жидкостной хроматографией [HPLC] в процессе). Эту реакционную смесь охлаждали до приблизительно 2-7 С и затем гасили с использованием охлажденного раствора дихлорметана (ДХМ, 482,8 кг), 26% NH4OH (251,3 кг) и воды (900 л). Полученную смесь нагревали до приблизительно 20-25 С, и фазы разделяли. Органическую фазу фильтровали через слой AW hyflo supercel NF (целит; 5,4 кг) и этот фильтрующий слой промывали ДХМ (118,9 кг). Объединенную органическую фазу промывали солевым раствором (282,9 кг) и смешивали с водой (120 л). Эти фазы разделяли, и органическую фазу концентрировали вакуумной перегонкой с удалением растворителя (приблизительно 95 л оставшегося объема). ДХМ (686,5 кг) загружали в реактор, содержащий органическую фазу, и концентрировали вакуумной перегонкой с удалением растворителя (приблизительно 90 л оставшегося объема). Затем загружали метил-трет-бутиловый эфир (МТВЕ, 226,0 кг), и температуру этой смеси корректировали с -20 до -25 С и поддерживали в течение 2,5 ч, что приводило к твердому осадку, который затем отфильтровывали и промывали н-гептаном (92,0 кг) и сушили на фильтре при приблизительно 25 С в атмосфере азота с получением указанного в заголовке соединения (35,6 кг). Получение 4-(6,7-диметоксихинолин-4-илокси)фениламина. 4-аминофенол (24,4 кг), растворенный в N,N-диметилацетамиде (DMA, 184,3 кг), загружали в реактор, содержащий 4-хлор-6,7-диметоксихинолин (35,3 кг), натрий-трет-бутоксид (21,4 кг) и DMA (167,2 кг) при 20-25 С. Затем эту смесь нагревали до 100-105 С в течение приблизительно 13 ч. После завершения реакции, определяемого с использованием ВЖХ-анализа в процессе (2% оставшегося исходного материала), содержимое реактора охлаждали при 15-20 С и загружали воду (предварительно охлажденную, 2-7 С, 587 л) при скорости, достаточной для поддержания температуры 15-30 С. Полученный осадок твердого вещества отфильтровывали, промывали смесью воды (47 л) и ДМА (89,1 кг) и наконец во- 12024563 дой (214 л). Затем этот фильтровальный осадок сушили при приблизительно 25 С на фильтре с получением неочищенного 4-(6,7-диметоксихинолин-4-илокси) фениламина (59,4 кг сырой массы, 41,6 кг сухой массы, рассчитанной на LOD). Неочищенный 4-(6,7-диметоксихинолин-4-илокси) фениламин нагревали в колбе с обратным холодильником (приблизительно 75 С) в смеси с тетрагидрофураном (ТГФ, 211,4 кг) и ДМА (108,8 кг) в течение приблизительно 1 ч и затем охлаждали до 0-5 С и подвергали старению в течение приблизительно 1 ч, после чего твердое вещество фильтровали, промывали ТГФ (147,6 кг) и сушили на фильтре в вакууме при приблизительно 25 С с получением 4-(6,7-диметоксихинолин-4 илокси)фениламина (34,0 кг). Получение 1-(4-фторфенилкарбамоил)циклопропанкарбоновой кислоты. Триэтиламин (19,5 кг) добавляли к охлажденному (приблизительно 5 С) раствору циклопропан-1,1 дикарбоновой кислоты (24,7 кг) в ТГФ (89,6 кг) при такой скорости, что температура загрузки не превышала 5 С. Раствор перемешивали в течение приблизительно 1,3 ч и затем добавляли тионилхлорид (23,1 кг), поддерживая температуру загрузки ниже 10 С. После завершения добавления этот раствор перемешивали в течение приблизительно 4 ч, поддерживая температуру ниже 10 С. Затем добавляли раствор 4 фторанилина (18,0 кг) в ТГФ (33,1 кг) при такой скорости, что температура загрузки не превышала 10 С. Эту смесь перемешивали в течение приблизительно 10 ч, после чего эту реакция считали завершенной. Затем эту реакционную смесь разбавляли изопропилацетатом (218,1 кг). Этот раствор промывали последовательно водным гидроксидом натрия (10,4 кг, 50% растворенным в 119 л воды), дополнительно разбавляли водой (415 л), затем водой (100 л) и наконец водным раствором хлорида натрия (20,0 кг, растворенным в 100 л воды). Органический раствор концентрировали вакуумной перегонкой (оставшийся объем 100 л) ниже 40 С с последующим добавлением н-гептана (171,4 кг), что приводило к осаждению твердого вещества. Это твердое вещество извлекали фильтрованием и промывали н-гептаном (102,4 кг) с получением сырой неочищенной 1- (4-фторфенилкарбамоил)циклопропанкарбоновой кислоты (29,0 кг). Неочищенную 1-(4-фторфенилкарбамоил)циклопропановую кислоту растворяли в метаноле (139,7 кг) при приблизительно 25 С с последующим добавлением воды (320 л), что приводило к суспензии, которую извлекали фильтрованием, промывали последовательно водой (20 л) и н-гептаном (103,1 кг) и затем сушили на фильтре при приблизительно 25 С в атмосфере азота с получением указанного в заголовке соединения (25,4 кг). Получение 1-(4-фторфенилкарбамоил)циклопропанкарбонилхлорида. Оксалилхлорид (12,6 кг) добавляли к раствору 1-(4-фторфенилкарбамоил)циклопропановой кислоты (22,8 кг) в смеси ТГФ (96,1 кг) и N,N-диметилформамида (ДМФ; 0,23 кг) при такой скорости, что температура загрузки не превышала 25 С. Этот раствор использовали в следующей стадии без дополнительной обработки. Получение [4-(6,7-диметоксихинолин-4-илокси)фенил]амид-(4-фторфенил)амида циклопропан-1,1 дикарбоновой кислоты. Раствор из предыдущей стадии, содержащий 1-(4-фторфенилкарбамоил)циклопропанкарбонилхлорид, добавляли к смеси соединения 4-(6,7-диметоксихинолин-4-илокси)фениламина (23,5 кг) и карбоната калия (31,9 кг) в ТГФ (245,7 кг) и воде (116 л) при такой скорости, что температура загрузки не превышала 30 С. После завершения этой реакции (приблизительно за 20 мин) добавляли воду (653 л). Эту смесь перемешивали при 20-25 С в течение приблизительно 10 ч, что приводило к осаждению этого продукта. Этот продукт извлекали фильтрованием, промывали предварительно приготовленным раствором ТГФ (68,6 кг) и водой (256 л) и сушили сначала на фильтре в атмосфере азота при приблизительно 25 С и затем при приблизительно 45 С в вакууме с получением указанного в заголовке соединения (41,0 кг, 38,1 кг, как рассчитано на основе LOD). Получение (L)-малатной соли [4-(6,7-диметоксихинолин-4-илокси)фенил]амид-(4-фторфенил)амида циклопропан-1,1-дикарбоновой кислоты.[4-(6,7-диметоксихинолин-4-илокси)фенил]амид-(4-фторфенил)амид циклопропан-1,1-дикарбоновой кислоты (1-5; 13,3 кг), L-яблочную кислоту (4,96 кг), метилэтилкетон (МЭК; 188,6 кг) и воду (37,3 кг) загружали в реактор, и эту смесь нагревали с обратным холодильником (приблизительно 74 С) в течение приблизительно 2 ч. Температуру реактора уменьшали до 50-55 С, и содержимое реактора фильтровали. Эти последовательные стадии, описанные выше, повторяли еще два раза, начиная со сходных количеств (1-5, 13,3 кг), L-яблочной кислоты (4,96 кг), МЭК (198,6 кг) и воды (37,2 кг). Объединенный фильтрат сушили азеотропно при атмосферном давлении с использованием МЭК (1133,2 кг) (приблизительный оставшийся объем 711 л; KF0,5% м/м) при приблизительно 74 С. Температуру содержимого реактора уменьшали до 20-25 С и поддерживали в течение приблизительно 4 ч, что приводило к твердому осадку, который отфильтровывали, промывали МЭК (448 кг) и сушили в вакууме при 50 С с получением указанного в заголовке соединения (45,5 кг). Пример 2. Введение соединения N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамида во время одновременной фазы пациентам. Пример 2 А.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1 дикарбоксамид вводят в начале 6-7-недельной одновременной фазы RT и TMZ. Некоторые пациенты,которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7 бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качествеединственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в виде доз 25 и 100 мг (которые могут находиться в капсулах или таблетках). За этой одновременной фазой следует фаза покоя, которая будет продолжаться в течение приблизительно 4 недель.TMZ, когда он вводится, предоставляется в виде доз 5, 20, 100, 250, 140 и 180 мг (которые могут быть в капсулах или таблетках). В другом варианте осуществления начальная доза TMZ равна 75 мг/м 2/день с одновременной RT в течение 6 недель. Для целей этой патентной заявки термин "м 2" относится к площади поверхности тела, измеряемой в квадратных метрах. Пациенты получают RT, состоящую из фракционного локального облучения, вводимого с использованием 1,8-2 Gy на фракцию, один раз в день в течение 5 дней в неделю в течение 6-7 недель с получением общей дозы до 60 Gy. Пример 2 В.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в начале 6-7-недельной одновременной фазы RT и TMZ. Некоторые пациенты, которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7-бис(метилокси)хинолин-4 ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качествеединственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан 1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 мг (которые могут находиться в капсулах или таблетках). За этой одновременной фазой следует фаза покоя, которая будет продолжаться в течение приблизительно 4 недель. TMZ, когда он вводится, предоставляется в виде доз 5 мг (которые могут быть в капсулах или таблетках). Пациенты получают RT, состоящую из фракционного локального облучения, вводимого с использованием 1,8-2 Gy на фракцию,один раз в день в течение 5 дней в неделю в течение 6-7 недель с получением общей дозы до 60 Gy. Пример 2 С.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в начале 6-7-недельной одновременной фазы RT и TMZ. Некоторые пациенты, которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7-бис(метилокси)хинолин-4 ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качествеединственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан 1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 50 мг (которые могут находиться в капсулах или таблетках). За этой одновременной фазой следует фаза покоя, которая будет продолжаться в течение приблизительно 4 недель. TMZ, когда он вводится, предоставляется в виде доз 5 мг (которые могут быть в капсулах или таблетках). Пациенты получают RT, состоящую из фракционного локального облучения, вводимого с использованием 1,8-2 Gy на фракцию,один раз в день в течение 5 дней в неделю в течение 6-7 недель с получением общей дозы до 60 Gy. Пример 2D.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в начале 6-7-недельной одновременной фазы RT и TMZ. Некоторые пациенты, которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7-бис(метилокси)хинолин-4 ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качествеединственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан 1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 75 мг (которые могут находиться в капсулах или таблетках). За этой одновременной фазой следует фаза покоя, которая будет продолжаться в течение приблизительно 4 недель. TMZ, когда он вводится, предоставляется в виде доз 5 мг (которые могут быть в капсулах или таблетках). Пациенты получают RT, состоящую из фракционного локального облучения с использованием 1,8-2 Gy на фракцию, один раз в день в течение 5 дней в неделю в течение 6-7 недель с получением общей дозы до 60 Gy. Пример 2 Е.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в начале 6-7-недельной одновременной фазы RT и TMZ. Некоторые пациенты, которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7-бис(метилокси)хинолин-4 ил]оксифенил)-N'- (4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан 1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). За этой одновременной фазой следует фаза покоя, которая будет продолжаться в течение приблизительно 4 недель. TMZ, когда он вводится, предоставляется в виде доз 5 мг (которые могут быть в капсулах или таблетках). Пациенты получают RT, состоящую из фракционного локального облучения с использованием 1,8-2 Gy на фракцию, один раз в день в течение 5 дней в неделю в течение 6-7 недель с получением общей дозы до 60 Gy. Пример 2F.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в начале 6-7-недельной одновременной фазы RT и TMZ. Некоторые пациенты, которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7-бис(метилокси)хинолин-4 ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качествеединственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан 1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 100 мг (которые могут находиться в капсулах или таблетках). За этой одновременной фазой следует фаза покоя, которая будет продолжаться в течение приблизительно 4 недель. TMZ, когда он вводится, предоставляется в виде доз 20 мг (которые могут быть в капсулах или таблетках). Пациенты получают RT, состоящую из фракционного локального облучения с использованием 1,8-2 Gy на фракцию, один раз в день в течение 5 дней в неделю в течение 6-7 недель с получением общей дозы до 60 Gy. Пример 2G.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в начале 6-7-недельной одновременной фазы RT и TMZ. Некоторые пациенты, которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7-бис(метилокси)хинолин-4 ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качествеединственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан 1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 50 мг (которые могут находиться в капсулах или таблетках). За этой одновременной фазой следует фаза покоя, которая будет продолжаться в течение приблизительно 4 недель. TMZ, когда он вводится, предоставляется в виде доз 20 мг (которые могут быть в капсулах или таблетках). Пациенты получают RT, состоящую из фракционного локального облучения с использованием 1,8-2 Gy на фракцию, один раз в день в течение 5 дней в неделю в течение 6-7 недель с получением общей дозы до 60 Gy. Пример 2 Н.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в начале 6-7-недельной одновременной фазы RT и TMZ. Некоторые пациенты, которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7-бис(метилокси)хинолин-4 ил]оксифенил)-N'- (4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан 1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 75 мг (которые могут находиться в капсулах или таблетках). За этой одновременной фазой следует фаза покоя, которая будет продолжаться в течение приблизительно 4 недель. TMZ, когда он вводится, предоставляется в виде доз 20 мг (которые могут быть в капсулах или таблетках). Пациенты получают RT, состоящую из фракционного локального облучения с использованием 1,8-2 Gy на фракцию, один раз в день в течение 5 дней в неделю в течение 6-7 недель с получением общей дозы до 60 Gy. Пример 2I.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в начале 6-7-недельной одновременной фазы RT и TMZ. Некоторые пациенты, которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7-бис(метилокси)хинолин-4 ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан 1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). За этой одновременной фазой следует фаза покоя, которая будет продолжаться в течение приблизительно 4 недель. TMZ, когда он вводится, предоставляется в виде доз 20 мг (которые могут быть в капсулах или таблетках). Пациенты получают RT, состоящую из фракционного локального облучения с использованием 1,8-2 Gy на фракцию, один раз в день в течение 5 дней в неделю в течение 6-7 недель с получением общей дозы до 60 Gy. Пример 2J.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в начале 6-7-недельной одновременной фазы RT и TMZ. Некоторые пациенты, которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7-бис(метилокси)хинолин-4- 15024563 ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан 1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 100 мг (которые могут находиться в капсулах или таблетках). За этой одновременной фазой следует фаза покоя, которая будет продолжаться в течение приблизительно 4 недель. TMZ, когда он вводится, предоставляется в виде доз 20 мг (которые могут быть в капсулах или таблетках). Пациенты получают RT, состоящую из фракционного локального облучения с использованием 1,8-2 Gy на фракцию, один раз в день в течение 5 дней в неделю в течение 6-7 недель с получением общей дозы до 60 Gy. Пример 2K.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в начале 6-7-недельной одновременной фазы RT и TMZ. Некоторые пациенты, которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7-бис(метилокси)хинолин-4 ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан 1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 мг (которые могут находиться в капсулах или таблетках). За этой одновременной фазой следует фаза покоя, которая будет продолжаться в течение приблизительно 4 недель. TMZ, когда он вводится, предоставляется в виде доз 100 мг (которые могут быть в капсулах или таблетках). Пациенты получают RT,состоящую из фракционного локального облучения с использованием 1,8-2 Gy на фракцию, один раз в день в течение 5 дней в неделю в течение 6-7 недель с получением общей дозы до 60 Gy. Пример 2L. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан 1,1-дикарбоксамид вводят в начале 6-7-недельной одновременной фазы RT и TMZ. Некоторые пациенты,которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7 бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 50 мг (которые могут находиться в капсулах или таблетках). За этой одновременной фазой следует фаза покоя, которая будет продолжаться в течение приблизительно 4 недель. TMZ,когда он вводится, предоставляется в виде доз 100 мг (которые могут быть в капсулах или таблетках). Пациенты получают RT, состоящую из фракционного локального облучения с использованием 1,8-2 Gy на фракцию, один раз в день в течение 5 дней в неделю в течение 6-7 недель с получением общей дозы до 60 Gy. Пример 2 М.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в начале 6-7-недельной одновременной фазы RT и TMZ. Некоторые пациенты, которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7-бис(метилокси)хинолин-4 ил]оксифенил)-N'- (4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан 1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 75 мг (которые могут находиться в капсулах или таблетках). За этой одновременной фазой следует фаза покоя, которая будет продолжаться в течение приблизительно 4 недель. TMZ, когда он вводится, предоставляется в виде доз 100 мг (которые могут быть в капсулах или таблетках). Пациенты получают RT,состоящую из фракционного локального облучения с использованием 1,8-2 Gy на фракцию, один раз в день в течение 5 дней в неделю в течение 6-7 недель, с получением общей дозы до 60 Gy. Пример 2N.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в начале 6-7-недельной одновременной фазы RT и TMZ. Некоторые пациенты, которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7-бис(метилокси)хинолин-4 ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан 1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). За этой одновременной фазой следует фаза покоя, которая будет продолжаться в течение приблизительно 4 недель. TMZ, когда он вводится, предоставляется в виде доз 100 мг (которые могут быть в капсулах или таблетках). Пациенты получают RT,состоящую из фракционного локального облучения с использованием 1,8-2 Gy на фракцию, один раз в день в течение 5 дней в неделю в течение 6-7 недель с получением общей дозы до 60 Gy. Пример 2O. самид вводят в начале 6-7-недельной одновременной фазы RT и TMZ. Некоторые пациенты, которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7-бис(метилокси)хинолин-4 ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан 1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 100 мг (которые могут находиться в капсулах или таблетках). За этой одновременной фазой следует фаза покоя, которая будет продолжаться в течение приблизительно 4 недель. TMZ, когда он вводится, предоставляется в виде доз 100 мг (которые могут быть в капсулах или таблетках). Пациенты получают RT,состоящую из фракционного локального облучения с использованием 1,8-2 Gy на фракцию, один раз в день в течение 5 дней в неделю в течение 6-7 недель с получением общей дозы до 60 Gy. Пример 2 Р.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в начале 6-7-недельной одновременной фазы RT и TMZ. Некоторые пациенты, которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7-бис(метилокси)хинолин-4 ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан 1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 мг (которые могут находиться в капсулах или таблетках). За этой одновременной фазой следует фаза покоя, которая будет продолжаться в течение приблизительно 4 недель. TMZ, когда он вводится, предоставляется в виде доз 140 мг (которые могут быть в капсулах или таблетках). Пациенты получают RT,состоящую из фракционного локального облучения с использованием 1,8-2 Gy на фракцию, один раз в день в течение 5 дней в неделю в течение 6-7 недель с получением общей дозы до 60 Gy. Пример 2Q.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в начале 6-7-недельной одновременной фазы RT и TMZ. Некоторые пациенты, которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7-бис(метилокси)хинолин-4 ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан 1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 50 мг (которые могут находиться в капсулах или таблетках). За этой одновременной фазой следует фаза покоя, которая будет продолжаться в течение приблизительно 4 недель. TMZ, когда он вводится, предоставляется в виде доз 140 мг (которые могут быть в капсулах или таблетках). Пациенты получают RT,состоящую из фракционного локального облучения с использованием 1,8-2 Gy на фракцию, один раз в день в течение 5 дней в неделю в течение 6-7 недель с получением общей дозы до 60 Gy. Пример 2R.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в начале 6-7-недельной одновременной фазы RT и TMZ. Некоторые пациенты, которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7-бис(метилокси)хинолин-4 ил]оксифенил)-N'- (4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан 1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 75 мг (которые могут находиться в капсулах или таблетках). За этой одновременной фазой следует фаза покоя, которая будет продолжаться в течение приблизительно 4 недель. TMZ, когда он вводится, предоставляется в виде доз 140 мг (которые могут быть в капсулах или таблетках). Пациенты получают RT,состоящую из фракционного локального облучения с использованием 1,8-2 Gy на фракцию, один раз в день в течение 5 дней в неделю в течение 6-7 недель с получением общей дозы до 60 Gy. Пример 2S.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в начале 6-7-недельной одновременной фазы RT и TMZ. Некоторые пациенты, которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7-бис(метилокси)хинолин-4 ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан 1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). За этой одновременной фазой следует фаза покоя, которая будет продолжаться в течение приблизительно 4 недель. TMZ, когда он вводится, предоставляется в виде доз 140 мг (которые могут быть в капсулах или таблетках). Пациенты получают RT,состоящую из фракционного локального облучения с использованием 1,8-2 Gy на фракцию, один раз в день в течение 5 дней в неделю в течение 6-7 недель с получением общей дозы до 60 Gy. Пример 2 Т.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в начале 6-7-недельной одновременной фазы RT и TMZ. Некоторые пациенты, которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7-бис(метилокси)хинолин-4 ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан 1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 100 мг (которые могут находиться в капсулах или таблетках). За этой одновременной фазой следует фаза покоя, которая будет продолжаться в течение приблизительно 4 недель. TMZ, когда он вводится, предоставляется в виде доз 140 мг (которые могут быть в капсулах или таблетках). Пациенты получают RT,состоящую из фракционного локального облучения с использованием 1,8-2 Gy на фракцию, один раз в день в течение 5 дней в неделю в течение 6-7 недель с получением общей дозы до 60 Gy. Пример 2U.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в начале 6-7-недельной одновременной фазы RT и TMZ. Некоторые пациенты, которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7-бис(метилокси)хинолин-4 ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан 1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 мг (которые могут находиться в капсулах или таблетках). За этой одновременной фазой следует фаза покоя, которая будет продолжаться в течение приблизительно 4 недель. TMZ, когда он вводится, предоставляется в виде доз 180 мг (которые могут быть в капсулах или таблетках). Пациенты получают RT,состоящую из фракционного локального облучения с использованием 1,8-2 Gy на фракцию, один раз в день в течение 5 дней в неделю в течение 6-7 недель с получением общей дозы до 60 Gy. Пример 2V.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в начале 6-7-недельной одновременной фазы RT и TMZ. Некоторые пациенты, которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7-бис(метилокси)хинолин-4 ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан 1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 50 мг (которые могут находиться в капсулах или таблетках). За этой одновременной фазой следует фаза покоя, которая будет продолжаться в течение приблизительно 4 недель. TMZ, когда он вводится, предоставляется в виде доз 180 мг (которые могут быть в капсулах или таблетках). Пациенты получают RT,состоящую из фракционного локального облучения с использованием 1,8-2 Gy на фракцию, один раз в день в течение 5 дней в неделю в течение 6-7 недель с получением общей дозы до 60 Gy. Пример 2W.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в начале 6-7-недельной одновременной фазы RT и TMZ. Некоторые пациенты, которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7-бис(метилокси)хинолин-4 ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан 1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 75 мг (которые могут находиться в капсулах или таблетках). За этой одновременной фазой следует фаза покоя, которая будет продолжаться в течение приблизительно 4 недель. TMZ, когда он вводится, предоставляется в виде доз 180 мг (которые могут быть в капсулах или таблетках). Пациенты получают RT,состоящую из фракционного локального облучения с использованием 1,8-2 Gy на фракцию, один раз в день в течение 5 дней в неделю в течение 6-7 недель с получением общей дозы до 60 Gy. Пример 2 Х.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в начале 6-7-недельной одновременной фазы RT и TMZ. Некоторые пациенты, которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7-бис(метилокси)хинолин-4 ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан 1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). За этой одновременной фазой следует фаза покоя, которая будет продолжаться в течение приблизительно 4 недель. TMZ, когда он вводится, предоставляется в виде доз 180 мг (которые могут быть в капсулах или таблетках). Пациенты получают RT,состоящую из фракционного локального облучения с использованием 1,8-2 Gy на фракцию, один раз в день в течение 5 дней в неделю в течение 6-7 недель с получением общей дозы до 60 Gy. Пример 2Y.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в начале 6-7-недельной одновременной фазы RT и TMZ. Некоторые пациенты, которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7-бис(метилокси)хинолин-4 ил]оксифенил)-N'- (4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан 1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 100 мг (которые могут находиться в капсулах или таблетках). За этой одновременной фазой следует фаза покоя, которая будет продолжаться в течение приблизительно 4 недель. TMZ, когда он вводится, предоставляется в виде доз 180 мг (которые могут быть в капсулах или таблетках). Пациенты получают RT,состоящую из фракционного локального облучения с использованием 1,8-2 Gy на фракцию, один раз в день в течение 5 дней в неделю в течение 6-7 недель с получением общей дозы до 60 Gy. Пример 2Z.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в начале 6-7-недельной одновременной фазы RT и TMZ. Некоторые пациенты, которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7-бис(метилокси)хинолин-4 ил]оксифенил)-N'- (4-фторфенил)циклопропан-1,1-дикарбоксамид в качест-ве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан 1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 мг (которые могут находиться в капсулах или таблетках). За этой одновременной фазой следует фаза покоя, которая будет продолжаться в течение приблизительно 4 недель. TMZ, когда он вводится, предоставляется в виде доз 250 мг (которые могут быть в капсулах или таблетках). Пациенты получают RT,состоящую из фракционного локального облучения с использованием 1,8-2 Gy на фракцию, один раз в день в течение 5 дней в неделю в течение 6-7 недель с получением общей дозы до 60 Gy. Пример 2 АА.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в начале 6-7-недельной одновременной фазы RT и TMZ. Некоторые пациенты, которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7-бис(метилокси)хинолин-4 ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан 1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 50 мг (которые могут находиться в капсулах или таблетках). За этой одновременной фазой следует фаза покоя, которая будет продолжаться в течение приблизительно 4 недель. TMZ, когда он вводится, предоставляется в виде доз 250 мг (которые могут быть в капсулах или таблетках). Пациенты получают RT,состоящую из фракционного локального облучения с использованием 1,8-2 Gy на фракцию, один раз в день в течение 5 дней в неделю в течение 6-7 недель с получением общей дозы до 60 Gy. Пример 2 АВ.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в начале 6-7-недельной одновременной фазы RT и TMZ. Некоторые пациенты, которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7-бис(метилокси)хинолин-4 ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан 1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 75 мг (которые могут находиться в капсулах или таблетках). За этой одновременной фазой следует фаза покоя, которая будет продолжаться в течение приблизительно 4 недель. TMZ, когда он вводится, предоставляется в виде доз 250 мг (которые могут быть в капсулах или таблетках). Пациенты получают RT,состоящую из фракционного (парциального) локального облучения с использованием 1,8-2 Gy на фракцию, один раз в день в течение 5 дней в неделю в течение 6-7 недель с получением общей дозы до 60 Gy. Пример 2 АС.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в начале 6-7-недельной одновременной фазы RT и TMZ. Некоторые пациенты, которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7-бис(метилокси)хинолин-4 ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан 1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). За этой одновременной фазой следует фаза покоя, которая будет продолжаться в течение приблизительно 4 недель. TMZ, когда он вводится, предоставляется в виде доз 250 мг (которые могут быть в капсулах или таблетках). Пациенты получают RT,состоящую из фракционного (парциального) локального облучения с использованием 1,8-2 Gy на фракцию, один раз в день в течение 5 дней в неделю в течение 6-7 недель с получением общей дозы до 60 Gy. Пример 2AD.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в начале 6-7-недельной одновременной фазы RT и TMZ. Некоторые пациенты, которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7-бис(метилокси)хинолин-4 ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан 1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 100 мг (которые могут находиться в капсулах или таблетках). За этой одновременной фазой следует фаза покоя, которая будет продолжаться в течение приблизительно 4 недель. TMZ, когда он вводится, предоставляется в виде доз 250 мг (которые могут быть в капсулах или таблетках). Пациенты получают RT,состоящую из фракционного (парциального) локального облучения с использованием 1,8-2 Gy на фракцию, один раз в день в течение 5 дней в неделю в течение 6-7 недель с получением общей дозы до 60 Gy. Пример 3. Введение соединения N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамида во время одновременной фазы пациентам. Пример 3 А.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). Некоторые пациенты, которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7 бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). TMZ, когда он вводится, предоставляется в виде доз 5, 20, 100, 250, 140, 180 и 200 мг (которые могут находиться в капсулах или таблетках), предоставляемых в течение 5 последовательных дней и повторяемых каждые 28 дней. Для целей этого описания термин м 2 предназначен для обозначения площади поверхности тела в пациентах, измеряемой в квадратных метрах. Фаза поддержания в примере 3 А может быть объединена с одновременной фазой любого из примеров 2 А, 2 В, 2 С, 2D, 2 Е, 2F, 2G, 2 Н, 2I, 2J, 2K, 2L, 2 М, 2N, 2O, 2 Р,2Q, 2R, 2S, 2 Т, 2U, 2V, 2W, 2 Х, 2Y, 2Z, 2 АА, 2 АВ, 2 АС и 2AD. Пример 3 В.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в дозах 25 мг (которые могут находиться в капсулах или таблетках). Некоторые пациенты,которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7 бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). TMZ, когда он вводится, предоставляется в виде доз 5 мг (которые могут находиться в капсулах или таблетках), предоставляемых в течение 5 последовательных дней и повторяемых каждые 28 дней. Фаза поддержания в примере 3 В может быть объединена с одновременной фазой любого из примеров 2 А, 2 В, 2 С, 2D, 2 Е, 2F,2G, 2 Н, 2I, 2J, 2K, 2L, 2 М, 2N, 2O, 2 Р, 2Q, 2R, 2S, 2 Т, 2U, 2V, 2W, 2 Х, 2Y, 2Z, 2 АА, 2 АВ, 2 АС и 2AD. Пример 3 С.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в дозах 50 мг (которые могут находиться в капсулах или таблетках). Некоторые пациенты,которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7 бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). TMZ, когда он вводится, предоставляется в виде доз 5 мг (которые могут находиться в капсулах или таблетках), предоставляемых в течение 5 последовательных дней и повторяемых каждые 28 дней. Фаза поддержания в примере 3 С может быть объединена с одновременной фазой любого из примеров 2 А, 2 В, 2 С, 2D, 2 Е, 2F,- 20024563N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в дозах 75 мг (которые могут находиться в капсулах или таблетках). Некоторые пациенты,которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7 бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). TMZ, когда он вводится, предоставляется в виде доз 5 мг (которые могут находиться в капсулах или таблетках), предоставляемых в течение 5 последовательных дней и повторяемых каждые 28 дней. Фаза поддержания в примере 3D может быть объединена с одновременной фазой любого из примеров 2 А, 2 В, 2 С, 2D, 2 Е, 2F,2G, 2 Н, 2I, 2J, 2K, 2L, 2 М, 2N, 2O, 2 Р, 2Q, 2R, 2S, 2 Т, 2U, 2V, 2W, 2 Х, 2Y, 2Z, 2 АА, 2 АВ, 2 АС и 2AD. Пример 3 Е.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в дозах 100 мг (которые могут находиться в капсулах или таблетках). Некоторые пациенты,которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7 бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). TMZ, когда он вводится, предоставляется в виде доз 5 мг (которые могут находиться в капсулах или таблетках), предоставляемых в течение 5 последовательных дней и повторяемых каждые 28 дней. Фаза поддержания в примере 3 Е может быть объединена с одновременной фазой любого из примеров 2 А, 2 В, 2 С, 2D, 2 Е, 2F,2G, 2 Н, 2I, 2J, 2K, 2L, 2 М, 2N, 2O, 2 Р, 2Q, 2R, 2S, 2 Т, 2U, 2V, 2W, 2 Х, 2Y, 2Z, 2 АА, 2 АВ, 2 АС и 2AD. Пример 3F.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в дозах 25 мг (которые могут находиться в капсулах или таблетках). Некоторые пациенты,которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7 бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). TMZ, когда он вводится, предоставляется в виде доз 20 мг (которые могут находиться в капсулах или таблетках), предоставляемых в течение 5 последовательных дней и повторяемых каждые 28 дней. Фаза поддержания в примере 3F может быть объединена с одновременной фазой любого из примеров 2 А, 2 В, 2 С, 2D, 2 Е, 2F,2G, 2 Н, 2I, 2J, 2K, 2L, 2 М, 2N, 2O, 2 Р, 2Q, 2R, 2S, 2 Т, 2U, 2V, 2W, 2 Х, 2Y, 2Z, 2 АА, 2 АВ, 2 АС и 2AD. Пример 3G.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в дозах 50 мг (которые могут находиться в капсулах или таблетках). Некоторые пациенты,которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7 бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). TMZ, когда он вводится, предоставляется в виде доз 20 мг (которые могут находиться в капсулах или таблетках), предоставляемых в течение 5 последовательных дней и повторяемых каждые 28 дней. Фаза поддержания в примере 3G может быть объединена с одновременной фазой любого из примеров 2 А, 2 В, 2 С, 2D, 2 Е, 2F,2G, 2 Н, 2I, 2J, 2K, 2L, 2 М, 2N, 2O, 2 Р, 2Q, 2R, 2S, 2 Т, 2U, 2V, 2W, 2 Х, 2Y, 2Z, 2 АА, 2 АВ, 2 АС и 2AD. Пример 3 Н.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в дозах 75 мг (которые могут находиться в капсулах или таблетках). Некоторые пациенты,которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7 бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). TMZ, когда он вводится, предоставляется в виде доз 20 мг (которые могут находиться в капсулах или таблетках), предоставляемых в течение 5 последовательных дней и повторяемых каждые 28 дней. Фаза поддержания в примере 3 Н может быть объединена с одновременной фазой любого из примеров 2 А, 2 В, 2 С, 2D, 2 Е, 2F,2G, 2 Н, 2I, 2J, 2K, 2L, 2 М, 2N, 2O, 2 Р, 2Q, 2R, 2S, 2 Т, 2U, 2V, 2W, 2 Х, 2Y, 2Z, 2 АА, 2 АВ, 2 АС и 2AD. Пример 3I.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в дозах 100 мг (которые могут находиться в капсулах или таблетках). Некоторые пациенты,которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7 бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). TMZ, когда он вводится, предоставляется в виде доз 20 мг (которые могут находиться в капсулах или таблетках), предоставляемых в течение 5 последовательных дней и повторяемых каждые 28 дней. Фаза поддержания в примере 31 может быть объединена с одновременной фазой любого из примеров 2 А, 2 В, 2 С, 2D, 2 Е, 2F,2G, 2 Н, 2I, 2J, 2K, 2L, 2 М, 2N, 2O, 2 Р, 2Q, 2R, 2S, 2 Т, 2U, 2V, 2W, 2 Х, 2Y, 2Z, 2 АА, 2 АВ, 2 АС и 2AD. Пример 3J.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в дозах 2 5 мг (которые могут находиться в капсулах или таблетках). Некоторые пациенты,которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7 бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). TMZ, когда он вводится, предоставляется в виде доз 100 мг (которые могут находиться в капсулах или таблетках), предоставляемых в течение 5 последовательных дней и повторяемых каждые 28 дней. Фаза поддержания в примере 3J может быть объединена с одновременной фазой любого из примеров 2 А, 2 В, 2 С, 2D, 2 Е, 2F,2G, 2 Н, 2I, 2J, 2K, 2L, 2 М, 2N, 2O, 2 Р, 2Q, 2R, 2S, 2 Т, 2U, 2V, 2W, 2 Х, 2Y, 2Z, 2 АА, 2 АВ, 2 АС и 2AD. Пример 3K.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в дозах 50 мг (которые могут находиться в капсулах или таблетках). Некоторые пациенты,которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7 бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). TMZ, когда он вводится, предоставляется в виде доз 100 мг (которые могут находиться в капсулах или таблетках), предоставляемых в течение 5 последовательных дней и повторяемых каждые 28 дней. Фаза поддержания в примере 3K может быть объединена с одновременной фазой любого из примеров 2 А, 2 В, 2 С, 2D, 2 Е, 2F,2G, 2 Н, 2I, 2J, 2K, 2L, 2 М, 2N, 2O, 2 Р, 2Q, 2R, 2S, 2 Т, 2U, 2V, 2W, 2 Х, 2Y, 2Z, 2 АА, 2 АВ, 2 АС и 2AD. Пример 3L.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в дозах 75 мг (которые могут находиться в капсулах или таблетках). Некоторые пациенты,которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7 бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'- (4 фторфенил)циклопропан-1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). TMZ, когда он вводится, предоставляется в виде доз 100 мг (которые могут находиться в капсулах или таблетках), предоставляемых в течение 5 последовательных дней и повторяемых каждые 28 дней. Фаза поддержания в примере 3L может быть объединена с одновременной фазой любого из примеров 2 А, 2 В, 2 С, 2D, 2 Е, 2F,2G, 2 Н, 2I, 2J, 2K, 2L, 2 М, 2N, 2O, 2 Р, 2Q, 2R, 2S, 2 Т, 2U, 2V, 2W, 2 Х, 2Y, 2Z, 2 АА, 2 АВ, 2 АС и 2AD. Пример 3 М.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в дозах 100 мг (которые могут находиться в капсулах или таблетках). Некоторые пациенты,которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7 бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). TMZ, когда он вводится, предоставляется в виде доз 100 мг (которые могут находиться в капсулах или таблетках), предоставляемых в течение 5 последовательных дней и повторяемых каждые 28 дней. Фаза поддержания в примере 3 М может быть объединена с одновременной фазой любого из примеров 2 А, 2 В, 2 С, 2D, 2 Е, 2F,2G, 2 Н, 2I, 2J, 2K, 2L, 2 М, 2N, 2O, 2 Р, 2Q, 2R, 2S, 2 Т, 2U, 2V, 2W, 2 Х, 2Y, 2Z, 2 АА, 2 АВ, 2 АС и 2AD. Пример 3N.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в дозах 25 мг (которые могут находиться в капсулах или таблетках). Некоторые пациенты,которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7 бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). TMZ, когда он вводится, предоставляется в виде доз 140 мг (которые могут находиться в капсулах или таблетках), предоставляемых в течение 5 последовательных дней и повторяемых каждые 28 дней. Фаза поддержания в примере 3N может быть объединена с одновременной фазой любого из примеров 2 А, 2 В, 2 С, 2D, 2 Е, 2F,2G, 2 Н, 2I, 2J, 2K, 2L, 2 М, 2N, 2O, 2 Р, 2Q, 2R, 2S, 2 Т, 2U, 2V, 2W, 2 Х, 2Y, 2Z, 2 АА, 2 АВ, 2 АС и 2AD. Пример 3 О.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в дозах 50 мг (которые могут находиться в капсулах или таблетках). Некоторые пациенты,которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7 бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). TMZ, когда он вводится, предоставляется в виде доз 140 мг (которые могут находиться в капсулах или таблетках), предоставляемых в течение 5 последовательных дней и повторяемых каждые 28 дней. Фаза поддержания в примере 30 может быть объединена с одновременной фазой любого из примеров 2 А, 2 В, 2 С, 2D, 2 Е, 2F,2G, 2 Н, 2I, 2J, 2K, 2L, 2 М, 2N, 2O, 2 Р, 2Q, 2R, 2S, 2 Т, 2U, 2V, 2W, 2 Х, 2Y, 2Z, 2 АА, 2 АВ, 2 АС и 2AD. Пример 3 Р.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в дозах 75 мг (которые могут находиться в капсулах или таблетках). Некоторые пациенты,которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7 бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). TMZ, когда он вводится, предоставляется в виде доз 140 мг (которые могут находиться в капсулах или таблетках), предоставляемых в течение 5 последовательных дней и повторяемых каждые 28 дней. Фаза поддержания в примере 3 Р может быть объединена с одновременной фазой любого из примеров 2 А, 2 В, 2 С, 2D, 2 Е, 2F,2G, 2 Н, 2I, 2J, 2K, 2L, 2 М, 2N, 2O, 2 Р, 2Q, 2R, 2S, 2 Т, 2U, 2V, 2W, 2 Х, 2Y, 2Z, 2 АА, 2 АВ, 2 АС и 2AD. Пример 3Q.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в дозах 100 мг (которые могут находиться в капсулах или таблетках). Некоторые пациенты,которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7 бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). TMZ, когда он вводится, предоставляется в виде доз 140 мг (которые могут находиться в капсулах или таблетках), предоставляемых в течение 5 последовательных дней и повторяемых каждые 28 дней. Фаза поддержания в примере 3Q может быть объединена с одновременной фазой любого из примеров 2 А, 2 В, 2 С, 2D, 2 Е, 2F,2G, 2 Н, 2I, 2J, 2K, 2L, 2 М, 2N, 2O, 2 Р, 2Q, 2R, 2S, 2 Т, 2U, 2V, 2W, 2 Х, 2Y, 2Z, 2 АА, 2 АВ, 2 АС и 2AD. Пример 3R. которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7 бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). TMZ, когда он вводится, предоставляется в виде доз 180 мг (которые могут находиться в капсулах или таблетках), предоставляемых в течение 5 последовательных дней и повторяемых каждые 28 дней. Фаза поддержания в примере 3R может быть объединена с одновременной фазой любого из примеров 2 А, 2 В, 2 С, 2D, 2 Е, 2F,2G, 2 Н, 2I, 2J, 2K, 2L, 2 М, 2N, 2O, 2 Р, 2Q, 2R, 2S, 2 Т, 2U, 2V, 2W, 2 Х, 2Y, 2Z, 2 АА, 2 АВ, 2 АС и 2AD. Пример 3S.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в дозах 50 мг (которые могут находиться в капсулах или таблетках). Некоторые пациенты,которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7 бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). TMZ, когда он вводится, предоставляется в виде доз 180 мг (которые могут находиться в капсулах или таблетках), предоставляемых в течение 5 последовательных дней и повторяемых каждые 28 дней. Фаза поддержания в примере 3S может быть объединена с одновременной фазой любого из примеров 2 А, 2 В, 2 С, 2D, 2 Е, 2F,2G, 2 Н, 2I, 2J, 2K, 2L, 2 М, 2N, 2O, 2 Р, 2Q, 2R, 2S, 2 Т, 2U, 2V, 2W, 2 Х, 2Y, 2Z, 2 АА, 2 АВ, 2 АС И 2AD. Пример 3 Т.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в дозах 75 мг (которые могут находиться в капсулах или таблетках). Некоторые пациенты,которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7 бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). TMZ, когда он вводится, предоставляется в виде доз 180 мг (которые могут находиться в капсулах или таблетках), предоставляемых в течение 5 последовательных дней и повторяемых каждые 28 дней. Фаза поддержания в примере 3 Т может быть объединена с одновременной фазой любого из примеров 2 А, 2 В, 2 С, 2D, 2 Е, 2F,2G, 2 Н, 2I, 2J, 2K, 2L, 2 М, 2N, 2O, 2 Р, 2Q, 2R, 2S, 2 Т, 2U, 2V, 2W, 2 Х, 2Y, 2Z, 2 АА, 2 АВ, 2 АС и 2AD. Пример 3U.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в дозах 100 мг (которые могут находиться в капсулах или таблетках). Некоторые пациенты,которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7 бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). TMZ, когда он вводится, предоставляется в виде доз 180 мг (которые могут находиться в капсулах или таблетках), предоставляемых в течение 5 последовательных дней и повторяемых каждые 28 дней. Фаза поддержания в примере 3U может быть объединена с одновременной фазой любого из примеров 2 А, 2 В, 2 С, 2D, 2 Е, 2F,2G, 2 Н, 2I, 2J, 2K, 2L, 2 М, 2N, 2O, 2 Р, 2Q, 2R, 2S, 2 Т, 2U, 2V, 2W, 2 Х, 2Y, 2Z, 2 АА, 2 АВ, 2 АС и 2AD. Пример 3V.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в дозах 25 мг (которые могут находиться в капсулах или таблетках). Некоторые пациенты,которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7 бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). TMZ, когда он вводится, предоставляется в виде доз 200 мг/м 2/день, предоставляемых в течение 5 последовательных дней и повторяемых каждые 28 дней. Фаза поддержания в примере 3V может быть объединена с одновременной фазой любого из примеров 2 А, 2 В, 2 С, 2D, 2 Е, 2F, 2G, 2 Н, 2I, 2J, 2K, 2L, 2 М, 2N, 2O, 2 Р, 2Q,2R, 2S, 2 Т, 2U, 2V, 2W, 2 Х, 2Y, 2Z, 2 АА, 2 АВ, 2 АС и 2AD.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в дозах 50 мг (которые могут находиться в капсулах или таблетках). Некоторые пациенты,которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7 бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). TMZ, когда он вводится, предоставляется в виде доз 200 мг/м 2/день, предоставляемых в течение 5 последовательных дней и повторяемых каждые 28 дней. Фаза поддержания в примере 3W может быть объединена с одновременной фазой любого из примеров 2 А, 2 В, 2 С, 2D, 2 Е, 2F, 2G, 2 Н, 2I, 2J, 2K, 2L, 2 М, 2N, 2O, 2 Р, 2Q,2R, 2S, 2 Т, 2U, 2V, 2W, 2 Х, 2Y, 2Z, 2 АА, 2 АВ, 2 АС И 2AD. Пример 3 Х.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в дозах 75 мг (которые могут находиться в капсулах или таблетках). Некоторые пациенты,которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7 бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). TMZ, когда он вводится, предоставляется в виде доз 200 мг/м 2/день, предоставляемых в течение 5 последовательных дней и повторяемых каждые 28 дней. Фаза поддержания в примере 3 Х может быть объединена с одновременной фазой любого из примеров 2 А, 2 В, 2 С, 2D, 2 Е, 2F, 2G, 2 Н, 2I, 2J, 2K, 2L, 2 М, 2N, 2O, 2 Р, 2Q,2R, 2S, 2 Т, 2U, 2V, 2W, 2 Х, 2Y, 2Z, 2 АА, 2 АВ, 2 АС и 2AD. Пример 3Y.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в дозах 100 мг (которые могут находиться в капсулах или таблетках). Некоторые пациенты,которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7 бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). TMZ, когда он вводится, предоставляется в виде доз 200 мг/м 2/день, предоставляемых в течение 5 последовательных дней и повторяемых каждые 28 дней. Фаза поддержания в примере 3Y может быть объединена с одновременной фазой любого из примеров 2 А, 2 В, 2 С, 2D, 2 Е, 2F, 2G, 2 Н, 2I, 2J, 2K, 2L, 2 М, 2N, 2O, 2 Р, 2Q,2R, 2S, 2 Т, 2U, 2V, 2W, 2 Х, 2Y, 2Z, 2 АА, 2 АВ, 2 АС и 2AD. Пример 3Z.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в дозах 25 мг (которые могут находиться в капсулах или таблетках). Некоторые пациенты,которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7 бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). TMZ, когда он вводится, предоставляется в виде доз 250 мг (которые могут находиться в капсулах или таблетках), предоставляемых в течение 5 последовательных дней и повторяемых каждые 28 дней. Фаза поддержания в примере 3Z может быть объединена с одновременной фазой любого из примеров 2 А, 2 В, 2 С, 2D, 2 Е, 2F,2G, 2 Н, 2I, 2J, 2K, 2L, 2 М, 2N, 2O, 2 Р, 2Q, 2R, 2S, 2 Т, 2U, 2V, 2W, 2 Х, 2Y, 2Z, 2 АА, 2 АВ, 2 АС И 2AD. Пример 3 АА.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в дозах 50 мг (которые могут находиться в капсулах или таблетках). Некоторые пациенты,которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7 бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). TMZ, когда он вводится, предоставляется в виде доз 250 мг (которые могут находиться в капсулах или таблетках), пре- 25024563 доставляемых в течение 5 последовательных дней и повторяемых каждые 28 дней. Фаза поддержания в примере 3 АА может быть объединена с одновременной фазой любого из примеров 2 А, 2 В, 2 С, 2D, 2 Е,2F, 2G, 2 Н, 2I, 2J, 2K, 2L, 2 М, 2N, 2O, 2 Р, 2Q, 2R, 2S, 2 Т, 2U, 2V, 2W, 2 Х, 2Y, 2Z, 2 АА, 2 АВ, 2 АС и 2AD. Пример 3 АВ.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в дозах 75 мг (которые могут находиться в капсулах или таблетках). Некоторые пациенты,которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7 бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). TMZ, когда он вводится, предоставляется в виде доз 200 мг/м 2/день, предоставляемых в течение 5 последовательных дней и повторяемых каждые 28 дней. Фаза поддержания в примере 3 АВ может быть объединена с одновременной фазой любого из примеров 2 А, 2 В, 2 С, 2D, 2 Е, 2F, 2G, 2 Н, 2I, 2J, 2K, 2L, 2 М, 2N, 2O, 2 Р, 2Q,2R, 2S, 2 Т, 2U, 2V, 2W, 2 Х, 2Y, 2Z, 2 АА, 2 АВ, 2 АС и 2AD. Пример 3 АС.N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид вводят в дозах 100 мг (которые могут находиться в капсулах или таблетках). Некоторые пациенты,которые имеют мутацию в промоторе МГМТ, где мутированный промотор МГМТ является неметилированным промотором, могут не получать TMZ и вместо этого получают N-(4-[6,7 бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4-фторфенил)циклопропан-1,1-дикарбоксамид в качестве единственного агента в комбинации с RT. N-(4-[6,7-бис(метилокси)хинолин-4-ил]оксифенил)-N'-(4 фторфенил)циклопропан-1,1-дикарбоксамид вводят в качестве единственного перорального агента, предоставляемого в дозах 25 и 100 мг (которые могут находиться в капсулах или таблетках). TMZ, когда он вводится, предоставляется в виде доз 250 мг (которые могут находиться в капсулах или таблетках), предоставляемых в течение 5 последовательных дней и повторяемых каждые 28 дней. Фаза поддержания в примере 3 АС может быть объединена с одновременной фазой любого из примеров 2 А, 2 В, 2 С, 2D, 2 Е,2F, 2G, 2 Н, 2I, 2J, 2K, 2L, 2 М, 2N, 2O, 2 Р, 2Q, 2R, 2S, 2 Т, 2U, 2V, 2W, 2 Х, 2Y, 2Z, 2 АА, 2 АВ, 2 АС и 2AD. Предыдущее раскрытие изобретения было описано подробно посредством иллюстрации и примеров для целей ясности и понимания. Настоящее изобретение было описано со ссылкой на различные конкретные и предпочтительные варианты и способы осуществления. Однако, должно быть понятно, что могут быть произведены многочисленные вариации и модификации без отклонения от идеи и объема данного изобретения. Квалифицированному в данной области специалисту будет очевидно, что изменения и модификации могут быть применены на практике в пределах объема прилагаемой формулы изобретения. Таким образом, должно быть понятно, что представленное выше описание предназначено для иллюстрации и не является ограничивающим. Таким образом, объем настоящего изобретения не должен определяться ссылкой на представленное выше описание, а должен вместо этого определяться ссылкой на следующую прилагаемую формулу изобретения, вместе с полным объемом эквивалентов, на которые эта формула изобретения дает право. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Применение соединения, имеющего структуру или его фармацевтически приемлемой соли в комбинации с темозоломидом и лучевой терапией(RT) для лечения рака, который выбран из астроцитомы, глиобластомы, гигантоклеточной глиобластомы, глиосаркомы и глиобластомы с олигодендроглиальными компонентами. 2. Применение по п.1, где соединение представлено следующей структурой: 3. Применение по п.1, где соединение или его фармацевтически приемлемую соль вводят в составе фармацевтической композиции, содержащей фармацевтически приемлемый носитель, эксципиент или разбавитель. 4. Применение по п.1, где одновременная фаза равна 6-7 неделям по продолжительности, фаза покоя равна приблизительно 4 неделям по продолжительности и фаза поддержания имеет продолжительность, достаточную для замедления роста рака. 5. Применение по п.1, где TMZ вводят пациенту в дозах 5-180 мг один раз в день во время одновременной фазы; RT вводят пациенту во время одновременной фазы с использованием 1,8-2 Gy на фракцию,один раз в день в течение 5 дней в неделю для общей дозы до 60 Gy; соединение формулы I вводят пациенту в дозах 25-125 мг один раз в день во время фазы поддержания и TMZ вводят пациенту в дозах 5-180 мг в течение 5 последовательных дней и повторяют каждые 28 дней, пока рост рака не замедлится.
МПК / Метки
МПК: A61K 45/06, A61K 31/517, A61K 31/47, A61P 35/00
Метки: с-мет-модуляторов, применение, рака, терапии, комбинированной
Код ссылки
<a href="https://eas.patents.su/28-24563-primenenie-s-met-modulyatorov-v-kombinirovannojj-terapii-raka.html" rel="bookmark" title="База патентов Евразийского Союза">Применение с-мет-модуляторов в комбинированной терапии рака</a>
Предыдущий патент: Способ лечения эффектов воздействия облучения
Следующий патент: Способ и система для генерирования сигнала для устройства видеоотображения
Случайный патент: Статиновая терапия для усиления поддержания когнитивной функции












