Способ получения гидрохлорида оксикодона, содержащего менее 25 ч./млн 14- гидроксикодеинона
Номер патента: 13208
Опубликовано: 30.04.2010
Авторы: Чапмен Роберт, Кайл Доналд, Хонг Ки, Куппер Роберт, Райдер Лонн С.
Формула / Реферат
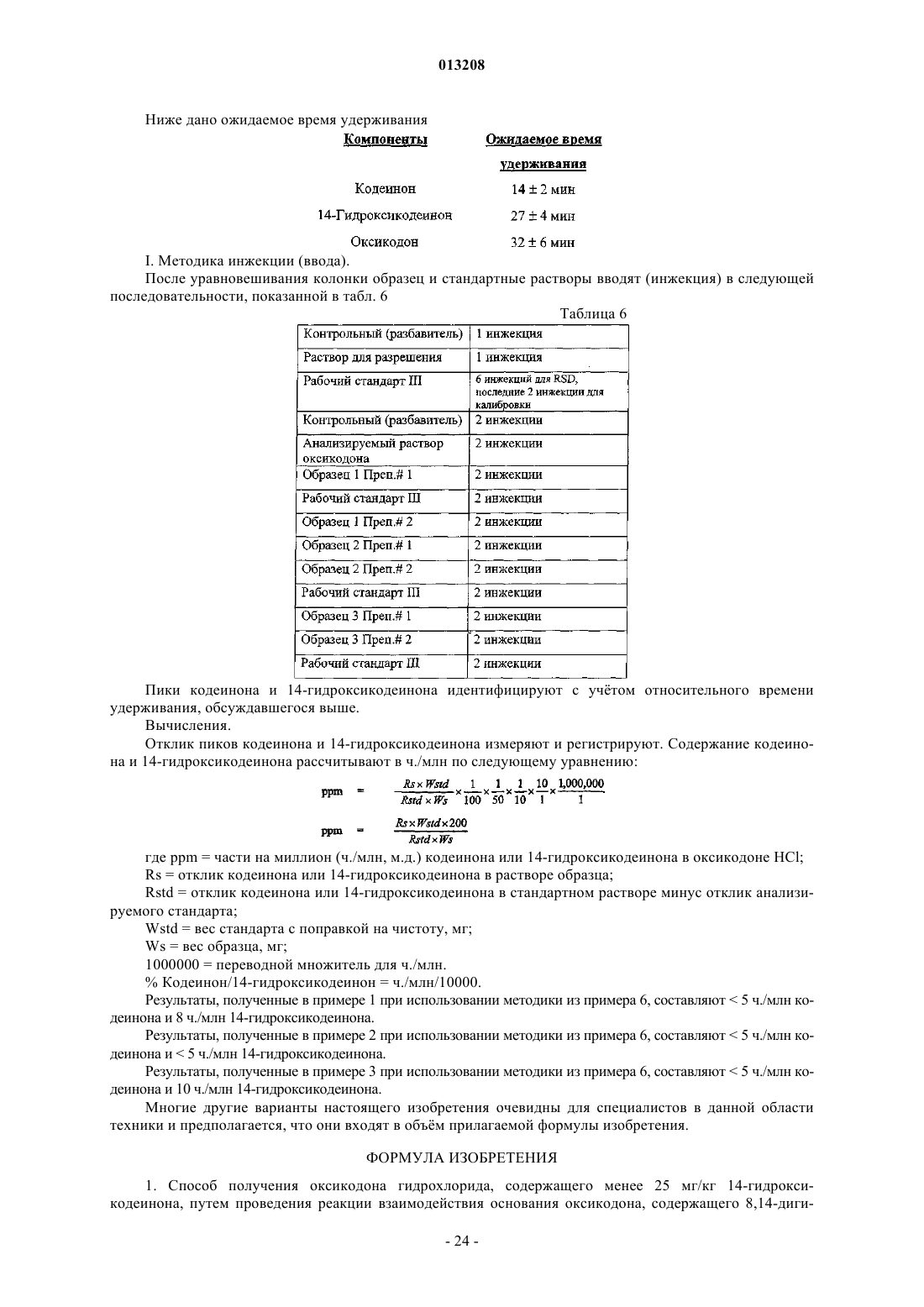
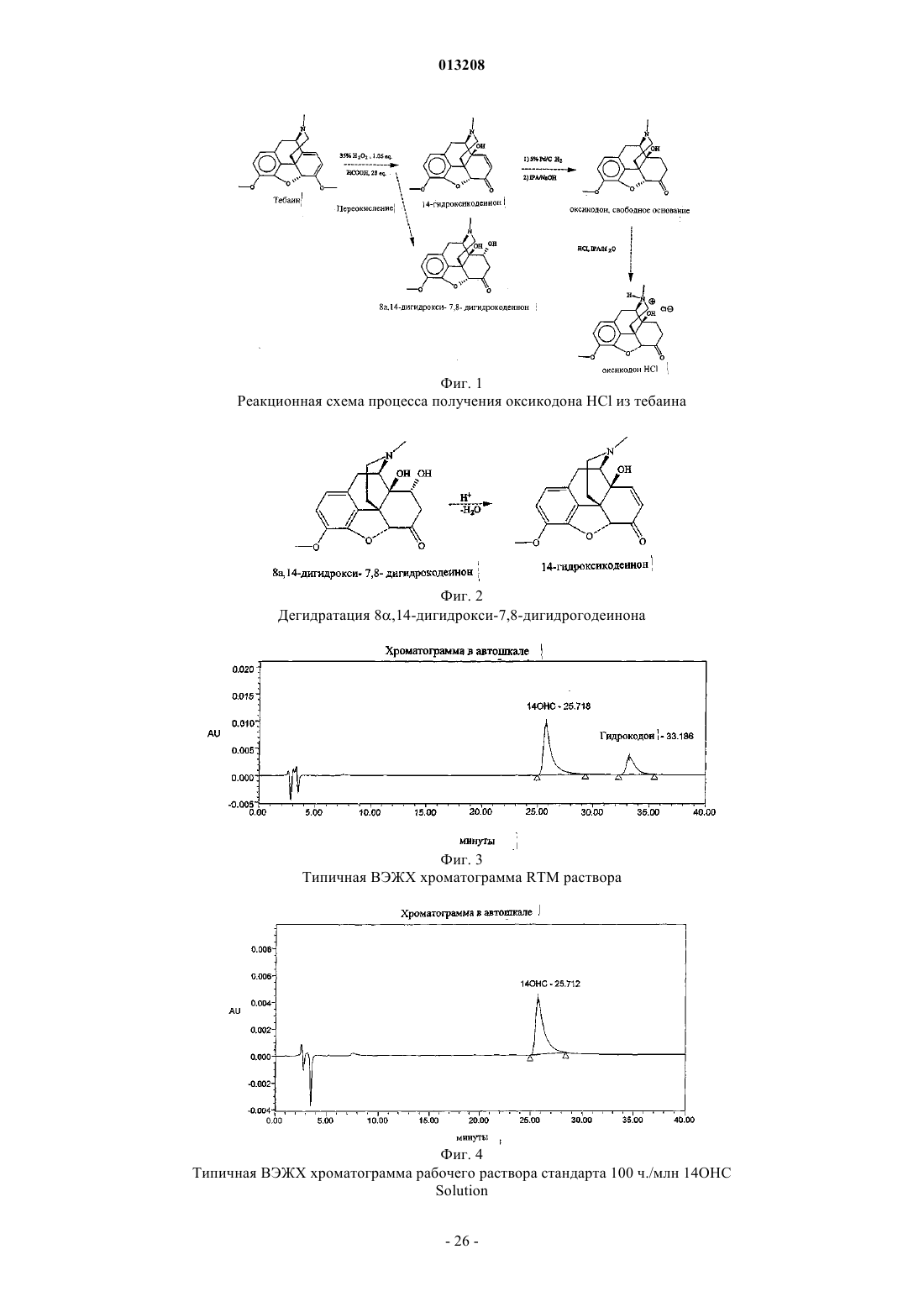
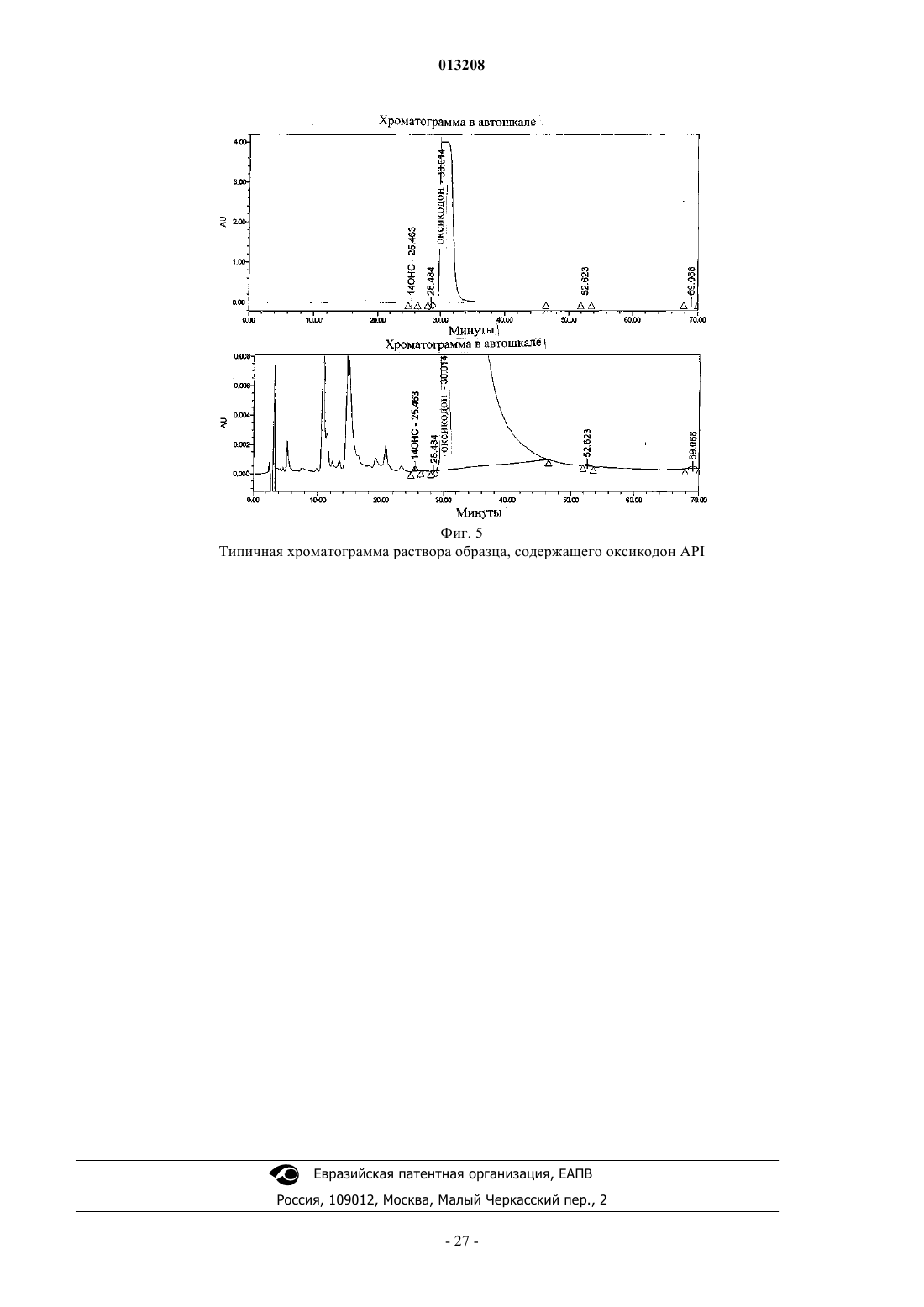
1. Способ получения оксикодона гидрохлорида, содержащего менее 25 мг/кг 14-гидроксикодеинона, путем проведения реакции взаимодействия основания оксикодона, содержащего 8,14-дигидрокси-7,8-дигидрокодеинон, с соляной кислотой в условиях, способствующих дегидратации 8,14-дигидрокси-7,8-дигидрокодеинона с образованием 14-гидроксикодеинона в процессе солеобразования и в восстановительных условиях для преобразования 14-гидроксикодеинона в оксикодон.
2. Способ по п.1, в котором оксикодон гидрохлорид содержит менее 15 мг/кг 14-гидроксикодеинона.
3. Способ по п.1, в котором оксикодон гидрохлорид содержит менее 10 мг/кг 14-гидроксикодеинона.
4. Способ по п.1, в котором оксикодон гидрохлорид содержит менее 5 мг/кг 14-гидроксикодеинона.
5. Способ по любому из пп.1-4, в котором полученный оксикодон гидрохлорид, содержащий менее 25 мг/кг 14-гидроксикодеинона, дополнительно гидрируют для дальнейшего восстановления содержащегося в нем количества 14-гидроксикодеинона.
6. Способ по любому из пп.1-5, в котором проводят извлечение оксикодона гидрохлорида, содержащего менее 25 мг/кг 14-гидроксикодеинона.
7. Способ по любому из пп.1-6, в котором основание оксикодона, содержащее 8,14-дигидрокси-7,8-дигидрокодеинон, вводят в реакцию с соляной кислотой в количестве более 1,0 мольного эквивалента в сравнении с составом основания оксикодона.
8. Способ по п.7, в котором количество соляной кислоты превышает 1,2 мольных эквивалентов.
9. Способ по п.7, в котором количество соляной кислоты превышает 1,4 мольных эквивалентов.
10. Способ по п.7, в котором количество соляной кислоты превышает 1,5 мольных эквивалентов.
11. Способ по любому из пп.1-10, в котором реакцию проводят при температуре около 20°С.
12. Способ по любому из пп.1-10, в котором реакцию проводят при температуре от 40 до 85°С.
13. Способ по любому из пп.1-12, в котором время реакции составляет от 10 мин до 36 ч.
14. Способ по любому из пп.1-13, в котором реакцию проводят при рН ниже 5.
15. Способ по любому из пп.1-13, в котором реакцию проводят при рН ниже 3.
16. Способ по любому из пп.1-13, в котором реакцию проводят при рН ниже 1.
17. Способ по любому из пп.1-16, в котором восстановительные условия обеспечиваются катализатором с донором водорода.
18. Способ по п.1, альтернативно проводимый путем реакции взаимодействия основания оксикодона, содержащего 8,14-дигидрокси-7,8-дигидрокодеинон, с соляной кислотой в условиях, способствующих дегидратации 8,14-дигидрокси-7,8-дигидрокодеинона, с получением 14-гидроксикодеинона при солеобразовании, с последующим введением его в контакт с веществом, удаляющим 14-гидроксикодеинон.
19. Способ по п.18, в котором указанное вещество представляет собой гель.
20. Способ по п.19, в котором указанная композиция и указанный гель образуют суспензию.
21. Способ по п.1, альтернативно проводимый путем реакции взаимодействия основания оксикодона, содержащего 8,14-дигидрокси-7,8-дигидрокодеинон, с соляной кислотой в условиях, способствующих дегидратации 8,14-дигидрокси-7,8-дигидрокодеинона, с получением 14-гидроксикодеинона при солеобразовании и последующим хроматографическим разделением.
22. Способ по любому из пп.1-21, в котором 8,14-дигидрокси-7,8-дигидрокодеинон представляет собой 8a,14-дигидрокси-7,8-дигидрокодеинон.
23. Способ получения оксикодона гидрохлорида, содержащего менее 25 мг/кг 14-гидроксикодеинона, путем гидрирования оксикодона гидрохлорида, содержащего более 100 мг/кг 14-гидроксикодеинона, до тех пор пока количество 14-гидроксикодеинона не уменьшится до уровня ниже 25 мг/кг.
24. Способ по п.23, в котором гидрирование проводят при температуре около 20°С.
25. Способ по п.23, в котором гидрирование проводят при температуре от 40 до 85°С.
26. Способ по любому из пп.1-25, в котором время гидрирования составляет от 10 мин до 36 ч.
27. Способ по любому из пп.1-26, в котором гидрирование проводят при рН ниже 5.
28. Способ по любому из пп.1-26, в котором гидрирование проводят при рН ниже 3.
29. Способ по любому из пп.1-26, в котором гидрирование проводят при рН ниже 1.
Текст
013208 Область техники Настоящее изобретение относится к способу уменьшения количества 14-гидроксикодеинона в препарате "оксикодона гидрохлорид". Уровень техники Оксикодон представляет собой полусинтетический опиоидный анальгетик, который вызывает агонистический эффект в специфических рецепторах насыщаемых опиоидов в ЦНС (CNS) и других тканях. У человека оксикодон может вызывать любой из множества эффектов, в том числе аналгезию.Purdue Pharma L.P. в настоящее время продат оксикодон пролонгированного действия в виде лекарственных форм, содержащих 10, 20, 40 и 80 мг оксикодона гидрохлорида под торговым названиемOxyContin. В патентах США 5266331; 5508042; 5549912 и 5656295 раскрываются препараты оксикодона пролонгированного действия. Тебаин, соединение, полученное из опиума, хотя само по себе не имеет применения в медицине,применимо в качестве исходного материала в синтетических схемах для получения оксикодона. В других схемах в качестве исходного для получения оксикодона можно применять кодеин. 14-Гидроксикодеинон является непосредственным предшественником оксикодона в этих схемах. О способах получения тебаина или 14-гидроксипроизводных опиума сообщалось, например, в патентах США 3894026 и 4045440. Окисление кодеина в кодеинон, начальная стадия в синтезе производных опиума, описана в Европейском патенте ЕР 0889045, патенте США 6008355 и в J. Am. Chem. Soc, 1051, 73, 4001 (Findlay). Реакция превращения кодеинона в 14-гидроксикодеинон описана в патенте США 6008355 и в Tetrahedron 55, 1999 (Coop and Rice). Метилирование кодеинона в тебаин описано в Heterocycles, 1988, 49, 43-7 (Rice) и в Европейском патенте ЕР 889045. В патенте США 6177567 описано гидрирование 14-гидроксикодеинона в оксикодон восстановлением дифенилсиланом и Pd(Ph3P)/ZnCl2 или гипофосфитом в присутствии катализатора Pd/C в водной уксусной кислоте.Krabnig et al. в "Optimization of the Synthesis of Oxycodone and 5-Methyloxycodone", Arch. Pharm.,(1996), 329(6), (325-326) описывает гидрирование 14-гидроксикодеинона в растворе в ледяной уксусной кислоте Pd/С в качестве катализатора при 30 psi (206,84 кПа) в указанных условиях. При окислении тебаина с образованием 14-гидроксикодеинона образуется несколько продуктов гиперокисления, включая 8,14-дигидрокси-7,8-дигидрокодеинон. В процессе получения свободного основания оксикодона из 14-гидроксикодеинона 8,14-дигидрокси-7,8-дигидрокодеинон не изменяется. При превращении свободного основания оксикодона в оксикодона гидрохлорид примесь претерпевает дегидратацию, катализируемую кислотой, и превращается в 14-гидроксикодеинон. Поэтому в конечной композиции оксикодона гидрохлорида присутствует 14-гидроксикодеинон. Оксикодона гидрохлорид APIMatthey и Mallincrodt. Уровень 14-гидроксикодеинона в выпускаемом в настоящее время оксикодона гидрохлориде API и в оксикодона гидрохлориде, получаемом известными методами, составляет более 100 ч./млн. Имеется настоятельная потребность получить композицию оксикодона гидрохлорида, которая содержит пониженные количества 14-гидроксикодеинона по сравнению с композициями, известными в уровне техники. Сущность изобретения Целью настоящего изобретения является создание способа снижения содержания 14-гидроксикодеинона в композиции оксикодона гидрохлорида до менее чем 25 ч./млн, менее чем примерно 15 ч./млн, менее чем примерно 10 ч./млн или менее чем примерно 5 ч./млн. Целью некоторых вариантов настоящего изобретения является создание способа реакции композиции оксикодона основания с хлористо-водородной кислотой в условиях, при которых образуется композиция основания оксикодона гидрохлорида, содержащая 14-гидроксикодеинон в количестве менее чем 25 ч./млн, менее чем примерно 15 ч./млн, менее чем примерно 10 ч./млн или менее чем примерно 5 ч./млн. Другой целью некоторых вариантов настоящего изобретения является получение композиции оксикодона гидрохлорида с содержанием 14-гидроксикодеинона в количестве менее чем 25 ч./млн, менее чем примерно 15 ч./млн, менее чем примерно 10 ч./млн или менее чем примерно 5 ч./млн. Другой целью некоторых вариантов настоящего изобретения является создание способа получения композиции оксикодона гидрохлорида с содержанием 14-гидроксикодеинона в количестве менее чем 25 ч./млн по реакции композиции оксикодона основания с хлористо-водородной кислотой в условиях,пригодных для промотирования дегидратации 8,14-дигидрокси-7,8-дигидрокодеинона в 14-гидроксикодеинон, в процессе солеобразования и в условиях восстановления таким образом, чтобы превратить 14-гидроксикодеинон в оксикодон. В некоторых вариантах настоящее изобретение относится к способу получения композиции окси-1 013208 кодона гидрохлорида с содержанием 14-гидроксикодеинона менее 25 ч./млн, заключающемуся в реакции композиции оксикодона гидрохлорида с содержанием 14-гидроксикодеинона более 100 ч./млн, в условиях, при которых количество 14-гидроксикодеинона снижается до уровня менее 25 ч./млн, менее чем примерно 15 ч./млн, менее чем примерно 10 ч./млн или менее чем примерно 5 ч./млн. В некоторых вариантах данное изобретение относится к композиции оксикодона гидрохлорида с содержанием 14-гидроксикодеинона менее 25 ч./млн, менее чем примерно 15 ч./млн, менее чем примерно 10 ч./млн или менее чем примерно 5 ч./млн. В некоторых вариантах данное изобретение относится к способу получения композиции оксикодона гидрохлорида с содержанием 14-гидроксикодеинона менее 25 ч./млн, заключающемуся в гидрировании композиции с уровнем 14-гидроксикодеинона выше 100 ч./млн до такой степени, чтобы содержание 14-гидроксикодеинона в композиции снижалось до количества менее 25 ч./млн, менее чем примерно 15 ч./млн, менее чем примерно 10 ч./млн или менее чем примерно 5 ч./млн. В некоторых вариантах, раскрываемых в данном описании, композицию оксикодона, содержащую менее 25 ч./млн 14-гидроксикодеинона, гидрируют для того, чтобы дополнительно понизить содержание 14-гидроксикодеинона, например, примерно с 15 ч./млн до примерно 10 ч./млн. В одном варианте изобретения, в котором исходным материалом является композиция оксикодона гидрохлорида, содержащая 14-гидроксикодеинон в количестве 100 ч./млн или выше, в конечной композиции оксикодона гидрохлорида уровень 14-гидроксикодеинона составляет менее 25 ч./млн, менее чем примерно 15 ч./млн, менее чем примерно 10 ч./млн или менее чем примерно 5 ч./млн. В другом варианте изобретения, в котором исходным материалом является композиция оксикодона гидрохлорида, содержащая 14-гидроксикодеинон в количестве 15-25 ч./млн, в конечной композиции оксикодона гидрохлорида уровень 14-гидроксикодеинона составляет менее чем примерно 10 ч./млн или менее чем примерно 5 ч./млн. В другом варианте изобретения, в котором исходным материалом является композиция оксикодона гидрохлорида, содержащая 14-гидроксикодеинон в количестве 10-25 ч./млн, в конечной композиции оксикодона гидрохлорида уровень 14-гидроксикодеинона составляет менее чем примерно 5 ч./млн. В некоторых вариантах настоящего изобретения способ получения композиции оксикодона гидрохлорида с содержанием 14-гидроксикодеинона менее 25 ч./млн заключается в гидрировании исходного материала при кипении. В некоторых вариантах изобретения способ дополнительно содержит регенерацию полученной композиции оксикодона гидрохлорида с содержанием 14-гидроксикодеинона менее 25 ч./млн. В некоторых вариантах данное изобретение относится к способу получения композиции оксикодона гидрохлорида с содержанием 14-гидроксикодеинона менее 25 ч./млн, включающему гидрирование при кипячении исходной композиции оксикодона гидрохлорида с уровнем 14-гидроксикодеинона выше 100 ч./млн в подходящем растворителе в течение времени, достаточного для получения композиции оксикодона с содержанием 14-гидроксикодеинона менее 25 ч./млн, менее чем примерно 15 ч./млн, менее чем примерно 10 ч./млн или менее чем примерно 5 ч./млн; и регенерацию композиции оксикодона гидрохлорида с содержанием 14-гидроксикодеинона менее 25 ч./млн кристаллизацией и выделением из растворителя (например, фильтрованием). В некоторых вариантах композиции оксикодона гидрохлорида по настоящему изобретению нижний предел содержания 14-гидроксикодеинона составляет 0,25 ч./млн, 0,5 ч./млн, 1 ч./млн, 2 ч./млн или 5 ч./млн. В некоторых вариантах настоящее изобретение относится к способу получения композиции оксикодона гидрохлорида с содержанием 14-гидроксикодеинона менее 25 ч./млн, включающему реакцию в подходящем растворителе композиции оксикодона основания с хлористо-водородной кислотой в количестве более 1,0 мол.экв. относительно содержания оксикодона основания, причм эту стадию реакции проводят в условиях восстановления с образованием композиции оксикодона гидрохлорида с содержанием 14-гидроксикодеинона менее 25 ч./млн. В некоторых вариантах данное изобретение относится к способу получения композиции оксикодона гидрохлорида, содержащей менее 25 ч./млн 14-гидроксикодеинона, включающему гидрирование 14-гидроксикодеинона с образованием оксикодона в виде свободного основания; превращение оксикодона в виде свободного основания в оксикодона гидрохлорид и гидрирование оксикодона гидрохлорида с образованием композиции оксикодона, содержащей менее 25 ч./млн 14-гидроксикодеинона. В некоторых вариантах данное изобретение относится к способу получения композиции оксикодона гидрохлорида, содержащей менее 25 ч./млн 14-гидроксикодеинона, включающему гидрирование композиции 14-гидроксикодеинона с образованием оксикодона в виде свободного основания; превращение композиции оксикодона в виде свободного основания в оксикодона гидрохлорид; выделение оксикодона гидрохлорида и гидрирование оксикодона гидрохлорида с образованием композиции оксикодона, содержащей менее 25 ч./млн 14-гидроксикодеинона. В некоторых вариантах данное изобретение относится к способу получения композиции оксикодона гидрохлорида, содержащей менее 25 ч./млн 14-гидроксикодеинона, включающему окисление композиции тебаина с образованием композиции 14-гидроксикодеинона, причм окисление проводят при таком значении рН, чтобы свести к минимуму или исключить образование 8,14-дигидрокси-7,8-дигидро-2 013208 кодеинона в композиции 14-гидроксикодеинона; гидрирование композиции 14-гидроксикодеинона с образованием композиции оксикодона основания и превращение композиции оксикодона основания в композицию оксикодона гидрохлорида, содержащую менее 25 ч./млн 14-гидроксикодеинона. В некоторых вариантах данное изобретение относится к способу получения 14-гидроксикодеинона,включающему окисление композиции тебаина с образованием композиции 14-гидроксикодеинона, причм окисление проводят при таком значении рН, чтобы свести к минимуму или исключить образование 8,14-дигидрокси-7,8-дигидрокодеинона в композиции 14-гидроксикодеинона. В некоторых вариантах данное изобретение относится к способу получения композиции оксикодона гидрохлорида, заключающемуся в реакции композиции оксикодона основания с кислотой, имеющей рН выше хлористо-водородной кислоты, с образованием соответствующей соли присоединения кислоты оксикодона и в превращении соли присоединения кислоты оксикодона в оксикодона гидрохлорид. В некоторых вариантах данное изобретение относится к способу получения композиции оксикодона гидрохлорида, уровень 14-гидроксикодеинона в которой составляет менее 25 ч./млн, включающему контактирование композиции оксикодона основания, содержащей некоторое количество 8,14-дигидрокси-7,8-дигидрокодеинона, с веществом, которое предпочтительно удаляет 8,14-дигидрокси-7,8-дигидрокодеинон по сравнению с оксикодона основанием; и превращение композиции оксикодона основания в композицию оксикодона гидрохлорида с содержанием 14-гидроксикодеинона менее 25 ч./млн. В некоторых вариантах данное изобретение относится к способу получения композиции оксикодона гидрохлорида, уровень 14-гидроксикодеинона в которой составляет менее 25 ч./млн, включающему хроматографическое разделение композиции оксикодона основания, содержащей некоторое количество 8,14-дигидрокси-7,8-дигидрокодеинона, с целью предпочтительного удаления 8,14-дигидрокси-7,8-дигидрокодеинона по сравнению с оксикодона основанием и превращение композиции оксикодона основания в композицию оксикодона гидрохлорида, уровень 14-гидроксикодеинона в которой составляет менее 25 ч./млн. В некоторых вариантах данное изобретение относится к способу получения композиции оксикодона гидрохлорида, уровень 14-гидроксикодеинона в которой составляет менее 25 ч./млн, включающему реакцию в подходящем растворителе композиции оксикодона основания, содержащей некоторое количество 8,14-дигидрокси-7,8-дигидрокодеинона, с полистиролом, содержащим бор; и превращение композиции оксикодона основания в композицию оксикодона гидрохлорида, содержание 14-гидроксикодеинона в которой составляет менее 25 ч./млн. В некоторых вариантах данное изобретение относится к способу получения композиции оксикодона гидрохлорида, включающему реакцию в подходящем растворителе композиции оксикодона основания с полистиролом, содержащим бор; и превращение композиции оксикодона основания в композицию оксикодона гидрохлорида. В некоторых вариантах данное изобретение относится к способу получения композиции оксикодона гидрохлорида, уровень 14-гидроксикодеинона в которой составляет менее 25 ч./млн, включающему смешение хлористо-водородной кислоты и композиции оксикодона основания, содержащей некоторое количество 8,14-дигидрокси-7,8-дигидрокодеинона, в растворителе с образованием раствора и распылительную сушку раствора с образованием композиции оксикодона гидрохлорида, содержащей 14-гидроксикодеинон в количестве менее 25 ч./млн. В некоторых вариантах данное изобретение относится к способу получения композиции оксикодона гидрохлорида, уровень 14-гидроксикодеинона в которой составляет менее 25 ч./млн, включающему смешение хлористо-водородной кислоты и композиции оксикодона основания, содержащей некоторое количество 8,14-дигидрокси-7,8-дигидрокодеинона, в растворителе с образованием раствора и лиофилизацию раствора с образованием композиции оксикодона гидрохлорида, содержащей 14-гидроксикодеинон в количестве менее 25 ч./млн. В некоторых вариантах данное изобретение относится к способу получения композиции оксикодона гидрохлорида, включающему смешение хлористо-водородной кислоты и композиции оксикодона основания в растворителе с образованием раствора; и распылительную сушку раствора с образованием оксикодона гидрохлорида. В некоторых вариантах данное изобретение относится к способу получения композиции оксикодона гидрохлорида, включающему смешение хлористо-водородной кислоты и композиции оксикодона основания в растворителе с образованием раствора; и лиофилизацию раствора с образованием оксикодона гидрохлорида. Термин "масса" обозначает количество материала по меньшей мере 1 кг. В некоторых вариантах изобретения количество может составлять около 10-1000 кг или около 10-500 кг. В некоторых вариантах изобретения количество составляет около 20-100 кг; около 20 кг или около 50 кг. Массу композиции оксикодона гидрохлорида можно упаковать в фармацевтически приемлемую упаковку, такую как гофрированные коробки (сделанные, например, из пластика и/или из бумаги); в цилиндрические контейнеры (например, из металла или металлического композитного материала) или в тканые фабричные пакеты (мешки), обычно называемые "гибкие контейнеры для грузов средней тяжести" (FIBC). В каждом из этих способов используются прокладки различной конфигурации, обычно из полиэтилена или полипропилена, которые подгоняются к гофрированной коробке, цилиндру или к FIBC для предупреждения-3 013208 загрязнения продукта при перевозке. Предпочтительно в этих способах упаковки используют контейнеры, оснащнные таким образом, чтобы удерживаться и переноситься на транспортных стеллажах (носилках). Термин ч./млн по данному описанию означает "части на миллион". По отношению к 14-гидроксикодеинону "ч./млн" означает части на миллион 14-гидроксикодеинона в конкретном образце. Термин 8,14-дигидрокси-7,8-дигидрокодеинон включает либо 8,14-дигидрокси-7,8-дигидрокодеинон, либо 8,14-дигидрокси-7,8-дигидрокодеинон, либо может включать смесь обоих соединений. Препарат оксикодона гидрохлорида может являться, например, оксикодон-активным фармацевтическим ингредиентом (API), таким как оксикодона гидрохлоридом USP, объединнным или необъединнным с одним или более других ингредиентов. Например, препарат оксикодона может быть конечной фармацевтической лекарственной формой или промежуточным препаратом для конечной лекарственной формы, который можно проверять на присутствие 14-гидроксикодеинона и/или кодеинона, например, с целью гарантии качества. Предпочтительно препарат оксикодона гидрохлорида представляет собой оксикодона гидрохлорид API и содержит по меньшей мере 98% оксикодона гидрохлорида, по меньшей мере 99% оксикодона гидрохлорида или по меньшей мере 99,9% оксикодона гидрохлорида. Способ детектирования присутствия 14-гидроксикодеинона в препарате оксикодона можно осуществить в соответствии с предварительной патентной заявкой США 60/557502, озаглавленной "Способы обнаружения 14-гидроксикодеинона", поданной 29 марта 2004, и в соответствии с предварительной заявкой США, озаглавленной "Способы обнаружения 14-гидроксикодеинона", поданной 31 января 2005. Краткое описание фигур На фиг. 1 дана схема превращения тебаина в оксикодона гидрохлорид, включая окисление тебаина в 14-гидроксикодеинон и примесь 8,14-дигидрокси-7,8-дигидрокодеинон; на фиг. 2 - схема дегидратации 8,14-дигидрокси-7,8-дигидрокодеинона в 14-гидроксикодеинон; на фиг. 3 изображено разделение раствора из примера 4 для испытания пригодности системы; на фиг. 4 - ВЭЖХ хроматограмма стандартного рабочего раствора из примера 4, содержащего 100 ч./млн 14 ОНС; на фиг. 5 - ВЭЖХ хроматограмма раствора образца оксикодона API из примера 4. Подробное описание изобретения В некоторых вариантах данное изобретение относится к способу снижения количества 14-гидроксикодеинона в композиции оксикодона гидрохлорида (например, оксикодона гидрохлорида API) и к полученной при этом композиции с содержанием 14-гидроксикодеинона менее 25 ч./млн. В некоторых вариантах настоящее изобретение относится к способу уменьшения количества 14-гидроксикодеинона в композиции оксикодона гидрохлорида, включающему реакцию оксикодона гидрохлорида с каталитически эффективным количеством переходного металла и с газом, представляющим собой водород, при такой температуре и в течение такого периода времени, которые достаточны для снижения содержания 14-гидроксикодеинона до уровня, когда полученная композиция оксикодона гидрохлорида содержит 14-гидроксикодеинон в количестве менее чем 25 ч./млн, менее чем примерно 15 ч./млн, менее чем примерно 10 ч./млн или менее чем примерно 5 ч./млн. Способ по настоящему изобретению может также привести к снижению содержания других альфа,бета ненасыщенных кетонов в композициях оксикодона, помимо 14-гидроксикодеинона, таких, например, как кодеинон. В соответствии с некоторыми вариантами настоящего изобретения композицию оксикодона гидрохлорида (например, оксикодона гидрохлорид API) и растворитель загружают в прибор для реакции. Затем композицию гидрируют в соответствующих условиях в течение достаточного времени, катализатор удаляют из растворителя, а композицию оксикодона гидрохлорида с содержанием 14-гидроксикодеинона менее чем 25 ч./млн выделяют, например, кристаллизацией и фильтрованием. Гидрирование 14-гидроксикодеинона в способах по настоящему изобретению можно проводить,используя, например, каталитическое гидрирование под давлением или гидрирование с каталитическим переносом водорода в подходящей кислоте, например в уксусной кислоте. В особой реакции гидрирования используется газообразный водород или NaHPO2 с палладием на угле в качестве катализатора. В некоторых вариантах изобретения донор водорода для гидрирования 14-гидроксикодеинона можно выбрать из водорода, первичного и вторичного спиртов, первичного и вторичного аминов, карбоновых кислот и их эфиров и солей аминов, легко дегидрирующихся углеводородов (например, низших алкилзамещнных ароматических углеводородов, таких как этилбензол, диэтилбензол, изопропилбензол, диизопропилбензол, о-этилтолуол, м-этилтолуол, п-этилтолуол, о-изопропилтолуол, м-изопропилтолуол, пизопропилтолуол, этилнафталин, пропилнафталин, изопропилнафталин и диэтилнафталин; парафины,такие как этан, пропан, н-бутан, изобутан, н-пентан, изопентан, н-гексан, н-гептан, н-октан, н-нонан, ндекан и их изомеры с разветвлнной цепью; циклопарафины, такие как циклобутан, циклопентан, циклогексан, метилциклопентан, метилциклогексан и этилциклопентан; олефины, такие как этилен, пропилен,1-бутен, 2-бутен, 1-пентен, 2-пентен, 1-гексен, 2-гексен, 3-гексен и их производные с разветвлнной цепью) и очищенные восстановители (например, оловоорганические гидриды на полимерных носителях) и-4 013208 их любые комбинации. В некоторых вариантах изобретения гидрирование можно проводить, как описано в предварительной заявке США 60/477968, поданной 12 июня 2003, озаглавленной "Гидрирование опиоидов в отсутствие газообразного водорода". В некоторых вариантах изобретения гидрирование проводят под давлением около 5-200 psig (около 34,47-1378,95 кПа) или около 40-60 psig (около 275,79-413,68 кПа). В некоторых вариантах изобретения гидрирование проводят при температуре около 20-100 С или около 40-85 С. В некоторых вариантах изобретения гидрирование проводят при рН ниже 5, ниже 3 или ниже 1, например при рН около 0,5. В некоторых вариантах настоящего изобретения 14-гидроксикодеинон превращают в оксикодон гидрированием в присутствии дифенилсилана и Pd(Ph3P)/ZnCl2 и в присутствии гипофосфита натрия сPd/C в качестве катализатора в водной органической кислоте; или гидрированием каталитическим переносом водорода в присутствии катализатора Pd/C. Общее время реакции гидрирования достаточно для того, чтобы уменьшить содержание 14-гидроксикодеинона до уровня менее чем 25 ч./млн, менее чем примерно 15 ч./млн, менее чем примерно 10 ч./млн или менее чем примерно 5 ч./млн. Действительное время реакции может меняться в зависимости от температуры и эффективности гидрирующей системы (системы гидрогенизации). В зависимости от условий гидрирования (например, температуры и давления) общее время реакции для достижения заданного уменьшения содержания 14-гидроксикодеинона может быть, например, от около 10 мин до около 36 ч. Гидрирование 14-гидроксикодеинона можно проводить в присутствии благородного металла в качестве катализатора. В некоторых вариантах изобретения подходящие катализаторы можно выбирать, среди прочих, из кобальта Ренея, никеля Ренея, палладия на угле, платины на угле, палладия на оксиде алюминия, оксида платины, рутения на оксиде алюминия, родия на оксиде алюминия или родия на угле. Одним из конкретных катализаторов такого восстановления является 5% палладий на угле. Количество катализатора палладия на угле может составлять около 0,05-50 вес.% или около 0,05-5 вес.% от обрабатываемой композиции. Реакцию можно проводить в растворителе, таком как вода; спирт (например, такой как изопропанол, метанол или этанол); тетрагидрофуран; ароматический углеводород (такой как бензол); простой эфир (такой как диоксан); эфир низшей алкановой кислоты (такой как метилацетат или этилацетат); амид(например, такой как диметилформамид, диэтилформамид, диметилацетамид или N-алкилзамещнные амиды других низших жирных кислот); N-метилпирролидон; формилморфолин; -метоксипропионитрил; карбоновая кислота (такая как муравьиная, уксусная, пропионовая кислота или другая низшая алкановая кислота) или подходящая смесь любых двух или более вышеуказанных растворителей. Заслуживающей особого внимания смесью сорастворителей является смесь изопропанол/вода. В некоторых вариантах изобретения растворитель перед процессом гидрирования обычно смешивают с композицией, содержащей 14-гидроксикодеинон (например, композицией оксикодона). В некоторых вариантах данное изобретение относится к превращению композиции оксикодона свободного основания (с 8,14-дигидрокси-7,8-дигидрокодеиноном в качестве компонента) в оксикодона гидрохлорид. В ходе известной в уровне техники реакции образования соли 8,14-дигидрокси-7,8-дигидрокодеинон превращается в 14-гидроксикодеинон за счт катализируемой кислотой дегидратации. Таким образом, содержание 14-гидроксикодеинона в конечном продукте повышается. Благодаря настоящему изобретению это содержание можно понизить, увеличивая (перегружая) количество хлористоводородной кислоты при получении соли с целью промотировать реакцию 8,14-дигидрокси-7,8-дигидрокодеинона в 14-гидроксикодеинон и создавая условия восстановления, достаточные для того, чтобы 14-гидроксикодеинон легко превращался в оксикодон. В таком варианте изобретения количество хлористоводородной кислоты составляет более 1 мол.экв. по отношению к оксикодона свободному основанию. В некоторых вариантах количество хлористо-водородной кислоты может быть больше примерно 1,2 мол.экв. или больше примерно 1,4 мол.экв. относительно оксикодона свободного основания. В некоторых вариантах изобретения количество хлористо-водородной кислоты может составлять около 1,5 мол.экв. Условия восстановления, достаточные для превращения 14-гидроксикодеинона в оксикодон,можно создавать, например, с помощью катализатора и донора протонов. Кроме того, в процессе образования соли скорость дегидратации 8,14-дигидрокси-7,8 дигидрокодеинона в 14-гидроксикодеинон снижается по мере повышения рН раствора. Поэтому в некоторых вариантах рН раствора можно доводить до величины около 1,5-2,5, предпочтительно примерно до 1,8 (например, от рН ниже 1), добавляя соответствующий основной агент, например гидроксид натрия. Это дополнительно сводит к минимуму образование 14-гидроксикодеинона из 8,14-дигидрокси-7,8 дигидрокодеинона в процессе кристаллизации. Предпочтительно коррекцию рН осуществляют после стадии гидрирования и перед удалением катализатора и выделением оксикодона с содержанием 14-гидроксикодеинона менее 25 ч./млн. В некоторых вариантах может быть необходимо осуществлять способ по настоящему изобретению или одну или более релевантных стадий способа по настоящему изобретению более одного, для того чтобы понизить количество 14-гидроксикодеинона до заданного уровня, например менее чем примерно 10 ч./млн или менее чем примерно 5 ч./млн.-5 013208 В некоторых вариантах настоящего изобретения композиции оксикодона гидрохлорида можно получать определнными альтернативными способами. Такие альтернативные способы предпочтительно дают в результате композицию оксикодона гидрохлорида с содержанием 14-гидроксикодеинона менее 25 ч./млн. Один такой альтернативный способ представляет собой способ получения композиции оксикодона гидрохлорида с содержанием 14-гидроксикодеинона менее 25 ч./млн, включающий окисление композиции тебаина с образованием композиции 14-гидроксикодеинона, при этом окисление проводят при соответствующем рН с целью свести к минимуму или исключить образование 8,14-дигидрокси-7,8-дигидрокодеинона в композиции 14-гидроксикодеинона; гидрирование композиции 14-гидроксикодеинона с образованием композиции оксикодона основания и превращение композиции оксикодона основания в композицию оксикодона гидрохлорида, содержащую менее 25 ч./млн 14-гидроксикодеинона. Другой альтеранативный способ относится к способу получения 14-гидроксикодеинона, включающему окисление композиции тебаина, с образованием композиции 14-гидроксикодеинона, причм окисление осуществляют при соответствующем значении рН с целью свести к минимуму или исключить образование 8,14-дигидрокси-7,8-дигидрокодеинона в композиции 14-гидроксикодеинона. Другой альтернативный способ относится к способу получения композиции оксикодона гидрохлорида, включающему реакцию композиции оксикодона основания с кислотой с более высоким значением рН, нежели хлористо-водородная кислота, с целью образования соли присоединения к оксикодону соответствующей кислоты и превращение соли присоединения оксикодона в оксикодона гидрохлорид. В таком варианте изобретения кислоту можно выбрать из группы, состоящей из винной кислоты, щавелевой кислоты, фумаровой кислоты, фосфорной кислоты, серной кислоты и их смесей. Другой альтернативный способ относится к способу получения композиции оксикодона гидрохлорида, содержащей менее 25 ч./млн 14-гидроксикодеинона, включающий контактирование композиции оксикодона основания с содержанием некоторого количества 8,14-дигидрокси-7,8-дигидрокодеинона с веществом, которое предпочтительно удаляет 8,14-дигидрокси-7,8-дигидрокодеинон, а не оксикодона основание; и превращение композиции оксикодона основания в композицию оксикодона гидрохлорида,содержащую менее 25 ч./млн 14-гидроксикодеинона. В предпочтительных вариантах изобретения контактирующее вещество может быть гелем. В других вариантах изобретения контактирование может включать пропускание раствора, содержащего композицию оксикодона основания, через вещество или может включать суспензию с композицией оксикодона основания и геля. Другой альтернативный способ относится к способу получения композиции оксикодона гидрохлорида, содержащей менее 25 ч./млн 14-гидроксикодеинона, включающему хроматографическое разделение композиции оксикодона основания, содержащей некоторое количество 8,14-дигидрокси-7,8-дигидрокодеинона, с целью предпочтительного удаления 8,14-дигидрокси-7,8-дигидрокодеинона по сравнению с оксикодона основанием; и превращение композиции оксикодона основания в композицию оксикодона гидрохлорида, уровень 14-гидроксикодеинона в которой составляет менее 25 ч./млн. В предпочтительных вариантах изобретения хроматографическое разделение представляет собой разделение на моделированном подвижном слое. Другой альтернативный способ относится к способу получения композиции оксикодона гидрохлорида, уровень 14-гидроксикодеинона в которой составляет менее 25 ч./млн, включающему контактирование композиции оксикодона гидрохлорида, содержащей некоторое количество 14-гидроксикодеинона,с веществом, которое удаляет предпочтительно 14-гидроксикодеинон по сравнению с оксикодона гидрохлоридом; и регенерацию композиции оксикодона гидрохлорида, содержание 14-гидроксикодеинона в которой составляет менее 25 ч./млн. В предпочтительных вариантах изобретения контактирующим веществом может быть гель. В других вариантах изобретения контактирование может представлять собой прохождение раствора, содержащего композицию оксикодона гидрохлорид, через вещество или может представлять собой образование суспензии композиции оксикодона гидрохлорида и геля. Другой альтернативный способ по данному изобретению относится к способу получения композиции оксикодона гидрохлорида, содержание 14-гидроксикодеинона в которой составляет менее 25 ч./млн,включающему хроматографическое разделение композиции оксикодонаоснования, содержащей некоторое количество 14-гидроксикодеинона, с целью предпочтительного удаления 14-гидроксикодеинона по сравнению с оксикодона основанием и регенерацию композиции оксикодона гидрохлорида, уровень 14-гидроксикодеинона в которой составляет менее 25 ч./млн. В предпочтительных вариантах изобретения хроматографическое разделение представляет собой разделение на моделированном подвижном слое. Другой альтернативный способ по данному изобретению относится к способу получения композиции оксикодона гидрохлорида, уровень 14-гидроксикодеинона в которой составляет менее 25 ч./млн,включающему реакцию в подходящем растворителе композиции оксикодона основания, содержащей некоторое количество 8,14-дигидрокси-7,8-дигидрокодеинона, с полистиролом, содержащим бор; и превращение композиции оксикодона основания в композицию оксикодона гидрохлорида, содержание 14-гидроксикодеинона в которой составляет менее 25 ч./млн. Предпочтительно реакцию осуществляют при температуре ниже примерно 20 С. Другой альтернативный способ по данному изобретению относится к способу получения компози-6 013208 ции оксикодона гидрохлорида, включающему реакцию в подходящем растворителе композиции оксикодона основания с полистиролом, содержащим бор; и превращение композиции оксикодона основания в композицию оксикодона гидрохлорида. Предпочтительно реакцию осуществляют при температуре ниже примерно 20 С. Другой альтернативный способ по данному изобретению относится к способу получения композиции оксикодона гидрохлорида, уровень 14-гидроксикодеинона в которой составляет менее 25 ч./млн,включающему смешение хлористо-водородной кислоты и композиции оксикодона основания, содержащей некоторое количество 8,14-дигидрокси-7,8-дигидрокодеинона, в растворителе с образованием раствора и распылительную сушку раствора с образованием композиции оксикодона гидрохлорида, содержащей 14-гидроксикодеинон в количестве менее 25 ч./млн. Другой альтернативный способ по данному изобретению относится к способу получения композиции оксикодона гидрохлорида, уровень 14-гидроксикодеинона в которой составляет менее 25 ч./млн,включающему смешение хлористо-водородной кислоты и композиции оксикодона основания, содержащей некоторое количество 8,14-дигидрокси-7,8-дигидрокодеинона, в растворителе с образованием раствора и лиофилизацию раствора с образованием композиции оксикодона гидрохлорида, содержащей 14-гидроксикодеинон в количестве менее 25 ч./млн. Другой альтернативный способ по данному изобретению относится к способу получения композиции оксикодона гидрохлорида, включающему смешение хлористо-водородной кислоты и композиции оксикодона основания в растворителе с образованием раствора и распылительную сушку раствора с образованием оксикодона гидрохлорида. Другой альтернативный способ по данному изобретению относится к способу получения композиции оксикодона гидрохлорида, включающему смешение хлористо-водородной кислоты и композиции оксикодона основания в растворителе с образованием раствора и лиофилизацию раствора с образованием оксикодона гидрохлорида. Другие варианты изобретения Оксикодона гидрохлорид, содержание 14-гидроксикодеинона в котором составляет менее 25 ч./млн,можно вводить в фармацевтические лекарственные формы, например, смешением оксикодона гидрохлорида, содержание 14-гидроксикодеинона в котором составляет менее 25 ч./млн, с обычными эксципиентами, т.е. фармацевтически приемлемыми органическими или неорганическими носителями. В случае оральных препаратов лекарственные формы могут обеспечивать пролонгированное высвобождение активного компонента. Подходящие фармацевтически приемлемые носители включают, но без ограничения, спирты, аравийскую камедь, растительные масла, бензиловые спирты, полиэтиленгликоли, загуститель (желатин), углеводы, такие как лактоза, амилоза или крахмал, стеарат магния, тальк, кремниевая кислота, парафин с высокой вязкостью, парфюмерное масло, моноглицериды и диглицериды жирных кислот, эфиры пентаэритрита и жирных кислот, гидроксиметилцеллюлозы, поливинилпирролидон и т.д. Фармацевтические препараты могут быть стерилизованными и при желании их можно смешивать с добавками, такими как смазки, вещества, способствующие расщеплению, консерванты, стабилизаторы,увлажняющие агенты, эмульгаторы, соли в качестве осмотических буферов при изменении осмотического давления, красители, вещества, придающие вкус и/или запах, и т.п. Композиции, предполагаемые для орального применения, можно приготовить методами, известными в уровне техники, и такие композиции могут содержать один или более агентов, выбранных из группы, состоящей из инертных нетоксических фармацевтически приемлемых эксципиентов, пригодных для изготовления таблеток. Такие эксципиенты включают, например, инертный разбавитель, такой как лактоза; агенты для грануляции и измельчения, такие как кукурузный крахмал; связующие, такие как крахмал; и смазки, такие как стеарат магния. Таблетки могут быть непокрыты оболочкой или они могут быть покрыты известными в уровне техники способами из эстетических соображений или для пролонгирования высвобождения активных ингредиентов. Препараты для орального применения могут также быть в виде тврдых желатиновых капсул, в которых активный ингредиент смешан с инертным разбавителем. Оральные лекарственные формы по настоящему изобретению могут быть в виде таблеток (пролонгированного и/или мгновенного действия), пастилок, лепшек, порошков или гранул, тврдых или мягких капсул, микрочастиц(например, микрокапсул, микросфер и т.п.), трансбуккальных таблеток, суппозиториев, растворов, суспензий и т.д. В некоторых вариантах настоящее изобретение охватывает способ лечения боли путм введения больному человеку лекарственных форм по данному описанию. Оральная лекарственная форма по данному изобретению содержит около 10-320 мг оксикодона гидрохлорида, уровень 14-гидроксикодеинона в котором составляет менее 25 ч./млн. Особенно предпочтительные дозы для прима дважды в день составляют около 5, около 10, около 15, около 20, около 30,около 40, около 50, около 60, около 80, около 100 или около 160 мг. Особенно предпочтительные дозы для однократного суточного прима составляют около 10, около 20, около 30, около 40, около 60, около 80, около 100, около 120, около 160 или около 320 мг. Оксикодона гидрохлорид, уровень 14-гидроксикодеинона в котором составляет менее 25 ч./млн, можно также готовить в виде препарата с фармацевтически активными эксципиентами, для того чтобы обеспечить пролонгированное высвобождение оксико-7 013208 дона гидрохлорида, уровень 14-гидроксикодеинона в котором составляет менее 25 ч./млн. Такие препараты можно готовить в соответствии с патентами США 5266331; 5508042; 5549912 и 5656295. Из оксикодона гидрохлорид, уровень 14-гидроксикодеинона в котором составляет менее 25 ч./млн,можно также готовить препарат пролонгированного действия в виде любой подходящей таблетки, таблетки, покрытой оболочкой, или препарат в виде отдельных частиц ("мультичастиц"), известный специалистам в данной области техники. Лекарственная форма пролонгированного действия может включать материал пролонгированного действия, который вводится в матрицу наряду с оксикодоном или его солью. Лекарственная форма пролонгированного действия может, необязательно, включать частицы, содержащие оксикодон, уровень 14-гидроксикодеинона в котором составляет менее 25 ч./млн. В некоторых вариантах частицы имеют диаметр около 0,1-2,5 мм, предпочтительно около 0,5-2 мм. Предпочтительно частицы покрыты плнкой материала, который обеспечивает пролонгированное высвобождение в водной среде. Плночное покрытие выбирают таким образом, чтобы достичь нужных свойств высвобождения в сочетании с другими постулированными свойствами. Материал покрытия для препаратов пролонгированного действия по настоящему изобретению предпочтительно должен создавать прочную непрерывную плнку, однородную и эстетичную, способную удерживать пигменты и другие добавки в оболочке,нетоксическую, инертную и нелипнущую. Гранулы, покрытые оболочкой В некоторых вариантах настоящего изобретения используют гидрофобный материал для покрытия инертных фармацевтических гранул, таких как nu pariel 18/20 гранулы, а затем множество полученных тврдых гранул пролонгированного действия можно поместить в желатиновую капсулу в количестве,достаточном для создания эффективной дозы пролонгированного действия при проглатывании и контактировании с окружающей жидкостью, например жидкостью в желудке или растворяющей средой. Препараты в виде гранул пролонгированного действия по настоящему изобретению медленно высвобождают активное вещество по настоящему соединению, например, при проглатывании и экспозиции с желудочными жидкостями, а затем с "кишечными жидкостями". Профиль пролонгированного высвобождения препаратов по изобретению можно изменять, варьируя количество защитного покрытия из гидрофобного материала, изменяя способ добавления пластификатора к гидрофобному материалу, варьируя количество пластификатора относительно гидрофобного материала, включая дополнительные ингредиенты или эксципиенты, изменяя способ производства и т.д. Профиль растворения конечного продукта также можно модифицировать, например, повышая или понижая вязкость замедляющего покрытия. Сфероиды или гранулы, покрытые агентом(ами) по настоящему изобретению, готовят, например,растворяя агент(ы) в воде, а затем напыляя раствор на субстрат, например на nu panel 18/20 гранулы, сопло фирмы Вурстер (Wurster). Необязательно, перед покрытием гранул также добавляют дополнительные ингредиенты, чтобы способствовать связыванию активного вещества с гранулами и/или для окрашивания раствора и т.д. Например, продукт, который включает гидроксипропилметилцеллюлозу и т.д. с красителем или без красителя (например, Опадри, выпускаемый Colorcon, Inc.), можно добавлять к раствору, и раствор перемешивают (например, около 1 ч), прежде чем применять его для напыления на гранулы. Полученный покрытый оболочкой субстрат, в данном примере гранулы, можно затем, необязательно, наносить на защитный(е) агент(ы) для отделения активного вещества (активных веществ) от гидрофобного покрытия пролонгированного высвобождения. Примером подходящего защитного агента является защитный агент, который содержит гидроксипропилметилцеллюлозу. Однако можно использовать любое формоообразующее вещество, известное в технике. Предпочтительно защитный агент не влияет на скорость растворения конечного продукта. Затем гранулы покрывают водной дисперсией гидрофобного материала. Водная дисперсия гидрофобного материала предпочтительно дополнительно включает эффективное количество пластификатора,например триэтилцитрата. Можно использовать готовые водные дисперсии этилцеллюлозы, такие какAquacoat или Surelease. Если используют Surelease, необязательно отдельно добавлять пластификатор. Или же можно применять готовые водные дисперсии акриловых полимеров, такие как Eudragit. Растворы для покрытия по настоящему изобретению предпочтительно помимо плнкообразователя содержат пластификатор, растворитель (т.е. воду), краситель для эстетичности и в качестве отличительного признака продукта. Краситель можно добавлять в раствор терапевтически активного агента вместо,или помимо, водной дисперсии гидрофобного материала. Например, можно придать цвет Aquacoat,используя окрашенные дисперсии на основе спирта или пропиленгликоля, красочные лаки с тонкоизмельчнным алюминием и замутнители, такие как диоксид титана, добавляя красящее вещество со сдвигом к раствору водорастворимого полимера, а затем используя низкий сдвиг для пластицированногоAquacoat. Или же можно использовать любой подходящий способ придания цвета препаратам по настоящему изобретению. Подходящие ингредиенты для придания цвета препарату, когда используют водную дисперсию акрилового полимера, включают диоксид титана и цветные пигменты, такие как пигменты оксида железа. Однако введение пигментов может повысить задерживающий эффект покрытия.-8 013208 Пластицированный гидрофобный материал можно наносить на субстрат, содержащий агент(ы),распылением с применением подходящего оборудования для распыления, известного в технике. В предпочтительном способе используется система с псевдоожиженным слоем фирмы Вурстер, в которой инжекция с помощью воздушного сопла, расположенного внизу, псевдоожижает материал ядра и сушит его, в то время как напыляется акриловое полимерное покрытие. Можно подавать достаточное количество гидрофобного материала, для того чтобы достичь установленного пролонгированного высвобождения агента(ов) при экспозиции покрытого оболочкой субстрата с водными растворами, например с желудочной жидкостью. После покрытия гидрофобным материалом гранулы, необязательно, покрываются дополнительной оболочкой плнкообразователя, такого как Опадри. Это покрытие наносят, если его вообще наносят, чтобы значительно уменьшить спекание (агломерацию) гранул. На высвобождение агента(ов) из препарата пролонгированного действия по настоящему изобретению можно воздействовать далее, т.е. доводить до нужной скорости, добавляя один или более агентов,модифицирующих скорость, или обеспечивая с помощью покрытия один или более путей для прохождения (каналов). Отношение гидрофобного материала к водорастворимому материалу определяется, среди прочих факторов, требуемой скоростью высвобождения и характеристиками растворимости выбранного материала. Модифицирующие высвобождение агенты, которые действуют как порофоры (вспениватели), могут быть органическими или неорганическими и включать материалы, которые могут растворяться, экстрагироваться или вымываться из покрытия в среде, в которой они применяются. Порофоры могут содержать один или более гидрофильных материалов, таких как гидроксипропилметилцеллюлоза. Покрытия для пролонгированного высвобождения по настоящему изобретению могут также включать агенты, стимулирующие разрушение (эрозию), такие как крахмал и камеди (смолы). Покрытия для пролонгированного высвобождения по настоящему изобретению могут также включать материалы, пригодные для получения микропористого слоя в среде, в которой они применяются,такие как поликарбонаты, состоящие из линейных полиэфиров карбоновой кислоты, в полимерной цепи которых повторяются карбонатные группы. Агент, модифицирующий высвобождение, может также представлять собой полупроницаемый полимер. В некоторых предпочтительных вариантах изобретения агент, модифицирующий высвобождение,выбирают из гидроксипропилметилцеллюлозы, лактозы, стеаратов металлов и любых их смесей. Покрытия, обеспечивающие пролонгированное высвобождение по настоящему изобретению, могут также включать способы вывода, включающие по меньшей мере один путь прохождения, вход и т.п. Путь прохождения может создаваться методами, описанными в патентах США 3845770; 3916899,4063064 и 4088864. Матричные препараты В других вариантах настоящего изобретения препараты пролонгированного высвобождения получают с помощью матрицы, необязательно имеющей покрытие, обеспечивающей пролонгированное высвобождение по данному описанию. Материалы, пригодные для включения в матрицу, обеспечивающую пролонгированное высвобождение, могут зависеть от метода, применяемого для получения матрицы. Например, матрица, помимо оксикодона гидрохлорида с содержанием 14-гидроксикодеинона менее 25 ч./млн, может включать гидрофильные и/или гидрофобные материалы, такие как камеди, простые эфиры целлюлозы, акриловые полимеры, белковые материалы; этот перечень не предполагает быть эксклюзивным, и любой фармацевтически приемлемый гидрофобный или гидрофильный материал, способный сообщать агенту(ам) пролонгированное высвобождение и плавящийся (или размягчающийся до такой степени, чтобы подвергаться экструзии), можно применять по настоящему изобретению; легко усвояемые замещнные или незамещнные углеводороды с длинной цепью (C8-C50, особенно С 12-С 40), такие как жирные кислоты, жирные спирты, эфиры глицерина и жирных кислот, минеральные и растительные масла, и природные и синтетические воски, и стеариловый спирт; и полиалкиленгликоли. Из этих полимеров предпочтительными являются акриловые полимеры, особенно Eudragit RSPO,- простые эфиры целлюлозы, особенно гидроксиалкилцеллюлозы и карбоксиалкилцеллюлозы. Оральная лекарственная форма может содержать около 1-80 вес.% по меньшей мере одного гидрофильного или гидрофобного материала. Если гидрофобный материал представляет собой углеводород, его температура плавления предпочтительнонаходится в интервале между 25 и 90 С. Из углеводородных материалов с длинной цепью предпочтительными являются жирные (алифатические) спирты. Оральная лекарственная форма может содержать до 60 вес.% по меньшей мере одного легко усвояемого длинноцепного углеводорода. Предпочтительно оральная лекарственная форма содержит до 60 вес.% по меньшей мере одного полиалкиленгликоля. Гидрофобный материал предпочтительно выбирают из группы, состоящей из алкилцеллюлоз, полимеров и сополимеров акриловой и метакриловой кислот, шеллака, цеина, гидрогенизированного кас-9 013208 торового масла, гидрогенизированного растительного масла или их смесей. В некоторых предпочтительных вариантах настоящего изобретения гидрофобный материал представляет собой фармацевтически приемлемый акриловый полимер, включая, но без ограничения, сополимеры акриловой и метакриловой кислот, метилметакрилат, сополимеры метилметакрилата, этоксиэтилметакрилаты, цианоэтилметакрилат, сополимер аминоалкилметакрилата, полиакриловую кислоту, полиметакриловую кислоту, сополимер метакриловой кислоты алкиламина, полиметилметакрилат, поли(метакриловую кислоту)(ангидрид),полиметакрилат, полиакриламид, полимер ангидрида метакриловой кислоты и сополимеры глицидилметакрилата. В других вариантах изобретения гидрофобный материал выбирают из материалов, таких как гидроксиалкилцеллюлозы, например гидроксипропилметилцеллюлоза и смеси вышеописанных материалов. Предпочтительные гидрофобные материалы являются водонерастворимыми с более или менее выраженными гидрофильными и/или гидрофобными тенденциями. Предпочтительно гидрофобные материалы, применимые по изобретению, имеют температуру плавления примерно от 25-30 С до примерно 200 С, предпочтительно около 45-90 С. А именно гидрофобный материал может включать природные или синтетические воски, жирные спирты (такие как лауриловый, миристиловый, стеариловый, цетиловый или предпочтительно цетостеариловый спирт), жирные кислоты, включая, но без ограничения, эфиры жирных кислот, глицериды жирных кислот (моно-, ди- и триглицериды), гидрогенизированные жиры,углеводороды, обычные воски, стеариновую добавку, стеариловый спирт и гидрофобные и гидрофильные материалы, имеющие углеводородный каркас. Подходящие воски включают, например, пчелиный воск, сладкий воск (glycowax), касторовый воск и карнаубский воск. Для целей настоящего изобретения воскообразное вещество определяется как любой материал, который обычно является тврдым при комнатной температуре и имеет температуру плавления около 25-100 С. Подходящие гидрофобные материалы, которые можно использовать в соответствии с настоящим изобретением, включают перевариваемые замещнные или незамещнные углеводороды с длинной цепью (С 8-С 50, особенно С 12-С 40), такие как жирные кислоты, жирные спирты, эфиры глицерина и жирных кислот, минеральные и растительные масла и природные и синтетические воски. Предпочтительными являются углеводороды, температура плавления которых предпочтительно находится в интервале между 25 и 90 С. Из углеводородных материалов с длинной цепью предпочтительными в некоторых вариантах изобретения являются жирные (алифатические) спирты. Оральная лекарственная форма может содержать до 60 вес.% по меньшей мере одного легкоусвояемого (перевариваемого) длинноцепного углеводорода. В состав матричных препаратов предпочтительно входит комбинация двух или более гидрофобных материалов. Если вводится дополнительный гидрофобный материал, его предпочтительно выбирают из природных и синтетических восков, жирных кислот, жирных спиртов и их смесей. Примеры включают пчелиный воск, карнаубский воск, стеариновую кислоту и стеариловый спирт. Предполагается, что этот перечень не является эксклюзивным. Одна особая подходящая матрица содержит по меньшей мере одну водорастворимую гидроксиалкилцеллюлозу, предпочтительно по меньшей мере один С 12-С 36, предпочтительно С 14-С 22 алифатический спирт и, необязательно, один полиалкиленгликоль. По меньшей мере одна гидроксиалкилцеллюлоза представляет собой предпочтительно гидрокси(С 1-С 6)алкилцеллюлозу, такую как гидроксипропилцеллюлоза, гидроксипропилметилцеллюлоза и особенно гидроксиэтилцеллюлоза. Количество по меньшей мере одной гидроксиалкилцеллюлозы в оральной лекарственной форме по настоящему изобретению определяется, среди прочего, точной скоростью высвобождения нужного оксикодона гидрохлорида. По меньшей мере этот один алифатический спирт может являться, например, лауриловым спиртом, миристиловым спиртом или стеариловым спиртом. Однако в особенно предпочтительных вариантах оральной лекарственной формы по настоящему изобретению по меньшей мере один алифатический спирт представляет собой цетиловый спирт или цетостеариловый спирт. Количество по меньшей мере одного алифатического спирта в оральной лекарственной форме по настоящему изобретению определяется, как указано выше, точной скоростью нужного высвобождения опиоидоксикодона. Это также зависит от того,присутствует или отсутствует в оральной лекарственной форме по меньшей мере один полиалкиленгликоль. В отсутствие по меньшей мере одного полиалкиленгликоля оральная лекарственная форма, предпочтительно оральная лекарственная форма, предпочтительно содержит 20-50 вес.% по меньшей мере одного алифатического спирта. Когда в оральной лекарственной форме присутствует по меньшей мере один полиалкиленгликоль, тогда общий вес по меньшей мере одного алифатического алкоголя и по меньшей мере одного полиалкиленгликоля предпочтительно составляет 20-50 вес.% от общей лекарственной формы. В одном варианте изобретения отношение, например, по меньшей мере одной гидроксиалкилцеллюлозы или акрилового полимера по меньшей мере к одному алифатическому спирту/полиэтиленгликолю определяется весовым отношением (вес./вес.), причм предпочтительным является отношение,например, по меньшей мере одной гидроксиалкилцеллюлозы или акрилового полимера по меньшей мере к одному алифатическому спирту/полиэтиленгликолю между 1:2 и 1:4 и особенно предпочтительно отношение между 1:3 и 1:4.- 10013208 По меньшей мере один полиалкиленгликоль может представлять собой, например, полипропиленгликоль или, что более предпочтительно, полиэтиленгликоль. Среднечисленная молекулярная масса по меньшей мере одного полиалкиленгликоля предпочтительно равна 1000-15000, особенно предпочтительно 1500-12000. Другая подходящая матрица, обеспечивающая пролонгированное высвобождение, содержит алкилцеллюлозу (особенно этилцеллюлозу), алифатический спирт С 12-С 36 и, необязательно, полиалкиленгликоль. В другом предпочтительном варианте изобретения матрица включает фармацевтически приемлемую комбинацию по меньшей мере двух гидрофобных материалов. Помимо вышеприведнных ингредиентов, матрица с пролонгированным высвобождением может также содержать соответствующие количества других материалов, например разбавителей, смазок, связующих, веществ, способствующих грануляции, красителей, веществ, придающих вкус и запах, и веществ, способствующих проглатыванию, обычных в области фармацевтики. Матрицы-макрочастицы Для упрощения приготовления тврдой оральной лекарственной формы пролонгированного действия по настоящему изобретению можно использовать любой известный специалистам в данной области техники способ приготовления матричного препарата. Например, включение в матрицу можно осуществлять, (а) создавая гранулы, содержащие по меньшей мере одну водорастворимую гидроксиалкилцеллюлозу и оксикодона гидрохлорид с содержанием 14-гидроксикодеинона менее 25 ч./млн; (б) смешивая гранулы, содержащие гидроксиалкилцеллюлозу по меньшей мере с одним С 12-С 36 алифатическим спиртом; и (в), необязательно, прессование и формование гранул. Предпочтительно гранулы формуют влажной грануляцией гидроксиалкилцеллюлозных гранул с водой. В других альтернативных вариантах изобретения осуществляют сфероидизацию агента, придающего сфероидную форму, вместе с активным агентом. Предпочтительным сфероидизирующим агентом является микрокристаллическая целлюлоза. Подходящей микрокристаллической целлюлозой является,например, материал, продаваемый под названием Avicel РН 101 (Trade Mark, FMC Corporation). В таких вариантах изобретения, помимо активного ингредиента и сфероидизирующего агента, сфероид (эллипсоид вращения) может также содержать связующее. Подходящие связующие, такие как низковязкие водорастворимые полимеры, общеизвестны специалистам в области фармацевтики. Однако предпочтительной является водорастворимая гидрокси(низший алкил)целлюлоза, такая как гидроксипропилцеллюлоза. Кроме того (или же в качестве альтернативы), сфероиды могут содержать водонерастворимый полимер, в особенности акриловый полимер, акриловый сополимер, такой как сополимер метакриловой кислоты и этилакрилата, или этилцеллюлозу. В таких вариантах изобретения покрытие, обеспечивающее пролонгированное высвобождение, как правило, включает гидрофобный материал, такой как (а) воск,либо самостоятельно, либо в смеси с жирным спиртом; или (б) шеллак или цеин. Матрица, полученная экструзией в расплаве Матрицы пролонгированного действия можно также получать методами грануляции расплава или экструзией расплава. Обычно методы грануляции расплава включают плавление тврдого при обычной температуре гидрофобного материала, например воска, и смешение с ним лекарства в виде порошка. Для получения лекарственной формы пролонгированного действия может быть необходимо ввести в расплавленный гидрофобный воск дополнительное гидрофобное вещество, например этилцеллюлозу или водонерастворимый акриловый полимер. Примеры препаратов пролонгированного действия, полученных методами грануляции расплава, имеются в патенте США 4861598. Дополнительный гидрофобный материал может содержать один или более водонерастворимых воскообразных термопластичных веществ, возможно, в смеси с одним или более воскообразных термопластичных веществ, менее гидрофобных, нежели указанные один или более водонерастворимых воскообразных веществ. Для того чтобы достичь постоянного высвобождения, индивидуальные воскообразные вещества в препарате должны практически не разрушаться и не растворяться в желудочно-кишечных жидкостях на начальных фазах выделения. Применяемыми водонерастворимыми воскообразными веществами могут быть такие водонерастворимые воскообразные вещества, у которых растворимость в воде ниже примерно 1:5000 (вес./вес.). Помимо вышеуказанных ингредиентов матрица пролонгированного действия может также содержать соответствующие количества других материалов, например разбавителей, смазок, связующих, гранулирующих агентов, красителей, веществ, придающих вкус и запах, и веществ, способствующих проглатыванию, обычных в фармацевтической технике. Количества этих добавок должно быть достаточно для того, чтобы оказать нужное действие на заданный препарат. Помимо вышеуказанных ингредиентов, матрица пролонгированного действия, содержащая отдельные частицы ("мультичастицы"), полученные экструзией расплава, могут также содержать подходящие количества других материалов, например разбавителей, смазок, связующих, гранулирующих агентов,красителей, веществ, придающих вкус и запах, и веществ, способствующих проглатыванию, обычных в фармацевтической технике, в количествах, при необходимости составляющих около 50% от веса макрочастиц.- 11013208 Конкретные примеры фармацевтически приемлемых носителей и эксципиентов, которые можно использовать для приготовления оральных лекарственных форм, описаны в Handbook of PharmaceuticalExcipients, American Pharmaceutical Association (1986). Отдельные частицы ("мультичастицы"), полученные экструзией расплава Приготовление соответствующей матрицы экструзией расплава по настоящему изобретению может, например, включать стадии смешения оксикодона гидрохлорида с содержанием 14-гидроксикодеинона менее 25 ч./млн по меньшей мере с одним гидрофобным материалом и предпочтительно с дополнительным гидрофобным материалом для получения гомогенной смеси. Затем гомогенную смесь нагревают до температуры, достаточной, по меньшей мере, для размягчения смеси до состояния, при котором возможна е экструзия. Затем полученную гомогенную смесь экструдируют, получая нити. Экструдат предпочтительно охлаждают и разрезают на отдельные частицы любыми известными в уровне техники методами. Затем "мультичастицы" делят на стандартные дозы. Экструдат предпочтительно имеет диаметр около 0,1-5 мм и обеспечивает пролонгированное высвобождение терапевтически активного агента примерно в течение 8-24 ч. Возможный способ экструзии расплава по настоящему изобретению включает прямую дозированную подачу в экструдер гидрофобного материала, оксикодона гидрохлорида с содержанием 14-гидроксикодеинона менее 25 ч./млн и необязательного связующего; нагревание гомогенной смеси; экструзию гомогенной смеси с образованием при этом нитей; охлаждение нитей, содержащих гомогенную смесь; разрезание нитей на частицы размером около 0,1-12 мм и разделение указанных частиц на стандартные дозы. В данном аспекте изобретения реализуется более или менее непрерывный способ производства. Диаметр щели или выходного отверстия экструдера можно также корректировать таким образом,чтобы менять толщину выдавливаемых нитей. Кроме того, выходное отверстие (участок) экструдера на выходе необязательно должно быть круглым; оно может быть продолговатым, прямоугольным. Выходящие нити можно разрезать на частицы с помощью резака с нагретой проволокой, гильотинных ножниц и т.д. Отдельные частицы, полученные экструзией расплава, могут быть в форме гранул, сфероидов или шариков в зависимости от выходного отверстия экструдера. Для целей настоящего изобретения выражения "отдельная(ые) частица(ы) ("мультичастицы"), полученные экструзией расплава", или "системы отдельных частиц, полученных экструзией расплава", или "частицы, полученные экструзией расплава" относятся к множеству элементов предпочтительно аналогичного размера и/или аналогичной конфигурации, содержащих один или более активных агентов и один или более эксципиентов, предпочтительно включающих гидрофобный материал по данному описанию. Отдельные частицы ("мультичастицы"),полученные экструзией расплава, имеют длину около 0,1-12 мм и диаметр около 0,1-5 мм. Кроме того,следует понимать, что отдельные частицы ("мультичастицы"), полученные экструзией расплава, могут иметь в пределах этих размеров любую форму. Или же экструдат можно просто разрезать на отрезки заданной длины и делить на стандартные дозы терапевтически активного агента, исключив стадию сфероидизации. В одном предпочтительном варианте изобретения оральные лекарственные формы готовят, помещая в капсулу эффективное количество отдельных частиц ("мультичастиц"), полученных экструзией расплава. Например, множество полученных экструзией расплава отдельных частиц можно поместить в желатиновую капсулу в количестве, достаточном для обеспечения эффективной дозы пролонгированного действия после проглатывания и контакта с желудочной жидкостью. В другом предпочтительном варианте изобретения подходящее количество экструдата из отдельных частиц ("мультичастиц") стандартными методами прессуют в оральную таблетку, используя обычное оборудование для таблетирования. Методы и композиции для изготовления таблеток (прессованных и формованных), капсул (тврдых и мягких желатиновых) и пилюль также описаны в Remington's Pharmaceutical Sciences, (Arthur Osol, editor), 1553-1593 (1980). Ещ в одном предпочтительном варианте изобретения экструдат может быть в форме таблеток, как представлено в патенте США 4957681 (Klimesch et al.), как более подробно описано выше. Необязательно, системы полученных экструзией в расплаве отдельных частиц или таблетки могут иметь покрытие, или желатиновая капсула, содержащая "мультичастицы", может иметь дополнительное покрытие, при этом покрытие, обеспечивающее пролонгированное освобождение, таково, как описанные выше покрытия для пролонгированного высвобождения. Такие покрытия предпочтительно включают достаточное количество гидрофобного материала, для того чтобы выигрыш в потере веса составлял около 2-30%, хотя внешнее покрытие, среди прочего, может больше зависеть от заданной скорости высвобождения. В полученные экструзией в расплаве стандартные лекарственные формы по настоящему изобретению можно перед инкапсулированием дополнительно включать комбинации экструдированных из расплава частиц. Кроме того, стандартные лекарственные формы могут также включать некоторое количество агента мгновенного действия, для того чтобы вызвать высвобождение. Агент мгновенного высвобождения можно включать, например, в виде отдельных частиц (пеллет) в желатиновую капсулу или им можно покрывать поверхность "мультичастиц" после приготовления лекарственных форм (например,- 12013208 покрытие или матрица пролонгированного высвобождения). Для достижения нужного эффекта стандартные лекарственные формы по настоящему изобретению могут также содержать комбинацию гранул пролонгированного высвобождения и матричных отдельных частиц ("мультичастиц"). Препараты пролонгированного действия по настоящему изобретению предпочтительно медленно высвобождают агент(ы), например, при проглатывании и экспозиции с желудочными жидкостями, а затем с "кишечными жидкостями". Профиль пролонгированного высвобождения экструдированных из расплава препаратов по изобретению может изменяться, например, путм изменения количества замедлителя, например гидрофобного материала, путм изменения количества пластификатора относительно гидрофобного материала и путм включения дополнительных ингредиентов или эксципиентов путм изменения метода производства и т.д. В других вариантах изобретения экструдированный из расплава материал получают без включения оксикодона гидрохлорида с содержанием 14-гидроксикодеинона менее 25 ч./млн, который добавляют позже к экструдату. Такие препараты обычно содержат агенты, смешиваемые с экструдированным материалом матрицы, а затем смесь таблетируют, получая препарат пролонгированного действия. Покрытия Лекарственные формы по настоящему изобретению могут, необязательно, покрываться одним или более материалом, пригодным для регуляции высвобождения или для защиты препарата. В одном варианте изобретения покрытия создаются для того, чтобы сделать возможным рН-зависимое или рН-независимое высвобождение. рН-зависимое покрытие служит для высвобождения активного вещества в заданных областях желудочно-кишечного (GI) тракта (ЖКТ), например в желудке или тонком кишечнике, так что получается кривая (профиль) всасывания, позволяющая обеспечить аналгезию у пациента, по меньшей мере, в течение примерно восьми часов и предпочтительно около двенадцати-двадцати четырх часов. Когда желательно рН-независимое покрытие, создают покрытие для оптимального высвобождения вне зависимости от изменения рН в окружающей жидкости, например в ЖКТ. Также можно готовить композиции, которые высвобождают часть дозы в одной заданной области ЖКТ, например желудке, и выделяют остальную часть дозы в другой области ЖКТ, например в тонком кишечнике. Препараты согласно изобретению, в которых применяются рН-зависимые покрытия, могут также придавать эффект повторного действия, когда незащищенное лекарство, нанеснное поверх энтеросолюбильной оболочки, выделяется в желудке, тогда как остальная часть, защищенная энтеросолюбильной оболочкой, выделяется ниже, в ЖКТ. рН-зависимые покрытия, которые можно использовать по настоящему изобретению, включают шеллак, ацетатфталат целлюлозы (САР), поливинилацетатфталат (PVAP),фталат гидроксипропилметилцеллюлозы и сополимеры эфиров метакриловой кислоты, цеин и т.п. В некоторых предпочтительных вариантах изобретения субстрат (например, гранула ядра таблетки,матричная частица), содержащий оксикодона гидрохлорид с содержанием 14-гидроксикодеинона менее 25 ч./млн, покрывают гидрофобным материалом, выбранным из (i) алкилцеллюлозы; (ii) акрилового полимера или (iii) их смесей. Покрытие можно наносить в виде органического или водного раствора или дисперсии. Покрытие можно наносить, чтобы получить выигрыш в весе субстрата около 2-25% при достижении заданного профиля пролонгированного действия. Покрытия, получаемые при использовании водных дисперсий, подробно описаны, например, в патентах США 5273760 и 5286493. Другие примеры препаратов и покрытий пролонгированного действия, которые можно применять по данному изобретению, включают препараты и покрытия, описанные в патентах США 5324351 и 5472712. Полимеры алкилцеллюлозы Материалы и полимеры целлюлозы, включая алкилцеллюлозы, обеспечивают гидрофобные материалы, которые очень подходят для покрытия гранул по изобретению. Лишь в качестве примера, предпочтительным полимером алкилцеллюлозы является этилцеллюлоза, хотя специалист в данной области техники понимает, что можно применять другие полимеры целлюлозы и/или алкилцеллюлозы, самостоятельно или в комбинации, в качестве целого гидрофобного покрытия по данному изобретению или в качестве его части. Акриловые полимеры В других предпочтительных вариантах настоящего изобретения гидрофобный материал, представляющий покрытие пролонгированного высвобождения, представляет собой фармацевтически приемлемый акриловый полимер, включая, но без ограничения, сополимеры акриловой кислоты и метакриловой кислоты, этоксиэтилметакрилаты, цианоэтилметакрилат, полиакриловую кислоту, сополимер метакриловой кислоты алкиламида, полиметилметакрилат, полиметакрилат, сополимер полиметилметакрилата,полиакриламид, сополимер аминоалкилметакрилата, поли(метакриловой кислоты ангидрид) и сополимеры глицидилметакрилата. В некоторых предпочтительных вариантах изобретения акриловый полимер состоит из одного или более сополимеров метакрилата аммония. Сополимеры метакрилата аммония общеизвестны в технике и описаны в NF XVII как полностью полимеризованные сополимеры эфиров акриловой и метакриловой кислот с низким содержанием четвертичных аммониевых групп. Для получения желательного профиля растворения может быть необходимо ввести два или более- 13013208 сополимера аммония метакрилата с различными физическими свойствами, такие как различные молярные соотношения четвертичных аммониевых групп с нейтральными метакриловыми эфирами. Некоторые полимеры типа полимеров эфиров метакриловой кислоты применимы для получения рН-зависимых покрытий, которые можно использовать по настоящему изобретению. Например, имеется семейство сополимеров, синтезированных из диэтиламиноэтилметакрилата и других нейтральных метакриловых эфиров, также известных как сополимеры метакриловой кислоты или полимерные метакрилаты, выпускаемые промышленностью под названием Eudragit от Rohm Tech, Inc. Существует несколько различных типов Eudragit. Например, Eudragit E является примером сополимера метакриловой кислоты, который набухает и растворяется в кислых средах. Eudragit L является сополимером метакриловой кислоты, который не набухает при рН 5,7 и растворим примерно при рН 6. Eudragit S не набухает при рН 6,5 и растворим примерно при рН 7. Eudragit RL и Eudragit RS набухают в воде, и количество воды, адсорбируемое этими полимерами, зависит от значения рН, однако лекарственные формы, покрытые Eudragit RL и Eudragit RS, являются рН-независимыми. В некоторых предпочтительных вариантах изобретения акриловые покрытия содержат смесь двух акриловых полимерных лаков, промышленно выпускаемых Rohm Pharma под торговой маркой EudragitRL30D и Eudragit RS30D соответственно. Eudragit RL30D и Eudragit RS30D являются сополимерами акрилового и метакрилового эфиров с низким содержанием четвертичных аммониевых групп, молярное отношение аммониевых групп к оставшимся нейтральным метакриловым эфирным группам составляет 1:20 в Eudragit RL30D и 1:40 в Eudragit RS30D. Средняя молекулярная масса составляет около 150000. Кодовые названия RL (высокая проницаемость) и RS (низкая проницаемость) относятся к свойствам проницаемости этих агентов. Смеси Eudragit RL/RS являются нерастворимыми в воде и усвояемыми жидкостями. Однако покрытия из них набухают и являются проницаемыми в водных растворах и способствующих пищеварению жидкостях. Дисперсии Eudragit RL/RS по настоящему изобретению можно смешивать друг с другом в любых желательных пропорциях, для того чтобы в конце получить препарат пролонгированного действия с нужным профилем растворения. Заданные препараты пролонгированного действия можно получать, например, с применением замедляющих покрытий, полученных из 100% Eudragit RL, 50% Eudragit RL и 50% Eudragit RS и 10% Eudragit RL:90% Eudragit RS. Конечно, специалист в данной области техники понимает, что можно также применять другие акриловые полимеры, такие, например, какEudragit L. Пластификаторы В вариантах по настоящему изобретению, в которых покрытия содержат водную суспензию гидрофобного материала, включение эффективного количества пластификатора в водную дисперсию гидрофобного материала дополнительно улучшает физические свойства покрытия пролонгированного высвобождения. Например, так как этилцеллюлоза имеет относительно высокую температуру стеклования и не образует гибких плнок при нормальных условиях покрытия, предпочтительно, перед тем как использовать его в качестве материала для покрытия, вводить пластификатор в этилцеллюлозное покрытие пролонгированного действия. Как правило, количество пластификатора, включнного в плнкообразующий раствор, определяется исходя из концентрации плнкообразователя, например наиболее часто оно составляет около 1-50% от веса плнкообразующего вещества. Концентрацию пластификатора, однако,можно по-настоящему определить только после тщательных экспериментов с использованием конкретного раствора для покрытия и способа применения. Примеры подходящих пластификаторов для этилцеллюлозы включают водонерастворимые пластификаторы, такие как дибутилсебацинат, диэтилфталат, триэтилцитрат, трибутилцитрат и триацетин, хотя можно использовать другие водонерастворимые пластификаторы (такие как ацетилированные моноглицериды, эфиры фталевых кислот, касторовое масло и т.д.). Триэтилцитрат является особенно предпочтительным пластификатором для водных дисперсий этилцеллюлозы по данному изобретению. Примеры подходящих пластификаторов для акриловых полимеров по настоящему изобретению включают, но без ограничения, эфиры лимонной кислоты, такие как триэтилцитрат NF XVI, трибутилцитрат, дибутилфталат и, возможно, 1,2-пропиленгликоль. Другие пластификаторы, оказавшиеся подходящими для повышения эластичности плнок, образованных из акриловых плнок, таких как растворы лаков Eudragit RL/RS, включают полиэтиленгликоли, пропиленгликоли, диэтилфталат, касторовое масло и триацетин. Триэтилцитрат является особенно предпочтительным пластификатором для водных дисперсий этилцеллюлозы по данному изобретению. Далее было найдено, что добавление малого количества талька снижает тенденцию водной дисперсии к слипанию в ходе процессирования и действует как полирующий агент. Осмотическая лекарственная форма пролонгированного действия Лекарственные формы пролонгированного действия по настоящему изобретению можно также приготовить в виде осмотических лекарственных препаратов. Осмотические лекарственные формы предпочтительно включают двухслойное ядро, содержащее слой лекарства (включающий оксикодона гидрохлорид с уровнем 14-гидроксикодеинона ниже 25 ч./млн), и слой средства доставки или "вытес- 14013208 няющий, подталкивающий" слой, причм двухслойное ядро окружено полупроницаемой стенкой и, необязательно, содержит по меньшей мере один расположенный в нм проход (для лекарства). Выражение "проход" ("путь"), применяемое в целях настоящего изобретения, включает отверстие,выход, канал, пору, пористый элемент, с помощью которых оксикодона гидрохлорид с содержанием 14-гидроксикодеинона менее 25 ч./млн может прокачиваться, диффундировать или мигрировать через волокно, капиллярную трубку, пористый наружный слой, пористое включение, микропористый элемент или пористую композицию. Проход может также включать соединение, которое эродирует или вымывается со стенки в используемой жидкой среде, образуя по меньшей мере один проход. Типичные соединения для образования прохода включают эродируемую полигликолевую кислоту или полимолочную кислоту на стенке; студенистую (желатинозную) нить; удаляемый водой поливиниловый спирт; вымываемые жидкостью порообразующие полисахариды, кислоты, соли или оксиды. Проход может образовываться при вымывании соединения со стенки, например сорбита, сахарозы, лактозы, мальтозы или фруктозы, с образованием соизмеримого с порой прохода пролонгированного действия. Лекарственную пору можно выпускать с одним или более проходами на расстоянии друг от друга на одной или более поверхностях лекарственной формы. Проход и оборудование для образования прохода раскрывается в патентах США 3845770; 3916899; 4063064 и 4088864. Проходы, имеющие соответствующие размеры, форму и адаптированные для пролонгированного высвобождения, в виде пор для высвобождения, образованных вымыванием водой таким образом, чтобы создать пору для высвобождения со скоростью, необходимой для пролонгированного действия, раскрываются в патентах США 4200098 и 4285987. В некоторых вариантах изобретения слой лекарства может также включать по меньшей мере один полимерный гидрогель. Полимерный гидрогель может иметь среднюю молекулярную массу около 500-6000000. Примеры полимерных гидрогелей включают, но без ограничения, полимер мальтодекстрина формулы (C6H12O5)nH2O, где n обозначает 3-7500, а среднечисленная молекулярная масса полимера мальтодекстрина составляет 500-1250000; полиалкиленоксид, например полиэтиленоксид и полипропиленоксид, имеют среднечисленную молекулярную массу 50000-750000, и, более конкретно, среднечисленная молекулярная масса полиэтиленоксида равна по меньшей мере одной из масс 100000, 200000,300000 или 400000; щелочную карбоксиалкилцеллюлозу, где щелочной металл представляет собой натрий или калий, алкил обозначает метил, этил, пропил или бутил, со среднечисленной молекулярной массой 10000-175000 и сополимер этилена и акриловой кислоты, включая метакриловую и этакриловую кислоту, со среднечисленной молекулярной массой 10000-500000. В некоторых вариантах настоящего изобретения слой для доставки или "вытесняющий, подталкивающий" слой содержит осмополимер. Примеры осмополимера включают, но без ограничения, представителя, выбранного из группы, состоящей из полиалкиленоксида и карбоксиалкилцеллюлозы. Среднечисленная молекулярная масса полиалкиленоксида составляет 1000000-10000000. Полиалкиленоксид можно выбирать из группы, состоящей из полиметиленоксида, полиэтиленоксида, полипропиленоксида со средней молекулярной массой 1000000, полиэтиленоксида со средней молекулярной массой 5000000,полиэтиленоксида со средней молекулярной массой 7000000, сшитого полиметиленоксида со средней молекулярной массой 1000000 и полипропиленоксида со средней молекулярной массой 1200000. Типичный осмополимер карбоксиалкилцеллюлозу выбирают из группы, состоящей из щелочной карбоксиалкилцеллюлозы, натрийкарбоксиметилцеллюлозы, калийкарбоксиметилцеллюлозы, натрийкарбоксиэтилцеллюлозы, литийкарбоксиметилцеллюлозы, карбоксиалкилгидроксиалкилцеллюлозы, карбоксиметилгидроксиэтилцеллюлозы, карбоксиэтилгидроксиэтилцеллюлозы и карбоксиметилгидроксипропилцеллюлозы. У осмополимеров, применяемых для вытесняющего слоя, наблюдается градиент осмотического давления по полупроницаемой стенке. Осмополимеры всасывают жидкость в лекарственную форму, при этом набухая и увеличиваясь в объме как осмотический гидрогель (также известный как осмогель), в результате чего они вытесняют (выталкивают) оксикодона гидрохлорид, содержащий менее 25 ч./млн 14-гидроксикодеинона. Выталкивающий (вытесняющий) слой может также включать одно или более осмотически активных соединений, также известных как "осмотические агенты" или осмотически эффективные растворнные вещества. Они всасывают окружающую жидкость, например, из желудочно-кишечного тракта в лекарственную форму и способствуют кинетике доставки вытесняющего слоя. Примеры осмотически активных соединений включают представителей, выбранных из группы, состоящей из осмотических солей и осмотических углеводов. Примеры конкретных осмотических агентов включают, но без ограничения,хлорид натрия, хлорид калия, сульфат магния, фосфат лития, хлорид лития, фосфат натрия, сульфат калия, сульфат натрия, фосфат калия, фруктозу и мальтозу. Вытесняющий (выталкивающий) слой может, необязательно, включать гидроксипропилалкилцеллюлозу со среднечисленной молекулярной массой 9000-450000. Гидроксипропилалкилцеллюлозу выбирают из группы, состоящей из гидроксипропилметилцеллюлозы, гидроксипропилэтилцеллюлозы, гидроксипропилизопропилцеллюлозы, гидроксипропилбутилцеллюлозы и гидроксипропилпентилцеллюлозы. Вытесняющий слой, необязательно, может содержать нетоксический пигмент или краситель. Примеры пигментов или красителей включают, но без ограничения, краситель Управления по лекарственным средствам и пищевым продуктам США (FDC), такой как FDC1 синий краситель, FDC4- 15013208 красный краситель, красную окись железа, жлтую окись железа, диоксид титана, угольно-чрный и индиго. Вытесняющий слой может также, необязательно, содержать антиоксидант для ингибирования окисления ингредиентов. Некоторые примеры антиоксидантов включают, но без ограничения, представителей группы, состоящей из аскорбиновой кислоты, аскорбилпальмитата, бутилированного гидроксианизола, смеси 2 и 3-трет-бутил-4-гидроксианизола, бутилированного гидрокситолуола, изоаскорбата натрия, дигидрогваретовой кислоты, сорбата калия, бисульфата натрия, метабисульфата натрия, сорбиновой кислоты, аскорбата калия, витамина Е, витамина Е, 4-хлор-2,6-дитрет-бутилфенола, альфа-токоферола и пропилгаллата. В некоторых альтернативных вариантах изобретения лекарственные формы содержат гомогенное ядро, включающее оксикодона гидрохлорид с уровнем 14-гидроксикодеинона менее 25 ч./млн, фармацевтически приемлемый полимер (например, полиэтиленоксид), необязательно, вещество, вызывающее дезинтеграцию (например, поливинилпирролидон), необязательно, энхансер всасывания (например,жирная кислота, поверхностно-активное вещество, хелатирующий агент, соль желчной кислоты и т.д.). Гомогенное ядро окружено полупроницаемой стенкой (перегородкой), имеющей проход (описанный выше) для высвобождения оксикодона гидрохлорида с уровнем 14-гидроксикодеинона менее 25 ч./млн. В некоторых вариантах изобретения полупроницаемая стенка (перегородка) содержит вещество,выбранное из группы, состоящей из полимера сложного эфира целлюлозы, полимера простого эфира целлюлозы и полимера сложного-простого эфиров целлюлозы. Типичные полимеры для стенок (перегородок) выбирают из группы, состоящей из ацилата целлюлозы, диацилата целлюлозы, триацилата целлюлозы, ацетата целлюлозы, диацетата целлюлозы, триацетата целлюлозы, алкенилатов моно-, ди- и трицеллюлозы и алкинилатов моно-, ди- и трицеллюлозы. Полицеллюлоза, применяемая по данному изобретению, имеет среднечисленную молекулярную массу 20000-7500000. Другие полупроницаемые полимеры для целей настоящего изобретения представляют собой ацетальдегид диметилцеллюлозы ацетата, этилкарбамат ацетата целлюлозы, метилкарбамат ацетата целлюлозы, пропилкарбамат диацетата целлюлозы, ацетата целлюлозы диэтиламиноацетат; полупроницаемый полиамид; полупроницаемый полиуретан; полупроницаемый сульфированный полистирол; полупроницаемый сшитый полимер, образующийся при совместном осаждении полианиона и поликатиона, раскрываемом в патентах США 3173876; 3276586; 3541005; 3541006 и 3546876; полупроницаемые полимеры, раскрываемые Loeb и Sourirajan в патенте США 3133132; полупроницаемые сшитые полистиролы; полупроницаемый сшитый поли(стиролсульфонат натрия); полупроницаемый сшитый поли(винилбензилтриметиламмония хлорид) и полупроницаемые полимеры с проницаемостью жидкости 2,510-8-2,510-2 (см 2/чатм), выражаемой на атмосферу разницы гидростатического или осмотического давления вдоль полупроницаемой стенки. Другие полимеры, применимые по настоящему изобретению,известны в технике в патентах США 3845770; 3916899 и 4160020 и в Handbook of Common Polymers,Scott, J.R. and W.J. Roff, 1971, CRC Press, Cleveland, Ohio. В некоторых вариантах предпочтительная полупроницаемая стенка является нетоксической, инертной и сохраняет свою физическую и химическую целостность в период высвобождения лекарства. В некоторых вариантах изобретения лекарственная форма содержит связующее. Пример связующего включает, но без ограничения, терапевтически приемлемый виниловый полимер со средневязкостной молекулярной массой 5000-350000, выбранный из группы, состоящей из поли-н-виниламида, поли-нвинилацетамида, поливинилпирролидона, также называемого поли-н-винилпирролидон, поли-н-винилкапролактона, поли-н-винил-5-метил-2-пирролидона и сополимеров поли-н-винилпирролидона с соединением, выбранным из группы, состоящей из винилацетата, винилового спирта, винилхлорида, винилфторида, винилбутирата, виниллаурата и винилстеарата. Другие связующие включают, например, камедь(гуммиарабик), крахмал, желатин и гидроксипропилалкилцеллюлозу со средней молекулярной массой 9200- 250000. В некоторых вариантах изобретения лекарственная форма содержит смазки, которые можно использовать в процессе производства лекарственной формы для предупреждения прилипания к стенке пресс-формы или к поверхностям пуансона. Примеры смазок включают, но без ограничения, стеарат магния, стеарат натрия, стеариновую кислоту, стеарат кальция, олеат магния, олеиновую кислоту, олеат калия, каприловую кислоту, стеарилфумарат натрия и пальмитат магния. В некоторых предпочтительных вариантах настоящее изобретение включает терапевтическую композицию, содержащую некоторое количество оксикодона гидрохлорида с уровнем 14-гидроксикодеинона менее 25 ч./млн, эквивалентное 10-40 мг оксикодона гидрохлорида, 25-500 мг полиалкиленоксида со средней молекулярной массой 150000-500000, 1-50 мг поливинилпирролидона со средней молекулярной массой 40000 и от 0 до около 7,5 мг смазки. Суппозитории Препараты пролонгированного действия по настоящему изобретению могут быть приготовлены в виде суппозитория для ректального введения, содержащего соответствующую основу суппозитория и оксикодона гидрохлорид с уровнем 14-гидроксикодеинона менее 25 ч./млн. Получение препаратов пролонгированного действия в виде суппозиториев описано в патенте США 5215758.- 16013208 Перед всасыванием лекарство должно быть в растворе. В случае суппозиториев образованию раствора должно предшествовать растворение основы суппозитория или плавление (размягчение) основы с последующим выделением лекарства из основы суппозитория в ректальную жидкость. Всасывание лекарства в организм можно изменять с помощью основы суппозитория. Поэтому конкретную основу суппозитория для применения с конкретным лекарством следует выбирать, принимая во внимание физические свойства лекарства. Например, лекарства, растворимые в липидах, не без труда выделяются в ректальную жидкость, но лекарства, лишь слаборастворимые в липидной основе, легко выделяются в ректальную жидкость. Среди различных факторов, влияющих на время растворения (или время высвобождения) лекарств,площадь поверхности лекарства, соприкасающаяся (презентирующая) со средой растворителя, рН раствора, растворимость вещества в конкретной среде растворителя и движущая сила концентрации насыщения растворнных материалов в среде растворителя. Обычно факторы, влияющие на всасывание лекарств из суппозиториев, применяемых ректально, включают носитель суппозитория, рН в месте всасывания, pKa лекарства, степень ионизации и растворимость в липидах. Выбранная основа суппозитория должна быть совместима с активным компонентом по данному изобретению. Кроме того, основа суппозитория предпочтительно является нетоксической и нераздражающей в отношении слизистых мембран, плавится или растворяется в ректальных жидкостях и устойчива при хранении. В некоторых предпочтительных вариантах настоящего изобретения в случае как водорастворимых,так и водонерастворимых лекарств основа суппозиториев содержит воск на основе жирных кислот, выбранный из группы, состоящей из моно-, ди- и триглицеридов насыщенных природных жирных кислот с длиной цепи С 12-С 18. Для получения суппозиториев по настоящему изобретению могут применяться другие эксципиенты. Например, для придания нужной формы, подходящей для ректального введения, может применяться воск. Эта система может применяться в отсутствие воска, но с добавлением разбавителя, помещаемого в желатиновую капсулу как для ректального, так и для орального введения. Примеры подходящих промышленных моно-, ди- и триглицеридов включают насыщенные природные жирные кислоты с цепью из 12-18 углеродных атомов, выпускаемых под торговой маркой trade nameNovata ТМ (типы АВ, АВ, В, ВС, BD, ВВС, Е, BCF, С, D и 299), производятся фирмой Henkel, a Witepsol ТМ (типы Н 5, Н 12, Н 15, Н 175, Н 185, Н 19, Н 32, Н 35, Н 39, Н 42, W25, W31, W35, W45, S55, S58, Е 75, Е 76 и Е 85) производятся фирмой Dynamit Nobel. Другие фармацевтически приемлемые основы суппозиториев можно применять, целиком или частично, вместо вышеуказанных моно-, ди- и триглицеридов. Количество основы в суппозитории определяется размером (т.е. действительной массой) лекарственной формы, количеством основы (например,альгината) и применяемого лекарства. Обычно количество основы суппозитория составляет около 20-90 вес.% от общего веса суппозитория. Предпочтительно количество основы суппозитория в суппозитории составляет около 65-80 вес.% от общего веса суппозитория. Дополнительные варианты изобретения Оксикодона гидрохлорид с содержанием 14-гидроксикодеинона менее 25 ч./млн можно использовать как заместитель вместо оксикодона гидрохлорида в любом существующем промышленном продукте, например, таком как Tylox, Roxilox, Roxicet, Percocet, Oxycet, Percodan, Roxycodone,OxyContin и OxylR. Такие препараты перечислены в PDR 58th Edition (2004) и в FDA Orange Book. Нижеприведнные примеры иллюстрируют различные аспекты настоящего изобретения. Они представлены для того, чтобы никоим образом не ограничить формулу изобретения. Пример 1. В примере 1 37,7 г оксикодона HCl (35,4 сухого основания, около 500 ч./млн 14-гидроксикодеинона) помещают в реакционный сосуд Парра на 500 мл и смешивают с 0,55 г 5% Pd/C, влажность 50% (Johnson Matthey type 87L) и 182,2 г 61,9% смеси изопропанол/вода (вес./вес.). Смесь помещают в инертную атмосферу и нагревают при встряхивании при 45-50 С. После растворения исходного давление в сосуде спускают в атмосферу и 4 ч выдерживают в атмосфере водорода (45 PSIG, 310,26 кПа). К концу гидрирования давление водорода выпускают и раствор оставляют охлаждаться до комнатной температуры. На следующий день смесь нагревают до 75 С для растворения кристаллических веществ, а затем фильтруют в вакууме (отсос) через PTFE мембрану 0,2 мкм в цилиндрическую колбу на 1 л с рубашкой(снабжнную обратным холодильником, вводом азота, механической мешалкой, термопарой типа K и программируемым охлаждаемым рециркулятором). Сосуд Парра промывают деионизированной водой(11,7 г), которую через фильтр добавляют в колбу на 1 л. В колбу добавляют изопропанол (1 л), смесь снова нагревают при перемешивании до 75 С и выдерживают до растворения всех кристаллических веществ. Раствор охлаждают при перемешивании до 0-10 С в течение 8 ч (линейное уменьшение температуры) и выдерживают при 0-10 С в течение 20 ч. Выпавшие кристаллы отфильтровывают в вакууме и промывают с помощью 107 г холодной смеси 95:5 изопропанол/вода (вес./вес.).- 17013208 Для удаления из продукта изопропанола смоченный растворителем материал переносят в чашку(блюдо) для сушки и помещают в вакуум-эксикатор над открытой мкостью с деионизированной водой. Выдерживают в вакууме в течение ночи. Затем материал сушат в вакууме при 60 С. Анализ высушенного материала с применением метода определения низкого содержания 14-гидроксикодеинона из примера 4, см. ниже, дат результат 6 ч./млн 14-гидроксикодеинона. Анализ высушенного материала с применением метода из примера 6, см. ниже, дат результат 5 ч./млн кодеинона и 8 ч./млн. 14-гидроксикодеинона. Пример 2. В примере 2 35,0 г оксикодона HCl (33,3 г сухого основания, около 4000 ч./млн. 14-гидроксикодеинона) помещают в реакционный сосуд Парра на 500 мл и смешивают с 0,49 г 5% Pd/C, 50% влажности (Johnson Matthey type 87L) и 159,9 г 62,3% смеси изопропанол/вода. Смесь помещают в инертную атмосферу и нагревают при встряхивании при 45-50 С. После растворения исходного давление газа в сосуде спускают в атмосферу и заменяют на водород (45 PSIG, 310,26 кПа). После встряхивания в течение 5,25 ч водород выпускают и раствор оставляют охлаждаться до комнатной температуры. Смесь снова нагревают на следующий день и гидрирование продолжают в течение 4,75 ч. Смесь нагревают до 75 С, а затем фильтруют в вакууме (отсос) через PTFE мембрану 0,2 мкм в цилиндрическую колбу на 1 л с рубашкой (снабжнную дистилляционной насадкой, вводом азота, механической мешалкой, термопарой типа K и программируемым охлаждаемым рециркулятором). Сосуд Парра промывают деионизированной водой (11,7 г), которую через фильтр добавляют в колбу на 1 л. В колбу добавляют изопропанол (295,6 г) и смесь нагревают до кипения (около 81 С). Для удаления воды и повышения выхода азеотроп изопропанол/вода отгоняют из колбы до тех пор, пока не отгонится 305,7 г. Прибавляют свежую порцию изопропанола (305.6 г), дистилляционную насадку убирают и заменяют на обратный холодильник. Смесь охлаждают при перемешивании от температуры кипения до 0-10 С в течение 8 ч (линейное уменьшение температуры) и выдерживают при 0-10 С в течение 20 ч. Выпавшие кристаллы отфильтровывают в вакууме и промывают с помощью 107 г холодной смеси 95:5 изопропанол/вода. Анализ высушенного материала с применением метода определения низкого содержания 14-гидроксикодеинона из примера 4, см. ниже, дат результат 5 ч./млн 14-гидроксикодеинона. Анализ высушенного материала с применением метода из примера 6, см. ниже, дат результат 5 ч./млн кодеинона и 5 ч./млн 14-гидроксикодеинона. Пример 3. В примере 3 27,83 г влажного свободного основания оксикодона (24,57 г сухого основания, 0,0779 моль, около 3000 ч./млн 14-гидроксикодеина), 39,8 г деионизированной воды, 81,9 г изопропанола, 0,49 г 5% Pd/C (катализатор) 50% влажности (Johnson Matthey type 87L) и конц. HCl (11,3 г, 0,117 моль,1,50 экв. в расчте на 37,7% HCl) смешивают в сосуде Парра на 500 мл для шейкера. Смесь помещают в атмосферу инертного газа и нагревают до 75 С при встряхивании. Давление в сосуде снижают и в систему под давлением подают водород (45 PSIG, 310,26 кПа). Раствор выдерживают в этих условиях в течение 21,7 ч. ВЭЖХ анализ показывает, что за это время отношение площади пика 8,14-дигидрокси-7,8-дигидрокодеинона к площади пика оксикодона уменьшается с 0,29 до 0,04%. Давление водорода стравливают и систему помещают в инертную атмосферу. Чтобы предупредить дальнейшую дегидратацию любого количества оставшегося 8,14-дигидрокси-7,8-дигидрокодеинона, рН раствора с 0,5 доводят до 1,8, добавляя изопропанол, насыщенный 20,7 г NaOH (также присутствует некоторое количество тврдого гидроксида натрия). Раствор снова нагревают до 75 С и фильтруют под давлением через PTFE мембранный фильтр 0,2 мкм, закреплнный в держателе для фильтров 47 мм SS с подогревом, в цилиндрический реактор на 500 мл с рубашкой (обратный холодильник, N2, механическая мешалка, программируемый охлаждаемый рециркулятор). Сосуд Парра промывают деионизированной водой (8.6 г), которую через фильтр добавляют в колбу. К раствору в колбе добавляют изопропанол (225.5 г) и полученную суспензию нагревают до 75 С,чтобы снова растворить тврдые вещества. После достижения нужной температуры раствор выдерживают при ней в течение двух часов (обычное время реакции). После этого 14-гидроксикодеинон совсем не обнаруживается в кристаллической смеси. Включают циркуляционный насос, чтобы охладить с 80 до 0 С за 8 ч. Примерно через 24 ч после начала программы охлаждения осадок отсасывают на фильтре и три раза промывают смесью 95:5 изопропанол/вода (всего 232,8 г). Материал сушат, как описано в примере 1. Анализ высушенного материала с применением метода определения низкого содержания 14-гидроксикодеинона из примера 4, см. ниже, дат результат 5 ч./млн 14-гидроксикодеинона. Анализ высушенного материала с применением метода примера 6, см. ниже, дат результат 5 ч./млн кодеинона и 10 ч./млн 14-гидроксикодеинона. Пример 4. Анализ образца для определения уровня 14-гидроксикодеинона. Продукты из примеров 1-3 анализируют для определения уровня 14-гидроксикодеинона ниже- 18013208 100 ч./млн методом ВЭЖХ на колонке Waters Atlantis 5 мкм dC18, 3 X 250 мм при температуре 50 С в режиме изократической элюции при рН 9,35, элюент буфер 17 мМ карбоната аммония и метанол (60:40). Количественное определение осуществляют, измеряя изменение площади пика с помощью УФ-спектроскопии при 220 нм, используя внешний стандарт. В данном методе используют подвижную фазу с летучими компонентами, что совместимо с анализом LC/MS. Используют следующие реагенты. 1. Аммония карбонат, аналитической степени чистоты (ч.д.а.) (Aldrich). 2. Вода для анализов методом ВЭЖХ. 3. Метанол для ВЭЖХ. 4. Уксусная кислота, х.ч. (ледяная уксусная кислота J.T. Baker). 5. Гидроксид аммония, х.ч. 6. Фосфорная кислота, около 85%, A.C.S. реактив. 7. 14-Гидроксикодеинон, эталон, от Albany Molecular Research, Inc. Используют следующее оборудование.A. Система ВЭЖХ. 1. Система ВЭЖХ, способная подавать 0,4 мл/мин подвижной фазы (Waters Alliance). 2. Детектор УФ/видимого излучения, установленный для того, чтобы проводить мониторинг элюента при 220 нм (Waters 2487 UV/Vis). 3. Автосэмплер, позволяющий инъецировать 6 мкл. 4. Интегратор или соответствующая система регистрации данных (хроматографическая системаWaters Millenium 32). 5. Колонка Waters Atlantis dC18, 3 X 250 мм, 5 мкм. 6. Нагреватель колонки, способный поддерживать постоянную температуру 50 С. 7. Он-лайн вакуумный дегазатор.B. Оборудование для приготовления подвижной фазы. 1. рН-метр предпочтительно с автоматической компенсацией температуры (АТС). 2. Ультразвуковая баня, Model 5200, Branson. 3. Мембранные фильтры 0,45 мкм для водного растворителя, Whatman или микропористые из ацетата целлюлозы или найлоновые. Растворы. 17 мМ Карбонат аммония, рН 9,35. 1,60,1 г карбоната аммония взвешивают и помещают в химический стакан на 1 л. В стакан помещают 1000 мл воды и перемешивают магнитной мешалкой до растворения карбоната аммония. рН доводят до 9,35-9,40 с помощью гидроксида аммония.B. Подвижная фаза. 400 мл метанола для ВЭЖХ смешивают с 600 мл 17 мМ карбоната аммония, рН 9,35-9,40, приготовленного ранее. Смесь фильтруют через мембранные фильтры для растворителя, а затем дегазируют,используя он-лайн вакуумный дегазатор в ВЭЖХ системе. С. 0,85% раствор фосфорной кислоты. 10,0 мл 85% Н 3 РО 4 пипеткой добавляют в мерную колбу на 1 л, водой доводят до объма 1 л и тщательно перемешивают.D. Рабочие растворы стандартного 14-гидроксикодеинона. Для приготовления исходного раствора стандартного 14-гидроксикодеинона взвешивают 252 мг эталонного материала 14-гидроксикодеинона и переносят его в мерную колбу на 250 мл. Около 100 мл 0,85% раствора Н 3 РО 4 прибавляют в колбу и обрабатывают ультразвуком около 2 мин до растворения. Раствор доводят до объма 250 мл, добавляя 0,85% раствора Н 3 РО 4, и тщательно перемешивают. Получают исходный стандартный раствор 14-гидроксикодеинона. Рабочий раствор с содержанием 100 ч./млн стандартного раствора 14-гидроксикодеинона для проверки пригодности системы готовят, добавляя пипеткой в мерную колбу на 100 мл 5 мл исходного раствора стандартного 14-гидроксикодеинона, доводят до метки водой и тщательно перемешивают. Рабочий раствор с содержанием 10 ч./млн стандартного раствора 14-гидроксикодеинона для проверки чувствительности готовят, добавляя пипеткой в мерную колбу на 50 мл 5 мл рабочего раствора с содержанием 100 ч./млн стандартного 14-гидроксикодеинона, доводят до метки водой и тщательно перемешивают.E. Рабочий раствор стандартного гидрокодона. Для приготовления исходного раствора стандарта гидрокодона взвешивают 252 мг эталонного материала и переносят его в мерную колбу на 250 мл. Около 100 мл 0,85% раствора Н 3 РО 4 прибавляют в колбу и обрабатывают ультразвуком около 2 мин до растворения. Раствор доводят до метки, добавляя 0,85% раствора Н 3 РО 4, и тщательно перемешивают.F. Эталонные растворы. Эталонный раствор готовят, взвешивая 250 мг образца оксикодона API в сцинтилляционный фла- 19013208 кон. Во флакон пипеткой вносят 5,0 мл воды для растворения образца. Флакон плотно закрывают и подвергают действию ультразвука около 5 мин или до растворения образца. Затем содержимое встряхивают и тщательно перемешивают.G. Раствор смеси для проверки разделения (RTM). Раствор, содержащий два компонента, 14-гидроксикодеинон и гидрокодон, получают из соответствующих исходных стандартных растворов. Смесь для проверки разделения (разрешения пиков) (RTM) получают, перенося пипеткой по отдельности 10,0 мл каждого исходного стандартного раствора гидрокодона (см. выше) и 14-гидроксикодеинона (см. выше) в одну и ту же мерную колбу на 100 мл, доводя до заданного объма прибавлением достаточного количества воды и тщательно перемешивая. Н. Условия ВЭЖХ. Применяются следующие условия ВЭЖХ:I. Проверка смеси для тестирования разделения (RTM). Прежде, чем проверять пригодность системы, новую колонку уравновешивают в течение ночи (по меньшей мере 12 ч), прокачивая через не насосом подвижную фазу со скоростью 0,4 мл/мин. После того как новая колонка уравновешена, в уравновешенную систему вводят 6 мкл раствора RTM, для того чтобы удостовериться, что пики двух элюируемых компонентов не налагаются друг на друга. Типичное разделение раствора для проверки пригодности системы показано на фиг. 3.J. Проверка пригодности системы. Тест системы на пригодность осуществляют, вводя рабочий раствор с содержанием 100 ч./млн стандарта 14-гидроксикодеинона в систему и осуществляя тест на пригодность системы, описанный вUSP 621, в шести различных опытах инъецируя по 6 мкл. Результаты теста на пригодность системы отвечают следующим критериям, перечисленным ниже, в табл. 1. Таблица 1 Примечание: (1) - в тестах 1-3 используют рабочий раствор с содержанием 100 ч./млн стандартного 14-гидроксикодеинона;(3) - в тесте 5 используют рабочий раствор с содержанием 10 ч./млн стандартного 14-гидроксикодеинона. До начала эксперимента вводят (инжекция) 6 мкл воды, чтобы удостовериться, что отсутствуют пики, элюирующиеся вместе с пиком 14-гидроксикодеинона. Затем проводят следующую процедуру. Рабочий раствор с содержанием 100 ч./млн 14-гидроксикодеинона стандарта шесть раз вводят в различных опытах и систему проверяют на соответствие характеристикам теста на пригодность системы,перечисленным в приведнной выше табл. 1, тесты 1, 2 и 3. Вводят раствор RTM и пропускают один раз через ВЭЖХ систему, чтобы удостовериться, что система отвечает характеристике теста на пригодность системы, приведнной в приведнной выше табл. 1,тест 4. Вводят рабочий раствор с содержанием 10 ч./млн 14-гидроксикодеинона стандарта и пропускают один раз через ВЭЖХ систему, чтобы удостовериться, что отношение сигнал/шум S/N выше или равно 10, как указано в приведнной выше табл. 1, тест 5. После того как система прошла все указанные выше тесты, осуществляют следующую процедуру ВЭЖХ. Рабочий раствор с содержанием 100 ч./млн 14-гидроксикодеинона стандарта и рабочий раствор с содержанием 10 ч./млн 14-гидроксикодеинона стандарта инъецируют по отдельности. Оба рабочих стан- 20013208 дартных раствора используют для определения количественных характеристик образцов. Установочные параметры и параметры интегрирования перечислены ниже в табл. 2. Таблица 2 Типичные ВЭЖХ хроматограммы рабочего раствора, содержащего 100 ч./млн 14 гидроксикодеинона стандарта, и раствора образца оксикодона API, показаны на фиг. 4 и 5 соответственно. Время удерживания 14-гидроксикодеинона и других родственных веществ представлены ниже в табл. 3. Таблица 3 Проводят следующие расчты, используя полученные выше результаты. Используя программу Millenium, вводят параметры следующим образом: в группе образцов стандартные концентрации для обоих рабочих стандартов (10 и 100 ч./млн) вычисляют следующим образом:corrected for purity обозначает с поправкой на чистоту. Вводятся также следующие данные. Вес образца = вес образца в мг. Разведение = 5 мл (разведение образца). Индекс = 0,0001 (для перевода результатов в ч./млн). Количество 14-гидроксикодеинона (сокращнно ОНС) в образце оксикодона в ч./млн можно определять автоматически с помощью линейной калибровочной кривой, используя два стандарта (100 ч./млн и 10 ч./млн) и уравнение для расчта, см. ниже.Yintercept = отрезок Y на прямой линейной регрессии, полученной с применением двух стандартов;Slope = тангенс угла наклона прямой линейной регрессии, полученной с применением двух стандартов;Wsam = вес образца, мг; 1000000 = условный множитель для перевода результата, ч./млн. Пример 5. 3,0 г соли оксикодона гидрохлорида, содержащей 154 ч./млн 14-гидроксикодеинона, растворяют в 20 мл воды, получают прозрачный раствор в реакционном сосуде Парра на 250 мл. К раствору прибавляют 0,05 г 5% Pd/C (катализатор) 50% влажности (Johnson Matthey type 87L) и 1 мл 88% муравьиной кислоты. Смесь помещают в атмосферу инертного газа без подачи водорода, а затем нагревают до 45-50 С. После встряхивания в течение 2 ч отбирают пробу, для того чтобы проверить, остался ли 14-гидроксикодеинон. Проверка методом ВЭЖХ, описанным выше, в примере 4, показывает отсутствие 14-гидроксикодеинона. Затем раствор фильтруют в вакууме через PTFE мембранный фильтр 0,2 мкм для удаления катализатора. Из раствора фильтрата (около 18 мл) отбирают аликвоту 0,2 мл. К этому раствору прибавляют 2,0 мл изопропилового спирта, получают прозрачный раствор, а затем прибавляют 4,0 мл этилацетата.- 21013208 Раствор перемешивают, охлаждают и оставляют при 0-5 С на 20 ч, получают кристаллы оксикодона гидрохлорида. Кристаллический осадок отфильтровывают в вакууме. Влажное тврдое вещество сушат в сушильном шкафу при 50 С и в вакууме 10 мм Hg (1,3332 кПа). Вес сухого тврдого продукта 0,12 г. Анализ методом ВЭЖХ (см. выше пример 4) показывает, что в композиции соли оксикодона гидрохлорида присутствует около 11 ч./млн 14-гидроксикодеинона. К другой аликвоте 2 мл концентрированного раствора-фильтрата оксикодона гидрохлорида прибавляют 16-18 мл изопропилового спирта с последующей кристаллизацией и сушкой. Получают соль оксикодона гидрохлорид, содержащий около 6,8 ч./млн 14-гидроксикодеинона. Пример 6. Анализ образца для определения 14-гидроксикодеинона и кодеинона. Продукты из примеров 1-3 анализируют следующим альтернативным методом для определения содержания 14-гидроксикодеинона. В данном методе используют колонку Waters Symmetry C18 при температуре 40 С в режиме изократической элюции с применением в качестве подвижной фазы натрийфосфатного буфера, додецилсульфата натрия (SDS), ацетонитрила (ACN) и метанола (МеОН). Используют следующие реагенты. 1. Вода для анализов методом ВЭЖХ или е эквивалент. 2. Фосфорная кислота, около 85%, для анализов ВЭЖХ или эквивалент; 3. Фосфат натрия, одноосновный, моногидрат, чистый для ферментного анализа или эквивалент. 4. Натрия додецилсульфат (99%+), сверхчистый, Fluka, или эквивалент. 5. Ацетонитрил для ВЭЖХ или эквивалент. 6. Метанол для ВЭЖХ или эквивалент. 7. Гидроксид натрия, х.ч. ACS или эквивалент. 8. Оксикодон HCl с низким содержанием ABUK для применения в качестве компонента матрицы в стандартном препарате. 9. Эталон (стандарт) кодеинона от Rhodes Technologies или эквивалент. 10. 14-Гидроксикодеинон, эталон, от Albany Molecular Research или эквивалент. Используют следующее оборудование. А. Система ВЭЖХ. Для этого анализа используют систему ВЭЖХ с детектором с двойной длиной волны, способную работать в режиме изократической элюции при скорости потока 0,7 мл/мин с УФ-детектированием при 220 нм и температуре колонки 40 С. В. Система фильтрации подвижной фазы. Для этого анализа применяют ВЭЖХ устройство для вакуумного фильтрования с найлоновым мембранным фильтром (0,45 мкм). Растворы.i. 50% Раствор гидроксида натрия (вес./об.) 50 г гранулированного гидроксида натрия взвешивают и переносят в мерную колбу на 100 мл. Затем добавляют 60 мл воды и подвергают действию ультразвука до полного растворения гранул. Водой доводят до нужного объма и хорошо перемешивают. (Можно также использовать продажный 50% вес./об., раствор NaOH).ii. Раствор фосфорной кислоты (8,5% Н 3 РО 4). 10,0 мл концентрированной фосфорной кислоты (85%) переносят в мерную колбу на 100 мл, содержащую около 50 мл воды. Водой доводят до нужного объма, а затем перемешивают.iii. Раствор фосфорной кислоты (0,85% Н 3 РО 4). 10,0 мл 85% Н 3 РО 4 пипеткой добавляют в мерную колбу на 1000 мл, водой доводят до нужного объма и тщательно перемешивают. Этот раствор служит разбавителем для образца и стандартного препарата.iv. Подвижная фаза. 3,450,1 г моногидрата одноосновного фосфата натрия взвешивают в колбе на 1 л. Прибавляют 1000 мл воды, а затем перемешивают магнитной мешалкой до растворения. Прибавляют 5,410,1 г додецилсульфата натрия и тщательно перемешивают до растворения. Этот раствор фильтруют в вакууме через найлоновый мембранный фильтр 0,45 мкм. рН этого раствора доводят до конечной величины рН 7,500,05, добавляя 50% раствор NaOH. 722,5 мл полученного выше раствора смешивают затем со 157,5 мл ацетонитрила, к раствору добавляют 120 мл метанола и хорошо перемешивают. Под конец рН раствора доводят до 7,800,01, добавляя 8,5% раствор фосфорной кислоты. Подвижную фазу подвергают действию ультразвука в течение 5 мин для удаления растворнного воздуха.i. Приготовление стандартного раствора в расчте на образцы сухого вещества. А. Исходный раствор I кодеинона/14-гидроксикодеинона. 252 мг эталонных материалов кодеинона и 14-гидроксикодеинона взвешивают и переносят в мерную колбу на 100 мл, доводят до нужного объма и растворяют с помощью 0,85% раствора фосфорной кислоты II.ii. Исходный стандарт II с содержанием 100 ч./млн. 1 мл исходного раствора I пипеткой переносят в мерную колбу на 50 мл, доводят до нужного объма с помощью 0,85% раствора фосфорной кислоты II, а затем перемешивают.iii. Рабочий стандарт III с содержанием 10 ч./млн. 5005 мг материала ABUK оксикодона с низким содержанием взвешивают в мерную колбу на 10 мл. Пипеткой вносят 1 мл исходного стандарта II и доводят до нужного объма, добавляя 0,85% раствор фосфорной кислоты II, а затем перемешивают.iv. Анализируемый раствор оксикодона. 5005 мг материала ABUK оксикодона с низким содержанием взвешивают в мерную колбу на 10 мл, доводят до нужного объма, добавляя 0,85% раствор фосфорной кислоты II, а затем перемешивают (этот раствор используют для расчта остаточного содержания как кодеинона, так и 14-гидроксикодеинона в рабочем стандарте).E. Смесь для проверки разделения (RTM). 1,0 мл исходного раствора кодеинона/14-гидроксикодеинона I пипеткой переносят в мерную колбу на 50 мл. Микропипеткой вводят 100 мкл анализируемого раствора оксикодона и доводят до заданного объма прибавлением 0,85% раствора фосфорной кислоты II. Концентрация кодеинона, 14-гидроксикодеинона и оксикодеинона составляет около 100 ч./млн.i. Раствор образца с содержанием 50 мг/мл оксикодона HCl 5005 мг оксикодона HCl взвешивают в двойном повторе, в отдельных мерных колбах для каждого образца из примеров 1, 2 и 3. Затем оксикодон HCl доводят до нужного объма, добавляя 0,85% раствор фосфорной кислоты II, и перемешивают(круговыми движениями) для растворения образца. Достаточное количество этого образца переносят в пузырк для ВЭЖХ инжекции. 2. Условия ВЭЖХ. Применяются следующие условия ВЭЖХ: Таблица 4 Условия ВЭЖХ Параметр можно корректировать для достижения времени удерживания Н. Пригодность системы. Делают одну инжекцию (5 мкл) раствора для холостого (контрольного) опыта (0,85% раствор фосфорной кислоты II), а затем одну инжекцию RTM, чтобы определить, есть ли налагающиеся пики в контрольном растворе. Делают 6 инжекций рабочего стандарта III. Затем делают инжекции для проверки пригодности системы, чтобы удостовериться, что они отвечают следующим критериям пригодности системы, перечисленным ниже, в табл. 1. Таблица 5 Критерии пригодности системы- 23013208 Ниже дано ожидаемое время удерживанияI. Методика инжекции (ввода). После уравновешивания колонки образец и стандартные растворы вводят (инжекция) в следующей последовательности, показанной в табл. 6 Таблица 6 Пики кодеинона и 14-гидроксикодеинона идентифицируют с учтом относительного времени удерживания, обсуждавшегося выше. Вычисления. Отклик пиков кодеинона и 14-гидроксикодеинона измеряют и регистрируют. Содержание кодеинона и 14-гидроксикодеинона рассчитывают в ч./млн по следующему уравнению: где ppm = части на миллион (ч./млн, м.д.) кодеинона или 14-гидроксикодеинона в оксикодоне HCl;Rs = отклик кодеинона или 14-гидроксикодеинона в растворе образца;Rstd = отклик кодеинона или 14-гидроксикодеинона в стандартном растворе минус отклик анализируемого стандарта;Ws = вес образца, мг; 1000000 = переводной множитель для ч./млн.% Кодеинон/14-гидроксикодеинон = ч./млн/10000. Результаты, полученные в примере 1 при использовании методики из примера 6, составляют 5 ч./млн кодеинона и 8 ч./млн 14-гидроксикодеинона. Результаты, полученные в примере 2 при использовании методики из примера 6, составляют 5 ч./млн кодеинона и 5 ч./млн 14-гидроксикодеинона. Результаты, полученные в примере 3 при использовании методики из примера 6, составляют 5 ч./млн кодеинона и 10 ч./млн 14-гидроксикодеинона. Многие другие варианты настоящего изобретения очевидны для специалистов в данной области техники и предполагается, что они входят в объм прилагаемой формулы изобретения. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ получения оксикодона гидрохлорида, содержащего менее 25 мг/кг 14-гидроксикодеинона, путем проведения реакции взаимодействия основания оксикодона, содержащего 8,14-диги- 24013208 дрокси-7,8-дигидрокодеинон, с соляной кислотой в условиях, способствующих дегидратации 8,14-дигидрокси-7,8-дигидрокодеинона с образованием 14-гидроксикодеинона в процессе солеобразования и в восстановительных условиях для преобразования 14-гидроксикодеинона в оксикодон. 2. Способ по п.1, в котором оксикодон гидрохлорид содержит менее 15 мг/кг 14-гидроксикодеинона. 3. Способ по п.1, в котором оксикодон гидрохлорид содержит менее 10 мг/кг 14-гидроксикодеинона. 4. Способ по п.1, в котором оксикодон гидрохлорид содержит менее 5 мг/кг 14-гидроксикодеинона. 5. Способ по любому из пп.1-4, в котором полученный оксикодон гидрохлорид, содержащий менее 25 мг/кг 14-гидроксикодеинона, дополнительно гидрируют для дальнейшего восстановления содержащегося в нем количества 14-гидроксикодеинона. 6. Способ по любому из пп.1-5, в котором проводят извлечение оксикодона гидрохлорида, содержащего менее 25 мг/кг 14-гидроксикодеинона. 7. Способ по любому из пп.1-6, в котором основание оксикодона, содержащее 8,14-дигидрокси-7,8 дигидрокодеинон, вводят в реакцию с соляной кислотой в количестве более 1,0 мол.экв. в сравнении с составом основания оксикодона. 8. Способ по п.7, в котором количество соляной кислоты превышает 1,2 мол.экв. 9. Способ по п.7, в котором количество соляной кислоты превышает 1,4 мол.экв. 10. Способ по п.7, в котором количество соляной кислоты превышает 1,5 мол.экв. 11. Способ по любому из пп.1-10, в котором реакцию проводят при температуре около 20 С. 12. Способ по любому из пп.1-10, в котором реакцию проводят при температуре от 40 до 85 С. 13. Способ по любому из пп.1-12, в котором время реакции составляет от 10 мин до 36 ч. 14. Способ по любому из пп.1-13, в котором реакцию проводят при рН ниже 5. 15. Способ по любому из пп.1-13, в котором реакцию проводят при рН ниже 3. 16. Способ по любому из пп.1-13, в котором реакцию проводят при рН ниже 1. 17. Способ по любому из пп.1-16, в котором восстановительные условия обеспечиваются катализатором с донором водорода. 18. Способ по п.1, альтернативно проводимый путем реакции взаимодействия основания оксикодона, содержащего 8,14-дигидрокси-7,8-дигидрокодеинон, с соляной кислотой в условиях, способствующих дегидратации 8,14-дигидрокси-7,8-дигидрокодеинона, с получением 14-гидроксикодеинона при солеобразовании, с последующим введением его в контакт с веществом, удаляющим 14-гидроксикодеинон. 19. Способ по п.18, в котором указанное вещество представляет собой гель. 20. Способ по п.19, в котором указанная композиция и указанный гель образуют суспензию. 21. Способ по п.1, альтернативно проводимый путем реакции взаимодействия основания оксикодона, содержащего 8,14-дигидрокси-7,8-дигидрокодеинон, с соляной кислотой в условиях, способствующих дегидратации 8,14-дигидрокси-7,8-дигидрокодеинона, с получением 14-гидроксикодеинона при солеобразовании и последующим хроматографическим разделением. 22. Способ по любому из пп.1-21, в котором 8,14-дигидрокси-7,8-дигидрокодеинон представляет собой 8,14-дигидрокси-7,8-дигидрокодеинон. 23. Способ получения оксикодона гидрохлорида, содержащего менее 25 мг/кг 14-гидроксикодеинона, путем гидрирования оксикодона гидрохлорида, содержащего более 100 мг/кг 14-гидроксикодеинона, до тех пор пока количество 14-гидроксикодеинона не уменьшится до уровня ниже 25 мг/кг. 24. Способ по п.23, в котором гидрирование проводят при температуре около 20 С. 25. Способ по п.23, в котором гидрирование проводят при температуре от 40 до 85 С. 26. Способ по любому из пп.1-25, в котором время гидрирования составляет от 10 мин до 36 ч. 27. Способ по любому из пп.1-26, в котором гидрирование проводят при рН ниже 5. 28. Способ по любому из пп.1-26, в котором гидрирование проводят при рН ниже 3. 29. Способ по любому из пп.1-26, в котором гидрирование проводят при рН ниже 1. Фиг. 1 Реакционная схема процесса получения оксикодона HCl из тебаина Фиг. 3 Типичная ВЭЖХ хроматограмма RTM раствора Фиг. 4 Типичная ВЭЖХ хроматограмма рабочего раствора стандарта 100 ч./млн 14 ОНС Фиг. 5 Типичная хроматограмма раствора образца, содержащего оксикодон API
МПК / Метки
МПК: C07D 489/08, C07D 489/00
Метки: оксикодона, содержащего, получения, гидрохлорида, гидроксикодеинона, способ, менее
Код ссылки
<a href="https://eas.patents.su/28-13208-sposob-polucheniya-gidrohlorida-oksikodona-soderzhashhego-menee-25-ch-mln-14-gidroksikodeinona.html" rel="bookmark" title="База патентов Евразийского Союза">Способ получения гидрохлорида оксикодона, содержащего менее 25 ч./млн 14- гидроксикодеинона</a>
Предыдущий патент: Ингибиторы вирусной полимеразы
Следующий патент: Производные дифенилоксиндол-2-она и их применение для лечения рака
Случайный патент: Способ и устройство для выращивания растений