Способ получения оксикодона
Номер патента: 9392
Опубликовано: 28.12.2007
Авторы: Прокса Богумил, Ратковская Любица, Снупарек Владислав
Формула / Реферат
1. Способ получения оксикодона формулы I, отличающийся тем, что тебаин формулы II или его аналог формулы III, где R представляет собой C2-C5алкил, алкиларил, предпочтительно бензил, метоксибензил или аллил,
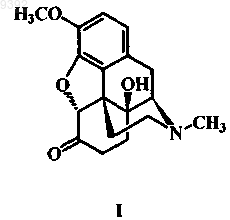
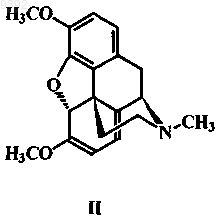
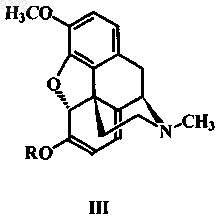
смешивают с перекисью водорода или пероксокислотами в присутствии щавелевой кислоты и другой органической кислоты, из образовавшегося в результате кристаллического осадка 14-гидроксикодеинона оксалата путем добавления основания получают 14-гидроксикодеинон формулы IV, который гидрируют водородом в присутствии катализатора с получением оксикодона (I).
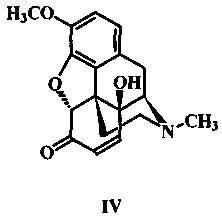
2. Способ получения оксикодона по п.1, в котором указанной другой органической кислотой является муравьиная кислота и уксусная кислота.
3. Способ получения оксикодона по п.1 или 2, в котором концентрация муравьиной кислоты составляет от 80 до 90%, предпочтительно 88%.
4. Способ получения оксикодона по п.1, где концентрация перекиси водорода составляет от 25 до 33%.
5. Способ получения оксикодона по п.1, в котором указанной пероксокислотой является перуксусная кислота, пербензойная кислота или мета-хлорпербензойная кислота.
6. Способ получения оксикодона по п.1, в котором молярное соотношение тебаин или его аналог:щавелевая кислота:другая органическая кислота:перекись водорода или пероксокислота составляет 0,8-2,0:1,0:2,0-3,0:2,0-3,0, предпочтительно 1,5-2,0:1,0:2,3-2,7:2,3-2,7.
7. Способ получения оксикодона по п.1, при котором температура в ходе протекания реакции тебаина или его аналогов с перекисью водорода или пероксокислотами составляет от 0 до 35шС, предпочтительно от 15 до 25шС.
8. Способ получения оксикодона по п.1, при котором кристаллический осадок 14-гидроксикодеинона оксалата отделяют фильтрованием, центрифугированием или декантацией, полученное твердое вещество растворяют в воде и добавлением основания получают 14-гидроксикодеинон либо реакционную смесь, содержащую 14-гидроксикодеинона оксалат, подщелачивают добавлением основания и выпавший в осадок 14-гидроксикодеинон отделяют фильтрованием, декантацией или центрифугированием.
9. Способ получения оксикодона по любому из пп.1 и 5, при котором рН реакционной смеси, содержащей 14-гидроксикодеинон оксалат, при подщелачивании составляет от 9 до 10, предпочтительно 9,2-9,6.
10. Способ получения оксикодона по п.1, при котором 14-гидроксикодеинон, растворенный в водном растворе органической кислоты, гидрируют водородом в присутствии катализатора.
11. Способ получения оксикодона гидрохлорида, при котором оксикодон, полученный способом по любому из пп.1-10, растворяют в разбавленной соляной кислоте при температуре от 70 до 90шС и, медленно охлаждая раствор, кристаллизуют оксикодона гидрохлорид.
Текст
009392 Область техники Настоящее изобретение относится к фармацевтическому производству, а именно к получению оксикодона (I), который является сильным болеутоляющим средством, применяемым в терапевтической практике в форме гидрохлорида, или который используют в качестве промежуточного продукта в процессе производства антагонистов морфина, таких как налоксон или налтрексон. Предшествующий уровень техники Оксикодон получают двумя основными способами. а) Превращением тебаина (II), природного алкалоида, выделенного из растения Papaver somniferumL. или его аналогов (III), где R представляет собой алкокси- или аминоалкильный остаток. В данной методике (схема 1) тебаин взаимодействует в кислотной среде с перекисью водорода, пероксокислотами или другими окислителями с образованием 14-гидроксикодеинона (IV), который гидрируют с получением оксикодона (I). Схема 1 Тебаин, растворенный в горячей концентрированной уксусной кислоте, превращают в 14-гидроксикодеинон в реакции с 30% перекисью водорода (Freund M., Speyer E.: J. Prakt. Chem. 94, 135 (1916);Lutz R.E., Small L.: J. Org. Chem. 4, 220-233 (1939); DE 286431) с приблизительным выходом 30%. Приблизительно тот же самый выход был получен при окислении тебаина хромовой кислотой (DE 286431;DE 411530) или ацетатом марганца (Viebock F.: Chem. Ber. 67, 197 (1934. Значительно больший выход(приблизительно 75%) был обнаружен для реакции тебаина (II) с перекисью водорода в уксусной кислоте при температуре, не превышающей 40 С (Feldman I.Ch., Liutenberg A.I.: Zh. Prikl. Khim. 18, 715(1945, или в смеси серной кислоты и 88% муравьиной кислоты (Krassnig R., Hederer Ch., SchmidhammerH.: Arch. Pharm. 329, 325 (1996. Сравнимые результаты были достигнуты при взаимодействии тебаина (II) с пероксокислотами, например мета-хлорпербензойной кислотой, в смеси уксусной кислоты и трифторуксусной кислоты(Hauser F.M., Chen T-K., Carroll F.I.: J. Med. Chem. 17, 1117 (1974; однако, Ijima с сотр. установил, что данная реакция не дает воспроизводимых выходов (приблизительно 25%) и образуется много нежелательных продуктов (Ijima I., Rice K.C., Brossi A.: Helv. Chim. Acta 60, 2135 (1977. В модифицированной методике вместо тебаина (II) можно использовать кодеин (V), см. схему 2, который сначала окисляют до кодеинона (VI), а затем в реакции либо с ацилирующим, либо с алкилирующим агентом превращают в енол-эфир/сложный эфир VII (ЕР 889045, US 5869669, US 4639520), по существу, аналог тебаина, который далее последовательно превращают в 14-гидроксикодеинон любым из вышеупомянутых способов. Схема 2 Также возможно к этой группе отнести способ Sankyo (GB 1260699), в котором используют в качестве исходного соединения кодеинон (VI), который превращают в кодеинонпирролидиниленамин (VIII) с использованием пирролидина в апротонных растворителях, см. схему 3. Последующая реакция с переки-1 009392 сью водорода, хромовой кислотой, органическими пероксокислотами (перуксуной, пербензойной) или перманганатом в водной уксусной кислоте, фосфорной кислоте и т.п. дает 14-гидроксикодеинон (IV). Схема 3 б) Окислением кодеинона (VI) под действием пероксокислот, комбинации органических кислот и перекиси водорода или под действием неорганических окислителей (например, солей Со 3+) с максимальным выходом 14-гидроксикодеинона 57%, который гидрируют с получением оксикодона (I) (Coop A.,Rice K.C.: Tetrahedron 55, 11429 (1999. Двойную связь С 7-С 8 14-гидроксикодеинона гидрировали каталитически согласно СН 75110 (US 1468805) на черненой Pt, коллоидном Pd или в присутствии PdCb (US 1485673) в разбавленной уксусной кислоте. Ijima, так же, как и Lutz R.E. и Small L. (J. Org. Chem. 4, 220 (1939, использовал в этой реакции в качестве катализатора Pd/BaSO4 (J. Med. Chem. 21, 398 (1978. Известно также использование 10%Pd/C в концентрированной уксусной кислоте с выходом приблизительно 70% (Krassnig R., Hederer Ch.,Schmidhammer H.: Arch. Pharm. 329, 325 (1996. Feldmann и Liutenberg (Zh. Prikl. Khim. 18, 715 (1945 гидрировали гидрохлорид 14-гидроксикодеинона на никеле Ренея в горячем этаноле с выходом гидрохлорида оксикодона 74%. Все вышеупомянутые способы получения оксикодона (I) имеют ряд недостатков: реакция перекиси/пероксокислот с тебаином или его аналогами не дает воспроизводимых результатов, образуется смесь плохоотделимых побочных продуктов, и значения выходов низкие. Данные недостатки преодолеваются способом по настоящему изобретению. Сущность изобретения Настоящее изобретение представляет способ получения оксикодона формулы I путем осуществления взаимодействия тебаина (II) или его аналогов формулы III, где R представляет собой С 2-С 5 алкил,алкиларил, предпочтительно бензил, метоксибензил или аллил, с перекисью водорода или пероксокислотами, например такими, как перуксусная кислота, пербензойная кислота или мета-хлорпербензойная кислота, в присутствии щавелевой кислоты и другой органической кислоты, например муравьиной кислоты или уксусной кислоты, в результате чего осаждаются кристаллы оксалата 14-гидроксикодеинона, из которого добавлением основания получают 14-гидроксикодеинон формулы IV, который гидрируют водородом в присутствии катализатора с получением оксикодона (I). Реакция тебаина или его аналогов формулы III с перекисью водорода или пероксокислотами в присутствии щавелевой кислоты и другой органической кислоты дает 14-гидроксикодеинон, который с щавелевой кислотой образует плохорастворимый кристаллический осадок оксалата 14-гидроксикодеинона. Таким путем равновесие превращения тебаина смещается и подавляются последующие и нежелательные побочные реакции, такие как окисление тебаина до транс-10-гидрокситебаина или присоединение воды к 14-гидроксикодеинону, приводящее к образованию (8S)-гидроксиоксикодона, и т.п. Когда в качестве другой органической кислоты используют муравьиную кислоту, ее концентрация составляет предпочтительно от 80 до 90%, более предпочтительно 88%. Концентрация перекиси водорода составляет предпочтительно от 25 до 33%. Молярное соотношение реагентов тебаин или его аналог:щавелевая кислота:другая органическая кислота:перекись водорода или пероксокислота составляет предпочтительно 0,8-2,0:1,0:2,0-3,0:2,0-3,0, более предпочтительно 1,5-2,0:1,0:2,3-2,7:2,3-2,7. Температура в ходе реакции тебаина или его аналогов с перекисью водорода или пероксокислотами составляет предпочтительно от 0 до 35 С, более предпочтительно от 15 до 25 С. В ранее известных способах окисление тебаина/аналогов тебаина проводили перекисью водорода/пероксокислотами в присутствии органической или неорганической кислоты (важно осуществить протонизацию азота в молекуле тебаина для того, чтобы избежать образования N-оксида или достигнуть требуемой растворимости субстрата). В способе Krassnig R. и сотр., Arch. Pharm. 329, 325 (1996), используется смесь тебаина, серной кислоты, муравьиной кислоты и перекиси водорода; система является гомогенной на протяжении всего хода реакции. По завершении окисления реакционную смесь выливают в лед и подщелачивают, добавляя гидроксид аммония. Продукт, 14-гидроксикодеинон, экстрагируют дихлорметаном. Преимущество способа по настоящему изобретению состоит в том, что в результате окисления тебаина/его аналогов перекисью водорода или пероксокислотами в присутствии щавелевой кислоты и другой органической кислоты (муравьиной, уксусной) продукт (14-гидроксикодеинон) образуется в виде осадка, т.е. получается гетерогенная система, которая сдвигает равновесие в реакции окисления и предотвращает дальнейшее превращение продукта (14-гидроксикодеинона) реакцией с окислителем, приводя тем самым к более высокой степени превращения и получению чистого продукта. После завершения реакции реакционную смесь (суспензию) охлаждают, подщелачивают (освобождая основание 14-гидроксикодеинон из его солей) и выпавший в осадок продукт (14-гидроксикодеинон) отфильтровывают, промывают и сушат. Данным способом получают продукт с более высоким выходом и большей чистоты по сравнению с ранее известными способами. В известных способах (например, Arch. Pharm. 329, 325 (1996, где использовали реакцию тебаина с перекисью водорода в присутствии серной кислоты и муравьиной кислоты, выход 14-гидроксикодеинона составлял 74,3 и 78,5%, соответственно, а чистота продукта составляла 88,3 и 90,1% (25 С), соответственно. В способе по данному изобретению при использовании молярного соотношения реагирующих веществ тебаин:щавелевая кислота:муравьиная кислота:перекись водорода, равного 16:8,6:22:21, выход составляет 91,3% и чистота продукта составляет 93,3% (25 С). Реакционная смесь, представляющая собой, после превращения введенного тебаина, суспензию 14 гидроксикодеинона оксалата в реакционной среде, может быть подвергнута разделению фаз суспензии центрифугированием, декантацией или фильтрованием, с дальнейшим растворением 14-гидроксикодеинона оксалата в горячей воде и осаждением, путем регулирования рН добавлением основания, 14-гидроксикодеинона, который отделяют, промывают и сушат. Другой способ выделения 14-гидроксикодеинона представляет собой методику, по которой реакционную смесь, в которой диспергирован 14-гидроксикодеинона оксалат, подщелачивают, добавляя основание, до достижения рН 9-10, предпочтительно 9,2-9,6,затем 14-гидроксикодеинон отделяют центрифугированием или фильтрованием или, возможно, экстрагируют из щелочной среды органическим растворителем. Полученный данным способом 14-гидроксикодеинон гидрируют известным методом в присутствии катализатора из группы редких металлов, таких как Pt, или Pd, или Ni, в водном растворе органической кислоты, например уксусной кислоты. Полученный оксикодон осаждают из реакционной среды, регулируя рН путем добавления щелочи; осадок отделяют фильтрованием или центрифугированием и продукт сушат. Способ получения оксикодона гидрохлорида включает стадию, при которой полученный оксикодон-3 009392 растворяют в разбавленной соляной кислоте при температуре от 70 до 90 С, и при медленном охлаждении начинает кристаллизоваться оксикодона гидрохлорид. Данная методика дает продукт, оксикодон гидрохлорид, в форме кристаллов, охарактеризованных RTG-дифракционным анализом, результаты которого представлены в табл. 1. Оксикодон или оксикодона гидрохлорид, полученный согласно данному изобретению, может быть использован в качестве активного компонента фармацевтического препарата, содержащего помимо него по крайней мере один фармацевтически приемлемый эксципиент. Таблица 1 Характеристические пики RTG-дифракционной картины оксикодона гидрохлорида Настоящий способ является полезным, так как позволяет получить продукт с низким содержанием примесей и выходами, сильно превышающими выходы, описанные в предшествующем уровне техники. Следующие примеры описывают способ по настоящему изобретению более подробно, однако, они не ограничивают сущность изобретения. Примеры Пример 1. а) Щавелевую кислоту массой 18,66 кг растворяли в воде, добавляли 84,8 кг тебаина и после его растворения добавляли 19,50 кг 88% муравьиной кислоты и 42,4 кг 30% перекиси водорода. Реакционную смесь перемешивали при 25 С до полного превращения тебаина (определяли капиллярным электрофорезом; капилляр 50 см х 0,05 мм, электролит 100 мМ ТРИС/фосфат, рН 2,7, 5 мМ диметоксициклодекстрин, температура 25 С 30 кВ; время движения тебаина 5,6 мин). Реакционную смесь охлаждали до 5 С, добавляли при перемешивании 10% водный раствор KOH до рН 9,2. Выпавшие в осадок кристаллы 14-гидроксикодеинона центрифугировали, промывали водой и сушили. Получали приблизительно 76 кг 14-гидроксикодеинона (89%). б) 14-Гидроксикодеинон массой 72,50 кг растворяли в 10% водном растворе уксусной кислоты, добавляли катализатор 5% Pd/C и смесь гидрировали под избыточным давлением электролитического водорода 104-106 кПа при температуре от 30 до 35 С. Реакционную смесь разбавляли 200 л воды, фильтровали, фильтрат охлаждали до 5 С и осаждали оксикодон в форме основания доведением значения рН до 9,2 путем добавления этанольного раствора аммиака. Суспензию центрифугировали, оксикодон промывали водой и сушили при 70-80 С. Получали по меньшей мере 67 кг (92%, чистота 98,5%) оксикодона. в) Водный раствор HCl (87,0 кг воды и 13,00 кг конц. HCl) перемешивали с 48 кг основания оксикодона при 80 С, добавляли активированный уголь и диатомовую землю и после перемешивания в течение 15 мин суспензию фильтровали, фильтрат постепенно охлаждали до конечной температуры от 1 до 3 С. Выпавшие в осадок кристаллы центрифугировали, промывали этанолом и сушили оксикодона гидрохлорид при температуре от 70 до 80 С. Получали 51,2 кг (91%) оксикодона гидрохлорида, Т.кип. 219 С,[]D20 -145, содержание воды 6,0%, чистота 99,4% (RP C8 колонка, 150 х 3,9 мм, 5 мкм, с RP C8 предколонкой, 20 х 3,9 мм, 5 мкм, подвижная фаза 0,005 моль/л гексансульфонат натрия:метанол:фосфорная кислота:триэтиламин (об./об.) (900:100:5:2), рН 2,5 достигнут с помощью NaOH; скорость потока 1,5 мл/мин; температура 50 С; УФ, =206 нм), содержание 100,03% (титрование). Пример 2. Тебаин (1 кг) растворяли в водном растворе щавелевой кислоты (0,21 кг в 1 л воды). Добавляли 0,23 кг 88% муравьиной кислоты и 0,81 кг 39% перуксусной кислоты. Реакционную смесь перемешивали при 25 С до полного превращения тебаина (оценивали путем CZE). Реакционную смесь охлаждали до 5 С,добавляли при перемешивании 10% водный раствор гидроксида натрия до рН 9,2. Выпавшие в осадок-4 009392 кристаллы 14-гидроксикодеинона центрифугировали, промывали с водой и сушили. Получали приблизительно 0,92 кг 14-гидроксикодеинона (91,8%). Дальнейшая процедура получения оксикодона гидрохлорида проводится согласно примерам 1(б) и 1(с). Пример 3. 6-Бензилокси-4,5-эпокси-3-метокси-17-метилморфин-6,8(14)-диен (52,5 г) растворяли в растворе,полученном растворением 9,8 г щавелевой кислоты в 35 мл воды, добавляли 10 мл уксусной кислоты и 21,2 мл 30% перекиси водорода. Реакционную смесь перемешивали при 20 С до полного превращения указанного бензилового аналога тебаина, реакционную смесь охлаждали до 2 С и добавляли при перемешивании 8% водный раствор NaOH до рН 9,2. Выпавшие в осадок кристаллы 14-гидроксикодеинона фильтровали, промывали водой и сушили. Выход составил приблизительно 37 г 14-гидроксикодеинона(82%). Дальнейшая процедура получения оксикодона гидрохлорида проводится согласно примерам 1(б) и 1(с). Пример 4. 4,5-Эпокси-6-этокси-3-метокси-17-метилморфин-6,8(14)-диен (22,1 г) растворяли в растворе 10 г щавелевой кислоты в 35 мл воды; добавляли муравьиную кислоту (9,8 мл, 88%) и перекись водорода(21,2 мл). Смесь перемешивали при 30 С в течение 30 ч, охлаждали до 10 С, выпавший в осадок 14-гидроксикодеинона оксалат фильтровали и промывали. Влажный 14-гидроксикодеинона оксалат растворяли в 80 мл воды при 65 С и добавляли 10% гидроксид калия до рН 9,3, суспензию 14-гидроксикодеинона охлаждали до 15 С, твердый остаток отфильтровывали, промывали и сушили. Получали приблизительно 17,6 г 14-гидроксикодеинона (выход 83%, чистота 93,2%). Промышленная применимость Производство оксикодона формулы I и его гидрохлорида, описанное здесь, обладает значительным преимуществом в отношении экономического фактора спроса и безопасности окружающей среды по сравнению с известными способами. Оксикодона гидрохлорид используется для получения фармацевтических препаратов с болеутоляющим эффектом. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ получения оксикодона формулы I, отличающийся тем, что тебаин формулы II или его аналог формулы III, где R представляет собой C2-C5 алкил, алкиларил, предпочтительно бензил, метоксибензил или аллил, смешивают с перекисью водорода или пероксокислотами в присутствии щавелевой кислоты и другой органической кислоты, из образовавшегося в результате кристаллического осадка 14-гидроксикодеинона оксалата путем добавления основания получают 14-гидроксикодеинон формулы IV, который гидрируют водородом в присутствии катализатора с получением оксикодона (I). 2. Способ получения оксикодона по п.1, в котором указанной другой органической кислотой является муравьиная кислота и уксусная кислота. 3. Способ получения оксикодона по п.1 или 2, в котором концентрация муравьиной кислоты составляет от 80 до 90%, предпочтительно 88%. 4. Способ получения оксикодона по п.1, где концентрация перекиси водорода составляет от 25 до 33%. 5. Способ получения оксикодона по п.1, в котором указанной пероксокислотой является перуксусная кислота, пербензойная кислота или мета-хлорпербензойная кислота. 6. Способ получения оксикодона по п.1, в котором молярное соотношение тебаин или его аналог:щавелевая кислота:другая органическая кислота:перекись водорода или пероксокислота составляет 0,8-2,0:1,0:2,0-3,0:2,0-3,0, предпочтительно 1,5-2,0:1,0:2,3-2,7:2,3-2,7. 7. Способ получения оксикодона по п.1, при котором температура в ходе протекания реакции тебаина или его аналогов с перекисью водорода или пероксокислотами составляет от 0 до 35 С, предпочтительно от 15 до 25 С. 8. Способ получения оксикодона по п.1, при котором кристаллический осадок 14-гидроксикодеинона оксалата отделяют фильтрованием, центрифугированием или декантацией, полученное твердое вещество растворяют в воде и добавлением основания получают 14-гидроксикодеинон либо реакционную смесь, содержащую 14-гидроксикодеинона оксалат, подщелачивают добавлением основания и выпавший в осадок 14-гидроксикодеинон отделяют фильтрованием, декантацией или центрифугированием. 9. Способ получения оксикодона по любому из пп.1 и 5, при котором рН реакционной смеси, содержащей 14-гидроксикодеинон оксалат, при подщелачивании составляет от 9 до 10, предпочтительно 9,2-9,6. 10. Способ получения оксикодона по п.1, при котором 14-гидроксикодеинон, растворенный в водном растворе органической кислоты, гидрируют водородом в присутствии катализатора. 11. Способ получения оксикодона гидрохлорида, при котором оксикодон, полученный способом по любому из пп.1-10, растворяют в разбавленной соляной кислоте при температуре от 70 до 90 С и, медленно охлаждая раствор, кристаллизуют оксикодона гидрохлорид.
МПК / Метки
МПК: C07D 489/08
Метки: оксикодона, способ, получения
Код ссылки
<a href="https://eas.patents.su/7-9392-sposob-polucheniya-oksikodona.html" rel="bookmark" title="База патентов Евразийского Союза">Способ получения оксикодона</a>











