Бис-оксимовые производные триазолина и изоксалина
Номер патента: 435
Опубликовано: 26.08.1999
Авторы: Цурфлух Рене, О Сулливан Антони Корнелиус, Циглер Хуго, Трах Стефан
Формула / Реферат
1. Производные бис-оксима формулы I
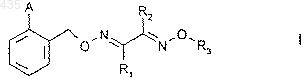
где А обозначает

где W обозначает кислород или серу, а другие обозначения являются заместителями, которые определены следующим образом:
R1 означает водород, С1-С4-алкил, циклопропил;
R2 означает водород, С1-С6-алкил, гало(С1-С6)алкил, С2-С6-алкоксиалкил, С3-С6-циклоалкил, замещенный или незамещенный арил, замещенный или незамещенный гетероарил, циано, С1-С6-алкоксикарбонил, С1-С6-алкил-S(O)n, замещенный или незамещенный арил-S(O)n, C1-C6-алкокси, замещенный или незамещенный арилокси, замещенный или незамещенный гетероарилокси, незамещенный или от моно- до триметилзамещенный гетероциклил, замещенный или незамещенный арил-С1-С6-алкил, замещенный или незамещенный гетероарил-С1-С6-алкил;
R3 означает водород, С1-С6-алкил, С1-С6-галоалкил, имеющий от 1 до 5 атомов галогена, С1-С4-алкокси-С1-С2-алкил, незамещенный или от моно- до тригалозамещенный С2-С6-алкенил, С2-С6-алкинил, незамещенный или от моно- до тетрагалозамещенный С3-С6-циклоалкил-С1-С4-алкил;
n означает 0-2;
R8 означает водород, С1-С4-алкил, С1-С4-галоалкил, С3-С6-циклоалкил;
Х означает OR5, SR5, NR6R7, галоген (особенно хлор);
R6, R7 независимо один от другого обозначают водород, С1-С4-алкил, С3-С4 алкенил, С3-С4-алкинил;
R5 означает С1-C4-алкил, С1-С3-галоалкил.
2. Соединение по п.1, отличающееся тем, что R8 обозначает метил и Х обозначает метокси, R2 имеет определенные выше значения, за исключением гало(С1-С6)алкила, и R1, R3, n и W имеют определенные выше значения.
3. Соединение по п.1, отличающееся тем, что
R1 обозначает водород, метил, этил или циклопропил;
R2 обозначает группу фенила, которая замещена на незамещенную или замещенную группу этинила, возможными заместителями которой являются C1-С4-алкил, С1-С4-гидроксиалкил, галоген, С1-С4-галоалкил, циано, С1-С5-алкоксикарбонил или циклопропилметоксикарбонил; С2-С5-алкенил, который не замещен или замещен С2-С4-алкокси и/или галогеном; N-метил-N-метоксикарбамоил; незамещенный или замещенный фенил [при этом заместители выбирают из группы, состоящей из С1-С4-алкила, С1-С4-алкокси, СF3, CN, галогена и ОСF3]; незамещенный или замещенный, пяти- или шестичленный гетероарил, заместителями которого являются галоген, циано, метил, метокси или гидроксил; и
R3 обозначает метил, этил или аллил.
4. Соединение по п.2, отличающееся тем, что
R1 обозначает водород, метил, этил или циклопропил;
R2 обозначает водород, метил, этил, циклопропил, циано, метоксикарбонил, -S(O)nС1-С4-алкил или С1-С5-алкокси;
или обозначает кольцевую систему нафтила, бифенила, феноксифенила или фенилтиофенила, причем каждая из них может быть незамещенной или замещенной 1-3 заместителями, выбранными из группы, состоящей из галогена и С1-С2-алкила;
или обозначает радикал фенила, присоединенный непосредственно или через кислород, S(O)n или СН2, который не замещен или замещен не более, чем тремя заместителями, выбранными из группы, состоящей из С1-С4-алкила, C1-С4-алкокси, галогена, CF3, ОСF3, С2-С4-алкинила, NO2, -S(O)n-C1-C4-алкила и группы циклопропилметокси, которая не замещена или замещена в кольце одним или двумя атомами галогена;
или обозначает кольцо пиридина или пиримидина, которое присоединено непосредственно или через кислород или СН2;
или обозначает кольцо тиазолина или оксазолина, которое не замещено или является моно- или двухзамещенным, идентично или отлично, метилом или галогеном;
тогда как R3 и n имеют определенные в формуле I значения.
5. Соединение по п.2, отличающееся тем, что R1 и R3 обозначают метил и R2 обозначает метил, циано, пиридил или фенил, присоединенный непосредственно или с помощью кислорода, -S(O)n или СН2, который не замещен или замещен не более, чем тремя заместителями, выбранными из группы, состоящей из метила, метилтио, метокси, фтора, хлора, брома, CF3, OCF3, пропин-2-ила, NO2 и циано; или обозначает кольцо тиазола или кольцевую систему нафтила, бифенила или феноксифенила, которая является незамещенной или замещенной в каждом случае дважды, идентично или отлично, метилом и/или галогеном; тогда как А и n имеют определенные в формуле I значения.
6. Соединение по п.1, отличающееся тем, что R1, R2 и R3 обозначают метил и А обозначает указанную кольцевую систему.
Текст
1 Настоящее изобретение относится к новым производным бис-оксима. Из уровня техники известны производные бис-оксима, описанные вWO-A-9007493 и WO-A-9514009. Однако в указанных публикациях не упоминается о связи бис-оксимовых фрагментов с микробицидной,инсектицидной и акарицидной видами активности. Основная задача настоящего изобретения заключается в создании новой группы химических соединений, обладающих вышеуказанными видами активности. Поставленная задача решается производными бис-оксима формулы I, обладающими микробицидным, инсектицидным и акарицидным действием, где А означает где W обозначает кислород или серу, а другие обозначения являются заместителями, которые определены следующим образом:R2 означает водород, C1-C6-алкил; гало(С 1 С 6)алкил; С 2-С 6-алкоксиалкил; С 3-С 6-циклоалкил, замещенный или незамещенный арил, замещенный или незамещенный гетероарил, циано, C1-C6-алкоксикарбонил; С 1-С 6-алкил-S(O)n, замещенный или незамещенный арил-S(O)n;C1-C6-алкокси, замещенный или незамещенный арилокси, замещенный или незамещенный гетероарилокси, незамещенный или от моно- до триметилзамещенный гетероциклил, замещенный или незамещенный арил-С 1-С 6 алкил, замещенный или незамещенный гетероарил-С 1-С 6-алкил;R3 означает водород, C1-C6-алкил, C1-C6 галоалкил, имеющий от 1 до 5 атомов галогена; С 1-С 4-алкокси-С 1-С 2-алкил, незамещенный или от моно- до тригалозамещенный С 2-С 6-алкенил,С 2-С 6-алкинил, незамещенный или от моно- до тетрагалозамещенный С 3-С 6-циклоалкил-С 1-С 4 алкил;R6, R7 независимо один от другого обозначают водород, С 1-С 4-алкил, С 3-С 4-алкенил, С 3 С 4-алкинил; 2 В более узком смысле и в качестве особенно важной подгруппы настоящее изобретение относится к соединениям формулы I, в которой А обозначает структурный элемент где W обозначает кислород или серу, R2 имеет вышеприведенные значения, за исключением гало(C1-С 6)алкила, a R1, R3 и n имеют вышеприведенные значения. Заместители по выбору замещенных групп арила, гетероарила, арил-S(O)n, арилокси, гетероарилокси, арил-С 1-С 6-алкила и гетероарил-С 1 С 6-алкила включают С 1-С 4-алкил, С 1-С 6 алкокси, С 1-С 4-галоалкил, С 1-С 4-галоалкокси,C1-С 4-алкилтио, С 1-С 4-алкилсульфинил, С 1-С 4 алкилсульфонил, галоген, нитро, циано, замещенный или незамещенный арил, замещенный или незамещенный арилокси, замещенный или незамещенный арилтио, замещенный или незамещенный гетероарил, замещенный или незамещенный гетероарилокси, замещенный или незамещенный гетероарилтио, незамещенный,моно- или дигалозамещенный и/или моно- или диметилзамещенный циклопропилметокси, замещенный или незамещенный С 2-С 6-алкинил,незамещенный или замещенный моно- или тригалозамещенный С 2-С 6-алкенил и незамещенный или замещенный бензилокси. Пригодными заместителями для только что упомянутых групп арила и гетероарила являются галоген, С 1-С 4-алкил, С 1-С 4-алкокси, С 1 С 4-галоалкил (например CF3) и С 1-С 4 галоалкокси (например -OCF3). Пригодными заместителями для замещенной или незамещенной группы C2-С 6-алкинила,связанной с R2, когда R2 означает арил (особенно фенил), являются С 1-С 4-алкил, С 1-С 4 алкокси, С 1-С 4-галоалкил (например CF3), С 1-С 4 галоалкокси (например -OCF3), С 1-С 4-алкилтио,С 1-С 4-алкилсульфинил, С 1-С 4-алкилсульфонил,галоген, нитро, циано, замещенный или незамещенный фенил, пиридоил или бензоил (причем заместителями на этих шестичленных кольцах, возможно, являются С 1-С 4-алкил, C1-C4 алкокси, С 1-С 4-галоалкил (например CF3), С 1-С 4 галоалкокси (например -OCF3), С 1-С 4-алкилтио,С 1-С 4-алкилсульфинил, С 1-С 4-алкилсульфонил,галоген, нитро, циано), а также незамещенный или С 1-С 4-ацилированный илиO-С 1-С 4 алкилированный С 1-C4-гидроксиалкил, С 1-С 5 алкоксикарбонил,N,N-ди(С 1-С 4 алкил)карбамоил,N-(С 1-С 4-алкил)-N-(С 1-С 4 алкокси)карбамоил, незамещенный или галозамещенный циклопропилоксикарбонил или С 2 С 5-алкенил, который не замещен или замещен С 2-С 4-алкокси и/или галогеном, а также пятиили шестичленный гетероарил с одним или бо 3 лее гетероатомами N, О, S, которые могут быть незамещенными или замещенными одним или более заместителями из числа галогена, циано,гидроксила, а также алкила, алкенила, алкокси,алкенилокси, алкинилокси, которые имеют в каждом случае до 4 атомов углерода. Каждый заместитель может независимо от других присутствовать от 1 до 3 раз. Важную подгруппу активных веществ в этом отношении составляют те, в которых:R2 обозначает группу фенила, которая замещена на незамещенную или замещенную группу этинила, возможными заместителями которой являются С 1-С 4-алкил (например метил,этил), С 1-С 4-гидроксиалкил, галоген, С 1-С 4 галоалкил, циано, С 1-С 5-алкоксикарбонил или циклопропилметоксикарбонил; С 2-С 5-алкенил,который не замещен или замещен С 2-С 4-алкокси и/или галогеном; N-метил-N-метоксикарбамоил; незамещенный или замещенный фенил [при этом заместители выбирают из группы, состоящей из С 1-С 4-алкила, С 1-С 4-алкокси, СF3, CN,галогена (например хлора) и OCF3]; незамещенный или замещенный, пяти- или шестичленный гетероарил [например пиридил, пиразинил, пиримидинил, тиенил, изотиазолил], (заместителями которого могут быть галоген, циано, метил, метокси или гидроксил); иR3 обозначает метил, этил или аллил. Что касается другой важной подгруппы, то предлагаемое изобретение относится к соединениям формулы I, в которойR2 обозначает водород, метил, этил, циклопропил, циано, метоксикарбонил, -S(O)n С 1 С 4-алкил или C1-C5-алкокси; или обозначает кольцевую систему нафтила, бифенила, феноксифенила или фенилтиофенила, причем каждая из них может быть незамещенной или замещенной 1-3 заместителями,выбранными из группы, состоящей из галогена и С 1-С 2-алкила; или обозначает радикал фенила, присоединенный непосредственно или через кислород,S(O)n или СН 2, который не замещен или замещен не более чем тремя заместителями, выбранными из группы, состоящей из С 1-С 4 алкила, C1-С 4-алкокси, циано, галогена, CF3,OCF3, С 2-С 4-алкинила, NO2, -S(O)n-C1-С 4-алкила и группы циклопропилметокси, которая не замещена или замещена в кольце одним или двумя атомами галогена; или обозначает кольцо пиридина или пиримидина, которое присоединено непосредственно или через кислород или СН 2; или обозначает кольцо тиазолина или оксазолина, которое не замещено или является моно- или двухзамещенным, идентично или отлично, метилом или галогеном; 4 тогда как R3 и n имеют определенные в формуле I значения. Важную подгруппу последних соединений составляют те, в которых R1 и R3 обозначают метил и R2 обозначает метил, циано, пиридил или фенил, присоединенный непосредственно или с помощью кислорода, S(O)n или СН 2, который не замещен или замещен не более чем тремя заместителями, выбранными из группы, состоящей из метила, метилтио, метокси, фтора,хлора, брома, CF3, OCF3, пропин-2-ила, NO2 и циано; или обозначает кольцо тиазола или кольцевую систему нафтила, бифенила или феноксифенила, которая является незамещенной или замещенной в каждом случае дважды, идентично или отлично, метилом и/или галогеном; тогда как А и n имеют определенные в формуле I значения. Особенно важная группа включает те соединения формулы I, в которой R1, R2 и R3 обозначают метил и А обозначает указанную кольцевую систему. Новые соединения формулы I обладают фунгицидными, акарицидными и инсектицидными свойствами и пригодны в качестве сельскохозяйственно-активных ингредиентов для использования в сельском хозяйстве. Предлагаемое изобретение дополнительно относится к способу получения новых соединений, к фунгицидным, акарицидным и инсектицидным композициям, содержащим такие соединения в качестве ингредиентов, а также к использованию таких соединений и композиций для борьбы с фитопатогенными грибками, акаридами и насекомыми и для предотвращения заражения грибками, акаридами и насекомыми. Когда соединения формулы I содержат асимметрические атомы углерода, они встречаются в оптически активной форме. Вследствие присутствия алифатических двойных связей и оксиминодвойных связей соединения в любом случае могут находиться в формах [Е] и/или [Z]. Может встречаться атропный изомеризм. Предполагается, что формула I охватывает все эти возможные изомерные формы и их смеси, например рацемические смеси и любые желательные смеси [E/Z]. В зависимости от числа атомов углерода,группы алкила и алкокси являются прямоцепочечными или разветвленными и обозначают,например, метил, этил, н-пропил, изопропил, нбутил, втор.-бутил, изобутил, трет.-бутил, нпентил, неопентил, втор.-пентил, трет.-пентил,н-гексил и так далее. Циклоалкил обозначает циклопропил, циклобутил, циклопентил или циклогексил. Алкенил обозначает прямоцепочечный или разветвленный алкенил, например винил, 1 метилвинил, аллил, 1-бутенил или изопропенил. Алкинил обозначает, например, этинил, 1 пропинил, 1-бутинил или 1,3-бутандинил. 5 Галоген обозначает фтор, хлор, бром или йод, предпочтительно фтор, хлор или бром. Галоалкил может содержать идентичные или различные атомы галогена. Арил обозначает фенил или нафтил, предпочтительно фенил. Гетероарил обозначает группы, имеющие от 5 до 9 членов кольца в одном или двух кольцах, из которых от 1 до 3 членов являются гетероатомами, выбранными из группы, состоящей из кислороды, серы и азота. Можно, чтобы 1 или 2 бензольных кольца были конденсированы на гетероцикле, при этом присоединение остальной части молекулы осуществляется посредством либо гетероциклической части, либо бензольной части. Следует упомянуть примеры бензимидазолила, бензизоксазолила, бензизотиазолила, бензокумаринила, бензофурила, бензотиадиазолила, бензотиазолила, бензотиенила, бензоксазолила, бензодиазолила, хиназолинила, хинолила,хиноксалинила, карбазолила, дигидробензофурила, фурила, имидазолила, индазолила, индолила, изохинолинила, изотиазолила, изоксазолила, метилендиоксифенила, этилендиоксифенила, нафтиридинила, оксазолила, фенантридинила, фталазинила, птеридинила, пуринила, пиразинила,пиразолила, пиридазинила, пиразо[3,4-b]пиридила, пиридила, пиримидинила,пирролила, тетразолила, оксадиазолила, тиадиазолила, тиазолила, тиенила, триазинила и триазолила. Предпочтительными являются пиридил,пиримидинил, тиазолил, хинолил и тиенил. Гетероцикл обозначает 5-7-членное неароматическое кольцо, имеющее от 1 до 3 гетероатомов, выбранных из группы, состоящей из N, О и S. Предпочтение отдается ароматическим 5- и 6-членным кольцам, содержащим атом азота в качестве гетероатома, и, если желательно, дополнительный гетероатом, предпочтительно азот или серу, особенно предпочтительно азот. Предпочтительными являются тиазолинил и оксазолинил. А) Соединение формулы I может быть получено путем взаимодействия оксима формулыI, a U обозначает отщепляемую группу. Эта реакция представляет собой нуклеофильное замещение, которое можно осуществить при обычных для таких реакций условиях. Отщепляемая группа U, присутствующая в соединении формулы III или IV, предпочтительно обозначает хлор, бром, йод, мезилокси или тозилокси. Реакция происходит преимущественно в инертном органическом разбавителе, таком как циклический эфир, например тетрагидрофуран или диоксан, ацетон, диметилформамид или диметилсульфоксид, в присутствии основания,такого как гидрид натрия, карбонат натрия или калия, амид натрия, третичный амин, например триалкиламин, особенно диазабициклононан или диазабициклоундекан, или оксид серебра,при температуре от -20 до +80 С, предпочтительно при температуре от 0 до 50 С. Альтернативно реакцию можно осуществлять в присутствии межфазного катализатора в органическом растворителе, таком как, например, метиленхлорид или толуол, в присутствии водного основного раствора, например раствора гидроксида натрия, и межфазного катализатора,такого как кислый сульфат тетрабутиламмония,при комнатной температуре. Полученные таким образом соединения формулы I можно выделить и очистить известными per se методами. Полученные смеси изомеров, например смеси изомеров E/Z, можно пептизировать в чистые изомеры также известными per se методами, например хроматографией или фракционированной кристаллизацией. Оксимы общей формулы II, используемые в качестве исходных веществ, либо известны,либо могут быть получены известными per se методами [J. Chem. Soc., Perkin Trans. II 537Chem. 262. 305 (1891)]. Аналогичным образом соединения общих формул III и IV либо известны, либо могут быть получены известными методами. Б) Соединения общей формулы I, в которой R1, R2 и R3 имеют вышеприведенные значения, a W означает серу, могут быть дополнительно получены путем осторожного взаимодействия соединений общей формулы I, в которой W означает кислород, с сульфирующим агентом, например P2S5 или реагентом Лавессона, например 2,4-бис(4-метоксифенил)-1,3 дитиа-2,4-дифосфетан 2,4-дисульфидом [см. в 7 этой связи работу Cava + Lawesson, Tetrahedron 41, 5061 (1985)]. В) Соединения формулы I, в которой А обозначает группу и W обозначает кислород, могут быть дополнительно получены в соответствии со схемой 1,представленной ниже. Отдельные стадии реакции можно осуществлять по аналогии с теми, которые описаны в работе Rolf H. Prager и Jason A. Smith в журнале Соединение 1 получают путем взаимодействия оксима общей формулы II в которой R1, R2 и R3 имеют вышеприведенные значения, с производным иодбензола общей формулы в которой U обозначает отщепляемую группу. Соединение 14 получают, подвергая производное нитробензола общей формулы VI каталитической гидрогенизации. Как можно видеть, производные сложного малонового эфира формулы 3 и производные изоксазолона формулы 8 являются важными промежуточными соединениями в способе согласно схеме 1. Г) Соединения формулы I, в которой А обозначает группу могут быть дополнительно получены в соответствии со схемой 2, представленной ниже. Отдельные стадии реакции можно осуществлять по аналогии с теми, которые описаны в работе Arndt et al. в журнале Rev. Fac. Sci. Istanbul [A] 13, 127ff. [Beilstein E III/IV 26, 674]. Как очевидно, производные нитробензола формулы VI, производные анилина формулы 14,изо(тио)цианаты формулы 17 и производные(тио)гуанидина формулы 19 являются важными промежуточными соединениями при получении производных (тио)триазолона формул 22 и 23. Изобретение относится дополнительно к этим промежуточным, в которых R1-R8, Х и W имеют определенные в формуле I значения. Соединения общей формулы VI в свою очередь получают путем взаимодействия оксима общей формулы II производными нитробензола общей формулы где U обозначает отщепляемую группу. Было обнаружено, что соединения формулы I имеют микробицидный спектр действия, 9 который соответствует практическим требованиям при борьбе с фитопатогенными микроорганизмами, особенно грибками. Они обладают чрезвычайно полезными лечебными, превентивными и, в особенности, системными свойствами и могут быть использованы для защиты целого ряда растений. При использовании активных ингредиентов формулы I паразиты,встречающиеся на растениях или частях растений (плоды, цветы, листва, стебли, клубни, корни) различных сельскохозяйственных культур,могут сдерживаться или уничтожаться при одновременной защите от фитопатогенных микроорганизмов, которые развиваются впоследствии на частях растений. Соединения формулы I также могут быть использованы в качестве протравителя для обработки семян (плодов, клубней, посевного материала) и растительных черенков, то есть для обработки материала разведения всех типов, для защиты от грибкового заражения и от фитопатогенных грибков, которые встречаются в почве. Соединения формулы I эффективны, например, в отношении следующих классов фитопатогенных грибков: Fungi imperfecti (особенноBasidiomycetes (например Rhizoctonia, Hemileia,Puccinia), Ascomycetes (например Venturia, Erysiphe, Podosphaera, Monilinia, Uncinula), но особенно в отношении Oomycetes (например Phytophthora, Peronospora, Bremia, Pythium, Plasmopara). Соединения формулы I также обладают инсектицидным и акарицидным действием, особенно против жалящих и сосущих насекомых. Группу растений, для которой используется защита в пределах объема настоящего изобретения, составляют следующие виды растений (даны в качестве примера): зерновые (пшеница, ячмень, рожь, овес, тритикале, рис, кукуруза, сорго и родственные виды); свекловичные культуры (свекла сахарная и свекла кормовая); семечковые плоды, косточковые плоды и сочные плоды (яблоки, груши, слива, персики,миндаль, вишня, земляника, крыжовник, малина и ежевика); бобовые (бобы, чечевица, горох,соя); масличные культуры (масличное семя рапса, горчица, мак, маслина европейская, подсолнечник, кокосовый орех, касторка, какао-боб,земляные орехи); тыквенные (тыква, огурцы,дыни); прядильные растения (хлопчатник, лен,конопля посевная, джут круглоплодный); цитрусовые (апельсины, лимоны, грейпфрут, мандарины); овощи (шпинат, салат, спаржа, капуста, морковь, лук, томаты, картофель, стручковый перец); семейство лавровых (авокадо, коричное дерево, камфора) и такие растения как табак, орехи, сахарный тростник, чай, перец и другие специи, вина, хмель, баклажаны, семейство банановых, латекс, а также цветы и декоративные растения. 10 Активные ингредиенты соединений формулы I обычно используются в форме композиций и могут применяться одновременно или последовательно с другими активными компонентами в отношении обрабатываемых растений или площадей, на которых они произрастают. Этими другими активными компонентами могут быть удобрения, микроэлементы или другие препараты, которые оказывают влияние на рост растений. В этой связи также можно использовать селективные гербициды, а также инсектициды, фунгициды, бактерициды, нематоциды,моллюскициды или смеси двух или более таких препаратов, если желательно, то с дополнительными носителями, поверхностно-активными веществами или иными стимулирующими добавками, которые являются традиционными в технологии приготовления препаратов и которые не оказывают отрицательного воздействия на соединения формулы I. Пригодные носители и добавки могут быть твердыми или жидкими и соответствовать веществам, применение которых целесообразно в технологии приготовления препаратов и примерами которых могут быть натуральные или регенерированные минеральные вещества, растворители, диспергаторы, смачивающие вещества,вещества для повышения клейкости, загустители, связующие или удобрения. Пригодными растворителями являются ароматические углеводороды, предпочтительно фракции C8-C12, например смеси ксилола или замещенные нафталины, фталаты, такие как дибутилфталат или диоктилфталат, алифатические углеводороды, такие как циклогексан или парафины, спирты и гликоли, а также их простые и сложные эфиры, такие как этанол,этиленгликоль, монометиловый эфир или моноэтиловый эфир этиленгликоля, кетоны, такие как циклогексанон, сильно полярные растворители, такие как N-метил-2-пирролидон, диметилсульфоксид или диметилформамид, и немодифицированные или эпоксидированные растительные масла, такие как эпоксидированное кокосовое масло или соевое масло, либо вода. Твердые носители, которые, как правило,используются, например, для дустов и диспергируемых порошков, включают натуральные грунтовые минералы, такие как кальцит, тальк,монтмориллонит или аттапульгит. Особенно предпочтительными промотирующими добавками, которые могут привести к значительно пониженной дозе внесения, являются натуральные (животные или растительные) или синтетические фосфолипиды из ряда цефалинов и лецитинов, которые могут быть получены, например, из сои культурной. Пригодными поверхностно-активными веществами, в зависимости от природы активного компонента формулы I, являются неионные, катионные и/или анионные поверхностноактивные вещества, которые обладают хороши 11 ми эмульгирующими, диспергирующими и смачивающими свойствами. Термин поверхностноактивные вещества следует понимать как включающий в себя смеси поверхностно-активных веществ. Пригодными анионными поверхностноактивными веществами могут быть так называемые водорастворимые мыла и также водорастворимые синтетические поверхностноактивные соединения. Мылами являются соли щелочных металлов, соли щелочно-земельных металлов или замещенные или незамещенные аммониевые соли высших жирных кислот (С 10-С 22), например натриевые соли или калиевые соли олеиновой или стеариновой кислоты, или смеси натуральных жирных кислот, которые могут быть получены,например, из кокосового масла или животного масла. Следует также упомянуть метилтауриновые соли жирных кислот. Пригодными неионными поверхностноактивнымии веществами являются производные полигликолевого эфира алифатических или циклоалифатических спиртов, насыщенных или ненасыщенных жирных кислот и алкилфенолов,которые могут содержать от 3 до 30 групп гликолевого эфира и от 8 до 20 атомов углерода в алифатическом углеводородном радикале и от 6 до 18 атомов углерода в алкильном радикале алкилфенолов. Примерами неионных поверхностноактивных веществ являются нонилфеноксиполиэтоксиэтанолы,полигликолевые эфиры касторового масла, аддукты полипропилена и полиэтиленоксида, трибутилфеноксиполиэтоксиэтанол, полиэтиленгликоль и октилфеноксиполиэтоксиэтанол. Также пригодны сложные эфиры жирных кислот и полиоксиэтиленсорбита, такие как триолеат полиоксиэтиленсорбита. Катионные поверхностно-активные вещества включают, в частности, соли четвертичного аммониевого основания, которые в качестве заместителя на атоме азота содержат, по крайней мере, один алкильный радикал, имеющий от 8 до 22 атомов углерода, а в качестве другого заместителя включают радикалы низшего, незамещенного или галогенированного алкила, радикалы бензила или радикалы низшего гидроксиалкила. Анионные, неионные или катионные поверхностно-активные вещества, известные в области технологий приготовления рецептур,знакомы среднему специалисту в данной области техники или могут быть почерпнуты из соответствующей технической литературы:- Dr. Helmut Stache "Tensid-Taschenbuch",Carl Hanser Verlaf, Munich/Vienna 1982. Как правило, агрохимические составы обычно включают от 0,1 до 99%, предпочтительно от 0,1 до 95%, активного компонента формулы I, от 99,9 до 1%, предпочтительно от 99,9 до 5%, твердой или жидкой добавки и от 0 до 25%, предпочтительно от 0,1 до 25%, поверхностно-активного вещества. В то время как коммерческие продукты предпочтительно составлены в виде концентрированных композиций, конечный пользователь обычно применяет разбавленные композиции. Композиции в соответствии с настоящим изобретением также могут включать в себя другие добавки, такие как стабилизаторы, противовспениватели, регуляторы вязкости, связующие,вещества для повышения клейкости и удобрения, а также другие активные ингредиенты для достижения специфических эффектов. Составы, то есть композиции, препараты или комбинации, содержащие активный компонент формулы I вместе, если желательно, с твердой или жидкой добавкой, получают известным способом, например путем однородного смешивания и/или измельчения активного компонента с наполнителем, например с растворителем (смесью), твердым носителем и, если подходит, поверхностно-активными веществами(или сурфактантами). Предпочтительный метод применения активного компонента формулы I или агрохимической композиции, содержащей, по крайней мере, один из числа этих активных компонентов, заключается в нанесении на листву (некорневое нанесение). Частота и доза внесения зависят в этом случае от уровня разрушения в результате нападения рассматриваемого патогенного организма. Однако активные компоненты формулы I также могут достигать растения через корневую систему (общее действие), путем пропитки локуса растения жидким препаратом или путем введения веществ в твердой форме в почву, например в форме гранул (почвенное внесение). В случае риса такие гранулы можно вводить в отмеренном количестве в рисовое поле с затоплением. Для обработки семян соединения формулы I также могут быть нанесены на ядра семян (покрытие) либо путем пропитки ядер зерен жидким составом активного компонента, либо путем их покрытия твердым составом. В принципе, любой тип материала для размножения растений может быть защищен с использованием соединений формулы I, и примерами являются семена, корни, стебли, ветви или ростки. В данном контексте соединения формулы I используются в чистом виде или, предпочтительно, вместе с адъювантами, традиционно применяемыми в технологии приготовления препаратов. Для этой цели их целесообразно производить известным способом, например, 13 получая эмульгируемые концентраты, пасты,предназначенные для покрытия, непосредственно распыляемые или разбавляемые растворы,разбавленные эмульсии, смачиваемые порошки,растворимые порошки, дусты, гранулы и инкапсулированные формы (например, в полимерных веществах). Методы применения, такие как разбрызгивание, распыление, опудривание, рассеяние, окрашивание или выливание, а также вид композиции выбирают в соответствии с предполагаемыми задачами и преобладающими обстоятельствами. Благоприятные дозы внесения обычно составляют от 1 г до 2 кг активного компонента на гектар, предпочтительно от 25 до 800 г активного компонента на гектар, наиболее предпочтительно от 50 до 400 г активного компонента на гектар. В случае использования для протравления семян дозы внесения составляют от 0,001 до 1,0 г активного компонента на 1 кг семян. Следующие примеры предназначены для более подробной иллюстрации изобретения без какого-либо ограничения его объема. Примеры получения Пример 1. Получение 0,22 г 60% дисперсии гидрида натрия промывают гексаном и добавляют 5 мл N,Nдиметилформамида. К этой суспензии добавляют 1,5 г 4-(орто-бромметилфенил)-2,3-дигидро 5-метокси-2-метил-3-изоксазолона и 0,65 г 3 метоксимино-2-бутаноноксима и реакционную смесь перемешивают в течение 1 ч. Затем добавляют ледяную воду и смесь подвергают экстракции этилацетатом. Органическую фазу промывают насыщенным раствором кислого углекислого натрия и затем насыщенным раствором хлорида натрия. После сушки в присутствии безводного сульфата натрия растворитель отгоняют в вакууме и остаток хроматографируют на силикагеле с использованием этилацетата/гексана (1:2), получая соединение 1.1; температура плавления 100-107 С. Пример 2. Получение 0,7 г реагента Лавессона добавляют к раствору 1 г соединения, полученного в примере 1, в 10 мл 14 толуола и образовавшуюся суспензию нагревают при температуре 100 С в течение 2 ч. Затем ее разбавляют этилацетатом и промывают водой. Органическую фазу сушат в присутствии сульфата натрия и растворитель отгоняют в вакууме. Остаток хроматографируют на силикагеле с использованием этилацетата:гексана (1:3),получая соединение 2.1 в виде желтого масла. Пример 3. Получение[1,2,4]триазол-3-она (получен в соответствии с заявкой РСТWO 95/14009) и 7,83 г Nбромсукцинимида помещают в 50 мл тетрахлорметана с последующим добавлением каталитического количества дибензоилпероксида. Затем суспензию перемешивают при температуре дефлегмации с освещением (фотографическая лампа 500 Вт) в течение 1,5 ч. Суспензию концентрируют упариванием и остаток хроматографируют непосредственно на силикагеле с использованием гексана:этилацетата (6:4). Рекристаллизация из толуол/гептана (1:1) приводит к получению 4-(2-бромметилфенил)-5-хлор 2-метил-2,4-дигидро[1,2,4]триазол-3-она в виде кристаллов белого цвета; температура плавления 131,5-133 С. 1H-ЯМР (СDСl3)7,52 (m, 3 Н); 7,23 (m,1H); 4,6 (d, 1H); 4,33 (d, 1H); 3,57 (s, 3H). б) 1,6 г 1-метоксимино-1-(2,4-дифторфенил)-2-пропаноноксима и 2,12 г 4-(2-бромметилфенил)-5-хлор-2-метил-2,4-дигидро [1,2,4] триазол-3-она перемешивают при температуре дефлегмации в присутствии 1,45 г карбоната калия в 20 мл ацетонитрила в течение 2,5 ч. Смесь концентрируют и остаток хроматографируют непосредственно на силикагеле с использованием гексана/этилацетата (65:35) с получением соединения 6.91 в виде воска. 1(s, 3H). Таким способом или по аналогии с одним из способов, указанных выше, можно получить следующие соединения, которые принадлежат к более узкому диапазону в соответствии с настоящим изобретением. 42 Высокодисперсная кремниевая кислота 5% 10% 10% Каолин 62% 27% Активный компонент тщательно смешивают с добавками и смесь тщательно измельчают в подходящей мельнице. Получают смачиваемый порошок, который можно разбавить водой с получением суспензии любой желательной концентрации. 2.2. Эмульгируемый концентрат. Активный компонент из таблиц 1-9 Октилфениловый эфир полиэтиленгликоля (4-5 моль оксида этилена) Додецилбензолсульфонат кальция Циклогексанон Смесь ксилолов Эмульсии любой желательной степени разбавления могут быть получены при разбавлении водой. 2.3. Дуст Активный компонент из таблиц 1-9 Тальк Каолин Готовые к употреблению дусты получают путем смешивания активного компонента с носителем и измельчения в подходящей мельнице. 2.4. Экструдированные гранулы Активный компонент из таблиц 1-9 Лигнинсульфонат натрия Карбоксиметилцеллюлоза Каолин 2. Примеры приготовления композиции с активными компонентами формулы (% означает процент по массе). 2.1. Смачиваемый порошок. а)b) с) Активный компонент из таблиц 1-9 25% 50% 75% Лигнинсульфонат натрия 5% 5% Лаурилсульфат натрия 3% 5% Диизобутилнафталинсульфонат натрия 6% 10% Октилфеноловый эфир полиэтиленгликоля (7-8 моль оксида этилена) 2% Активный компонент смешивают с добавками и смесь измельчают и увлажняют водой. Смесь экструдируют и затем сушат в потоке воздуха. 2.5. Гранулы с покрытием. Активный компонент из таблиц 1-9 3% Полиэтиленгликоль (ММ 200) 3% Каолин 94%(MM означает молекулярная масса). Тонко измельченный активный компонент наносят равномерно в смесителе на каолин, увлажненный полиэтиленгликолем. Таким образом, получают гранулы с покрытием, не содержащие пыли. 2.6. Суспензионный концентрат. Активный компонент из таблиц 1-9 40% Этиленгликоль 10% 43 Нонилфениловый эфир полиэтиленгликоля (15 моль оксида этилена) 6% Лигнинсульфонат натрия 10% Карбоксиметилцеллюлоза 1% 37% водный раствор формальдегида 0,2% Силиконовое масло в форме 75% водной эмульсии 0,8% Вода 32% Тонко измельченный активный компонент тщательно смешивают с добавками с получением суспензионного концентрата, из которого суспензии с любой желательной степенью разбавления можно получить путем разбавления водой. 3. Биологические примеры. Пример В-1. Действие против возбудителей заболевания Phytophthora на растениях томата. а) Лечебное действие. Растения томатов сорта "Roter Gnom" выращивают в течение 3 недель, а затем опрыскивают зооспоровой суспензией грибка и инкубируют в кабине при температуре 18-20 С в насыщенной влагой атмосфере. Увлажнение прерывают через 24 ч. После сушки растений их опрыскивают смесью, содержащей активный компонент, которая составлена как смачиваемый порошок, при концентрации 200 частей на миллион. После высыхания покровного слоя растения возвращают во влажную кабину на 4 дня. Величину и размер типичной листовой пятнистости, которая проявилась по истечении этого периода, используют для оценки активности испытуемых веществ. б) Превентивно-системное действие. Активный компонент в составе смачиваемого порошка вносят при концентрации 60 частей на миллион (относительно объема почвы) в поверхность почвы трехнедельных растений томатов сорта "Roter Gnom" в горшках. По истечении 3 дней нижнюю сторону листьев опрыскивают зооспоровой суспензией возбудителей заболевания Phytophthora. Затем растения содержат в течение 5 дней в кабине при температуре 18-20 С в насыщенной влагой атмосфере. По истечении этого периода развивается типичная листовая пятнистость, величину и размер которой используют для оценки активности испытуемых веществ. Если необработанные, но зараженные контрольные растения показывают уровень заражения 100%, то активные компоненты формулы I в соответствии с одной из таблиц 1-9 подавляют заражение в одном или двух тестах до 10% или менее. Особенно хорошее действие показано соединением 3.87. Пример В-2. Действие против Plasmopara 44 Виноградные черенки сорта "Chasselas" выращивают в теплице. Когда они достигают фазы распускания 10 листьев, три растения опрыскивают смесью активного компонента (200 частей на миллион активного компонента). После высыхания покровного слоя нижнюю сторону листьев опрыскивают суспензией спор грибков. Затем растения возвращают во влажную кабину на 8 дней. По истечении этого периода заметные симптомы заболевания очевидны на контрольных растениях. Количество и размер сайтов заражения на обработанных растениях используют для оценки активности испытуемых веществ. б) Лечебное действие. Виноградные черенки сорта "Chasselas" выращивают в теплице и по достижении фазы распускания 10 листьев их заражают путем нанесения на нижнюю сторону листьев споровой суспензии Plasmopara viticola. По истечении 24 ч нахождения во влажной кабине растения опрыскивают смесью активного компонента (200 частей на миллион активного компонента). После высыхания покровного слоя растения возвращают во влажную кабину на 7 дней. По истечении этого периода заметные симптомы заболевания очевидны на контрольных растениях. Величину и размер сайтов заражения на обработанных растениях используют для оценки активности испытуемых веществ. По сравнению с контрольными растениями заражение растений, обработанных активными компонентами формулы I, составляет 20% или менее. Особенно хорошее действие показано соединением 3.87. Пример В-3. Действие против Pythium debaryanum на растениях сахарной свеклы (Betavulgaris). а) Действие после внесения в почву. Грибок выращивают на стерильных зернах овса и добавляют в смесь грунта и песка. Почву,зараженную таким путем, помещают в цветочные горшки и засевают семенами сахарной свеклы. Сразу же после посева испытуемые препараты в виде смачиваемых порошков выливают на почву в форме водной суспензии (20 частей на миллион активного компонента относительно объема почвы). Затем горшки помещают в теплицу на 2-3 недели при температуре 20-24C. Все время почву поддерживают равномерно увлажненной путем ее опрыскивания водой. После оценки тестов определяют всхожесть растений сахарной свеклы и отношение здоровых растений к больным. б) Действие после протравливания семян. Грибок выращивают на стерильных зернах овса и добавляют в смесь грунта и песка. Почву,зараженную таким путем, помещают в цветочные горшки и засевают семенами сахарной свеклы, которые были протравлены с помощью испытуемых препаратов в виде порошков для протравливания семян (1000 частей на миллион 45 активного компонента относительно массы семян). Затем горшки помещают в теплицу на 2-3 недели при температуре 20-24 С. Все время почву поддерживают равномерно увлажненной путем ее опрыскивания водой. После оценки тестов определяют всхожесть растений сахарной свеклы и отношение здоровых растений к больным. После обработки активными компонентами формулы I свыше 80% растений всходят и имеют здоровый внешний вид. В контрольных горшках взошли только несколько растений, имеющих нездоровый внешний вид. Пример В-4. Остаточно-защитное действие против Cercospora arachidicola на растениях земляного ореха. Растения земляного ореха высотой 10-15 см опрыскивают в месте удлиненных кончиков листьев водной смесью для опрыскивания(0,02% активного вещества), а через 48 ч заражают конидиевой суспензией грибка. Растения инкубируют в течение 72 ч при температуре 21 С и высокой атмосферной влажности, после чего помещают в теплицу вплоть до появления типичной пятнистости на листьях. Действие активного вещества оценивают через 12 дней после заражения на основании величины и размера пятнистости листьев. Активные компоненты формулы I приводят к заметному снижению пятнистости листьев, приблизительно до уровня менее 10% от площади поверхности листьев. В некоторых случаях болезнь подавляется полностью (0-5% инвазии). Пример В-5. Действие против Pucciniagraminis на растениях пшеницы. а) Остаточно-защитное действие. Через 6 дней после посева растения пшеницы опрыскивают в месте удлиненных кончиков листьев водной смесью для опрыскивания(0,02% активного вещества), а через 24 ч заражают уредоспоровой суспензией грибка. По истечении периода инкубации, равного 48 ч (условия: относительная атмосферная влажность 95-100% при температуре 20 С), растения помещают в теплицу при температуре 22 С. Развитие телейтопустул (спороношение ржавчинного гриба) оценивают через 12 дней после заражения. б) Системное действие. Через 5 дней после посева водную смесь для опрыскивания (0,006% активного вещества относительно объема почвы) вливают рядом с растениями пшеницы. Старательно избегают контакта распыляемой смеси с воздушными частями растений. Через 48 ч растения заражают уредоспоровой суспензией грибка. По истечении периода инкубации, равного 48 ч (условия: относительная атмосферная влажность 95100% при температуре 20 С), растения помещают в теплицу при температуре 22 С. Развитие телейтопустул (спороношение ржавчинного 46 гриба) оценивают через 12 дней после заражения. Соединения формулы I приводят к заметному снижению объема грибковой инвазии, в некоторых случаях до 10-0%, например такие соединения как 1.1; 3.1; 3.7; 3.13; 3.16; 3.19; 7.2; 7.12; 7.5; 7.7; 7.43; 8.10; 8.27; 8.40; 8.43; 8.55; 8.57; 8.61; 8.62; 9.1; 9.13 и другие. Пример В-6. Действие против Pyriculariaoryzae на растениях риса. а) Остаточно-защитное действие. Растения риса выращивают в течение 2 недель и опрыскивают в месте удлиненных кончиков листьев водной смесью для опрыскивания(0,02% активного вещества), а через 48 ч заражают конидиевой суспензией грибка. Грибковую инвазию оценивают через 5 дней после заражения и в течение этого периода относительную атмосферную влажность поддерживают на уровне 95-100%, а температуру на уровне 22 С. б) Системное действие. Водную смесь для опрыскивания (0,006% активного вещества относительно объема почвы) вливают рядом с двухнедельными растениями риса. Старательно избегают контакта распыляемой смеси с воздушными частями растений. Затем горшки наполняют водой так, чтобы погрузились нижние части стеблей растений риса. Через 96 ч растения заражают конидиевой суспензией грибка и выдерживают в течение 5 дней при относительной атмосферной влажности 95-100% и при температуре 24 С. В большинстве случаев соединения формулы I предотвращают вспышку заболевания на зараженных растениях. Пример В-7. Остаточно-защитное действие против Venturia inaequalis на яблонях. Черенки яблонь, имеющие свежие побеги длиной от 10 до 20 см, опрыскивают в месте удлиненных кончиков листьев водной смесью для опрыскивания (0,02% активного вещества),а через 24 ч заражают конидиевой суспензией грибка. Растения инкубируют в течение 5 дней при относительной атмосферной влажности на уровне 90-100%, а затем помещают на 10 дней в теплицу при температуре на уровне 20-24 С. Заражение паршой оценивают через 15 дней после инвазии. Большинство соединений формулы I из таблиц 1-9 имеют устойчивое действие против заболеваний, вызванных паршой. Пример В-8. Действие против Erysiphegraminis на растениях ячменя. а) Остаточно-защитное действие. Растения ячменя длиной около 8 см опрыскивают в месте удлиненных кончиков листьев водной смесью для опрыскивания (0,02% активного вещества), а через 3-4 ч посыпают конидиевой суспензией грибка. Зараженные растения помещают в теплицу при температуре 22 С. Грибковую инвазию оценивают через 10 дней после заражения. 47 б) Системное действие. Водную смесь для опрыскивания (0,002% активного вещества относительно объема почвы) вливают рядом с растениями ячменя высотой приблизительно 8 см. Старательно избегают контакта распыляемой смеси с воздушными частями растений. Через 48 ч растения посыпают конидиевой суспензией грибка. Зараженные растения помещают в теплицу при температуре 22 С. Грибковую инвазию оценивают через 10 дней после заражения. Соединения формулы I приводят в основном к снижению уровня заболевания до менее чем 20%, а в некоторых случаях полностью исключают заболевание. Это такие соединения,как 1.1; 3.1; 3.7; 3.13; 3.16; 3.19; 7.2; 7.12; 7.5; 7.7; 7.43; 8.10; 8.27; 8.40; 8.43; 8.55; 8.57; 8.61; 8.62; 9.1; 9.13 и другие. Пример В-9. Остаточно-защитное действие против Podosphaera leucotricha на побегах яблонь. Черенки яблонь, имеющие свежие побеги длиной около 15 см, опрыскивают в месте удлиненных кончиков листьев водной смесью для опрыскивания (0,06% активного вещества), а через 24 ч обработанные растения заражают конидиевой суспензией грибка. Растения помещают в кабину с регулируемой средой при относительной атмосферной влажности на уровне 70% и при температуре на уровне 20 С. Грибковую инвазию оценивают через 12 дней после заражения. Активные компоненты формулы I подавляют уровень заражения примерно до 20%. Контрольные растения показывают уровень заболевания 100%. Пример В-10. Действие против Botrytis cinerea на плодах яблонь. Остаточно-защитное действие. Яблоки с искусственными порезами обрабатывают наносимой по каплям смесью для опрыскивания (0,02% активного вещества) на порезы. Обработанные плоды затем заражают споровой суспензией грибка и инкубируют при высокой атмосферной влажности и температуре около 20 С в течение 1 недели. Фунгицидное действие испытуемого вещества оценивают по числу порезов, проявляющих признаки гниения. Активные компоненты формулы I из таблиц 1-9 способны предотвращать распространение гниения, а в некоторых случаях полностью предотвращают его. Пример В-11. Действие против Helminthosporium gramineum. Зерна пшеницы заражают споровой суспензией грибка и сушат. Зараженные зерна протравливают суспензией испытуемого вещества(600 частей на миллион активного компонента относительно массы семян). Через 2 дня зерна помещают в пригодные чашки, содержащие агар, и через 4 дня оценивают развитие грибковых колоний вокруг семян. Количество и размер 48 грибковых колоний используют для оценки активности испытуемого вещества. Соединения формулы I показывают в некоторых случаях хорошее действие, то есть хорошее ингибирование грибковых колоний. Пример В-12. Действие против Colletotrichum lagenarium на огурцах. Растения огурцов выращивают в течение 2 недель, а затем опрыскивают смесью для распыления (концентрация 0,002%). Через 2 дня растения заражают споровой суспензией (1,5 х 105 спор/мл) грибка и инкубируют в течение 36 ч при температуре 23 С и высокой атмосферной влажности. Затем инкубацию продолжают при нормальной атмосферной влажности и температуре около 22-23 С. Проявленную грибковую инвазию оценивают через 8 дней после заражения. Необработанные, но зараженные контрольные растения проявляют грибковую инвазию на уровне 100%. Соединения формулы I показывают в некоторых случаях почти полное ингибирование заболевания. Пример В-13. Действие против Fusariumnivale на ржи посевной. Семена ржи посевной сорта Tetrahell, зараженные Fusarium nivale, протравливают испытуемым фунгицидом, используя смесительный валок. При этом пользуются следующими концентрациями: 20 и 6 частей на миллион активного компонента относительно массы семян. С использованием рядовой сеялки производят сев зараженной и обработанной ржи в октябре в поле, применяя делянки размером 3 м с 6 бороздами, при этом на каждую концентрацию используют 3 повтора. До начала оценки инвазии испытуемые растения выращивают в нормальных полевых условиях (предпочтительно в районе, полностью покрытым снегом в течение зимних месяцев). Для оценки фитотоксичности прорастание семян измеряют осенью, тогда как отношение количества растений на площадь к числу побегов на каждое растение измеряют весной. Для определения активности активного компонента, весной, как только снег начинает таять, определяют процент растений, зараженных Fusarium. Количество зараженных растений составляет менее 5% в случае обработки соединением формулы I. Проросшие растения имеют здоровый вид. Пример В-14. Действие против Septorianodorum на пшенице. Растения пшеницы фазы распускания трех листьев опрыскивают смесью для опрыскивания(60 частей на миллион активного компонента),полученной из смачиваемого порошка активных веществ. Через 24 ч обработанные растения заражают конидиевой суспензией грибка. Затем растения инкубируют в течение 2 дней при относительной атмосферной влажности на уровне 90 49 100% и помещают на 10 дней в теплицу при температуре на уровне 20-24 С. Грибковое заражение оценивают через 13 дней после инвазии. Менее 1% растений пшеницы проявляют заболевание. Пример В-15. Действие против Rhizoctoniasolani на рисе. Защитно-местное внесение в почву. Десятидневные растения риса, содержащиеся в цветочных горшках, смачивают суспензией (смесью для распыления), полученной из испытуемого вещества, без заражения воздушных частей растений суспензией. Через 3 дня растения заражают, поместив в каждый горшок стебель ячменной соломки,зараженныйRhizoctonia solani, между рисовыми растениями. Через 6 дней инкубации в помещении с регулируемой средой при дневной температуре 29 С и ночной температуре 26 С и относительной атмосферной влажности 95% оценивают грибковую инвазию. Заражено менее 5% растений риса. Растения имеют здоровый вид. Защитно-местное нанесение на листву. Двенадцатидневные растения риса опрыскивают суспензией, полученной из испытуемых веществ. Через один день растения заражают, поместив в каждый горшок стебель ячменной соломки, зараженный Rhizoctonia solani,между рисовыми растениями. Через 6 дней инкубации в помещении с регулируемой средой при дневной температуре 29 С и ночной температуре 26 С и относительной атмосферной влажности 95% оценивают грибковую инвазию. Необработанные, но зараженные контрольные растения проявляют грибковую инвазию на уровне 100%. Соединения формулы I показывают в некоторых случаях почти полное ингибирование заболевания. Инсектицидное действие. Пример В-16. Действие против Heliothis virescens. Молодые растения сои культурной опрыскивают водно-эмульсионной смесью для распыления, которая содержит 100 частей на миллион активного компонента. Затем, после высыхания покровного слоя, растения заселяют 10 гусеницами Heliothis virescens первой возрастной стадии, после чего помещают в пластмассовый контейнер. Через 6 дней, сравнивая количество мертвых гусениц с поражением обработанных и необработанных растений, определяют снижение процента популяции и процента поражения (% действия). Соединения формулыI проявляют в данном тесте хорошее действиеlittoralis. Молодые растения сои культурной опрыскивают водно-эмульсионной смесью для распыления, которая содержит 100 частей на миллион активного компонента. Затем, после высыхания покровного слоя, растения заселяют 10 50 гусеницами Spodoptera littoralis третьей возрастной стадии, после чего помещают в пластмассовый контейнер. Через 3 дня, сравнивая количество мертвых гусениц с поражением обработанных и необработанных растений, определяют снижение процента популяции и процента поражения (% действия). Соединения формулыI из таблиц 1-9 проявляют в данном тесте хорошее действие. Пример В-22. Действие против гусеницPlutella xylostella. Молодые растения капусты опрыскивают водно-эмульсионной смесью для распыления, которая содержит 100 частей на миллион активного компонента. Затем, после высыхания покровного слоя, растения заселяют 10 гусеницами Plutella xylostella третьей возрастной стадии, после чего помещают в пластмассовый контейнер. Оценку осуществляют через 3 дня. Сравнивая количество мертвых гусениц с поражением обработанных и необработанных растений, определяют снижение процента популяции и, соответственно, снижение процента поражения (% действия). Соединения из таблиц проявляют в данном тесте хорошее действие. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Производные бис-оксима формулы I где W обозначает кислород или серу, а другие обозначения являются заместителями, которые определены следующим образом:R2 означает водород, С 1-С 6-алкил, гало(С 1 С 6)алкил,С 2-С 6-алкоксиалкил,С 3-С 6 циклоалкил, замещенный или незамещенный арил, замещенный или незамещенный гетероарил, циано; С 1-С 6-алкоксикарбонил, С 1-С 6 алкил-S(O)n, замещенный или незамещенный арил-S(O)n, C1-C6-алкокси, замещенный или незамещенный арилокси, замещенный или незамещенный гетероарилокси, незамещенный или от моно- до триметилзамещенный гетероциклил, замещенный или незамещенный арил-С 1 С 6-алкил, замещенный или незамещенный гетероарил-С 1-С 6-алкил;R3 означает водород, С 1-С 6-алкил, С 1-С 6 галоалкил, имеющий от 1 до 5 атомов галогена,С 1-С 4-алкокси-С 1-С 2-алкил, незамещенный или от моно- до тригалозамещенный С 2-С 6-алкенил,С 2-С 6-алкинил, незамещенный или от моно- до тетрагалозамещенный С 3-С 6-циклоалкил-С 1-С 4 алкил;R6, R7 независимо один от другого обозначают водород, С 1-С 4-алкил, С 3-С 4 алкенил, С 3 С 4-алкинил;R5 означает С 1-C4-алкил, С 1-С 3-галоалкил. 2. Соединение по п.1, отличающееся тем,что R8 обозначает метил и Х обозначает метокси, R2 имеет определенные выше значения, за исключением гало(С 1-С 6)алкила, и R1, R3, n и W имеют определенные выше значения. 3. Соединение по п.1, отличающееся тем,чтоR2 обозначает группу фенила, которая замещена на незамещенную или замещенную группу этинила, возможными заместителями которой являютсяC1-С 4-алкил,С 1-С 4 гидроксиалкил, галоген, С 1-С 4-галоалкил, циано,С 1-С 5-алкоксикарбонил или циклопропилметоксикарбонил, С 2-С 5-алкенил, который не замещен или замещен С 2-С 4-алкокси и/или галогеном; Nметил-N-метоксикарбамоил; незамещенный или замещенный фенил [при этом заместители выбирают из группы, состоящей из С 1-С 4-алкила,С 1-С 4-алкокси, СF3, CN, галогена и ОСF3]; незамещенный или замещенный, пяти- или шестичленный гетероарил, заместителями которого являются галоген, циано, метил, метокси или гидроксил; иR2 обозначает водород, метил, этил, циклопропил, циано, метоксикарбонил, -S(O)nС 1-С 4 алкил или С 1-С 5-алкокси; или обозначает кольцевую систему нафтила, бифенила, феноксифенила или фенилтиофе 52 нила, причем каждая из них может быть незамещенной или замещенной 1-3 заместителями,выбранными из группы, состоящей из галогена и С 1-С 2-алкила; или обозначает радикал фенила, присоединенный непосредственно или через кислород,S(O)n или СН 2, который не замещен или замещен не более, чем тремя заместителями, выбранными из группы, состоящей из С 1-С 4 алкила, C1-С 4-алкокси, галогена, CF3, ОСF3, С 2 С 4-алкинила, NO2, -S(O)n-C1-C4-алкила и группы циклопропилметокси, которая не замещена или замещена в кольце одним или двумя атомами галогена; или обозначает кольцо пиридина или пиримидина, которое присоединено непосредственно или через кислород или СН 2; или обозначает кольцо тиазолина или оксазолина, которое не замещено или является моно- или двухзамещенным, идентично или отлично, метилом или галогеном; тогда как R3 и n имеют определенные в формуле I значения. 5. Соединение по п.2, отличающееся тем,что R1 и R3 обозначают метил и R2 обозначает метил, циано, пиридил или фенил, присоединенный непосредственно или с помощью кислорода, -S(O)n или СН 2, который не замещен или замещен не более, чем тремя заместителями,выбранными из группы, состоящей из метила,метилтио, метокси, фтора, хлора, брома, CF3,OCF3, пропин-2-ила, NO2 и циано; или обозначает кольцо тиазола или кольцевую систему нафтила, бифенила или феноксифенила, которая является незамещенной или замещенной в каждом случае дважды, идентично или отлично,метилом и/или галогеном; тогда как А и n имеют определенные в формуле I значения. 6. Соединение по п.1, отличающееся тем,что R1, R2 и R3 обозначают метил и А обозначает указанную кольцевую систему.
МПК / Метки
МПК: A01N 43/80, C07C 251/52, C07D 261/12
Метки: триазолина, производные, бис-оксимовые, изоксалина
Код ссылки
<a href="https://eas.patents.su/27-435-bis-oksimovye-proizvodnye-triazolina-i-izoksalina.html" rel="bookmark" title="База патентов Евразийского Союза">Бис-оксимовые производные триазолина и изоксалина</a>
Предыдущий патент: Фармацевтическая композиция, получаемая экструзией расплава
Следующий патент: Способ получения паклитаксела
Случайный патент: Антагонисты рецепторов простагландина d2












