Производные о-бензилового эфира оксима и его возможные изомеры и смеси изомеров
Формула / Реферат
1. Производные O-бензилового эфира оксима общей формулы I
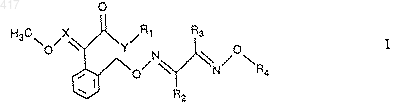
и его возможные изомеры и смеси изомеров, где
а) Х обозначает атом азота и Y обозначает атом кислорода или NH, или
б) Х обозначает СН и Y обозначает атом кислорода;
R1 обозначает С1-C4-алкил;
R2 обозначает водород, C1-C6-алкил или циклопропил;
R3 обозначает С1-С6-алкокси, который не замещен или замещен 1-5 атомами галогена, замещенный или незамещенный арилокси, С1-С6-алкилтио, который не замещен или замещен 1-5 атомами галогена, замещенный или незамещенный арилтио, замещенный или незамещенный гетероарилокси, замещенный или незамещенный гетероарилтио, замещенный или незамещенный аралкил, замещенный или незамещенный бифенил, замещенный или незамещенный С2-C4-алкинилфенил, замещенный или незамещенный гетероарилметил; и
R4 обозначает С1-С6-алкил, С1-С6-галоидалкил, имеющий от 1 до 5 атомов галогена, С1-C4-алкокси-С1-С2-алкил, С2-С6-алкенил, который не замещен или замещен 1-3 атомами галогена; С2-С6-алкинил, С3-С6-циклоалкил-С1-C4-алкил, который не замещен или замещен 1-4 атомами галогена; причем R3 имеет значение иное, чем дихлорбензил, когда одновременно R1 обозначает метил, R2 обозначает водород, Х обозначает СН, Y обозначает кислород и R4 обозначает С1-C4-алкил.
2. Соединение по п.1, отличающееся тем, что R3 обозначает С1-С6-алкокси, С1-C4-галоидалкокси, замещенный или незамещенный фенокси, C1-С6-алкилтио, который не замещен или замещен 1-3 заместителями, выбранными из галогена, С1-C4-алкила, С1-C4-алкокси, CF3 и замещенного фенилтио; или обозначает незамещенный или в каждом случае галоидзамещенный пиридилокси, пиримидинилокси, хинолилокси, хиназолинилокси или хиноксазолинил; или обозначает незамещенный или С1-C4-алкил-, или галоидзамещенный радикал бензотиазолилтио, бензоксазолилтио, имидазолилтио или тетразолилтио; или обозначает дифенил, С2-C4-алкинилфенил, бензил или нафтилметил, который не замещен или замещен 1-3 заместителями, выбранными из галогена, С1-С4-алкила, С1-C4-алкокси, CF3 и CN; R4 обозначает C1-C6-алкил, С1-С6-галоидалкил, незамещенный или галоидзамещенный С2-C4-алкенил, С3-C4-алкинил, незамещенный или галоидзамещенный циклопропилметил, тогда как X, Y, R1 и R2 имеют значения, определенные для формулы I.
3. Соединение по п.2, отличающееся тем, что R1 обозначает метил, R2 обозначает водород, метил или циклопропил, тогда как X, Y, R3 и R4 имеют определенные выше значения.
4. Соединение по п.1, отличающееся тем, что Х обозначает СН или N, Y обозначает кислород, R1 обозначает метил или этил, R2 обозначает метил или циклопропил, тогда как R3 и R4 имеют определенные для формулы I значения.
5. Соединение по п.1, отличающееся тем, что Х обозначает азот, Y обозначает NH, R1 обозначает метил, этил или изопропил, R2 обозначает метил или циклопропил, тогда как R3 и R4 имеют определенные для формулы I значения.
6. Соединение по п.1, отличающееся тем, что R1 обозначает метил, R2 обозначает метил, R4 обозначает С1-С6-алкил, тогда X, Y и R3 имеют определенные для формулы I значения.
7. Соединение по п.1, отличающееся тем, что R1 обозначает метил, R2 обозначает метил, R3 обозначает замещенный или незамещенный C1-C6-алкокси или замещенный или незамещенный С1-С6-алкилтио, тогда X, Y и R4 имеют определенные для формулы I значения.
8. Соединение по п.1, отличающееся тем, что R1 обозначает метил, R2 обозначает метил, R3 обозначает замещенный или незамещенный арилокси или замещенный или незамещенный арилтио, тогда X, Y и R4 имеют определенные для формулы I значения.
9. Соединение по п.1, отличающееся тем, что R1 обозначает метил, R2 обозначает метил, R3 обозначает замещенный или незамещенный гетероарилокси или замещенный или незамещенный гетероарилтио, тогда X, Y и R4 имеют определенные для формулы I значения.
10. Соединение по п.1, отличающееся тем, что R1 обозначает метил, R2 обозначает метил, R3 обозначает замещенный или незамещенный бензил или замещенный или незамещенный гетероарилметил, тогда X, Y и R4 имеют определенные для формулы I значения.
11. Соединение по п.1, отличающееся тем, что R1 обозначает метил, R2 обозначает метил, R3 обозначает замещенный или незамещенный бифенил или замещенный или незамещенный С2-C4-алкинилфенил, тогда X, Y и R4 имеют определенные для формулы I значения.
12. Соединение по п.11, отличающееся тем, что R4 обозначает метил, этил или аллил, R3 обозначает группу незамещенного или замещенного С2-С4-алкинилфенила, в которой возможный заместитель находится в алкинильной группе и обозначает С1-C4-алкил, С1-C4-алкокси, С1-C4-галоидалкил (особенно СF3), С1-C4-галоидалкокси (особенно ОСF3), С1-C4-алкилтио, галоген, нитро, циано, С1-C4-алкилсульфинил, С1-C4-алкилсульфонил, незамещенный или замещенный фенил (где заместители фенила выбирают из С1-C4-алкила, С1-C4-алкокси, гидроксила, С1-C4-галоидалкила, C1-C4-галоидалкокси, С1-C4-алкилтио, галогена, нитро и циано); С1-C4-гидроксиалкил, который может быть O-ацилированным(С1-C4) или O-алкилированным(С1-C4); С1-С5-алкоксикарбонил, карбамоил, N-(С1-C4-алкил)карбамоил, N, N-ди(С1-C4-алкил) карбамоил, N-С1-C4-алкил-N-С1-C4-алкоксикарбамоил; незамещенный или галоидзамещенный циклопропилметоксикарбонил, незамещенный, С1-C4-алкоксизамещенный или галоидзамещенный С2-С5-алкенил и пяти- или шестичленное кольцо гетероарила, которое не замещено или замещено галогеном, циано, гидроксилом, а также алкилом, алкенилом, алкокси, алкенилокси или алкинилокси, каждый из которых содержит не более 4 атомов углерода.
13. Соединение по п.12, отличающееся тем, что R3 обозначает группу незамещенного или замещенного этинилфенила, при этом возможный заместитель в этинильной группе выбирают из С1-C4-алкила, С1-C4-алкокси, С1-С2-галоидалкила, С1-С2-галоидалкокси; фтора, хлора, брома, йода; нитро, циано; фенила, который не замещен или замещен до 3 раз (где заместители фенила выбирают из С1-C4-алкила, С1-C4-алкокси, С1-C4-галоидалкила, C1-C4-галоидалкокси, гидроксила, галогена, нитро и циано); С1-C4-гидроксиалкила, который может быть O-алкилированным(С1-C4); С1-C4-алкоксикарбонила; N-метил-N-метоксикарбамоила и незамещенного или замещенного С2-С5-алкенила, возможные заместители которого выбирают из галогена и С1-С2-алкокси.
14. Соединение по п.11, отличающееся тем, что R3 обозначает группу незамещенного или замещенного этинилфенила, при этом заместитель в этинильной группе означает пяти- или шестичленное кольцо гетероарила, которое не замещено или замещено до трех раз галогеном, циано, С1-С4-алкилом, С1-C4-алкокси или гидроксилом.
15. Соединение по п.14, отличающееся тем, что кольцо гетероарила выбирают из пиридина, пиримидина, пиразина, пиридазина, триазина, (изо)тиазола, (изо)оксазола, пиррола, пиразола, имидазола, триазола и тиофена, и оно не замещено или замещено заместителями в количестве до 3, выбранными из метила, этила, изопропила, CN, галогена, метокси и гидроксила.
16. Соединение по п.13, отличающееся тем, что заместитель в этинильной группе выбирают из С1-С4-алкила, С1-C4-алкокси, С1-С2-галоидалкила, С1-С2-галоидалкокси; хлора, брома, йода; нитро, циано; С1-С4-гидроксиалкила, который может быть О-алкилированным(С1-С4); С1-С4-алкоксикарбонила; N-метил-N-метоксикарбамоила и незамещенного или замещенного С2-С5-алкенила, возможные заместители которого выбирают из галогена и метокси.
17. Соединение по п.12, отличающееся тем, что R3 обозначает группу незамещенного или замещенного 3- или 4-(С2-C4-алкинил) фенила.
18. Соединение по п.1, отличающееся тем, что двойная связь Х=С имеет Е-конфигурацию.
19. Соединение по п.11, отличающееся тем, что R4 обозначает метил и R3 обозначает 4-этинилфенил.
20. Соединение по п.14, отличающееся тем, что R4 обозначает метил и R3 обозначает 4-(пиразинилэтинил) фенил.
21. Соединение по п.14, отличающееся тем, что R4 обозначает метил и R3 обозначает 4-(пиридилэтинил) фенил.
22. Соединение по п.21, отличающееся тем, что R3 обозначает 4-(3'-пиридилэтинил) фенил.
23. Соединение по п.14, отличающееся тем, что R4 обозначает метил и R3 обозначает 4-(5'-пиримидинилэтинил) фенил.
Текст
1 Настоящее изобретение относится к производным O-бензилового эфира оксима общей формулы I и их возможным изомерам и смесям изомеров,где а) Х обозначает атом азота и Y обозначает атом кислорода или NH, или б) Х обозначает СН и Y обозначает атом кислорода, R1 обозначает С 1-С 4-алкил;R3 обозначает С 1-С 6-алкокси, который не замещен или замещен 1-5 атомами галогена,замещенный или незамещенный арилокси, C1C6-алкилтио, который не замещен или замещен 1-5 атомами галогена, замещенный или незамещенный арилтио, замещенный или незамещенный гетероарилокси, замещенный или незамещенный гетероарилтио, замещенный или незамещенный аралкил, замещенный или незамещенный бифенил, замещенный или незамещенный С 2-С 4-алкинилфенил, замещенный или незамещенный гетероарилметил; и R4 обозначаетC1-C6-алкил, C1-С 6-галоидалкил, имеющий от 1 до 5 атомов галогена; С 1-С 4-алкокси-С 1-С 2 алкил, С 2-С 6-алкенил, который не замещен или замещен 1-3 атомами галогена; С 2-С 6-алкинил,С 3-С 6-циклоалкил-С 1-С 4-алкил, который не замещен или замещен 1-4 атомами галогена; причем R3 имеет значение иное, чем дихлорбензил,когда одновременно R1 обозначает метил, R2 обозначает водород, Х обозначает СН, Y обозначает кислород и R4 обозначает С 1-С 4-алкил. Соединения в соответствии с настоящим изобретением обладают микробицидными, акарицидными и инсектицидными свойствами и могут быть использованы в сельском хозяйстве в качестве сельскохозяйственно-активных ингредиентов. Изобретение также относится к способу получения соединений в соответствии с изобретением и к фунгицидным, акарицидным и инсектицидным композициям, содержащим такие соединения в качестве активных ингредиентов,а также к использованию таких соединений и композиций для борьбы с фитопатогенными грибками, акаридами и насекомыми и для предотвращения подобного заражения. Когда соединения формулы I содержат асимметрические атомы углерода, соединения могут находиться в оптически активной форме. Вследствие присутствия алифатических двойных связей и оксимино двойных связей соединения в любом случае могут быть в [Е] и/или[Z] формах. Может встречаться атропный изомеризм. Предполагается, что формула I охватывает все эти возможные изомерные формы, а 2 также их смеси, например рацемические смеси и любые желательные смеси [E/Z]. В зависимости от числа атомов углерода,группы алкила и алкокси являются прямоцепочечными или разветвленными. Алкильные радикалы в этих группах обозначают, например,метил, этил, н-пропил, изопропил, н-бутил,втор.-бутил, изобутил, трет.-бутил, н-пентил,неопентил, втор.-пентил, трет.-пентил, н-гексил и так далее. Циклоалкил обозначает циклопропил, циклобутил, циклопентил или циклогексил. Алкенил обозначает прямоцепочечный или разветвленный алкенил, например винил, 1 метилвинил, аллил, 1-бутенил, изопропенил. Алкинил обозначает, например, этинил, 1 пропинил или 1-бутинил. С 2-C4-алкинилфенил обозначает алкинил, связанный с остаточной молекулой через группу фенила.C4 алкинилфенил включает 1,3-бутади-1 инилфенил. Галоген обозначает фтор, хлор, бром или йод, предпочтительно фтор, хлор или бром. Галоидалкил может содержать идентичные или различные атомы галогена. Заместители арилокси, арилтио, гетероарилокси, гетероарилтио, аралкила, гетероарилметила, бифенила и С 2-C4-алкинилфенила, являются, где это подходит, inter alia, С 1-C4-алкил,С 1-С 4- алкокси, С 1-C4-галоидалкил (особенноCF3), С 1-C4-галоидалкокси (особенно OCF3), С 1C4-алкилтио, галоген, нитро, циано, С 1-C4 алкилсульфинил, С 1-C4-алкилсульфонил. Другими заместителями, особенно в радикале алкинила группы замещенного или незамещенного С 2-C4-алкинилфенила, являются замещенный или незамещенный фенил, пиридоил или бензоил (причем заместителями на этих шестичленных кольцах могут быть С 1-C4-алкил, С 1-С 4 алкокси, С 1-С 4-галоидалкил (особенно CF3), С 1C4-галоидалкокси (особенно OCF3), С 1-С 4 алкилтио, галоген, нитро, циано, С 1-C4 алкилсульфинил, С 1-C4-алкил-сульфонил), а также свободный или С 1-C4-ацилированный илиN-(С 1-C4-алкил)-N-С 1-C4-алкоксикарбамоил; незамещенный или галоидзамещенный циклопропилоксикарбонил или С 2-С 5-алкенил,который не замещен или замещен С 2-C4-алкокси и/или галогеном; а также пяти- или шестичленный гетероарил, который может быть не замещен или замещен одним или более заместителями из числа галогена, циано, гидроксила, а также алкила, алкенила, алкокси, алкенилокси или алкинилокси, которые имеют в каждом случае до 4 атомов углерода. Каждый заместитель может независимо от других присутствовать от 1 до 3 раз. Арил обозначает фенил или нафтил, предпочтительно фенил. 3 Термин гетероарил включает, inter alia, 5 или 6-членные ароматические кольца, имеющие от 1 до 3 идентичных или различных гетероатомов, выбранных из группы, состоящей из N, О иS, с которыми, при желании, может быть конденсировано бензольное кольцо. Примерами являются пиридин, пиримидин, пиразин, пиридазин, триазин, хинолин, изохинолин, хиназолин, хиноксалин, бензотиазол, бензоксазол, 1 метилимидазол, 1-метилтетразол, 4-метил-1,2,4 триазол. В заявке на европейский патент ЕР 0414153 и в заявке на патент РСТ WO 90/07493 раскрыты аналогичные соединения, которые используются в качестве фунгицидов. Соединения формулы I в соответствии с настоящим изобретением полезны в качестве фунгицидов и инсектицидов. Наличие сдвоенной оксимной боковой цепи в структуре соединения делает молекулу более стабильной. Важная подгруппа соединений включает те соединения формулы I, в которых R3 обозначает С 1-C6-алкокси, С 1-С 4-галоидалкокси, замещенный или незамещенный фенокси, C1-C6 алкилтио, который не замещен или замещен 1-3 заместителями, выбранными из галогена, С 1-C4 алкила, С 1-С 4 -алкокси, CF3 и замещенного фенилтио; или обозначает незамещенный или в каждом случае галоидзамещенный пиридилокси, пиримидинилокси, хинолилокси, хиназолинилокси или хиноксазолинил; или обозначает незамещенный или С 1 -C4-алкил- или галоидзамещенный радикал бензотиазолилтио, бензоксазолилтио, имидазолилтио или тетразолилтио; или обозначает дифенил, С 2-С 4-алкинилфенил,бензил или нафтилметил, который не замещен или замещен 1-3 заместителями, выбранными из галогена,С 1-C4-алкила, С 1-C4-алкокси, СF3 и CN;R4 обозначает С 1-С 6-алкил, C1-C6-галоидалкил, незамещенный или галоидзамещенный С 2-C4-алкенил, С 3-C4-алкинил, незамещенный или галоидзамещенный циклопропилметил, тогда как X, Y, R1 и R2 имеют значения, определенные для формулы I. Среди только что упомянутых соединений предпочтительны те, в которых R1 обозначает метил, R2 обозначает водород, метил или циклопропил, тогда как X, Y, R3 и R4 имеют определенные выше значения. В контексте предлагаемого изобретения предпочтительны следующие комбинации заместителей. 1) Cоединения формулы I, в которых: Х обозначает СН или N, Y обозначает кислород, R1 обозначает метил или этил, R2 обозначает метил или циклопропил, тогда как R3 иR4 имеют определенные для формулы I значения. 2) Соединения формулы I, в которых: Х обозначает азот, Y обозначает NH, R1 обозначает метил, этил или изопропил, R2 обозначает метил или циклопропил, тогда как R3 иR4 имеют определенные для формулы I значения. 3) Соединения формулы I, в которых:R1 обозначает метил, R2 обозначает метил,R4 обозначает С 1-С 6-алкил, тогда X, Y и R3 имеют определенные для формулы I значения. 4) Соединения формулы I, в которых:R1 обозначает метил, R2 обозначает метил,R3 обозначает замещенный или незамещенный С 1-С 6-алкокси или замещенный или незамещенный С 1-С 6-алкилтио, тогда X, Y и R4 имеют определенные для формулы I значения. 5) Соединения формулы I, в которых:R1 обозначает метил, R2 обозначает метил,R3 обозначает замещенный или незамещенный арилокси или замещенный или незамещенный арилтио, тогда X, Y и R4 имеют определенные для формулы I значения. 6) Соединения формулы I, в которых:R1 обозначает метил, R2 обозначает метил,R3 обозначает замещенный или незамещенный гетероарилокси или замещенный или незамещенный гетероарилтио, тогда X, Y и R4 имеют определенные для формулы I значения. 7) Соединения формулы I, в которых:R1 обозначает метил, R2 обозначает метил,R3 обозначает замещенный или незамещенный бензил или замещенный или незамещенный гетероарилметил, тогда X, Y и R4 имеют определенные для формулы I значения. 8) Соединения формулы I, в которых:R1 обозначает метил, R2 обозначает метил,R3 обозначает замещенный или незамещенный бифенил или замещенный или незамещенный С 2-С 4-алкинилфенил, тогда X, Y и R4 имеют определенные для формулы I значения. 9) В пределах только что упомянутой подгруппы 8) предпочтительны те соединения, в которых R4 обозначает метил, этил или аллил,R3 обозначает группу незамещенного или замещенного С 2-C4-алкинилфенила, в которой возможный заместитель находится в алкинильной группе и обозначает C1-C4-алкил, С 1-C4-алкокси,С 1-С 4-галоидалкил (особенно CF3), С 1-С 4-галоидалкокси (особенно OCF3), С 1-C4-алкилтио,галоген, нитро, циано, C1-C4-алкилсульфинил,С 1-C4-алкилсульфонил, незамещенный или замещенный фенил (где заместители фенила выбирают из С 1-C4-алкила, С 1-C4-алкокси, гидроксила,С 1-C4-галоидалкила,С 1-C4-галоидалкокси, С 1-C4-алкилтио, галогена, нитро и циано); С 1-C4-гидроксиалкил, который может бытьO-алкилированным(С 1-C4); С 1-C4-алкоксикарбонил, карбамоил, N-(С 1-C4-алкил)карбамоил, N,N-ди(С 1-C4 алкил)карбамоил, N-С 1-С 4-алкил-N-С 1-С 4-алкоксикарбамоил; незамещенный или галоидзамещенный циклопропилметоксикарбонил, незамещенный C1-C4-алкоксизамещенный или галоидзамещенный С 2-С 5-алкенил, и пяти- или шестичленное кольцо гетероарила, которое не замещено или замещено галогеном, циано, гидро 5 ксилом, а также алкилом, алкенилом, алкокси,алкенилокси или алкинилокси, каждый из которых содержит не более 4 атомов углерода. 10) Среди соединений подгруппы 9) важную группу составляют те, в которых R3 обозначает группу незамещенного или замещенного этинилфенила, при этом возможный заместитель в этинильной группе выбирают из С 1-С 4 алкила, С 1-С 4-алкокси, С 1-С 2-галоидалкила, С 1 С 2-галоидалкокси; фтора, хлора, брома, йода; нитро, циано; фенила, который не замещен или замещен до 3 раз (где заместители фенила выбирают из С 1-C4-алкила, С 1-C4-алкокси, C1-C4 галоидалкила, С 1-C4-галоидалкокси, гидроксила,галогена, нитро и циано); С 1-C4-гидроксиалкила, который может быть O-алкилированным(С 1-C4); С 1-C4-алкоксикарбонила; N-метил-N-метоксикарбамоила и незамещенного или замещенногоC2-C5 алкенила, возможные заместители которых выбирают из галогена и С 1-С 2-алкокси. 11) Среди соединений подгруппы 9) другую важную группу составляют те, в которых R3 обозначает группу незамещенного или замещенного этинил-фенила, при этом заместитель в этинильной группе означает пяти- или шестичленное кольцо гетероарила, которое не замещено или замещено до трех раз галогеном (например, хлором или бромом), циано, С 1-C4 алкилом (например, метилом, этилом, изопропилом), С 1-C4-алкокси (например, метокси) или гидроксилом. 12) Среди только что упомянутых соединений гетероарилэтинилфенила, которые входят в подгруппу 11), предпочтительными являются те, в которых кольцо гетероарила выбирают из пиридина, пиримидина, пиразина, пиридазина,триазина, (изо)тиазола, (изо)оксазола, пиррола,пиразола, имидазола, триазола и тиофена, и которое не замещено или замещено до 3 заместителей, выбранных из метила, этила, изопропила,CN, галогена (особенно хлора), метокси и гидроксила. Производные, имеющие радикалы незамещенного, одно- и двузамещенного гетероарила, являются важной группой активных компонентов. Они включают производные пиразинилэтинилфенила и пиридинилэтинилфенила и другие. 13) В пределах подгруппы 10) предпочтительными активными веществами являются те соединение, в которых заместитель в этинильной группе выбирают из С 1-C4-алкила (например, метила, этила, изопропила, н-бутила), С 1 С 4-алкокси (например, метокси, этокси), С 1-С 2 галоидалкила(например,CF3),С 1-С 2 галоидалкокси (например, OCF3); хлора, брома,йода; нитро, циано; C1 -C4-гидроксиалкила, который может быть O-алкилированным(С 1-C4) 6 или замещенного С 2-С 5-алкенила (например,аллила, металлила, бутенила), возможные заместители которого выбирают из галогена (например, хлора) и метокси. Важными соединениями в качестве активных компонентов и промежуточных продуктов в этой только что упомянутой группе являются,например, те, в которых RЗ обозначает группу гидроксиалкилэтинилфенила. 14) Кроме того, предпочтительными соединениями формулы I являются те, в которых двойная связь Х=С имеет Е-конфигурацию. Предпочтение также подходит ко всем подгруппам, упомянутым выше в отдельности. 15) В соединениях группы 9) и ее производных подгруппах одной из предпочтительных подгрупп является та, в которой заместитель R3 обозначает группу незамещенного или замещенного 3- или 4-(С 2-C4-алкинил) фенила, то есть радикал замещенного или незамещенного С 2-С 4-алкинила присоединен к молекуле через фенильное кольцо в мета- или пара-положении. Предпочтительные отдельные соединения включают соединения 1.1, 1.6, 1.8, 1.12, 1.13,1.15, 1.28, 1.55, 1.56, 1.68, 1.77, 1.85, 1.87, 1.88;2.1, 2.6, 2.8, 2.12, 2.13, 2.15, 2.28, 2.55, 2.56,2.68, 2.77, 2.85, 2.87, 2.88;3.1, 3.6, 3.8, 3.12,3.13, 3.15, 3.28, 3.55, 3.56, 3.68, 3.77, 3.85, 3.87,3.88, упомянутые ниже, а также соединения из таблиц 4 и 4 а. А) Соединение формулы I, в котором X, Y,R1, R2, R3 и R4 имеют определенные для формулы I значения, можно получить следующим образом. Оксим общей формулы II где R2-R4 имеют вышеприведенные значения,подвергают взаимодействию с соединением общей формулы III где X, Y и R1 имеют вышеприведенные значения, a U обозначает отщепляемую группу. Эта реакция представляет собой нуклеофильное замещение, которое можно осуществить при обычных для таких реакций условиях. Отщепляемая группа U, присутствующая в соединении формулы III, предпочтительно обозначает хлор, бром, йод, мезилокси, бензолсульфонилокси, нитробензолсульфонилокси или тозилокси. Реакцию проводят преимущественно в инертном органическом разбавителе, таком как циклический эфир, например тетрагидрофуран или диоксан, ацетон, ацетонитрил, диметилформамид или диметилсульфоксид, в при 7 сутствии основания, такого как гидрид натрия,карбонат натрия или калия, амид натрия, третичный амин, например, триалкиламин, особенно диазабициклононан или диазабициклоундекан, или оксид серебра, при температуре от -20 до +80 С, предпочтительно при температуре от 0 до 50 С. Альтернативно, реакцию можно проводить при комнатной температуре в присутствии межфазного катализатора в органическом растворителе, таком как, например, толуол, в присутствии водного основного раствора, например, раствора гидроксида натрия, и межфазного катализатора, такого как кислый сульфат тетрабутиламмония. Б) Для получения соединения формулы I, в которой Y-R1 обозначает NH (С 1-C4-алкил), соединение формулы I, в которой Y-R1 Y обозначает OCH3, подвергают взаимодействию, например, с C1-С 4-алкиламином, например, метиламином. Взаимодействие целесообразно осуществлять в этаноле, который уже использовался в качестве растворителя для алкиламинов,при температуре от 0 до 40 С, предпочтительно при комнатной температуре. Полученные таким образом соединения формулы I можно выделить и очистить известными per se методами. Полученные смеси изомеров, например смеси изомеров E/Z, можно выделить в чистые изомеры также известнымиper se методами, например хроматографией или фракционной кристаллизацией. Оксимы общей формулы II, используемые в качестве исходных веществ, получают путем взаимодействия кетона общей формулы IV с гидроксиламином или одной из его солей, например гидрохлоридом. Взаимодействие целесообразно осуществлять в пиридине или метаноле в качестве растворителя, причем при использовании метанола необходимо основание,например карбонат щелочного металла, такой как карбонат калия, третичный амин, такой как триэтиламин или диазабициклононан, пиридин или оксид серебра, при температуре от -20 С до+80 С, или при температуре кипения метанола,предпочтительно при температуре от 0 до 50 С. Кетоны общей формулы IV либо известны,либо могут быть получены известными per se методами (например, заявка на европейский патент ЕР 56161; Arthur F.Ferris, J. Org. Chem. 24, 1726, 1959; и J. Irrure Perez и др., An. Quim. 75, 958, 1979). Новые соединения формул II и IV также составляют предмет настоящего изобретения. Исходные соединения формулы III также могут быть получены известными per se методами, например, как описано в опубликованной заявке на европейский патент ЕР 203606 и в 8 литературе, цитируемой в данной работе, или в журнале Angew. Chem. 71, 349-365, 1959. В) Для получения соединения формулы I, в которой X, Y, R1, R2 и R4 имеют определенные для формулы I значения, a R3 обозначает замещенный или незамещенный бензил или замещенный или незамещенный гетероарилметил,или замещенный или незамещенный бифенил или замещенный или незамещенный С 2-C4 алкинилфенил, оксим общей формулы V в которой X, Y, R1, R2 и R3 имеют определенные выше значения, подвергают взаимодействию с соединением общей формулыU - R4 ,VI где R4 имеет значения, определенные для формулы I, a U имеет значения, определенные для формулы III. Реакция представляет собой нуклеофильное замещение, как описано в разделе А). В.а) Для получения оксима формулы V, в которой значения X, Y, R1, R2 и R3 определены в разделе В),кетон общей формулы VII в которой значения X, Y, R1, R2 и R3 определены выше, подвергают взаимодействию с гидроксиламином или одной из его солей, например гидрохлоридом. Взаимодействие целесообразно осуществлять в пиридине или метаноле в качестве растворителя, причем при использовании метанола необходимо основание, например,карбонат щелочного металла, такой как карбонат калия, третичный амин, такой как триэтиламин или диазабициклононан, пиридин или оксид серебра, при температуре от -20 до +80 С,или при температуре кипения метанола, предпочтительно при температуре от 0 до 50 С. Получение кетона общей формулы VII осуществляют аналогично методу, описанному в разделе А). Аналогичные кетоны и их получение описаны, например, в заявке на европейский патент ЕР 370629, заявке на европейский патент ЕР 506149, заявке на европейский патент ЕР 403618, заявке на европейский патент ЕР 414153, заявке на европейский патент ЕР 463488, заявке на европейский патент ЕР 472300, заявке на европейский патент ЕР 460575, международной заявке РСТWO 92/18494 и других. Г) Соединение формулы I, где X, Y и R-R4 имеют значения, определенные для формулы I, 9 можно получить метилированием енола или оксима общей формулы VIII где X, Y и R-R4 имеют значения, определенные выше, с помощью метилирующего агента, например метилиодида, диметилсульфата или диазометана. Реакцию целесообразно осуществлять в присутствии основания, такого как карбонат калия или гидрид натрия, в пригодном растворителе и при пригодной температуре реакции (см., например, H.S.Anker и H.T.Clarke,Organic Synthesis, Coll. vol.3, 172). Г.а) Соединение формулы VIII, где X, Y иR-R4 имеют значения, определенные для формулы I, a R3 имеет значение иное, чем "замещенный или незамещенный бензил" и "замещенный или незамещенный гетероарилметил",также можно получить путем нитрозирования производного фенилуксусной кислоты формулы где Y и R1-R4 имеют определенные выше значения, с использованием сложного эфира муравьиной кислоты (например, НСООСН 3), в присутствии основания, аналогично методу, описанному в заявке на европейский патент ЕР 178826(X = СН), или из соединения IX, используя азотистую кислоту HONO или сложный эфир азотистой кислоты, в присутствии основания или кислоты, аналогично методу, описанному в заявке на европейский патент ЕР 254426 А. Соединение формулы I может быть получено из соединения VIII, как описано в разделе Г), путем метилирования. Г.б) Другая возможность синтеза соединения формулы I состоит в следующей реакции: Сложный кетоэфир формулы Х где Y и R1-R4 имеют значения, определенные для формулы I, подвергают взаимодействию с метоксиметилентрифенилфосфораном аналогично методу, описанному в заявке на европейский патент ЕР 178826 А, или с 0 метилгидроксиламином (или его солью) аналогично методу, описанному в заявке на европейский патент ЕР 254426 А. 10 Новые соединения формул VII, VIII, IX и Х также составляют предмет настоящего изобретения. Обнаружено, что соединения формулы I имеют микробицидный спектр, который благоприятен для практических требований при борьбе с фитопатогенными микроорганизмами,особенно грибками. Они обладают чрезвычайно полезными лечебными, превентивными и в особенности системными свойствами, и могут быть использованы для защиты целого ряда растений. При использовании активных ингредиентов формулы I паразиты, встречающиеся на растениях или частях растений (плоды, цветы, листва, стебли, клубни, корни) различных сельскохозяйственных культур, могут сдерживаться или уничтожаться при одновременной защите от фитопатогенных микроорганизмов, которые развиваются впоследствии на частях растений. Соединения формулы I также могут быть использованы в качестве протравителя для обработки семян (плодов, клубней, зерен) и черенков растений, то есть для обработки материала разведения всех типов, для защиты от грибкового заражения и от фитопатогенных грибков, которые встречаются в почве. Соединения формулы I эффективны, например, в отношении следующих классов фитопатогенных грибков: Fungi imperfecti (особенноBasidiomycetes (например, Rhizoctonia, Hemileia,Puccinia); Ascomycetes (например, Venturia, Erysiphe, Podosphaera, Monilinia, Uncinula); но особенно в отношении Oomycetes (например, Phytophthora, Peronospora, Bremia, Pythium, Plasmopara). Соединения формулы I также обладают инсектицидным и акарицидным действием, особенно против жалящих и сосущих насекомых, а также против вредителей отряда Acarina. В пределах объема настоящего изобретения раскрываются следующие виды растений(даны в качестве примера), для которых используется фитозащита: зерновые (пшеница, ячмень,рожь, овес, тритикале, рис, кукуруза, сорго и родственные виды); свекловичные культуры(тыква пепо, огурцы, дыни); прядильные растения (хлопчатник, лен, конопля посевная, джут круглоплодный); цитрусовые (апельсины, лимоны, грейпфрут, мандарины); овощные культуры (шпинат, кочанный салат, спаржа, капуста,морковь, лук, томаты, картофель, стручковый перец); семейство лавровых (авокадо, коричное дерево, камфора) и такие растения, как табак, 11 орехи, кофе, сахарный тростник, чай, перец и другие пряные растения, виноград, хмель, баклажаны, банановые, каучуковые растения, а также цветы и декоративные растения. Активные ингредиенты соединений формулы I обычно используются в форме комбинаций и могут применяться одновременно или последовательно с другими активными компонентами в отношении обрабатываемых растений или площадей, на которых они произрастают. Этими другими активными компонентами могут быть удобрения, вещества, поставляющие микроэлементы или другие препараты, которые оказывают влияние на рост растений. В этой связи также можно использовать селективные гербициды, а также инсектициды, фунгициды,бактерициды, нематициды, моллюскициды или смеси двух или более таких препаратов, если желательно, то с дополнительными носителями,поверхностно-активными веществами или иными стимулирующими добавками, которые являются традиционными в технологии приготовления препаратов и которые не оказывают отрицательного воздействия на соединения формулы I. Пригодные носители и добавки могут быть твердыми или жидкими и соответствовать веществам, применение которых целесообразно в технологии приготовления препаратов и примерами которых могут быть натуральные или регенерированные минеральные вещества, растворители, диспергаторы, смачивающие вещества, вещества для повышения клейкости, загустители, связующие или удобрения. Пригодными растворителями являются ароматические углеводороды, предпочтительно фракции С 8-С 12, например, смеси ксилола или замещенные нафталины, сложные эфиры фталевой кислоты, такие как дибутилфталат или диоктилфталат, алифатические углеводороды, такие как циклогексан или парафины, спирты и гликоли, а также их простые и сложные эфиры,такие как этанол, этиленгликоль, монометиловый эфир или моноэтиловый эфир этиленгликоля, кетоны, такие как циклогексанон, сильно полярные растворители, такие как N-метил-2 пирролидон, диметилсульфоксид или диметилформамид, а также, если желательно, эпоксидированные растительные масла, такие как эпоксидированное кокосовое масло или соевое масло, либо вода. Твердые носители, которые, как правило,используются, например, для дустов и диспергируемых порошков, включают натуральные грунтовые минералы, такие как кальцит, тальк,монтмориллонит или аттапульгит. Особенно предпочтительными стимулирующими добавками, которые могут привести к значительно пониженной дозе внесения, являются натуральные (животные или растительные) или синтетические фосфолипиды из ряда 12 цефалинов и лецитинов, которые могут быть получены, например, из сои культурной. Пригодными поверхностно-активными веществами, в зависимости от природы активного компонента формулы I, входящего в состав, являются неионные, катионные и/или анионные поверхностно-активные вещества, которые обладают хорошими эмульгирующими,диспергирующими и смачивающими свойствами. Термин поверхностно-активные вещества следует понимать как включающий в себя смеси поверхностно-активных веществ. Пригодными анионными поверхностноактивными веществами могут быть так называемые водорастворимые мыла и также водорастворимые синтетические поверхностноактивные соединения. Мылами являются соли щелочных металлов, соли щелочно-земельных металлов или замещенные или незамещенные аммониевые соли высших жирных кислот (C10-C22), например натриевые соли или калиевые соли олеиновой или стеариновой кислоты, или смеси натуральных жирных кислот, которые могут быть получены, например, из кокосового масла или животного масла. Следует также упомянуть метилтауриновые соли жирных кислот. Возможными неионными поверхностноактивными веществами являются производные полигликолевого эфира алифатических или циклоалифатических спиртов, насыщенных или ненасыщенных жирных кислот и алкилфенолов,которые могут содержать от 3 до 30 групп гликолевого эфира и от 8 до 20 атомов углерода в алифатическом углеводородном радикале и от 6 до 18 атомов углерода в алкильном радикале алкилфенолов. Примерами неионных поверхностноактивных веществ являются нонилфеноксиполиэтоксиэтанолы,полигликолевые эфиры касторового масла, аддукты полипропилен- и полиэтиленоксида, трибутилфеноксиполиэтоксиэтанол, полиэтиленгликоль и октилфеноксиполиэтоксиэтанол. Также пригодны сложные эфиры полиоксиэтиленсорбита и жирных кислот, такие как триолеатполиоксиэтиленсорбита. Катионные поверхностно-активные вещества включают, в частности, соли четвертичного аммониевого основания, которые в качестве Nзаместителей содержат, по крайней мере, один алкильный радикал, имеющий от 8 до 22 атомов углерода, а в качестве других заместителей содержат радикалы низшего незамещенного или галогенированного алкила, радикалы бензила или радикалы низшего гидроксиалкила. Анионные, неионные или катионные поверхностно-активные вещества, известные в области технологии приготовления композиций,знакомы среднему специалисту в данной области или могут быть почерпнуты из соответствующей технической литературы:[Surfactant Handbook], Carl Hanser Verlag, Munich/Vienna, 1981. Как правило, агрохимические препараты обычно содержат от 0,1 до 99%, предпочтительно от 0,1 до 95%, активного компонента формулы I, от 99,9 до 1%, предпочтительно от 99,9 до 5, твердой или жидкой добавки и от 0 до 25%,предпочтительно от 0,1 до 25%, поверхностноактивного вещества. В то время как коммерческие продукты предпочтительно составлены в виде концентрированных композиций, конечный пользователь обычно применяет разбавленные композиции. Композиции в соответствии с настоящим изобретением также могут включать в себя другие добавки, такие как стабилизаторы, противовспениватели, регуляторы вязкости, связующие,вещества для повышения клейкости и удобрения, а также другие активные ингредиенты для достижения специальных эффектов. Составы, то есть композиции, препараты или комбинации, содержащие активный компонент формулы I и, если желательно, твердую или жидкую добавку, получают известным способом, например, путем однородного смешивания и/или растирания активного компонента с наполнителем, например, с растворителем (смесью), твердым носителем и, если желательно,поверхностно-активными веществами (или сурфактантами). Предпочтительный метод применения активного компонента формулы I или агрохимической композиции, содержащей, по крайней мере, один из числа этих активных компонентов, заключается в нанесении на листву (некорневое нанесение). Частота и доза внесения зависят в этом случае от уровня разрушения в результате нападения рассматриваемого болезнетворного организма. Однако активные компоненты формулы I также могут достигать растение через корневую систему (системное действие), путем пропитки локуса растения жидким препаратов или путем введения веществ в твердой форме в почву, например, в форме гранул(почвенное внесение). В случае рисовых культур, такие гранулы можно добавлять в затопленное рисовое поле. Для обработки семян соединения формулы I также могут быть нанесены на ядра семена (покрытие) либо путем пропитки ядер зерен жидким составом активного компонента, либо путем их покрытия твердым составом. В принципе, любой тип материала для размножения растений может быть защищен с использованием соединений формулы I, и примерами являются семена, корни, стебли, 000417 14 мерами являются семена, корни, стебли, ветви,побеги или ростки. В данном контексте соединения формулы I используются в немодифицированном виде или предпочтительно вместе с адъювантами, традиционно применяемыми в технологии приготовления препаратов. Для этой цели их целесообразно перерабатывать известным способом, например, получая эмульгируемые концентраты,пасты, предназначенные для покрытия, непосредственно распыляемые или разбавляемые растворы, разбавленные эмульсии, смачиваемые порошки, растворимые порошки, дусты, гранулы и инкапсулированные формы (например, в полимерных веществах). Методы применения,такие как разбрызгивание, распыление, опудривание, рассеивание, разбрасывание или выливание, выбирают в соответствии с предполагаемыми задачами и преобладающими обстоятельствами. Благоприятные дозы внесения обычно составляют от 1 г до 2 кг активного компонента(а.к.) на гектар, предпочтительно от 25 до 800 г а.к. на гектар, наиболее предпочтительно от 50 до 400 г а.к. на гектар. В случае использования для протравления семян дозы внесения, как правило, составляют от 0,001 до 1,0 г активного компонента на 1 кг семян. Следующие примеры предназначены для более подробной иллюстрации изобретения без какого-либо ограничения его объема. 1. Примеры получения Пример Н-1. Получение соединения 0,22 г 60% дисперсии гидрида натрия промывают гексаном и обрабатывают 5 мл N,Nдиметилформамида. К этой суспензии добавляют 1,43 г метил 2-(-бром-о-толил)-3-метоксиакрилата и 1,03 г 3-метоксимино-4-фенил-2 бутаноноксима, и реакционную смесь перемешивают в течение 1 ч. Затем добавляют ледяную воду, после чего образовавшееся масло кристаллизуется по истечении короткого периода времени. Кристаллы отфильтровывают отсосом, промывают водой и перекристаллизовывают из этилацетата/гексана. Конечный продукт получают в форме белых кристаллов с температурой плавления 124-126 С (cоединение 1.1). Пример Н-2. Получение соединения 0,36 г 60% дисперсии гидрида натрия промывают гексаном и обрабатывают 10 мл N,N 15 диметилформамида. К этой суспензии добавляют 2,55 г O-метилоксима метил 2-(2 бромметилфенил)-глиоксилата и 1,83 г 3 метоксимино-4-фенил-2-бутаноноксима, и реакционную смесь перемешивают в течение 1 ч. Затем добавляют ледяную воду, после чего образовавшееся масло кристаллизуется по истечении короткого периода времени. Кристаллы отфильтровывают отсосом, промывают водой и перекристаллизовывают из диэтилового эфира/гексана. Конечный продукт получают в форме желтоватых кристаллов с температурой плавления 86-88 С (cоединение 2.1). Пример Н-3: Получение соединения 1,0 г соединения, полученного в примере Н-2, перемешивают при комнатной температуре в течение 2 ч в 5 мл 33% этанольного раствора метиламина. Этанол и избыток метиламина отгоняют и остаток кристаллизуют из диэтилового эфира/гексана. Конечный продукт получают в форме желтоватых кристаллов с температурой плавления 119-120 С (соединение 3.1). Следующие соединения, принадлежащие к ограниченному кругу настоящего изобретения,можно получить подобным образом или аналогично одному из методов, указанных выше. 9,9 г К 2 СО 3 добавляют к раствору 6,2 г 2 гидроксимино-3-(4-этинилфенил)-3-метоксиминопропана и 8,2 г метил 2-(-бром-о-толил)-3 метоксиакрилата в 200 мл ацетонитрила. Реакционную смесь перемешивают при температуре 65 С в течение 6 ч и затем фильтруют, после чего фильтрат упаривают. Маслянистый остаток хроматографируют на силикагеле (гексан/ диизопропиловый эфир/толуол, 2:1:1), получая 9,2 г указанного в заголовке соединения ( 1.88) с температурой плавления 127-129 С. Пример Н-5. Получение соединения в соответствии с примером Н-4, в котором Т = 3 пиридил. 0,3 г иодида меди (1) и 0,8 г Pd(TPP)2Cl2 добавляют к раствору 20 г соединения, полученного в соответствии с примером Н-4, и 10 г 3-иодпиридина в 400 мл триэтиламина и 50 мл тетрагидрофурана. Реакционную смесь перемешивают при температуре 65 С в течение 2 ч и затем фильтруют, после чего фильтрат упаривают. Маслянистый остаток хроматографируютOметилоксим метиламида глиоксиловой кислоты,упомянутый как соединение 3.88 в таблице 3,может быть получен из O-метилоксима метилглиоксилата, полученного в соответствии с примером Н-6 путем взаимодействия с этанольным раствором метиламина. Таблица 1 36 нием гексана. Получают 3-метоксимино-4 фенил-2-бутанон в виде бесцветного масла. б) 5,7 г масла, полученного выше, и 2,8 г гидрохлорида гидроксиламина в 30 мл пиридина перемешивают при температуре 40 С в течение 5 ч. Смесь вливают в ледяную воду, и кристаллы, образовавшиеся в течение ночи из осажденного масла, отфильтровывают. Исходное вещество получают в виде белых кристаллов,температура плавления 94-95 С (Соединение 5.1). Пример Z-2. Получение исходного вещества формулы Соединения 4a.1-4a.105 в этой таблице соответствуют в той же последовательности структурным деталям для X, Y и R3 таблицы 4,содержащей соединения 4.1-4.105. Помимо фунгицидного действия, соединения таблицы 4 а в особенности проявляют инсектицидное и акарицидное действие. Получение промежуточных соединений Пример Z-1. Получение исходного вещества формулы а) 2,6 г 60% дисперсии гидрида натрия промывают гексаном и обрабатывают 50 млN,N-диметилформамида. К этой суспензии порциями добавляют 8,9 г 3-гидроксимино-4 фенил-2-бутанона (получен в соответствии с работой A.F. Ferris, J. Org. Chem. 24, 172, 1959). После завершения выделения водорода смесь охлаждают в ледяной бане, и по каплям добавляют 3,4 мл метилиодида. После перемешивания при комнатной температуре в течение 1 ч смесь вливают в ледяную воду и экстрагируют этилацетатом. После концентрации органической фазы на роторном испарителе остаток хроматографируют на силикагеле с использова 2-Гидроксимино-3-(4-этинилфенил)-3 метоксиминопропан а) 26 мл 3- метил -1-бутин-3-ола и 0,3 г иодида меди (I), а также 0,8 г Pd(TPP)2Cl2 добавляют при перемешивании к раствору 51,5 г 4 бромпропио-фенона в 600 мл триэтиламина. После нагревания до температуры около 65 С реакционную смесь перемешивают в течение 1,5 ч, затем остаток отфильтровывают отсосом и фильтрат упаривают. Оставшееся масло хроматографируют на силикагеле (элюент : диэтиловый эфир). Получают 52 г 4-(3-гидрокси-3 метил-1-бутинил)пропиофенона,температура плавления 56-58 С. б) 3 г порошка NaOH добавляют к раствору 44 г промежуточного соединения, полученного в (а), в 500 мл толуола, и реакционную смесь перемешивают при температуре 100 С в течение 5 ч, затем упаривают, и маслянистый остаток хроматографируют на силикагеле (этилацетат/гексан, 1:5). Получают 26,7 г 4-этинилпропиофенона, температура плавления 65-67 С. в) Газообразный НСl пропускают в раствор 94 г 4-этинилпропиофенона в 1200 мл диоксана в течение 1 мин. Затем добавляют по каплям 90 г изопентилнитрита при перемешивании в течение нескольких минут. Реакционную смесь перемешивают при комнатной температуре в течение 2 ч. После добавления 10 мл триэтиламина твердое вещество отфильтровывают отсосом и фильтрат упаривают. Маслянистый остаток хроматографируют на силикагеле(этилацетат/гексан, 2:7). Получают 89 г 2 гидроксимино-3-(4-этинилфенил)пропан-3-она,температура плавления 131-132 С. г) 8 г гидрохлорида метоксиамина добавляют к раствору 15 г промежуточного соединения, полученного в (в), в 100 мл пиридина. После перемешивания при температуре 100 С в течение 2,5 ч реакционную смесь упаривают и дважды экстрагируют встряхиванием с использованием каждый раз 200 мл диэтилового эфира. Объединенную эфирную фазу дважды промывают каждый раз 100 мл воды,концентрируют и хроматографируют на 37 ют и хроматографируют на силикагеле (гексан/диизопропиловый эфир, 3:1). Получают 8,35 г кристаллов указанного в заголовке соединения, температура плавления 149-151 С (cоединение 5.88). Кроме того, получают 5,8 г Zизомера, температура плавления 111-113 С. Пример Z-3. Получение 2-гидроксимино-3(4-этинилфенил)-3-метоксиминопропана. а) 0,35 г (0,5 ммоль) Pd(TPP)2Cl2 и 0,12 г(0,6 ммоль) иодида меди (I) и с перемешиванными в течение нескольких минут 10,7 г (0,13 ммоль) 1-метил-3-бутин-1-ола добавляют к раствору 21,3 г (0,1 моль) 4-бромфенилацетона в 250 мл триэтиламина. Смесь нагревают до температуры 55 С с последующим ее медленным повышением до 80 С в течение 4 ч. После охлаждения смесь фильтруют и фильтрат концентрируют. Оставшееся масло хроматографируют на силикагеле. Получают 17,4 г (90,3% от теоретического выхода) 4-(3-гидрокси-3-метил-1 бутинил)фенилацетона, температура плавления 67-69 С. б) 11 г (0,2 моль) КОН добавляют к раствору 41 г (0,19 моль) промежуточного соединения, полученного в (а), в 800 мл толуола, и реакционную смесь перемешивают при температуре 85-96 С в течение 35 мин. После фильтрации фильтрат упаривают и маслянистый остаток хроматографируют на силикагеле. Получают 19,6 г (65,2% от теоретического выхода) 4 этинилфенилацетона; Н-ЯМР (CDCl3; 250 МГц): 2,18(с). 3,08(с), 3,71(с), 7,17(м), 7,47(м). в) 8 г Na (0,35 моль) растворяют при комнатной температуре в 300 мл метанола. К этому раствору добавляют 44 г (0,28 моль) 4 этинилфенилацетона, и 34,2 г (0,29 моль) изопентилнитрита добавляют по каплям за несколько минут, в течение которых реакционную смесь нагревают до температуры около 32 С. Затем ее перемешивают в течение 1,5 ч и упаривают. Получают 48,5 г (93,2% от теоретического выхода) 1-гидроксимино-1-(4'-этинилфенил) пропан-2-она; Н-ЯМР: 2,47(с), 3,07(с), 7,20(м),7,48(м), 8,01(с). г) 72,8 г (0,51 моль) метилиодида и 71,6 г(0,32 моль) продукта, полученного в (в), в 500 мл ацетонитрила. Смесь перемешивают при температуре 40-42 С в течение 19 ч, концентрируют до объема около 200 мл и охлаждают, после чего неорганический компонент отфильтровывают. Фильтрат концентрируют далее. Остается 60,7 г (94,6% от теоретического выхода) 1 метоксимино-1-(4'-этинилфенил) пропан-2-она в виде масла; Н-ЯМР: 2,53(с), 3,10(с), 4,07(с),7,27(м), 7,52(м). д) 60,7 г (0,3 моль) 1-метоксимино-1-(4'этинилфенил)пропан-2-она растворяют в 600 мл этанола и обрабатывают 22 г (0,315 моль) гидрохлорида гидроксиламина и 29,4 г (0,372 моль) пиридина. После перемешивания при комнатной температуре в течение 15 ч раствор упари 000417 38 вают и фильтруют, и концентрированный маслянистый фильтрат очищают на силикагеле. Получают 55,3 г (84,7% от теоретического выхода) [Е]-2-гидроксимино-3-(4-этинилфенил)-3 метоксиминопропанона; Н-ЯМР: 1,98 (с),2,90(с), 3,73 (с), 6,98(м), 7,32(м), 8,07(с). Температура плавления 150-151 С (cоединение 5.88). При использовании этого метода соответствующий [Z]-изомер образуется только в очень небольших количествах. Таблица 5 (Промежуточные соединения) 44 2.4. Экструдированные гранулы. Активный компонент из таблицы 1-4 а Лигносульфонат натрия Карбоксиметилцеллюлоза Каолин Активный компонент смешивают с добавками и смесь измельчают и увлажняют водой. Смесь экструдируют и затем сушат в потоке воздуха. 2.5. Гранулы с покрытием. Активный компонент из таблицы 1-4 а Полиэтиленгликоль (ММ 200) Каолин Тонкоизмельченный активный компонент наносят равномерно в смесителе на каолин, увлажненный полиэтиленгликолем. Таким образом получают гранулы с покрытием, не содержащие пыли. 2. Примеры приготовления композиции с активными компонентами формулы I (% = процент по массе). 2.1. Смачиваемый порошок. Активный компонент из таблицы 1-4 а Лигносульфонат натрия Лаурилсульфат натрия Диизобутилнафталинсульфонат натрия Октилфениловый эфир полиэтиленгликоля (7-8 моль оксида этилена) Высокодисперсная кремниевая кислота Каолин Активный компонент тщательно смешивают с добавками и смесь тщательно измельчают в подходящей мельнице. Получают смачиваемые порошки, которые можно разбавить водой с получением суспензий любой желательной концентрации. 2.2. Эмульгируемый концентрат. Активный компонент из таблицы 1-4 а Октилфениловый эфир полиэтиленгликоля (4-5 моль оксида этилена) Додецилбензолсульфонат кальция Циклогексанон Смесь ксилола Эмульсии любой желательной степени разбавления могут быть получены при разбавлении этого концентрата водой. 2.3. Дуст. Активный компонент из таблицы 1-4 а Тальк Каолин Готовые к употреблению дусты получают путем смешивания активного компонента с носителем и измельчения в подходящей мельнице. 2.6. Суспензионный концентрат. Активный компонент из таблицы 1-4 а Этиленгликоль Нонилфениловый эфир полиэтиленгликоля(15 моль оксида этилена) Лигносульфонат натрия Карбоксиметилцеллюлоза 37% водный раствор формальдегида Силиконовые масло в форме 75% водной эмульсии Вода Тонкоизмельченный активный компонент тщательно смешивают с добавками с получением суспензионного концентрата, из которого суспензии с любой желательной степенью разбавления можно получить путем разбавления водой. 3. Биологические примеры Пример В-1. Действие против возбудителей заболевания Phytophthora на растениях томата. а) Лечебное действие. Растения томатов сорта "Roter Gnom" выращивают в течение 3 недель, а затем опрыскивают зооспоровой суспензией грибка и инкубируют в кабине при температуре 18-20 С в насыщенной влагой атмосфере. Увлажнение прерывают через 24 ч. После сушки растений их опрыскивают жидкой смесью, содержащей активный компонент, которая составлена как смачиваемый порошок, при концентрации 200 частей на миллион. После высыхания покровного слоя растения возвращают во влажную кабину на 4 дня. Величину и размер типичной листовой пятнистости, которая проявилась по истечении этого периода, используют для оценки активности испытуемых веществ. б) Превентивно-системное действие. Активный компонент в составе смачиваемого порошка вносят при концентрации 60 частей на миллион (относительно объема почвы) в 45 поверхность почвы трехнедельных растений томатов сорта "Roter Gnom" в горшках. По истечении 3 дней ожидания нижнюю сторону листьев опрыскивают зооспоровой суспензией возбудителей заболевания Phytophthora. Затем растения содержат в течение 5 дней в кабине при температуре 18-20 С в насыщенной влагой атмосфере. По истечении этого периода развивается типичная листовая пятнистость, величина и размер которой используют для оценки активности испытуемых веществ. Если необработанные, но зараженные контрольные растения показывают уровень заражения 100%, то активные компоненты формулы I в соответствии с одной из таблиц 1-3 подавляют заражение в одном или двух тестах до 10% или менее, в частности, такие соединения, как 1.2,1.6, 1.8, 1.28, 1.77, 1.85, 1.88; 2.2, 2.6, 2.8, 2.28,2.55, 2.77, 2.85, 2.88; 3.1, 3.2, 3.6, 3.8, 3.28, 3.77,3.85, 3.88. Огромное большинство соединений из таблицы 4 проявляет исключительно хорошее действие (подавление заражения до уровня от 10% до 0%). Пример В-2: Действие против Plasmoparaviticola (Bert. et Curt.) (Berl. et De Toni) на растениях винограда. а) Остаточное превентивное действие. Виноградные черенки сорта "Chasselas" выращивают в теплице. Когда они достигают фазы распускания 10 листьев, три растения опрыскивают жидкостью с активным компонентом (концентрация 200 частей на миллион). После высыхания покровного слоя растения равномерно заражают, нанося на нижнюю часть листа споровую суспензию грибка. Затем растения содержат во влажной кабине в течение 8 дней. По истечении этого периода заметные симптомы заболевания очевидны на контрольных растениях. Количество и размер сайтов заражения на обработанных растениях используют в качестве шкалы оценки на эффективность испытуемых веществ. б) Лечебное действие. Виноградные черенки сорта "Chasselas" выращивают в теплице и по достижении фазы распускания 10 листьев их заражают путем нанесения на нижнюю сторону листьев споровой суспензии Plasmopara viticola. По истечении 24 ч нахождения во влажной кабине растения опрыскивают жидкостью с активным компонентом (концентрация 200 частей на миллион активного компонента). Затем растения содержат во влажной кабине в течение 7 дней. По истечении этого периода заметные симптомы заболевания очевидны на контрольных растениях. Величину и размер сайтов заражения на обработанных растениях используют в качестве шкалы оценки на эффективность испытуемых веществ. По сравнению с контрольными растениями, заражение растений, обработанных активными компонентами формулы I, составляет 20% 46 или менее. Препараты, упомянутые в тесте В-1,подавляют заражение до уровня от 10% до 0%. Пример В-3. Действие против Pythium debaryanum на растениях сахарной свеклы (Betavulgaris). а) Действие после внесения в почву. Грибок культивируют на стерильных зернах овса и добавляют в смесь грунта и песка. Почву, зараженную таким путем, помещают в цветочные горшки и засевают семенами сахарной свеклы. Сразу же после посева испытуемые препараты в виде смачиваемых порошков выливают на почву в форме водной суспензии (20 частей на миллион активного компонента относительно объема почвы). Затем горшки помещают в теплицу на 2-3 недели при температуре 20-24 С. Все время почву поддерживают равномерно увлажненной путем ее опрыскивания водой. После оценки тестов определяют всхожесть растений сахарной свеклы и отношение здоровых растений к больным. б) Действие после протравливания семян. Грибок выращивают на стерильных зернах овса и добавляют в смесь грунта и песка. Почву,зараженную таким путем, помещают в цветочные горшки и засевают семенами сахарной свеклы, которые были протравлены с помощью испытуемых препаратов в виде порошков для протравливания семян (1000 частей на миллион активного компонента относительно массы семян). Затем горшки помещают в теплицу на 2-3 недели при температуре 20-24 С. Все время почву поддерживают равномерно увлажненной путем ее опрыскивания водой. При оценке тестов определяют всхожесть растений сахарной свеклы и отношение здоровых растений к больным. После обработки активными компонентами формулы I свыше 80% растений всходят и имеют здоровый внешний вид. В контрольных горшках взошли только несколько растений,имеющих нездоровый внешний вид. Пример В-4. Остаточно-защитное действие против Cercospora arachidicola на растениях земляного ореха. Растения земляного ореха высотой 10-15 см опрыскивают водной смесью для опрыскивания (0,02% активного вещества) до скапывания влаги, а через 48 ч заражают конидиевой суспензией грибка. Растения инкубируют в течение 72 ч при температуре 21 С и высокой атмосферной влажности, после чего помещают в теплицу вплоть до появления типичной пятнистости на листьях. Действие активного вещества оценивают через 12 дней после заражения на основе величины и размера пятнистости листьев. Активные компоненты формулы I приводят к заметному снижению пятнистости листьев, приблизительно до уровня менее 10% от площади поверхности листьев. В некоторых случаях болезнь подавляется полностью (0-5% инвазии).graminis на растениях пшеницы. а) Остаточно-защитное действие. Через 6 дней после посева растения пшеницы опрыскивают водной смесью для опрыскивания (0,2% активного вещества) до скапывания влаги, а через 24 ч заражают уредоспоровой суспензией грибка. По истечении периода инкубации, равного 48 ч (условия: относительная влажность атмосферы 95-100% при температуре 20 С), растения помещают в теплицу при температуре 22 С. Развитие телейтопустул(спороношение ржавчинного гриба) оценивают через 12 дней после заражения. б) Системное действие. Через 5 дней после посева растения пшеницы поливают водной смесью для опрыскивания (0,006% активного вещества, на основе объема почвы). Старательно избегают контакта жидкой смеси с наземными частями растений. Через 48 ч растения заражают уредоспоровой суспензией грибка. По истечении периода инкубации, равного 48 ч (условия: относительная атмосферная влажность 95-100% при температуре 20 С), растения помещают в теплицу при температуре 22 С. Развитие телейтопустул(спороношение ржавчинного гриба) оценивают через 12 дней после заражения. Соединения формулы I приводят к заметному снижению объема гибковой инвазии, в некоторых случаях до 10-0%, например, такие соединения, как 1.1, 1.2, 1.6, 1.8, 1.28, 1.55, 1.56,1.68, 1.77, 1.85, 1.87, 1.88; 2.1, 2.2, 2.6, 2.8, 2.28,2.55, 2.56, 2.68, 2.77, 2.85, 2.87, 2.88; 3.1, 3.2, 3.6,3.8, 3.28, 3.55, 3.56, 3.68, 3.77, 3.85, 3.87, 3.88 и другие. Необычайно устойчивое действие проявляется соединениями подгруппы 9) формулыoryzae на растениях риса. а) Остаточно-защитное действие. Растения риса выращивают в течение 2 недель и опрыскивают до скапывания влаги водной смесью для опрыскивания (0,02% активного вещества), а через 48 ч заражают конидиевой суспензией грибка. Грибковую инвазию оценивают через 5 дней после заражения, и в течение этого периода относительную влажность атмосферы поддерживают на уровне 95-100%, а температуру на уровне 22 С. б) Системное действие. Водную смесь для опрыскивания (0,006% активного вещества, на объем почвы) вливают в 2-х недельные растения риса. Старательно избегают контакта жидкой смеси с наземными частями растений. Затем горшки наполняют водой так, чтобы погрузились нижние части стеблей растений риса. Через 96 ч растения заражают конидиевой суспензией грибка и сохраняют в течение 5 дней при относительной влажности 48 атмосферы 95-100% и при температуре 24 С. Соединения формулы I заметно предотвращают вспышку заболевания на зараженных растениях. Пример В-7. Остаточно-защитное действие против Venturia inaequalis на яблонях. Черенки яблонь, имеющие свежие побеги длиной от 10 до 20 см, опрыскивают до скапывания влаги водной смесью для опрыскивания(0,02% активного вещества), а через 24 ч заражают конидиевой суспензией грибка. Растения инкубируют в течение 5 дней при относительной влажности атмосферы на уровне 90-100%, а затем помещают на 10 дней в теплицу при температуре на уровне 20-24 С. Заражение паршой оценивают через 15 дней после инвазии. Соединения формулы I из таблиц 1-3 имеют устойчивое действие против заболеваний,вызванных паршой. Даже более отчетливым является действие соединений подгруппы 9. Пример В-8. Действие против Ervsiphegraminis на растениях ячменя. а) Остаточно-защитное действие. Растения ячменя высотой около 8 см опрыскивают до скапывания влаги водной смесью для опрыскивания (0,2% активного вещества), а через 3-4 ч посыпают конидиевой суспензией грибка. Зараженные растения помещают в теплицу при температуре 22 С. Грибковую инвазию оценивают через 10 дней после заражения. б) Системное действие. Водную смесь для опрыскивания (0,002% активного вещества, на объеме почвы) вливают в растения ячменя высотой приблизительно 8 см. Старательно избегают контакта жидкой смеси с наземными частями растений. Через 48 ч растения посыпают конидиевой суспензией грибка. Зараженные растения помещают в теплицу при температуре 22 С. Грибковую инвазию оценивают через 10 дней после заражения. Соединения формулы I приводят в основном к снижению уровня заболевания до менее чем 20%, а в некоторых случаях полностью исключают заболевание. Это такие соединения,как 1.1, 1.2, 1.6, 1.8, 1.28, 1.55, 1.56, 1.68, 1.77,1.85, 1.87, 1.88; 2.1, 2.2, 2.6, 2.8, 2.28, 2.55, 2.56,2.68, 2.77, 2.85, 2.87, 2.88; 3.1, 3.2, 3.6, 3.8, 3.28,3.55, 3.56, 3.68, 3.77, 3.85, 3.87, 3.88 и другие. Соединения из таблицы 4 отличаются особой эффективностью. Это такие соединения, как,например, соединения 4.13, 4.14, 4.24, 4.27 и другие. Пример В-9. Остаточно-защитное действие против Podosphaera leucotricha на побегах яблонь. Черенки яблонь, имеющие свежие побеги длиной около 15 см, опрыскивают до скапывания влаги водной смесью для опрыскивания(0,06% активного вещества), а через 24 ч обработанные растения заражают конидиевой суспензией грибка. Растения помещают в кабину с регулируемой средой при относительной влажности атмосферы на уровне 70% и при темпера 49 туре 20 С. Грибковую инвазию оценивают через 12 дней после заражения. Активные соединения формулы I подавляют уровень заражения примерно до 20%. Контрольные растения показывают уровень заболевания 100%. Пример В-10. Действие против Botrytis cinerea на плодах яблонь. Остаточно-защитное действие. Яблоки с искусственными порезами обрабатывают наносимой по каплям смесью для опрыскивания (0,02% активного вещества) на порезы. Обработанные плоды затем заражают споровой суспензией грибка и инкубируют при высокой влажности атмосферы и температуре около 20 С в течение 1 недели. Фунгицидное действие испытуемого вещества оценивают по числу порезов, проявляющих признаки гниения. Активные компоненты формулы I из таблиц 1-3 способны предотвращать распространение гниения, а в некоторых случаях полностью предотвращают его. Особенно хорошее действие показано соединениями из таблицы 4 как пример алкинилфениловых соединений подгруппы 9. Пример В-11. Действие против Helminthosporium gramineum. Зерна пшеницы заражают споровой суспензией грибка и сушат. Зараженные зерна протравливают суспензией испытуемого вещества(600 частей на миллион активного компонента,на массу семян). Через 2 дня зерна помещают в пригодные чашки, содержащие агар, и через 4 дня оценивают развитие грибковых колоний вокруг зерен. Количество и размер грибковых колоний используют для оценки активности испытуемого вещества. Соединения формулы I показывают в некоторых случаях хорошее действие, то есть хорошее ингибирование грибковых колоний. Пример В-12. Действие против Colletotrichum lagenarium на огурцах. Растения огурцов выращивают в течение 2 недель, а затем опрыскивают смесью для распыления (концентрация 0,002%). Через 2 дня растения заражают споровой суспензией (1,5 х 105 спор/мл) грибка и инкубируют в течение 36 ч при температуре 23 С и высокой влажности атмосферы. Затем инкубацию продолжают при нормальной влажности атмосферы и температуре около 22-23 С. Проявленную грибковую инвазию оценивают через 8 дней после заражения. Необработанные, но зараженные контрольные растения проявляют грибковую инвазию на уровне 100%. Соединения формулы I показывают в некоторых случаях почти полное ингибирование заболевания. Пример В-13. Действие против Fusariumnivale на ржи посевной. Рожь посевную сорта Tetragell, зараженную Fusarium nivale, протравливают испытуемым фунгицидом, используя смесительный ва 000417 50 лок. При этом пользуются следующими концентрациями: 20 или 5 частей на миллион активного компонента (на массу семян). Зараженную и обработанную рожь сеют в октябре в открытом поле с помощью рядовой сеялки, применяя делянки длиной 3 м с 6 бороздами. На каждую концентрацию используют 3 повтора. До начала оценки инвазии испытуемые растения выращивают в нормальных полевых условиях (предпочтительно в районе, полностью покрытым снегом в течение зимних месяцев). Для оценки фитотоксичности прорастание семян измеряют осенью, тогда как отношение количества растений на площадь к числу побегов на каждое растение измеряют весной. Для определения активности активного компонента, весной, как только снег начинает таять, определяют процент растений, зараженных Fusarium. Количество зараженных растений составляет менее 5% в случае обработки соединением формулы I. Проросшие растения имеют здоровый вид. Пример В-14. Действие против Septorianodorum на пшенице. Растения пшеницы фазы распускания 3 листьев опрыскивают смесью для опрыскивания(600 частей на миллион активного компонента),полученной из смачиваемого порошка активных веществ. Через 24 ч обработанные растения заражают конидиевой суспензией грибка. Затем растения инкубируют в течение 2 дней при относительной влажности атмосферы на уровне 90100% и помещают на 10 дней в теплицу при температуре на уровне 20-24 С. Грибковое заражение оценивают через 13 дней после инвазии. Менее 1% растений пшеницы проявляют заболевание. Пример В-15. Действие против Rhizoctoniasolani на рисе. Защитно-местное внесение в почву. Десятидневные растения риса, содержащиеся в цветочных горшках, поливают суспензией (смесью для распыления), полученной из испытуемого вещества, не затрагивая наземные части растений. Через 3 дня растения заражают,поместив в каждый горшок стебель ячменной соломки, зараженный Rhizoctonia solani, между рисовыми растениями. Через 6 дней инкубации в помещении с регулируемой средой при дневной температуре 29 С и ночной температуре 26 С и относительной влажности атмосферы 95% оценивают грибковую инвазию. Заражено менее 5% растений риса. Растения имеют здоровый вид. Защитно-местное нанесение на листву. Двенадцатидневные растения риса опрыскивают суспензией, полученной из испытуемых веществ. Через 1 день растения заражают,поместив в каждый горшок стебель ячменной 51 соломки, зараженной Rhizoctonia solani, между рисовыми растениями. Через 6 дней инкубации в помещении с регулируемой средой при дневной температуре 29 С и ночной температуре 26 С и относительной атмосферной влажности 95% оценивают грибковую инвазию. Необработанные, но зараженные контрольные растения проявляют грибковую инвазию на уровне 100%. Соединения формулы I показывают в некоторых случаях полное ингибирование заболевания. Инсектицидное действие Пример В-16. Действие против Heliothis virescens. Молодые растения сои культурной опрыскивают жидкой водной эмульсией для опрыскивания, которая содержит 100 частей на миллион активного компонента. Затем, после высыхания покровного слоя, растения заселяют десятью гусеницами Heliothis virescens первой возрастной стадии, после чего помещают в пластмассовый контейнер. Через 6 дней, сравнивая количество мертвых гусениц с поражением обработанных и необработанных растений, определяют снижение процента популяции и процента поражения (% действия). Соединения формулы I проявляют в данном тесте хорошее действие. Соединения группы 9 из таблиц 4 и 4 а, например соединение 4.1, являются особенно активными. Пример В-17. Действие против Spodopteralittoralis. Молодые растения сои культурной опрыскивают жидкой водной эмульсией для опрыскивания, содержащей 100 частей на миллион активного компонента. Затем, после высыхания покровного слоя, растения заселяют десятью гусеницами Spodoptera littoralis третьей возрастной стадии, после чего помещают в пластмассовый контейнер. Через 3 дня, сравнивая количество мертвых гусениц с поражением обработанных и необработанных растений, определяют снижение процента популяции и процента поражения (% действия). Соединения из таблиц проявляют в данном тесте хорошее действие, но особенно хороши алкинилфениловые соединения из таблиц 4 и 4 а, такие как соединение 4.1. Пример В-22. Действие против гусеницPlutella xylostella. Молодые растения капусты опрыскивают жидкой водной эмульсией для опрыскивания,содержащей 100 частей на миллион активного компонента. Затем, после высыхания покровного слоя, растения заселяют десятью гусеницамиPlutella xylostella третьей возрастной стадии,после чего помещают в пластмассовый контейнер. Оценку осуществляют через 3 дня. Сравнивая количество мертвых гусениц с поражением обработанных и необработанных растений, определяют снижение процента популяции и, соответственно, процента поражения (% действия). Соединения из таблиц проявляют в данном 52 тесте хорошее действие, но особенно хороши соединения из таблиц 4 и 4 а, например соединение 4.1. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Производные O-бензилового эфира оксима общей формулы I и его возможные изомеры и смеси изомеров, где а) Х обозначает атом азота и Y обозначает атом кислорода или NH, или б) Х обозначает СН и Y обозначает атом кислорода;R3 обозначает С 1-С 6-алкокси, который не замещен или замещен 1-5 атомами галогена,замещенный или незамещенный арилокси, С 1 С 6-алкилтио, который не замещен или замещен 1-5 атомами галогена, замещенный или незамещенный арилтио, замещенный или незамещенный гетероарилокси, замещенный или незамещенный гетероарилтио, замещенный или незамещенный аралкил, замещенный или незамещенный бифенил, замещенный или незамещенный С 2-C4-алкинилфенил, замещенный или незамещенный гетероарилметил; иR4 обозначает С 1-С 6-алкил, С 1-С 6-галоидалкил, имеющий от 1 до 5 атомов галогена, С 1C4-алкокси-С 1-С 2-алкил, С 2-С 6-алкенил, который не замещен или замещен 1-3 атомами галогена; С 2-С 6-алкинил, С 3-С 6-циклоалкил-С 1-C4 алкил, который не замещен или замещен 1-4 атомами галогена; причем R3 имеет значение иное, чем дихлорбензил, когда одновременно R1 обозначает метил, R2 обозначает водород, Х обозначает СН, Y обозначает кислород и R4 обозначает С 1-C4-алкил. 2. Соединение по п.1, отличающееся тем,что R3 обозначает С 1-С 6-алкокси, С 1-C4-галоидалкокси, замещенный или незамещенный фенокси, C1-С 6-алкилтио, который не замещен или замещен 1-3 заместителями, выбранными из галогена, С 1-C4-алкила, С 1-C4-алкокси, CF3 и замещенного фенилтио; или обозначает незамещенный или в каждом случае галоидзамещенный пиридилокси, пиримидинилокси, хинолилокси, хиназолинилокси или хиноксазолинил; или обозначает незамещенный или С 1-C4 алкил-, или галоидзамещенный радикал бензотиазолилтио, бензоксазолилтио, имидазолилтио или тетразолилтио; или обозначает дифенил, С 2C4-алкинилфенил, бензил или нафтилметил,который не замещен или замещен 1-3 заместителями, выбранными из галогена, С 1-С 4-алкила,С 1-C4-алкокси, CF3 и CN; R4 обозначает C1-C6 53 алкил, С 1-С 6-галоидалкил, незамещенный или галоидзамещенный С 2-C4-алкенил,С 3-C4 алкинил, незамещенный или галоидзамещенный циклопропилметил, тогда как X, Y, R1 и R2 имеют значения, определенные для формулы I. 3. Соединение по п.2, отличающееся тем,что R1 обозначает метил, R2 обозначает водород,метил или циклопропил, тогда как X, Y, R3 и R4 имеют определенные выше значения. 4. Соединение по п.1, отличающееся тем,что Х обозначает СН или N, Y обозначает кислород, R1 обозначает метил или этил, R2 обозначает метил или циклопропил, тогда как R3 иR4 имеют определенные для формулы I значения. 5. Соединение по п.1, отличающееся тем,что Х обозначает азот, Y обозначает NH, R1 обозначает метил, этил или изопропил, R2 обозначает метил или циклопропил, тогда как R3 иR4 имеют определенные для формулы I значения. 6. Соединение по п.1, отличающееся тем,что R1 обозначает метил, R2 обозначает метил,R4 обозначает С 1-С 6-алкил, тогда X, Y и R3 имеют определенные для формулы I значения. 7. Соединение по п.1, отличающееся тем,что R1 обозначает метил, R2 обозначает метил,R3 обозначает замещенный или незамещенныйC1-C6-алкокси или замещенный или незамещенный С 1-С 6-алкилтио, тогда X, Y и R4 имеют определенные для формулы I значения. 8. Соединение по п.1, отличающееся тем,что R1 обозначает метил, R2 обозначает метил,R3 обозначает замещенный или незамещенный арилокси или замещенный или незамещенный арилтио, тогда X, Y и R4 имеют определенные для формулы I значения. 9. Соединение по п.1, отличающееся тем,что R1 обозначает метил, R2 обозначает метил,R3 обозначает замещенный или незамещенный гетероарилокси или замещенный или незамещенный гетероарилтио, тогда X, Y и R4 имеют определенные для формулы I значения. 10. Соединение по п.1, отличающееся тем,что R1 обозначает метил, R2 обозначает метил,R3 обозначает замещенный или незамещенный бензил или замещенный или незамещенный гетероарилметил, тогда X, Y и R4 имеют определенные для формулы I значения. 11. Соединение по п.1, отличающееся тем,что R1 обозначает метил, R2 обозначает метил,R3 обозначает замещенный или незамещенный бифенил или замещенный или незамещенный С 2-C4-алкинилфенил, тогда X, Y и R4 имеют определенные для формулы I значения. 12. Соединение по п.11, отличающееся тем, что R4 обозначает метил, этил или аллил,R3 обозначает группу незамещенного или замещенного С 2-С 4-алкинилфенила, в которой возможный заместитель находится в алкинильной группе и обозначает С 1-C4-алкил, С 1-C4-алкокси,С 1-C4-галоидалкил (особенно СF3), С 1-C4 000417(особенно ОСF3),С 1-C4 алкилтио, галоген, нитро, циано, С 1-C4 алкилсульфинил, С 1-C4-алкилсульфонил, незамещенный или замещенный фенил (где заместители фенила выбирают из С 1-C4-алкила, С 1C4-алкокси, гидроксила, С 1-C4-галоидалкила, C1C4-галоидалкокси, С 1-C4-алкилтио, галогена,нитро и циано); С 1-C4-гидроксиалкил, который может быть O-ацилированным(С 1-C4) или Oалкилированным(С 1-C4); С 1-С 5-алкоксикарбонил, карбамоил, N-(С 1-C4-алкил)карбамоил, N,N-ди(С 1-C4-алкил) карбамоил, N-С 1-C4-алкил-NС 1-C4-алкоксикарбамоил; незамещенный или галоидзамещенный циклопропилметоксикарбонил, незамещенный, С 1-C4-алкоксизамещенный или галоидзамещенный С 2-С 5-алкенил и пятиили шестичленное кольцо гетероарила, которое не замещено или замещено галогеном, циано,гидроксилом, а также алкилом, алкенилом, алкокси, алкенилокси или алкинилокси, каждый из которых содержит не более 4 атомов углерода. 13. Соединение по п.12, отличающееся тем, что R3 обозначает группу незамещенного или замещенного этинилфенила, при этом возможный заместитель в этинильной группе выбирают из С 1-C4-алкила, С 1-C4-алкокси, С 1-С 2 галоидалкила, С 1-С 2-галоидалкокси; фтора, хлора, брома, йода; нитро, циано; фенила, который не замещен или замещен до 3 раз (где заместители фенила выбирают из С 1-C4-алкила, С 1-C4 алкокси, С 1-C4-галоидалкила, C1-C4-галоидалкокси, гидроксила, галогена, нитро и циано); С 1C4-гидроксиалкила, который может быть Oалкилированным(С 1-C4); С 1-C4-алкоксикарбонила; N-метил-N-метоксикарбамоила и незамещенного или замещенного С 2-С 5-алкенила, возможные заместители которого выбирают из галогена и С 1-С 2-алкокси. 14. Соединение по п.11, отличающееся тем, что R3 обозначает группу незамещенного или замещенного этинилфенила, при этом заместитель в этинильной группе означает пятиили шестичленное кольцо гетероарила, которое не замещено или замещено до трех раз галогеном, циано, С 1-С 4-алкилом, С 1-C4-алкокси или гидроксилом. 15. Соединение по п.14, отличающееся тем, что кольцо гетероарила выбирают из пиридина, пиримидина, пиразина, пиридазина, триазина, (изо)тиазола, (изо)оксазола, пиррола, пиразола, имидазола, триазола и тиофена, и оно не замещено или замещено заместителями в количестве до 3, выбранными из метила, этила, изопропила, CN, галогена, метокси и гидроксила. 16. Соединение по п.13, отличающееся тем, что заместитель в этинильной группе выбирают из С 1-С 4-алкила, С 1-C4-алкокси, С 1-С 2 галоидалкила, С 1-С 2-галоидалкокси; хлора, брома, йода; нитро, циано; С 1-С 4-гидроксиалкила,который может быть О-алкилированным(С 1-С 4); С 1-С 4-алкоксикарбонила; N-метил-N-метокси 55 карбамоила и незамещенного или замещенного С 2-С 5-алкенила, возможные заместители которого выбирают из галогена и метокси. 17. Соединение по п.12, отличающееся тем, что R3 обозначает группу незамещенного или замещенного 3- или 4-(С 2-C4-алкинил) фенила. 18. Соединение по п.1, отличающееся тем,что двойная связь Х=С имеет Е-конфигурацию. 19. Соединение по п.11, отличающееся тем, что R4 обозначает метил и R3 обозначает 4 этинилфенил.
МПК / Метки
МПК: C07C 251/60, C07D 241/12, A01N 37/36
Метки: эфира, оксима, смеси, возможные, о-бензилового, изомеров, производные, изомеры
Код ссылки
<a href="https://eas.patents.su/29-417-proizvodnye-o-benzilovogo-efira-oksima-i-ego-vozmozhnye-izomery-i-smesi-izomerov.html" rel="bookmark" title="База патентов Евразийского Союза">Производные о-бензилового эфира оксима и его возможные изомеры и смеси изомеров</a>
Предыдущий патент: Устройство для обеззараживания воздуха
Следующий патент: Запорный механизм для устройства с пружинным приводом
Случайный патент: Tat вич-1 или его производные для профилактической и лечебной вакцинации












