Специфичные к меланокортиновым рецепторам пептиды для лечения сексуальной дисфункции
Формула / Реферат
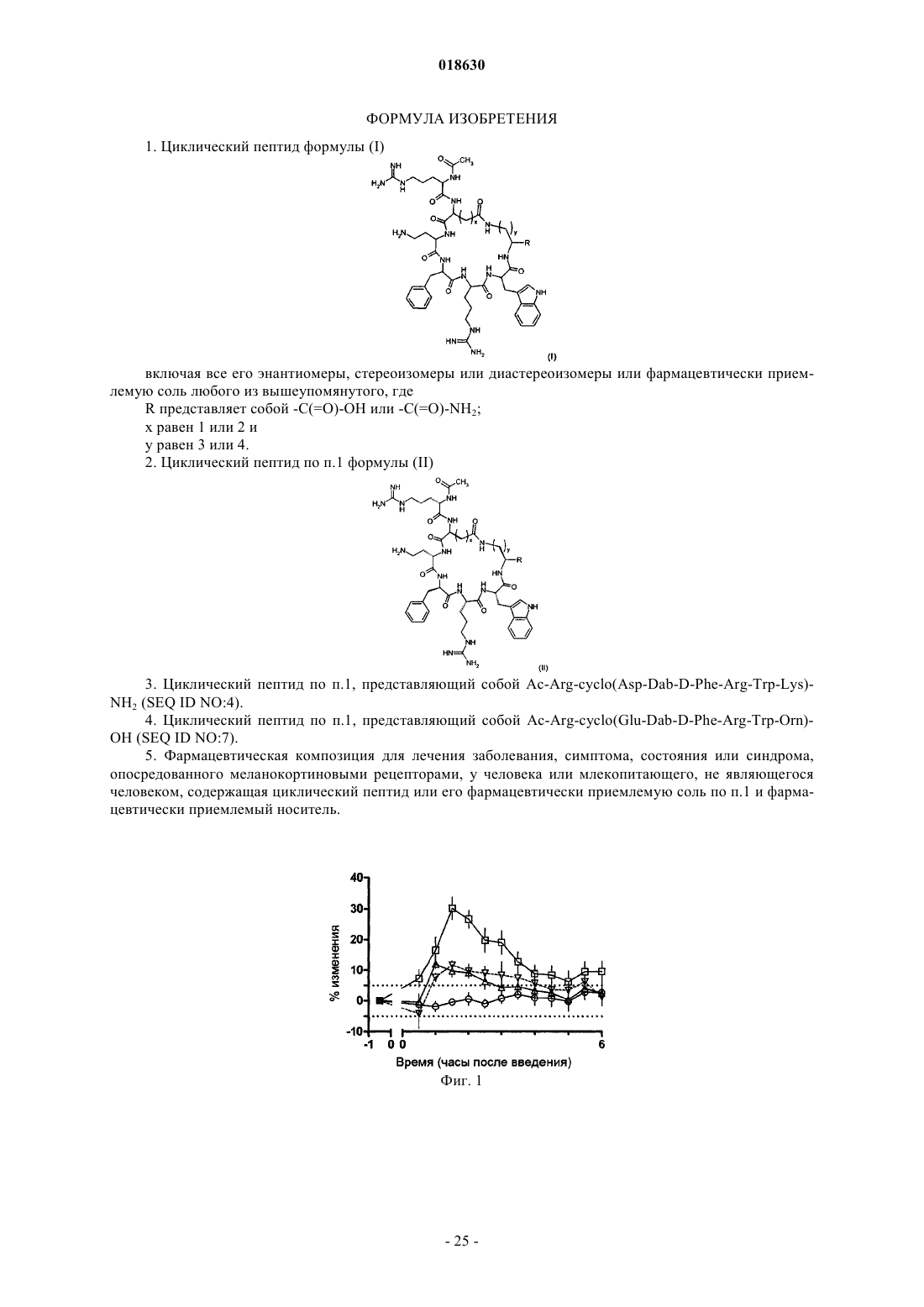
1. Циклический пептид формулы (I)
включая все его энантиомеры, стереоизомеры или диастереоизомеры или фармацевтически приемлемую соль любого из вышеупомянутого, где
R представляет собой -С(=О)-ОН или -C(=O)-NH2;
х равен 1 или 2 и
у равен 3 или 4.
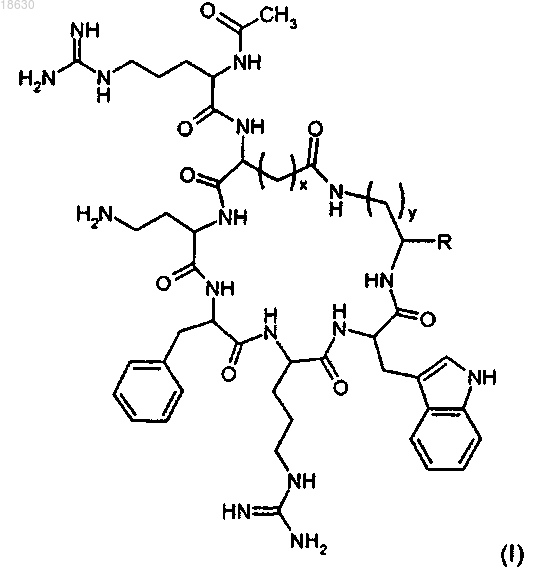
2. Циклический пептид по п.1 формулы (II)
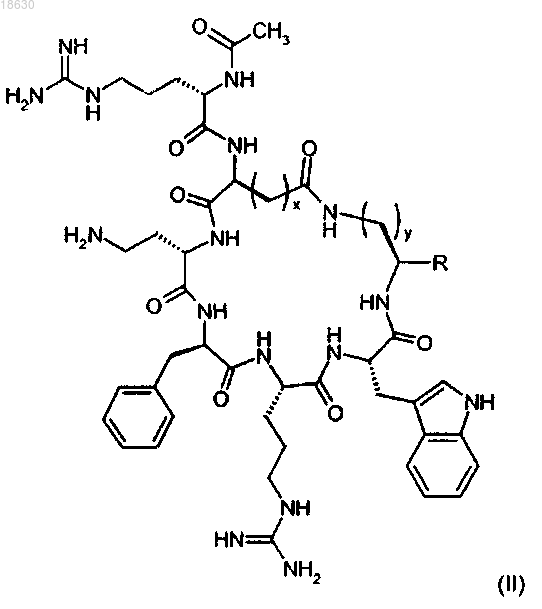
3. Циклический пептид по п.1, представляющий собой Ac-Arg-cyclo(Asp-Dab-D-Phe-Arg-Trp-Lys)-NH2 (SEQ ID NO:4).
4. Циклический пептид по п.1, представляющий собой Ac-Arg-cyclo(Glu-Dab-D-Phe-Arg-Trp-Orn)-OH (SEQ ID NO:7).
5. Фармацевтическая композиция для лечения заболевания, симптома, состояния или синдрома, опосредованного меланокортиновыми рецепторами, у человека или млекопитающего, не являющегося человеком, содержащая циклический пептид или его фармацевтически приемлемую соль по п.1 и фармацевтически приемлемый носитель.
Текст
СПЕЦИФИЧНЫЕ К МЕЛАНОКОРТИНОВЫМ РЕЦЕПТОРАМ ПЕПТИДЫ ДЛЯ ЛЕЧЕНИЯ СЕКСУАЛЬНОЙ ДИСФУНКЦИИ где R, х и у являются такими, как определено в описании, представляющий собой агонист меланокортинового рецептора, композиции и препараты, содержащие пептид приведенной выше формулы, и способы предупреждения, улучшения или лечения заболеваний, симптомов,состояний и синдромов, опосредованных меланокортиновыми рецепторами, включая сексуальную дисфункцию, такую как мужская эректильная дисфункция и женская сексуальная дисфункция. 018630 В настоящей заявке испрашивается приоритет и преимущество подачи предварительной заявки на патент США 61/059910, озаглавленной "Melanocortin Receptor-Specific Peptides for Treatment of SexualDysfunction", поданной 9 июня 2008 г., и ее описание и формула изобретения включены в данное описание путем ссылки. Предшествующий уровень техники Область изобретения (область техники) Изобретение относится к специфичным к меланокортиновым рецепторам циклическим пептидам,которые можно применять в лечении опосредованных меланокортиновыми рецепторами заболеваний,симптомов, состояний и синдромов. Описание уровня техники Нижеследующее описание ссылается на ряд публикаций по автору(ам) и году публикации, и вследствие недавних дат публикации некоторые публикации не следует рассматривать в качестве прототипов по отношению к настоящему изобретению. Рассмотрение таких публикаций приведено здесь для более полного представления о предшествующем уровне техники, и его не следует толковать как признание таких публикаций прототипами для целей установления патентоспособности. Идентифицировано семейство типов и подтипов меланокортиновых рецепторов, в том числе рецепторы меланокортина-1 (MC1-R), экспрессируемые в нормальных меланоцитах человека и клетках меланомы, рецепторы меланокортина-2 (MC2-R) для АСТН (адренокортикотропин), экспрессируемые в клетках надпочечника, рецепторы меланокортина-3 и меланокортина-4 (MC3-R и MC4-R), экспрессируемые главным образом в клетках гипоталамуса, среднего мозга и стволовой части мозга, и рецепторы меланокортина-5 (MC5-R), экспрессируемые в разнообразных периферических тканях. Выполнена значительная работа по определению структуры меланокортиновых рецепторов, включая как последовательности нуклеиновых кислот, кодирующие рецепторы, так и аминокислотные последовательности, составляющие рецепторы. MC4-R представляет собой сопряженный с G-белком рецептор, имеющий 7 трансмембранных доменов, который, как полагают, главным образом экспрессируется в мозге. Полагают, что специфичные к MC4-R пептиды и, во вторую очередь, специфичные к MC3-R пептиды полезны в регуляции энергетического гомеостаза млекопитающих, включая использование в качестве агентов для уменьшения потребления пищи и прироста массы тела. Считают, что пептиды, представляющие собой агонисты MC4-R, полезны для лечения сексуальной дисфункции, включая мужскую эректильную дисфункцию, и для снижения потребления пищи и прироста массы тела, например для лечения ожирения. Пептиды, представляющие собой агонисты MC4-R, также можно применять для уменьшения добровольного потребления алкоголя, лечения наркотических зависимостей и тому подобного. Кроме того, такие пептиды, также как и пептиды, представляющие агонисты MC1-R и MC3-R, можно применять для лечения циркуляторного шока, ишемии, геморрагического шока, воспалительных заболеваний и связанных с ними заболеваний, симптомов, состояний и синдромов. Наоборот, пептиды, представляющие собой антагонисты MC4-R, как полагают, полезны для прироста массы, например для применения в лечении кахексии, саркопении, вастинг-синдрома или болезни и анорексии. Такие пептиды также можно применять для лечения депрессии и связанных с нею расстройств. Специфичные к меланокортиновым рецепторам пептиды включают пептиды аналоги циклического-меланоцитстимулирующего гормона ("-MSH"), такие как Ac-Nle-cyclo(-Asp-His-D-Phe-Arg-Trp-Lys)NH2 (SEQ ID NO:1) (см. патенты США 5674839 и 5576290) и Ac-Nle-cyclo(-Asp-His-D-Phe-Arg-TrpLys)-OH (SEQ ID NO:2) (см. патенты США 6579968 и 6794489). Эти и другие специфичные к меланокортиновым рецепторам пептиды обычно содержат центральную тетрапептидную последовательность нативного -MSH, His6-Phe7-Arg8-Trp9 (SEQ ID NO:3), или его миметика или вариации, включая замещение Phe7 на D-Phe. Другие пептиды или пептидоподобные соединения, которые, как утверждается, являются специфичными к одному или более меланокортиновым рецепторам, раскрыты в патентах США 5731408, 6054556, 6350430, 6476187, 6600015, 6613874, 6693165, 6699873, 6887846, 6951916, 7008925 и 7176279; в публикациях заявок на патент США 2001/0056179, 2002/0143141, 2003/0064921,2003/0105024, 2003/0212002, 2004/0023859, 2005/0130901, 2005/0187164, 2005/0239711, 2006/0105951,2006/0111281, 2006/0293223, 2007/0027091, 2007/0105759, 2007/0123453, 2007/0244054 и 2008/0039387 и в международных патентных заявках WO 98/27113, WO 99/21571, WO 00/05263, WO 99/54358, WO 00/35952, WO 00/58361, WO 01/30808, WO 01/52880, WO 01/74844, WO 01/85930, WO 01/90140, WO 02/18437, WO 02/26774, WO 03/006604, WO 2004/046166, WO 2005/000338, WO 2005/000339, WO 2005/000877, WO 2005/030797, WO 2005/060985, WO 2006/048449, WO 2006/048450, WO 2006/048451,WO 2006/048452, WO 2006/097526, WO 2007/008684, WO 2007/008704 и WO 2007/009894. Несмотря на значительный научный и фармацевтический интерес к специфичным к меланокортиновым рецепторам пептидам, о котором свидетельствуют многочисленные статьи в научной литературе и многочисленные заявки на патенты и выданные патенты, ни один специфичный к меланокортиновым рецепторам пептид не был одобрен в качестве лекарственного средства для какого-либо терапевтического показания. Более того, нет никаких сообщений о каком-либо специфичном к меланокортиновым ре-1 018630 цепторам пептиде для какого-либо терапевтического показания, который преодолел бы вторую стадию клинических испытаний. Остается существенная и значительная потребность в специфичных к меланокортиновым рецепторам пептидах для применения в фармацевтике, в частности для лечения сексуальной дисфункции. Настоящее изобретение направлено на преодоление этой проблемы. Краткое изложение сущности изобретения В одном аспекте настоящее изобретение относится к циклическому пептиду формулы (I) или его фармацевтически приемлемой соли, где:R представляет собой -С(=О)-ОН или -C(=O)-NH2; х равен 1 или 2 и у равен 3 или 4. Циклический пептид может представлять собой пептид формулы (II) Таким образом, циклический пептид может представлять собой В другом аспекте настоящего изобретения предложена фармацевтическая композиция, содержащая циклический пептид или его фармацевтически приемлемую соль по изобретению и фармацевтически приемлемый носитель. В ещ одном аспекте настоящего изобретения предложена фармацевтическая композиция на основе специфичного к меланокортиновым рецепторам пептида для применения в лечении опосредованных меланокортиновыми рецепторами заболеваний, симптомов, состояний и синдромов. В ещ одном аспекте настоящего изобретения предложен специфичный к меланокортиновым рецепторам фармацевтический препарат на основе пептида, где пептид представляет собой селективныйMC4-R лиганд, для применения в лечении сексуальной дисфункции и других ассоциированных с MC4-R расстройств. В ещ одном аспекте настоящего изобретения предложены пептиды, которые являются специфичными к MC4-R и которые являются агонистами. В ещ одном аспекте настоящего изобретения предложен специфичный к меланокортиновым рецепторам фармацевтический препарат для применения в лечении сексуальной дисфункции без существенных неблагоприятных воздействий на сердечно-сосудистую систему, в том числе без значительного увеличения кровяного давления. В ещ одном аспекте настоящего изобретения предложен специфичный к MC4-R циклический пептид, который эффективен в значительном диапазоне доз. Другие аспекты, новые признаки и дополнительные области применения настоящего изобретения частично изложены в следующем подробном описании вместе с прилагаемыми графическими материалами и частично будут очевидны специалистам в области техники после ознакомления с этим описанием или могут быть понятны при осуществлении изобретения на практике. Аспекты изобретения могут быть реализованы и осуществлены с помощью средств и комбинаций, указанных, в частности, в прилагаемой формуле изобретения. Краткое описание графических материалов Прилагаемые графические материалы, которые включены в описание и составляют его часть, иллюстрируют одно или более воплощений настоящего изобретения и вместе с описанием служат для разъяснения принципов изобретения. Графические материалы приведены только с целью иллюстрации одного или более предпочтительных воплощений изобретения, и их не следует толковать как ограничивающие изобретение. Фиг. 1 относится к графику систолического кровяного давления, измеренного в перекрестном исследовании с использованием хирургически имплантированных телеметрически управляемых датчиков давления после введения разбавителя введения бремеланотида внутривенной (IV) инъекцией в дозе 1 мкмоль/кг и введения циклического пептида примера 8.1 подкожной инъекцией в дозах 0,84 мкмоль/кг и 3,0 мкмоль/кг Фиг. 2 относится к графику систолического кровяного давления, измеренного в перекрестном исследовании с использованием хирургически имплантированных телеметрически управляемых датчиков давления после введения двух различных партий циклического пептида примера 8.4 подкожной инъекцией в дозах 1 мг/кг и введения бремеланотида внутривенной инъекцией (IV) в дозе 1 мг/кг Подробное описание изобретения 1.0. Определения. Описанию изобретения предшествуют определения некоторых терминов, изложенные ниже. В последовательностях, предоставленных для пептидов по настоящему изобретению, аминокислотные остатки имеют свое общепринятое значение, как указано в главе 2400 (Chapter 2400) из Manual ofPatent Examining Procedure, 8th Ed., United States Patent and Trademark Office. Таким образом, "Nle" представляет собой норлейцин, "Asp" представляет собой аспарагиновую кислоту, "His" представляет собой гистидин, "Phe" представляет собой фенилаланин, "Arg" представляет собой аргинин, "Trp" представляет собой триптофан, "Lys" представляет собой лизин и так далее. Следует понимать, что "D" изомеры обозначаются с помощью "D-" перед трехбуквенным кодом или названием аминокислоты, так что, например, D-Phe представляет собой D-фенилаланин. Аминокислотные остатки, не охватываемые указанным выше, имеют следующие обозначения: Термин "Ас" означает ацетильную группу СН 3-С(=О)-."Амид" включает соединения, которые имеют трехвалентный азот, присоединенный к карбонильной группе (-C(=O)-NH2), такие как, например, метиламид, этиламид, пропиламид и тому подобные."Амин" включает соединения, которые содержат аминогруппу (-NH2). Термин "композиция" в контексте фармацевтической композиции предназначен для охватывания продукта, содержащего активный(е) ингредиент(ы) и инертный(е) ингредиент(ы), составляющий(е) носитель, а также любой продукт, который прямо или косвенно является результатом комбинации, комплексообразования или агрегации любых двух или более ингредиентов, или диссоциации одного или более ингредиентов, или других типов реакций или взаимодействий одного или более ингредиентов. Соответственно, фармацевтические композиции, используемые в настоящем изобретении, охватывают любую композицию, полученную путем смешивания активного ингредиента и одного или более фармацевтически приемлемых носителей."Агонист" меланокортинового рецептора означает эндогенное вещество, лекарственное вещество или соединение, включая такие соединения, как пептиды по настоящему изобретению, которое может взаимодействовать с меланокортиновым рецептором и инициировать фармакологический ответ, характерный для меланокортинового рецептора, включая активацию аденилциклазы, но не ограничиваясь ею. Для настоящего изобретения предпочтителен агонист меланокортинового рецептора, который является агонистом рецептора меланокортина-4 (MC4-R); для некоторых применений предпочтителен агонист меланокортинового рецептора, который является агонистом как MC4-R, так и рецептора меланокортина 1 (MC1-R), а для других применений предпочтителен агонист меланокортинового рецептора, который является агонистом одного или более следующих рецепторов: MC1-R, рецептора меланокортина-3 (MC3R), MC4-R и рецептора меланокортина-5 (MC5-R)."ЕС 50" означает молярную концентрацию агониста, в том числе частичного агониста, которая приводит к 50% от максимально возможного ответа для такого агониста. Например, тестируемое соединение, которое в концентрации 72 нМ приводит к 50% от максимально возможного ответа для этого соеди-3 018630 нения при определении в тесте на сАМР (циклический аденозинмонофосфат) в MC4-R клеточной экспрессирующей системе, имеет ЕС 50 72 нМ. Если не указано иное, молярная концентрация, ассоциируемая с определением ЕС 50, дается в наномолях на литр (нМ)."Ki (нМ)" означает равновесную константу диссоциации ингибитора, представляющую собой молярную концентрацию конкурирующего соединения, которое связывается с половиной сайтов связывания рецептора, при равновесии в отсутствие радиолиганда или других конкурентов. В общем, численное значение Ki находится в обратно пропорциональной связи к аффинности соединения в отношении рецептора, так что если Ki имеет низкое значение, то аффиность является высокой. Значение Ki может быть определено с использованием уравнения Ченга-Прусоффа (Cheng Y., Prusoff W. H., Biochem. Pharmacol. 22: 3099-3108, 1973): где "лиганд" представляет собой концентрацию радиолиганда, и KD представляет собой величину,обратную аффинности радиолиганда в отношении рецептора, при которой обеспечивается 50%-ное заполнение рецепторов радиолигандом. Если не указано иное, молярная концентрация, ассоциируемая с определением Ki, дается в нМ. Ki может быть представлена для специфических рецепторов (например,MC1-R, MC3-R, MC4-R или MC5-R) и специфических лигандов (например, -MSH или NDPMSH)."Ингибирование" означает процентное ослабление или снижение связывания с рецептором в анализе конкурентного ингибирования по сравнению с известным стандартом. Таким образом, "ингибирование при 1 мкМ (NDPMSH)" означает процентное снижение связывания NDPMSH путем добавления определенного количества тестируемого соединения, например 1 мкМ тестируемого соединения,например, в описанных ниже условиях анализа. Например, тестируемое соединение, которое не ингибирует связывание NDPMSH, имеет ингибирование 0%, а тестируемое соединение, которое полностью ингибирует связывание NDPMSH, имеет ингибирование 100%. Обычно, как описано ниже, для исследования конкурентного ингибирования используют радиоанализ, такой как с I125-меченным NDPMSH,или флуоресцентный анализ с лантанидным хелатом, такой как с Eu-NDPMSH. Однако известны и другие методы исследования конкурентного ингибирования, включая использование метки или систем меток (tag systems), не являющихся радиоактивными изотопами, и, в общем, любой известный в области техники метод исследования конкурентного ингибирования может быть использован в этом изобретении. Тем самым, можно видеть, что "ингибирование" является одним из критериев определения того,ослабляет ли тестируемое соединение связывание -MSH с меланокортиновыми рецепторами."Аффинность связывания" означает способность соединения или лекарственного средства связываться со своей биологической мишенью, выраженную в данном описании в виде Ki (нМ)."Внутренняя активность" означает максимальную функциональную активность, достигаемую соединением в определенной клеточной системе, экспрессирующей меланокортиновый рецептор, такую как максимальная стимуляция аденилилциклазы. Максимальную стимуляцию, достигаемую -MSH илиNDPMSH, обозначают как внутреннюю активность, равную 1,0 (или 100%), а соединение, способное стимулировать половину от максимальной активности -MSH или NDPMSH, обозначают как имеющее внутреннюю активность, равную 0,5 (или 50%). Соединение по этому изобретению, которое в описанных здесь условиях анализа имеет внутреннюю активность, равную 0,7 (70%) или выше, классифицируют в качестве агониста, соединение с внутренней активностью от 0,1 (10%) до 0,7 (70%) классифицируют в качестве частичного агониста, а соединение с внутренней активностью ниже 0,1 (10%) классифицируют в качестве неактивного или не имеющего внутренней активности. В одном из аспектов циклические пептиды по настоящему изобретению могут быть в основном охарактеризованы в качестве частичного агониста MC4-R по отношению к -MSH или NDPMSH. В общем, "функциональная активность" является критерием передачи сигнала рецептора или критерием изменения передачи сигнала, ассоциированного с рецептором, таким как меланокортиновый рецептор и, в частности, MC4-R или hMC4-R, после стимуляции соединением. Меланокортиновые рецепторы инициируют трансдукцию сигнала посредством активации гетеротримерных G-белков. В одном из аспектов меланокортиновые рецепторы передают сигнал посредством Gas, который катализирует продуцирование сАМР аденилилциклазой. Таким образом, определение стимуляции аденилилциклазы, такое как определение максимальной стимуляции аденилилциклазы, является одним из критериев функциональной активности и первичным критерием, приведенным здесь. Однако следует понимать, что при осуществлении этого изобретения на практике могут быть использованы альтернативные критерии функциональной активности, и они специально предполагаются и включены в объем этого изобретения. Так, например, свободный внутриклеточный кальций можно измерить с использованием способов, описанных и раскрытых в Mountjoy K.G. et al., Melanocortin receptor-medicated mobilization of intracellular freeScreening 7: 233-246, 2002. Также, можно определить активацию путем измерения продукции инозит-4 018630 трифосфата или диацилглицерина из фосфатидилинозит-4,5-бисфосфата, например путем использования радиоанализа. Еще одним критерием функциональной активности является рецепторная интернализация,являющаяся результатом активации регупяторных путей, например, с использованием способов, раскрытых в Nickolls S.A. et al., Functional selectivity of melanocortin 4 receptor peptide and nonpeptide agonists:evidence for ligand specific conformational states. J Pharm Exper Therapeutics 313: 1281-1288, 2005. Еще одним критерием функциональной активности является обмен и скорость обмена нуклеотидов, ассоциированных с активацией рецептора G-белка, например обмен GDP (гуанозиндифосфат) на GTP (гуанозинтрифосфат) на -субъединице G-белка, который может быть измерен любым количеством способов,включая радиоанализ с использованием гуанозин-5'-(-[35S]тио)-трифосфата, как раскрыто в Manningreceptors. Mol Pharmacol 62: 451-452, 2002. Для измерения активации G-сопряженных белков разработаны различные генетические тесты, такие как раскрытые в Chen W. et al., A colorimetric assay from measuring activation of Gs-and Gq-coupled signaling pathways. Anal Biochem 226. 349-354, 1995; Kent T.C. et al.,Development of a generic dual-reporter gene assay for screening G-protein-coupled receptors. Biomol Screening, 5: 437-446, 2005; или Kotarsky K. et al., Improved receptor gene assays used to identify ligands acting onorphan seven-transmembrane receptors. PharmacologyToxicology 93: 249-258, 2003. Для применения в измерении активации меланокортиновых рецепторов адаптирован колориметрический тест Чена и др.,как раскрыто в Hruby V.J. et al., Cyclic lactam -melanocortin analogues of Ac-Nle4-cyclo[Asp5,D-Phe7,Lys10]-melanocyte-stimulating hormone-(4-10)-NH2 with bulky aromatic amino acids at position 7 shows high antagonist potency and selectivity at specific melanocortin receptors. J Med Chem 38: 3454-3461, 1995. В общем,функциональная активность может быть измерена любым способом, включая способы определения активации и/или передачи сигнала G-сопряженным рецептором, а также включая способы, которые могут быть разработаны или описаны в дальнейшем. Каждая из упомянутых выше статей и раскрытые в них способы включены в данное описание путем ссылки, как если бы были изложены полностью. Термины "лечить" и "лечение", используемые в данном описании, предполагают действие, которое имеет место, в то время как пациент страдает от конкретного заболевания или расстройства, и которое снижает серьезность этого заболевания или расстройства. Термин "терапевтически эффективное количество", используемый в данном описании, означает количество соединения, в том числе пептида по изобретению, которое будет вызывать биологический или медицинский ответ у млекопитающего, находящегося на лечении у врача или другого клинициста. Термин "профилактически эффективное" или "предупредительное", используемый в данном описании, означает количество соединения, в том числе пептида по изобретению, которое будет предупреждать или подавлять недуг, или смягчать недуг у млекопитающего, находящегося в таком медицинском состоянии, которое врач или другой клиницист пытается предупредить, подавить или смягчить, прежде чем пациент начнет страдать от указанного заболевания или расстройства."Сексуальная дисфункция" означает любое состояние, которое подавляет или ухудшает нормальную сексуальную функцию, включая коитус. Термин не ограничен физиологическими состояниями и включает психогенные состояния или ощущаемое ухудшение без формального диагноза патологии или расстройства. Сексуальная дисфункция включает эректильную дисфункцию у млекопитающего-самца и женскую сексуальную дисфункцию у млекопитающего-самки."Эректильная дисфункция" представляет собой расстройство, приводящее млекопитающее-самца к нарушению достижения функциональной эрекции, эякуляции или того и другого. Соответственно, эректильная дисфункция является синонимом импотенции и включает неспособность достигнуть или поддержать эрекцию с ригидностью, достаточной для коитуса. Симптомы эректильной дисфункции включают неспособность достигнуть или удержать эрекцию, нарушение эякуляции, преждевременную эякуляцию или неспособность достижения оргазма. Увеличение эректильной дисфункции часто связано с возрастом или может быть вызвано физическим заболеванием, или может быть побочным действием лечения лекарственным средством."Женская сексуальная дисфункция" представляет собой расстройство, включающее расстройство полового возбуждения. Термин "расстройство полового возбуждения" включает постоянное или повторяющееся нарушение достижения или удержания реакции на половое возбуждение, представляющее собой выделение смазочной жидкости и набухание, до завершения сексуальной активности. Сексуальная дисфункция у женщин также может включать подавленный оргазм и диспареунию, то есть болезненный или затрудненный коитус. Женская сексуальная дисфункция включает ряд категорий заболеваний, состояний и расстройств, в том числе гипоактивное расстройство полового влечения, сексуальную ангедонию, расстройство полового возбуждения, диспареунию и вагинизм, но не ограничивается ими. Гипоактивное расстройство полового влечения включает расстройство, при котором сексуальные фантазии и желание сексуальной активности постоянно или периодически убывают или отсутствуют, вызывая явный дистресс или межличностные затруднения. Гипоактивное расстройство полового влечения может быть вызвано скукой или несчастьем при длительных отношениях, депрессией, зависимостью от алкоголя или психотропных средств, побочными действиями предписанных лекарственных средств или гормо-5 018630 нальными недостатками. Сексуальная ангедония включает пониженное или отсутствующее удовольствие при сексуальной активности. Сексуальная ангедония может быть вызвана депрессией, лекарственными средствами или межличностными факторами. Расстройство полового возбуждения может быть вызвано пониженным эстрогеном, заболеванием или лечением с применением диуретиков, антигистаминных средств, антидепрессантов или гипотензивных агентов. Диспареуния и вагинизм представляют собой сексуальные болевые расстройства, характеризуемые болью в результате проникновения, и могут быть вызваны, например, лекарственными препаратами, снижающими смазывание, эндометриозом, воспалением тазовых органов, воспалительным заболеванием кишечника или проблемами с мочевыми путями. 2.0. Клинические показания и применение. Композиции и способы, раскрытые в данном описании, можно применять как по медицинским показаниям, так и в животноводстве или ветеринарным показаниям. Как правило, способы применяют в отношении людей, но также можно применять в отношении других млекопитающих. Подразумевается,что термин "пациент" означает особь-млекопитающее и в таком значении используется во всем описании и формуле изобретения. Основные применения настоящего изобретения затрагивают людей, но настоящее изобретение можно применять к лабораторным, сельскохозяйственным, зоопарковым, диким, домашним, спортивным или другим животным. Пептиды, композиции и способы по настоящему изобретению можно применять для лечения сексуальной дисфункции, включая как мужскую эректильную дисфункцию, так и женскую сексуальную дисфункцию. В одном из конкретных воплощений пептиды, композиции и способы по настоящему изобретению применяют для увеличения эректильной функции у пациентов мужского пола, включая увеличение эректильной функции для предоставления возможности вагинального полового сношения, но не ограничиваясь им. В другом конкретном воплощении пептиды, композиции и способы по настоящему изобретению применяют для лечения женской сексуальной дисфункции, включая увеличение доли успешных случаев сексуального возбуждения, доли успешных случаев влечения, уровней полового возбуждения и влечения, но не ограничиваясь ими. Для женской сексуальной дисфункции конечные точки могут быть определены, хотя и не обязательно, любым из ряда утвержденных инструментариев, включая шкалу сексуального дистресса женщин, женский профиль сексуальных отношений, индекс сексуальных функций женщин и общий опросный оценочный лист, но не ограничиваясь ими. Пациенты, подвергаемые лечению женской сексуальной дисфункции, могут быть женщинами в предменопаузном периоде или женщинами в постменопаузном периоде. 3.0. Комбинированная терапия при некоторых показаниях. Пептиды, композиции и способы по настоящему изобретению можно применять при лечении любого из упомянутых выше заболеваний, симптомов, состояний или синдромов, или любого заболевания,симптома, состояния или синдрома, опосредованного меланокортиновым рецептором, путем введения в комбинации с одним или более другими фармацевтически активными соединениями. Такое комбинированное введение можно осуществлять посредством единичной лекарственной формы, которая содержит как пептид по настоящему изобретению, так и еще одно другое фармацевтически активное соединение, и которая включает таблетку, капсулу, спрей, ингаляционный порошок, инъецируемую жидкость или тому подобное. Альтернативно, комбинированное введение можно осуществлять посредством введения двух разных лекарственных форм, причем одна лекарственная форма содержит пептид по настоящему изобретению, а другая лекарственная форма включает иное фармацевтически активное соединение. В этом случае лекарственные формы могут быть одинаковыми или разными. Ниже, без намерения ограничить комбинированные терапии, следуют примеры некоторых комбинированных терапий, которые могут быть использованы. 3.1 Комбинированная терапия сексуальной дисфункции. Допускается и предполагается применение циклических пептидов по настоящему изобретению в комбинации с другими лекарственными средствами или агентами для лечения сексуальной дисфункции. Эти другие лекарственные средства и агенты могут включать агенты, которые стимулируют эректильную активность, в том числе ингибиторы фосфодиэстеразы-5 (PDE-5), тестостерон, простагландин и тому подобные. В предпочтительном воплощении изобретения циклические пептиды по изобретению применяют в комбинации с терапевтически эффективным количеством ингибитора фосфодиэстеразы, специфической к циклическому GMP, или антагониста альфа-адренергического рецептора. Идеи и описание заявки на патент США , патента США 7235625, озаглавленного "Multiple Agent Therapy for SexualDysfunction", включены в данное описание путем ссылки, как если бы были изложены полностью. Таким образом, в настоящем изобретении предложены способы лечения сексуальной дисфункции,включающие стадию введения пациенту, имеющему сексуальную дисфункцию, или подвергающемуся риску получить сексуальную дисфункцию, терапевтически эффективного количества циклического пептида по настоящему изобретению в комбинации с терапевтически эффективным количеством второго фармацевтического агента для лечения сексуальной дисфункции. Циклический пептид по настоящему изобретению можно вводить одновременно с введением, до введения или после введения терапевтически эффективного количества второго фармацевтического агента для лечения сексуальной дисфункции.-6 018630 Предпочтительно пептид по настоящему изобретению вводят в пределах одного часа, предпочтительно в пределах менее получаса, после введения терапевтически эффективного количества второго фармацевтического агента для лечения сексуальной дисфункции. Однако для некоторых форм комбинированной терапии, таких как, например, в комбинации с терапевтически эффективным количеством гормонального или связанного с гормоном фармацевтического агента для лечения сексуальной дисфункции, гормональный или связанный с гормоном фармацевтический агент для лечения сексуальной дисфункции можно вводить по независимому расписанию, так что нет никакой последовательности или специальной временной зависимости между введением пептида по настоящему изобретению и гормонального или связанного с гормоном фармацевтического агента для лечения сексуальной дисфункции. Таким образом,например, гормональный или связанный с гормоном фармацевтический агент для лечения сексуальной дисфункции можно вводить в суточной или другой дозе, или посредством пластырей, или других графиков непрерывного введения, а введение пептида по настоящему изобретению осуществлять по желанию пациента или необходимости. Таким образом, в настоящем изобретении предложены способы лечения сексуальной дисфункции,включающие стадию введения пациенту, имеющему сексуальную дисфункцию или подвергающемуся риску получить сексуальную дисфункцию, терапевтически эффективного количества циклического пептида по настоящему изобретению в комбинации с другим соединением, которое полезно при лечении сексуальной дисфункции. В предпочтительном воплощении комбинированной терапии сексуальная дисфункция представляет собой женскую сексуальную дисфункцию. В особенно предпочтительном воплощении комбинированной терапии сексуальная дисфункция представляет собой эректильную дисфункцию. Также в настоящем изобретении предложены фармацевтические композиции, содержащие циклический пептид по настоящему изобретению и дополнительное соединение, полезное для лечения сексуальной дисфункции. В воплощении композиции, дополнительные соединения, полезные для лечении сексуальной дисфункции, предпочтительно выбраны из группы, состоящей из ингибитора фосфодиэстеразы; ингибитора фосфодиэстеразы, специфической к циклическому GMP; простагландинов; апоморфина; модуляторов окситоцина; альфа-адренергических антагонистов; андрогенов; селективных модуляторов андрогенных рецепторов (SARM); бупропиона; вазоактивного пептида кишечника (VIP); ингибиторов нейтральной эндопептидазы (NEP) и антагонистов нейропептидных Y рецепторов (NPY), но не ограничены ею. В воплощении способа и композиции второй фармацевтический агент для лечения сексуальной дисфункции представляет собой тестостерон. В другом воплощении комбинированной терапии второй фармацевтический агент для лечения сексуальной дисфункции представляет собой ингибитор фосфодиэстеразы типа V (PDE-5). Например, ингибитором PDE-5 может быть Viagra, товарный знак силденафила, Levitra, товарный знак моногидрохлоридной соли варденафила, или Cialis, товарный знак тадалафила. Другие ингибиторы PDE-5 раскрыты в патенте США 7235625, выданном 22 июня 2007 г., и озаглавленном "Multiple Agent Therapyfor Sexual Dysfunction", который включен в данное описание путем ссылки. В другом воплощении указанной выше композиции соединение, полезное для лечения сексуальной дисфункции, представляет собой агонист/антагонист эстрогена. В одном из воплощений агонист/антагонист эстрогена представляет собой (-)цис-6-фенил-5-[-4-(2-пирролидин-1-ил-этокси)фенил]-5,6,7,8 тетрагидронафталин-2-ол (также известный как лазофоксифен) или его оптический или геометрический изомер; фармацевтически приемлемая соль, N-оксид, сложный эфир, четвертичная аммониевая соль или его пролекарство. Более предпочтительно, агонист/антагонист эстрогена находится в форме Dтартратной соли. В еще одном воплощении указанной выше композиции агонист/антагонист эстрогена выбран из группы, состоящей из тамоксифена, 4-гидрокситамоксифена, ралоксифена, дролоксифена, торемифена,центхромана, идоксифена, 6-(4-гидроксифенил)-5-[4-(2-пиперидин-1-ил-этокси)бензил]нафталин-2-ола,4-[2-(2-азабицикло[2.2.1]гепт-2-ил)этокси]фенил-[6-гидрокси-2-(4-гидроксифенил)бензо[b]тиофен-3 ил]метанона, ЕМ-652, ЕМ-800, GW 5368, GW 7604, TSE-424 и их оптических или геометрических изомеров; и их фармацевтически приемлемых солей, N-оксидов, сложных эфиров, четвертичных аммониевых солей и пролекарств. В еще одном воплощении циклический пептид по настоящему изобретению можно применять в комбинации с любыми известными вспомогательными механизмами или устройствами. Также в настоящем изобретении предложены наборы для лечения сексуальной дисфункции (в том числе эректильной дисфункции), содержащие: первую фармацевтическую композицию, содержащую циклический пептид по настоящему изобретению; вторую фармацевтическую композицию, содержащую второе соединение, полезное для лечения сексуальной дисфункции, и контейнер для первой и второй композиций. 4.0. Способы введения и применения. Способ введения и применения варьируют в зависимости от характеристики конкретных пептидов-7 018630 по настоящему изобретению, заболевания, симптома, состояния или синдрома, подвергаемого лечению,и других факторов, известных специалистам в области техники. В общем, любой способ введения и применения, известный в области техники или разработанный в дальнейшем, может быть использован с пептидами по настоящему изобретению. Без ограничения изложенного выше следующие способы введения и применения имеют специальное приложение для указанных показаний. Композиции, содержащие один или более пептидов по настоящему изобретению, можно вводить подкожной инъекцией. В одном из аспектов циклический пептид по настоящему изобретению приготовлен для глубокой внутримышечной инъекции, такой как в ягодичную или дельтовидную мышцу, в препарате с полиэтиленгликолем, таким как полиэтиленгликоль 3350, и возможно с одним или более дополнительными эксципиентами и консервантами, включая такие эксципиенты, как соли, полисорбат 80, гидроксид натрия или соляная кислота для корректировки рН и тому подобные, но не ограничиваясь ими. В другом аспекте циклический пептид по настоящему изобретению приготовлен с поли(сложным ортоэфиром), который может представлять собой автокатализируемый поли(сложный ортоэфир) с любым переменным процентным содержанием молочной кислоты в скелете полимера и возможно с одним или более дополнительными эксципиентами. В одном из аспектов применяют полимер поли(D,L-лактид-согликолид). В общем, любой из ряда инъецируемых и биоразрушаемых полимеров, которые предпочтительно также являются адгезивными полимерами, можно применять в инъецируемом препарате замедленного высвобождения. Альтернативно, можно применять другие препараты замедленного высвобождения, включая препараты, допускающие подкожную инъекцию, которые могут содержать одну(один) или более нано/микросферы (такие как композиции, содержащие PLGA полимеры), липосомы, эмульсии(такие как эмульсии "масло в воде"), гели, нерастворимые соли или суспензии в масле. Препарат может быть таким, что инъекция будет требоваться ежедневно, еженедельно, ежемесячно или с другой периодичностью в зависимости от концентрации и количества циклического пептида, скорости замедленного высвобождения применяемых веществ и других факторов, известных специалистам в области техники. Композиции, содержащие один или более пептидов по настоящему изобретению, можно вводить перорально в индивидуальной лекарственной форме, такой как таблетка или капсула. В одном из аспектов индивидуальная лекарственная форма содержит энтеросолюбильное покрытие и возможно один или более агентов для улучшения усвоения, уменьшения расщепления протеазы, увеличения клеточной проницаемости и тому подобного. При сексуальной дисфункции в предпочтительном аспекте один или более пептидов по настоящему изобретению приготовлены так, что их можно вводить по требованию, например примерно менее чем за час, менее чем за два часа или менее чем за четыре часа до ожидаемой сексуальной активности. В одном из аспектов композиция приготовлена для подкожной инъекции. В другом аспекте композиция приготовлена для одного из множества трансдермальных путей введения, включая трансбуккальное введение,назальное введение, ингаляционное введение и тому подобное. В другом аспекте композиция приготовлена для назального введения, такого как посредством дозирующего распылительного устройства, доставляющего водную композицию объемом от примерно 20 до примерно 200 мкл, содержащую любой из множества других агентов, включая агенты, улучшающие проницаемость. 5.0. Способы получения. В общем, пептиды по настоящему изобретению могут быть синтезированы путем твердофазного синтеза и очищены в соответствии со способами, известными в области техники. Для получения пептидов по настоящему изобретению может быть использован любой из ряда хорошо известных методов,использующих множество смол и реагентов. Циклические пептиды по настоящему изобретению могут быть легко синтезированы с помощью известных общепринятых методов образования пептидной связи между аминокислотами. Такие общепринятые методы включают, например, любой способ в жидкой фазе, допускающий конденсацию между свободной альфа-аминогруппой аминокислоты или ее остатка, у которых защищены карбоксильная группа и другие реакционноспособные группы, и свободной первичной карбоксильной группой другой аминокислоты или ее остатка, у которых защищены аминогруппа или другие реакционноспособные группы. Согласно предпочтительному общепринятому методу циклические пептиды по настоящему изобретению могут быть синтезированы путем твердофазного синтеза и очищены в соответствии со способами, известными в области техники. Для получения пептидов по настоящему изобретению может быть использован любой из ряда хорошо известных методов, использующих множество смол и реагентов. Процесс синтеза циклических пептидов можно осуществлять методом, при котором каждую аминокислоту в желаемой последовательности по одной добавляют подряд к другой аминокислоте или ее остатку, или методом, при котором сначала общеизвестными способами синтезируют пептидные фрагменты с желаемой последовательностью аминокислот, а потом осуществляют конденсацию для получения желаемого пептида. Полученный пептид затем циклизуют с получением циклического пептида по изобретению. Способы твердофазного пептидного синтеза хорошо известны и имеют практическое применение в области техники. Согласно таким способам синтез пептидов по изобретению можно осуществлять путем последовательного введения желаемых аминокислотных остатков по одному в растущую пептидную-8 018630 цепь в соответствии с общими принципами твердофазных способов. Эти способы раскрыты в многочисленных ссылках, включая Merrifield, R.B., Solid phase synthesis (Nobel lecture). Angew Chem 24: 799-810Academic Press 1-284 (1980). В ходе химических синтезов пептидов реакционноспособные группы боковых цепей различных аминокислотных остатков защищают подходящими защитными группами, которые предотвращают протекание химической реакции в этом месте до тех пор, пока не удалена защитная группа. Также распространена защита альфа-аминогруппы аминокислотного остатка или фрагмента, тогда как остаток или фрагмент реагирует по карбоксильной группе, с дальнейшим селективным удалением альфааминозащитной группы, предоставляющим возможность для протекания следующей реакции в этом месте. Конкретные защитные группы описаны и известны для способов твердофазного и способов синтеза в жидкой фазе. Альфа-аминогруппы могут быть защищены подходящей защитной группой, включая защитную группу уретанового типа, такую как бензилоксикарбонил (Z) и замещенный бензилоксикарбонил, например п-хлорбензилоксикарбонил (Z-Cl), п-нитробензилоксикарбонил (X-NO2), п-бромбензилоксикарбонил (Z-Br), п-бифенилизопропоксикарбонил, 9-флуоренилметоксикарбонил (Fmoc) и п-метоксибензилоксикарбонил (Moz), и алифатические защитные группы уретанового типа, например третбутилоксикарбонил (Boc), диизопропилметоксикарбонил, изопропоксикарбонил и аллилоксикарбонил(Alloc). Для защиты альфа-аминогрупп предпочтительной является Fmoc. Гуанидиновые группы могут быть защищены подходящей защитной группой, такой как нитро, птолуолсульфонил (Tos), Z, пентаметилхромансульфонил (Pmc), адамантилоксикарбонил, пентаметилдигидробензофуран-5-сульфонил (Pbf) и Boc. Pbf и Pmc являются предпочтительными защитными группами для Arg. Описанные здесь пептиды по изобретению получали, используя твердофазный синтез, например посредством автоматизированного синтезатора пептидов Symphony Multiplex Peptide Synthesizer (RaininInstrument Company) с использованием программных модулей, поставляемых производителем, и следуя протоколам, изложенным в руководстве производителя. Твердофазный синтез начинают с С-конца пептида путем связывания защищенной альфааминокислоты с подходящей смолой. Такой исходный материал получают путем присоединения альфааминозащищенной аминокислоты посредством сложноэфирной связи к п-бензилоксибензиловой спиртовой смоле (смоле Ванга), 2-хлортритил-хлоридной смоле или оксимной смоле, посредством амидной связи между Fmoc-линкером, таким как п-[(R,S)[1-(9 Н-флуорен-9-ил)метоксиформамидо]-2,4 диметилоксибензил]феноксиуксусная кислота (линкер Ринка), и бензгидриламинной (ВНА) смолой, или другими способами, хорошо известными в области техники. Подложки Fmoc-линкер-ВНА смолы имеются в продаже и обычно используются, когда это возможно. Смолы проходят необходимое количество повторяющихся циклов для последовательного присоединения аминокислот. Альфа-аминозащитные группы Fmoc удаляют в щелочных условиях. Для этой цели могут быть использованы пиперидин, пиперазин, диэтиламин или морфолин (20-40% об./об.) в N,N-диметилформамиде (DMF). После удаления альфа-аминозащитной группы последующие защищенные аминокислоты подвергают поэтапному сочетанию в желаемом порядке с получением промежуточного защищенного соединения пептид-смола. Активирующие реагенты, используемые для сочетания аминокислот в твердофазном синтезе пептидов, хорошо известны в области техники. После того как пептид синтезирован, защитные группы ортогонально защищенных боковых цепей могут быть удалены с использованием способов, хорошо известных в области техники, если это необходимо, для дальнейшего получения производных пептида. Как правило, ортогональные защитные группы используют в качестве подходящих. Например, пептиды по изобретению содержат многочисленные аминокислоты с боковой цепью, содержащей аминогруппу. В одном из аспектов используют схему защиты Allyl-Alloc (аллил/аллилоксикарбонил) с аминокислотами, образующими лактамный мостик посредством своих боковых цепей, и ортогональными защитными группами, отщепляемыми в разных реакционных условиях, для других аминокислот с боковыми цепями, содержащими аминогруппу. Таким образом, например, аминокислоты Fmoc-Lys(Alloc)-OH,Fmoc-Orn(Alloc)-OH, Fmoc-Dap(Alloc)-OH, Fmoc-Dab(Alloc)-OH, Fmoc-Asp(OAII)-OH или FmocGlu(OAII)-OH могут быть использованы для положений, приводящих к образованию лактамного мостика после циклизации, тогда как другие аминокислоты с боковыми цепями, содержащими аминогруппу,имеют другую и ортогональную защитную группу, такую как Fmoc-Arg(Pbf)-OH, Fmoc-Lys(Pbf)-OH,Fmoc-Dab(Pbf)-OH или тому подобную. Другие защитные группы могут быть использованы аналогичным образом; в качестве примера и без ограничения, Mtt/OPp (4-метилтритил/2-фенилизопропил) могут быть использованы с боковыми цепями, образующими лактамный мостик после циклизации, с используемыми для других положений ортогональными защитными группами, которые не отщепляются в условиях, подходящих для отщепления Mtt/OPp. Реакционноспособные группы в пептиде могут быть селективно модифицированы либо в процессе твердофазного синтеза, либо после отсоединения от смолы. Например, пептиды могут быть модифици-9 018630 рованы с получением N-концевых модификаций, таких как ацетилированные, пока находятся на смоле,или могут быть удалены со смолы путем использования расщепляющего реагента и затем модифицированы. Аналогично, способы модификации боковых цепей аминокислот хорошо известны специалистам в области пептидного синтеза. Выбор модификаций, сделанный в отношении присутствующих в пептиде реакционноспособных групп, определяется, частично, характеристиками, желаемыми для пептида. В пептидах по настоящему изобретению в одном из предпочтительных воплощений N-концевую группу модифицируют путем введения N-ацетильной группы. В одном из аспектов используют способ,при котором после удаления защитной группы на N-конце пептид, связанный со смолой, подвергают взаимодействию с уксусным ангидридом в дихлорметане в присутствии органического основания, такого как диизопропилэтиламин. В области техники известны другие способы ацетилирования N-конца, включая ацетилирование в жидкой фазе, которые могут быть использованы. В одном из воплощений пептид может быть циклизован перед отщеплением от пептидной смолы. Для циклизации посредством реакционноспособных группировок боковых цепей с желаемых боковых цепей снимают защиту, и пептид суспендируют в подходящем растворителе и добавляют циклический связывающий реагент. Подходящие растворители включают, например, DMF, дихлорметан (DCM) или 1-метил-2-пирролидон (NMP). Подходящие циклические связующие реагенты включают, например, тетрафторборат 2-(1 Н-бензотриазол-1-ил)-1,1,3,3-тетераметилурония (TBTU), гексафторфосфат 2-(1 Нбензотриазол-1-ил)-1,1,3,3-тетераметилурония (HBTU), гексафторфосфат бензотриазол-1-ил-окситрис(диметиламино)фосфония (ВОР), гексафторфосфат бензотриазол-1-ил-окси-трис(пирролидино) фосфония (РуВОР), тетрафторборат 2-(7-аза-1 Н-бензотриазол-1-ил)-1,1,3,3-тетраметилурония (TATU),тетрафторборат 2-(2-охо-1(2 Н)-пиридил)-1,1,3,3-тетраметилурония (TPTU) или N,N'-дициклогексилкарбодиимид-1-гидроксибензотриазол (DCCI/HOBt). Сочетание обычно инициируют путем использования подходящего основания, такого как N,N-диизопропилэтиламин (DIPEA), сим-коллидин или N-метилморфолин (NMM). Затем циклизованные пептиды могут быть отщеплены от твердой фазы с использованием любого подходящего реагента, такого как этиламин в DCM, или различных комбинаций агентов, таких как трифторуксусная кислота (TFA), триизопропилсилан (TIS), диметоксибензол (DMB), вода и тому подобные. Полученный неочищенный пептид сушат, а оставшиеся защитные группы аминокислотных боковых цепей, если таковые есть, отщепляют с использованием подходящего реагента, такого как TFA в присутствии воды, TIS, 2-меркаптопетан (ME) и/или 1,2-этандитиол (EDT). Конечный продукт осаждают путем добавления холодного эфира и собирают фильтрованием. Окончательную очистку осуществляют высокоэффективной жидкостной хроматографией с обращенной фазой (RP-HPLC) с использованием подходящей колонки, такой как колонка C18, или также могут быть использованы другие способы разделения или очистки, например способы, основанные на размере или заряде пептида. После очистки пептид может быть охарактеризован любым количеством методов, таких как высокоэффективная жидкостная хроматография (HPLC), аминокислотный анализ, масс-спектрометрия и тому подобными. Несмотря на то что синтез в основном описан путем ссылки на твердофазную Fmoc-химию, следует понимать, что для получения циклических пептидов по изобретению можно использовать другие химические процессы и способы синтеза, такие как, для примера и без ограничения, способы, использующие Вос-химию, химические процессы в растворе и другие химические процессы и способы синтеза. 6.0. Препараты. В зависимости от желаемого пути введения, препарат композиции, содержащей один или более циклических пептидов по настоящему изобретению, можно варьировать. Так, препарат может быть пригоден для подкожной инъекции или внутривенной инъекции, для местных применений, для глазных применений, для применений в качестве назального спрея, для ингаляционных применений, для других трансдермальных применений и тому подобного. 6.1. Солевая форма циклических пептидов по настоящему изобретению. Циклические пептиды по настоящему изобретению могут быть в форме любой фармацевтически приемлемой соли. Термин "фармацевтически приемлемые соли" относится к солям, полученным из фармацевтически приемлемых нетоксичных оснований или кислот, в том числе неорганических или органических оснований и неорганических или органических кислот. Соли, полученные из неорганических оснований, включают соли алюминия, аммония, кальция, меди, трехвалентного железа, двухвалентного железа, лития, магния, трехвалентного марганца, двухвалентного марганца, калия, натрия, цинка и тому подобных. Особенно предпочтительными являются соли аммония, кальция, лития, магния, калия и натрия. Соли, полученные из фармацевтически приемлемых органических нетоксичных оснований, включают соли первичных, вторичных и третичных аминов, замещенных аминов, в том числе природных замещенных аминов, циклических аминов, и основных ионообменных смол, таких как аргинин, бетаин,кофеин, холин, N,N'-дибензилэтилендиамин, диэтиламин, 2-диэтиламиноэтанол, 2-диметиламиноэтанол,этаноламин, этилендиамин, N-этилморфолин, N-этилпиперидин, глюкамин, глюкозамин, гистидин, гидрабамин, изопропиламин, лизин, метилглюкамин, морфолин, пиперазин, пиперидин, полиаминные смолы, прокаин, пурины, теобромин, триэтиламин, триметиламин, трипропиламин, трометамин и тому подобных.- 10018630 Если циклический пептид по настоящему изобретению является основным, то соли присоединения кислот могут быть получены из фармацевтически приемлемых нетоксичных кислот, в том числе неорганических и органических кислот. Такие кислоты включают уксусную, бензолсульфоновую, бензойную,камфорсульфоновую, карбоновую, лимонную, этансульфоновую, муравьиную, фумаровую, глюконовую,глутаминовую, бромистоводородную, соляную, изэтионовую, молочную, малеиновую, яблочную, миндальную, метансульфоновую, малоновую, муциновую, азотную, памовую, пантотеновую, фосфорную,пропионовую, янтарную, серную, винную, п-толуолсульфоновую, трифторуксусную кислоту и тому подобные. Соли присоединения кислот для пептидов по настоящему изобретению получают в подходящем растворителе из пептида и избытка кислоты, такой как соляная, бромистоводородная, серная, фосфорная,уксусная, трифторуксусная, лимонная, винная, малеиновая, янтарная и метансульфоновая кислота. Особенно полезными являются формы ацетатной соли, аммонийацетатной соли и соли трифторуксусной кислоты. В тех случаях, когда пептиды по настоящему изобретению содержат кислотную группировку,подходящие фармацевтически приемлемые соли могут включать соли щелочных металлов, такие как соли натрия или калия, или соли щелочно-земельных металлов, такие как соли кальция или магния. 6.2. Фармацевтические композиции. Согласно данному изобретению предложена фармацевтическая композиция, содержащая циклический пептид по настоящему изобретению и фармацевтически приемлемый носитель. Носитель может быть жидкой композицией, и предпочтительно является буферным, изотоническим, водным раствором. Фармацевтически приемлемые носители также включают эксципиенты, такие как разбавители, носители и тому подобные, и добавки, такие как стабилизирующие агенты, консерванты, солюбилизирующие агенты, буферы и тому подобные, как описано ниже. Композиции циклического пептида по настоящему изобретению могут быть изготовлены или составлены в виде фармацевтических композиций, содержащих по меньшей мере один циклический пептид по настоящему изобретению вместе с одним или более фармацевтически приемлемыми носителями,включая эксципиенты, такие как разбавители, носители и тому подобные, и добавки, такие как стабилизирующие агенты, консерванты, солюбилизирующие агенты, буферы и тому подобные, если они могут потребоваться. Эксципиенты препарата могут включать поливинилпирролидон, желатин, гидроксицеллюлозу, гуммиарабик, полиэтиленгликоль, маннит, хлорид натрия и цитрат натрия. Для инъекционных препаратов или других препаратов для жидкого введения предпочтительна вода,содержащая по меньшей мере один или более буферных компонентов; также могут быть использованы стабилизирующие агенты, консерванты и солюбилизирующие агенты. Для препаратов для твердого введения может быть использована любая из множества добавок, представляющих собой загуститель, наполнитель, объемообразующий агент и носитель, таких как крахмалы, сахара, жирные кислоты и тому подобные. Для препаратов, предназначенных для местного введения, может быть использован любой из множества кремов, мазей, гелей, лосьонов и тому подобных. Для большинства фармацевтических препаратов большую часть препарата, по массе или по объему, составляют неактивные ингредиенты. Для фармацевтических препаратов также предполагается, что могут быть использованы любые из множества препаратов и добавок для измеренного высвобождения, медленного высвобождения и высвобождения с выдержкой по времени, так что доза может быть изготовлена таким образом, чтобы осуществлять доставку пептида по настоящему изобретению в течение периода времени. В общем, фактическое количество циклических пептидов по настоящему изобретению, вводимое пациенту, можно варьировать в достаточно широких диапазонах в зависимости от режима введения, используемого препарата и желаемой реакции. При практическом применении циклические пептиды по изобретению можно смешивать в качестве активного ингредиента с фармацевтическим носителем согласно общепринятым фармацевтическим методам составления лекарственных средств. Носитель может принимать широкое множество форм в зависимости от требующейся для введения формы препарата, например пероральной, парентеральной (включая внутривенную), уретральной, вагинальной, ректальной, назальной, трансбуккальной, сублингвальной или тому подобной. При приготовлении композиций для пероральной лекарственной формы может быть использована(ы) любая(ые) из обычных фармацевтических сред, таких как, например, вода, гликоли,масла, спирты, корригенты, консерванты, красители и тому подобные, в случае пероральных жидких препаратов, таких как, например, суспензии, эликсиры и растворы; или носителей, таких как крахмалы,сахара, микрокристаллическая целлюлоза, разбавители, гранулирующие агенты, смазывающие вещества,связующие вещества, разрыхлители и тому подобные, в случае пероральных твердых препаратов, таких как, например, порошки, твердые и мягкие капсулы и таблетки. Благодаря своей легкости введения таблетки и капсулы представляют собой предпочтительные пероральные стандартные лекарственные формы. Если требуется, таблетки могут быть покрыты стандартными водными или неводными методами. Количество активного пептида в таких терапевтически полезных композициях является таким, при котором получают эффективную дозировку. В другой предпочтительной стандартной лекарственной форме могут быть использованы сублингвальные конструктивные элементы, такие как пластины, вафли, таблетки или тому подобные. Таблетки, пилюли, капсулы и тому подобные также могут содержать связующее вещество, такое- 11018630 как трагакантовая камедь, гуммиарабик, кукурузный крахмал или желатин; эксципиенты, такие как дикальцийфосфат; разрыхлитель, такой как кукурузный крахмал, картофельный крахмал или альгиновая кислота; смазывающее вещество, такое как стеарат магния; и подсластитель, такой как сахароза, лактоза или сахарин. Если стандартная лекарственная форма представляет собой капсулу, то она может содержать в дополнение к веществам указанного выше типа жидкий носитель, такой как жирное масло. В качестве покрытий или для модификации физической формы единицы дозирования могут быть использованы различные другие материалы. Например, таблетки могут быть покрыты шеллаком, сахаром или и тем, и другим. Сироп или эликсир может содержать в дополнение к активному ингредиенту сахарозу в качестве подсластителя, метил- и пропилпарабены в качестве консервантов, краситель и корригент, такой как вишневый или апельсиновый корригент. Циклические пептиды также можно вводить парентерально. Растворы или суспензии этих активных пептидов могут быть приготовлены в воде, соответствующим образом смешанной с поверхностноактивным веществом, таким как гидроксипропилцеллюлоза. Также могут быть приготовлены дисперсии в глицерине, жидких полиэтиленгликолях и их смесях. Эти препараты, возможно, могут содержать консерванты для предотвращения роста микроорганизмов. Фармацевтические формы, подходящие для применения путем инъекции, включают стерильные водные растворы или дисперсии и стерильные порошки для приготовления стерильных инъецируемых растворов или дисперсий для немедленного приема. Во всех случаях форма должна быть стерильной и должна быть достаточно жидкой для того, чтобы ее можно было ввести с помощью шприца. Форма должна быть стабильной в условиях производства и хранения и должна быть защищена от загрязняющего действия микроорганизмов, таких как бактерии и грибы. Носитель может представлять собой растворитель или дисперсионную среду, содержащую, например, воду, этанол, полиол, например глицерин,пропиленгликоль или жидкий полиэтиленгликоль, их подходящие смеси и растительные масла. Циклические пептиды по настоящему изобретению можно применять в терапевтических целях посредством назального введения. "Назальное введение" означает любую форму интраназального введения любого из циклических пептидов по настоящему изобретению. Пептиды могут находиться в водном растворе, таком как раствор, включающий солевые, цитратные или другие обычные эксципиенты или консерванты. Также пептиды могут входить в сухой или порошковый препарат. Циклические пептиды по настоящему изобретению могут быть приготовлены вместе с любым из множества агентов, которые увеличивают эффективную назальную абсорбцию лекарственных средств,включая пептидные лекарственные средства. Эти агенты должны увеличивать назальную абсорбцию без недопустимого повреждения слизистой оболочки. В патентах США 5693608, 5977070 и 5908825, среди прочих, указан ряд фармацевтических композиций, которые могут быть использованы, включающих усилители абсорбции, и идея каждого из указанных выше патентов и все ссылки и патенты, процитированные в них, включены путем ссылки. В водном растворе циклические пептиды могут быть соответствующим образом буферизованы посредством солевого, ацетатного, фосфатного, цитратного, ацетатного или других буферных агентов, которые могут привести к любому физиологически приемлемому рН, обычно от примерно рН 4 до примерно рН 7. Также может быть использована комбинация буферных агентов, например фосфатнобуферный солевой раствор, солевой и ацетатный буфер и тому подобные. В случае солевого раствора может быть использован 0,9%-ный солевой раствор. В случае ацетата, фосфата, цитрата и тому подобного может быть использован 50 мМ раствор. В дополнение к буферным агентам может быть использован подходящий консервант с целью предотвращения или ограничения роста бактерий и других микробов. Одним из таких консервантов, который может быть использован, является 0,05% хлорида бензалкония. В альтернативном воплощении циклические пептиды по настоящему изобретению можно вводить непосредственно в легкое. Внутрилегочное введение можно осуществлять посредством дозирующего ингалятора, устройства, позволяющего пациенту при вдыхании самостоятельно вводить отмеренную дозу пептида по настоящему изобретению при приведении устройства в действие. В одном из аспектов этого воплощения циклический пептид может быть в сухой форме в виде частиц, например частиц от примерно 0,5 до 0,6 мкм, так что частицы имеют массу, достаточную для того, чтобы лечь на поверхность легкого и не быть выдохнутыми, но являются довольно малыми, чтобы не осаждаться на поверхностях дыхательных путей до достижения легкого. Для получения микрочастиц сухого порошка может быть использована любая из множества различных методик, включая микроизмельчение, сушку распылением и быстрое замораживание аэрозоля с последующей лиофилизацией, но не ограничиваясь ими. Посредством микрочастиц пептиды могут осаждаться глубоко в легком, обеспечивая, тем самым, быструю и эффективную абсорбцию в кровоток. Кроме того, для такого подхода не требуется усилителей проницаемости, которые иногда желательны в случае трансдермального, назального или перорального,относящегося к слизистой оболочке путей доставки. Может быть использован любой из множества ингаляторов, включая аэрозоли на основе пропеллентов, небулайзеры, сухие порошковые ингаляторы с однократной дозой и многодозовые сухие порошковые ингаляторы. Распространенные в настоящее время устройства включают дозирующие ингаляторы, которые используют для доставки лекарств для лечения астмы, хронического обструктивного заболевания легких и тому подобного. Предпочтительные устрой- 12018630 ства включают сухие порошковые ингаляторы, разработанные для того, что сформировать облако или аэрозоль мелкодисперсного порошка с размером частиц, который всегда менее примерно 6,0 мкм. Размер микрочастиц, включая распределение среднего размера, можно контролировать посредством способа изготовления. Для микроизмельчения размер микрочастиц контролируют размером измельчающей головки, скоростью ротора, временем обработки и тому подобным. Для сушки распылением размер микрочастиц контролируют размером форсунки, скоростью потока, степенью нагрева сушилки и тому подобным. Для изготовления посредством быстрого замораживания аэрозоля с последующей лиофилизацией размер микрочастиц контролируют размером форсунки, скоростью потока, концентрацией распыляемого раствора и тому подобным. Эти и другие параметры могут быть использованы для контроля размера микрочастиц. Циклические пептиды по настоящему изобретению можно терапевтически вводить посредством инъекции, обычно глубокой внутримышечной инъекции, такой как в ягодичную или дельтовидную мышцу, инъецируемого препарата с высвобождением с выдержкой по времени. В одном из воплощений циклический пептид по настоящему изобретению приготовлен с полиэтиленгликолем, таким как полиэтиленгликоль 3350, и, возможно, с одним или более дополнительными эксципиентами и консервантами,включая такие эксципиенты, как соли, полисорбат 80, гидроксид натрия или соляная кислота для регулировки рН и тому подобные, но не ограничиваясь ими. В другом воплощении циклический пептид по настоящему изобретению приготовлен с поли(сложным ортоэфиром), который может представлять собой автокатализируемый поли(сложный ортоэфир) с любым переменным процентным содержанием молочной кислоты в скелете полимера и возможно одним или более дополнительными эксципиентами. В одном из воплощений применяют полимер поли(D,L-лактид-со-гликолид). В общем, любой из множества инъецируемых и биоразрушаемых полимеров, которые предпочтительно также являются адгезивными полимерами, можно применять в инъецируемом препарате с высвобождением с задержкой по времени. Препарат может быть таким, что инъекция будет требоваться еженедельно, ежемесячно или с другой периодичностью в зависимости от концентрации и количества циклического пептида, скорости биоразрушения полимера и других факторов, известных специалистам в области техники. 6.3. Пероральные препараты пептидов по настоящему изобретению. В одном из аспектов циклические пептиды по настоящему изобретению приготовлены для пероральной доставки. Пептид предпочтительно приготавливают и делают таким, чтобы он был покрыт энтеросолюбильным защитным веществом, более предпочтительно таким, чтобы он не высвободился до тех пор, пока таблетка или капсула не пройдет через желудок и, кроме того, возможно, не пройдет через часть тонкой кишки. В контексте этой заявки следует понимать, что термин "энтеросолюбильное покрытие или энтеросолюбильный материал" относится к покрытию или веществу, которое(ый) будет проходить через желудок, по существу, нетронутым, но будет быстро разрушаться в тонкой кишке, высвобождая активное лекарственное вещество. Один из растворов энтеросолюбильного покрытия, который может быть использован, содержит ацетатфталат целлюлозы и, возможно, другие ингредиенты, такие как гидроксид аммония, триацетин, этиловый спирт, метиленовый синий и очищенную воду. Ацетатфталат целлюлозы представляет собой полимер, который применяли в фармацевтической промышленности для энтеросолюбильного покрытия индивидуальных лекарственных форм, таких как таблетки и капсулы, и не растворяется в воде при рН менее чем примерно 5,8. Энтеросолюбильные покрытия, включающие ацетатфталат целлюлозы, обеспечивают защиту от кислой среды желудка, но начинают растворяться в среде двенадцатиперстной кишки (рН примерно 6-6,5) и полностью растворяются к тому времени, когда лекарственная форма достигнет подвздошной кишки (рН примерно 7-8). Кроме ацетатфталата целлюлозы известны другие энтеросолюбильные покрывающие материалы, и они могут быть использованы с пептидами по настоящему изобретению, включая сукцинат гидроксипропилметилцеллюлозы, фталат гидроксипропилметилцеллюлозы, фталат поливинилацетата и сополимер метакриловой кислоты и метилметакрилата, но не ограничиваясь ими. Используемое энтеросолюбильное покрытие содействует растворению лекарственной формы главным образом в месте за пределами желудка и может быть выбрано таким, чтобы оно растворялось при рН приблизительно по меньшей мере 6,0, более предпочтительно при рН от примерно 6,0 до примерно 8,0. В одном из предпочтительных аспектов энтеросолюбильное покрытие растворяется и разрушается вблизи подвздошной кишки. Любой из множества усилителей проникновения может быть использован для улучшения усвоения в кишечнике после растворения энтеросолюбильного покрытия. В одном из аспектов усилители проникновения увеличивают либо парацеллюлярную, либо трансцеллюлярную транспортную системы. Увеличение парацеллюлярного транспорта может быть достигнуто путем раскрытия плотных соединений клеток; увеличение трансцеллюлярного транспорта может быть достигнуто путем увеличения текучести клеточной мембраны. Типичные, неограничивающие примеры таких усилителей проникновения включают кальциевые хелаторы, соли желчных кислот (такие как холат натрия) и жирные кислоты. Пептиды по настоящему изобретению могут быть в индивидуальной лекарственной форме, покрытой энтеросолюбильным покрытием, которая включает жирную кислоту, такую как, например, олеат, пальмитат,стеарат, капрат натрия или конъюгированная линолевая кислота, в капсуле, покрытой энтеросолюбильным покрытием, для увеличения парацеллюлярного транспорта.- 13018630 В одном из аспектов индивидуальная лекарственная форма, такая как таблетка или капсула, возможно, дополнительно включает общепринятые фармацевтические связующие вещества, такие как повидон, разбавители, глиданты, наполнители, такие как микрокристаллическая целлюлоза, смазывающие вещества, такие как стеарат магния, разрыхлители, такие как кроскармеллоза натрия, консерванты, красители и тому подобные в их общеизвестных объемах и количествах. В некоторых воплощениях дополнительно добавляют пептиды или полипептиды, которые действуют в качестве субстратов для кишечных протеаз. 6.4. Пути введения. Если композицию, содержащую один или более пептидов по настоящему изобретению, вводят путем инъекции, то инъекция может быть внутривенной, подкожной, внутримышечной, интраперитонеальной или иной, известной в области техники. Пептиды по настоящему изобретению могут быть приготовлены в виде препарата любым из способов, известных в области техники, включая такие препараты, как таблетки, капсулы, каплеты, суспензии, порошки, лиофилизированные препараты, суппозитории, глазные капли, кожные пластыри, пероральные растворимые препараты, спреи, аэрозоли и тому подобные,но не ограничиваясь ими, и могут быть смешаны и приготовлены с буферами, связующими веществами,эксципиентами, стабилизаторами, антиоксидантами и другими агентами, известными в области техники. В общем, любой путь введения, посредством которого пептиды по изобретению вводятся через эпидермальный слой клеток, может быть использован. Таким образом, способы введения могут включать введение через слизистые оболочки, трансбуккальное введение, пероральное введение, дермальное введение, ингаляционное введение, назальное введение, уретральное введение, вагинальное введение, ректальное введение и тому подобное. 6.5 Терапевтически эффективное количество. В общем, фактическое количество пептида по настоящему изобретению, вводимого пациенту, вводимое пациенту, можно варьировать в достаточно широких пределах в зависимости от режима введения,используемого препарата и желаемой реакции. Дозировка для лечения представляет собой введение любым из упомянутых выше способов или любыми другими способами, известными в области техники,количества, достаточного для осуществления желаемого терапевтического эффекта. Таким образом, терапевтически эффективное количество включает количество пептида или фармацевтической композиции по настоящему изобретению, которое является достаточным для терапевтического смягчения сексуальной дисфункции пациента или для предупреждения или задержки появления или повторного проявления сексуальной дисфункции. В общем, циклические пептиды по настоящему изобретению являются высокоактивными. Например, циклический пептид можно вводить в дозе примерно 0,1, 0,5, 1, 5, 50, 100, 500, 1000, или 5000 мкг/кг массы тела, в зависимости от конкретного выбранного пептида, желаемой терапевтической реакции, пути введения, препарата и других факторов, известных специалистам в области техники. 7.0. Тесты и анализы, используемые при оценке пептидов по настоящему изобретению. Специфичные в отношении меланокортиновых рецепторов циклические пептиды по настоящему изобретению можно тестировать с помощью множества систем тестов и животных моделей для определения связывания, функционального состояния и эффективности. 7.1. Анализ конкурентного ингибирования с использованием [I125]-NDPMSH. Анализ конкурентного ингибирования связывания осуществляют с использованием мембранных гомогенатов, полученных из клеток НЕК-293, которые экспрессируют рекомбинантные hMC4-R, hMC3R или hMC5-R, и из клеток В-16 мышиной меланомы (содержащих эндогенный MC1-R). В некоторых случаях использовали клетки НЕК-293, которые экспрессируют рекомбинантный hMC1-R. В следующих ниже примерах все значения для МС 3-R, MC4-R и MC5-R относятся к человеческим рекомбинантным рецепторам. Значения для MC1-R относятся к клеткам В-16 мышиной меланомы, если заголовком не является "hMC1-R", в этом случае значение относится к человеческому рекомбинантному MC1-R. Анализы выполняли в 96-луночных GF/B Millipore Multiscreen фильтровальных планшетах (MAFB NOB10),предварительно покрытых 0,5% бычьим сывороточным альбумином (BSA) (фракция V). Мембранные гомогенаты инкубировали с 0,2 нМ (для hMC4-R), 0,4 нМ (для MC3-R и MC5-R) или 0,1 нМ (для мышиных В 16 MC1-R или hMC1-R) [I125]-NDPMSH (PerkinElmer) и возрастающими концентрациями циклических пептидов по настоящему изобретению в буфере, содержащем 25 мМ HEPES буфера (рН 7,5) с 100 мМ NaCl, 2 мМ CaCl2, 2 мМ MgCl2, 0,3 мМ 1,10-фенантролина и 0,2% бычьего сывороточного альбумина. После инкубации в течение 60 минут при 37 С анализируемую смесь фильтровали и мембраны промывали три раза ледяным буфером. Фильтры сушили и подсчитывали гамма-счетчиком на связанную радиоактивность. Неспецифическое связывание измеряли путем ингибирования связывания [I125]-NDP-MSH в присутствии 1 мкМ NDPMSH. Максимальное специфическое связывание (100%) определяли как разность радиоактивностей (имп/мин), связанных клеточными мембранами, в отсутствие и в присутствии 1 мкМ NDPMSH. Для определения процента ингибирования связывания [I125]-NDPMSH полученную в присутствии тестируемых соединений радиоактивность (имп/мин), нормализовали по отношению к 100%-ному специфическому связыванию. Каждый анализ проводили три раза, представлены- 14018630 фактические средние значения, результаты меньшие 0% представлены как 0%. Значения Ki для циклических пептидов по настоящему изобретению определяли с использованием программного обеспечения для подбора кривых Graph-Pad Prism. Представленные здесь данные для связывания hMC1-R и hMC4R, a также некоторые данные для hMC3-R, получены с использованием [I125]-NDPMSH. 7.2. Анализ конкурентного связывания с использованием Eu-NDPMSH. Альтернативно, анализ конкурентного ингибирования связывания осуществляли с помощью EuNDPMSH (PerkinElmer Life Sciences, каталожный No. AD0225) с использованием для измерений флуорометрии с временным разрешением (TRF) лантанидных хелатов. Такие же величины были получены для процента ингибирования и Ki в пределах погрешности эксперимента в сравнительных исследованиях с [I125]-NDPMSH. Как правило, конкурентные эксперименты по определению значений Ki проводили путем инкубации мембранных гомогенатов, полученных из клеток HEK-293, которые экспрессируют рекомбинантные hMC4-R, с 9 различными концентрациями циклических пептидов по настоящему изобретению и 1 нМ Eu-NDPMSH в растворе, содержащем 25 мМ HEPES буфера (рН 7,5) с 100 мМNaCl, 2 мМ CaCl2, 2 мМ MgCl2, 0,1% BSA и 0,3 мМ 1,10-фенантролина. После инкубации в течение 90 минут при 37 С реакцию останавливали путем фильтрования через 96-луночные фильтровальные планшеты AcroWell (Pall Life Sciences). Фильтровальные планшеты промывали 4 раза 200 мкл ледяного фосфатно-буферного солевого буфера. В каждую лунку добавляли раствор DELFIA Enhancement Solution(PerkinElmer Life Sciences). Планшеты инкубировали на шейкере в течение 15 минут и снимали показания при длине волны возбуждения 340 нм и длине волны излучения 615 нм. Каждый анализ проводили два раза, и использовали средние значения. Значения Ki определяли подбором кривых с помощью программного обеспечения Graph-Pad Prism, используя модель конкурентного связывания с фиксированным углом наклона кривой в одном месте. Представленные здесь данные для связывания hMC5-R и некоторые данные для hMC3-R и hMC4-R получены с использованием Eu-NDPMSH. 7.3. Анализ конкурентного связывания с использованием [I125]-AgRP (83-132). Исследования конкурентного связывания с помощью [I125]-AgRP (83-132) проводят с использованием мембранных гомогенатов, отделенных от клеток, которые экспрессируют hMC4-R. Анализы выполняли в 96-луночных GF/B Millipore Multiscreen фильтровальных планшетах (MAFB NOB10), предварительно покрытых 0,5% бычьим сывороточным альбумином (фракция V). Смесь для анализа содержала 25 мМ HEPES буфера (рН 7,5) с 100 мМ NaCl, 2 мМ CaCl2, 2 мМ MgCl2, 0,3 мМ 1,10-фенантролина и 0,5% бычьего сывороточного альбумина, мембранные гомогенаты, радиолиганд [I125]-AgRP (83-132) (PerkinElmer) и возрастающие концентрации пептидов по настоящему изобретению в суммарном объеме 200 мкл. Связывание измеряли при концентрациях радиолиганда 0,2 нМ. После инкубации в течение 1 часа при 37 С реакционную смесь фильтровали и промывали аналитическим буфером, содержащим 500 мМNaCl. Высушенные диски выталкивали из планшета и подсчитывали с помощью гамма-счетчика. Общее связывание радиолиганда не превышало 10% от количеств, добавленных к реакционной смеси. ЗначенияKi для циклических пептидов по настоящему изобретению определяли с использованием программного обеспечения для подбора кривых Graph-Pad Prism. 7.4. Анализ агонистической активности. Для измерения способности циклических пептидов по настоящему изобретению вызывать функциональный ответ в клетках HEK-293, которые экспрессируют MC4-R, изучают накопление внутриклеточного сАМР. Конфлюэнтные клетки HEK-293, которые экспрессируют рекомбинантный hMC4-R, отделяли от культуральных планшетов инкубацией в буфере для разделения клеток, не содержащем ферментов. Дисперсные клетки суспендировали в сбалансированном солевом растворе Эрла, содержащем 10 мМ HEPES (рН 7,5), 1 мМ MgCl, 1 мМ глютамина, 0,5% альбумина и 0,3 мМ 3-изобутил-1 метилксантина (IBMX), ингибитора фосфодиэстеразы. Клетки помещали в 96-луночные планшеты с плотностью 0,5105 клеток на лунку и предварительно инкубировали в течение 30 мин. Клетки подвергали воздействию в течение 1 часа при температуре 37 С для тестирования циклических пептидов по настоящему изобретению, растворенных в DMSO (диметилсульфоксид) (конечная концентрация DMSO 1%), в диапазоне концентраций 0,05-5000 нМ в суммарном объеме для анализа 200 мкл. В качестве стандартного агониста использовали NDPMSH. После окончания инкубационного периода клетки разрушали путем добавления 50 мкл лизирующего буфера (набор cAMP EIA, Amersham) с последующим энергичным пипетированием. Уровни сАМР в лизатах определяли с использованием набора cAMP EIA(Amersham). Анализ данных проводили путем нелинейного регрессионного анализа с программным обеспечением Graph-Pad Prism. Максимальные эффективности циклических пептидов по настоящему изобретению сравнивали с эффективностью, достигаемой стандартным меланокортиновым агонистомNDPMSH. 7.5. Изменение потребления пищи и массы тела. Для отобранных пептидов, вводимых путем внутривенной (IV) или подкожной инъекции, оценивают изменение в потреблении пищи и массе тела. Самцов крыс линии Sprague-Dawley получают от HilltopLab Animals, Inc. (Scottsdale, PA) или других поставщиков. Животных по одному помещают в обычные полистирольные подвесные клетки и поддерживают контролируемый световой цикл: 12 ч присутствия- 15018630 света /12 ч отсутствия света. Предоставляют свободный доступ к воде и гранулированному корму. Крысам IV путем дозируют разбавитель или отобранные пептиды (от 0,3 до 1,0 мг/кг) или подкожно вводят разбавитель или отобранные пептиды (в дозах до 30 мг/кг). Изменения в массе тела и потреблении пищи определяют в течение 24-часового периода после дозирования. Также измеряют изменения в массе тела и потреблении пищи в течение 48- и 72-часового периодов после дозирования для определения возврата изменений в массе тела и эффектов на потребление пищи назад к исходным уровням. 7.6. Возбуждение пенильной эрекции. Отобранные пептиды оценивают на способность пептидов по настоящему изобретению индуцировать пенильную эрекцию (РЕ) у самцов крыс. Самцов крыс линии Sprague-Dawley массой 250-300 г содержат при световом цикле: 12 ч присутствия света /12 ч отсутствия света со свободным доступом к корму и воде. Все поведенческие исследования проводят между 9 и 16 ч. Группам из 6-8 крыс IV путем вводят пептиды во множестве доз. Непосредственно после введения крыс помещают в индивидуальные полистирольные клетки (длиной 27 см, шириной 16 см и высотой 25 см) для наблюдения за их поведением, как правило, при помощи дистанционного видеоконтроля. За крысами наблюдают в течение одного часа и регистрируют количество зевков, актов груминга и РЕ в 10-минутные интервалы. 8.0. Пептиды по изобретению. Циклические пептиды, охватываемые формулой (I), содержат один или более асимметричных элементов, таких как стереогенные центры, стереогенные оси и тому подобные, так что пептиды, охватываемые формулой (I), могут существовать в различных стереоизомерных формах. Подразумевается, что в данное описание включены все формы изомеров по всем хиральным или другим центрам изомерии, в том числе энантиомеры и диастереомеры, как для конкретных пептидов, так и для пептидов, описанных в общем, включая пептиды, охватываемые формулой (I). Каждый из пептидов по изобретению содержит многочисленные хиральные центры и его можно применять в виде рацемической смеси или энантиомерно обогащенной смеси, в дополнение к применению пептидов по изобретению в энантиомерно чистых препаратах. Обычно пептиды по изобретению синтезируют с использованием хирально чистых реагентов, таких как конкретные L- или D-аминокислоты, используя реагенты, условия и способы, при которых сохраняется энантиомерная чистота, но допускается и предполагается, что могут быть получены рацемические смеси. Такие рацемические смеси, возможно, могут быть разделены с использованием хорошо известных методик, и индивидуальный энантиомер может быть использован по отдельности. В случаях и в условиях особых температур, растворителей и значений рН, при которых пептиды могут существовать в таутомерных формах, предполагается, что каждая таутомерная форма включена в это изобретение независимо от того, существует ли она в равновесии или преимущественно в одной форме. Таким образом,одиночный энантиомер пептида формулы (I), который представляет собой оптически активную форму,может быть получен асимметричным синтезом, синтезом из оптически чистых предшественников или разделением рацематов. Пептиды формулы (II) являются конкретными стереоизомерными формами пептидов формулы (I),но изобретение не следует толковать как ограниченное стереоизомерными формами, охватываемыми формулой (II). Кроме того, подразумевается, что изобретение включает пролекарства настоящих пептидов, которые после введения, прежде чем стать активными фармакологическими пептидами, претерпевают химическое превращение в ходе метаболических процессов. В общем, такие пролекарства являются функциональными производными настоящих пептидов, которые легко превращаются in vivo в пептид формулы(I). Пролекарства представляют собой любые ковалентно связанные соединения, которые высвобождают активное исходное пептидное лекарственное средство формулы (I) in vivo. Общепринятые способы выбора и получения подходящих пролекарственных производных описаны, например, в "Design of Prodrugs", ed. H. Bundgaard, Elsevier, 1985. Типичные примеры пролекарств имеют биологически лабильные защитные группы на функциональной группировке, такие как, например, в результате этерификации функциональных гидроксильных, карбоксильных или аминогрупп. Таким образом, в качестве примера и без ограничения, пролекарство включает пептиды формулы (I), где использована сложноэфирная пролекарственная форма, например, низшие сложные алкиловые эфиры R группы формулы (I), например, гдеR представляет собой -ОН, причем низшие сложные алкиловые эфиры могут включать от 1 до 8 углеродов в алкильном радикале, или аралкиловые сложные эфиры, которые имеют 6-12 углеродов в аралкильном радикале. В общих чертах, пролекарства включают соединения, которые могут быть окислены, восстановлены, аминированы, деаминированы, гидроксилированы, дегидроксилированы, гидролизованы,дегидролизованы, алкилированы, деалкилированы, ацилированы, деацилированы, фосфорилированы или дефосфорилированы для получения активного исходного пептидного лекарственного средства формулы(I) in vivo. Объект изобретения также включает пептиды, которые идентичны пептидам, представленным формулой (I), за исключением того, что один или более атомов в формуле (I) заменены атомом, имеющим атомную массу или массовое число, отличные от атомной массы или массового числа, обычно встречающихся в природе. Примеры изотопов, которые могут быть введены в соединения по изобретению,включают изотопы водорода, углерода, азота и кислорода, такие как 2 Н, 3 Н, 13 С, 14 С, 15N, 18O и 17 О, соот- 16018630 ветственно. Пептиды по настоящему изобретению и фармацевтически приемлемые соли или сольваты указанных соединений, которые содержат вышеупомянутые изотопы и/или другие изотопы других атомов, входят в объем этого изобретения. Некоторые меченные изотопами соединения по настоящему изобретению, например соединения, в которые введены такие радиоактивные изотопы, как 3 Н и 14 С, могут иметь применение во множестве анализов, например анализах распределения лекарственного средства и/или субстрата в тканях. Замещение более тяжелыми изотопами, такое как замещение одного или более атомов водорода дейтерием (2 Н), в некоторых случаях может предоставить фармакологические преимущества, включая повышенную метаболическую стабильность. Меченные изотопами пептиды формулы(I) обычно могут быть получены заменой немеченного изотопом реагента реагентом, меченным изотопом. 8.1. Синтезирован пептид следующей структуры: Этот пептид имеет аминокислотную последовательность Ac-Arg-cyclo(Asp-Dab-D-Phe-Arg-TrpLys)-NH2. Циклический пептид Примера 8.1 получили в формах ацетатной (АсОН) соли и соли трифторуксусной кислоты (TFA). Циклический пептид Примера 8.1 имеет молекулярную формулу C48H71N17O9 и рассчитанную молекулярную массу 1030,19. Молекулярная масса циклического пептида примера 8.1 в форме ацетатной соли составила 1210,34; в форме соли TFA составила 1372,25. Циклический пептид примера 8.1 оценивали в отношении связывания MC1-R, MC3-R, MC4-R иMC5-R в конкурентных исследованиях с использованием NDPMSH, и было обнаружено, что он является селективным для MC4-R и имеет значение Ki 4,0 нМ к MC4-R (средняя величина четырех анализов),значение Ki 9 нМ для MC1-R (средняя величина пяти анализов), значение Ki 150 нМ к MC3-R (средняя величина двух анализов) и значение Ki 2270 нМ к MC5-R (средняя величина двух анализов). В ходе функциональных исследований было установлено, что циклический пептид примера 8.1 является агонистом MC4-R с внутренней активностью 91% к MC4-R, причем NDPMSH принимают за 100%, и с EC50 0,3 нМ (средняя величина пяти анализов). В ходе исследований пенильной эрекции у крыс с использованием бремеланотида (неспецифический MC4-R агонист формулы Ac-Nle-cyclo(Asp-His-D-Phe-Arg-Trp-Lys)-OH) в качестве положительного контроля было обнаружено, что на крысиной модели циклический пептид примера 8.1 привел к статистически значимому увеличению наблюдаемых спонтанных эрекций по сравнению с контролями разбавителя. Разбавитель, введенный отдельно подкожным путем, привел к среднему числу спонтанных эрекций 0,4290,202 у крысы за один час (n = 7), тогда как циклический пептид примера 8.1, введенный подкожно, в дозе 0,3 мг/кг привел к среднему числу спонтанных эрекций 2,2860,286 у крысы за один час(n = 7), а в дозе 1,0 мг/кг привел к среднему числу спонтанных эрекций 4,5711,088 у крысы за один час(n = 7). Положительный контроль, бремеланотид, введенный IV в дозе 1 мг/кг, привел к среднему числу спонтанных эрекций 40,535 у крысы за один час (n = 7). На крысиных моделях систолического кровяного давления с использованием хирургически имплантированных телеметрически управляемых датчиков неожиданно было обнаружено преимущество циклического пептида примера 8.1, заключающееся в том, что он привел к меньшему увеличению систолического кровяного давления по сравнению с бремеланотидом в дозе, приводящей к сравнимым результатам при исследованиях пенильной эрекции. На фиг. 1 представлены результаты перекрестных исследований с использованием 8 животных с имплантированными датчиками, получавших циклический пептид примера 8.1 в дозах 0,84 мкмоль/кг и 3,0 мкмоль/кг подкожной инъекцией и бремеланотид в дозе 1 мкмоль/кг IV инъекцией, где сопутствующие исследования показали, что результаты пенильной эрекции у крысы в час при тех же самых дозах и путях введения являются такими же или выше у циклического пептида примера 8.1 в дозе 3,0 мкмоль/кг, чем у бремеланотида в дозе 1 мкмоль/кг. В других исследованиях, включая сопоставления одинаковых количеств циклического пептида примера 8.1 и бремеланотида при введении одинаковыми путями, были получены, по существу, сходные результаты. 8.2. Синтезирован пептид следующей структуры: Этот пептид имеет аминокислотную последовательность Ас-Arg-cyclo(Asp-Dab-D-Phe-Arg-TrpLys)-OH. Циклический пептид примера 8.2 получили в форме соли TFA. Циклический пептид примера 8.2 имеет молекулярную формулу C48H70N16O10 и рассчитанную молекулярную массу 1031,17. Молекулярная масса циклического пептида Примера 8.2 в форме соли TFA составила 1373,23. Циклический пептид примера 8.2 оценивали в отношении связывания MC1-R, MC3-R, MC4-R иMC5-R в конкурентных исследованиях с использованием NDPMSH, и было обнаружено, что он является селективным для MC4-R и имеет значение Ki 57 нМ к MC4-R (средняя величина двух анализов),значение Ki 234 нМ для MC1-R (средняя величина трех анализов), значение Ki 5804 нМ для MC3-R(средняя величина двух анализов) и значение Ki более 10000 нМ для MC5-R (средняя величина двух анализов). В ходе функциональных исследований было установлено, что циклический пептид примера 8.1 является агонистом MC4-R с внутренней активностью 91% к МС 4-R, причем NDPMSH принимают за 100%, и с ЕС 50 4 нМ (средняя величина четырех анализов). 8.3. Синтезирован пептид следующей структуры: Этот пептид имеет аминокислотную последовательность Ас-Arg-cyclo(Glu-Dab-D-Phe-Arg-TrpOrn)-NH2. Циклический пептид примера 8.3 получили в форме соли TFA. Циклический пептид примера 8.3 имеет молекулярную формулу C48H71N17O9 и рассчитанную молекулярную массу 1030,19. Молекулярная масса циклического пептида примера 8.3 в форме соли TFA составила 1372,25. Циклический пептид примера 8.3 оценивали в отношении связывания MC1-R, MC3-R, MC4-R иMC5-R в конкурентных исследованиях с использованием NDPMSH, и было обнаружено, что он имеет значение Ki 0,65 нМ к MC4-R (средняя величина двух анализов), значение Ki 1 нМ для MC1-R (средняя величина трех анализов), значение Ki 74 нМ для MC3-R (средняя величина двух анализов) и значение Ki 300 нМ для MC5-R (средняя величина двух анализов). В ходе функциональных исследований было установлено, что циклический пептид примера 8.3 является агонистом MC4-R с внутренней активностью 94% к MC4-R, причем NDPMSH принимают за 100%, и с ЕС 50 0,3 нМ (средняя величина пяти анализов). 8.4. Синтезирован пептид следующей структуры: Этот пептид имеет аминокислотную последовательность Ac-Arg-cyclo(Glu-Dab-D-Phe-Arg-TrpOrn)-OH. Циклический пептид примера 8.4 получили в формах ацетатной соли и соли TFA. Циклический пептид примера 8.4 имеет молекулярную формулу C48H70N16O10 и рассчитанную молекулярную массу 1031,17. Молекулярная масса циклического пептида примера 8.4 в форме ацетатной соли составила 1211,32; в форме соли TFA составила 1373,23.- 18018630 Циклический пептид примера 8.4 оценивали в отношении связывания MC1-R, MC3-R, MC4-R иMC5-R в конкурентных исследованиях с использованием NDPMSH, и было обнаружено, что он имеет значение Ki 8 нМ к MC4-R (средняя величина двух анализов), значение Ki 4 нМ для МС 1-R (один анализ), значение Ki 410 нМ для MC3-R (один анализ) и значение Ki 2366 нМ для MC5-R (средняя величина двух анализов). В ходе функциональных исследований было установлено, что циклический пептид Примера 8.4 является агонистом MC4-R с внутренней активностью 91% к МС 4-R, причем NDPMSH принимают за 100%, и с EC50 3 нМ (средняя величина девяти анализов). В ходе исследований пенильной эрекции у крыс с использованием бремеланотида в качестве положительного контроля было обнаружено, что на крысиной модели циклический пептид примера 8.4 привел к статистически значимому увеличению наблюдаемых спонтанных эрекций по сравнению с контролями разбавителя. Разбавитель, введенный отдельно подкожным путем, привел к среднему числу спонтанных эрекций 0,4290,202 у крысы за один час (n = 7), тогда как циклический пептид примера 8.4,введенный подкожно в дозе 0,3 мг/кг привел к среднему числу спонтанных эрекций 2,5710,685 у крысы за один час (n = 7), а в дозе 1,0 мг/кг привел к среднему числу спонтанных эрекций 5,2860,918 у крысы за один час (n = 7). Положительный контроль, бремеланотид, введенный IV в дозе 1 мг/кг привел к среднему числу спонтанных эрекций 40,535 у крысы за один час (n = 7). На крысиных моделях систолического кровяного давления с использованием хирургически имплантированных телеметрически управляемых датчиков неожиданно было обнаружено преимущество циклического пептида примера 8.4, заключающееся в том, что он привел к меньшему увеличению систолического кровяного давления по сравнению с бремеланотидом в дозе, приводящей к сравнимым результатам при исследованиях пенильной эрекции. На фиг. 2 представлены результаты перекрестных исследований с использованием 8 животных с имплантированными датчиками, получавших циклический пептид Примера 8.4 в дозе 1 мг/кг подкожной инъекцией и бремеланотид в дозе 1 мг/кг IV инъекцией, где сопутствующие исследования показали, что результаты пенильной эрекции у крысы в час при тех же самых дозах и путях введения являются такими же или выше у циклического пептида примера 8.4 в дозе 1 мг/кг, чем у бремеланотида в дозе 1 мг/кг. В других исследованиях, включая сопоставления одинаковых количеств циклического пептида примера 8.1 и бремеланотида при введении одинаковыми путями, были получены, по существу, сходные результаты. Несмотря на то что изобретение подробно описано с конкретной ссылкой на предпочтительные воплощения, в других воплощениях могут быть достигнуты такие же результаты. Изменения и модификации настоящего изобретения очевидны специалистам в области техники, и подразумевается, что настоящее изобретение охватывает все такие модификации и эквиваленты. Полные описания всех ссылок, заявок, патентов и публикаций, процитированных выше, включены путем ссылки.- 24018630 ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Циклический пептид формулы (I) включая все его энантиомеры, стереоизомеры или диастереоизомеры или фармацевтически приемлемую соль любого из вышеупомянутого, гдеR представляет собой -С(=О)-ОН или -C(=O)-NH2; х равен 1 или 2 и у равен 3 или 4. 2. Циклический пептид по п.1 формулы (II) 3. Циклический пептид по п.1, представляющий собой Ac-Arg-cyclo(Asp-Dab-D-Phe-Arg-Trp-Lys)NH2 (SEQ ID NO:4). 4. Циклический пептид по п.1, представляющий собой Ac-Arg-cyclo(Glu-Dab-D-Phe-Arg-Trp-Orn)OH (SEQ ID NO:7). 5. Фармацевтическая композиция для лечения заболевания, симптома, состояния или синдрома,опосредованного меланокортиновыми рецепторами, у человека или млекопитающего, не являющегося человеком, содержащая циклический пептид или его фармацевтически приемлемую соль по п.1 и фармацевтически приемлемый носитель.
МПК / Метки
МПК: A61K 38/00, A61K 31/44, C07K 14/685
Метки: рецепторам, меланокортиновым, дисфункции, специфичные, сексуальной, пептиды, лечения
Код ссылки
<a href="https://eas.patents.su/27-18630-specifichnye-k-melanokortinovym-receptoram-peptidy-dlya-lecheniya-seksualnojj-disfunkcii.html" rel="bookmark" title="База патентов Евразийского Союза">Специфичные к меланокортиновым рецепторам пептиды для лечения сексуальной дисфункции</a>
Предыдущий патент: Производные фенил- и бензодиоксинилзамещенных индазолов
Следующий патент: Способ и система для очистки воды и генерирования водяного пара
Случайный патент: Способ идентификации сектора, мобильная станция и система мобильной связи