Способ лечения ожирения, стимулирования потери массы тела и снижения аппетита с использованием производных бензоконденсированного гетероциклического сульфамида
Формула / Реферат
1. Способ лечения ожирения, стимулирования потери массы тела или снижения аппетита, включающий введение субъекту терапевтически эффективного количества соединения формулы (I)
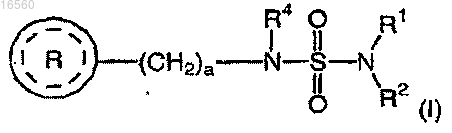
где R1 и R2, каждый независимо, выбирают из группы, включающей водород и (С1-4)алкил;
R4 выбирают из группы, включающей водород и (С1-4)алкил;
а означает целое число 1 или 2;

выбирают из группы, включающей
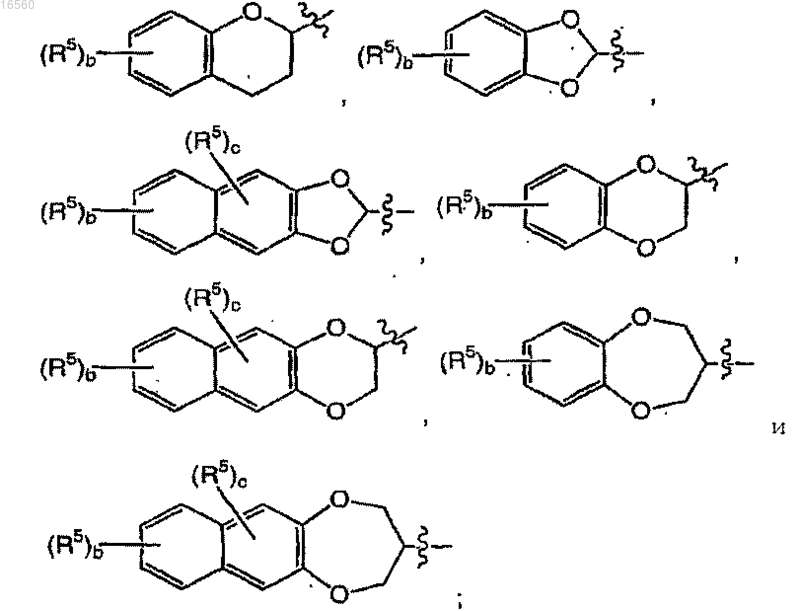
где b означает целое число от 0 до 4, с означает целое число от 0 до 2;
каждый R5 независимо выбирают из группы, включающей галоген, (С3-4)алкил и нитро;
при условии, что когда
означает
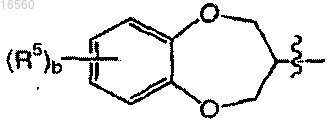
или
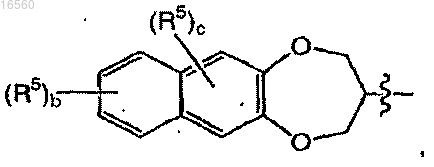
а равно 1;
или его фармацевтически приемлемой соли.
2. Способ по п.1, в котором в соединении формулы I R1 и R2, каждый независимо, выбирают из группы, включающей водород и (C1-4) алкил;
R4 выбирают из группы, включающей водород и (C1-4)алкил;
а означает целое число 1 или 2;

выбирают из группы, включающей
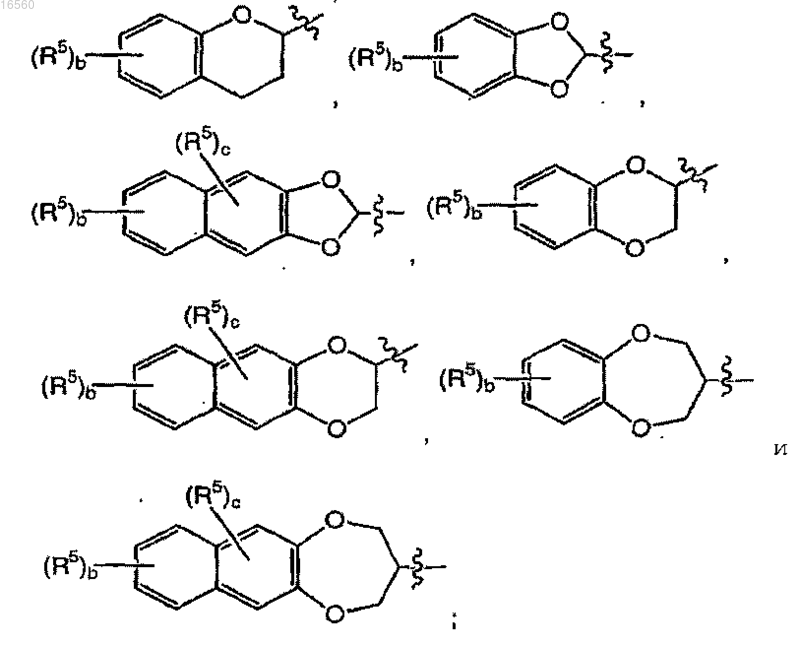
где b означает целое число 1 или 2, с означает целое число от 0 до 1;
каждый R5 независимо выбирают из группы, включающей галоген, (С1-4)алкил и нитро;
при условии, что когда
означает

а равно 1;
или это соединение формулы I вводят в виде фармацевтически приемлемой соли.
3. Способ по п.2, в котором в соединении формулы I
R1 и R2, каждый независимо, выбирают из группы, включающей водород и (C1-4)алкил;
R4 выбирают из группы, включающей водород и (C1-4)алкил;
а означает целое число 1 или 2;

выбирают из группы, включающей
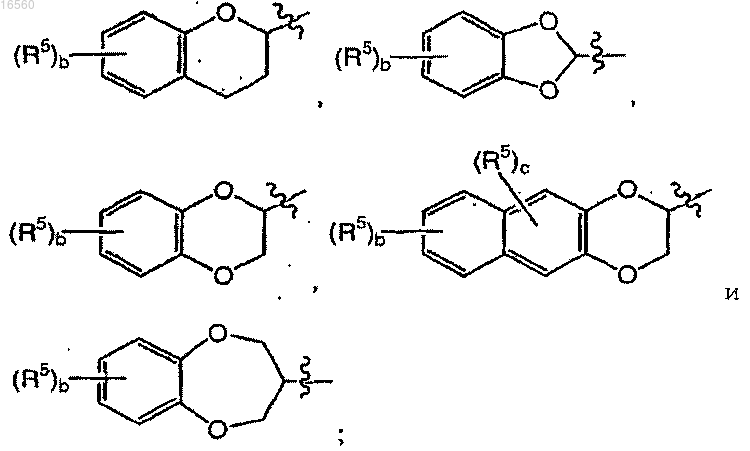
где b означает целое число 1 или 2, с означает 0;
каждый R5 независимо выбирают из группы, включающей галоген, (C1-4)алкил и нитро;
при условии, что когда
означает
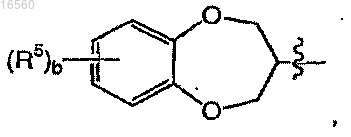
а равно 1;
или это соединение формулы I вводят в виде фармацевтически приемлемой соли.
4. Способ по п.3, в котором в соединении формулы I
R1 и R2, каждый независимо, выбирают из группы, включающей водород и (C1-4)алкил;
R4 выбирают из группы, включающей водород и метил;
а означает целое число 1 или 2;

выбирают из группы, включающей
2-(2,3-дигидробензо[1,4]диоксинил),
2-(бензо[1,3]диоксолил),
2-(3,4-дигидро-2Н-бензо[1,4]диоксепинил),
2-(2,3-дигидробензо[1,4]диоксинил),
2-(6-хлор-2,3-дигидробензо[1,4]диоксинил),
2-(6-фтор-2,3-дигидробензо[1,4]диоксинил),
2-(хроманил),
2-(5-фтор-2,3-дигидробензо[1,4]диоксинил),
2-(7-хлор-2,3-дигидробензо[1,4]диоксинил),
2-(6-хлорбензо[1,3]диоксолил),
2-(7-нитро-2,3-дигидробензо[1,4]диоксинил),
2-(7-метил-2,3-дигидробензо[1,4]диоксинил),
2-(5-хлор-2,3-дигидробензо[1,4]диоксинил),
2-(6-бром-2,3-дигидробензо[1,4]диоксинил),
2-(6,7-дихлор-2,3-дигидробензо[1,4]диоксинил),
2-(8-хлор-2,3-дигидробензо[1,4]диоксинил),
2-(2,3-дигидронафто[2,3-b][1,4]диоксинил) и
2-(4-метилбензо[1,3]диоксолил);
при условии, что когда
означает 2-(3,4-дигидро-2Н-бензо[1,4]диоксепинил), а равно 1;
или это соединение формулы I вводят в виде фармацевтически приемлемой соли.
5. Способ по п.4, в котором в соединении формулы I R1 и R2, каждый независимо, выбирают из группы, включающей водород и метил;
R4 выбирают из группы, включающей водород и метил;
а означает целое число 1 или 2;

выбирают из группы, включающей
2-(бензо[1,3]диоксолил),
2-(2,3-дигидробензо[1,4]диоксинил),
2-(2,3-дигидробензо[1,4]диоксинил),
2-(6-хлор-2,3-дигидробензо[1,4]диоксинил),
2-(7-хлор-2,3-дигидробензо[1,4]диоксинил),
2-(7-метил-2,3-дигидробензо[1,4]диоксинил),
2-(6-бром-2,3-дигидробензо[1,4]диоксинил) и
2-(6,7-дихлор-2,3-дигидробензо[1,4]диоксинил);
или это соединение формулы I вводят в виде фармацевтически приемлемой соли.
6. Способ по п.1, в котором соединение формулы (I) представляет собой (2S)-(-)-N-(6-хлор-2,3-дигидробензо[1,4]-диоксин-2-илметил)сульфамид и его фармацевтически приемлемую соль .
7. Способ лечения ожирения, включающий введение субъекту терапевтически эффективного количества соединения, представляющего собой (2S)-(-)-N-(6-хлор-2,3-дигидробензо[1,4]диоксин-2-илметил)сульфамид и его фармацевтически приемлемой соли.
8. Способ стимулирования потери массы тела, включающий введение субъекту терапевтически эффективного количества соединения, представляющего собой (2S)-(-)-N-(6-хлор-2,3-дигидробензо[1,4]диоксин-2-илметил)сульфамид, и его фармацевтически приемлемой соли.
9. Способ снижения аппетита, включающий введение субъекту терапевтически эффективного количества соединения, представляющего собой (2S)-(-)-N-(6-хлор-2,3-дигидробензо[1,4]диоксин-2-илметил)сульфамид, и его фармацевтически приемлемой соли.
10. Способ лечения ожирения, стимулирования потери массы тела или снижения аппетита, включающий введение субъекту терапевтически эффективного количества соединения формулы (II)
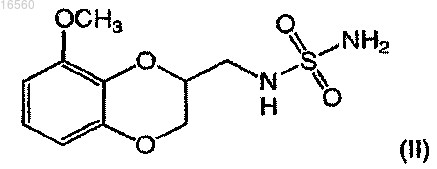
или его фармацевтически приемлемой соли.
Текст
СПОСОБ ЛЕЧЕНИЯ ОЖИРЕНИЯ, СТИМУЛИРОВАНИЯ ПОТЕРИ МАССЫ ТЕЛА И СНИЖЕНИЯ АППЕТИТА С ИСПОЛЬЗОВАНИЕМ ПРОИЗВОДНЫХ БЕНЗОКОНДЕНСИРОВАННОГО ГЕТЕРОЦИКЛИЧЕСКОГО СУЛЬФАМИДА Настоящее изобретение относится к способу лечения ожирения, стимулирования потери массы тела и/или снижения аппетита, который включает введение нуждающемуся в этом субъекту терапевтически эффективного количества одного или нескольких новых производных бензоконденсированного гетероциклического сульфамида формулы (I), представленных в настоящем описании изобретения. 016560 Область техники, к которой относится изобретение Настоящее изобретение относится к применению производных бензоконденсированного гетероциклического сульфамида для лечения ожирения, стимулирования потери массы тела и/или снижения аппетита. Уровень техники Ожирение представляет собой состояние, характеризующееся избыточной массой жировой ткани. Несмотря на то что ожирение часто считается эквивалентом повышенной массы тела, это не всегда является верным, так как у худых, но мускулистых людей может быть избыточная масса тела в соответствии с произвольными стандартами при отсутствии ожирения. Показатели массы тела у населения постоянно меняются, так что обоснованное с медицинской точки зрения различие между худобой и ожирением является в некоторой степени произвольным. Поэтому ожирение можно более эффективно определить по показателям заболеваемости или смертности. Наиболее широко применяемым методом измерения ожирения, который нельзя считать прямым показателем ожирения, является индекс массы тела (BMI), равный массе тела/рост 2 (в кг/м 2). Другие методы количественного определения ожирения включают антропометрию (измерение толщины кожных складок), денсиметрию (подводное взвешивание), компьютерную томографию (СТ), магнитнорезонанскую томографию (MRI) или электрический импеданс. На основании данных таблиц жизни в столице индексы массы тела (BMI) для средних значений роста и телосложения как у мужчин, так и у женщин находятся в пределах от 19 до 26 кг/м 2; при одинаковых значениях BMI женщины имеют больше жировой ткани, чем мужчины. С учетом точных данных заболеваемости индекс массы тела, равный 30, обычно считается порогом ожирения у мужчин и женщин. Широкомасштабные эпидемиологические исследования позволяют предположить, что заболеваемость болезнями обмена веществ и сердечнососудистыми болезнями, возникающими по разным причинам, повышается (хотя и медленно) при индексе массы тела 25, из чего следует, что пороговая точка ожирения должна быть снижена. Некоторые специалисты используют термин "избыточная масса тела" (вместо ожирения) для определения лиц с индексами массы тела в пределах от 25 или 27 до 30. Индекс массы тела от 25 до 30 следует рассматривать как показатель, значимый в медицинском отношении и требующий терапевтического вмешательства, особенно при наличии факторов риска, на которые влияет ожирение, таких как гипертензия и непереносимость глюкозы. Данные, недавно полученные в результате исследования питания и здоровья нации (NHANES), показывают, что процентное значение взрослого населения Америки, страдающего ожирением (BMI30),увеличилось с 14,5% (в период с 1976 по 1980 г.) до 22,5% (в период с 1998 по 2004 г.). В период с 1998 по 2001 г. у 50% взрослого населения США в возрасте 20 лет была обнаружена избыточная масса тела(определяемая в виде BMI25). Так как у многих лиц с BMI от 25 до 30 существуют значительные проблемы со здоровьем, особого внимания заслуживает все большее распространение значимого в медицинском отношении ожирения. Ожирение чаще встречается у женщин и в бедных слоях общества; постоянно возрастающее распространение ожирения у детей также вызывает беспокойство. Ожирение вредно влияет на здоровье. Заболеваемость лиц, страдающих ожирением (200% от идеальной массы тела), вызывает 20-кратное увеличение смертности. Коэффициенты смертности возрастают по мере увеличения ожирения, в частности, в тех случаях, когда ожирение связано с увеличением внутрибрюшинного жира (см. выше). Кроме того, очевидно, что на степень поражения ожирением определенных органов влияют гены подверженности, которые являются различными у населения. Для указанных лиц характерен 50-100% повышенный риск преждевременной смерти по любым причинам по сравнению с лицами, имеющими нормальную массу тела. В США с ожирением может быть связано более 300000 смертей в год. Существует потребность в эффективном лечении ожирения. Сущность изобретения Настоящее изобретение относится к способу лечения ожирения, стимулирования потери массы тела и/или снижения аппетита, который включает введение нуждающемуся субъекту терапевтически эффективного количества соединения формулы (I)R4 выбирают из группы, включающей водород и (С 1-4)алкил; а означает целое число от 1 до 2; выбирают из группы, включающей где b означает целое число от 0 до 4 и с означает целое число от 0 до 2; каждый R5 независимо выбирают из группы, включающей галоген, (С 1-4)алкил и нитро; при условии, что когда тогда а равно 1; или его фармацевтически приемлемой соли. Настоящее изобретение далее относится к способу лечения ожирения, потери массы тела и/или снижения аппетита, который включает введение нуждающемуся субъекту терапевтически эффективного количества соединения формулы (II) или его фармацевтически приемлемой соли. Показана возможность применения настоящего изобретения в способе лечения ожирения, стимулирования потери массы тела и/или снижения аппетита, который включает совместную терапию с использованием терапевтически эффективного количества по крайней мере одного средства, стимулирующего потерю массы тела, и/или по крайней мере одного средства, снижающего аппетит, и соединения формулы (I) или формулы (II) по настоящему изобретению. Один вариант применения настоящего изобретеия относится к способу лечения ожирения и/или стимулирования потери массы тела, который включает совместную терапию с использованием по крайней мере одного средства, стимулирующего потерю массы тела, и соединения формулы (I) по настоящему изобретению, предпочтительно соединения 8, представленного в настоящем описании изобретения. В качестве примера, иллюстрирующего настоящее изобретение, приведен способ лечения ожирения, включающий введение нуждающемуся субъекту терапевтически эффективного количества любого из вышеописанных соединений. Другой пример осуществления изобретения относится к способу стимулирования потери массы тела, который включает введение нуждающемуся субъекту терапевтически эффективного количества любого из вышеописанных соединений. Другой пример осуществления изобретения относится к способу снижения аппетита, который включает введение нуждающемуся субъекту терапевтически эффективного количества любого из вышеописанных соединений. В качестве еще одного примера, иллюстрирующего настоящее изобретение, приведен способ задержки опорожнения желудка,-2 016560 который включает введение нуждающемуся субъекту терапевтически эффективного количества любого из соединений, рассмотренных в настоящем описании изобретения. Подробное описание изобретения Настоящее изобретение относится к способу лечения ожирения, стимулирования потери массы тела и/или снижения аппетита, который включает введение нуждающемуся субъекту терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли, где а R1, R2 и R4 имеют значения, указанные в настоящем описании изобретения. Настоящее изобретение далее относится к способу задержки опорожнения желудка, который включает введение нуждающемуся субъекту терапевтически эффективного количества любых соединений,рассмотренных в настоящем описании изобретения. Настоящее изобретение далее относится к лечению ожирения, которое включает совместное введение нуждающемуся субъекту терапевтически эффективного количества по крайней мере одного средства, стимулирующего потерю массы тела, и/или по крайней мере одного средства, снижающего аппетит, и соединения формулы (I) или формулы (II) по настоящему изобретению. Один из вариантов осуществления настоящего изобретения относится к способам лечения ожирения, которые включают введение нуждающемуся субъекту терапевтически эффективного количества вышеописанных соединений формулы (I) или (II) или их фармацевтически приемлемых солей, при этом потеря массы тела происходит за счет жира и в более предпочтительном варианте осуществления изобретения за счет белой жировой ткани. Один из вариантов осуществления настоящего изобретения относится к способам стимулирования потери массы тела, которые включают введение субъекту, нуждающемуся в потере массы тела или желающему похудеть, терапевтически эффективного количества вышеописанных соединений формулы (I) или (II) или их фармацевтически приемлемых солей, при этом потеря массы тела происходит за счет жира и в более предпочтительном варианте осуществления изобретения за счет белой жировой ткани. В используемом здесь значении термин "ожирение" определяется как индекс массы тела (BMI),равный примерно 25, предпочтительно выше или равный примерно 30. Таким образом, в используемом здесь значении термин "ожирение" относится как к субъектам с избыточной массой тела, так ик субъектам, страдающим клиническим ожирением. В используемом здесь значении термин "средство, стимулирующее потерю массы тела" означает любое лекарственное средство, которое стимулирует потерю массы тела. Приемлемые примеры включают, не ограничиваясь ими, римонабант, орлистат, сибутрамин, мазиндол, бензфетамин, фенметразин,фентермин, диэтилпропион, мазиндол, фенилпропаноламин, эфедрин, хипазин, флуоксетин, сертралин,фенфлурамин, дексфенфлурамин, апоморфин, эксендин, дегидроэпиандростерон, этиохоландион, тестостерон, оксандролон, топирамат и тому подобные. Средство, стимулирующее потерю массы тела, предпочтительно является римонабантом, топираматом, орлистатом или сибутрамином. Аналогичным образом в используемом здесь значении термин "средство, снижающее аппетит" означает любое лекарственное средство или естественный продукт, снижающий аппетит, включающее, не ограничиваясь ими, средства, снижающие аппетит, которые действуют через адренергические механизмы, такие как бензфетамин, фенметразин, фентермин, диэтилпропион, мазиндол, сибутрамин, фенилпропаноламин или эфедрин; средства, снижающие аппетит, которые действуют через серотонергические механизмы, такие как хипазин, флуоксетин, сертралин, фенфлурамин или дексфенфлурамин; средства, снижающие аппетит,которые действуют через допаминовые механизмы, такие как, например, апоморфин; средства, снижающие аппетит, которые действуют через гистаминергические механизмы (например, миметики гистамина,модуляторы рецептора Н 3); усилители потребления энергии, такие как адренергические агонисты бета-3 и стимуляторы функции несвязывающего белка; лептин и миметики лептина; антагонисты нейропептидаY; модуляторы рецепторов меланокортина-1, 3 и 4; агонисты холецистокинина; миметики и аналоги глюкагоноподобного пептида-1 (GLP-1) (например, эксендин); андрогены (например, дегидроэпиандростерон и его производные, такие как этиохоландион), тестостерон, анаболические стероиды (например,оксандролон) и стероидные гормоны; антагонисты рецептора галанина; цитокины, такие как цилиарный нейротрофический фактор; ингибиторы амилазы; агонисты/миметики энтеростатина; антагонисты орексина/гипокретина; антагонисты урокортина; агонисты бомбезина; модуляторы протеинкиназы А; миметики фактора высвобождения кортикотропина; миметики кокаин- и амфетаминрегулируемого транскрипта; миметики пептида, относящегося к гену кальцитонина; и ингибиторы синтазы жирной кислоты. Термин "субъект" в используемом здесь значении означает животное, предпочтительно млекопитающее, наиболее предпочтительно человека, который является объектом лечения, наблюдения или ис-3 016560 следования. Термин "терапевтически эффективное количество" в используемом здесь значении означает такое количество активного соединения или лекарственного средства, которое вызывает биологическую или медицинскую реакцию в системе ткани, у животного или человека, предполагаемую исследователем,ветеринаром, лечащим врачом или другим клиницистом, и включает ослабление симптомов заболевания или нарушения, подвергаемого лечению. Применительно к совместной или комбинированной терапии, включающей введение одного или нескольких соединений формулы (I) или формулы (II) и одного или нескольких средств, стимулирующих потерю массы тела, и/или по крайней мере одного средства, снижающего аппетит, термин "терапевтически эффективное количество" означает такое количество комбинации вместе взятых средств, объединенное действие которых вызывает требуемую биологическую или медицинскую реакцию. Например, терапевтически эффективное количество в случае совместной терапии, включающей введение соединения формулы (I) или формулы (II) и по крайней мере одного средства, стимулирующего потерю массы тела,и/или по крайней мере одного средства, снижающего аппетит, представляет собой такое количество соединения формулы (I) или формулы (II) и количество средства, стимулирующего потерю массы тела,и/или по крайней мере одного средства, снижающего аппетит, которое при совместном или последовательном введении оказывает объединенное терапевтически эффективное действие. Кроме того, специалисту в данной области должно быть известно, что в случае совместной терапии с использованием терапевтически эффективного количества, указанного в приведенном выше примере, количество соединения формулы (I) или формулы (II) и/или количество средства, стимулирующего потерю массы тела, и/или по крайней мере одного средства, снижающего аппетит, может быть или не быть терапевтически эффективным. В используемом здесь значении термины "совместная терапия" и "комбинированная терапия" означают лечение нуждающегося субъекта путем введения одного или нескольких соединений формулы (I) или формулы (II) в комбинации с одним или несколькими средствами, стимулирующими потерю массы тела, и/или средствами, снижающими аппетит, при этом соединения формулы (I) или формулы (II) и средство, стимулирующее потерю массы тела, и/или средство, снижающее аппетит, вводят любым приемлемым способом одновременно, последовательно, раздельно или в одном фармацевтическом препарате. Когда соединения формулы (I) или формулы (II), средство, стимулирующее потерю массы тела, и/или средство, снижающее аппетит, вводят в разных лекарственных формах, число доз, вводимых в сутки, для каждого соединения может быть одинаковым или разным. Соединения формулы (I) или формулы (II),средство, стимулирующее потерю массы тела, и/или средство, снижающее аппетит, можно вводить одинаковыми или разными способами введения. Примеры приемлемых способов введения включают, не ограничиваясь ими, оральное, внутривенное (iv), внутримышечное (im), подкожное (sc), чрескожное и ректальное введение. Соединения могут быть также введены непосредственно в нервную систему такими способами введения, которые включают, не ограничиваясь ими, интрацеребральное, интравентрикулярное, интрацеребровентрикулярное, интратекальное, внутриполостное, интраспинальное и/или периспинальное введение при помощи игл и/или катетеров для внутричерепного или интравертебрального введения с использованием насосных устройств или без них. Соединения формулы (I) или формулы (II),средство, стимулирующее потерю массы тела, и/или средство, снижающее аппетит, могут быть введены в соответствии с одновременной или поочередной схемой введения в одно или разное время в течение всего курса лечения, одновременно в виде раздельных или общих лекарственных форм. В одном из вариантов осуществления настоящего изобретения R1 выбирают из группы, включающей водород и метил. В другом варианте осуществления настоящего изобретения R2 выбирают из группы, включающей водород и метил. В другом варианте осуществления настоящего изобретения оба R1 иR2 означают водород или оба R1 и R2 означают метил. В одном из вариантов осуществления настоящего изобретения -(СН 2)a- выбирают из группы, включающей -СН 2- и -СН 2-СН 2-. В другом варианте осуществления настоящего изобретения -(СН 2)a означает СН 2- . В одном из вариантов осуществления настоящего изобретения R4 выбирают из группы, включающей водород и метил, причем R4 предпочтительно является водородом. В одном из вариантов осуществления настоящего изобретения а означает 1. В одном из вариантов осуществления настоящего изобретения b означает целое число от 0 до 2. В другом варианте осуществления настоящего изобретения с означает целое число от 0 до 2. В другом варианте осуществления настоящего изобретения b означает целое число от 0 до 1. В другом варианте осуществления настоящего изобретения с означает целое число от 0 до 1. В другом варианте осуществления настоящего изобретения сумма b и с равна целому числу от 0 до 2, предпочтительно целому числу от 0 до 1. В другом варианте осуществления настоящего изобретения b означает целое число от 0 до 2 и с равно 0. В одном из вариантов осуществления настоящего изобретения В другом из вариантов осуществления настоящего изобретения В одном варианте осуществления настоящего изобретения выбирают из группы, включающей 2-(2,3-дигидробензо[1,4]диоксинил),2-(бензо[1,3]диоксолил),3-(3,4-дигидробензо[1,4]диоксепинил),2-(6-хлор-2,3-дигидробензо[1,4]диоксинил),2-(6-фтор-2,3-дигидробензо[1,4]диоксинил),2-(хроманил),2-(5-фтор-2,3-дигидробензо[1,4]диоксинил),2-(7-хлор-2,3-дигидробензо[1,4]диоксинил),2-(6-хлорбензо[1,3]диоксолил),2-(7-нитро-2,3-дигидробензо[1,4]диоксинил),2-(7-метил-2,3-дигидробензо[1,4]диоксинил),2-(5-хлор-2,3-дигидробензо[1,4]диоксинил),2-(6-бром-2,3-дигидробензо[1,4]диоксинил),2-(6,7-дихлор-2,3-дигидробензо[1,4]диоксинил),2-(8-хлор-2,3-дигидробензо[1,4]диоксинил),2-(2,3-дигидронафто[2,3-b][1,4]диоксинил) и 2-(4-метилбензо[1,3]диоксолил). В другом варианте осуществления настоящего изобретения выбирают из группы, включающей 2-(бензо[1,3]диоксолил),2-(2,3-дигидробензо[1,4]диоксинил),2-(6-хлор-2,3-дигидробензо[1,4]диоксинил),2-(7-хлор-2,3-дигидробензо[1,4]диоксинил),2-(7-метил-2,3-дигидробензо[1,4]диоксинил),2-(6-бром-2,3-дигидробензо[1,4]диоксинил) и 2-(6,7-дихлор-2,3-дигидробензо[1,4]диоксинил). В другом варианте осуществления настоящего изобретения выбирают из группы, включающей 2-(2,3-дигидробензо[1,4]диоксинил),2-(7-метил-2,3-дигидробензо[1,4]диоксинил) и 2-(6-бром-2,3-дигидробензо[1,4]диоксинил). В одном из вариантов осуществления настоящего изобретения R5 выбирают из группы, включающей галоген и низший алкил. В другом варианте осуществления настоящего изобретения R5 выбирают из группы, включающей хлор, фтор, бром и метил.-5 016560 В одном из вариантов осуществления настоящего изобретения стереоцентр соединения формулы (I) находится в S-конфигурации. В другом варианте осуществления настоящего изобретения стереоцентр соединения формулы (I) находится в R-конфигурации. В одном из вариантов осуществления настоящего изобретения соединение формулы (I) присутствует в виде энантиомерно обогащенной смеси, в которой % энантиомерного обогащения (% ее) превышает примерно 75%, предпочтительно примерно 90%, более предпочтительно примерно 95%, наиболее предпочтительно примерно 98%. Дополнительными вариантами осуществления настоящего изобретения являются варианты, в которых заместители, выбираемые для одной или нескольких указанных переменных (то есть R1, R2, R3, R4,X-Y и А), являются любым отдельным заместителем или любой подгруппой заместителей, выбираемых из полного списка, приведенного в настоящем описании изобретения. Типичные соединения по настоящему изобретению приведены в нижеследующей табл. 1. Дополнительные соединения по настоящему изобретению приведены в табл. 3. В нижеследующих табл. 1 и 2 в колонке, озаглавленной "стерео", указана стереоконфигурация у атома углерода гетероцикла, присоединенного в месте отмеченной звездочкой связи. Отсутствие обозначения показывает, что соединение было получено в виде смеси стереоконфигураций. Обозначение "R" или "S" показывает, что стереоконфигурация была получена с использованием энантиомерно обогащенного исходного вещества. Таблица 1. Типичные соединения формулы (I) Таблица 2. Дополнительные соединения по настоящему изобретению Термин "галоген" в используемом здесь значении за исключением особо оговоренных случаев означает хлор, бром, фтор и йод. Термин "алкил" в используемом здесь значении за исключением особо оговоренных случаев означает прямые и разветвленные цепи как в виде отдельной группы, так и в виде части замещающей группы. Например, алкильные радикалы включают метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил,трет-бутил, пентил и тому подобные. За исключением особо оговоренных сучаев термин "низший" применительно к алкилу означает углеродную цепь, состоящую из 1-4 атомов углерода. Термин "алкокси" в используемом здесь значении за исключением особо оговоренных случаев означает замещенный кислородом эфирный радикал вышеуказанных алкильных групп с прямой или разветвленной цепью. Например, метокси, этокси, н-пропокси, втор-бутокси, трет-бутокси, н-гексилокси и тому подобные. Обозначение в используемом здесь значении означает наличие стереогенного центра."Замещенная" группа (например, алкил, арил и т.д.) может иметь один или несколько заместителей,предпочтительно от одного до пяти заместителей, более предпочтительно от одного до трех заместителей, наиболее предпочтительно от одного до двух заместителей, независимо выбираемых из перечня заместителей. Термин "независимо" применительно к заместителям означает, что при наличии более одного заместителя такие заместители могут иметь одинаковые или разные значения. В стандартной номенклатуре, используемой в настоящем описании изобретения, первой указана концевая часть обозначенной боковой цепи, затем функциональная группа, расположенная рядом с точ-7 016560 кой присоединения. Так, например, "фенилалкиламинокарбонилалкильный" заместитель означает группу формулы В настоящем описании изобретения на схемах и в примерах использованы следующие аббревиатуры: Соединения по настоящему изобретению, имеющие по крайней мере один хиральный центр, могут существовать в виде энантиомеров. Соединения, имеющие два или более хиральных центров, могут дополнительно существовать в виде диастереомеров. Очевидно, что все такие изомеры и их смеси входят в объем настоящего изобретения. Кроме того, некоторые кристаллические формы указанных соединений могут существовать в виде полиморфов, которые входят в объем настоящего изобретения. Некоторые соединения могут образовывать сольваты с водой (то есть гидраты) или с обычными органическими растворителями, и такие сольваты также входят в объем настоящего изобретения. Соли соединений по настоящему изобретению, предназначенные для использования в медицине,являются нетоксичными "фармацевтически приемлемыми солями". Однако другие соли могут быть также пригодны для получения соединений по настоящему изобретению или их фармацевтически приемлемых солей. Фармацевтически приемлемые соли соединений включают кислотно-аддитивные соли, которые, например, могут быть получены путем смешивания раствора соединения с раствором фармацевтически приемлемой кислоты, такой как хлористо-водородная кислота, серная кислота, фумаровая кислота,малеиновая кислота, янтарная кислота, уксусная кислота, бензойная кислота, лимонная кислота, винная кислота, угольная кислота или фосфорная кислота. Кроме того, фармацевтически приемлемые соли соединений по настоящему изобретению, содержащих кислотную часть, могут включать соли щелочных металлов, например соли натрия или калия; соли щелочно-земельных металлов, например соли кальция или магния; и соли, образованные приемлемыми органическими лигандами, например соли четвертичного аммония. Таким образом, типичные фармацевтически приемлемые соли включают ацетат, бензол-8 016560 сульфонат, бензоат, бикарбонат, бисульфат, битартрат, борат, бромид, эдетат кальция, камсилат, карбонат, хлорид, клавуланат, цитрат, дигидрохлорид, эдетат, эдисилат, эстолат, эзилат, фумарат, глюцептат,глюконат, глутамат, гликолиларсанилат, гексилрезорцинат, гидрабамин, гидробромид, гидрохлорид,гидроксинафтоат, иодид, изотионат, лактат, лактобионат, лаурат, малат, малеат, манделат, мезилат, метилбромид, метилнитрат, метилсульфат, мукат, напсилат, нитрат, аммониевая соль N-метилглюкамина,олеат, памоат (эмбонат), пальмитат, пантотенат, фосфат/дифосфат, полигалактуронат, салицилат, стеарат, сульфат, субацетат, сукцинат, таннат, тартрат, теоклат, тозилат, триэтиодид и валерат. Типичные кислоты и основания, которые могут быть использованы при получении фармацевтически приемлемых солей, включают кислоты, такие как уксусная кислота, 2,2-дихлоруксусная кислота,ацилированные аминокислоты, адипиновая кислота, альгиновая кислота, аскорбиновая кислота, Lаспарагиновая кислота, бензолсульфоновая кислота, бензойная кислота, 4-ацетамидобензойная кислота,(+)-камфорная кислота, камфорсульфоновая кислота, (+)-(1S)-камфор-10-сульфоновая кислота, каприновая кислота, капроновая кислота, каприловая кислота, коричная кислота, лимонная кислота, цикламовая кислота, додецилсерная кислота, этан-1,2-дисульфоновая кислота, этансульфоновая кислота, 2 гидроксиэтансульфоновая кислота, муравьиная кислота, фумаровая кислота, галактаровая кислота, гентизиновая кислота, глюкогептоновая кислота, D-глюконовая кислота, D-глюкуроновая кислота, Lглутаминовая кислота, -оксоглутаровая кислота, гликолевая килота, гиппуровая кислота, бромистоводородная кислота, хлористо-водородная кислота, (+)-L-молочная кислота, (+)-DL-молочная кислота,лактобионовая кислота, малеиновая кислота, (-)-L-яблочная кислота, малоновая кислота, -DLминдальная кислота, метансульфоновая кислота, нафталин-2-сульфоновая кислота, нафталин-1,5 дисульфоновая кислота, 1-гидрокси-2-нафтойная кислота, никотиновая кислота, азотная кислота, олеиновая кислота, оротовая кислота, щавелевая кислота, пальмитиновая кислота, памовая кислота, фосфорная кислота, L-пироглутаминовая кислота, салициловая кислота, 4-аминосалициловая кислота, себациновая кислота, стеариновая кислота, янтарная кислота, серная кислота, дубильная кислота, (+)-L-винная кислота, тиоциановая кислота, п-толуолсульфоновая кислота и ундециленовая кислота; и основания, такие как аммиак, L-аргинин, бенэтамин, бензатин, гидроксид кальция, холин, деанол,диэтаноламин, диэтиламин, 2-(диэтиламино)этанол, этаноламин, этилендиамин, N-метилглюкамин, гидрабамин, 1 Н-имидазол, L-лизин, гидроксид магния, 4-(2-гидроксиэтил)морфолин, пиперазин, гидроксид калия, 1-(2-гидроксиэтил)пирролидин, вторичный амин, гидроксид натрия, триэтаноламин, трометамин и гидроксид цинка. Соединения формулы (I) могут быть получены способом, показанным на схеме 1. Схема 1 Соответствующим образом замещенное соединение формулы (X), известное соединение или соединение, полученное известными методами, подвергают взаимодействию с сульфамидом, известным соединением, предпочтительно в количестве от около 2 до около 5 эквивалентов, в органическом растворителе, таком как ТГФ, диоксан и тому подобные, предпочтительно при повышенной температуре в интервале от около 50 до около 100 С, более предпочтительно примерно при температуре рефлюкса, получая при этом соответствующее соединение формулы (Ia). Альтернативно соответствующим образом замещенное соединение формулы (X), известное соединение или соединение, полученное известными методами, подвергают взаимодействию с соответствующим образом замещенным соединением формулы (XI), известным соединением или соединением, полученным известными методами, в присутствии основания, такого как TEA, DIPEA, пиридин и тому подобные, в органическом растворителе, таком как ДМФА, ДМСО и тому подобные, получая при этом соответствующее соединение формулы (I). Соединение формулы (X), в котором может быть получено способом, показанным на схеме 2. Схема 2 Соответствующим образом замещенное соединение формулы (XII), известное соединение или соединение, полученное известным методом (например, как показано на схеме 2, выше), подвергают взаимодействию с NH4OH, известным соединением, необязательно в органическом растворителе, таком как ацетонитрил и тому подобные, получая при этом соответствующее соединение формулы (XIII). Соединение формулы (XIII) подвергают взаимодействию с правильно выбранным восстановителем,таким как LAH и тому подобные, в органическом растворителе, таком как ТГФ, диэтиловый эфир и тому подобные, получая при этом соответствующее соединение формулы (Ха). Соединения формулы (X), в которых могут быть получены способом, показанным на схеме 3. Схема 3 Соответствующим образом замещенное соединение формулы (XIV), известное соединение или соединение, полученное известными методами, подвергают взаимодействию с NH4OH в присутствии связующего вещества, такого как DCC и тому подобные, необязательно в органическом растворителе, таком как ацетонитрил и тому подобные, получая при этом соответствующее соединение формулы (XV). Соединение формулы (XV) подвергают взаимодействию с правильно выбранным восстановителем,таким как LAH и тому подобные, в органическом растворителе, таком как ТГФ, диэтиловый эфир и тому подобные, получая при этом соответствующее соединение формулы (Хb). Соединения формулы (X), в которых и а равно 2, могут быть получены способом, показанным на схеме 4. Соответствующим образом замещенное соединение формулы (XVI), в котором J1 означает приемлемую удаляемую группу, такую как Br, Cl, I, тозил, мезил, трифлил и тому подобные, известное соединение или соединение, полученное известными методами (например, путем активации соответствующего соединения, в котором J1 означает ОН), подвергают взаимодействию с цианидом, таким как цианид калия, цианид натрия и тому подобные, в органическом растворителе, таком как ДМСО, ДМФА, ТГФ и тому подобные, получая при этом соответствующее соединение формулы (XVII). Соединение формулы (XVII) восстанавливают известными методами, например, в результате взаимодействия с приемлемым восстановителем, таким как LAH, боран и тому подобные, получая при этом соответствующее соединение формулы (Хс). Соединения формулы (X) , в которых и а равно 1, могут быть получены способом, показанным на схеме 5. Схема 5 Соответствующим образом замещенное соединение формулы (XVIII), известное соединение или соединение, полученное известными методами, активируют известным методом, получая при этом соответствующее соединение формулы (XIX), в котором J2 означает приемлемую удаляемую группу, такую как тозилат, Cl, Br, I, мезилат, трифлат и тому подобные. Соединение формулы (XIX) подвергают взаимодействию с солью фталимида, такой как фталимид калия, фталимид натрия и тому подобные, в органическом растворителе, таком как ДМФА, ДМСО, ацетонитрил и тому подобные, предпочтительно при повышенной температуре в интервале от 50 до около 200 С, более предпочтительно примерно при температуре рефлюкса, получая при этом соответствующее соединение формулы (XX). Соединение формулы (XX) подвергают взаимодействию с N2H4, известным соединением, в органическом растворителе, таком как этанол, метанол и тому подобные, предпочтительно при повышенной температуре в интервале от около 50 до около 100 С, более предпочтительно примерно при температуре рефлюкса, получая при этом соответствующее соединение формулы (Xd). Специалисту в данной области должно быть известно, что соединения формулы (X), в которых могут быть получены известными методами или, например, способами, показанными на приведенных выше схемах 2-5, путем выбора и замены бензоконденсированных исходных веществ соответствующими нафтилконденсированными соединениями. Специалисту в данной области должно быть также известно, что при желании получить один энантиомер (или смесь энантиомеров, в которой один энантиомер присутствует в большем количестве) соединения формулы (X) вышеуказанные способы, показанные на схемах 1-5, могут быть выполнены при замене исходного вещества соответствующим одним энантиомером (или смесью энантиомеров, в которой один энантиомер присутствует в большем количестве). Специалисту в данной области должно быть известно, что в том случае, когда стадия реакции по настоящему изобретению может быть выполнена в разных растворителях или системах растворителей,указанная стадия реакции может быть также выполнена в смеси приемлемых растворителей или систем растворителей. Когда в результате выполнения способов по настоящему изобретению образуется смесь стереоизомеров, указанные изомеры могут быть разделены стандартными методами, такими как препаративная хроматография. Указанные соединения могут быть получены в рацемической форме, либо отдельные энантиомеры могут быть получены в результате энантиоспецифического синтеза или разделения. Например, соединения могут быть разделены на отдельные энантиомеры стандартными методами, такими как образование диастереомерных пар в результате образования соли с оптически активной кислотой,такой как (-)-ди-п-толуоил-D-винная кислота и/или (+)-ди-п-толуоил-L-винная кислота, с последующей фракционированной кристаллизацией и восстановлением свободного основания. Указанные соединения могут быть также разделены путем образования диастереомерных сложных эфиров или амидов с последующим хроматографическим разделением и удалением хирального вспомогательного соединения. Альтернативно указанные соединения могут быть разделены при помощи колонки для хиральной HPLC. При выполнении способов получения соединений по настоящему изобретению может быть необходимо и/или желательно защитить чувствительные или реакционноспособные группы в любых рассматриваемых молекулах. Подобная защита может быть обеспечена при помощи стандартных защитных групп, аналогичных описанным в публикациях Protective Groups in Organic Chemistry, ed. J.F.W. McOmie,Plenum Press, 1973; и T.W. GreeneP.G.M. Wuts, Protective Groups in Organic Synthesis, John WileySons, 1991. Защитные группы могут быть удалены на последующей стадии методами, известными в данной области. Фармацевтические композиции, содержащие одно или несколько соединений по настоящему изобретению в качестве активного ингредиента, могут быть получены путем тщательного смешивания одного или нескольких соединений с фармацевтическим носителем при помощи стандартных фармацевтических методов смешивания. Носитель может быть в любой форме в зависимости от требуемого способа введения (например, орального, парентерального). Таким образом, приемлемыми носителями и добавками для жидких препаратов для орального введения, таких как суспензии, эликсиры и растворы, являются вода, гликоли, масла, спирты, ароматизаторы, консерванты, стабилизаторы, красители и тому подобные; приемлемыми носителями и добавками для твердых препаратов для орального введения, таких как порошки, капсулы и таблетки, являются крахмалы, сахара, разбавители, гранулирующие вещества, смазывающие вещества, связывающие вещества, дезинтеграторы и тому подобные. На твердые препараты для орального введения может быть также нанесено покрытие такими веществами, как сахара или энтеросолюбильное покрытие, которое позволяет модулировать основное место абсорбции. Носитель для парентерального введения обычно включает стерильную воду с добавлением других ингредиентов, используемых для улучшения растворимости или консервации. Инъецируемые суспензии или растворы могут- 12016560 быть также получены с использованием водных носителей вместе с соответствующими добавками. Для получения фармацевтических композиций одно или несколько соединений по настоящему изобретению, используемых в качестве активного ингредиента, тщательно смешивают с фармацевтическим носителем при помощи стандартных фармацевтических методов смешивания, при этом носитель может быть использован в разных формах в зависимости от формы препарата, предназначенного для введения,например, для орального или парентерального введения, такого как внутримышечное введение. При получении композиций в виде лекарственной формы для орального введения могут быть использованы любые обычные фармацевтические среды. Таким образом, приемлемые носители и добавки для жидких препаратов для орального введения, таких как, например, суспензии, эликсиры и растворы, включают воду, гликоли, масла, спирты, ароматизаторы, консерванты, красители и тому подобные; приемлемые носители и добавки для твердых препаратов для орального введения, таких как, например, порошки, капсулы, драже, леденцы и таблетки, включают крахмалы, сахара, разбавители, гранулирующие вещества,смазывающие вещества, связывающие вещества, дезинтеграторы и тому подобные. Благодаря простоте введения таблетки и капсулы являются наиболее предпочтительными лекарственными формами для орального введения, в которых использованы твердые фармацевтические носители. При желании на таблетки может быть нанесено покрытие из сахара или энтеросолюбильное покрытие стандартными методами. В препаратах для парентерального введения носителем обычно является стерильная вода, хотя могут быть использованы и другие ингредиенты, например, для улучшения растворимости или консервирования. Могут быть также получены инъецируемые суспензии, в которых могут быть использованы соответствующие жидкие носители, суспендирующие агенты и тому подобные. Фармацевтические композиции по настоящему изобретению содержат в одной лекарственной форме, такой как таблетка, капсула,порошок, инъецируемый препарат, чайная ложка и тому подобные, такое количество активного ингредиента, которое необходимо для доставки эффективной дозы в соответствии с приведенным выше описанием. Фармацевтические композиции содержат в одной лекарственной форме, такой как таблетка, капсула, порошок, инъецируемый препарат, суппозиторий, чайная ложка и тому подобные, около 0,1-1000 мг и могут быть введены в дозе около 0,01-200,0 мг/кг/сутки, предпочтительно около 0,1-100 мг/кг/сутки,более предпочтительно около 0,5-50 мг/кг/сутки, более предпочтительно около 1,0-25,0 мг/кг/сутки, более предпочтительно около 0,5-10,0 мг/кг/сутки, наиболее предпочтительно от около 1,0 до около 5,0 мг/кг/сутки или в любой другой дозе в указанном диапазоне. Дозы, однако, могут изменяться в зависимости от потребности субъектов, тяжести подлежащего лечению состояния и используемого соединения. Препараты по настоящему изобретению можно вводить ежедневно или периодически. Указанные композиции предпочтительно получают в виде стандартных лекарственных форм, таких как таблетки, пилюли, капсулы, порошки, гранулы, стерильные растворы или суспензии для парентерального введения, дозируемый аэрозоль или жидкие распыляемые растворы, капли, ампулы, автоинжекторы или суппозитории, для орального, парентерального, назального, подъязычного или ректального введения либо для введения путем ингаляции или инсуффляции. Альтернативно композиция может быть получена в форме, пригодной для введения один раз в неделю или один раз в месяц; например, нерастворимая соль активного соединения, такая как деканоат, может быть использована для получения препарата-депо для внутримышечного введения. Для получения твердых композиций, таких как таблетки, основной активный ингредиент смешивают с фармацевтическим носителем, например, со стандартными таблетирующими ингредиентами, такими как кукурузный крахмал, лактоза, сахароза, сорбит, тальк,стеариновая кислота, стеарат магния, дикальцийфосфат или камеди, и другими фармацевтическими разбавителями, такими как вода, с образованием твердой предварительной композиции, содержащей гомогенную смесь соединения по настоящему изобретению или его фармацевтически приемлемой соли. Указанные предварительные композиции считаются гомогенными, если активный ингредиент равномерно распределен во всей композиции, поэтому указанная композиция может быть легко разделена на одинаково эффективные лекарственные формы, такие как таблетки, пилюли и капсулы. Указанную твердую предварительную композицию делят на стандартные лекарственные формы вышеописанного типа, содержащие от 0,1 до около 1000 мг активного ингредиента по настоящему изобретению. На таблетки или пилюли из новой композиции может быть нанесено покрытие для получения лекарственной формы пролонгированного действия. Например, таблетка или пилюля может содержать внутренний компонент и наружный компонент, причем последний компонент в виде оболочки, закрывающей первый компонент. Оба компонента могут быть разделены энтеросолюбильным слоем, который препятствует дезинтеграции в желудке и позволяет внутреннему компоненту пройти в интактном состоянии в двенадцатиперстную кишку или отсрочить его высвобождение. Такие энтеросолюбильные слои или покрытия могут быть изготовлены из разных материалов, которые включают ряд полимерных кислот с такими веществами, как шеллак, цетиловый спирт и ацетат целлюлозы. Жидкие формы, которые могут содержать новые композиции по настоящему изобретению, предназначенные для орального или парентерального введения, включают водные растворы, ароматизированные сиропы, водные или масляные суспензии, ароматизированные эмульсии и эликсиры, полученные с использованием съедобных масел, таких как хлопковое масло, кунжутное масло, кокосовое масло или арахисовое масло и подобные фармацевтические наполнители. Приемлемые диспергирующие или сус- 13016560 пендирующие агенты для водных суспензий включают синтетические и природные камеди, такие как трагакант, аравийская камедь, альгинат, декстран, натрийкарбоксиметилцеллюлоза, метилцеллюлоза,поливинилпирролидон или желатин. Суточная доза продуктов может изменяться в широких пределах от 0,01 до 150 мг/кг взрослого человека в сутки. Композиции для орального введения предпочтительно получают в форме таблеток, содержащих 0,01, 0,05, 0,1, 0,5, 1,0, 2,5, 5,0, 10,0, 15,0, 25,0, 50,0, 100, 150, 200, 250, 500 и 1000 мг активного ингредиента для симптоматического регулирования дозы, вводимой подлежащему лечению субъекту. Эффективное количество лекарственного средства обычно вводят в дозе от около 0,01 до около 1500 мг/кг массы тела в сутки. Предпочтительный диапазон находится в пределах от около 0,1 до около 100,0 мг/кг массы тела в сутки, более предпочтительно от около 0,5 до около 50 мг/кг, еще предпочтительнее от около 1,0 до около 25,0 мг/кг массы тела в сутки. Соединения по настоящему изобретению можно вводить 1-4 раза в сутки. Специалисты в данной области могут легко определить оптимальные дозы, которые могут изменяться в зависимости от конкретного используемого соединения, способа введения, активности препарата и тяжести заболевания. Кроме того, доза может быть изменена с учетом факторов, связанных с конкретным субъектом, подлежащим лечению, которые включают возраст, массу тела, режим питания субъекта и время введения. Специалисту в данной области должно быть известно, что испытания in vivo и in vitro с использованием приемлемых, известных и обычно применяемых клеток и/или животных моделей, позволяют прогнозировать способность испытуемого соединения лечить или предотвращать данное заболевание. Специалисту в данной области должно быть также известно, что клинические испытания с участием людей, включающие первичное испытание на человеке, испытания по определению дозы и эффективности у здоровых субъектов и/или субъектов, страдающих данным заболеванием, могут быть выполнены методами, хорошо известными в клинической и медицинской областях. Нижеследующие примеры приведены для лучшего понимания изобретения и не ограничивают объем изобретения, представленного в формуле изобретения. Пример 1. 3,4-Дигидро-2 Н-бензо[b][1,4]диоксепин-3-ил)метил)сульфамид (соединение 3) Катехин (5,09 г, 46,2 ммоль) и карбонат калия объединяли в ацетонитриле и нагревали при температуре рефлюкса в течение одного часа. Добавляли 2-хлорметил-3-хлор-1-пропен (5,78 г, 46,2 ммоль) и реакционную смесь продолжали нагревать при температуре рефлюкса в течение 24 ч. Раствор охлаждали до комнатной температуры и фильтровали. Фильтрат упаривали, остаток разбавляли водой и экстрагировали диэтиловым эфиром (3 раза). Объединенный органический раствор сушили над MgSO4 и концентрировали. В результате выполнения хроматографии (2% этилового эфира в гексане) был получен 3 метилен-3,4-дигидро-2 Н-бензо[b][1,4]диоксепин в виде бесцветного масла. МС (ESI): 163,2 (М+Н+) 1(100 мл). Добавляли раствор борана в ТГФ (1,0 М раствор в ТГФ, 10,3 мл) при 0 С. Реакционную смесь перемешивали при комнатной температуре в течение 5 ч. Добавляли аминосульфоновую кислоту (6,97 г,61,6 ммоль). Реакционную смесь нагревали при температуре рефлюкса в течение ночи. Реакционную смесь охлаждали до комнатной температуры и добавляли водный раствор гидроксида натрия (3,0 М раствор, 100 мл). Раствор экстрагировали этилацетатом (3100 мл). Объединенный органический раствор сушили над MgSO4. Раствор концентрировали в вакууме и очищали хроматографией (2-8% метанола в дихлорметане), получая при этом 3,4-дигидро-2 Н-бензо[b][1,4]диоксепин-3-ил)метил)амин в виде бесцветного масла. МС (ESI): 180,1 (М+Н+) 1H ЯМР (300 МГц, ДМСО) : 6,92 (м, 4 Н), 4,21 (м, 2 Н), 4,07 (м, 2 Н), 3,33 (ушир., 2 Н), 3,16 (д, J = 4 Гц, 1 Н), 2,72 (д, J = 4 Гц, 1 Н), 2,30 (м, 1 Н). 3,4-Дигидро-2 Н-бензо[b][1,4]диоксепин-3-ил)метил)амин (2,90 г, 16,2 ммоль) и сульфамид (3,11 г,32,4 ммоль) объединяли в сухом диоксане (60 мл) и нагревали при температуре рефлюкса в течение ночи. Добавляли хлороформ и осадок удаляли фильтрованием. Фильтрат концентрировали в вакууме и очищали хроматографией (2-8% ацетона в дихлорметане), получая при этом указанное в заголовке соединение в виде беловатого твердого вещества. 258,8 (M+Н+) 1 Рацемический 2,3-дигидро-1,4-бенздиоксин-2-илметиламин (4,4 г, 26 ммоль) и сульфамид (5,1 г, 53 ммоль) объединяли в 1,4-диоксане (100 мл) и нагревали при температуре рефлюкса в течение 2 ч. Реакционную смесь охлаждали до комнатной температуры и отфильтровывали небольшое количество твердого вещества, которое выбрасывали. Фильтрат упаривали в вакууме и остаток очищали флэшхроматографией на колонке (DCM:метанол=10:1) с образованием белого твердого вещества. Твердое вещество перекристаллизовывали из DCM, получая при этом указанное в заголовке соединение в виде белого твердого вещества. Т.п.: 97,5-98,5 С Элементный анализ: Вычислено: С, 44,25; Н, 4,95; N, 11,47; S, 13,13 Найдено: С, 44,28; Н, 4,66; N, 11,21; S, 13,15 Н 1 ЯМР (ДМСО-d6)6,85 (м, 4 Н), 6,68 (ушир.с, 3 Н, NH), 4,28 (м, 2 Н), 3,97 (дд, J = 6,9, 11,4 Гц, 1 Н),3,20 (м, 1 Н), 3,10 (м, 1 Н). Пример 3. (Бензо[1,3]диоксол-2-илметил)сульфамид (соединение 2) Катехин (10,26 г, 93,2 ммоль), метоксид натрия (25 мас.% в метаноле, 40,3 г, 186 ммоль) и метилдихлорацетат (13,3 г, 93,2 ммоль) объединяли в сухом метаноле (100 мл). Раствор нагревали при температуре рефлюкса в течение ночи. Реакционную смесь охлаждали до комнатной температуры, подкисляли,добавляя концентрированную хлористо-водородную кислоту, и доводили объем в вакууме примерно до 50 мл. Добавляли воду и смесь экстрагировали диэтиловым эфиром (3100 мл). Объединенный органический раствор сушили над MgSO4, концентрировали до образования коричневого твердого вещества и хроматографировали (2% этилацетата в гексане), получая при этом метиловый эфир бензо[1,3]диоксол-2 карбоновой кислоты в виде бесцветного масла. МС (ESI): 195,10 (М+Н+). 1 Н ЯМР (300 МГц, CDCl3) : 6,89 (ушир., 4 Н), 6,29 (с, 1 Н), 4,34 (кв., J = 7 Гц, 2 Н), 1,33 (т, J = 7 Гц,3 Н). К метиловому эфиру бензо[1,3]диоксол-2-карбоновой кислоты (7,21 г, 40,0 ммоль) добавляли гидроксид аммония (29% в воде, 10 мл) и ацетон в количестве, достаточном для получения гомогенной смеси (5 мл). Раствор перемешивали в течение двух часов при комнатной температуре и затем добавляли дистиллированную воду. Амид бензо[1,3]диоксол-2-карбоновой кислоты, выпавший в осадок в виде белого твердого вещества, собирали фильтрованием и использовали без дальнейшей очистки. МС (ESI): 160,00 (М+Н+) 1 Н ЯМР (300 МГц, ДМСО) : 7,99 (с, ушир., 1 Н), 7,72 (с, ушир., 1 Н), 6,94 (м, 2 Н) 6,86 (м, 2 Н), 6,30(ТГФ, 100 мл). К полученному раствору медленно добавляли алюмогидрид лития (LAH, 1 М раствор в ТГФ, 39,5 мл, 39,5 ммоль) при комнатной температуре. Реакционную смесь перемешивали при комнатной температуре в течение 24 ч. Добавляли дистиллированную воду для разрушения избытка LAH. Добавляли водный раствор гидроксида натрия (3,0 М, 100 мл) и раствор экстрагировали этилацетатом(3x100 мл). Объединенный органический раствор промывали водой и сушили над MgSO4. Растворитель выпаривали, получая при этом С-бензо[1,3]диоксол-2-илметиламин в виде бесцветного масла. МС (ESI): 152,1 (М+Н+) 1 Н ЯМР (300 МГц, CDCl3) : 6,87 (м, 4 Н), 6,09 (т, J = 4 Гц, 1 Н), 3,13 (д, J = 4 Гц, 2 Н). С-Бензо[1,3]диоксол-2-илметиламин (2,94 г, 19,4 ммоль) и сульфамид (3,74 г, 38,9 ммоль) объединяли в сухом диоксане (50 мл) и раствор нагревали при температуре рефлюкса в течение ночи. Реакционную смесь концентрировали и остаток хроматографировали (2-10% ацетона в дихлорметане), получая при этом указанное в заголовке соединение в виде белого твердого вещества. МС (ESI): 230, 0 (М+Н+) 1 Н ЯМР (300 МГц, CDCl3) : 6,87 (м, 4 Н), 6,25 (т, J = 4 Гц, 1 Н), 4,79 (ушир., 1 Н), 4,62 (ушир., 1 Н),3,64 (д, J = 4 Гц, 2 Н). Пример 4. (2S)-(-)-N-(2,3-Дигидробензо[1,4]диоксин-2-илметил)сульфамид (соединение 4) Катехин (13,2 г, 0,12 моль) и карбонат калия (16,6 г, 0,12 моль) перемешивали в ДМФА (250 мл),добавляли (2R)-глицидилтозилат (22,8 г, 0,10 моль) и реакционную смесь перемешивали при 60 С в течение 24 ч. Реакционную смесь охлаждали до комнатной температуры, разбавляли смесью воды со льдом(1 л) и экстрагировали диэтиловым эфиром (4 раза). Объединенный органический раствор промывали 3 раза 10% раствором карбоната калия, один раз водой, один раз насыщенным раствором соли и упаривали в вакууме с образованием белого твердого вещества, которое очищали флэш-хроматографией на колонке(DCM:метанол=50:1), получая при этом 2S)-2,3-дигидробензо[1,4]диоксин-2-ил)метанол в виде твердого вещества. Твердое вещество (13,3 г, 68 ммоль) растворяли в пиридине (85 мл), охлаждали до 0 С, добавляли пара-толуолсульфонилхлорид (13,0 г, 68 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 20 ч. Реакционную смесь разбавляли диэтиловым эфиром (1 л) и 1 н. раствором HCl (1,2 л). Органический слой отделяли и промывали 2 раза 1 н раствором HCl (500 мл), 4 раза водой (150 мл) и один раз насыщенным раствором соли, сушили (MgSO4) и упаривали в вакууме с образованием белого твердого вещества, которое очищали флэш-хроматографией (гептан:ЕА=2:1), получая при этом (2S)-2,3-дигидробензо[1,4]диоксин-2-илметиловый эфир толуол-4-сульфоновой кислоты в виде белого твердого вещества. Белое твердое вещество объединяли с фталимидом калия (14,4 г, 78 ммоль) в ДМФА (250 мл) и нагревали при температуре рефлюкса в течение 1 ч, охлаждали до комнатной температуры, выливали в интенсивно перемешиваемую воду (1,5 мл) и перемешивали в течение 30 мин. Белое твердое вещество фильтровали, твердое вещество промывали несколько раз водой, 2% NaOH и снова водой и подвергали воздушной сушке, получая при этом (2S)-2-(2,3-дигидробензо[1,4]диоксин-2-илметил)изоиндол-1,3-дион в виде белого порошкообразного твердого вещества. Порошкообразное белое твердое вещество объединяли с гидразином (2,75 г, 86 ммоль) в EtOH (225 мл), нагревали при температуре рефлюкса в течение 2 ч, охлаждали до комнатной температуры, добавляли 1 н. раствор HCl до рН 1,0 и перемешивали в течение 15 мин. Белое твердое вещество фильтровали и промывали свежим EtOH (твердое вещество выбрасывали), фильтрат упаривали в вакууме с образованием твердого вещества, которое распределяли между диэтиловым эфиром и разбавленным водным раствором NaOH. Раствор в диэтиловом эфире сушили (Na2SO4) и упаривали в вакууме с образованием светло-желтого масла. Масло очищали флэш-хроматографией на колонке (DCM:MeOH=10:1) с образованием масла. Часть масла (4,82 г, 29 ммоль) в 2-пропаноле (250 мл) обрабатывали 1 н. раствором НСl (30 мл) и нагревали на паровой бане до образования гомогенной смеси и затем оставляли охлаждаться до комнатной температуры. Через 3 ч смесь охлаждали на льду в течение 2 ч. Белое хлопьевидное твердое вещество (соответствующая хлористо-водородная соль (2S)-С-(2,3-дигидробензо[1,4]диоксин-2 ил)метиламина) отфильтровывали и снова перекристаллизовывали из 2-пропанола с образованием белого твердого вещества.[]D=-69,6 (c=1,06, EtOH) Белое твердое вещество распределяли между DCM и разбавленным раствором NaOH; DCM сушили[]D=-57,8 (c=1,40, CHCl3) Масло (2,1 г, 12,7 ммоль) и сульфамид (2,44 г, 25,4 ммоль) нагревали при температуре рефлюкса в диоксане (75 мл) в течение 2 ч и неочищенный продукт очищали флэш-хроматографией на колонке(DCM:MeOH=10:1) с образованием белого твердого вещества, которое перекристаллизовывали из DCM,получая при этом указанное в заголовке соединение в виде белого кристаллического твердого вещества. Т.п.: 102-103 С- 16016560 г, 15 ммоль) объединяли в ДМФА (10 мл) и охлаждали на бане со льдом, добавляя диметилсульфамоилхлорид (1,44 г, 10 ммоль). Реакционную смесь затем перемешивали при охлаждении в течение 3 ч. Реакционную смесь распределяли между этилацетатом и водой, раствор в этилацетате промывали насыщенным раствором соли, сушили (MgSO4) и упаривали в вакууме с образованием масла. Масло очищали флэш-хроматографией на колонке (этилацетат:гептан=1:1) с образованием белого твердого вещества,которое перекристаллизовывали (этилацетат/гексан), получая при этом указанное в заголовке соединение в виде белого хлопьевидного твердого вещества. Т.п.: 76-78 С МС: 273 (МН+) Элементный анализ: Вычислено: С, 48,52; Н, 5,92; N, 10,29; S, 11,78 Найдено: С, 48,63; Н, 5,62; N, 10,20; S, 11,90 1 Рацемический 2,3 дигидро-1,4-бензодиоксин-2-илметиламин (825 мг, 5 ммоль) растворяли в этилформиате (15 мл), нагревали при температуре рефлюкса в течение 30 мин и упаривали в вакууме с образованием N-(2,3-дигидробензо[1,4]диоксин-2-илметил)формамида в виде масла. Масло в диэтиловом эфире (25 мл) обрабатывали 1 М раствором LAH в ТГФ (9,0 мл, 9,0 ммоль) при 0 С и перемешивали в течение 5 ч при комнатной температуре. Реакционную смесь охлаждали на бане со льдом и гасили водой (0,50 мл), затем 3 н. раствором NaOH (0,50 мл) и водой (0,50 мл). Затем смесь перемешивали при комнатной температуре в течение 1 ч. Твердое вещество фильтровали и фильтрат упаривали в вакууме с образованием остатка, который распределяли между 1 н раствором HCl и диэтиловым эфиром. Водную фазу подщелачивали 1 н. раствором NaOH и экстрагировали диэтиловым эфиром. Органическую фазу сушили (MgSO4) и упаривали в вакууме с образованием (2,3 дигидробензо[1,4]диоксин-2-илметил)метиламина в виде масла. МС: 180 (МН+) 1 Н ЯМР (CDCl3)6,85 (м, 4 Н), 4,30 (м, 2 Н), 4,02 (дд, J = 7,9, 11,6 Гц, 1 Н), 2,85 (м, 2 Н), 2,50 (с, 3 Н). Масло (380 мг, 2,1 ммоль) и сульфамид (820 мг, 8,5 ммоль) объединяли в диоксане (15 мл), нагревали при температуре рефлюкса в течение 1,5 ч и упаривали в вакууме с образованием неочищенного остатка. Остаток очищали хроматографией на колонке (этилацетат/гептан=1:1) и образовавшееся твердое вещество перекристаллизовывали из этилацетата/гексана, получая при этом указанное в заголовке соединение в виде белого твердого вещества. Т.п.: 97-98 С МС: 257 (М-1) Элементный анализ: Вычислено: С, 46,50; Н, 5,46; N, 10,85; S, 12,41 Найдено: С, 46,48; Н, 5,65; N, 10,90; S, 12,07 1 Н ЯМР (CDCl3)6,86 (м, 4 Н), 4,52 (ушир.с, 2 Н), 4,46 (м, 1 Н), 4,29 (дд, J = 2,3, 11,5 Гц, 1 Н), 4,05 4-Хлоркатехин подвергали взаимодействию способом, описанным в приведенном выше примере 4,получая при этом смесь (2S)-С-(7-хлор-2,3-дигидробензо[1,4]диоксин-2-ил)метиламина и (2S)-С-(6-хлор 2,3-дигидробензо[1,4]диоксин-2-ил)метиламина (изомеры 6-хлор:7-хлор с примерным соотношением 3:1 по результатам жидкостной хроматографии высокого давления с обращенной фазой). Смесь растворяли в 2-пропаноле (100 мл) и добавляли 1 н. раствор HCl в диэтиловом эфире до рН 1,0. Выпавшую в осадок хлористо-водородную соль фильтровали (2,65 г) и перекристаллизовывали из метанола/IPA с образованием белых кристаллов. Белые кристаллы распределяли между DCM и разбавленным раствором NaOH. DCM сушили и упаривали в вакууме, получая при этом очищенный (2S)-С-(6 хлор-2,3-дигидробензо[1,4]диоксин-2-ил)метиламин в виде масла. []D=-67,8 (c = 1,51, CHCl3). Масло (7,75 ммоль) и сульфамид (1,50 г, 15,5 ммоль) объединяли в диоксане (50 мл) и нагревали при температуре рефлюкса в течение 2,0 ч, охлаждали до комнатной температуры и упаривали в вакууме- 17016560 с образованием твердого вещества. Продукт очищали флэш-хроматографией на колонке с использованием DCM/метанола в отношении 20:1, получая при этом указанное в заголовке соединение в виде белого твердого вещества.(2S)-С-(6-хлор-2,3 дигидробензо[1,4]диоксин-2-ил)метиламина выделяли (изомеры 6-хлор:7-хлор с примерным соотношением 1:1) и упаривали в вакууме с образованием твердого вещества, которое распределяли между DCM(200 мл) и разбавленным раствором NaOH (0,5 М, 50 мл). Раствор в DCM промывали один раз насыщенным раствором соли, сушили (Na2SO4) и упаривали в вакууме с образованием масла, которое очищали при помощи HPLC с обращенной фазой (10-50% ACN с 0,16% ТФУ в воде с 0,20% ТФУ), получая при этом (2S)-С-(7-хлор-2,3-дигидробензо[1,4]диоксин-2-ил)метиламин в виде остатка. Остаток объединяли с сульфамидом (0,90 г, 9,4 ммоль) в диоксане (25 мл) и нагревали при температуре рефлюкса в течение 2,5 ч, охлаждали до комнатной температуры и упаривали в вакууме с образованием масла. Масло очищали флэш-хроматографией на колонке с использованием DCM/метанола в отношении 10:1, получая при этом (2S)-(-)-N-(7-хлор-2,3-дигидробензо[1,4]диоксин-2-илметил)сульфамида в виде белого твердого вещества. МС: 277 (М-1) 1 Хроман-2-карбоновую кислоту (4,5 г, 25 ммоль) и НОВТ (3,86 г, 25 ммоль) объединяли в DCM (40 мл) и ДМФА (10 мл). Добавляли диметиламинопропилэтилкарбодиимид (EDC, 4,84 г, 25 ммоль) при комнатной температуре и реакционную смесь перемешивали в течение 30 мин. Затем добавляли гидроксид аммония (2,26 мл, 33,4 ммоль) и реакционную смесь перемешивали в течение 16 ч. Реакционную смесь разбавляли DCM (50 мл) и водой (50 мл) и значение рН смеси доводили примерно до рН 3,0, добавляя 1 н. раствор HCl. DCM отделяли и водную фазу дважды экстрагировали DCM. Объединенную фазу в DCM сушили (Na2SO4) и упаривали в вакууме с образованием масла, которое очищали флэшхроматографией на колонке (этилацетат) с образованием масла. Масло (5,35 г, 30 ммоль) в ТГФ (90 мл) перемешивали, добавляя 1 М раствор LAH в ТГФ (36 мл, 36 ммоль), после чего реакционную смесь перемешивали при комнатной температуре в течение 20 ч. Реакционную смесь гасили водой и перемешивали в течение 2 ч, раствор декантировали, сушили (Na2SO4) и упаривали в вакууме с образованием С-хроман-2-илметиламина в виде маслянистого амина. Маслянистый амин (1,63 г, 10 ммоль) и сульфамид (1,92 г, 20 ммоль) объединяли в диоксане (50 мл) и нагревали при температуре рефлюкса в течение 2 ч. Раствор охлаждали и упаривали в вакууме с образованием масла, которое очищали хроматографией на колонке (DCM:метанол, 10:1) с образованием белого твердого вещества. Твердое вещество перекристаллизовывали из этилацетата/гексана, получая при этом хроман-2-илметилсульфамид в виде белого твердого вещества. Т.п.: 100-101 С МС: 241 (М-1) Элементный анализ: Вычислено: С, 49,57; Н, 5,82; N, 11,56; S, 13,23 Найдено: С, 49,57; Н, 5,80; N, 11,75; S, 13,33 Пример 9. 2-(2,3-Дигидробензо[1,4]диоксин-2-ил)этилсульфамид (соединение 16) Цианид калия (2,05 г, 31,5 ммоль) добавляли к 2-бромметил-(2,3-дигидробензо[1,4]диоксину) (6,87 г, 30 ммоль) в ДМСО (90 мл) и перемешивали при температуре окружающей среды в течение 20 ч. Затем реакционную смесь разбавляли водой (250 мл) и дважды экстрагировали диэтиловым эфиром. Диэтиловый- 18016560 эфир промывали водой, затем дважды промывали насыщенным раствором соли, сушили (Na2SO4) и упаривали в вакууме, получая при этом 2-цианометил-(2,3-дигидробензо[1,4]диоксин) в виде белого твердого вещества. 1H ЯМР (CDCl3)6,89 (м, 4 Н), 4,50 (м, 1 Н), 4,31 (дд, J = 2,3, 11,5 Гц, 1 Н) , 4,08 (дд, J = 6,2, 11,6 Гц,1 Н), 2,78 (д, J = 6,1, Гц, 2 Н). 2-Цианометил-(2,3-дигидробензо[1,4]диоксин) растворяли в ТГФ (50 мл) и добавляли 1 М раствор ВН 3 в ТГФ (80 мл, 80 ммоль), реакционную смесь нагревали при температуре рефлюкса в течение 5 ч и перемешивали при температуре окружающей среды в течение 16 ч. Реакционную смесь охлаждали на бане со льдом и добавляли 2 н. раствор HCl до достижения рН 1,0. Затем реакционную смесь перемешивали в течение 1 ч при комнатной температуре и упаривали в вакууме с образованием масла. Масло распределяли между 3 н. раствором NaOH и диэтиловым эфиром, раствор в диэтиловом эфире промывали насыщенным раствором соли, сушили (Na2SO4) и упаривали в вакууме с образованием неочищенного 2(2,3-дигидробензо[1,4]-диоксин-2-ил)этиламина. МС (М+Н)+ 180 Неочищенный 2-(2,3-дигидробензо[1,4]диоксин-2-ил)этиламин в диоксане (100 мл) объединяли с сульфамидом (3,0 г, 31 ммоль) и нагревали при температуре рефлюкса в течение 2 ч. Раствор охлаждали и упаривали в вакууме с образованием оранжевого твердого вещества, которое очищали хроматографией на колонке (DCM:MeOH=10:1) с образованием белого твердого вещества. Твердое вещество перекристаллизовывали из DCM, получая при этом указанное в заголовке соединение в виде твердого вещества. МС (М-1) 257 Т.п.: 101-103 С (корр.) 1(200 мл). Добавляли (2R)-глицидилтозилат (9,12 г, 40 ммоль) и реакционную смесь перемешивали при 60 С в течение 24 ч. Реакционную смесь охлаждали до комнатной температуры, разбавляли смесью воды со льдом (600 мл) и экстрагировали диэтиловым эфиром (4 раза). Объединенный органический раствор трижды промывали 10% карбонатом калия, дважды насыщенным раствором соли, сушили (MgSO4) и упаривали в вакууме,получая при этом вязкое масло(2S)-2-(6,7-дихлор-2,3 дигидробензо[1,4]диоксин)метанола. Масло (2S)-2-(6,7-дихлор-2,3-дигидробензо[1,4]диоксин)метанола (6,4 г, 27 ммоль) растворяли в пиридине (50 мл), охлажденном до 0 С. Затем добавляли пара-толуолсульфонилхлорид (5,2 г, 27 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 20 ч. Реакционную смесь разбавляли диэтиловым эфиром и 1 н. раствором HCl (750 мл), органический слой отделяли и промывали 2 раза 1 н. раствором HCl (250 мл), один раз водой (150 мл), дважды насыщенным раствором соли, сушили (MgSO4) и упаривали в вакууме, получая при этом светло-желтое твердое вещество (2S)-6,7-дихлор 2,3-дигидробензо[1,4]диоксин-2-илметилового эфира толуол-4-сульфоновой кислоты. 1(2S)-6,7-Дихлор-2,3-дигидробензо[1,4]диоксин-2-илметиловый эфир толуол-4-сульфоновой кислоты (8,0 г, 20,5 ммоль) объединяли с фталимидом калия (6,1 г, 33 ммоль) в ДМФА (75 мл), нагревали при температуре рефлюкса в течение 1 ч, охлаждали до комнатной температуры, выливали в интенсивно перемешиваемую воду (0,5 л) и затем перемешивали в течение 30 мин. Белое твердое вещество фильтровали, несколько раз промывали водой, 2% NaOH и еще раз водой и подвергали воздушной сушке, получая при этом (2S)-2-(6,7-дихлор-2,3-дигидробензо[1,4]диоксин-2-илметил)изоиндол-1,3-дион (6,0 г, 80%) в виде белого порошкообразного твердого вещества. Белое порошкообразное твердое вещество объединяли с гидразином (1,06 г, 33 ммоль) в EtOH (80 мл), нагревали при температуре рефлюкса в течение 2 ч, затем охлаждали до комнатной температуры. Затем добавляли 1 н. раствор HCl, чтобы довести значение рН реакционной смеси до рН 1,0 и реакционную смесь перемешивали в течение 15 мин. Белое твердое вещество фильтровали, промывали свежимEtOH (твердое вещество выбрасывали) и фильтрат упаривали в вакууме до образования твердого веще- 19016560 ства, которое распределяли между диэтиловым эфиром и разбавленным водным раствором NaOH. Раствор в диэтиловом эфире сушили (Na2SO4) и упаривали в вакууме, получая при этом вязкое масло (2S)-2 аминометил-(6,7-дихлор-2,3-дигидробензо[1,4]диоксин). 1H ЯМР (CDCl3)6,98 (с, 1 Н), 6,96 (с, 1 Н), 4,25 (дд, J = 2,0, 11,2 Гц, 1 Н), 4,15 (м, 1 Н), 4,0 (м, 1 Н),2,97 (д, J = 5,5 Гц, 2 Н). Часть масла (3,8 г, 16 ммоль) и сульфамид (3,1 г, 32,4 ммоль) нагревали при температуре рефлюкса в диоксане (100 мл) в течение 2 ч и неочищенный продукт очищали флэш-хроматографией на колонке(DCM:MeOH=20:1) с образованием указанного в заголовке соединения в виде белого твердого вещества,которое перекристаллизовывали из этилацетата/гексана, получая при этом указанное в заголовке соединение в виде белого кристаллического твердого вещества. МС [М-Н]- 311,0 т.п.: 119-121 С Указанное в заголовке соединение было получено способом, описанным в приведенном выше примере 4, с использованием в качестве исходного вещества 4-метилкатехина; полученное белое твердое вещество перекристаллизовывали из этилацетата/гексана с образованием указанного в заголовке соединения в виде белого твердого вещества. МС [М-Н]- 257 1H ЯМР (CDCl3)6,76 (м, 1 Н), 6,66 (м, 2 Н), 4,80 (м, 1 Н), 4,57 (ушир.с, 1 Н), 4,40 (м, 1 Н), 4,28 (м,1 Н), 4,03 (дд, J = 6,9, 11,4 Гц, 1 Н), 3,45 (м, 2 Н), 2,25 (с, 3 Н). Элементный анализ: Вычислено: С, 46,50; Н, 5,46; N, 10,85; S, 12,41 Найдено: С, 46,65; Н, 5,60; N, 10,84; S, 12,61 Пример 13. Исследование in vivo страдающих ожирением мышей AKR/J Как известно в данной области, мыши AKR/J подвержены ожирению, вызываемому рационом питания (Rossmeisl M., Rim J.S., Koza R.A., Kozak L.P., Diabetes. 2003 Aug.; 52(8): 1958-66). Самцов мышей AKR/J (20 г) в возрасте 4-5 недель (Jackson Laboratories, Bar Harbor, ME) содержали по одному в клетках в виде коробки для обуви при 21 С с 12-часовым циклом чередования света и темноты. Мышей кормили кормом с высоким содержанием жиров в течение 8 недель, чтобы вызвать ожирение. Рацион в энергетическом отношении состоял из 45% жиров, 20% белков и 35% углеводов (Research Diets, D12451, New Brunswick, NJ). Для исследования отбирали страдающих ожирением мышей с массой тела от 35 до 46 г. Мышей произвольно распределяли на основании массы тела в экспериментальные группы в возрасте 13 недель. Один раз в сутки мышам принудительно через рот вводили (0,2 мл в 15:00-17:00 часов) контрольный наполнитель (0,5% метилцеллюллоза, рН 7,4) или наполнитель, содержащий соединение 8 (300 мг/кг). Массу тела мышей и потребление корма мышами контролировали каждые несколько дней. На 11-й день мышей анестезировали пентобарбиталом натрия (1 мл/кг, внутрибрюшинно, Sleepaway, Fort Dodge,Iowa). Затем иссекали и взвешивали белую жировую ткань (WAT) (забрюшинный жир) и скелетные мышцы (мышцы, относящиеся к желудку и большеберцовой кости, и мышцы подошвы). Приведенные ниже данные выражены в виде среднего значения и стандартной ошибки, вычисленных с использованием 9-10 мышей в одной экспериментальной группе. Для статистического анализа использовали двоичный t-критерий Стьюдента. Все исследования животных были выполнены в соответствии с руководством Комитета по защите и использованию животных. После 10-дневного лечения у мышей, которым вводили соединение 8, наблюдалась большая потеря массы тела по сравнению с мышами, которым вводили наполнитель. Потеря массы тела сопровождалась потерей белой жировой ткани; у мышей, которым вводили соединение 8, было отмечено 26,6% уменьшение забрюшинного жира по сравнению с мышами, которым вводили наполнитель, при этом не было обнаружено значительных изменений в массе скелетных мышц. Таким образом, отношение массы жира к мышечной ткани (белая жировая ткань/скелетные мышцы) уменьшилось на 16,8% у мышей, которым вводили соединение 8, по сравнению с мышами, которым вводили наполнитель (наполнитель:- 20016560 8,90,4 по сравнению с соединением 8: 7,40,5, р 0,05). У мышей, которым вводили соединение 8,было также отмечено сокращение потребления корма с 4-го по 10-й день по сравнению с контрольными животными. Было также установлено, что соединение 8 задерживает опорожнение желудка на статистически значимом уровне (р 0,05). Данные измерения массы тела, потребления корма, массы жира и мышц у мышей, которым вводили наполнитель и соединение 8, суммированы в нижеследующей табл. 4. Таблица 4. Результаты исследования страдающих ожирением мышей in vivo Таким образом, данные показывают, что соединение 8 эффективно стимулировало потерю массы тела, при этом потеря массы тела происходила за счет жира, а не мышечной массы, и, кроме того, данное соединение позволяло эффективно сократить потребление корма (то есть снижало аппетит). Пример 14. Исследования ожирения in vivo Соединение 8 суспендировали в 0,5% метоцеле с использованием ручного гомогенизатора для уменьшения размера частиц и магнитной мешалки и перемешивали для однородного суспендирования частиц на протяжении всего периода введения. В качестве наполнителя/контрольного вещества использовали 0,5% гидроксипропилметилцеллюлозу (метоцель). Для исследования потери массы тела использовали самцов мышей AKR/J с массой тела от 35 до 46 г. Мыши AKR/J подвержены ожирению, вызываемому рационом питания. Самцов мышей AKR/J (средняя масса тела около 20 г) в возрасте 4-5 недель (приобретенных в компании Jackson Laboratories, BarHarbor, ME) содержали группами (по пять животных в одной клетке) в клетках в виде коробки для обуви при 21 С с 12-часовым циклом чередования света и темноты. Всех мышей подвергали карантину в течение одной недели, прежде чем перевести в помещение для исследования животных. Мышей кормили кормом с высоким содержанием жиров в течение 8 недель, чтобы вызвать ожирение. Рацион в энергетическом отношении состоял из 45% жиров, 20% белков и 35% углеводов (приобретен в компании ResearchDiets, D12451, New Brunswick, NJ). В качестве контрольных животных, не страдающих ожирением, была создана дополнительная группа мышей, соответствующих друг другу по возрасту и массе тела, которым давали корм с низким содержанием жиров (приобретен в компании Research Diets, D12450B, New Brunswick, NJ). Для исследования потери массы тела были отобраны только мыши, страдающие ожирением,определяемым на основании массы тела от 35 до 46 г. Животных разделяли и содержали в клетках по одному по крайней мере в течение трех дней до введения лекарственного средства для акклиматизации в новом окружении. Было выполнено два отдельных исследования: в первом исследовании 10 мышам вводили контрольный наполнитель, представляющий собой 0,5% метоцель; 10 мышам вводили 300 мг/кг соединения 8 в наполнителе и 10 мышам вводили в качестве положительного контрольного вещества 10 мг/кг сибутрамина (средство для снижения массы тела) в наполнителе. Во втором исследовании 48 мышей распределяли в 4 экспериментальные группы по 12 мышей в каждой. Затем мышам в четырех группах вводили соответственно 0,5% метоцель (наполнитель), 10 мг/кг соединения 8, 30 мг/кг соединения 8 и 100 мг/кг соединения 8 в наполнителе. Мышам принудительно через рот один раз в сутки (в 15:00-17:00 ч) в течение 10 дней вводили контрольный наполнитель (0,5% метоцель, рН 7,4) или наполнитель, содержащий соединение 8. Вводимый объем был равен 5 мл/кг массы тела (0,2 мл для мышей с массой тела 40 г). Массу тела и потребление корма мышами периодически контролировали в течение всего исследования. На 11-й день мышей не кормили в течение 4 ч во время светлого цикла (корм были удален в период с 06:00 до 10:00 ч). Аутопсию выполняли через 18 ч после последнего введения. Мышей анестезировали пентобарбиталом натрия(1 мл/кг, внутрибрюшинная [i.p.] инъекция, SleepAway, Fort Dodge, Iowa); кровь удаляли через сердечную пункцию при помощи 1 мл шприца и собирали в обработанные гепарином пробирки. Белую жировую ткань (WAT) (забрюшинный и паховой жир), бурую жировую ткань (ВАТ), скелетные мышцы(мышцы, относящиеся к желудку и большеберцовой кости, и мышцы подошвы) и содержимое желудка иссекали и взвешивали. Образцы плазмы, полученные центрифугированием цельной крови с ускорением 2000-3000 g в течение 10-20 мин при 4 С, хранили при -20 С для последующего измерения инсулина,HDL, LDL, общего холестерина и триглицерида. У мышей отбирали два микролитра крови через хвостовую пункцию и измеряли уровни глюкозы в крови при помощи глюкометра (OneTouch UltraSmart, Lifescan, Milpitas, CA). Концентрации инсулина в плазме измеряли при помощи набора для выполнения твердофазного иммуноферментного анализа(ELISA) у крыс/мышей (EZRMI-13K, LINCO Research, St. Charles, Missouri). Пробы крови разводили в- 21016560 отношении 1:4 в сыворотке мыши, пропущенной через активированный уголь, входящей в комплект набора для ELISA. Исследование выполняли в соответствии с инструкциями изготовителей. Общую флуоресценцию детектировали при помощи люминометра для микропланшетов Orion 1 (Berthold Detection(HDL), липопротеина низкой плотности (LDL) и триглицерида в плазме измеряли при помощи химического анализатора крови ADVIA 1650 фирмы Bayer (Bayer Healthcare LLC, Diagnostic Division, Tarrytown,NY). Холестерин измеряли в соответствии с инструкциями изготовителей ферментативным методом с превращением холестеролэстеразы и холестеролоксидазы с выполнением конечной стадии методом Триндера; HDL и LDL измеряли методом удаления каталазы; триглицерид измеряли ферментативным методом с выполнением конечной стадии методом Триндера. Данные, полученные в результате выполнения исследований, были подвергнуты анализу при помощи двоичного t-критерия Стьюдента и выражены в виде средних значений и стандартных ошибок в приведенных ниже таблицах. Соотношение жира и мышц высчитывали следующим образом: общая масса пахового и забрюшинного жира/мышечная масса. Величины, приведенные в таблицах, выражены в виде среднего значениястандартная ошибка (n=9-10). Средняя масса тела мышей AKR/J до начала скармливания рациона с высоким содержанием жиров была равна 21,70,49 г. Средняя масса тела мышей после получения рациона с высоким содержанием жиров в течение восьми недель была равна 37,60,45 г. Для введения соединения 8 или наполнителя отбирали мышей с наибольшим увеличением массы тела. Как показано в нижеследующей табл. 5, при выполнении первого исследования у мышей, которым вводили 300 мг/кг соединения 8, наблюдалась значительная потеря массы тела по сравнению с мышами, которым вводили наполнитель, через 10 дней после начала лечения. Эффект потери массы тела был отмечен через 3 дня после начала лечения и сохранялся до конца исследования. Значительное уменьшение потребления корма также было обнаружено через три дня после начала лечения соединением 8 по сравнению с наполнителем. В отличие от этого мыши, которым вводили средство против ожирения сибутрамин, теряли в массе через 3 дня после начала лечения, но в конце исследования не было отмечено различий в массе тела с контрольными мышами. Сокращение потребления корма у мышей, которым вводили сибутрамин, также имело место с 0-го дня до 3-го дня, но отсутствовало с 4-го дня по 9-й день. Общее содержимое желудка, измеренное в конце исследования, было значительно больше (0,270,05 г,р 0,05) при введении соединения 8 по сравнению с введением наполнителя (0,160,02 г). Таблица 5 р 0,05,р 0,01,р 0,001 соответственно по сравнению с контрольным наполнителем У мышей, которым вводили соединение 8, наблюдалось также уменьшение массы белой жировой ткани по сравнению с введением наполнителя через 10 дней после начала лечения. В результате этого уменьшалось отношение массы жира к мышечной массе в группе мышей, которым вводили соединение 8, как показано в приведенной ниже табл. 6. Отношение массы жира к мышечной массе, приведенное в нижеследующей табл. 6, вычисляли следующим образом: общая масса пахового и забрюшинного жира/мышечная масса. р 0,05 по сравнению с контрольным наполнителем. Как показано в нижеследующей табл. 7, при выполнении второго исследования реакции на дозу не было выявлено значительной (Р 0,05) потери массы тела или сокращения потребления корма у мышей,которым вводили 10, 30 и 100 мг/кг соединения 8. В данном исследовании ткань не собирали и поэтому не определяли показатели для жира и мышц. Таблица 7 Пример 15. Конкретный вариант осуществления настоящего изобретения относится к композиции для орального введения, которую получают, смешивая 100 мг соединения 8, полученного способом по примеру 7,с достаточно тонко измельченной лактозой до общего количества, равного 580-590 мг, которым заполняют твердую гелевую капсулу размером О. Несмотря на то, что в приведенном выше описании изобретения представлены общие принципы осуществления настоящего изобретения, проиллюстрированные приведенными примерами, очевидно,что применение изобретения предполагает все возможные варианты, адаптации и/или модификации,входящие в объем нижеследующей формулы изобретения и ее эквивалентов. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ лечения ожирения, стимулирования потери массы тела или снижения аппетита, включающий введение субъекту терапевтически эффективного количества соединения формулы (I)R4 выбирают из группы, включающей водород и (С 1-4)алкил; а означает целое число 1 или 2; выбирают из группы, включающей где b означает целое число от 0 до 4, с означает целое число от 0 до 2; каждый R5 независимо выбирают из группы, включающей галоген, (С 3-4)алкил и нитро; при условии, что когда или а равно 1; или его фармацевтически приемлемой соли. 2. Способ по п.1, в котором в соединении формулы I R1 и R2, каждый независимо, выбирают из группы, включающей водород и (C1-4) алкил;R4 выбирают из группы, включающей водород и (C1-4)алкил; а означает целое число 1 или 2; выбирают из группы, включающей где b означает целое число 1 или 2, с означает целое число от 0 до 1; каждый R5 независимо выбирают из группы, включающей галоген, (С 1-4)алкил и нитро; при условии, что когда а равно 1; или это соединение формулы I вводят в виде фармацевтически приемлемой соли. 3. Способ по п.2, в котором в соединении формулы IR4 выбирают из группы, включающей водород и (C1-4)алкил; а означает целое число 1 или 2; выбирают из группы, включающей где b означает целое число 1 или 2, с означает 0; каждый R5 независимо выбирают из группы, включающей галоген, (C1-4)алкил и нитро; при условии, что когда а равно 1; или это соединение формулы I вводят в виде фармацевтически приемлемой соли. 4. Способ по п.3, в котором в соединении формулы IR4 выбирают из группы, включающей водород и метил; а означает целое число 1 или 2; выбирают из группы, включающей 2-(2,3-дигидробензо[1,4]диоксинил),2-(бензо[1,3]диоксолил),2-(3,4-дигидро-2 Н-бензо[1,4]диоксепинил),2-(2,3-дигидробензо[1,4]диоксинил),2-(6-хлор-2,3-дигидробензо-[1,4]диоксинил),2-(6-фтор-2,3-дигидробензо[1,4]диоксинил),2-(хроманил),2-(5-фтор-2,3-дигидробензо[1,4]диоксинил),2-(7-хлор-2,3-дигидробензо[1,4]диоксинил),2-(6-хлорбензо[1,3]диоксолил),2-(7-нитро-2,3-дигидробензо[1,4]диоксинил),2-(7-метил-2,3-дигидробензо[1,4]диоксинил),2-(5-хлор-2,3-дигидробензо[1,4]диоксинил),2-(6-бром-2,3-дигидробензо[1,4]диоксинил),2-(6,7-дихлор-2,3-дигидробензо[1,4]диоксинил),2-(8-хлор-2,3-дигидробензо[1,4]диоксинил),2-(2,3-дигидронафто[2,3-b][1,4]диоксинил) и 2-(4-метилбензо[1,3]диоксолил); означает 2-(3,4-дигидро-2 Н-бензо[1,4]диоксепинил), а равно 1; при условии, что когда или это соединение формулы I вводят в виде фармацевтически приемлемой соли. 5. Способ по п.4, в котором в соединении формулы I R1 и R2, каждый независимо, выбирают из группы, включающей водород и метил;R4 выбирают из группы, включающей водород и метил; а означает целое число 1 или 2; выбирают из группы, включающей 2-(бензо[1,3]диоксолил),2-(2,3-дигидробензо[1,4]диоксинил),2-(2,3-дигидробензо[1,4]диоксинил),2-(6-хлор-2,3-дигидробензо[1,4]диоксинил),2-(7-хлор-2,3-дигидробензо[1,4]диоксинил),2-(7-метил-2,3-дигидробензо[1,4]диоксинил),2-(6-бром-2,3-дигидробензо[1,4]диоксинил) и 2-(6,7-дихлор-2,3-дигидробензо[1,4]диоксинил); или это соединение формулы I вводят в виде фармацевтически приемлемой соли. 6. Способ по п.1, в котором соединение формулы (I) представляет собой (2S)-(-)-N-(6-хлор-2,3- 25016560 дигидробензо[1,4]-диоксин-2-илметил)сульфамид и его фармацевтически приемлемую соль . 7. Способ лечения ожирения, включающий введение субъекту терапевтически эффективного количества соединения, представляющего собой (2S)-(-)-N-(6-хлор-2,3-дигидробензо[1,4]диоксин-2-илметил) сульфамид и его фармацевтически приемлемой соли. 8. Способ стимулирования потери массы тела, включающий введение субъекту терапевтически эффективного количества соединения, представляющего собой (2S)-(-)-N-(6-хлор-2,3-дигидробензо[1,4] диоксин-2-илметил)сульфамид, и его фармацевтически приемлемой соли. 9. Способ снижения аппетита, включающий введение субъекту терапевтически эффективного количества соединения, представляющего собой (2S)-(-)-N-(6-хлор-2,3-дигидробензо[1,4]диоксин-2-илметил) сульфамид, и его фармацевтически приемлемой соли. 10. Способ лечения ожирения, стимулирования потери массы тела или снижения аппетита, включающий введение субъекту терапевтически эффективного количества соединения формулы (II) или его фармацевтически приемлемой соли.
МПК / Метки
МПК: A61K 31/357, A61K 31/353, A61P 3/04
Метки: лечения, потери, использованием, способ, бензоконденсированного, массы, снижения, сульфамида, производных, ожирения, аппетита, гетероциклического, стимулирования, тела
Код ссылки
<a href="https://eas.patents.su/27-16560-sposob-lecheniya-ozhireniya-stimulirovaniya-poteri-massy-tela-i-snizheniya-appetita-s-ispolzovaniem-proizvodnyh-benzokondensirovannogo-geterociklicheskogo-sulfamida.html" rel="bookmark" title="База патентов Евразийского Союза">Способ лечения ожирения, стимулирования потери массы тела и снижения аппетита с использованием производных бензоконденсированного гетероциклического сульфамида</a>
Предыдущий патент: Фармацевтические композиции с ингибиторами dpp iv
Следующий патент: Углеводсодержащие функциональные напитки на основе гидролизата белка, содержащие изомальтулозу и/или лейкрозу
Случайный патент: Способ выполнения теплоизоляционного стыка предварительно теплоизолированных трубопроводов