Применение ингибиторов сох-2 для лечения шизофрении, аффективных расстройств или осложнений, связанных с тиком
Формула / Реферат
1. Применение ингибитора СОХ-2 при получении лекарственного средства для лечения шизофрении, аффективных расстройств и связанных с тиком осложнений.
2. Применение по п.1 для лечения хронических шизофренических психозов, шизоаффективных психозов, приступов депрессии, приступов рецидивирующей депрессии, маниакальных осложнений и биполярных аффективных расстройств.
3. Применение по одному из пп.1-2, отличающееся тем, что ингибитор СОХ-2 выбирают из целекоксиба, рофекоксиба, мелоксикама, пироксикама, деракоксиба, парекоксиба, валдекоксиба, эторикоксиба, производного хромена, производного хромана, N-(2-циклогексилоксинитрофенил)метансульфонамида, COX189, АВТ963 или JTE-522, их фармацевтически приемлемых солей, пролекарств или смесей.
4. Применение по п.3, отличающееся тем, что целекоксиб или его фармацевтически приемлемую соль используют в качестве ингибитора СОХ-2.
5. Применение по п.4, отличающееся тем, что целекоксиб или его фармацевтически приемлемую соль вводят в количестве 50-1600 мг/день, предпочтительно 200-600 мг/день, наиболее предпочтительно 400 мг/день.
6. Применение по одному из предшествующих пунктов, отличающееся тем, что лекарственное средство вводят перорально.
Текст
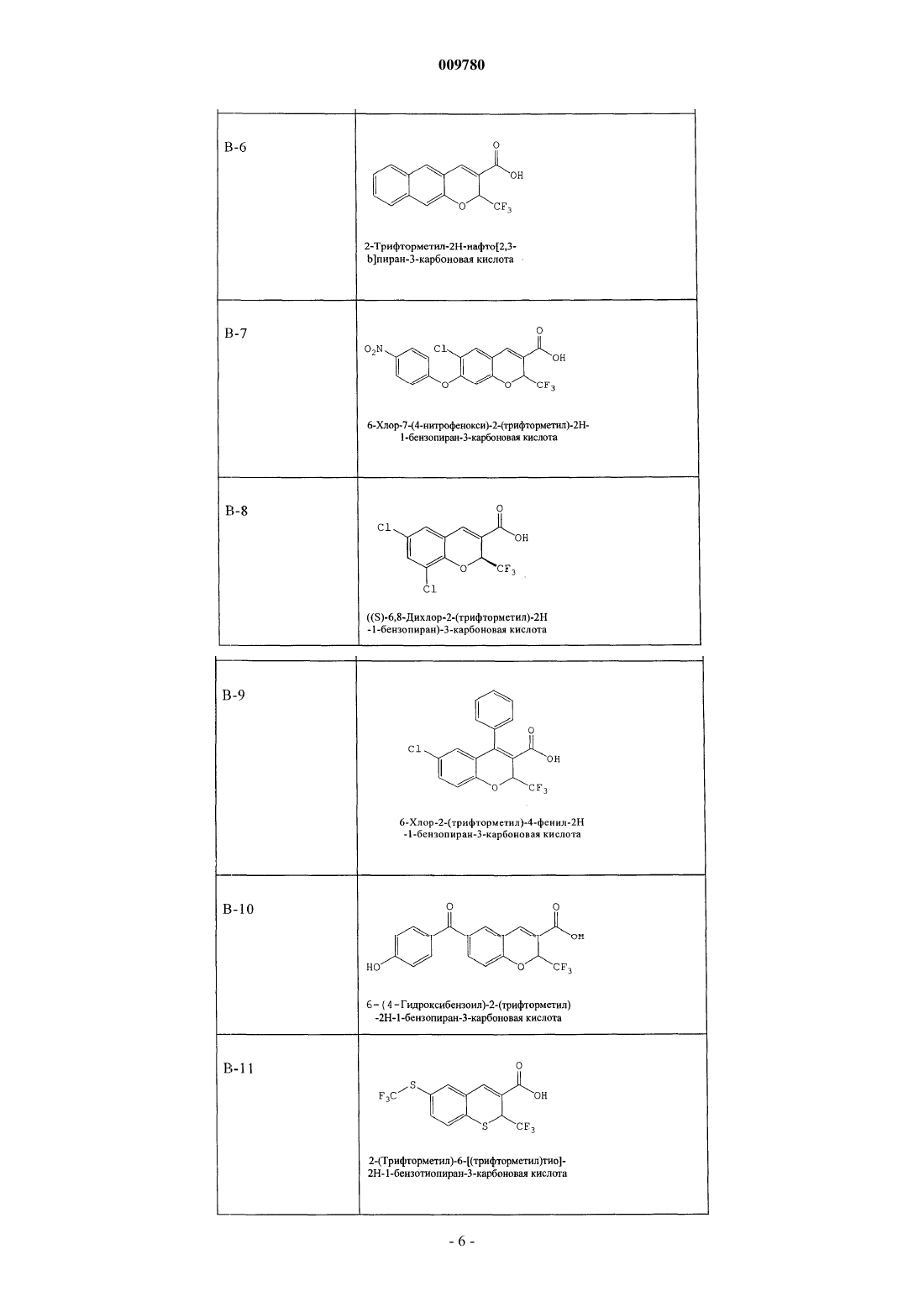
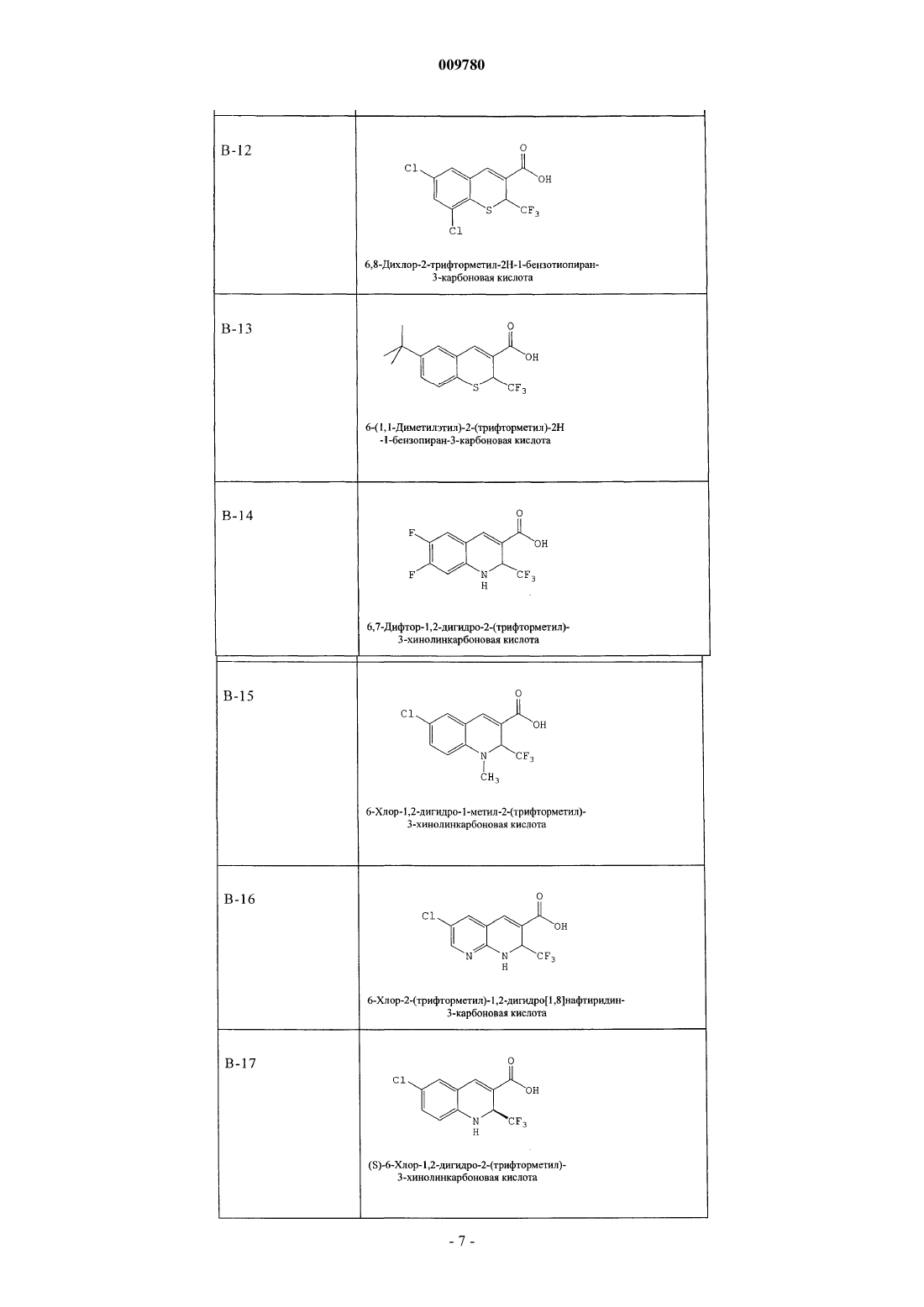
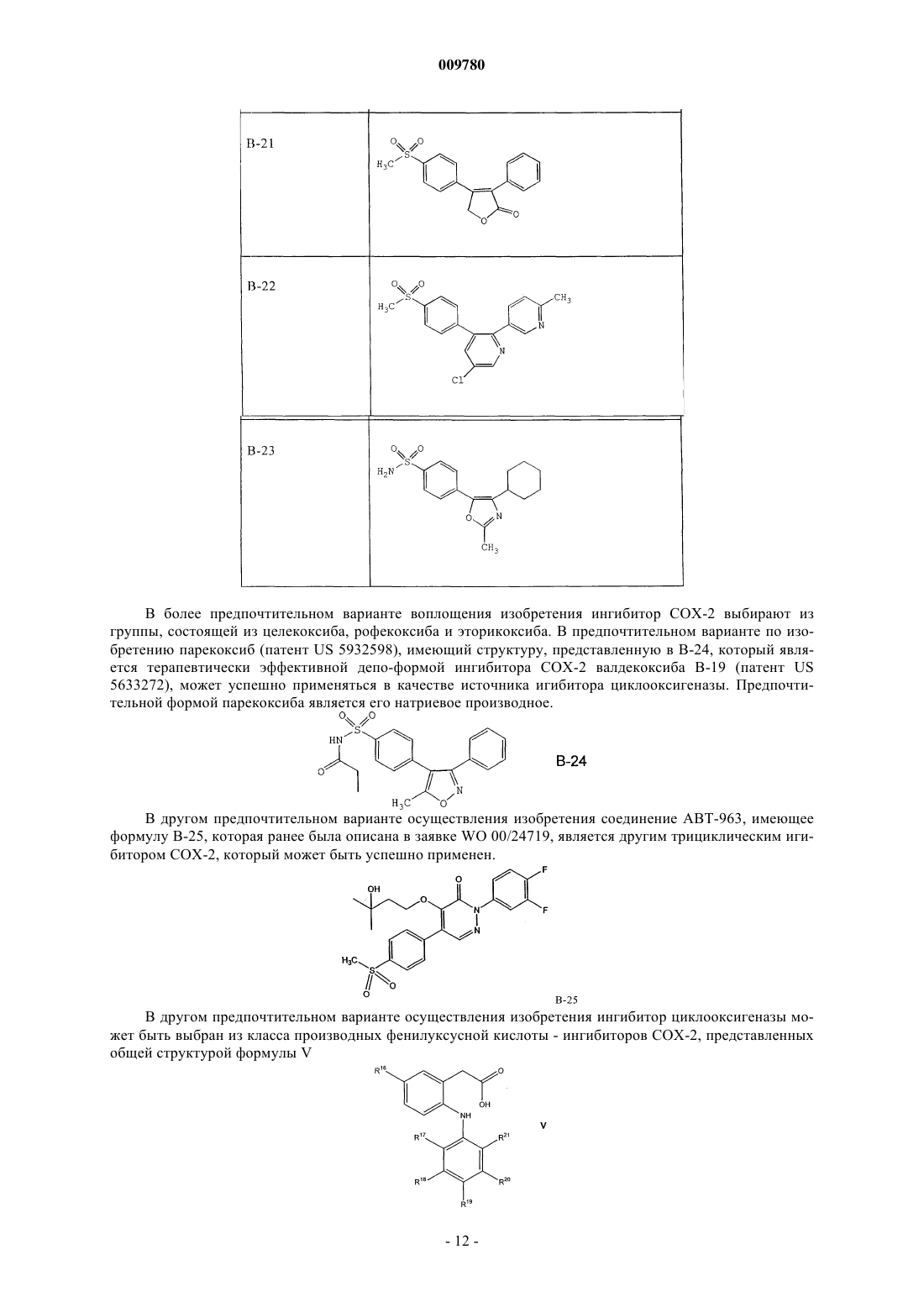
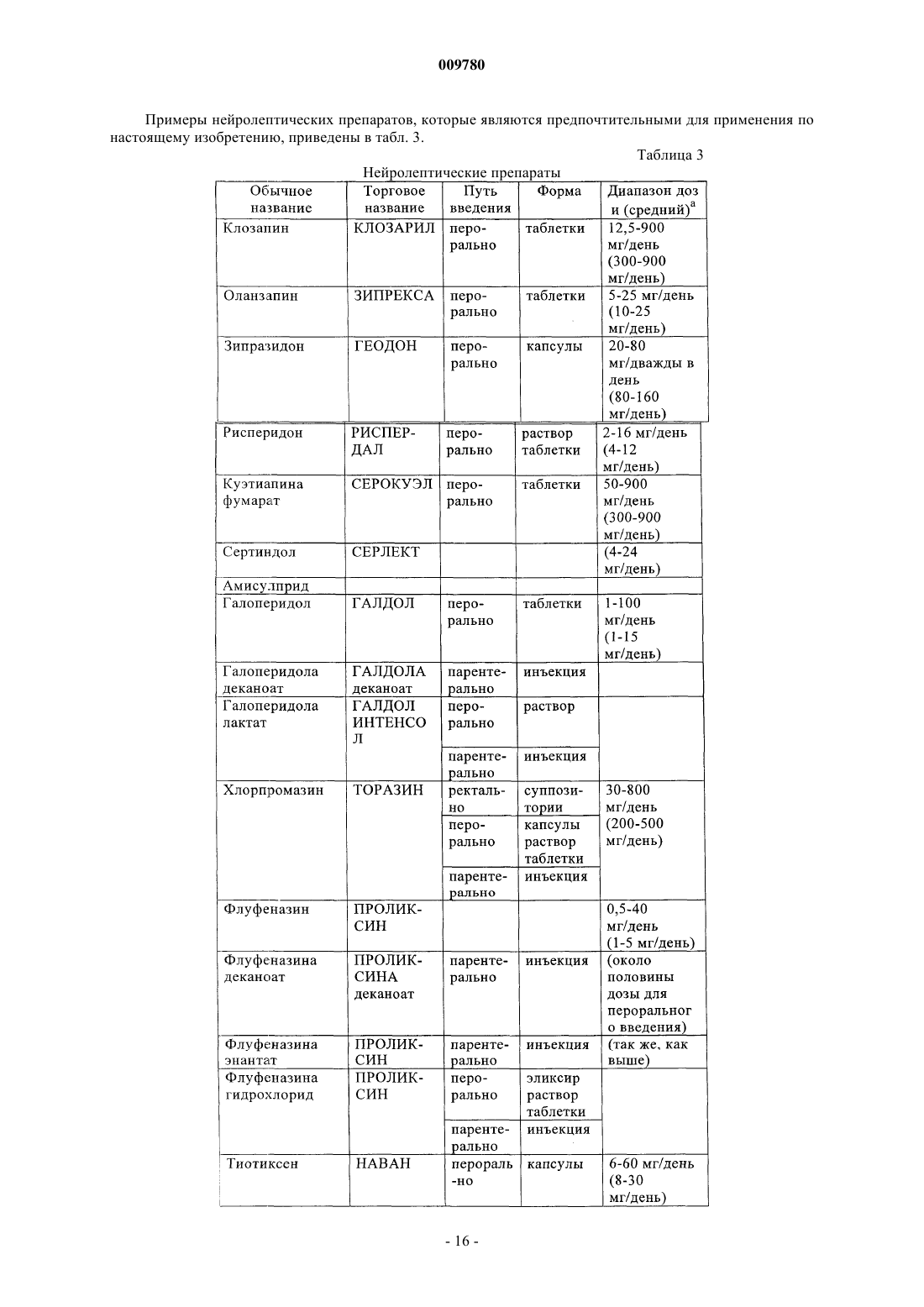
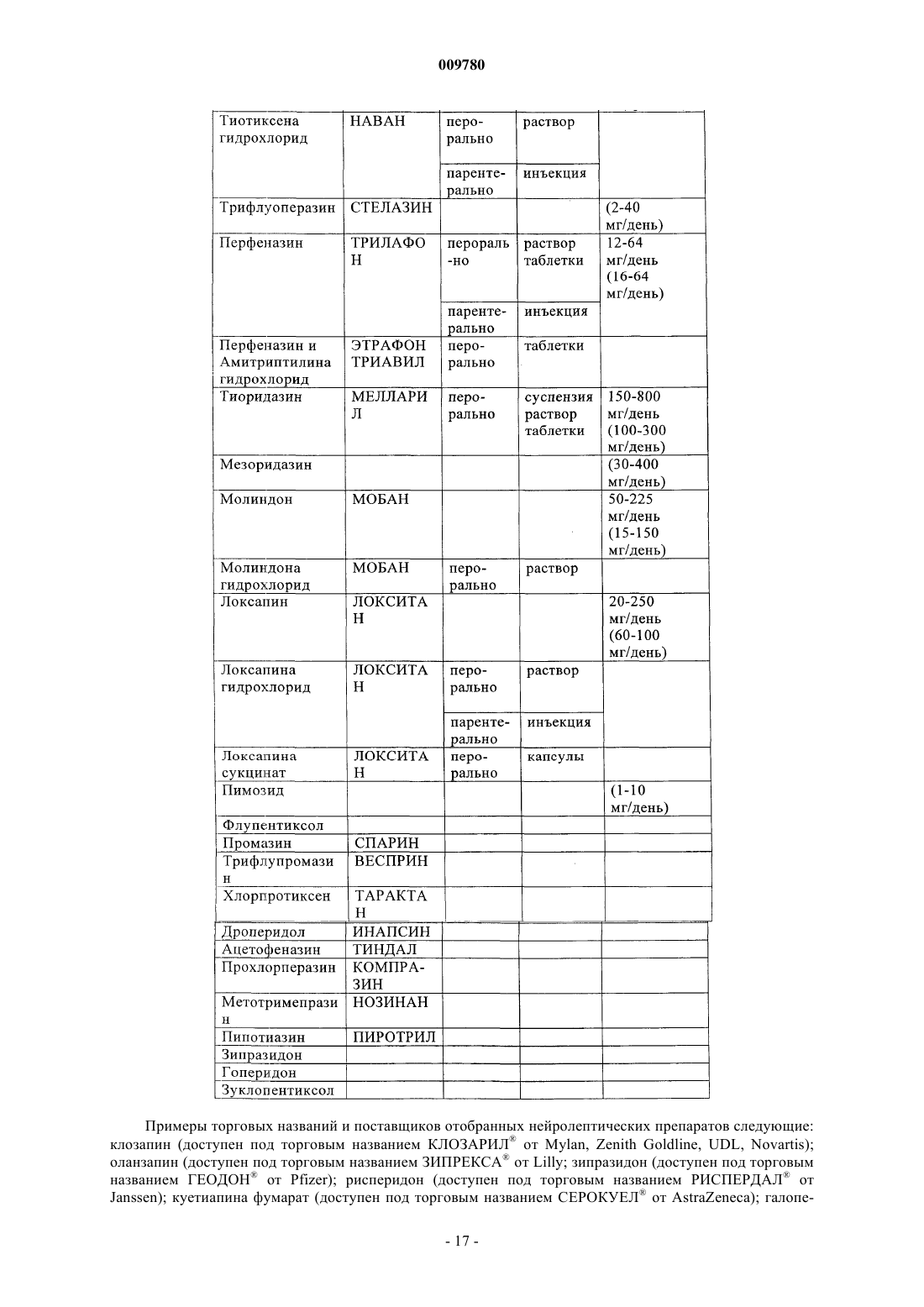
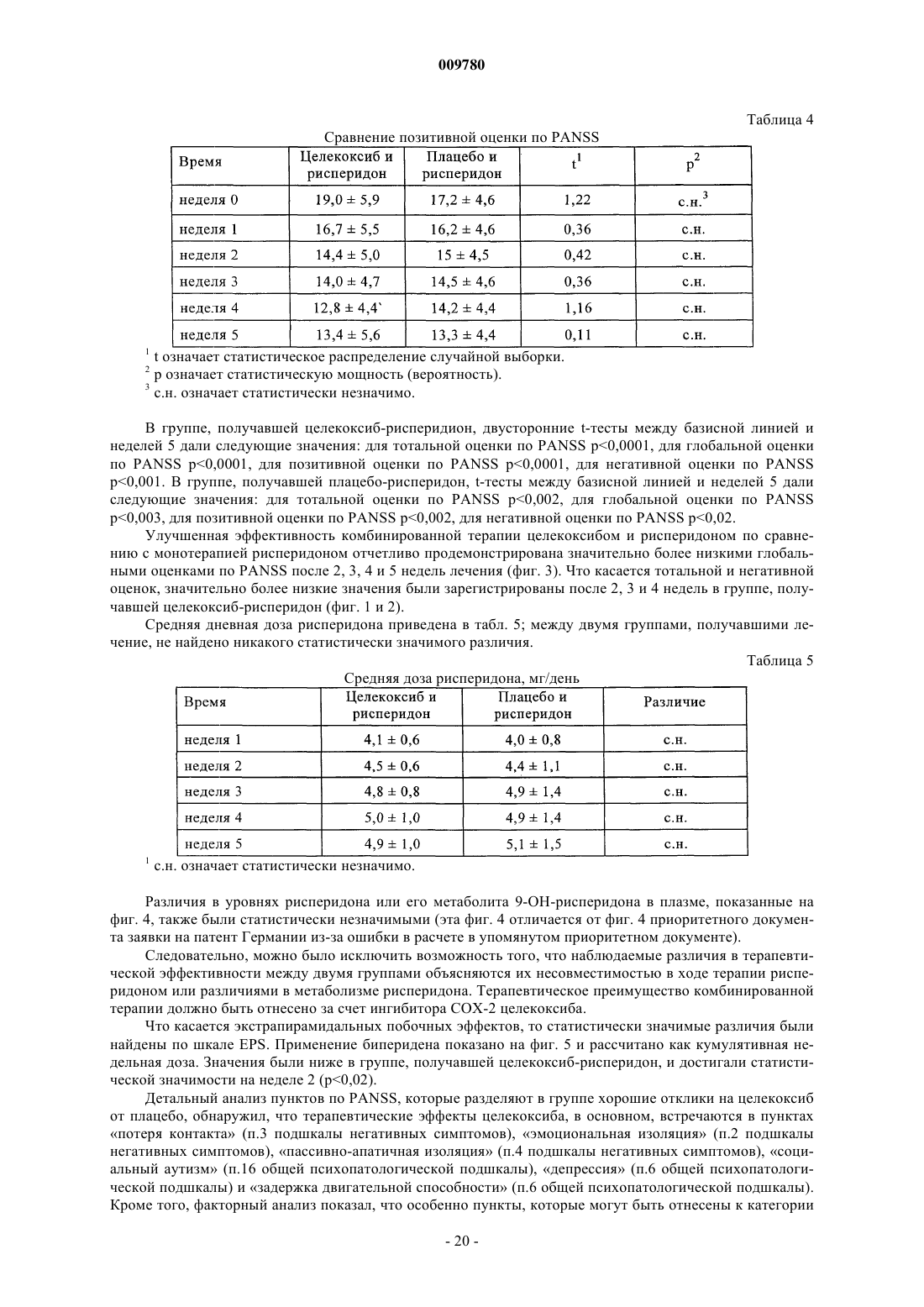
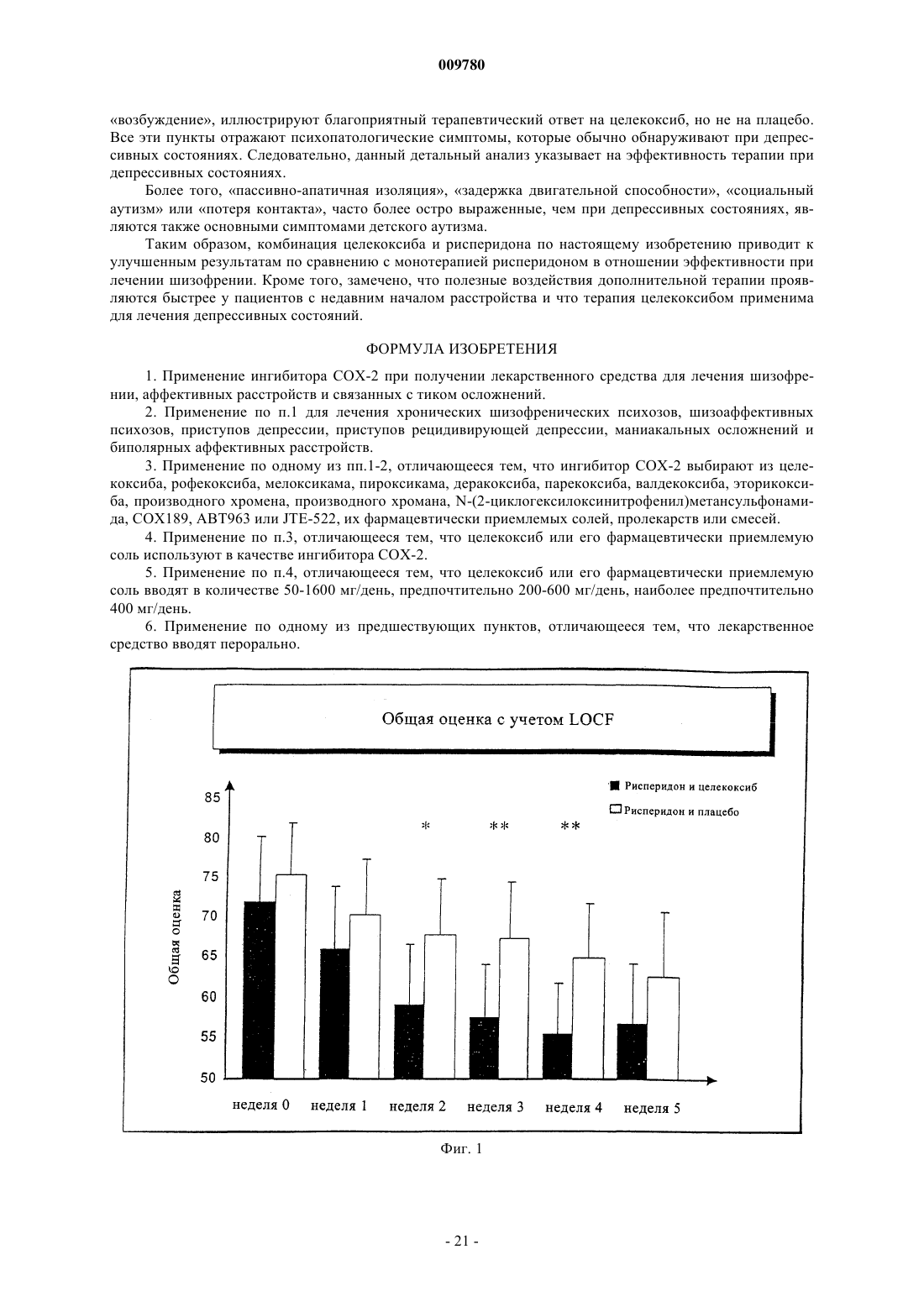
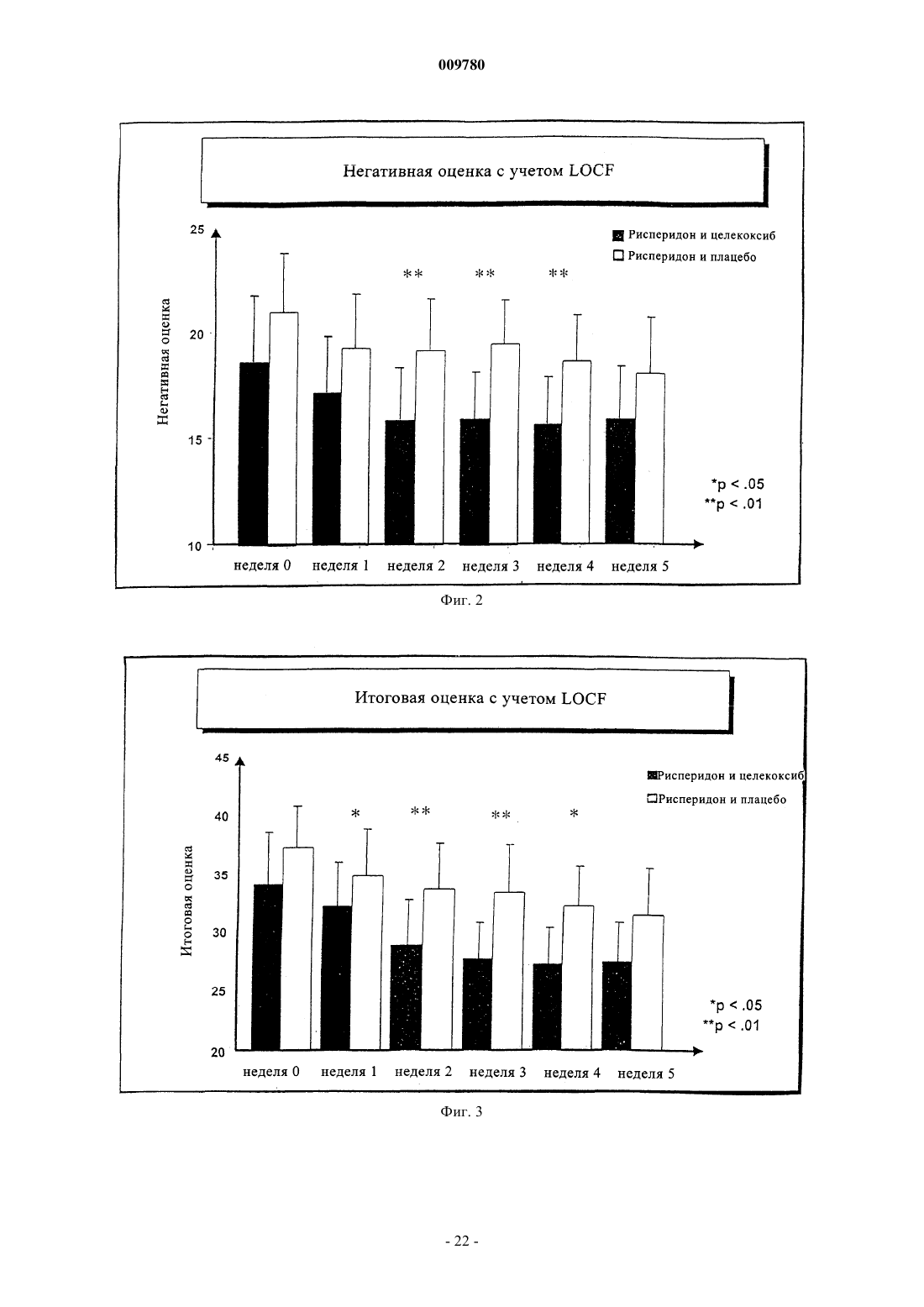
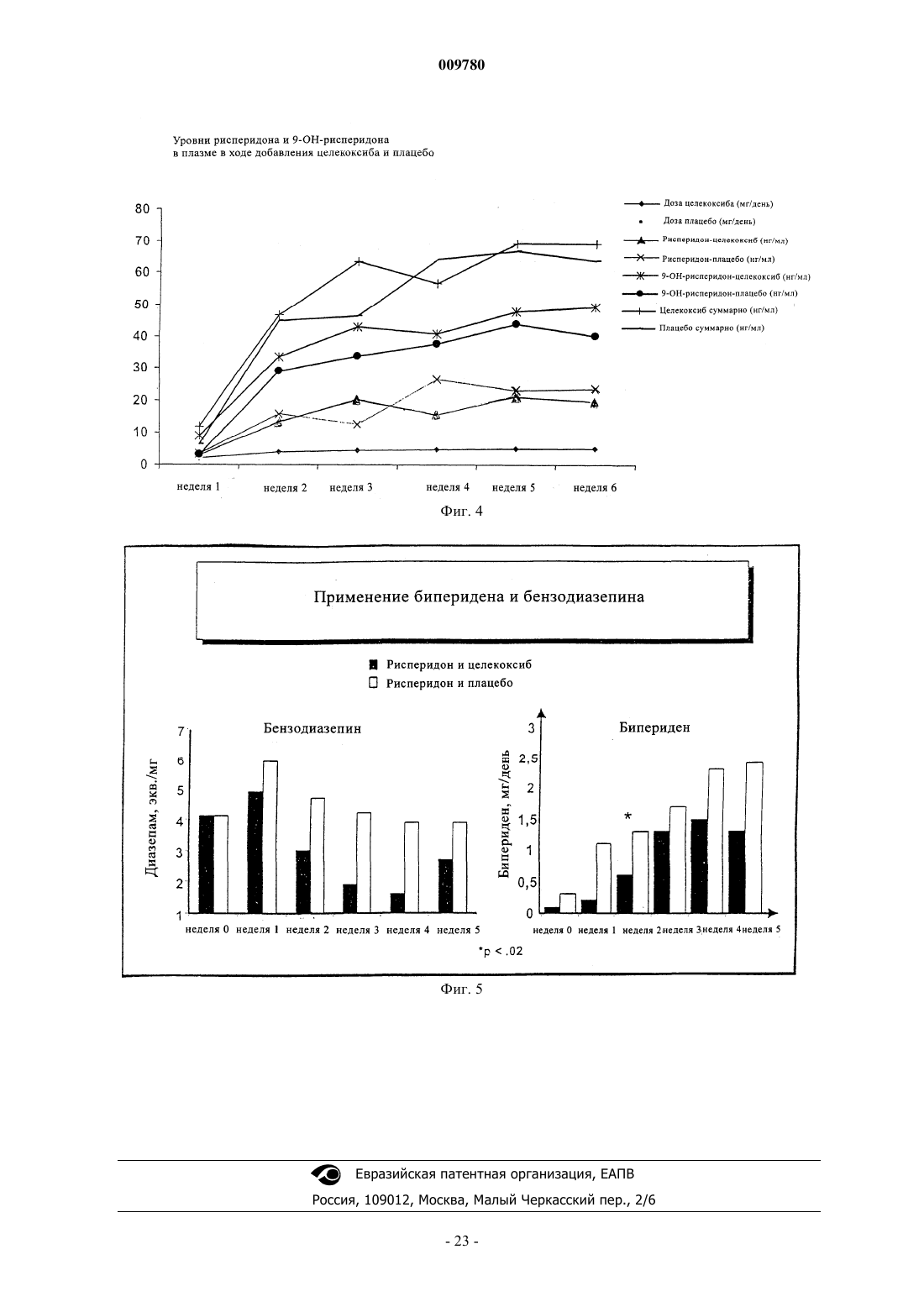
009780 Изобретение имеет отношение к применению ингибитора циклооксигеназы-2 (СОХ-2) для лечения психиатрических нарушений, таких как шизофрения, аффективные расстройства или осложнения, связанные с тиком, в особенности хронические шизофренические психозы и шизоаффективные психозы,временные острые психотические расстройства, приступы депрессии, приступы рецидивирующей депрессии, маниакальные осложнения и биполярные аффективные расстройства. Кроме того, изобретение относится к применению ингибитора СОХ-2 в комбинации с нейролептическим препаратом или антидепрессантом для лечения психиатрических нарушений, таких как шизофрения, аффективные расстройства или осложнения, связанные с тиком. Связь между иммунологическими дисфункциями и психотическими заболеваниями, такими как шизофрения или аффективные расстройства, обсуждалась с разногласиями в оценках в течение последнего столетия. В случае шизофрении, например, патогенез до сих пор не известен, но многие данные свидетельствуют о том, что шизофрения является синдромом, основанным на различных патогенетических процессах. Воспалительный/иммунологический патогенез был обсужден для подгруппы пациентов с шизофренией (Yolken R.H., Torrey E.F.: Вирусы, шизофрения и биполярное расстройство. Clin. Microbiol. Rev. 1995; 8: 131-145; Korschenhausen D., Hampel H., Ackenheil M., Penning R., Muller N.: Продукты деградации фибрина в посмертной мозговой ткани шизофреников: возможный маркер лежащих в основе воспалительных процессов. Schizophr. Res. 1996; 19: 103-109; Muller N., Ackenheil M.: Психонейроиммунология и цитокиновая сеть в ЦНС: вовлеченность в психиатрические расстройства. Prog. Neuropsychopharmacol.Biol. Psychiat. 1998; 22: 1-33). Исследования показали, что количество таких активирующих цитокинов,как интерлейкин-1 (IL-I) и IL-2, в спинно-мозговой жидкости увеличивается у пациентов с шизофренией по сравнению с контролями (Sirota P., Schild K., Elizur A., Djaldetti M., Fishman P.: Повышенная, подобная интерлейкину-1 и интерлейкину-3 активность у пациентов с шизофренией. Prog. Neuropsychopharmacol.Biol. Psychiatry. 1995; 19: 85-83; Licinio J., Seibyl, J.P., Altemus M., Charney D.S., Krystal J.H.: Повышенные уровни интерлейкина-2 у шизофреников, не принимавших нейролептические средства. Am. J. Psychiatry 1993; 150: 408-1410) и что увеличенные уровни IL-2 в спинно-мозговой жидкости (CSF) являются прогнозом повышенной вероятности рецидива шизофрении (McAllister C.G., van Kamen D.P., Rehn T.J., Miller A.L.,Gurklis J., Kelley M.E., Yao J., Peters J.L.: Повышение в CSF уровней интерлейкина-2 при шизофрении: эффекты рецидива психоза и статус лекарственной терапии. Am. J. Psychiatry. 1995; 152: 1291-1297). С другой стороны, в подгруппе пациентов с шизофренией наблюдался сниженный иммунный ответ по сравнению с контролями, возможно, из-за нарушения презентации антигена или распознавания антигена (Schwarz M.J., Riedel M., Ackenheil M., Muller N.: Сниженные уровни растворимой межклеточной адгезионной молекулы-1 (sICAM-1) у не леченных и леченных пациентов с шизофренией. Biol. Psychiatry. 2000; 47: 29-33), например усиленная иммунная реакция в центральной нервной системе может не быть адекватно регулируемой в периферической иммунной системе. Это наблюдается, в основном, у пациентов при острой шизофрении с недавним началом заболевания. Однако другая группа пациентов с шизофренией, по-видимому, представляет повышенную активацию периферической иммунной системы в смысле аутоиммунных реакций (Radaport M.H., Muller N.: Иммунологические состояния, ассоциированные с шизофренией. В: Ader R., Felten D.L., Cohen N. (ред.)Psychoneuroimmunology, третье издание. T. 2, San Diego, Academic Press, 2001; стр. 373-382; Radaport M.H.,McAllister C.G., Kim Y.S., Han J.H., Pickar D., Nelson D.M., Kirch D.G., Paul S.M.: Повышенные уровни растворимых рецепторов интерлейкина-2 у кавказских и корейских пациентов с шизофренией. Biol.Psychiatry. 1994; 35: 767-771). В некоторых исследованиях наблюдались повышенные титры антител против белка теплового шока 60 (Kilidireas K., Latov N., Strauss D.H., Aviva D.G., Hashim G.A., Gorman J.M.,Sadiq S.А.: Антитела к человеческому белку теплового шока 60 кД у пациентов с шизофренией. Lancet. 1992; 340: 69-572), причем повышение сопровождалось увеличением растворимых рецепторов IL-2 в сыворотке и повышением титров растворимой адгезионной молекулы sICAM-1 (Radaport M.H., Muller N.: Иммунологические состояния, ассоциированные с шизофренией. В: Ader R., Felten D.L., Cohen N. (ред.)Psychoneuroimmunology, третье издание. T. 2, San Diego, Academic Press, 2001; стр. 373-382; Schwarz M.J.,Riedel M., Gruber R., Ackenheil M., Muller N.: Антитела к белкам теплового шока у пациентов с шизофренией - вовлеченность в механизм заболевания. Am. J. Psychiatry. 1999; 156, 1103, 1104). Тесная взаимосвязь между высокими титрами sICAM и более выраженными негативными симптомами шизофрении(Schwarz M.J., Riedel M., Gruber R., Ackenheil M., Muller N.: Уровни растворимых адгезионных молекул при шизофрении: связь с психопатологией. В: N. Muller (гл. ред.) Psychiatry, Psychoneuroimmunology,and Viruses. Springer Verlag, Wien, 1999; NY, стр. 121-130), а также между высокими уровнями IgG в спинно-мозговой жидкости и более выраженными негативными симптомами поддерживает дополнительно это наблюдение (Muller N., Ackenheil M.: Содержание иммуноглобулина и альбумина в спинно-мозговой жидкости у пациентов с шизофренией: взаимосвязь с негативной симптоматологией. Schizophrenia Res. 1995; 14: 223-228). Аффективные расстройства, особенно депрессивные заболевания, могут также иметь воспалительное происхождение. Это проявляется в том факте, что общие воспалительные заболевания сопровождаются депрессивными синдромами повышенной степени, а также в том факте, что при депрессивных за-1 009780 болеваниях признаки воспаления наблюдаются чаще по сравнению с физиологически здоровыми людьми. Научно это было отражено в моноцитной/макрофаговой гипотезе депрессии. Проявление тиков во многих случаях тоже обсуждалось как последствие воспалительных реакций. В основе изобретения лежит идея о том, что вещества с иммуномодулирующими свойствами могли быть применены для лечения психиатрических расстройств, таких как шизофрения, аффективные расстройства или расстройства, связанные с тиком, которые, по крайней мере, частично основаны на иммунологических патогенетических реакциях. Например, для лечения шизофрении стало доступным большое количество нейролептических препаратов (так называемых классических и атипичных нейролептиков), среди которых появившиеся недавно атипичные нейролептики отличаются сравнительно хорошей эффективностью при более благоприятном профиле побочных эффектов. В отличие от классических нейролептиков, которые, главным образом,эффективны в лечении позитивных симптомов шизофрении, атипичные нейролептики улучшают как позитивные симптомы (галлюцинации, бред и понятийное расстройство), так и негативные симптомы шизофрении (апатию, аутизм, аффективное уплощение и скудость речи). Вдобавок к этому, повидимому, из-за их измененного профиля связывания с рецепторами, атипичные нейролептики вызывают минимальные экстрапирамидальные симптомы и редко являются причиной отсроченных дискинезий. Как бы то ни было, в большинстве случаев нейролептики действуют в качестве ориентированной на синдром терапии и реже в качестве причинной терапии. Следовательно, существует необходимость в дополнительных лекарственных средствах для лечения психиатрических расстройств, таких как шизофрения, аффективные расстройства или осложнения,связанные с тиком. Настоящее изобретение направлено на применение ингибиторов СОХ-2 в качестве единственного действующего вещества в препарате при получении лекарственного средства для лечения психиатрических расстройств, таких как шизофрения, аффективные расстройства или осложнения, связанные с тиком, особенно хронического шизофренического психоза и шизоаффективного психоза, временных острых психотических расстройств, приступов депрессии, приступов рецидивирующей депрессии, маниакальных осложнений и биполярных аффективных расстройств. В контексте по настоящему изобретению лечение заболевания или расстройства означает охват современной терапии, а также поддерживающей терапии и профилактики рецидива. Ингибиторы СОХ-2 по настоящему изобретению принадлежат к классу нестероидных противовоспалительных препаратов (NSAIDs). В течение некоторого времени было известно, что многие из общеизвестных NSAIDs модулируют синтез простагландинов путем ингибирования циклооксигеназы, которая катализирует превращение арахидоновой кислоты - первый этап простагландинового синтетического пути обмена. Однако применение высоких доз общеизвестных NSAIDs может дать тяжелые побочные эффекты, что ограничивает их терапевтический потенциал. При попытке уменьшить нежелательные побочные эффекты обычных NSAIDs было обнаружено, что две циклооксигеназы вовлечены в трансформацию арахидоновой кислоты в качестве первого этапа в простагландиновом синтетическом пути обмена. Эти ферменты были названы циклооксигеназой-1 (COX-1) и циклооксигеназой-2 (СОХ-2) (Needleman, P. и др., J. Rheumatol, 24, Suppl. 49: 6-8 (1997); Fu, J.Y., и др., J. Biol. Chem., 265 (28): 16737-40 (1990. Было показано, что COX-1 является постоянно продуцируемым ферментом, т.е. вовлеченным во многие невоспалительные регуляторные функции, ассоциированные с простагландинами. С другой стороны, СОХ 2 является индуцируемым ферментом со значительным вовлечением в воспалительную реакцию. Воспаление вызывает индукцию COX-2, приводящую к высвобождению простаноидов, которые сенсибилизируют окончания болевых рецепторов и продуцируют локализованную болевую гиперчувствительность(Samad, T.А. и др., Nature, 410 (6827): 471-5 (2001. В настоящее время известно, что обычные NSAIDs являются ингибиторами как COX-1, так и СОХ-2. Соответственно, при введении в достаточно высоких концентрациях эти NSAIDs воздействуют не только на воспалительные последствия активности СОХ-2,но также и на полезные виды активности COX-1. Недавно были открыты соединения, которые избирательно ингибируют СОХ-2 в большей степени, чем активность COX-1. Считается, что эти новые ингибиторы СОХ-2 имеют преимущества в том, что обладают способностью предупреждать или ослаблять воспаление, при этом лишены вредных побочных воздействий, ассоциируемых с ингибированием COX-1,таких как побочные воздействия на желудочно-кишечный такт и почки, а также ингибирование агрегации тромбоцитов. Известно применение ингибиторов СОХ-2 в терапии артритов и родственных состояний. Патент US 5760068 описывает применение ингибиторов СОХ-2 для лечения ревматоидного артрита и остеоартрита. Заявка WO 00/32189 раскрывает получение фармацевтических композиций, содержащих ингибитор СОХ-2 целекоксиб, и применение целекоксиба для лечения ревматоидного артрита или в качестве болеутоляющего средства. Термин ингибиторы СОХ-2 охватывает соединения, которые избирательно ингибируют циклооксигеназу-2 по отношению к циклооксигеназе-1, и также включает их фармацевтически приемлемые соли. В объем по настоящему изобретению включены также соединения, которые действуют как пролекарства ингибиторов циклооксигеназы-2. Термин пролекарство, как он использован в контексте при упомина-2 009780 нии ингибиторов СОХ-2, относится к химическому соединению, которое может быть превращено в активный ингибитор СОХ-2 метаболическим или простым химическим способом в организме субъекта. Ингибитором СОХ-2 по настоящему изобретению может быть, например, ингибитор СОХ-2 мелоксикам или его пролекарство. В другом варианте воплощения изобретения ингибитором СОХ-2 может быть ингибитор СОХ-2 RS 57067, 6-5-(4-хлорбензоил)-1,4-диметил-1H-пиррол-2-ил]метил]-3(2H)-пиридазинон, формула В-2 (регистрационный номер CAS 179382-91-3), или его фармацевтически приемлемая соль, или его пролекарство. В предпочтительном варианте воплощения изобретения ингибитор СОХ-2 является производным хромена, т.е. замещенным бензопираном или аналогом замещенного бензопирана, и еще более предпочтительно выбран из группы, состоящей из замещенных бензотиопиранов, дигидрохинолинов или дигидронафталинов со структурой любого из соединений, имеющих строение, представленное общими формулами I, II или III, приведенными ниже, и в качестве примера, а не ограничения имеющий структуры,раскрываемые в табл. 1, включая его диастереомеры, энантиомеры, рацематы, таутомеры, соли, сложные эфиры, амиды и пролекарства. Бензопирановые ингибиторы СОХ-2, используемые в практических целях по настоящему изобретению, описаны в патентах US 6034256 и 6077850. Формула IR1 выбирают из группы, состоящей из водорода и арила;R3 выбирают из группы, состоящей из галоидалкила, алкила, аралкила, циклоалкила и арила, необязательно замещенного одним радикалом или несколькими, выбираемыми из алкилтио, нитро и алкилсульфонила; иR4 выбирают из группы, состоящей из одного радикала или нескольких, выбираемых из водорода, галоида, алкила, аралкила, алкокси, арилокси, гетероарилокси, аралкилокси, гетероаралкилокси, галоидалкила, галоидалкокси, алкиламино, ариламино, аралкиламино, гетероариламино, гетероарилалкиламино, нитро, амино, аминосульфонила, алкиламиносульфонила, ариламиносульфонила, гетероариламиносульфонила, аралкиламиносульфонила, гетероаралкиламиносульфонила, гетероциклосульфонила, алкилсульфонила,гидроксиарилкарбонила, нитроарила, необязательно замещенного арила, необязательно замещенного гетероарила, аралкилкарбонила, гетероарилкарбонила, арилкарбонила, аминокарбонила и алкилкарбонила; илиR4 вместе с кольцом E образует нафтильный радикал; или изомер или фармацевтически приемлемая соль на ее основе, включая диастереомеры, энантиомеры,рацематы, таутомеры, соли, сложные эфиры, амиды и пролекарства. Формула IIR6 выбирают из группы, состоящей из галоидалкила, алкила аралкила, циклоалкила и арила, где каждый галоидалкил, алкил, аралкил, циклоалкил и арил является независимо и необязательно замещенным одним или несколькими радикалами, выбираемыми из группы, состоящей из алкилтио, нитро и алкилсульфонила; иR7 означает один или несколько радикалов, выбираемых из группы, состоящей из водорода, галоида, алкила, аралкила, алкокси, арилокси, гетероарилокси, аралкилокси, гетероаралкилокси, галоидалкила,галоидалкокси, алкиламино, ариламино, аралкиламино, гетероариламино, гетероарилалкиламино, нитро,амино, аминосульфонила, алкиламиносульфонила, ариламиносульфонила, гетероариламиносульфонила,аралкиламиносульфонила, гетероаралкиламиносульфонила, гетероциклосульфонила, алкилсульфонила,необязательно замещенного арила, необязательно замещенного гетероарила, аралкилкарбонила, гетероарилкарбонила, арилкарбонила, аминокарбонила и алкилкарбонила; илиR7 вместе с кольцом А образует нафтильный радикал; или изомер или фармацевтически приемлемая соль на этой основе. Ингибитор СОХ-2 может также быть соединением формулы II, гдеY выбирают из группы, состоящей из кислорода и серы;R7 означает один или несколько радикалов, выбираемых из группы, состоящей из водорода, галоида,(низш.)алкила, (низш.)алкокси, (низш.)галоидалкила, (низш.)галоидалкокси, (низш.)алкиламино, нитро,амино, аминосульфонила, (низш.)алкиламиносульфонила, 5-членного гетероарилалкиламиносульфонила,6-членного гетероарилалкиламиносульфонила, (низш.)аралкиламиносульфонила, 5-членного азотсодержащего гетероциклосульфонила, 6-членного азотсодержащего гетероциклосульфонила, (низш.)алкилсульфонила, необязательно замещенного фенила, (низш.)аралкилкарбонила и (низш.)алкилкарбонила; илиR7 вместе с кольцом А образует нафтильный радикал; или его изомером или фармацевтически приемлемой солью. Ингибитор СОХ-2 может быть также соединением формулы II, гдеR7 означает один или несколько радикалов, выбираемых из группы, состоящей из водорода, галоида, (низш.)алкила, (низш.)галоидалкила, (низш.)галоидалкокси, (низш.)алкиламино, амино, аминосульфонила, (низш.)алкиламиносульфонила, 5-членного гетероарилалкиламиносульфонила, 6-членного гетероарилалкиламиносульфонила, (низш.)аралкиламиносульфонила, (низш.)алкилсульфонила, 6-членного азотсодержащего гетероциклосульфонила, необязательно замещенного фенила, (низш.)аралкилкарбонила иR7 вместе с кольцом А образует нафтильный радикал; или его изомером, или фармацевтически приемлемой солью. Ингибитор СОХ-2 может быть также соединением формулы II, гдеR7 означает один или несколько радикалов, выбираемых из группы, состоящей из водорода, хлора,фтора, брома, йода, метила, этила, изопропила, трет-бутила, бутила, изобутила, пентила, гексила, метокси,этокси, изопропилокси, трет-бутилокси, трифторметила, дифторметила, трифторметокси, амино, N,N-диметиламино, N,N-диэтиламино, N-фенилметиламиносульфонила, N-фенилэтиламиносульфонила, N-(2 фурилметил)аминосульфонила, нитро, N,N-диметиламиносульфонила, аминосульфонила, N-метиламиносульфонила, N-этилсульфонила, 2,2-диметилэтиламиносульфонила, N,N-диметиламиносульфонила, N(2-метилпропил)аминосульфонила, N-морфолиносульфонила, метилсульфонила, бензилкарбонила, 2,2 диметилпропилкарбонила, фенилацетила и фенила; илиR2 вместе с кольцом А образует нафтильный радикал; или его изомером, или фармацевтически приемлемой солью. Ингибитор СОХ-2 может быть также соединением формулы II, гдеR6 выбирают из группы, состоящей из трифторметила и пентафторэтила; иR7 означает один или несколько радикалов, выбираемых из группы, состоящей из водорода, хлора,фтора, брома, йода, метила, этила, изопропила, трет-бутила, метокси, трифторметила, трифторметокси,N-фенилметиламиносульфонила, N-фенилэтиламиносульфонила, N-(2-фурилметил)аминосульфонила,N,N-диметиламиносульфонила, N-метиламиносульфонила, N-(2,2-диметилэтил)аминосульфонила, диметиламиносульфонила, 2-метилпропиламиносульфонила, N-морфолиносульфонила, метилсульфонила,бензилкарбонила и фенила; илиR7 вместе с кольцом А образует нафтильный радикал; или его изомером, или пролекарством. Ингибитор СОХ-2 по настоящему изобретению может также быть соединением, имеющим структуру формулы IIIR9 выбирают из группы, состоящей из водорода и галоида;R12 выбирают из группы, состоящей из водорода, галоида, (низш.)алкила, (низш.)алкокси и арила; или его изомером, или пролекарством. Ингибитор СОХ-2 может быть также соединением, имеющим структуру формулы III, гдеR8 выбирают из группы, состоящей из трифторметила и пентафторэтила;R12 выбирают из группы, состоящей из водорода, хлора, брома, фтора, метила, этила, трет-бутила,метокси и фенила; или его изомером, или пролекарством. Таблица 1 Примеры хроменовых ингибиторов СОХ-2 в качестве вариантов воплощения изобретения-7 009780 Специфические соединения, которые полезны как ингибиторы СОХ-2, включают:y1) [2-трифторметил-5-(3,4-дифторфенил)-4-оксазолил]бензолсульфонамид; у 2) 4-[2-метил-4-фенил-5-оксазолил]бензолсульфонамид или; у 3) 4-[5-(3-фтор-4-метоксифенил-2-трифторметил)-4-оксазолил]бензолсульфонамид; или их фармацевтически приемлемая соль, или пролекарство. В дополнительном предпочтительном варианте осуществления изобретения ингибитор циклооксигеназы может быть выбран из класса трициклических игибиторов СОХ-2, представленных общей струк- 10009780 турой формулы IV где Z выбирают из группы, состоящей из частично ненасыщенных или ненасыщенных гетероциклильных или частично ненасыщенных или ненасыщенных карбоциклических колец;R13 выбирают из группы, состоящей из гетероциклила, циклоалкила, циклоалкенила и арила, где R13 необязательно замещен в замещаемом положении одним или несколькими радикалами, выбираемыми из алкила, галоидалкила, циано, карбоксила, алкоксикарбонила, гидроксила, гидроксиалкила, галоидалкокси,амино, алкиламино, ариламино, нитро, алкоксиалкила, алкилсульфинила, галоида, алкокси и алкилтио;R14 выбирают из группы, состоящей из метила или амино; иR15 выбирают из группы, состоящей из радикала, выбираемого из водорода, галоида, алкила, алкенила,алкинила, оксо, циано, карбоксила, цианоалкила, гетероциклилокси, алкилокси, алкилтио, алкилкарбонила,циклоалкила, арила, галоидалкила, гетероциклила, циклоалкенила, аралкила, гетероциклилалкила, ацила, алкилтиоалкила, гидроксиалкила, алкоксикарбонила, арилкарбонила, аралкилкарбонила, аралкенила, алкоксиалкила, арилтиоалкила, арилоксиалкила, аралкилтиоалкила, аралкоксиалкила, алкоксиаралкоксиалкила, алкоксикарбонилалкила, аминокарбонила, аминокарбонилалкила, алкиламинокарбонила, N-ариламинокарбонила, N-алкил-N-ариламинокарбонила, алкиламинокарбонилалкила, карбоксиалкила, алкиламино, N-ариламино, N-аралкиламино, N-алкил-N-аралкиламино, N-алкил-N-ариламино, аминоалкила, алкиламиноалкила,N-ариламиноалкила, N-аралкиламиноалкила, N-алкил-N-аралкиламиноалкила, N-алкил-N-ариламиноалкила,арилокси, аралкокси, арилтио, аралкилтио, алкилсульфинила, алкилсульфонила, аминосульфонила, алкиламиносульфонила, N-ариламиносульфонила, арилсульфонила, N-алкил-N-ариламиносульфонила; или его пролекарство. В предпочтительном варианте воплощения изобретения ингибитор СОХ-2, представленный выше формулойIV, выбирают из группы соединений, изображенных в табл. 2, которая включает целекоксиб (B-18), валдекоксиб(B-19), деракоксиб (В-20), рофекоксиб (В-21), эторикоксиб (МК-663; В-22), JTE-522 (В-23) или их депо-формы. Дополнительная информация о выбранных примерах ингибиторов СОХ-2, обсужденных выше, может быть найдена следующим образом: целекоксиб (регистрационный номер CAS 169590-42-5, С-2779, SC-58653 и в патенте US 5466823); деракоксиб (регистрационный номер CAS 169590-41-4); рофекоксиб (регистрационный номер CASS 162011-90-7); соединение В-24 (патент US 5840924); соединение В-26 (заявка WO 00/25779); и эторикоксиб (регистрационный номер CAS 202409-33-4, МК-663, SC-86218 и в заявке WO 98/03484). Таблица 2 Примеры трициклических ингибиторов СОХ-2 как варианты воплощения изобретения В более предпочтительном варианте воплощения изобретения ингибитор СОХ-2 выбирают из группы, состоящей из целекоксиба, рофекоксиба и эторикоксиба. В предпочтительном варианте по изобретению парекоксиб (патент US 5932598), имеющий структуру, представленную в В-24, который является терапевтически эффективной депо-формой ингибитора СОХ-2 валдекоксиба B-19 (патент US 5633272), может успешно применяться в качестве источника игибитора циклооксигеназы. Предпочтительной формой парекоксиба является его натриевое производное. В другом предпочтительном варианте осуществления изобретения соединение АВТ-963, имеющее формулу В-25, которая ранее была описана в заявке WO 00/24719, является другим трициклическим игибитором СОХ-2, который может быть успешно применен. В другом предпочтительном варианте осуществления изобретения ингибитор циклооксигеназы может быть выбран из класса производных фенилуксусной кислоты - ингибиторов СОХ-2, представленных общей структурой формулы V- 12009780 где R16 означает метил или этил;R17 означает хлор или фтор;R18 означает водород или фтор;R20 означает водород или фтор;R21 означает хлор, фтор, трифторметил или метил, при условии, что R17, R18, R19 и R20 не все означают фтор, когда R16 означает этил, и R19 означает H. Особенно предпочтительным производным фенилуксусной кислоты - ингибитором СОХ-2, который описан в заявке WO 99/11605, является соединение, которое имеет обозначение COX189 (регистрационный номер CAS 346670-74-4) и структуру, представленную формулой V, гдеR21 означает метил. Соединения, имеющие структуру, подобную той, что представлена формулой V, которые могут служить в качестве ингибиторов СОХ-2 по настоящему изобретению, описаны в патентах US 6310099 и 6291523. Другие предпочтительные ингибиторы СОХ-2, которые могут применяться по настоящему изобретению, имеют общую структуру, представленную формулой VI, где группа J означает карбоцикл или гетероцикл. Особенно предпочтительные варианты имеют структуру(NS-398, регистрационный номер CAS 123653-11-2), имеющего такую структуру, как представленная формулой В-26, описана, например, Yoshimi N. и др., Japanese J. Cancer Res., 90 (4): 406-412 (1999); Оценка противовоспалительной активности ингибитора СОХ-2 RWJ 63556 на модели воспаления у собак описана Kirchner и др., J. Pharmacol. Exp. Ther. 282, 1094-1101 (1997). Другие вещества, которые могут служить в качестве ингибиторов СОХ-2 по настоящему изобретению, включают производные диарилметилиденфурана, которые описаны в патенте US 6180651. Такие производные диарилметилиденфурана имеют приведенную ниже общую формулу VII где T и M означают независимо фенильный радикал, нафтильный радикал, радикал, полученный из гетероцикла 5- или 6-членного и обладающего 1-4 гетероатомами, или радикал, полученный из насыщенного углеводородного кольца, имеющего 3-7 атомов углерода; по меньшей мере один из заместителей Q1, Q2, L1 или L2 означает группу -S(O)nR, гдеR означает (низш.)алкильный радикал, имеющий 1-6 атомов углерода, или (низш.)галоидалкильный радикал, имеющий 1-6 атомов углерода, или группу -SO2NH2; и расположен в пара-положении, другие означают независимо атом водорода, атом галоида, (низш.)алкильный радикал, имеющий 1-6 атомов углерода, трифторметильный радикал или O-(низш.)алкильный радикал, имеющий 1-6 атомов углерода,илиR24, R25, R26 и R27 означают независимо атом водорода, атом галоида, (низш.)алкильный радикал,имеющий 1-6 атомов углерода, (низш.)галоидалкильный радикал, имеющий 1-6 атомов углерода, или ароматический радикал, выбираемый из группы, состоящей из фенила, нафтила, тиенила, фурила и пиридила; илиR24, R25 или R26, R27 образуют вместе с атомом углерода, к которому они присоединены, насыщенное углеводородное кольцо, имеющее 3-7 атомов углерода; или их изомер, или пролекарство. Особые вещества, которые включены в эту семью соединений и которые могут служить в качестве ингибиторов СОХ-2 по настоящему изобретению, включают N-(2-циклогексилнитрофенил)метансульфонамид и (E)-4-[(4-метилфенил)(тетрагидро-2-оксо-3-фуранилиден)метил]бензолсульфонамид. Ингибиторы СОХ-2, которые полезны по настоящему изобретению, включают дарбуфелон (Pfizer),CS-502 (Sankyo), LAS 34475 (Almirall Profesfarma), LAS 34555 (Almirall Profesfarma), S-33516 (Servier, см. Новости рубрики современные препараты в http://www.current-drugs.com/NEWS/Inflaml.htm, 10/04/2001),BMS-347070 (Bristol Myers Squibb, описанный в патенте US 6180651), MK-966 (Merck), L-783003 (Merck),T-614 (Toyama), D-1367 (Chiroscience), L-748731 (Merck), CT3 (Atlantic Pharmaceutical), CGP-28238 (Novartis),BF-389 (Biofor/Scherer), GR-253035 (Glaxo Wellcome), 6-диоксо-9H-пурин-8-илкоричная кислота (GlaxoWellcome) и S-2474 (Shionogi). Ингибиторы СОХ-2, которые полезны по изобретению, могут включать соединения, описанные в патентах US 6310079; 6306890 и 6303628 (бициклические карбонилиндолы); патенте US 6300363 (индольные соединения); патентах US 6297282 и 6004948 (замещенные производные бензосульфонамидов); патентах US 6239173, 6169188, 6133292; 6020343; 6071954; 5981576 метилсульфонил)фенилфураноны); патенте US 6083969 (диарилциклоалкано- и циклоалкенопираззолы); патенте US 6222048 (диарил-2-(5H)фураноны); патенте US 6077869 (арилфенилгидразины); патентах US 6071936 и 6001843 (замещенные пиридины); патенте US 6307047 (пиридазиноновые соединения); патенте US 6140515 (3-арил-4-арилоксифуран-5-оны); патентах US 6204387 и 6127545 (диарилпиридины); патенте US 6057319 (3,4-диарил-2 гидрокси-2,5-дигидрофураны); патенте US 6046236 (карбоциклические сульфонамиды) и патентах US 6002014; 5994381 и 5945539 (производные оксазола). Предпочтительные ингибиторы СОХ-2 для применения по настоящему изобретению включают целекоксиб (Celebrex), рофекоксиб (Vioxx), мелоксикам, пироксикам, деракоксиб, парекоксиб, валдекок- 14009780 сиб, эторикокси, производное хромена, производое хромана, N-(2-циклогексилоксинитрофенил)метансульфонамид, COX189, АВТ 963, JTE-522, их фармацевтически приемлемые соли, депо-формы или смеси. Более предпочтительными ингибиторами СОХ-2 являются целекоксиб, парекоксиб, валдекоксиб,эторикоксиб и рофекоксиб. В соответствии с предпочтительным вариантом осуществления изобретения применяют целекоксиб(Celebrex) или его фармацевтически приемлемую соль. Термин фармацевтически приемлемая соль включает соли, которые могут быть получены согласно известным способам специалистами в данной области, из соответствующего соединения по настоящему изобретению, например общепринятые соли с ионом металла или органические соли. Целекоксиб может быть введен в дозе 50-1600 мг в день, предпочтительно 200-600 мг, наиболее предпочтительно 400 мг в день. Введение может проводиться 1 или несколько раз в день, предпочтительно дважды. Количество целекоксиба может быть адаптировано в зависимости от возраста, массы тела и/или возможных других заболеваний пациента. Предпочтительно целекоксиб применяют в форме таблеток (Celebrex) для перорального введения. Без намерения создать определенную теорию в качестве объяснения наблюдаемого воздействия ингибиторов СОХ-2 рассматриваются следующие механизмы действия. Несомненно, что активация СОХ-2 опосредует воспалительные реакции и что СОХ-2 экспрессируется в тканях мозга. СОХ-2 может активироваться цитокинами подобно IL-2, IL-6 и IL-10, и активируемая цитокинами экспрессия СОХ-2 опосредует дальнейшие воспалительные реакции. Сообщалось, что уровни IL-2 и растворимых рецепторов IL-2 (Licino J., Seibyl J.P., Altemus M., Charney D.S., Krystal J.H. Повышенные уровни интерлейкина-2 у шизофреников, не принимающих нейролептики. Am. J. Psychiatry,1993; 150: 1408-1410) (McAllister С.G., van Kemmen D.P., Rehn T.J., Miller A.L., Gurklis J., Kelley M.E.,Yao J., Peters J.L. Увеличение в спинно-мозговой жидкости уровней интерлейкина-2 при шизофрении: эффекты рецидива психоза и статус лекарственного лечения. Am. J. Psychiatry, 1995; 152: 1291-1297),растворимых рецепторов IL-6 в качестве функциональной части системы IL-6 (Muller N., Dobmeier P.,Empel M., Riedel M., Schwarz M., Ackenheil M. Растворимые рецепторы IL-6 в сыворотке и спинно-мозговой жидкости пациентов с параноидной формой шизофрении. Eur. Psychiatry, 1997; 12: 294-299) и IL10 (Van Kammen D.P., McAllister-Sistilli C.G., Kelley M.E. Взаимосвязь между иммунными и поведенческими измерениями при шизофрении. В: G. Wieselmann (ред.) Current Update in Psychoimmunology,Springer Verlag, 1997; Wien, NY, стр. 51-55) повышаются в спинно-мозговой жидкости пациентов с шизофренией - повышение уровня цитокинов в ЦНС может сопровождаться усилением экспрессии СОХ-2. Эффективность ингибиторов СОХ-2, таких как целекоксиб, в лечении шизофрении может быть основана на заключении о том, что целекоксиб понижающе регулирует индуцируемую цитокинами ЦНС активацию СОХ-2. Более того, ингибирование активности СОХ-2, по-видимому, регулирует экспрессию адгезионных молекул (Schwarz M.J., Ackenheil M., Riedel M., Muller N. Нарушение барьера кровь-CSF как индикатор иммунной реакции при шизофрении. Neurosci. Letters, 1998; 253: 201-203). Поскольку регуляция адгезионных молекул при шизофрении нарушена, приводя к дисбалансу и потере связи между иммунными системами - периферической и ЦНС, воздействия ингибиторов СОХ-2, таких как целекоксиб, при лечении шизофрении могут также иметь отношение к адгезионным молекулам - межклеточной адгезионной молекуле-1 (ICAM-1) и экспрессируемой васкулярными клетками адгезионной молекуле-1 (VCAM-1),что особенно касается негативных симптомов (Schwarz M.J., Riedel M., Gruber R., Ackenheil M., Muller N. Уровни растворимых адгезионных молекул при шизофрении: связь с психопатологией. В: N. MullerMuller N., Ackenheil M. Содержание иммуноглобулина и альбумина в спинно-мозговой жидкости у пациентов с шизофренией: связь с негативной симптоматологией. Schizophrenia Res. 1995; 14: 223-228). Ингибитор СОХ-2 применяют в комбинации с нейролептическим препаратом или антидепрессантом для терапии психиатрических нарушений, таких как шизофрения, бредовые расстройства, аффективные расстройства, аутизм или связанные с тиком осложнения. Комбинации могут также включать смесь одного или нескольких ингибиторов СОХ-2 с одним или несколькими нейролептическими агентами или антидепрессантами. В частности, комбинация ингибитора СОХ-2 с нейролептическим препаратом полезна для лечения шизофрении, тогда как комбинация ингибитора СОХ-2 с антидепрессантом применима для лечения депрессивных расстройств. Как классические, так и атипичные нейролептики могут быть использованы для дополнительного применения по изобретению, причем атипичные нейролептики являются предпочтительными. Примеры нейролептических препаратов, которые применимы по настоящему изобретению, включают, но без ограничения, бутирофеноны, такие как галоперидол, пимозид и дроперидол; фенотиазины,такие как хлорпромазин, тиоридазин, мезоридазин, трифлуоперазин, перфеназин, флуфеназин, тифлупромазин, прохлорперазин и ацетофеназин; тиоксантены, такие как тиотиксен и хлорпротиксен; тиенобензодиазепины; дибензодиазепины; бензизоксазолы; дибензотиазепины; имидазолидиноны; бензизотиазолилпиперазины; дибензоксазепины, такие как локсапин; дигидроиндолоны, такие как молиндон; арипипразол; и их производные, которые обладают антипсихотической активностью.- 15009780 Примеры нейролептических препаратов, которые являются предпочтительными для применения по настоящему изобретению, приведены в табл. 3. Таблица 3 Нейролептические препараты Примеры торговых названий и поставщиков отобранных нейролептических препаратов следующие: клозапин (доступен под торговым названием КЛОЗАРИЛ от Mylan, Zenith Goldline, UDL, Novartis); оланзапин (доступен под торговым названием ЗИПРЕКСА от Lilly; зипразидон (доступен под торговым названием ГЕОДОН от Pfizer); рисперидон (доступен под торговым названием РИСПЕРДАЛ отJanssen); куетиапина фумарат (доступен под торговым названием СЕРОКУЕЛ от AstraZeneca); галопе- 17009780 ридол (доступен под торговым названием ГАЛДОЛ от Ortho-McNeil); хлорпромазин (доступен под торговым названием ТОРАЗИН от SmithKline Beecham); флуфеназин (доступен под торговым названием ПРОЛИКСИН от Apothecon, Copley, Schering, Teva и American Pharmaceutical Partners, Pasadena); тиотиксен (доступен под торговым названием HABAH от Pfizer); трифлуоперазин (10-[3-(4-метил-1-пиперазинил)пропил]-2-(трифторметил)фенотиазина дигидрохлорид (доступен под торговым названием СТЕЛАЗИН от SmithKlein Beckman); перфеназин (доступен под торговым названием ТРИЛАФОН отSchering); тиоридазин (доступен под торговым названием МЕЛЛАРИЛ от Novartis, Roxane, Hi-Tech,Teva и Alpharma); молиндон (доступен под торговым названием МОБАН от Endo) и локсапин (доступен под торговым названием ЛОКСИТАН от Watson). Кроме того, могут быть использованы бенперидол(Глианимон), перазин (Таксилан) или мелперон (Эунерпан). Другие предпочтительные нейролептические препараты включают промазин (доступный под торговым названием СПАРИН), трифлурпромазин (доступный под торговым названием ВЕСПРИН),хлорпротиксен (доступный под торговым названием TAPAKTAH), дроперидол (доступный под торговым названием ИНАПСИН), ацетофеназин (доступный под торговым названием ТИНДАЛ), прохлорперазин (доступный под торговым названием КОМПРАЗИН), метотримепразин (доступный под торговым названием НОЗИНАН), пипотиазин (доступный под торговым названием ПИПОТРИЛ), зипразидон и гоперидон. Предпочтительные нейролептические препараты включают рисперидон и арипипразол (от BristolMyers Squibb Company, см., например, Stahl S.M. Стабилизаторы допаминовой системы, арипипразол и следующее поколение антипсихотических средств, часть I, воздействия "золотой головки" на допаминовые рецепторы; J. Clin. Psychiatry 2001, 62, 11: 841-842). Наиболее предпочтительным нейролептическим препаратом по настоящему изобретению является рисперидон (Риспердал), его получение и фармакологическая активность описаны в EP 0196132. Рисперидон действует как антагонист нейромедиаторов, в частности допамина, и применяется для лечения психозов. По настоящему изобретению нейролептик рисперидон может быть введен в дозе 2-6 мг/день, предпочтительно 4-5 мг/день. Доза целекоксиба может находиться в диапазоне 50-1600 мг, предпочтительно 200-600 мг, более предпочтительно 400 мг. Предпочтительно введение осуществляют дважды в день (утром и вечером). Различные типы антидепрессантов могут использоваться для дополнительного применения по настоящему изобретению. Примеры антидепрессантов, которые полезны по настоящему изобретению,включают, но без ограничения, трициклические антидепрессанты, такие как амитриптилин (5-(3-диметиламинопропилиден)-10,11-дигидро-5H-дибензо[a,d]циклогептен), амитриптилина оксид, дезипрамин(10,11-дигидро-5-(3-метиламинопропил)-5H-дибенз[b,f]азепин), дибензепин (10-(2-диметиламиноэтил)-5,11 дигидро-5-метил-11H-дибензо[b,е][1,4]диазепин-11-он), досулепин (3-(6H-дибензо[b,е]тиепин-11-илиден)N,N-диметилпропиламин), доксепин (3-(6H-дибенз[b,е]оксепин-11-илиден)диметилпропиламин), хлороимипрамин, имипрамин (5-(3-диметиламинопропил)-5,11-дигидро-5H-дибенз[b,f]азепин), нортриптилин (3(10,11-дигидро-5H-дибензо[а,d]циклогептен-5-илиден)-N-метил-1-пропанамин), миансерин (1,2,3,4,10,14bгексагидро-2-метилдибензо[с,f]пиразино[1,2-]азепин), мапротилин (N-метил-9,10-этаноантрацен-9(10H)пропанамин), тримипрамин (5-[3-диметиламино)-2-метилпропил]-10,11-дигидро-5H-дибенз[b,f]азепин) или вилоксазин (RS)-2-(2-этоксифеноксиметил)морфолин), современные антидепрессанты, такие как тразодон (2-3-[4-(3-хлорфенил)-1-пиперазинил]пропил-1,2,4-триазоло[4,3-а]пиридин-3(2H)-он), нефазодон(транс-2-фенилциклопропиламин), брофаромин или моклобемид (4-хлор-N-(2-морфолиноэтил)бензамид),селективные ингибиторы поглощения серотонина, такие как циталопрам, пароксетин, флуоксетин RS)-Nметил-3-фенил-3-[4-(трифлорметил)фенокси]пропиламин, доступный под торговым названием ПРОЗАК),флувоксамин E)-5-метилокси-4'-(трифторметил)валерофенон-O-(2-аминоэтил)оксим) или сертралин 1Sцис)-(+)-4-(3,4-дихлорфенил)-1,2,3,4-тетрагидро-N-метил-1-нафталинамин) и растительные антидепрессанты, такие как гиперикум (сухой экстракт травы зверобоя продырявленного Hypericum perforatum L.). Лекарственная форма, содержащая нейролептический препарат, и вторая лекарственная форма, содержащая ингибитор СОХ-2, могут вводиться одновременно. Фармацевтический объект может быть введен энтерально (перорально) или парентерально. Парентеральное введение включает подкожное, внутримышечное, внутрикожное, интрамаммарное, внутривенное и другие способы введения, известные специалистам в этой области. Энтеральное введение включает раствор, таблетки, капсулы с замедленным высвобождением, капсулы с покрытием, растворимым в кишечнике, и сиропы. Предпочтительно ингибитор СОХ-2 и нейролептик или антидепрессант вводят энтерально (перорально) в форме таблеток. Лечение психиатрических расстройств ингибиторами СОХ-2, только ими или в комбинации с нейролептиком или антидепрессантом может осуществляться в дополнение к дальнейшей лекарственной- 18009780 терапии. Так, транквилизаторы можно применять для лечения возбуждения, страха или расстройств сна. Предпочтительно применяют лоразепам, который принадлежит к классу бензодиазепинов. В дальнейшем изобретение будет обсуждаться более детально со ссылкой на патентное исследование. Другие варианты воплощения изобретения в объеме контекста пунктов формулы изобретения будут очевидными для специалистов в этой области при рассмотрении описания и практического применения по изобретению, как это раскрывается в контексте. Результаты патентного исследования представлены графически на приложенных фигурах, которые будут обсуждаться более подробно далее. Фиг. 1 иллюстрирует сравнение оценки по шкале позитивных и негативных синдромов (PANSS) в ходе лечения рисперидоном-целекоксибом или рисперидоном-плацебо. Фиг. 2 иллюстрирует сравнение негативной оценки по шкале позитивных и негативных синдромов(PANSS) в ходе лечения рисперидоном-целекоксибом или рисперидоном-плацебо. Фиг. 3 иллюстрирует сравнение глобальной оценки по шкале позитивных и негативных синдромов(PANSS) в ходе лечения рисперидоном-целекоксибом или рисперидоном-плацебо. Фиг. 4 иллюстрирует уровни рисперидона и 9-ОН-рисперидона в плазме в ходе лечения рисперидоном-целекоксибом или рисперидоном-плацебо. Фиг. 5 иллюстрирует применение биперидена и бензодиазепина в ходе лечения рисперидоном-целекоксибом или рисперидоном-плацебо. Исследование проводили в одном центре, в параллельных группах, рандомизированным двойным слепым способом под контролем плацебо для оценки комбинированной терапии целекоксибом и рисперидоном по сравнению с монотерапией рисперидоном и плацебо у больных шизофренией. Исследование включало 50 пациентов, соответствующих критериям диагноза шизофрения согласно Диагностическому и статистическому руководству (DSM IV) (American Psychiatric Association (1994), Diagnostic and StatisticalManual of Mental Disorders, 1 издание, American Psychiatric Press, Washington DC), из которых 25 относились к группе, получавшей рисперидон-плацебо, и 25 - к группе, получавшей рисперидон-целекоксиб. Не было никаких достоверных различий между двумя группами пациентов в отношении возраста, пола,продолжительности или тяжести заболевания или психопатологии, дозы рисперидона или уровней рисперидона в плазме. Пациенты получали 2-6 мг/день рисперидона (риспердала) и в зависимости от того, к какой группе они принадлежали, 400 мг/день целекоксиба (2x200 мг целебрекса, утром и вечером) или плацебо в течение 5 недель после короткого периода вымывания ранее принимаемого антипсихотического препарата. В течение периода вымывания, если необходимо, назначался бензодиазепиновый препарат (в основном,лоразепам). Пациентам с признаками возбуждения, страха или проблемами, связанными со сном, в ходе исследования также назначали лоразепам. Психопатологию пациентов оценивали, используя шкалу позитивных и негативных синдромов(PANSS) (Kay и др., Schizophr. Bull. 1987, 13: 261-276). Экстрапирамидальные побочные эффекты оценивали по одноименной шкале (EPS) (Simpson и Angus,Acta Psychiat. Scand. 1970 (доп.), 212). Применение биперидена контролировали в качестве возможного индикатора побочных эффектов антипсихотического препарата. Чтобы исключить вероятность того, что возможные различия в терапевтической эффективности между двумя группами могли быть из-за несогласованности в ходе терапии рисперидоном или различий в метаболизме рисперидона, в ходе исследования контролировали уровни рисперидона или 9-ОНрисперидона в плазме. Статистические расчеты проводили в соответствии с критерием последнего наблюдения, отнесенного вперед (LOCF), т.е. последние оценки по PANSS пациентов, которые выбыли из исследования до его окончания, переносили вперед на все последующие дни наблюдения. Для сравнения основного параметра эффективности, среднего изменения по PANSS между двумя получавшими лечение группами, использовали t-тесты для независимых выборок. Со ссылкой на основную гипотезу о лучшем результате в группе, получавшей целекоксиб-рисперидон, значение р 0,05 вычисляли в одностороннем t-тесте и использовали в качестве основы для определения объема выборки (статистической мощности) и для сравнения групп. Для всех других сравнений использовали двусторонние t-тесты. В начале исследования в группе, получавшей рисперидон-целекоксиб (средний возраст 35,912,8 лет), тотальная оценка по PANSS составила 71,817,1, глобальная оценка по PANS составила 34,08,5,позитивная оценка по PANSS составила 19,05,9 и негативная оценка по PANSS составила 18,76,3. В группе, получавшей рисперидон-плацебо (средний возраст 35,513,6 лет), тотальная оценка по PANSS составила 75,412,9, глобальная оценка по PANS составила 37,27,1, позитивная оценка по PANSS составила 17,24,6 и негативная оценка по PANSS составила 21,15,5. Следовательно, не было значительного различия в тотальной оценке по PANSS или любой из подшкал. В ходе 5-недельной терапии наблюдалось значительное улучшение тотальной оценки по PANSS и подшкалам в обеих группах пациентов с шизофренией. Результаты тотальной оценки по PANSS показаны на фиг. 1, негативной оценки по PANSS - на фиг. 2, глобальной оценки по PANSS - на фиг. 3 и позитивной оценки по PANSS - в табл. 4.- 19009780 Таблица 4 Сравнение позитивной оценки по PANSSt означает статистическое распределение случайной выборки. р означает статистическую мощность (вероятность). 3 с.н. означает статистически незначимо. 2 В группе, получавшей целекоксиб-рисперидион, двусторонние t-тесты между базисной линией и неделей 5 дали следующие значения: для тотальной оценки по PANSS р 0,0001, для глобальной оценки по PANSS р 0,0001, для позитивной оценки по PANSS р 0,0001, для негативной оценки по PANSS р 0,001. В группе, получавшей плацебо-рисперидон, t-тесты между базисной линией и неделей 5 дали следующие значения: для тотальной оценки по PANSS р 0,002, для глобальной оценки по PANSS р 0,003, для позитивной оценки по PANSS р 0,002, для негативной оценки по PANSS р 0,02. Улучшенная эффективность комбинированной терапии целекоксибом и рисперидоном по сравнению с монотерапией рисперидоном отчетливо продемонстрирована значительно более низкими глобальными оценками по PANSS после 2, 3, 4 и 5 недель лечения (фиг. 3). Что касается тотальной и негативной оценок, значительно более низкие значения были зарегистрированы после 2, 3 и 4 недель в группе, получавшей целекоксиб-рисперидон (фиг. 1 и 2). Средняя дневная доза рисперидона приведена в табл. 5; между двумя группами, получавшими лечение, не найдено никакого статистически значимого различия. Таблица 5 Средняя доза рисперидона, мг/день Различия в уровнях рисперидона или его метаболита 9-ОН-рисперидона в плазме, показанные на фиг. 4, также были статистически незначимыми (эта фиг. 4 отличается от фиг. 4 приоритетного документа заявки на патент Германии из-за ошибки в расчете в упомянутом приоритетном документе). Следовательно, можно было исключить возможность того, что наблюдаемые различия в терапевтической эффективности между двумя группами объясняются их несовместимостью в ходе терапии рисперидоном или различиями в метаболизме рисперидона. Терапевтическое преимущество комбинированной терапии должно быть отнесено за счет ингибитора СОХ-2 целекоксиба. Что касается экстрапирамидальных побочных эффектов, то статистически значимые различия были найдены по шкале EPS. Применение биперидена показано на фиг. 5 и рассчитано как кумулятивная недельная доза. Значения были ниже в группе, получавшей целекоксиб-рисперидон, и достигали статистической значимости на неделе 2 (р 0,02). Детальный анализ пунктов по PANSS, которые разделяют в группе хорошие отклики на целекоксиб от плацебо, обнаружил, что терапевтические эффекты целекоксиба, в основном, встречаются в пунктах потеря контакта (п.3 подшкалы негативных симптомов), эмоциональная изоляция (п.2 подшкалы негативных симптомов), пассивно-апатичная изоляция (п.4 подшкалы негативных симптомов), социальный аутизм (п.16 общей психопатологической подшкалы), депрессия (п.6 общей психопатологической подшкалы) и задержка двигательной способности (п.6 общей психопатологической подшкалы). Кроме того, факторный анализ показал, что особенно пункты, которые могут быть отнесены к категории- 20009780 возбуждение, иллюстрируют благоприятный терапевтический ответ на целекоксиб, но не на плацебо. Все эти пункты отражают психопатологические симптомы, которые обычно обнаруживают при депрессивных состояниях. Следовательно, данный детальный анализ указывает на эффективность терапии при депрессивных состояниях. Более того, пассивно-апатичная изоляция, задержка двигательной способности, социальный аутизм или потеря контакта, часто более остро выраженные, чем при депрессивных состояниях, являются также основными симптомами детского аутизма. Таким образом, комбинация целекоксиба и рисперидона по настоящему изобретению приводит к улучшенным результатам по сравнению с монотерапией рисперидоном в отношении эффективности при лечении шизофрении. Кроме того, замечено, что полезные воздействия дополнительной терапии проявляются быстрее у пациентов с недавним началом расстройства и что терапия целекоксибом применима для лечения депрессивных состояний. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Применение ингибитора СОХ-2 при получении лекарственного средства для лечения шизофрении, аффективных расстройств и связанных с тиком осложнений. 2. Применение по п.1 для лечения хронических шизофренических психозов, шизоаффективных психозов, приступов депрессии, приступов рецидивирующей депрессии, маниакальных осложнений и биполярных аффективных расстройств. 3. Применение по одному из пп.1-2, отличающееся тем, что ингибитор СОХ-2 выбирают из целекоксиба, рофекоксиба, мелоксикама, пироксикама, деракоксиба, парекоксиба, валдекоксиба, эторикоксиба, производного хромена, производного хромана, N-(2-циклогексилоксинитрофенил)метансульфонамида, COX189, АВТ 963 или JTE-522, их фармацевтически приемлемых солей, пролекарств или смесей. 4. Применение по п.3, отличающееся тем, что целекоксиб или его фармацевтически приемлемую соль используют в качестве ингибитора СОХ-2. 5. Применение по п.4, отличающееся тем, что целекоксиб или его фармацевтически приемлемую соль вводят в количестве 50-1600 мг/день, предпочтительно 200-600 мг/день, наиболее предпочтительно 400 мг/день. 6. Применение по одному из предшествующих пунктов, отличающееся тем, что лекарственное средство вводят перорально.
МПК / Метки
МПК: A61P 25/18, A61K 31/42, A61K 31/54, A61K 31/365, A61K 31/435, A61K 31/635, A61P 25/24
Метки: ингибиторов, аффективных, расстройств, связанных, применение, осложнений, шизофрении, тиком, лечения, сох-2
Код ссылки
<a href="https://eas.patents.su/24-9780-primenenie-ingibitorov-soh-2-dlya-lecheniya-shizofrenii-affektivnyh-rasstrojjstv-ili-oslozhnenijj-svyazannyh-s-tikom.html" rel="bookmark" title="База патентов Евразийского Союза">Применение ингибиторов сох-2 для лечения шизофрении, аффективных расстройств или осложнений, связанных с тиком</a>
Предыдущий патент: Лечение латентного туберкулёза
Следующий патент: Фармацевтическая композиция и ее применение для лечения нарушений функции мочевого пузыря
Случайный патент: Преобразование прямолинейного возвратно-поступательного движения во вращательное движение