Способ сульфинилирования производной пиразола
Номер патента: 16304
Опубликовано: 30.04.2012
Авторы: Кун Оливер, Зукопп Мартин, Грёнинг Карстен, Кайл Михаэль, Лонглет Джон Дж.
Формула / Реферат
1. Способ сульфинилирования производного пиразола, характеризующийся тем, что 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол-3-карбонитрил (II) подвергают реакции с сульфинилирующим агентом S в присутствии по крайней мере одного амино/кислотного комплекса, в котором амин(ы) является(ются) выбранным(и) из вторичных и/или третичных аминов, а кислота(ы) является(ются) выбранной(ыми) из хлористо-водородной, фтористо-водородной, п-толуолсульфоновой кислоты, бензолсульфоновой кислоты, 4-этилбензолсульфоновой кислоты, 4-хлорбензолсульфоновой кислоты, ксиленсульфоновой кислоты, 2,3-диметилбензолсульфоновой кислоты, 2,4-диметилбензолсульфоновой кислоты, 2,5-диметилбензолсульфоновой кислоты, 2,6-диметилбензолсульфоновой кислоты, 1-нафталинсульфоновой кислоты, 2-нафталинсульфоновой кислоты, смесей двух или более изомеров диметилбензолсульфоновой кислоты, мезитиленсульфоновой кислоты, метансульфоновой кислоты, камфорсульфоновой кислоты и трифторметилсульфоновой кислоты при добавлении галогенирующего агента, где S представляет собой
[CF3S(O)]2O или CF3S(O)X,
где X означает фтор, хлор, бром, йод, группу гидрокси, или соль щелочного или щелочно-земельного металла гидроксигруппы;
или их смеси, где температура реакционной смеси никогда не превышает 39°C.
2. Способ в соответствии с п.1, где галогенирующий агент является выбранным из тионилхлорида, тионилбромида, фосфороксихлорида, оксалилхлорида, фосгена, трифосгена ((CCl3)2C(=O)), хлорформиатов, фосфорпентахлорида, фосфортрихлорида, трихлорметилхлорметаноата и хлорида ксиленсульфоновой кислоты.
3. Способ в соответствии с п.1 или 2, где галогенирующий агент представляет собой хлорирующий агент, выбранный из тионилхлорида и фосфороксихлорида.
4. Способ в соответствии с любым из пп.1-3, где амино/кислотный комплекс является выбранным из
третичных алкиламинов, таких как триметиламин, триэтиламин, трипропиламин, триизопропиламин, трибутиламин, диметилэтиламин, диэтилметиламин, диметил н-пропиламин, диизопропилэтиламин, DBU (1,8-диазобицикло[5.4.0]ундец-7-ена), DBN (1,5-диазобицикло[4.3.0]нон-5-ена), метилморфолин, этилморфолин, N,N-диметиланилин, метилпиперидин, метилпирролидин и метилдиабензиламин; и
третичных ароматических аминов, таких как пиридин, DMAP (диметиламинопиридин), коллидин, лутидин, пиримидин, пиразин и пиперазин; и
вторичных алкиламинов, таких как диметилэтиламин, диэтиламин, дипропиламин, диизопропиламин, дибутиламин, этилметиламин, изопропилметиламин и изопропилэтиламин; и
циклических вторичных аминов, таких как пиперидин, пиперидин, который является замещенным C1-C8-алкилом или C1-C8-галоалкилом, такой как 2-метилпиперидин или 4-метилпиперидин, пирролидин, имидазолидин, пиррол, пиперазин и морфолин.
5. Способ в соответствии с любым из пп.1-4, где амин амино/кислотного комплекса является выбранным из триметиламина, триэтиламина, трипропиламина, триизопропиламина, диметилэтиламина, диэтилметиламина, диметил н-пропиламина, диизопропилэтиламина, DBU (1,8-диазобицикло[5.4.0]ундец-7-ена), DBN (1,5-диазобицикло[4.3.0]нон-5-ена), метилморфолина, этилморфолина, N,N-диметиланилина, метилпиперидина, метилпирролидина, метилдиабензиламина, пиридина, DMAP (диметиламинопиридина), коллидина, лутидина, пиримидина, пиразина и пиперазина.
6. Способ в соответствии с любым из пп.1-5, где амин амино/кислотного комплекса является выбранным из триметиламина, триэтиламина, диметилэтиламина, диэтилметиламина, диметил н-пропиламина, метилморфолина, этилморфолина, N,N-диметиланилина, метилпиперидина, метилпирролидина, метилдибензиламина и пиридина.
7. Способ в соответствии с любым из пп.1-4, где амин амино/кислотного комплекса является выбранным из диметилэтиламина, диэтиламина, дипропиламина, диизопропиламина, дибутиламина, этилметиламина, изопропилметиламина и изопропилэтиламина, пиперидина, пиперидина, который является замещенным C1-C8-алкилом или C1-C8-галоалкилом, такого как 2-метилпиперидин или 4-метилпиперидин, пирролидина, пирролидина, который является замещенным C1-C8-алкилом или C1-C8-галоалкилом, такого как 2-метилпирролидин или 4-метилпирролидин, имидазолидина, пиррола, пиперазина и морфолина.
8. Способ в соответствии с любым из пп.1-6, где кислота амино/кислотного комплекса является выбранной из хлористо-водородной кислоты, п-толуолсульфоновой кислоты, бензолсульфоновой кислоты и ксиленсульфоновой кислоты.
9. Способ в соответствии с любым из пп.1-7, где кислота амино/кислотного комплекса является выбранной из п-толуолсульфоновой кислоты, бензолсульфоновой кислоты, 4-этилбензолсульфоновой кислоты, 4-хлорбензолсульфоновой кислоты, ксиленсульфоновой кислоты, 2,3-диметилбензолсульфоновой кислоты, 2,4-диметилбензолсульфоновой кислоты, 2,5-диметилбензолсульфоновой кислоты, 2,6-диметилбензолсульфоновой кислоты, 1-нафталинсульфоновой кислоты, 2-нафталинсульфоновой кислоты, смесей двух или более изомеров диметилбензолсульфоновой кислоты, мезитиленсульфоновой кислоты, метансульфоновой кислоты, камфорсульфоновой кислоты и трифторметилсульфоновой кислоты, предпочтительно из п-толуолсульфоновой кислоты, бензолсульфоновой кислоты и ксиленсульфоновой кислоты.
10. Способ в соответствии с любым из пп.1-9, где сульфинилирующий агент S является выбранным из CF3S(O)Cl, CF3S(O)OH, [CF3S(O)]2O, CF3S(O)ONa, CF3S(O)OK и их смесей.
11. Способ в соответствии с любым из пп.1-10, где реакцию проводят в органическом растворителе, выбранном из толуола, бензола, ксилена, трифторметилбензола, монохлорбензола, этилбензола и дихлорбензола.
12. Способ в соответствии с любым из пп.1-11, где сульфинилирующий агент прибавляют к реакционному раствору смеси амино/кислотного комплекса и галогенирующего агента перед прибавлением 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол-3-карбонитрила.
13. Способ в соответствии с любым из пп.1-12, где 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол-3-карбонитрил прибавляют к реакционной смеси сульфинилирующего агента, амино/кислотного комплекса и галогенирующего агента.
14. Способ в соответствии с любым из пп.1-13, где используют от 1,4 до 2,2 мол.экв. амино/кислотного комплекса по отношению к 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол-3-карбонитрилу.
15. Способ в соответствии с любым из пп.1-14, где используют от 1,15 до 1,35 мол.экв. галогенирующего агента по отношению к 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол-3-карбонитрилу.
16. Способ в соответствии с любым из пп.1-15, где используют от 1,0 до 1,35 мол.экв. сульфинилирующего агента по отношению к 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол-3-карбонитрилу.
17. Способ в соответствии с любым из пп.1-16, где после соединения 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол-3-карбонитрила, сульфинилирующего агента, амино/кислотного комплекса и галогенирующего агента температуру повышают до 30-39°C в течение 5-60 мин.
18. Способ в соответствии с любым из пп.1-17, где продукт реакции 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-4-(трифторметилсульфинил)пиразол-3-карбонитрил выкристаллизовывают из раствора монохлорбензола, дихлорбензола, этилбензола или толуола.
19. Способ в соответствии с любым из пп.1-18, где на дополнительном этапе 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-4-(трифтометилсульфинил)пиразол-3-карбонитрил вводят в пестицидную композицию.
20. Способ в соответствии с любым из пп.1-18, где на дополнительном этапе 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-4-(трифтометилсульфинил)пиразол-3-карбонитрил вводят в паразитицидную композицию.
Текст
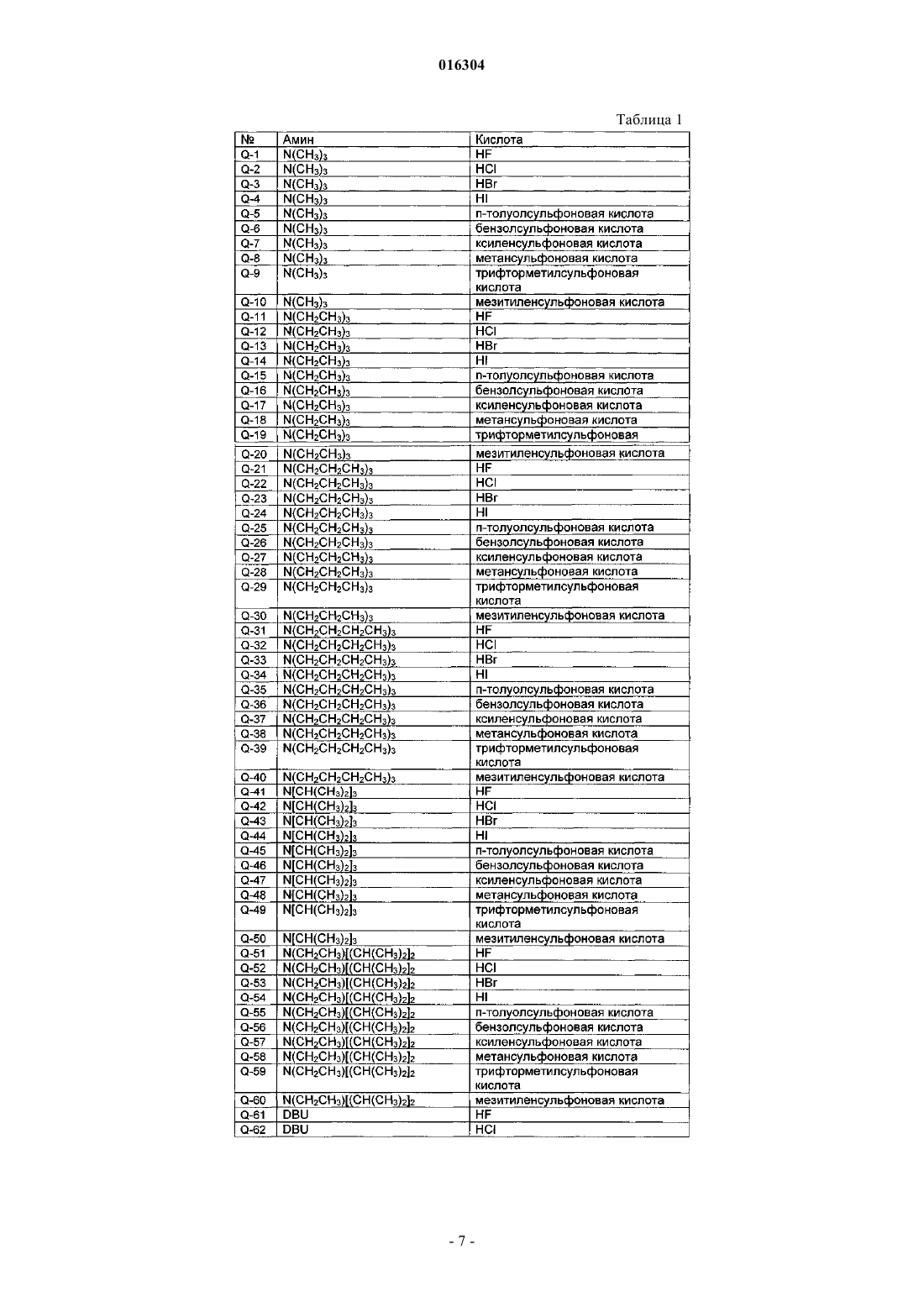
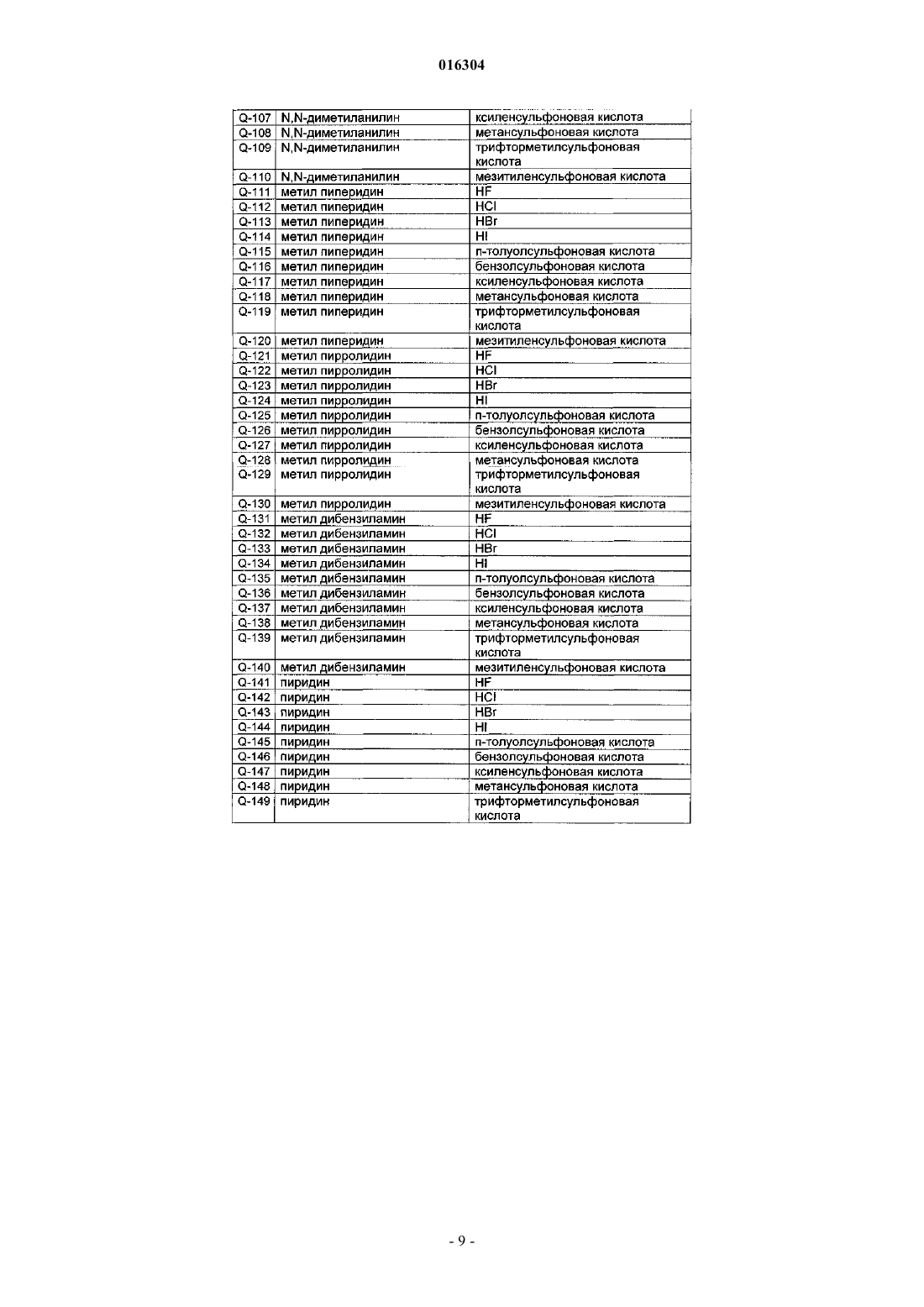
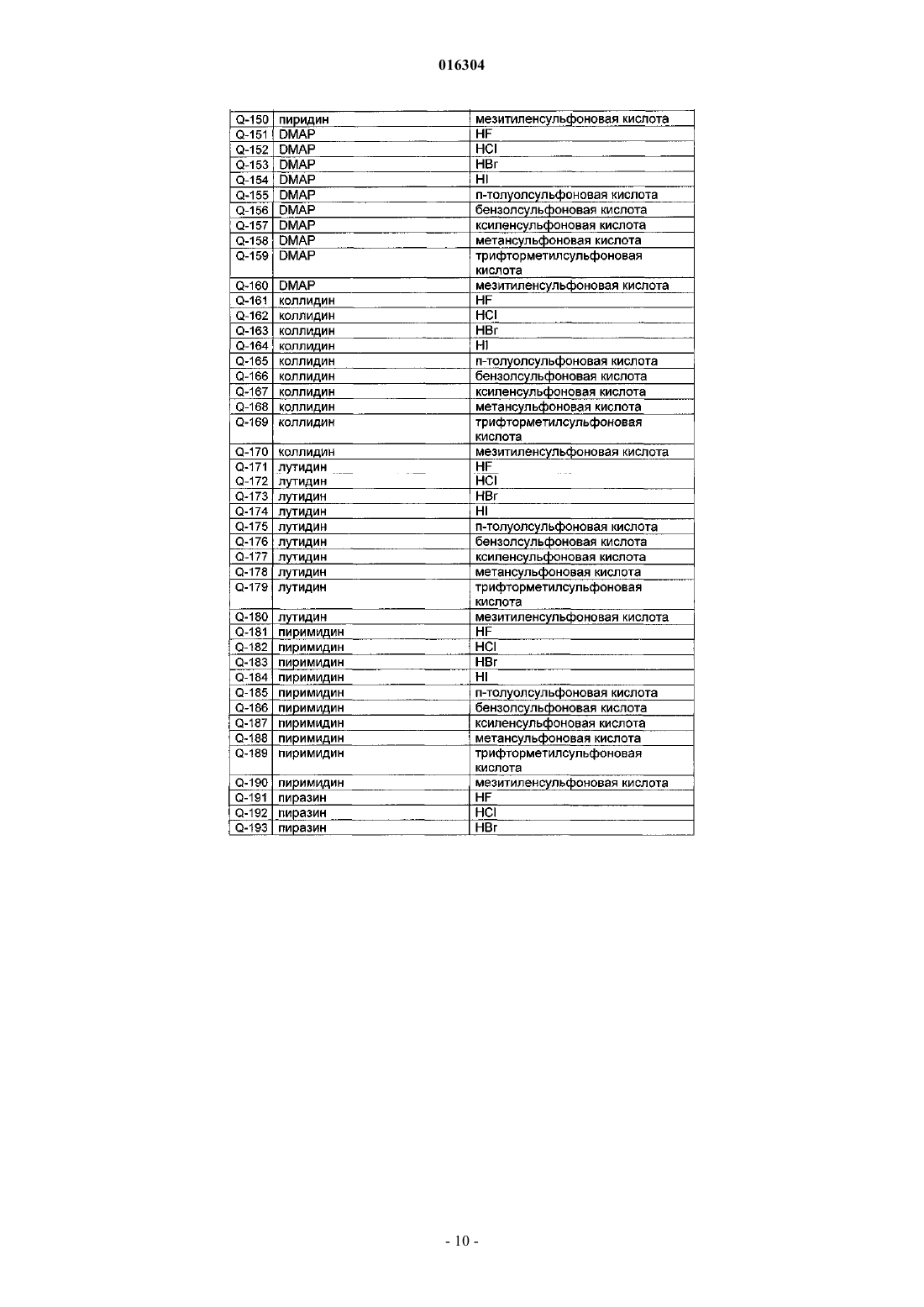
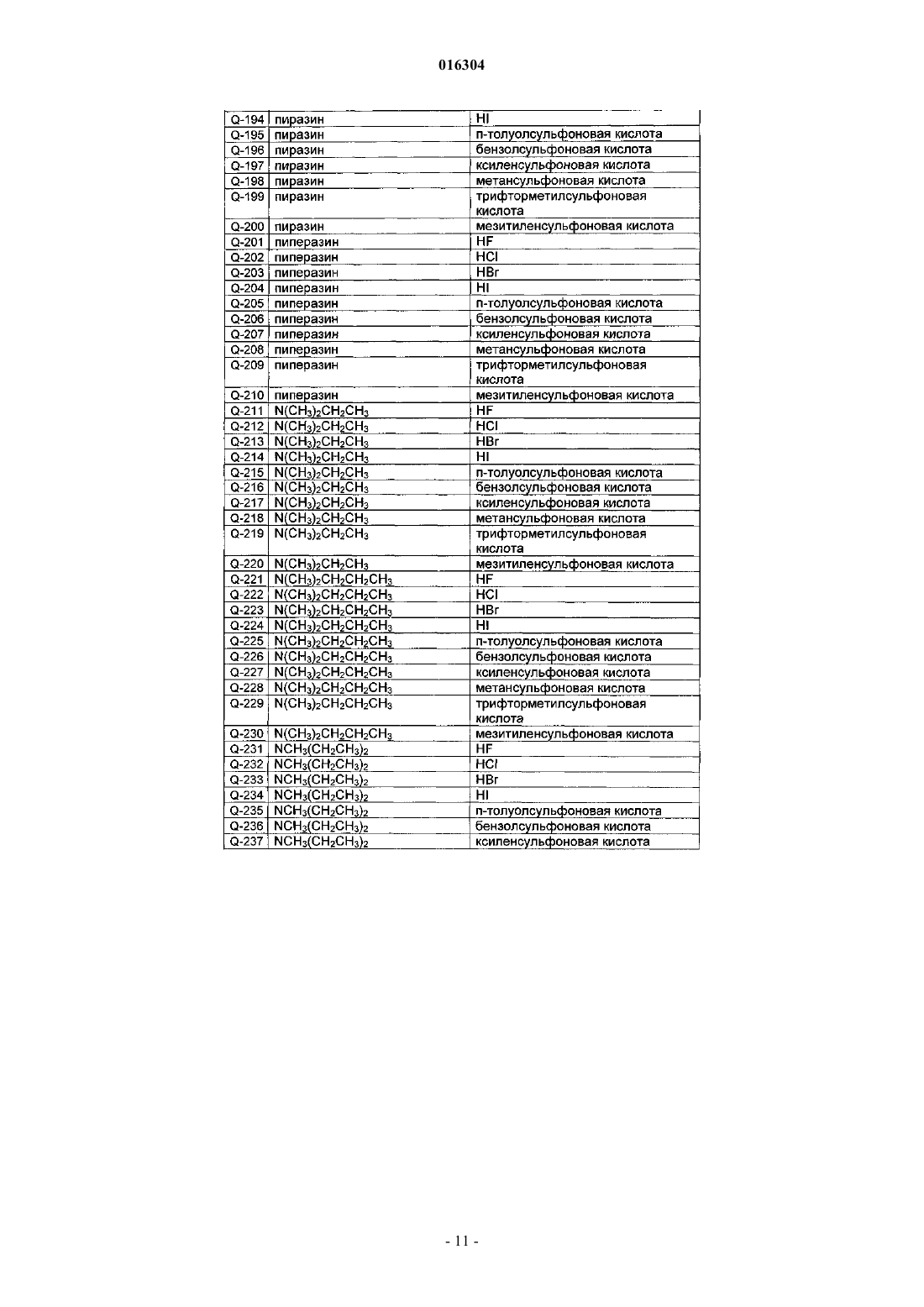
СПОСОБ СУЛЬФИНИЛИРОВАНИЯ ПРОИЗВОДНОЙ ПИРАЗОЛА Настоящее изобретение относится к новому способу сульфинилирования производной пиразола,характеризующемуся тем, что 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол-3 карбонитрил (II) подвергают реакции с сульфинилирующим агентом S в присутствии по крайней мере одного амино/кислотного комплекса, в котором амин(ы) является(ются) выбранным(и) из вторичных и/или третичных аминов, а кислота(ы) является(являются) выбранной(ыми) из фтористо-водородной, хлористо-водородной, бромисто-водородной и йодисто-водородной кислот и производных сульфоновой кислоты, при добавлении галогенирующего агента, где S представляет собой [CF3S(O)]2O или CF3S(O)X, где X означает фтор, хлор, бром, йод, гидроксигруппу или соль щелочного или щелочно-земельного металла гидроксигруппы; или их смеси, где температура реакционной смеси никогда не превышает 39C. 016304 Настоящее изобретение относится к новому способу сульфинилирования производной пиразола, характеризующемуся тем, что 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол-3 карбонитрил (II) подвергают реакции с сульфинилирующим агентом S в присутствии по крайней мере одного амино/кислотного комплекса, где амин(ы) является(ются) выбранным(и) из вторичных и/или третичных аминов, а кислота(ы) является(ются) выбранной(ыми) из фтористо-водородной, хлористоводородной, бромисто-водородной, йодисто-водородной кислот и производных сульфоновой кислоты, с добавлением галогенирующего агента, где S представляет собой[CF3S(O)]2O или CF3S(O)X,где X означает фтор, хлор, бром, йод, гидроксигруппу или соль щелочного или щелочно-земельного металла гидроксигруппы; или их смеси, где температура реакционной смеси никогда не превышает 39C. Сульфинилирование соединения пиразольного типа относится к замещению атома водорода на атоме углерода пиразольного гетероцикла RS(=O)-группой. Непосредственное сульфинилирование различных органических молекул (не включая производные пиразола) при использовании смеси P(O)Cl3 и CF3S(O)ONa было описано в T. Billard, A. Greiner,В.R. Langlois, Tetrahedron. 55 (1999), p. 7243-7250. Кроме того, C. Wakselman, M. Tordeux, C. Freslon,L. Saint-Jalmes, Synlett. 2001, p. 550-552, показали, что непосредственное сульфинилирование ароматических соединений происходит с помощью CF3S(O)ONa или CF3S(O)OK в присутствии трифлатной кислоты (CF3S(O)2OH). Способы для непосредственного сульфинилирования 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол-3-карбонитрила (II) были описаны в EP-A-668269, EP-A1-331222, CN-A 1374298 и у(2004), сер.1008-1542 (2004), 02-0018-03. В EP 668269 было описано сульфинилирование 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1Hпиразол-3-карбонитрила (II) с помощью трифторметилсульфиновой кислоты CF3S(O)OH и ее производных CF3S(O)Cl, CF3S(O)ONa, CF3S(O)N(CH3)2 или CF3S(O)N(CH2CH3)2. В качестве хлорирующего реагента упоминаются фосген, хлорформиаты, PCl5 и SOCl2. Описывается, что реагент ("соединение C") является выбранным из группы, которая состоит из тозилатов, гидрохлоридов и мезилатов первичного,вторичного или четвертичного амина, предпочтительно из диметиламина, пиридина, триметиламина,диэтиламина или изопропиламина или газообразного хлористого водорода, необязательно в присутствии эквимолярного количества паратолуолсульфоновой кислоты, может прибавляться для завершения реакции. Реакцию можно осуществлять при температурах от 30 до 50C. Приводятся примеры для следующих комбинаций реагентов и температур:CF3S(O)ONa, диметиламин п-тозилат, SOCl2; в соответствии с этим частным примером SOCl2 сначала прибавляют при 5C, потом реакционную смесь выдерживают при комнатной температуре в течение нескольких часов, после чего температуру повышают до 50C. Реакции, которые осуществляют при использовании CF3S(O)Cl в качестве сульфинилирующего агента, дают самый высокий выход конечного продукта. Способ, описанный в CN-A 1374298, был усовершенствован для преодоления некоторых недостатков процесса, описанного в EP 668269. CN-A 1374298 ссылается на то, что CF3S(O)Cl является крайне нестабильным соединением, CF3S(O)N(CH3)2 и CF3SOOH являются относительно сложными для получения, а реактивность CF3S(O)ONa невысока, а также что выход реакции сульфинилирования является соответственно низким. CN-A 1374298 описывает сульфинилирование 5-амино-1-[2,6-дихлор-4(трифторметил)фенил]-1H-пиразол-3-карбонитрила (II) при использовании калиевой соли трифторметилсульфиновой кислоты, CF3S(O)OK или смесей калиевой и натриевой солей трифторметилсульфиновой кислоты, CF3S(O)OK с CF3S(O)ONa, где сульфинилирующий агент соединяют с POCl3, PCl3, SOCl2,COCl2 или трихлорметилхлорметаноатом. Необязательно, амино/кислотный комплекс диметиламин п-тозилат может прибавляться для завершения реакции. Приводятся примеры для следующих комбинаций реагентов:CF3S(O)OK/Na; диметиламин п-тозилат; SOCl2. Приведенные температуры примеров реакционных смесей составляли от 40 до 60C.Huilong и др. описывает реакцию 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол-3 карбонитрила (II) с натриевой солью трифторметилсульфиновой кислоты (CF3S(O)ONa), диметиламин п-тозилатом и SOCl2 с добавлением каталитических количеств ДМФ (диметилформамида). Температуру поддерживали на уровне 3C в течение 10 мин, после чего ее поднимали до комнатной температуры, а потом до 50C (10 ч).-1 016304 Как описано в EP-A-1331222, 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол-3 карбонитрил (II) подвергают сульфинилированию при использовании N-трифторметилсульфинилсукцинимида в качестве сульфинилирующего агента в присутствии триэтиламина и без прибавления хлорирующего реагента. Изолируют промежуточное соединение N-трифторметилсульфиниламинопиразол и в условиях перестановки Тиа-Фриса при температурах от 35 до 55C превращают его в заключительный продукт 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-4-(трифторметилсульфинил)пиразол-3-карбонитрил. Таким образом, сульфинилированию 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол 3-карбонитрила (II) до заключительного продукта 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-4(трифторметилсульфинил)пиразол-3-карбонитрила (обычное название: фипронил) было уделено значительное внимание в литературе, при этом центр внимания был направлен на оптимизацию сульфинилирующего агента. Усовершенствования процесса, описанные в литературе, применяют п-тозилат диметиламина и температуры на уровне приблизительно 50C в качестве стандартных условий реакции. Однако, а также в соответствии с тем, что указано в недавней обзорной статье "Исследовательский прогресс в синтезе фипронила и его основные промежуточные соединения", Chinese Journal of Pesticides,2004, vol. 43,12, 529-531, сульфинилирование пиразольного промежуточного соединения все еще является в общем случае неприемлемым для промышленного получения в больших количествах. Продуктом реакции настоящего процесса сульфинилирования является фипронил, который представляет собой рыночный инсектицид значительного интереса. В общем случае процессы технического производства пестицидов должны соответствовать высоким требованиям в отношении выхода и чистоты продукта по причинам рентабельности, а также, что является более важным, для того, чтобы избежать присутствия потенциально токсических побочных продуктов. Это особенно относится к фипронилу, поскольку он также используется в продуктах для защиты животных и, таким образом, контактирует с домашними животными. Кроме того, узаконенным требованием к процессу технического производства является избежание воздействия на работников фабрики, а также на окружающую среду реагентов, которые могут иметь вредное влияние на здоровье работников или окружающую среду. Таким образом, является желательным иметь процесс технического производства, который позволяет избежать применения газообразных реагентов, таких как диметиламин. Кроме того, при переводе процесса от лабораторных масштабов к техническим масштабам могут возникать проблемы, которых не существовало как таковых или которые до определенной степени нельзя было предсказать в лаборатории. Например, загрузка и/или растворение объемных исходных материалов может занять намного больше времени при больших масштабах, чем в маленькой колбе, с тем эффектом, что кинетика реакции существенно изменяется и, таким образом, изменяется процесс превращения и спектр получаемых продуктов. Другой пример, который может быть упомянут, представляет собой появление побочных продуктов, которые благодаря их растворимости или структуре сложно отделить от желательного основного продукта в больших масштабах. Могут возникать проблемы с экстракцией, фильтрованием и засорением фильтра. Нерастворимые исходные материалы или побочные продукты реакции могут также потребовать перемешивания, нагревания при растворении или прокачивания с помощью насоса, что, таким образом, приводит к образованию негомогенных реакционных смесей. Еще одной проблемой является контроль температуры реакции при крупномасштабных процессах. Температурные режимы в общем случае являются более низкими, что может оказывать влияние на спектр побочных продуктов. Поскольку высокие значения температуры реакции и/или агрессивная реакционная среда могут вызвать коррозию, а также по экономическим причинам, умеренные условия реакции (низкие температуры) являются предпочтительными. Гигроскопические свойства твердых веществ могут осложнять реакции, которые благоприятно проходят в условиях при существенном отсутствии воды. Например, когда процесс, как определено выше,проводят с использованием амино/кислотного комплекса, где кислота представляет собой H2SO4, а не кислоты, как определено для процесса в соответствии с изобретением, выход продукта реакции может быть крайне низким. В процессе в соответствии с изобретением преимущественно используются нереакционноспособные катализаторы для того, чтобы избежать образования побочных продуктов реакции. Специфические вторичные или первичные амины могут реагировать с сульфинилирующим агентом и образовывать нерастворимые твердые вещества, которые вызывают проблемы с перемешиванием реакционной смеси. В целях улучшения процесса обработки преимущественно используют реагенты, которые могут быть удалены при использовании процесса дистилляции. Твердые вещества удаляют путем промывания кислотными или щелочными растворителями. Не является предпочтительным использовать реагенты,которые обладают свойствами межфазных катализаторов и могут препятствовать разделению фаз в процессе обработки.-2 016304 В этом контексте и учитывая тот факт, что одним из основных исходных материалов для современного промышленного получения фипронила является CF3Br (см., например, WO 01/30760), который демонстрирует высокую токсичность для окружающей среды и предусматривается как такой, который подлежит изъятию из процесса производства в соответствии с Монреальским Протоколом по веществам,которые истощают озоновый слой (он может использоваться только в качестве исходного материала для продукции), задачей настоящего изобретения является разработка нового крупномасштабного промышленного способа производства фипронила, который обеспечивает получение фипронила с высокой степенью чистоты и высоким выходом, позволяя в то же время избежать применения опасных реагентов и избежать проблем, связанных с техническим контролем реакции. Таким образом, был открыт способ, определенный в начале. Несмотря на то что примеры приведены для определенных амино/кислотных комплексов, которые прибавляются вначале или в процессе реакции сульфинилирования, не существует догм относительно критической важности специфической природы амино/кислотного комплекса в отношении контроля реакции или в отношении выхода и/или чистоты заключительного продукта фипронила. В EP-A1-668269 приведены общие рекомендации по проведению реакции в интервале температур от 0 до 100C, предпочтительно от 3 до 60C и наиболее предпочтительно от 30 до 55C. В соответствии с прописями примеров температура реакции в каждом случае достигает 50C и поддерживается на этом уровне в течение нескольких часов. Подобно этому в CN-A 1374298 и у Huilong et al. приведены примеры для температурного интервала от 40 до 60C (CN-A 1374298) и 50C (Huilong et al.). Документы уровня техники не упоминают проблему оптимизации контроля реакции для того, чтобы получить высокую степень чистоты заключительного продукта фипронила. При том обстоятельстве,что температурам не уделяется особого внимания в области техники - в то время, как интенсивно обсуждается выбор сульфинилирующего агента - было особенно удивительным обнаружить сильное влияние температуры реакции на спектр побочных продуктов. Новым объектом настоящего изобретения, таким образом, является способ сульфинилирования производной пиразола, характеризующийся тем, что 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1Hпиразол-3-карбонитрил (II) подвергают реакции с сульфинилирующим агентом S, как определено выше,в присутствии по крайней мере одного амино/кислотного комплекса, где амин(ы) является(ются) выбранным(и) из вторичных и/или третичных аминов, а кислота(ы) является(ются) выбранной(ыми) из фтористо-водородной, хлористо-водородной, бромисто-водородной, йодисто-водородной кислоты и производных сульфоновой кислоты, с добавлением галогенирующего агента. Схема реакции может быть представлена так, как показано ниже. Температуры реакции не превышают 36C. Самая высокая температура предпочтительно составляет от 25 до 39C, даже более предпочтительно от 31 до 39C, предпочтительно от 32 до 36C. Сульфинилирующий агент предпочтительно является выбранным из трифторметилсульфинилфторида, трифторметилсульфинилхлорида, трифторметилсульфинилбромида, трифторметилсульфинилйодида, трифторметилсульфиновой кислоты, ангидрида трифторметилсульфиновой кислоты, соли трифторметилсульфината натрия, соли трифторметилсульфината калия и их смесей. Сульфинилирующий агент более предпочтительно является выбранным из трифторметилсульфиновой кислоты, ангидрида трифторметилсульфиновой кислоты, соли трифторметилсульфината натрия, соли трифторметилсульфината калия и их смесей. В соответствии с предпочтительным воплощением изобретения трифторметилсульфинилфторид,трифторметилсульфинилхлорид, трифторметилсульфинилбромид или трифторметилсульфинилйодид,более предпочтительно трифторметилсульфинилхлорид, используются в качестве сульфинилирующего агента. В соответствии с предпочтительным воплощением изобретения соль трифторметилсульфинат натрия используется в качестве сульфинилирующего агента. В соответствии с другим предпочтительным воплощением настоящего изобретения соль трифторметилсульфинат калия используется в качестве сульфинилирующего агента. В соответствии с еще одним предпочтительным воплощением настоящего изобретения трифторметилсульфиновая кислота используется в качестве сульфинилирующего агента.-3 016304 В соответствии с еще одним предпочтительным воплощением настоящего изобретения ангидрид трифторметилсульфиновой кислоты используется в качестве сульфинилирующего агента. В соответствии с предпочтительным воплощением изобретения смесь солей трифторметилсульфината натрия и калия в соотношении от 0,01:99,99 до 50:50 вес. % используется в качестве сульфинилирующего агента. Является предпочтительным, когда используется от 1,0 до 1,35 мол.экв., наиболее предпочтительно 1,2 мол. экв. сульфинилирующего агента по отношению к 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол-3-карбонитрилу. В предпочтительном воплощении сульфинилирующий агент высушивают перед его применением до получения его в существенно свободной от воды форме. "Свободный от воды" означает, что содержание воды в твердом веществе не превышает 5-100 част./млн. Галогенирующий агент является выбранным из тионилхлорида, тионилбромида, фосфороксихлорида, оксалилхлорида, фосгена, трифосгена CCl3)2C(=O, хлорформиатов, фосфорпентахлорида, фосфортрихлорида, трихлорметилхлорметаноата и хлорида ксиленсульфоновой кислоты. В соответствии с предпочтительным воплощением изобретения хлорирующий агент используется в качестве галогенирующего агента. Предпочтительно, когда тионилхлорид или фосфороксихлорид применяют в качестве хлорирующего агента. В соответствии с другим предпочтительным воплощением настоящего изобретения фосфороксихлорид используется в качестве хлорирующего агента. Наиболее предпочтительно, когда тионилхлорид используется в качестве хлорирующего агента. Предпочтительно используют от 1,15 до 1,35 мол.экв., наиболее предпочтительно приблизительно 1,2 мол.экв. галогенирующего агента по отношению к 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]1H-пиразол-3-карбонитрилу. Авторы обнаружили, что, кроме выбора температуры реакции, выбор амино/кислотного комплекса играет ключевую роль в сульфинилировании 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1Hпиразол-3-карбонитрила. Критические свойства, которые оказывают влияние на реакцию сульфинилирования, представляют собой пространственные (объемные) свойства, значения pK, растворимость и молекулярный вес. Реакция сульфинилирования в соответствии с настоящим изобретением представляет собой синтез,который происходит в одном сосуде, двухэтапной реакции. Первый этап вовлекает прибавлениеCF3S(O)-группы к аминогруппе пиразольного кольца. На втором этапе образуется фипронил посредством перестановки Тиа-Фриса: Амино/кислотный комплекс имеет две функции в этой двухэтапной реакции: (1) когда сульфинилаты используются в качестве сульфинилирующих агентов, он катализирует активацию сульфинилата с помощью галогенирующего агента посредством промежуточного образования сульфиновой кислоты. Для этого необходимы каталитические количества от 0,01 до 1,0 мол.экв. амино/кислотного комплекса по отношению к пиразольному соединению II. (2) Это ускоряет перестановку Тиа-Фриса и оказывает большое влияние на селективность. С целью получения высокого выхода продукта и высокой степени чистоты общие количества свыше 1 мол.экв. амино/кислотного комплекса по отношению к пиразольному соединению II преимущественно используются для этапа 2. Предпочтительными являются амино/кислотные комплексы, которые демонстрируют низкую гигроскопичность или существенно не имеют гигроскопичности, поскольку способ сульфинилирования в соответствии с настоящим изобретением преимущественно осуществляют при существенном отсутствии воды (т.е. от 5 до 100 част./млн).-4 016304 Предпочтительные амины для использования в настоящем изобретении представляют собой третичные амины, такие как алкиламины, такие как триметиламин, триэтиламин, трипропиламин,триизопропиламин, трибутиламин, диметилэтиламин, диэтилметиламин, диметил н-пропиламин, диизопропилэтиламин, DBU (1,8-диазобицикло[5.4.0]ундец-7-ен), DBN (1,5-диазобицикло[4.3.0]нон-5-ен), метилморфолин, этилморфолин, N,N-диметиланилин, метилпиперидин, метилпирролидин или метилдиабензиламин; или ароматические амины, такие как пиридин, DMAP (диметиламинопиридин), коллидин, лутидин,пиримидин, пиразин или пиперазин; или вторичные амины, такие как алкиламины, такие как диметилэтиламин, диэтилметиламин, дипропиламин, диизопропиламин, дибутиламин, этилметиламин, изопропилметиламин или изопропилэтиламин; или циклические вторичные амины формулы NHR1R2, где R1 и R2 вместе с атомом азота, к которому они присоединены, образуют 3-10-членную насыщенную или частично ненасыщенную гетероциклическую кольцевую систему, которая является незамещенной или замещенной 1-3 C1-C8-алкильными илиC1-C8-галоалкильными группами и которая может содержать от 1 до 3 дополнительных гетероатомов,выбранных из кислорода, азота и серы, предпочтительно из кислорода и азота. Предпочтительные амины для использования в настоящем изобретении представляют собой вторичные амины. Предпочтительные вторичные амины представляют собой алкиламины диметилэтиламин, диэтилметиламин, дипропиламин, диизопропиламин, дибутиламин, этилметиламин, изопропилметиламин или изопропилэтиламин. Предпочтительно, когда циклические вторичные амины амино/кислотного комплекса определяются формулой NHR1R2, где R1 и R2 вместе с атомом азота, к которому они присоединены, образуют 3-10-членную насыщенную или частично ненасыщенную гетероциклическую кольцевую систему, предпочтительно 5-6-членную насыщенную гетероциклическую кольцевую систему, которая является незамещенной или замещенной 1-3 C1-C8-алкильными или C1-C8-галоалкильными группами, предпочтительно 1-3 C1-C3-алкильными или C1-C3-галоалкильными группами, наиболее предпочтительно 1-3 C1-C3 алкильными группами, наиболее предпочтительно 1-3 метильными группами и которая может содержать от 1 до 3 дополнительных гетероатомов, выбранных из кислорода, азота и серы, предпочтительно из кислорода и азота. Кроме того, предпочтительные вторичные амины представляют собой циклические вторичные амины, такие как пиперидин, пиперидин, который является замещенным C1-C8-алкилом илиC1-C8-алкилом или C1-C8-галоалкилом, такой как 2-метилпирролидин или 3-метилпирролидин. В случае, когда используются вторичные амины, соответствующая кислота амино/кислотного комплекса предпочтительно является выбранной из производной сульфоновой кислоты. Особенно предпочтительные амины для использования в настоящем изобретении представляют собой третичные амины. Предпочтительные третичные амины представляют собой алкиламины, такие как триметиламин, триэтиламин, трипропиламин, триизопропиламин,трибутиламин, диметилэтиламин, диэтилметиламин, диметил н-пропиламин, диизопропилэтиламин,DBU (1,8-диазобицикло[5.4.0]ундец-7-ен), DBN (1,5-диазобицикло[4.3.0]нон-5-ен), метилморфолин,этилморфолин, N,N-диметиланилин, метилпиперидин, метилпирролидин или метилдиабензиламин; или ароматические амины, такие как пиридин, DMAP (диметиламинопиридин), коллидин, лутидин, пиримидин, пиразин или пиперазин. В дополнительном предпочтительном воплощении третичный амин является выбранным из триэтиламина, трипропиламина, триизопропиламина, трибутиламина, диизопропилэтиламина, DBUDMAP (диметиламинопиридина), коллидина, лутидина, пиримидина, пиразина и пиперазина. В другом предпочтительном воплощении третичные амины являются выбранными из триметиламина, триэтиламина, диметилэтиламина, диэтилметиламина, диметил н-пропиламина, метилморфолина, N,N-диметиланилина, метилпиперидина, метилпирролидина, метилдиабензиламина и пиридина. Особенно предпочтительными являются триметиламин, триэтиламин, диметилэтиламин, диметил н-пропиламина или пиридин. Весьма предпочтительными являются триэтиламин и пиридин. В весьма предпочтительном воплощении амин представляет собой триэтиламин. Кроме того, в весьма предпочтительном воплощении амин представляет собой пиридин. В весьма предпочтительном воплощении амин также представляет собой триметиламин. Кроме того, в весьма предпочтительном воплощении по крайней мере одна из алкильных групп, присоединенных к атому азота амина, представляет собой метильную группу. В самом предпочтительном воплощении атом азота группы амина являетсяsp3-гибридизованным, т.е. он не образует двойной связи с соседним атомом. Предпочтительные кислоты амино/кислотного комплекса для использования в настоящем изобретении представляют собой хлористо-водородную кислоту, фтористо-водородную кислоту, бромистоводородную кислоту, йодисто-водородную кислоту или производные сульфоновой кислоты, например п-толуолсульфоновую кислоту, бензолсульфоновую кислоту, 4-этилбензолсульфоновую кислоту,4-хлорбензолсульфоновую кислоту, ксиленсульфоновую кислоту, 2,3-диметилбензолсульфоновую кислоту,2,4-диметилбензолсульфоновую кислоту,2,5-диметилбензолсульфоновую кислоту,2,6-диметилбензолсульфоновую кислоту, 1-нафталинсульфоновую кислоту, 2-нафталинсульфоновую кислоту, смеси двух или более изомеров диметилбензолсульфоновых кислот или мезитиленсульфоновую кислоту; или алкилсульфоновые кислоты, например метансульфоновую кислоту или камфорсульфоновую кислоту; или галоалкилсульфоновые кислоты, например трифторметилсульфоновую кислоту. Особенно предпочтительными являются кислоты со значением pK ниже 2. Наиболее предпочтительные кислоты представляют собой хлористо-водородную кислоту,п-толуолсульфоновую кислоту, ксиленсульфоновую кислоту, бензолсульфоновую кислоту, метансульфоновую кислоту, трифторметилсульфоновую кислоту, мезитиленсульфоновую кислоту, особенно п-толуолсульфоновую кислоту, ксиленсульфоновую кислоту и бензолсульфоновую кислоту. В случае, когда амин представляет собой вторичный амин, применение производных сульфоновой кислоты является предпочтительным. Из амино/кислотных комплексов, которые используются в настоящем изобретении, те, которые имеют значение pK ниже 6, предпочтительно 5 и выше 10, являются предпочтительными. Предпочтительные амино/кислотные комплексы Q приведены в табл. 1. Когда амин представляет собой третичный амин, то аминокислотные комплексы табл. 1, в которых кислота является хлористо-водородной кислотой или бромисто-водородной кислотой, в частности хлористо-водородной кислотой, являются предпочтительными. Кроме того, амино/кислотные комплексы табл. 1, в которых амин является третичным амином, а кислота представляет собой п-толуолсульфоновую кислоту, бензолсульфоновую кислоту или ксиленсульфоновую кислоту, являются предпочтительными.- 13016304 Амино/кислотные комплексы табл. 1 Q-2, Q-5, Q-12, Q-17, Q-22, Q-32, Q-42, Q-52, Q-142, Q-145,Q-147, Q-162, Q-165, Q-172, Q-175, Q-212, Q-215, Q-222, Q-225, Q-232 или Q-235 являются предпочтительными. Более предпочтительными являются амино/кислотные комплексы табл. 1 Q-2, Q-5, Q-6, Q-7, Q-12,Q-82, Q-85, Q-86, Q-87, Q-102, Q-105, Q-106, Q-107, Q-112, Q-115, Q-116, Q-117, Q-122, Q-125, Q-126,Q-127, Q-132, Q-135, Q-136, Q-137, Q-142, Q-145, Q-146, Q-147, Q-212, Q-215, Q-216, Q-217, Q-222, Q225, Q-226, Q-227, Q-232, Q-235, Q-236 или Q-237. Наиболее предпочтительными являются амино/кислотные комплексы табл. 1 Q-2, Q-5, Q-6, Q-7,Q-12, Q-142, Q-145, Q-146, Q-147, Q-212, Q-215, Q-216, Q-217, Q-222, Q-225, Q-226, Q-227, Q-232, Q-235,Q-236 или Q-237. Аминокислотные комплексы табл. 1, в которых амин представляет собой алкиламин Q-241, Q-242,Q-243, Q-247 или Q-249, являются предпочтительными. Аминокислотные комплексы табл. 1, в которых амин представляет собой вторичный амин Q-277,Q-278, Q279, Q-283, Q-284, Q-285, Q-295, Q-296, Q-297, Q-314, Q-315, Q-316, Q-320, Q-321, Q-323, Q-326,Q-327 или Q-328, являются предпочтительными. В отношении их применения в способе в соответствии с изобретением комбинации сульфинилирующего агента и амино/кислотного комплекса, приведенные в таблицах, представленных ниже, являются особенно предпочтительными. Таблица 2. Соль трифторметилсульфинат натрия используется в качестве сульфинилирующего агента, а амино/кислотный комплекс в каждом случае представляет собой строку табл.1. Таблица 3. Соль трифторметилсульфината калия используется в качестве сульфинилирующего агента, а амино/кислотный комплекс в каждом случае представляет собой строку табл. 1. Таблица 4. Трифторметилсульфиновая кислота используется в качестве сульфинилирующего агента, а амино/кислотный комплекс в каждом случае представляет собой строку табл. 1. Таблица 5. Ангидрид трифторметилсульфиновой кислоты используется в качестве сульфинилирующего агента, а амино/кислотный комплекс в каждом случае представляет собой строку табл. 1. Таблица 6. Смесь солей трифторметилсульфината натрия и калия, взятых в соотношении от 0,01:99,99 до 50:50 вес.%, используется в качестве сульфинилирующего агента, а амино/кислотный комплекс в каждом случае представляет собой строку табл. 1. Таблица 7. Трифторметилсульфинилфторид используется в качестве сульфинилирующего агента, а амино/кислотный комплекс в каждом случае представляет собой строку табл. 1. Таблица 8. Трифторметилсульфинилхлорид используется в качестве сульфинилирующего агента, а амино/кислотный комплекс в каждом случае представляет собой строку табл. 1. Таблица 9. Трифторметилсульфинилбромид используется в качестве сульфинилирующего агента, а амино/кислотный комплекс в каждом случае представляет собой строку табл. 1. Таблица 10. Трифторметилсульфинилйодид используется в качестве сульфинилирующего агента, а амино/кислотный комплекс в каждом случае представляет собой строку табл. 1. Кроме того, в дополнительном воплощении настоящего изобретения кислоты Льюиса, такие какAlCl3, FeCl3, CaCl2, ZnCl2, BF3, TiCl4 или ZrCl4, могут использоваться в обмене для протонных кислот,приведенных выше. Может быть предпочтительным прибавлять амино/кислотный комплекс в виде двух частей, одну часть для этапа 1, а другую часть после прибавления пиразола формулы II. Может быть предпочтительным использовать два различных амино/кислотных комплекса во время осуществления реакции. Например, первый амино/кислотный комплекс может прибавляться на этапе 1 в количествах от 0,2 до 1 мол.экв. по отношению к пиразолу II, катализируя активацию сульфинилата с помощью галогенирующего агента. После прибавления пиразола формулы II на этапе 2 перестановки Тиа-Фриса прибавляют второй амино/кислотный комплекс, отличный от первого, в количествах от 0,2 до 1 мол.экв. по отношению к пиразолу II. Предпочтительно, когда используют от 1,4 до 2,2 мол.экв., наиболее предпочтительно от 1,5 до 1,8 мол.экв. амино/кислотного комплекса в соответствии с настоящим изобретением по отношению к 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол-3-карбонитрилу.- 14016304 Когда сульфинилирующий агент представляет собой трифторметилсульфиновую кислоту или смесь, содержащую трифторметилсульфиновую кислоту, молярное количество амино/кислотного комплекса, которое является молярным эквивалентным молярному количеству трифторметилсульфиновой кислоты, предпочтительно получают in situ путем добавления амина, а оставшееся молярное количество,необходимое для получения требуемых 1,4-2,2 мол.экв., прибавляют в виде амино/кислотного комплекса. В предпочтительном воплощении амино/кислотный комплекс высушивают перед его применением до тех пор, пока он не станет существенно свободным от воды. "Свободный от воды" означает, что содержание воды в твердом веществе не превышает количества от 5 до 100 част./млн. К реакционной смеси могут предпочтительно прибавляться дополнительные добавки, такие как фторид калия, пентафторфенол, диметилформамид или 2,4-динитрофенол. Эти добавки предпочтительно прибавляют к реакционной смеси, или раствору, или суспензии исходных материалов соответственно перед началом реакции или в начале реакции. Наиболее предпочтительно, когда добавки прибавляют при низкой температуре в интервале от 5 до 10C. В предпочтительном воплощении от 0,1 до 1,5 мол.экв. фторида калия по отношению к 5-амино-1[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол-3-карбонитрилу прибавляют к реакционной смеси, или раствору, или суспензии исходных материалов соответственно при температуре от 5 до 10C во время и в начале реакции. Является предпочтительным прибавлять пентафторфенол,диметилформамид или 2,4-динитрофенол в каталитических количествах или в количестве 0,10 мол.экв. по отношению к 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол-3-карбонитрилу. В предпочтительном воплощении добавку высушивают перед применением до состояния, существенно свободного от воды. "Свободный от воды" означает, что содержание воды в твердом веществе не превышает от 5 до 100 част./млн. Реакцию можно проводить в инертном органическом растворителе, предпочтительно выбранном из алифатических, алициклических или ароматических, необязательно галогенированных углеводородов, таких как ароматические органические углеводороды, например толуол, ксилен, трифторметилбензол, бензол, нитробензол, монохлорбензол, дихлорбензол и этилбензол, предпочтительно толуол и ксилен, наиболее предпочтительно толуол; или алифатических или алициклических, необязательно галогенированных углеводородов, таких как гексан, циклогексан, бензин, 1,2-дихлорэтан, дихлорметан, трихлорметан (хлороформ), четыреххлористый углерод, предпочтительно 1,2-дихлорэтан, дихлорметан, трихлорметан; и этеров, например диэтилэтера, диоксана, тетрагидрофурана, 2-метилтетрагидрофурана или этиленгликоль диметилового или диэтилового этера; и кетонов, например ацетона или бутанона; и нитрилов, например ацетонитрила или пропионитрила; и амидов, например диметилформамида, DMI (1,3-диметил-2-имидазолидинон), диметилацетамида,N-метилформанилида, N-метилпирролидона или триамида гексаметилфосфорной кислоты; и сульфоксидов, например диметилсульфоксида. В предпочтительном воплощении используются растворители, которые являются существенно свободными от воды. "Свободный от воды" означает, что содержание воды в твердом веществе не превышает от 5 до 100 част./млн. Наиболее предпочтительный растворитель представляет собой толуол, свободный от воды. Реакцию осуществляют в атмосфере инертного газа, такого как аргон, или в атмосфере азота. В предпочтительном воплощении используют в общей сложности от 3,0 до 8,0 мол.экв., более предпочтительно от 4,0 до 7,5 мол.экв. и наиболее предпочтительно от 4,5 до 6,5 мол.экв. растворителя по отношению к 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол-3-карбонитрилу. Такая относительно высокая концентрация исходных материалов максимально повышает превращение в сульфинамидное промежуточное соединение. В случаях, когда исходные материалы растворяются и/или суспендируются соответственно, до их объединения используют приблизительно от 25 до 40% растворителя для растворения и/или суспендирования 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол-3-карбонитрила. В общем случае последовательность прибавления исходных материалов 5-амино-1-[2,6-дихлор-4(трифторметил)фенил]-1H-пиразол-3-карбонитрила, амино/кислотного комплекса, сульфинилирующего агента и галогенирующего агента может быть выбрана любой. Предпочтительно, когда соответствующие исходные материалы растворяют или суспендируют соответственно в реакционном растворителе перед прибавлением к реакционной смеси. Галогенирующий агент предпочтительно не прибавляется к 5-амино-1-[2,6-дихлор-4(трифторметил)фенил]-1H-пиразол-3-карбонитрилу при отсутствии амино/кислотного комплекса или сульфинилирующего агента в реакционной смеси. В предпочтительном воплощении галогенирующий агент растворяют в растворителе и прибавляют к реакционной смеси, содержащей 5-амино-1-[2,6 дихлор-4-(трифторметил)фенил]-1H-пиразол-3-карбонитрил, амино/кислотный комплекс и сульфинили- 15016304 рующий агент, все растворяют или суспендируют соответственно в растворителе. В предпочтительном воплощении галогенирующий агент и амино/кислотный комплекс смешивают с растворителем и прибавляют растворенный или суспендированный сульфинилирующий агент к реакционной смеси перед прибавлением 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол-3 карбонитрила. В предпочтительном воплощении 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол-3 карбонитрил (II) соединяют со смесью, содержащей сульфинилирующий агент, амино/кислотный комплекс и галогенирующий агент. В этом случае может быть предпочтительно включать первую порцию(равную приблизительно 1 мол.экв. по отношению к соединению II) галогенирующего агента в смесь,содержащую сульфинилирующий агент, амино/кислотный комплекс и галогенирующий агент, а потом прибавлять вторую порцию (равную приблизительно от 0,1 до 0,2 мол.экв. по отношению к соединениюII) после прибавления соединения II и перемешивания в течение приблизительно от 30 до 60 мин и непосредственно перед повышением температуры до 30-39C. Когда сульфинилирующий агент представляет собой трифторметилсульфиновую кислоту, может быть предпочтительным одновременно прибавлять трифторметилсульфиновую кислоту и галогенирующий агент к раствору или суспензии амино/кислотного комплекса, после чего осуществляют прибавление раствора 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол-3-карбонитрила к реакционной смеси. В другом предпочтительном воплощении растворенную или суспендированную смесь сульфинилирующего агента, амино/кислотного комплекса и галогенирующего агента в растворителе (предпочтительно толуоле) охлаждают до приблизительно 3-10C, и раствор 5-амино-1-[2,6-дихлор-4(трифторметил)фенил]-1H-пиразол-3-карбонитрила в растворителе (предпочтительно толуоле), который является нагретым до температуры 90-110C, соединяют с охлажденной смесью. Объемные соотношения растворителей выбирают таким образом, чтобы быть уверенным в том, что температура не будет превышать 39C. В предпочтительном воплощении после соединения 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол-3-карбонитрила, сульфинилирующего агента, амино/кислотного комплекса и хлорирующего агента температуру повышают до 30-39C, предпочтительно не выше 35C в течение 5-60 мин. Является также предпочтительным выдерживать реакционную смесь сначала при температуре-20-10C в течение 5-60 мин, предпочтительно 20-40 мин, после чего повысить температуру до 30-55C при скорости 5-45C/мин. Является предпочтительным, когда для получения продуктов высокой чистоты температуру реакционной смеси повышают до температуры не выше 35C. Когда сульфинилирующий агент представляет собой или содержит CF3S(O)OH, то изначальная температура реакции предпочтительно составляет -20-5C, в случае солей трифторметилсульфината щелочных или щелочно-земельных металлов изначальная температура реакции предпочтительно составляет -5-10C. Типично время реакции будет составлять приблизительно от 5 до 15 ч, предпочтительно от 10 до 15 ч. В дополнительном предпочтительном воплощении реакцию осуществляют в аппарате высокого давления при давлении от 1,013 бар (1 атм) до приблизительно 4 бар. После завершения реакции фипронил можно изолировать путем использования традиционных способов, таких как гашение реакции с помощью гидрокарбонатов, таких как NaHCO3, карбонатов, таких как NaCO3, или гидроксидов, таких как NaOH, экстракция фипронила с помощью неполярного органического растворителя, такого как этилацетат или метил-трет-бутиловый этер, промывание экстракта, например, с помощью гидрокарбонатов, таких как NaHCO3, концентрирование экстракта, например, в вакууме, кристаллизация фипронила и т.п. Изолированный фипронил может подвергаться очистке с помощью способа, такого как хроматография, перекристаллизация и т.п., в случае необходимости. Кристаллизацию заключительного продукта 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-4(трифторметилсульфинил)пиразол-3-карбонитрила обычно осуществляют из раствора неполярного,инертного, предпочтительно ароматического, растворителя с нереактивным заместителем, таким как хлор, фтор, циано, нитро, C1-C8-алкил или C1-C8-галоалкил, в частности, из раствора в бензоле, этилбензоле, монохлорбензоле, монофторбензоле, 1,2-дихлорбензоле, 1,3-дихлорбензоле, 1,4-дихлорбензоле,толуоле, о-ксилене, м-ксилене, п-ксилене, стирене, изопропиле, бензоле, н-пропилбензоле,2-хлортолуоле, 3-хлортолуоле, 4-хлортолуоле, трет-бутилбензоле, втор-бутилбензоле, изобутилбензоле,н-бутилбензоле, 1,3-диизопропилбензоле, 1,4-диизопропилбензоле, 2-нитротолуоле, 3-нитротолуоле,4-нитротолуоле, нитробензоле, бензонитриле, мезитилене, трифторметилбензоле, 1,2-дихлорэтане, ацетонитриле, диметилсульфоксиде, тетрагидрофуране, ацетоне, спиртах, таких как метанол, этанол,н-пропанол, изопропанол, н-бутанол, изобутанол, 2-бутанол или трет-бутанол, предпочтительно из раствора в монохлорбензоле, дихлорбензоле, этилбензоле или толуоле.- 16016304 Может быть предпочтительным прибавлять приблизительно от 1 до 30% полярного растворителя,такого как кетоны, амиды, спирты, эстеры или этеры, предпочтительно эстеры, кетоны или этеры, такие как ацетон метил этилкетон, пентан-2-он, диэтилкетон, 4-метил-2-пентанон, 3-метилбутан-2-он, третбутил-метил-кетон, циклогексанон, метилацетат, этилацетат, изопропилацетат, N-бутилацетат, изобутилацетат, диэтилкарбонат, 2-бутоксиэтилацетат, диметилформамид, диметилацетамид, диметилсульфоксид, нитрометан, нитроэтан, вода, этанол, метанол, пропан-1-ол, пропан-2-ол, бутан-1-ол, бутан-2-ол,трет-бутанол, 2-метилпропан-1-ол, 2-метилпропан-2-ол, пентан-3-ол, 2-метилбутан-1-ол, 3-метилбутан-1 ол, 1,2-этандиол, 1,3-пропандиол, 1,2-пропандиол, циклогексанол, диоксан, тетрагидрофуран, диэтиловый этер, метил трет-бутиловый этер, 2-метилтетрагидрофуран, ацетонитрил, пропионитрил или их смеси. В другом воплощении фипронил кристаллизуется из воды, необязательно, с добавлением приблизительно 1-30% полярного органического растворителя. Предпочтительно кристаллизацию осуществляют из монохлорбензола. Предпочтительно кристаллизацию осуществляют из дихлорбензола. Предпочтительно кристаллизацию осуществляют из этилбензола. Предпочтительно кристаллизацию осуществляют из толуола. Очистку сырьевого продукта можно осуществлять посредством фильтрации через древесный уголь или двуокись кремния или промывания водой. При получении способом в соответствии с настоящим изобретением полученный продукт фипронил в сырьевой реакционной смеси до кристаллизации содержит менее 3,0 вес.% при подсчете без растворителя, соединения F, типичного биологически активного побочного продукта синтеза фипронила. После очистки сырьевого продукта с помощью приемлемых способов, таких как промывание и (перекристаллизация, фипронил, полученный способом в соответствии с изобретением, содержит менее 1,0 вес.% соединения F. Кроме того, полученный продукт фипронил представляет собой соединение, свободное от соединения D, которое является обычным побочным продуктом современного крупномасштабного промышленного способа, как описано, например, в WO 01/30760, даже после очистки. Фипронил, полученный способом в соответствии с изобретением в инертной атмосфере, содержит менее 300 част./млн соединений,содержащих серу в своем окисленном состоянии (IV). Он также является свободным от соединения E,которое типично может образовываться как побочный продукт при современном промышленном процессе. Кроме того, полученный продукт фипронил является также свободным от трифторуксусной кислоты, которая является реагентом, используемым в современном промышленном процессе. Более того, когда хлорирующий агент используется в качестве галогенирующего агента, то полученный продукт фипронил является практически свободным от брома, это подразумевает, что он содержит не более чем 5-20 част./млн брома.- 17016304 Примеры ВЭЖХ проводили на Hewlett Packard HP 1200, Chemstation, оснащенном колонкойJ'Sphere ODS-H80, 4 мкм, 4,6250 мм (YMC), элюент A: 90 вес.% воды + 10 вес.% ацетонитрила; элюент В: 10 вес.% воды + 90 вес.% ацетонитрила, скорость истечения: 0,85 мл/мин,определение: 235 нм, Выходы, приведенные ниже, представлены в мольных процентах полученного очищенного кристаллического продукта после обработки. Чистота приведена в вес.% полученного твердого вещества. Пример 1. Сульфинилирование 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол-3 карбонитрила с использованием гидрохлорида триэтиламина, трифторметилсульфината калия и тионилхлорида в 4,5 мол.экв. толуола при при 35C. В трехгорлую круглодонную колбу на 50 мл, оснащенную магнитной мешалкой и термометром,помещали высушенный в вакууме трифторметилсульфинат калия (5,16 г, 30 ммоль), высушенный в вакууме гидрохлорид триэтиламина (5,16 г, 37,5 ммоль) и 10,4 г безводного толуола (4,5 мол.экв. по отношению к 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол-3-карбонитрилу) в атмосфере аргона. После охлаждения до температуры 0-5C с внешним охлаждением прибавляли тионилхлорид (3,57 г, 30 ммоль) в течение 15 мин при поддержании температуры реакции ниже 5C. После перемешивания в течение последующих 30 мин высушенный в вакууме 5-амино-1-(2,6-дихлор-4-трифторметилфенил)-1Hпиразол-3-карбонитрил (8,03 г, 25 ммоль, 99% чистоты) прибавляли при температуре 5C и реакционную смесь выдерживали при температуре 5C в течение 60 мин, а потом нагревали до 35C в течение 45 мин. Поддерживали температуру на уровне 35C в течение 3 ч перед добавлением 4,6 г толуола. Еще через 7 ч при 35C реакцию гасили с помощью 20 г раствора гидроокиси натрия(10 вес.%). Полученную суспензию разводили 30 мл этилацетата. После разделения фаз органический слой промывали один раз раствором гидроокиси натрия (10 вес.%). После разделения фаз органический слой подвергали анализу с помощью количественной ВЭЖХ (выход - 80,4%). Содержание соединения F составляло ниже 4,9 вес.% в сырьевой смеси (без растворителя). Продукт выкристаллизовывали из смеси этилацетата и толуола с получением указанного в заглавии соединения в виде белого кристаллического порошка 7,98 г, выход - 73%, 98%-ная чистота, как оценивали с помощью количественной ВЭЖХ. Пример 2. Сульфинилирование 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол-3 карбонитрила с использованием гидрохлорида триэтиламина, трифторметилсульфината калия и тионилхлорида в 6,5 мол.экв. толуола при 35C. В реактор на 750 мл с механической мешалкой и термометром помещали высушенный в вакууме трифторметилсульфинат калия (50,4 г, 296 ммоль), высушенный в вакууме гидрохлорид триэтиламина(51,1 г, 368 ммоль) и 147 г безводного толуола (6,5 мол.экв. по отношению к 5-амино-1-[2,6-дихлор-4(трифторметил)фенил]-1H-пиразол-3-карбонитрилу в атмосфере аргона. После охлаждения до температуры 0-5C с внешним охлаждением прибавляли тионилхлорид (35,7 г, 294 ммоль) в течение 15 мин при поддержании температуры реакции ниже 5C. После перемешивания в течение последующих 30 мин высушенный в вакууме 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол-3-карбонитрил (79,5 г, 245 ммоль, 99% чистоты) прибавляли при температуре 5C и реакционную смесь выдерживали при температуре 5C в течение 60 мин, а потом нагревали до 35C в течение 45 мин. Поддерживали температуру на этом уровне в течение 10 ч перед гашением реакции с 200 г гидроокиси натрия (10 вес.%). Полученную суспензию разводили 176 мл этилацетата. После разделения фаз органический слой промывали один раз раствором гидроокиси натрия (10 вес.%). После разделения фаз органический слой подвергали анализу с помощью количественной ВЭЖХ, получая при этом неизолированный фипронил. Сравнительный пример C1. Сульфинилирование 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]1H-пиразол-3-карбонитрила с использованием гидрохлорида триэтиламина, трифторметилсульфината калия и тионилхлорида в 6,5 мол.экв. толуола при 45C. Сравнительный пример C1 осуществляли в соответствии с процедурой, описанной в примере 2, но температуру реакционной смеси поддерживали на уровне 5C в течение 60 мин, а потом нагревали смесь до 45 вместо 35C в течение 45 мин.- 18016304 Пример 3. Сульфинилирование 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол-3 карбонитрила с использованием тионилхлорида, гидрохлорида триэтиламина и добавления порций трифторметилсульфината калия. В реактор на 750 мл с механической мешалкой и термометром помещали высушенный в вакууме гидрохлорид триэтиламина (51,1 г, 368 ммоль), 147 г безводного толуола (6,5 мол.экв. по отношению к 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол-3-карбонитрилу) и тионилхлорид (35,7 г,294 ммоль) в атмосфере аргона. После охлаждения до температуры 0-5C с внешним охлаждением прибавляли высушенный в вакууме трифторметилсульфинат калия (50,4 г, 296 ммоль) тремя равными порциями каждые 10 мин, поддерживая температуру реакции ниже 5C. После перемешивания в течение последующих 30 мин прибавляли высушенный в вакууме 5-амино-1-[2,6-дихлор-4(трифторметил)фенил]-1H-пиразол-3-карбонитрил (79,5 г, 245 ммоль, 99%-ная чистота) при 5C и реакционную смесь выдерживали при 5C в течение 60 мин, а потом нагревали до 35C в течение 45 мин. Температуру 35C поддерживали в течение последующих 10 ч перед тем, как погасить реакцию с помощью 200 г раствора гидроокиси натрия (10 вес.%). Полученную суспензию разводили 176 мл этилацетата. После разделения органический слой промывали один раз с помощью раствора гидроокиси натрия (10 вес.%). После разделения фаз органический слой подвергали анализу с помощью количественной ВЭЖХ (выход - 86%). Содержание соединения F составляло ниже 2,5 вес.% в сырьевой смеси (без растворителя). Продукт выкристаллизовывали из смеси этилацетата и толуола, получая при этом указанное в заглавии соединение в виде белого кристаллического порошка (80,3 г, выход - 75%, 98%-ная чистота, как оценивали с помощью количественной ВЭЖХ). Пример 4. Сульфинилирование 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол-3 карбонитрила с использованием тионилхлорида, тозилата морфолина и добавления порций трифторметилсульфината калия. Получение осуществляли так, как описано в примере 3, приведенном выше. После разделения фаз органический слой подвергали анализу с помощью количественной ВЭЖХ (выход - 83%). Содержание соединения F составляло ниже 0,5 вес.% в сырьевой смеси (без растворителя). Продукт выкристаллизовывали из смеси этилацетата и толуола, получая при этом указанное в заглавии соединение в виде белого кристаллического порошка (67 г, выход - 98%, 98%-ная чистота, как оценивали с помощью количественной ВЭЖХ). Сравнительный пример C2. Сравнительный пример C2 осуществляли в соответствии с процедурой, описанной для примера 4,но реакционную смесь выдерживали при 5C в течение 60 мин, а потом нагревали до 50 вместо 35C в течение 45 мин. Продукт выкристаллизовывали из толуола, получая при этом указанное в заглавии соединение в виде белого кристаллического порошка (выход - 69%, 98%-ная чистота, как оценивали с помощью количественной ВЭЖХ). Пример повторяли дважды. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ сульфинилирования производного пиразола, характеризующийся тем, что 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол-3-карбонитрил (II) подвергают реакции с сульфинилирующим агентом S в присутствии по крайней мере одного амино/кислотного комплекса,в котором амин(ы) является(ются) выбранным(и) из вторичных и/или третичных аминов, а кислота(ы) является(ются) выбранной(ыми) из хлористо-водородной, фтористо-водородной,п-толуолсульфоновой кислоты, бензолсульфоновой кислоты, 4-этилбензолсульфоновой кислоты,4-хлорбензолсульфоновой кислоты, ксиленсульфоновой кислоты, 2,3-диметилбензолсульфоновой кислоты,2,4-диметилбензолсульфоновой кислоты,2,5-диметилбензолсульфоновой кислоты,2,6-диметилбензолсульфоновой кислоты, 1-нафталинсульфоновой кислоты, 2-нафталинсульфоновой кислоты, смесей двух или более изомеров диметилбензолсульфоновой кислоты, мезитиленсульфоновой кислоты, метансульфоновой кислоты, камфорсульфоновой кислоты и трифторметилсульфоновой кислоты при добавлении галогенирующего агента, где S представляет собой[CF3S(O)]2O или CF3S(O)X,где X означает фтор, хлор, бром, йод, группу гидрокси, или соль щелочного или щелочноземельного металла гидроксигруппы; или их смеси, где температура реакционной смеси никогда не превышает 39C. 2. Способ в соответствии с п.1, где галогенирующий агент является выбранным из тионилхлорида,тионилбромида, фосфороксихлорида, оксалилхлорида, фосгена, трифосгена CCl3)2C(=O, хлорформиа- 19016304 тов, фосфорпентахлорида, фосфортрихлорида, трихлорметилхлорметаноата и хлорида ксиленсульфоновой кислоты. 3. Способ в соответствии с п.1 или 2, где галогенирующий агент представляет собой хлорирующий агент, выбранный из тионилхлорида и фосфороксихлорида. 4. Способ в соответствии с любым из пп.1-3, где амино/кислотный комплекс является выбранным из третичных алкиламинов,таких как триметиламин,триэтиламин,трипропиламин,триизопропиламин, трибутиламин, диметилэтиламин, диэтилметиламин, диметил н-пропиламин, диизопропилэтиламин, DBU (1,8-диазобицикло[5.4.0]ундец-7-ена), DBN (1,5-диазобицикло[4.3.0]нон-5-ена),метилморфолин, этилморфолин, N,N-диметиланилин, метилпиперидин, метилпирролидин и метилдиабензиламин; и третичных ароматических аминов, таких как пиридин, DMAP (диметиламинопиридин), коллидин,лутидин, пиримидин, пиразин и пиперазин; и вторичных алкиламинов, таких как диметилэтиламин, диэтиламин, дипропиламин,диизопропиламин, дибутиламин, этилметиламин, изопропилметиламин и изопропилэтиламин; и циклических вторичных аминов, таких как пиперидин, пиперидин, который является замещеннымC1-C8-алкилом или C1-C8-галоалкилом, такой как 2-метилпиперидин или 4-метилпиперидин, пирролидин,имидазолидин, пиррол, пиперазин и морфолин. 5. Способ в соответствии с любым из пп.1-4, где амин амино/кислотного комплекса является выбранным из триметиламина, триэтиламина, трипропиламина, триизопропиламина,диметилэтиламина, диэтилметиламина, диметил н-пропиламина, диизопропилэтиламина, DBU(1,8-диазобицикло[5.4.0]ундец-7-ена), DBN (1,5-диазобицикло[4.3.0]нон-5-ена), метилморфолина, этилморфолина, N,N-диметиланилина, метилпиперидина, метилпирролидина, метилдиабензиламина, пиридина, DMAP (диметиламинопиридина), коллидина, лутидина, пиримидина, пиразина и пиперазина. 6. Способ в соответствии с любым из пп.1-5, где амин амино/кислотного комплекса является выбранным из триметиламина, триэтиламина, диметилэтиламина, диэтилметиламина, диметил н-пропиламина, метилморфолина, этилморфолина, N,N-диметиланилина, метилпиперидина, метилпирролидина, метилдибензиламина и пиридина. 7. Способ в соответствии с любым из пп.1-4, где амин амино/кислотного комплекса является выбранным из диметилэтиламина, диэтиламина, дипропиламина, диизопропиламина, дибутиламина,этилметиламина, изопропилметиламина и изопропилэтиламина, пиперидина, пиперидина, который является замещенным C1-C8-алкилом или C1-C8-галоалкилом, такого как 2-метилпиперидин или 4-метилпиперидин, пирролидина, пирролидина, который является замещенным C1-C8-алкилом илиC1-C8-галоалкилом, такого как 2-метилпирролидин или 4-метилпирролидин, имидазолидина, пиррола,пиперазина и морфолина. 8. Способ в соответствии с любым из пп.1-6, где кислота амино/кислотного комплекса является выбранной из хлористо-водородной кислоты, п-толуолсульфоновой кислоты, бензолсульфоновой кислоты и ксиленсульфоновой кислоты. 9. Способ в соответствии с любым из пп.1-7, где кислота амино/кислотного комплекса является выбранной из п-толуолсульфоновой кислоты, бензолсульфоновой кислоты, 4-этилбензолсульфоновой кислоты, 4-хлорбензолсульфоновой кислоты, ксиленсульфоновой кислоты, 2,3-диметилбензолсульфоновой кислоты,2,4-диметилбензолсульфоновой кислоты,2,5-диметилбензолсульфоновой кислоты,2,6-диметилбензолсульфоновой кислоты, 1-нафталинсульфоновой кислоты, 2-нафталинсульфоновой кислоты, смесей двух или более изомеров диметилбензолсульфоновой кислоты, мезитиленсульфоновой кислоты, метансульфоновой кислоты, камфорсульфоновой кислоты и трифторметилсульфоновой кислоты, предпочтительно из п-толуолсульфоновой кислоты, бензолсульфоновой кислоты и ксиленсульфоновой кислоты. 10. Способ в соответствии с любым из пп.1-9, где сульфинилирующий агент S является выбранным из CF3S(O)Cl, CF3S(O)OH, [CF3S(O)]2O, CF3S(O)ONa, CF3S(O)OK и их смесей. 11. Способ в соответствии с любым из пп.1-10, где реакцию проводят в органическом растворителе,выбранном из толуола, бензола, ксилена, трифторметилбензола, монохлорбензола, этилбензола и дихлорбензола. 12. Способ в соответствии с любым из пп.1-11, где сульфинилирующий агент прибавляют к реакционному раствору смеси амино/кислотного комплекса и галогенирующего агента перед прибавлением 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол-3-карбонитрила. 13. Способ в соответствии с любым из пп.1-12, где 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]1H-пиразол-3-карбонитрил прибавляют к реакционной смеси сульфинилирующего агента, амино/кислотного комплекса и галогенирующего агента. 14. Способ в соответствии с любым из пп.1-13, где используют от 1,4 до 2,2 мол.экв. амино/кислотного комплекса по отношению к 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол 3-карбонитрилу. 15. Способ в соответствии с любым из пп.1-14, где используют от 1,15 до 1,35 мол.экв. галогенирующего агента по отношению к 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол-3- 20016304 карбонитрилу. 16. Способ в соответствии с любым из пп.1-15, где используют от 1,0 до 1,35 мол.экв. сульфинилирующего агента по отношению к 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-1H-пиразол-3 карбонитрилу. 17. Способ в соответствии с любым из пп.1-16, где после соединения 5-амино-1-[2,6-дихлор-4(трифторметил)фенил]-1H-пиразол-3-карбонитрила, сульфинилирующего агента, амино/кислотного комплекса и галогенирующего агента температуру повышают до 30-39C в течение 5-60 мин. 18. Способ в соответствии с любым из пп.1-17, где продукт реакции 5-амино-1-[2,6-дихлор-4(трифторметил)фенил]-4-(трифторметилсульфинил)пиразол-3-карбонитрил выкристаллизовывают из раствора монохлорбензола, дихлорбензола, этилбензола или толуола. 19. Способ в соответствии с любым из пп.1-18, где на дополнительном этапе 5-амино-1-[2,6-дихлор 4-(трифторметил)фенил]-4-(трифтометилсульфинил)пиразол-3-карбонитрил вводят в пестицидную композицию. 20. Способ в соответствии с любым из пп.1-18, где на дополнительном этапе 5-амино-1-[2,6-дихлор 4-(трифторметил)фенил]-4-(трифтометилсульфинил)пиразол-3-карбонитрил вводят в паразитицидную композицию.
МПК / Метки
МПК: A61P 33/00, A61K 31/415, A01N 43/56, A01N 43/00, C07D 231/44
Метки: производной, сульфинилирования, способ, пиразола
Код ссылки
<a href="https://eas.patents.su/22-16304-sposob-sulfinilirovaniya-proizvodnojj-pirazola.html" rel="bookmark" title="База патентов Евразийского Союза">Способ сульфинилирования производной пиразола</a>
Предыдущий патент: Метаболическая инженерия сбраживающих арабинозу дрожжевых клеток
Следующий патент: Способ разработки залежи природных солей подземным растворением
Случайный патент: Самокомпенсирующаяся балансовая пружина для механического осциллятора системы балансовая пружина / баланс хода часового механизма, и способ ее изготовления