Способ получения защищенных производных l-аланина
Номер патента: 18913
Опубликовано: 29.11.2013
Авторы: Фейбуш Пенина, Анцалоне Луиджи, Виллани Фрэнк Дж.
Формула / Реферат
1. Способ получения соединения формулы (I)

где PG1 представляет собой защитную группу для атома азота;
R0 представляет собой водород или C1-4алкил;
R6 представляет собой водород;
R4 представляет собой фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из С1-6алкила, циано, карбамоила,
а также его фармацевтически приемлемых энантиомеров, фармацевтически приемлемых диастереомеров, фармацевтически приемлемых рацематов и фармацевтически приемлемых солей, включающий следующие стадии:
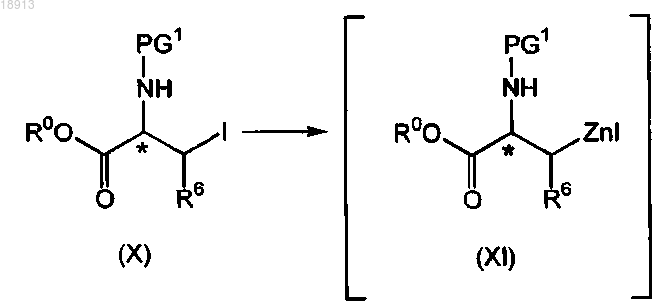
взаимодействие соединения формулы (X), где PG1 представляет собой защитную группу для атома азота, с цинком; в присутствии йода; в первом органическом растворителе или смеси органических растворителей, причем указанный первый органический растворитель нереакционноспособен по отношению к используемому йоду; с получением соответствующего соединения формулы (XI);
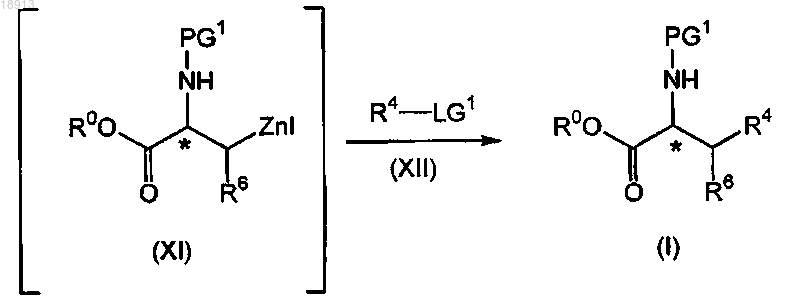
взаимодействие соединения формулы (XI) с соединением формулы (XII), где LG1 представляет собой уходящую группу; в присутствии палладиевого катализатора и фосфиновой лигандной системы; во втором органическом растворителе или смеси органических растворителей; с получением соответствующего соединения формулы (I).
2. Способ по п.1, где PG1 представляет собой Boc.
3. Способ по п.1, где R0 представляет собой метил.
4. Способ по п.1, где цинк представляет собой цинковую пыль.
5. Способ по п.4, где от 0,5 до 1,5 моль цинковой пыли присутствует на каждый моль соединения (X).
6. Способ по п.1, где от 0,1 до 0,5 моль йода присутствует на каждый моль соединения (X).
7. Способ по п.1, где первый органический растворитель представляет собой DMAc.
8. Способ по п.1, где соединение формулы (X) подвергают взаимодействию с цинком при температуре менее чем 10°C.
9. Способ по п.1, где цинк и йод смешивают перед добавлением к соединению формулы (X).
10. Способ по п.1, где LG1 представляет собой бром.
11. Способ по п.1, где от 0,25 до 1,0 моль соединения формулы (XII) присутствует на каждый моль соединения (XI).
12. Способ по п.1, где палладиевый катализатор и фосфиновая лигандная система представляют собой сочетание Pd2(dba)3 и P(o-tol)3.
13. Способ по п.1, где второй органический растворитель представляет собой DMAc.
14. Способ по п.1, где соединение формулы (X) подвергают взаимодействию с соединением формулы (XII) при температуре в диапазоне от 50 до 100°C.
15. Способ по п.1, где соединение формулы (XI) добавляют к смеси соединения формулы (XII), палладиевого катализатора и фосфиновой лигандной системы.
16. Способ получения соединения формулы (I-B)
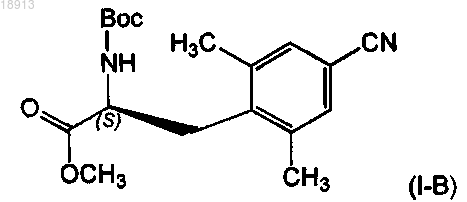
включающий следующие стадии:
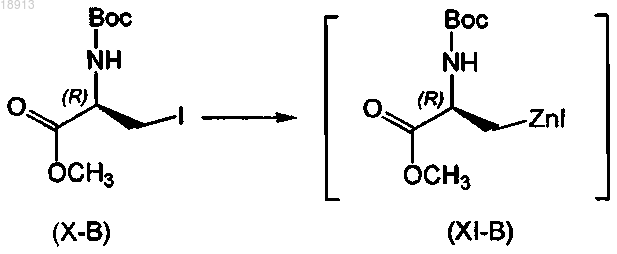
взаимодействие соединения формулы (Х-В) с цинком; в присутствии йода; в первом органическом растворителе или смеси органических растворителей, причем указанный первый органический растворитель нереакционноспособен по отношению к используемому йоду; с получением соответствующего соединения формулы (XI-B);
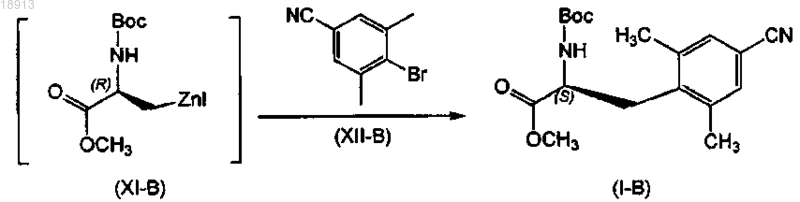
взаимодействие полученного соединения формулы (XI-B) с соединением формулы (XII-B); в присутствии палладиевого катализатора и фосфиновой лигандной системы; во втором органическом растворителе или смеси органических растворителей; с получением соответствующего соединения формулы (I-B).
17. Способ по п.16, где цинк представляет собой цинковую пыль.
18. Способ по п.17, где от 0,5 до 1,5 моль цинковой пыли присутствует на каждый моль соединения (Х-В).
19. Способ по п.16, где от 0,1 до 0,5 моль йода присутствует на каждый моль соединения (Х-В).
20. Способ по п.16, где первый органический растворитель представляет собой DMAc.
21. Способ по п.16, где соединение формулы (Х-В) подвергают взаимодействию с цинком при температуре менее чем 10°C.
22. Способ по п.16, где цинк и йод смешивают перед добавлением к соединению формулы (Х-В).
23. Способ по п.16, где от 0,25 до 1,0 моль соединения формулы (XII-B) присутствует на каждый моль соединения (XI-B).
24. Способ по п.16, где палладиевый катализатор и фосфиновая лигандная система представляют собой сочетание Pd2(dba)3 и P(o-tol)3.
25. Способ по п.16, где второй органический растворитель представляет собой DMAc.
26. Способ по п.16, где соединение формулы (Х-В) подвергают взаимодействию с соединением формулы (XII-B) при температуре в диапазоне от 50 до 100°C.
27. Способ по п.16, где соединение формулы (XI-В) добавляют к смеси соединения формулы (XII-B), палладиевого катализатора и фосфиновой лигандной системы.
28. Способ получения соединения формулы (II-В)
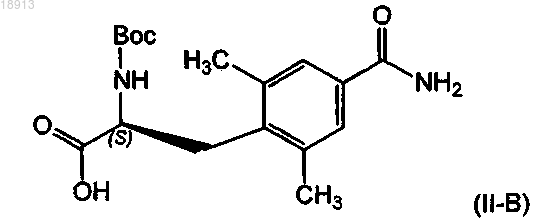
а также его фармацевтически приемлемой соли, включающий следующие стадии:
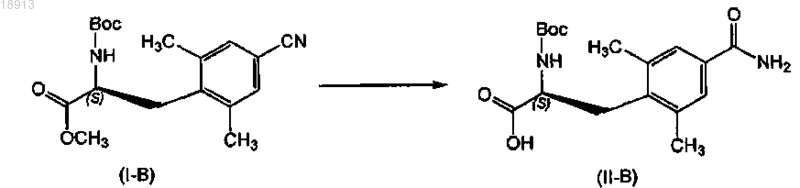
взаимодействие соединения формулы (I-B) с окисляющим агентом; в присутствии неорганического основания; в третьем органическом растворителе; с получением соответствующего соединения формулы (II-В).
29. Способ по п.28, где окисляющий агент выбран из группы, состоящей из перекиси водорода, LiOH и LiOOH.
30. Способ по п.29, где окисляющий агент представляет собой перекись водорода.
31. Способ по п.28, где окисляющий агент представляет собой 30% перекись водорода и присутствует в избыточном количестве.
32. Способ по п.28, где неорганическое основание представляет собой карбонат калия.
33. Способ по п.28, где от 1,0 до 3,0 моль неорганического основания присутствует на каждый моль соединения (I-B).
34. Способ по п.28, где третий органический растворитель представляет собой DMSO.
35. Способ по п.28, где соединение формулы (I-B) подвергается взаимодействию с указанным окисляющим агентом при температуре в диапазоне от комнатной температуры до 60°C.
Текст
СПОСОБ ПОЛУЧЕНИЯ ЗАЩИЩЕННЫХ ПРОИЗВОДНЫХ L-АЛАНИНА Изобретение направлено на создание нового способа получения защищенных производныхL-аланина, которые могут найти применение в качестве промежуточных продуктов в синтезе соединений, применимых в качестве модуляторов мю/дельта опиоидных рецепторов.(71)(73) Заявитель и патентовладелец: ЯНССЕН ФАРМАЦЕВТИКА НВ (BE) Область применения изобретения Настоящее изобретение направлено на создание нового способа получения защищенных производных L-аланина, которые могут найти применение в качестве промежуточных продуктов в синтезе соединений, применимых в качестве модуляторов мю/дельта-опиоидных рецепторов. Предпосылки создания изобретения Опиоидные рецепторы обнаружили в середине 1970-х годов и сразу классифицировали на три подтипа рецепторов (мю-, дельта-и каппа-). Позднее три исходных типа рецепторов были дополнительно классифицированы на подгруппы. Также известно, что семейство опиоидных рецепторов принадлежит к суперсемейству рецепторов, сопряженных с G-белком (GPCR). Большую физиологическую важность имеют признанные факты о том, что опиоидные рецепторы присутствуют в центральной и периферической нервной системе многих видов млекопитающих, в том числе человека, и что модуляция соответствующих рецепторов может привести к многочисленным, хотя и различным, биологическим эффектам,как желательным, так и нежелательным (D.S. Fries, "Analgesics", в Principles of Medicinal Chemistry, 4thTherapeutic Agents, John WileySons, Inc., 1996, p. 321-441). В более поздних изданиях сообщалось о возможности гетеродимеризации подклассов опиоидных рецепторов, при этом соответствующие физиологические реакции пока еще не определены (Pierre J.M. Riviere and Jean-Louis Junien, "Opioid receptors:Targets for new gastrointestinal drug development", Drug Development 2000, p. 203-238). Идентификация различных биологических действий модуляторов опиоидных рецепторов привела к созданию множества полезных лекарственных средств. Наиболее важными из них являются многочисленные централизованно действующие модуляторы-агонисты мю-опиоидных рецепторов, поступающие на рынок как анальгетики для ослабления боли (например, морфин), а также периферически действующие агонисты мю-рецепторов для регуляции перистальтики (например, лоперамид). Сегодня продолжаются клинические исследования по оценке возможности медицинского применения селективных модуляторов дельта-, мю- и каппа-рецепторов, а также соединений, обладающих комбинированными модуляционными свойствами по отношению к рецепторам нескольких подтипов. Ожидается, что исследования такого рода могут привести к созданию веществ с новыми полезными свойствами или веществ с минимальными побочными эффектами по сравнению с присутствующими сегодня на рынке препаратами(примеры побочных эффектов морфина включают запор, угнетение дыхательной функции и потенциальную наркотическую зависимость). В области гастроэнтерологии сегодня изучаются возможности применения опиоидных модуляторов селективного или смешанного типов для таких целей, как лечение различных диарейных синдромов, расстройств перистальтики (послеоперационная кишечная непроходимость, запоры) и внутренних болей (послеоперационный болевой синдром, синдром раздраженного кишечника и воспалительные расстройства кишечника) (Pierre J.M. Riviere и Jean-Louis Junien, "Opioidreceptors: Targets for new gastrointestinal drug development". Drug Development, 2000, p. 203-238). Практически одновременно с идентификацией опиоидных рецепторов был также идентифицирован набор эндогенных опиоидных лигандов-энкефалинов (D.S. Fries, "Analgesics", в Principles of MedicinalChemistry, 4th ed.; W.O. Foye; T.L. Lemke and D.A. Williams, Eds.; Williams and Wilkins: Baltimore, Md.,1995; p. 247-269). Шиллер обнаружил, что укорочение исходных пентапептидных энкефалинов до более простых дипептидов дало набор соединений, которые сохранили опиоидную активность (Р. Schiller, патент WO 96/06855). Однако одним из потенциальных недостатков подобных соединений является их вероятная естественная нестабильность (P.W. Schiller et al., Int. J. Pept. Protein Res. 1993, 41(3), p. 313-316). Позднее был описан набор опиоидных псевдопептидов, содержащих гетероароматические или гетероалифатические ядра, однако было обнаружено, что эти соединения имеют функциональный профиль, отличный от описанного в указанных выше работах Шиллера (L.H. Lazarus et al., Peptides 2000, 21,p. 1663-1671). Кроме того, Вентланд и др. опубликовали результаты своих работ с морфиноподобными структурами, в которых были получены карбоксамидопроизводные морфина и их аналоги (М.Р. Wentland et al.,Biorg. Med. Chem. Letters 2001, 11, p. 1717-1721; M.P. Wentland et al., Biorg. Med. Chem. Letters 2001, 11,p. 623-626). Вентланд обнаружил, что замещение фенольным фрагментом морфиноподобных структур с первичным карбоксамидом приводит к активностям от равных до в 40 раз меньших, в зависимости от опиоидного рецептора и карбоксамида. Также было обнаружено, что любое дополнительное замещение по атому N карбоксадида значительно понижает желательную связывающую активность. Модуляторы, агонисты или антагонисты опиоидных рецепторов применяются для лечения и профилактики различных патологических состояний у млекопитающих, например болевых синдромов и желудочно-кишечных расстройств, таких как диарейные синдромы, расстройства перистальтики, включая послеоперационную непроходимость кишечника и запор, и внутренние боли, включая послеоперационный болевой синдром, синдром раздражнного кишечника и воспалительные расстройства кишечника. Бреслин и соавторы в патенте США 2005/0203143 А 1, опубликованном 15 сентября 2005 г., содержание которого полностью включено в настоящее описание путем ссылки, раскрыли модуляторы опиоидных рецепторов, фармацевтические композиции с использованием таких модуляторов и способы ле-1 018913 чения с применением таких модуляторов. Настоящее изобретение направлено на создание способов получения промежуточных продуктов, которые могут найти применение в синтезе модуляторов опиоидных рецепторов, описанных в патенте США 2005/0203143 А 1. Краткое описание изобретения Настоящее изобретение направлено на создание способа получения соединений формулы (I) где PG1 представляет собой защитную группу для атома азота;R6 выбран из группы, состоящей из водорода и С 1-6 алкила;R4 представляет собой арил или гетероарил; причем указанный арил или гетероарил необязательно замещен 1-5 заместителями, независимо выбираемыми из группы, состоящей из С 1-6 алкила, С 1-6 алкокси,арил-С 1-6 алкокси, арил-С 1-6 алкилкарбонилокси, гетероарил-С 1-6 алкилкарбонилокси, гетероарила, гидрокси, галогена, аминосульфонила, формиламино, аминокарбонила, С 1-6 алкиламинокарбонила,ди(С 1-6 алкил)аминокарбонила, гетероциклилкарбонила, карбокси и циано; причем указанный С 1-6 алкил необязательно замещен амино, С 1-6 алкиламино или (С 1-6 алкил)2 аминогруппу; и арильный фрагмент указанного арил-С 1-6 алкилкарбонилокси необязательно замещен 1-4 заместителями, независимо выбираемыми из группы, состоящей из С 1-6 алкила, С 1-6 алкокси, галогена, циано, амино и гидрокси,а также их фармацевтически приемлемых энантиомеров, фармацевтически приемлемых диастереомеров,фармацевтически приемлемых рацематов и их фармацевтически приемлемых солей; включающего, состоящего и/или по существу состоящего из следующих стадий: взаимодействие соединения формулы (X), где PG1 представляет собой защитную группу для атома азота, с цинком; в присутствии источника йода; в первом органическом растворителе или смеси органических растворителей, причем указанный первый органический растворитель нереакционноспособен по отношению к используемому источнику йода; с получением соответствующего соединения формулы взаимодействие соединения формулы (XI) с соединением формулы (XII), где LG1 представляет собой уходящую группу; в присутствии палладиевого катализатора и фосфиновой лигандной системы; во втором органическом растворителе или смеси органических растворителей; с получением соответствующего соединения формулы (I). Настоящее изобретение дополнительно направлено на создание способа получения соединения формулы (I-B) включающего, состоящего и/или по существу состоящего из следующих стадий: взаимодействие соединения формулы (Х-В) с цинком; в присутствии источника йода; в первом органическом растворителе или смеси органических растворителей, причем указанный первый органический растворитель нереакционноспособен по отношению к используемому источнику йода; с получени-2 018913 ем соответствующего соединения формулы (XI-B); взаимодействие соединения формулы (XI-B) с соединением формулы (XII-B); в присутствии палладиевого катализатора и фосфиновой лигандной системы; во втором органическом растворителе или смеси органических растворителей; с получением соответствующего соединения формулы (I-B). Настоящее изобретение дополнительно направлено на создание способа получения соединения формулы (II-B) либо его фармацевтически приемлемой соли; включающего, состоящего и/или по существу состоящего из следующих стадий: взаимодействие соединения формулы (I-B) с окисляющим агентом; в присутствии неорганического основания; в третьем органическом растворителе; с получением соответствующего соединения формулы(II-B). Настоящее изобретение дополнительно направлено на продукты, получаемые в соответствии с любым из описанных в данном документе способов. Предпочтительно соединения, получаемые в соответствии с описанными в данном документе способами, являются, по существу, чистыми. Подробное описание изобретения Настоящее изобретение направлено на создание нового способа получения соединений формулы (I) где PG1, R0, R4 и R6 определены согласно приведенному описанию,а также их фармацевтически приемлемых энантиомеров, диастереомеров, рацематов и их солей. Соединения формулы (I) могут применяться в качестве промежуточных продуктов при получении модуляторов опиоидных рецепторов, как описано в патенте США US2005/0203143 А 1, опубликованном 15 сентября 2005 г., который полностью включен в настоящее описание путем ссылки. В одном осуществлении настоящее изобретение направлено на создание способа получения соединения формулы (I-A) и дополнительно направлено на создание способа получения соединения формулы (I-B) также известного как метиловый диметилфенил)пропионовой кислоты. Настоящее изобретение дополнительно направлено на создание способа получения соединения формулы (II-A) либо его фармацевтически приемлемой соли и дополнительно направлено на создание способа получения соединения формулы (II-B) также известного как (S)-2-трет-бутоксикарбониламино-3-(4-карбамоил-2,6-диметилфенил)пропионовая кислота, либо его фармацевтически приемлемой соли. В одном из осуществлений настоящего изобретения защитную группу PG1 выбирают из группы, состоящей из Boc и Cbz. В другом осуществлении настоящего изобретения защитная группа PG представляет собой Boc. В одном из осуществлений настоящего изобретения R0 выбирают из группы, состоящей из С 1-4 алкила и бензила. В другом осуществлении настоящего изобретения R0 выбирают из группы, состоящей из метила, этила, изопропила, т-бутила и бензила. В другом осуществлении настоящего изобретенияR0 представляет собой метил или бензил. В другом осуществлении настоящего изобретения R0 представляет собой метил. В другом осуществлении настоящего изобретения R0 отличен от атома водорода. В одном из осуществлений настоящего изобретения R6 выбирают из группы, состоящей из водорода и метила. В другом осуществлении настоящего изобретения R6 представляет собой водород. В одном из осуществлений настоящего изобретения R4 выбирают из группы, состоящей из С 6-10 арила и гетероарила; причем указанный гетероарил выбирают из группы, состоящей из фурила, тиенила, пирролила, оксазолила, тиазолила, имидазолила, пиразолила, пиридинила, пиримидинила, пиразинила, индолила, изоиндолила, индолинила, бензофурила, бензотиенила, бензимидазолила, бензтиазолила,бензоксазолила, хинолизинила, хинолинила, изохинолинила и хиназолинила; и R4 необязательно замещен 1-3 заместителями, независимо выбранными из группы, состоящей из C1-6 алкила (причем указанный С 1-6 алкил необязательно замещен амино, С 1-6 алкиламино или ди(С 1-6 алкил)аминогруппой); С 1-6 алкокси; фенил-С 1-6 алкокси; фенил-C1-6 алкилкарбонилокси (причем С 1-6 алкильный фрагмент необязательно замещен аминогруппой; при этом фенильный фрагмент фенил-C1-6 алкилкарбонилоксильного заместителя необязательно замещен С 1-6 алкилом, С 1-6 алкокси, галогеном, циано, амино или гидроксигруппой); неконденсированного 5-членного гетероарил-C1-6 алкилкарбонилокси; неконденсированного 5-членного гетероарила; гидрокси; галогена; аминосульфонила; формиламино; аминокарбонила; С 1-6 алкиламинокарбонила (где С 1-6 алкильный фрагмент необязательно замещен амино, С 1-6 алкиламино или (C1-6 алкил)2 аминогруппой); ди(С 1-6 алкил)аминокарбонила (причем каждый С 1-6 алкильный фрагмент необязательно замещен амино, C1-6 алкиламино или (С 1-6 алкил)2 аминогруппой); гетероциклилкарбонила(причем указанный гетероциклил представляет собой 5-7-членное азотсодержащее кольцо и указанный гетероциклил присоединен к карбонильному атому углерода через атом азота); карбокси и циано. В другом осуществлении настоящего изобретения R4 представляет собой С 6-10 арил, который необязательно замещен 1-3 заместителями, независимо выбранными из группы, состоящей из (C1-3)алкила,(С 1-6)алкокси,фенил(С 1-6)алкокси; гидрокси; галогена; формиламино; аминокарбонила; С 1-6 алкиламинокарбонила; (С 1-6 алкил)2 аминокарбонила; гетероциклилкарбонила, причем гетероциклил представляет собой 5-7-членное азотсодержащее кольцо и указанный гетероциклил присоединен к карбонильному атому углерода через атом азота; карбокси и циано; при условии, что не более чем один из заместителей представляет собой формиламино,аминокарбонил,C1-6 алкиламинокарбонил,(С 1-6 алкил)2 аминокарбонил, гетероциклилкарбонил, гидрокси, карбокси или фенилсодержащий заместитель. В другом осуществлении настоящего изобретения R4 представляет собой фенил, который необязательно замещен 1-3 заместителями, независимо выбранными из группы, состоящей из (С 1-3)алкила,(С 1-3)алкокси, фенил(С 1-3)алкокси, гидрокси, С 1-6 алкиламинокарбонила и аминокарбонила; при условии,что не более чем один из заместителей представляет собой аминокарбонил, С 1-6 алкиламинокарбонил,гидрокси или фенилсодержащий заместитель. В другом осуществлении настоящего изобретения R4 представляет собой фенил, замещенный в 4-м положении гидрокси, С 1-3 алкиламинокарбонилом или аминокарбонилом и дополнительно необязательно замещенный 1-2 заместителями, независимо выбранными из группы, состоящей из метила, метокси и бензилокси. В другом осуществлении настоящего изобретения R4 представляет собой фенил, замещен-4 018913 ный в 4-м положении гидрокси, С 1-3 алкиламинокарбонилом или аминокарбонилом, и дополнительно необязательно замещенный 1-2 метильными заместителями. В другом осуществлении настоящего изобретения R4 представляет собой фенил, замещенный в 4-м положении гидрокси, С 1-3 алкиламинокарбонилом или аминокарбонилом и дополнительно замещенный метильными заместителями во 2- и 6-м положении. В одном из осуществлений настоящее изобретение направлено на создание способа получения соединения формулы (I), в котором отмеченный знаком стереоцентр присутствует в виде энантиомерного избытка (R)-энантиомера. В другом осуществлении настоящее изобретение направлено на создание способа получения соединения формулы (I), в котором отмеченный знаком стереоцентр присутствует в виде энантиомерного избытка (S)-энантиомера. Если иное не оговорено особо, термин "алкил", используемый в настоящем изобретении самостоятельно или в качестве части названия заместителя, относится к линейной или разветвленной углеродной цепи, содержащей от 1 до 8 атомов углерода либо любое число атомов углерода в пределах означенного интервала. Используемый в настоящем изобретении термин "алкокси" относится к заместителю типа-О-алкил, где "алкил" применяется в оговоренном выше смысле. Алкильная и алкоксильная цепи могут быть замещены на одном атоме углерода. В заместителях с несколькими алкильными группами, таких как ди(С 1-6 алкил)амино-, С 1-6 алкильные группы указанной диалкиламиногруппы могут быть одинаковыми или различными. Используемый в настоящем изобретении термин "гетероциклил" относится к 5-7-членному неароматическому кольцу, в котором от 1 до 2 членов представляют собой атомы азота, либо к 5-7-членному неароматическому кольцу, в котором ноль, один или два члена представляют собой атомы азота и до двух членов представляют собой атомы кислорода или серы; причем указанное кольцо необязательно содержит от нуля до одной ненасыщенной связи, и, необязательно, если кольцо состоит из 6 или 7 членов, оно содержит до двух ненасыщенных связей. Используемый в настоящем изобретении термин "гетероциклил" включает 5-7-членное моноциклическое гетероциклическое кольцо, конденсированное с бензольным кольцом (бензоконденсированный гетероциклил), 5- или 6-членным гетероароматическим кольцом (содержащим один из О, S или N и, необязательно, дополнительно еще один атом азота), 5-7 членным циклоалкильным или циклоалкенильным кольцом, 5-7-членным гетероциклильным кольцом (в определенном выше смысле, за исключением наличия дополнительного конденсированного кольца), либо конденсированное по одному атому углерода циклоалкильного, циклоалкенильного или гетероциклильного кольца с образованием спирофрагмента. Для соединений, составляющих предмет настоящего изобретения, кольцевые атомы углерода, образующие указанное гетероциклильное кольцо, всегда полностью насыщены. Другие соединения в соответствии с настоящим изобретением могут иметь частично насыщенное гетероциклильное кольцо. Используемый в настоящем изобретении термин "гетероциклил" дополнительно включает 5-7-членный моноциклический гетероциклил с мостиковыми группами, представляющими собой бициклические кольца. Подобные соединения не считаются полностью ароматическими и не включаются в понятие гетероароматического соединения. Примеры гетероциклильных групп без ограничений включают следующие группы: пирролинил (включая 2H-пиррол, 2-пирролинил или 3-пирролинил), пирролидинил, 2-имидазолинил, имидазолидинил, 2-пиразолинил, пиразолидинил, пиперидинил, морфолинил, тиоморфолинил и пиперазинил. Используемый в настоящем изобретении термин "арил" относится к ненасыщенному ароматическому моноциклическому кольцу из 6 атомов углерода или к ненасыщенному ароматическому полициклическому кольцу из 10-14 атомов углерода. Примеры подобных арильных колец включают фенил, нафталенил или антраценил. Предпочтительными арильными группами для практического осуществления настоящего изобретения являются фенил и нафталенил. Используемый в настоящем изобретении термин "гетероарил" относится к 5- или 6-членному ароматическому кольцу, причем указанное кольцо состоит из атомов углерода и содержит по меньшей мере один гетероатом. Соответствующие целям настоящего изобретения гетероатомы включают N, O или S. В случае 5-членных колец указанное гетероарильное кольцо содержит один атом из группы N, O, S и может дополнительно содержать до трех атомов азота. В случае 6-членных колец указанное гетероарильное кольцо может содержать от одного до трех атомов азота. В том случае, когда указанное 6-членное кольцо содержит три атома азота, не более двух атомов азота находятся в соседних положениях. Кроме того,гетероарильное кольцо может необязательно быть конденсировано с бензольным кольцом (бензоконденсированный гетероарил), 5- или 6-членным гетероарильным кольцом (содержащим один из O, S, N и,необязательно, дополнительно еще один атом азота), 5-7-членным циклоалкильным кольцом или 5-7-членным гетероциклильным кольцом (в определенном выше смысле, за исключением наличия дополнительного конденсированного кольца). Примеры гетероарильных групп без ограничений включают следующие группы: фурил, тиенил, пирролил, оксазолил, тиазолил, имидазолил, пиразолил, изоксазолил,изотиазолил, оксадиазолил, триазолил, тиадиазолил, пиридинил, пиридазинил, пиримидинил и пиразинил; конденсированные гетероарильные группы включают индолил, изоиндолил, индолинил, бензофурил, бензотиенил, индазолил, бензимидазолил, бензтиазолил, бензоксазолил, бензизоксазолил, бензотиадиазолил, бензотриазолил, хинолизинил, хинолинил, изохинолинил и хиназолинил. Используемый в настоящем изобретении термин "арилалкил" означает алкильную группу, замещеннуюарильной группой (например, бензил или фенэтил). Сходным образом используемый в настоящем изобретении термин "арилалкокси" означает алкоксильную группу, замещенную арильной группой(например, бензилокси). Используемый в настоящем изобретении термин "галоген" относится к фтору, хлору, брому и йоду. Заместители, замещенные галогенами по нескольким положениям, замещаются таким образом, чтобы получить в итоге устойчивое соединение. Если термин "алкил" или "арил" либо любой из образованных от этих корней префиксов появляется в названии заместителя (например, арилалкил, алкиламино), при этом подразумевается, что все оговоренные выше ограничения для терминов "алкил" и "арил" переносятся и на производные названия. Указание числа атомов углерода (например, C1-C6) относится независимо к числу атомов углерода в алкильном фрагменте или алкильной части более крупного заместителя, в названии которого корень алкил используется в качестве префикса. Для алкильных и алкоксильных заместителей указанное число атомов углерода включает все независимые члены приведенного диапазона по отдельности, а также любые сочетания диапазонов в пределах указанных границ. Например, указатель "С 1-6 алкил" включает метил,этил, пропил, бутил, пентил и гексил по отдельности, а также поддиапазоны указанного диапазона (например, C1-2, C1-3, C1-4, C1-5, C2-6, C3-6, C4-6, C5-6, C2-5 и т.д.). Если некоторая группа описывается как "замещенная" (например, алкил, циклоалкил, арил, гетероарил, гетероциклоалкил и т.д.), указанная группа может нести один или более заместителей, предпочтительно от одного до пяти заместителей, более предпочтительно от одного до трех заместителей, наиболее предпочтительно от одного до двух заместителей, независимо выбираемых из приведенного списка возможных заместителей. По отношению к заместителям термин "независимо" означает, что при возможности ввести более одного из подобных заместителей вводимые заместители могут быть одинаковы или различны. Используемый в настоящем изобретении знак означает наличие стереогенного центра. В случаях, когда соединения в соответствии с настоящим изобретением имеют по меньшей мере один хиральный центр, они могут соответственно существовать в форме энантиомеров. В тех случаях, когда соединения обладают двумя или более хиральными центрами, они дополнительно могут существовать в форме диастереомеров. Необходимо понимать, что все подобные изомеры и их смеси попадают в рамки настоящего изобретения. Предпочтительно, если соединение присутствует в форме энантиомера, указанный энантиомер присутствует в энантиомерном избытке не менее приблизительно 80%, более предпочтительно в энантиомерном избытке не менее приблизительно 90%, еще более предпочтительно в энантиомерном избытке не менее приблизительно 95%, еще более предпочтительно в энантиомерном избытке не менее приблизительно 98%, наиболее предпочтительно в энантиомерном избытке не менее приблизительно 99%. Сходным образом, когда соединение присутствует в форме диастереомера, указанный диастереомер присутствует в диастереомерном избытке не менее приблизительно 80%, более предпочтительно в диастереомерном избытке не менее приблизительно 90%, еще более предпочтительно в диастереомерном избытке не менее приблизительно 95%, еще более предпочтительно в диастереомерном избытке не менее приблизительно 98%, наиболее предпочтительно в диастереомерном избытке не менее приблизительно 99%. Кроме того, некоторые из кристаллических форм соединений в соответствии с настоящим изобретением могут существовать в виде полиморфов, и в таком качестве они также считаются попадающими в рамки действия настоящего изобретения. Кроме того, некоторые из описываемых соединений могут образовывать сольваты с водой (т.е. гидраты) или широко распространенные органические растворители,при этом считается, что такие сольваты также попадают в рамки действия настоящего изобретения. В рамках используемой в раскрытии настоящего изобретения стандартной номенклатуры первой указывается концевая часть описываемой боковой цепи, затем перечисляются следующие функциональные группы в направлении к точке присоединения заместителя. Так, например, описание заместителя Следующие сокращения использованы в спецификации, в частности в схемах и примерах. Если иное не оговорено особо, используемый в настоящем изобретении термин "по существу чистое соединение" означает, что мольная доля примесей в выделенном соединении составляет менее чем приблизительно 5 мол.%, предпочтительно менее чем приблизительно 2 мол.%, более предпочтительно менее чем приблизительно 0,5 мол.%, наиболее предпочтительно менее чем приблизительно 0,1 мол.%. В одном из осуществлений настоящего изобретения соединение формулы (I) получено в виде по существу чистого соединения. В одном из осуществлений настоящего изобретения соединение формулы (I-A) получено в виде по существу чистого соединения. В другом осуществлении настоящего изобретения соединение формулы (I-B) получено в виде по существу чистого соединения. В одном из осуществлений настоящего изобретения соединение формулы (II-A) получено в виде по существу чистого соединения. В другом осуществлении настоящего изобретения соединение формулы (II-B) получено в виде по существу чистого соединения. Если иное не оговорено особо, термин "по существу свободное от соответствующей солевой формы(форм)", используемый в настоящем изобретении для описания соединений формулы (I), означает, что мольная доля соответствующей солевой формы (форм) в выделенном свободном основании соединения формулы (I) составляет менее чем приблизительно 5 мол.%, предпочтительно менее чем приблизительно 2 мол.%, более предпочтительно менее чем приблизительно 0,5 мол.%, наиболее предпочтительно менее чем приблизительно 0,1 мол.%. В одном из осуществлений настоящего изобретения соединение формулы (I) получено в форме, по существу свободной от соответствующей солевой формы (форм). В одном из осуществлений настоящего изобретения соединение формулы (II-A) получено в форме, по существу свободной от соответствующей солевой формы (форм). В другом осуществлении настоящего изобретения соединение формулы (II-B) получено в форме, по существу свободной от соответствующей солевой формы (форм). Многократно используемые в настоящем письменном изложении такие термины, как "взаимодействует" и "подвергают взаимодействию", в целях настоящего изложения относятся к химическому соединению или форме, которые представляют собой:(а) указанное в тексте описания химическое соединение или форму и(б) любую из возможных форм данного химического соединения, в которых оно может присутствовать в среде, рассматриваемой при описании соединения. Специалист в данной области определит, что, если не указано иное, для получения необходимого продукта все стадии реакции проводятся согласно известным способам в надлежащих условиях. Специалист в данной области дополнительно определит, что в представленном описании и пунктах формулы изобретения, когда некоторый реагент или класс/тип реагента (например, основание, растворитель и т.д.) упоминается более чем для одной стадии процесса, индивидуальные реагенты выбирают независимо для каждой из стадий, и они могут совпадать или различаться. Например, если при описании двух стадий некоторого процесса в качестве реагента указывается органическое или неорганическое основание, органическое или неорганическое основание, выбираемое для первой стадии процесса, может совпадать с или отличаться от органического или неорганического основания, используемого для второй стадии. Далее специалист в данной области определит, что если некоторая реакционная стадия в соответствии с настоящим изобретением может быть проведена в различных растворителях или системах растворителей, то указанная реакционная стадия может также быть проведена и в смеси соответствующих растворителей или систем растворителей. Специалист в данной области дополнительно определит, что если две последовательные стадии реакции или процесса проводятся без выделения промежуточного продукта(т.е. продукта первой из двух последовательных стадий реакции или процесса), то указанные первая и вторая стадии реакции или процесса могут проводиться в одном и том же растворителе или системе растворителей; или, альтернативно, они могут проводиться в разных растворителях или системах растворителей после замены растворителя, которая может быть выполнена любыми известными способами. Для большей краткости описания некоторые из используемых в настоящем изобретении количественных выражений не сопровождаются модификатором "приблизительно". При этом подразумевается,что вне зависимости от того, используется ли явно термин "приблизительно" или нет, каждое приводимое в настоящем изобретении количество подразумевает действительное численное значение, а также подразумевает разумное приближение к таковому численному значению, основанное на имеющихся у специалиста знаниях, включая приближение, основанное на экспериментальных условиях и/или измерениях, имеющих отношение к таковому численному значению. Для большей краткости описания ряд приводимых в данном изобретении количественных выражений дается в виде диапазона от приблизительно количества X до приблизительно количества Y. Подразумевается, что при указании диапазона значений указанный диапазон не ограничивается указанными верхней и нижней границами, но включает полный диапазон от приблизительно количества X до приблизительно количества Y или любой входящий в него меньший диапазон. Примеры соответствующих целям настоящего изобретения растворителей, оснований, температур и иных условий проведения реакции и используемых компонентов даются в приведенных ниже подробных описаниях. Специалист в данной области определит, что список указанных примеров не призван и ни в коей мере не должен восприниматься как ограничение сущности настоящего изобретения, изложенного в приведенных далее пунктах формулы изобретения. Если иное не оговорено особо, используемый в настоящем изобретении термин "уходящая группа" означает заряженный или незаряженный атом или группу атомов, уходящие в ходе реакции замещения или вытеснения. Соответствующие примеры уходящих групп без ограничений включают Cl, Br, I, мезилат, тозилат и т.п. В ходе процессов получения соединений, составляющих предмет настоящего изобретения, может возникнуть необходимость в защите чувствительных или реакционноспособных групп на любой из рассматриваемых молекул. Для этих целей могут использоваться соответствующие защитные группы, например, описанные в книгах Protective Groups in Organic Chemistry, ed. J.F.W. McOmie, Plenum Press,1973 и T.W. GreeneP.G.M. Wuts, Protective Groups in Organic Synthesis, John WileySons, 1991. Введенные защитные группы могут быть в последующем удалены на любой удобной для этого стадии с применением известных специалистам способов. Если иное не оговорено особо, используемый в настоящем изобретении термин "защитная группа для атома азота" относится к некоторой группе, которая может быть присоединена к атому азота для защиты указанного атома азота от участия в реакции и которая может быть легко снята после проведения реакции. Соответствующие целям настоящего изобретения защитные группы для атома азота включают карбаматы - группы с общей формулой -C(O)O-R, где R представляет собой, например, метил, этил, тбутил, бензил, фенилэтил, CH2=CH-CH2- и т.п.; амиды - группы с общей формулой -C(O)-R', где R' представляет собой, например, метил, фенил, трифторметил и т.п.; N-сульфонильные производные - группы с общей формулой -SO2-R", где R" представляет собой, например, толил, фенил, трифторметил, 2,2,5,7,8 пентаметилхроман-6-ил-, 2,3,6-триметил-4-метоксибензол и т.п. Другие, соответствующие целям настоящего изобретения защитные группы для атома азота могут быть найдены в таких руководствах, какT.W. GreeneP.G.M. Wuts, Protective Groups in Organic Synthesis, John WileySons, 1991. Специалист в данной области определит, что если некоторая реакционная стадия в соответствии с настоящим изобретением может быть проведена в различных растворителях или системах растворителей, то указанная реакционная стадия может также быть проведена и в смеси соответствующих растворителей или систем растворителей. В тех случаях, когда способы получения соединений в соответствии с данным изобретением приводят к образованию смеси стереоизомеров, эти изомеры могут быть разделены при помощи стандартных способов, таких как препаративная хроматография. Соединения могут быть получены в форме рацематов либо индивидуальные энантиомеры могут быть получены в результате энантиоспецифического синтеза либо посредством разделения. Соединения могут, например, быть разделены на составляющие их энантиомеры при помощи стандартных способов, таких как формирование диастереомерных пар путем образования солей с оптически активными кислотами, как, например, (-)-ди-п-толуоил-D-виннокаменная кислота и/или (+)-ди-п-толуоил-L-виннокаменная кислота с последующей фракционной кристаллизацией и восстановлением свободного основания. Соединения могут также быть разделены с помощью образова-8 018913 ния диастереомерных эфиров или амидов с последующим хроматографическим разделением и удалением хирального партнера. Альтернативно, такие соединения могут быть разделены при помощи хиральной колонки для ВЭЖХ. Кроме того, хиральная ВЭЖХ в сравнении со стандартом может также применяться для определения процентного энантиомерного избытка (%ее). Энантиомерный избыток рассчитывается следующим образом: где R моль и S моль представляют собой мольные доли R- и S-энантиомеров, так чтоR моль+S моль=1. Альтернативно, энантиомерный избыток может быть следующим образом рассчитан из величин удельного вращения искомого энантиомера и полученной смеси: Для использования в медицинских целях соли соединений, составляющих предмет настоящего изобретения, относятся к нетоксичным "фармацевтически приемлемым солям". Однако для получения соединений, составляющих предмет настоящего изобретения, либо их фармацевтически приемлемых солей могут применяться и другие соли. Соответствующие целям настоящего изобретения фармацевтически приемлемые соли включают соли присоединения к кислотам, которые могут быть получены, например,путем смешивания раствора соединения с раствором фармацевтически приемлемой кислоты, такой как соляная, серная, фумаровая, малеиновая, янтарная, уксусная, бензойная, лимонная, винная, угольная и фосфорная кислоты. Далее, если в соединении в соответствии с настоящим изобретением присутствует кислотный фрагмент, соответствующие фармацевтически приемлемые соли такого соединения могут включать соли щелочных металлов, например соли натрия или калия; соли щелочно-земельных металлов, например соли кальция или магния; и соли с соответствующими органическими лигандами, например четвертичные аммониевые соли. Так, типичные примеры фармацевтически приемлемых солей включают следующие соли: ацетаты, бензолсульфонаты, бензоаты, бикарбонаты, бисульфаты, битартраты, бораты, бромиды, кальция эдетаты, камсилаты, карбонаты, хлориды, клавуланаты, цитраты, дигидрохлориды, эдетаты, эдисилаты, эстолаты, эсилаты, фумараты, глуцептаты, глюконаты, глутаматы, гликоллиларсанилаты, гексилрезорцинаты, гидрабамины, гидробромиды, гидрохлориды, гидроксинафтоаты,йодиды, изотионаты, лактаты, лактобионаты, лаураты, малаты, малеаты, манделаты, мезилаты, метилбромиды, метилнитраты, метилсульфаты, мукаты, напсилаты, нитраты, N-метилглюкамина аммониевые соли, олеаты, памоаты (эмбонаты), пальмитаты, пантотенаты, фосфаты/дифосфаты, полигалактуронаты,салицилаты, стеараты, сульфаты, субацетаты, сукцинаты, таннаты, тартраты, теоклаты, тозилаты, триэтиодиды и валераты. Типичные кислоты, которые могут применяться для получения фармацевтически приемлемых солей, включают следующие кислоты: уксусную, 2,2-дихлоруксусную, ацилированные аминокислоты,адипиновую, альгиновую, аскорбиновую, L-аспарагиновую, бензолсульфоновую, бензойную,4-ацетамидобензойную, (+)-камфорную, камфорсульфоновую, (+)-(1S)-камфор-10-сульфоновую,каприновую, капроновую, каприловую, коричную, лимонную, цикламовую, додецилсерную,этан-1,2-дисульфоновую, этансульфоновую, 2-гидроксиэтансульфоновую, муравьиную, фумаровую, галактаровую, гентизиновую, глюкогептоновую, D-глюконовую, D-глюкороновую, L-глутаминовую,-оксоглутаровую, гликолевую, гипуровую, бромисто-водородную, соляную, (+)-L-молочную,-DL-молочную, лактобионовую, малеиновую, (-)-L-яблочную, малоновую, -DL-миндальную, метансульфоновую, нафталин-2-сульфоновую, нафталин-1,5-дисульфоновую, 1-гидрокси-2-нафтойную,никотиновую, азотную, олеиновую, оротовую, щавелевую, пальмитиновую, памовую, фосфорную,L-пироглутаминовую, салициловую, 4-аминосалициловую, себациновую, стеариновую, янтарную, серную, дубильную, (+)-L-винную, роданисто-водородную, п-толуолсульфоновую и ундеценовую кислоты. Типичные основания, которые могут применяться для получения фармацевтически приемлемых солей, включают следующие основания: аммиак, L-аргинин, бенетамин, бензатин, гидроксид кальция, холин, динол, диэтаноламин, диэтиламин, 2-(диэтиламино)этанол, этаноламин, этилендиамин,N-метилглюкамин, гидрабамин, 1 Н-имидазол, L-лизин, гидроксид магния, 4-(2-гидроксиэтил)морфолин,пиперазин, гидроксид калия, 1-(2-гидроксиэтил)пирролидин, вторичные амины, гидроксид натрия, триэтаноламин, трометамин и гидроксид цинка. Настоящее изобретение направлено на создание способа получения соединений формулы (I), более подробно показанного на схеме 1. В соответствии со схемой 1 соответствующим образом замещенное соединение формулы (X), известное соединение или соединение, полученное известными способами, где PG1 представляет собой соответствующим образом выбранную защитную группу для атома азота, такую как Boc, Cbz и т.п.,предпочтительно Boc подвергается взаимодействию с цинком, предпочтительно с цинковой пылью; причем цинк предпочтительно присутствует в количестве в диапазоне от приблизительно 0,5 до приблизительно 3,0 мол.экв., более предпочтительно присутствует в количестве в диапазоне от приблизительно 0,5 до приблизительно 1,5 мол.экв., более предпочтительно в количестве приблизительно 1,1 мол.экв.; в присутствии источника йода, предпочтительно йода; причем источник йода предпочтительно присутствует в количестве в диапазоне от приблизительно 0,1 до приблизительно 1,0 мол.экв., более предпочтительно присутствует в количестве в диапазоне от приблизительно 0,1 до приблизительно 0,5 мол.экв.,более предпочтительно в количестве приблизительно 0,3 мол.экв., более предпочтительно в каталитическом количестве, достаточном для активации цинка; в первом органическом растворителе или смеси растворителей, причем первый органический растворитель нереакционноспособен по отношению к источнику йода и представляет собой, например, DMAc, смесь DMAc и 2-метил-THF, THF, толуол, DMF и т.п., более предпочтительно DMAc; предпочтительно при температуре в диапазоне от приблизительно-20 до приблизительно 10C, более предпочтительно при температуре менее чем приблизительно 10C,более предпочтительно при температуре приблизительно -8C; с получением соответствующего соединения формулы (XI). Предпочтительно соединение формулы (XI) не выделяют из реакционной смеси. Предпочтительно цинк и источник йода смешивают перед добавлением к соединению формулы (X) для активации цинка. Соединение формулы (XI) затем подвергают взаимодействию с соответствующим образом замещенным соединением формулы (XII), где LG1 представляет собой соответствующим образом выбранную уходящую группу, такую как Cl, Br, I и т.п., предпочтительно Br; причем соединение формулы (XII) предпочтительно присутствует в количестве в диапазоне от приблизительно 0,1 до приблизительно 3,0 мол.экв., более предпочтительно в количестве в диапазоне от приблизительно 0,25 до приблизительно 1,0 мол.экв., более предпочтительно в количестве в диапазоне от приблизительно 0,5 до приблизительно 1,1 мол.экв.; в присутствии палладиевого катализатора и фосфиновой лигандной системы, таких как Pd2(dba)3 в сочетании с P(o-tol)3, хлорид палладия в сочетании с PPh3, Pd(PPh3)2Cl2, Pd(PPh3)4 и т.п.,более предпочтительно Pd2(dba)3 в сочетании с P(o-tol)3, где палладиевый катализатор и фосфиновая лигандная система предпочтительно присутствуют в каталитическом количестве; во втором органическом растворителе или смеси растворителей, таком как DMAc, смесь DMAc и 2-метил-THF, THF, DMF, толуол и т.п., более предпочтительно DMAc; предпочтительно в том же растворителе, который использовался на предыдущей стадии; предпочтительно при температуре в диапазоне от приблизительно 50 до приблизительно 100C, более предпочтительно при температуре приблизительно 80C; с получением соответствующего соединения формулы (I). Предпочтительно соединение (XI) добавляют к смеси соединения формулы (XII), палладиевого катализатора и фосфинового агента. Настоящее изобретение дополнительно направлено на создание способа получения соединений формулы (I-A), более подробно показанного на схеме 2. Схема 2 В соответствии со схемой 2 соответствующим образом замещенное соединение формулы (X-A), известное соединение или соединение, полученное известными способами, где PG1 представляет собой соответствующим образом выбранную защитную группу для атома азота, такую как Boc, Cbz и т.п.,предпочтительно Boc; подвергают взаимодействию с цинком, предпочтительно с цинковой пылью; причем цинк предпочтительно присутствует в количестве в диапазоне от приблизительно 0,5 до приблизительно 3,0 мол.экв., более предпочтительно присутствует в количестве в диапазоне от приблизительно 0,5 до приблизительно 1,5 мол.экв., более предпочтительно в количестве приблизительно 1,1 мол.экв.; в присутствии источника йода, предпочтительно йода; причем источник йода предпочтительно присутствует в количестве в диапазоне от приблизительно 0,1 до приблизительно 1,0 мол.экв., более предпочтительно присутствует в количестве в диапазоне от приблизительно 0,1 до приблизительно 0,5 мол.экв.,более предпочтительно в количестве приблизительно 0,3 мол.экв., более предпочтительно в каталитическом количестве, достаточном для активации цинка; в первом органическом растворителе или смеси растворителей, причем первый органический растворитель нереакционноспособен по отношению к источнику йода и представляет собой, например, DMAc, смесь DMAc и 2-метил-THF, THF, толуол, DMF и т.п., более предпочтительно DMAc; предпочтительно при температуре в диапазоне от приблизительно-20 до приблизительно 10C, более предпочтительно при температуре менее чем приблизительно 10C,более предпочтительно при температуре приблизительно -8C; с получением соответствующего соединения формулы (XI-A). Предпочтительно соединение формулы (XI-A) не выделяют из реакционной смеси. Предпочтительно цинк и источник йода смешивают перед добавлением к соединению формулы(Х-А) для активации цинка. Соединение формулы (XI-A) затем подвергают взаимодействию с соответствующим образом замещенным соединением формулы (XII-А), где LG1 представляет собой соответствующим образом выбранную уходящую группу, такую как Cl, Br, I и т.п., предпочтительно Br; причем соединение формулы(XII-A) предпочтительно присутствует в количестве в диапазоне от приблизительно 0,1 до приблизительно 3,0 мол.экв., более предпочтительно в количестве в диапазоне от приблизительно 0,25 до приблизительно 1,0 мол.экв., более предпочтительно в количестве в диапазоне от приблизительно 0,5 до приблизительно 1,1 мол.экв.; в присутствии палладиевого катализатора и фосфиновой лигандной системы,таких как Pd2(dba)3 в сочетании с P(o-tol)3, хлорид палладия в сочетании с PPh3, Pd(PPh3)2Cl2, Pd(PPh3)4 и т.п., более предпочтительно Pd2(dba)3 в сочетании с P(o-tol)3, где палладиевый катализатор и фосфиновая лигандная система предпочтительно присутствуют в каталитическом количестве; во втором органическом растворителе или смеси растворителей, таком как DMAc, смесь DMAc и 2-метил-THF, THF, DMF,толуол и т.п., более предпочтительно DMAc; предпочтительно в том же растворителе, который использовался на предыдущей стадии; предпочтительно при температуре в диапазоне от приблизительно 50 до приблизительно 100C, более предпочтительно при температуре приблизительно 80C; с получением соответствующего соединения формулы (I-A). Предпочтительно соединение (XI-A) добавляют к смеси соединения формулы (XII-A), палладиевого катализатора и фосфинового агента. Настоящее изобретение дополнительно направлено на создание способа получения соединений формулы (I-B), более подробно показанного на схеме 3. Схема 3 В соответствии со схемой 3 соответствующим образом замещенное соединение формулы (X-B), известное соединение или соединение, полученное известными способами, подвергают взаимодействию с цинком, предпочтительно с цинковой пылью; причем цинк предпочтительно присутствует в количестве в диапазоне от приблизительно 0,5 до приблизительно 3,0 мол.экв., более предпочтительно присутствует в количестве в диапазоне от приблизительно 0,5 до приблизительно 1,5 мол.экв., более предпочтительно в количестве приблизительно 1,1 мол.экв.; в присутствии источника йода, предпочтительно йода; причем источник йода предпочтительно присутствует в количестве в диапазоне от приблизительно 0,1 до приблизительно 1,0 мол.экв., более предпочтительно присутствует в количестве в диапазоне от приблизительно 0,1 до приблизительно 0,5 мол.экв., более предпочтительно в количестве приблизительно 0,3 мол.экв., более предпочтительно в каталитическом количестве, достаточном для активации цинка; в первом органическом растворителе или смеси растворителей, причем первый органический растворитель нереакционноспособен по отношению к источнику йода и представляет собой, например, DMAc, смесьDMAc и 2-метил-THF, THF, толуол, DMF и т.п., более предпочтительно DMAc; предпочтительно при температуре в диапазоне от приблизительно -20 до приблизительно 10C, более предпочтительно при температуре менее чем приблизительно 10C, более предпочтительно при температуре приблизительно 8C; с получением соответствующего соединения формулы (XI-B). Предпочтительно соединение формулы (XI-B) не выделяют из реакционной смеси. Предпочтительно цинк и источник йода смешивают перед добавлением к соединению формулы (X-B) для активации цинка. Соединение формулы (XI-B) затем подвергают взаимодействию с соответствующим образом замещенным соединением формулы (XII-В), причем соединение формулы (XII-B) предпочтительно присутствует в количестве в диапазоне от приблизительно 0,1 до приблизительно 3,0 мол.экв., более предпочтительно в количестве в диапазоне от приблизительно 0,25 до приблизительно 1,0 мол.экв., более предпочтительно в количестве в диапазоне от приблизительно 0,5 до приблизительно 1,1 мол.экв.; в присутствии палладиевого катализатора и фосфиновой лигандной системы, таких как Pd2(dba)3 в сочетании сPd2(dba)3 в сочетании с P(o-tol)3, где палладиевый катализатор и фосфиновая лигандная система предпочтительно присутствуют в каталитическом количестве; во втором органическом растворителе или смеси растворителей, таком как DMAc, смесь DMAc и 2-метил-THF, THF, DMF, толуол и т.п., более предпочтительно DMAc; предпочтительно в том же растворителе, который использовался на предыдущей стадии; предпочтительно при температуре в диапазоне от приблизительно 50 до приблизительно 100C, более предпочтительно при температуре приблизительно 80C; с получением соответствующего соединения формулы (I-B). Предпочтительно соединение формулы (XI-B) добавляют к смеси соединения формулы (XII-B), палладиевого катализатора и фосфинового агента. Настоящее изобретение дополнительно направлено на создание способа получения соединений формулы (II-A), более подробно показанного на схеме 4. Схема 4 В соответствии со схемой 4 соответствующим образом замещенное соединение формулы (I-A), гдеR0 предпочтительно отличен от водорода и где PG1 представляет собой соответствующим образом выбранную защитную группу для атома азота, такую как Boc, Cbz и т.п., предпочтительно PG1 представляет собой Boc, подвергается взаимодействию с соответствующим образом выбранным окисляющим агентом,таким как перекись водорода, LiOH, LiOOH и т.п., предпочтительно 30% перекисью водорода; причем окисляющий агент предпочтительно присутствует в избыточном количестве; в присутствии неорганического основания, такого как карбонат калия, карбонат натрия, перкарбонат натрия и т.п., предпочтительно карбоната калия; причем неорганическое основание предпочтительно присутствует в количестве в диапазоне от приблизительно 1,0 до приблизительно 3,0 мол.экв., более предпочтительно в количестве приблизительно 1,6 мол.экв.; в третьем органическом растворителе, таком как DMSO, DMF, DMAc, NMP и т.п., предпочтительно DMSO; при температуре в диапазоне от приблизительно комнатной температуры до приблизительно 60C, предпочтительно при температуре приблизительно 45C; с получением соответствующего соединения формулы (II-A). В одном из осуществлений настоящее изобретение направлено на создание способа получения соединений формулы (II-B), более подробно показанного на схеме 5. Схема 5 В соответствии со схемой 5 соответствующим образом замещенное соединение формулы (I-B) подвергают взаимодействию с соответствующим образом выбранным окисляющим агентом, таким как перекись водорода, LiOH, LiOOH и т.п., предпочтительно 30% перекисью водорода; причем окисляющий агент предпочтительно присутствует в избыточном количестве; в присутствии неорганического основания, такого как карбонат калия, карбонат натрия, перкарбонат натрия и т.п., предпочтительно карбоната калия; причем неорганическое основание предпочтительно присутствует в количестве в диапазоне от приблизительно 1,0 до приблизительно 3,0 мол.экв., более предпочтительно в количестве приблизительно 1,6 мол.экв.; в третьем органическом растворителе, таком как DMSO, DMF, DMAc, NMP и т.п., предпочтительно DMSO; при температуре в диапазоне от приблизительно комнатной температуры до приблизительно 60C, предпочтительно при температуре приблизительно 45C; с получением соответствующего соединения формулы (II-B). Следующие примеры предлагаются для облегчения понимания сути настоящего изобретения и ни в коей мере не призваны ограничить каким-либо образом рамки данного изобретения, раскрываемого в следующих далее пунктах его формулы. В последующих примерах некоторые синтетические продукты упоминаются как изолированные в виде остатков. Специалист в данной области определит, что термин "остаток" не ограничивает физическое состояние, в котором продукт был получен, и может включать, например, твердый продукт, масло,пену, смолу, сироп и т.п. Пример 1. Получение метилового эфира 2-трет-бутоксикарбониламино-3-(4-карбамоил-2,6 диметилфенил)пропионовой кислоты Стадия A. В четырехгорлую круглодонную колбу объемом 3 л с установленными капельной воронкой, механической мешалкой, нагревательной рубашкой, холодильником и термопарой в атмосфере азота поместили сухой DMAc (300 мл), 2-Me-THF (150 мл), I2 (25,4 г, 0,10 моль) и цинковую пыль (294,3 г, 4,5 моль). Полученную суспензию перемешали до исчезновения красной окраски I2 (приблизительно 2 мин). В процессе добавления наблюдали повышение температуры реакционной смеси (от 23 до 43C). Полученную смесь охладили на бане лед/NaCl до температуры в диапазоне приблизительно от -5 до -2C. Поддерживая реакционную смесь при указанной температуре, в течение 2 ч медленно добавили растворBocйодаланин-ОСН 3 (также известного как метиловый эфир 2-трет-бутоксикарбониламино-3 йодпропионовой кислоты, 658,3 г, 2,0 моль) в смеси DMAc (250 мл) и 2-Me-THF (500 мл). Поддерживая температуру ниже 10C, смесь выдержали в течение приблизительно 1-2 ч на ледяной бане и затем прогрели до температуры приблизительно 15C, получив итоговую смесь. Полученную охлажденную смесь использовали на следующей стадии без дальнейшей обработки. Стадия В. В четырехгорлую круглодонную колбу объемом 5 л с установленными механической мешалкой,нагревательной рубашкой, холодильником, термопарой и вводом для газообразного азота поместили 4-йод-3,5-диметилбензамид (275 г, 1,0 моль), 2-Me-THF (500 мл) и DMA (200 мл). Затем добавилиP(o-tol)3 (24,5 г, 0,08 моль) и Pd2(dba)3 (36,6 г, 0,04 моль) и подогрели полученную суспензию до температуры 45-50C. Поддерживая реакционную смесь при указанной температуре, в течение 1,5-2 ч по трубочке добавили полученную на стадии А смесь. Затем реакционную смесь охладили до комнатной температуры. В смесь добавили окись кремния (275 г) и перемешали полученную суспензию в течение приблизительно 30 мин. Полученный слой окиси кремния промыли 2-Me-THF (3500 мл) и EtOAc (31 л). Полученный раствор погасили 2 л 1,0 н. водной HCl и разделили фазы. Кислотную фазу экстрагировалиEtOAc (21 л). Органическую фазу упарили до объема приблизительно 5,0 л на роторном испарителе и промыли водой (31 л) и затем 50% солевым раствором (2,0 л). Затем растворители отогнали на роторном испарителе и получили твердое вещество серовато-белого цвета. Искомое соединение кристаллизовали из EtOAc (2 л) и гептана (2 л). Через 16 ч полученную смесь на 2 ч поместили на ледяную баню и добавили еще порцию гептана (500 мл) для завершения осаждения. Выпавшее твердое вещество отфильтровали и высушили в вакуумной печи при температуре 55C в течение 48 ч, получив искомое соединение в виде твердого вещества белого цвета.(S)-2-трет-бутоксикарбониламино-3-(4-циано-2,6 В трехгорлую круглодонную колбу объемом 50 мл с установленными капельной воронкой, магнитной мешалкой, нагревательной рубашкой и термопарой в атмосфере азота поместили сухой DMAc(2 мл), I2 (38,1 мг, 0,15 ммоль) и активированную цинковую пыль (промытую 10% HCl, затем H2O и ацетоном) (393 мг, 6 ммоль). Полученную суспензию перемешали при температуре 23C до исчезновения красной окраски I2 (2 мин). Медленно добавили раствор метилового эфира Bocйодаланина (1 г,3 ммоль) в DMAc (2 мл), (температура при этом поднялась с 21 до 29C), перемешали полученную смесь при температуре 80C в течение 0,5-1,0 ч и затем охладили ее до температуры 35C. В полученную смесь последовательно добавили 4-бром-3,5-диметилбензонитрил (315 мг, 1,5 ммоль) в DMAc (6 мл), P(o-tol)3(36,5 мг, 0,12 ммоль) и Pd2(dba)3 (55 мг, 0,06 ммоль). Полученную смесь в течение 1 ч перемешивали при температуре 70C и затем охладили до комнатной температуры. Полученную смесь разбавили EtOAc(15 мл) и профильтровали через целит STAND SUPER-CEL 815520. Полученный раствор в EtOAc погасили 1 н. раствором HCl (40 мл) и экстрагировали этилацетатом (20 мл). Объединенные органические фазы промыли Н 2 О (250 мл) и затем 50% солевым раствором, высушили над Na2SO4, профильтровали и упарили досуха при пониженном давлении, получив твердое вещество коричневого цвета. Искомое соединение кристаллизовали из EtOAc (5 мл) и гептана (40 мл), получив твердое вещество белого цвета. Пример 3. Получение метилового эфира Стадия А. Метиловый эфир Bocйодаланина. В четырехгорлую круглодонную колбу объемом 2 л с установленными вводом для газообразного азота, механической мешалкой, капельной воронкой и термопарой поместили безводный DMAc (500 мл) и йод (16,8 г, 0,06 моль), получив раствор красного цвета. К полученному раствору при перемешивании добавили цинковую пыль (143,9 г, 2,2 моль). После добавления цинковой пыли красная окраска раствора исчезла в течение приблизительно 2 мин, при этом наблюдался разогрев смеси (с 22 до приблизительно 36C). Полученную смесь охладили до температуры -8C и в течение 2 ч без перемешивания медленно добавили раствор метилового эфира N-(трет-бутоксикарбонил)-3-йод-L-аланина (658 г, 2,0 моль) в безводном DMAc (500 мл), поддерживая температуру смеси ниже приблизительно 10C. Полученную охлажденную смесь использовали на следующей стадии без дальнейшей обработки. Стадия В. Метиловый эфир(S)-2-трет-бутоксикарбониламино-3-(4-циано-2,6 диметилфенил)пропионовой кислоты. В трехгорлую круглодонную колбу объемом 5 л с установленными вводом для газообразного азота,механической мешалкой, капельной воронкой и термопарой поместили 4-йод-3,5-диметилбензонитрил(210 г, 1,0 моль) и DMAc (750 мл). Полученную суспензию при перемешивании подогрели до температуры 35C для растворения твердых веществ. К полученной смеси затем добавили P(o-tol)3 (6,0 г,0,02 моль), Pd2(dba)3 (9,2 г, 0,01 моль) и нагрели полученную смесь до температуры приблизительно 75-80C. Затем через трубочку медленно добавили полученную на стадии А выше охлажденную смесь со скоростью, при которой температура реакционной смеси поддерживалась на уровне приблизительно 75-80C (в течение приблизительно 2 ч). Полученную суспензию охладили до комнатной температуры и выдержали ночь при умеренном перемешивании. Затем полученную суспензию нагрели до температуры приблизительно 35-40C и профильтровали через окись кремния (540 г). Полученный слой окиси кремния промыли DMAc (2400 мл), объединенные растворы в DMAc охладили до температуры приблизительно 0-5C и затем медленно добавили их к смеси льда и деионизованной воды. Полученную смесь выдержали на холоде в течение 2 ч, при этом из раствора начал выпадать твердый осадок белого цвета. Полученную смесь затем прогрели до комнатной температуры и выдержали ночь. Выпавший твердый осадок собрали вакуумной фильтрацией на воронке Бюхнера. Осадок на фильтре промыли деионизованной водой (31 л), высушили в течение ночи на воздухе и затем в течение ночи в вакуумной печи. К полученному твердому веществу добавили МеОН (1 л), полученную суспензию охладили до температуры приблизительно 0-5C и выдержали при указанной температуре в течение 1 ч при перемешивании. Выпавшее твердое вещество собрали фильтрованием, промыли холодным метанолом (400 мл) и высушили в вакуумной печи при температуре 45C, получив искомое соединение в виде твердого вещества сероватобелого цвета. Пример 4. Получение 4-бром-3,5-диметилбензонитрила В трехгорлую круглодонную колбу объемом 2 л с установленными капельной воронкой, механической мешалкой и термопарой поместили 4-бром-3,5-диметилфенол (50,0 г, 0,25 моль, Aldrich 99%) и пиридин (250 мл). Полученную смесь охладили до 0C и в течение 2 ч по каплям добавили трифторметансульфоновый ангидрид (80,5 г, 0,285 моль, Aldrich 99%). По окончании добавления полученную смесь выдержали при 0C в течение 15 мин и затем оставили на ночь при комнатной температуре. Через 16 ч полученную смесь охладили на ледяной бане и погасили Н 2 О (1,7 л) и EtOAc (1,7 л). Слои образовавшейся двухфазной смеси разделили, органическую фазу обработали 2 н. раствором HCl (21,0 л), затем промыли один раз водой (1,0 л) и один раз 50% солевым раствором. Затем органическую фазу высушили над Na2SO4, упарили досуха на роторном испарителе и получили 4-бром-3,5-диметилфениловый эфир трифторметансульфоновой кислоты в виде густого масла. В трехгорлую круглодонную колбу объемом 2 л с установленными механической мешалкой,вводом для газообразного азота, нагревательной рубашкой и термопарой поместили 4-бром-3,5-диметилфениловый эфир трифторметансульфоновой кислоты (79,8 г, 0,24 моль) и AcCN(500 мл). Затем в полученный раствор добавили Pd(PPh3)4 (27,7 г, 0,024 моль), CuI (9,2 г, 0,048 моль) иZn(CN)2 (79,8 г, 0,24 моль). Полученную смесь перемешали в течение 45 мин при температуре 50C, добавили DMAc (150 мл), подняли температуру до 80-88C и оставили реакционную смесь при этой температуре на ночь. Полученную смесь охладили до комнатной температуры, разбавили EtOAc (200 мл) и профильтровали через целит STAND SUPER-CEL 815520. Полученный слой целита промыли EtOAcNH4Cl:концентрированного NH4OH:H2O (240 мл:60 мл:240 мл). Слои разделили и органическую фазу промыли один раз водой (500 мл) и один раз солевым раствором (500 мл), затем упарили досуха при пониженном давлении, получив густое масло красного цвета. Искомое соединение кристаллизовали из В трехгорлую круглодонную колбу объемом 50 мл с установленными магнитной мешалкой и термопарой в атмосфере азота поместили метиловый эфир (S)-2-трет-бутоксикарбониламино-3-(4-циано 2,6-диметилфенил)пропионовой кислоты (166,2 мг, 0,5 ммоль), DMSO (5,0 мл) и K2CO3 (75 мг,0,5 ммоль) и охладили полученную смесь на ледяной бане. Затем к полученной смеси по каплям через шприц добавили 30% Н 2 О 2 (110 мкл). Полученной смеси дали прогреться до комнатной температуры,при этом твердые вещества растворились с образованием прозрачного раствора. После перемешивания в течение приблизительно 2 ч при температуре 45-50C добавили воду (10 мл), смесь охладили и фильтрованием собрали выпавший в осадок продукт. Собранное твердое вещество белого цвета промыли водой(225 мл) и затем высушили в течение 24 ч на насосе высокого вакуума, получив искомое соединение в виде твердого вещества белого цвета. Пример 6. Получение 2-трет-бутоксикарбониламино-3-(4-карбамоил-2,6-диметилфенил)пропионовой кислоты В трехгорлую круглодонную колбу объемом 5 л с установленными капельной воронкой, механической мешалкой, нагревательной рубашкой, обратным холодильником, термопарой и вводом для газообразного азота поместили метиловый эфир 2-трет-бутоксикарбониламино-3-(4-карбамоил-2,6 диметилфенил)пропионовой кислоты (250 г, 0,713 моль), DMSO (750 мл) и 30% Н 2 О 2 (250 мл). Карбонат калия (158 г, 1,14 моль, 1,6 экв.) растворили в воде (750 мл) и добавили по каплям в течение 30 мин. В процессе добавления температура смеси поднялась с 23 до 34C. Полученную смесь нагрели до температуры приблизительно 42-45C, за ходом реакции следили с помощью ВЭЖХ. Через 3 ч в теплую смесь добавили активированный уголь (ECOSORB-941) (37,5 г, 15 вес.%). Полученную суспензию в течение 1 ч кипятили с обратным холодильником и затем горячей профильтровали через целит. Полученный слой целита промыли H2O (1,5 л). Полученную смесь охладили до температуры приблизительно 10C и погасили 2,0 н. раствором HCl (рН 2, 1,22 л), получив смесь с выпавшим твердым осадком белого цвета. Полученную смесь при перемешивании выдержали на ледяной бане в течение приблизительно 4 ч, затем отфильтровали и высушили в течение 48 ч в вакуумной печи, получив искомое соединение в виде твердого кристаллического вещества белого цвета. Приведенное выше техническое описание содержит сведения о принципах, лежащих в основе настоящего изобретения, и иллюстрирующие его примеры, однако следует понимать, что практическое применение изобретения распространяется на все обычные вариации, адаптации и/или модификации в соответствии с нижеприведенными пунктами формулы изобретения и их эквивалентами. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ получения соединения формулы (I) где PG1 представляет собой защитную группу для атома азота;R0 представляет собой водород или C1-4 алкил;R4 представляет собой фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из С 1-6 алкила, циано, карбамоила,а также его фармацевтически приемлемых энантиомеров, фармацевтически приемлемых диастереомеров, фармацевтически приемлемых рацематов и фармацевтически приемлемых солей, включающий следующие стадии: взаимодействие соединения формулы (X), где PG1 представляет собой защитную группу для атома азота, с цинком; в присутствии йода; в первом органическом растворителе или смеси органических растворителей, причем указанный первый органический растворитель нереакционноспособен по отношению к используемому йоду; с получением соответствующего соединения формулы (XI);- 16018913 взаимодействие соединения формулы (XI) с соединением формулы (XII), где LG1 представляет собой уходящую группу; в присутствии палладиевого катализатора и фосфиновой лигандной системы; во втором органическом растворителе или смеси органических растворителей; с получением соответствующего соединения формулы (I). 2. Способ по п.1, где PG1 представляет собой Boc. 3. Способ по п.1, где R0 представляет собой метил. 4. Способ по п.1, где цинк представляет собой цинковую пыль. 5. Способ по п.4, где от 0,5 до 1,5 моль цинковой пыли присутствует на каждый моль соединения (X). 6. Способ по п.1, где от 0,1 до 0,5 моль йода присутствует на каждый моль соединения (X). 7. Способ по п.1, где первый органический растворитель представляет собой DMAc. 8. Способ по п.1, где соединение формулы (X) подвергают взаимодействию с цинком при температуре менее чем 10C. 9. Способ по п.1, где цинк и йод смешивают перед добавлением к соединению формулы (X). 10. Способ по п.1, где LG1 представляет собой бром. 11. Способ по п.1, где от 0,25 до 1,0 моль соединения формулы (XII) присутствует на каждый моль соединения (XI). 12. Способ по п.1, где палладиевый катализатор и фосфиновая лигандная система представляют собой сочетание Pd2(dba)3 и P(o-tol)3. 13. Способ по п.1, где второй органический растворитель представляет собой DMAc. 14. Способ по п.1, где соединение формулы (X) подвергают взаимодействию с соединением формулы (XII) при температуре в диапазоне от 50 до 100C. 15. Способ по п.1, где соединение формулы (XI) добавляют к смеси соединения формулы (XII),палладиевого катализатора и фосфиновой лигандной системы. 16. Способ получения соединения формулы (I-B) взаимодействие соединения формулы (Х-В) с цинком; в присутствии йода; в первом органическом растворителе или смеси органических растворителей, причем указанный первый органический растворитель нереакционноспособен по отношению к используемому йоду; с получением соответствующего соединения формулы (XI-B); взаимодействие полученного соединения формулы (XI-B) с соединением формулы (XII-B); в присутствии палладиевого катализатора и фосфиновой лигандной системы; во втором органическом растворителе или смеси органических растворителей; с получением соответствующего соединения формулы(I-B). 17. Способ по п.16, где цинк представляет собой цинковую пыль. 18. Способ по п.17, где от 0,5 до 1,5 моль цинковой пыли присутствует на каждый моль соединения(Х-В). 19. Способ по п.16, где от 0,1 до 0,5 моль йода присутствует на каждый моль соединения (Х-В). 20. Способ по п.16, где первый органический растворитель представляет собой DMAc. 21. Способ по п.16, где соединение формулы (Х-В) подвергают взаимодействию с цинком при температуре менее чем 10C. 22. Способ по п.16, где цинк и йод смешивают перед добавлением к соединению формулы (Х-В). 23. Способ по п.16, где от 0,25 до 1,0 моль соединения формулы (XII-B) присутствует на каждый моль соединения (XI-B). 24. Способ по п.16, где палладиевый катализатор и фосфиновая лигандная система представляют собой сочетание Pd2(dba)3 и P(o-tol)3. 25. Способ по п.16, где второй органический растворитель представляет собой DMAc. 26. Способ по п.16, где соединение формулы (Х-В) подвергают взаимодействию с соединением формулы (XII-B) при температуре в диапазоне от 50 до 100C. 27. Способ по п.16, где соединение формулы (XI-В) добавляют к смеси соединения формулы(XII-B), палладиевого катализатора и фосфиновой лигандной системы. 28. Способ получения соединения формулы (II-В) а также его фармацевтически приемлемой соли, включающий следующие стадии: взаимодействие соединения формулы (I-B) с окисляющим агентом; в присутствии неорганического основания; в третьем органическом растворителе; с получением соответствующего соединения формулы(II-В). 29. Способ по п.28, где окисляющий агент выбран из группы, состоящей из перекиси водорода,LiOH и LiOOH. 30. Способ по п.29, где окисляющий агент представляет собой перекись водорода. 31. Способ по п.28, где окисляющий агент представляет собой 30% перекись водорода и присутствует в избыточном количестве. 32. Способ по п.28, где неорганическое основание представляет собой карбонат калия. 33. Способ по п.28, где от 1,0 до 3,0 моль неорганического основания присутствует на каждый моль соединения (I-B). 34. Способ по п.28, где третий органический растворитель представляет собой DMSO. 35. Способ по п.28, где соединение формулы (I-B) подвергается взаимодействию с указанным окисляющим агентом при температуре в диапазоне от комнатной температуры до 60C.
МПК / Метки
МПК: C07C 229/12, C07C 227/16
Метки: l-аланина, получения, защищенных, производных, способ
Код ссылки
<a href="https://eas.patents.su/19-18913-sposob-polucheniya-zashhishhennyh-proizvodnyh-l-alanina.html" rel="bookmark" title="База патентов Евразийского Союза">Способ получения защищенных производных l-аланина</a>
Предыдущий патент: Сушильная машина, оборудованная теплообменником с облицовкой
Следующий патент: Стиральная машина
Случайный патент: Способ получения олефиновых производных












