Жидкие композиции солей 4-[2-(4-метилфенилсульфанил)фенил]пиперидина
Номер патента: 19695
Опубликовано: 30.05.2014
Авторы: Ласскоген Гудрун, Стенсбель Тине Брайан, Лопес Де Диего Хейди
Формула / Реферат
1. Жидкая фармацевтическая композиция, содержащая соль 4-[2-(4-метилфенилсульфанил)фенил]пиперидина, выбранную из соли присоединения DL-молочной кислоты, соли присоединения глутаровой кислоты, соли присоединения L-аспарагиновой кислоты и соли присоединения глутаминовой кислоты.
2. Жидкая композиция по п.1, в которой солью является соль присоединения DL-молочной кислоты.
3. Жидкая композиция по п.1, в которой солью является соль присоединения глутаровой кислоты.
4. Жидкая композиция по п.1, в которой солью является соль присоединения L-аспарагиновой кислоты.
5. Жидкая композиция по п.1, в которой солью является соль присоединения глутаминовой кислоты.
6. Жидкая композиция по любому из пп.1-5, в которой концентрация соли составляет выше 5 мг/мл.
7. Способ лечения заболевания, выбранного из расстройства настроения, большого депрессивного расстройства, генерализованного тревожного расстройства, атипичной депрессии, биполярной депрессии, социального тревожного расстройства, обсессивно-компульсивного расстройства, панического расстройства, посттравматического стрессового расстройства, злоупотребления лекарственным средством, нарушения питания, расстройства сна, болезни Альцгеймера, деменции, хронической боли, депрессии, связанной с когнитивными нарушениями, депрессии, связанной с психозом, когнитивных нарушений при шизофрении, депрессии или тревоги, связанной с болью, нарушений поведения у пожилых, синдрома дефицита внимания с гиперактивностью, меланхолии, депрессии, не поддающейся лечению, или депрессии с остаточными симптомами, причем упомянутый способ включает введение терапевтически эффективного количества жидкой композиции по любому из пп.1-6 нуждающемуся в ней пациенту.
8. Способ по п.7, в котором дозируют предварительно определенный объем жидкой композиции и полученный в результате объем композиции добавляют в стакан с жидкостью, после чего жидкость вводят пациенту.
9. Применение соли 4-[2-(4-метилфенилсульфанил)фенил]пиперидина, выбранной из соли присоединения DL-молочной кислоты, соли присоединения глутаровой кислоты, соли присоединения L-аспарагиновой кислоты и соли присоединения глутаминовой кислоты, для получения жидкого лекарственного средства для лечения заболевания, выбранного из расстройства настроения, большого депрессивного расстройства, генерализованного тревожного расстройства, атипичной депрессии, биполярной депрессии, социального тревожного расстройства, обсессивно-компульсивного расстройства, панического расстройства, посттравматического стрессового расстройства, злоупотребления лекарственным средством, нарушения питания, расстройства сна, болезни Альцгеймера, деменции, хронической боли, депрессии, связанной с когнитивными нарушениями, депрессии, связанной с психозом, когнитивных нарушений при шизофрении, депрессии или тревоги, связанной с болью, нарушения поведения у пожилых, синдрома дефицита внимания с гиперактивностью, меланхолии, депрессии, устойчивой к лечению, или депрессии с остаточными симптомами.
10. Применение по п.9, в котором солью является соль присоединения DL-молочной кислоты.
11. Применение по п.9, в котором солью является соль присоединения глутаровой кислоты.
12. Применение по п.9, в котором солью является соль присоединения L-аспарагиновой кислоты.
13. Применение по п.9, в котором солью является соль присоединения глутаминовой кислоты.
14. Применение по любому из пп.9-13, в котором лекарственное средство содержит более 5 мг/мл соли.
Текст
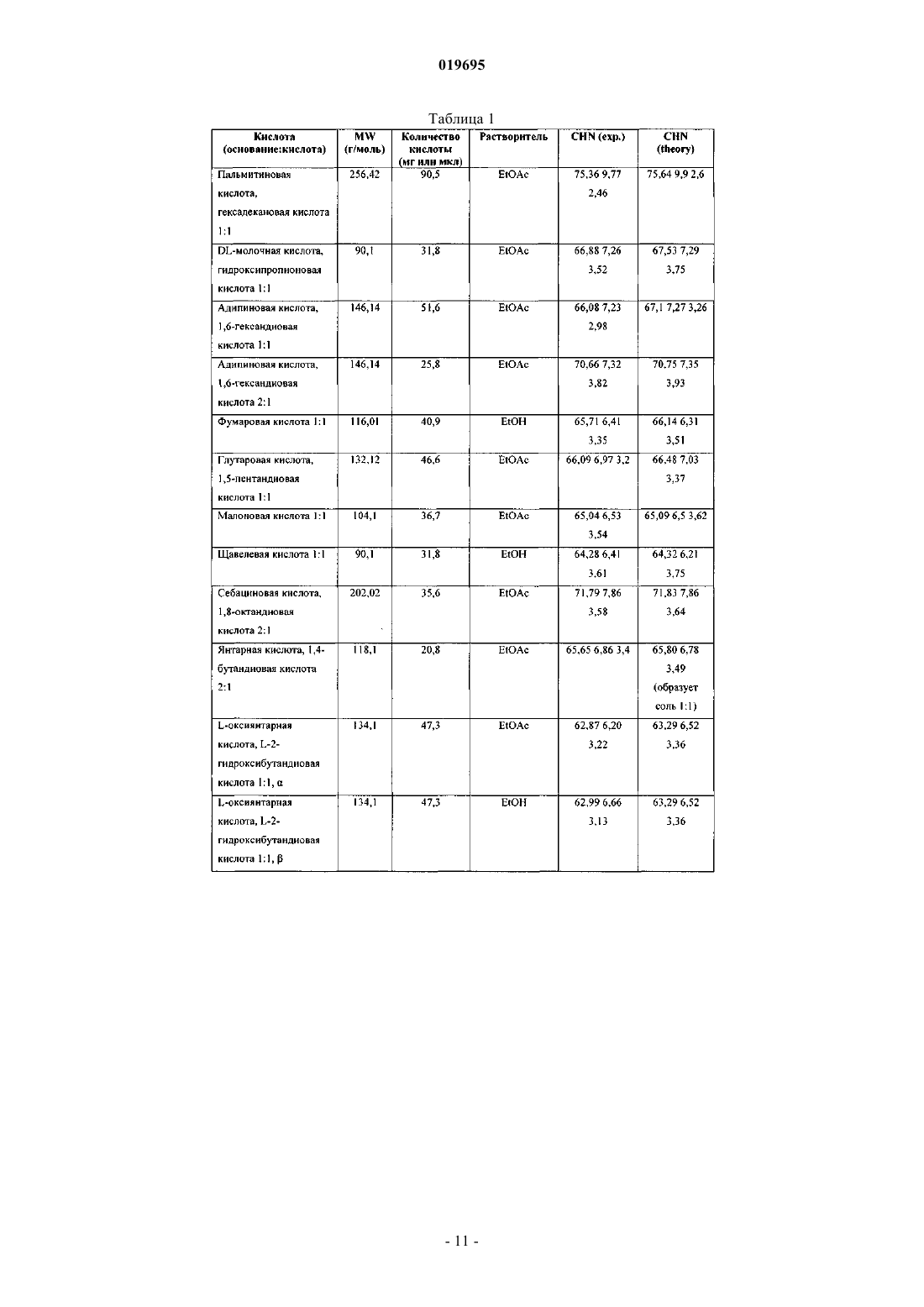
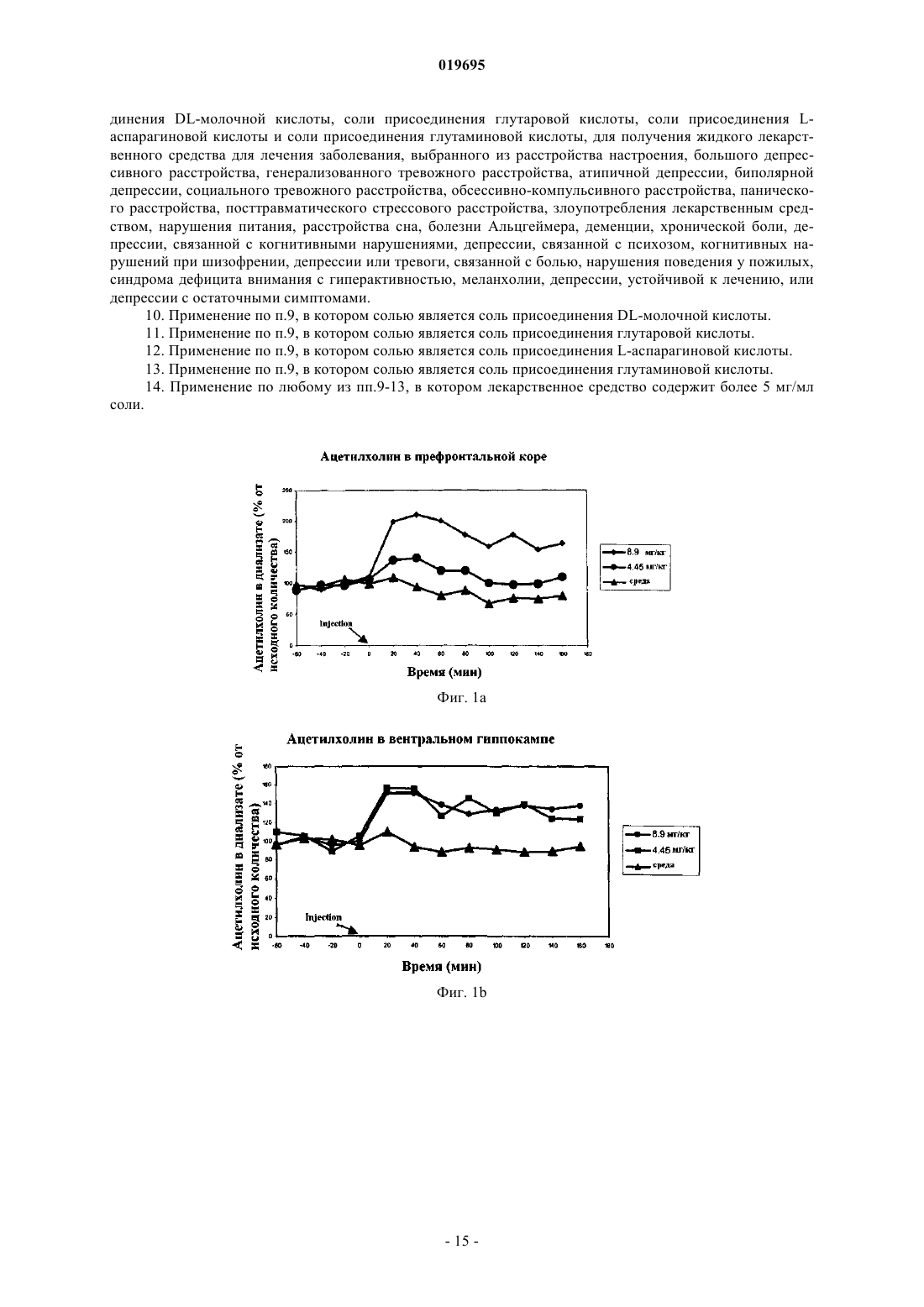
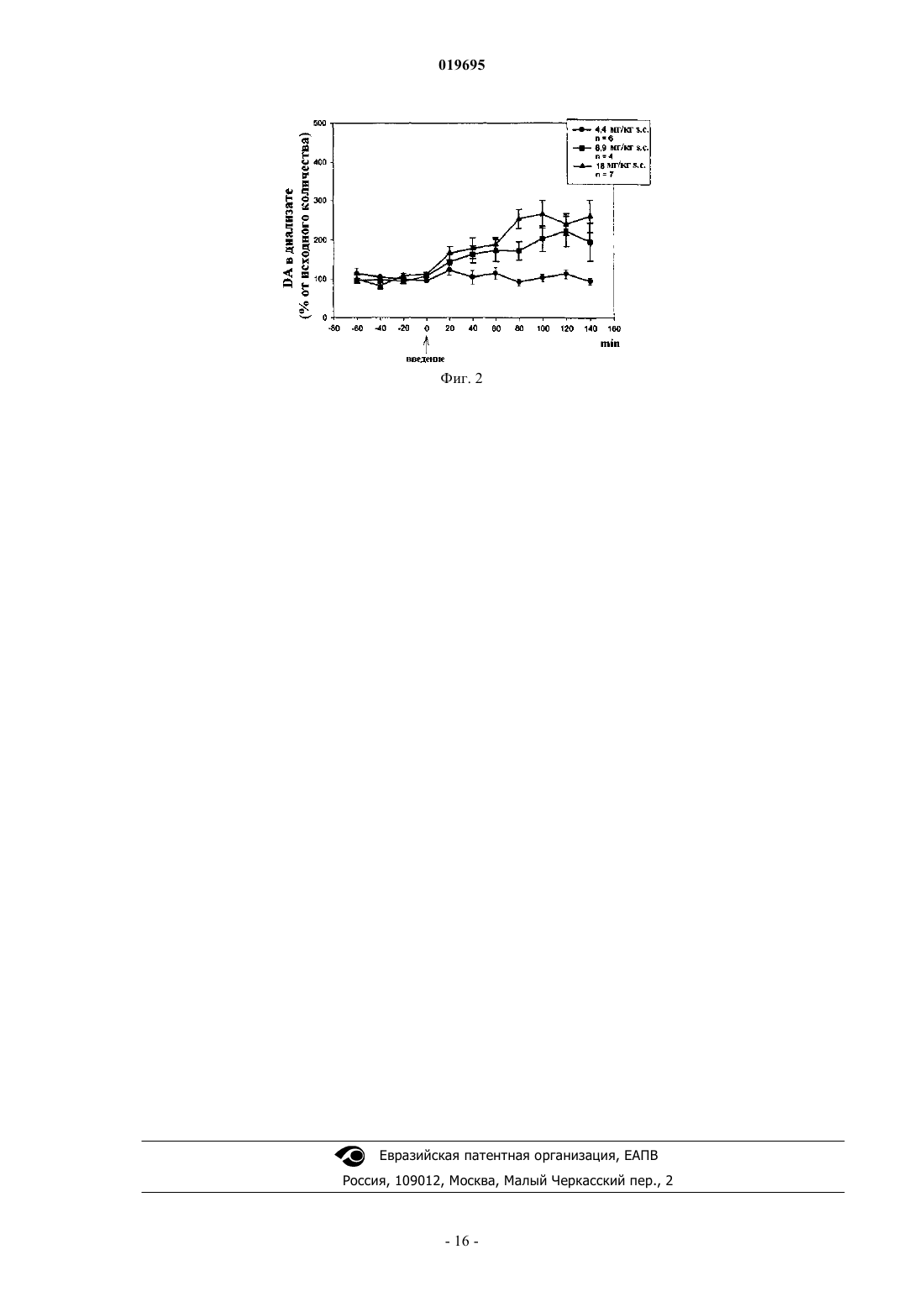
ЖИДКИЕ КОМПОЗИЦИИ СОЛЕЙ 4-[2-(4-МЕТИЛФЕНИЛСУЛЬФАНИЛ)ФЕНИЛ] ПИПЕРИДИНА Настоящее изобретение относится к жидким композициям солей DL-молочной кислоты,глутаровой кислоты, L-аспарагиновой кислоты и глутаминовой кислоты с 4-[2-(4 метилфенилсульфанил)фенил]пиперидином и их применению в получении лекарственного средства, которое применяют в лечении ЦНС заболевания. Ласскоген Гудрун, Стенсбель Тине Брайан, Лопес Де Диего Хейди (DK) Медведев В.Н. (RU) Область техники, к которой относится изобретение Настоящее изобретение относится к жидкой фармацевтической композиции. Уровень техники Международная патентная заявка, опубликованная, как WO 2003/029232, описывает, например, соединение 4-[2-(4-метилфенилсульфанил)фенил]пиперидин (соединение I) в виде свободного основания,соответствующую соль присоединения HCl. Сообщают, что соединение является ингибитором транспортера серотонина и серотонинового рецептора 2 С (5-НT2C), и говорят, что оно пригодно для лечения аффективных расстройств, например депрессии и тревоги. Найдено, что соединение I также является мощным антагонистом серотонинового рецептора 3 (5-НТ 3) и серотонинового рецептора 2 А (5-НТ 2A), по этой причине соединение I можно применять для лечения более широкого диапазона заболеваний, включая боль и когнитивные нарушения. Данные фармакологические результаты также описаны в WO 2007/144006. Для многих фармацевтических соединений пероральный прием таблеток, капсул, пилюль или аналогичных лекарственных форм, предназначенных для глотания, является предпочтительной формой приема. Однако некоторые пациенты, например пожилые пациенты, могут иметь сложности с глотанием, и жидкие растворы могут быть подходящей альтернативной формой, избегающей необходимости глотания таблетки, капсулы, пилюли и т.д. Кроме того, жидкий раствор обеспечивает возможность гибкого режима дозирования. Для того чтобы ограничить объем жидкого раствора, необходимо обладать высокой концентрацией активного ингредиента в растворе, которая к тому же требует высокой растворимости активного ингредиента. Настоящее изобретение относится к жидкой композиции соединения I. Сущность настоящего изобретения Изобретатели настоящего изобретения неожиданно обнаружили, что соль присоединения DLмолочной кислоты (=DL-лактат), соль присоединения глутаровой кислоты (=глутарат), соль присоединения L-аспарагиновой кислоты (=L-аспартат) и соль присоединения глутаминовой кислоты (=глутамат) 4[2-(4-метилфенилсульфанил)фенил]пиперидина являются исключительно растворимыми. Соответственно, настоящее изобретение относится к жидкой фармацевтической композиции, содержащей соль 4-[2(4-метилфенилсульфанил)фенил]пиперидина, выбранную из соли присоединения DL-молочной кислоты,соли присоединения глутаровой кислоты, соли присоединения L-аспарагиновой кислоты и соли присоединения глутаминовой кислоты. Предпочтительно концентрация упомянутой соли в композиции составляет выше 5 мг/мл. Изобретение также относится к способу лечения заболевания, выбранного из расстройства настроения, большого депрессивного расстройства, генерализованного тревожного расстройства, атипичной депрессии, биполярной депрессии, социального тревожного расстройства, обсессивно-компульсивного расстройства, панического расстройства, посттравматического стрессового расстройства, злоупотребления лекарственным средством, нарушения питания, расстройства сна, болезни Альцгеймера, деменции,хронической боли, депрессии, связанной с когнитивными нарушениями, депрессии, связанной с психозом, когнитивных нарушений при шизофрении, депрессии или тревоги, связанной с болью, нарушений поведения у пожилых, синдрома дефицита внимания с гиперактивностью, меланхолии, депрессии, не поддающейся лечению, или депрессии с остаточными симптомами, причем упомянутый способ включает введение терапевтически эффективного количества жидкой композиции согласно изобретению нуждающемуся в ней пациенту. При этом дозируют предварительно определенный объем упомянутой жидкой композиции, и полученный в результате объем упомянутой композиции добавляют в стакан с жидкостью, после чего данная жидкость вводится пациенту. Далее изобретение включает применение соли 4-[2-(4-метилфенилсульфанил)фенил]пиперидина,выбранной из соли присоединения DL-молочной кислоты, соли присоединения глутаровой кислоты, соли присоединения L-аспарагиновой кислоты и соли присоединения глутаминовой кислоты, в получении жидкого лекарственного средства для лечения заболевания, выбранного из расстройства настроения,большого депрессивного расстройства, генерализованного тревожного расстройства, атипичной депрессии, биполярной депрессии, социального тревожного расстройства, обсессивно-компульсивного расстройства, панического расстройства, посттравматического стрессового расстройства, злоупотребление лекарственным средством, нарушения питания, расстройства сна, болезни Альцгеймера, деменции, хронической боли, депрессии, связанной с когнитивными нарушениями, депрессии, связанной с психозом,когнитивных нарушений при шизофрении, депрессии или тревоги, связанной с болью, нарушения поведения у пожилых, синдрома дефицита внимания с гиперактивностью, меланхолии, депрессии, устойчивой к лечению или депрессии с остаточными симптомами. Изобретение также относится к соли 4-[2-(4-метилфенилсульфанил)фенил]пиперидина, которая выбрана из соли присоединения DL-молочной кислоты, соли присоединения глутаровой кислоты, соли присоединения L-аспарагиновой кислоты и соли присоединения глутаминовой кислоты для применения в лечении заболевания, выбранного из расстройства настроения, большого депрессивного расстройства,генерализованного тревожного расстройства, атипичной депрессии, биполярной депрессии, социального тревожного расстройства, обсессивно-компульсивного расстройства, панического расстройства, посттравматического стрессового расстройства, злоупотребления лекарственным средством, нарушения питания, расстройства сна, болезни Альцгеймера, деменции, хронической боли, депрессии, связанной с когнитивными нарушениями, депрессии, связанной с психозом, когнитивных нарушений при шизофрении, депрессии или тревоги, связанной с болью, нарушения поведения у пожилых, синдрома дефицита внимания с гиперактивностью, меланхолии, депрессии, устойчивой к лечению, или депрессии с остаточными симптомами, где упомянутая соль находится в жидкой фармацевтической композиции. Фигуры Фиг. 1 - концентрации ацетилхолина в префронтальной коре и вентральном гиппокампе при приеме соединения I. Фиг. 2 - концентрации дофамина в префронтальной коре при приеме соединения I Подробное описание настоящего изобретения Все композиции, к которым относится настоящее изобретение, являются фармацевтическими композициями. Табл. 2 в примерах отражает растворимость различных солей 4-[2-(4-метилфенилсульфанил)фенил]пиперидина. Как очевидно на основании этих данных, соли присоединения DLмолочной кислоты, L-аспарагиновой кислоты, глутаминовой кислоты и глутаровой кислоты обладают исключительно высокой растворимостью. Для удобства данные соли называют солями настоящего изобретения.DL-Молочная кислота также известна, как DL-2-гидроксипропионовая кислота, и она образует 1:1 соль присоединения с 4-[2-(4-метилфенилсульфанил)фенил]пиперидином, который применяют в настоящем изобретении. Глутаровая кислота также известна, как 1,5-пентандиовая кислота, и она образует 1:1 соль присоединения с 4-[2-(4-метилфенилсульфанил)фенил]пиперидином, который применяют в настоящем изобретении.L-Аспарагиновая кислота образует 1:1 соль присоединения с 4-[2-(4-метилфенилсульфанил)фенил]пиперидином, который применяют в настоящем изобретении. Глутаминовая кислота образует 1:1 соль присоединения с 4-[2-(4-метилфенилсульфанил)фенил]пиперидином, который применяют в настоящем изобретении. 4-[2-(4 метилфенилсульфанил)фенил]пиперидин можно получить, как описано в WO 2003/029232. Альтернативно, 4-[2-(4-метилфенилсульфанил)фенил]пиперидин можно получить, как описано в примерах. Соли настоящего изобретения можно приготовить добавлением подходящей кислоты с последующим осаждением, где осаждение можно достигнуть, например, охлаждением, удалением растворителя, добавлением другого растворителя или их смесей. Примеры описывают конкретные схемы получения солей. Жидкие композиции могут предназначаться для перорального или парентерального приема. Жидкие композиции для парентерального приема, которые включают инфузионные растворы, являются во многих аспектах аналогичными другим жидким композициям, но дополнительно характеризуются стерильностью и изотоничностью. Жидкая пероральная композиция настоящего изобретения может быть представлена сиропом, эликсиром, пероральным раствором, суспензией или концентрированной пероральной композицией. Одно из преимуществ данных форм приема заключается в том, что пациент не должен глотать твердую форму,что может быть сложно, в особенности для пожилых пациентов или для пациентов с повреждениями рта или гортани. Сиропы и эликсиры обычно являются подслащенными, ароматизированными жидкостями, содержащими активный фармацевтический ингредиент. Сиропы обычно имеют более высокое содержание сахара, и эликсиры также часто содержат спирт. Пероральный раствор является раствором активного ингредиента. Суспензия является двухфазной системой, содержащей твердые частицы, диспергированные в жидкости. Прием сиропов, эликсиров, пероральных растворов и суспензий обычно включает потребление относительно больших количеств жидкости, например 10-50 мл. В противоположность этому концентрированные пероральные композиции настоящего изобретения принимаются пациентом дозированием предварительно определенного объема упомянутой композиции из подходящего дозирующего устройства, добавлением полученного в результате количества в стакан с жидкостью (напитком, например, водой, соком или аналогичном напитком), после чего пациент выпивает жидкость. Для удобства объем дозируют в маленьком количестве, например меньше чем 2 мл, таком как меньше чем 1 мл, таком как меньше чем 0,5 мл. В конкретном варианте осуществления концентрированные пероральные композиции настоящего изобретения принимаются пациентом дозированием предварительно определенного количества капель упомянутой композиции из подходящего дозирующего устройства, например емкости с капельным устройством, добавлением капель в стакан с жидкостью (водой, соком или аналогичным напитком), после чего пациент выпивает жидкость. В данном контексте капельное устройство является устройством, снабженным емкостью, которое действует таким образом,что жидкость, находящуюся внутри упомянутой емкости, можно извлекать из упомянутой емкости в виде отдельных капель. Концентрация соли настоящего изобретения в концентрированных пероральных композициях определяется количеством капель (или объемом), которое желательно получить, и количеством соли, кото-2 019695 рое желательно принять. Обычно считают, что дозирование в районе 10-20 капель является оптимальным компромиссом между безопасностью/эффективностью лечения с одной стороны и удобством с другой. Если концентрация соли настоящего изобретения будет слишком высокой, т.е. если нужно дозировать только очень небольшое количество капель, это может ставить под удар безопасность или эффективность лечения. Относительно небольшое количество капель, добавление на одну или две капли больше или меньше, чем требуется, будет значительно увеличивать неопределенность в обеспечиваемой дозе. С другой стороны, если концентрация соли настоящего изобретения будет слишком низкой, количество капель, которые нужно дозировать, будет большим, что является неудобным для пациента или лица,осуществляющего уход. Относительно дневных доз солей настоящего изобретения 5 мг, могла бы быть подходящей концентрированная пероральная композиция с концентрацией 5 мг активного ингредиента на мл. Концентрация 5 мг на мл, и число капель - 20 капель на мл делали бы возможным прием 20 капель для дозы 5 мг. Относительно дневных доз солей настоящего изобретения 5 мг могла бы быть подходящей концентрированная пероральная композиция с концентрацией 10 мг активного ингредиента на мл. Концентрация 10 мг на мл и число капель 20 капель на мл делали бы возможным прием 10 капель для дозы 5 мг. Относительно дневных доз соединений настоящего изобретения 10 мг могла бы быть подходящей концентрированная пероральная композиция с концентрацией 20 мг активного ингредиента на мл. Концентрация 20 мг на мл, и число капель 20 капель на мл делали бы возможным прием 10 капель для дозы 10 мг. Относительно дневных доз соединений настоящего изобретения 20 мг, могла бы быть подходящей концентрированная пероральная композиция с концентрацией 40 мг активного ингредиента на мл. Концентрация 40 мг на мл, и число капель - 20 капель на мл делали бы возможным прием 10 капель для дозы 20 мг. Относительно дневных доз соединений настоящего изобретения 30 мг могла бы быть подходящей концентрированная пероральная композиция с концентрацией 60 мг активного ингредиента на мл. Концентрация 60 мг на мл и число капель 20 капель на мл делали бы возможным прием 10 капель для дозы 30 мг. Относительно дневных доз соединений настоящего изобретения 40 мг могла бы быть подходящей концентрированная пероральная композиция с концентрацией 80 мг активного ингредиента на мл. Концентрация 80 мг на мл и число капель 20 капель на мл делали бы возможным прием 10 капель для дозы 40 мг. Относительно дневных доз соединений настоящего изобретения 50 мг могла бы быть подходящей концентрированная пероральная композиция с концентрацией 100 мг активного ингредиента на мл. Концентрация 100 мг на мл и число капель 20 капель на мл делали бы возможным прием 10 капель для дозы 50 мг. В одном варианте осуществления концентрированную пероральную капельную композицию принимают из прибора с дозирующим устройством подобным шприц-ручке или шприцу. Примеры таких устройств для приема представлены, например, в WO 03/061508, US 2004/0186431, US 2003-089743. Данные устройства содержат концентрированную пероральную композицию настоящего изобретения в герметичной камере, например картридже, и они имеют приспособления для получения отмеренного количества концентрированного перорального раствора. Для того чтобы ограничить размер устройства, объем концентрированного перорального раствора является маленьким (0,01-1 мл), который снова требует того, чтобы соль была хорошо растворимой. Данные дозирующие устройства, подобные шприц-ручке или шприцу, являются удобными для пациента, потому что их можно носить, например, в нагрудном кармане, и подходящая конструкция устройства может служить для того, чтобы скрывать то,что оно является дозирующим устройством лекарственного средства. Относительно дневных доз солей настоящего изобретения 5-10 мг, могла бы быть подходящей концентрированная пероральная композиция с концентрацией 100 мг активного ингредиента на мл. Это могло бы значить, что принимают 0,05 мл для дозы 5 мг и что принимают 0,1 мл для дозы 10 мг. Относительно дневных доз соединений настоящего изобретения 20-50 мг, могла бы подходить концентрированная пероральная композиция с концентрацией 200 мг активного ингредиента на мл. Это могло бы значить, что принимают 0,1 мл для дозы 20 мг, и что принимают 0,25 мл для дозы 50 мг. Соответственно концентрированные пероральные композиции настоящего изобретения содержат приблизительно 5-250 мг/мл солей настоящего изобретения. Конкретные примеры включают приблизительно 10-100 мг/мл, приблизительно 20-200 мг/мл, приблизительно 150-200 мг/мл, приблизительно 2080 мг/мл, приблизительно 30-70 мг/мл и приблизительно 10, 20, 30, 40, 50, 60, 70, 80, 90 или 100 мг/мл. В одном варианте осуществления пероральная капельная композиция настоящего изобретения содержит по меньшей мере 5 мг/мл солей настоящего изобретения. В одном варианте осуществления пероральная капельная композиция настоящего изобретения содержит по меньшей мере 10 мг/мл солей настоящего изобретения. В одном варианте осуществления пероральная капельная композиция настоящего изобретения содержит по меньшей мере 20 мг/мл соли настоящего изобретения. В одном варианте осуществления пероральная капельная композиция настоящего изобретения содержит по меньшей мере 30 мг/мл соли настоящего изобретения. В одном варианте осуществления пероральная капельная композиция настоящего изобретения содержит по меньшей мере 50 мг/мл соли настоящего изобретения. В одном варианте осуществления пероральная капельная композиция настоящего изобретения содержит по меньшей мере 80 мг/мл соли настоящего изобретения. В добавление к солям настоящей заявки, пероральные растворы настоящей заявки, и в особенности концентрированные пероральные композиции могут содержать растворители, буферы, поверхностноактивные вещества, модификаторы поверхностного натяжения, модификаторы вязкости, консерванты,антиоксиданты, красящие вещества, вещества, исправляющие вкус лекарственного средства, ароматизирующие вещества и т.д. Примеры растворителей включают воду и другие растворители, которые смешиваются с водой, или агенты, повышающие растворимость, и являются подходящими для пероральных целей. Примерами подходящих растворителей являются этанол, пропиленгликоль, глицерин, полиэтиленгликоли, полоксамеры, сорбитол, бензиловый спирт. Растворимость в воде активного ингредиента можно, кроме того,повысить добавлением к раствору фармацевтически приемлемого сорастворителя, циклодекстрина или его производного. Можно применять буферную систему для того, чтобы поддерживать рН композиции в оптимальном рН-диапазоне. Буферная система является смесью подходящего количества слабой кислоты, такой как уксусная, метафосфорная, янтарная, винная, молочная или лимонная кислота и ее сопряженного основания. Идеально, буферная система обладает достаточной емкостью для того, чтобы сохранять рН в требуемом диапазоне при разбавлении нейтральным, слегка кислым или слегка основным напитком. Поверхностно-активные вещества являются веществами, которые повышают растворимость активных соединений, которые являются недостаточно растворимыми в водной среде, обычно с образованием мицелл. Предпочтительно используемое поверхностно-аткивное вещество должно быть неионным в виду малой токсичности. Можно применять высокие концентрации поверхностно-активных веществ для того, чтобы учитывать разбавление в процессе приема без осаждения. Примеры поверхностноактивных веществ включают твины, спаны и моно- и диглицериды. Модификаторы поверхностного натяжения можно добавлять для того, чтобы стандартизировать число капель для пероральных капельных композиций. Примером модификатора поверхностного натяжения является этанол, который уменьшает поверхностное натяжение и увеличивает число капель. Можно добавлять модификаторы вязкости для того, чтобы регулировать вязкость капли для концентрированных пероральных композиций. Вязкость капли для композиции, которую нужно дозировать,в отдельных каплях из емкости, снабженной капельным устройством не должна, для удобства, превышать 2 капель в секунду. Примеры модификаторов вязкости включают этанол, гидроксиэтилцеллюлозу,карбоксиметилцеллюлозу натрия, метилцеллюлозу, поливиниловый спирт, поливинилпирролидон, полиэтиленгликоль и глицерин. Можно добавлять консерванты для того, чтобы предотвратить рост микроорганизмов, таких как бактерии, дрожжи и грибки в жидкой композиции, которая, вероятно, будет применяться повторно. Подходящие консерванты должны быть фармацевтически приемлемыми, физикохимически стабильными и эффективными в требуемом рН диапазоне. Примеры консервантов включают этанол, бензойную кислоту, сорбиновую кислоту, метилпарабен, пропилпарабен и бензиловый спирт. Т.к. активное вещество является более чувствительным к разложению в растворенной, чем в твердой форме, может быть необходимо добавлять в жидкую композицию антиоксидант. Примеры антиоксидантов включают пропилгаллат, аскорбилпальмитат, аскорбиновую кислоту, сульфит натрия, лимонную кислоту и EDTA. В некоторых композициях можно применять окрашивающие вещества для того, чтобы обеспечить однообразный внешний вид продукта. Некоторые активные ингредиенты могут быть, кроме того, очень чувствительными к свету, и это может обосновывать необходимость добавления окрашивающих веществ к капельным композициям для того, чтобы защитить их от света и с целью стабилизации. Подходящие окрашивающие вещества включают, например, тартразин и желтый солнечного заката. Подсластители могут скрывать неприятный вкус, связанный с некоторыми композициями или для того, чтобы получить желаемый вкус. Примерами подсластителей являются сахарин, натриевая соль сахарина, глюкоза, сорбитол, глицерин, ацесульфам калия и неогесперидин дигидрохалкон. Вкус можно,кроме того, оптимизировать добавлением одного или более ароматизирующих веществ. Подходящими ароматизирующими веществами являются фруктовые ароматизирующие вещества, такие как вишневый,малиновый, черносмородиновый, лимонный или клубничный запах или другие ароматизирующие вещества, такие как лакрица, анис, мята, карамель и т.д. Конкретными примерами концентрированной пероральной композиции, которую можно принимать с капельным устройством, являются (4-[2-(4-метилфенилсульфанил)фенил]пиперидин = Соединение I) 0,73% глутарата соединения I, соответствующего 0,5% свободного основания соединения I, достаточное количество воды до 100%; 1,58% глутамата соединения I, соответствующего 1% свободного основания соединение I, 0,08% метилпарагидроксибензоата, 0,02% пропилпарагидроксибензоата, достаточное количество воды до 100%; 2,94% L-аспартата соединения I, соответствующего 2% свободного основания соединение I, 0,08% метилпарагидроксибензоата, 0,02% пропилпарагидроксибензоата, 7% этанола, достаточное количество воды до 100%; 10,54% DL-лактата соединения I, соответствующего 8% свободного основания соединения I, 0,08% метилпарагидроксибензоата, 0,02% пропилпарагидроксибензоата, достаточное количество воды до 100%. Конкретным примером концентрированной пероральной композиции, который можно принимать с помощью устройства, подобного шприц-ручке или шприцу, является 26,36% DL-лактата соединения I,соответствующего 20% свободного основания соединения I, 0,08% метилпарагидроксибензоата, 0,02% пропилпарагидроксибензоата, достаточное количество воды до 100%. Фармацевтический профиль солей настоящего изобретения описывают в примерах. Вкратце, соли настоящего изобретения являются ингибиторами транспортера серотонина и серотонинового рецептора 2 С (5-HT2C) и антагонистов серотонинового рецептора 3 (5-НТ 3), серотонинового рецептора 2 А (5-HT2A) и 1 адренергического рецептора и они, по-видимому, приводят к увеличению внеклеточной концентрации ацетилхолина в префронтальной коре и вентральном гиппокампе и концентрации дофамина в префронтальной коре. Дополнительно, соли настоящего изобретения являются эффективными в лечении боли, как показано в примерах. Ожидают, что фармакологический профиль в комбинации с предклиническими данными будет отражаться в полезности клинического применения солей настоящего изобретения. Следовательно, считают, что соли настоящего изобретения являются пригодными в лечении заболеваний, включая расстройства настроения, большое депрессивное расстройство, генерализованное тревожное расстройство, атипичную депрессию, биполярную депрессию, социальное тревожное расстройство, обсессивно-компульсивное расстройство, паническое расстройство, посттравматическое стрессовое расстройство, злоупотребление лекарственным средством, нарушение питания, расстройство сна, Болезнь Альцгеймера, деменцию, хроническую боль, депрессию, связанную с когнитивными нарушениями,депрессию, связанную с психозом, когнитивные нарушения при шизофрении, депрессию или тревогу,связанную с болью, нарушения поведения у пожилых, синдром дефицита внимания с гиперактивностью,депрессию, устойчивую к лечению меланхолии, и депрессию с остаточными синдромами. 5-HT2C рецепторы располагаются, например, на дофаминергических нейронах, где активация оказывает тоническое ингибиторное влияние на высвобождение дофамина, и 5-HT2C антагонисты будут увеличивать концентрацию дофамина. Данные, представленные в примерах, показывают, что соединение I,действительно, приводит к увеличению концентрации внеклеточного дофамина в мозге. На основании этого можно сделать предположение, что 5-HT2C антагонисты являются особенно хорошо подходящими для лечения депрессии, которая не поддается лечению селективными ингибиторами обратного захвата серотонина. Эта гипотеза находит подтверждение в нескольких клинических исследованиях, показывающих, что комбинация митразипина и SSRI является более совершенной, чем один SSRI для лечения пациентов с депрессией с неадекватной клинической реакцией (депрессия, устойчивая к лечению, TRD или резистентная депрессия) [Psychother. Psychosom., 75, 139-153, 2006]. Миртазапин является также 5 НТ 2 и 5-НТ 3 антагонистом, что свидетельствует, что соединения, проявляющие ингибирование обратного захвата серотонина в комбинации с 5-НТ 2 и 5-НТ 3 антагонизмом, такие как соединение I, являются пригодными для лечения TRD, т.е., будут увеличивать скорость наступления ремиссии у пациентов, страдающих от депрессии, устойчивой к лечению. Данные, представленные в примерах, показывают, что соединение I вызывает увеличение внеклеточной концентрации ацетилхолина в мозге. Имеется давние клинические данные, что увеличение концентрации ацетилхолина в мозге, является способом лечения болезни Альцгеймера и когнитивных нарушений вообще, подтверждая применение ингибиторов ацетилхолинэстеразы в лечении болезни Альцгеймера. На основании этого считают, что соединение I является пригодным в лечении болезни Альцгеймера и когнитивных нарушений, и также расстройств настроения, таких как депрессия, связанная с болезнью Альцгеймера и когнитивными нарушениями. Часть пациентов с депрессией будут реагировать на лечение, например, SSRI в том смысле, что они будут поправляться по клинической шкале соответствующей депрессии, такой как MADRD и HAMD, но где другие симптомы, такие как нарушения сна и когнитивные нарушения, будут сохраняться. В настоящем контексте, данных пациентов называют частично реагирующими и страдающими от депрессии с остаточными симптомами. В результате обсуждаемого выше действия на концентрации ацетилхолина,ожидают, что соединение будет пригодным в лечении когнитивных нарушений в дополнение к депрессии. Клинические исследования показали, что соединение празосин, которое является антагонистом -1 адренергического рецептора, ослабляет нарушения сна [Raskind, Biol. Psychiatry, 2006 in press]. Более того, также считают, что 5-HT2A и 5-HT2C антагонизм соединений настоящего изобретения обладает седативным, улучшающим сон действием [Neuropharmacol, 33, 467-471, 1994], по этой причине соединения настоящего изобретения являются пригодными для лечения частично реагирующих пациентов (с депрессией с остаточными симптомами), или, другими словами, лечение пациентов с депрессией настоящим соединением будет уменьшать долю частично реагирующих пациентов. В одном варианте осуществления настоящее изобретение относится к способу лечения заболевания,выбранного из расстройства настроения, большого депрессивного расстройства, генерализованного тревожного расстройства, атипичной депрессии, биполярной депрессии, социального тревожного расстройства, обсессивно-компульсивного расстройства, панического расстройства, посттравматического стрессового расстройства, злоупотребления лекарственным средством, нарушения питания, расстройства сна,-5 019695 болезни Альцгеймера, деменции, хронической боли, депрессии, связанной с когнитивными нарушениями, депрессии, связанной с психозом, когнитивных нарушений при шизофрении, депрессии или тревоги,связанной с болью, нарушения поведения у пожилых, синдрома дефицита внимания с гиперактивностью,меланхолии, депрессии, устойчивой к лечению, или депрессии с остаточными симптомами, причем упомянутый способ включает прием терапевтически эффективного количества жидкой композиции настоящего изобретения нуждающимся в ней пациентом. В одном варианте осуществления упомянутой жидкой композицией является концентрированная пероральная композиция. В одном варианте осуществления пациенту, которого нужно лечить, ставят диагноз заболевания,причем упомянутый пациент лечится от данного заболевания. В одном варианте осуществления соединение настоящего изобретения принимают в количестве от приблизительно 0,001 до приблизительно 100 мг/кг веса тела в день. Стандартная пероральная доза находится в диапазоне от приблизительно 0,001 до приблизительно 100 мг/кг веса тела в день, предпочтительно от приблизительно 0,01 до приблизительно 50 мг/кг веса тела в день, принимаемая в виде одной или более доз, таких как 1-3 дозы. Точная доза будет зависеть от частоты и способа приема, пола, возраста, веса и общего состояния субъекта, подвергаемого лечению, природы и тяжести вылечиваемого состояния и любых сопутствующих симптомов заболевания, которое нужно лечить, и других факторов,очевидных специалистам в данной области техники. Стандартная пероральная доза для взрослых находится в диапазоне 1-100 мг в день соединения настоящего изобретения, такая как 1-30 мг в день или 5-25 мг в день. Это обычно достигается приемом 0,150 мг, таким как 1-25 мг, таким как 1, 5, 10, 15, 20 25, 30, 40, 50 или 60 мг соединения настоящего изобретения один раз или дважды в день. "Терапевтически эффективное количество" соединения, как используется в данном изобретении, обозначает количество, достаточное для того, чтобы лечить, облегчать или частично приостанавливать клиническое проявление данного заболевания и его осложнений при лечебном воздействии, включающем прием упомянутого соединения. Количество, достаточное для достижения этого, определяют, как "терапевтически эффективное количество". Термин также относится к количествам, достаточным для того, чтобы лечить, облегчать или частично приостанавливать клиническое проявление данного заболевания и его осложнений при лечении, включающем прием упомянутого соединения. Эффективные количества для этих целей будут зависеть от тяжести заболевания или повреждения, также как от веса и общего состояния субъекта. Ясно, что определение подходящей дозы можно достигнуть, применяя стандартные эксперименты, составляя матрицу величин и испытывая различные точки в матрице, что находится в компетенции квалифицированного лечащего врача. Термин "лечение", как используется в данном изобретении, обозначает лечение и уход за пациентом с целью борьбы с состоянием, таким как заболевание или расстройство. Подразумевается, что термин включает полный спектр лечения данного состояния, от которого страдает пациент, такой как прием активного соединения, для того чтобы облегчить симптомы или осложнения, задержать развитие заболевания, расстройства или состояния, облегчить или ослабить симптомы и осложнения, и/или вылечить или устранить заболевание, расстройство или состояние, также как предотвратить состояние, где предотвращение понимается как лечение и уход за пациентом с целью борьбы с заболеванием, состоянием или расстройством и включает прием активных соединений для того, чтобы предотвратить начало симптомов или осложнений. Тем не менее, профилактическое (предупреждающее) и терапевтическое (лечебное) лечение являются двумя отдельными аспектами настоящего изобретения. Пациент, которого нужно лечить, является предпочтительно млекопитающим, в частности человеком. В одном варианте осуществления настоящее изобретение относится к применению соли настоящего изобретения для приготовления жидкой композиции для лечения заболевания, выбранного из расстройства настроения, большого депрессивного расстройства, генерализованного тревожного расстройства,атипичной депрессии, биполярной депрессии, социального тревожного расстройства, обсессивнокомпульсивного расстройства, панического расстройства, посттравматического стрессового расстройства, злоупотребление лекарственным средством, нарушения питания, расстройства сна, болезни Алыдгеймера, деменции, хронической боли, депрессии, связанной с когнитивными нарушениями, депрессии,связанной с психозом, когнитивных нарушений при шизофрении, депрессии или тревоги, связанной с болью, нарушений поведения у пожилых, синдрома дефицита внимания с гиперактивностью, меланхолии, депрессии, устойчивой к лечению или депрессии с остаточными симптомами. В одном варианте осуществления упомянутая жидкая композиция является концентрированной пероральной композицией. В одном варианте осуществления настоящее изобретение относится к соли настоящего изобретения для применения в лечении заболевания, выбранного из расстройства настроения, большого депрессивного расстройства, генерализованного тревожного расстройства, атипичной депрессии, биполярной депрессии, социального тревожного расстройства, обсессивно-компульсивного расстройства, панического расстройства, посттравматического стрессового расстройства, злоупотребления лекарственным средством,нарушения питания, расстройства сна, болезни Альцгеймера, деменции, хронической боли, депрессии,связанной с когнитивными нарушениями, депрессии, связанной с психозом, когнитивных нарушений при шизофрении, депрессии или тревоги, связанной с болью, нарушений поведения у пожилых, синдро-6 019695 ма дефицита внимания с гиперактивностью, меланхолии, депрессии, устойчивой к лечению или депрессии с остаточными симптомами, где упомянутая соль находится в жидкой композиции. В одном варианте осуществления упомянутая жидкая композиция является концентрированной пероральной капельной композицией. Соли настоящего изобретения можно принимать как отдельно, так и в комбинации с другим терапевтически активным соединением, где два соединения можно принимать как одновременно, так и последовательно. Примеры терапевтически активных соединений, которые предпочтительно смешивают с соединением I, включают седативные средства или снотворные средства, такие как бензодиазепины; противосудорожные средства, такие как ламотригин, вальпроевая кислота, топирамат, габапентин, карбамазепин; нормотимик, такой как литий; дофаминергические лекарственные средства, такие как агонисты дофамина и L-дофа; лекарственные средства для лечения синдрома дефицита внимания с гиперактивностью, такие как атомоксетин; психостимуляторы, такие как модафинил, кетамин, метилфенидат и амфетамин; другие антидепрессанты, такие как миртазапин, миансерин и бупроприон; гормоны, такие как Т 3, эстроген, DHEA и тестостерон; нестандартные нейролептики, такие как оланзапин и арипипразол; стандартные нейролептики, такие как галоперидол; лекарственные средства для лечения болезни Альцгеймера, такие как ингибиторы холинэстеразы и мемантин, фолат; S-аденозилметионин; иммуномодуляторы, такие как интерфероны; опиаты, такие как бепренорфины; антагонисты рецептора 1 ангиотензина II (ATI антагонисты); АСЕ ингибиторы; статины; и альфа адренергический антагонист, такой как празосин. Все ссылки, включая публикации, патентные заявки и патенты, цитируемые в данном изобретении, вводятся в данное описание полностью с помощью ссылки, и в одинаковой степени, как если бы каждая ссылка была отдельно и специально обозначена для введения с помощью ссылки, и они излагаются полностью в данном описании (до максимального объема, разрешенного законом), независимо от любого отдельно данного включения конкретных документов, сделанного в другом месте данного описания. Применение терминов "а" и "an" и "the" и аналогичных референтов в контексте описания настоящего изобретения истолковывается, как включающее как форму единственного числа, так и форму множественного числа, если не указано особо в данном описании или ясно противоречит контексту. Например,фраза "соединение" следует понимать как ссылку на различные "соединения" настоящего изобретения или конкретно описанный аспект, если не указано особо. Если не указано особо, все точные величины, представленные в описании, являются представителями соответствующих приблизительных величин (например, по необходимости, все точные величины примеров, данные относительно конкретного фактора или измерения, можно рассматривать как данные относительно соответствующего приблизительного измерения, измененные путем добавления "приблизительно"). Предполагается, что описание в настоящем изобретении любого аспекта или аспекта настоящего изобретения, применяя термины, такие как "содержащий", "обладающий", "включающий" относительно элемента или элементов подтверждает аналогичный аспект или аспект настоящего изобретения при применении терминов "состоит из", "в основном состоит из" или "в основном содержит" относительно данного конкретного элемента или элементов, если не указано особо в данном описании или ясно противоречит контексту (например, композицию, описанную в данном изобретении, как содержащую конкретный элемент, следует понимать также как описание композиции, состоящей из данного элемента,если не указано особо в данном описании или ясно противоречит контексту). Примеры Пример 1. Фармакологический профиль Пример 1 А. Ингибирование обратного захвата серотонина (5-НТ) и норэпинефрина (NE) Аликвоты испытуемого соединения и заготовки крысиной кортикальной синаптосомы предварительно выдерживали в течение 10 мин при 37 С и затем добавляли [3H]NE или [3 Н]5-НТ (конечная концентрация 10 нМ). Неспецифический захват определяли в присутствии 10 мкм талсупрама или циталопрама и суммарный захват определяли в присутствии буфера. Определенные количества выдерживали в течение 15 мин при 37 С. После выдерживания [3H]NE или [3 Н]5-НТ, поглощенный синаптосомами, отделяли фильтрацией через Unifilter GF/C, предварительно пропитанный 0, 1% PEI в течение 30 мин, применяя программу Tomtec Cell Harvester. Фильтры промывали и считали в счетчике Wallac MicroBeta. ПриNET соединение I показывало величину IC50, равную 23 нМ. При SERT соединение I показывало величину IC50, равную 8 нМ. Пример IB. 5-HT2A антагонизм Соединение I испытывали на сродство к серотониновым рецепторам и было обнаружено, что оно проявляет антагонистический профиль со сродством к 5-HT2A рецепторам (K1 54 нМ). Сродство вычисляли из Y=100/(1+10(x-logIC50, где Y обозначает % связывания и X обозначает концентрацию соединения. Применяли 5 концентраций соединения (1, 10, 30, 100, 1000 нМ) для того, чтобы вычислить величинуIC50. K1 вычисляли из уравнения Cheng Prusoff K1=(IC50/(1+([L]/Kd. Сродство определяли под MDLPharmaservices номером по каталогу 271650. В клетках млекопитающих, экспрессирующих 5-HT2A рецепторы, соединение I показало конкурентные антагонистические свойства. Соединение связывается с 5-HT2A рецепторами с Ki100 нМ, и в-7 019695 функциональном анализе соединения вызывают антагонизм 5-НТ, вызывая высвобождение Са 2+ из их внутриклеточных запасов с Kb 67 нМ. Анализ Шилда обнаружил конкурентный антагонизм с Kb 100 нМ. Эксперимент проводили следующим образом. За 2 или 3 дня перед экспериментом СНО клетки,экспрессирующие 250 фемтомоль/мг человеческих 5-HT2A рецепторов, помещали с плотностью, достаточной для того, чтобы получить непрерывный монослой ко дню эксперимента. Клетки выдерживали с красителем (Са 2+ - набор от Molecular Devices) в течение 60 мин при 37 С в 5% СО 2 инкубаторе при влажности 95%. Базальную флуоресценцию наблюдали в флуорометрическом спектрофотометре для прочтения планшетов или FLIPR от Molecular Devices (Sunnyvale, CA) с длиной волны возбуждения 488 нМ и диапазоном излучения 500-560 нМ. Интенсивность лазера устанавливали на подходящий уровень для того, чтобы получить базальные величины, приблизительно, 8000-10000 единиц флуоресценции. Отклонение в базальной флуоресценции должно быть меньше, чем 10%. Величины ЕС 50 оценивали,применяя повышенные концентрации испытуемого соединения, включая по меньшей мере 3 десятка. Величины рА 2 оценивали, рассматривая кривые эффекта полной дозы 5-НТ с четырьмя различными концентрациями соединения (150, 400 1500 и 4000 нМ). Величины Kb также оценивали, рассматривая 2 десятка концентраций испытуемых вещество с EC85 5-НТ. Испытуемые вещества добавляли к клеткам за 5 мин до 5-НТ. Величины K1 вычисляли, применяя уравнение Cheng-Prusoff. Пример 1 С. Антагонизм 5-HT3A рецептора В ооцитах, экспрессирующих гомомерные человеку 5-HT3A рецепторы, 5-НТ активировал токи с ЕС 50, равной 2600 нМ. Данный ток можно антагонизировать классическими 5-НТ 3 антагонистами, такими как ондансетрон. В данной системе ондансетрон показывает величину K1 ниже 1 нМ. Соединение I проявляет мощный антагонизм при меньших концентрациях (0,1 нМ-100 нМ) (IC50-10 нМ/ Kb 2 нМ) и агонистические свойства, при применении больших концентраций (100-100000 нМ) (ЕС 50 2600 нМ),достигая максимального тока приблизительно 70-80% максимального тока, вызванного самим 5-НТ. В ооцитах, экспрессирующих гомомерные крысе 5-HT3A рецепторы, 5-НТ активирует токи с ЕС 50, равной 3,3 мкМ. Эксперименты проводили следующим образом. Ооциты удаляли хирургически из зрелых особей Xenepus laevis женского пола, анастезируя 0,4% MS-222 в течение 10-15 мин. Затем, ооциты выдерживали при комнатной температуре в течение 2-3 ч с 0,5 мг/мл коллагеназы (тип IA Sigma-Aldrich) в OR2 буфере (82,5 мМ NaCl, 2,0 мМ KCl, 1,0 мМ MgCl2 и 5,0 мМ HEPES, рН 7,6). Ооциты, избавившиеся от слоя фолликулярных клеток, отбирали и выдерживали в течение 24 ч в модифицированном солевом буфере Барта [88 мМ NaCl, 1 мМ KCl, 15 мМ HEPES, 2,4 мМ NaHCO3, 0,41 мМ CaCl2, 0,82 мМ MgSO4, 0,3 мМ Ca(NO3)2], пополненным 2 мМ пируватом натрия, 0,1 U/1 пенициллином и 0,1 мг/1 стрептомицином. Обнаруживали ооциты стадий IV-IV и вводили 12-48 нл воды, свободной от нуклеазы, содержащей 14-50 пг cRNA, кодирующей человеческие 5-HT3A рецепторы, и выдерживали при 18 С до их применения в электрофизиологических опытах (1-7 дней после введения). Ооциты с экспрессией 5-НТ 3 рецепторов помещали в 1 мл баню и опрыскивали буфером Рингера (115 мМ NaCl 2,5 мМ KCl, 10 мМ HEPES, 1,8 мМ CaCl2, 0,1 мМ MgCl2, рН 7,5). Клетки наносили уколом на агар, снабженный 0,5-1 M электродами,содержащий 3 М KCl, с напряжением, фиксированным на -90 мВ усилителем GeneClamp 500B. Ооциты непрерывно опрыскивали буфером Рингера и применяли на перфузате лекарственные средства. Применяли растворы антагониста 5-НТ в течение 10-30 с. Активности антагонистов 5-НТ 3 рецепторов анализировали измерением концентрационного отклика относительно 10 мкМ 5-НТ стимуляции. Пример 1D. Антагонизм 1A рецепторов Соединение I испытывали на сродство к 1A рецептору и обнаружили, что оно обладает антагонистическим профилем со средним сродством к 1A рецепторам (Ki=34 нМ). В день экспериментов мембраны (см. ниже описание приготовления мембран) размораживали и гомогенизировали в буфере, применяя ultra turrax, и разбавляли до требуемой концентрации (5 мкг/лунка 5 мкг/900 мкл, хранили на льду до использования). Эксперимент начинали смешением 50 мкл испытуемого соединения, 50 мкл[3 Н]-празосина и 900 мкл мембран, и смесь выдерживали в течение 20 мин при 25 С. Неспецифическое связывание определяли в присутствии 10 мкм WB-4101 и суммарное связывание в присутствии буфера. После выдерживания связанные лиганды отделяли от несвязанных лигандов фильтрацией через Unifilter GF/B, предварительно пропитанный 0,1% PEI в течение 30 мин, применяя программу Tomtec Cell Harvester (D4.24). 96 лунок. Фильтры промывали 3 раза 1 мл ледяного буфера,сушили при 50 С и добавляли к фильтрам 35 мкл сцинтилляционной жидкости на лунку. Радиоактивность связанных лигандов считали в Wallac OY 1450 MicroBeta. Сродство вычисляли из Y=100/(1+10(xlogIC ) 50 ), в котором Y обозначает % связывания и X обозначает концентрацию соединения. Применяли концентрации соединения, включающие 2 десятка для того, чтобы вычислить величину IC50. Ki вычисляли из уравнения Cheng Prusoff Ki=(IC50/(1+( [L]/Kd. В функциональном анализе соединения настоящего изобретения вызывали антагонизм адреналина,вызывая высвобождение Са 2+ из внутриклеточных запасов, и функциональный анализ показал, что соединения являются антагонистами. Данные эксперименты проводили главным образом так, как описано ниже. Все клетки выращивали в DMEM среде, дополненной 10% BCS, 4 мМ L-глутамина (или 2 мМ в случае COS-7) и 100 едениц/мл пенициллина плюс 100 мкг/мл стрептомицина при 37 С в 5% СО 2. За 24 ч до анализов СНО клетки, экспрессирующие человеческий альфа 1A-7 рецепторы, засевали в 384-луночные титрационные микропланшеты с черными стенками, покрытые поли-D-лизином. Культуральную среду отсасывали, и клетки насыщали красителем с 1,5 мкм Fluo-4 в буфере для анализа, состоящем из сбалансированного солевого раствора Ханка (138 мМ NaCl, 5 мМ KCl, 1,3 мМ CaCl2, 0,5 мМMgCl2, 0,4 мМ MgSO4, 0,3 мМ KH2PO4, 0,3 мМ Na2HPO4, 5,6 мМ глюкозы) плюс 20 мМ HEPES рН 7,4,0,05% BSA и 2,5 мМ пробенецида (50 мкл/лунка) в течение 1 ч в 5% СО 2 при 37 С. После удаления избытка красителя клетки промывали буфером для анализа и наносили слоем с конечным объемом, равным 45 мкл/лунка (или 30 мкл/лунка в анализе на антагонизм). В случае оценки антагонизма добавляли на данном этапе антагонист или среду в виде 15 мкл аликвоты в 4% DMSO-содержащем буфере при 4 кратной конечной концентрации (конечная концентрация DMSO=1%), с последующим 20-минутным выдерживанием. Базальную флуоресценцию наблюдали в флуорометрическом спектрофотометре для прочтения планшетов или FLIPR от Molecular Devices (Sunnyvale, CA) с длиной волны возбуждения 488 нМ и диапазоном излучения 500-560 нМ. Интенсивность лазера устанавливали так, чтобы получить величины базальной флуоресценции равные приблизительно 8000 относительных единиц флуоресценции (RFU). Затем, клетки стимулировали при комнатной температуре агонистами, разбавленными в буфере для анализа (15 мкл), и RFU измеряли при 1,5-секундных интервалах в течение периода времени 2,5 мин. Рассчитывали для каждой лунки максимальное изменение флуоресценции. Кривые концентрационного отклика, полученные из максимального изменения флуоресценции, анализировали нелинейной регрессией (уравнение Хилла). Для определения антагонистической активности после 20-минутного выдерживания соединения (как показано выше) добавляли установленные концентрации стандартного агониста серотонина. Пример 2A. HBr соль 4-[2-(4-метилфенилсульфанил)фенил]пиперидина 2-(4-толилсульфонил)фенилбромид В перемешиваемом заполненном азотом реакторе N-метил-пирролидон, NMP (4,5 л) продували азотом в течение 20 мин. Добавляли 4-метилбензолтиол (900 г, 7,25 ммоль) и затем добавляли 1,2 дибромбензол (1709 г, 7,25 ммоль). Наконец, в качестве последнего вещества, вступающего в реакцию,добавляли трет-бутоксид калия (813 г, 7,25 ммоль). Реакционную смесь нагревали до 70 С за счет экзотермичности реакции. Затем реакционную смесь грели при 120 С в течение 2-3 ч. Реакционную смесь охлаждали до комнатной температуры. Добавляли этилацетат (4 л) и водный раствор хлорида натрия(15%, 2,5 л). Смесь перемешивали в течение 20 мин. Водную фазу отделяли и экстрагировали другой порцией этилацетата (2 л). Водную фазу отделяли, и органические фазы собирали и промывали раствором хлорида натрия (15%, 2,5 л) Органическую фазу отделяли, сушили над сульфатом натрия и упаривали при пониженном давлении до красного масла, которое содержало 20-30% NMP. Масло разбавляли до двойного объема метанолом и смесь кипятили с обратным холодильником. Добавляли большее количество метанола до образования прозрачного красного раствора. Раствор медленно охлаждали до комнатной температуры при затравливании. Продукт кристаллизовался в виде грязно-белых кристаллов, их выделяли фильтрацией и промывали метанолом, и сушили при 40 С в вакуумной печи до постоянного веса. Этил 4-гидрокси-4-(2-(4-толилсульфанил)фенил)пиперидин-1-карбоксилат В перемешиваемом реакторе под азотом суспендировали 2-(4-толилсульфанил)фенилбромид (600 г,2,15 ммоль) в гептане (4,5 л). Добавляли при комнатной температуре в течение 10 минут 10 М BuLi в гексане (235 мл, 2,36 ммоль). Обнаружили только небольшой экзотермический эффект. Суспензию перемешивали в течение 1 ч при температуре окружающей среды и затем охлаждали до -40 С. Добавляли 1 карбэтокси-4-пиперидон (368 г, 2,15 ммоль), растворенный в THF (1,5 л), с такой скоростью, чтобы температура реакционной среды была ниже -40 С. Когда реакция подходила к концу, реакционную смесь нагревали до 0 С и добавляли 1 М HCl (1 л), поддерживая температуру ниже 10 С. Кислую водную фазу отделяли и экстрагировали этилацетатом (1 л). Органические фазы объединяли и экстрагировали раствором хлорида натрия (15%, 1 л). Органическую фазу сушили над сульфатом натрия и упаривали до полукристаллической массы. Ее суспендировали в этиловом эфире (250 мл) и отфильтровывали. Сушили в вакуумной печи при 40 С до постоянного веса. Этил 4-(2-(4-толилсульфанил)фенил)пиперидин-1-карбоксилат Трифторуксусную кислоту (2,8 кг, 24,9 ммоль) и триэтилсилан (362 г, 3,1 ммоль) загружали в реактор с эффективной мешалкой. Добавляли через насыпную воронку порциями этил 4-гидрокси-4-(2-(4 толилсульфанил)фенил)пиперидин-1-карбоксилат (462 г, 1,24 ммоль). Реакция была слегка экзотермической. Температура повышалась до 50 С. После завершения добавления реакционную смесь грели при 60 С в течение 18 ч. Реакционную смесь охлаждали до комнатной температуры. Добавляли толуол (750 мл) и воду (750 мл). Органическую фазу отделяли, и водную фазу экстрагировали другой порцией толуола (750 мл). Органические фазы объединяли и промывали раствором хлорида натрия (15%, 500 мл) и сушили над сульфатом натрия. Сульфат натрия отфильтровывали, фильтрат упаривали при пониженном давлении до красного масла, которое дополнительно обрабатывали в следующей стадии. 4-(2-(4-толилсульфанил)фенил)пиперидин гидробромид Неочищенный этил 4-(2-(4-толилсульфанил)фенил)пиперидин-1-карбоксилат в виде красного масла из примера 3 добавляли при перемешивании в реактор с бромоводородной кислотой в уксусной кислоте(40%, 545 мл, 3,11 ммоль). Смесь грели при 80 С в течение 18 ч. Реакционную смесь охлаждали до комнатной температуры. В процессе охлаждения продукт кристаллизовался. Через 1 ч при комнатной температуре к реакционной смеси добавляли этиловый эфир (800 мл), и смесь перемешивали в течение следующего часа. Продукт отфильтровывали, промывали этиловым эфиром и сушили в вакуумной печи при 50 С до постоянного веса. Пример 2 В. HBr соль 4-[2-(4-метилфенилсульфанил)фенил]пиперидина К 442 г перемешиваемого и слегка нагретого (приблизительно, 45 С) этилового эфира 4-(2-птолилсульфанилфенил)пиперидин-1-карбоновой кислоты в виде масла добавляли 545 мл 33 вес.% HBr в АсОН (5,7 М, 2,5 экв.). Данное смешение давало 10 С экзотерм. После окончания добавления реакционную смесь нагревали до 80 С и выдерживали в течение 18 ч. Отбирали образец и анализировали с помощью ВЭЖХ, и если реакция не завершилась, добавляли большее количество 33 вес.% HBr в АсОН. В противоположном случае смесь охлаждали до 25 С, что вызывало осаждение продукта гидробромида 4(2-п-толилсульфанилфенил)пиперидина. Через 1 ч при 25 С добавляли к густой суспензии 800 мл диэтилового эфира. Перемешивание продолжали в течение следующего часа перед тем, как выделить продукт фильтрацией, промывали его 400 мл диэтилового эфира и сушили в вакууме при 40 С в течение ночи. Гидробромид соединения I отделяли в виде белого твердого остатка. Пример 2 С. Перекристаллизация HBr соли 4-[2-(4-метилфенилсульфанил)фенил]пиперидина Смесь 10 г HBr соли, например, полученной, как показано выше, нагревали до температуры кипения в 100 мл H2O. Смесь становилась прозрачной и полностью растворялась при 80-90 С. К прозрачному раствору добавляли 1 г угля и кипячения продолжали в течение 15 мин перед фильтрованием и охлаждением до комнатной температуры. В процессе охлаждения выпадал белый твердый осадок, и суспензию перемешивали в течение 1 ч при комнатной температуре. Фильтрация и сушка в вакууме при 40 С в течение ночи давали 6,9 г (69%) соли присоединения HBr к 4-[2-(4-метилфенилсульфанил)фенил]пиперидину. Пример 3. Дополнительные соли 4-[2-(4-метилфенилсульфанил)фенил]пиперидина Получение основных растворов свободного основания Смесь 500 мл этилацетата и 200 мл Н 2 О добавляли к 50 г HBr соли, получая двухфазную суспензию. К данной суспензии добавляли приблизительно 25 мл конц. NaOH, которая вызывала образование прозрачного двухфазного раствора (рН было равно 13-14). Раствор интенсивно перемешивали в течение 15 мин и органическую фазу отделяли. Органическую фазу промывали 200 мл Н 2 О, сушили над Na2SO4,фильтровали и упаривали в вакууме при 60 С, получая свободное основание с выходом 38 г (99%) в виде почти бесцветного масла. Растворение 10 г масла и доведение объема до 150 мл, применяя этилацетат, давали 0,235 М основной раствор в этилацетате, из которого отбирали аликвоту 1,5 мл (100 мг свободного основания). Растворение 10 г масла и доведение объема до 100 мл, применяя 96% по объему EtOH, давали 0,353 М основной раствор в этилацетате, из которого отбирали аликвоту 1,0 мл (100 мг свободного основания). Получение солей, применяя основные растворы свободного основания Данные аликвоты помещали в пробирки и при перемешивании добавляли подходящее количество кислоты, как показано в табл. 1. Если кислота была жидкой, ее добавляли в чистом виде, иначе ее растворяли в данном растворителе перед добавлением. После смешения и выпадения осадка, перемешивание продолжали в течение ночи, и осадок собирали фильтрацией. В табл. 2 показана растворимость солей 4-[2-(4-метилфенилсульфанил)фенил]пиперидина. Пример 4. Действие на концентрации ацетилхолина Эксперимент предназначался для оценки действия соединения I на внеклеточные концентрации ацетилхолина в префронтальной коре и вентральном гиппокампе свободно-подвижных крыс. Применяли мужские особи крыс линии Sprague-Dawley, первоначально весившие 275-300 г. Животных содержали при 12-часовом цикле день/ночь при контролируемых условиях для постоянной комнатной температуре (212 С) и влажности (555%) со свободным доступом пищи и водопроводной воды. Хирургия и микродиалитические эксперименты Крыс анестезировали гипнорм/дормикумом (2 мл/кг) и внутрицеребральные проводящие канюли(CMA/12) стереотаксически имплантировали в гиппокамп, имея целью поместить наконечник зонда для диализа в вентральном гиппокампе (координаты: 5,6 мм после брегмы, удаление от средней линии - 5,0 мм, 7,0 мМ над вентральной верхушкой проводящей канюли до твердой мозговой оболочки или в лобной коре (координаты: 3,2 мм перед брегмой; удаление от средней линии 0,8 мм; 4,0 мм над вентральной верхушкой проводящей канюли до твердой мозговой оболочки). Анкерный болт и акрилатный цемент применяли для фиксации проводящих канюль. Температуру тела животных отслеживали с помощью прямокишечного зонда и поддерживали равной 37 С. Крыс оставляли восстанавливаться после операции в течение 2 дней, содержа их в клетках по одной. В день эксперимента через проводящую канюлю вставляли зонд для микродиализа (СМА/12, 0,5 мм диаметр, 3 мм длина). Зонды соединяли через двухканальный вертлюг к насосу для микроинъекций. Перфузию зонда для микродиализа отфильтрованным раствором Рингера (145 мМ NaCl, 3 мМ KCl, 1 мМ MgCl2, 1,2 мМCaCl2, содержащими 0,5 мкм неостигмина) начинали незадолго до введения зонда в мозг и продолжали в течение эксперимента при постоянной скорости потока 1 мкл/мин. Через 180 мин стабилизации начинали эксперименты. Диализаты собирали каждые 20 мин. После экспериментов животных умерщвляли,удаляли их мозг, замораживали и нарезали для проверки размещения зонда. Анализы ацетилхолина в диализате Концентрацию ацетилхолина (ACh) в диализатах анализировали с помощью ВЭЖХ с электрохимическим детектированием, применяя подвижную фазу, содержащую 100 мМ гидрофосфата натрия, 2,0 мМ октановой серной кислоты, 0,5 мМ тетраметиламмоний хлорида и 0,005% MB (ESA), рН 8,0. В находящемся перед колонкой ферментном реакторе (ESA), содержащем иммобилизованную оксидазу холина,удаляли холин из введенного образца (10 мкл) перед выделением ACh на аналитической колонке (ESAACH-250); скорость потока 0,35 мкл/мин, температура: 35 С. После аналитической колонки образец пропускали через находящийся после колонки твердофазный реактор (ESA), содержащий иммобилизованные ацетилхолинэстеразу и оксидазу холина. В последнем реакторе происходило превращение ACh в холин и впоследствии холина до бетаина и Н 2 О 2. Последний детектировали электрохимически, применяя платиновый электрод (Analytical cell: ESA, model 5040). Представление данных В экспериментах на единичное введение среднее значение 3 последовательных ACh выборок, непосредственно предшествующих приему соединения, служило в качестве исходной концентрации для каждого эксперимента, и данные переводили в проценты относительно исходной концентрации (среднее значение исходной концентрации перед введением, нормированное к 100%). Данные представлены на фиг. 1 а и 2b. Данные, представленные на фиг. 1 а и 1b, показывают зависимое от дозы увеличение внеклеточной концентрации ацетилхолина в мозге. Ожидают, что данное доклиническое открытие будет превращено в знание в клинической ситуации, пригодное, например, для лечения когнитивных нарушений и заболеваний, характеризующихся когнитивными нарушениями. Пример 5. Действие на концентрации дофамина Единичное введение соединения I увеличивало зависимым от дозы способом внеклеточные концентрации дофамина (DA) в лобной коре крыс. Соединение настоящего изобретения с концентрацией 8,9 и 18 мг/кг, введенной подкожно, увеличивали концентрации DA приблизительно на 100 и 150%, соответственно больше исходных концентраций, как показано на фиг. 2. Количества рассчитывали для свободного основания. Способ Применяли мужские особи крыс линии Sprague-Dawley, первоначально весившие 275-300 г. Животных содержали при 12-часовом цикле день/ночь при контролируемых условиях для постоянной комнатной температуре (212 С) и влажности (555%) со свободным доступом пищи и водопроводной воды. В течение трехдневных терапевтических экспериментов применяли осмотический мининасос (Alzet,2ML 1). Насосы наполняли при асептических условиях и вводили подкожно при анестезии севофлураном. Настоящие эксперименты проводили с мининасосами в рабочем положении. В конце экспериментов собирали образцы крови для измерения концентраций в плазме испытуемого соединения после 3 дней лечения. Хирургия и микродиалитические эксперименты Крыс анестезировали гипнорм/дормикумом (2 мл/кг) и имплантировали внутрицеребральные проводящие канюли (СМА/12) стереотаксически в гиппкамп, помещая наконечник зонда для диализа в вентральном гиппокампе (координаты: 5,6 мм после брегмы, удаление от средней линии - 5,0, 7,0 мм над вентральной верхушкой проводящей канюли до твердой мозговой оболочки или в лобной коре (координаты: 3,2 мм перед брегмой; удаление от средней линии 3,0 мм; 4,0 мм над вентральной верхушкой проводящей канюли до твердой мозговой оболочки). Анкерный болт и акрилатный цемент применяли для фиксации проводящих канюль. Температуру тела животных отслеживали с помощью прямокишечного зонда и поддерживали равной 37 С. Крыс оставляли восстанавливаться после операции в течение 2 дней,содержа их в клетках по одной. В день эксперимента через проводящую канюлю вставляли зонд для микродиализа (СМА/12, 0,5 мм диаметр, 3 мм длина). Зонды соединяли через двухканальный вертлюг к насосу для микроинъекций. Перфузию зонда для микродиализа отфильтрованным раствором Рингера(145 мМ NaCl, 3 мМ KCl, 1 мМ MgCl2, 1,2 мМ CaCl2, содержащими 0,5 мкм неостигмина) начинали незадолго до введения зонда в мозг и продолжали в течение эксперимента при постоянной скорости потока 1 (1,3) мкл/мин. Через 180 мин стабилизации начинали эксперименты. Диализаты собирали каждые 20(30) мин. После экспериментов животных умерщвляли обезглавливанием, удаляли их мозг, заморажива- 13019695 ли и нарезали для проверки размещения зонда. Анализ диализата Концентрацию дофамина в диализатах анализировали с помощью ВЭЖХ с электрохимической детекцией. Моноамины отделяли обращено-фазной жидкостной хроматографией (ODS 1503 мм, 3 мкм). Дофамин: подвижная фаза, состоящая из 90 мМ NaH2PO4, 50 мМ цитрата натрия, 367 мг/л натриевой соли 1-октансульфоновой кислоты, 50 мкм EDTA и 8% ацетонитрила (рН 4,0) при скорости потока 0,5 мл в минуту. Электрохимическую детекцию осуществляли, применяя кулонометрический детектор; потенциал устанавливали на 250 мВ (защитный элемент на 350 мВ) (Coulochem II, ESA). Пример 6. Действие на нейропатическую боль Чтобы продемонстрировать эффективность против нейропатической боли, соединение I испытывали в формалиновой модели нейропатической боли [Neuropharm., 48, 252-263, 2005; Pain, 51, 5-17, 1992]. В данной модели мышам вводили формалин (4,5%, 20 мкл) в подошвенную поверхность левой задней лапы и впоследствии помещали в отдельные аналитические стаканы (2/ емкость) для наблюдения. Раздражение, вызванное введением формалина, вызывало характерную двухфазную поведенческую реакцию, выраженную количеством времени, потраченным на лизание поврежденной задней лапы. Первая фаза (-0-10 мин) представляет прямое химическое раздражение и ноцицепцию, тогда как полагают, что вторая фаза (-20-30 мин) представляет боль нейропатического происхождения. Две фазы разделялись периодом покоя, в течение которого поведение становилось нормальным. Измерение количества времени, затраченного на лизание поврежденной задней лапы в двух фазах, определяло эффективность испытуемых соединений для того, чтобы уменьшить болевой стимул. На группу испытывали восемь С 57/В 6 мышей (приблизительно 25 г). В табл. 3 ниже показано количество времени, затраченное на лизание поврежденной задней лапы в двух фазах, т.е. 0-5 мин и 20-30 мин после введения формалина. Количество принятого соединения рассчитывали для свободного основания. Таблица 3 Данные в табл. 3 показывают, что соединение I обладает слабым действием на первую фазу, представленную прямым химическим раздражением и ноцицепцией. Более заметно, данные также показывают отчетливое и зависимое от дозы уменьшение времени, затраченного на лизание поврежденной задней лапы во второй фазе, свидетельствуя о действии соединения I при лечении нейропатической боли. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Жидкая фармацевтическая композиция,содержащая соль 4-[2-(4 метилфенилсульфанил)фенил]пиперидина, выбранную из соли присоединения DL-молочной кислоты,соли присоединения глутаровой кислоты, соли присоединения L-аспарагиновой кислоты и соли присоединения глутаминовой кислоты. 2. Жидкая композиция по п.1, в которой солью является соль присоединения DL-молочной кислоты. 3. Жидкая композиция по п.1, в которой солью является соль присоединения глутаровой кислоты. 4. Жидкая композиция по п.1, в которой солью является соль присоединения L-аспарагиновой кислоты. 5. Жидкая композиция по п.1, в которой солью является соль присоединения глутаминовой кислоты. 6. Жидкая композиция по любому из пп.1-5, в которой концентрация соли составляет выше 5 мг/мл. 7. Способ лечения заболевания, выбранного из расстройства настроения, большого депрессивного расстройства, генерализованного тревожного расстройства, атипичной депрессии, биполярной депрессии, социального тревожного расстройства, обсессивно-компульсивного расстройства, панического расстройства, посттравматического стрессового расстройства, злоупотребления лекарственным средством,нарушения питания, расстройства сна, болезни Альцгеймера, деменции, хронической боли, депрессии,связанной с когнитивными нарушениями, депрессии, связанной с психозом, когнитивных нарушений при шизофрении, депрессии или тревоги, связанной с болью, нарушений поведения у пожилых, синдрома дефицита внимания с гиперактивностью, меланхолии, депрессии, не поддающейся лечению, или депрессии с остаточными симптомами, причем упомянутый способ включает введение терапевтически эффективного количества жидкой композиции по любому из пп.1-6 нуждающемуся в ней пациенту. 8. Способ по п.7, в котором дозируют предварительно определенный объем жидкой композиции и полученный в результате объем композиции добавляют в стакан с жидкостью, после чего жидкость вводят пациенту. 9. Применение соли 4-[2-(4-метилфенилсульфанил)фенил]пиперидина, выбранной из соли присое- 14019695 динения DL-молочной кислоты, соли присоединения глутаровой кислоты, соли присоединения Lаспарагиновой кислоты и соли присоединения глутаминовой кислоты, для получения жидкого лекарственного средства для лечения заболевания, выбранного из расстройства настроения, большого депрессивного расстройства, генерализованного тревожного расстройства, атипичной депрессии, биполярной депрессии, социального тревожного расстройства, обсессивно-компульсивного расстройства, панического расстройства, посттравматического стрессового расстройства, злоупотребления лекарственным средством, нарушения питания, расстройства сна, болезни Альцгеймера, деменции, хронической боли, депрессии, связанной с когнитивными нарушениями, депрессии, связанной с психозом, когнитивных нарушений при шизофрении, депрессии или тревоги, связанной с болью, нарушения поведения у пожилых,синдрома дефицита внимания с гиперактивностью, меланхолии, депрессии, устойчивой к лечению, или депрессии с остаточными симптомами. 10. Применение по п.9, в котором солью является соль присоединения DL-молочной кислоты. 11. Применение по п.9, в котором солью является соль присоединения глутаровой кислоты. 12. Применение по п.9, в котором солью является соль присоединения L-аспарагиновой кислоты. 13. Применение по п.9, в котором солью является соль присоединения глутаминовой кислоты. 14. Применение по любому из пп.9-13, в котором лекарственное средство содержит более 5 мг/мл соли.
МПК / Метки
МПК: A61K 31/451, A61K 9/08, A61P 25/00
Метки: солей, композиции, жидкие, 4-[2-(4-метилфенилсульфанил)фенил]пиперидина
Код ссылки
<a href="https://eas.patents.su/17-19695-zhidkie-kompozicii-solejj-4-2-4-metilfenilsulfanilfenilpiperidina.html" rel="bookmark" title="База патентов Евразийского Союза">Жидкие композиции солей 4-[2-(4-метилфенилсульфанил)фенил]пиперидина</a>
Предыдущий патент: Озоновая система очистки
Следующий патент: Гипоаллергенные варианты главного аллергена из пыльцы betula verrucosa
Случайный патент: Способ получения найлона-6