Производные циклопентенона
Номер патента: 2354
Опубликовано: 25.04.2002
Авторы: Кобаяси Ейдзи, Сиба Тецуо, Като Икуносин, Инами Каору, Кояма Нобуто
Формула / Реферат
1. Производное циклопентенона, представленное следующей формулой [I], или его оптически активное вещество, или его соль
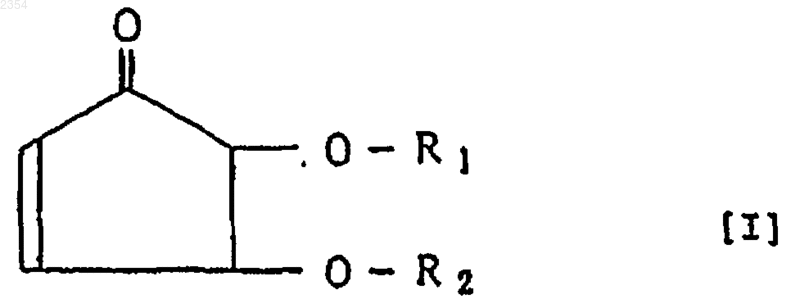
где R1 и R2 являются одинаковыми или различными и каждый из них является C1-C18 алкильной группой с прямой или разветвленной цепью, С3-С20 алкенильной группой с прямой или разветвленной цепью, С6-С10 арильной группой, С7-С9 арилалкильной группой или Н, при условии, что случай, когда R1=R2=бензильная группа, R1=R2=H или R1=бензильная группа и R2=H, исключен.
2. Способ получения производного циклопентенона, представленного формулой [II]
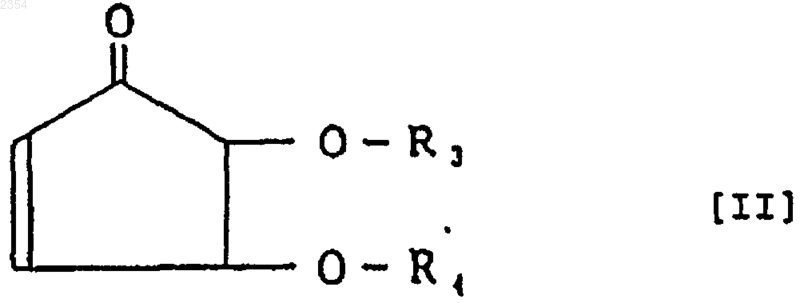
где R3 и R4 являются одинаковыми или различными и каждый из них является C1-C18 алкильной группой с прямой или разветвленной цепью, С3-С20 алкенильной группой с прямой или разветвленной цепью, С6-С10 арильной группой, С7-С9 арилалкильной группой или Н, при условии, что случай, когда R3=R4=H, исключен, отличающийся тем, что 4,5-дигидрокси-2-циклопентен-1-он, представленный следующей формулой (III)
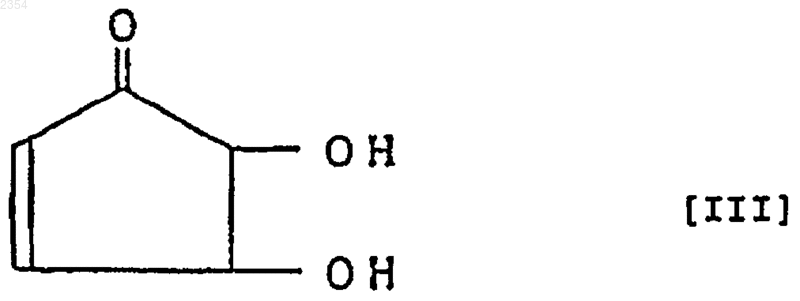
и/или его оптически активное производное подвергают взаимодействию либо одновременно, либо последовательно, со спиртом и/или его реакционноспособным производным, соответствующим R3 и R4 производного циклопентенона, представленного формулой [II].
3. Фармацевтическое средство, характеризующееся содержанием в качестве эффективного компонента, по меньшей мере, одного соединения, выбранного из производного циклопентенона, его оптически активного вещества или его соли по п.1.
4. Фармацевтическое средство по п.3, которое представляет собой противораковое средство.
5. Фармацевтическое средство по п.3, которое представляет собой апоптоз-индуцирующее средство.
6. Фармацевтическое средство, характеризующееся содержанием в качестве эффективного компонента, по меньшей мере, одного соединения, выбранного из производного циклопентенона, полученного способом по п.2, его оптически активного вещества или его соли.
7. Фармацевтическое средство по п.6, которое представляет собой противораковое средство.
8. Фармацевтическое средство по п.6, которое представляет собой апоптоз-индуцирующее средство.
Текст
1 Область техники Настоящее изобретение относится к производному циклопентенона, полезному в области фармацевтических средств, обладающих физиологической активностью, например противораковым действием, а также к способу получения таких соединений. Предшествующий уровень техники Фармацевтические средства, применяемые в клинической терапии, включают множество средств, например, противораковые средства,антибиотики, иммуностимуляторы, иммуномодуляторы и т.д. (например, алкилирующие средства, антиметаболиты и растительные алкалоиды), но едва ли можно сказать, что такая лекарственная терапия уже полностью создана. Сообщалось, что среди этих средств, из простагландинов, полученных из природных веществ, в качестве высокобезопасного противоракового средства, вследствие их ингибирования синтеза ДНК, можно применять простагландины А и J, имеющие ,-ненасыщенный карбонил в пятичленном кольце, и были синтезированы их различные прoизводные (смотри выложенную патентную публикацию ЯпонииSho-62/96438). Проблемы, решаемые изобретением Целью настоящего изобретения является получение производного циклопентенона, обладающего физиологическим действием, например, противораковым действием и т.д., и обеспечение способа получения упомянутых соединений и фармацевтических средств, содержащих такие соединения. Средства для решения проблем Настоящие изобретатели провели интенсивные исследования для достижения вышеназванных целей и обнаружили, что производное циклопентенона, представленное формулой [II],получают путем взаимодействия 4,5-дигидрокси-2-циклопентен-1-она (далее циклопентенон), представленного формулой [III], со спиртом и/или с его реакционноспособным производным, и что производное циклопентенона настоящего изобретения обладает различной сильной физиологической активностью, например, активностью, ингибирующей рост раковых клеток и т.д., на основе проведенных исследований и было создано настоящее изобретение. Настоящее изобретение можно кратко изложить следующим образом. Первый объект настоящего изобретения относится к производному циклопентенона, представленному следующей формулой (I), или его оптически активному веществу или его соли.(В формуле R1 и R2 являются одинаковыми или различными, и каждый из них является алкильной группой с прямой или разветвленной цепью, алкенильной группой с прямой или раз 002354 2 ветвленной цепью, ароматической группой,ароматической-алифатической группой или Н,при условии, что вариант, когда R1 = R2 = бензильная группа, R1 = R2 = Н или R1 = бензильная группа и R2 = Н, исключен). Второй объект настоящего изобретения относится к способу получения производного циклопентенона, представленного формулой[II], отличающемуся тем, что 4,5-дигидрокси-2 циклопентен-1-он, представленный следующей формулой [III], и/или его оптически активное производное взаимодействуют(ет), либо одновременно либо последовательно, со спиртом и/или его реакционно способным производным, соответствующим R3 и R4 производного циклопентенона,представленного формулой [II]. В формуле R3 и R4 являются одинаковыми или различными, и каждый из них является алкильной группой с прямой или разветвленной цепью, алкенильной группой с прямой или разветвленной цепью, ароматической группой,ароматической-алифатической группой или Н,при условии, что случай, когда R3=R4=H, исключен. Третьим объектом настоящего изобретения является фармацевтическое средство, которое характеризуется тем, что оно содержит в качестве активного компонента соединение, выбранное из производного циклопентенона, его оптически активного вещества или его соли,являющихся первым объектом настоящего изобретения. Четвертым объектом настоящего изобретения является фармацевтическое средство, которое характеризуется тем, что оно содержит в качестве активного компонента соединение,выбранное из производного циклопентенона,его оптически активного вещества или его соли,полученное способом, являющимся вторым объектом настоящего изобретения. В предпочтительном варианте третьего и четвертого объектов настоящего изобретения,упомянутое фармацевтическое средство представляет собой противораковое средство, индуктор апоптоза, или антибактериальное средство. Краткое описание рисунков Фиг. 1 показывает спектр 1H-ЯМР 4 бензилциклопентенонового эфира; фиг. 2 - спектр 1H-ЯМР 5-бензилциклопентенонового эфира; фиг. 3 - спектр 1H-ЯМР 4,5-дибензилциклопентенонового эфира;(+)циклопентенона; фиг. 9 - взаимосвязь между количеством 4 трет-бутилциклопентенонового эфира или 4,5 ди-трет-бутилциклопентенонового эфира и степенью увеличения отека стопы. Варианты исполнения изобретения Далее настоящее изобретение будет описано более подробно. Применяемый в настоящем изобретении циклопентенон, представленный формулой (III),охватывает оба изомера, у которых конфигурации гидроксильных групп в 4- и 5-положениях представляют собой цис- и транс-конфигурации. В настоящем изобретении может быть использован любой из цис-циклопентенона, трансциклопентенона и смеси цис- и транс-циклопентенона. Можно также применять их оптически активные вещества. Цис-циклопентенон может быть получен химическим синтезом [Helvetica Chimica Acta,Volume 55, pages 2838-2844 (1972)]. Трансциклопентенон может быть получен или путем химического синтеза [Carbohydrate Res., volume 247, pages 217-222 (1993)] или нагреванием уроновой кислоты, например, глюкуроновой кислоты, производного уроновой кислоты, например,глюкуронолактона и т.д. (смотри PCT/JP 97/03052). В настоящем изобретении можно также применять такой нагретый продукт или частично очищенный продукт, или очищенный продукт. Так например, когда в качестве уроновой кислоты применяют D-глюкуроновую кислоту и ее 1% раствор нагревают в течение четырех часов при 121 С, в термообработанном веществе получается циклопентенон. Находящийся в термообработанном веществе циклопентенон экстрагируют растворителем и экстракт концентрируют. Затем концентрированный экстракт разделяют посредством колоночной хроматографии на силикагеле, концентрируют фракцию элюированного циклопентенона, экстрагируют циклопентенон из концентрата хлороформом, и экстракт концентрата подвергают колоночной хроматографии с нормальной фазой, после чего выделяют находящийся в термообработанном веществе циклопентенон. Физические свойства циклопентенона представлены ниже. В данном случае масс 002354 4 спектрометрический анализ циклопентенона проводили с применением масс-спектрометра(изготовленного фирмой Nippon Denshi) проводили измерение ЯМР с применением в качестве растворителя тяжелого хлороформа. Постоянную оптического вращения измеряли посредством поляриметра DIP-370 (изготовленного фирмой Nippon Bunko); ультрафиолетовый спектр поглощения измеряли посредством спектрофотометра UV-2500 (изготовленного Shimadzu); и инфракрасный спектр поглощения (ИК) измеряли посредством инфракрасного спектрофотометра (изготовленного Shimadzu). MS m/z 115H ЯМР (CDCl3):4,20 (1 Н, д, J=2,4 Гц, 5 Н), 4,83 (1 Н, м, 4-Н), 6,30 (1 Н, дд, J=1,2, 6,1 Гц,2-Н), 7,48 (1H, дд, J=2,1, 6,1 Гц, 3-Н). В данном случае, значение химического сдвига 1H-ЯМР представлено на основе того,что значение химического сдвига СНСl3 составлило 7,26 час. на млн (ppm). Оптическое вращение: []D20 0 (с 1,3, вода) УФ: mах 215 нм (вода) ИК (метод КВr): поглощения были отмечены при 3400, 1715, 1630, 1115, 1060, 1025 см-1. Когда выделенный циклопентенон подвергают оптическому разделению, получают (-)4,5-дигидрокси-2-циклопентен-1-он и (+)-4,5 дигидрокси-2-циклопентен-1-он. Совершенно ясно, что циклопентенон, полученный методом синтеза, может быть также подвергнут оптическому разделению. Например, циклопентенон растворяют в этаноле. Затем к этанольному раствору для получения раствора циклопентенона добавляют гексан/этанол (94/6). Циклопентенон может быть оптически разделен, когда эту пробу раствора подвергают HPLC (высокоэффективной жидкостной хроматографии) с применением,например, Chiral Pack AS (изготовитель DaicelChemical Industries) при таком условии, что температура колонки составляет 40 С и подвижной фазой является гексан/этанол (94/6). Оптическое вращение оптически разделенного (-)-транс-4,5-дигидрокси-2-циклопентен-1-она (далее обозначен как (-)-циклопентенон) является следующим: []D20 -105 (с 0,30,этанол), тогда как оптическое вращение оптически разделенного (+)-транс-4,5-дигидрокси-2 циклопентен-1-она (далее (+)-циклопентенон) является следующим []D20 +104 (с 0,53, этанол). В данном случае, оптическое вращение измеряли вышеупомянутым поляриметром типа(-)циклопентенона и (+)-циклопентенона подвергали структурному анализу посредством анали 5 за и ядерного магнитного резонанса (ЯМР), измерению ультрафиолетового спектра поглощения и измерению инфракрасного спектра поглощения посредством вышеупомянутых методов. В результате оба оптически активных вещества показали такой же результат, какой показал циклопентенон перед оптическим разделением. Каждый из оптически разделенных (-)циклопентенона и (+)-циклопентенона превращали в производное n-диметиламинобензоила, с применением дисперсиметра типа J-720 для измерения кругового дихроизма (изготовленного фирмой Nippon Bunko) измерили спектр кругового дихроизма (CD) и к полученному результату для определения конфигурации применили правило хиральности дибензоата [J. Am. Chem.CD (круговой дихроизм) n-диметиламинобензоильного производного (-)-циклопентанона и стереоструктура (-)-циклопентенона показаны на фиг. 7. На фигуре на оси ординат показан молярный круговой дихроизм, тогда как на оси абсцисс показана длина волны (нм). В данном случае вышеприведенная стереоструктура представлена ниже в виде формулы [IV]:CD (круговой дихроизм) n-диметиламинобензоильного производного (+)-циклопентанона и стереоструктура (+)-циклопентенона показаны на фиг. 8. На фигуре на оси ординат показан молярный круговой дихроизм, тогда как на оси абсцисс показана длина волны (нм). В данном случае вышеприведенная стереоструктура представлена ниже в виде формулы [V]: Как показано на фиг. 7 и 8 и как следует из формулы [IV] и формулы [V] (-)-циклопентенон представляет собой(-)-(4R,5S)-транс-4,5 дигидрокси-2-циклопентен-1-он, тогда как (+)циклопентенон представляет собой (+)-(4S,5R)транс-4,5-дигидрокси-2-циклопентен-1-он. Вышеупомянутые циклопентеноны или их оптически активные вещества могут быть получены посредством любого способа, т.е. они могут быть получены посредством способа, раскрытого в этом описании, или посредством другого химического синтеза; в настоящем изобретении могут быть использованы транс- и цисциклопентенон, их смесь или их оптически активные вещества. Когда циклопентенон и/или его оптически активное вещество подвергают взаимодействию, или одновременно или последовательно,со спиртом и/или его реакционноспособным производным, имеющим алкильную группу с 6 прямой или разветвленной цепью, алкенильную группу с прямой или разветвленной цепью,ароматическую группу или ароматическуюалифатическую группу, в реакционном растворе получается производное циклопентенона настоящего изобретения, представленное формулой [II], или его оптически активное вещество. В качестве спирта, имеющего алкильную группу, может быть использован спирт, имеющий алкильную группу с прямой или разветвленной цепью, и длина алкильной цепи может быть подходяще выбрана в соответствии с биологической активностью, растворимостью и т.д. производного циклопентенона. Примерами подходящих спиртов, имеющих алкильную группу с прямой цепью, являются метанол, этанол, пропанол, бутанол, пентанол, гептанол, гексанол, октанол, нонанол,деканол, лауриловый спирт, миристиловый спирт, пальмитиловый спирт и стеариловый спирт. Примерами подходящих спиртов, имеющих алкильную группу с разветвленной цепью,являются изобутиловый спирт, трет-бутиловый спирт, изоамиловый спирт и трет-амиловый спирт. Что касается спирта, имеющего алкенильную группу, то может быть использован спирт,имеющий алкенильную группу с прямой или разветвленной цепью, и длина цепи, степень ненасыщенности и положение ненасыщенной связи алкенильной группы могут быть подходяще выбраны в соответствии с биологической активностью, растворимостью и т.д. производного циклопентенона. Примерами подходящих спиртов, имеющих алкенильную группу с прямой цепью, являются виниловый спирт, кротоновый спирт и 3-гексен-1-ол. Примерами подходящих спиртов, имеющих алкенильную группу с разветвленной цепью, являются гераниол, фарнезол, геранилгераниол, ретинол, линалоол, неролидол и нерол. Примерами подходящих спиртов, имеющих ароматическую группу, являются фенол,крезол, нитрофенол, хлорфенол, бромфенол,катехол, резорцин, гидрохинон и нафтол, и спирт, имеющий соответствующую ароматическую группу, может быть выбран в соответствии с биологической активностью, растворимостью и т.д. получаемого производного циклопентенона. Примерами подходящего спирта, имеющего ароматическую-алифатическую группу, являются бензиловый спирт, фенетиловый спирт,фенациловый спирт, стиролгликоль и фенилпропанол, и спирт, имеющий соответствующую аралкильную группу, может быть выбран в соответствии с биологической активностью, растворимостью и т.д. получаемого производного циклопентенона. 7 Примерами реакционноспособного производного спирта, применяемого в настоящем изобретении, являются галоидалкилы, галоидарилы, кислые эфиры, диазосоединения, соли и алкены, которые представляют собой дегидратированные продукты спирта, и в зависимости от цели может быть получено подлежащее применению реакционноспособное производное спирта. Реакцию спирта и/или его реакционноспособного производного с циклопентеноном можно осуществить таким образом, чтобы получитьR3 и R4 производного циклопентенона, представленного формулой (II), одинаковыми, оставить один из R3 и R4 непрореагировавшим водородом, или получить R3 и R4 различными. Таким образом, две гидроксильные группы циклопентенона могут быть подвергнуты одновременному взаимодействию; одна из них может быть подвергнута реакции; спирт, в котором R3 и R4 являются различными, и/или его реакционноспособное производное могут быть подвергнуты одновременному взаимодействию с циклопентеноном; или спирт, в котором R3 и R4 являются различными, и/или его реакционноспособное производное может быть подвергнуто последовательному взаимодействию с циклопентеноном. Можно эффективно получить производное циклопентенона, где спирт, в котором R3 и R4 являются различными, или производное циклопентенона, в котором одна из групп R3 и R4 этерифицирована, когда одна из гидроксильных групп циклопентенона защищена. В данном случае, в производном циклопентенона, представленном формулой (I) предложенным настоящим изобретением, R1 и R2 в указанном производном циклопентенона могут быть одинаковыми, один из R1 и R2 в нем может быть непрореагировавшим водородом, или R1 иR2 могут быть также различными. Производное циклопентенона или его оптически активное вещество, которое получают посредством реакции циклопентенона или его оптически активного вещества со спиртом и/или его реакционнoспособным производным имеет высокую ингибирующую активность в отношении роста онкогенов и могут быть очищены и выделены из реакционного раствора с использованием указанной активности в качестве показателя. Способы очистки и выделения могут быть известными способами очистки, например, химическими и физическими способами. Таким образом общеизвестные способы, например,гель-фильтрация, фракционирование с применением разделяющей по молекулярному весу мембраны, экстракция растворителем, фракционная перегонка и различные хроматографические методы, с применением ионного обмена,нормальной фазы, обращенной фазы и т.д., объединяются, посредством чего можно очистить и 8 выделить производное циклопентенона или его оптически активное вещество. Так, например, циклопентенон или его оптически активное вещество и трихлорацетимидат бензилового спирта или трет-бутилового спирта растворяют в потоке аргона и добавляют к смеси раствор комплекса трифторид борадиэтиловый эфир и подвергают взаимодействию с получением производного циклопентенона настоящего изобретения. Когда циклопентенон или его оптически активное вещество растворяют в тетрагидрофуране и затем к нему добавляют галоидалкил и гидрид натрия и подвергают взаимодействию,получают производное циклопентенона настоящего изобретения. Когда циклопентенон или его оптически активное вещество растворяют в диоксане и затем к нему добавляют гидроксид калия и диметилсульфат и подвергают взаимодействию,образуется производное циклопентенона настоящего изобретения. Когда циклопентенон или его оптически активное вещество растворяют в дихлорметане и затем добавляют диизопропилэтиламин и тетрафторборат триэтилоксония и подвергают взаимодействию, получают производное циклопентенона настоящего изобретения. Кроме того, производное циклопентенона настоящего изобретения получают, когда циклопентенон или его оптически активное вещество растворяют в дихлорметане и затем к нему добавляют трифторметансульфоновую кислоту и алкен и подвергают взаимодействию. Производное циклопентенона настоящего изобретения, которое получается как таковое, в случае необходимости, может быть очищено и выделено известными способами, например,экстракцией растворителем, колоночной хроматографией и тонкослойной хроматографией. Разделение оптически активных веществ производного циклопентенона, полученного по настоящему изобретению, можно осуществить подвергая рацемическую смесь механическому разделению, предпочтительной кристаллизации,разделению посредством кристаллизации в виде диастереомерных солей или в виде соединений включения, динамическому разделению с применением ферментов или микроорганизмов,разделению посредством хроматографии и т.д. В случае разделения посредством хроматографии могут быть применены газовая хроматография, жидкостная хроматография, тонкослойная хроматография и т.д., также может быть применена хиральная стационарная фаза, которая является подходящей для каждого из указанных методов. При оптическом разделении посредством жидкостной хроматографии может быть применен метод, использующий хиральную стационарную фазу, метод, использующий хиральный элюат, разделение в виде диастереомеров и т.д. 9 В качестве хиральной стационарной фазы могут быть использованы стационарная фаза типа амида, стационарная фаза типа мочевины,стационарная фаза лигандобменного типа, стационарная фаза на основе производного полисахарида-полисахарида, протеиновая стационарная фаза, стационарная фаза на основе полиметакрилата, стационарная фаза на основе полиметакриламида и т.д. Что касается элюирующей жидкости, то принимая во внимание сочетание с вышеупомянутой стационарной фазой могут быть подходяще использованы элюирующие жидкости типа гексана, спирта, воды (буфера) и т.д. Что касается соли соединения настоящего изобретения или его оптически активного вещества, то примерами таких солей могут служить соли, которые являются приемлемыми в качестве фармацевтических средств, и они могут быть получены путем превращения посредством известных способов. Производное циклопентенона настоящего изобретения, представленное формулой (I) или(II) (далее обозначенное производное циклопентенона настоящего изобретения), его оптически активное вещество или его соль обладают физиологической активностью, например, противораковой активностью, активностью ингибирования роста раковых клеток, апоптозиндуцирующей активностью, активностью ингибирования топоизомеразы II, активностью,индуцирующей дифференциацию раковых клеток, антиревматической активностью, активностью ингибирования хронического суставного ревматизма, активностью идуцирования продуцирование Fas-антигена, антибактериальной активностью, антивирусной активностью, активностью улучшения функции печени, активностью индуцирования белков теплового тока,активностью, нормализующей компоненты крови, активностью, повышающей противоопухолевый иммунитет, противовоспалительной активностью, ингибирующей активностью экспрессии фактора некроза опухоли, ингибирующей активностью в отношении продуцирования оксида азота, иммуномодулирующей активностью, например, ингибирующей активностью в отношении гиперчувствительности замедленного типа, ингибирующей активностью в отношении трансформации лимфоцитов, ингибирующей активностью в отношении реакции смешанных лимфоцитов, ингибирующей активностью в отношении продуцирования IgE и ингибирующей активностью в отношении отека, индуцированного карагиноном, и вследствие таких активностей, фармацевтическое средство, содержащее в качестве активного компонента, по меньшей мере, одно соединение, которое выбирают из производного циклопентенона настоящего изобретения, его оптически активного вещества или его соли, является пригодным в качестве лекарственного средства, действующего 10 на биоиммунитетную функцию, например, фармацевтического препарата, действующего на функцию продуцирования антител, противовоспалительного средства, противоревматического средства, индуцирующего интерферон, в качестве лекарственного средства, оказывающего действие на обмен сахаридов, например, лекарственного средства для лечения сахарного диабета, и в качестве лекарственного средства, действующего на патогенные организмы, например, в качестве антибактериального средства и антивирусного средства. Соответственно фармацевтическое средство, полученное настоящим изобретением, является полностью пригодным в качестве лекарственного средства для заболеваний, которые показывают чувствительность к соединению настоящего изобретения, его оптически активному веществу или его соли, т.е. в качестве лекарственного средства для терапии или профилактики, например, рака, вирусных заболеваний, ревматизма, сахарного диабета,аллергии, аутоаллергических болезней, воспалений и т.д. Производное циклопентенона настоящего изобретения, его оптически активное вещество или его соль обладают подавляющим действием роста клеток, действием на опухолевые клетки,например, клетки промиелоцитарного лейкоза человека HL-60, клетки острого лимфобластного лейкоза человека MOLT-3, легочные раковые клетки А-549, легочные раковые клетки WI38VA13, трансформированные SV-40, гепатомные клетки Нер G2, раковые клетки толстой кишки НСТ 116, раковые клетки толстой кишки человека SW 480, раковые клетки толстой кишки человека Wi Dr, раковые клетки желудкаAGS и клетки миеломы. Противораковое средство может быть получено, когда, по меньшей мере, одно из соединений, выбранное из производного циклопентенона настоящего изобретения, его оптически активного вещества или его соли, используют в качестве активного компонента и смешивают с известными фармацевтическими носителями для получения фармацевтического препарата. Механизм противораковой активности производного циклопентенона, его оптически активного вещества или его соли, полученных настоящим изобретением, совсем не огpаничивает объем настоящего изобретения, например,апоптоз-индуцирующее действие и активность ингибирования топоизомеразы на раковые клетки также охвачены противораковой активностью соединений настоящего изобретения. Обычно, соединение, выбранное из производного циклопентенона настоящего изобретения, его оптически активного вещества или его соли, смешивают с фармацевтически приемлемым жидким или твердым носителем и, если необходимо, добавляются растворитель, диспергатор, эмульгатор, буфер, стабилизатор, наполнитель, связующее вещество, разрыхлитель, 11 смазка и т.д., для получения противоракового средства, которое может быть в твердом виде,например в виде таблеток, гранул, разбавленных порошков, порошков, капсул и т.д., или в виде жидкости, например растворов, суспензий,эмульсий и т.д. Кроме того, противораковое средство может быть в виде сухого препарата,который может быть превращен перед применением в жидкость добавлением соответствующего носителя. Фармацевтический носитель может быть выбран в зависимости от вышеупомянутого способа введения и от формы препарата. В случае препаратов для перорального приема могут быть использованы крахмал, лактоза, сахар,маннит, карбоксиметилцеллюлоза, кукурузный крахмал, неорганические соли и т.д. При производстве препаратов для перорального приема с ними могут быть дополнительно смешаны связующие, разрыхлители, поверхностно-активные вещества, смазки, активаторы текучести, корректоры вкуса, красители, ароматизирующие добавки и т.д. С другой стороны, в случае препаратов для парентерального приема они могут быть получены посредством общепринятых способов, в которых соединение, выбранное из производного циклопентенона настоящего изобретения, его оптически активного вещества или его соли,которое является эффективным компонентом настоящего изобретения, растворяют или суспендируют в разбавителе, таком как дистиллированная вода для инъекций, физиологический раствор, водный раствор глюкозы, растительное масло для инъекций, кунжутное масло, арахисовое масло, соевое масло, кукурузное масло,пропиленгликоль, полиэтиленгликоль и затем, в случае необходимости, добавляют бактерициды,стабилизаторы, изотонические агенты, анальгетики и т.д. Противораковое средство настоящего изобретения вводят соответствующим способом,зависящим от формы препарата. На способ введения препарата нет конкретных ограничений, и препарат можно вводить перорально, наружно и в виде инъекций. Препараты для инъекций вводят, например, внутривенно, внутримышечно,подкожно, внутрикожно и т.д., тогда как препараты для наружного применения включают суппозитории и т.д. Доза противоракового средства определяется формой препарата, способом введения, целью применения и возрастом, массой тела, состоянием больного, подвepгаемого лечению, и не является постоянной, но обычно количество производного циклопентенона настоящего изобретения, его оптически активного вещества или его соли, содержащееся в препарате, составляет от 0,1 мкг до 200 мг/кг в день (для взрослых людей). Конечно, доза может изменяться в зависимости от различных обстоятельств, и, следовательно, в некоторых случаях 12 доза менее чем вышеприведенная, может быть достаточной, тогда как в других случаях может быть необходимой доза более вышеприведенной. Фармацевтическое средство настоящего изобретения можно вводить непосредственно перорально и, кроме того, его можно добавлять в любую пищу и напитки, так что средство может быть введено общепринятым путем. Производное циклопентенона настоящего изобретения, его оптически активное вещество или его соль обладают апоптоз-индуцирующим действием, когда средство, индуцирующее апоптоз, может быть превращено в фармацевтические препараты также как противораковое средство, то апоптоз-индуцирующее средство,содержащее в качестве эффективного компонента, по меньшей мeре, одно соединение, выбранное из производного циклопентенона настоящего изобретения, его оптически активного вещества или его соли, может быть получено и может быть введено таким же способом, как и противораковое средство. Доза апоптоз-индуцирующих средств устанавливается без особенностей, но она может быть соответственно определена в зависимости от лекарственной формы, способа введения,цели применения и возраста, массы тела, состояния и т.д. больного, которому назначено такое средство. Однако обычно количество соединения, выбранного из производного циклопентенона настоящего изобретения, его оптически активного вещества или его соли, содержащееся в препарате для взрослых составляет 0,1 мкг - 100 мг/кг в день. В сущности, доза может изменяться в зависимости от различных факторов, и, следовательно, в некоторых случаях доза менее вышеупомянутой может быть достаточной, тогда как в других случаях доза более вышеупомянутой может быть необходимой. Средство настоящего изобретения может быть введено перорально как таковое и, кроме того,средство можно вводить ежедневно после добавления в обычную пищу и/или в напитки также. В отличие от некроза, который является патогенным отмиранием клеток, апоптоз представляет собой отмирание, которое начально запрограммировано в гене самой клетки. Так,ген, который программирует апоптоз, активируется определенными экво- и эндогенными факторами, вследствие этого упомянутым геном вызывается запрограммированное им отмирание клеток, или, в некоторых случаях, активируются существующие в клетках белки, программирующие гибель клетки. Затем сама клетка разлагается и погибает за счет запрограммированной белком гибели. Вызывающее апоптоз средство настоящего изобретения является полностью пригодным, так как оно способно индуцировать в желательных тканях и клетках апоптоз и исключить ненужные клетки или опасные клетки 13 из находящегося в естественном состоянии живого организма. Индуцирующее апоптоз средство настоящего изобретения является эффективным, при удалении, например, инфицированных вирусом клеток, раковых клеток и аутореакционных лимфоцитов у пациентов, страдающих аутоиммунными заболеваниями, и в результате экспрессии апоптоза в желательных тканях или клетках стало возможным устранение ненужных или опасных клеток из живого организма, находящегося в естественном состоянии. Примеры заболеваний, для которых индуцирующее апоптоз средство настоящего изобретения является эффективным, включают системную красную волчанку, гломерулярный нефрит, рассеянный склероз, коллагеноз и другие аутоиммунные заболевания, а также ревматизм. Апоптоз-индуцирующее средство настоящего изобретения может быть использовано в способе индуцирования апоптоза. Так, когда в качестве эффективного компонента применяют производное циклопентенона, его оптически активное вещество или его соль, существует возможность индуцировать апоптоз и такой способ является пригодным, например, для установления механизма индуцирования апоптоза и для отбора апоптоз-индуцирующих средств и ингибиторов индуцирования апоптоза. Модель отека, индуцированного карагеинаном, является реакцией, в которой карагеинан, который представляет собой воспалительный индуктор, вводят подкожно в лапу животного для индуцирования воспалительных клеток, например, макрофага и нейтрофилов, посредством чего повышается проницаемость кровеносных сосудов за счет воспалительных факторов, продуцирующихся из этих клеток, индуцируя отек. Ингибирующее действие вышеупомянутого иммуномодулятора в отношении отека является пригодным для терапии или профилактики заболеваний, требующих контроля за повышением проницаемости кровеносных сосудов, например, хронического суставного ревматизма. Производное циклопентенона настоящего изобретения, его оптически активное вещество или его соль обладают подавляющим действием в отношении отека, вызванного карагеинаном, и фармацевтические средства, которые содержат в качестве активного компонента, по меньшей мере, одно соединение, выбранное из этих соединений, являются пригодными в качестве противовоспалительных и в качестве противоревматических средств, которые являются пригодными для терапии или профилактики воспалительных заболеваний, требующих контроля увеличения проницаемости кровеносных сосудов, например, ревматоидного артрита. Настоящее изобрeтение предлагает, кроме того, ингибитор топоизомеразы, содержащий в качестве активного компонента, по меньшей мере, одно соединение, выбранное из производ 002354 14 ного циклопентенона настоящего изобретения,его оптически активных веществ или его солей,а также способ ингибирования топоизомеразы, в котором в качестве активного компонента применяют одно соединение, выбранное из указанных соединений. Такой ингибитор топоизомеразы является пригодным в качестве противоракового средства, тогда как способ ингибирования топоизомеразы является пригодным при биохимических исследованиях и при отборе противораковых средств. Настоящее изобретение, кроме того, предлагает фармацевтические средства, оказывающие действие на биоиммунитетный механизм,например, препараты, оказывающие действие на механизм продуцирования антител, противовоспалительные средства, противоаллергические средства, противоревматические средства,средства индукции интерферона и т.д., фармацевтические средства, оказывающие действие на метаболизм сахаридов, например, фармацевтические средства для лечения сахарного диабета, фармацевтические средства, оказывающие действие на патогенные организмы, например,противомикробные средства, антивирусные средства и т.д., и ингибиторы топоизомеразы и подобные средства, содержащие в качестве активного компонента, по меньшей мере, одно соединение, выбранное из производных циклопентенона настоящего изобретения, их оптически активных веществ или их солей, причем упомянутые фармацевтические средства могут быть превращены в фармацевтические препараты теми же самыми способами, как и в случае противораковых средств и могут быть введены тем же самым способом и в таких же дозах, как и противораковые средства. Производное циклопентенона настоящего изобретения, его оптически активное вещество или его соль могут быть эффективно получены из циклопентенона и любого из предпочтительных спиртов или их реакционноспособных производных, и настоящее изобретение предлагает производное циклопентенона, представленное формулой (II), его оптически активное вещество или его соль. На способ производства пищевых продуктов и напитков, содержащих производное циклопентенона, его оптически активное вещество или его соль, полученные способом настоящего изобретения, не накладывается конкретных ограничений, и могут быть применены обычные способы кулинарной обработки продуктов, используемые для производства пищевых продуктов и напитков, при условии, что в образованном пищевом продукте или напитке будет содержаться эффективное количество производного циклопентенона, его оптически активного вещества или его соли. Производное циклопентенона настоящего изобретения, его оптически активное вещество или его соль при введении его дозы, которая 15 является эффективной для достижения физиологической активности, не проявляет токсичность. Так, например, в случае однократного перорального введения 300 мг/кг 4-третбутилциклопентенонового эфира, его оптически активного вещества или его соли или 4,5-дитретбутилциклопентенонового эфира, его оптически активного вещества или его соли гибели у мышей не наблюдалось. Суммируя вышеизложенное, производное циклопентенона настоящего изобретения, его оптически активное вещество или его соль, могут быть легко получены и, благодаря их различным физиологическим функциям, эти соединения являются полностью пригодными в широкой области фармацевтических средств,пищевых продуктов и т.д. Примеры Настоящее изобретение будет далее проиллюстрировано следующими примерами, хотя настоящее изобретение никоим образом не ограничивается этими примерами. Использованное в примерах обозначeние % в данном случае означает % по весу; NMR - ЯМР, s - синглет, m - мультиплет, d - дублет, t - триплет, dd двойной дуплет. Пример 1.(1) D-глюкуроновую кислоту (G5269; производимую фирмой Sigma) (10 г) растворили в 1 л воды, нагрели в течение 4-х часов при 121 С и концентрировали в вакууме до получения примерно 10 мл. Ее смешали с 40 мл верхнего слоя смеси, состоящей из бутилацетата, уксусной кислоты и воды, при соотношении компонентов в этой смеси 3:2:2, и центрифугировали и затем образованную надосадочную жидкость концентрировали в вакууме до получения примерно 10 мл. Вышеупомянутый экстракт помещали на силикагель (BW-300SP; 2 х 28 см; производимый фирмой Fuji Silycia) для проведения колоночной хроматографии и отделяли с применением в качестве элюата верхнего слоя смеси бутилацетата, уксусной кислоты и воды при соотношении компонентов в этой смеси 3:2:2, при скорости потока примерно 5 мл/мин, при давлении 0,2 кг/см 2 с применением компрессора. Для получения объема одной функции 10 мл осуществляли фракционирование и часть каждой фракции подвергали анализу тонкослойной хроматографией, после чего циклопентенон высокой чистоты содержался во фракциях от 61-ой до 80-ой. Эти фракции собрали, концентрировали в вакууме, экстрагировали 40 мл хлороформа и экстракт концентрировали в вакууме, при этом получали 100 мг циклопентенона. Посредством HPLC (высокоэффективной жидкостной хроматографии) с нормальной фазой с использованием колонки Palpack типа S,(изготовленную Tоkara Shuzo), отделяли фракцию и с помощью ультрафиолетового поглоще 002354 16 ния 215 нм осуществляли обнаружение, степень чистоты составила 98%. Вышеуказанный циклопентенон (113,9 мг) растворили в 2,85 мл этанола. К раствору этанола добавили 3,85 мл гексана/этанола (94/6) с получением раствора циклопентенона (17 мг/мл). Для получения пробы раствора для оптического разделения HPLC, раствор циклопентенона фильтровали через фильтр 0,5 м. Эту пробу раствора использовали для оптического разделения HPLC, каждую из фракций (-)-циклопентенона в более раннем пике и(+)-циклопентенона в более позднем пике и выпаривали досуха в вакууме, при этом получили 43,2 мг (-)-циклопентенона и 43,0 мг (+)циклопентенона. Условия для оптического разделения HPLC Колонки: Chiral Pack AS (производимые(2,55 мг). Каждый из полученных (-)-циклопентенона и (+)-циклопентенона содержал примерно 1% энантиомера и следовательно они снова подвергались оптическому разделению при вышеприведенных условиях. В результате, из 30,0 мг (-)-циклопентенона более раннего пика получили 19,7 мг (-)-циклопентенона, не содержащего энантиомера, тогда как из 37,4 мг (+)циклопентенона более позднего пика получили 27,7 мг (+)-циклопентенона, не содержащего энантиомера. В данном случае, время элюирования при оптическом разделении HPLC (-)циклопентенона и (+)-циклопентенона составило соответственно 33 мин и 40 мин.(2) В 2,5 мл дихлорметана (производимого фирмой Wako Pure Chemical; 135-02441) в потоке аргона растворили циклопентенон (44 мг) и 492 мг бензил-2,2,2-трихлорацетамидата (производимого фирмой Aldrich; 14033-3). К этой смеси при перемешивании постепенно добавили раствор 28 мкл/мл комплекса трифторид бора/диэтиловый эфир (производимого фирмойWako Pure Chemical; 022-08362) в 1 мл дихлорметана. После перемешивания при комнатной температуре в течение 8 ч смесь концентрировали в вакууме, затем подвергали тонкослойной силикагельной хроматографии на силикагеле с применением в качестве проявителя смеси хлороформа и метанола (19:1) для разделения 4 бензилциклопентенонового эфира, 5-бензилциклопентенонового эфира и 4,5-дибензилциклопентенонового эфира. Значение Rf 4 бенилциклопентенонового эфира и 4,5 дибензилциклопентенонового эфира составили соответственно 0,3, 0,45 и 0,8. Выходы 4 бензилциклопентенонового эфира,5 бензилциклопентенонового эфира и 4,5 17 дибензилциклопентенонового эфира составили соответственно 3,7, 3,7 и 2,5%.(3) Структуры 4-бензилциклопентенонового эфира, 5-бензилциклопентенонового эфира и 4,5-дибензилциклопентенонового эфира, полученных в примере 1-(2) подтвердили посредством ядерного магнитного резонанса(ЯМР). Применяемый для ядерного магнитного резонанса прибор представлял собой системуNippon Denshi). Представленные значения химического сдвига, определенные посредством 1H-ЯМР, основаны на том, что значение химического сдвига для тетраметил-силана равно 0 част. на млн (ррm). Результаты представлены ниже. 4-Бензилциклопентеноновый эфир. 1H-ЯМР:7,47 (1H, dd, J=6,27 Гц, J=1,98), 7,34 (10 Н, m),6,29 (1H, dd, J=6,10 Гц, J=1,49 Гц),4,88 (1H, d, J=11,85),4,74 (1H, d,J=11,85),4,71 (2H, d, J=11,55),4,56 (1H, m), 4,33 (1H, d, J=2,64). На фиг. 1-3 показаны данные спектра 1HЯМР этих производных. Таким образом, фиг. 1 показывает спектр ЯМР 4-бензилциклопентенонового эфира, фиг. 2 показывает спектр ЯМР 5 бензилциклопентенонового эфира, фиг. 3 показывает спектр ЯМР 4,5-дибензилциклопентенонового эфира. На фиг. 1-3 на оси абсцисс показаны значения химического сдвига (част.на млн.(ррm и на оси ординат показана интенсивность сигнала.(4) В 2,5 мл дихлорметана в потоке аргона растворили циклопентенон (44 мг) и 287 мг трет-бутил-2,2,2-трихлорацетимидата (производимого фирмой Aldrich; 36, 478-9). К этой смеси при перемешивании постепенно добавили 1 мл раствора 28 мкл/мл комплекса трифторида бора/диэтиловый эфир в дихлорметане. Смесь перемешали при комнатной температуре в течение 8 ч, концентрировали в вакууме и для разделения 4-трет-бутилциклопентенонового эфира, 5 трет-бутилциклопентенонового эфира и 4,5-дитрет-бутилциклопентенонового эфира подвергли тонкослойной хроматографии на силикагеле тем же самым способом, который описан в примере 1-(2). ЗначенияRf 4-третбутилциклопентенонового эфира, 5-третбутилциклопентенонового эфира и 4,5-ди-третбутилциклопентенонового эфира составили соответственно 0,35, 0,27 и 0,73. Выходы 4-трет 002354 18 бутилциклопентенонового эфира,5-третбутилциклопентенонового эфира и 4,5-ди-третбутилциклопентенонового эфира составили соответственно 9,2%, 1,9% и 11%.(5) Структуры 4-трет-бутилциклопентенонового эфира,5-трет-бутилциклопентенонового эфира и 4,5-ди-трет-бутилциклопентенонового эфира, полученных в примере 1-(4),подтвердили посредством ЯМР тем же самым способом, который представлен в примере 1-(3). Результаты представлены ниже. 4-трет-Бутилциклопентеноновый эфир. 1 Н-ЯМР:7,34 (1 Н, dd, J=5,94 Гц, J=0,99), 6,25 (1 Н, dd, J=6,10, J=1,49),4,59 (1 Н, m),4,08 (1 Н, d, J=2,31),2,85 (1H, m),1,33 (9H,s). 5-трет-Бутилциклопентеноновый эфир. 1 Н-ЯМР:7,37 (1H, dd, J=6,27 Гц, J=1,98), 6,23 (1H, dd, J=6,27, J=1,32),4,75 (1H, m),4,04 (1H, d, J=2,63),2,23 (1H, m),1,32 (9 Н, s). 4,5-ди-трет-Бутилциклопентеноновый эфир. 1 Н-ЯМР:7,35 (1 Н, dd, J=6,27 Гц, J=1,65), 6,24 (1 Н, dd, J=6,26, J=0,99),4,62 (1 Н, ddd,J=3,3, J=1,65, J=0,99),4,16 (1H, d, J=3,31),1,38 (18H, s). На фиг. 4-6 показаны данные спектра 1HЯМР этих производных. Таким образом, фиг. 4 показывает спектр ЯМР 4-трет-бутилциклопентенонового эфира, фиг. 5 показывает спектр ЯМР 5-трет-бутилциклопентенонового эфира и фиг. 6 показывает спектр 4,5-ди-трет-бутилциклопентенонового эфира. На фиг. 4-6 на оси абсцисс показаны значения химического сдвига(част. на млн. (ррm и на оси ординат показаны значения интенсивности сигнала. Пример 2.(1) 1,22, 2,44, 4,88, 9,77, 19,5, 39,1, 78,1,156, 313, 625, 1250, 2500, 5000 или 10000 мкг/мл раствора (10 мкл) (в 70% водном растворе этанола) 4-бензилциклопентенонового эфира, 5 бензилциклопентенонового эфира или 4,5 дибензилциклопентенонового эфира или 70% водный раствор этанола в качестве контроля (10 мкл) добавили в каждую лунку пластины микротитра, содержащей 96 лунок, и затем осушили воздухом. В среде RPMI 1640, содержащей 10% околоплодной сыворотки теленка, суспендировали штамм промиелоцитарных лейкозных клеток HL-60 (ATCC CCL-240) до степени 1 х 105 клеток/мл, каждые 100 мкл влили в каждую лунку пластины микротитра и инкубировали в течение 48 ч при температуре 37 С в присутствии 5% CO2. После добавления 10 мкл раствора(5 мг/мл) 3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолийбромида (ММТ, производимой фирмой Sigma) в водном соляном растворе с фосфатным буфером продолжили инкубацию в течение еще четырех часов и затем под микроскопом наблюдали состояние роста клеток. После этого добавили 100 мкл 2-пропанола, содержащего 0,04 N НСl, затем смесь хорошо пе 19 ремешали и измерили поглощающую способность при 590 нм. Результаты показали, что в секции, в которую добавили 2,44 мкг/мл 4-бензилциклопентенонового эфира (конечная концентрация: 0,244 мкг/мл; 1,20 мкМ), 19,5 мкг/мл 5 бензилциклопентенонового эфира (конечная концентрация: 1,95 мкг/мл; 9,56 мкм) или 156 мкг/мл 4,5-дибензилциклопентенонового эфира(конечная концентрация: 15,6 мкг/мл; 53,1 мкМ), рост клеток был полностью подавлен. Наблюдалось также образование апоптического тела. В данном случае в секциях, в которые добавили более низкие концентрации, чем вышеприведенные, не наблюдалось разницы между ними и контрольной секцией, в которую добавили воду.(2) Влияние 4-трет-бутилциклопентенонового эфира, 5-трет-бутилциклопентенонового эфира или 4,5-ди-трет-бутилциклопентенонового эфира на рост клеток HL-60 определили тем же самым способом, который представлен в примере 2-(1). Результаты показали, что рост клеток полностью был подавлен в секции, в которую добавили 313 мкг/мл 4-бензилциклопентенонового эфира (конечная концентрация: 31,3 мкг/мл; 180 мкМ), 78,1 мкг/мл 5-бензилциклопентенонового эфира (конечная концентрация: 7,81 мкг/мл; 46 мкМ) или 625 мкг/мл 4,5-ди-бензилциклопентенонового эфира (конечная концентрация: 62,5 мкг/мл; 280 мкМ). Наблюдалось также образование апоптического тела. В данном случае в секциях, в которые добавили более низкие концентрации, чем вышеприведенные, не наблюдалось разницы между ними и контрольной секцией, в которую добавили воду. Между тем, вышеупомянутые соединения показали активность подавления роста раковых клеток и активность индуцирования апоптоза. Оптически активные вещества этих соединений показали обе активности в такой же степени. Пример 3. У фирмы Seakku-Yoshitomi приобрели крыс Льюиса (мужские особи, возраст - 9 недель, вес тела: примерно 250 г) и получили модели воспалений, например, отека стопы, вызванного карагеинаном (модель ревматоидного артрита), посредством которой оценили испытуемые вещества. Так, крысам, которые перед началом эксперимента голодали в течение 18 ч, перорально вводили 4-трет-бутилциклопентеноновый эфир или 4,5-ди-трет-бутилциклопентеноновый эфир в различных концентрациях путем растворения в оливковом масле при дозе 1 мг/10 мл/кг или 10 мг/10 мл/кг. Через 0,5 ч после введения этих испытуемых лекарственных средств для индуцирования отека стопы в правую лапу крысы вводили 100 мкл/крысе 1% суспензии карагеинана (производимого фирмой Wako) в физиологическом рас 002354 20 творе (производимом Otsuka Pharmaceutical). Через три часа после инъекции карагеинана с помощью устройства для измерения объема стопы (изготовленного UGO BASILE) измерили объем правой лапы крысы. В данном случае,измеренное значение выразили путем подсчета степени увеличения от объема правой лапы каждой крысы, измеренного до введения карагеинана. Результат показан на фиг. 9. Таким образом фиг. 9 показывает взаимосвязь между количеством каждого соединения и степенью увеличения отека стопы, на этой фигуре ось ординат показывает степень увеличения (%), тогда как ось абсцисс показывает дозу каждого соединения (мг/кг). На фиг. 9 А представляет собой группу,которой вводили 4-трет-бутилциклопентеноновый эфир, тогда как В представляет собой группу,которой вводили 4,5-ди-третбутилциклопентеноновый эфир. Каждое из соединений показало подавляющее действие в отношении индуцированного карагеинаном отека. В данном случаена фиг. 9 означает, что это значительно отличается от контрольной группы при р 0,05. Другие производные циклопентенона настоящего изобретения, полученные в примере 1,показали также подавляющее действие в отношении отека, индуцированного карагеинаном,как вышеуказанные соединения. Пример 4.(1) К смеси, состоящей из 2 мкл топоизомеразы II (производимой TopoGEN, 2 ед./мкл), 2 мкл буфера, с 10-кратной разбавленной концентрацией [0,5 М Трис-НСl (рН 8,0), 1,2 М КСl, 0,1 М MgCl2, 5 мМ аденозинтрифосфата и 5 мМ дитиотреита], 2 мкл 0,1% бычьего сывороточного альбумина (производимого Takara Shuzo), 11 мкл дистиллированной воды и 2 мкл дистиллированной воды (контроль) или 4,5-ди-третбутилциклопентенонового эфира, имеющего различные концентрации после разбавления водой, добавили 1 мкл 0,25 мкг/мкл ДНК pBR 322 (от фирмы Takara Shuzo) и подвергли взаимодействию при 37 С. После протекания реакции в течение 30 мин путем добавления 2 мкл водного раствора 1% додецилсульфата натрия,50% глицерина и 0,02% бромфенола голубого реакцию останавливали. Вышеуказанный реакционный раствор (20 мкл) наносили на 1% гель агарозы, полученной из агарозы L03 (производимой фирмой TakaraShuzo) и ТАЕ буфера [40 мМ трис, 5 мМ ацетат натрия и 1 мМ динатрийэтилендиаминтетраацетата (EDTA); рН доводили до значения рН 7,8 уксусной кислотой] и проводили электрофорез в ТАЕ буфере. После электрофореза гель погрузили в водный раствор 1 мкл/мл этидийбромида и облучили ультрафиолетовым излучением с целью наблюдения электрофореграммы ДНК. В контрольном образце, который представлял со 21 бой водный раствор, тип ДНК полностью изменяли от суперспирального до релаксационного,но, когда активность топоизомеразы II была ингибирована, изменение от суперспирального типа до релаксационного типа было частично или полностью ингибировано. В результате 4,5-ди-трет-бутилциклопентеноновый эфир показал подавление активности топоизомеразы при концентрации в реакционном растворе не менее 250 мкМ. Таким образом,при концетрации 250 мкМ средний уровень сверхспиральной ДНК, при концентрации 500 мкМ оставалась большая часть сверхспиральной ДНК и при концентрации 1000 мкМ содержание сверхспиральной ДНК вообще не уменьшалось. Оптически активные вещества 4,5-ди-третбутилциклопентенонового эфира и других соединений настоящего изобретения, полученные в примере 1, включая их оптически активные вещества, также показали такую же активность. Соединения настоящего изобретения как таковые показали подавляющую активность в отношении топоизомеразы II, которая лишь временно выражена в нормальных клетках на стадии деления и которая сильно выражена во время всего клеточного периода в результате малигнизирования клеток. Пример 5. Препараты для инъекций.(1) Для получения препарата для инъекций к физиологическому раствору с концентрацией 1% (как перечислено в списке Фармакопеи Японии) добавили 4-бензилциклопентеноновый эфир или 5-бензилциклопентеноновый эфир.(2) Для получения препарата для инъекций к физиологическому раствору с концентрацией 0,5 и 0,1% соответственно (такой же, как приведен выше) добавили 4-бензилциклопентеноновый или 5-бензилциклопентеноновый эфир и глицирризиновую кислоту. Пример 6. Таблетки.(1) Для производства препарата в виде таблеток получили таблетку, содержащую 100 мг 4-бензилциклопентенонового эфира и соответствующее количество микрокристаллической целлюлозы, и покрыли ее сахаром.(2) Для производства препарата в виде таблеток получили таблетку, содержащую 0,1 мг 5-бензилциклопентенонового эфира, 10 мг дикалийглицирризината и соответствующее количество микрокристаллической целлюлозы,и покрыли сахаром. Достоинства изобретения Настоящее изобретение предлагает способ получения производного циклопентенона, его оптически активного вещества или его соли,которые проявляют физиологические активности, например, противораковую активность,активность, ингибирующую рост раковых клеток, активность, индуцирующую апоптоз и т.д. Фармацевтическое средство, в котором применяют в качестве эффективного компонента соединение, предложенное настоящим изобрете 002354 22 нием, является полезным фармацевтическим средством, особенно для сохранения гомеостаза живого организма. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Производное циклопентенона, представленное следующей формулой [I], или его оптически активное вещество или его соль где R1 и R2 являются одинаковыми или различными и каждый из них является C1-C18 алкильной группой с прямой или разветвленной цепью, С 3-С 20 алкенильной группой с прямой или разветвленной цепью, С 6-С 10 арильной группой,С 7-С 9 арилалкильной группой или Н, при условии, что случай, когда R1=R2=бензильная группа, R1=R2=H или R1=бензильная группа и R2=H,исключен. 2. Способ получения производного циклопентенона, представленного формулой [II] где R3 и R4 являются одинаковыми или различными, и каждый из них является C1-C18 алкильной группой с прямой или разветвленной цепью, С 3-С 20 алкенильной группой с прямой или разветвленной цепью, С 6-С 10 арильной группой,С 7-С 9 арилалкильной группой или Н, при условии, что случай, когда R3=R4=H, исключен, отличающийся тем,что 4,5-дигидрокси-2 циклопентен-1-он, представленный следующей формулой (III) и/или его оптически активное производное подвергают взаимодействию либо одновременно,либо последовательно, со спиртом и/или его реакционноспособным производным, соответствующим R3 и R4 производного циклопентенона, представленного формулой [II]. 3. Фармацевтическое средство, характеризующееся содержанием в качестве эффективного компонента, по меньшей мере, одного соединения, выбранного из производного циклопентенона, его оптически активного вещества или его соли по п.1. 4. Фармацевтическое средство по п.3, которое представляет собой противораковое средство. 5. Фармацевтическое средство по п.3, которое представляет собой апоптоз-индуцирующее средство. 6. Фармацевтическое средство, характеризующееся содержанием в качестве эффективного компонента, по меньшей мере, одного соединения, выбранного из производного циклопен 23 тенона, полученного способом по п.2, его оптически активного вещества или его соли. 7. Фармацевтическое средство по п.6, которое представляет собой противораковое средство. 24 8. Фармацевтическое средство по п.6, которое представляет собой апоптоз-индуцирующее средство.
МПК / Метки
МПК: A61K 31/122, A61P 35/00, C07C 49/597
Метки: производные, циклопентенона
Код ссылки
<a href="https://eas.patents.su/14-2354-proizvodnye-ciklopentenona.html" rel="bookmark" title="База патентов Евразийского Союза">Производные циклопентенона</a>
Предыдущий патент: Лептин как ингибитор пролиферации опухолевых клеток
Следующий патент: Гидрат соли малеиновой кислоты 5-[4-[2-(n-метил-n-(2-пиридил)амино)этокси]бензил]тиазолидин-2,4-диона
Случайный патент: Пестицидная и паразитицидная смесь и композиция, которая включает новую кристаллическую модификацию фипронила












