Металлические соли циклогексеноноксимовых эфиров
Номер патента: 1679
Опубликовано: 25.06.2001
Авторы: Вестфален Карл-Отто, Братц Маттиас, Ранг Харальд, Бенуа Реми, Мисслитц Ульф, Йэгер Карл-Фридрих
Формула / Реферат
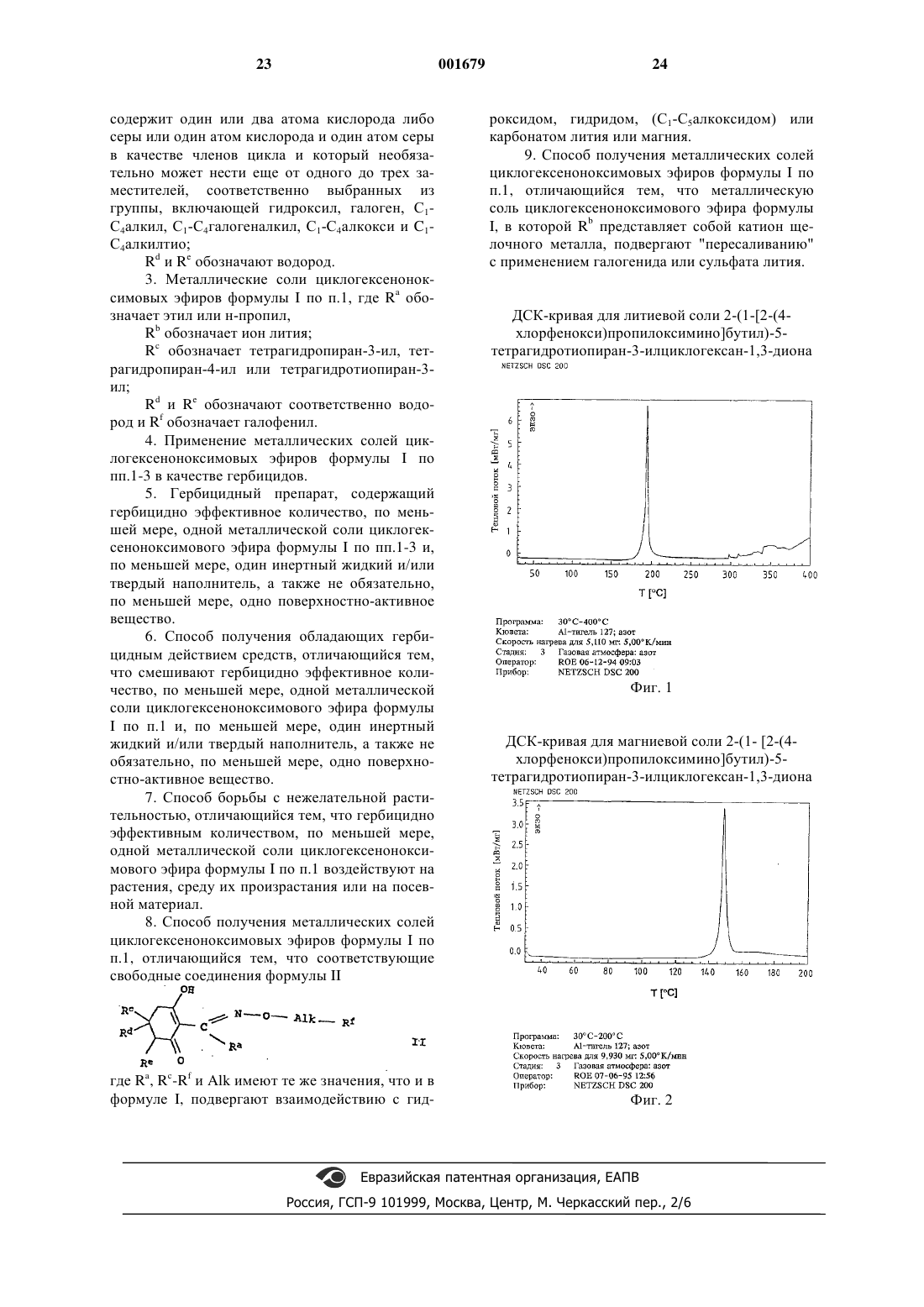
1. Металлические соли циклогексеноноксимовых эфиров общей формулы I
в которой Ra обозначает С1-С6алкил;
Rb обозначает ион лития;
Rc обозначает водород, циано, формил, С1-С6алкил, С1-С4алкокси-С1-С6алкил, С1-С4алкилтио-С1-С6алкил, фенокси-С1-С6алкильную, фенилтио-С1-С6алкильную, пиридилокси-С1-С6алкильную или пиридилтио-С1-С6алкильную группу, причем фенильные и пиридильные кольца этих групп при необходимости могут нести от одного до трех заместителей, соответственно выбранных из группы, включающей нитро, циано, галоген, С1-С4алкил, С1-С4галогеналкил, С1-С4алкокси, С1-С4галогеналкокси, С1-С4алкилтио, С3-С6алкенил, С3-С6алкенилокси, С3-С6алкинил, С3-С6алкинилокси и -NRgRh,
где Rg обозначает водород, С1-С4алкил, С3-С6алкенил, С3-С6алкинил, С1-С6ацил или бензоил, который в свою очередь необязательно может нести еще от одного до трех остатков, соответственно выбранных из группы, включающей нитро, циано, галоген, С1-С4алкил, С1-С4галогеналкил, С1-С4алкокси и С1-С4алкилтио, и
Rh обозначает водород, С1-С4алкил, С3-С6алкенил или С3-С6алкинил; С3-С7циклоалкильную или С5-С7циклоалкенильную группу, причем эти группы при необходимости могут нести от одного до трех заместителей, соответственно выбранных из группы, включающей гидроксил, галоген, С1-С4алкил, С1-С4галогеналкил, С1-С4алкокси, С1-С4алкилтио, бензилтио, С1-С4алкилсульфонил и С1-С4алкилсульфинил;
5-членный насыщенный гетероцикл, который наряду с атомами углерода содержит один или два атома кислорода либо серы или один атом кислорода и один атом серы в качестве членов цикла и который необязательно может нести еще от одного до трех заместителей, соответственно выбранных из группы, включающей С1-С4алкил, С1-С4галогеналкил, С1-С4алкокси и С1-С4алкилтио;
6- или 7-членный насыщенный либо одно или двукратно ненасыщенный гетероцикл, который наряду с атомами углерода содержит один или два атома кислорода либо серы или один атом кислорода и один атом серы в качестве членов цикла и который необязательно может нести еще от одного до трех заместителей, соответственно выбранных из группы, включающей гидроксил, галоген, С1-С4алкил, С1-С4галогеналкил, С1-С4алкокси и С1-С4алкилтио;
5-членный гетероароматический углеводород, который наряду с атомами углерода содержит один или два атома азота и один атом кислорода либо серы или от одного до трех атомов азота или один атом кислорода либо серы в качестве членов цикла и который необязательно может нести еще от одного до трех заместителей, соответственно выбранных из группы, включающей циано, галоген, С1-С4алкил, С1-С4галогеналкил, С1-С4алкокси, С1-С4галогеналкокси, С1-С4алкилтио, С2-С6алкенил, С2-С6алкенилокси, С3-С6алкинилокси и С1-С4алкокси-С1-С4алкил;
фенил или пиридил, оба которые необязательно могут нести от одного до трех заместителей, соответственно выбранных из группы, включающей нитро, циано, формил, галоген, С1-С4алкил, С1-С4галогеналкил, С1-С4алкокси, С1-С4галогеналкокси, С1-С4алкилтио, С3-С6алкенил, С3-С6алкенилокси, С3-С6алкинил, С3-С6алкинилокси и -NRkRl,
где Rk обозначает водород, С1-С4алкил, С3-С6алкенил или С3-С6алкинил и
Rl обозначает водород, С1-С4алкил, С3-С6алкенил, С3-С6алкинил, С1-С6ацил или бензоил, который в свою очередь необязательно может нести еще от одного до трех заместителей, соответственно выбранных из группы, включающей нитро, циано, галоген, С1-С4алкил, С1-С4галогеналкил, С1-С4алкокси и С1-С4алкилтио;
Rd обозначает водород, гидроксил или, если Rc представляет собой С1-С6алкил, также С1-С6алкил;
Re обозначает водород, циано, галоген, (С1-С4алкокси)карбонил или (С1-С4алкил)кетоксим;
Alk обозначает С1-С6алкиленовую, С3-С6алкениленовую или С3-С6алкиниленовую цепь, которая может нести соответственно метиленовую группу (=СН2) и/или от одного до трех заместителей, соответственно выбранных из галогена и С1-С3алкила;
3-6-членную алкиленовую или 4-6-членную алкениленовую цепь, которая необязательно может нести от одного до трех С1-С3алкильных заместителей и которая наряду с метиленовыми и метиновыми звеньями содержит один из следующих мостиковых членов: кислород, серу, -SO-, -SO2- или -N(Ri)-, где Ri представляет собой водород, С1-С4алкил, С3-С6алкенил или С3-С6алкинил;
Rf обозначает фенильную группу, галогенфенильную либо дигалогенфенильную группу, причем каждое фенильное кольцо необязательно может нести от одного до трех заместителей, соответственно выбранных из группы, включающей нитро, циано, формил, галоген, С1-С4алкил, С1-С4галогеналкил, С1-С4алкокси, С1-С4галогеналкокси, С3-С6алкенил, С3-С6алкенилокси, С3-С6алкинил, С3-С6алкинилокси и -NRkRl,
где Rk обозначает водород, С1-С4алкил, С3-С6алкенил или С3-С6алкинил и
Rl обозначает водород, С1-С4алкил, С3-С6алкенил, С3-С6алкинил, С1-С6ацил или бензоил, который необязательно может нести в свою очередь еще от одного до трех остатков, соответственно выбранных из группы, включающей нитро, циано, галоген, С1-С4алкил, С1-С4галогеналкил, С1-С4алкокси и С1-С4алкилтио.
2. Металлические соли цикогексеноноксимовых эфиров формулы I по п.1, где Rb обозначает ион лития;
Rc обозначает 6- или 7-членный насыщенный либо одно или двукратно ненасыщенный гетероцикл, который наряду с атомами углерода содержит один или два атома кислорода либо серы или один атом кислорода и один атом серы в качестве членов цикла и который необязательно может нести еще от одного до трех заместителей, соответствеээю выбранных из группы, включающей гидроксил, галоген, С1-С4алкил, С1-С4галогеналкил, С1-С4алкокси и C1-С4алкилтио;
Rd и Re обозначают водород.
3. Металлические соли циклогексеноноксимовых эфиров формулы I по п.1, где Ra обозначает этил или н-пропил,
Rb обозначает ион лития;
Rc обозначает тетрагидропиран-3-ил, тетрагидропиран-4-ил или тетрагидротиопиран-3-ил;
Rd и Re обозначают соответственно водород и Rf обозначает галофенил.
4. Применение металлических солей циклогексеноноксимовых эфиров формулы I по пп.1-3 в качестве гербицидов.
5. Гербицидный препарат, содержащий гербицидно эффективное количество, по меньшей мере, одной металлической соли циклогексеноноксимового эфира формулы I по пп.1-3 и, по меньшей мере, один инертный жидкий и/или твердый наполнитель, а также не обязательно, по меньшей мере, одно поверхностно-активное вещество.
6. Способ получения обладающих гербицидным действием средств, отличающийся тем, что смешивают гербицидно эффективное количество, по меньшей мере, одной металлической соли циклогексеноноксимового эфира формулы I по п.1 и, по меньшей мере, один инертный жидкий и/или твердый наполнитель, а также не обязательно, по меньшей мере, одно поверхностно-активное вещество.
7. Способ борьбы с нежелательной растительностью, отличающийся тем, что гербицидно эффективным количеством, по меньшей мере, одной металлической соли циклогексеноноксимового эфира формулы I по п.1 воздействуют на растения, среду их произрастания или на посевной материал.
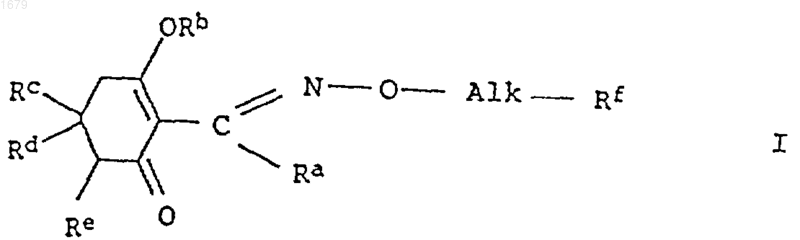
8. Способ получения металлических солей циклогексеноноксимовых эфиров формулы I по п.1, отличающийся тем, что соответствующие свободные соединения формулы II
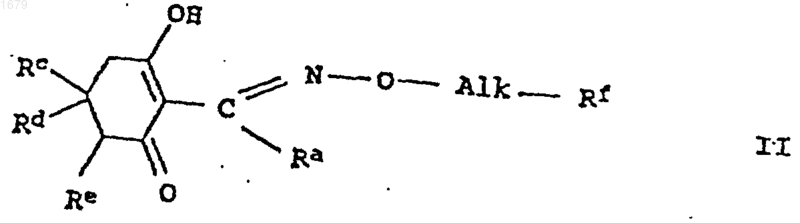
где Ra, Rc-Rf и Alk имеют те же значения, что и в формуле I, подвергают взаимодействию с гидроксидом, гидридом, (С1-С5алкоксидом) или карбонатом лития или магния.
9. Способ получения металлических солей циклогексеноноксимовых эфиров формулы I по п.1, отличающийся тем, что металлическую соль циклогексеноноксимового эфира формулы I, в которой Rb представляет собой катион щелочного металла, подвергают "пересаливанию" с применением галогенида или сульфата лития.
Текст
1 Настоящее изобретение относится к новым металлическим солям циклогексеноноксимовых эфиров формулы I в которой переменные имеют следующие значения:Rc обозначает водород, циано, формил, С 1 С 6 алкил, С 1-С 4 алкокси-С 1-С 6 алкил, С 1-С 4 алкилтио-С 1-С 6 алкил, фенокси-С 1-С 6 алкильную, фенилтио-С 1-С 6 алкильную,пиридилокси-С 1-С 6 алкильную или пиридилтио-С 1-С 6 алкильную группу, причем фенильные и пиридильные кольца этих групп при необходимости могут нести от одного до трех заместителей, соответственно выбранных из группы, включающей нитро, циано, галоген, С 1-С 4 алкил, С 1-С 4 галогеналкил, С 1-С 4 алкокси, С 1-С 4 галогеналкокси, С 1 С 4 алкилтио, С 3-С 6 алкенил, С 3-С 6 алкенилокси,С 3-С 6 алкинил, С 3-С 6 алкинилокси и -NRgRh, гдеRg обозначает водород, С 1-С 4 алкил, С 3 С 6 алкенил, С 3-С 6 алкинил, С 1-С 6 ацил или бензоил, который в свою очередь необязательно может нести еще от одного до трех остатков, соответственно выбранных из группы, включающей нитро, циано, галоген, С 1-С 4 алкил, С 1-С 4 галогеналкил, С 1-С 4 алкокси и С 1-С 4 алкилтио, иRh обозначает водород, С 1-С 4 алкил, С 3-С 6 алкенил или С 3-С 6 алкинил; С 3-С 7 циклоалкильную или С 5-С 7 циклоалкенильную группу, причем эти группы при необходимости могут нести от одного до трех заместителей, соответственно выбранных из группы, включающей гидроксил, галоген, С 1-С 4 алкил, С 1-С 4 галогеналкил, С 1-С 4 алкокси, С 1-С 4 алкилтио, бензилтио, С 1-С 4 алкилсульфонил и С 1-С 4 алкилсульфинил; 5-членный насыщенный гетероцикл, который наряду с атомами углерода содержит один или два атома кислорода либо серы или один атом кислорода и один атом серы в качестве членов цикла и который необязательно может нести еще от одного до трех заместителей, соответственно выбранных из группы, включающей С 1-С 4 алкил, С 1-С 4 галогеналкил, С 1-С 4 алкокси и С 1-С 4 алкилтио; 6- или 7-членный насыщенный либо одно или двукратно ненасыщенный гетероцикл, который наряду с атомами углерода содержит один или два атома кислорода либо серы или один атом кислорода и один атом серы в качестве членов цикла и который необязательно может нести еще от одного до трех заместителей, соответственно выбранных из группы, включающей гидроксил, галоген, С 1-С 4 алкил, С 1-С 4 галогеналкил, С 1-С 4 алкокси и С 1-С 4 алкилтио; 2 5-членный гетероароматический углеводород, который наряду с атомами углерода содержит один или два атома азота и один атом кислорода либо серы или от одного до трех атомов азота или один атом кислорода либо серы в качестве членов цикла и который необязательно может нести еще от одного до трех заместителей, соответственно выбранных из группы,включающей циано, галоген, С 1-С 4 алкил, С 1-С 4 галогеналкил, С 1-С 4 алкокси, С 1-С 4 галогеналкокси, С 1-С 4 алкилтио, С 2-С 6 алкенил, С 2-С 6 алкенилокси, С 3-С 6 алкинилокси и С 1-С 4 алкокси-С 1 С 4 алкил; фенил или пиридил, оба которые необязательно могут нести от одного до трех заместителей, соответственно выбранных из группы,включающей нитро, циано, формил, галоген, С 1 С 4 алкил, С 1-С 4 галогеналкил, С 1-С 4 алкокси, С 1 С 4 галогеналкокси, С 1-С 4 алкилтио, С 3-С 6 алкенил,С 3-С 6 алкенилокси, С 3-С 6 алкинил, С 3-С 6 алкинилокси и -NRkRl, гдеRlобозначает водород, С 1-С 4 алкил, С 3-С 6 алкенил, С 3-С 6 алкинил, С 1-С 6 ацил или бензоил,который в свою очередь необязательно может нести еще от одного до трех заместителей, соответственно выбранных из группы, включающей нитро, циано, галоген, С 1-С 4 алкил, С 1 С 4 галогеналкил, С 1-С 4 алкокси и С 1-С 4 алкилтио;Alk обозначает С 1-С 6 алкиленовую, С 3-С 6 алкениленовую или С 3-С 6 алкиниленовую цепь,которая может нести соответственно метиленовую группу (=СН 2) и/или от одного до трех заместителей, соответственно выбранных из галогена и С 1-С 3 алкила; 3-6-членную алкиленовую или 4-6 членную алкениленовую цепь, которая необязательно может нести от одного до трех С 1-С 3 алкильных заместителей и которая наряду с метиленовыми и метиновыми звеньями содержит один из следующих мостиковых членов: кислород, серу, -SO-, -SO2- или -N(Ri)-, где Ri представляет собой водород, С 1-С 4 алкил, С 3-С 6 алкенил или С 3-С 6 алкинил;Rf обозначает фенильную группу, галогенфенильную либо дигалогенфенильную группу,причем каждое фенильное кольцо необязательно может нести от одного до трех заместителей,соответственно выбранных из группы, включающей нитро, циано, формил, галоген, С 1-С 4 алкил, С 1-С 4 галогеналкил, С 1-С 4 алкокси, С 1-С 4 галогеналкокси, С 3-С 6 алкенил, С 3-С 6 алкенилокси, С 3-С 6 алкинил, С 3-С 6 алкинилокси и -NRkRl,гдеRl обозначает водород, С 1-С 4 алкил, С 3-С 6 алкенил, С 3-С 6 алкинил, С 1-С 6 ацил или бензоил,который необязательно может нести в свою очередь еще от одного до трех остатков, соответственно выбранных из группы, включающей нитро, циано, галоген, С 1-С 4 алкил, С 1-С 4 галогеналкил, С 1-С 4 алкокси и С 1-С 4 алкилтио. Кроме того, изобретение относится к применению соединений формулы I в качестве гербицидов, к гербицидным препаратам, содержащим соединения формулы I в качестве действующих субстанций, к способам получения соединений формулы I и гербицидных препаратов с применением соединений формулы I, а также к способу борьбы с нежелательной растительностью с помощью соединений формулы I. При создании средств защиты растений желательно в принципе постоянно повышать их специфическую (в данном случае гербицидную) эффективность и надежность действия. Существенным при этом является химическая устойчивость действующего вещества и стабильность при хранении готовой композиции средств защиты растений. Желательно, кроме того, обеспечить также определенную стабильность самого действующего вещества в условиях окружающей среды в течение некоторого периода времени после его применения. Из европейской патентной заявки ЕР-А 266068 уже известно, что гербициды из класса веществ, к которому относятся циклогексеноноксимовые эфиры, проявляют тенденцию к разложению. Особенно критическая ситуация складывается при хранении готовых к применению их композиций в течение продолжительного времени при повышенных температурах. Наряду с этой проблемой стабильности решающую роль играет далее такой фактор, как ограниченная возможность подвергать соединение длительным термическим нагрузкам при его получении и переработке в качестве средства защиты растений, например, в процессе очистки или сушки. В классе веществ, к которому относятся циклогексеноноксимовые эфиры, наряду со свободными соединениями указываются также их соли, обладающие гербицидным действием (см.,например, патент Японии JP-A 59/163363, где названы соли натрия, калия, кальция, магния,бария, никеля, марганца, кобальта, цинка и железа). Объектом изобретения в патенте ЯпонииJP-A 78/034753 является получение натриевых,калиевых, кальциевых, магниевых, бариевых,никелевых, медных, марганцевых, кобальтовых,цинковых, железных и серебряных солей определенных 2-алкилокси-, 2-алкенилокси-, 2 алкинилокси- и 2-бензилоксииминоалкилциклогексенонов. В патенте Японии JP-A 62/089653 описываются литиевые соли определенных производ 001679 4 ных циклогександионов, образующих, как указано в публикации, устойчивые кристаллы. В патенте США 4741768 представлены медные, литиевые и магниевые соли определенных 2-[1-(3-хлораллилоксиимино)алкилиден] циклогексан-1,3-дионов, обладающих повышенной устойчивостью в условиях хранения при соответствующей температуре и влажности(воздуха). При этом, однако, подчеркивается,что одна из особых солей лития отличается высокой гигроскопичностью. В европейской патентной заявке ЕР-А 085530 и патенте США 4952722 наряду с целым рядом циклогексеноноксимовых эфиров представлены также некоторые соли, причем в первой из вышеназванных публикаций в качестве катиона указан катион лития, натрия, калия или 1/2 меди, а во второй - катион лития, натрия, 1/2 меди или 1/2 никеля. Однако в обеих публикациях не указывается, каким особым преимуществом обладают эти соли. В патентной заявке Германии DE-A 3941160 представлены устойчивые при хранении соли ацилциклогександионоксимовых эфиров, обладающие гербицидным и регулирующим рост растений действием и проявляющие по сравнению со свободными соединениями более высокую стабильность в почве. Особо указаны соли с катионом лития, натрия, калия,1/2 магния, 1/2 кальция, 1/2 бария, 1/2 меди (II) или 1/2 цинка. В то же время подчеркивается,что соли при их получении часто кристаллизуются вместе с растворителем. В случае их последующего применения в качестве средств защиты растений этот фактор следовало бы рассматривать как недостаток. И последнее, касательно уровня техники: действующее вещество 2-(1-аллилоксииминобутил)-4-метоксикарбонил-5,5-диметил-3-оксоциклогексенол (общепринятое название: Аллоксидим) поставляется в торговую сеть в виде натриевой соли (ср. Meded. FAc. Landbouwwet. 1977, 42 (2, часть 2), 1597-1614; The PesticideManual, 9 е издание, 1991, стр. 21). Поскольку, таким образом, в литературе до настоящего времени были описаны циклогексеноноксимовые эфиры с самыми разными катионами, в отношении свободных соединений (II;Rb, следовательно, не обозначал бы Н), являющихся исходными для предлагаемых соединений формулы I, не представляется возможным точно определить, какие именно соли обладают особенно хорошими свойствами касательно устойчивости при хранении и температурного режима, подверженности воздействию влаги или их биологической эффективности. С учетом вышеизложенного в основу настоящего изобретения, исходя из циклогексеноноксимовых эфиров (II), была положена задача по получению гербицидных действующих веществ, обладающих более совершенными физическими свойствами. В соответствии с этой задачей были получены предлагаемые металлические соли циклогексеноноксимовых эфиров формулы I. Кроме того, были созданы гербицидные препараты,содержащие соединения формулы I и обладающие высокой гербицидной эффективностью. Далее было установлено, что соли I обладают исключительно высокой устойчивостью при хранении. Наряду с этим соли характеризуются отсутствием гигроскопичности и возможностью подвергаться более высоким термическим нагрузкам по сравнению со свободными кислотами (II), что, как подтверждают данные дифференциальной сканирующей калориметрии(ДСК), проявляется в термическом разложении,начинающемся лишь при температуре выше 100 С. Служащие исходными для получения солей I свободные циклогексеноноксимовые эфиры формулы II где Ra, Rc-Rf и Alk имеют те же значения, что и в формуле I, известны, например, из следующих публикаций: EP-A 368227, DE-A 4014983, DE-A 4014984, DE-A 4014986, DE-A 4014988 и U.S. 5228896. В качестве действующих веществ приемлемы как чистые энантиомеры I, так и их рацематы или смеси диастереомеров. Фрагменты органических молекул, указанные для Ra и Rc-Rl, а также для заместителей под обозначением Alk или (гетеро)циклов, представляют собой обобщающие понятия, включающие конкретные названия отдельных членов групп. Все углеродные цепи, т.е. все алкильные,галогеналкильные, алкилсульфонильные, алкилсульфинильные, алкоксильные, галогеналкоксильные, алкилтио-, алкенильные, алкенилокси-, алкинильные, алкинилокси- и ацильные фрагменты могут быть прямоцепочечными либо разветвленными. Галоидированные заместители несут предпочтительно от одного до пяти идентичных или различных атомов галогена. Поня 6 тием галоген обозначены соответственно фтор,бром, хлор или иод, прежде всего фтор или хлор. Особенно предпочтительными являются те металлические соли циклогексеноноксимовых эфиров формулы I, в которых заместители имеют следующие значения, а именно, соответственно индивидуально либо в определенном сочетании с другими:Ra обозначает этил или н-пропил;Rbобозначает ион щелочного металла или эквивалент катиона щелочно-земельного металла, прежде всего ион лития, натрия, калия или эквивалент иона магния; особенно предпочтителен ион лития;Rcобозначает 6- или 7-членный насыщенный либо одно- или двукратно ненасыщенный гетероцикл, который наряду с атомами углерода содержит один или два атома кислорода или серы либо один атом кислорода и один атом серы в качестве членов цикла и который необязательно может нести еще от одного до трех заместителей, соответственно выбранных из группы, включающей гидроксил, галоген, С 1-С 4 алкил, С 1-С 4 галогеналкил, С 1-С 4 алкокси и С 1-С 4 алкилтио, прежде всего тетрагидропиран-3-ил,тетрагидропиран-4-ил и тетрагидротиопиран-3 ил;Alk обозначает 3-6-членную алкиленовую цепь, которая необязательно может нести С 1-С 3 алкильный заместитель и которая наряду с метиленовыми или метиновыми звеньями содержит один атом кислорода либо серы в качестве мостикового члена, прежде всего этиленокси или 1,2-пропиленокси;Rfобозначает галогенфенил, прежде всего 4-фторфенил или 4-хлорфенил. В качестве особенно пригодных зарекомендовали себя металлические соли циклогексеноноксимовых эфиров формулы Ia (соответствует формуле I, где Rb обозначает Li; Rd, Re обозначают Н), прежде всего соединения, представленные в таблице 1. К особенно предпочтительным относятся далее металлические соли циклогексеноноксимовых эфиров формулы Ib, прежде всего соединения Ib.01-Ib.32, отличающиеся от соответствующих соединений Ia.01-Ia.32 лишь тем, что Rb обозначает эквивалент иона магния: Согласно полученным на сегодняшний день данным наиболее предпочтительными зарекомендовали себя соединенияIa.18 и Ib.18. В принципе возможность получения металлических солей циклогексеноноксимовых эфиров формулы I состоит в тем, что соответствующее свободное соединение (II) подвергают взаимодействию с гидридом, гидроксидом, алкоголятом либо карбонатом требуемого иона металла. Особенно рекомендуется при этом исходить из раствора соединения (II), образующегося при его получении из соединений III и IV(см., например, европейскую патентную заявку ЕР-А 456112), т.е. без предварительного выделения соединения II. Пригодными для соединений II растворителями являются прежде всего вода или смешиваемые с водой растворители, например, простые эфиры, такие как тетрагидрофуран и диоксан, или низшие спирты, такие как метанол и этанол. Гидрид, гидроксид, алкоксид или карбонат металла применяют, как правило, в растворенном либо суспендированном в одном из вышеназванных растворителей виде или же в твердой форме. Нейтрализацию соединений II осуществляют обычно при температуре в интервале от-100 до 200 С, предпочтительно от -40 до 120 С,прежде всего от -10 до 80 С. Образующуюся реакционную воду удаляют при этом предпочтительно азеотропной перегонкой. После отделения низкокипящих компонентов получают затем сухую металлическую соль циклогексеноноксимового эфира формулыI в кристаллическом или аморфном виде. Один из вариантов осуществления способа состоит в том, что свободное соединение формулы II растворяют в инертном, не смешиваемым с водой растворителем, например, в простом эфире, таком, как диэтиловый эфир, диизопропиловый эфир, метил-трет-бутиловый эфир, в кетоне, таком, как ацетон, в ароматическом углеводороде, таком, как толуол и ксилолы, в галоидированном углеводороде, таком, как метиленхлорид, хлороформ и 1,2-дихлорэтан,или в высшем спирте, таком, как 2-этилгексанол, и нейтрализуют гидридом, гидроксидом,алкоксидом либо карбонатом металла в твердом виде или в растворенном либо суспендированном в воде или в низшем спирте виде. Образующаяcя при этом металлическая соль циклогексеноноксимового эфира либо выпадает из реакционной смеси в осадок, либо после удаления растворителя ее получают в аморфной или кристаллической форме. 9 Другой вариант осуществления способа заключается в том, что соединение формулы II подвергают взаимодействию с примерно эквимолярным количеством алкоголята требуемого иона металла, причем соответствующий спирт служит в этом случае растворителем. Алкоголят можно использовать либо непосредственно, либо его можно получать in situ из металла и спирта. Выделение соединения I проводят в этом случае обычно концентрированием реакционного раствора или добавлением неполярного осадителя, например, ароматического углеводорода, такого, как бензол, толуол или ксилолы, углеводорода, такого, как н-пентан, н-гексан, петролейный эфир и циклогексан, или простого эфира, такого, как диэтиловый эфир, диизопропиловый эфир и метил-трет-бутиловый эфир, и отделением кристаллического или аморфного целевого продукта. Кроме того, из металлических солей циклогексеноноксимовых эфиров формулы I, где Rb обозначает ион щелочного металла, путем пересаливания можно получать другие соли. С этой целью обычно смешивают водный раствор хорошо растворимой соли I, например,соли Na, с (как правило, водным) раствором галогенида металла либо сульфата металла. При необходимости пересаливание можно проводить в присутствии смешиваемого с водой растворителя, например, простого циклического эфира, такого, как тетрагидрофуран и диоксан,или низшего спирта, либо в присутствии несмешиваемого с водой растворителя, например,ароматического углеводорода, такого, как толуол и ксилолы, простого эфира, такого, как диэтиловый эфир, диизопропиловый эфир и метил-трет-бутиловый эфир, кетона, такого, как ацетон, галоидированного углеводорода, такого,как метиленхлорид и хлороформ, или же высшего спирта, такого, как 2-этилгексанол. В случае соответственно малой растворимости требуемой соли I в воде ее осаждение из реакционной смеси начинается уже в ходе описанного процесса. При достаточной степени растворимости в органическом, несмешиваемым с водой растворителе требуемую соль I можно экстрагировать также с помощью этого растворителя. Растворенный галогенид обычно остается в этом случае в водной фазе. При получении металлических солей циклогексеноноксимовых эфиров формулы I последние могут быть получены в виде смесей изомеров, которые, однако, при необходимости по обычным в таких случаях методам, например, путем кристаллизации или посредством хроматографии, с использованием в том числе оптически активного адсорбата, могут разделяться на чистые изомеры. Чистые, оптически активные изомеры предпочтительно могут быть получены из соответствующих оптически активных исходных продуктов (II). 10 Металлические соли циклогексеноноксимовых эфиров формулы I пригодны для применения как в виде изомерных смесей, так и в виде чистых изомеров в качестве гербицидов. В основном они обладают совместимостью и тем самым избирательностью действия в широколистных культурах, а также по отношению к однодольным растениям, не относящимся к злаковым. Некоторые из солей I по изобретению могут применяться также для селективной борьбы с нежелательными травами в посевах злаковых. Этот эффект достигают прежде всего при низких нормах расхода. В зависимости от соответствующего метода обработки средства согласно изобретению могут применяться для уничтожения нежелательной растительности также в целом ряде других культурных растений. Среди таковых можно назвать, например, следующие культуры:vinifera и Zea mays. Кроме того, металлические соли циклогексеноноксимовых эфиров формулы I могут применяться также в культурах, которые благодаря методам селекции, включая методы генной инженерии, приобрели значительную устойчивость к действию гербицидов. Металлические соли циклогексеноноксимовых эфиров формулы I, соответственно содержащие их гербицидные препараты могут применяться, например, в виде предназначенных для непосредственного опрыскивания водных растворов, порошков, суспензий, в том числе высококонцентрированных водных, масляных или каких-либо других суспензий, или дисперсий, эмульсий, масляных дисперсий, паст,препаратов для опыливания, препаратов для опудривания или гранулятов, которые исполь 11 зуют для обработки самыми разными методами,такими, как опрыскивание, обработка в виде туманов, опыливание, опудривание или полив. Технология обработки и используемые формы целиком зависят при этом от целей применения,но во всех случаях должно быть обеспечено максимально тонкое и равномерное распределение солей I по изобретению. В качестве инертных вспомогательных веществ могут рассматриваться в основном следующие: фракции нефтяного топлива с температурой кипения от средней до высокой, такие,как керосин или дизельное топливо, далее каменноугольные масла, а также масла растительного или животного происхождения, алифатические, циклические и ароматические углеводороды, например, парафины, тетрагидронафталин, алкилированные нафталины и их производные, алкилированные бензолы и их производные, спирты, такие, как метанол, этанол,пропанол, бутанол и циклогексанол, кетоны,такие, как циклогексанон, сильно полярные растворители, например амины, такие, как Nметилпирролидон, и вода. Водные формы применения могут приготавливаться из эмульсионных концентратов,суспензий, паст, смачивающихся порошков или диспергируемых в воде гранулятов добавлением воды. Для приготовления эмульсий, паст или масляных дисперсий субстраты как таковые либо после их растворения в масле или растворителе можно с помощью смачивателей, прилипателей, диспергаторов или эмульгаторов гомогенизировать в воде. Возможно также из действующего вещества, смачивателей, прилипателей, диспергаторов или эмульгаторов и необязательно растворителей или масла получать концентраты, пригодные для разбавления водой. В качестве поверхностно-активных веществ могут использоваться соли щелочных и щелочноземельных металлов и аммониевые соли ароматических сульфокислот, например,лигнин-, фенол-, нафталин- и дибутилнафталинсульфокислоты, а также соли жирных кислот,алкил- и алкиларилсульфонаты, алкилсульфаты,сульфаты лаурилового эфира и жирных спиртов и соли сульфатированных гекса-, гепта- и октадеканолов, а также гликолевых эфиров жирных спиртов, продукты конденсации сульфированного нафталина и его производных с формальдегидом, продукты конденсации нафталина,соответственно нафталинсульфокислот с фенолом и формальдегидом, полиоксиэтиленоктилфеноловый эфир, этоксилированный изооктил-,октил- или нонилфенол, полигликолевые эфиры алкилфенила и трибутилфенила, алкилариловые полиэфиры спиртов, изотридециловый спирт,конденсаты этиленоксида и жирных спиртов,этоксилированное касторовое масло, полиоксиэтилен- или полиоксипропиленалкиловые эфиры, ацетат эфира лаурилового спирта и поли 001679 12 гликоля, сложные эфиры сорбита, отработанный лигнинсульфитный щелок или метилцеллюлоза. Порошковые препараты, препараты для опыливания и опудривания могут приготавливаться путем смешения или совместного измельчения действующих веществ с каким-либо твердым наполнителем. Грануляты, например, грануляты в оболочке, импрегнированные грануляты и гомогенные грануляты могут быть получены за счет связывания действующих веществ с твердыми наполнителями. В качестве таких твердых наполнителей могут служить минеральные земли,в частности кремниевые кислоты, силикагели,силикаты, тальк, каолин, известняк, известь,мел, болюс, лесс, глина, доломит, диатомовая земля, сульфат кальция и магния, оксид магния,измельченные синтетические материалы, удобрения, такие, как сульфат аммония, фосфат аммония, нитрат аммония, мочевины и растительные продукты, такие, как мука зерновых, мука из коры деревьев, древесная мука и мука из ореховой скорлупы, целлюлозные порошки или какие-либо другие твердые наполнители. Концентрацию действующих веществ формулы I в готовых для применения композициях можно варьировать в широких пределах, а именно, приблизительно от 0,001 до 98 мас.%,предпочтительно от 0,01 до 95 мас.%. Действующие вещества применяют при этом со степенью чистоты от 90% до 100%, предпочтительно от 95% до 100% (согласно ЯМРспектру). Предлагаемые соли формулы I, соответственно их композиции могут применяться в методах как предвсходовой, так и послевсходовой обработки, преимущественно путем опрыскивания листьев. Если действующие вещества обладают недостаточной совместимостью с некоторыми культурными растениями, то рекомендуется применять такую технологию обработки,при которой гербицидные препараты следует распылять с помощью соответствующих опрыскивателей таким образом, чтобы они по возможности не попадали на листья чувствительных культур, а были направлены на листья растущих среди них нежелательных растений или на открытые участки почвы (способ направленного опрыскивания, способ ленточного опрыскивания). Нормы расхода действующего вещества формулы I составляют в зависимости от цели обработки, времени года, обрабатываемых растений и стадии роста от 0,001 до 3,0, предпочтительно от 0,01 до 1,0 кг/га активной субстанции(а.с.). Обработку при этом можно проводить,используя, например, воду в качестве носителя,по обычной технологии опрыскивания при нормах расхода соответствующего раствора от порядка 100 до 1000 л/га. Возможно также применение гербицидных препаратов в так называемом способе низких объемов илиUltralow Volume), равно как и их применение в виде гранулятов. Для расширения спектра действия и достижения синергетического эффекта металлические соли циклогексеноноксимовых эфиров формулы I можно смешивать с многочисленными представителями других групп активных веществ, обладающих гербицидным и регулирующим рост действием, и применять их для совместной обработки. В качестве сокомпонентов для таких смесей могут рассматриваться среди прочих, например, 1,2,4-тиадиазолы,1,3,4-тиадиазолы, амиды, аминофосфорная кислота и ее производные, аминотриазолы, анилиды, арилокси-/гетероарилоксиалкановые кислоты и их производные, бензойная кислота и ее производные, бензотиадиазиноны, 2-(гетароил/ ароил)-1,3-циклогександионы, гетероарил-арилкетоны, бензилизоксазолидиноны, мета-CF3 фенильные производные, карбаматы, хинолинкарбоновая кислота и ее производные, хлорацетанилиды, производные циклогексан-1,3-диона,диазины, дихлорпропионовая кислота и ее производные, дигидробензофураны, дигидрофуран 3-оны, динитроанилины, динитрофенолы, дифениловые эфиры, дипиридилы, галогенкарбоновые кислоты и их производные, мочевины, 3 фенилурацилы, имидазолы, имидазолиноны, Nфенил-3,4,5,6-тетрагидрофталимиды, оксадиазолы, оксираны, фенолы, эфиры арилокси- и гетероарилоксифеноксипропионовой кислоты,фенилуксусная кислота и ее производные, 2 фенилпропионовая кислота и ее производные,пиразолы, фенилпиразолы, пиридазины, пиридинкарбоновая кислота и ее производные, пиримидиловые эфиры, сульфонамиды, сульфонилмочевины, триазины, триазиноны, триазолиноны, триазолкарбоксамиды и урацилы. Особенно пригодными для использования в указанных целях являются N-(бутоксиметил)2-хлор-N-(2,6-диэтилфенил)ацетамид 15 Кроме того, может оказаться полезным и целесообразным применять металлические соли циклогексеноноксимовых эфиров формулы I индивидуально или в сочетании с другими гербицидами также в смесях с целым рядом других средств защиты растений для совместной обработки, например, со средствами борьбы против вредителей или фитопатогенных грибов, соответственно бактерий. Интерес представляет далее возможность смешения с растворами минеральных солей, предназначенными для компенсации недостатка питательных веществ и микроэлементов. Можно также вводить добавки нефитотоксичных масел и масляных концентратов. Примеры по получению Пример 1. Получение натриевой соли 2-1[2-(4-хлорфенокси)пропилоксимино]бутил-5 тетрагидротиопиран-3-илциклогексан-1,3 диона. К раствору 2-1-[2-(4-хлорфенокси)пропилоксимино]бутил-5-тетрагидротиопиран-3 илциклогексан-1,3-диона (12,4 г) в 10 мл толуола при интенсивном перемешивании добавляли раствор гидроксида натрия (1,04 г) в 13,4 мл воды. По истечении 20 мин водную фазу отделяли и концентрировали ее под вакуумом. Выход: 11,5 г требуемой натриевой соли. В другом эксперименте целевой продукт получали путем сублимационного обезвоживания. Пример 2. Получение калиевой соли 2-1[2-(4-хлорфенокси)пропилоксимино]бутил-5 тетрагидротиопиран-3-илциклогексан-1,3-диона Работали аналогично примеру 1 с тем, однако, отличием, что вместо гидроксида натрия применяли 1,81 г гидроксида калия. После концентрирования водной фазы под вакуумом получили 12,0 г требуемой калиевой соли. Пример 3. Получение магниевой соли 21-[2-(4-хлорфенокси)пропилоксимино]бутил 5-тетрагидротиопиран-3-илциклогексан-1,3 диона. К раствору 2-1-[2-(4-хлорфенокси)пропилоксимино]бутил-5-тетрагидротиопиран-3 илциклогексан-1,3-диона (698 г) в 1,5 л метанола при 20-30 С добавляли по каплям раствор метанолята магния (90 г) в 0,5 л метанола. По завершении процесса добавления нагревали еще в течение 2 ч до температуры дефлегмации, после чего метанол отгоняли. Остаточные количества метанола полностью удаляли добавками толуола и последующим концентрированием смеси. С целью очистки остаток смешивали с метил-трет-бутиловым эфиром, после чего его повторно отделяли. После сушки получили 556 г требуемой магниевой соли. Пример 4. Получение кальциевой соли 21-[2-(4 хлорфенокси)пропилоксимино]бутил 5-тетрагидротиопиран-3-илциклогексан-1,3 диона. 16 К раствору 2-1-[2-(4-хлорфенокси)пропилоксимино]бутил-5-тетрагидротиопиран-3 илциклогексан-1,3-диона (2,5 г) в 80 мл метанола при интенсивном перемешивании добавляли суспензию гидроксида кальция (0,2 г) в 30 мл метанола. Затем смесь в течение 5 ч перемешивали при комнатной температуре, после чего растворитель удаляли под вакуумом. Выход: 2,6 г кальциевой соли. Пример 5. Получение литиевой соли 2-1[2-(4-хлорфенокси)пропилоксимино]бу-тил-5 тетрагидротиопиран-3-илциклогексан-1,3 диона. Раствор 2-1-[2-(4-хлорфенокси)пропилоксимино]бутил-5-тетрагидротиопиран-3 илциклогексан-1,3-диона (300 г) в 900 мл метилтрет-бутилового эфира при интенсивном перемешивании добавляли к раствору гидроксида лития (16,8 г) в 500 мл воды. Затем образовавшийся твердый продукт отделяли и сушили в вакуумно-сушильном шкафу. Выход: 285 г литиевой соли со степенью чистоты 97%. Пример 6. Получение литиевой соли 2-1[2-(4-хлорфенокси)пропилоксимино]бутил-5 тетрагидротиопиран-3-илциклогексан-1,3 диона. Раствор гидроксида лития (1,85 г) в 60 мл воды при интенсивном перемешивании добавляли к раствору 2-1-[2-(4-хлорфенокси) пропилоксимино]бутил-5-тетрагидротиопиран-3 илциклогексан-1,3-диона (43,5 г) в 100 мл толуола, после чего перемешивали в течение ночи при комнатной температуре. Затем образовавшийся твердый продукт отделяли и сушили в вакуумно-сушильном шкафу. Выход: 28 г литиевой соли. Пример 7. Получение литиевой соли 2-1[2-(4-хлорфенокси)пропилоксимино]бутил-5 тетрагидротиопиран-3-илциклогексан-1,3 диона. Раствор гидроксида лития (1,85 г) в 60 мл воды при интенсивном перемешивании добавляли в раствор сырого продукта 2-1-[2-(4 хлорфенокси)про-пилоксимино]бутил-5 тетрагидротиопиран-3-илциклогексан-1,3-диона(56,7%-ный; 43,5 г) в 100 мл метил-третбутилового эфира. После перемешивания в течение 2 ч при комнатной температуре образовавшийся твердый продукт отделяли и сушили в вакуумно-сушильном шкафу. Таким путем получили 27,1 г литиевой соли со степенью чистоты 86,8% (выход: 94,3% от теории). Пример 8. Получение натриевой соли 2-1[2-(4-хлорфенокси)пропилоксимино]бутил-5 тетрагидротиопиран-3-илциклогексан-1,3 диона. Раствор гидроксида натрия (2,64 г) в 90 мл воды добавляли к раствору 2-1-[2-(4-хлорфенокси)пропилоксимино]бутил-5-тетрагидротиопиран-3-илциклогексан-1,3-диона (90,5%-ный; 32,4 г) в 100 мл толуола. После перемешивания в течение 1/4 ч при комнатной температуре фа 17 зы разделяли. Выход: 142,4 г водного раствора целевого продукта. Пример 9. Получение литиевой соли 2-1[2-(4-хлорфенокси)пропилоксимино]бутил-5 тетрагидротиопиран-3-илциклогексан-1,3-диона за счет обмена натрий/литий. Половину полученного в примере 8 раствора натриевой соли охлаждали до 10 С и по каплям добавляли к охлажденному до 10 С раствору хлорида лития (1,4 г) в 110 мл воды. Затем перемешивали в течение ночи при комнатной температуре, после чего твердый продукт отделяли и сушили. Таким путем получили 13,4 г литиевой соли со степенью чистоты 97,8%(выход: 88% от теории). Пример 10. Получение литиевой соли 2-1[2-(4-хлорфенокси)пропилоксимино]бутил-5 тетрагидротиопиран-3-илциклогексан-1,3-диона за счет обмена натрий/литий. Вторую половину полученного в примере 8 раствора натриевой соли охлаждали до 10 С и по каплям добавляли в охлажденную до 10 С смесь из 100 мл метил-трет-бутилового эфира и раствора хлорида лития (1,4 г) в 110 мл воды. Затем смесь перемешивали в течение ночи при комнатной температуре, после чего твердый продукт отделяли и сушили. Таким путем получили 12,5 г литиевой соли со степенью чистоты 99,5% (выход: 84% от теории). Исследование физических свойств 1) Определение абсорбции водяных паров(гигроскопичность). Для определения абсорбции водяных паров исследуемые пробы действующих веществ сначала сушили в течение 48 ч при 50 С под вакуумом, а затем при температуре окружающей среды 20 С выдерживали в условиях относительной влажности воздуха 32, 52 или 66%. По истечении 14 дней определяли затем, на сколько увеличивался вес проб. В таблице 2 представлена абсорбция водяных паров различными солями 2-1-[2-(4-хлорфенокси)пропилоксимино]бутил-5-тетрагидротиопиран-3-илциклогексан-1,3-диона (в процентном выражении по отношению к исходному весу). Таблица 2 Относительная влажность воздуха Соль 32% 52% 66% Литиевая соль 0% 0,3% 0,5% Магниевая соль 0% 1% 2% Натриевая соль 3% 8% 11% Калиевая соль 4% 8% 12% 2) Построение ДСК кривых: Измерения проводили в интервале температур от 20 до 400 С при скорости нагрева 5 К/мин. До начала измерений пробы действующих веществ подвергали сушке. Для прове 001679 18 дения собственно измерений использовали прибор DSC 200 фирмы Netzsch. Как видно на ДСК-кривых, разложение литиевой, натриевой, магниевой и кальциевой солей 2-1-[2-(4-хлорфенокси)пропилоксимино] бутил-5-тетрагидротиопиран-3-илциклогексан 1,3-диона [фиг. 1-2] начинается лишь при температуре выше примерно 140 С. ДСК - дифференциальная сканирующая калориметрия. 3) Определение устойчивости при хранении. С этой целью различные пробы действующих веществ помещали на хранение в плотно закрытые стеклянные сосуды, где их выдерживали в течение определенного периода времени при различных температурах. Затем определяли содержание действующих веществ в пробах и сравнивали с этим показателем до начала процесса хранения (нулевое значение). В таблице 3 представлено содержание действующих веществ в относительных долях от нулевого значения. Таблица 3. Сравнительная характеристика устойчивости различных солей 2-1-[2-(4-хлорфенокси) пропилоксимино]бутил-5-тетрагидротиопиран 3-илциклогексан-1,3-диона (II) при хранении по истечении 3 месяцев. Соль Натриевая соль Магниевая соль Литиевая соль Устойчивость при хранении при 20 С 30 С 40 С 50 С 100% 87% 43% В отличие от представленных результатов показатель относительного содержания действующих веществ у свободного соединения (II)[в виде 87%-ного технического действующего вещества] по истечении 3 месяцев хранения при 20 С составлял лишь несколько более 69%. Примеры композиций Пример 11. Эмульсионный концентрат. 10 мас. частей литиевой соли 2-1-[2(4 хлорфенокси)пропилоксимино]бутил-5 тетрагидротиопиран-3-илциклогексан-1,3-диона растворяли в смеси, состоящей из 80 мас. частей алкилированного бензола и 20 мас. частей продукта присоединения 8 молей этеленоксида к одному молю нонилфенила. Таким путем получили устойчивый эмульсионный концентрат. Пример 12. 5%-ная гранулированная композиция: 5 мас.% магниевой соли 2-1-[2-(4 хлорфенокси)пропилоксимино]бутил-5 тетрагидротиопиран-3-илциклогексан-1,3 диона,3 мас.% конденсата фенолсульфоновой кислоты и формальдегида, 19 3 мас.% конденсата фенола, формальдегида и сульфита,20 мас.% метасиликата натрия и остальное до 100 мас.% мел,после тщательного перемешивания размалывали с помощью ротационной быстродействующей мельницы. Затем смесь увлажняли водой и экструдировали с помощью экструдера корзиночного типа. Полученный гранулят сушили. После непродолжительного хранения в течение 14 дней при 54 С содержание действующего вещества составляло все еще 88% от первоначального. Пример 13. Диспергируемый в воде порошок. 12,5 мас.% литиевой соли 2-1-[2-(4 хлорфенокси)пропилоксимино]бутил-5 тетрагидротиопиран-3-илциклогексан-1,3 диона,7 мас.% конденсата нафталинсульфоновой кислоты и формальдегида,14 мас.% лигнинсульфоната натрия,3 мас.% конденсата фенолсульфоновой кислоты и формальдегида и остальное до 100 мас.% мел,после тщательного перемешивания размалывали с помощью ротационной быстродействующей мельницы. Таким путем получили диспергируемый в воде порошок. Пример 14. Диспергируемый в воде гранулят. 70 мас.% литиевой соли 2-1-[2-(4-хлорфенокси)пропилоксимино]бутил-5-тетрагидротиопиран-3-илциклогексан-1,3-диона и остальное до 100 мас.% конденсат нафталинсульфоновой кислоты и формальдегида тщательно перемешивали, а затем размалывали с помощью ротационной быстродействующей мельницы, увлажняли и экструдировали с помощью экструдера корзиночного типа. Полученный гранулят сушили. После непродолжительного хранения при 54 С в течение 14 дней содержание действующего вещества все еще составляло 99% от исходного показателя. Пример по применению Гербицидное действие металлических солей циклогексеноноксимовых эфиров формулыI было подтверждено при проведении в теплице следующих опытов: Сосудами для культур служили пластиковые цветочные горшки с суглинком, содержавшим приблизительно 3,0% гумуса в качестве субстрата. Семена опытных растений высевали раздельно по видам. Предвсходовую обработку проводили суспендированными или эмульгированными в воде действующими веществами непосредственно после высевания с помощью соответствующих сопел, обеспечивающих мелкокапельное опрыскивание. Сосуды подвергали легкому дождеванию с целью обеспечить прорастание и последующий рост, после чего их закрывали прозрач 001679 20 ными пластиковыми крышками, пока растения не пошли в рост. Такие крышки способствуют равномерному прорастанию опытных растений,пока еще этот процесс не подвержен воздействию активных веществ. Для проведения послевсходовой обработки опытные растения в зависимости от экстерьера выращивали сначала до достижения ими высоты от 3 до 15 см и лишь после этого обрабатывали суспендированными или эмульгированными в воде действующими веществами. С этой целью опытные растения либо непосредственно высевали и выращивали в одних и тех же сосудах, либо их сначала выращивали в качестве зародышевых растений раздельно и только лишь за несколько дней до обработки пересаживали в опытные сосуды. Нормы расхода при послевсходовой обработке составляли 0,25 кг/га а.с. (активной субстанции). Растения выдерживали раздельно по их видам при температурах в интервале от 10 до 25 С, соответственно от 20 до 35 С. Опыты проводились в течение 2-4 недель. В течение этого периода времени за растениями вели тщательный уход и определяли их реакцию на каждую из проведенных обработок. Оценку результатов производили по шкале с градацией от 0 до 100. При этом показатель 100 означает, что растения не взошли, соответственно имеет место полная гибель по меньшей мере их надземных частей, а показатель 0 означает отсутствие повреждений, соответственно нормальный процесс роста. Опыты в теплице проводили на растениях следующих видов: Латинское название Русское названиеSetaria viridis Щетинник зеленый При норме расхода 0,25 кг/га а.с. литиевая соль 2-1-[2-(4-хлорфенокси)пропилоксимино] бутил-5-тетрагидротиопиран-3-илциклогексан 1,3-диона при ее применении в методе послевсходовой обработки проявила очень высокую эффективность действия против вышеуказанных сорняков. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Металлические соли циклогексеноноксимовых эфиров общей формулы IRc обозначает водород, циано, формил, С 1 С 6 алкил, С 1-С 4 алкокси-С 1-С 6 алкил, С 1-С 4 алкилтио-С 1-С 6 алкил, фенокси-С 1-С 6 алкильную, фенилтио-С 1-С 6 алкильную,пиридилокси-С 1-С 6 алкильную или пиридилтио-С 1-С 6 алкильную группу, причем фенильные и пиридильные кольца этих групп при необходимости могут нести от одного до трех заместителей, соответственно выбранных из группы, включающей нитро, циано, галоген, С 1-С 4 алкил, С 1-С 4 галогеналкил, С 1-С 4 алкокси, С 1-С 4 галогеналкокси, С 1 С 4 алкилтио, С 3-С 6 алкенил, С 3-С 6 алкенилокси,С 3-С 6 алкинил, С 3-С 6 алкинилокси и -NRgRh,где Rg обозначает водород, С 1-С 4 алкил, С 3 С 6 алкенил, С 3-С 6 алкинил, С 1-С 6 ацил или бензоил, который в свою очередь необязательно может нести еще от одного до трех остатков, соответственно выбранных из группы, включающей нитро, циано, галоген, С 1-С 4 алкил, С 1-С 4 галогеналкил, С 1-С 4 алкокси и С 1-С 4 алкилтио, иRh обозначает водород, С 1-С 4 алкил, С 3 С 6 алкенил или С 3-С 6 алкинил; С 3-С 7 циклоалкильную или С 5-С 7 циклоалкенильную группу,причем эти группы при необходимости могут нести от одного до трех заместителей, соответственно выбранных из группы, включающей гидроксил, галоген, С 1-С 4 алкил, С 1-С 4 галогеналкил, С 1-С 4 алкокси, С 1-С 4 алкилтио, бензилтио, С 1-С 4 алкилсульфонил и С 1-С 4 алкилсульфинил; 5-членный насыщенный гетероцикл, который наряду с атомами углерода содержит один или два атома кислорода либо серы или один атом кислорода и один атом серы в качестве членов цикла и который необязательно может нести еще от одного до трех заместителей, соответственно выбранных из группы, включающей С 1-С 4 алкил, С 1-С 4 галогеналкил, С 1-С 4 алкокси и С 1-С 4 алкилтио; 6- или 7-членный насыщенный либо одно или двукратно ненасыщенный гетероцикл, который наряду с атомами углерода содержит один или два атома кислорода либо серы или один атом кислорода и один атом серы в качестве членов цикла и который необязательно может нести еще от одного до трех заместителей, соответственно выбранных из группы, включающей гидроксил, галоген, С 1-С 4 алкил, С 1-С 4 галогеналкил, С 1-С 4 алкокси и С 1-С 4 алкилтио; 5-членный гетероароматический углеводород, который наряду с атомами углерода содержит один или два атома азота и один атом кислорода либо серы или от одного до трех атомов азота или один атом кислорода либо серы в качестве членов цикла и который необязательно может нести еще от одного до трех заместителей, соответственно выбранных из группы,включающей циано, галоген, С 1-С 4 алкил, С 1-С 4 галогеналкил, С 1-С 4 алкокси, С 1-С 4 галогеналкокси, С 1-С 4 алкилтио, С 2-С 6 алкенил, С 2-С 6 алкенилокси, С 3-С 6 алкинилокси и С 1-С 4 алкокси-С 1 С 4 алкил; 22 фенил или пиридил, оба которые необязательно могут нести от одного до трех заместителей, соответственно выбранных из группы,включающей нитро, циано, формил, галоген, С 1 С 4 алкил, С 1-С 4 галогеналкил, С 1-С 4 алкокси, С 1 С 4 галогеналкокси, С 1-С 4 алкилтио, С 3-С 6 алкенил,С 3-С 6 алкенилокси, С 3-С 6 алкинил, С 3-С 6 алкинилокси и -NRkRl,где Rk обозначает водород, С 1-С 4 алкил, С 3 С 6 алкенил или С 3-С 6 алкинил иRl обозначает водород, С 1-С 4 алкил, С 3-С 6 алкенил, С 3-С 6 алкинил, С 1-С 6 ацил или бензоил,который в свою очередь необязательно может нести еще от одного до трех заместителей, соответственно выбранных из группы, включающей нитро, циано, галоген, С 1-С 4 алкил, С 1-С 4 галогеналкил, С 1-С 4 алкокси и С 1-С 4 алкилтио;Alk обозначает С 1-С 6 алкиленовую, С 3-С 6 алкениленовую или С 3-С 6 алкиниленовую цепь,которая может нести соответственно метиленовую группу (=СН 2) и/или от одного до трех заместителей, соответственно выбранных из галогена и С 1-С 3 алкила; 3-6-членную алкиленовую или 4-6 членную алкениленовую цепь, которая необязательно может нести от одного до трех С 1 С 3 алкильных заместителей и которая наряду с метиленовыми и метиновыми звеньями содержит один из следующих мостиковых членов: кислород, серу, -SO-, -SO2- или -N(Ri)-, где Ri представляет собой водород, С 1-С 4 алкил, С 3-С 6 алкенил или С 3-С 6 алкинил;Rf обозначает фенильную группу, галогенфенильную либо дигалогенфенильную группу,причем каждое фенильное кольцо необязательно может нести от одного до трех заместителей,соответственно выбранных из группы, включающей нитро, циано, формил, галоген, С 1 С 4 алкил, С 1-С 4 галогеналкил, С 1-С 4 алкокси, С 1 С 4 галогеналкокси, С 3-С 6 алкенил, С 3-С 6 алкенилокси, С 3-С 6 алкинил, С 3-С 6 алкинилокси иRl обозначает водород, С 1-С 4 алкил, С 3-С 6 алкенил, С 3-С 6 алкинил, С 1-С 6 ацил или бензоил,который необязательно может нести в свою очередь еще от одного до трех остатков, соответственно выбранных из группы, включающей нитро, циано, галоген, С 1-С 4 алкил, С 1-С 4 галогеналкил, С 1-С 4 алкокси и С 1-С 4 алкилтио. 2. Металлические соли цикогексеноноксимовых эфиров формулы I по п.1, где Rb обозначает ион лития;Rc обозначает 6- или 7-членный насыщенный либо одно или двукратно ненасыщенный гетероцикл, который наряду с атомами углерода содержит один или два атома кислорода либо серы или один атом кислорода и один атом серы в качестве членов цикла и который необязательно может нести еще от одного до трех заместителей, соответственно выбранных из группы, включающей гидроксил, галоген, С 1 С 4 алкил, С 1-С 4 галогеналкил, С 1-С 4 алкокси и C1 С 4 алкилтио;Rd и Re обозначают водород. 3. Металлические соли циклогексеноноксимовых эфиров формулы I по п.1, где Ra обозначает этил или н-пропил,Rb обозначает ион лития;Rd и Re обозначают соответственно водород и Rf обозначает галофенил. 4. Применение металлических солей циклогексеноноксимовых эфиров формулы I по пп.1-3 в качестве гербицидов. 5. Гербицидный препарат, содержащий гербицидно эффективное количество, по меньшей мере, одной металлической соли циклогексеноноксимового эфира формулы I по пп.1-3 и,по меньшей мере, один инертный жидкий и/или твердый наполнитель, а также не обязательно,по меньшей мере, одно поверхностно-активное вещество. 6. Способ получения обладающих гербицидным действием средств, отличающийся тем,что смешивают гербицидно эффективное количество, по меньшей мере, одной металлической соли циклогексеноноксимового эфира формулыI по п.1 и, по меньшей мере, один инертный жидкий и/или твердый наполнитель, а также не обязательно, по меньшей мере, одно поверхностно-активное вещество. 7. Способ борьбы с нежелательной растительностью, отличающийся тем, что гербицидно эффективным количеством, по меньшей мере,одной металлической соли циклогексеноноксимового эфира формулы I по п.1 воздействуют на растения, среду их произрастания или на посевной материал. 8. Способ получения металлических солей циклогексеноноксимовых эфиров формулы I по п.1, отличающийся тем, что соответствующие свободные соединения формулы II где Ra, Rc-Rf и Alk имеют те же значения, что и в формуле I, подвергают взаимодействию с гид 24 роксидом, гидридом, (С 1-С 5 алкоксидом) или карбонатом лития или магния. 9. Способ получения металлических солей циклогексеноноксимовых эфиров формулы I по п.1, отличающийся тем, что металлическую соль циклогексеноноксимового эфира формулыI, в которой Rb представляет собой катион щелочного металла, подвергают "пересаливанию" с применением галогенида или сульфата лития. ДСК-кривая для литиевой соли 2-(1-[2-(4 хлорфенокси)пропилоксимино]бутил)-5 тетрагидротиопиран-3-илциклогексан-1,3-диона Фиг. 1 ДСК-кривая для магниевой соли 2-(1- [2-(4 хлорфенокси)пропилоксимино]бутил)-5 тетрагидротиопиран-3-илциклогексан-1,3-диона
МПК / Метки
МПК: C07C 251/42, A01N 43/14
Метки: металлические, эфиров, циклогексеноноксимовых, соли
Код ссылки
<a href="https://eas.patents.su/13-1679-metallicheskie-soli-ciklogeksenonoksimovyh-efirov.html" rel="bookmark" title="База патентов Евразийского Союза">Металлические соли циклогексеноноксимовых эфиров</a>
Предыдущий патент: Способ получения монохромата натрия
Следующий патент: Производные бензопирана, обладающие антагонистическим действием в отношении лейкотриена.
Случайный патент: Ингалятор для вдыхания лекарственных веществ и способ сборки ингалятора