Водные суспензии сложных эфиров жирной кислоты 9-гидроксирисперидона
Номер патента: 536
Опубликовано: 28.10.1999
Авторы: Боргхейс Херман Карел, Эмбрехтс Роже Каролус Аугуста, Франсуа Марк Карел Йозеф, Монбалиу Йохан
Формула / Реферат
1. Фармацевтическая композиция, пригодная в качестве депо-препарата для внутримышечного или подкожного введения, содержащая:
1) в качестве активного ингредиента терапевтически эффективное количество сложного эфира жирной кислоты 9-гидроксирисперидона, имеющего формулу:
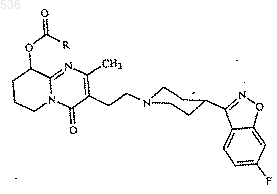
или его соли, или стереоизомера или стереоизомерной смеси, где R представляет собой неразветвленный С9-19-алкильный радикал; и
2) фармацевтически приемлемый носитель, отличающийся тем, что фармацевтически приемлемым носителем является вода и в ней суспендирован активный ингредиент.
2. Композиция по п.1, отличающаяся тем, что R представляет собой неразветвленную C15-цепь (пентадецильную) и активным ингредиентом является пальмитат 9-гидроксирисперидона.
3. Композиция по п.1, отличающаяся тем, что композиция дополнительно содержит суспендирующий агент и смачивающее вещество и необязательно один или несколько ингредиентов, выбранных из консерванта, буфера и изотонирующего средства.
4. Композиция по п.3, отличающаяся тем, что суспендирующим агентом является натрийкарбоксиметилцеллюлоза и смачивающим веществом является полисорбат 20.
5. Композиция по п.4, отличающаяся тем, что консервантом является бензиловый спирт и изотонирующим средством является маннит или фосфатный буфер.
6. Композиция по п.1, отличающаяся тем, что имеет вязкость менее 75 мРаъс.
7. Композиция по п.1, отличающаяся тем, что содержит по весу в расчете на общий объем композиции:
a) от 3 до 20% (вес./об.) пролекарства;
b) от 0,05 до 0,2% (вес./об.) смачивающего вещества;
c) от 0,5 до 2% (вес./об.) суспендирующего агента;
d) до 2% (вес./об.) консервантов;
e) необязательно одно или несколько изотонирующих средств, достаточных для того, чтобы сделать композицию изотонической с помощью сыворотки; и
f) воды до 100%.
8. Способ приготовления фармацевтической композиции по одному любому из пп.1-7, отличающийся тем, что осуществляют однородное смешивание активного ингредиента с носителем.
9. Способ по п.8, включающий стадии:
a) смешивания смачивающего вещества с водой;
b) добавления к смеси во время смешивания консерванта;
c) диспергирования в смесь во время смешивания суспендирующего агента;
d) необязательного растворения в смеси во время смешивания изотонирующего средства;
e) диспергирования в смесь во время смешивания активного ингредиента и последующей гомогенизации смеси.
10. Применение композиции по одному любому из пп.1-7 для получения лекарственного средства для лечения шизофрении, психозов нешизофренического происхождения, поведенческих расстройств, связанных с нейродегенеративными нарушениями, например со слабоумием, поведенческих нарушений, связанных с задержкой психического развития и аутизмом, биполярным маниакальным синдромом, депрессией и тревогой.
Текст
1 Настоящее изобретение относится к фармацевтической композиции, пригодной в качестве препарата замедленного всасывания для внутримышечного или подкожного введения,содержащей: 1) в качестве активного ингредиента терапевтически эффективное количество эфира жирной кислоты 9-гидроксирисперидона или его соли или стериоизомера или стериоизомерной смеси и 2) фармацевтически приемлемый носитель; где фармацевтически приемлемым носителем является вода и в ней суспендирован активный ингредиент; и к способу получения такой композиции. Кроме того, изобретение включает применение такой фармацевтической композиции в качестве лекарственного средства для лечения шизофрении, психозов нешизофренического происхождения, поведенческих расстройств, связанных с нейродегенеративными нарушениями, например со слабоумием, поведенческих нарушений, связанных с задержкой психического развития и аутизмом, биполярным маниакальным синдромом, депрессией и тревогой. Рисперидон представляет собой 3-[2-[4-(6 фтор-1,2-бензиз-оксазол-3-ил)-1-пиперидинил]этил]-6,7,8,9-тетрагидро-2-метил-4 Н-пиридо[1,2-а]пиримидин-4-он. Его получение и фармакологическая активность описаны в ЕР 0196132 (патент-аналог US-4804663). В качестве примера могут служить различные общепринятые фармацевтические лекарственные формы,включающие таблетки, капсулы, капли, суппозитории, растворы для перорального введения и растворы для инъекций. На практике рисперидон обычно вводят в качестве основного ингредиента в таблетки или в буферный раствор для перорального или внутримышечного введения. Конкретные растворы для перорального или внутримышечного введения описаны в WO96/01652. Рисперидон представляет собой сильнодействующее лекарственное средство, имеющее относительно узкий терапевтический индекс. Он может оказывать нежелательное побочное действие при передозировке, вызывая, особенно, экстрапирамидное нарушение (EPS) и, в меньшей степени, артериальную гипотензию(вследствие периферической альфаадренаргической активности). С целью получения антипсихотического эффекта общая суточная доза рисперидона для больного составляет от около 2 до около 8 мг; для смягчения поведенческих расстройств, связанных с нейродегенеративными нарушениями, общая суточная доза обычно является меньшей и предпочтительно составляет от около 0,5 до около 2 мг. Доза может быть изменена в зависимости от индивидуальных особенностей больного и при комбинированной лекарственной терапии. 2 В силу ряда причин рисперидон желательно вводить в виде препарата длительного или замедленного действия (замедленного всасывания), который является эффективным в течение продолжительного периода времени, предпочтительно в течение 3-х недель или более.WO-94/25460 (аналог ЕР-0697019) относится к первому такому препарату замедленного всасывания и касается соли рисперидона, слабоводорастворимой солевой формы рисперидона,которая может быть суспендирована в фармацевтически приемлемом носителе, например в воде или в масле, и может быть введена подкожно или внутримышечно. Однако эта соль имеет менее чем оптимальные фармакологические свойства. Выделение из этого препарата активного ингредиента является слишком быстрым, что приводит к относительно высоким исходным уровням в плазме и неадекватной средней продолжительности действия, обе эти характеристики при применении действительно эффективного препарата замедленного всасывания могут быть заметно улучшены.WO-95/13814 касается препарата пролонгированного действия для парентерального введения, где рисперидон находится в микроинкапсулированной форме, т.е. включен в биосовместимый, биоразлагаемый, образующий стенки материал (например полимер, такой как ди-полилактид, сополимеризованный с гликолидом). Микроинкапсулированные препараты имеют подходящие фармакокинетические свойства, но способы их получения на фармацевтических заводах являются весьма усложненными. Поэтому в настоящее время все еще существует потребность в эффективном и легкодоступном препарате замедленного всасывания на основе рисперидона или соединения, похожего на рисперидон. Известно, что рисперидон в ходе обмена веществ преобразуется в 9-гидроксирисперидон,который имеет фармакологический профиль и активность, сравнимые с таковыми исходного лекарственного препарата рисперидона, но при этом имеет более длительный период полувыведения. Рисперидон распределяется и выводится из тканей головного мозга более быстро, чем его метаболит 9-гидроксирисперидон. 9 Гидроксирисперидон, его энантиомерные формы и его сложные эфиры С 2-20-алкановой кислоты описаны в ЕР-0368388 (патенты-аналоги US5158952 и US-5254556). Такие эфиры рассматривают как потенциально ценные пролекарства активного метаболита рисперидона, применяемого в препаратах замедленного всасывания. Проблем, связанных с генетическим полиморфизмом при метаболизме рисперидона до его активного метаболита 9-гидроксирисперидона, можно, вероятно, избежать путем введения вместо самого рисперидона метаболита или его длительного действующего пролекарства. 3 Действительно, при метаболизме рисперидона особую роль играет генетический полиморфизм дебризохинонового типа. Как следствие, людей на основе их метаболического показателя можно разделить на следующие фенотипы: с плохим, средним и интенсивным обменом веществ. Такой метаболический показатель определяют как отношение дебризохина, выделившегося с мочой, к дебризохину, выделившемуся с 4-гидроксиметаболитом, в течение 8 ч после перорального введения 10 мг дебризохина. Более 99% населения стран Востока является фенотипами с интенсивным обменом веществ,люди с плохим обменом веществ здесь встречаются довольно редко. Однако у кавказской расы только около 90% населения являются фенотипами с интенсивным или средним обменом веществ. Примерно 10% населения имеют плохой обмен веществ и недостаточное количество фермента дебризохин-гидроксилазы. Продолжительность действия и пиковые уровни активных ингредиентов в плазме (рисперидона и 9-гидроксирисперидона) зависят от дебризохинового метаболического показателя человека, подвергнутого лечению рисперидоном. Более конкретно, у людей с плохим обменом веществ высокие временные пиковые уровни рисперидона по всей вероятности достигаются в том случае, когда общую суточную дозу вводят в виде однократной дозы. Это может привести к нежелательным побочным эффектам, например к экстрапирамидному синдрому(EPS) и артериальной гипотензии. На метаболизм рисперидона, кроме того,оказывают влияние индивидуальные особенности человека, а также тот факт, что в клинической практике субъекты, подвергаемые лечению рисперидоном, обычно получают дополнительное медикаментозное лечение, например транквилизаторы, нейролептические средства, например галооперидол, антидепрессанты и т.д.,все из которых могут конкурировать с рисперидоном из-за фермента дебризохингидроксилазы. Такие взаимодействия лекарственных веществ могут оказывать значительное влияние на метаболизм рисперидона, особенно у людей с интенсивным обменом веществ, и могут привести к появлению нежелательного действия лекарственного средства у больных,получающих такое дополнительное медикаментозное лечение. Настоящее изобретение является результатом исследований, направленных на создание эффективного, хорошо переносимого препарата длительного или замедленного действия (замедленного всасывания) на основе эфира алкановой кислоты 9-гидроксирисперидона, который является терапевтическим эффективным в течение,по меньшей мере, трех недель или более. Выражение эффективный в течение, по меньшей мере, трех недель или более означает, что уровни активного ингредиента 9-гидро 000536 4 ксирисперидона в плазме (свободного спирта,выделившегося посредством гидролиза из сложного эфира алкановой кислоты) должны составлять примерно выше 10 нг/мл. С другой стороны для того, чтобы состав можно было назвать эффективным, уровни активного ингредиента в плазме должны все время оставаться ниже порогового значения, равного примерно 100 нг/мл. Пороговое значение представляет собой средний уровень активного ингредиента в плазме в течение значительного периода времени, например в течение более 15 мин, выше которого больные могут испытывать нежелательные побочные эффекты, или наоборот значение уровня активного ингредиента в плазме, при котором все чаще является приемлемой системная толерантность к препарату. Вследствие, например, неожиданного всплеска выделения активного ингредиента пороговое значение не удерживает высокие уровни в плазме в течение короткого периода времени, например в течение менее 15 мин. Обе упомянутые выше особенности уровни активного ингредиента в плазме, которые должны находиться выше минимальной терапевтической концентрации, но ниже порогового значения, вызывающего побочное действие, - следует рассматривать как основные требования, которым должен соответствовать препарат замедленного всасывания для того, чтобы он был приемлемым для лечения больных. Ограничение количества введений лекарственного средства и появление нежелательных побочных эффектов после каждого введения, несомненно,улучшит податливость больных терапии. Однако кроме этих основных требований, может быть высказан ряд добавочных пожеланий, которые дополнительно улучшат податливость больных терапии, наиболее важными из них являются хорошая местная толерантность к лекарственному средству и облегчение его введения. Хорошая местная толерантность означает минимальную чувствительность и воспаление в месте инъекций, облегчение введения лекарственного средства зависит от размера иглы и продолжительности времени, необходимого для введения дозы конкретного лекарственного средства. Кроме того, препарат замедленного всасывания должны быть устойчивыми и иметь срок годности при нормальных условиях, по меньшей мере, 2 года. Исследования, направленные на создание эффективного, хорошо переносимого препарата длительного или замедленного действия (замедленного всасывания) на основе сложного эфира алкановой кислоты 9-гидроксирисперидона,который удовлетворяет вышеуказанным требованиям, привели к обнаружению того, что фармацевтическая композиция, подходящая в качестве препарата замедленного всасывания для 5 внутримышечного или подкожного введения,должна содержать: 1) в качестве активного ингредиента терапевтически эффективное количество сложного эфира жирной кислоты 9-гидроксирисперидона,имеющего формулу: или его соли или стереоизомера или стереоизомерной смеси, где R представляет собой неразветвленный С 9-19-алкильный радикал; и 2) фармацевтически приемлемый носитель; и она отличается тем, что фармацевтически приемлемым носителем является вода и в ней суспендирован активный ингредиент. Неожиданно было обнаружено, что водные суспензии сложных эфиров С 10-20-алкановых кислот 9-гидроксирисперидона (где R представляет собой неразветвленный C9-19-алкильный радикал) являются сравнимыми с соответствующими суспензиями в неводной среде и масляными суспензиями, и в некоторых отношениях они представляют собой по сравнению с ними гораздо лучшие препараты с точки зрения замедленности всасывания. Это явилось неожиданным, поскольку в данной области существует догмат, согласно которому препараты замедленного всасывания должны содержать липофильные лекарственные вещества, растворенные или суспендированные в липофильной среде. Поэтому до сих пор сложные эфиры С 10-20 алкановых кислот 9-гидроксирисперидона растворяли или суспендировали в маслах, подходящих для внутримышечного введения, в частности в кунжутном масле. С 10-20-алкановые кислоты выбирают из группы, состоящей из декановой (каприновой), ундекановой, додекановой(миристиновой), пентадекановой, гексадекановой (пальмитиновой), гептадекановой, октадекановой (стеариновой), нонадекановой и эйкозановой кислот. Полагали, что вследствие ограниченной растворимости в воде, сложные эфиры следует суспендировать в маслах. Было найдено, что сложный эфир, имеющий C15 (пентадецильную) цепь и активный ингредиент, соответствующий пальмитату 9-гидроксирисперидона, является превосходным эфиром как с фармакокинетической точки зрения, так и с точки зрения толерантности. Для дополнительного улучшения толерантности к лекарственному средству далее бу 000536 6 дут рассмотрены несколько суспензий с различным размером частиц пальмитата 9 гидроксирисперидона в кунжутном масле, необязательно в присутствии моностеарата алюминия. Было установлено, что между суспензиями с малым и большим размером частиц пролекарства не существует значительной разницы. Присутствие моностеарата алюминия оказывало влияние только на вязкость препарата и на облегчение его введения. В еще одной серии экспериментов было обнаружено, что при уменьшении в препарате замедленного всасывания концентрации пролекарства толерантность к вводимому лекарственному препарату дополнительно улучшалась. Испытания показали, что поскольку масляные суспензии тяжело набираются в шприц, эксперименты начали осуществлять с применением менее вязких носителей, в частности с применением триглицерида со средней цепью (Miglyol), и в противоположность существующему догмату, с применением в качестве носителя воды. Системная и местная толерантность к препаратам на основеMiglyol значительно меньше, чем к препаратам на основе кунжутного масла. Совершенно неожиданно было установлено, что водные суспензии пальмитата 9-гидроксирисперидона являются более эффективными, чем препараты на основе кунжутного масла. Они не обладают лишь соответствующей продолжительностью действия, но системная и местная толерантность к ним является приемлемой, и, кроме того, измененние фармакокинетических свойств в зависимости от индивидуальных особенностей больного является поразительно ограниченным. Фармакокинетические свойства водных суспензий в соответствии с настоящим изобретением могут в ограниченной степени дополнительно зависеть от физико-химических свойств твердого пальмитата 9-гидроксирисперидона,например от размера частиц и формы кристаллов. Водные композиции в соответствии с настоящим изобретением дополнительно содержат суспендирующий агент и смачивающее вещество и необязательно один или несколько консервантов, буфер и изотонизирующее средство. Некоторые ингредиенты могут одновременно выполнять две или несколько функций, например функцию консерванта и буфера, или функцию буфера и изотонирующего средства. Суспендирующими агентами, подходящими для применения в водных суспензиях в соответствии с настоящим изобретением, являются производные целлюлозы, например метилцеллюлоза, натрийкарбоксиметилцеллюлоза и оксипропилметилцеллюлоза, поливинилпирролидон, альгинаты, хитозан, декстраны, желатин,полиэтиленгликоли, полоксиэтиленовые и полиоксипропиленовые эфиры. Натрийкарбоксиметилцеллюлозу предпочтительно применяют при концентрации от 0,5 до 2%, наиболее 7 предпочтительно при концентрации 1%(вес./об.). Смачивающими веществами, подходящими для применения в водных суспензиях в соответствии с настоящим изобретением, являются полиоксиэтиленовые производные сложных эфиров сорбитана, например полисорбат 20 и полисорбат 80, лецитин, полиоксиэтиленовые и полиоксипропиленовые эфиры, деоксихолат натрия. Полисорбат 20 предпочтительно применяют при концентрации от 0,05 до 0,3%, более предпочтительно от 0,05 до 0,2%, наиболее предпочтительно при концентрации 0,1%(вес./об.). Консерванты представляют собой противомикробные средства и антиокислители, которые можно выбрать из группы, состоящей из бензойной кислоты, бензилового спирта, бутилированного гидроксианизола, бутилированного гидрокситолуола, хлорбутола, галлата, гидроксибензоата, EDTA (этилендиаминтетрауксусной кислоты), фенола, хлоркрезола, метакрезола,бензетонийхлорида,миристил-пикколинхлорида, фенилацетата ртути и тимерозаля. В частности, бензиловый спирт можно использовать при концентрации до 2%(вес./об.), предпочтительно до 1,5% (вес./об.). Изотонирующими средствами являются, например, хлорид натрия, декстроза, маннит, сорбит,лактоза, сульфат натрия. Суспензии подходяще содержат от 1 до 10% (вес./об.) изотонирующего средства. Маннит предпочтительно применяют при концентрации от 2 до 7%, более предпочтительно около 5%. Для предотвращения флокуляции суспендированного сложного эфира и получения изотонической суспензии наиболее предпочтительно применяют один или несколько электролитов при концентрации от около 1 до около 3% (вес./об.), в особенности от около 1,5 до около 2% (вес./об.), поскольку ионы помогают избежать флокуляции. Кроме того, некоторые электролиты способны к буферированию водной суспензии. В особенности предпочтительным является применение смеси вторичного кислого фосфата натрия (безводного)(обычно около 0,9% (вес./об.) и моногидрата первичного кислого фосфата натрия (обычно около 0,6% (вес./об.), при этом получают изотонический, нейтральный раствор, который менее склонен к флокуляции суспензированного в нем сложного эфира. В особенности желательным свойством инъецируемого препарата замедленного всасывания является облегчение его введения. В частности, такое введение (инъекция) должно осуществляться с применением иглы настолько тонкой и небольшой, насколько это возможно, и в течение максимально возможного короткого периода времени. Это можно осуществить путем поддержания вязкости водных суспензий настоящего изобретения ниже около 75 мРас,предпочтительно ниже 60 мРас. Водные сус 000536 8 пензии с такой или меньшей вязкостью можно легко набрать в шприц (например, из ампулы) и ввести через посредство тонкой иглы (например иглы 21G 11/2, 22G 2 или 22G 1/4). В идеале водные композиции в соответствии с настоящим изобретением, для сохранения минимального объема инъецируемого препарата и минимально возможного содержания других ингредиентов, должны содержать максимальную дозу пролекарства. В частности такая композиция будет содержать по весу в расчете на общий объем композиции:e) необязательно одно или несколько изотонирующих средств, достаточных для того,чтобы сделать композицию изотонической с помощью сыворотки; иf) воды до 100%. Водные суспензии в соответствии с настоящим изобретением могут быть получены следующими известными в данной области способами приготовления суспензий, характеризующимися однородным смешиванием активного ингредиента с носителем. Такой способ может включать стадии:a) смешивания смачивающего вещества с водой;b) добавления к смеси во время смешивания консерванта;c) диспергирования в смесь во время смешивания суспендирующего агента;d) необязательного растворения в смеси во время смешивания изотонирующего средства; е) диспергирования в смесь во время смешивания активного ингредиента и последующей гомогенизации смеси. Ввиду полезности 9-гидроксирисперидона для лечения ряда заболеваний, настоящее изобретение также относится к описанной здесь выше фармакологической композиции, применяемой в качестве лекарственного средства для лечения шизофрении, психозов нешизофренического происхождения, поведенческих расстройств, связанных с нейродегенеративными нарушениями, например со слабоумием, поведенческих расстройств, связанных с задержкой психического развития и аутизмом, биполярным маниакальным синдромом, депрессией и тревогой. Кроме того, настоящее изобретение относится к применению описанной здесь выше композиции для получения лекарственного средства для лечения шизофрении, психозов нешизофренического происхождения, поведенческих расстройств, связанных с нейродегенеративными нарушениями, например со слабоумием, поведенческих расстройств, связанных с 9 задержкой психического развития и аутизмом,биполярным маниакальным синдромом, депрессией и тревогой. Настоящее изобретение, кроме того, относится к способу лечения теплокровных, в особенности людей, страдающих от шизофрении,психозов нешизофренического происхождения,поведенческих расстройств, связанных с нейродегенеративными нарушениями, например со слабоумием, поведенческих расстройств, связанных с задержкой психического развития и аутизмом, биполярным маниакальным синдромом, депрессией и тревогой; способ включает введение терапевтически эффективного количества описанной здесь выше водной суспензии. Обычно такой препарат вводят примерно через каждые три недели или даже, если это возможно, с более продолжительными интервалами. Лекарственная доза обычно составляет от около 2 до 4 мг/кг массы тела. Для дальнейшей иллюстрации настоящего изобретения приведены последующие примеры. Экспериментальная часть А. Получение пальмитата 9 гидроксирисперидона К раствору гексадекановой кислоты (1,54 г; 6 ммолей) в дихлорметане (140 мл) добавилиN,N'-дициклогексилкарбодиимид (1,39 г; 6,8 ммоля) и перемешали при комнатной температуре в течение 10 мин. К реакционной смеси добавили 9-гидроксирисперидон (2,13 г; 5 ммолей), затем 4-пирролидинопиридин (93 мг; 0,63 ммолей). Смесь перемешали при комнатной температуре в течение 3-х дней. К реакционной смеси добавили воду (200 мл) и три раза экстрагировали хлороформом (100 мл). Смешанные органические слои сушили (МgSO4), фильтровали и выпарили. Смесь растерли в порошок в диизопропиловом эфире (100 мл), фильтровали и перекристаллизовали в изопропаноле (60 мл),кристаллы отфильтровали и сушили, при этом получили пальмитат 9-гидроксирисперидона(2,67 г; 80,4%). В. Примеры композиций Каждый из нижеприведенных препаратов получили в соответствии со следующей методикой. Смачивающее вещество смешали с водой при комнатной температуре и добавили консервант. При перемешивании в смесь диспергировали суспендирующий агент и при необходимости добавляли изотонирующее средство. Затем в перемешанную смесь диспергировали активный ингредиент и ее гомогенизировали и поместили в стерильные емкости. Все ингредиенты и вся аппаратура, применяемая во время приготовления водных суспензий, были стерильными. В нижеприведенных таблицах все концентрации приведены в % по весу в расчете на объем всего препарата [%(вес./об.)]. 10 Препарат 1 (F1) пальмитат 9-гидроксирис- 15,6% (10% 9-гидроксиперидона рисперидон) полисорбат 20 0,2% натрийкарбоксиметил 2% целлюлоза 30 мРас бензиловый спирт 1,5% вода до 100% Сложный эфир измельчили, но не просеяли. Физико-химические свойства F1 рН=6,52 вязкость=20 мРас осмомолярность=210 мО см/кг Препарат 2 а, 2b и 2 с (F2a, F2b, F2c) пальмитат 9-гидроксирисперидона полисорбат 20 натрийкарбоксиметилцеллюлоза 30 мРас бензиловый спирт маннит вода до Сложный эфир измельчили сеивания на три фракции: рН=6,86 осмомолярность=280 мО см/кг Препарат 3 а, 3b и 3 с (F3a, F3b, F3c) пальмитат 9-гидроксирис- 15,6% (10% 9-гидроксиперидона рисперидон) полисорбат 20 0,2% натрийкарбоксиметил 1% целлюлоза 30 мРас бензиловый спирт 1,5% маннит 2% вода до 100% Сложный эфир измельчили и путем просеивания разделили на три фракции: вязкость=60 рН=6,74 осмомолярность=280 мО см/кг Препарат 4 (F4) пальмитат 9 гидроксирисперидона полисорбат 20 натрийкарбоксиметилцеллюлоза 30 мРас бензиловый спирт (для парентерального введения) безводный вторичный кислый фосфат натрия моногидрат первичного кислого фосфата вода до Сложный эфир измельчили и просеяли с применением соответствующих стандартных сит, при этом активный ингредиент имел следующий гранулометрический состав: 90% частиц (по объему)0,5 м 50% частиц (по объему)5 м 10% частиц (по объему)15 м Эфир стерилизовали путем облучения дозой 25 кГу 90 Y и смешали с растворителемF5a Пальмитат 9-гидроксирисперидона полисорбат 20 Натрийкарбоксиметилцеллюлоза 30 мРас бензиловый спирт (для парентерального введения) безводный вторичный кислый фосфат натрия С. Примеры фармакологических испытаний С 1. Фармакологическое испытание F1 и аналогичных масляных препаратов Четырем гончим собакам с применением иглы 21G внутримышечно ввели дозу F1, равную 2,5 мг/кг массы тела. В таком же эксперименте применяли подобный препарат на основеMiglyol (F) и на основе кунжутного маслаMiglyol, а оба препарата на основе кунжутного масла ввели с применением иглы 19G. Из экспериментальных данных рассчитали следующие фармакокинетические препараты: моногидрат первичного кислого фосфата натрия вода до рН=7 вязкость (мРас) осмомолярность (мО см/кг) С помощью шприца с размером иглы 22G 11/4 ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Фармацевтическая композиция, пригодная в качестве депо-препарата для внутримышечного или подкожного введения, содержащая: 1) в качестве активного ингредиента терапевтически эффективное количество сложного эфира жирной кислоты 9-гидроксирисперидона,имеющего формулу: или его соли, или стереоизомера или стереоизомерной смеси, где R представляет собой неразветвленный С 9-19-алкильный радикал; и 2) фармацевтически приемлемый носитель,отличающийся тем, что фармацевтически при Ссредн. емлемым носителем является вода и в ней суспендирован активный ингредиент. 2. Композиция по п.1, отличающаяся тем,что R представляет собой неразветвленную C15 цепь (пентадецильную) и активным ингредиентом является пальмитат 9-гидроксирисперидона. 3. Композиция по п.1, отличающаяся тем,что композиция дополнительно содержит суспендирующий агент и смачивающее вещество и необязательно один или несколько ингредиентов, выбранных из консерванта, буфера и изотонирующего средства. 4. Композиция по п.3, отличающаяся тем,что суспендирующим агентом является натрийкарбоксиметилцеллюлоза и смачивающим веществом является полисорбат 20. 5. Композиция по п.4, отличающаяся тем,что консервантом является бензиловый спирт и изотонирующим средством является маннит или фосфатный буфер. 6. Композиция по п.1, отличающаяся тем,что имеет вязкость менее 75 мРас. 7. Композиция по п.1, отличающаяся тем,что содержит по весу в расчете на общий объем композиции:e) необязательно одно или несколько изотонирующих средств, достаточных для того,чтобы сделать композицию изотонической с помощью сыворотки; иf) воды до 100%. 8. Способ приготовления фармацевтической композиции по одному любому из пп.1-7,отличающийся тем, что осуществляют однородное смешивание активного ингредиента с носителем. 9. Способ по п.8, включающий стадии:a) смешивания смачивающего вещества с водой;b) добавления к смеси во время смешивания консерванта;c) диспергирования в смесь во время смешивания суспендирующего агента;d) необязательного растворения в смеси во время смешивания изотонирующего средства;e) диспергирования в смесь во время смешивания активного ингредиента и последующей гомогенизации смеси. 10. Применение композиции по одному любому из пп.1-7 для получения лекарственного средства для лечения шизофрении, психозов нешизофренического происхождения, поведенческих расстройств, связанных с нейродегенеративными нарушениями, например со слабоумием, поведенческих нарушений, связанных с задержкой психического развития и аутизмом,биполярным маниакальным синдромом, депрессией и тревогой.
МПК / Метки
МПК: A61K 31/505
Метки: эфиров, водные, 9-гидроксирисперидона, жирной, кислоты, суспензии, сложных
Код ссылки
<a href="https://eas.patents.su/8-536-vodnye-suspenzii-slozhnyh-efirov-zhirnojj-kisloty-9-gidroksirisperidona.html" rel="bookmark" title="База патентов Евразийского Союза">Водные суспензии сложных эфиров жирной кислоты 9-гидроксирисперидона</a>
Предыдущий патент: Новые противосудорожные i-ar(алк)ил-имидазолин-2-оны, содержащие в 4-положении двузамещенный остаток амина, и способ их получения
Следующий патент: Способ центрирования узла шины и обода колеса транспортного средства
Случайный патент: Производные изохинолин-1(2h)-она в качестве ингибиторов parp-1, способы их получения, фармацевтическая композиция на их основе и применение












