Сочетание ингибитора тирозинкиназы и химической стерилизации для лечения рака предстательной железы
Формула / Реферат
1. Способ ингибирования прогрессирования опухоли предстательной железы у млекопитающих, включающий введение указанному млекопитающему терапевтически эффективного количества ингибитора тирозинкиназы, выбранного из группы, состоящей из trkA ингибитора, trkB ингибитора и trkC ингибитора, и вместе с ним введение указанному млекопитающему терапевтически эффективного количества средства для химической стерилизации, выбранного из группы, состоящей из эстрогена, агониста ЛГ-РФ, антагониста ЛГ-РФ и антиандрогена.
2. Способ по п.1, отличающийся тем, что указанным млекопитающим является человек.
3. Способ по п.1, отличающийся тем, что терапевтически эффективное количество ингибитора тирозинкиназы и терапевтически эффективное количество средства для химической стерилизации ингибируют рост опухоли синергическим образом.
4. Способ по п.1, отличающийся тем, что указанный ингибитор тирозинкиназы представляет собой индолокарбазол.
5. Способ по п.4, в соответствии с которым индолокарбазол имеет следующую структуру:
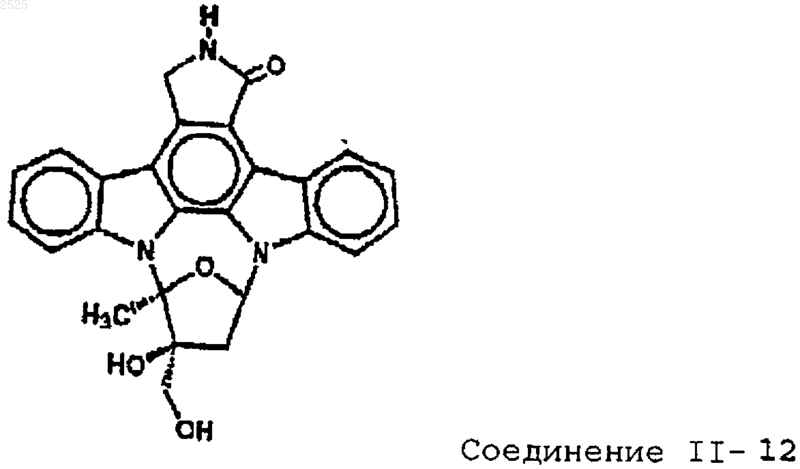
6. Способ по п.4, в соответствии с которым индолокарбазол имеет следующую структуру:

7. Способ по п.4, в соответствии с которым индолокарбазол имеет следующую структуру:
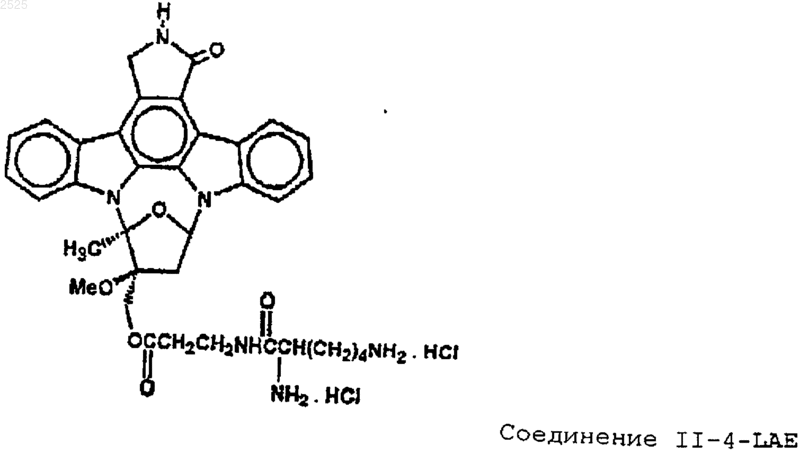
8. Способ по п.1, отличающийся тем, что указанный ингибитор тирозинкиназы представляет собой конденсированный пирролокарбазол.
9. Способ по п.1, отличающийся тем, что указанный ингибитор тирозинкиназы вводится перорально.
10. Способ по п.1, отличающийся тем, что указанный ингибитор тирозинкиназы вводится парентерально.
11. Способ по п.1, отличающийся тем, что указанный агонист ЛГ-РФ представляет собой ацетат леупролида.
12. Способ по п.1, отличающийся тем, что указанный антиандроген представляет собой флутамид.
13. Способ по п.1, отличающийся тем, что указанное средство для химической стерилизации представляет собой сочетание агониста ЛГ-РФ и антиандрогена.
14. Способ по п.13, отличающийся тем, что указанный агонист ЛГ-РФ представляет собой ацетат леупролида и указанный антиандроген представляет собой флутамид.
15. Способ по п.1, отличающийся тем, что указанный ингибитор тирозинкиназы и указанное средство для химической стерилизации вводятся в виде раздельных композиций.
16. Способ по п.1, отличающийся тем, что указанный ингибитор тирозинкиназы и указанное средство для химической стерилизации вводятся вместе в виде одной композиции.
17. Композиция, включающая ингибитор тирозинкиназы, выбранный из группы, состоящей из trkA ингибитора, trkB ингибитора и trkC ингибитора, и средство для химической стерилизации, выбранное из группы, состоящей из эстрогена, агониста ЛГ-РФ, антагониста ЛГ-РФ и антиандрогена.
18. Композиция по п.17, в которой ингибитор тирозинкиназы представляет собой индолокарбазол.
19. Композиция по п.18, при том, что входящий в нее индолокарбазол выбирают из группы, состоящей из индолокарбазола, имеющего структуру

индолокарбазола, имеющего структуру

и индолокарбазола, имеющего структуру
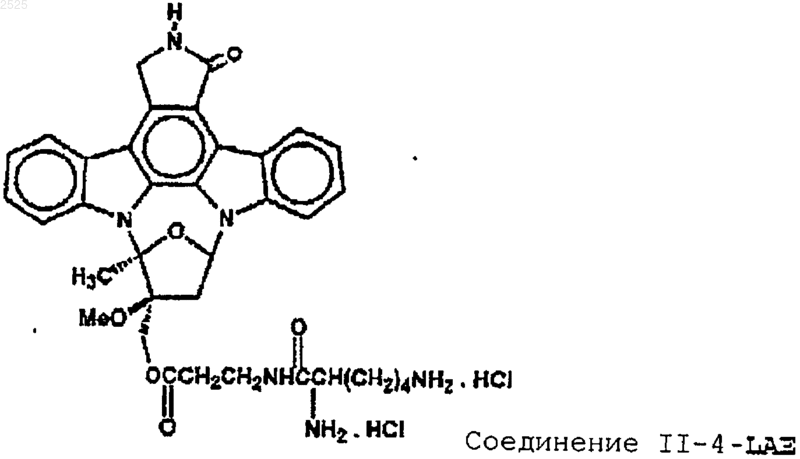
20. Композиция по п.17, в которой ингибитор тирозинкиназы представляет собой конденсированный пирролокарбазол.
21. Композиция по п.17, отличающаяся тем, что указанную композицию составляют для перорального введения.
22. Композиция по п.17, отличающаяся тем, что указанную композицию составляют для парентерального введения.
23. Композиция по п.17, в которой агонист ЛГ-РФ представляет собой ацетат леупролида.
24. Композиция по п.17, в которой антиандроген представляет собой флутамид.
25. Композиция по п.17, отличающаяся тем, что указанное средство для химической стерилизации представляет собой сочетание агониста ЛГ-РФ и антиандрогена.
26. Композиция по п.17, в которой указанный агонист ЛГ-РФ представляет собой ацетат леупролида и антиандроген представляет собой флутамид.
Текст
1 Предпосылки создания изобретения Настоящее изобретение относится к онкологии, эндокринологии, андрологии и фармакологии. Рак предстательной железы относится к наиболее часто диагностируемому виду рака у мужчин, от которого в Соединенных Штатах ежегодно умирает примерно 41000 человек(Parker, S.L., et al. (1996) CA Cancer J. Clin.,65:5-27). На ранней стадии, будучи ограниченным одним органом, рак предстательной железы часто поддается лечению хирургическим путем или лучевой терапией, если пациент не умирает от других, не связанных с раком причин. Карциномы, такие как рак молочной железы, рак толстой кишки и аденокарцинома, характеризуются быстрым клеточным делением. И, следовательно, их можно лечить химиотерапевтическими средствами, которые способны ингибировать быстрое клеточное деление. В отличие от них для рака предстательной железы не характерно быстрое клеточное деление. И в этой связи традиционные химиотерапевтические средства обычно демонстрируют низкую эффективность при использовании их против рака предстательной железы. Рак предстательной железы часто проявляет чувствительность к гормональным изменениям. В настоящее время одобрен метод лечения рака предстательной железы, который включает хирургическую стерилизацию, химическую стерилизацию или сочетание хирургической и химической стерилизации. Удаление яичек, являющихся основным органом, продуцирующим тестостерон, снижает менее чем до 5% от нормы уровень циркулирующих андрогенов. Такое снижение уровня андрогенов ингибирует рост опухоли предстательной железы. Несмотря на то, что хирургическая стерилизация действует непосредственно на опухоль ее противоопухолевый эффект может быть временным. При этом хирургическая стерилизация часто ведет к клонируемой селекции андроген-независимых опухолевых клеток предстательной железы. Это приводит к возобновлению роста опухоли предстательной железы, которая пролиферирует без стимуляции тестостероном или ДГТ (Isaacs et al.(1989) N. Engl. Med. 321:419-424). Химическую стерилизацию (называемую также медицинской стерилизацией) часто используют как замену хирургической стерилизации на начальном этапе лечения. Химическая стерилизация может быть проведена при введении эстрогенов, например, диэтилстилбестрола(ДЭС); аналогов ЛГ-РФ, например, ацетата леупролида (Лупрон, LUPRON) или ацетата гозерелина (Золадекс, ZOLADEX); стероидных антиандрогенов, например, ацетата ципротерона (ЦПА, СРА); нестероидных антиандрогенов, например, флутамида, нилутамида или 2 Казодекса (CAZODEX) или при определенном сочетании указанных средств. Связанные с рецептором тирозинкиназы представляют собой трансмембранные белки,которые содержат домен связывания с внеклеточным лигандом, трансмембранную последовательность, и домен для цитоплазматической тирозинкиназы. Функция тирозинкиназ состоит в трансдукции клеточного сигнала. Пролиферация клеток, их дифференциация, миграция, метаболизм и запрограммированная смерть являются примерами клеточных реакций, опосредованных тирозинкиназой. Тирозинкиназы принимают участие в трансформации эпителиальных клеток предстательной железы и в прогрессировании опухоли. Участвующие в этих процессах тирозинкиназы включают рецепторы фактора роста фибробластов (ФРФ; FGF), рецепторы эпидермального фактора роста (ЭФР; EGF) и рецепторы фактора роста, полученного из тромбоцитов (ФРПТ;PDGF). Принимают участие также рецепторы фактора роста нервной ткани (ФРНТ; NGF),рецепторы нейротропного фактора, полученного из мозга (НФПМ; BDNF), а тaкже рецепторы нейротропина-3 (НТ-3; NT-3) и рецепторы нейротропина-4 (НТ-4; NT-4). В патентах США 5516771, 5654427 и 5650407 рассматриваются ингибиторы тирозинкиназы индолокарбазолового типа и вопросы лечения рака предстательной железы. А в патентах США . 5475110, 5591855 и 5594009,а также в заявке WO 96/11933, рассматриваются ингибиторы тирозинкиназы пирролокарбазолового типа и вопросы лечения рака предстательной железы. Краткое описание сущности изобретения Авторами неожиданно было обнаружено,что ингибиторы тирозинкиназы осуществляют свое противоопухолевое действие при лечении рака предстательной железы у млекопитающих посредством гормоннезависимого механизма. Далее было показано, что сочетание лечения с использованием ингибитора тирозинкиназы и лечения, направленного на подавление гормональной активности, дает синергический эффект. На основании этих открытий был разработан метод лечения рака предстательной железы у млекопитающих, например у человека, составляющий суть настоящего изобретения. Метод включает введение терапевтически эффективного количества ингибитора тирозинкиназы млекопитающему при совместном введении млекопитающему средства для химической стерилизации. При этом ингибитор тирозинкиназы и средство для химической стерилизации могут действовать синергически по ингибированию роста опухоли. Предпочтительные ингибиторы тирозинкиназы включают индолокарбазолы. Предпочтительные индолокарбазолы включают следующие соединения: 4 киназы и средство для химической стерилизации. Предпочтительный ингибитор тирозинкиназы в композиции представляет собой trkA ингибитор, trkB ингибитор и trkC ингибитор. Предпочтительно, ингибитор тирозинкиназы в композиции представляет собой индолокарбазол. Предпочтительные индолокарбазолы представляют собой: Соединение II-4-LAE представляет собой сложный эфир лизилаланина соединения II-4 или фармакологически приемлемую соль этого эфира, например дигидрохлоридную соль. Соединение II-12 описано в патенте США 4923986 ("соединение 20"). Соединение II-4 описано в патенте США 5461146. Соединение II-4-LAE описано в патенте США 5650407 (пример 14). Ингибитор тирозинкиназы также может представлять собой конденсированный пирролокарбазол. Ингибитор тирозинкиназы может быть введен любым приемлемым способом, например перорально или парентерально. Средства химической стерилизации, применяемые в настоящем изобретении, включают эстрогены; агонисты ЛГ-РФ, например ацетат леупролида (Лупрон, LUPRON) и ацетат гозерелина (Золадекс, ZOLADEX); антагонисты ЛГ-РФ, например Антид (ANTIDE)(Akzo Nobel) и антиандрогены, например флутамид и нилутамид. Ингибитор тирозинкиназы и средство для химической стерилизации могут вводиться в виде отдельных композиций. Альтернативно, их можно объединить и вводить в виде одной композиции. Настоящее изобретение также относится к композиции, включающей ингибитор тирозин и Альтернативно ингибитор тирозинкиназы в композиции может представлять собой конденсированный пирролокарбазол. Композиция может быть приготовлена для перорального введения или парентерального введения. Средство для химической стерилизации может представлять собой эстроген, аналог ЛГ-РФ или антиандроген, или комбинацию двух или более таких соединений. Предпочтительным для включения в настоящую композицию аналогом ЛГ-РФ является ацетат леупролида. Предпочтительным для включения в настоящую композицию антиандрогеном является флутамид. Средство для химической стерилизации, включаемое в композицию по настоящему изобретению,может представлять собой сочетание аналога ЛГ-РФ и антиандрогена, например ацетат леупролида и флутамида. В контексте настоящего описания термин"средство для химической стерилизации" означает соединение, которое: 1) ингибирует про 5 дукцию сывороточных андрогенов, 2) блокирует связывание сывороточных андрогенов с рецепторами андрогена или 3) ингибирует превращение тестостерона в ДГТ, а также сочетание двух или более таких соединений. Если особо не определено иное, все технические и научные термины, используемые в настоящем описании, имеют общепринятые значения в той области техники, к которой относится настоящее изобретение. Тогда как случаи возможных неоднозначных толкований в настоящем описании особо определяются. Все публикации, патентные заявки и другие цитированные материалы включены в настоящее изобретение в качестве ссылок. Несмотря на то, что все методы и материалы, подобные или эквивалентные приведенным в настоящем описании, могут использоваться для осуществления или проверки настоящего изобретения, ниже будут приведены предпочтительные методы и материалы. При этом материалы, методы и примеры приведены лишь с целью иллюстрации и никоим образом не ограничивают настоящее изобретение. Другие особенности и преимущества настоящего изобретения излагаются в подробном описании и в формуле изобретения. Краткое описание чертежей На фиг. 1 показан график зависимости относительного объема опухоли (кратные изменения) от времени (дни) на модельной системе опухоли предстательной железы крысы in vivo. Кружочками обозначен контроль в виде носителя; смотрящие вверх треугольники обозначают контроль, состоящий из монотерапии соединением II-4; квадраты обозначают контроль на стерилизацию; перевернутые треугольники обозначают комбинированное лечение соединениемII-4/стерилизацией. Дозировка соединения II-4 составляет 10 мг/кг при подкожной инъекции. Введение соединения II-4 указано прямоугольниками со знаками плюс на оси X. Фиг. 2 представляет собой график зависимости относительного объема опухоли (кратные изменения опухоли Dunning H) от времени (дни) у стерилизованных крыс. Кружочки обозначают контроль в виде носителя; квадраты обозначают соединение II-4. Время введения соединения II4 указывается прямоугольниками на оси X. Фиг. 3 представляет собой график зависимости относительного объема опухоли (кратные изменения) от времени (дни) у крыс, которым предварительно вводили соединение II-4. Кружочки обозначают соединение II-4; квадраты обозначают лечение с использованием соединения II-4/стерилизации. Время введения соединения II-4 указано прямоугольниками на оси X. Фиг. 4 представляет собой график зависимости относительного объема опухоли (кратные изменения) от времени (дни) на модельной системе in vivo опухоли предстательной железы крыс. Кружочки обозначают контроль в виде 6 носителя; смотрящие вверх треугольники обозначают контроль на монотерапию соединениемII-12; квадраты обозначают контроль на химическую стерилизацию с применением ацетата леупролида (LUPRON); перевернутые треугольники обозначают комбинированное лечение с использованием соединения II-4 ацетата леупролида. Соединение II-4 вводится в дозе 10 мг/кг, дважды в день, перорально. Введение соединения II-12 указано примоугольниками на оси X. Подробное описание изобретения Совместное введение ингибитора тирозинкиназы и средства для химической стерилизации может осуществляться в режиме одновременного введения отдельных форм, например,композиции с ингибитором тирозинкиназы и композиции, содержащей средство для химической стерилизации. Введение раздельных форм препарата совпадает по времени, если фармакологическая активность ингибитора тирозинкиназы и средства для химической стерилизации проявляются одновременно у млекопитающих при лечении указанными препаратами. В некоторых вариантах реализации настоящего изобретения совместное введение ингибитора тирозинкиназы и средства для химической стерилизации осуществляют с использованием единой композиции, содержащей их. Предпочтительно, дозировка ингибитора тирозинкиназы составляет от 1 мкг/кг до 1 г/кг веса тела в день. Более предпочтительно, дозировка ингибитора тирозинкиназы составляет от 0,01 до 100 мг/кг веса тела в день. Оптимальная дозировка ингибитора тирозинкиназы варьирует в зависимости от ряда факторов, таких как тип и степень прогрессирования рака предстательной железы, общее состояние здоровья пациента,активность ингибитора тирозинкиназы и способ его введения. При этом подбор оптимальной дозы тирозинкиназы может выполнить любой специалист со средним уровнем знаний в данной области. В технике известны различные ингибиторы тирозинкиназы, приемлемые для использования в рамках настоящего изобретения. Предпочтительно используемый в настоящем изобретении ингибитор тирозинкиназы представляет собой trk А ингибитор, trk В ингибитор илиtrk С ингибитор. Информацию о приемлемых ингибиторах тирозинкиназы индолокарбазолового типа можно получить из следующего ряда документальных источников (Dionne et al., патент США 5516771, Dionne et al., патент США 5654427, Lewis et al., патент США 5461146 и Mallamo et al., патент США 5650407). В ряде вариантов реализации настоящего изобретения соединение II-4-LAE получают и вводят больному человеку с помощью следующей процедуры. Соединение II-4-LAE (дигидрохлорид) и осмотически приемлемое количест 7 во маннита растворяют в дистиллированной воде и доводят значение рН раствора примерно до 3,5. Указанный раствор лиофилизируют с получением порошка. Для удобства хранения и использования готовят аликвоты лиофилизированного порошка, содержащие 27,5 мг соединения II-4-LAE и 55 мг маннита. К моменту использования аликвоту лиофилизированного порошка вновь растворяют в стерильной воде для инъекции (фармакопея США) с получением 1,1 мл раствора, содержащего 50 мг/мл маннита и 25 мг/мл соединения II-4-LAE (дигидрохлорида). Этот воссозданный раствор затем разбавляют определенным объемом 5% раствора декстрозы для инъекций (фармакопея США) для введения желательной дозы соединения II-4LAE внутривенной инфузией в течение примерно одного часа. Применение в указанной процедуре соединения II-4-LAE можно начинать с дозы 1 мг/м 2/день и постепенно увеличивать,например, до 64 мг/м 2/день или 501 мг/м 2/день,в зависимости от данных мониторинга, оценивающих состояние пациента. Известны различные средства для химической стерилизации. Применяемые в рамках настоящего изобретения средства для химической стерилизации иногда классифицируют на следующие группы: эстрогены, агонисты рилизингфактора лютеинизирующего гормона (ЛГ-РФ),антагонисты ЛГ-РФ и антиандрогены. Антиандрогены могут далее подразделяться на стероидные и нестероидные. Эстрогены, например диэтилстилбестрол(ДЭС), повышают уровень глобулина, связанного с половым гормоном, и уровень пролактина в плазме. Это, в свою очередь, снижает секрецию ЛГ и синтез тестостерона в яичках по типу отрицательной обратной связи. Дозировка ДЭС зачастую составляет от 1 до 5 мг/день. Предпочтительно избегают более высоких доз ДЭС в связи с возможным риском развития сердечнососудистых осложнений. Другим предпочтительным агонистом ЛГРФ, применяемым в настоящем изобретении,является ацетат леупролида, коммерчески доступный как Люпрон (LUPRON (Takeda Abbott Pharmaceuticals, Inc Химическое наименование ацетата леупролида следующее: ацетат 5-оксо-L-пролил-L-гистидил-L-триптофил-Lсерил-L-тирозил-D-лейцил-L-лейцил-L-аргинил-N-этил-L-пролинамида (соль). Ацетат леупролида как агонист ЛГ-РФ является мощным ингибитором секреции гонадотропина в случае его непрерывного введения в терапевтических дозах. Этот эффект обратим, что достигается при отмене введения ацетата леупролида. Считается, что ацетат леупролида, например Люпрон депо (LUPRON DEPOT) действует по механизму отрицательной обратной связи. У людей одновременное введение однократных дневных доз ацетата леупролида вызывает начальное повышение уровня лютеини 002525 8 зирующего гормона (ЛГ) в сыворотке. У мужчин в течение двух-четырех недель после начала введения ацетата леупролида содержание тестостерона в сыворотке падает до уровня стерилизации. При использовании в рамках настоящего изобретения ацетат леупролида вводят подкожно, внутримышечно или внутривенно. Ацетат леупролида может вводиться, например, путем подкожной инъекции 1 мг в день. В некоторых вариантах реализации настоящего изобретения ацетат леупролида вводят в виде депо-формы. Депо-форма обеспечивает постоянное высвобождение лекарственного средства в течение длительного периода времени, например, от 1 до 4 месяцев. Пример депо-формы включает суспензию микросфер ацетат леупролида, очищенный желатин, сополимер DL-молочной и гликолевой кислот и D-маннит. Микросферы могут быть суспендированы в носителе, содержащем натрий-карбоксиметилцеллюлозу, D-маннит и воду. Такие депо-формы коммерчески доступны в виде Люпрона депо (LUPRON DEPOT (Takeda Abbott Pharmaceuticals, который пригоден для внутримышечной инъекции. Другим агонистом ЛГ-РФ, применяемым в рамках настоящего изобретения, является ацетат гозерелина, коммерчески доступный в виде Золадекса (ZOLADEX (Zeneca. Ацетат гозерелина имеет следующую химическую формулу: ацетат пиро-Glu-His-Trp-Ser-Tyr-D-Ser(BUt)-Leu-Arg-Pro-Azgly-NH2. Золадекс поставляется в виде композиции, пригодной для подкожной инъекции с постоянным высвобождением в течение 28-дневного периода. Примером антагониста ЛГ-РФ, применяемого в настоящем изобретении, является Антид (ANTIDE (Ares -Serono, химическое наименование которого следующее:N-ацетил-3-(2-нафталенил)-Dаланил-4-хлор-D-фенилаланил-3-(3-пиридинил)D-аланил-L-серил-N6-(3-пиридинилкарбонил)L-лизил-N6-(3-пиридинилкарбонил)-D-лизил-Lлeйцил-N6-(1-метилэтил)-L-лизил-L-пролил. Другим примером используемого антагониста ЛГ-РФ является Ганиреликс (GANIRELIX(Roche/Akzo Nobel, химическое название которого N-Ac-D-Nal, D-pCl-Phe, D-Pal, DhArg(Et)2, hArg(Et)2, D-Ala. Примерами стероидных антиандрогенов являются ацетат ципротерона (ЦПА; СРА), и ацетат мегестрола, коммерчески доступный как Мегас (MEGACE (Bristol-Myers Oncology. Стероидные антиандрогены могут блокировать рецепторы андрогенов в предстательной железе. Они могут также ингибировать высвобождение ЛГ. ЦПА, предпочтительно, вводят больному человеку в дозировках от 100 до 250 мг/день. Нестероидные антиандрогены блокируют рецепторы андрогена. Они также могут вызвать повышение в сыворотке уровня ЛГ и тестостерона. Предпочтительным нестероидным 9 антиандрогеном является флутамид (2-метил-N[4-нитро-3-(трифторметил)фенил]пропанамид),коммерчески доступный как Эулексин(EULEXIN (Schering Corp Флутамид проявляет свое антиандрогенное действие за счет ингибирования поглощения андрогена, путем ингибирования в целевых тканях ядерного связывания андрогена или при использовании обоих механизмов. Флутамид в типичном случае вводят перорально, например, в виде капсулы. Одним из примеров дозировки флутамида является дозировка в 250 мг, принимаемая три раза в день, т.е. в количестве 750 мг в день. Другим нестероидным антиандрогеном является нилутамид, химическое наименование которого 5,5-диметил-3-[4-нитро-3-(трифторметил)-фенил]-2,4-имидазолидиндион. Нилутамид в рамках настоящего изобретения может использоваться, например, в дозировке 300 мг в день, с последующим снижением дозы до 150 мг/день. В некоторых вариантах реализации настоящего изобретения средство для химической стерилизации представляет собой сочетание агониста ЛГ-РФ, такого как ацетат леупролида и антиандрогена, такого как флутамид или нилутамид. Ацетат леупролида, например, может вводиться подкожной, внутримышечной или внутривенной инъекцией, при этом одновременно может перорально вводиться флутамид. Ингибитор тирозинкиназы может вводиться отдельно в виде третьей формы, или он может быть объединен с агонистом ЛГ-РФ или с антиандрогеном в составе одной композиции. Другим нестероидным антиандрогеном,применяемым в настоящем изобретении, является Казодекс (CASODEX). Одним из примеров дозировки Казодекса является доза от 5 до 500 мг в день, предпочтительно примерно 50 мг в день. Пример комбинированной формы по настоящему изобретению включает 1-20 мг соединения 11-12 и 100-1000 мг флутамида в составе капсулы, пригодной для перорального введения больному человеку один, два или три раза в день. В предпочтительном варианте реализации изобретения композиция включает носитель,содержащий полисорбат 80 и полиэтиленгликоль в соотношении 1:1 (объем/объем) для усиления биологической доступности соединенияII-12. В некоторых вариантах реализации изобретения пероральное введение указанной композиции соединения II-12/флутамида сопровождается внутримышечной инъекцией ацетата леупролида в форме депо, например, Люпрона депо (LUPRON DEPOT). Другой ингибитор тирозинкиназы, такой как соединение II-4 или соединение II-4-LAE, может заменять соединение II-12 в указанной композиции. Другим примером комбинированной композиции по настоящему изобретению является композиция, 002525 10 включающая соединение II-12, соединение II-4 и соединение II-4-LAE, а также химическое средство для стерилизации, объединенные в виде одного раствора, пригодного для внутривенной инфузии. Ингибиторы тирозинкиназы и средства для химической стерилизации могут быть включены в фармацевтические композиции, в виде индивидуальных форм или в сочетании, путем смешения с фармацевтически приемлемыми нетоксическими наполнителями и носителями. Могут быть получены композиции для использования в режиме парентерального введения, в частности, в виде жидких растворов или суспензий,для перорального введения, в частности, в виде жидкости, таблеток или капсул или для интраназального введения, в частности, в виде порошков, назальных капель или аэрозолей. Композиция может вводиться в виде стандартной дозированной формы, при этом она может быть получена с использованием любых известных в технике методов. Такие методы описаны в литературе (например, Remington'sPharmaceutical Sciences (Mack Pub. Co., Easton,Pa., 1980. Жидкие дозированные формы, пригодные для перорального введения, включают фармацевтически приемлемые эмульсии, микроэмульсии, растворы, суспензии, сиропы и эликсиры. Жидкие дозированные формы, кроме активного соединения, могут содержать инертные наполнители, используемые обычно в фармацевтической технике, например, воду или другие растворители, солюбилизирующие агенты и эмульгаторы, такие как этиловый спирт, изопропиловый спирт, этилкарбонат, этилацетат, бензиловый спирт, бензил-бензоат, пропиленгликоль,1,3-бутиленгликоль, диметилформамид, масла(в частности, хлопковое, арахисовое, кукурузное, масло из зародышей пшеницы, оливковое,касторовое и кунжутное масла), глицерин, тетрагидрофурфуриловый спирт, полиэтиленгликоли, сложные эфиры жирных кислот и сорбитана, а также их смеси. Кроме инертных разбавителей, пероральные композиции могут также включать адъюванты, такие как смачивающие средства, эмульгаторы и средства, способствующие суспендированию, подсластители, вкусовые добавки и отдушки. Инъецируемые депо-формы получают при микроинкапсулировании матриц лекарственного средства в биодеградируемые полимеры, такие как полилактид-полигликолид. Используя разные соотношения лекарственного средства и полимера, а также меняя природу используемого полимера, можно контролировать скорость высвобожения лекарственного средства. Примеры других биодеградируемых полимеров включают поли(ортоэфиры) и поли(ангидриды). Инъецируемые депо-формы также получают при введении лекарственного средства в ли 11 посомы или микроэмульсии, которые должны быть совместимыми с тканями организма. Твердые дозированные формы, пригодные для перорального введения, включают капсулы,таблетки, пилюли, порошки и гранулы. В таких твердых дозированных формах активное соединение смешано, по меньшей мере, с одним инертным фармацевтически приемлемым наполнителем или носителем, таким как цитрат натрия или двукальциевый фосфат и/или а) с наполнителями или разбавителями, такими как крахмалы, лактоза, сахароза, глюкоза, маннит и кремневая кислота, б) со связывающими веществами, такими как, например, карбоксиметилцеллюлоза, альгинаты, желатин, поливинилпирролидон, сахароза и аравийская камедь,в) с увлажнителями, такими как глицерин, г) с веществами, способствующими дезинтеграции,такими как агар-агар, карбонат кальция, крахмал из картофеля или тапиоки, альгиновая кислота, некоторые силикаты и карбонат натрия,д) с растворами средств, задерживающих высвобождение, таких как парафин, е) с ускорителями поглощения, такими как четвертичные аммониевые соединения, ж) увлажняющими средствами, такими как, например, цетиловый спирт и глицеринмоностеарат, з) с абсорбентами, такими как каолин и бентонитовая глина и и) с замасливателями, такими как тальк, стеарат кальция, стеарат магния, твердые полиэтиленгликоли, лаурилсульфат натрия и их смеси. В случае капсул, таблеток и пилюль дозированная форма может также включать забуферивающие средства. Твердые композиции аналогичного типа могут также использоваться в качестве наполнителей для мягких и твердых желатиновых капсул, при этом в них используются такие наполнители, как лактоза или молочный сахар, а также высокомолекулярные полиэтиленгликоли и др. В ходе изготовления твердые дозированные формы в виде таблеток, драже, капсул, пилюль и гранул могут быть покрыты оболочкой,при этом покрытия, такие как энтеросолюбильные оболочки и другие виды покрытия известны в фармацевтической технике. Они также могут необязательно содержать средства, придающие форме непрозрачность, а также могут быть композицией, которая высвобождает активный(ые) ингредиент(ы) только или, предпочтительно, в определенной части желудочно-кишечного тракта, в том числе, необязательно, в режиме задержки. Примеры композиций с погруженным внутрь нее активным ингредиентом, которые могут использоваться в рамках настоящего изобретения, включают полимерные вещества и воски. Твердые композиции аналогичного типа могут также использоваться в качестве наполнителей в твердых и мягких желатиновых капсулах с использованием для этого таких наполнителей, как лактоза, или молочный сахар, а 12 также высокомолекулярных полиэтиленгликолей и др. Как было отмечено выше, активные соединения могут также быть микроинкапсулированы с введением в такую форму одного или более наполнителей. В твердых дозированных формах активное соединение может быть смешано, по меньшей мере, с одним инертным разбавителем,таким как сахароза, лактоза или крахмал. Указанные дозированные формы могут также включать, как это происходит в обычной практике, вспомогательные вещества, отличные от инертных разбавителей, например, замасливатели для приготовления таблеток и другие вспомогательные вещества, такие как стеарат магния и микрокристаллическая целлюлоза. В случае капсул, таблеток и пилюль дозированные формы могут также включать забуферивающие средства. Они могут, необязательно, содержать средства для придания препарату непрозрачности, а также могут быть композицией, которая высвобождает активный(ые) ингредиент(ы) только или, предпочтительно, в определенной части желудочно-кишечного тракта, в том числе, необязательно, в режиме задержки. Примеры композиций с погруженным в них активным ингредиентом, которые могут использоваться в настоящем изобретении, включают полимерные вещества и воски. Ниже настоящее изобретение иллюстрируется приведенными примерами. Указанные примеры даются только с целью иллюстрации описания и никоим образом не ограничивают рамки или содержание изобретения. Примеры Пример 1. Соединение II-4, объединенное с химической стерилизацией. Данные, полученные в экспериментах на животных, которые включают введение ингибитора тирозинкиназы в сочетании с хирургической стерилизацией, рассматриваются как релевантные для случая введения ингибитора тирозинкиназы в сочетании с химической стерилизацией. В приведенных экспериментах используют опухоль Dunning R-3327 Н (полученную из спонтанной опухоли предстательной железы у старых крыс Copenhagen) в связи с ее чувствительностью к андрогенам с низкой скоростью роста (Isaacs, 1989, Cancer Res. 49:6290-6294). Предпосылкой эксперимента является тот факт,что хирургическая стерилизация крыс с опухолями Dunning H ведет к практически мгновенной остановке роста опухоли с последующей регрессией примерно через 5-6 недель после стерилизации андроген-нечувствительной опухоли (Isaacs et al., (1981) Cancer Res. 41: 50705075). Регрессия опухоли Dunning H, индуцированная соединением II-4, связана с эффектом не на андрогенном уровне, поскольку эксперименты выполнялись на крысах с имплантированными силастиновыми капсулами, высвобождаю 13 щие тестостерон. Капсулы имплантировали таким образом, чтобы поддерживать количество циркулирующего в крови тестостерона на физиологическом уровне. Измерения в конце эксперимента уровня тестостерона в сыворотке подтвердили, что содержание тестостерона составляет 1-2 нг/мл. Приведенный ниже эксперимент имеет три цели: 1) определить, обладает ли сочетание соединения II-4 с хирургической стерилизацией большей противоопухолевой эффективностью,чем одно только соединение II-4 или одна только хирургическая стерилизация; 2) определить может ли соединение II-4 вызывать регрессию опухолей Dunning H, нечувствительных к гормону, которые возникли путем отбора при предыдущей стерилизации животных; 3) определить, будут ли опухоли, обработанные соединением II-4 в течение нескольких циклов дозирования, все еще чувствительными к хирургической стерилизации. Соединение II-4 было синтезировано в(ПЭГ 1000, Spectrum, Los Angeles, CA), 10% поливинилпирролидона (С 30, ISP Boundbrook,NJ), 2% бензилового спирта (Spectrum, Los Angeles, CA) в воде (48%). Взрослых инбредных крыс Copenhagen(Indianapolis, IN), содержат их в клетках по три крысы и дают им коммерческую диету (PurinaFormulab 5001) и воду ad libitum. Животных содержат в контролируемых условиях влажности и температуры, с 12-часовыми циклами освещения/темноты. Крыс выдерживают на карантине в течение одной недели перед проведением эксперимента. Опухоли рака предстательной железы Dunning R-3327H трансплантируют крысам с использованием троакара. Взрослых самцов крыс Copenhagen, имеющих опухольDunning H, умерщвляют и выделяют опухоль. Указанную опухоль вырезают и небольшие кусочки инокулируют подкожно взрослым самцам крыс Copenhagen. Эксперименты проводят в соответствии с руководством, имеющимся в отделении для животных Университета Джона Хопкинса (JohnsHopkins University Animal Care), и с использованием протокола КомитетаRA91M517, а также в рамках руководства отдела по работе с животными института Цефалон (Cephalon Institutional Animal Care) и протокола Комитета 03008. Для проведения хирургической стерилизации крыс с установленными опухолями DunningH анестезируют внутримышечной инъекцией Кетамина (KETAMINE) (4,1 мг/100 г веса тела) и Ксилазина (Xylazine) (0,85 мг/100 г веса тела). Каждую крысу кладут на спину, делают небольшой надрез (0,5-1 см) по коже на заднем кончике мошонки. Другой разрез делают 14 так, чтобы вскрыть соединительную оболочку,окружающую яички. Эпидидимис, семенники,семявыводящий проток и семенные кровеносные сосуды, а также жир выщипывают и отделяют. Возвращают назад все оставшиеся ткани и разрез закрывают автозажимами. Автозажимы удаляют через 5-7 дней после проведения хирургической процедуры. Тридцать шесть крыс с опухолью DunningH (размером 0,9-18 см 3) разделяют на четыре группы по девять животных в каждой. Группа 1 служит в качестве контроля, принимающего носитель. Животных в группе 2 стерилизуют в 1 день. Животным в группе 3 делают инъекции соединения II-4 (10 мг/кг, пк), как описано ниже. Животных в группе стерилизуют в 1 день и затем инъецируют им соединение II-4, как описано ниже. Животным в группах 1 и 3 в 1 день имплантируют подкожно (на боку) закрытую силастиновую трубку длиной 2 см, заполненную тестостероном. Силастинового имплантата указанного размера достаточно для поддержания содержания тестостерона в сыворотке в физиологическом диапазоне 1-3 мг/мл хронически в течение шести месяцев. Соединение II-4 периодически вводят подкожно (10 мг/кг/день) животным в группах 3 и 4 с длительностью цикла дозирования 5 дней и примерно с 10-дневными периодами между циклами. Лекарственное средство вводят в дни 1-5, 1,4-18, 29-33 и 42-46. Фармацевтический носитель вводят животным в группах 1-2 по той же схеме, что и соединениеII-4 в экспериментальных группах. На 60 день восемь крыс из второй группы распределяют по двум группам с включением в каждую группу по четыре крысы. Одной группе животных вводят соединение II-4 в дозе 10 мг/кг (подкожно) в течение 5 дней с последующей отменой лекарственного средства в течение 9 дней, и затем проводят второй пятидневный режим введения препарата в дозе 10 мг/кг/день(подкожно). Второй группе животных вводят носитель по той же схеме дозирования. На 60 день семь крыс из 3 группы животных, принимавших участие в предшествующих экспериментах, распределяют по двум группам. В одной группе (N=3) проводят стерилизацию крыс. Обеим группам животных вводят соединение II-4 в дозе 10 мг/кг (подкожно) в течение 5 дней с последующей отменой лекарственного средства в течение 9 дней, и затем проводят второй пятидневный режим введения дозирования, как описано ранее. Размер опухоли измеряют у анастезированных животных (с использованием ингаляции изофлуораном в течение примерно 1-2 мин) в указанные интервалы с использованием циркуля. Объем опухоли вычисляют с использованием формулы: 15 Для статистического анализа полученных данных с использованием программы Сигмастат(Sigmastat) используют тест Даннета (Dunnett's(Paired t Test) или симптоматический ранжированный тест (Signed Rank) значимости. Рост опухоли Dunning H у интактных крыс, принимавших носитель, был линейным,при этом наблюдалось примерно 3,5-кратное увеличение объема опухоли в течение 60 дней наблюдения (фиг. 1). Хирургическая стерилизация вызывает быструю регрессию опухоли, например, на 25% к 5 дню. Повторный рост опухоли у стерилизованных крыс наблюдается к 12 дню, и 38 дню достигается полное восстановление прежнего объема регрессирующей опухоли. Соединение II-4 при введении его одного(10 мг/кг, пк; 4 независимых цикла лечения соединением II-4: 5 дней введения препарата с последующей отменой препарата в течение примерно 10 дней) вызывает полное ингибирование роста опухоли или индуцирует регрессию опухоли. Средний объем опухоли у животных,получавших препарат, был значительно меньше(р 0,01), чем у контрольных животных, принимавших носитель, после каждого цикла введения соединения II-4 (в дни 5, 19, 34 и 47, данные не показаны). Кроме того, каждый цикл введения соединения II-4 вызывает регрессию относительно объема опухоли, имевшегося в начале каждого цикла дозирования (данные не показаны). Сочетание введения соединения II-4 с хирургической стерилизацией вызывает полное ингибирование роста опухоли или индуцирует регрессию опухоли (фиг. 1) . В целом, сочетание введения соединения II-4 и хирургической стерилизации оказывается значительно более эффективным, чем одна только хирургическая стерилизация. In vivo наблюдается повторный рост опухоли после отмены введения соединения II-4 у стерилизованных, так и у не стерилизованных животных. Однако повторный рост был минимальный у стерилизованных животных (р 0,01,фиг. 1). Эти результаты показывают, что соединение II-4 может использоваться в сочетании с хирургической стерилизацией для максимизации степени и/или длительности регрессии опухолей на принятой модели in vivo рака предстательной железы. Дальнейшие эксперименты были проведены для определения, вызывает ли лечение соединением II-4 регрессию опухолей, отобранных по нечувствительности к гормону в ходе предшествующей аблации андрогена. Восемь крыс из группы стерилизованных животных в предыдущем эксперименте (которым не проводили предварительного введения соединения II4) разделяют на 60 день на две группы по четыре крысы в каждой группе. Одной группе жи 002525 16 вотных вводят соединение II-4 в дозе 10 мг/кг,пк в течение 5 дней с последующей отменой препарата в течение 9 дней и затем проводят второй пятидневный режим введения в дозе 10 мг/кг/день, пк. Второй группе животных вводят носитель по той же схеме дозирования. Введение соединения II-4 вызывает на 3 день значительную регрессию роста нечувствительной к андрогену опухоли Dunnung H у стерилизованных животных (р 0,05; фиг. 2). Максимальная регрессия наблюдается на 6 день(р 0,05). Отмена введения препарата вновь приводит к росту опухоли. При этом объем опухоли у крыс, которым вводят соединение II-4, значительно меньше (р 0,05), чем у животных, принимавших носитель, даже в течение 10 дней после окончания первого цикла приема соединения II-4. Опухоли Dunning H, отобранные по нечувствительности к гормону при предыдущей аблации андрогена, остаются чувствительными к противоопухолевому действию соединения II4. Были проведены также эксперименты для определения того, может ли предварительное введение соединения II-4 крысам с опухолямиDunning H вызвать селекцию опухолей по нечувствительности к последующей аблации андрогена через хирургическую стерилизацию. Семь крыс из группы, принимавшей соединениеII-4 в предыдущем эксперименте, были разделены на 60 день на две группы. Животных в одной группе (N=3) стерилизуют, как описано выше. Обеим группам животных вводят соединение II4 в дозе 10 мг/кг, пк в течение 5 дней с последующей отменой введения препарата в течение 9 дней и затем проводят второй пятидневный цикл дозирования, как описано ранее. Хирургическая стерилизация вызывает статистически незначимую регрессию опухолей, которые подвергались обработке соединением II-4 в течение 4 предшествующих циклов и двух одновременных циклов (фиг. 3). В целом, полученные данные указывает на то, что повторное воздействие соединения II-4 не приводит к селекции популяции опухолей Dunning H, нечувствительных к андрогену. Стерилизация, введение соединения II-4 и сочетание введения соединения II-4 с хирургической стерилизацией хорошо переносились животными. Ограниченная летальность отмечалась в группах контрольных и стерилизованных животных, которым давали носитель или соединение II-4. В каждом случае смерть наступала во время измерения размеров опухоли, скорее всего, в связи с передозировкой анестезирующего средства. Пример 2. Сочетание введения соединенияII-12 и химической стерилизации. Соединение II-12 было синтезировано компанией Cephalon, Inc. Дигидрохлорид соединения II-12 готовят (10 мг/мл) в носителе,содержащем в соотношении 3:2 (объем/объем)Gelucire (Gattefosse, Saint-Priest, France) в пропиленгликоле (Spectrum, Gardena, CA). В этом эксперименте используют взрослых инбредных самцов крыс Copenhagen (200-240 г),полученных от Harlan Sprague Dawley (Indianapolis, IN). Содержание крыс, постановку опытов и трансплантацию опухолей Dunning R-3327 Н проводят, как описано в примере 1 (выше). Сорок шесть крыс (вес: 3808 г), имеющих опухоли Dunning Н (размером 1/6-33,2 см 3) разделяют на четыре группы. Группа 1 (N=12) служит в качестве контроля, принимающего носитель (1 мл/кг, перорально, дважды в день,дни 0-20 и 31-45). Животным в группе 2 (N=10) вводят ацетат леупролида (LUPRON DEPOT)(5,2 мл/кг, пк в дни 0 и 21). Животным в группе 3 (N=12) дают соединение II-12 (10 мг/кг, перорально, дважды в день в дни 0-20 и 31-45). Животным в группе 4 (N=12) дают сочетание ацетата леупролида (5,2 мл/кг, пк в дни 0 и 21) и соединения II-12 (10 мл/кг, перорально, дважды в день в дни 0-20 и 31-45). Животным в группах 1 и 3 имплантируют подкожно силастиновую капсулу длиной в 2 см с тестостероном. Измерение размера опухоли и статистический анализ полученных данных проводят, как описано в примере 1 (выше). Рост опухолей Dunning H in vivo идет непрерывно у животных, принимающих носитель. К 53 дню отмечается примерно 2,5-кратное увеличение объема опухоли. При этом начало каждого цикла лечения соединением II-12 (10 мл/кг,дважды в день, перорально в течение 21 дня с промежуточным десятидневным периодом без приема препарата) ингибируют рост опухолиDunning Н и вызывает заметную регрессию опухоли. Ингибирование роста опухоли, наблюдаемое в группе приема соединения II-12, является статистически значимым, в сравнении с контрольной группой приема носителя. Указанное различие наблюдается уже на самой ранней стадии измерения опухоли, то есть, начиная с 4 дня до окончания эксперимента. Введение одного только ацетата леупролида также приводит к регрессии опухоли. При этом наблюдается медленный повторный рост опухоли примерно через 32 дня после начала введения леупролида(фиг. 4). В сравнении с режимом введения одного леупролида или одного соединения II-12, введение сочетания соединения II-12/леупролида является значительно более эффективным режимом лечения (р 0,05), способствующим поддержанию сниженной скорости роста опухоли,чем применение любого из препаратов поодиночке (фиг. 4). Повторный рост опухоли наблюдается в группе лечения соединением II-12 и в группе лечения леупролидом, и происходит это примерно через тридцать дней после начала лечения. В отличие от этих вариантов, в группе лечения указанным сочетанием отмечается более длительный период сниженной скорости 18 роста опухоли, и эти значения статистически отличаются от данных, полученных для группы приема соединения II-12 и группы приема леупролида, начиная с 35 дня до 39 дня, соответственно, вплоть до окончания эксперимента на 54 день (р 0,05; фиг. 4). Результаты указанных экспериментов показывают, что сочетание введения соединенияII-12 с химической стерилизацией действует синергическим образом на проявление противоопухолевой эффективности (фиг. 1 и 4). Другие варианты реализации настоящего изобретения будут очевидны из приведенной ниже формулы изобретения. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ ингибирования прогрессирования опухоли предстательной железы у млекопитающих, включающий введение указанному млекопитающему терапевтически эффективного количества ингибитора тирозинкиназы, выбранного из группы, состоящей из trkA ингибитора,trkB ингибитора и trkC ингибитора, и вместе с ним введение указанному млекопитающему терапевтически эффективного количества средства для химической стерилизации, выбранного из группы, состоящей из эстрогена, агониста ЛГ-РФ, антагониста ЛГ-РФ и антиандрогена. 2. Способ по п.1, отличающийся тем, что указанным млекопитающим является человек. 3. Способ по п.1, отличающийся тем, что терапевтически эффективное количество ингибитора тирозинкиназы и терапевтически эффективное количество средства для химической стерилизации ингибируют рост опухоли синергическим образом. 4. Способ по п.1, отличающийся тем, что указанный ингибитор тирозинкиназы представляет собой индолокарбазол. 5. Способ по п.4, в соответствии с которым индолокарбазол имеет следующую структуру: 6. Способ по п.4, в соответствии с которым индолокарбазол имеет следующую структуру: 19 7. Способ по п.4, в соответствии с которым индолокарбазол имеет следующую структуру: индолокарбазола, имеющего структуру 8. Способ по п.1, отличающийся тем, что указанный ингибитор тирозинкиназы представляет собой конденсированный пирролокарбазол. 9. Способ по п.1, отличающийся тем, что указанный ингибитор тирозинкиназы вводится перорально. 10. Способ по п.1, отличающийся тем, что указанный ингибитор тирозинкиназы вводится парентерально. 11. Способ по п.1, отличающийся тем, что указанный агонист ЛГ-РФ представляет собой ацетат леупролида. 12. Способ по п.1, отличающийся тем, что указанный антиандроген представляет собой флутамид. 13. Способ по п.1, отличающийся тем, что указанное средство для химической стерилизации представляет собой сочетание агониста ЛГРФ и антиандрогена. 14. Способ по п.13, отличающийся тем, что указанный агонист ЛГ-РФ представляет собой ацетат леупролида и указанный антиандроген представляет собой флутамид. 15. Способ по п.1, отличающийся тем, что указанный ингибитор тирозинкиназы и указанное средство для химической стерилизации вводятся в виде раздельных композиций. 16. Способ по п.1, отличающийся тем, что указанный ингибитор тирозинкиназы и указанное средство для химической стерилизации вводятся вместе в виде одной композиции. 17. Композиция, включающая ингибитор тирозинкиназы, выбранный из группы, состоящей из trkA ингибитора, trkB ингибитора и trkC ингибитора, и средство для химической стерилизации, выбранное из группы, состоящей из эстрогена, агониста ЛГ-РФ, антагониста ЛГ-РФ и антиандрогена. 18. Композиция по п.17, в которой ингибитор тирозинкиназы представляет собой индолокарбазол. 19. Композиция по п.18, при том, что входящий в нее индолокарбазол выбирают из груп и индолокарбазола, имеющего структуру 20. Композиция по п.17, в которой ингибитор тирозинкиназы представляет собой конденсированный пирролокарбазол. 21. Композиция по п.17, отличающаяся тем, что указанную композицию составляют для перорального введения. 22. Композиция по п.17, отличающаяся тем, что указанную композицию составляют для парентерального введения. 23. Композиция по п.17, в которой агонист ЛГ-РФ представляет собой ацетат леупролида. 24. Композиция по п.17, в которой антиандроген представляет собой флутамид. 25. Композиция по п.17, отличающаяся тем, что указанное средство для химической стерилизации представляет собой сочетание агониста ЛГ-РФ и антиандрогена. 26. Композиция по п.17, в которой указанный агонист ЛГ-РФ представляет собой ацетат леупролида и антиандроген представляет собой флутамид.
МПК / Метки
МПК: A61K 45/06, A61P 35/00
Метки: железы, предстательной, ингибитора, лечения, рака, тирозинкиназы, сочетание, химической, стерилизации
Код ссылки
<a href="https://eas.patents.su/12-2525-sochetanie-ingibitora-tirozinkinazy-i-himicheskojj-sterilizacii-dlya-lecheniya-raka-predstatelnojj-zhelezy.html" rel="bookmark" title="База патентов Евразийского Союза">Сочетание ингибитора тирозинкиназы и химической стерилизации для лечения рака предстательной железы</a>
Предыдущий патент: Способ разработки мощных пологопадающих рудных залежей
Следующий патент: Применение фанхинона для лечения болезни альцгеймера
Случайный патент: Балонный катетер с лекарственным покрытием












