Способ получения гепатопротекторного средства на основе пиностробина из почек тополя бальзамического (populus balsamifera l.)
Формула / Реферат
Способ получения гепатопротекторного средства на основе пиностробина из почек тополя бальзамического (Populus balsamifera L.), включающий экстракцию растительного сырья, его обработку, отличающийся тем, что экстракцию проводят баротермическим способом при температуре 150-160°С, давлении 1,9 атм, в течение 60 мин, хроматографическим разделением и очисткой густого экстракта при элюировании колонки петролейным эфиром и смесью петролейный эфир-этилацетат 49:1, перекристаллизацией выделенного технического пиностробина с последующим синтезом на его основе оксима пиностробина (субстанция для лекарственной формы).
Текст
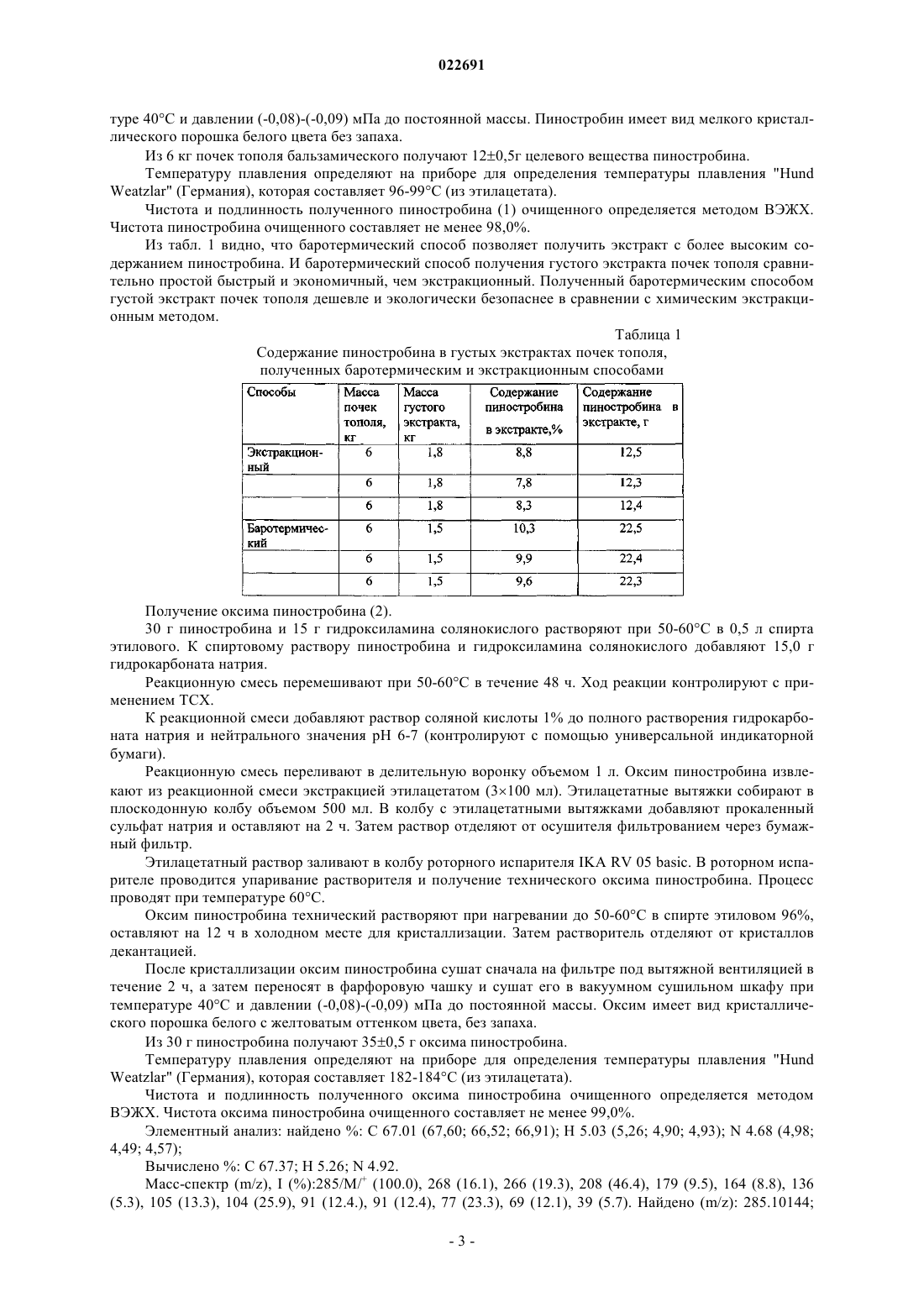
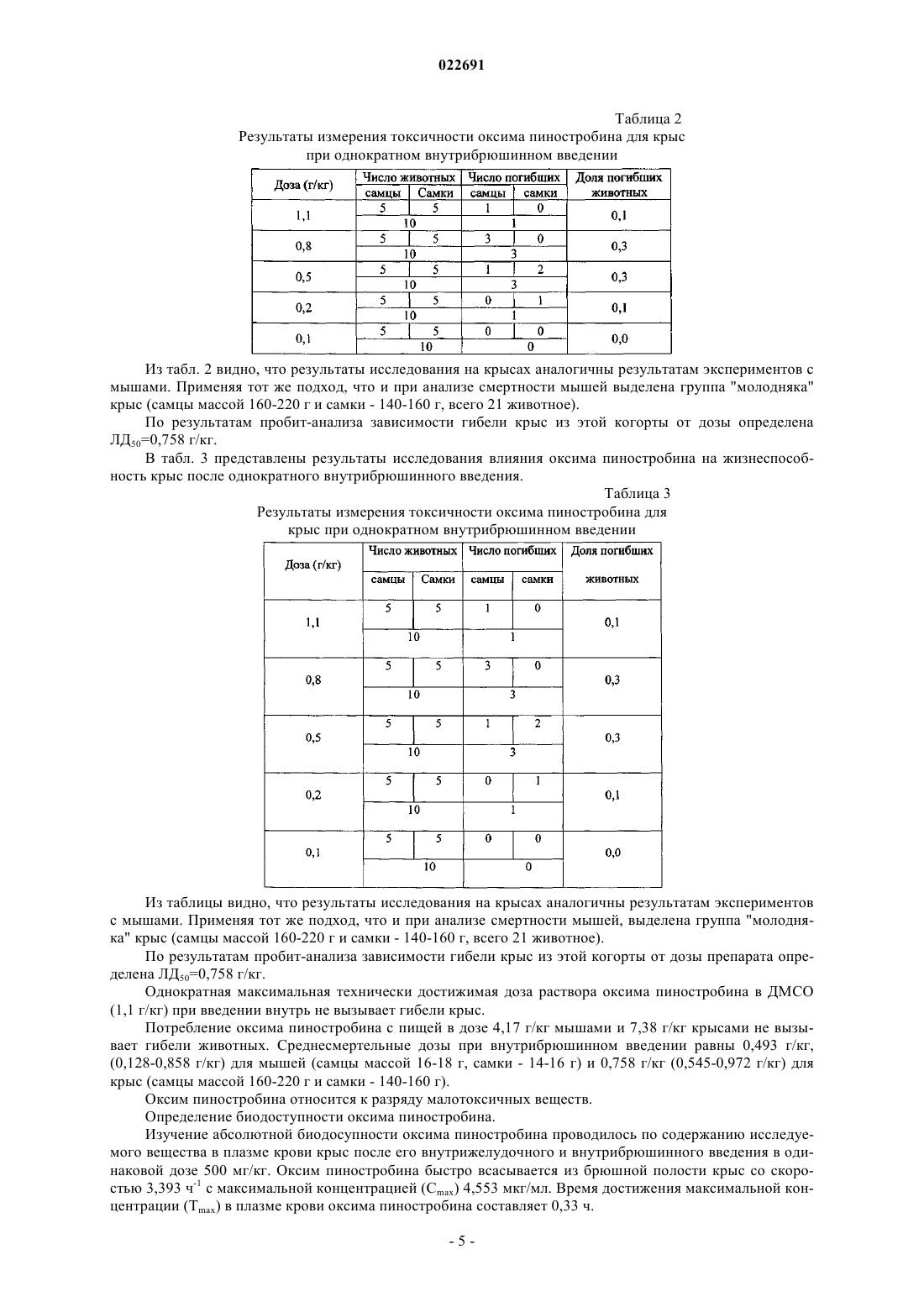
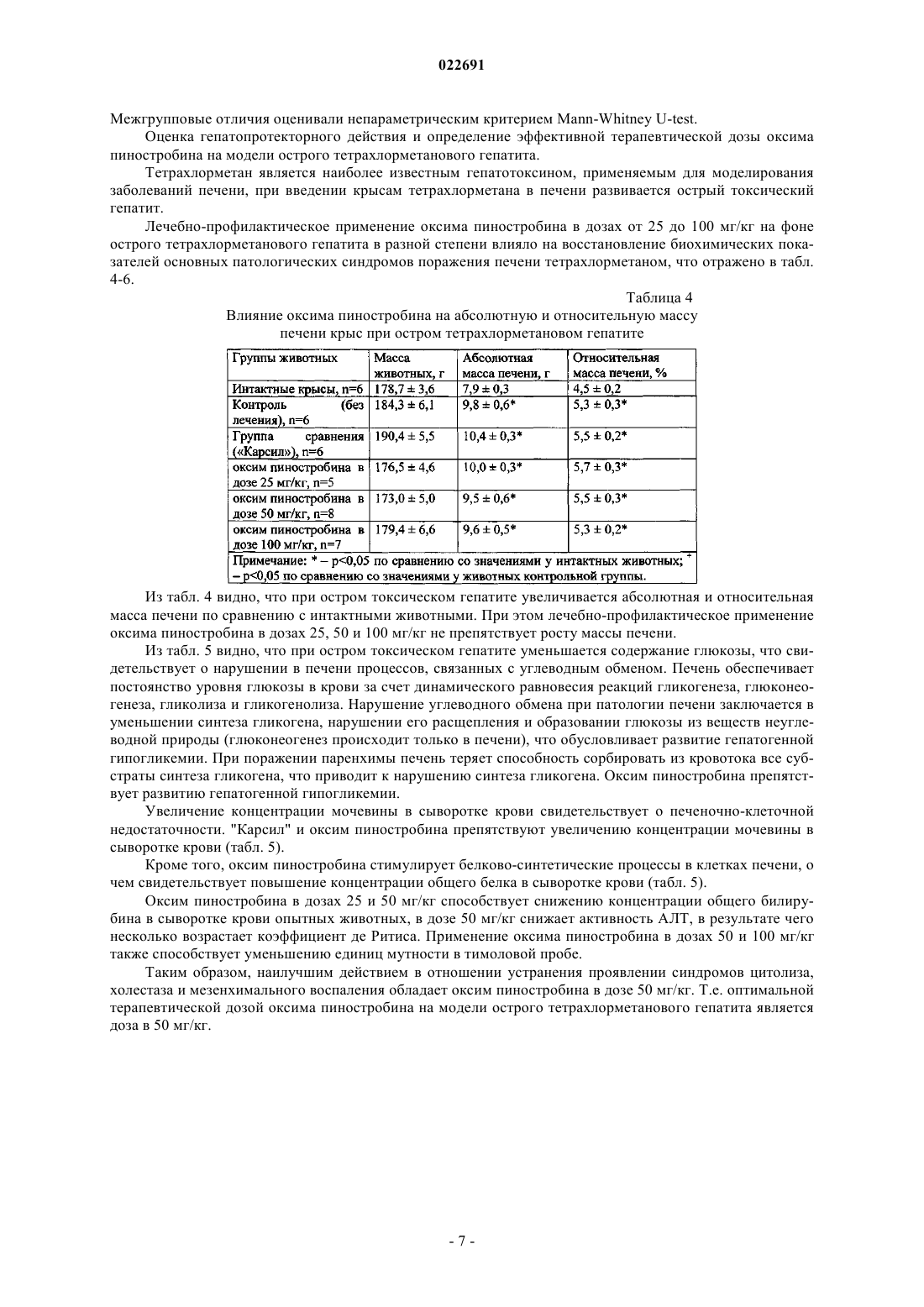
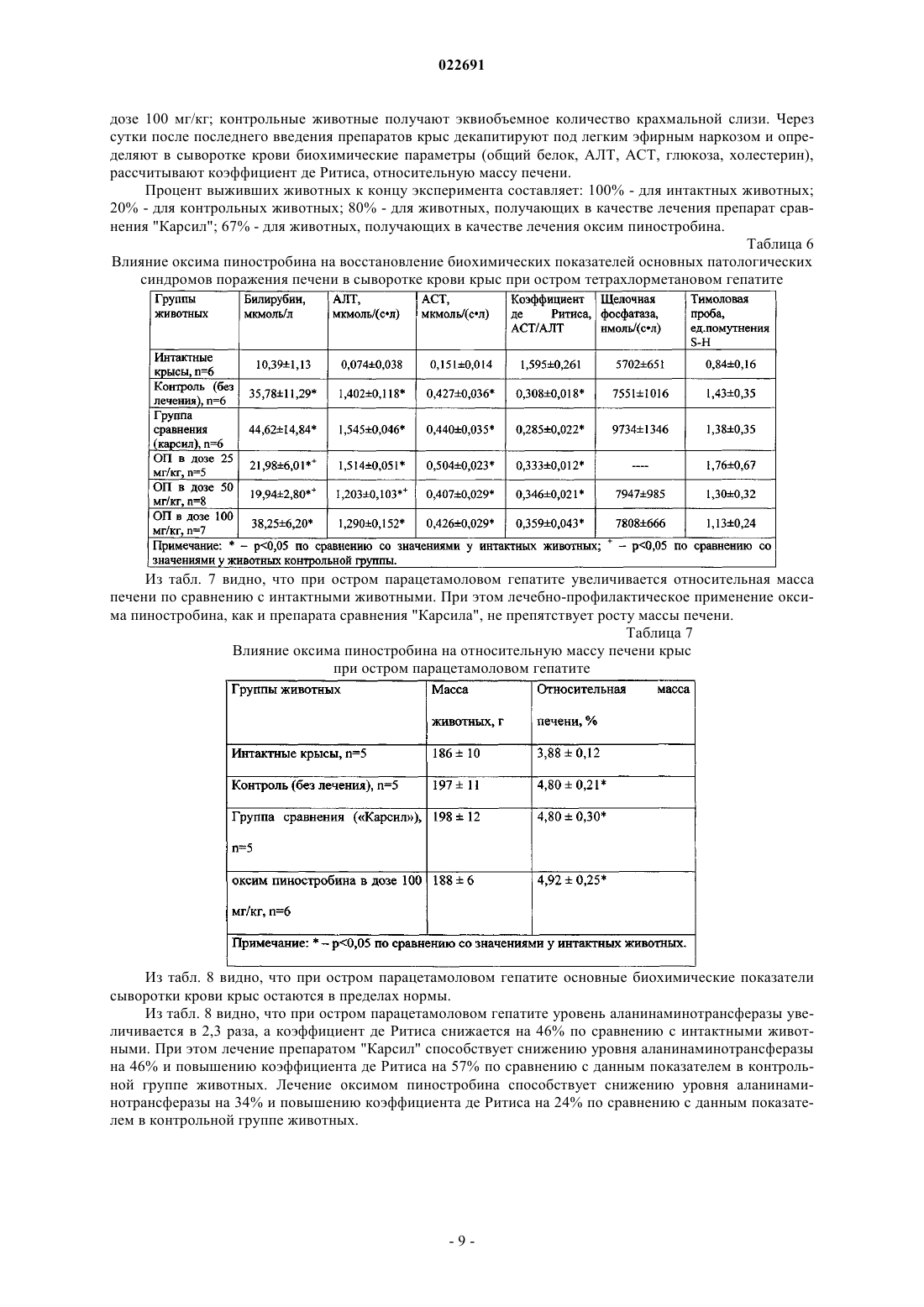
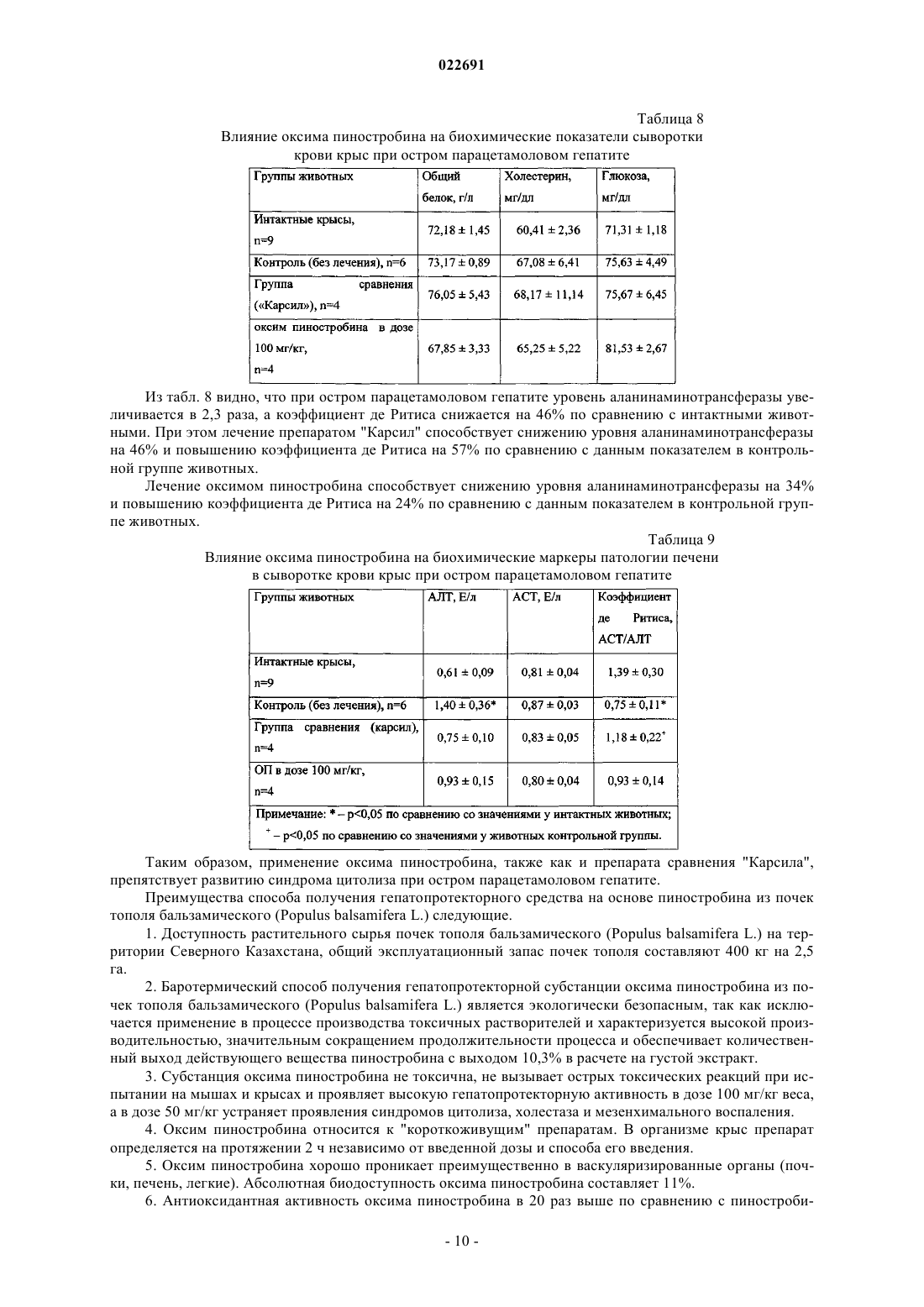
СПОСОБ ПОЛУЧЕНИЯ ГЕПАТОПРОТЕКТОРНОГО СРЕДСТВА НА ОСНОВЕ ПИНОСТРОБИНА ИЗ ПОЧЕК ТОПОЛЯ БАЛЬЗАМИЧЕСКОГО (POPULUS(56) ПОЛЯКОВ В.В. и др. Перспективы внедрения новых оригинальных препаратов на основе почек тополя бальзамического (Populus Изобретение относится к области биоорганической химии, фармацевтической химии и технологии лекарств и касается способов получения препаратов из растительного сырья, обладающих гепатопротекторной активностью. Технический результат заявляемого изобретения достигается тем, что используется экологически безопасный баротермический способ получения экстракта почек тополя бальзамического (Populus balsamifera L.) с содержанием флавоноида пиностробина 0,9% в расчете на воздушно-сухое сырье, экстракцией сырья при температуре 150-160 С, давлении 1,9 атм, в течение 60 мин, разделением и очисткой густого экстракта методом колоночной хроматографии при элюировании петролейным эфиром и смесью петролейный эфир-этилацетат 49:1, перекристаллизацией выделенного технического пиностробина с последующим синтезом на его основе оксима пиностробина (субстанция для лекарственной формы). Субстанция оксима пиностробина не токсична, не вызывает острых токсических реакций при испытании на мышах и крысах и проявляет высокую гепатопротекторную активность в дозе 100 мг/кг веса, а в дозе 50 мг/кг устраняет проявления синдромов цитолиза, холестаза и мезенхимального воспаления. Оксим пиностробина относится к "короткоживущим" препаратам. В организме крыс препарат определяется на протяжении 2 ч, независимо от введенной дозы и способа его введения, хорошо проникает преимущественно в васкуляризированные органы (почки, печень, легкие) и абсолютная биодоступность оксима пиностробина составляет 11%. Антиоксидантная активность оксима пиностробина в 20 раз выше по сравнению с пиностробином. Оксим пиностробина не оказывает токсического действия на печень, снижает в ней интенсивность липопероксидации, содержание триацилглицеридов на 26% и повышает уровень фосфолипидов на 21%, ингибирует процессы перекисного окисления липидов в гепатоцитах, снижая содержание диеновых конъюгатов на 35%, повышая активность ферментов антиперекисной защиты - глутатионпероксидазы и глутатионредуктазы до 54%.sciences. London, August 16-23, 2012 ЛОЖКИНА Г.А. и др. Влияние различных факторов на процесс экстракции почек тополя бальзамического. Химия растительного сырья,Барнаул, 2007,2, с. 51-54 ИСАЕВА Е.В. и др. Комлексное использование вегетативной части тополя бальзамического. Материалы III Всероссийской конференции, книга 2, Барнаул, 2007, с. 301-302(71)(72)(73) Заявитель, изобретатель и патентовладелец: АДЕКЕНОВ СЕРГАЗЫ МЫНЖАСАРОВИЧ (KZ) Изобретение относится к области биоорганической химии, фармацевтической химии и технологии лекарств и касается способов получения препаратов из растительного сырья, обладающих гепатопротекторной активностью. Задачей изобретения является разработка способа получения на основе природного флавоноида пиностробина (1) и его оксима (2), обладающего гепатопротекторной активностью. Известны способы выделения пиностробина. Способ 1. Почки тополя бальзамического (Populus balsamifera L.) настаивают 65-96% этиловым спиртом в условиях дробной мацерации, сочетающей в себе настаивание при комнатной температуре 24 ч с последующим извлечением целевых веществ при нагревании не выше 80 С в течение 1 ч и объединением первого и второго извлечений. Получают сумму флавоноидов и фенилпропаноидов с содержанием 2,7% (патент РФ 2135201 от 27.08.1998 г. Браславский В.Б., Куркин В.А., Запесочная Г.Г., Жданов И.П. "Способ получения настойки тополя бальзамического для лечения гнойно-воспалительных заболеваний мягких тканей"). Способ 2. Почки тополя бальзамического (Populus balsamifera L.) экстрагируют 96% этиловым при соотношении сухое сырье:экстрагент=1:20, этанольный экстракт упаривают под вакуумом, остаток растворяют в горячей воде, флавоноиды извлекают этилацетатом, при температуре - 70 С, времени 5 ч. Содержание пиностробина в экстракте 0,17% в пересчете на единицу абсолютно сухого сырья (Ложкина Г.А., Исаева Е.В., Рязанова Т.В. Влияние различных факторов на процесс экстракции почек тополя бальзамического. Химия растительного сырья. - 2007. -2. - С. 51-54). Способ 3. Околоплодник грецкого ореха (Juglans regia L.) экстрагируют 96% этиловым спиртом,полученную сумму веществ разделяют на колонке с силикагелем смесью петролейный эфир-этилацетат(15:1), элюаты объединяют и перекристаллизацией из этилацетата получают пиностробин и бетаситостерина с чистотой 98% (European Patent CN 101475459 А; 08.07.2009, Ke Yuan, Yuanhui Liu, ZhijunZhang "Method for extracting pinostrobin and beta-sitosterin from hickory nut epicarp"). Недостатками вышеописанных способов являются: 1) низкий выход целевого вещества пиностробина (0,17% в пересчете на воздушно-сухое сырье); 2) использование токсичных и легковоспламеняющихся растворителей, применение которых в фармацевтическом производстве запрещено по стандартам надлежащей производственной практики(GMP); 3) длительность по времени процессов в вышеприведенных способах выделения и очистки пиностробина; 4) один из природных источников пиностробина - грецкий орех - имеет узкий ареал произрастания(Заилийский Алатау, Каратау, Западный Тянь-Шань). В качестве растительного сырья в предлагаемом нами способе используют почки тополя бальзамического (Populus balsamifera L.), который широко распространен на территории Северного Казахстана. Эксплуатационные запасы почек тополя в Северо-Казахстанской области составляют 400 кг на 2,5 га. Технический результат заявляемого изобретения достигается тем, что используется экологически безопасный баротермический способ получения экстракта почек тополя бальзамического (Populus balsamifera L.) с содержанием флавоноида пиностробина 0,9% в расчете на воздушно-сухое сырье, экстракцией сырья при температуре 150-160 С, давлении 1,9 атм, в течение 60 мин, разделением и очисткой сгущенного экстракта методом колоночной хроматографии при элюировании петролейным эфиром и смесью петролейный эфир-этилацетат (49:1), перекристаллизацией технического пиностробина с последующим синтезом оксима пиностробина (субстанция для лекарственной формы). Флавоноид пиностробин из почек тополя бальзамического (Populus bahamifera L.) выделяют следующим способом. Способ А. Экстракцию почек тополя бальзамического проводят баротермическим способом. В реактор помещают 6 кг почек тополя бальзамического и нагревают при температуре 150-160 С, давлении 1,9 атм в течение 60 мин до полноты извлечения масла, получают густой экстракт (с выходом 35% от веса сырья) и эфирное масло тополя бальзамического (выход 0,9% от веса сырья). Густой экстракт массой 0,25 кг смешивают с силикагелем (0,5 кг) в соотношении 1:2 (0,5 кг) и тщательно перемешивают до получения однородной массы. Сгущнный экстракт, смешанный с силикагелем, раскладывают на ровную поверхность (противень из нержавеющей стали или стекло) тонким слоем и помещают под вытяжную вентиляцию. Сухой экстракт с силикагелем измельчают, взвешивают, его масса составляет 0,7 кг. Хроматографическая колонка заполняется силикагелем "сухим способом". Масса засыпаемого силикагеля 1,0 кг, объем петролейного эфира 5,0 л. Колонку элюируют сначала петролейным эфиром, а затем смесью петролейный эфир-этилацетат (49:1). Фракции упаривают на роторном испарителе ИР-10 М. Сухой остаток фракций контролируют методом ТСХ и объединяют этилацетатом. Фракции, содержащие пиностробин, промывают петролейным эфиром и высушивают под тягой. Получают 220,5 г пиностробина технического. 25,0 г пиностробина технического перекристаллизовывают. Испарительную колбу с пиностробином техническим устанавливают на водяную баню при температуре 60-70 С, растворяют в этилацетате и оставляют на 12 ч. Выпавшие кристаллы промывают петролейным эфиром. После кристаллизации пиностробин сушат сначала на фильтре под вытяжной вентиляцией в течение 2 ч, а затем переносят в фарфоровую чашку и сушат их в вакуумном сушильном шкафу при температуре 40 С и давлении (-0,08)-(-0,09) мПа до постоянной массы. Пиностробин имеет вид мелкого кристаллического порошка белого цвета без запаха. Из 6 кг почек тополя бальзамического получают 220,5 г действующего вещества пиностробина. Температуру плавления определяют на приборе для определения температуры плавления "HundWeatzlar" (Германия), которая составляет 96-99 С (из этилацетата). Чистота и подлинность полученного пиностробина (1) очищенного определяется методом ВЭЖХ. Чистота пиностробина очищенного составляет не менее 99,5%. Элементный анализ: найдено %: С 70.6 (71.57; 71.11; 70.64); Н 4.9 (5.18; 5.30; 4,79); Вычислено %: С 71.0; Н 5.09. Масс-спектр (m/z), I (%):270/М/+ (100.0), 252 (6.1), 193 (35.8), 166 (62.4), 138 (29.6), 114 (6.9), 110(ОСН 3, с.). 13 С ЯМР (CDCl3, 300 МГЦ,(м.д.: 79,10 (С-2, д.), 43,26 (С-3, тр.), 167.00 (С-4, с.), 162.66 (С-5, с),95,02 (С-6, д.), 195,63 (С-7, д.), 94,14 (С-8, д.), 164,02 (С-9, с), 103,02 (С-10, с), 138,25 (С-1', с), 126,01 (С 2', д.), 128,75 (С-3', д.), 126.01 (С-4, д.), 128.75 (С-5, д.), 126.01 (С-6, д.), 55,22 (ОСН 3, к.). Способ Б. 6 кг почек тополя в мешке, сшитом из "бязи", помещают в емкость для экстрагирования сырья, затем заливают заранее приготовленный экстрагент - спирт этиловый 95% в количестве 33,064 кг(40 л), экстрагируют при температуре 60 С. После охлаждения жидкий экстракт сливают и экстракцию повторяют еще 2 раза при тех же условиях. По истечении времени экстрагирования жидкий экстракт заливают в роторный испаритель. В роторном испарителе проводится процесс сгущения жидкого экстракта при температуре 60 С. Получают 250 г густого экстракта почек тополя бальзамического. Очищенный густой экстракт массой 0,25 кг из испарительной колбы сливают в выпарительную фарфоровую чашку, остатки экстракта со стенок колбы смывают небольшим количеством спирта этилового (0,2 кг). Смыв объединяют вместе с густым экстрактом в выпарительной чашке и тщательно перемешивают до получения однородной массы достаточно жидкой консистенции. К растворенному экстракту добавляют силикагель в соотношении 1:2 (0,5 кг) и тщательно перемешивают до получения однородной кашицеобразной массы. Сгущнный экстракт, смешанный с силикагелем, раскладывают на ровную поверхность (противень из нержавеющей стали или стекло) тонким слоем для быстрого испарения спирта этилового под вытяжной вентиляцией. Сухой экстракт с силикагелем измельчают, взвешивают, его масса составляет 0,7 кг. Хроматографическая колонка заполняется силикагелем "сухим способом". Масса засыпаемого силикагеля 1,0 кг, объем петролейного эфира 5,0 л. Колонку элюируют сначала петролейным эфиром, а затем смесью петролейный эфир-этилацетат 98:2. Фракции упаривают на роторном испарителе ИР-10 М. Сухой остаток фракций контролируют методом ТСХ и объединяют этилацетатом. Фракции, содержащие пиностробин, промывают петролейным эфиром и высушивают под тягой. Получают 120,5 г пиностробина технического. 12 г пиностробина технического перекристаллизовывают следующим способом: испарительную колбу с пиностробином техническим устанавливают на водяную баню при температуре 60-70 С, растворяют в этилацетате и оставляют на 12 ч. Выпавшие кристаллы промывают петролейным эфиром. После кристаллизации пиностробин сушат сначала на фильтре под вытяжной вентиляцией в течение 2 ч, а затем переносят в фарфоровую чашку и сушат их в вакуумном сушильном шкафу при темпера-2 022691 туре 40 С и давлении (-0,08)-(-0,09) мПа до постоянной массы. Пиностробин имеет вид мелкого кристаллического порошка белого цвета без запаха. Из 6 кг почек тополя бальзамического получают 120,5 г целевого вещества пиностробина. Температуру плавления определяют на приборе для определения температуры плавления "HundWeatzlar" (Германия), которая составляет 96-99 С (из этилацетата). Чистота и подлинность полученного пиностробина (1) очищенного определяется методом ВЭЖХ. Чистота пиностробина очищенного составляет не менее 98,0%. Из табл. 1 видно, что баротермический способ позволяет получить экстракт с более высоким содержанием пиностробина. И баротермический способ получения густого экстракта почек тополя сравнительно простой быстрый и экономичный, чем экстракционный. Полученный баротермическим способом густой экстракт почек тополя дешевле и экологически безопаснее в сравнении с химическим экстракционным методом. Таблица 1 Содержание пиностробина в густых экстрактах почек тополя,полученных баротермическим и экстракционным способами Получение оксима пиностробина (2). 30 г пиностробина и 15 г гидроксиламина солянокислого растворяют при 50-60 С в 0,5 л спирта этилового. К спиртовому раствору пиностробина и гидроксиламина солянокислого добавляют 15,0 г гидрокарбоната натрия. Реакционную смесь перемешивают при 50-60 С в течение 48 ч. Ход реакции контролируют с применением ТСХ. К реакционной смеси добавляют раствор соляной кислоты 1% до полного растворения гидрокарбоната натрия и нейтрального значения рН 6-7 (контролируют с помощью универсальной индикаторной бумаги). Реакционную смесь переливают в делительную воронку объемом 1 л. Оксим пиностробина извлекают из реакционной смеси экстракцией этилацетатом (3100 мл). Этилацетатные вытяжки собирают в плоскодонную колбу объемом 500 мл. В колбу с этилацетатными вытяжками добавляют прокаленный сульфат натрия и оставляют на 2 ч. Затем раствор отделяют от осушителя фильтрованием через бумажный фильтр. Этилацетатный раствор заливают в колбу роторного испарителя IKA RV 05 basic. В роторном испарителе проводится упаривание растворителя и получение технического оксима пиностробина. Процесс проводят при температуре 60 С. Оксим пиностробина технический растворяют при нагревании до 50-60 С в спирте этиловом 96%,оставляют на 12 ч в холодном месте для кристаллизации. Затем растворитель отделяют от кристаллов декантацией. После кристаллизации оксим пиностробина сушат сначала на фильтре под вытяжной вентиляцией в течение 2 ч, а затем переносят в фарфоровую чашку и сушат его в вакуумном сушильном шкафу при температуре 40 С и давлении (-0,08)-(-0,09) мПа до постоянной массы. Оксим имеет вид кристаллического порошка белого с желтоватым оттенком цвета, без запаха. Из 30 г пиностробина получают 350,5 г оксима пиностробина. Температуру плавления определяют на приборе для определения температуры плавления "HundWeatzlar" (Германия), которая составляет 182-184 С (из этилацетата). Чистота и подлинность полученного оксима пиностробина очищенного определяется методом ВЭЖХ. Чистота оксима пиностробина очищенного составляет не менее 99,0%. Элементный анализ: найдено %: С 67.01 (67,60; 66,52; 66,91); Н 5.03 (5,26; 4,90; 4,93); N 4.68 (4,98; 4,49; 4,57); Вычислено %: С 67.37; Н 5.26; N 4.92. Масс-спектр (m/z), I (%):285/M/+ (100.0), 268 (16.1), 266 (19.3), 208 (46.4), 179 (9.5), 164 (8.8), 136(ОН, с), 3.7 (ОСН 3, с). 13 С ЯМР (DMSO-d6, 300 МГЦ,(м.д.: 79,10 (С-2, д.), 43,26 (С-3, тр.), 152.8 (С-4, с.), 159.2 (С-5, с),95,55 (С-6, д.), 162,24 (С-7, д.), 94,17 (С-8, д.), 157,93 (С-9, с), 98,62 (С-10, с), 139,83 (С-1', с), 126,68 (C-2',д.), 128,65 (C-3', д.), 126.68 (С-4', д.), 128.65 (С-5, 'д.), 126.68 (С-6', д.), 55,55 (ОСН 3, к.). Изучение острой токсичности оксима пиностробина (2). В экспериментах используют 2 вида животных: беспородные белые мыши и белые крысы. Каждая группа состоит из 5 животных. Для изучения острой токсичности оксима пиностробина используют его растворы в диметилсульфоксиде (ДМСО), эмульгированном с подсолнечным маслом. Максимальная технически достижимая доза оксима пиностробина определяется его растворимостью в ДМСО (0,56 г/мл) и безопасной дозой ДМСО, в качестве которой была принята доза 1,8 мл/кг. Для энтерального введения препарата готовят кормовые гранулы, смешивая равные весовые части оксима пиностробина и сырого яйца. Для формования гранул к смеси прибавляют хлебные крошки. Кормовые гранулы содержат 0,1 г оксима пиностробина. Кормовые гранулы даются животным, находящимся в отдельных клетках, в утренние часы в период от получаса до 3 ч. Доза оксима пиностробина, полученная животными в составе кормовых гранул, составляет для мышей 4,17 г/кг и для крыс 7,38 г/кг. Энтеральное введение осуществляется двумя способами - внутрижелудочно (с помощью зонда) и в составе кормовых гранул; парентеральное - внутрибрюшинно. В течение двухнедельного периода за состоянием животных осуществляется ежедневное наблюдение, и они трижды взвешивались. Павшие животные вскрываются, органы с выраженными изменениями отбираются для гистологического анализа. По окончании срока наблюдения выживших животных забивают декапитацией, вскрывают, органы взвешивают и отбирают пробы тканей для гистологического изучения. Органы, взятые для гистологического исследования, фиксируют в 10% нейтральном формалине, заливают в воск-парафин. Срезы толщиной 5-7 мкм окрашивают гематоксилином и эозином. Все гистопрепараты исследуют на микроскопе МБИ-15 на всех режимах увеличения (от 70 до 1000 крат). После получения оксима пиностробина в составе кормовых гранул (в среднем 4,17 г/кг) в поведении и внешнем виде мышей не проявляется признаков токсического воздействия препарата. Крысы получили наибольшую дозу препарата 8 и 10 г/кг (в среднем 7,38 г/кг). У животных не отмечается каких-либо отклонений. Макроскопическое исследование как мышей, так и крыс, получивших препарат с кормовыми гранулами, выявило умеренно выраженное полнокровие внутренних органов и вещества мозга. У животных, получивших оксим пиностробина в растворе ДМСО в дозе 1,1 г/кг, определялось следующее: мозг - полнокровие сосудов мягкой мозговой оболочки; сердце - умеренно выраженная дилатация полостей сердца; печень - умеренно выраженное полнокровие; почки - без макроскопических особенностей; селезенка - умеренно полнокровная, обычных размеров; семенники и яичники - без особенностей. Гистологически: определялись умеренно выраженные дистрофические изменения паренхиматозных и стромальных клеточных элементов внутренних органов и мозга. Таким образом, проведенное морфологическое исследование у животных, получавших оксим пиностробина внутрижелудочно в максимальных технически достижимых дозах, не выявляет токсических проявлений. После внутрибрюшинного введения оксима пиностробина отмечается снижение двигательной активности мышей, нарушение координация движений. Мыши гибнут начиная с 6-18 ч после введения препарата вплоть до окончания периода наблюдения - 14 суток. При вскрытии павших животных макроскопически выявлено: мозг - мягкие оболочки полнокровные, вещество мозга желеобразной консистенции, в желудочках отмечается наличие небольшое количество прозрачной жидкости; сердце - полости дилатированы, заполнены жидкой кровью, миокард дряблый; печень - буро-серого цвета, резко увеличена в размерах, при затрагивании пинцетом легко разрушается; почки - набухшие, темно-бурого цвета, на разрезе корковый слой дифференцируется нечетко; селезенка - увеличена в размерах, полнокровная; гонады - полнокровные. По результатам пробит-анализа зависимости гибели "молодняка" мышей внутрибрюшинно вводимого препарата определена средне - смертельная доза (ЛД 50)=0,493 г/кг. В табл. 2 представлены результаты исследования влияния оксима пиностробина на жизнеспособность крыс после однократного внутрибрюшинного введения. Таблица 2 Результаты измерения токсичности оксима пиностробина для крыс при однократном внутрибрюшинном введении Из табл. 2 видно, что результаты исследования на крысах аналогичны результатам экспериментов с мышами. Применяя тот же подход, что и при анализе смертности мышей выделена группа "молодняка" крыс (самцы массой 160-220 г и самки - 140-160 г, всего 21 животное). По результатам пробит-анализа зависимости гибели крыс из этой когорты от дозы определена ЛД 50=0,758 г/кг. В табл. 3 представлены результаты исследования влияния оксима пиностробина на жизнеспособность крыс после однократного внутрибрюшинного введения. Таблица 3 Результаты измерения токсичности оксима пиностробина для крыс при однократном внутрибрюшинном введении Из таблицы видно, что результаты исследования на крысах аналогичны результатам экспериментов с мышами. Применяя тот же подход, что и при анализе смертности мышей, выделена группа "молодняка" крыс (самцы массой 160-220 г и самки - 140-160 г, всего 21 животное). По результатам пробит-анализа зависимости гибели крыс из этой когорты от дозы препарата определена ЛД 50=0,758 г/кг. Однократная максимальная технически достижимая доза раствора оксима пиностробина в ДМСО(1,1 г/кг) при введении внутрь не вызывает гибели крыс. Потребление оксима пиностробина с пищей в дозе 4,17 г/кг мышами и 7,38 г/кг крысами не вызывает гибели животных. Среднесмертельные дозы при внутрибрюшинном введении равны 0,493 г/кг,(0,128-0,858 г/кг) для мышей (самцы массой 16-18 г, самки - 14-16 г) и 0,758 г/кг (0,545-0,972 г/кг) для крыс (самцы массой 160-220 г и самки - 140-160 г). Оксим пиностробина относится к разряду малотоксичных веществ. Определение биодоступности оксима пиностробина. Изучение абсолютной биодосупности оксима пиностробина проводилось по содержанию исследуемого вещества в плазме крови крыс после его внутрижелудочного и внутрибрюшинного введения в одинаковой дозе 500 мг/кг. Оксим пиностробина быстро всасывается из брюшной полости крыс со скоростью 3,393 ч-1 с максимальной концентрацией (Cmax) 4,553 мкг/мл. Время достижения максимальной концентрации (Tmax) в плазме крови оксима пиностробина составляет 0,33 ч. Препарат также быстро элиминирует из организма после его внутрибрюшинного введения. Об этом свидетельствует значение параметра tl/2el - 0,37 ч. Была рассчитана величина AUC0-2 и AUC0- оксима пиностробина после его внутрибрюшинного введения, которая позволила определить абсолютную биодоступность препарата, равную 11%. Тканевая доступность оксима пиностробина. Изучена тканевая доступность оксима пиностробина в печени, почках, легких, брыжейке, мозге,сердце. Оксим пиностробина регистрируется во всех исследуемых органах и тканях. Вещество определяется в плазме крови и органах в течение 2 ч. Анализ абсолютных величин тканевой доступности оксима пиностробина показал, что исследуемое соединение наиболее интенсивно распределяется в хорошо васкуляризированных органах (почки, печень, легкие), и наименее - в умеренно васкуляризированных органах (сердце, мозг, брыжейка). Разработана валидированная методика количественного определения оксима пиностробина в биологических материалах на основе высокоэффективной жидкостной хроматографии (ВЭЖХ) с тандемным масс-спектрометрическим и спектрофотометрическим детектированием. С помощью ВЭЖХ и массспектрометрии после внутрижелудочного введения оксима пиностробина крысам в дозе 50 мг/кг в их суточной моче обнаружено, что оксим пиностробина выводится с мочой преимущественно в неизменном виде. Изучение фармакокинетики оксима пиностробина в плазме крови крыс проводилось после его введения внутрь в дозах 50,0 и 500 мг/кг. После внутрижелудочного введения оксима пиностробина (50 и 500 мг/кг) животным, вещество быстро всасывается из желудочно-кишечного тракта (ЖКТ) со скоростью 1,917-2,188 ч-1 (Cmax/AUC0) и определяется в плазме крови на протяжении 2 ч исследования (в интервале 4-12 ч после введения препарата исследуемое вещество не регистрировалось даже в следовых количествах). Учитывая, что период полуэлиминации не превышал 0,23-0,28 ч, оксим пиностробина можно отнести к группе "короткоживущих" лекарственных препаратов. Антиоксидантная активность в тесте окисления ABTS (ТЕАС). Антиоксидантную активность оксима пиностробина исследуют с использованием набора реактивовAntioxidant Assay Kit (Sigma). Метод основан на регистрации катион-радикала 2,2'-азино-бис-(3 этилбензотиазолин-6-сульфоновой кислоты) (ABTS+), образующегося в реакции ABTS с феррил миоглобином. Антиоксиданты препятствуют продукции катион-радикала, и антиоксидантная активность оценивается в сравнении с активностью водорастворимого аналога витамина Е - "Тролокса". Использование"Тролокса" позволяет оценить эффективность антирадикального действия через так называемый "тролоксовый эквивалент антиоксидантной эффективности" (Trolox Equivalent Antioxidant Capacity, TEAC). Значения ТЕАС указывают, какое количество тролокса в мг/мл подавляет ABTS+ с той же эффективностью, как и 1 мг/мл анализируемого соединения. Антиоксидантный эффект пиностробина в пересчте на значения ТЕАС является минимальным и составляет 0, 011 мг/мл, в то время как уровень антиоксидантной активности оксима пиностробина по сравнению с пиностробином выше более чем в 20 раз и составляет 0,265 мг/мл. Модель острого CCl4-гепатита. Острый CCl4-гепатит воспроизводят путм введения per os с помощью зонда 3 раза через день 50% раствора CCl4 в вазелиновом масле в дозе 0,15 мл/100 г массы тела животного. Оксим пиностробина исследуют в диапазоне доз 25, 50 и 100 мг/кг при пероральном введении в виде суспензии в 1% крахмальной слизи по лечебно-профилактической схеме: в течение 7 дней до CCl4, а затем на фоне воспроизведения модели (5 дней). Оксим пиностробина вводят ежедневно в одно и то же время до кормления животных за 1 ч до введения гепатотоксина. Препарат сравнения "Карсил" изучают в дозе 100 мг/кг. Хроническую алкоголизацию проводят путем перорального введения 40% этилового спирта в дозе 14 мл/кг в течение 60 дней. Лечебное действие оксима пиностробина изучают в дозах 50 и 100 мг/кг в сравнении с "Карсилом" в дозе 100 мг/кг. Через сутки после 60-дневной алкоголизации начинают вводить исследуемые вещества в течение 21 дня на фоне приема этанола в вышеуказанных дозах. Затем проводят забой животных опытных и соответствующих контрольных групп. Контролем служат животные, которые продолжают получать только 40% этанол в дозе 14 мл/кг 21 день. Модель парацетамолового гепатита. Острый гепатит вызывают введением внутрижелудочно парацетамола в дозе 2500 мг на 1 кг массы тела в виде суспензии на 1% крахмальной слизи в течение 2 дней. С третьего дня эксперимента в течение 5 дней крысам вводят внутрь исследуемые вещества. Через сутки после последнего введения препаратов крыс декапитируют под легким эфирным наркозом, и определяют в сыворотке крови биохимические параметры (общий белок, АЛТ, ACT, билирубин, глюкоза, холестерина), а также абсолютную и относительную массы печени. Статистическую обработка результатов проводят с использованием пакета программ "Statistica 6,0". Нормальность распределения показателей оценивают с использованием критерия Shapiro-Wilk's W-test. Межгрупповые отличия оценивали непараметрическим критерием Mann-Whitney U-test. Оценка гепатопротекторного действия и определение эффективной терапевтической дозы оксима пиностробина на модели острого тетрахлорметанового гепатита. Тетрахлорметан является наиболее известным гепатотоксином, применяемым для моделирования заболеваний печени, при введении крысам тетрахлорметана в печени развивается острый токсический гепатит. Лечебно-профилактическое применение оксима пиностробина в дозах от 25 до 100 мг/кг на фоне острого тетрахлорметанового гепатита в разной степени влияло на восстановление биохимических показателей основных патологических синдромов поражения печени тетрахлорметаном, что отражено в табл. 4-6. Таблица 4 Влияние оксима пиностробина на абсолютную и относительную массу печени крыс при остром тетрахлорметановом гепатите Из табл. 4 видно, что при остром токсическом гепатите увеличивается абсолютная и относительная масса печени по сравнению с интактными животными. При этом лечебно-профилактическое применение оксима пиностробина в дозах 25, 50 и 100 мг/кг не препятствует росту массы печени. Из табл. 5 видно, что при остром токсическом гепатите уменьшается содержание глюкозы, что свидетельствует о нарушении в печени процессов, связанных с углеводным обменом. Печень обеспечивает постоянство уровня глюкозы в крови за счет динамического равновесия реакций гликогенеза, глюконеогенеза, гликолиза и гликогенолиза. Нарушение углеводного обмена при патологии печени заключается в уменьшении синтеза гликогена, нарушении его расщепления и образовании глюкозы из веществ неуглеводной природы (глюконеогенез происходит только в печени), что обусловливает развитие гепатогенной гипогликемии. При поражении паренхимы печень теряет способность сорбировать из кровотока все субстраты синтеза гликогена, что приводит к нарушению синтеза гликогена. Оксим пиностробина препятствует развитию гепатогенной гипогликемии. Увеличение концентрации мочевины в сыворотке крови свидетельствует о печеночно-клеточной недостаточности. "Карсил" и оксим пиностробина препятствуют увеличению концентрации мочевины в сыворотке крови (табл. 5). Кроме того, оксим пиностробина стимулирует белково-синтетические процессы в клетках печени, о чем свидетельствует повышение концентрации общего белка в сыворотке крови (табл. 5). Оксим пиностробина в дозах 25 и 50 мг/кг способствует снижению концентрации общего билирубина в сыворотке крови опытных животных, в дозе 50 мг/кг снижает активность АЛТ, в результате чего несколько возрастает коэффициент де Ритиса. Применение оксима пиностробина в дозах 50 и 100 мг/кг также способствует уменьшению единиц мутности в тимоловой пробе. Таким образом, наилучшим действием в отношении устранения проявлении синдромов цитолиза,холестаза и мезенхимального воспаления обладает оксим пиностробина в дозе 50 мг/кг. Т.е. оптимальной терапевтической дозой оксима пиностробина на модели острого тетрахлорметанового гепатита является доза в 50 мг/кг. Таблица 5 Влияние "Оксима пиностробина" на биохимические показатели сыворотки крови крыс при остром тетрахлорметановом гепатите Наряду с этим введение оксима пиностробина существенно снижает содержание первичных продуктов перекисного окисления липидов (ПОЛ)-диеновых конъюгатов в пересчете на фосфолипиды в печени экспериментальных животных на 58%, что свидетельствует о выраженном антиоксидантном эффекте оксима пиностробина in vivo. Курсовое введение оксима пиностробина приводит к снижению содержания триацилглицеридов в печени на 29% и повышению уровня фосфолипидов на 18%. При этом отношение фосфолипидов к триацилглицеридам (ТАГ) увеличивается до 8,7 раз, что свидетельствует об улучшении липидного обмена печени. Введение оксима пиностробина не приводит к существенному изменению содержания холестерола в печени экспериментальных животных. Таким образом, курсовое введение оксима пиностробина (25 мг/кг в день) не оказывает токсического действия на печень, снижает в ней интенсивность липопероксидации, содержание триацилглицеридов и повышает уровень фосфолипидов. Курсовое введение оксима пиностробина на фоне токсического гепатита, индуцированного четыреххлористым углеродом, достоверно снижает выход маркерных ферментов аланинаминотрансферазы(АЛТ) и аспартаминотрансферазы (ACT) в сыворотку крови на 44 и 20% соответственно. В механизме гепатопротективного эффекта оксима пиностробина in vivo лежит его способность ингибировать процессы ПОЛ в гепатоцитах, о чем свидетельствует существенное снижение содержания диеновых конъюгатов на 35%. Ингибирование ПОЛ защищает фосфолипиды мембран гепатоцитов от окислительной деструкции. Значительно повышается активность ферментов антиперекисной зашиты глутатионпероксидазы и глутатионредуктазы до 54%. Введение оксима пиностробина на фоне токсического повреждения печени снижает содержание в ней ТАГ на 26% и повышает уровень фосфолипидов на 21%, при этом соотношение ФЛ/ТАГ увеличиваются до 0,9. Таким образом, на модели токсического гепатита индуцированного тетрахлорметаном установлен гепатопротективный эффект оксима пиностробина. В основе механизма гепатопротективного эффекта исследуемого соединения лежит способность оксима пиностробина повышать уровень восстановленного глутатиона и индуцировать активность глутатионзависимых ферментов антиперекисной защиты - глутатионпероксидазы и глутатионредуктазы. Другой моделью определения гепатопротекторного действия изучаемого соединения является алкогольный гепатоз, связанный с окислительной деградацией этанола, протекающей в печени при участии алкогольдегидрогеназы и микросомальной монооксигеназной системы. При хроническом алкогольном гепатозе в группе без лечения снижается белок-синтетическая функция печени, о чем свидетельствует снижение концентрации общего белка в сыворотке крови. "Карсил" и оксим пиностробина в дозе 100 мг/кг восстанавливают белок-синтетическую функцию печени. Все остальные биохимические показатели остаются в пределах нормальных значений (табл. 6). Изучение гепатопротекторного действия оксима пиностробина на модели острого тетрахлорметанового гепатита показало, что наилучшим действием в отношении устранения проявлений синдромов цитолиза, холестаза и мезенхимального воспаления обладает оксим пиностробина в дозе 50 мг/кг. Изучение гепатопротекторного действия оксима пиностробина на модели хронического алкогольного гепатоза показало, что оксим пиностробина в дозе 100 мг/кг восстанавливает белок-синтетическую функцию печени. Исследовано влияние оксима пиностробина в сравнении с действием эталонного препарата "Карсил" на метаболизм печени при остром гепатите, вызванном у крыс парацетамолом. В течение 5 дней крысам вводят внутрь оксим пиностробина в дозе 100 мг/кг; препарат "Карсил" - в дозе 100 мг/кг; контрольные животные получают эквиобъемное количество крахмальной слизи. Через сутки после последнего введения препаратов крыс декапитируют под легким эфирным наркозом и определяют в сыворотке крови биохимические параметры (общий белок, АЛТ, ACT, глюкоза, холестерин),рассчитывают коэффициент де Ритиса, относительную массу печени. Процент выживших животных к концу эксперимента составляет: 100% - для интактных животных; 20% - для контрольных животных; 80% - для животных, получающих в качестве лечения препарат сравнения "Карсил"; 67% - для животных, получающих в качестве лечения оксим пиностробина. Таблица 6 Влияние оксима пиностробина на восстановление биохимических показателей основных патологических синдромов поражения печени в сыворотке крови крыс при остром тетрахлорметановом гепатите Из табл. 7 видно, что при остром парацетамоловом гепатите увеличивается относительная масса печени по сравнению с интактными животными. При этом лечебно-профилактическое применение оксима пиностробина, как и препарата сравнения "Карсила", не препятствует росту массы печени. Таблица 7 Влияние оксима пиностробина на относительную массу печени крыс при остром парацетамоловом гепатите Из табл. 8 видно, что при остром парацетамоловом гепатите основные биохимические показатели сыворотки крови крыс остаются в пределах нормы. Из табл. 8 видно, что при остром парацетамоловом гепатите уровень аланинаминотрансферазы увеличивается в 2,3 раза, а коэффициент де Ритиса снижается на 46% по сравнению с интактными животными. При этом лечение препаратом "Карсил" способствует снижению уровня аланинаминотрансферазы на 46% и повышению коэффициента де Ритиса на 57% по сравнению с данным показателем в контрольной группе животных. Лечение оксимом пиностробина способствует снижению уровня аланинаминотрансферазы на 34% и повышению коэффициента де Ритиса на 24% по сравнению с данным показателем в контрольной группе животных. Таблица 8 Влияние оксима пиностробина на биохимические показатели сыворотки крови крыс при остром парацетамоловом гепатите Из табл. 8 видно, что при остром парацетамоловом гепатите уровень аланинаминотрансферазы увеличивается в 2,3 раза, а коэффициент де Ритиса снижается на 46% по сравнению с интактными животными. При этом лечение препаратом "Карсил" способствует снижению уровня аланинаминотрансферазы на 46% и повышению коэффициента де Ритиса на 57% по сравнению с данным показателем в контрольной группе животных. Лечение оксимом пиностробина способствует снижению уровня аланинаминотрансферазы на 34% и повышению коэффициента де Ритиса на 24% по сравнению с данным показателем в контрольной группе животных. Таблица 9 Влияние оксима пиностробина на биохимические маркеры патологии печени в сыворотке крови крыс при остром парацетамоловом гепатите Таким образом, применение оксима пиностробина, также как и препарата сравнения "Карсила",препятствует развитию синдрома цитолиза при остром парацетамоловом гепатите. Преимущества способа получения гепатопротекторного средства на основе пиностробина из почек тополя бальзамического (Populus balsamifera L.) следующие. 1. Доступность растительного сырья почек тополя бальзамического (Populus balsamifera L.) на территории Северного Казахстана, общий эксплуатационный запас почек тополя составляют 400 кг на 2,5 га. 2. Баротермический способ получения гепатопротекторной субстанции оксима пиностробина из почек тополя бальзамического (Populus balsamifera L.) является экологически безопасным, так как исключается применение в процессе производства токсичных растворителей и характеризуется высокой производительностью, значительным сокращением продолжительности процесса и обеспечивает количественный выход действующего вещества пиностробина с выходом 10,3% в расчете на густой экстракт. 3. Субстанция оксима пиностробина не токсична, не вызывает острых токсических реакций при испытании на мышах и крысах и проявляет высокую гепатопротекторную активность в дозе 100 мг/кг веса,а в дозе 50 мг/кг устраняет проявления синдромов цитолиза, холестаза и мезенхимального воспаления. 4. Оксим пиностробина относится к "короткоживущим" препаратам. В организме крыс препарат определяется на протяжении 2 ч независимо от введенной дозы и способа его введения. 5. Оксим пиностробина хорошо проникает преимущественно в васкуляризированные органы (почки, печень, легкие). Абсолютная биодоступность оксима пиностробина составляет 11%. 6. Антиоксидантная активность оксима пиностробина в 20 раз выше по сравнению с пиностроби- 10022691 ном. 7. Оксим пиностробина не оказывает токсического действия на печень, снижает в ней интенсивность липопероксидации, содержание триацилглицеридов на 26% и повышает уровень фосфолипидов на 21%, ингибирует процессы перекисного окисления липидов в гепатоцитах, снижая содержание диеновых конъюгатов на 35%, повышая активность ферментов антиперекисной защиты - глутатионпероксидазы и глутатионредуктазы до 54%. ФОРМУЛА ИЗОБРЕТЕНИЯ Способ получения гепатопротекторного средства на основе пиностробина из почек тополя бальзамического (Populus balsamifera L.), включающий экстракцию растительного сырья, его обработку, отличающийся тем, что экстракцию проводят баротермическим способом при температуре 150-160 С, давлении 1,9 атм, в течение 60 мин, хроматографическим разделением и очисткой густого экстракта при элюировании колонки петролейным эфиром и смесью петролейный эфир-этилацетат 49:1, перекристаллизацией выделенного технического пиностробина с последующим синтезом на его основе оксима пиностробина (субстанция для лекарственной формы).
МПК / Метки
МПК: A61P 1/16, A61K 36/76, B01D 11/02
Метки: populus, balsamifera, пиностробина, тополя, бальзамического, средства, способ, получения, гепатопротекторного, основе, почек
Код ссылки
<a href="https://eas.patents.su/12-22691-sposob-polucheniya-gepatoprotektornogo-sredstva-na-osnove-pinostrobina-iz-pochek-topolya-balzamicheskogo-populus-balsamifera-l.html" rel="bookmark" title="База патентов Евразийского Союза">Способ получения гепатопротекторного средства на основе пиностробина из почек тополя бальзамического (populus balsamifera l.)</a>
Предыдущий патент: Имидазопиридиновые производные, способ их получения и терапевтическое использование
Следующий патент: Почвообрабатывающее орудие
Случайный патент: Пептиды, увеличивающие продукцию бактериоцинов, способы увеличения продукции бактериоцинов и выделенные бактериоцины