Применение высокой дозы фолиевой кислоты при ишемии миокарда
Формула / Реферат
1. Применение высокой дозы фолиевой кислоты, по меньшей мере 200 мг, или эквивалентной дозы производного фолиевой кислоты для ослабления дисфункции миокарда во время ишемии и для улучшения постреперфузионного повреждения.
2. Применение по п.1, где указанная дисфункция миокарда представляет собой уменьшение сократимости миокарда.
3. Применение по п.1, где указанная дисфункция миокарда представляет собой смерть клеток миокарда.
4. Применение по п.1, где указанная дисфункция миокарда представляет собой индуцируемые инфарктом аритмии.
5. Применение высокой дозы фолиевой кислоты, по меньшей мере 200 мг, или эквивалентной дозы производного фолиевой кислоты в качестве раннего лечения во время активной фазы ишемии перед реперфузией.
6. Применение по любому из пп.1-5, где указанная высокая доза составляет по меньшей мере 600 мг.
7. Применение по любому из пп.1-6, где указанную высокую дозу вводят перорально.
8. Применение по любому из пп.1-6, где введение указанной дозы является внутримышечным, внутривенным или чрескожным.
9. Применение фолиевой кислоты в качестве кардиопротекторного или терапевтического агента для улучшения или восстановления пониженного уровня высокоэнергетических фосфатов при сердечно-сосудистых расстройствах с пониженным уровнем АТФ/АДФ.
Текст
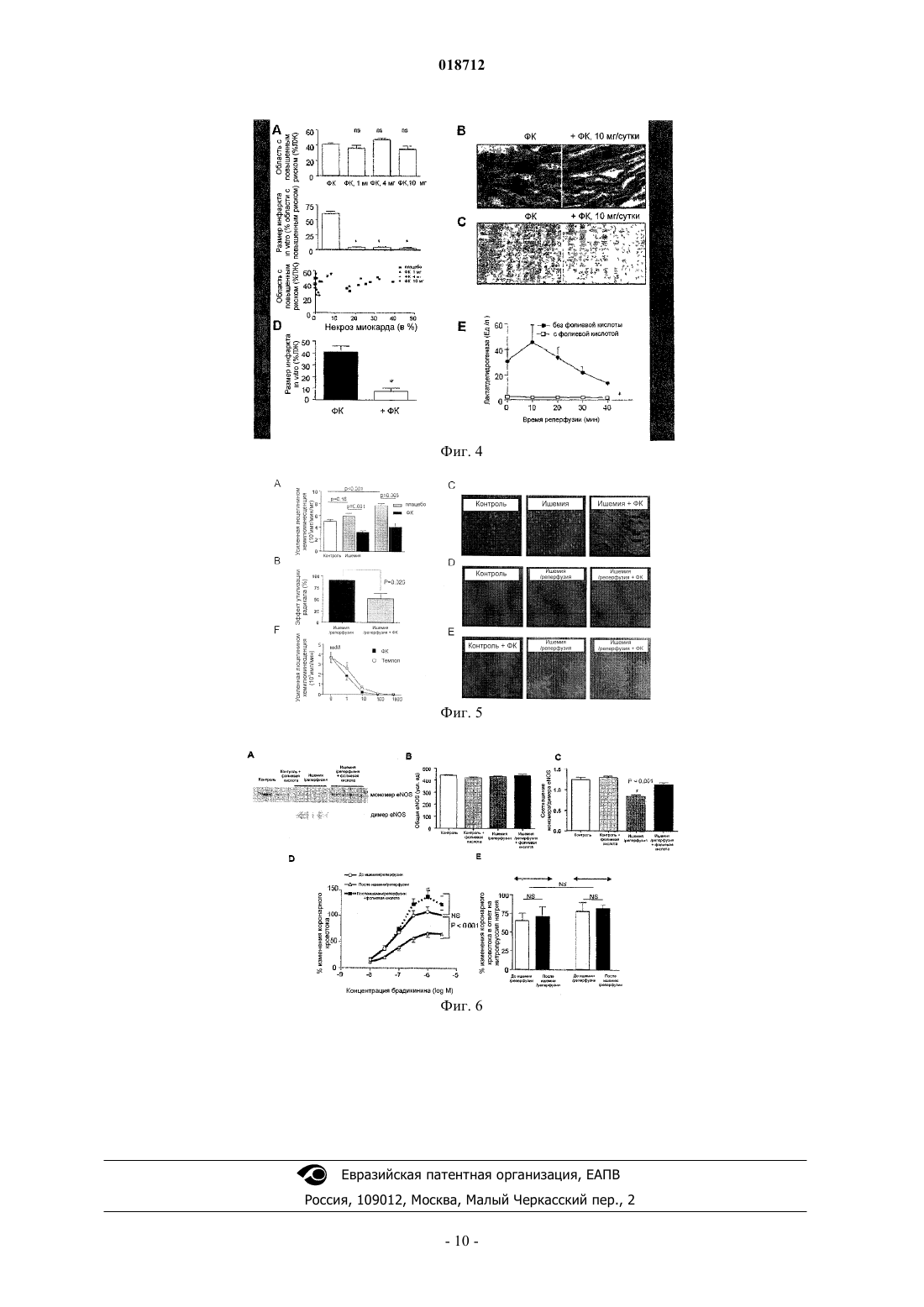
ПРИМЕНЕНИЕ ВЫСОКОЙ ДОЗЫ ФОЛИЕВОЙ КИСЛОТЫ ПРИ ИШЕМИИ МИОКАРДА Изобретение относится к применению высокой дозы фолиевой кислоты или эквивалентной дозы одного из ее биологически активных производных для ослабления дисфункции миокарда во время ишемии для улучшения постреперфузионного повреждения. Изобретение конкретно относится к раннему лечению путем применения высокой дозы, по меньшей мере 200 мг, фолиевой кислоты или эквивалентной дозы производного во время активной фазы ишемии перед реперфузией. Область техники, к которой относится изобретение Настоящее изобретение относится к применению высокой дозы фолиевой кислоты или эквивалентной дозы одного из ее биологически активных производных для ослабления дисфункции миокарда во время ишемии и для улучшения постреперфузионного повреждения. Изобретение конкретно относится к раннему лечению путем применения высокой дозы, по меньшей мере 200 мг, фолиевой кислоты или эквивалентной дозы производного во время активной фазы ишемии перед реперфузией. Предшествующий уровень техники Во время острой коронарной окклюзии перфузия миокарда и доставка кислорода становятся недостаточными для подержания активного мышечного сокращения. В ишемической зоне миокарда содержание высокоэнергетических фосфатов падает, содержание неорганических фосфатов растет и ткань становится ацидозной (Jennings and Steenbergen, 1985), что в результате приводит к региональной дискинезии и к общей дисфункции. Коронарная реперфузия после ишемии ограничивает тканевое повреждение, но дат токсичность из-за активации реактивных форм кислорода (РФК), кальциево-зависимых протеаз,таких как кальпаин, контрактуры миофиламента, микрососудистой дисфункции и цитокинов воспаления(Gross and Gross, 2006). Истощение АТФ во время ишемии также может способствовать реперфузионному повреждению (Gunduz, et al., 2006). Кроме того, считается, что РФК, генерируемые как во время ишемии (Klawitter et al., 2002), так и реперфузии (Zweier and Talukder, 2006), играют центральную роль, и для компенсации этого повреждения тестировались разнообразные антиоксидантные стратегии. Один способ ограничения ишемического/реперфузионного повреждения заключается в том, что сердца подвергаются краткой ишемии перед более продолжительным воздействием, явление, которое называется ишемическое пре-кондиционирование. Оно включает в себя множество механизмов, в том числе активацию протеинкиназы С (Yamamura et al., 2005), стимулирование митохондриальных KATPканалов и повышенный синтез оксида азота (Jones and Bolli, 2006), причем последний играет центральную роль. Размер инфаркта после ишемии-реперфузии больше у eNOS-дефицитных мышей (Jones et al.,1999), чем у мышей, сверхэкспрессирующих eNOS (Jones et al., 2004). Снижение синтеза NO и повышение генерации РФК посредством NOS случаются, когда NOS из-за истощения/окисления теряет функциональную связь с облигатным кофактором тетрагидробиоптерином (ВН 4) (Hevel and Marietta, 1992;Vasquez-Vivar et al., 1998). Потенциальная роль NOS в ишемически-реперфузионном повреждении привела к усилиям по усилению ферментной функции, включая введение BH4 in vitro (Wajima et al., 2006). Гораздо менее дорогостоящей альтернативой может быть фолиевая кислота (ФК), витамин В, важный для нормального синтеза митохондриальных белков и нуклеиновых кислот (Depeint et al., 2006), но который также стабилизирует BH4 путем усиления аффинности его связывания с eNOS (Stroes et al., 2006; Hyndman et al., 2002) и усиливает регенерацию BH4 из окисленного и неактивного BH2. ФК или ее активный метаболит - 5 метилтетрагидрофолат (5-MTHF) - улучшает функцию эндотелия (Verhaar et al., 1998; Shirodaria et al.,2007; Moat et al., 2006). Низкие дозы ФК тестировали у пациентов с заболеваниями сердечно-сосудистой системы, но недавние клинические исследования, проверяющие применимость ФК для снижения хронического сердечно-сосудистого риска, оказались в некоторой степени разочаровывающими (Bazzano et al., 2006) и определенно не окончательными. Действительно, ФК исследовали в клинических испытаниях, особенно для проверки ее потенциала для снижения сердечно-сосудистого риска у пациентов с заболеванием сосудов миокарда. Например, Oster (1981) продемонстрировал, что продолжительное лечение фолиевой кислотой(-10 лет) с дозой гораздо выше, чем обычно используемая (40-80 мг/день), уменьшало возникновение инфаркта миокарда, стенокардии и потребность в нитроглицерине для пациентов с коронарноартериальным заболеванием. Это наблюдение не подтвердилось ни плацебо-контролируемым исследованием, ни изученным механизмом. Другие исследования фокусировались на способности ФК снижать уровень гомоцистеина и обнаружили 3 мкмоль/л снижение гомоцистеина в сыворотке (достигаемое при дозе 0,8 мг/сутки). Несмотря на эти положительные результаты, метаанализы множества испытаний ФК для использования в профилактике сердечно-сосудистых заболеваний не были впечатляющими (JAMA 2002; Wang et al., 2007; Wald et al., 2006) и остается неясным, чем это объясняется: дозой, продолжительностью лечения, целевой популяцией или другими факторами. Дозы, использованные в предыдущих сердечно-сосудистых интервенционных исследованиях (5-25 мг/70 кг/сутки) или в профилактических испытаниях (500 мкг-1 мг), являются низкими по сравнению с дозой по изобретению.WO 0130352 описывает дозу 30-500 мг фолата, предпочтительно 30-100 мг фолата для лечения гипергомоцистеинемии. Хотя гипергомоцистеинемия рассматривается как фактор риска сердечнососудистых заболеваний, механизм того, как высокий уровень гомоцистеина приводит к сердечнососудистым заболеваниям, неизвестен, и заявка не описывает какой-либо эффект на сердечнососудистые заболевания, как таковой, особенно когда пациент не страдает от гипергомоцистеинемии.WO 2006113389 описывает способ улучшения дилятации сосудов, содержащий введение пациенту высокой дозы (20-100 мг) фолиевой кислоты, и заявляет, что суточной дозой 20-100 мг можно избежать или минимизировать развитие отдельного сердечного заболевания. Нет указаний ни на то, что дисфункция миокарда во время ишемии может быть ослаблена, ни на то, что постреперфузионное повреждение-1 018712 может быть смягчено с помощью этого лечения. Сущность изобретения Неожиданно мы обнаружили, что высокая доза ФК (по меньшей мере 200 мг на пациента) предварительного лечения и/или лечения во время ишемии перед реперфузией может улучшить ишемическиреперфузионное повреждение, и исследовали механизм такого эффекта. Данные демонстрируют постреперфузионное благоприятное действие, но, что более поразительно, обнаруживают заметный и неожиданный эффект предварительного лечения с помощью ФК на снижение региональной и полостной дисфункции и на генерацию РФК в период ишемии. Это благоприятное действие, по-видимому, связано с изменениями в пуриновом катаболизме и в сохранении уровня высокоэнергетического фосфата во время ишемии. В данном исследовании мы впервые продемонстрировали, что предварительное лечение высокими дозами перорально вводимой фолиевой кислоты заметно снижает тяжесть ишемической дисфункции во время коронарной окклюзии и усиливает функцию и уменьшает размер инфаркта после реперфузии. Эти эффекты связаны с сохраненными во время ишемии высокоэнергетическими фосфатами, несмотря на ослабление кровотока, с улучшением общей и региональной функции, снижением некроза и окислительного стресса и с сохранением eNOS-сопряжения при реперфузии. Способность предварительного лечения с помощью ФК поддерживать сокращение миокарда, по существу, несмотря на уменьшенный коронарный кровоток, является необычной и достаточно отличной от воздействия антиоксидантов и классических пре-кондиционирующих препаратов. Они, как правило, имеют слабое влияние во время ишемии,но оказывают благоприятное воздействие на сердце после реперфузии. Фактически, благоприятное воздействие ФК на снижение размера инфаркта, даже если ФК вводится после ишемии, наводит на мысль о существовании другого механизма. Первый аспект изобретения представляет собой применение высокой дозы фолиевой кислоты, по меньшей мере 200 мг, предпочтительно по меньшей мере 600 мг, еще более предпочтительно по меньшей мере 1000 мг, или эквивалентной дозы производного фолиевой кислоты для ослабления дисфункции миокарда во время ишемии и/или для улучшения постреперфузионного повреждения. Производные фолиевой кислоты известны специалисту в данной области и включают, в частности, фолат и 5 метилтетрагидрофолат. Дисфункция миокарда при использовании в настоящем документе включает, в частности, уменьшение сократимости миокарда, смерть клеток миокарда и/или индуцированные инфарктом аритмии. Одно предпочтительное воплощение представляет собой применение высокой дозы фолиевой кислоты или эквивалентной дозы производного фолиевой кислоты, где указанная дисфункция миокарда представляет собой уменьшение сократимости миокарда. Другое предпочтительное воплощение представляет собой применение высокой дозы фолиевой кислоты или эквивалентной дозы производного фолиевой кислоты, где указанная дисфункция миокарда представляет собой смерть клеток миокарда. Еще одно предпочтительное воплощение представляет собой применение высокой дозы фолиевой кислоты или эквивалентной дозы производного фолиевой кислоты, где указанная дисфункция миокарда представляет собой индуцированные миокардом аритмии. Предпочтительно высокую дозу вводят в виде однократной дозы. Еще более предпочтительно дозу вводят во время ишемии перед реперфузией. В одном предпочтительном воплощении введение является пероральным введением. В другом предпочтительном воплощении дозу вводят внутривенной инъекцией. Альтернативно, доза может вводиться чрескожно или внутримышечной инъекцией. Другой аспект изобретения представляет собой применение высокой дозы фолиевой кислоты, по меньшей мере 200 мг, предпочтительно по меньшей мере 600 мг, еще более предпочтительно по меньшей мере 1000 мг, или эквивалентной дозы производного фолиевой кислоты в качестве раннего лечения во время активной фазы ишемии перед реперфузией. Раннее лечение при использовании в настоящем документе обозначает, что лечение начинают после начала активной фазы ишемии, но перед реперфузией. Предпочтительно высокую дозу вводят в виде однократной дозы. Еще более предпочтительно дозу вводят во время ишемии перед реперфузией. В одном предпочтительном воплощении введение является пероральным введением. В другом предпочтительном воплощении дозу вводят внутривенной инъекцией. Альтернативно, доза может вводиться чрескожно или внутримышечной инъекцией. Еще один аспект изобретения представляет собой применение фолиевой кислоты или эквивалентной дозы производного фолиевой кислоты в качестве кардиозащитного или терапевтического агента для улучшения или восстановления пониженного уровня высокоэнергетического фосфата при сердечнососудистых расстройствах с понижением АТФ/АДФ-уровней. Предпочтительно указанное применение фолиевой кислоты представляет собой применение высокой дозы. Еще более предпочтительно указанная высокая доза составляет по меньшей мере 200 мг, наиболее предпочтительно по меньшей мере 600 мг. Улучшение при использовании в настоящем документе обозначает, что уровень высокоэнергетического фосфата увеличивается с помощью лечения, не достигая при этом нормального уровня здорового субъекта. Восстановление при использовании в настоящем документе обозначает, что уровень высокоэнергетического фосфата после лечения сравним с уровнем здорового субъекта или превышает его. Краткое описание чертежей Фиг. 1 - сердечная функция, измеренная с помощью анализа петли давление/объем. Фиг. 1 А - при-2 018712 мер петель давление/объем в исходной точке (1), в конце ишемии (2) и после 90 мин реперфузии (3) для животного, получавшего плацебо (выше), и животного, получавшего предварительное лечение ФК (ниже). Предварительное лечение ФК улучшило функцию и во время ишемии и после реперфузии. Фиг. 1 В суммарная гемодинамика для полного протокола ишемии/реперфузии показывает зависимость от времени для систолических и диастолических параметров (p-уровни из повторных измерений ANOVA, время х- взаимодействие при лечении/эффект при лечении). Фиг. 2 - эхокардиография открытой грудной клетки. На верхней левой панели показаны примеры эхокардиографии в М-режиме в исходной точке и через 30 мин ишемии в группе плацебо и в группе ФК. Суммарные кривые демонстрируют результаты, полученные на основании этих эхокардиограмм в зависимости от времени. Фракция выброса и утолщение стенки передне-перегородочной области снижались в группе плацебо, но оставались неизменными в группе ФК (p-уровни для эффекта лечения представлены с помощью RMANOVA). Фиг. 3 - ВЭЖХ-анализ параметров метаболизма высокоэнергетических фосфатов (HEP) и состояния окисления-восстановления. В исходных условиях предварительное лечение ФК не изменяло уровень высокоэнергетических фосфатов (АТФ, АДФ, АМФ), но увеличивало количество инозинмонофосфата(ИМФ) и его катаболитов (оксипуринов: ксантина, гипоксантина и мочевой кислоты). Через 30 мин ишемии уровень высокоэнергетических фосфатов лучше поддерживался в сердцах с предварительным лечением ФК по сравнению с животными, получавшими плацебо. Уровень оксипуринов заметно вырос после ишемии у животных, получавших лечение в виде плацебо, а у крыс, получавших лечение в виде ФК, подобного не наблюдалось. Р-уровни получены на основании двухфакторного анализа ANOVA, с первой величиной, выявляющей эффект ишемии, и второй величиной взаимодействия между группой лечения и ишемией. Фиг. 4 - эффект фолиевой кислоты на некроз миокарда. Фиг. 4 А - пероральное (7 дней) предварительное лечение ФК уменьшало размер инфаркта in vivo (: р 0,001; критерий Манна-Уитни). Верхняя панель: область с повышенным риском (AAR) была сравнима у всех групп. Средняя панель: размер инфаркта, выраженный как % AAR, был значительно меньше в группах ФК. Нижняя панель: графикдиаграмма индивидуальной корреляции между некрозом миокарда и AAR. Фиг. 4 В - предварительное лечение ФК in vivo уменьшает некроз полосы сокращения (р=0,001). Фиг. 4 С - предварительное лечение ФК in vivo уменьшает апоптоз (TUNEL-окрашивание) (р=0,005 и р=0,001). Фиг. 4D - предварительное лечение ФК in vivo уменьшает некроз миокарда на -80% в сердцах, исследованных in vitro (: р 0,0001). Фиг. 4 Е - повышенный уровень лактатдегидрогеназы (ЛДГ) после ишемии-реперфузии достигал максимума через 10-20 мин, тогда как в сердцах, получавших предварительное лечение ФК, было минимальное высвобождение ЛДГ (р 0,001). Фиг. 5 - эффекты лечения ФК на генерацию РФК. Фиг. 5 А - усиленная люцигенином детекция супероксида при предварительном лечении ФК демонстрирует заметное уменьшение индуцированного ишемией и ишемией-реперфузией супероксида. Фиг. 5 В - образование O2- в сердцах с ишемией/реперфузией, получавших лечение в виде контроля-носителя, заметно подавлялось при экстренном введении ВН 4, тогда как оно ослабевало примерно наполовину в экстрактах миокарда, полученных из сердец, предварительно обработанных ФК. В окрашенном Фиг. 5C, D - DHE и фиг. 5 Е - DCF ишемическом миокарде или в миокарде с ишемией-реперфузией обнаруживалась повышенная генерация РФК,которая была, по существу, понижена в сердце, предварительно обработанном ФК. Фиг. 5F - прямые антиоксидантные эффекты ФК по сравнению с Темполом. Супероксид генерировался ксантин/ксантин оксидазой in vitro и измерялся с помощью усиленной люцигенином хемилюминесценцией при варьировании добавляемых концентраций либо ФК, либо темпола. Фиг. 6 - эффект предварительного лечения ФК на NO-каскад. Фиг. 6 А - ДСН-ПААГ гель демонстрирует повышенный уровень eNOS-мономера в миокарде с ишемией/реперфузией, который был уменьшен по отношению к контрольному уровню с помощью предварительного лечения ФК. Фиг. 6 В, С - суммарные денситометрические данные анализа в геле, продемонстрированные на панели А. Предварительное лечение ФК уменьшало соотношение мономер/димер, но не оказывало эффекта на общую экспрессию белка eNOS. Фиг. 6D - брадикинин, вводимый в сердца in vitro перед ишемией/реперфузией и вводимый после ишемии/реперфузии, демонстрировал заметное уменьшение эндотелиально-зависимого ответа кровотока. Последний восстанавливался до нормального ответа при предварительном лечении с помощью ФК. Фиг. 6 Е - лечение ФК не оказывало влияния на ответ кровотока на нитропруссид натрия,подтверждая факт того, что несоответствие, наблюдаемое при лечении брадикинином, имело эндотелийзависимый характер. Сведения, подтверждающие возможность осуществления изобретения Примеры Материалы и методы для примеров. Этический комитет. Эксперименты проводили согласно "Руководству по уходу и использованию лабораторных животных", опубликованному Национальным институтом здравоохранения США (NIH-Публикация,85-23) и одобренному этическими комитетами университета Антверпена и медицинской школы университетаIn vivo-модель ишемии. Взрослые крысы "Wistar" получали ФК (10 мг/сутки, если не указано по-другому) или плацебо с помощью перорального зонда за 7 дней до проведения эксперимента ишемии/реперфузии (IR). Всего использовали 131 крысу, объем выборки, отражающий требование множества анализов, которые не могут быть проведены для каждого животного, но могут быть получены в различных подгруппах общей группы. Животных подвергали анестезии (пентобарбитал 60 мг/кг), интубировали посредством трахеотомии и насыщали кровь кислородом ("Harvard Apparatus", Массачусетс). Отслеживали ЭКГ и поддерживали температуру на уровне 37,5C. Левую переднюю артерию обнажали через 4-5-е межреберье, помещали вокруг нее нить и проводили транзиторное лигирование коронарной артерии в течение 30 мин с 90-минутной реперфузией (n=85) или без нее (n=46). В одной подгруппе реперфузированных животных(n=9) ФК давали через 10 мин после проявления окклюзии левой передней нисходящей коронарной артерии (LAD) (т.е. за 20 мин перед проявлением реперфузии), доставляя ее в виде IV-болюса (внутривенного болюса).In vivo-гемодинамика. Функцию левого желудочка (ЛЖ) оценивали in vivo с помощью петель давления/объема (n=14) и во время ишемии и после реперфузии. Катетер давления/объема "1.4F" (SciSense, Лондон-Онтарио, Канада) продвигали через апикальную часть, расположенную вдоль продольной оси, и присоединяли к стимулятору/анализатору (IOX 1.8.9.19, Emka Tech., Париж). Данные по объему калибровали с использованием метода гипертонического солевого раствора, предполагая увеличение=1. У двух животных было смещение катетера во время ишемии, и их данные по объему не использовали. Движение передней стенки миокарда при открытой грудной клетке также измеряли с использованием "Sequoia-Acuson C256", оборудованном линейным преобразователем с частотой 15 МГц (Sequoia C256 Система Эхокардиографии, Корпорация Acuson, Маунтин Вью, Калифорния), в окологрудной проекции полости левого желудочка, как описано ранее. Оценка окислительно-восстановительного потенциала и энергетического метаболизма. Быстрозамороженные образцы (n=24) из передней стенки (лечение ФК; 30-минутная ишемия, без реперфузии) освобождали от белков и подвергали ВЭЖХ-анализу водорастворимые низкомолекулярные соединения, отражающие тканевой окислительно-восстановительный потенциал и энергетический статус. Высокоэнергетические фосфаты, оксипурины (гипоксантин, ксантин и мочевая кислота), нуклеозиды (инозин и аенозин), малондиальегид и восстановленный и окисленный глутатион измеряли с помощью ВЭЖХ с образованием ионных пар, как описано ранее (Takimoto et al., 2005). Измерения кровотока миокарда. Региональный кровоток миокарда оценивали (n=12) с помощью микросфер с активированным ядром (диаметр 15 мкМ, BioPal, Вустер, Массачусетс), инъецированных в левое предсердие (0,3 мл 2,5106 сфер/мл) в исходной точке и через 5 и 30 мин ишемии (Reinhardt et al., 2001). Общее число импульсов в минуту (имп./мин) нормализовали по массе и результаты на основе ишемической зоны нормализовали по дистанционной области с получением относительного кровотока перед ишемией и во время нее.In vitro IR-модель. Взрослых крыс "Wistar" (n=28) подвергали анестезии (пентобарбитал 60 мг/кг) и сердца быстро оперативно удаляли и монтировали на ретроградную перфузионную систему (Emka, Париж, Франция) с использованием подогретого, насыщенного кислородом забуференного раствора Кребса (Krebs-Henseleit) с постоянным перфузионным давлением (75 мм рт.ст.). Сердцам задавали скорость 300 ударов в минуту,и поддерживали в ненагруженном состоянии. Коронарный кровоток измеряли с помощью осевого ультразвукового потокового зонда (Transonic Systems, Итака, Нью-Йорк, США). После 30-минутного равновесия сосудорасширяющие лекарственные средства (брадикинин и нитропруссид натрия) инфузировали болюсной инъекцией (50 мкл, 10-8-10-5,5 М i.c.) и оценивали ресурс коронарного кровотока при постоянном перфузионном давлении. После обновления исходной точки сердца получали ФК (4,5 10-6 М i.c.) или носитель в течение 30 мин. Затем сердца подвергали 40-минутному исходному коронарному кровотоку с последующей 40-минутной реперфузией. Коронарный экссудат собирали, концентрировали (SartoriusSipan, Лиер, Бельгия) и анализировали на присутствие лактат дегидрогеназы (Vitros 950AT, О. С. D., Берсе, Бельгия). Дилятационные реакции коронарных артерий на те же два агента повторяли после реперфузии. Анализ размера инфаркта и гистология. Анализ размера инфаркта оценивали у 31 крысы с определением области риска (AAR) путем негативного окрашивания голубым Эванса, инъецированным во время коронарной окклюзии, и с последующим окрашиванием с помощью "ТТС" для детектирования некроза миокарда. ЛЖ (свободная стенка + вся перегородка), AAR (негативная по окрашиванию голубым Эванса) и область некроза (ТТС-белая) измеряли с помощью планиметрии (Soft Imaging system GmbH, "Analysis pro" версия 3.00), и оцифрованные изображения подвергали эквивалентному удалению фона, усилению яркости и контрастности для улучшения четкости и резкости. Для исследований in vitro окрашиванию "ТТС" не предшествовало ок-4 018712 рашивание голубым Эванса, поскольку создавали общую ишемию. Некроз полосы сокращения оценивали в in vivo сердцах крыс (n=22), фиксированных в растворе Карнуа, и окрашенных трихромом по Массону. Последовательные соседние области исследовали для всех полных ЛЖ для расчета процента миокарда с присутствием полосы сокращения. Подобные анализы проводили для получения положительных проб по TUNEL (Chemicon Intern, Темекула, Калифорния), также выражая результаты в виде процента области ЛЖ. Определение РФК. Супероксид оценивали с помощью усиленной люцигенином (5 мкМ) хемилюминесценции (Beckman LS6000IC, n=23)22 и флуоресцентной микротопографии (дихлордигидро-флуоресцеин диацетат,DCF, n=16, и дигидроэтидий, DHE, n=24) (Gupte et al., 2005). Прямые антиоксидантные эффекты фолиевой кислоты анализировали с использованием in vitro-системы ксантин/ксантиноксидазы (Antoniades et(n=16) с использованием низкотемпературного ДСН-ПААГ, как описано ранее (Takimoto et al., 2005). Ферментативную активность NOS оценивали с помощью анализа превращения аргинина в цитруллин в экстрактах, полученных из замороженного миокарда (n=15) (Takimoto et al., 2005). Анализ данных. Данные представлены как среднее значениестандартная ошибка среднего с p-уровнями 0,05, которые считаются статистически значимыми. Данные сохранения коронарного кровотока и in vivo данные гемодинамики анализировали с помощью повторных измерений ANOVA. Для других сравнений использовали или однофакторный анализ ANOVA, или критерий Краскела-Уоллиса для сравнения между множеством независимых групп с поправкой Бонферрони для множественных сравнений. В анализе использовали "SPS6" версии 11.0 (Чикаго, Иллинойс). Пример 1. Предварительное лечение фолиевой кислотой улучшает сердечную функцию с ишемией/реперфузией. Фиг. 1 А демонстрирует пример отношения давления к объему и суммарные данные для систолической и диастолической функции желудочка в сердцах с предварительным лечением ФК (10 мг/сутки) или без него. Данные измеряли в исходной точке на открытой грудной клетке крыс во время 30 мин коронарной окклюзии после 90-минутной реперфузии. Контрольные сердца демонстрировали заметно уменьшенную сердечную функцию со смещением вправо вниз петель давления/объема через 30 мин LADокклюзии (окклюзии левой передней нисходящей коронарной артерии), которая сохранялась после реперфузии (верхняя панель). При предварительном лечении ФК систолическая и диастолическая функции лучше сохранялись во время ишемических и реперфузионных периодов (нижняя панель). Суммарные данные (фиг. 1 В) подтверждают эти примеры. Максимальное ЛЖ-давление (т.е. систолическое давление крови) мало изменялось, несмотря на LAD-окклюзию у крыс, получавших предварительное лечение ФК,но падало примерно на 25% в контролях. Аналогичные расхождения наблюдались в dP/dtmax. Минутный объем сердца и систолическая работа также меньше уменьшались у животных, получавших предварительное лечение ФК, конкретно, в поздней стадии ишемии и реперфузии. Таким образом, сердечная функция усиливалась во время периода ишемии и после реперфузии с помощью предварительного лечения ФК. Относительное сохранение общей функции во время ишемии было несколько удивительным и предполагало региональную дисфункцию, несмотря на коронарную окклюзию, в сердцах крыс, получавших предварительное лечение ФК. Чтобы это протестировать, мы провели эхокардиографию на открытой грудной клетке для измерения утолщения стенки и зависимости от времени дисфункции во время 30 мин LAD-окклюзии (фиг. 2). Пример записей в М-режиме (верхняя левая панель) демонстрирует заметное уменьшение утолщения передней стенки во время ишемии в контролях, но сохранение утолщения у животных, получавших предварительное лечение ФК. Фракция выброса была гораздо выше, несмотря на ишемию (72,81,2% против плацебо: 27,42,2%, р 0, 001 через 30 мин), что соответствует результатам анализа петли давления/объем, как было в случае утолщения стенки передне-перегородочной области (375,3% против плацебо 5,10,6%, р=0,004). Таким образом, предварительное лечение ФК улучшало региональную дисфункцию в ишемической зоне, несмотря на коронарную окклюзию, и это состояние сохранялось или еще улучшалось после реперфузии. Пример 2. Фолиевая кислота и кровоток миокарда. Так как предварительное лечение ФК улучшало и региональную и общую функцию во время LADокклюзии, мы тестировали, улучшало ли оно кровоток миокарда для уменьшения ишемического инсульта как такового. Однако через 5 мин LAD-лигирования соотношение ишемической/дистанционной зоны перфузии миокарда, полученное с помощью анализа с использованием микросфер, одинаково уменьшалось и в группе плацебо, и в группе предварительного лечения ФК (-73,76,0% и -77,75,1% соответственно). Кровоток оставался низким в обеих группах в течение 30 мин (-78,49,3% против плацебо-71,213,8% по сравнению с отдаленной областью). Пример 3. Фолиевая кислота сохраняет уровень высокоэнергетических фосфатов миокарда.-5 018712 Так как улучшенная перфузия не могла объяснить эффект лечения ФК, мы далее проверили, изменяла ли ФК метаболизм высокоэнергетических фосфатов (HEP) в исходной точке и конкретно во время ишемии. Как продемонстрировано на фиг. 3, предварительное лечение ФК не изменяло HEP в исходной точке, но повышало уровень инозинмонофосфата (ИМФ) и его катаболитов (оксипуринов: ксантина, гипоксантина, мочевой кислоты). Во время ишемии уровень АТФ и АДФ миокарда уменьшался более чем на 66% в контролях, что соответствует опубликованным изменениям. Однако и АТФ, и АДФ поддерживались на более высоком уровне в сердцах крыс, получавших предварительное лечение ФК (р 0,001 для взаимодействия лечения ФК и ответной реакции ишемии). Уровень оксипуринов заметно вырос во время ишемии в контролях, что соответствует уменьшению HEP и повышению катаболизма АМФ; однако они мало изменялись или уменьшались в сердцах крыс, получавших лечение ФК. Наконец, мы исследовали состояние окисления-восстановления, упорядоченное с помощью малонового диальдегида (маркер перекисного окисления липидов) и относительного соотношения восстановленного/окисленного глутатиона. И то, и другое мало изменялось при предварительном лечении ФК при ишемии миокарда или без нее. Пример 4. Предварительное лечение фолиевой кислотой уменьшает размер инфаркта миокарда. Потенциальное следствие улучшения обеих функций и метаболизма HEP во время ишемии заключается в том, что размер последующего инфаркта уменьшается. Как продемонстрировано на фиг. 4 А,размер инфаркта составил 60,34,1% области риска у животных, получавших плацебо, против 3,81,2% у предварительно получавших ФК (р 0,002). В отдельных исследованиях мы обнаружили это уменьшение размера инфаркта, происходящее при предварительном лечении с помощью 40 и даже 10% целевой дозы ФК (т.е. 1 и 4 мг/сутки). Реперфузионный некроз полосы сокращения наблюдали на протяжении 26,72,6% ЛЖ в сердцах крыс, получавших носитель, но только 4,61,2% в сердцах крыс, получавших ФК (р=0,001, фиг. 4 В). Аналогично, при получении носителя доминировали позитивные по TUNEL миоциты (63,05,8% областей ЛЖ), но не при получении ФК (4,31,3%) (р=0,001, фиг. 4 С). Ишемия инициировала летальную смертельную желудочковую аритмию у 36,7% контрольных крыс (против 8,3%, получавших ФК), в то время как реперфузионная аритмия встречалась у 6,1% контролей и отсутствовала у животных, получавших ФК (р 0,01 для обоих случаев). Так как постреперфузионный размер инфаркта in vivo частично связан с сопряжением функции с коронарной реперфузией, мы также тестировали на изолированных сердцах влияние предварительного получения ФК. ФК заметно уменьшала размер инфаркта (7,72,8% против 41,14,9% соответственно,р 0,0001, фиг. 4D), а уровень лактатдегидрогеназы в коронарном экссудате был меньше (фиг. 4 Е), что согласовывалось с уменьшением некроза клеток. Пример 5. Сравнение предварительного получения фолата с острым введением фолата. В отдельной группе из 9 животных ФК вводили после 10-минутной коронарной окклюзии (10 мг в.в.), времени, в течение которого функциональная реакция проявляла первые отклонения (c.f. фиг. 1, 2). Интересно, что наблюдались аналогичные благоприятные воздействия на уменьшение размера инфаркта относительно AAR (n=5; 3,02,2%, р 0,001 против плацебо), в то время как область AAR сама была аналогична как при получении плацебо (52,45,5%). Гистологию проводили на 4 животных и демонстрировали уменьшение окрашивания по TUNEL (4,31,3% ЛЖ, р 0,0001 против плацебо) и некроза полосы сокращения (5,1 0,7% ЛЖ, р 0,001 против плацебо). Таким образом, эффект ФК на уменьшение инфаркта, по-видимому, не является эффектом классического пре-кондиционирования, поскольку он мог проявляться введением ФК после того, как начиналась ишемия. Пример 6. Предварительное введение фолата уменьшает генерацию РФК. Супероксид в миокарде (хемилюминесценция люцигенина) уменьшался почти на 50% у животных,предварительно получавших ФК, во время ишемии и после 90-минутной реперфузии (фиг. 5 А). Когда экстракты предварительно инкубировали с 100 мкМ ВН 4, генерирование O2- уменьшалось на 90,90,7% в сердцах крыс, получавших носитель, но еще меньше в сердцах крыс, предварительно получавших ФК(52,111,3%, р 0,03, фиг. 5 В). Это предполагает, что антиоксидантный каскад, опосредованный ВН 4 (например, NOS-взаимодействие) или отсутствовал в сердцах крыс, предварительно получавших ФК, или был уже улучшен с помощью ФК-терапии. Эффект ФК на РФК, индуцированные ишемией и индуцированные ишемией/реперфузией, дополнительно исследовали с помощью окислительной флуоресцентной микротопографии. Как срезы миокарда, окрашенные DHE, так и срезы, окрашенные DCF, демонстрировали заметное генерирование РФК в группе плацебо, которое уменьшалось при предварительном получении ФК. Фиг. 5 С-Е демонстрирует изображения примеров, данные значений были получены при n=4 для каждой группы и согласуются с этими примерами. Для тестирования потенциальных прямых антиоксидантных эффектов ФК мы проводили in vitro-анализ с использованием генерирующей O2- системы ксантин/ксантиноксидазы (фиг. 5F). По этому анализу видно, что ФК обладает, по существу, антиоксидантными эффектами, аналогичными тем, что получены с помощью Темпола, миметика супероксиддисмутазы. Пример 7. Предварительное получение фолата улучшает димеризацию и активность eNOS и эндотелиальную функцию. Так как ФК и ее активный метаболит 5-MTHF физически связаны с BH4-опосредованным улучше-6 018712 нием функции NOS, включая уменьшение получаемого NOS супероксида, мы исследовали влияет ли ФК на взаимодействие NOS в сердцах с ишемией/реперфузией. Фиг. 6 А демонстрирует примерный иммуноблот для eNOS с фрагментами мономера (140 кДа) и димера (280 кДа). Общее содержание eNOS (сумма обоих) было одинаковым при различных условиях (фиг. 6 В), однако соотношение димер/мономер уменьшалось в сердцах крыс с ишемией/реперфузией, получавших носитель, что отражает отсутствие взаимодействия NOS (р 0,001, фиг. 6 С), но было близко к нормальному уровню в сердцах крыс, предварительно получавших ФК. Активность NOS, измеренная с помощью превращения аргинин-цитруллин,однако была на пограничном уровне, без значительных улучшений в сердцах крыс, получавших ФК по сравнению с не получавшими ее (р=0,08, не показано). Коронарная эндотелиальная функция также улучшалась с помощью предварительного получения ФК. Брадикинин индуцировал максимальное возрастание 108,39,2% коронарного кровотока в изолированных контрольных сердцах, но только на 67,18,1% после ишемии/реперфузии (р 0,001 фиг. 6D). Коронарный кровоток восстанавливался до контрольного уровня в сердцах крыс, предварительно получавших ФК (122.011.3%), без какого-либо изменения базальной дилятации. Отсутствовали изменения коронарного кровотока между группами в исходной точке (плацебо: 10,20,7 мл/мин, ФК: 11,413,8 мл/мин, р=0,5) или после ишемии (плацебо: 9,80,7 мл/мин и ФК: 8,91,4 мл/мин, р=0,5). В отличие от стимулирования брадикинином нитропруссид натрия одинаково увеличивал коронарный кровоток в контрольных и ишемических условиях (фиг. 6 Е), что подтверждает факт эндотелиальной зависимости предыдущего эффекта. Цитированные публикации.Zweier J.L., Talukder M.A. The role of oxidants and free radicals in reperfusion injury, Cardiovasc Res.,2006, 70:181-190. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Применение высокой дозы фолиевой кислоты, по меньшей мере 200 мг, или эквивалентной дозы производного фолиевой кислоты для ослабления дисфункции миокарда во время ишемии и для улучшения постреперфузионного повреждения. 2. Применение по п.1, где указанная дисфункция миокарда представляет собой уменьшение сократимости миокарда. 3. Применение по п.1, где указанная дисфункция миокарда представляет собой смерть клеток миокарда. 4. Применение по п.1, где указанная дисфункция миокарда представляет собой индуцируемые инфарктом аритмии. 5. Применение высокой дозы фолиевой кислоты, по меньшей мере 200 мг, или эквивалентной дозы производного фолиевой кислоты в качестве раннего лечения во время активной фазы ишемии перед реперфузией. 6. Применение по любому из пп.1-5, где указанная высокая доза составляет по меньшей мере 600 мг. 7. Применение по любому из пп.1-6, где указанную высокую дозу вводят перорально. 8. Применение по любому из пп.1-6, где введение указанной дозы является внутримышечным,внутривенным или чрескожным. 9. Применение фолиевой кислоты в качестве кардиопротекторного или терапевтического агента для улучшения или восстановления пониженного уровня высокоэнергетических фосфатов при сердечнососудистых расстройствах с пониженным уровнем АТФ/АДФ.
МПК / Метки
МПК: A61P 9/00, A61K 31/519
Метки: дозы, фолиевой, высокой, ишемии, миокарда, применение, кислоты
Код ссылки
<a href="https://eas.patents.su/11-18712-primenenie-vysokojj-dozy-folievojj-kisloty-pri-ishemii-miokarda.html" rel="bookmark" title="База патентов Евразийского Союза">Применение высокой дозы фолиевой кислоты при ишемии миокарда</a>