Производные фенотиазина, окрашивающие диспластические ткани in vivo
Формула / Реферат
1. Соединение структурной формулы
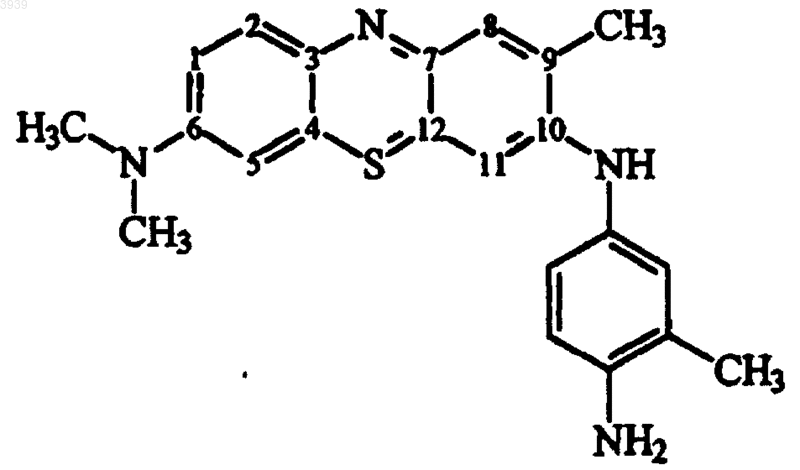
2. Соединение структурной формулы
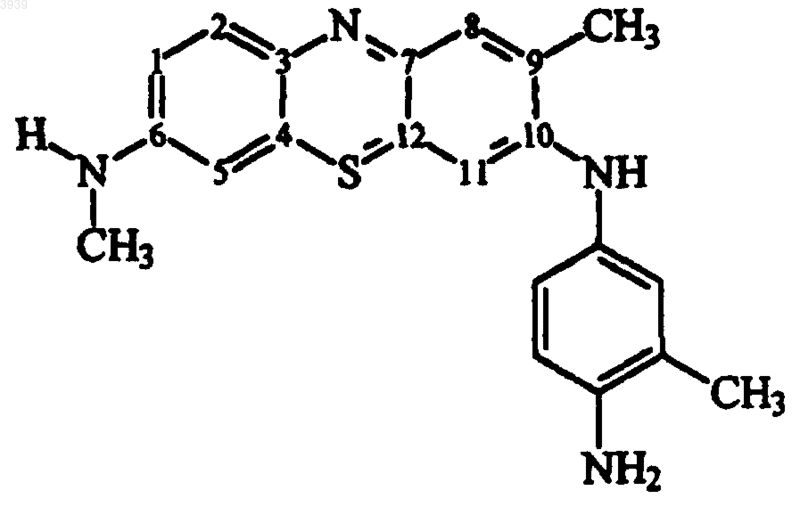
3. Соединение структурной формулы
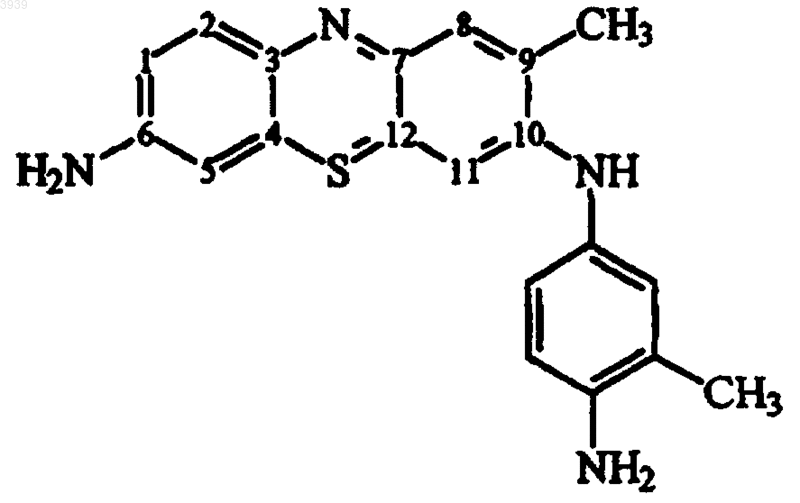
4. Способ обнаружения диспластической ткани, включающий стадию применения к эпителиальной ткани композиции для биологического окрашивания, селективно окрашивающей диспластическую ткань, отличающийся тем, что в указанном способе используют соединение структурной формулы по пп.1-3.
Текст
1 Данное изобретение относится к новым соединениям для биологического окрашивания,полезным для местного применения in vivo человеком. В другом аспекте изобретение относится к способам применения in vivo таких соединений для идентификации ткани с подозрением на дисплазию, т.е. атипичной ткани. Еще в одном аспекте изобретение относится к новым соединениям и их применению при диагностических методах in vivo, специально приспособленным для обнаружения ткани ротовой полости с подозрением на дисплазию, в особенности, раковой и предраковой ткани. Различные варианты воплощения изобретения и их практического применения будут очевидны для специалистов в этой области техники из последующего подробного описания изобретения и прилагаемого чертежа. Чертеж представляет собой схему технологического процесса, изображающую способ синтеза новых соединений настоящего изобретения. Предпосылки создания изобретения Большинство эпителиальных повреждений является результатом травмы. Однако другие повреждения представляют собой диспластические опухоли, из которых некоторые могут быть доброкачественными, но некоторые могут быть или раковыми, или предраковыми. Кроме того,многие диспластические повреждения небольшие по размеру и могут быть просто не замечены врачами при обычном визуальном обследовании, в особенности, повреждения в полостях организма, таких как полость рта. Известен диагностический тест in vivo,идентифицирующий и очерчивающий ткань с подозрением на дисплазию. Такой скринингтест с использованием толуидинового синего О(толонийхлорида) в качестве красителя in vivo,селективно окрашивающего раковую и предраковую ткань, в общих чертах описан в патенте США 4321251, Mashberg и в патенте США 5372801, Tucci et аl. Как только повреждение с подозрением на дисплазию идентифицировано по схеме Mashberg, можно брать систематические биоптаты и подвергать их гистологической проверке, чтобы подтвердить, является ли повреждение злокачественным или предраковым. Наборы для осуществления такого теста, содержащие предварительно приготовленную смесь с красителем и растворы для полоскания в надлежащих количествах и концентрациях, запатентованы Zila, Inc., и доступны коммерчески в ряде стран под товарными знакамиORASCREEN и ORATEST. Краткое описание изобретения В настоящее время автором обнаружены новые соединения, полезные в качестве биологических красителей in vivo для селективного окрашивания и очерчивания диспластической 2 ткани. Такие соединения имеют структурную формулуR представляет собой метил или В качестве иллюстрации такие соединения включают Краткое описание способа получения Соединения изобретения синтезируют способом, подобным (за исключением отмеченного ниже) способу, описанному в патенте США 418055, выданном 30 ноября 1889 г. на имя Dandliker et al. на получение толуидинового синего О ("ТВО"). Синтез Dandliker представляет собой ряд процессов из трех стадий окисления: (1) окисление N,N-диметил-п-фенилендиамина, например бихроматом калия, с образованием 2-амино-5-диметиламинофенилтиосульфоновой кислоты; (2) конденсация тиосульфоновой кислоты с O-толуидином с образованием соответствующей индаминтиосульфоновой кислоты; и (3) замыкание в цикл индаминтиосульфоновой кислоты, например, в присутствии комплексообразователя при температуре кипения в течение примерно 30 мин, с образованием толуидинового синего O. Затем реакционную смесь охлаждают и высаливают продукт реакции комплекс с замкнутым циклом. Очистку комплекса можно осуществить путем повторения операций растворения и осаждения. Способы получения соединений настоящего изобретения отличаются от синтеза Dandliker в том, что комплексообразователь добавляют до третьей стадии окисления, предпочтительно - во время первой стадии окисления, и новые продукты настоящего изобретения извлекают и выделяют из осажденного комплекса методом высокоэффективной жидкостной хроматографии 3 Краткое описание применения продуктов для обнаружения эпителиального рака Новые соединения изобретения используют, согласно протоколу Mashberg, для селективного окрашивания диспластической эпителиальной ткани, за исключением того, что вместо толуидинового синего О используют каждое из указанных соединений. Таким образом, настоящее изобретение также относится к способу обнаружения in vivo диспластической ткани у человека, включающему стадию применения к эпителиальной ткани человека композиции, содержащей один из описанных выше новых продуктов или их смесь. Подробное описание технологических приемов для получения продуктов настоящего изобретения Чертеж представляет собой схему технологического процесса, отображающую способ получения новых соединений настоящего изобретения. Исходное вещество 10 для синтеза представляет собой коммерчески доступный N,Nдиметил-а-фенилендиамин высокой степени чистоты. Получение первой реакционной смеси Водный раствор исходного вещества 10 окисляют (11) предпочтительно при температуре ниже 10 С, в частности при температуре ниже примерно 5 С, путем взаимодействия с подходящим окислителем 12, например бихроматом калия 12, в присутствии кислоты, сульфата алюминия и реагента 13 (который, как предполагается, образует комплекс с промежуточным(и) соединением(ями) и используется на более поздней стадии способа для образования комплекса с компонентами продукта реакции),например хлорида цинка. Затем добавляют источник тиосульфат-ионов 14, например тиосульфат натрия, и получают первую реакционную смесь 15, содержащую первое промежуточное соединение 2-амино-5-диметиламинофенилтиосульфоновую кислоту. Получение второй реакционной смеси Затем первую реакционную смесь 15 вводят в дальнейшее взаимодействие предпочтительно при температуре не выше примерно 10 С, с добавочным окислителем 16, например бихроматом калия, и гидрохлоридом отолуидина 17 на стадии конденсации 18 с образованием во второй реакционной смеси 19 продукта конденсации - второго промежуточного соединения индаминтиосульфоновой кислоты. Получение третьей реакционной смеси Затем вторую реакционную смесь 19 вводят в дальнейшее взаимодействие, предпочтительно добавляя подходящий окислитель 22,например бихромат калия, при температуре не выше примерно 10 С. Затем добавляют сульфат меди, комплексообразователь хлорид цинка,кислоту и смесь греют при 100 С для осуществления замыкания индаминового цикла, причем в 4 третьей реакционной смеси 24 образуется конечный продукт реакции. В указанный момент продукт реакции выделяют из третьей реакционной смеси и очищают. Выделение/очистка продукта третьей реакции Например, в приведенном здесь предпочтительном варианте воплощения способа настоящего изобретения продукт реакции осаждают из третьей реакционной смеси путем образования комплекса 24 с подходящим комплексообразователем 25, например хлоридом цинка,с образованием комплексной двойной соли с хлоридом цинка. Осадок отделяют от жидкой фазы фильтрацией 26 и промывают раствором хлорида натрия 27. Затем промытый остаток на фильтре снова растворяют 28 в критическом(если взять воды слишком много, это препятствует выделению продукта реакции. Если используется слишком мало воды, (1) весь продукт реакции не растворяется, причем снижается выход, и (2) снижается степень чистоты продукта) объеме воды 29 с образованием раствора продукта реакции 30, который затем фильтруют 31 для удаления нерастворившихся твердых веществ 32 а, которые отбрасывают. Затем к фильтрату 32 добавляют хлорид цинка и затем критический (если хлорида натрия используется слишком мало, продукт не будет высаливаться полностью, причем снижается выход. Если хлорида натрия используется слишком много, это будет вызывать осаждение примесей вместе с продуктом реакции, причем снижается степень чистоты продукта) объем/концентрацию хлорида натрия 33, чтобы снова осадить двойную соль хлорида цинка. Двойную соль отделяют от смеси фильтрацией и получают остаток на фильтре 34. Как показано пунктирной линией 34 а, остаток на фильтре 34 можно снова растворять, фильтровать и снова осаждать и выделять многократно до достижения нужной степени чистоты и выхода продукта реакции двойной соли. Затем очищенный остаток на фильтре конечного комплексного продукта 34 растворяют в воде и новые соединения настоящего изобретения выделяют и разделяют методами ВЭЖХ, описанными ниже. Рабочие примеры Приведенные далее примеры представлены для иллюстрации практического осуществления изобретения с той целью, чтобы дать возможность специалистам в этой области техники получить новые соединения изобретения и применить на практике новые диагностические методы с использованием таких новых соединений, что все вместе образует различные варианты воплощения изобретения, и с целью показать специалистам в этой области техники известные в настоящее время наилучшие способы практического использования различных вариантов воплощения изобретения. Данные примеры 5 приводятся только с целью иллюстрации, а не как указывающие пределы объема настоящего изобретения, который определяется только прилагаемой формулой изобретения. Пример 1. Способ получения. Данный пример иллюстрирует необходимые процедуры для получения партии комплекса красителя и выделения новых соединений изобретения из комплексного продукта методом ВЭЖХ. Получение растворов исходных материалов. Оборудование/принадлежности А. Весы IP15KS, Ohaus В. Весы HV150KAI, AnD С. Весы Н 90-5150, FairbanksF. Пробоотборники, такие как стальные совки, цилиндрические пробоотборники и т.п.G. Колбы Эрленмейера, химические стаканы, бутыли и другая соответствующая стеклянная посуда Н. Этикетки для полученных растворов Меры безопасности. При работе с химикатами следует надевать защитные приспособления, такие как перчатки,защитные стекла, спецодежду и респираторы,согласно нормам MSDS. Процедура получения растворов исходных материалов. К соляной кислоте (1346,25,5 г) добавляют 1364,2 г (5,5 г) очищенной по USP воды. Перемешивают до тех пор, пока раствор не станет прозрачным. К гексагидрату сульфата алюминия(1779,17,0 г) добавляют 2548,9 г (10,0 г) очищенной по USP воды. Перемешивают до тех пор, пока раствор не станет прозрачным. К хлориду цинка (7384,630,0 г) добавляют 2786,7 г (11,0 г) очищенной по USP воды. Перемешивают до тех пор, пока раствор не станет прозрачным. К бихромату калия (2101,98,0 г) добавляют 25203,8 г (100 г) очищенной по USP воды. Перемешивают до тех пор, пока раствор не станет прозрачным. К пентагидрату тиосульфата натрия(1526,66,0 г) добавляют 2043,6 г (8,0 г) очищенной по USP воды. Перемешивают до тех пор, пока раствор не станет прозрачным. К пентагидрату сульфата меди (509,72,0 г) добавляют 1613,1 г (6,0 г) очищенной поUSP воды. Перемешивают до тех пор, пока раствор не станет прозрачным. К серной кислоте (600,02,0 г) добавляют 600,0 г (2,0 г) очищенной по USP воды. Перемешивают до тех пор, пока раствор не станет прозрачным. К хлориду натрия (70,4 кг 250 г) добавляют 234,4 кг ( 850 г) очищенной по USP воды. 6 Перемешивают до тех пор, пока раствор не станет прозрачным. Синтез Оборудование для синтеза и принадлежности. Регулятор LFE (3000) Футерованные стеклом резервуары для очистки с кожухами и крышками емкостью 75,7 дм 3 (20 галлонов) (Е 71224) Два футерованных стеклом резервуара для очистки с кожухами и крышками емкостью 378,5 дм 3 (100 галлонов) (Р 1, РТ-001) (Р 2, L13621) Охладитель с рециркуляцией(RC96C032) и охлаждаемый резервуар для хранения емкостью 1892,7 дм 3 (500 галлонов)(Rl, 01960763) (P1, 01960764) (Р 2, 08950727) Три 12-кВт устройства для рециркуляции жидкости в кожухе (Watlow, BLC726C3S 20) Три рециркуляционных насоса (Sta-Rite,JBHD-62S, C48J2EC15) Пальчиковый шланговый насос Masterflex(A94002806) Шланговый насос Masterflex (L95003320) Шланговый насос Cole Parmer (B96002074) Установка нутч-фильтрации (70-2038,43421-1) Две установки фильтрации по Бюхнеру(Z11,624-6, Z10,441-8) Вакуумный насос Siemens (F2BV2) Футерованный стеклом сборный резервуар с крышкой емкостью 227,1 дм 3 (60 галлонов)(9502312538) Регулятор подачи (3-5500) (69705069190) Шесть устройств управления загрузкой (35600) ( 1 69705069191,2 69705069199,3 69705069194,4 69705058829,5 69705058805,6 69705069195) Шесть датчиков расхода( 1 69704295165,2 69704024995,3 69704024994,4 69704025027,5 69612178606,6 69703120990) Четыре диафрагменных насоса (M1) Четыре ограничителя перенапряжения(А 301 Н) ( 2 15557,3 15561,4 15558,5 15559) Четыре воздушных регулятора (CFR10) Четыре электромагнитных клапана (используемых в качестве воздушных регуляторов) Четыре датчика низкого расхода (FS-500) Три электромагнитных клапанаPTFE/F06R113AC Фильтрующие среды, Polypropylene (7211-1) Фильтрующие среды, Whatman, сорт 52 Трубопровод PharMed (-18, -82, -90) рН-Метр; Hanna 9321 (13003675) и Orion 620 (001911) Спектрофотометр 20 (3MU722070) Вакуумная сушильная печь Fisher Scientific(9502-033) Воздушный термостат с принудительной вентиляцией VWR 1370 FM (1370FM) Респиратор против пыли/тумана Мельница Thomas Wiley Laboratory (3375E10) Смеситель Patterson-Kelley (Blendmaster,C416578) Весы TS4KD, OHAUS Весы IP15KS, OHAUS Весы AG 104, Mettler Весы HV150KA1, AnD Весы Н 90-5150, Fairbanks Принтер AS123, OHAUS Принтер AS142, OHAUS Многофункциональный принтер AD-8121 Матричное печатающее устройство iDP 3540, Citizen Установка ВЭЖХ Hewlett Packard (1050) Ультразвуковой очиститель (8892-DTH,QCC9601 005 С) Термограф с термоэлементом типа К (КТх,6292752, 6355146) Колбы Эрленмейера (8, 6, 4, 1 л) Химические стаканы (8, 6 л, 500, 250 мл) Бутыли (4, 10, 50 л) Бочки (208,2 дм 3 (55 галлонов), 378,5 3 дм (100 галлонов Мерные колбы (100 мл) Пластиковая воронка Пастерки с шариками и градуированные пипетки (10, 5 мл) с шариком Мембранные коробки (25, 50 мл) Бумага Weigh Шпатели Упаковочный материал(контейнеры,крышки, этикетки) Растворы исходных материалов Синтез, стадия 1 Синтез 2-амино-5-диметиламинофенилтиосульфоновой кислоты. Проверяют целостность системы подачи воды USP. В реактор загружают взвешенное количество очищенной воды степени чистоты по USP (28000100,0 г) и перемешивают при 19010 об./мин. Добавляют N,N-диметил-1,4-фенилендиамин (5,128 моль, 720,03,0 г). Материал необходимо добавлять в виде порошка (без комков). Перемешивают 105 мин. Добавляют соляную кислоту (6N, 1136,95,0 г). Перемешивают 155 мин. 8 Отбирают образец реакционной смеси приблизительно в 10 мл с использованием пластикового устройства для отбора образцов. Проверяют рН. рН должен составлять 2,8-3,8 при 255 С. Добавляют раствор гексагидрата сульфата алюминия (4328,021,0 г). Перемешивают 105 мин при 27510 об./мин. Добавляют раствор хлорида цинка (3641,518,0 г). Охлаждают до 41 С. Как только температура (PV1) достигнет 41 С, добавляют раствор бихромата калия(6532,432,0 г) в течение 205 мин. После завершения добавления смесь перемешивают 205 мин. Поддерживая температуру на уровне ниже примерно 10 С, добавляют раствор пентагидрата тиосульфата натрия (3570,218,0 г). Раствор перемешивают при 10 С в течение 305 мин. Изменяют установку температуры на 60 С. Когда температура (PV1) достигнет 603,0 С,реакционную смесь перемешивают в течение 53 мин и изменяют установку на регулятореLFE на 10,0. Как только температура достигнет 13,02,0 С, проверяют рН. рН должен составлять 3,14,1 при 255 С. Синтез, стадия 2 Синтез индаминтиосульфоновой кислоты. Взвешивают о-толуидин (604,42,5 г) и охлаждают до 183 С на ледяной бане. К отолуидину постепенно добавляют соляную кислоту (6N, 1230,75,0 г). Удаляют гидрохлорид о-толуидина с ледяной бани и оставляют раствор охлаждаться до 383 С. Добавляют раствор к реакционной смеси и перемешивают смесь 53 мин. Добавляют раствор бихромата калия(6532,432,0 г) в течение 205 мин. После завершения добавления смесь перемешивают 105 мин. Изменяют установку регулятора (SPI) на 60,0. Как только температура реакционной смеси достигнет 60,03,0 С, реакционную смесь перемешивают 255 мин. Будет образовываться осадок, состоящий из зеленого индамина. Синтез, стадия 3 Синтез двойной соли хлорида цинка. Устанавливают регулятор LFE на 7,0. Как только температура реакционной смеси достигнет 10,03,0 С, добавляют раствор бихромата калия (6532,432,0 г) в течение 205 мин. После завершения добавления смесь перемешивают 20 мин. Добавляют раствор бихромата калия(5225,926,0 г) в течение 205 мин. После завершения добавления смесь перемешивают 205 мин. Добавляют раствор хлорида цинка (3641,518,0 г). Перемешивают в течение 205 мин при 35010 об./мин. 9 Добавляют раствор пентагидрата сульфата меди (2122,810,0 г). Перемешивают 155 мин. Изменяют установку регулятора (SPI) на 100,0. Как только температура реакционной смеси достигнет 67,03,0 С, начинают добавлять раствор серной кислоты до рН 2,90,3,добавляя аликвоты (500, 250, 125 мл и т.д.). Реакционную смесь перемешивают 5-10 мин после каждого добавления и проверяют рН. Как только температура реакционной смеси достигнет 100,03,0 С, смесь перемешивают 355 мин. Изменяют установку регулятора (SPI) на 35,0. Как только температура реакционной смеси достигнет 70,03,0 С, изменяют установку регулятора (SPI) на 2,5. Осуществляют охлаждение до 2,5 С за 4 ч и выдерживают при 2,52,0 С в течение 4-18 ч. Очистка, стадия 1 Фильтруют реакционную смесь через подходящую фильтрующую среду (Whatman Grade 52). Когда реактор выгружен, взвешивают 24,0 кг 150,0 г 30% раствора NaCl и добавляют 24,0 кг 150,0 г воды по USP. Закрывают донный клапан реактора и добавляют в реактор 15% раствор NaCl. Кратковременно перемешивают раствор. Когда фильтрация завершена, в установку фильтрации добавляют раствор NaCl для промывания остатка на фильтре. Проверяют состояние футерованного стеклом, снабженного кожухом 378,5-дм 3 резервуара для очистки 1, очищают резервуар и снабжают резервуар крышкой HDPE, мешалкой Caframo, шпинделем, лопастью и термопарой,встроенной в пластиковое углубление для термоэлемента. Проверяют, закрыт ли донный клапан, и заглушают выходное отверстие. Взвешивают 190,01,0 кг воды по USP в контейнере HDPE и перемещают воду в резервуар для очистки 1. Перемешивают смесь при 350 об./мин. Как только промывка остатка на фильтре NaCl завершается, остаток на фильтре при перемешивании загружают в резервуар для очистки 1. Перемешивают смесь 2-4 ч. Устанавливают регулятор LFE резервуара для очистки 1 на 75,0 (SP1). Когда температура смеси (PV1) достигнет 75,03,0 С, переставляют регулятор на 40,0. Перемешивают смесь при 40 С и 350 об./мин в течение 12-36 ч. Отбирают образец (через донный клапан) приблизительно в 50 мл. Отмеряют 1,0 мл образца 1,0-мл пипеткой и разбавляют до 100 мл в мерной 100-мл колбе. Затем отбирают 10,0 мл полученного раствора 10,0-мл пипеткой и разбавляют до 100 мл в мерной 100-мл колбе. Измеряют поглощение полученного образца с использованием Spectronic 20+. Поглощение образца должно составлять 0,220. 10 Очистка, стадия 2 Фильтруют смесь через фильтрующую среду в установке фильтрации. Собирают фильтрат в тарированный контейнер HDPE с крышкой. Снабжают футерованный стеклом, снабженный кожухом 378,5-дм 3 резервуар для очистки 2 крышкой HDPE, мешалкой Caframo,шпинделем, лопастью и термопарой, встроенной в пластиковое углубление для термоэлемента. В чистый контейнер HDPE отвешивают 30% раствор NaCl в количестве, равном объему раствора, зарегистрированному выше, с использованием формулы Отбирают образец фильтрата в 10 мл и проверяют рН. рН должен составлять 3,0-4,0. Перемещают фильтрат в резервуар для очистки 2. Перемешивают раствор при 350 об./мин. Добавляют раствор хлорида цинка (1636,36,5 г). Перемещают раствор NaCl (по массе) в резервуар для очистки 2. Устанавливают регулятор LFE резервуара для очистки 2 на 75,0 (SP1). Когда температура смеси (PV1) достигнет 75,03,0 С, переставляют регулятор на 5,0. Охлаждают смесь до 5 С 6 ч и выдерживают при 5,04,0 С в течение 4-24 ч. Обработкаi. Фильтрация. Фильтруют смесь через затаренную фильтрующую среду (Whatman, сорт 52) в установке фильтрации. Взвешивают 12 кг 50 г 30% раствора хлорида натрия и разбавляют 12 кг 50 г воды по USP. Промывают остаток на фильтре 15% раствором хлорида натрия, добавляя раствор непосредственно в воронку Бюхнера. Когда фильтрация завершается, осторожно извлекают фильтровальную бумагу, содержащую продукт.ii. Сушка. Помещают очищенный комплексный продукт реакции в печь и сушат при 50,03,0 С в течение 51 ч. Извлекают комплексный продукт из печи с принудительной циркуляцией воздуха и помещают в вакуумную печь. Сушат при 45,03,0 С при 282 мм рт.ст. в течение 102 ч.Thomas Wiley Laboratory. Присоединяют чистую емкость к жлобу для выпуска. Заслонка камеры должна быть закрыта и зафиксирована. Закрывают шибер на дне бункера, снимают крышку и загружают высушенный комплекс. Возвращают крышку на место. Включают мельницу и немного открывают шибер. Подают продукт в мельницу достаточно медленно, чтобы мельница не тормозилась или не забивалась. 11 Как только измельчение завершается, осторожно отделяют емкость от жлоба для выпуска.Patterson-Kelly Lab и закрывают крышку. Устанавливают таймер на 155 мин. Процедура ВЭЖХ для выделения и разделения В данном примере описывается процедура ВЭЖХ, подходящая для разделения и выделения новых соединений настоящего изобретения из высушенного, измельченного и перемешанного комплекса, полученного так, как описано выше. А. Приборы и оборудование. 1. Процедуры ВЭЖХ а. Хроматографическая система для ВЭЖХ НР 1100b. Детектор с диодной матрицей НР 1100 с. Четверной насос для ВЭЖХ НР 1100 2. Сбор фракций и очистка а. 10-Канальный сборник фракций ISCOb. Роторный испаритель Bchi, модель R124 с. Патрон Sep-pak, C18, Varian 3. Масс-спектральный анализ а. Масс-спектрометрия с ионизацией электронным ударом (EI-MS) 1. Масс-спектрометр VG аналитическийZAB 2-SE 2. Температура источника 200 С 3. Напряжение 70 эВ 4. Зонд для образца: зонд для твердых веществ 5. Температура зонда 280 Сb. Жидкостная хроматография/масс-спектрометрия (LC-MS) 1. Двойной насос НР 1100 с вакуумным дегазатором 2. Растворитель А - вода:АСN (ацетонитрил) (88:12), об/об, содержит 0,1% TEA 3. Растворитель В - вода:АСN (1:1), об/об,содержит 0,1% TEA 4. Градиент от 0% растворителя В до 30% растворителя В за 18 мин; повышение содержания растворителя В до 100% через 27 мин, выдержка 3 мин 5. Скорость потока 1,5 мл/мин 6. Колонка Water Symmetry C18, колонка 4,6 х 250 мм, 5 мкм 7. Температура колонки 40 С 8. Детектор УФ с переменной длиной волны, 290 нм 9. МС-прибор тройной квадрупольный масс-спектрометр VG Bio-Q 10. Принцип действия - по типу положительной ионизации распылением электроновZAB 2-SE 2. Ввод образца: цезиевая ионная пушка 3. Система данных: аналитическая VH 11250J с PDP 11/73d. Масс-спектрометр с электронным распылением (ESI-MS) 1. Масс-спектрометр VG квадрупольный анализатор Biotech Bio-Q 2. Принцип действия: прямое внедрение отрицательно заряженных ионов 3. Объем вводимой пробы 50-75 мкл 4. Элюент 50% водный ACN, содержащий 0,1% ТФК 5. Скорость потока 10 мкл/мин е. МС с электронным распылением/МС(ESI-MS/MS) 1. Масс-спектрометр тройной квадрупольный анализатор VG Quattro II Bio-Q 2. Газ для столкновений аргон 3. Аликвота образца 50-75 мкл 4. Элюент 50% водный ACN, содержащий 0,1% ТФК 5. Скорость потока 10 мкл/минZAB 2-SE 2. Ввод образца: цезиевая ионная пушка 3. Система данных: аналитическая VH 11250J с PDP 11/73 4. Спектрометрия ядерного магнитного резонанса (ЯМР) а. ЯМР Varian Inova, 400 МГц 5. Рентгеноструктурный анализ монокристаллов а. Нониус CD-4, модель 586, автоматизированный дифрактометр для монокристаллаb. Рентгеновская трубка Сu, тонкая фокусировка (=1,5418) с. Приспособление для фотографии с разупорядоченной ориентацией, Polaroid, модель 573d. Программное обеспечение по сбору данных EXPRESS е. Программное обеспечение по обработке данных MOLEN В. Химикаты, реагенты и эталоны. 1. Химикаты и реагенты а. Ацетонитрил (ACN), чистый для ВЭЖХb. Метанол (МеОН), чистый для ВЭЖХ с. Хлороформ (СНСl3), чистый для ВЭЖХd. Ледяная уксусная кислота (GAA), чистая по требованиям ACS е. Соляная кислота (НСl), чистая по требованиям ACSn. Соляная кислота дейтерированная (DCl) о. Тетрафенилборат натрия, степени чистоты "реактивный" Система 2 начальной препаративной ВЭЖХ для сбора фракций соединений Начальный сбор фракций. Водный разбавитель - получают 0,1 М раствор уксусной кислоты и доводят рН до 6,10,1 с помощью NaOH. Подвижная фаза А - водный разбавитель :ACN = 50:50. Получение образцов. Получают 15 мг/мл раствор высушенного смешанного комплексного продукта реакции в водном разбавителе. Загружают раствор аликвотами по 30-40 мл для разделения в патроны SPE с 10 г C18, промывают приблизительно 20 мл водного разбавителя и затем промывают приблизительно 10 мл воды. Элюируют приблизительно 10 мл 0,01N раствора НСl в МеОН. Выпаривают очищенный образец в роторном испарителе досуха и снова растворяют в водном разбавителе. Хроматографическая система. Систему для ВЭЖХ АР 1100 с подогревателем колонок снабжают колонкой с C18, 7 мкм, 30,0 см 7,8 мм и подходящим УФ-детектором для детекции при 290 нм и диодной матрицей, устанавливают скорость потока в 5,0 мл/мин и температуру колонки 20 С. Используют элюирование с градиентом, указанным ниже. Время, мин 0 15 15,1 25 25,1 Процедура. Аликвоты образца в 900 мкл вводят в хроматографическую систему и собирают пики, представляющие интерес, с использованием многоканального сборника фракций. Как только соберут все фракции, каждую фракцию упаривают на роторном испарителе для удаления большей части ACN, затем концентрируют на патроне SPE с C18, промывают водой и элюируют приблизительно 5 мл 0,01N раствора НСl в МеОН. Испаряют элюат на роторном испарителе досуха и оставляют для дальнейшей очистки. Заключительный сбор фракций. 14 Подвижная фаза А - 0,1% TEA : ACN = 88:12. Подвижная фаза В - 0,1% TEA : ACN = 50:50. Получение образцов. Получают растворы высушенных фракций из начального сбора фракций и разбавляют подвижной фазой А. Хроматографическая система. Систему для ВЭЖХ НР 1100 с подогревателем колонок снабжают колонкой с C18, 7 мкм, 30,0 см 7,8 мм и подходящим УФ-детектором для детекции при 290 нм и диодной матрицей, устанавливают скорость потока в 5,0 мл/мин и температуру колонки 30 С. Используют элюирование с градиентом, указанным ниже. Время, мин 0 8 8,1 9 16 16,1 Процедура. Аликвоты образца в 200 мкл вводят в хроматографическую систему и собирают пики, представляющие интерес, с использованием многоканального сборника фракций. Как только соберут все фракции, каждую фракцию сначала упаривают на роторном испарителе для удаления большей части ACN, затем концентрируют на патроне SРЕ с C18, промывают водой и элюируют приблизительно 5 мл 0,01N раствора НСl в МеОН. Затем фракции высушивают досуха в потоке сухого азота и оставляют для осуществления анализов для идентификации. Характеристика соединения IV Отделение и выделение. Соединение IV выделяют с использованием метода полупрепаративной ВЭЖХ. Фракцию собирают, удаляют большую часть ACN на роторном испарителе, и затем концентрируют с использованием патрона SPE с C18, промывают водой и элюируют приблизительно 5 мл 0,01N раствора НСl в МеОН. Затем фракцию высушивают досуха в потоке сухого азота. Часть вещества повторно растворяют в подвижной фазе и вносят в систему ВЭЖХ для определения чистоты фракции. Инжекция соединения IV показывает чистоту примерно 95%, и методом ЯМР проверяют 8,2 мг. Масс-спектральный анализ. Предварительные данные масс-спектрального анализа методом LC-MS измельченного смешанного комплексного продукта реакции показывают, что молекулярная масса соединения IV составляет приблизительно 375,3 m/z. Дальнейшие исследования методом HR-MS с использованием фракций, собранных при LS 15MS, показывают для соединения IV массу 375,1655 m/z и молекулярную формулуC22H23N4S1. Осколки исходного иона в 375 m/z соединения IV проверяют с использованием положительной ESI-MS/MS. Картина фрагментации показывает преимущественные потери 16 и 4 ат.ед.массы из молекулярного иона соединения IV, отражая строение соединения IV. Данное соединение и его N- и N,N-диметилированные производные соединения V и VI образуются при вторичном взаимодействии исходного соединения (ТВО) и избытка исходного вещества O-толуидина. Характеристика соединения I Отделение и выделение. Соединение I выделяют с использованием метода полупрепаративной ВЭЖХ. Фракцию собирают, удаляют большую часть ACN на роторном испарителе и затем фракцию концентрируют с использованием патрона SРЕ с C18,промывают водой и элюируют приблизительно 5 мл 0,01N раствора НСl в МеОН. Затем фракцию высушивают досуха в потоке сухого азота. Часть вещества повторно растворяют в подвижной фазе и вносят в систему ВЭЖХ для определения чистоты фракции. Инжекция соединения I показывает чистоту примерно 95%, и методом ЯМР проверяют 18,9 мг. Масс-спектральный анализ. Предварительные данные масс-спектрального анализа методом LC-MS высушенного смешанного комплексного продукта реакции показывают, что молекулярная масса соединения I составляет приблизительно 284,1223 m/z и молекулярную формулу для соединения IC16H18N3S1. Осколки исходного иона в 284 m/z соединения I проверяют с использованием положительнойESI-MS/MS. Предполагаемая структура и картина фрагментации, показывающая преимущественные потери 16, 30 и 59 ат.ед.массы из молекулярного иона, дают строение соединения I. Соединение I и его N- и N,Nдиметилированные производные соединения II и III образуются при свободно-радикальном захвате метильной группы из другой диметилированной молекулы соответствующим исходным изомером ТВО. Соединения II, III, V и VI выделяют и характеризуют с помощью процедур, описанных выше для выделения и характеристики соединений VI и I. Пример 2. Протокол клинических испытаний. Получение растворов для клинических испытаний. Данный пример иллюстрирует применение каждого из продуктов примера 1 при идентификации дисплазии полости рта. Соединение I, малиновую отдушку (IFFRaspberry IC563457), буферное вещество тригидрат ацетата натрия и консервант H2O2 (30%,USP) (см. патент США 5372801) растворяют в 16 очищенной воде (USP), ледяной уксусной кислоте и этиловом спирте SD 18 и получают испытываемый раствор состава, указанного в табл. А. Таблица А Компонент Масса, % Соединение I 1,00 Отдушка 0,20 Буферное вещество 2,45 Консервант 0,41 Уксусная кислота 4,61 Этиловый спирт 7,48 Вода 83,85 100,00 Приготавливают растворы для предварительного полоскания перед испытанием и последующего полоскания, содержащие 1 мас.% уксусной кислоты в очищенной воде, консервант бензоат натрия и малиновую отдушку. Клинический протокол. Пациенту надевают нагрудник, чтобы защитить одежду. Ожидается отплевывание, поэтому пациенту дают 300-мл (10 унций) чашку,которую затем можно положить в емкость для инфицированных отходов или содержимое которой можно вылить непосредственно в сливное отверстие раковины, чтобы избежать окрашивания раковины. Поверхности вокруг участка испытаний или предметы, которые могут окраситься, закрывают или удаляют. Проводят визуальное обследование полости рта на рак без применения каких-либо инструментов, которые могут поцарапать или порезать мягкие ткани. Перед окрашиванием отмечают внешний вид мягких тканей и зубов. Пациент полощет полость рта приблизительно 15 мл раствора для предварительного полоскания в течение приблизительно 20 с и сплевывает, чтобы удалить избыток слюны и обеспечить сообразную среду полости рта. Затем эту стадию повторяют с новой порцией раствора для предварительного полоскания. Затем пациент промывает и полощет горло водой в течение 20 с и сплевывает. Затем пациент промывает и полощет горло 30 мл испытываемого раствора в течение 1 мин и сплевывает. Затем пациент полощет рот 15 мл раствора для постполоскания в течение 20 с и сплевывает. Затем эта стадия повторяется. Затем проводят обследование полости рта,используя соответствующие методы обследования мягких тканей, включая ретракцию, равномерное освещение и, при необходимости, увеличение. Оценивают и регистрируют расположение, размер, морфологию, цвет и характеристики поверхности подозрительных повреждений, сохранивших синюю окраску. Для того чтобы уменьшить число ложных положительных оценок, пациента через 10-14 дней приглашают на повторное обследование по вышеописанному протоколу. Такой срок дает время для заживления любого язвенного или травматического повреждения или раздражения в период первого обследования. Положительное окрашивание после второго обследования подозрительного участка, выявленного при первом обследовании, рассматривают как указание на раковую или предраковую ткань, и проводят биопсию для подтверждения такого заключения. Ранние эритропластические повреждения окрашиваются в синий цвет, часто в виде штрихов или пятен. Однако естественно для красителя сохраняться в неправильных папиллярных бороздках на тыльной поверхности языка, что не является положительным показанием. К другим участкам, где остается синий краситель, но которые не рассматриваются как положительные, относятся зубной налет, дсенные края каждого зуба, мягкое нбо, окрашенное за счет диффузии вследствие переноса красителя с оставшейся окрашенной тыльной стороны языка,и язвенные повреждения, которые легко различаются. Во всех случаях, когда повреждение является весьма подозрительным, но не окрашивается при данном испытании, тем не менее,проведение биопсии является обязательным. Примеры 3-7. Повторяют процедуры, описанные выше,за исключением того, что вместо соединения I используют соединения II, III, IV, V и VI. Получают схожие результаты. На основании описания изобретения с целью предоставления возможности специалистам в данной области техники понять его и применить на практике, и при наличии идентифицированных и предпочтительных вариантов его воплощения, автор предоставляет формулу изобретения. 4. Способ обнаружения диспластической ткани, включающий стадию применения к эпителиальной ткани композиции для биологического окрашивания, селективно окрашивающей диспластическую ткань, отличающийся тем, что в указанном способе используют соединение структурной формулы по пп.1-3.
МПК / Метки
МПК: C07D 279/36, A61K 31/5415
Метки: ткани, фенотиазина, производные, окрашивающие, диспластические
Код ссылки
<a href="https://eas.patents.su/10-3939-proizvodnye-fenotiazina-okrashivayushhie-displasticheskie-tkani-in-vivo.html" rel="bookmark" title="База патентов Евразийского Союза">Производные фенотиазина, окрашивающие диспластические ткани in vivo</a>
Предыдущий патент: Способ получения гидразингидрата
Следующий патент: Усеченный по амино-концу хемокин rantes и способы его использования
Случайный патент: Жидкость для обработки ствола скважины, способ модифицирования поверхности порошкообразного твёрдого материала и твердые частицы












