Усовершенствованный способ получения невирапина
Номер патента: 7497
Опубликовано: 27.10.2006
Авторы: Ло Юн С., Гаптон Бернард Франклин, Босуэлл Роберт Ф.Джр.
Формула / Реферат
1. Способ получения невирапина, заключающийся в том, что
(а) подвергают взаимодействию 2-гало-3-пиридинкарбонитрил формулы
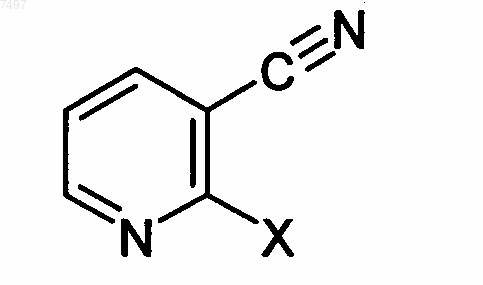
где X обозначает атом фтора, хлора, брома или йода, предпочтительно хлора или брома, с циклопропиламином с получением 2-(циклопропиламино)-3-пиридинкарбонитрила;
(б) гидролизуют 2-(циклопропиламино)-3-пиридинкарбонитрил с получением 2-(циклопропиламино)-3-пиридинкарбоновой кислоты;
(в) выделяют 2-(циклопропиламино)-3-пиридинкарбоновую кислоту из реакционной среды;
(г) обрабатывают 2-(циклопропиламино)-3-пиридинкарбоновую кислоту хлорирующим агентом с получением 2-(циклопропиламино)-3-пиридинкарбонилхлорида;
(д) подвергают взаимодействию 2-(циклопропиламино)-3-пиридинкарбонилхлорид с 2-гало-4-метил-3-пиридинамином формулы
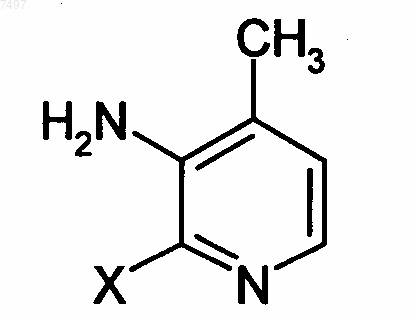
где X обозначает атом фтора, хлора, брома или йода, предпочтительно хлора или брома с получением N-(2-гало-4-метил-3-пиридинил)-2-(циклопропиламино)-3-пиридинкарбоксамида формулы
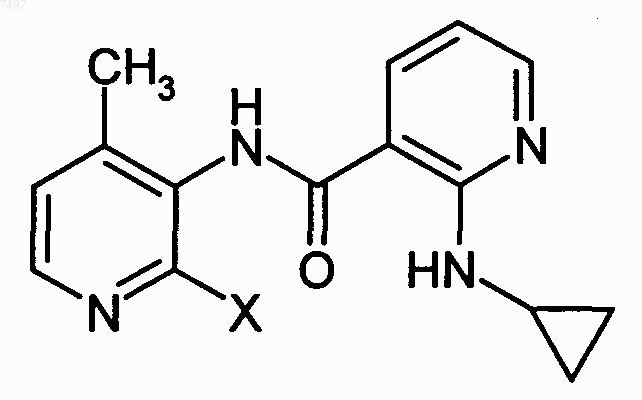
где X обозначает атом фтора, хлора, брома или йода, предпочтительно хлора или брома; и
(е) циклизуют N-(2-гало-4-метил-3-пиридинил)-2-(циклопропиламино)-3-пиридинкарбоксамид путем обработки сильным основанием с получением невирапина.
2. 2-(Циклопропиламино)-3-пиридинкарбоновая кислота.
3. 2-(Циклопропиламино)-3-пиридинкарбонилхлорид.
4. Способ получения 2-(циклопропиламино)-3-пиридинкарбоновой кислоты, заключающийся в том, что
(а) подвергают взаимодействию 2-гало-3-пиридинкарбонитрил формулы
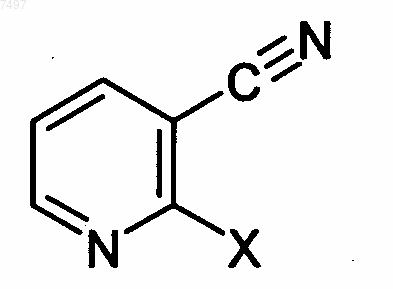
где X обозначает атом фтора, хлора, брома или йода, предпочтительно хлора или брома, с циклопропиламином с получением 2-(циклопропиламино)-3-пиридинкарбонитрила; и
(б) гидролизуют 2-(циклопропиламино)-3-пиридинкарбонитрил с получением 2-(циклопропиламино)-3-пиридинкарбоновой кислоты.
5. Способ получения N-(2-гало-4-метил-3-пиридинил)-2-(циклопропиламино)-3-пиридинкарбоксамида формулы
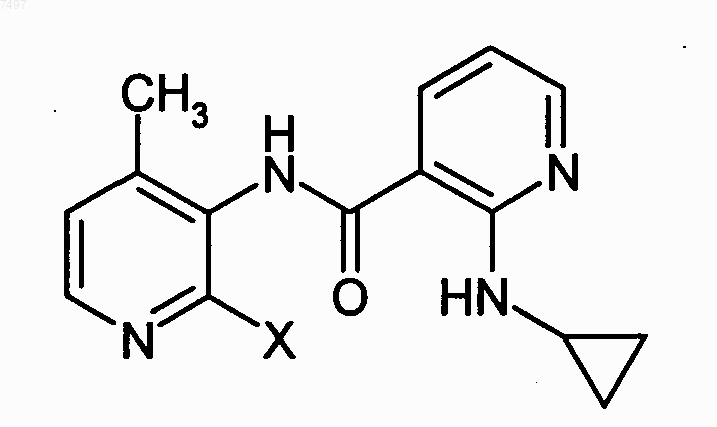
где X обозначает атом фтора, хлора, брома или йода, предпочтительно хлора или брома, заключающийся в том, что
(а) обрабатывают 2-(циклопропиламино)-3-пиридинкарбоновую кислоту хлорирующим агентом с получением 2-(циклопропиламино)-3-пиридинкарбонилхлорида; и
(б) подвергают взаимодействию 2-(циклопропиламино)-3-пиридинкарбонилхлорид с 2-гало-4-метил-3-пиридинамином формулы
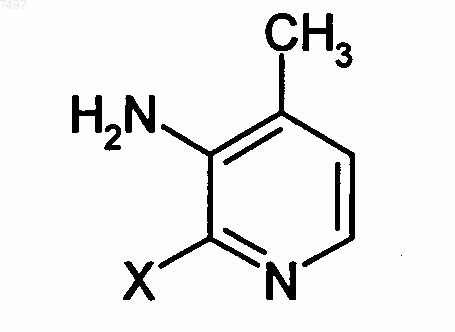
где X обозначает атом фтора, хлора, брома или йода, предпочтительно хлора или брома с получением N-(2-гало-4-метил-3-пиридинил)-2-(циклопропиламино)-3-пиридинкарбоксамида.
6. Способ получения N-(2-гало-4-метил-3-пиридинил)-2-(циклопропиламино)-3-пиридинкарбоксамида, заключающийся в том, что подвергают взаимодействию 2-(циклопропиламино)-3-пиридинкарбонилхлорид с 2-гало-4-метил-3-пиридинамином формулы
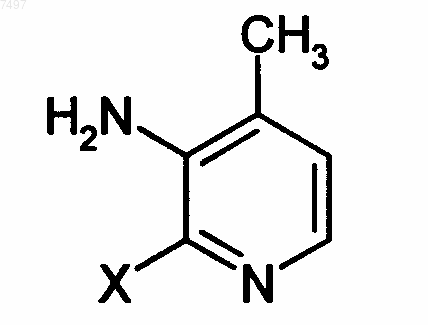
где X обозначает атом фтора, хлора, брома или йода, предпочтительно хлора или брома.
Текст
007497 Предпосылки создания изобретения 1. Область техники, к которой относится изобретение. Изобретение относится к усовершенствованному способу получения невирапина и определенным новым промежуточным продуктам, которые получают при осуществлении усовершенствованного способа. 2. Предпосылки создания изобретения. Невирапин представляет собой ненуклеозидный ингибитор обратной транскриптазы ВИЧ, который можно применять при лечении ВИЧ-инфекции у человека. Химическое название невирапина - 11 циклопропил-5,11-дигидро-4-метил-6 Н-дипиридо[3,2-b:2',3'-е][1,4]диазепин-6-он. Он имеет следующую структурную формулу: Впервые синтез невирапина был описан Hargrave и др. в US 5366972. Использованный метод синтеза изображен на представленной ниже реакционной схеме 1. Схема 1 Согласно методу, разработанному Hargrave с соавторами, 2-хлорникотиноилхлорид получают путем взаимодействия 2-хлорникотиновой кислоты с тионилхлоридом. Затем, как проиллюстрировано на схеме 1, путем взаимодействия 2-хлорникотиноилхлорида с 2-хлор-4-метил-3-пиридинамином получают 2-хлор-N-(2-хлор-4-метил-3-пиридинил)-3-пиридинкарбоксамид. Его подвергают взаимодействию с циклопропиламином, получая N-(2-хлор-4-метил-3-пиридинил)-2-(циклопропиламино)-3-пиридинкарбоксамид. Конечная стадия, на которой получают невирапин, представляет собой реакцию циклизации,которую осуществляют путем обработки последнего промежуточного продукта гидридом натрия. В настоящее время для промышленного производства невирапина используют указанный выше усовершенствованный процесс, который описан Schneider и др. в US 5569760. В этом усовершенствованном варианте синтеза взаимодействие 2-хлор-N-(2-хлор-4-метил-3-пиридинил)-3-пиридинкарбоксамида с циклопропиламином осуществляют в присутствии нейтрализующего агента, представляющего собой оксид или гидроксид элемента второй основной группы или второй подгруппы Периодической таблицы. Предпочтительно применять в качестве нейтрализующего агента оксид или гидроксид щелочно-земельного металла или цинка, причем особенно предпочтительным является оксид кальция. Хотя в настоящее время наиболее широко применяют метод синтеза, описанный в US 5366972, он имеет определенные существенные недостатки. Во-первых, поскольку взаимодействие циклопропиламина с 2-хлор-N-(2-хлор-4-метил-3-пиридинил)-3-пиридинкарбоксамидом осуществляют при повышенной температуре (от 130 до 150 С) и поскольку циклопропиламин является очень летучим, эту реакцию не-1 007497 обходимо проводить в аппарате высокого давления. Во-вторых, 2-хлор-N-(2-хлор-4-метил-3-пиридинил)3-пиридинкарбоксамид становится термически нестабильным при температуре свыше примерно 145 С и,если позволить температуре реакционной смеси подняться выше указанной температуры, возникает риск взрыва. Поэтому целесообразно тщательно контролировать температуру реакционной смеси так, чтобы она оставалась ниже 145 С до тех пор, пока не прореагирует практически весь указанный продукт. Осуществление такого строгого контроля температуры реакционной смеси в целом является трудным и в данном случае оно еще более затруднено вследствие того, что сама реакция является экзотермической. В-третьих, нейтрализующий агент необходимо удалять фильтрацией. Наконец, вследствие образования побочных продуктов общий выход при таком синтезе составляет лишь примерно 25%. Таким образом, существует необходимость в разработке улучшенного способа синтеза невирапина. Краткое описание изобретения В настоящем изобретении предложен способ синтеза невирапина, который является более безопасным, более производительным и более экономичным по сравнению с любым из известных в настоящее время методов. Подробное описание изобретения Усовершенствованный способ синтеза невирапина, предлагаемый в настоящем изобретении, проиллюстрирован на приведенной ниже реакционной схеме 2. На первой стадии реакции 2-гало-3-пиридинкарбонитрил (1) формулы где X обозначает атом фтора, хлора, брома или йода, предпочтительно хлора или брома, подвергают взаимодействию с циклопропиламином (2), получая 2-(циклопропиламино)-3-пиридинкарбонитрил (3). Эту реакцию осуществляют в инертном органическом растворителе, содержащем или не содержащем-2 007497 воду, при повышенной температуре. Пригодными органическими растворителями являются C1-С 6 спирты с прямой или разветвленной цепью, тетрагидрофуран, диметилформамид, диглим, толуол и т.п. Предпочтительными растворителями являются этанол и 1-пропанол, содержащие или не содержащие воду. В качестве акцептора кислоты необязательно можно добавлять органическое или неорганическое основание, такое как триэтиламин, диизопропилэтиламин, фосфат калия, карбонат натрия, карбонат калия и т.п. Реакцию можно осуществлять при температуре от температуры окружающей среды до температуры дефлегмации, но предпочтительно при температуре от 77 до 100 С. Затем 2-(циклопропиламино)-3-пиридинкарбонитрил гидролизуют, получая 2-(циклопропиламино)3-пиридинкарбоновую кислоту (4), которая присутствует в основном в виде цвиттериона при выделении с помощью описанных процессов, которые представлены на схеме 2. Выделение нитрила перед осуществлением гидролиза является необязательным. Гидролиз нитрила с образованием карбоновой кислоты можно осуществлять стандартным методом с использованием раствора сильной кислоты или сильного основания. Гидролиз предпочтительно осуществляют с использованием водной смеси перекиси водорода и сильного основания, такого как гидроксид натрия или калия, или водной смеси сильного основания,такого как гидроксид натрия или калия, и спирта, содержащего 1-6 атомов углерода. Наиболее предпочтительно гидролиз осуществляют с использованием водного раствора 1-пропанола и гидроксида калия. При нагреве до температуры дефлегмации скорость гидролиза повышается. Затем из реакционной смеси выделяют 2-(циклопропиламино)-3-пиридинкарбоновую кислоту. Это,как правило, осуществляют путем доведения значения рН до изоэлектрической точки, которая соответствует примерно рН 6. В результате образуется продукт, представляющий собой цвиттерион, который осаждается, и который затем отделяют фильтрацией и сушат. Если для осуществления гидролиза применяют водный спирт и основание, то сначала путем дистилляции удаляют спирт. Затем 2-(циклопропиламино)-3-пиридинкарбоновую кислоту обрабатывают хлорирующим агентом,получая 2-(циклопропиламино)-3-пиридинкарбонилхлорид (5). Пригодными хлорирующими агентами являются, например, тионилхлорид, оксихлорид фосфора, трихлорид фосфора, пентахлорид фосфора,фосген и оксалилхлорид. Хлорирование осуществляют методом, известным специалистам в области органического синтеза. Как правило, предпочтительно осуществляют кипячение с обратным холодильником карбоновой кислоты (4) с хлорирующим агентом, который применяют либо в чистом виде, либо в растворе в пригодном апротонном растворителе, таком, например, как толуол, ацетонитрил, тетрагидрофуран или т.п. Предпочтительно хлорирование осуществляют при кипячении с обратным холодильником с использованием чистого тионилхлорида, любой избыток которого позднее можно легко удалять путем выпаривания. Поскольку большинство хлорирующих агентов приводят к получению соляной кислоты,продукт (5) на этой стадии реакции на схеме 2 представлен в виде гидрохлорида. Затем 2-(циклопропиламино)-3-пиридинкарбонилхлорид (5) подвергают взаимодействию с 2-гало 4-метил-3-пиридинамином (6) формулы где X обозначает атом фтора, хлора, брома или йода, предпочтительно хлора или брома. Наиболее предпочтительным реактантом является 2-хлор-4-метил-3-пиридинамин. В результате получают N-(2-гало-4 метил-3-пиридинил)-2-(циклопропиламино)-3-пиридинкарбоксамид (7), где X обозначает атом фтора,хлора, брома или йода, предпочтительно хлора или брома. Важно, прежде всего, удалять любой оставшийся хлорирующий агент, поскольку он может взаимодействовать с пиридинамином. Если обладающий высокой летучестью хлорирующий агент, такой как тионилхлорид, применяют в чистом виде, его можно удалять путем выпаривания, получая в качестве остатка хлорангидрид (5) в виде твердого вещества. Если хлорирование осуществляют в растворителе, то предпочтительно применять растворитель с высокой температурой кипения так, чтобы хлорирующий агент можно было удалять выпариванием, сохраняя хлорангидрид в растворенном виде в растворителе. В любом случае хлорангидрид (5) следует поддерживать в безводных условиях. Хлорангидрид (5) и пиридинамин (6) подвергают взаимодействию путем растворения в пригодном безводном растворителе, таком, например, как ацетонитрил, тетрагидрофуран, диглим, диметилформамид, диоксан, метиленхлорид или толуол. К реакционной смеси необязательно можно добавлять в качестве акцептора кислотыоснование либо органическое, либо неорганическое, такое как триэтиламин, диизопропилэтиламин, фосфат калия, вторичный кислый фосфат калия,карбонат натрия, гидроксид натрия, гидроксид калия или т.п. Скорость реакции можно повышать путем нагрева вплоть до температуры кипения растворителя. Наконец, карбоксамид (7) циклизуют, получая невирапин. Циклизацию индуцируют путем обработки карбоксамида (7) сильным основанием, таким как гидрид натрия (NaH) или гексаметилдисилазан натрия (NaHMDS) в инертном безводном органическом растворителе, таком как диглим, толуол или тетрагидрофуран, при температуре от -30 до 130 С.-3 007497 Синтез промежуточного продукта 2-(циклопропиламино)-3-пиридинкарбонитрила путем взаимодействия 2-хлор-3-пиридинкарбонитрила с циклопропиламином описан у G. E. Hardtmann и др., J. Med.Chem. 17, 1974, с. 636. Промежуточные продукты 2-(циклопропиламино)-3-пиридин карбоновая кислота (4) и 2(циклопропиламино)-3-пиридинкарбонилхлорид (5) являются новыми и они являются объектами изобретения. Предпочтительно в качестве исходного продукта (1) используют 2-хлор-3-пиридинкарбонитрил,поскольку метод синтеза этого соединения является известным и оно поступает в продажу. Аналогичным методом можно легко синтезировать другие 2-гало-3-пиридинкарбонитрилы. Циклопропиламин, представляющий собой исходный продукт (2), также поступает в продажу. В качестве реагента (6) предпочтительно применять 2-хлор-4-метил-3-пиридинамин, поскольку синтез этого соединения описан в патентах US 6399781, 5686618, 5668287, 5654429 и 5200522. Аналогичным методом можно легко синтезировать другие 2-гало-4-метил-3-пиридинамины. В приведенных ниже примерах более подробно проиллюстрировано получение невирапина с помощью усовершенствованного способа, предлагаемого в настоящем изобретении. Хотя каждую стадию последовательности реакций можно осуществлять, выделяя сначала продукт, получаемый на предыдущей стадии, некоторые из стадий реакции можно осуществлять последовательно в одном реакционном сосуде без выделения промежуточного продукта, образующегося на предыдущей стадии, уменьшая тем самым стоимость, связанную с продолжительностью использования сосуда, его очисткой, и трудозатраты. В приведенных ниже примерах 1-6 проиллюстрирован подход, при котором выделяют промежуточный продукт, образующийся после завершения каждой стадии. В примерах 7 и 8 проиллюстрировано как некоторые реакционные стадии можно осуществлять последовательно в одном реакционном сосуде без выделения промежуточного продукта, образовавшегося на предыдущей стадии. Пример 1. Получение 2-(циклопропиламино)-3-пиридинкарбонитрила. В реакционную колбу, снабженную механической мешалкой, регулятором температуры, обратным холодильником и капельной воронкой, загружали 2-хлор-3-пиридинкарбонитрил (69,25 г, 0,50 моля), 300 мл этанола и 200 мл воды. При перемешивании в течение 30 мин при температуре 30 С добавляли по каплям циклопропиламин (114 г, 2,0 моля). После завершения добавления реакционную смесь нагревали при перемешивании до температуры дефлегмации в течение 20 ч. Реакционную смесь охлаждали до 60 С и затем избыток циклопропиламина и этанола, составляющий 350 мл, удаляли путем вакуумной дистилляции с помощью вакуума, создаваемого водоструйным насосом. Оставшийся водный раствор охлаждали до температуры окружающей среды и давали выстояться в течение ночи. Твердый продукт собирали фильтрацией и промывали водой. Выход составлял 81,51 г (теоретический выход составлял 79,5 г). Пример 2. Получение 2-(пиклопропиламино)-3-пиридинкарбоновой кислоты (цвиттерион). 45%-ный водный раствор KОН (187 г, 1,5 моля) вносили в смесь, содержащую продукт, полученный в примере 1, и 300 мл 1-пропанола. Смесь выдерживали при температуре дефлегмации в течение примерно 5 ч, после чего по данным ТСХ полностью завершался гидролиз нитрила. Реакционную смесь охлаждали до температуры окружающей среды и обрабатывали 94 г воды, что требовалось для удаления 1-пропанола путем азеотропной дистилляции. Примерно 330 г азеотропной смеси вода/1-пропанол отгоняли при 62 С и давлении 21,1 дюймов рт. столба. К реакционной смеси добавляли воду (130 г) и смесь охлаждали до 5-10 С. Добавляли концентрированную соляную кислоту (148 г, 1,5 моля) с такой скоростью, чтобы температура поддерживалась на уровне ниже 30 С. После добавления примерно 80-90% кислоты начиналось осаждение цвиттериона, в результате чего смесь становилась довольно густой. После добавления всего количества кислоты твердый продукт собирали фильтрацией, используя 90 мл холодной воды для отмывки реакционного сосуда от осадка на фильтре. Продукт сушили, получая 68,12 г цвиттериона. Пример 3. Получение 2-(циклопропиламино)-3-пиридинкарбонилхлорида. Тионилхлорид (25 мл, 40,8 г, 0,343 моля) вносили слабой струей в 9,00 г, 0,048 моля 2-(циклопропиламино)-3-пиридинкарбоновой кислоты, полученной согласно методу, описанному в примере 2, в ацетонитриле. Смесь выдерживали при температуре дефлегмации в течение 30 мин. Смеси давали охладиться и тионилхлорид отгоняли при 40 С/23 дюйма рт. столба до тех пор, пока содержимое резервуара не становилось густым. Добавляли толуол (25 мл) и продолжали осуществлять отгонку тионилхлорида и толуола при 40 С до тех пор, пока не отгоняли примерно половину жидкости. Оставшемуся раствору давали остыть и его перемешивали для активизации кристаллизации. К смеси при перемешивании добавляли гептан (25 мл) и смесь фильтровали в атмосфере азота, получая указанное в заголовке соединение. Пример 4. Получение N-(2-хлор-4-метил-3-пиридинил)-2-(циклопропиламино)-3-пиридинкарбоксамида. Раствор 2-хлор-4-метил-3-пиридинамина (5,70 г, 0,040 моля) в 10 мл ацетонитрила быстро добавляли по каплям к смеси, содержащей хлорангидрид, полученный согласно методу, описанному в примере 3, измельченный безводный фосфат калия (8,49 г, 0,04 моля) и 40 мл ацетонитрила. Реакционную смесь выдерживали при 50 С в течение 20 ч и осуществляли мониторинг хода реакции с помощью ЖХВР. По-4 007497 сле завершения реакции реакционную смесь охлаждали до температуры окружающей среды и обрабатывали 50 мл воды, получая раствор с рН примерно 4,5-5. Смесь подкисляли до рН 1 путем добавления разбавленного раствора НСl и перемешивали в течение 30 мин при температуре окружающей среды. Реакционную смесь фильтровали для удаления любого нерастворенного продукта и фильтрат подщелачивали до рН 9-10 с помощью разбавленного раствора гидроксида натрия и перемешивали в течение 30 мин при температуре окружающей среды. Затем смесь подкисляли до рН 7-8 путем добавления разбавленной НС 1, в результате чего на поверхности раствора образовывался темный масляный слой. Добавляли воду,поскольку в предыдущих экспериментах аналогичного типа было установлено, что это ускоряет кристаллизацию. Масляный слой медленно кристаллизовался при перемешивании в течение ночи. Собирали твердый продукт и сушили в вакуумной печи при 50 С, получая 9,37 г указанного в заголовке соединения. Пример 5. Получение 11-циклопропил-5,11-дигидро-4-метил-6 Н-дипиридо[3,2-b:2',3'-е 1][1,41]диазепин-6-она (невирапин) с использованием гексаметилдисилазана натрия. Реакционную колбу, снабженную магнитной мешалкой, термопарой, капельной воронкой и обратным холодильником с масляным барботером для того, чтобы не допускать поступление воздуха из окружающей среды, заполняли инертным газом-азотом и в нее загружали 3,02 г (0,010 моля) N-(2-хлор-4 метил-3-пиридинил)-2-(циклопропиламино)-3-пиридинкарбоксамида, полученного согласно методу,описанному в примере 4, и 30 мл безводного ТГФ. Добавляли по каплям 40%-ный раствор гексаметилдисилазана в ТГФ (12,7 мл, 0,025 моля), поддерживая температуру реакционной смеси на уровне не выше 30 С. После завершения добавления раствора NaHMDS реакционную смесь нагревали до температуры дефлегмации (примерно 63-66 С). После завершения реакции (по данным ЖХВР-анализа), смесь охлаждали до температуры окружающей среды. Реакционную смесь обрабатывали 1,55 г (0,050 моля) метанола и 0,45 г воды (0,025 моля). Смесь концентрировали на роторном испарителе при давлении 25-30 дюймов рт. столба в водяной бане с температурой 50-60 С. Оставшийся продукт массой 4,44 г растирали с 50 мл воды и раствор, имеющий значение рН 10-12, подкисляли до рН 3 путем добавления 10%-ного раствора НСl. Твердый продукт собирали фильтрацией и осадок на фильтре промывали трижды порциями воды по 10 мл. Осадок на фильтре сушили в вакуумной печи при 50-60 С, получая невирапин. Пример 6. Получение 11-циклопропил-5,11-дигидро-4-метил-6 Н-дипиридо[3,2-b:2',3'-е][1,4]диазепин-6-она (невирапин) с использованием гидрида натрия. 4-х горлую круглодонную колбу вместимостью 500 мл, снабженную мешалкой, термопарой, капельной воронкой и обратным холодильником с масляным барботером для того, чтобы не допускать поступление воздуха из окружающей среды, заполняли инертным газом-азотом и в нее загружали 15,00 г 60%-ного гидрида натрия в виде суспензии в минеральном масле и 120 мл диглима. Смесь нагревали до 130 С и обрабатывали, добавляя по каплям раствор, содержащий N-(2-хлор-4-метил-3-пиридинил)-2(циклопропиламино)-3-пиридинкарбоксамида (41,7 г, 0,138 моля), полученного согласно методу, описанному в примере 4, в 70 мл диглима при 80 С. Реакционную смесь выдерживали при 130 С до тех пор,пока не прекращалось выделение водорода. Смесь охлаждали до температуры окружающей среды и осторожно по каплям добавляли воду (6,75 г). После прекращения выделения водорода добавляли дополнительно 100 мл воды. Добавляли уксусную кислоту (20 мл) для уменьшения значения рН смеси от 11-13 до примерно 7. Добавляли еще 100 мл воды и реакционную смесь перемешивали при температуре окружающей среды в течение 30 мин, при этом происходила кристаллизация продукта. Твердый продукт собирали фильтрацией и осадок на фильтре промывали 100 мл воды, а затем 50 мл циклогексана для удаления любых остатков минерального масла из суспензии гидрида натрия в минеральном масле. Влажный осадок сушили в вакуумной печи при 50 С в течение 18 ч, получая 35,58 г невирапина. Пример 7. Синтез 2-(циклопропиламино)-3-пиридин карбоновой кислоты из 2-хлор-3-пиридинкарбонитрила в одном сосуде.-5 007497 В 4-х горлую круглодонную колбу вместимостью 1 л, снабженную мешалкой, обратным холодильником, термопарой и капельной воронкой, вносили 2-хлор-3-пиридинкарбонитрил (27,70 г, 0,20 моля), а затем 120 мл 1-пропанола и 80 мл воды. Добавляли триэтиламин (20,2 г, 0,20 моля) в виде одной порции,а затем циклопропиламин (17,10 г, 0,30 моля) в течение 2 мин. Реакционную смесь выдерживали при температуре дефлегмации (86-87 С) и через 2,5 ч путем анализа с помощью ТСХ (тонкослойная хроматография) (силикагель, подвижная фаза метил-трет-бутиловый эфир (МТБЭ было установлено, что произошло образование некоторого количества продукта. После перемешивания при температуре дефлегмации в течение 16 ч, путем анализа с помощью ТСХ было выявлено небольшое количество оставшегося исходного продукта. Анализ с помощью ЖХВР позволил выявить 22% исходного продукта и 75% 2(циклопропиламино)-3-пиридинкарбонитрила. Добавляли дополнительно 0,1 моля (10,1 г) триэтиламина(общее количество триэтиламина составляло 30,3 г, 0,30 моля) и 0,03 моля циклопропиламина (1,70 г) и смесь продолжали выдерживать при температуре дефлегмации в течение еще 3 ч. Анализ с помощью ЖХВР позволил выявить, что осталось 15% исходного продукта. Добавляли еще 4,0 г циклопропиламина(всего 0,40 моля) и смесь выдерживали при температуре дефлегмации в течение еще 18 ч. По окончании этого периода времени по данным анализа с помощью ЖХВР оставалось 2,9% исходного продукта. Добавляли гидроксид калия (33,6 г, 0,60 моля) и смесь нагревали в вакууме до температуры примерно 40 С в течение примерно 15 мин для удаления любых летучих аминов. Затем смесь выдерживали при температуре дефлегмации в течение 5 ч при атмосферном давлении для того, чтобы гидролизовать нитрил в карбоновую кислоту. Добавляли воду (80 мл) и отгоняли н-пропанол в виде азеотропа с водой(азеотропная температура кипения 87,7 С, 28,3% воды, 71,7% н-пропанола). Когда температура в дистилляционной насадке повышалась до 92 С, отгонку прекращали и реакционной смеси давали охладиться. Реакционную смесь охлаждали примерно до 10 С с помощью бани лед-метанол и добавляли по каплям 50 мл (59,2 г) 37%-ного раствора НСl, поддерживая температуру реакционной смеси на уровне не выше 25 С. После добавления всего количества НСl и после перемешивания в течение еще примерно 2 мин начиналась кристаллизация 2-(циклопропиламино)-3-пиридинкарбоновой кислоты и продукт начинал осаждаться. Для того, чтобы растворить твердую массу и сделать смесь пригодной к перемешиванию добавляли воду (100 мл). Примерно через 30 мин твердый продукт собирали фильтрацией. Дополнительную порцию твердого продукта получали путем концентрирования фильтрата. После вакуумной сушки в течение примерно 2 ч масса влажного твердого осадка составляла 23,02 г. По данным ЖХВР содержание 2-(циклопропиламино)-3-пиридин карбоновой кислоты составляло 97%, при этом были обнаружены два небольших пика неизвестных примесей, концентрация которых составляла 1,8 и 1,3%. Твердый продукт сушили в вакуумной печи при 50 С в течение 65 ч, получая выход 18,19 г. Пример 8. Синтез в одном сосуде N-(2-хлор-4-метил-3-пиридинил)-2-(циклопропиламино)-3 пиридинкарбоксамида из 2-хлор-4-метил-3-пиридинамина и 2-(циклопропиламино)-3-пиридин карбоновой кислоты цвиттерион). В 4-х горлую круглодонную колбу вместимостью 250 мл, снабженную механической мешалкой,конденсатором, капельной воронкой и термопарой и капельной воронкой, вносили 2(циклопропиламино)-3-пиридин карбоновую кислоту (18,46 г, 0,10 моля). В реакционную колбу добавляли при перемешивании тонкой струей тионилхлорид (22 мл, 0,30 моля) и смесь нагревали до температуры дефлегмации в течение 32 мин. Реакционную смесь охлаждали и конденсатор заменяли вакуумной дистилляционной насадкой. Тионилхлорид отгоняли при 40 С в вакууме при давлении 23 дюйма рт. столба до тех пор, пока содержимое дистилляционного сосуда не становилось густым. Добавляли толуол(30 мл) и продолжали дистилляцию до тех пор, пока не отгоняли большую часть жидкости. Добавляли еще одну порцию толуола (30 мл) и примерно половину растворителя отгоняли в вакууме. К остатку смеси добавляли ацетонитрил (60 мл). По каплям добавляли раствор 2-хлор-4-метил-3-пиридинамина(11,4 г, 0,080 моля) в 40 мл ацетонитрила и реакционную смесь нагревали до 50 С и перемешивали в течение ночи. После добавления 2-хлор-4-метил-3-пиридинамина добавляли тонкоизмельченный фосфат калия. После выдерживания в течение 16 ч при 50 С к реакционной смеси (рН 4-5) при перемешивании добавляли 100 мл воды. Реакционную смесь фильтровали для удаления небольшого количества нерас-6 007497 творившегося продукта. Фильтрат (2 слоя) подщелачивали до рН 10-11 с помощью 50%-ного водного раствора NaOH и затем снова подкисляли до рН 8. По данным ЖХВР-анализа большая часть продукта находилась в толуоловом слое. Толуоловый слой экстрагировали 300 мл разбавленного раствора НСl (рН 1). Водный слой подщелачивали до рН 8 с помощью 10%-ного водного раствора NaOH, в результате чего происходило отделение масляного слоя, который медленно кристаллизовался при растирании. После выстаивания в течение 2 дней твердый продукт собирали и сушили в вакууме при 50 С, получая 21,40 г указанного в заголовке твердого соединения рыжевато-коричневого цвета. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ получения невирапина, заключающийся в том, что где X обозначает атом фтора, хлора, брома или йода, предпочтительно хлора или брома, с циклопропиламином с получением 2-(циклопропиламино)-3-пиридинкарбонитрила;(в) выделяют 2-(циклопропиламино)-3-пиридинкарбоновую кислоту из реакционной среды;(г) обрабатывают 2-(циклопропиламино)-3-пиридинкарбоновую кислоту хлорирующим агентом с получением 2-(циклопропиламино)-3-пиридинкарбонилхлорида; где X обозначает атом фтора, хлора, брома или йода, предпочтительно хлора или брома с получением N(2-гало-4-метил-3-пиридинил)-2-(циклопропиламино)-3-пиридинкарбоксамида формулы где X обозначает атом фтора, хлора, брома или йода, предпочтительно хлора или брома; и(е) циклизуют N-(2-гало-4-метил-3-пиридинил)-2-(циклопропиламино)-3-пиридинкарбоксамид путем обработки сильным основанием с получением невирапина. 2. 2-(Циклопропиламино)-3-пиридинкарбоновая кислота. 3. 2-(Циклопропиламино)-3-пиридинкарбонилхлорид. 4. Способ получения 2-(циклопропиламино)-3-пиридинкарбоновой кислоты, заключающийся в том,что где X обозначает атом фтора, хлора, брома или йода, предпочтительно хлора или брома, с циклопропиламином с получением 2-(циклопропиламино)-3-пиридинкарбонитрила; и где X обозначает атом фтора, хлора, брома или йода, предпочтительно хлора или брома, заключающийся в том, что(а) обрабатывают 2-(циклопропиламино)-3-пиридинкарбоновую кислоту хлорирующим агентом с получением 2-(циклопропиламино)-3-пиридинкарбонилхлорида; и где X обозначает атом фтора, хлора, брома или йода, предпочтительно хлора или брома с получением N-(2-гало-4-метил-3-пиридинил)-2-(циклопропиламино)-3-пиридинкарбоксамида. 6. Способ полученияN-(2-гало-4-метил-3-пиридинил)-2-(циклопропиламино)-3 пиридинкарбоксамида, заключающийся в том, что подвергают взаимодействию 2-(циклопропиламино)3-пиридинкарбонилхлорид с 2-гало-4-метил-3-пиридинамином формулы где X обозначает атом фтора, хлора, брома или йода, предпочтительно хлора или брома.
МПК / Метки
МПК: C07D 213/85, C07D 243/00, A61K 31/551, C07D 471/14, C07D 213/82, C07D 213/78, C07D 221/00, C07D 213/80
Метки: невирапина, способ, получения, усовершенствованный
Код ссылки
<a href="https://eas.patents.su/9-7497-usovershenstvovannyjj-sposob-polucheniya-nevirapina.html" rel="bookmark" title="База патентов Евразийского Союза">Усовершенствованный способ получения невирапина</a>
Следующий патент: Способ и устройство для определения моды движения бурильной колонны
Случайный патент: Устройство управления электрическим аппаратом












