Способ получения аморфной формы полукальциевой соли (3r, 5r) -7- [3-фенил-4-фенилкарбамил-2-(4-фторфенил)-5-изопропил-пиррол-1-ил]-3, 5-дигидроксигептановой кислоты (аторвастатина)
Формула / Реферат
1. Способ получения аморфной формы полукальциевой соли (3R,5R)-7-[3-фенил-4-фенилкарбамил-2-(4-фторфенил)-5-изопропилпиррол-1-ил]-3,5-дигидроксигептановой кислоты формулы (I)
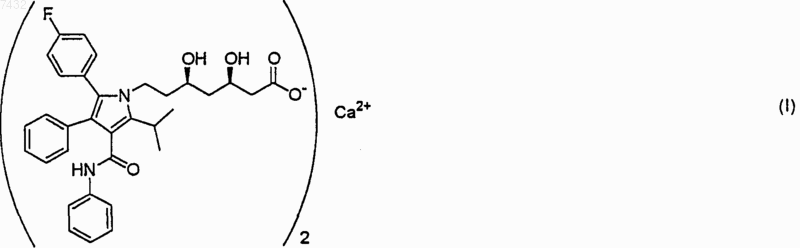
характеризующийся тем, что (3R,5R)-трет-бутил-(6-{2-[3-фенил-4-фенилкарбамил-2-(4-фторфенил)-5-изопропилпиррол-1-ил]этил}-2,2-диметил-[1,3]диоксан-4-ил)ацетат формулы II

подвергают сначала кислотному гидролизу, а затем щелочному гидролизу с образованием соли (3R,5R)-7-[3-фенил-4-фенилкарбамил-2-(4-фторфенил)-5-изопропилпиррол-1-ил]-3,5-дигидроксигептановой кислоты с щелочным металлом, которую затем после необязательного подкисления экстрагируют органическим растворителем, выбранным из группы сложных эфиров С1-С5-кислот и С1-С5-спиртов, и после операций очистки превращают путем обработки солью кальция, гидроксидом кальция или С1-С5-алкоголятом кальция в полукальциевую соль, которую осаждают с помощью С5-С12-углеводорода или диалкилового эфира формулы R1OR2, где R1 и R2 представляют собой С1-С5-алкильные группы.
2. Способ по п.1, отличающийся тем, что раствор соли (3R,5R)-7-[3-фенил-4-фенилкарбамил-2-(4-фторфенил)-5-изопропил-пиррол-1-ил]-3,5-дигидроксигептановой кислоты с катионом щелочного металла, полученный из соединения формулы (II), содержащий избыток хлорида и гидроксида соответствующего катиона, подкисляют и экстрагируют с получением раствора (3R,5R)-7-[3-фенил-4-фенилкарбамил-2-(4-фторфенил)-5-изопропилпиррол-1-ил]-3,5-дигидроксигептановой кислоты, который затем превращают путем реакции с гидроксидом или алкоголятом кальция в раствор полукальциевой соли.
3. Способ по п.1 или 2, отличающийся тем, что раствор (3R,5R)-7-[3-фенил-4-фенилкарбамил-2-(4-фторфенил)-5-изопропилпиррол-1-ил]-3,5-дигидроксигептановой кислоты в соответствующем сложном эфире С1-С5-кислоты и С1-С5-спирта превращают в раствор соли щелочного металла.
4. Способ по любому из пп.1-3, отличающийся тем, что полукальциевую соль осаждают из раствора в этилацетате.
5. Способ по любому из пп.1-4, отличающийся тем, что осаждение проводят путем добавления неполярного растворителя, выбранного из группы, включающей пентан, гексан, гептан, циклогексан, или диалкилового эфира формулы R1OR2, где R1 и R2 - С1-С5-алкильные группы, к раствору полукальциевой соли (3R,5R)-7-[3-фенил-4-фенилкарбамил-2-(4-фторфенил)-5-изопропил-пиррол-1-ил]-3,5-дигидрокси-гептановой кислоты в соответствующем растворителе.
6. Способ по любому из пп.1-5, отличающийся тем, что раствор полукальциевой соли (3R,5R)-7-[3-фeнил-4-фeнилкapбaмил-2-(4-фтopфeнил)-5-изoпpoпил-пиppoл-l-ил]-3,5-дигидроксигептановой кислоты в сложном эфире С1-С5-кислоты и С1-С5-спирта добавляют к неполярному растворителю, выбранному из группы, включающей пентан, гексан, гептан и циклогекстан, или к диалкиловому эфиру формулы R1OR2, где R1 и R2 - С1-С5-алкильные группы.
7. Способ по любому из пп.1-6, отличающийся тем, что раствор полукальциевой соли (3R, 5R)-7-[3-фенил-4-фенилкарбамил-2-(4-фторфенил)-5-изопропилпиррол-1-ил]-3,5-дигидроксигептановой кислоты в сложном эфире перед осаждением разбавляют 5-95%, предпочтительно 30-70%, дополнительного растворителя.
8. Способ по п.7, отличающийся тем, что в качестве дополнительного растворителя используют толуол, трет-бутилметиловый эфир или тетрагидрофуран.
Текст
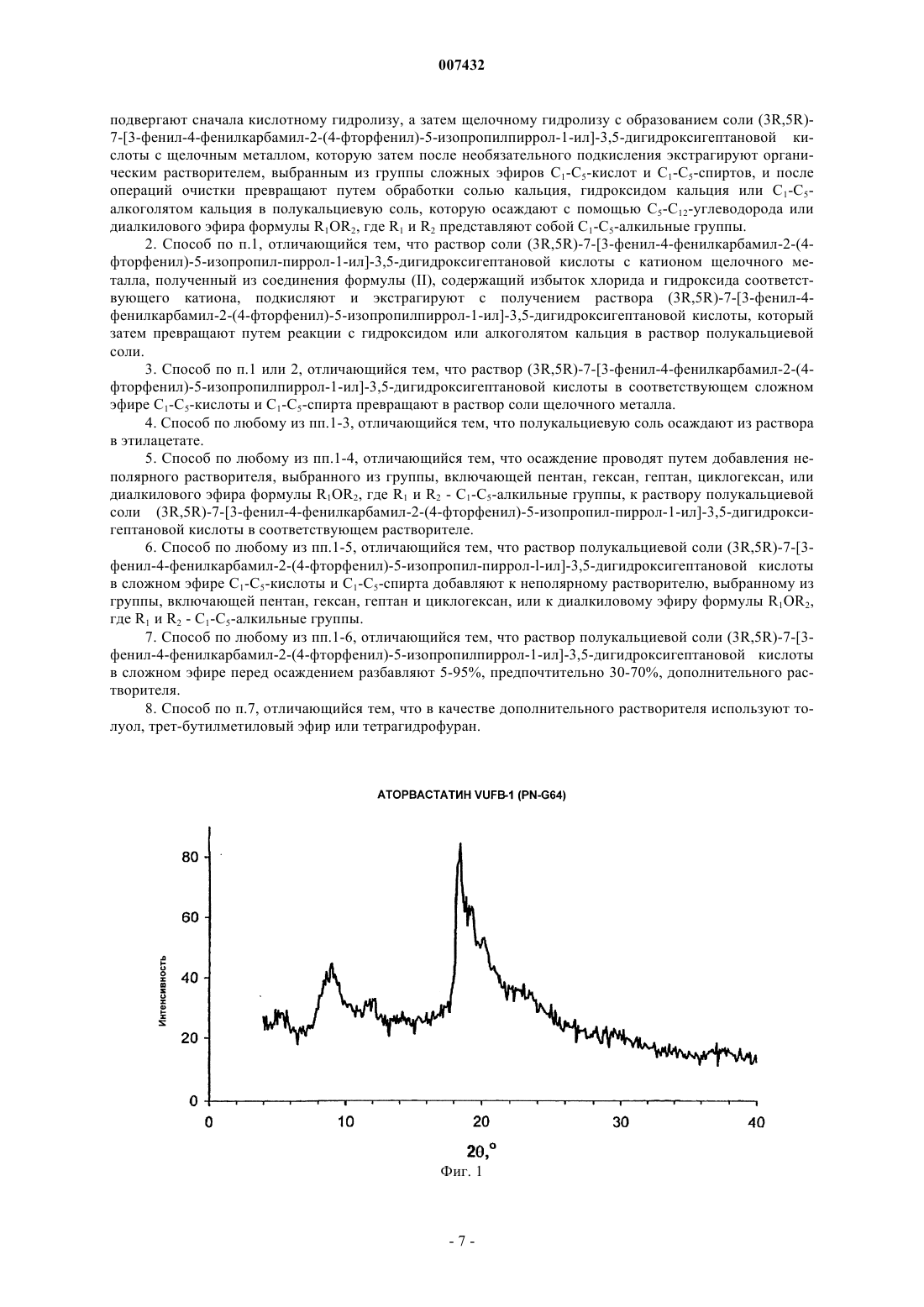
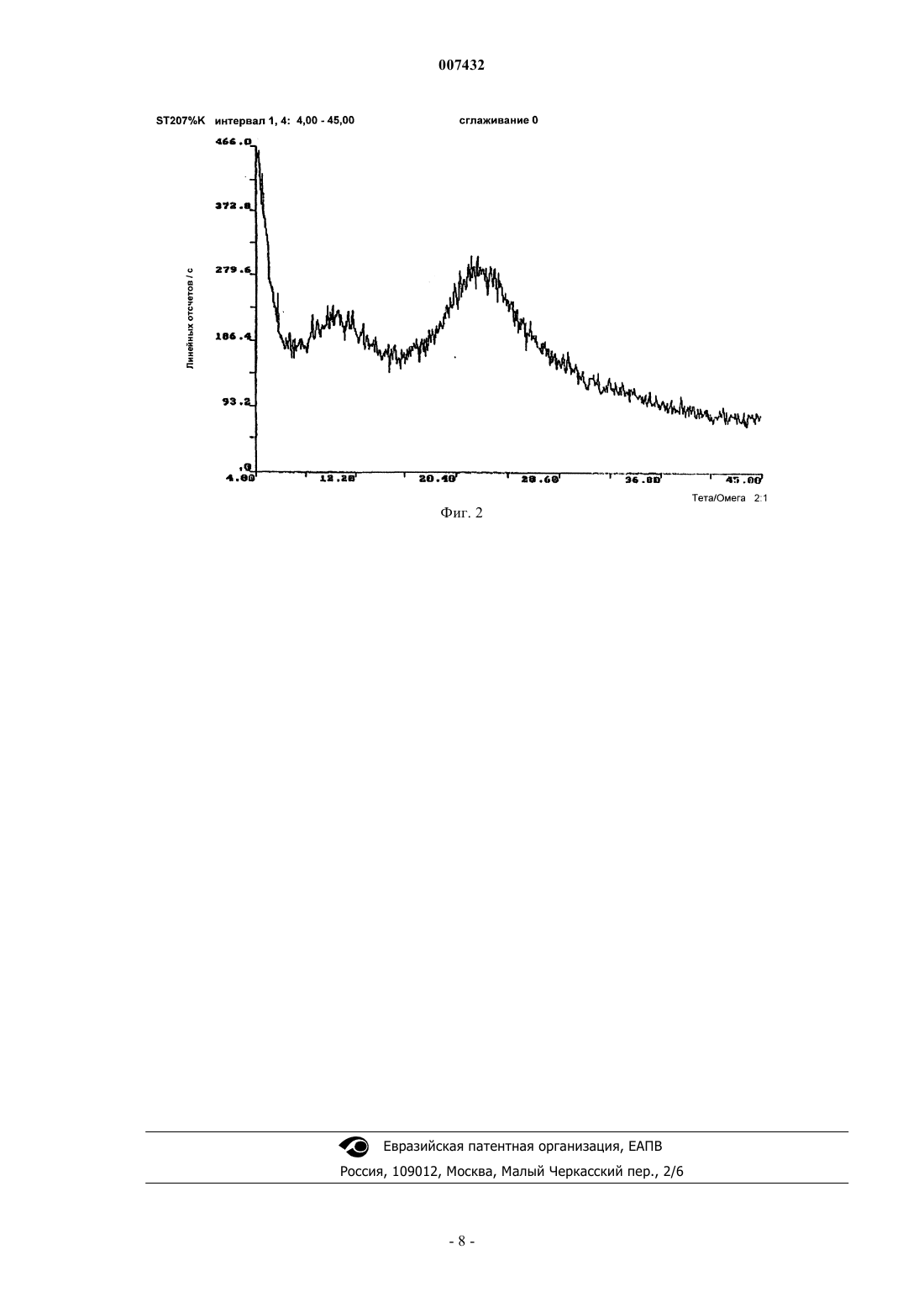
007432 Область техники Изобретение относится к новому способу получения аморфной формы полукальциевой соли (3R,5R)-7-[3-фенил-4-фенилкарбамил-2-(4-фторфенил)-5-изопропил-пиррол-1-ил]-3,5-дигидроксигептановой кислоты, известной под непатентованным названием аторвастатин. Данный препарат является важным представителем класса гиполипидемических и гипохолестерических препаратов. Предпосылки изобретения Аторвастатин (формула I) получают в соответствии с опубликованными патентами (США патенты.4681893, 5003080, 5097045, 5103024, 5124482, 5149837, 5155251,5216174, 5245047, 5248793, 5273995,5397792, 5342952) обычно из натриевой соли (3R,5R)-7-[3-фенил-4-фенилкарбамил-2-(4-фторфенил)-5 изопропил-пиррол-1-ил]-3,5-дигидроксигептановой кислоты и подходящей водорастворимой соли кальция, обычно ацетата или хлорида кальция. Исходная натриевая соль (3R,5R)-7-[3-фенил-4-фенилкарбамил-2-(4-фторфенил)-5-изопропилпиррол-1-ил]-3,5-дигидроксигептановой кислоты может быть получена из соответствующей кислоты,которую обычно получают из (3R,5R)-трет-бутил-(6-2-[3-фенил-4-фенилкарбамил-2-(4-фторфенил)-5 изопропил-пиррол-1-ил]этил-2,2-диметил-[1,3]диоксан-4-ил)ацетата (формула II). Этот ключевой промежуточный продукт превращают в натриевую соль соответствующей кислоты путем перемешивания с соляной кислотой с последующей обработкой значительным избытком гидроксида натрия, при этом, однако, в реакционной смеси остается значительное количество избыточного гидроксида натрия и хлорид натрия. Подкисление с последующей экстракцией позволяет получить раствор соответствующей кислоты (формула III) без неорганических примесей. Затем полученная кислота превращается в соответствующий лактон (формула IV), который можно очистить кристаллизацией, и очищенный лактон переводят в натриевую соль посредством реакции с эквивалентом гидроксида натрия. Избыток щелочи не используют, поскольку на следующей стадии при реакции с солью кальция он образует гидроксид кальция, который невозможно полностью удалить из продукта на следующих стадиях по способу, описанному в вышеперечисленных патентах. Однако при использовании эквивалентного количества гидроксида реакция требует длительного времени и ее ход необходимо контролировать при помощи ВЭЖХ. Другим недостатком этого способа является потеря приблизительно 20% конечного продукта. В зависимости от способа получения, аторвастатин может быть получен в некоторых из своих кристаллических форм или в виде аморфного вещества. В первых патентах (например, патентах США 4681893 и 5273995) не содержится указаний на форму вещества, получаемого по этим патентам. В более поздних патентах (патенты США 5969156 и 6121461), описывающих кристаллические формы аторвастатина, имеется указание на то, что вещество, полученное в соответствии с первыми патентами, было аморфным. В патенте ЕР 839132, в котором описан новый способ получения аморфной формы аторвастатина путем растворения кристаллического аторвастатина формулы I в негидроксилированных растворителях (в качестве примеров растворителей в патенте упоминаются тетрагидрофуран и смесь тетрагидрофурана и толуола) с последующей сушкой, также упоминается, что в ранних патентах получается аморфный аторвастатин; однако указывается, что эта методика плохо воспроизводима. Согласно нашему опыту, аторвастатин, получаемый в соответствии с ранними патентами (США 4681893, 5298627 и 5273995) не является абсолютно аморфным, в соответствии с результатами рентгеноструктурного анализа в нем имеются кристаллические компоненты (см. фиг. 1). Патент США 4681893 описывает также возможность очистки вещества неприемлемого качества путем растворения в этилацетате, фильтрации через диатомит Supercel с последующим осаждением из раствора гексаном при температуре 50 С. Заявка на патент Ranbaxy Laboratories (WO 00/71116 А 1) описывает превращение кристаллической формы аторвастатина в негидроксилированном растворителе и его осаждение из полученного раствора неполярным углеводородным растворителем. Аналогичный подход использован и в заявке на патент Lek (WO 01/42209 А 1), в которой описано превращение кристаллической формы аторвастатина путем растворения в различных растворителях, как негидроксилированных, так и низших спиртах, с последующим осаждением из растворов теми растворителями, в которых аторвастатин нерастворим. Эти растворители также разнообразны, в добавление к неполярным углеводородным растворителям в их число входят и алифатические эфиры. Целью данного изобретения была разработка нового способа получения аморфной формы полукальциевой соли (3R,5R)-7-[3-фенил-4-фенилкарбамил-2-(4-фторфенил)-5-изопропил-пиррол-1-ил]-3,5 дигидроксигептановой кислоты, который не имел бы недостатков описанных выше способов. Сущность изобретения Преимущества аморфного аторвастатина для некоторых применений подчеркивались в патенте ЕР 839132. Предметом данного изобретения является новый способ получения аморфной формы полукальциевой соли (3R,5R)-7-[3-фенил-4-фенилкарбамил-2-(4-фторфенил)-5-изопропил-пиррол-1-ил]-3,5 дигидроксигептановой кислоты, который заключается в превращении (3R,5R)-7-[3-фенил-4-фенилкарбамил-2-(4-фторфенил)-5-изопропил-пиррол-1-ил]-3,5-дигидроксигептановой кислоты или ее соли,содержащей катион М+, где М+ представляет собой катион щелочного металла или аммония общей формулы RNN+H4-N, в которой R - С 1-С 5 алкил, а N имеет значения от 0 до 3, без выделения промежуточного продукта в виде полукальциевой соли или другой соли, кислоты или лактона, в полу-кальциевую соль в растворе в результате взаимодействия с солью кальция, гидроксидом кальция или C1-C5-алкоголятом кальция, с последующим осаждением C1-C5-углеводородом или диалкиловым эфиром формулы R1OR2,где оба радикала, R1 и R2, представляют собой C1-C5-алкильные группы, с получением твердой аморфной фазы. Описанный выше способ основан на неожиданном открытии, что в этилацетате и некоторых родственных ему растворителях хорошо растворима не только соответствующая аторвастатину кислота, но и множество ее солей, например, соли натрия, калия, а также соли аммония, полученные из аммиака, первичных, вторичных и третичных аминов, а также сама полукальциевая соль. Ниже приводится более подробное описание изобретения. Аморфную форму аторвастатина предпочтительно получают непосредственным осаждением из раствора полукальциевой соли аторвастатина в подходящем растворителе, предпочтительно эфире C1-C5 кислоты и C1-C5-спирта, из которых наиболее предпочтителен этилацетат, неполярным растворителем,предпочтительно пентаном, гексаном, гептаном или циклогексаном, или диалкиловым эфиром R1OR2,-2 007432 где R1 и R2 представляют собой C1-C5-алкильные группы, предпочтительно диэтиловым эфиром, диизопропиловым эфиром или 7-бутилметиловым эфиром. Для повышения чистоты продукта признано полезным разбавлять раствор аторвастатина в этилацетате перед осаждением дополнительным растворителем,например, толуолом, трет-бутилметиловым эфиром или тетрагидрофураном в количестве от 5 до 95%,предпочтительнее от 30 до 70%. Аморфная форма может быть получена и при помощи обратного процесса, когда раствор полукальциевой соли в одном из подходящих растворителей добавляется к одному из указанных выше неполярных растворителей. Ни на одной из предыдущих стадий данного способа полукальциевую соль не выделяют в твердом виде и, таким образом, ни один из патентов, защищающих индивидуальные кристаллические формы этого вещества или способы превращения кристаллического аторвастатина в аморфный аторвастатин, не нарушается. Раствор полукальциевой соли аторвастатина в подходящем растворителе, предпочтительно эфиреC1-C5-кислоты и C1-C5-спирта, из которых наиболее предпочтителен этилацетат, может быть получен из раствора соответствующей свободной кислоты, полученной с использованием описанной выше методики из промежуточного вещества II. Этот раствор превращается в раствор полукальциевой соли путем встряхивания его с водным раствором гидроксида кальция, с суспензией гидроксида кальция в малом количестве воды или с раствором C1-C5-алкоголята кальция в подходящем растворителе, предпочтительно соответствующем спирте. Кроме того, можно использовать раствор любой из перечисленных выше солей аторвастатина в подходящем растворителе, предпочтительно этилацетате, и превратить его в раствор полукальциевой соли аторвастатина путем встряхивания с подходящей водорастворимой солью кальция, предпочтительно с ацетатом кальция. Избыток использованных солей затем легко удалить промыванием раствора аторвастатина в органическом растворителе водой или водными растворами, например, раствором соли, а затем водой. В зависимости от используемой осаждающей системы и способа осаждения раствор полукальциевой соли аторвастатина может быть использован далее на следующей стадии без осушения или предварительно осушен подходящим осушителем, предпочтительно сульфатом натрия, кальция или магния. Подходящие водорастворимые соли аторвастатина могут быть предпочтительно получены из раствора соответствующей свободной кислоты, синтезированной по описанным выше методикам из промежуточного вещества формулы II. Этот раствор далее превращается в соответствующую соль путем добавления раствора гидроксида щелочного металла в воде, аммиака в воде или соответствующего амина в воде с последующим встряхиванием. Предпочтительно использовать такие амины, как триэтиламин, которые являются жидкостями при нормальных условиях, потому что их можно добавлять к раствору свободной кислоты без использования растворителя. Растворы полученных солей можно в этих случаях сразу, без очистки использовать для превращения в раствор полукальциевой соли аторвастатина в соответствии с приведенной выше методикой. Растворы некоторых описанных ранее солей аторвастатина можно на этой стадии упарить и очистить путем кристаллизации из подходящего растворителя. Раствор натриевой или калиевой солей аторвастатина могут быть также успешно получены непосредственно после проведения реакции превращения промежуточного вещества формулы II. На конечной стадии в раствор,содержащий соответствующий хлорид щелочного металла и натриевую или калиевую соль аторвастатина, добавляют избыток использованного гидроксида щелочного металла. Было неожиданно обнаружено,что путем многократной экстракции этого раствора подходящим растворителем, чаще всего сложным эфиром C1-C5 кислоты и C1-C5 спирта, из которых наиболее предпочтителен этилацетат, соответствующая соль может быть почти количественно перенесена в органическую фазу, и в таком виде использоваться в дальнейших превращениях, как описано выше. Рентгеновская дифрактограмма аторвастатина, полученного по способу, описанному в настоящем изобретении, показывает, что его структура абсолютно аморфна (см. фиг. 2). Изобретение далее иллюстрируется приложенными рисунками и примерами. Примеры, иллюстрирующие наиболее предпочтительные альтернативы получения аторвастатина по этому изобретению, носят только иллюстративный характер и ни в коей мере не ограничивают объем охраны изобретения. Краткое описание рисунков Фиг. 1 представляет собой рентгеновскую дифрактограмму аторвастатина, полученного по способу,описанному в патенте США 5298627. Фиг. 2 представляет собой рентгеновскую дифрактограмму аторвастатина, полученного по способу,описанному в данном изобретении. Примеры Пример 1. К навеске эфира формулы II (5 г, 7.6 ммоль) добавляли тетрагидрофуран (75 мл), а затем, после растворения вещества, 10% HCl (17 мл). Смесь перемешивали при комнатной температуре в течение 6 ч. После этого в раствор в течение 5 мин добавили 40 % раствор NaOH (10 мл), температура при этом не поднималась выше 35 С; получившуюся гетерогенную смесь интенсивно перемешивали в течение 15 ч,после чего вылили в делительную воронку, содержащую деминерализованную воду (150 мл) и гексан (50 мл). После встряхивания органический слой отделили, а водный слой экстрагировали смесью гексана (40 мл) и тетрагидрофурана (10 мл). После полного разделения водный слой экстрагировали этилацетатом (1-3 007432 х 40 мл, 4 х 20 мл). Экстракт в этилацетате затем трижды встряхивали с деминерализованной водой (5 мл), содержащей 1 г ацетата кальция в 5 мл воды. Получившийся экстракт в этилацетате промывали деминерализованной водой (2x5 мл) и сконцентрировали в вакуумном испарителе до объема 20 мл. После фильтрации чистый раствор добавляли по каплям к гексану (200 мл) в течение 5 мин при интенсивном перемешивании, затем смесь перемешивали еще 20 мин, нерастворимую фракцию отделяли на вакуумфильтре, промывали гексаном (20 мл) и высушивали в вакууме при комнатной температуре. Было получено 4.1 г аморфного аторвастатина. Пример 2. Использовали способ, описанный в примере 1, однако для гидролиза эфира использовали гидроксид калия, а не гидроксид натрия, что привело к получению калиевой соли аторвастатина. Дальнейшая обработка была аналогична способу, описанному в примере 1. Пример 3. К навеске эфира формулы II (5 г, 7,6 ммоль) добавили тетрагидрофуран (75 мл), а затем, после растворения вещества, 10% HCl (17 мл). Смесь перемешивали при комнатной температуре в течение 24 ч. Затем в раствор в течение 5 мин добавили 40% раствор NaOH (10 мл), получившуюся гетерогенную смесь интенсивно перемешивали в течение 17 ч, после чего вылили в делительную воронку, содержащую деминерализованную воду (150 мл) и гексан (50 мл). После встряхивания органический слой отделили, а водный слой экстрагировали смесью гексана (40 мл) и тетрагидрофурана (10 мл). После полного разделения водный слой экстрагировали этилацетатом (1 х 40 мл, 3 х 20 мл). После упаривания экстракта получили 4 г натриевой соли аторвастатина. После перекристаллизации из этанола соль растворили в этилацетате (100 мл), и раствор трижды встряхивали с деминерализованной водой (5 мл), содержащей 1 г ацетата кальция в 5 мл воды. Полученный раствор в этилацетате промывали деминерализованной водой(2x5 мл) и после осушения сульфатом магния концентрировали в вакуумном испарителе до объема 30 мл. После фильтрации чистый раствор добавляли по каплям к гексану (200 мл) в течение 5 мин. при интенсивном перемешивании, затем смесь перемешивали еще 20 мин, нерастворимую фракцию отделяли на вакуум-фильтре, промывали гексаном (20 мл) и высушивали в вакууме при комнатной температуре. Было получено 3.1 г аморфного аторвастатина. Пример 4. К навеске эфира формулы II (5 г, 7.6 ммоль) добавили тетрагидрофуран (75 мл), а затем, после растворения вещества, 10% HCl (17 мл). Смесь перемешивали при комнатной температуре в течение 24 ч. После этого в раствор в течение 5 мин добавили 40 % раствор NaOH (10 мл), получившуюся гетерогенную смесь интенсивно перемешивали в течение 17 ч, после чего вылили в делительную воронку, содержащую деминерализованную воду (150 мл) и гексан (50 мл). Водный слой подкислили 10% HCl до рН=3 и экстрагировали этилацетатом (4 х 20 мл). Полученный экстракт перемешивали со смесью гидроксида кальция (0.87 г) в деминерализованной воде (15 мл) в течение 20 мин. После этого водный слой отделили, экстракт промыли деминерализованной водой (2x5 мл) и сушили сульфатом магния (10 г) в течение 1 ч. В осушенный экстракт при перемешивании добавили гексан (160 мл) и через 1 ч отделили нерастворимую фракцию на вакуум-фильтре. После сушки было получено 3.3 г аморфного аторвастатина. Пример 5. Использовался способ, описанный в примере 4, однако для превращения кислоты аторвастатина в ее кальциевую соль вместо гидроксида кальция применяли метилат кальция в метаноле. Дальнейшая обработка аналогично способу, описанному в примере 4. Пример 6. Навеску эфира формулы II (8.7 г, 13.3 ммоль) при перемешивании поместили в круглую колбу, содержащую смесь тетрагидрофурана (100 мл) и 10% HCl (30 мл, 0.082 моль). Полученный раствор перемешивали при комнатной температуре в течение 24 ч. Затем в течение 15 мин в раствор добавили по каплям 30% раствор NaOH (24 мл, 7.2 г, 0.18 моль); реакционная смесь разогрелась и стала мутной. Эту смесь перемешивали при комнатной температуре в течение 15 ч, после чего вылили в делительную воронку, содержащую гексан (100 мл) и деминерализованную воду (300 мл). После тщательного встряхивания и разделения слоев нижний водный слой встряхивали с добавлением дополнительного количества гексана (2x50 мл). Промытый водный слой подкислили 10% HCl до рН=4 и экстрагировали дихлорметаном (1 х 100 мл, 2 х 50 мл, 2 х 25 мл), органический слой промыли насыщенным раствором соли (2 х 25 мл) и высушили над CaSO4 (25 г) в течение ночи. Затем осушитель отфильтровали, промыли сухим дихлорметаном (50 мл), после чего в объединенные органические растворы добавили раствор триэтиламина (3 мл, 21.5 ммоль) в сухом дихлорметане (20 мл). После перемешивания при комнатной температуре в течение 0,5 ч раствор упарили до сухого вещества в ротационном вакуумном испарителе. Полученную твердую пену (приблизительно 10-11 г) смешали с сухим дихлорметаном (25 мл) и вновь упарили до сухого вещества (приблизительно 9 г). Эту процедуру повторили еще раз, после чего получили 8.34 г желтоватой твердой пены соли триэтиламмония (12.6 ммоль, 95%). Соль триэтиламмония растворили в этилацетате (50 мл) и перенесли раствор в делительную воронку. Затем в делительную воронку добавили раствор моногидрата ацетата кальция (1.2 г, 6.8 ммоль) в деминерализованной воде (10 мл), и содержимое делительной воронки встряхивали. После разделения водный слой удалили, органический слой-4 007432 встряхивали с водой (2x10 мл) и сушили сульфатом магния. После отделения органический слой промыли толуолом (50 мл) и при интенсивном перемешивании при комнатной температуре добавили по каплям гексан (25 мл). Затем температуру смеси подняли до 50 С и при этой температуре перемешивали до исчезновения образовавшейся сначала мутности. При интенсивном перемешивании смеси позволили охладиться до 30 С (раствор вновь стал мутным) и при этой температуре по каплям добавили гексан (100 мл) без дополнительного нагревания. Смесь перемешивали при комнатной температуре еще 10 мин, по каплям добавили оставшееся количество гексана (100 мл) и перемешивали в течение 1 ч при комнатной температуре. Полученный таким образом аторвастатин отделили на вакуум-фильтре, промыли гексаном(25 мл), высушили в вакууме до постоянного веса и растерли в агатовой ступке. Было получено 5.6 г аморфного аторвастатина. Пример 7. Навеску эфира формулы II (1 г) при перемешивании добавили к смеси тетрагидрофурана (20 мл) и 10% HCl (3.5 мл), полученный раствор перемешивали при комнатной температуре в течение 10 ч. Затем в течение 15 минут по каплям добавили к реакционной смеси 40 % раствор NaOH (2 мл), полученную смесь перемешивали при комнатной температуре в течение 15 ч, после чего вылили в делительную воронку, содержащую гексан (10 мл) и деминерализованную воду (30 мл). После тщательного встряхивания и разделения слоев нижний водный слой встряхивали с дополнительным количеством гексана (2x5 мл). Промытый водный слой подкислили 10% HCl до рН=4 и экстрагировали диэтиловым эфиром (2x10 мл, 2x5 мл), органический слой промыли насыщенным раствором соли (2x5 мл) и высушили над Na2SO4. Затем осушитель отфильтровали, промыли сухим диэтиловым эфиром, после чего в объединенный раствор добавили триэтиламин (0.3 мл) и раствор упарили до сухого вещества в ротационном вакуумном испарителе при комнатной температуре при перемешивании в течение 0,5 ч. Полученная твердая пена была смешана с сухим диэтиловым эфиром (25 мл) и смесь вновь упарена до сухого вещества (приблизительно 0.9 г). Соль триэтиламмония растворили в этилацетате (10 мл) и раствор перенесли в делительную воронку. В воронку был добавлен раствор моногидрата ацетата кальция (0.13 г) в деминерализованной воде (1 мл), и содержимое воронки встряхивали. После удаления водного слоя органический слой встряхивали с водой. После разделения к органическому слою по каплям при интенсивном перемешивании при комнатной температуре добавляли пентан. После добавления приблизительно 3 мл пентана раствор значительно помутнел. Смесь перемешивалась при комнатной температуре в течение 15 мин. Затем к смеси быстро добавили по каплям еще 7.5 мл пентана и перемешивали при комнатной температуре в течение 1 ч, после чего оставили на ночь. Полученный таким образом аторвастатин отделили на вакуумфильтре, промыли пентаном (2 мл), высушили на воздухе до постоянного веса и растерли в агатовой ступке. Было получено 0,6 г аморфного аторвастатина. Пример 8. Использовался способ, описанный в примере 7, однако для экстракции кислоты применялся не диэтиловый эфир, а этилацетат. Было получено аналогичное количество аторвастатина. Пример 9. Использовался способ, описанный в примере 7, однако для осаждения применялся не пентан, а гексан. Было получено аналогичное количество аторвастатина. Пример 10. Использовали способ, описанный в примере 7, однако для осаждения применяли не пентан, а гептан. Было получено аналогичное количество аторвастатина. Пример 11. Использовали способ, описанный в примере 7, однако для осаждения применяли не пентан, а циклогексан. Было получено аналогичное количество аторвастатина. Пример 12. Использовали способ, описанный в примере 7, однако для осаждения применялся не пентан, а диэтиловый эфир. Было получено аналогичное количество аторвастатина. Пример 13. Использовали способ, описанный в примере 7, однако для осаждения применяли не пентан, а диизопропиловый эфир. Было получено аналогичное количество аторвастатина. Пример 14. Использовали способ, описанный в примере 7, однако для осаждения применяли не пентан, а третбутилметиловый эфир. Было получено аналогичное количество аторвастатина. Пример 15. Использовали способ, описанный в примере 7, однако перед осаждением гексаном раствор аторвастатина в этилацетате разбавили 5 мл толуола. Пример 16. Использовали способ, описанный в примере 7, однако перед осаждением гексаном раствор аторвастатина в этилацетате разбавили 3 мл трет-бутилметилового эфира.-5 007432 Пример 17. Использовали способ, описанный в примере 7, однако перед осаждением гексаном раствор аторвастатина в этилацетате разбавили 10 мл тетрагидрофурана. Пример 18. Навеску эфира формулы II (1 г) при перемешивании добавили к смеси тетрагидрофурана (15 мл) и 10% HCl (3.5 мл), полученный раствор перемешивали при комнатной температуре в течение 24 ч. Затем в течение 15 мин по каплям добавили к реакционной смеси 40% раствор NaOH (2 мл), и полученную смесь перемешивали при комнатной температуре в течение 17 ч, после чего вылили в делительную воронку,содержащую гексан (10 мл) и деминерализованную воду (30 мл). После тщательного встряхивания и разделения слоев нижний водный слой встряхивали с дополнительным количеством гексана (2x5 мл). Промытый водный слой подкислили 10% HCl до рН=4 и экстрагировали дихлорметаном (1x10 мл, 2x5 мл), к органическому слою добавили триэтиламин (0.3 мл) и высушили над MgSO4. Затем осушитель отфильтровали, промыли сухим дихлорметаном, после чего объединенный органический раствор упарили до постоянного веса в ротационном вакуумном испарителе (приблизительно 0,85 г.). Соль триэтиламмония растворили в этилацетате (10 мл) и раствор перенесли в делительную воронку. В воронку добавили раствор моногидрата ацетата кальция (0.13 г) в деминерализованной воде (1 мл), и содержимое воронки встряхивали. После отделения водного слоя органический слой встряхивали с водой. После разделения к органическому слою по каплям при интенсивном перемешивании при комнатной температуре добавляли гексан. Полученный таким образом аторвастатин отделили на вакуум-фильтре, промыли гексаном (2 мл),высушили на воздухе до постоянного веса и растерли в агатовой ступке. Было получено 0.6 г аморфного аторвастатина. Пример 19. К навеске эфира формулы II (5 г, 7.6 ммоль) добавили тетрагидрофуран (75 мл) и, после полного растворения вещества, 10% HCl (17 мл). Смесь перемешивали при комнатной температуре в течение 24 ч. Затем в течение 5 мин по каплям добавили к реакционной смеси 40% раствор NaOH (10 мл), и неоднородную смесь перемешивали при комнатной температуре в течение 17 ч, после чего вылили в делительную воронку, содержащую деминерализованную воду (150 мл) и гексан (50 мл). После тщательного встряхивания и повторной экстракции гексаном водный слой подкислили 5 мл концентрированной HCl и экстрагировали этилацетатом (4 х 20 мл). После промывания раствором соли (2x10 мл) к органическому слою добавили триэтиламин (1.5 мл), и трижды встряхивали с деминерализованной водой (10 мл), содержавшей всего 1 г ацетата кальция на 10 мл воды. Полученный раствор промывали деминерализованной водой (2x5 мл) и сушили сульфатом магния (10 г) в течение 1 ч. После этого к осушенному раствору при интенсивном перемешивании добавили гексан (50 мл). Полученную таким образом нерастворимую субстанцию после перемешивания в течение 1 ч отделили на вакуум-фильтре. После сушки было получено 3,35 г аморфного аторвастатина. Пример 20. Использовался способ, описанный в примере 19, однако вместо триэтиламина было использовано эквивалентное количество 40% водного раствора метиламина. Пример 21. Использовался способ, описанный в примере 19, однако вместо триэтиламина было использовано эквивалентное количество 35% водного раствора аммиака. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ получения аморфной формы полукальциевой соли (3R,5R)-7-[3-фенил-4-фенилкарбамил 2-(4-фторфенил)-5-изопропилпиррол-1-ил]-3,5-дигидроксигептановой кислоты формулы (I)-6 007432 подвергают сначала кислотному гидролизу, а затем щелочному гидролизу с образованием соли (3R,5R)7-[3-фенил-4-фенилкарбамил-2-(4-фторфенил)-5-изопропилпиррол-1-ил]-3,5-дигидроксигептановой кислоты с щелочным металлом, которую затем после необязательного подкисления экстрагируют органическим растворителем, выбранным из группы сложных эфиров С 1-С 5-кислот и С 1-С 5-спиртов, и после операций очистки превращают путем обработки солью кальция, гидроксидом кальция или С 1-С 5 алкоголятом кальция в полукальциевую соль, которую осаждают с помощью С 5-С 12-углеводорода или диалкилового эфира формулы R1OR2, где R1 и R2 представляют собой С 1-С 5-алкильные группы. 2. Способ по п.1, отличающийся тем, что раствор соли (3R,5R)-7-[3-фенил-4-фенилкарбамил-2-(4 фторфенил)-5-изопропил-пиррол-1-ил]-3,5-дигидроксигептановой кислоты с катионом щелочного металла, полученный из соединения формулы (II), содержащий избыток хлорида и гидроксида соответствующего катиона, подкисляют и экстрагируют с получением раствора (3R,5R)-7-[3-фенил-4 фенилкарбамил-2-(4-фторфенил)-5-изопропилпиррол-1-ил]-3,5-дигидроксигептановой кислоты, который затем превращают путем реакции с гидроксидом или алкоголятом кальция в раствор полукальциевой соли. 3. Способ по п.1 или 2, отличающийся тем, что раствор (3R,5R)-7-[3-фенил-4-фенилкарбамил-2-(4 фторфенил)-5-изопропилпиррол-1-ил]-3,5-дигидроксигептановой кислоты в соответствующем сложном эфире С 1-С 5-кислоты и С 1-С 5-спирта превращают в раствор соли щелочного металла. 4. Способ по любому из пп.1-3, отличающийся тем, что полукальциевую соль осаждают из раствора в этилацетате. 5. Способ по любому из пп.1-4, отличающийся тем, что осаждение проводят путем добавления неполярного растворителя, выбранного из группы, включающей пентан, гексан, гептан, циклогексан, или диалкилового эфира формулы R1OR2, где R1 и R2 - С 1-С 5-алкильные группы, к раствору полукальциевой соли (3R,5R)-7-[3-фенил-4-фенилкарбамил-2-(4-фторфенил)-5-изопропил-пиррол-1-ил]-3,5-дигидроксигептановой кислоты в соответствующем растворителе. 6. Способ по любому из пп.1-5, отличающийся тем, что раствор полукальциевой соли (3R,5R)-7-[3 фeнил-4-фeнилкapбaмил-2-(4-фтopфeнил)-5-изoпpoпил-пиppoл-l-ил]-3,5-дигидроксигептановой кислоты в сложном эфире С 1-С 5-кислоты и С 1-С 5-спирта добавляют к неполярному растворителю, выбранному из группы, включающей пентан, гексан, гептан и циклогексан, или к диалкиловому эфиру формулы R1OR2,где R1 и R2 - С 1-С 5-алкильные группы. 7. Способ по любому из пп.1-6, отличающийся тем, что раствор полукальциевой соли (3R,5R)-7-[3 фенил-4-фенилкарбамил-2-(4-фторфенил)-5-изопропилпиррол-1-ил]-3,5-дигидроксигептановой кислоты в сложном эфире перед осаждением разбавляют 5-95%, предпочтительно 30-70%, дополнительного растворителя. 8. Способ по п.7, отличающийся тем, что в качестве дополнительного растворителя используют толуол, трет-бутилметиловый эфир или тетрагидрофуран.
МПК / Метки
МПК: C07D 207/34
Метки: аторвастатина, 3-фенил-4-фенилкарбамил-2-(4-фторфенил)-5-изопропил-пиррол-1-ил]-3, формы, 5-дигидроксигептановой, полукальциевой, способ, получения, кислоты, аморфной, соли
Код ссылки
<a href="https://eas.patents.su/9-7432-sposob-polucheniya-amorfnojj-formy-polukalcievojj-soli-3r-5r-7-3-fenil-4-fenilkarbamil-2-4-ftorfenil-5-izopropil-pirrol-1-il-3-5-digidroksigeptanovojj-kisloty-atorvastatina.html" rel="bookmark" title="База патентов Евразийского Союза">Способ получения аморфной формы полукальциевой соли (3r, 5r) -7- [3-фенил-4-фенилкарбамил-2-(4-фторфенил)-5-изопропил-пиррол-1-ил]-3, 5-дигидроксигептановой кислоты (аторвастатина)</a>
Предыдущий патент: Андрогенная фармацевтическая композиция и способ для лечения депрессии
Следующий патент: Макролиды
Случайный патент: Способ и устройство для получения минеральных волокон