Фармацевтическая композиция, включающая кетопрофен и полиоксиалкиленовый эфир жирной оксикислоты
Формула / Реферат
1. Фармацевтическая композиция, включающая (i) кетопрофен; (ii) по меньшей мере один полиоксиалкиленовый эфир жирной оксикислоты; (iii) по меньшей мере одно гидроксизамещенное органическое соединение, выбранное из группы, состоящей по меньшей мере из одного спирта, по меньшей мере одного полиола и их смесей; и (iv) воды, при этом по меньшей мере один полиоксиалкиленовый эфир жирной оксикислоты получен в результате этерификации жирной оксикислоты, содержащей от 8 до 30 атомов углерода, полиоксиалкиленом с молекулярным весом в интервале от 200 до 6000, по меньшей мере один спирт выбран из группы, включающей этанол, 1-пропанол, 2-пропанол и их смеси, и по меньшей мере один полиол выбран из группы, включающей глицерин, пропиленгликоль, 1,3-бутиленгликоль и их смеси.
2. Фармацевтическая композиция по п.1, отличающаяся тем, что жирная оксикислота содержит от 14 до 24 атомов углерода и полиоксиалкилен имеет молекулярный вес в интервале от 400 до 1500.
3. Фармацевтическая композиция по любому из пп.1 и 2, отличающаяся тем, что жирная оксикислота представляет собой насыщенную или ненасыщенную жирную оксикислоту, выбранную из группы, состоящей из гидроксикаприловой кислоты, гидроксикапроновой кислоты, гидроксилауриновой кислоты, гидроксимиристиновой кислоты, гидроксипальмитиновой кислоты, гидроксистеариновой кислоты, гидроксиарахидовой кислоты, гидроксибегеновой кислоты, гидроксилигноцериновой кислоты, гидроксимиристолевой кислоты, гидроксипальмитолевой кислоты, гидроксиолеиновой кислоты, гидроксилинолевой кислоты, гидроксилиноленовой кислоты, гидроксиарахидоновой кислоты, гидроксиэйкозапентаеновой кислоты, гидроксиэруковой кислоты и гидроксидокозагексаеновой кислоты.
4. Фармацевтическая композиция по п.3, отличающаяся тем, что жирная оксикислота представляет собой насыщенную жирную оксикислоту, выбранную из группы, состоящей из гидроксилауриновой кислоты, гидроксимиристиновой кислоты, гидроксипальмитиновой кислоты, гидроксистеариновой кислоты и гидроксиарахидовой кислоты.
5. Фармацевтическая композиция по любому из пп.1-4, отличающаяся тем, что полиоксиалкилен выбран из группы, состоящей из полиэтиленгликоля 200 (PEG 200), полиэтиленгликоля 300 (PEG 300), полиэтиленгликоля 400 (PEG 400), полиэтиленгликоля 600 (PEG 600), полиэтиленгликоля 660 (PEG 660), полиэтиленгликоля 1000 (PEG 1000), полиэтиленгликоля 1500 (PEG 1500), полиэтиленгликоля 3000 (PEG 3000), полиэтиленгликоля 3350 (PEG 3350), полиэтиленгликоля 4000 (PEG 4000), полиэтиленгликоля 6000 (PEG 6000) и их смесей.
6. Фармацевтическая композиция по любому из пп.3-5, отличающаяся тем, что по меньшей мере один полиоксиалкиленовый эфир жирной оксикислоты выбран из группы, состоящей из полиэтиленгликоль 660 гидроксистеарата (SolutolÔ HS 15), полигликолевого эфира полиэтиленгликоля и 12-гидроксистеариновой кислоты и их смесей.
7. Фармацевтическая композиция по любому из пп.1-6, отличающаяся тем, что композиция включает количество кетопрофена в интервале значений от 2 до 15% (вес./об.), предпочтительно между 5 и 10% (вес./об.) или около 10% (вес./об.).
8. Фармацевтическая композиция по любому из пп.1-7, отличающаяся тем, что композиция включает количество по меньшей мере одного полиоксиалкиленового эфира жирной оксикислоты в интервале значений от 1 до 20% (вес./об.), предпочтительно от 2 до 15% (вес./об.), или от 5 до 15% (вес./об.). или от около 5 до около 10% (вес./об.).
9. Фармацевтическая композиция по любому из пп.1-8, отличающаяся тем, что композиция включает количество по меньшей мере одного спирта в интервале значений от 1 до 30% (вес./об.) или от 2 до 20% (вес./об.).
10. Фармацевтическая композиция по любому из пп.1-9, отличающаяся тем, что композиция включает количество по меньшей мере одного полиола в интервале значений от 1 до 30% (вес./об.) или от 2 до 20% (вес./об.).
11. Фармацевтическая композиция по любому из пп.1-10, отличающаяся тем, что композиция включает смесь по меньшей мере одного спирта и по меньшей мере одного полиола, где концентрация по меньшей мере одного спирта составляет от 5 до 15% (вес./об.) и концентрация по меньшей мере одного полиола составляет от 5 до 15% (вес./об.).
12. Фармацевтическая композиция по любому из пп.1-11, отличающаяся тем, что рН композиции составляет величину в интервале от 6,5 до 8,5 или от 7,0 до 8,0.
Текст
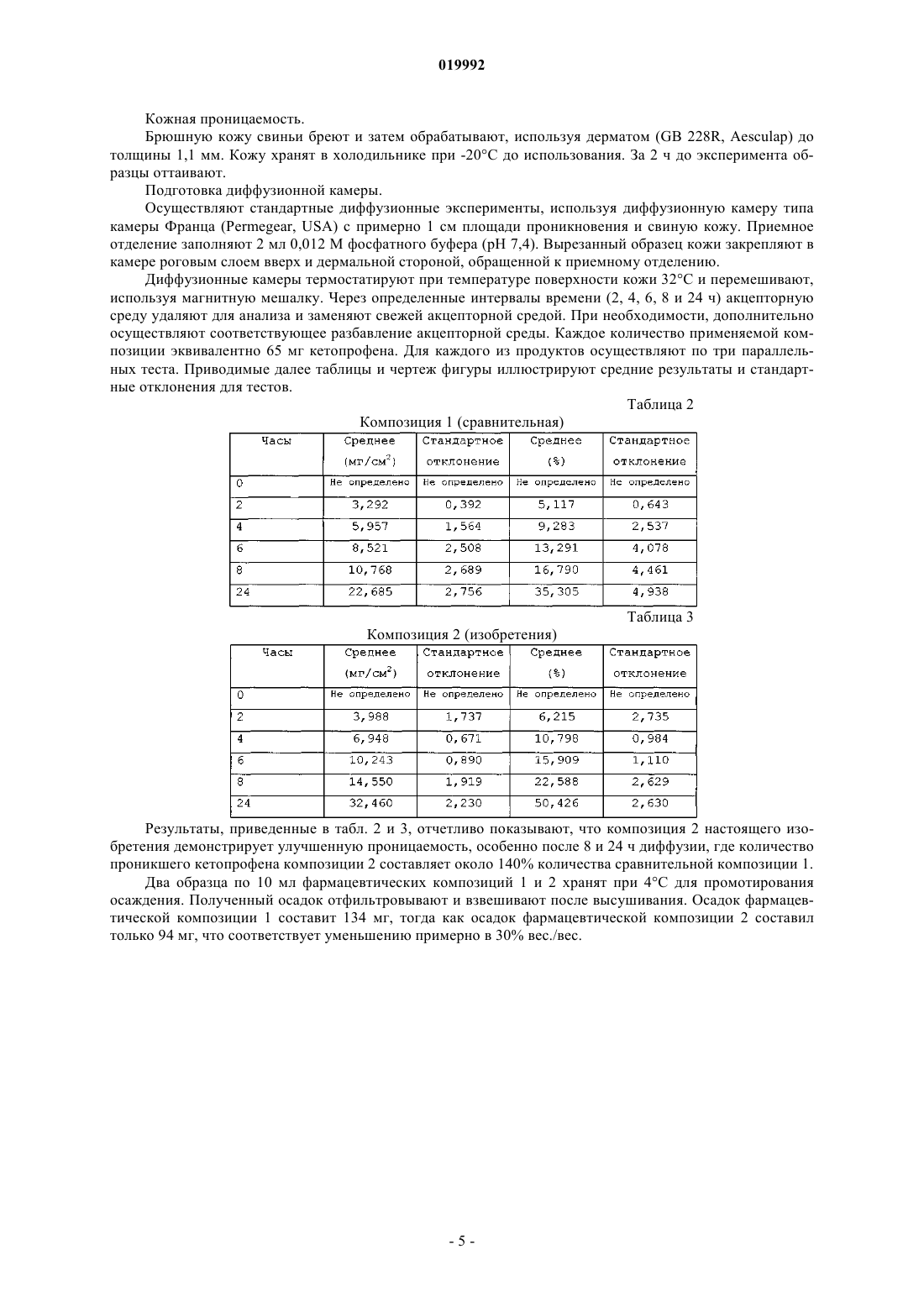
ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ВКЛЮЧАЮЩАЯ КЕТОПРОФЕН И ПОЛИОКСИАЛКИЛЕНОВЫЙ ЭФИР ЖИРНОЙ ОКСИКИСЛОТЫ Изобретение относится к фармацевтической композиции, включающей (i) кетопрофен; (ii) по меньшей мере один полиоксиалкиленовый эфир жирной оксикислоты; (iii) по меньшей мере одно гидроксизамещенное органическое соединение, выбранное из группы, состоящей по меньшей мере из одного спирта, по меньшей мере одного полиола и их смесей; и (iv) воды.(71)(73) Заявитель и патентовладелец: ЛЕКТИО ФАРМАЭНТВИКЛУНГСУНД ФЕРВЕРТУНГС ГМБХ (AT) Область, к которой относится настоящее изобретение Настоящее изобретение относится к фармацевтической композиции, включающей кетопрофен. Более конкретно, настоящее изобретение относится к фармацевтической композиции, включающей кетопрофен, для местного нанесения, обладающей повышенной проницаемостью и биодоступностью. Предпосылки изобретения Кетопрофен является членом группы арилпропионовых кислот нестероидных противовоспалительных лекарственных средств ("НПВС") с химическим наименованием 2-(3-бензоилфенил)пропионовая кислота (CAS RN: 22071-15-4), обладающим исключительными анальгетическими, противовоспалительными, антипиретическими и противоревматическими свойствами. Обычная дозировка для кетопрофена,который обычно вводят в кислотной форме, состоит из двух суточных доз по 100 мг или трех суточных доз по 50 мг. Точный метаболизм кетопрофена неизвестен, однако было установлено, что он также интенсивно метаболизируется в печени. Кетопрофен был введен в 1986 г. и приобрел широкое одобрение и применение для облегчения признаков и симптомов ревматоидного артрита и остеоартрита и для лечения дисменореи. Кетопрофен используют отдельно или в качестве вспомогательного вещества при лечении острой желчной колики,боли, связанной с почечной коликой, боли, связанной с хирургией в полости рта, сильной посттравматической боли и простуды. (PDR Generics, 1996, second edition, Medical Economics, Montvale, New Jersey,p. 1812). Кетопрофен можно использовать для костной регенерации (Alfano, М.С.; Troullos, E.S., USPatent No. 5902110). Однако очень трудно обеспечивать пациенту терапевтически эффективные уровни в плазме такого типа лекарственных средств с помощью лекарственной формы из-за малой скорости проникновения через кожу. Кетопрофен обычно вводят перорально в форме обычных таблеток или таблеток с покрытиями, устойчивыми в отношении желудочного сока, или ректально, или путем инъекций или поверхностно. Пероральное введение кетопрофена может вызвать серьезные вредные эффекты, наиболее ощутимо желудочно-кишечные нарушения, такие как диспепсия, гастродуоденальные кровотечения, язвы желудка и гастриты, особенно после длительного применения. Поэтому в последние годы были предприняты интенсивные исследования не пероральной доставки кетопрофена в попытке свести к минимуму вредные эффекты, связанные с пероральным введением. Лекарственные формы для наружного применения представляют собой привлекательные варианты,так как они позволяют избежать печеночного пресистемного метаболизма, уменьшить побочные эффекты, связанные с пероральным способом введения, они связаны с более точным соблюдением пациентом предписанного режима лечения и в некоторых случаях повышают терапевтическую эффективность лекарственных средств. Однако эффективность местного введения кетопрофена ограничена трудностью проникновения таких лекарственных средств через кожу и слабой растворимостью в воде. В некоторых патентах и патентных заявках были предприняты попытки решения вышеуказанных проблем с помощью лекарственных форм для наружного применения, содержащих несколько ингредиентов для повышения проницаемости кетопрофена. В патенте США 5654337 раскрыта фармацевтическая композиция для доставки НПВС, подобных ибупрофену или кетопрофену, через кожу, которая включает биосовместимый органический растворитель, полярный липид, поверхностно-активный агент, воду, мочевину и НПВС, которое необходимо доставить, при рН от около 6,0 до 8,0, где полярный липид представляет собой лецитин или фосфатидилхолин, биосовместимый органический растворитель представляет собой изопропиловый эфир, выбранный из группы, состоящей из изопропилмиристата и изопропилпальмитата, и мочевина присутствует в концентрации от около 5 до 20 мас.% конечной композиции. В патенте США 5885597 раскрыта композиция для местного применения, включающая анальгетик типа арилпропионовой кислоты, такой как ибупрофен или кетопрофен, и такое количество по меньшей мере одного фосфолипида, которое эффективно повышает проницаемость кожи, такого как лецитин и по меньшей мере один сополимер полиоксиэтиленполиоксипропилена. В патенте США 6083996 раскрыта водная фармацевтическая композиция полутвердой консистентности для местного нанесения НПВЛС, таких как кетопрофен, включающая (i) не основный полимерный усилитель проницаемости через кожу, выбранный из диспергируемого в воде кислотного полимера, полисахаридной смолы и их смесей; и (ii) липофильную смесь растворителей из алифатических С 2-C8 спиртов и алифатических С 8-C30 сложных эфиров. В патентах США 6759056 и 6946144 раскрыта система трансдермальной доставки, включающая смесь НПВЛС, такого как кетопрофен, этоксилированного масла, спирта и водного адъюванта, такого как вода или экстракты алоэ вера. ЕР 756870 раскрывает и заявляет фармацевтическую композицию спрея для местного применения,включающую водно-спиртовой раствор из кетопрофена, пропиленгликоля, полоксамеров или полиоксиэтилированного касторового масла, поливинилпирролидона и этаноламина. Касторовое масло представляет собой растительное триглицеридное масло, включающее ненасыщенные жирные кислоты, в кото-1 019992 ром приблизительно 90% цепочек жирных кислот представляет собой рицинолеиновую кислоту, с небольшими но значительными количествами олеиновой и линолевой кислот. Полиоксиэтилированное касторовое масло представляет собой продукт реакции касторового масла с этиленоксидом, где гидроксильные группы триглицерида касторового масла были этоксилированы этиленоксидом с образованием полиэтиленгликольных эфиров. Полиоксиэтилированное касторовое масло коммерчески доступно под торговой маркой Cremophor EL от BASF Corp. ЕР 707847 раскрывает кетопрофеновый липосомный гель и способ его получения, который отличается простотой способа получения за счет спонтанного образования кетопрофенсодержащих липосом из фосфолипидов или неионных амфифилов (таких как Cremophor RH 40, полиоксиэтилированное гидрированное касторовое масло, коммерчески доступное от BASF Corp). Гелевая композиция для местного применения, включающая кетопрофен, продается в ЕвропеPharmaforschungs GmbH под торговой маркой Ketospray. Композиция включает соевый лецитин в качестве солюбилизатора и спирты и гликоли в качестве сорастворителей. Другие подробности, касающиеся состава, можно найти в патенте США 5958379, в котором раскрыта распыляемая жидкая фармацевтическая композиция, содержащая по меньшей мере одно активное вещество, по меньшей мере один гель-образующий агент, состоящий из фосфолипида или смеси фосфолипидов, спирта или смеси легко испаряющихся спиртов и воды. Сущность изобретения Заявителю стало понятно, что, несмотря на ряд предпринятых специалистами попыток, все еще существует необходимость в создании фармацевтической композиции для местного введения кетопрофена,обладающей улучшенной проницаемостью и биодоступностью. Заявителю также стало понятно, что все еще существует необходимость в создании фармацевтической композиции для местного введения кетопрофена, включающей высокую концентрацию кетопрофена, такую как, например, выше чем 5% вес./об., и даже столь высокую, как 10% вес./об. или более, в виде жидкой композиции, которую можно использовать в виде спрея и/или можно распылять на поверхности кожи и/или слизистой, которые требуют обработки. Заявитель обнаружил, что вышеупомянутые проблемы можно преодолеть с помощью фармацевтической композиции, включающей (i) кетопрофен; (ii) по меньшей мере один полиоксиалкиленовый эфир жирной оксикислоты; (iii) по меньшей мере одно гидроксизамещенное органическое соединение, выбранное из группы, состоящей из спиртов, полиолов и их смесей; и (iv) воды. Заявитель неожиданно обнаружил, что фармацевтическая композиция настоящего изобретения обладает улучшенными характеристиками проницаемости и биодоступности. Более того, заявитель неожиданно обнаружил, что фармацевтическая композиция настоящего изобретения позволяет уменьшить образование осадка при хранении при низкой температуре около 0 С. Краткое описание чертежей Фигура демонстрирует диффузионные профили фармацевтической композиции 1 (линия 1) и 2 (линия 2), раскрытые в примерах. По оси ординат отложены значения, представляющие проникшее кумулятивное количество, выраженное в миллиграммах на квадратный сантиметр (мг/см 2), по оси абсцисс отложены значения, представляющие промежуток времени, выраженный в часах (ч). Подробное описание предпочтительного варианта изобретения Фармацевтическая композиция настоящего изобретения может демонстрировать одну или более из раскрытых здесь предпочтительных характеристик. Концентрация кетопрофена в фармацевтической композиции настоящего изобретения составляет предпочтительно величину между 2 и 15% (вес./об.), более предпочтительно между 5 и 10% (вес./об.). Предпочтительно, если концентрация кетопрофена в фармацевтической композиции настоящего изобретения составляет около 10% (вес./об.). Предпочтительно, если указанный по меньшей мере один полиоксиалкиленовый эфир жирной оксикислоты получают в результате этерификации жирной оксикислоты, содержащей от 8 до 30 атомов углерода, предпочтительно от 14 до 24 атомов углерода, полиоксиалкиленом с молекулярным весом в интервале от 200 до 6000, предпочтительно от 400 до 1500. Предпочтительно, если указанные жирные оксикислоты выбирают из группы кислот, содержащих насыщенные цепочки, таких как гидроксикаприловая кислота, гидроксикапроновая кислота, гидроксилауриновая кислота, гидроксимиристиновая кислота, гидроксипальмитиновая кислота, гидроксистеариновая кислота, гидроксиарахидовая кислота, гидроксибегеновая кислота, гидроксилигноцериновая кислота, и кислот, содержащих ненасыщенные цепочки, таких как гидроксимиристолевая кислота, гидроксипальмитолевая кислота, гидроксиолеиновая кислота, гидроксилинолевая кислота, гидроксилиноленовая кислота, гидроксиарахидоновая кислота, гидроксиэйкозапентаеновая кислота, гидроксиэруковая кислота и гидроксидокозагексаеновая кислота. Наиболее подходящие жирные оксикислоты выбирают из группы насыщенных жирных оксикислот,включающей гидроксилауриновую кислоту, гидроксимиристиновую кислоту, гидроксипальмитиновую кислоту, гидроксистеариновую кислоту и гидроксиарахидиновую кислоту. Заявитель обнаружил, что использование насыщенных жирных оксикислот предпочтительно, так как присутствие ненасыщенности в цепочках жирных кислот может привести к разложению в результате окисления и сократить срок жизни фармацевтической композиции. Особенно предпочтительной жирной оксикислотой является гидроксистеариновая кислота. Предпочтительно, если указанный полиоксиалкилен выбирают из группы, включающей полиэтиленгликоль 200 (PEG 200), полиэтиленгликоль 300 (PEG 300), полиэтиленгликоль 400 (PEG 400), полиэтиленгликоль 600 (PEG 600), полиэтиленгликоль 660 (PEG 660), полиэтиленгликоль 1000 (PEG 1000),полиэтиленгликоль 1500 (PEG 1500), полиэтиленгликоль 3000 (PEG 3000), полиэтиленгликоль 3350(PEG 3350), полиэтиленгликоль 4000 (PEG 4000), полиэтиленгликоль 6000 (PEG 6000) и их смесей. В соответствии с предпочтительным вариантом указанный полиоксиалкилен включает полиэтиленгликоль 400 (PEG 400), полиэтиленгликоль 600 (PEG 600), полиэтиленгликоль 660 (PEG 660), полиэтиленгликоль 1000 (PEG 1000), полиэтиленгликоль 1500 (PEG 1500) и их смеси. В соответствии с предпочтительным вариантом настоящего изобретения по меньшей мере один указанный полиоксиалкиленовый эфир жирной оксикислоты выбирают из группы, состоящей из Solutol HS 15 (полиэтиленгликоль 660 гидроксистеарат - Ph. Eur. Name: Макрогол 15 Гидроксистеарат),полигликолевого эфира полиэтиленгликоля и 12-гидроксистеариновой кислоты и их смесей.Solutol HS 15 представляет собой полиэтиленгликоль 660 гидроксистеарат, изготовляемый BASF(Parsippany, N.J.). Помимо свободного полиэтиленгликоля и его мономеров детектируются также сложные диэфиры. В соответствии с данными изготовителей типичный лот Solutol HS 15 содержит приблизительно 30% свободного полиэтиленгликоля и 70% сложных эфиров полиэтиленгликоля. Концентрация указанного по меньшей мере одного полиоксиалкиленового эфира жирной оксикислоты в фармацевтической композиции настоящего изобретения предпочтительно составляет от 1 до 20%(вес./об.), более предпочтительно от 2 до 15% (вес./об.) и наиболее предпочтительно от 5 до 15%(вес./об.). Предпочтительно, если концентрация эфиров полиоксиалкиленовых жирных оксикислот составляет от около 5 до около 10% (вес./об.). Предпочтительно, если фармацевтическая композиция настоящего изобретения включает по меньшей мере один спирт или по меньшей мере один полиол или их смесь. Предпочтительно, если указанный по меньшей мере один спирт выбирают из группы, включающей фармацевтически приемлемые спирты, такие как, например, этанол, 1-пропанол, 2-пропанол и их смеси. Предпочтительно, если указанный по меньшей мере один полиол выбирают из группы, включающей фармацевтически приемлемые полиолы, такие как, например, глицерин, пропиленгликоль,1,3-бутиленгликоль и их смеси. Предпочтительно, если фармацевтическая композиция настоящего изобретения включает смесь 2-пропанола и глицерина. Более предпочтительно, если фармацевтическая композиция настоящего изобретения включает смесь 2-пропанола и пропиленгликоля. Концентрация указанного по меньшей мере одного спирта в фармацевтической композиции настоящего изобретения составляет предпочтительно от 1 до 30% (вес./об.), более предпочтительно от 2 до 20% (вес./об.). Концентрация указанного по меньшей мере одного полиола в фармацевтической композиции настоящего изобретения составляет предпочтительно от 1 до 30% (вес./об.), более предпочтительно от 2 до 20% (вес./об.). Предпочтительно, если фармацевтическая композиция настоящего изобретения включает смесь по меньшей мере одного спирта и по меньшей мере одного полиола. После смешивания вместе полная концентрация указанного по меньшей мере одного спирта и указанного по меньшей мере одного полиола в фармацевтической композиции настоящего изобретения составляет предпочтительно от 1 до 30%(вес./об.), более предпочтительно от 10 до 30% (вес./об.). В таком случае предпочтительно, если концентрация указанного по меньшей мере одного спирта находится в интервале значений от 5 до 15% (вес./об.) и концентрация указанного по меньшей мере одного полиола находится в интервале значений от 5 до 15% (вес./об.). Величина рН фармацевтической композиции настоящего изобретения находится предпочтительно в интервале значений от 6,5 до 8,5, более предпочтительно от 7,0 до 8,0. Предпочтительно, если величина рН фармацевтической композиции настоящего изобретения находится в интервале значений от 7,3 до 7,6. Фармацевтическая композиция настоящего изобретения может включать далее несколько добавок,которые общеизвестны и используются специалистами. Такие несущественные добавки в фармацевтической композиции настоящего изобретения представляют собой, например, стабилизаторы, антиоксиданты, корректоры рН, буферы, поверхностно-активные агенты, красители и/или ароматизаторы. Фармацевтическую композицию в соответствии с настоящим изобретением можно приготовить в форме препаратов, которые обычно используют как формы препаратов для наружного применения. Предпочтительные для использования препаративные формы включают, но конкретно ими не ограничиваются, различные растворы, мази, кремы, спреи, пены, согревающие пластыри и т.п. Препараты для наружного применения в форме растворов и спреев особенно предпочтительны. Фармацевтическую композицию настоящего изобретения можно использовать в качестве анальгетиков для лечения различного типа боли, включая как хронические боли, так и эпизоды острой боли, например, для лечения скелетно-мышечных повреждений и повреждений суставов, таких как ревматоидный артрит, остеоартрит и анкилозирующий спондилоартрит; периартикулярные нарушения, такие как бурсит и тендонит; повреждения мягких тканей, такие как вывихи и растяжения; и других болезненных состояний, подобных тем, которые наблюдаются после некоторых хирургических процедур. Приводимые далее примеры проиллюстрируют по меньшей мере один вариант осуществления настоящего изобретения, однако, без какого-либо ограничения сущности изобретения, которое требуется запатентовать, которая определена в прилагаемой формуле изобретения. Пример 1. Сравнительная фармацевтическая композиция 1 представляет собой коммерческую фармацевтическую композицию, продаваемую Cyathus Exquirere Pharmaforschungs GmbH под торговой маркой Ketospray. Фармацевтическая композиция 2 настоящего изобретения содержит ингредиенты, указанные в табл. 1. Таблица 1 Фармацевтическую композицию 2 получают следующим образом. В реактор, снабженный магнитной мешалкой, помещают кетопрофен, Solutol HS 15, пропиленгликоль и изопропиловый спирт. Полученную смесь перемешивают около 20 мин, получая гомогенную массу (смесь А). В отдельный реактор, снабженный магнитной мешалкой, помещают NaH2PO4H2O, Na2HPO412H2O и воду. Полученную смесь перемешивают около 20 мин, получая прозрачный бесцветный раствор (смесь В). Затем смесь В медленно добавляют при перемешивании к смеси А. Перемешивание продолжают около 10 мин, получая молочный раствор с рН около 4,7. Величину рН доводят до 7,4, используя NaOH 10 н., получая прозрачный раствор. В конце к раствору добавляют масло перечной мяты и объем доводят до 100 мл, используя очищенную воду. Для сравнения кожной проницаемости для кетопрофена проводят стандартные диффузионные эксперименты, используя диффузионные камеры типа камеры Франца, через свиную кожу. ВЭЖХ анализ для количественного определения кетопрофена использует способ, раскрытый С.Valenta, M. Wanka, и J. Heidlas, "Evaluation of novel-soja lecithin formulations for dermal use containing ketoprofen as a model drug", J. Contr. ReI. 63, 165-173 (2000). Анализ осуществляют, используя ВЭЖХ (Perkin Elmer, US) с автоматическим пробоотборником,состоящим из автоматического автосэмплера ISS-200, насоса и УФ-диодно-матричного детектора. Колонку (2404 мм) с набивкой Nucelosil 100 - 5 С 18 элюируют при 45 С подвижной фазой, состоящей из ацетонитрила и фосфатного буфера, рН 5 (40:60 об./об.) при скорости потока 1,0 мл/мин. Концентрацию кетопрофена определяют путем сравнения пиковых площадей неизвестного со стандартной калибровочной кривой. Стандартные растворы содержат между 0,052 и 0,0065 мг/мл кетопрофена. Линейный регрессионный анализ пиковых площадей дает коэффициент корреляции 0,9965. Образцы (20 мкл) отбирают из приемной камеры и инжектируют непосредственно, используя автоматический дозатор. Параметры. Исходный раствор: 1,042 мг/мл метанол. Колонка: Nucleosil C18. Подвижная фаза: ацетонитрил/фосфатный буфер рН 5 (40:60/об.:об.). УФ-детектирование макс: 260 нм. Скорость потока: 1,0 мл/мин. Время удерживания: около 5,5 мин. Кожная проницаемость. Брюшную кожу свиньи бреют и затем обрабатывают, используя дерматом (GB 228R, Aesculap) до толщины 1,1 мм. Кожу хранят в холодильнике при -20 С до использования. За 2 ч до эксперимента образцы оттаивают. Подготовка диффузионной камеры. Осуществляют стандартные диффузионные эксперименты, используя диффузионную камеру типа камеры Франца (Permegear, USA) с примерно 1 см площади проникновения и свиную кожу. Приемное отделение заполняют 2 мл 0,012 М фосфатного буфера (рН 7,4). Вырезанный образец кожи закрепляют в камере роговым слоем вверх и дермальной стороной, обращенной к приемному отделению. Диффузионные камеры термостатируют при температуре поверхности кожи 32 С и перемешивают,используя магнитную мешалку. Через определенные интервалы времени (2, 4, 6, 8 и 24 ч) акцепторную среду удаляют для анализа и заменяют свежей акцепторной средой. При необходимости, дополнительно осуществляют соответствующее разбавление акцепторной среды. Каждое количество применяемой композиции эквивалентно 65 мг кетопрофена. Для каждого из продуктов осуществляют по три параллельных теста. Приводимые далее таблицы и чертеж фигуры иллюстрируют средние результаты и стандартные отклонения для тестов. Таблица 2 Композиция 1 (сравнительная) Результаты, приведенные в табл. 2 и 3, отчетливо показывают, что композиция 2 настоящего изобретения демонстрирует улучшенную проницаемость, особенно после 8 и 24 ч диффузии, где количество проникшего кетопрофена композиции 2 составляет около 140% количества сравнительной композиции 1. Два образца по 10 мл фармацевтических композиций 1 и 2 хранят при 4 С для промотирования осаждения. Полученный осадок отфильтровывают и взвешивают после высушивания. Осадок фармацевтической композиции 1 составит 134 мг, тогда как осадок фармацевтической композиции 2 составил только 94 мг, что соответствует уменьшению примерно в 30% вес./вес. Фармацевтические композиции 3-7 подвергались той же самой процедуре оценки кожной проницаемости, что и в примере 1, и сравнивались с фармацевтической композицией 1. Полученные результаты демонстрируют улучшения кожной проницаемости для фармацевтических композиций 3-7 по сравнению с фармацевтической композицией 1. Пример 3. Фармацевтические композиции 8-10 содержат ингредиенты, представленные в табл. 5. Таблица 5 Фармацевтические композиции 8-10 подвергались той же самой процедуре оценки кожной проницаемости, что и в примере 1, и сравнивались с фармацевтической композицией 1. Полученные результаты демонстрируют улучшения кожной проницаемости для фармацевтических композиций 8-10 по сравнению с фармацевтической композицией 1. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Фармацевтическая композиция, включающая (i) кетопрофен; (ii) по меньшей мере один полиоксиалкиленовый эфир жирной оксикислоты; (iii) по меньшей мере одно гидроксизамещенное органическое соединение, выбранное из группы, состоящей по меньшей мере из одного спирта, по меньшей мере одного полиола и их смесей; и (iv) воды, при этом по меньшей мере один полиоксиалкиленовый эфир жирной оксикислоты получен в результате этерификации жирной оксикислоты, содержащей от 8 до 30 атомов углерода, полиоксиалкиленом с молекулярным весом в интервале от 200 до 6000, по меньшей мере один спирт выбран из группы, включающей этанол, 1-пропанол, 2-пропанол и их смеси, и по меньшей мере один полиол выбран из группы, включающей глицерин, пропиленгликоль,1,3-бутиленгликоль и их смеси. 2. Фармацевтическая композиция по п.1, отличающаяся тем, что жирная оксикислота содержит от 14 до 24 атомов углерода и полиоксиалкилен имеет молекулярный вес в интервале от 400 до 1500. 3. Фармацевтическая композиция по любому из пп.1 и 2, отличающаяся тем, что жирная оксикислота представляет собой насыщенную или ненасыщенную жирную оксикислоту, выбранную из группы,состоящей из гидроксикаприловой кислоты, гидроксикапроновой кислоты, гидроксилауриновой кислоты, гидроксимиристиновой кислоты, гидроксипальмитиновой кислоты, гидроксистеариновой кислоты,гидроксиарахидовой кислоты, гидроксибегеновой кислоты, гидроксилигноцериновой кислоты, гидроксимиристолевой кислоты, гидроксипальмитолевой кислоты, гидроксиолеиновой кислоты, гидроксилинолевой кислоты, гидроксилиноленовой кислоты, гидроксиарахидоновой кислоты, гидроксиэйкозапентаеновой кислоты, гидроксиэруковой кислоты и гидроксидокозагексаеновой кислоты. 4. Фармацевтическая композиция по п.3, отличающаяся тем, что жирная оксикислота представляет собой насыщенную жирную оксикислоту, выбранную из группы, состоящей из гидроксилауриновой кислоты, гидроксимиристиновой кислоты, гидроксипальмитиновой кислоты, гидроксистеариновой кислоты и гидроксиарахидовой кислоты. 5. Фармацевтическая композиция по любому из пп.1-4, отличающаяся тем, что полиоксиалкилен выбран из группы, состоящей из полиэтиленгликоля 200 (PEG 200), полиэтиленгликоля 300 (PEG 300),полиэтиленгликоля 400 (PEG 400), полиэтиленгликоля 600 (PEG 600), полиэтиленгликоля 660 (PEG 660),полиэтиленгликоля 1000 (PEG 1000), полиэтиленгликоля 1500 (PEG 1500), полиэтиленгликоля 3000 (PEG 3000), полиэтиленгликоля 3350 (PEG 3350), полиэтиленгликоля 4000 (PEG 4000), полиэтиленгликоля 6000 (PEG 6000) и их смесей. 6. Фармацевтическая композиция по любому из пп.3-5, отличающаяся тем, что по меньшей мере один полиоксиалкиленовый эфир жирной оксикислоты выбран из группы, состоящей из полиэтиленгликоль 660 гидроксистеарата (Solutol HS 15), полигликолевого эфира полиэтиленгликоля и 12-гидроксистеариновой кислоты и их смесей. 7. Фармацевтическая композиция по любому из пп.1-6, отличающаяся тем, что композиция включает количество кетопрофена в интервале значений от 2 до 15% (вес./об.), предпочтительно между 5 и 10%(вес./об.) или около 10% (вес./об.). 8. Фармацевтическая композиция по любому из пп.1-7, отличающаяся тем, что композиция включает количество по меньшей мере одного полиоксиалкиленового эфира жирной оксикислоты в интервале значений от 1 до 20% (вес./об.), предпочтительно от 2 до 15% (вес./об.), или от 5 до 15% (вес./об.), или от около 5 до около 10% (вес./об.). 9. Фармацевтическая композиция по любому из пп.1-8, отличающаяся тем, что композиция включает количество по меньшей мере одного спирта в интервале значений от 1 до 30% (вес./об.) или от 2 до 20% (вес./об.). 10. Фармацевтическая композиция по любому из пп.1-9, отличающаяся тем, что композиция включает количество по меньшей мере одного полиола в интервале значений от 1 до 30% (вес./об.) или от 2 до 20% (вес./об.). 11. Фармацевтическая композиция по любому из пп.1-10, отличающаяся тем, что композиция включает смесь по меньшей мере одного спирта и по меньшей мере одного полиола, где концентрация по меньшей мере одного спирта составляет от 5 до 15% (вес./об.) и концентрация по меньшей мере одного полиола составляет от 5 до 15% (вес./об.). 12. Фармацевтическая композиция по любому из пп.1-11, отличающаяся тем, что рН композиции составляет величину в интервале от 6,5 до 8,5 или от 7,0 до 8,0.
МПК / Метки
МПК: A61K 9/12, A61K 47/14, A61K 31/192, A61K 9/06, A61K 9/08, A61K 47/10, A61K 9/70
Метки: эфир, включающая, оксикислоты, композиция, жирной, полиоксиалкиленовый, кетопрофен, фармацевтическая
Код ссылки
<a href="https://eas.patents.su/9-19992-farmacevticheskaya-kompoziciya-vklyuchayushhaya-ketoprofen-i-polioksialkilenovyjj-efir-zhirnojj-oksikisloty.html" rel="bookmark" title="База патентов Евразийского Союза">Фармацевтическая композиция, включающая кетопрофен и полиоксиалкиленовый эфир жирной оксикислоты</a>
Предыдущий патент: Устройство и способ для подъема и перемещения корпуса уплотнительного узла центробежного насоса
Следующий патент: Способ производства водонепроницаемой и проницаемой для пара обуви
Случайный патент: Средство для воздействия на организм