Фармацевтическая композиция
Номер патента: 3580
Опубликовано: 26.06.2003
Авторы: Симодзо Фумио, Охниси Норио, Ибуки Ринта, Уеда Сатоси, Тойода Тосихико, Яманака Масаюки
Формула / Реферат
1. Крем, содержащий трициклическое соединение формулы
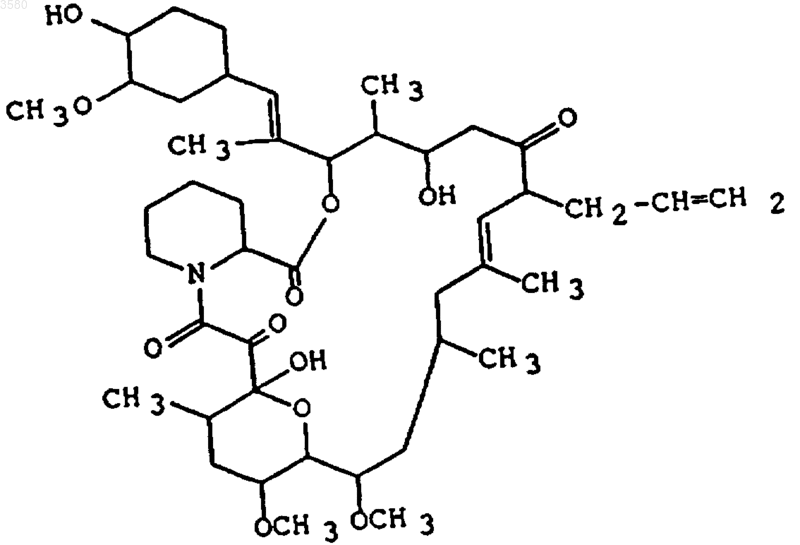
или его фармацевтически приемлемую соль, масляное вещество, которое представляет собой комбинацию изопропилмиристата и диэтилсебаката, поверхностно-активное вещество, которое выбирают из группы, состоящей из полиоксиэтиленалкилового простого эфира, полиоксиэтиленсорбитанового сложного эфира жирной кислоты, полиэтиленгликолевого сложного эфира жирной кислоты, пентаглицеринового сложного эфира жирной кислоты и глицеринового сложного эфира жирной кислоты, гидрофильное вещество, способное придавать жидкостям вязкость, и воду, и, необязательно, pH-контролирующий агент.
2. Крем по п.1, в котором количество поверхностно-активного вещества, масляного вещества и гидрофильного вещества составляют 0,1~15% (вес/вес), 2~50% (вес/вес) и 0,1~10% (вес/вес) от общей композиции, соответственно.
3. Крем по п.1, pH которого составляет 3,5-6.
4. Крем по п.1, в котором гидрофильное вещество представляет собой карбоксивинильный полимер.
5. Способ получения крема по п.1, включающий смешивание раствора, содержащего трициклическое соединение или его фармацевтически приемлемую соль, масляное вещество и поверхностно-активное вещество, с водой с получением эмульсии; и затем смешивание ее с гидрофильным веществом и, кроме того, необязательно, pH-контролирующим агентом.
6. Способ по п.5, включающий отдельное смешивание гидрофильного вещества и, необязательно, pH-контролирующего агента с водой; и затем смешивание с эмульсией, определенной по п.5.
Текст
1 Настоящее изобретение относится к фармацевтической композиции, в частности к крему,содержащей трициклическое соединение или его фармацевтически приемлемую соль, которая отличается стабильностью, прекрасной абсорбируемостью и/или пониженной способностью к раздражению. Данная фармацевтическая композиция используется для лечения или профилактики воспалительных или гиперпролиферативных кожных заболеваний или кожных проявлений иммунологически-опосредованных заболеваний. Известно, что многие трициклические соединения и их фармацевтически приемлемые соли обладают превосходной иммуноподавляющей активностью, противомикробной активностью и другими видами фармакологической активности и, вследствие этого, используются при лечении или для предотвращения реакции отторжения при трансплантации органов или тканей, болезненных состояний трансплантат-против-хозяина, аутоиммунных заболеваний и инфекционных заболеваний (Japanese KokaiFR900520, FR900523 и FR900525 представляют собой продукты, продуцируемые микроорганизмами рода Streptomyces, такими как Streptomyces tsukubaensis9933 [депонирован в Национальном институте Технологии биологических наук и человека Управления промышленной науки и технологии (ранее Институт ферментативных исследований Управления промышленной науки и технологии), 1-3 Higashi 1chome, Tsukubashi, Ibaraki, Япония, дата депонирования 5 октября 1984 г., регистрационный номер FERM ВР-927] или Streptomyces hydroscopicus, подвид yakushimaensis7238 [депонирован в Национальном институте Технологии биологических наук и человека Управления промышленной науки и технологии (ранее Институт ферментативных исследований Управления промышленной науки и технологии), 1-3Higashi 1-chome, Tsukuba-shi, Ibaraki, Япония,дата депонирования 12 января 1985 г., регистрационный номер FERM ВР-928]. Трициклическое соединение, обозначенное как FK506, имеет следующую химическую формулу:FK506 обладает абсолютно выдающейся иммуноподавляющей активностью и полезно при лечении или для предотвращения отторжения органов при трансплантации и при лечении и профилактике заболеваний в области офтальмологии. В патенте Японии Kokai Tokkyo Koho H1157913 показано, что раствор вещества FK506 в этаноле эффективен для подавления воспаления, и то, что вещество FK506 может быть введено в состав лосьона, геля или крема. Однако конкретные дозировочные формы такого типа не описаны. В патенте Японии Kokai Tokkyo Koho H117481 описана мазь, включающая трициклическое соединение или его фармацевтически приемлемую соль, по меньшей мере, достаточное количество промотора растворения/поглощения этого вещества для растворения и основу мази. В WO 94/28894 описан лосьон, включающий трициклическое соединение или его фармацевтически приемлемую соль и промотор растворения/поглощения, жидкую среду и, необязательно, эмульгатор и/или загущающий агент (модификатор реологии). До этого мази главным образом использовали для лечения кожных заболеваний. Однако необходимы различные дозировочные формы,подходящие для различных клинических проявлений заболеваний и для различных мест использования. Авторы настоящего изобретения исследовали возможные фармацевтические композиции для вещества FK506 и выявили дозировочную форму, обладающую многими желательными характеристиками, такими как высокая стабильность, высокая трансдермальная абсорбируемость и/или пониженное раздражение кожи. Таким образом, данное изобретение конкретно относится к гидрофильным полутвердым композициям для наружного применения, содержащим указанное трициклическое соединение. Согласно настоящему изобретению разработана фармацевтическая композиция в виде крема, содержащая трициклическое соединениеFK506 или его фармацевтически приемлемую соль, масляное вещество, поверхностноактивное вещество, гидрофильное вещество,воду и, кроме того, необязательно, рН-контролирующий агент. Вышеуказанное соединение или его фармацевтически приемлемая соль могут быть получены по той же технологии, которая описана в двух публикациях, на которые ссылались выше. В частности, трициклические соединения,полученные ферментированием Streptomycestsukubaensis9993 (FERM BP-927) или Streptomyces hygroscopicus подвид yakushimaensis7238 (FERM BP-928), известны под идентификационными номерами FR-900506, FR-900520, 3Koho S61-148181). Фармацевтически приемлемая соль соединения представляет обычную нетоксичную и фармацевтически приемлемую соль, такую как соль с неорганическими или органическими основаниями, особенно, соль щелочного металла, как, например, натриевая соль или калиевая соль, соль щелочно-земельного металла, такая как кальциевая соль и магниевая соль, соль аммония и соль амина, такая как соль триэтиламина и соль N-бензил-N-метиламина. Масляное вещество для применения в данном изобретении должно быть только веществом, способным растворять трициклическое соединение или его фармацевтически приемлемую соль. Сложные эфиры жирных кислот и жирные спирты являются предпочтительными. Сложные эфиры одноатомного спирта и жирных кислот (изопропилмиристат, этилмиристат, бутилмиристат, изоцетилмиристат, октилдодецилмиристат, изопропилпальмитат, изостеарилпальмитат, изопропилизостеарат, изоцетилизостеарат, бутилстеарат, изоцетилстеарат,цетилизооктаноат, этиллинолеат, изопропиллинолеат, гексиллаурат, этилолеат, децилолеат,олеилолеат, октилдодецилмиристат, гексилдецилдиметилоктаноат, октилдодецилнеодеканоат и т.д.). Сложные диэфиры двухосновных кислот(диизопропиладипат, диметиладипат, диэтиладипат, диизобутиладипат, диэтилсебакат, диизопропилсебакат, диэтилфталат, диэтилпимелат и т.д.). Спирты (олеиновый спирт, цетанол, стеариловый спирт, 2-октилдодеканол и т.д.). В данном изобретении вышеуказанные масляные вещества могут использоваться независимо сами по себе или в виде сочетания двух или более типов. В частности, с точки зрения стабильности дозировочной формы, абсорбируемости и/или раздражающего действия во многих случаях является предпочтительным использовать сочетание множества таких масляных веществ. Предпочтительное сочетание может, например,представлять собой смесь сложного эфира одноатомного спирта и жирной кислоты (например, изопропилмиристата) и сложного диэфира двухосновной кислоты (например, диэтилсебаката) в подходящем весовом соотношении (например, 0,110:1 (вес/вес), предпочтительно 0,52:1 (вес/вес. Наиболее предпочтительное весовое соотношение составляет 1:1 (вес/вес). Доля масляного вещества в фармацевтической композиции предпочтительно составляет 250% (вес/вес), более предпочтительно 1040% и наиболее предпочтительно 2030%. Далее будет описано поверхностноактивное вещество для применения в данном изобретении. 4 Поверхностно-активное вещество, которое может использоваться, включает фармацевтически приемлемые ионные или неионные поверхностноактивные вещества, но предпочтительно, оно является неионным поверхностно-активным веществом со значением ГЛБ не менее 10. В качестве более предпочтительных можно отметить следующие типы простых и сложных эфиров, являющихся поверхностно-активными веществами. Простые эфиры Полиоксиэтиленалкиловые простые эфиры(полиоксиэтиленолеиловый простой эфир, полиоксиэтиленстеариловый простой эфир, полиоксиэтиленцетиловый простой эфир, полиоксиэтиленлауриловый простой эфир (LauromacrogolJ.P.), полиоксиэтиленбегениловый простой эфир и т.д.). Сложные эфиры Полиоксиэтиленсорбитановые сложные эфиры жирных кислот. Полиоксиэтиленсорбитан моностеарат, полиоксиэтиленсорбитан моноолеат и т.д. (например, Tween 20, Tween 40, Tween 60, Tween 65,Tween 80 и т.д., все торговые названия). Полиэтиленгликолевые сложные эфиры жирных кислот (полиэтиленгликоль моноолеат,полиэтиленгликоль моностеарат (например, полиоксил стеарат 40 J.P.), полиэтиленгликоль монолаурат и т.д.). Пентаглицериновые сложные эфиры жирных кислот. Пентаглицерин монолаурат, пентаглицерин мономиристат, пентаглицерин моноолеат,пентаглицерин моностеарат и т.д. Глицериновые сложные эфиры жирных кислот. Глицерилмоностеарат и т.д. При использовании данного изобретения вышеуказанные поверхностно-активные вещества могут использоваться независимо или как сочетание двух или более видов. Доля поверхностноактивного вещества в фармацевтической композиции предпочтительно составляет 0,115% (вес/вес) и более предпочтительно 0,55% (вес/вес). Гидрофильное вещество для использования в данном изобретении может быть любым веществом, которое является фармацевтически приемлемым и способным придавать вязкость жидкостям, включая, таким образом, следующие органические или неорганические гидрофильные вещества.(2) Неорганические вещества Бентонит, синтетический силикат магния,алюмосиликат магния, оксид кремния и т.д. Доля гидрофильного вещества в фармацевтической композиции по данному изобретению выбирается в соответствии с желаемой вязкостью фармацевтической композиции и предпочтительно составляет 0,110% (вес/вес) и более предпочтительно 0,52%. Кроме того, в настоящем изобретении рН фармацевтической композиции поддерживают постоянным с точки зрения проблемы безопасности. Следовательно, может быть добавлен в подходящем количестве рН контролирующий агент, такой как буфер, водный раствор гидроксида натрия или тому подобные. Диапазон рН предпочтительно составляет 3,56 и более предпочтительно 45. Если это необходимо, в дополнение к вышеуказанным ингредиентам могут быть добавлены обычный эксципиент (например, петролатум, пропиленгликоль и т.д.), стабилизатор (антиоксидант и т.д.), красящий агент, подсластитель, вкусовая добавка, разбавитель, антисептик (например, парагидроксибензоаты, хлорид бензалькония, сорбиновая кислота и т.д.) и другие лекарственные вещества, эффективные при кожных заболеваниях. Между тем, фармацевтическая композиция по данному изобретению может быть получена способом, включающим следующие стадии.(1) Стадия, которая включает получение раствора, состоящего из указанного трициклического соединения или его фармацевтически приемлемой соли, масляного вещества и поверхностно-активного вещества;(2) стадия, которая включает смешивание раствора с водой с получением эмульсии; и(3) стадия, которая включает смешивание эмульсии с указанным гидрофильным веществом и дополнительно, необязательно, рН контролирующим агентом при перемешивании. В качестве альтернативы эта стадия может включать смешивание указанного гидрофильного вещества и,кроме того, необязательно, рН контролирующего агента с водой, а затем смешивание предварительно полученной смеси с эмульсией, полученной как указано выше, при перемешивании. Стадию (1) предпочтительно осуществляют при повышенной температуре, например,при 5090 С, предпочтительно при 6080 С. На стадии (2) используемую воду также предпочтительно нагревают заблаговременно до температуры, близкой к температуре раствора,полученного на стадии (1) и полученную эмульсию предпочтительно охлаждают до подходящей температуры, например, до 30 С, перед осуществлением стадии (3). 6 Дозировка трициклического соединения или его фармацевтически приемлемой соли зависит от возраста конкретного пациента и типа и серьезности заболевания, но обычно дневная терапевтическая доза составляет примерно 0,0011000 мг, предпочтительно примерно 0,005100 мг в виде активного ингредиента. Обычно в среднем на одну дозу вводят примерно 0,01, 0,05, 0,1, 0,5, 1, 5, 10, 25 или 50 мг. Рекомендуемая доля трициклического соединения в фармацевтической композиции составляет 0,00120% (вес/вес) предпочтительно 0,0110% (вес/вес) от общей композиции. Примеры Следующие примеры дополнительно подробно иллюстрируют настоящее изобретение, и следует понимать, что эти примеры не ограничивают объем изобретения. Пример 1. Первоначально при 6080 С смешивали следующие ингредиенты (а), (b) и (с), получая раствор, к которому добавляли предварительно нагретый до 6080 С ингредиент (d). Смесь равномерно превращали в эмульсию с помощью гомогенизатора и полученную эмульсию охлаждали до 30 С. Затем к эмульсии добавляли ингредиент (е) и перемешивали смесь целиком,получая фармацевтическую композицию в виде легко намазывающегося крема [состав (1)]. Пример 2. Фармацевтическая композиция (состав (2) была получена аналогично способу примера 1,за исключением того, что после добавления (е) рН смеси доводили до примерно 4,0 с помощью подходящего количества 1 Н водного раствора(3) и (4 получали способами, аналогичными способам примеров 1 и 2.(5)-(8 получали способами, аналогичными способам примеров 1 и 2. Состав 1,0 1,0 1,0 1,0 сколько сколько сколько сколько необх. необх. необх. необх.(9)-(12 получали аналогично способам примеров 1 и 2. Состав 1,0 1,0 1,0 1,0 сколько сколько сколько сколько необх. необх. необх. необх.(13)-(16 получали аналогично способам примеров 1 и 2. Состав 1,0 1,0 1,0 1,0 сколько сколько сколько сколько необх. необх. необх. необх. Пример 7. Следующие ингредиенты (а), (b) и (с) предварительно смешивали при 6080 С, получая раствор, к которому добавляли предварительно нагретый до 6080 С ингредиент (d1). Смесь равномерно гомогенизовали с использованием гомогенизатора, а затем охлаждали до 30 С. К этой эмульсии добавляли гель, полученный из (е), (d2) и (f), и смесь тщательно перемешивали, получая фармацевтическую композицию в виде хорошо намазывающегося крема(18 получали аналогично способу примера 7.(19)-(21 получали способами, аналогичными способу примера 7. Состав 56,47 56,4 56,2 1,0 1,0 1,0 сколько сколько сколько необх. необх. необх. 9 Пример 10. Далее описаны протокол и результаты эксперимента по трансдермальной абсорбируемости с использованием фармацевтических композиций по настоящему изобретению. Тест на трансдермальную абсорбируемость. Был осуществлен эксперимент на трансдермальную абсорбируемость in vivo с использованием составов 2, 3, 7, 12 и 20, полученных выше в примерах. В качестве экспериментальных животных использовали 3 самцов крыс SD 7-ми недельного возраста. Крысам, зафиксированным в положении на спине в стереотактическом устройстве, выстригали волосяной покров брюшной области электрическими ножницами, а затем использовали крем для депиляции (Eva-крем, производства Tokyo Tanabe Pharmaceutical). Обработанную таким образом область кожи промывали в течение 10 мин водой после применения крема для депиляции. Крыс возвращали в клетку и давали им возможность отдохнуть в течение 24 ч. После этого крысам, зафиксированным в положении на спине в стереотактическом устройстве помечали прямоугольную область размером 2,5 см х 4 см по четырем углам депилированной брюшной области и на эту площадь наносили 50 мг испытуемого образца. Через 1, 3, 5, 8 и 24 ч после такого использования отбирали 0,3 мл крови из подключичной вены с помощью шприца, предварительно обработанного ЭДТК (этилендиаминотетрауксусная кислота). После тщательного перемешивания с ЭДТК образцы крови хранили замороженными до анализа. Используя вышеуказанные образцы крови,определяли концентрацию вещества FK506 в цельной крови с помощью твердофазного иммуноферментного анализа, используя пероксидазу в качестве фермента (например, описано вJapanese Kokai Tokkyo Koho H1-92659). Для каждого испытуемого образца рассчитывали параметр трансдермальной абсорбции. Результаты показаны в таблице. В таблице ППК[0-24 ] представляет площадь под кривой концентрация в крови-время в течение 0-24 ч после применения. Параметр трансдермальной абсорбции(n=3, среднее значениесреднеквадратичная ошибка) ПППК [0-24 ч] Тест-образец нгч/мл Состав 2 30 Состав 3 30 Состав 7 30 Состав 12 30 Состав 20 30 Т.о. согласно данному изобретению разработана фармацевтическая композиция трициклического соединения, в частности гидрофильная полутвердая композиция для наружного 10 применения, которая стабильна, легка в использовании, приемлема по ощущениям при пользовании и с низким раздражающим действием и/или улучшенной кожной проницаемостью. Благодаря фармакологической активности,которой обладает трициклическое соединение,фармацевтическая композиция согласно изобретению полезна при лечении или профилактике воспалительных или гиперпролиферативных кожных заболеваний или кожных проявлений иммунологически-опосредованных заболеваний(лишай Вильсона), пузырчатка, буллезная рожа,эпидермолизный буллез, крапивница, сосудистая опухоль, васкулиты, эритема, кожная эозинофилия, красная волчанка, угри и гнездная плешивость). Кроме того, активный ингредиент, трициклическое соединение (I) используемый в фармацевтической композиции, полезен при лечении или профилактике следующих заболеваний. Реакции отторжения при трансплантации органов или тканей, таких как сердце, почка,печень, костный мозг, кожа, роговица, легкое,поджелудочная железа, тонкая кишка, лимб,мышца, нерв, межпозвоночный диск, трахея,миобласт, хрящ и т.д. Реакции трансплантат-против-хозяина после трансплантации костного мозга: аутоиммунные заболевания, такие как ревматоидный артрит, системная красная волчанка, тироидит Хашимото, рассеянный склероз, миастения, диабет I типа и т.д.; и инфекции, вызванные патогенными микроорганизмами (например, Aspergillus fumigatus,Fusarium oxysporum, Trichophyton asteroides и т.д.); аутоиммунные заболевания глаза (например, кератоконъюктивит, весенний конъюктивит, воспаление сосудистой оболочки глазного яблока, связанное с болезнью Бехкета, кератит,герпесный кератит, конический кератит, дистрофия эпителия роговицы, кератолейкома,пемфигус (пузырчатка) глаза, язва Моорена,воспаление склеры, связанная с диффузным токсическим зобом офтальмопатия, синдром Вогт-Коянаги-Харада (Vogt-Koyanagi-Harada),кератоконъюнктивидное заболевание (сухой глаз), фликтунелузное заболевание, иридоциклит (воспаление передних отделов глазного яблока), саркоидоз, эндокринная офтальмопатия и т.д.); заболевания обратимой обструкции (непроходимости) дыхательных путей [астма (например, бронхиальная астма, аллергическая астма, собственная астма, примесная астма, пылевая атсма), особенно хроническая или трудноизлечимая астма (например, поздняя астма и гиперреактивность дыхательных путей), бронхиты и т.д.]; 11 воспаления слизистой оболочки или сосудов (например, язва желудка, ишемическое или тромботическое повреждение сосудов, ишемические заболевания кишечника, энтериты, некротические энтероколиты, кишечные повреждения, связанные с термическими ожогами, лейкотриен В 4-опосредованные заболевания); кишечные воспаления/аллергии (например,проникающие заболевания, проктиты, эозинофильный гастроэнтерит, мастоцитоз, болезнь Крона и язвенный колит); аллергические заболевания, связанные с пищей, с симптоматическими проявлениями,удаленными от желудочно-кишечного тракта(например, мигрень, ринит и экзема); заболевания почек (например, интерстициальный нефрит, синдром Гудпастура (Goodpasture), гемолитический уремический синдром и диабетическая невропатия); заболевания нервов (например, множественный миозит, синдром Гуллиана-Барра, болезнь Меньера, полиневрит, одиночный неврит,инфаркт головного мозга, болезнь Альцгеймера,болезнь Паркинсона, боковой амиотрофический склероз (БАС) и радикулопатия); церебральное ишемическое заболевание(например, повреждения головы, кровоизлияние в мозг (например, субарахноидальное кровоизлияние, внутримозговое кровоизлияние), церебральный тромбоз, церебральная эмболия, остановка сердца, удар, кратковременный ишемический приступ (КИП), гипертензивная энцефалопатия); эндокринные заболевания (например, гипертироидизм и Базедова болезнь); заболевания крови (например, аплазия красных кровяных телец, апластическая анемия,гипопластическая анемия,идиопатическая тромбоцитопеническая пурпура, аутоиммунная гемолитическая анемия, агранулоцитоз, пернициозная анемия, анемия мегалобластов и анеритроплазия); заболевания костей (например, остеопороз); респираторные заболевания (например,саркоидоз, легочная форма фиброзита и идиопатическая интерстециальная пневмония); кожные заболевания (например, дерматомиозит, лейкодерма обыкновенная, ихтиоз обыкновенный, фоточувствительность и кожная Т-клеточная лимфома); заболевания системы кровообращения (например, артериосклероз, атеросклероз, синдром аортита, узловая форма полиартрита и миокардит); коллагенозные заболевания (например,склеродермия, гpанулема Вегенера и синдром Сджогрена (Sjogren); адипоз; эозинофильный фасциит (воспаление фасции); 12 периодонтальные заболевания (например,повреждения десен, периодонта, алвеолярной кости или вещества зубной костной ткани); невротический синдром (например, гломерулонефрит); мужская шаблонная алопеция (облысение),старческое облысение; мышечная дистрофия; пиодермия или синдром Сезари; болезнь Аддисона; заболевания, связанные с хромосомными аномалиями (например, синдром Дауна); активные кислород-опосредованные заболевания [например, повреждение органа (например, ишемические нарушения системы кровообращения органов (например, сердца, печени, почки, системы органов пищеварения и т.д.),связанные с консервированием, трансплантацией или ишемическими заболеваниями (например, тромбозом, кардиальным инфарктом и т.д.)]; кишечные заболевания (например, эндотоксический шок, псевдомембранный колит и колиты, вызванные лекарственными средствами или облучением); заболевания почек (например, ишемическая острая почечная недостаточность, хроническое повреждение почки); легочные заболевания (например, токсикоз, вызванные легочным кислородом или лекарственными средствами (например, паракорт,блеомицин и т.д.), рак легкого и легочная эмфизема; заболевания глаза (например, катаракта,заболевания отложения железа (сидероз глазного яблока), ретинит (воспаление сетчатки), пигментирование, старческие бляшки, рубцевание стекловидного тела, щелочной ожог роговицы; дерматит (например, эритема полиформенная, линейный иммуноглобулин А буллезный дерматит, цементный дерматит); и другие заболевания (например, гингивит,парадонтит, сепсис, панкреатит и заболевания,вызванные загрязнением окружающей среды(например, загрязнением воздуха), возрастом,карциногенами, метастазами рака и декомпрессией; заболевания, вызванные высвобождением гистамина или лейкотриена С 4; рестеноз коронарной артерии после ангиопластики и профилактика постхирургических срастаний; аутоиммунные заболевания и воспалительные состояния (например, первичный отек слизистой, аутоиммунный атрофический гастрит, преждевременная менопауза, мужское бесплодие, юношеский сахарный диабет, вульгарная пузырчатка, буллез, симпатический офтальмит, индуцированный линзами увеит, идиопатическая лейкопения, активный хронический гепатит, идиопатический цирроз, дисковая красная волчанка, аутоиммунный орхит (воспаление яичка), артрит (например, деформирующий артрит) или полихондрит; инфекции вируса иммунодефицита человека (ВИЧ), СПИД; аллергический конъюнктивит; гипертрофический рубец или келлоидный рубец вследствие травмы, ожога или хирургического вмешательства. Кроме того, трициклическое соединение(I) обладает регенерирующей активностью печени и/или активностью стимулирования гипертрофии и гиперплазии гепатоцитов (печеночных клеток). Следовательно, фармацевтическая композиция согласно изобретению пригодна при лечении или для профилактики заболеваний печени [например, иммуногенные заболевания (например, хронические аутоиммунные заболевания печени, такие как аутоиммунный гепатит, первичный желчный цирроз или склерозирующий холангит), частичная резекция печени, острый некроз печени (например, некроз,вызванный токсинами, вирусным гепатитом,шоком или гипоксией), гепатит-В, не-А не-В гепатит, гепатоцирроз и печеночная недостаточность (например, молниеносный гепатит,гепатит с поздним началом болезни и "остраяхроническая" паренхематозная недостаточность(острая печеночная недостаточность или хронические заболевания печени]. И кроме того, настоящая композиция пригодна для предотвращения или при лечении различных заболеваний благодаря своему полезному фармакологическому действию, такому как эффект нарастания химиотерапевтического действия, активность при цитомегаловирусной инфекции, противовоспалительное действие,ингибирующая активность против пептидилпролил изомеразы или ротамазы, противомалярийная активность, противоопухолевая активность и так далее. Среди различных составов фармацевтической композиции по данному изобретению, составы, обладающие пониженным раздражающим кожу действием, пригодны для лечения или профилактики атопических и других кожных заболеваний, тогда как составы с повышенной кожной абсорбируемостью особенно полезны при лечении или профилактике псориаза и других кожных заболеваний. 14 ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Крем, содержащий трициклическое соединение формулы или его фармацевтически приемлемую соль,масляное вещество, которое представляет собой комбинацию изопропилмиристата и диэтилсебаката, поверхностно-активное вещество, которое выбирают из группы, состоящей из полиоксиэтиленалкилового простого эфира, полиоксиэтиленсорбитанового сложного эфира жирной кислоты, полиэтиленгликолевого сложного эфира жирной кислоты, пентаглицеринового сложного эфира жирной кислоты и глицеринового сложного эфира жирной кислоты, гидрофильное вещество, способное придавать жидкостям вязкость, и воду, и, необязательно, рНконтролирующий агент. 2. Крем по п.1, в котором количество поверхностно-активного вещества, масляного вещества и гидрофильного вещества составляют 0,115% (вес/вес), 250% (вес/вес) и 0,110%(вес/вес) от общей композиции, соответственно. 3. Крем по п.1, рН которого составляет 3,56. 4. Крем по п.1, в котором гидрофильное вещество представляет собой карбоксивинильный полимер. 5. Способ получения крема по п.1, включающий смешивание раствора, содержащего трициклическое соединение или его фармацевтически приемлемую соль, масляное вещество и поверхностно-активное вещество, с водой с получением эмульсии; и затем смешивание ее с гидрофильным веществом и, кроме того, необязательно, рН-контролирующим агентом. 6. Способ по п.5, включающий отдельное смешивание гидрофильного вещества и, необязательно, рН-контролирующего агента с водой; и затем смешивание с эмульсией, определенной по п.5.
МПК / Метки
МПК: A61P 17/00, A61K 31/4025
Метки: фармацевтическая, композиция
Код ссылки
<a href="https://eas.patents.su/8-3580-farmacevticheskaya-kompoziciya.html" rel="bookmark" title="База патентов Евразийского Союза">Фармацевтическая композиция</a>
Предыдущий патент: Производные нодулиспоровой кислоты
Следующий патент: Способ получения чистого циталопрама
Случайный патент: Стерилизация жидкостей с использованием ультрафиолетового источника света












