Препараты для отпугивания насекомых
Формула / Реферат
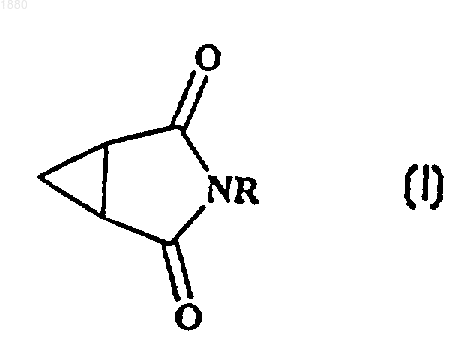
1. Препарат для отпугивания насекомых или акарид, содержащий соединение формулы I
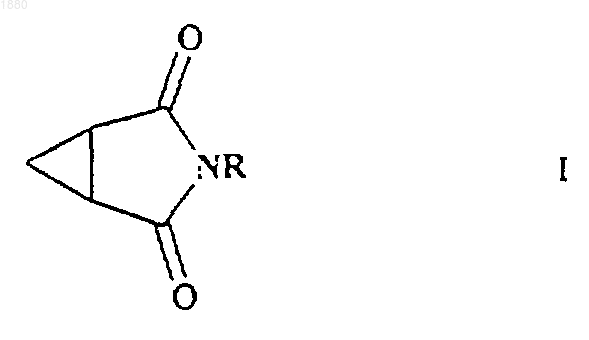
где R представляет собой С2-10алкил с прямой или разветвленной цепью, С2-10алкенил с прямой или разветвленной цепью или С2-10алкинил с прямой или разветвленной цепью, причем эти группы возможно замещены одной или более чем одной группой, выбранной из галогена, С4-8циклоалкила и С4-8циклоалкенила, и подходящие адьювант, разбавитель или носитель.
2. Препарат по п.1, где R представляет собой C2-10алкенил с прямой цепью.
3. Препарат по п.2, где R представляет собой 6-гептен-1-ил.
4. Препарат по п.1, где R представляет собой С2-10алкил с прямой цепью, возможно замещенный хлором.
5. Препарат по п.1, где R содержит С4-6 циклоалкильную группу.
6. Препарат по любому из пп.1-5, причем этот препарат является кремом или лосьоном.
7. Соединение формулы I, как определено в п.1, при условии, что R не представляет собой н-бутил или н-октил.
8. Способ отпугивания насекомых или акарид, при котором соединение формулы I, как определено в п.1, наносят на внешние поверхности млекопитающего.
9. Способ по п.8, где млекопитающее является человеком, домашним животным или домашним скотом.
10. Способ по п.8 или 9, где насекомые являются москитами, комарами или мошками.
11. Способ по п.8 или 9, где акариды являются клещами.
12. Способ получения соединения формулы I, как определено в п.7, при котором соединение формулы II

подвергают взаимодействию с соединением формулы RX, где R такой, как определено в п.1, а Х представляет собой галоген в присутствии основания.
13. Способ получения соединения формулы I, как определено в п.7, при котором соединение формулы III
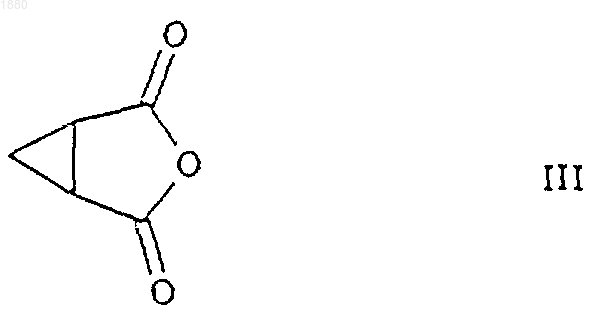
подвергают взаимодействию с соединением формулы RNH2, где R такой, как определено в п.1.
14. Способ получения соединения формулы I, как определено в п. 7, при котором соединение формулы II
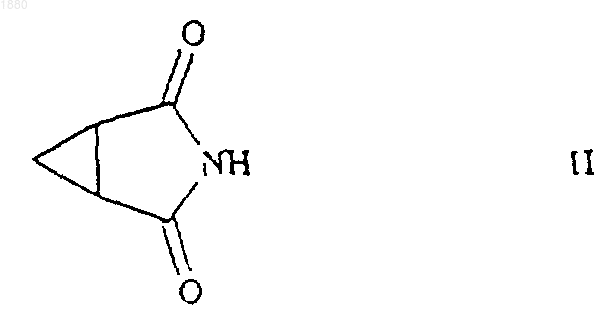
подвергают взаимодействию с диэтилазодикарбоксилатом, трифенилфосфином и соединением формулы ROH, где R такой, как определено выше, по реакции Мицунобу.
15. Способ получения соединения формулы I, как определено в п.7, при котором соединение формулы IV
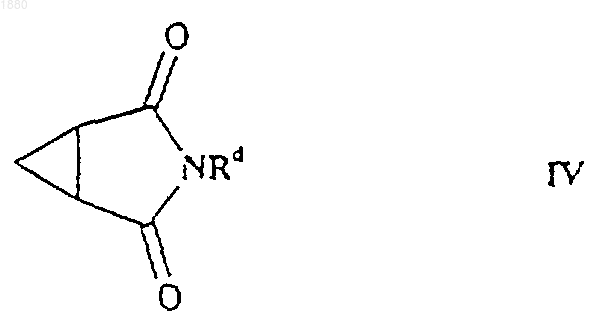
в котором Rd имеет такое же определение как R в п.1, за исключением того, что он замещен ОН или оксогруппой, подвергают взаимодействию с диэтиламинотрифторидом серы с получением соответствующего соединения формулы I, в котором каждая ОН или оксогруппа заменена одним или двумя атомами фтора, соответственно.
16. Соединение формулы IV, как определено в п.15
Текст
1 Изобретение относится к препаратам для отпугивания насекомых и акарид, новым соединениям для применения в таких препаратах и способам отпугивания насекомых и акарид. В международной патентной заявке WO 87/04594 указано, что группа 1-замещенных азациклоалканов полезна для применения в качестве средств для отпугивания насекомых (см. с. 51 и 52). В японских патентных заявках 59031702,58120878, 58072504 и 58072503 заявлена группа 1-замещенных азациклоалкенов в качестве средств для отпугивания насекомых. В японских патентных заявках 7118112,7046955, 6263605, 4225902 и 4036205, и в европейской патентной заявке ЕР 525893 раскрываются трициклические азациклоалканы, указанные как средства для отпугивания насекомых. 3-н-Бутил-3-азабицикло[3.1.0]гексан-2,4 дион раскрыт в качестве химического промежуточного соединения Тифариэлло и др. (Tetrahedron Letters, Vol 28,3, рр 267-270, 1987). 3-нOктил-3-азабицикло[3.1.0]гексан-2,4-дион стал доступным на неконфиденциальной основе. Согласно настоящему изобретению предложен препарат для отпугивания насекомых или акарид, содержащий соединение формулы I где R представляет собой С 2-10 алкил с прямой или разветвленной цепью, С 2-10 алкенил с прямой или разветвленной цепью или С 2-10 алкинил с прямой или разветвленной цепью, причем эти группы возможно замещены одной или более чем одной группой, выбранной из галогена, С 4-8 циклоалкила и С 4-8 циклоалкенила; и подходящие адьювант, разбавитель или носитель. Препараты по изобретению могут иметь преимущество, так как они являются более сильнодействующими или действующими более продолжительный период времени, чем те, которые известны из существующего уровня техники. Соединение формулы I может придавать приятный запах препаратам для людей. Предпочтительные препараты включают те, в которых(в) R содержит С 4-6 циклоалкильную группу (например R представляет собой 2 циклогексилэтил). Галоген означает фтор, хлор, бром и йод. Фтор и хлор представляют особый интерес. Согласно изобретению также предложено соединение формулы I, как определено выше, 001880 2 при условии, что R не представляет собой нбутил или н-октил. Согласно изобретению дополнительно предложен способ отпугивания насекомых или акарид, при котором соединение формулы I, как определено выше, наносят на внешние поверхности млекопитающего. Млекопитающее может быть человеком, домашним животным (например собакой или кошкой) или домашним скотом. Насекомыми, представляющими особый интерес, являются москиты, комары и мошки. Акаридами, представляющими особый интерес,являются клещи. Предпочтительно соединение формулы 1 применяется в препарате, как определено выше. Кроме того, согласно изобретению предложен способ получения соединения формулы I,как определено выше, при условии, что R не представляет собой н-бутил или н-октил, при котором в котором Rd имеет такое же определение как R,определенный выше, за исключением того, что он замещен ОН или оксогруппой, подвергают взаимодействию с диэтиламинотрифторидом серы с получением соответствующего соединения формулы I, в котором каждая ОН или оксогруппа заменена одним или двумя атомами фтора, соответственно. При способе (а) реакцию предпочтительно проводят при комнатной температуре или при температуре ниже комнатной в растворителе,который не имеет неблагоприятного влияния на реакцию (например в диметилформамиде). Под 3 ходящие основания включают в себя гидрид натрия. При способе (б) реакция может быть проведена в избытке амина в качестве растворителя при повышенной температуре. При способе (в) диэтилазодикарбоксилату и тирифенилфосфину дают возможность вступить в реакцию первыми при температуре ниже комнатной, а затем добавляют соединение формулы ROH, за которым следует соединение формулы II. После этого смеси дают возможность нагреться до комнатной температуры. Реакцию предпочтительно проводят в растворителе, который не имеет неблагоприятного влияния на реакцию (например в тетрагидрофуране). Более полное описание реакции Мицунобу приведено в J Am Chem Soc, 94,679 (1972). При способе (г) реакцию предпочтительно проводят при комнатной температуре или при температуре около комнатной в растворителе,который не имеет неблагоприятного влияния на реакцию (например, в дихлорметане). Соединения формул II, III, RX, ROH иRNH2 либо известны, либо могут быть получены известными способами. Например, синтез соединения формулы II известен из SyntheticCommunications, 1981, 11(6), 447-54. Синтез соединения формулы III известен из Synthesis,1983, (6), 469-70. Соединения формулы IV могут быть получены с помощью способов, описанных выше для получения соединений формулы I. Соединения формулы IV составляют дополнительный аспект изобретения. Для специалистов в данной области очевидно, что чувствительные функциональные группы могут нуждаться в защите и ее снятии в течение синтеза соединения формулы I. Это может быть достигнуто с помощью стандартных методик, например так, как описано в Protective Groups in Organic Synthesis (T.W. Greeneand P.G.M. Wuts, John Wiley and Sons Inc, 1991). Действенность соединений формулы I может быть испытана в тестах, представленных ниже. Тест А - испытание способности отпугивать клещей in vitro Испытуемое соединение, растворенное в приемлемом растворителе, наносят на дно испытательной трубки. Затем растворитель высушивают при 32 С от 1 до 24 ч. Личинку клеща помещают в горловину трубки и закупоривают ватной пробкой. Трубку помещают под подходящий источник света и фиксируют расстояние,на которое клещи перемещаются в трубке. Активность выражают в виде процента отпугивающей способности, вычисляемой как (АВ)/Ах 100%, где А - длина трубки, а В - расстояние, на которое клещи перемещаются в трубке. 4 Тест Б - испытание способности отпугивать москитов in vitro Испытуемое соединение, растворенное в подходящем растворителе, наносят на кусок хирургической гигроскопической марли. Затем растворитель высушивают при 32 С от 1 до 24 ч. Марлю натягивают на горловину пластиковой трубки с москитами. Отпугивающую способность определяли путем продувания углекислого газа через горловину трубки для обеспечения так называемого стимула поиска хозяина и подсчета числа москитов, которые садятся на обработанную марлю. Активность выражают в виде процента отпугивающей способности,вычисляемой как (C-D)/Cx100%, где С - число москитов, находящихся в трубке, a D - число москитов, севших на марлю вследствие стимуляции углекислым газом. Препараты по настоящему изобретению могут быть приготовлены с известными адьювантами, разбавителями и носителями известными способами. Например в тех случаях, когда млекопитающее, получающее препарат, не является человеком, препарат может быть препаратом, который льют, или наносимым пятнами препаратом, препаратом в аэрозольной упаковке, шампунем, душистым тальком, пропитанной лентой, мылом, биркой на уши или хвост или гелем. В тех случаях, когда млекопитающим,получающим препарат, является человек, препарат может быть порошком, мазью, лосьоном,салфеткой, кремом, мылом, смываемым карандашом или тканым пластырем. Препарат может включать антиоксиданты или поглотители УФлучей. Кремы и лосьоны представляют особый интерес и могут быть приспособлены для нанесения на кожу. Ниже приводятся примеры осуществления изобретения, в которых температуры плавления определялись с помощью прибора для определения температуры плавления Gallenkamp и являются неоткорректированными. Данные ядерного магнитного резонанса получали с помощью Bruker AC300 или АМ 300. Данные массспектрометрии получали с помощью FinniganMat. TSQ 7000 или Fisons Instruments Trio 1000. Вычисленные и наблюдаемые ионы приведены относительно изотопного состава наименьшей массы. Инфракрасные спектры получали с помощью Perkin Elmer Paragon 1000 FT-IR спектрометра. Пример А 1. 3-н-Децил-3-азабицикло[3.1.0] гексан-2,4-дион. 1-Иоддекан (1,21 г) добавляли к перемешанной смеси 3-азабицикло[3.1.0]гексан-2,4 диона (0,5 г), карбоната калия (0,62 г) и тетрабутиламмонийбромида(1,45 г) в дихлорметане (50 мл) при комнатной температуре и полученную в результате смесь перемешивали в течение 24 ч. Смесь фильтровали и затем фильтрат промывали водой (2 х 100 мл), сушили (MgSO4) и выпаривали в вакууме с получением коричневого 5 масла. Масло очищали хроматографией на силикагеле (100 г) с гексаном в качестве элюента. Объединение и выпаривание соответствующих фракций давали названное в заголовке соединение в виде бесцветного масла. ЯМР (CDCl3) 0,8 (т, 3 Н), 1,0-1,6 (м, 18 Н),2,46 (дд, 2 Н), 3,34 (т, 2 Н). МС (термическое разбрызгивание) M/Z [М +NH4] 269, C15H25NO2 + NH4 требует 269. ИК (полиэтилен) 2940, 2856, 1775, 1710,1440, 1395. Пример А 2. 3-(4-хлорбут-1-ил)-3-азабицикло[3.1.0]гексан-2,4-дион. Гидрид натрия (0,11 г, 60%-ая дисперсия в масле) добавляли к перемешанному раствору 3 азабицикло[3.1.0]гексан-2,4-диона (0,5 г) и 1 хлор-4-иодоктана (0,98 г) в безводном диметилформамиде (50 мл) в атмосфере азота при комнатной температуре. Полученную в результате смесь перемешивали 48 ч и затем добавляли по каплям в воду (50 мл). Водную смесь экстрагировали дихлорметаном (2 х 200 мл) и затем объединенные органические экстракты промывали водой (2 х 400 мл), сушили (MgSO4) и выпаривали в вакууме с получением масла. Масло очищали хроматографией на кремнеземе (80 г), используя в качестве элюента этилацетат/гексан(термическое разбрызгивание) M/Z [М + NH4] 219,C9H12ClNO2 + NH4 требует 219. ИК (полиэтилен) 2952, 2872, 1770, 1714, 1445, 1397,5. Пример A3. 3-н-Oктил-3-азабицикло[3.1.0] гексан-2,4-дион. Гидрид натрия (1,48 г, 60%-ая в масле) добавляли к перемешанному раствору 3 азабицикло[3.1.0]гексан-2,4-диона (4,0 г) и 1 иодоктана (8,88 г) в безводном диметилформамиде (70 мл) в атмосфере азота при 0 С. Реакционную смесь перемешивали при 0 С следующие 30 мин и затем перемешивали при комнатной температуре в течение 16 ч. Смесь разбавляли водой (100 мл), а затем экстрагировали эфиром (150 мл). Органический экстракт промывали водой (2 х 70 мл), сушили (MgSO4) и выпаривали в вакууме с получением коричневого масла. Масло очищали перегонкой в вакууме 6 Пример А 4. 3-н-Гептил-3-азабицикло[3.1.0] гексан-2,4-дион. Гидрид натрия (0,11 г) добавляли к раствору 3-азабицикло[3.1.0]гексан-2,4-диона (0,3 г) в безводном тетрагидрофуране (10 мл) в атмосфере азота при комнатной температуре. Суспензию перемешивали в течение 5 мин и затем к реакционной смеси добавляли одной порцией 1 иодгептан (0,61 г). После перемешивания в течение двух часов при комнатной температуре добавляли диметилформамид (5 мл) и реакционную смесь перемешивали в течение следующих 16 ч при комнатной температуре. Реакционную смесь разбавляли дихлорметаном и затем подвергали распределению с водой (20 мл). Водную фазу экстрагировали дихлорметаном(20 мл) и объединенные органические экстракты промывали водой (2 х 20 мл), сушили (MgSO4) и выпаривали в вакууме. Остаток очищали хроматографией на силикагеле (50 г), используя в качестве элюента 25-30% этилацетат/гексан, с получением названного в заголовке соединения в виде бесцветного масла. ЯМР (CDCl3) 0,88 (т, 3 Н), 1,12-1,37 (м, 9 Н),1,37 -1,55 (м, 3 Н), 2,45 (дд, 2 Н), 3,34 (т, 2 Н) МС(термическое разбрызгивание) M/Z [М + NH4] 227, C12H19NO2 + NH4 требует 227 ИК (полиэтилен) 2956, 2917, 2848, 1771,1715. Пример А 5. 3-[2-(циклогексил)этил]-3-азабицикло[3.1.0]гексан-2,4-дион. Гидрид натрия (0,11 г) добавляли к раствору 3-азабицикло[3.1.0]гексан-2,4-диона (0,3 г) и 1-бром-2-циклогексилэтана (0,52 г) в диметилформамиде (5 мл) и полученную в результате смесь перемешивали при комнатной температуре в атмосфере азота в течение 16 ч. Смесь разбавляли водой (15 мл) и затем экстрагировали толуолом (20 мл). Органический экстракт промывали водой (15 мл), сушили (MgSO4) и выпаривали в вакууме. Остаток очищали перегонкой по Kugelrohr (температура кипения 130-140 С при 0,1 мм.рт.ст.) с получением названного в заголовке соединения в виде бесцветного масла. ЯМР (CDCl3) 0,78-1,78 (м, 15 Н), 2,43 (дд,2 Н), 3,34 (т, 2 Н) МС (термическое разбрызгивание) M/Z [М + NH4] 239, C13H19NO2 + NH4 требует 239 ИК (полиэтилен) 2915, 2848, 1771,1714. Пример А 6. 3-(2-этилгекс-1-ил)-3-азабицикло[3.1.0]гексан-2,4-дион. Гидрид натрия (0,11 г) добавляли к раствору 3-азабицикло[3.1.0]гексан-2,4-диона (0,3 г) и 1-бром-2-этилгексана (0,52 г) в диметилформамиде (5 мл) и полученную в результате смесь перемешивали при комнатной температуре в атмосфере азота в течение 16 ч. Смесь разбавляли водой (15 мл) и затем экстрагировали толуолом (20 мл). Органический экстракт промывали водой (15 мл), сушили (MgSO4) и выпаривали в вакууме. Остаток очищали перегонкой по(5 мл) и полученную в результате смесь перемешивали при комнатной температуре в атмосфере азота в течение 16 ч. Смесь разбавляли водой (15 мл) и затем экстрагировали толуолом(20 мл). Органический экстракт промывали водой (15 мл), сушили (MgSO4) и выпаривали в вакууме. Остаток очищали перегонкой поKugelrohr (температура кипения 130-140 С при 0,1 мм.рт.ст.) с получением названного в заголовке соединения в виде бесцветного масла. ЯМР (CDCl3) 1,11-1,58 (м, 10 Н), 2,00 (дт,2 Н), 2,43 (дд, 2 Н), 3,32 (т, 2 Н), 4,90 (дд, 1 Н),4,95 (дд, 1 Н), 5,75 (м, 1 Н) ИК (полиэтилен) 3078, 2916, 2848, 1772, 1714, 1641. Пример А 8. 3-(3-метилбут-1-ил)-3-азабицикло[3.1.0]гексан-2,4-дион. Гидрид натрия (0,11 г) добавляли к раствору 3-азабицикло[3.1.0]гексан-2,4-диона (0,3 г) в безводном тетрагидрофуране (10 мл) в атмосфере азота при комнатной температуре. Суспензию перемешивали в течение 5 мин и затем к реакционной смеси добавляли одной порцией 1 иод-3-метилбутан (0,53 г). После перемешивания в течение двух часов при комнатной температуре добавляли диметилформамид (5 мл) и реакционную смесь перемешивали в течение следующих 16 ч при комнатной температуре. Реакционную смесь разбавляли дихлорметаном и затем подвергали распределению с водой (20 мл). Водную фазу экстрагировали дихлорметаном (20 мл) и объединенные органические экстракты промывали водой (2 х 20 мл), сушили(МgSО 4) и выпаривали в вакууме. Остаток очищали хроматографией на силикагеле (50 г), используя в качестве элюента 25% этилацетат/гексан, с получением названного в заголовке соединения в виде бесцветного масла. ЯМР (CDCl3) 0,89 (д, 6 Н), 1,29-1,39 (м,3 Н), 1,42 -1,56 (м, 2 Н), 2,45 (дд, 2 Н), 3,36 (д, 2 Н) ИК (полиэтилен) 2958, 2873, 1772, 1715 Пример А 9. 3-(2-октил)-3-азабицикло[3.1.0] гексан-2,4-дион. Гидрид натрия (0,11 г) добавляли к раствору 3-азабицикло[3.1.0]гексан-2,4-диона (0,3 г) и 2-бромоктана (0,52 г) в диметилформамиде (5 мл) и полученную в результате смесь перемешивали при комнатной температуре в атмосфере азота в течение 48 ч. Смесь разбавляли водой(15 мл) и затем экстрагировали толуолом (20 мл). Органический экстракт промывали водой(15 мл), сушили (MgSO4) и выпаривали в вакууме. Остаток очищали перегонкой по Kugelrohr(температура кипения 130-140 С при 0,1 мм.рт.ст.) с получением названного в заголовке соединения в виде бесцветного масла. ЯМР (CDCl3) 0,87 (т, 3 Н), 1,03-1,40 (м, 8 Н),1,30 (д, 3 Н), 1,42-1,66 (м, 3 Н), 1,79 - 1,95 (м, 1 Н),2,42 (дд, 2 Н), 3,96 (тк, 1 Н) МС (термическое разбрызгивание) M/Z [М + Н] 224, C13H21NO2 + Н требует 224 ИК (полиэтилен) 2956, 2916,2848, 1771, 1715. Пример Б 1. 3-н-Oктил-3-азабицикло[3.1.0] гексан-2,4-дион (альтернативный путь). Смесь н-октиламина (24,2 г) и 3 азабицикло[3.1.0]гексан-2,4-диона (20,0 г) нагревали при 180 С в течение 2,5 ч и затем охлаждали до комнатной температуры. Смесь перегоняли под вакуумом (температура кипения 140-142 С при 0,1 мм.рт.ст.) с получением названного в заголовке соединения в виде бесцветного масла. ЯМР (СDСl3) 0,83 (т, 3 Н), 1,15-1,30 (м,10 Н), 3,30-1,40 (м, 2 Н), 1,40-1,56 (м. 4 Н), 2,44(дд, 2 Н), 3,31 (т, 2 Н) МС (термическое разбрызгивание) M/Z [М + NH4] 241, C13H21NO2 + NH4 требует 241 ИК (полиэтилен) 2955, 2916, 2848,1771, 1715, 1445, 1395. Пример Б 2. 3-[2-(циклогексен-1-ил)этил]3-азабицикло[3.1.0]гексан-2,4-дион. Смесь 2-(цикпогексен-1-ил)этиламина (0,59 г) и 3-оксобицикло[3.1.0]гексан-2,4-диона (0,5 г) нагревали при 180 С в течение 3 ч. Полученную в результате смесь охлаждали до комнатной температуры с получением названного в заголовке соединения в виде твердого вещества желтого цвета, температура плавления 60-61 С. ЯМР (CDCl3) 1,33 (дт, 1 Н), 1,41-1,65 (м,5 Н), 1,87-2,00 (м, 4 Н), 2,13 (т, 2 Н), 2,41 (дд, 2 Н),3,44 (т, 2 Н), 5,30-5,37 (м, 1 Н) МС (термическое разбрызгивание) M/Z [М + Н] 220, C13H17NO2 + Н требует 220 ИК (полиэтилен) 3100, 2915,2848, 1761, 1714 Пример В 1. 3-(6-гептен-1-ил)-3-азабицикло[3.1.0]гексан-2,4-дион. Диэтилазодикарбоксилат (0,5 г) добавляли по каплям в течение одной минуты к перемешанному раствору трифенилфосфина (0,75 г) в тетрагидрофуране (20 мл) в атмосфере азота. Реакционную смесь перемешивали в течение 5 мин и затем на протяжении 1 мин добавляли по каплям 6-гептен-1-ол (0,36 г), с последующим перемешиванием при -78 С в течение 5 мин. Неопентанол (0,12 г) добавляли к реакционной смеси вслед за 3-азабицикло[3.1.0]гексан-2,4 дионом (0,32 г) и перемешивание продолжали в течение следующих 5 мин при -78 С. Реакционную смесь нагревали до комнатной температуры и перемешивали на протяжении ночи. Летучие соединения удаляли выпариванием в вакууме и остаток растирали в порошок в гексан/дихлорметане и затем фильтровали. Фильтрат выпаривали в вакууме и затем очищали 9 хроматографией на силикагеле, используя в качестве элюента 20% этилацетат/гексан. Названное в заголовке соединение получали в виде бесцветного масла (температура кипения 150160 С при 0,1 мм.рт.ст.). ЯМР (CDCl3) 1,17-1,59 (м, 8 Н), 1,96-2,08(3,46 г) в безводном диметилформамиде (15 мл) при 0 С в атмосфере азота. Реакционную смесь нагревали до комнатной температуры после прекращения бурного выделения газа и перемешивали при комнатной температуре в течение 3 дней. К реакционной смеси добавляли воду(20 мл) и водную смесь экстрагировали эфиром(3 х 20 мл) и затем объединенные органические экстракты промывали водой (2 х 40 мл), сушили(MgSO4) и выпаривали в вакууме. Остаток очищали перегонкой по Kugelrohr с получением названного в подзаголовке соединения в виде бесцветного масла. ЯМР (CDCl3) 0,05 (с, 6 Н), 0,88 (с, 9 Н),1,18-1,39 (м, 5 Н),1,40-1,58(м, 5 Н), 2,45 (дд, 2 Н),3,34 (т, 2 Н), 3,57 (т, 2 Н) МС (термическое разбрызгивание) M/Z [М + Н] 326, C17H31NO3 Si + Н требует 326 ИК (полиэтилен) 3094, 2951,2915, 2862, 1776, 1714(а), 2,2 г) растворяли в уксусная кислота:вода=2:1 и перемешивали при комнатной температуре в течение 7 дней. Реакционную смесь подщелачивали водным раствором бикарбоната натрия и затем экстрагировали эфиром(3 х 50 мл). Объединенные эфирные экстракты сушили (MgSO4) и выпаривали в вакууме с получением желтого масла. Масло перегоняли под вакуумом и затем очищали хроматографией на силикагеле, используя в качестве элюента 70% этилацетат/гексан, с получением названного в подзаголовке соединения в виде бесцветного масла. ЯМР (CDCl3) 1,19-1,43 (м, 5 Н), 1,44 - 1,61(в) 3-(6-фторгекс-1-ил)-3-азабицикло[3.1.0] гексан-2,4-дион Диэтиламиносульфотрифторид (76 мг) добавляли по каплям к перемешанному раствору 3-(6-гидроксигекс-1-ил)-3-азабицикло[3.1.0]гексан-2,4-диона (из стадии (б), 100 мг) в дихлорметане (2,0 мл) при комнатной температуре в атмосфере азота. Реакционную смесь перемешивали на протяжении ночи при комнатной температуре и затем добавляли воду (3 мл). Реакционную смесь экстрагировали эфиром (2 х 10 мл) и объединенные органические экстракты сушили (MgSO4) и выпаривали под вакуумом. Остаток очищали хроматографией на силикагеле (5 г), используя в качестве элюента 40% этилацетат/гексан, с получением названного в заголовке соединения в виде масла бледножелтого цвета. ЯМР (CDCl3) 1,19-1,75 (м, 10 Н), 2,44 (дд,2 Н), 3,34 (т, 2 Н), 4,39 (дт, 2 Н) МС (термическое разбрызгивание) M/Z [М(0,5 г), 1,7-гептандиола (2,46 г), трифенилфосфина (1,42 г) и молекулярные сита с размером пор 4 ангстрема (1,5 г) в безводном тетрагидрофуране (10 мл) в атмосфере азота. Реакционную смесь перемешивали при комнатной температуре в течение 2 дней и затем фильтровали. Твердые остатки промывали этилацетатом (2 х 50 мл) и объединенные фильтраты выпаривали в вакууме. Остаток очищали хроматографией на кремнеземе, используя в качестве элюента 6070% этилацетат/гексан с последующей перегонкой по Kugelrohr (температура кипения 200220 С при 1 мм рт.ст.) с получением названного в подзаголовке соединения в виде вязкого масла. ЯМР (CDCl3) 1,18-1,65 (м, 13 Н), 2,45 (дд,2 Н), 3,33 (т, 2 Н), 3,63 (т, 2 Н) МС (термическое разбрызгивание) M/Z [М + Н] 226, С 12 Н 19NО 3 + Н требует 226 ИК (полиэтилен) 3391, 2916, 2848, 1770, 1714,5,1695(б) 3-(7-оксогепт-1-ил)-3-азабицикло[3.1.0] гексан-2.4-дион Раствор диметилсульфоксида (0,28 мл) в дихлорметане (2 мл) добавляли по каплям на протяжении 5 мин к перемешанному раствору оксалилхлорида (0,16 мл) в дихлорметане (8 мл) при -60 С в атмосфере азота. Полученную в результате смесь перемешивали в течение 15 мин при -60 С и затем на протяжении 5 мин добавляли по каплям 3-(7-гидроксигепт-1-ил)-3 азабицикло[3.1.0]гексан-2,4-дион (из стадии (а), 11 0,37 г). Перемешивание продолжали при -60 С в течение следующих 15 мин и затем добавляли триэтиламин (1,15 мл) и после следующих 5 мин при -60 С реакционной смеси давали нагреться до комнатной температуры. После приблизительно 60 мин к реакционной смеси добавляли воду (10 мл) и перемешивание продолжали в течение 10 мин. Органическую фазу отделяли и водную фазу экстрагировали дихлорметаном (20 мл). Объединенные органические экстракты сушили (Na2SO4) и выпаривали в вакууме до получения желтого масла, которое очищали хроматографией на кремнеземе (10 г),используя в качестве элюента 40% этилацетат/гексан с получением названного в подзаголовке соединения в виде бледно-желтого масла. ЯМР (СDСl3) 1,20-1,40 (м, 5 Н), 1,41-1,70(в) 3-(7,7-дифтор-1-гептил)-3-азабицикло[3.1.0] гексан-2,4-дион Диэтиламиносульфотрифторид (48 мл) добавляли по каплям на протяжении 5 мин к перемешанному раствору 3-(7-оксогепт-1-ил)-3 азабицикло[3.1.0]гексан-2,4-дион (из стадии (б),77 мг) в дихлорметане (10 мл) при комнатной температуре в атмосфере азота и полученную в результате смесь перемешивали при комнатной температуре на протяжении ночи. К реакционной смеси добавляли воду (5 мл), которую затем экстрагировали эфиром (2 х 20 мл), и объединенные органические экстракты сушили (MgSО 4) и выпаривали под вакуумом. Неочищенный продукт очищали хроматографией на кремнеземе (5 г), используя в качестве элюента 50% этилацетат/гексан,с получением названного в заголовке соединения. ЯМР (СDСl3) 1,20-1,91 (м, 12 Н), 2,47 (дд,2 Н), 3,34 (т, 2 Н), 5,78 (тт, 1 Н) МС (термическое разбрызгивание) M/Z [М + Н] 294, C12H17F2NO2 + Н требует 294 ИК (полиэтилен) 3097, 2918, 2850, 1772,1714 Пример Д . Результат биологического теста. Соединение из примера A3 (и Б 1) испытывали в тесте А, приведенном выше. Было обнаружено, что при дозе 2,5 мкг/см 2 соединение проявляет 49% отпугивающую способность. После 24 ч соединение еще проявляло 33% отпугивающую способность. Пример Е. Крем для отпугивания насекомых. Эмульгирующая мазь Британская фармакопия 3-н-Oктил-3-азабицикло[3.1.0]гексан-2,4 дион Феноксиэтанол Очищенная вода, свежекипяченая и охлажденная 12 Крем может быть приготовлен путем растворения феноксиэтанола в очищенной воде с помощью осторожного нагревания. Эмульгирующую мазь расплавляют и затем к ней добавляют раствор феноксиэтанола вместе с 3-ноктил-3-азабицикло[3.1.0]гексан-2,4-дионом,пока мазь еще теплая. Смесь аккуратно помешивают до остывания. При применении для людей крем наносят на открытую кожу обычным образом. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Препарат для отпугивания насекомых или акарид, содержащий соединение формулы I где R представляет собой С 2-10 алкил с прямой или разветвленной цепью, С 2-10 алкенил с прямой или разветвленной цепью или С 2-10 алкинил с прямой или разветвленной цепью, причем эти группы возможно замещены одной или более чем одной группой, выбранной из галогена, С 4-8 циклоалкила и С 4-8 циклоалкенила, и подходящие адьювант, разбавитель или носитель. 2. Препарат по п.1, где R представляет собой C2-10 алкенил с прямой цепью. 3. Препарат по п.2, где R представляет собой 6-гептен-1-ил. 4. Препарат по п.1, где R представляет собой С 2-10 алкил с прямой цепью, возможно замещенный хлором. 5. Препарат по п.1, где R содержит С 4-6 циклоалкильную группу. 6. Препарат по любому из пп.1-5, причем этот препарат является кремом или лосьоном. 7. Соединение формулы I, как определено в п.1, при условии, что R не представляет собой н-бутил или н-октил. 8. Способ отпугивания насекомых или акарид, при котором соединение формулы I, как определено в п.1, наносят на внешние поверхности млекопитающего. 9. Способ по п.8, где млекопитающее является человеком, домашним животным или домашним скотом. 10. Способ по п.8 или 9, где насекомые являются москитами, комарами или мошками. 11. Способ по п.8 или 9, где акариды являются клещами. 12. Способ получения соединения формулы I, как определено в п.7, при котором соединение формулы II а Х представляет собой галоген в присутствии основания. 13. Способ получения соединения формулы I, как определено в п.7, при котором соединение формулы III подвергают взаимодействию с соединением формулы RNH2, где R такой, как определено в п.1. 14. Способ получения соединения формулы I, как определено в п. 7, при котором соединение формулы II 14 15. Способ получения соединения формулы I, как определено в п.7, при котором соединение формулы IV в котором Rd имеет такое же определение как R в п.1, за исключением того, что он замещен ОН или оксогруппой, подвергают взаимодействию с диэтиламинотрифторидом серы с получением соответствующего соединения формулы I, в котором каждая ОН или оксогруппа заменена одним или двумя атомами фтора, соответственно. 16. Соединение формулы IV, как определено в п.15.
МПК / Метки
МПК: A01N 43/38, C07D 209/52
Метки: насекомых, отпугивания, препараты
Код ссылки
<a href="https://eas.patents.su/8-1880-preparaty-dlya-otpugivaniya-nasekomyh.html" rel="bookmark" title="База патентов Евразийского Союза">Препараты для отпугивания насекомых</a>
Предыдущий патент: Продукты с покрытием и их применение на нефтяных месторождениях
Следующий патент: Форма d дигидрата оланзапина
Случайный патент: Устройство манипулирования пожнивными остатками












