Лекарственные средства, содержащие производные полигидроксиалкилпиразина, новые производные полигидроксиалкилпиразина и их получение
Номер патента: 3642
Опубликовано: 28.08.2003
Авторы: Карри Жан-Кристоф, Эвер Мишель, Филош Брюно, Башиард Жорж, Миньяни Серж
Формула / Реферат
1. Лекарственное средство, содержащее в качестве активного начала, по меньшей мере, одно соединение формулы

в которой
либо R2 обозначает цепь -CH2-(CHOH)2-CH3, a R3 обозначает атом водорода, либо R2 обозначает атом водорода, a R3 обозначает цепь -CH2-(CHOH)2-CH3,
или один из его стереоизомеров или одну из его солей с фармацевтически приемлемой минеральной или органической кислотой.
2. Лекарственное средство по п.1, содержащее в качестве активного начала, по меньшей мере, одно из следующих соединений:
1-[6-(2S,3S-дигидроксибутил)пиразин-2-ил]бутан-1S,2R,3S-триол,
1-[6-(2R,3R-дигидроксибутил)пиразин-2-ил]бутан-1R,2S,3R-триол,
1-[6-(2R,3S-дигидроксибутил)пиразин-2-ил]бутан-1S,2S,3S-триол,
1-[5-(2R,3S-дигидроксибутил)пиразин-2-ил]бутан-1S,2S,3S-триол,
или, по меньшей мере, одну из их солей с фармацевтически приемлемой минеральной или органической кислотой.
3. Соединения формулы I
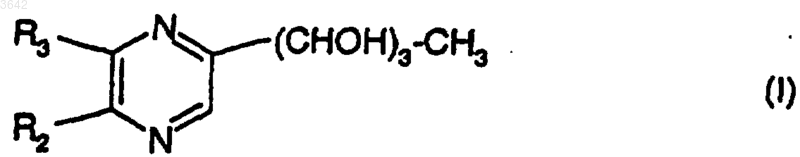
в которой либо R2 обозначает цепь -CH2-(CHOH)2-CH3, a R3 обозначает атом водорода, либо R2 обозначает атом водорода, a R3 обозначает цепь -CH2-(CHOH)2-CH3, за исключением следующих соединений:
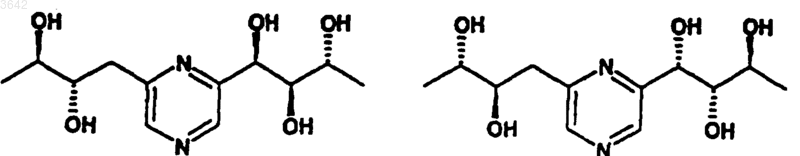
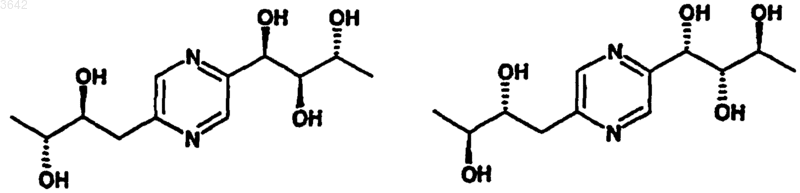
или один из их стереоизомеров, или одна из их солей с минеральной или органической кислотой.
4. Соединения формулы I по п.3, выбранные из следующих соединений:
1-[5-(2R,3S-дигидроксибутил)пиразин-2-ил]бутан-1S,2S,3S-триол,
1-[6-(2S,3S-дигидроксибутил)пиразин-2-ил]бутан-1S,2R,3S-триол,
1-[6-(2R,3R-дигидроксибутил)пиразин-2-ил]бутан-1R,2S,3R-тpиoл,
1-[6-(2S,3S-дигидроксибутил)пиразин-2-ил]бутан-1S,2S,3S-триол,
или соль этих соединений с минеральной или органической кислотой.
5. Способ получения соединений формулы I по п.3, отличающийся тем, что формиат аммония вводят в реакцию с одной или двумя альдозами формулы
H3C-(CHOH)3-CHOH-CHO (II)
выделяют продукт и, при необходимости, превращают его в соль с минеральной или органической кислотой.
6. Применение соединений формулы I
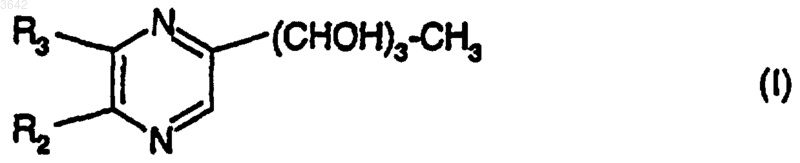
в которой либо R2 обозначает цепь -CH2-(CHOH)2-CH3, a R3 обозначает атом водорода, либо R2 обозначает атом водорода, a R3 обозначает цепь -CH2-(CHOH)2-CH3, или одного из его стереоизомеров, или одной из его солей с минеральной или органической кислотой для приготовления фармацевтических композиций, пригодных для лечения и профилактики диабета и осложнений диабета.
Текст
1 Настоящее изобретение относится к лекарственным средствам, содержащим в качестве активного начала, по меньшей мере, одно соединение формулы или один из его стереоизомеров или одну из его солей с минеральной или органической кислотой, к новым соединениям формулы I, их стереоизомерам, их солям с минеральными или органическими кислотами и к их получению. В формуле I либо R2 обозначает цепь -СН 2(СНОН)2-СН 3, a R3 обозначает атом водорода,либо R2 обозначает атом водорода, a R3 обозначает цепь -СН 2-(СНОН)2-СН 3. Соединения формулы I, содержащие несколько асимметрических атомов углерода, обладают стереоизомерными формами. Эти различные стереоизомеры составляют часть изобретения. Предпочтительными, согласно изобретению, лекарственными средствами являются те,которые содержат в качестве активного ингредиента, по меньшей мере, одно соединение формулы I, выбранное из следующих соединений: 1-[5-(2R,3S-дигидроксибутил)пиразин-2 ил]бутан-1S,2S,3S-триол 1-[5-(2R,3R-дигидроксибутил)пиразин-2 ил]бутан-1S,2S,3R-триол 1-[5-(2S,3S-дигидроксибутил)пиразин-2 ил]бутан-1S,2R,3S-триол 1-[5-(2S,3R-дигидроксибутил)пиразин-2 ил]бутан-1S,2R,3R-тpиoл 1-[5-(2R,3S-дигидроксибутил)пиразин-2 ил]бутан-1R,2S,3S-триол 1-[5-(2R,3R-дигидроксибутил)пиразин-2 ил]бутан-1R,2S,3R-триол 1-[5-(2S,3S-дигидроксибутил)пиразин-2 ил]бутан-1R,2R,3S-триол 1-[5-(2S,3R-дигидроксибутил)пиразин-2 ил]бутан-1R,2R,3R-тpиoл 1-[6-(2R,3S-дигидроксибутил)пиразин-2 ил]бутан-1S,2S,3S-триол 1-[6-(2R,3R-дигидpoкcибyтил)пиразин-2 ил]бутан-1S,2S,3R-триол 1-[6-(2S,3S-дигидроксибутил)пиразин-2 ил]бутан-1S,2R,3S-триол 1-[6-(2S,3R-дигидроксибутил)пиразин-2 ил]бутан-1S,2R,3R-тpиoл 1-[6-(2R,3S-дигидроксибутил)пиразин-2 ил]бутан-1R,2S,3S-триол 1-[6-(2R,3R-дигидpoкcибyтил)пиразин-2 ил]бутан-1R,2S,3R-триол 1-[6-(2S,3S-дигидроксибутил)пиразин-2 ил]бутан-1R,2R,3S-триол 1-[6-(2S,3R-дигидроксибутил)пиразин-2 ил]бутан-1R,2R,3R-триол и их соли с минеральными или органическими кислотами. 2 Особо предпочтительными лекарственными средствами являются те, которые содержат в качестве активного начала, по меньшей мере,одно соединение формулы I, выбранное из следующих соединений: 1-[6-(2S,3S-дигидроксибутил)пиразин-2 ил]бутан-1S,2R,3S-триол 1-[6-(2R,3R-дигидроксибутил)пиразин-2 ил]бутан-1R,2S,3R-триол 1-[6-(2R,3S-дигидроксибутил)пиразин-2 ил]бутан-1S,2S,3S-триол 1-[5-(2R,3S-дигидроксибутил)пиразин-2 ил]бутан-1S,2S,3S-триол и их соли с минеральными или органическими кислотами. Соединения приведенной ниже формулы I являются известными (патент JP78-90401): Никакой фармакологической активности для всех этих соединений описано не было. Остальные соединения формулы I, их стереоизомеры и их соли с минеральными или органическими кислотами являются новыми и составляют часть изобретения. Предпочтительными соединениями формулы I являются следующие соединения: 1-[6-(2S,3S-дигидроксибутил)пиразин-2 ил]бутан-1S,2R,3S-триол 1-[6-(2R,3R-дигидроксибутил)пиразин-2 ил]бутан-1R,2S,3R-триол и их соли с минеральными или органическими кислотами. Соединения формулы I могут быть получены действием формиата аммония на одну или две альдозы формулы: Н 3 С-(СНОН)3-СНОН-СНО (II) или один из их стереоизомеров. Эту реакцию обычно проводят в водной среде при температуре от 20 до 100 С. Альдозы Н 3 С-(СНОН)3-СНОН-СНО и их стереоизомеры поставляются в продажу и могут быть получены а) из имеющихся в продаже альдоз: реакциями эпимеризации с применением или адаптированием методов, описанных в Adv.Carbohydr. Chem., 13, 63 (1958), в частности в основной среде с помощью разбавленного водного раствора гидроксида натрия (0,03-0,05%) при температуре от 20 до 40 С; реакциями удлинения цепи с применением или адаптированием методов, описанных в "The(1972), и, в частности, с образованием циангидрина исходной альдозы (например действием 3 цианида натрия в водном растворе при температуре от 10 до 30 С в присутствии гидроксида натрия при рН, близком к 9) с последующим гидролизом образовавшейся при этом нитрильной функции в соответствующую кислотную группу с применением или адаптированием методов, описанных в Organic Synthesis, volume 1,p.436 и volume III, p.85 (например с помощью хлористо-водородной или концентрированной серной кислоты в водном растворе при температуре от 20 С до температуры кипения реакционной среды) с последующим восстановлением карбоксильной функции в соответствующую альдегидную с применением или адаптированием методов, описанных в J. Am. Chem. Soc., 71,122 (1949), в частности с помощью борогидрида щелочного металла (например борогидрида натрия) в водном растворе при температуре от 20 С до температуры кипения реакционной среды; реакциями укорочения цепи с применением или адаптированием методов, описанных вD.Horton, Academic Press, New-York, Volume IB,1980, p.929 или Chem. Ber., 83, 559 (1950) и, в частности, превращая альдегидную функцию альдозы в соответствующую гидросиламиновую группу, применяя или адаптируя методы, описанные в Organic Synthesis, volume 2, p. 314 (например с помощью гидрохлорида гидроксиламина в водном растворе в присутствии основания, такого как карбонат натрия при температуре от 20 до 50 С) с последующим действием 3,4 динитрофторбензолом в присутствии двуокиси углерода и основания, такого как бикарбонат натрия в водном растворе с алифатическим спиртом (например изопропиловым спиртом) при температуре от 50 до 80 С; реакциями дезоксигенирования с применением или адаптированием методов, описанных вCarbohydr. Res., 36, 392 (1974) и 28D, 357 (1996),в частности, превращая спиртовую функцию альдозы в соответствующую сульфонатную группу, применяя или адаптируя методы, описанные в Carbohydr. Res., 54, 105 (1977) и J. Carbohydr. Chem., 6, 169 (1987) и 6, 537, (1987), например с помощью метансульфонилхлорида или п-толуолсульфонилхлорида в присутствии основания с последующим действием борогидридом натрия или алюмогидридом лития в растворителе, таком как диметил-сульфоксид или бензол и диэтиловый эфир, соответственно, при температуре от 20 С до температуры кипения реакционной среды; b) из соответствующих аллиловых спиртов с применением или адаптированием методов, описанных в Science, 220, 949(1983), и, в частности, с помощью гидропероксида трет-бутила в присутствии комплекса титана (IV), такого как изопропилатный комплекс титана (IV) и оптически чистого диалкилтартрата (например ди-этилтартрата) с последующим последовательным действием тиофенолятом 4 натрия, п-хлорнадбензойной кислотой в уксусном ангидриде и гидридом диизопропилалюминия. Реакционные смеси, полученные в различных описанных выше процессах, обрабатывают,используя традиционные физические методы(например, упаривание, экстракцию, перегонку,хроматографию, кристаллизацию) или химические (например, образование солей). Соединения формулы I могут быть при необходимости превращены в солевые аддукты с минеральными или органическими кислотами при действии этими кислотами в органическом растворителе, таком как спирты, кетоны, простые эфиры или хлорсодержащие растворители. Эти соли также составляют часть изобретения. В качестве примеров фармацевтически приемлемых солей могут быть названы солевые аддукты с минеральными или органическими кислотами, такие как ацетат, пропионат, сукцинат, бензоат, фумарат, малеат, оксалат, метансульфонат, изетионат, теофиллинацетат, салицилат, метилен-бисоксинафтоат, гидрохлорид, сульфат, нитрат и фосфат. Изобретение иллюстрируют следующие примеры: Пример 1. Раствор 10 г L-фукозы и 19,2 г формиата аммония в 30 см 3 воды кипятят с обратным холодильником в течение 6 ч, после чего раствору дают охладиться до комнатной температуры. Смесь упаривают при пониженном давлении(2,7 кПа) и температуре 50 С. Пастообразный красно-коричневый остаток поглощают 50 см 3 этанола, растирают, фильтруют и промывают нерастворимую фракцию этанолом (повторяют операцию еще один раз). Фильтрат упаривают при пониженном давлении (2,7 кПа) и температуре 50 С, получая бурую пасту, которую очищают хроматографически на колонке с силикагелем (0,020-0,045 мм) под давлением приблизительно 1,5105 Па, элюируя смесью хлорформ/метанол/водно-аммиачный раствор (12/6/1 по объему). Фракции, содержащие искомый продукт, объединяют, упаривают при пониженном давлении (2,7 кПа) и температуре 50 С. Полученную бурую пасту поглощают 3 см 3 этанола и затем вновь упаривают при пониженном давлении (2,7 кПа) и температуре 50 С, получая красно-коричневую пасту. После лиофилизации получают 1,23 г 1-[6-(2S,3S-дигидроксибутил)пиразин-2-ил]бутан-1S,2R,3S-триола в виде бежевого цвета твердого вещества [Спектр ЯМР 1 Н (400 МГц, (СD3)2SO d6,в м.д.): 1,10 и 1,12 в 2), 4,55 (мт, 2 Н : ОН в 6b и ОН в 6); 4,61 (дд,J = 7 и 5 Гц, 1 Н : СН 2), 5,49 (д уширенный, J = 5 Гц, 1 Н : ОН в 2); 8,40 (с, 1 Н : =СН в 5), 8,48 (с,1 Н : =СН в 3). aD20=-37,6+/-1,0 (с=0,5/метанол)]. Пример 2. Раствор 2 г -L-рамнозы и 7 г формиата аммония в 8 см 3 воды кипятят с обратным холодильником в течение 0,5 ч, после чего дают охладиться до комнатной температуры. Смесь фильтруют и затем фильтрат упаривают при пониженном давлении (2,7 кПа) и температуре 45 С. Остаток трижды поглощают диэтиловым эфиром, который затем упаривают. Полученное таким образом пастообразное твердое вещество дважды экстрагируют 200 см 3 ацетона. Растворы поглощают при пониженном давлении (2,7 кПа) и температуре 45 С, остатки поглощают 100 см 3 этанола, фильтруют и объединяют растворы. Объединенный фильтрат упаривают при пониженном давлении (2,7 кПа) и температуре 45 С, после чего остаток поглощают дихлорметаном. Осадок отфильтровывают, получая бурое твердое вещество. Последнее хроматографируют на колонке с силикагелем (0,040-0,063 мм),элюируя смесью этилацетат/метанол/уксусная кислота (6/1/1 по объему). А - Фракции, содержащие продукт со значением Rf, близким к 0,3, объединяют и упаривают при пониженном давлении (2,7 кПа) и температуре 40 С. Полученное при этом масло вновь хроматографируют на колонке с силикагелем (0,040-0,063 мм), элюируя смесью этилацетат/этанол/водно-аммиачный раствор/вода(40/10/2/2 по объему). Фракции, содержащие искомый продукт, собирают и упаривают при пониженном давлении (2,7 кПа) и температуре 40 С. Полученное при этом масло растирают в диэтиловом эфире, после чего поглощают малым количеством этанола и отфильтровывают образовавшийся осадок, получая 64 мг 1-[6-(2R,3S-дигидроксибутил)пиразин-2-ил]бутан-1S,2S,3S-триола в виде белого порошка [Спектр ЯМР 1=СН в 5); 8,55 (с, 1 Н : =СН в 3). В - Фракции, содержащие продукт со значением Rf, близким к 0,35, объединяют и упаривают при пониженном давлении (2,7 кПа) и температуре 40 С. Полученное при этом масло вновь хроматографируют на колонке с силикагелем (0,0400,063 мм), элюируя смесью этилацетат/этанол/водно-аммиачный раствор/вода (40/10/2/2 по объему). Фракции, содержащие искомый продукт, 003642 6 собирают и упаривают при пониженном давлении(2,7 кПа) и температуре 40 С. Полученное при этом масло растирают в диэтиловом эфире, после чего поглощают малым количеством этанола и отфильтровывают образовавшийся при этом осадок, получая 48 мг 1-[5-(2R,3S-дигидроксибутил)пиразин-2-ил]бутан-1S,2S,3S-триола в виде белого порошка. Спектр ЯМР 1 Н (400 МГц, (CD3)2SO d6,в м.д.) : 1,12 (д, J = 6 Гц, 3H : СН 3 5d); 1,15 (д, J = 6 Гц, 3H : СН 3 2d); 2,69 и 3,05 (2 дд, соответственно, J = 14 и 9 Гц и J = 14 и 4 Гц, 1 Н каждый : СН 2 5); от 3,30 до 3,45 (мт, 1 Н : СН 2b); 3,49=СН в 6); 8,65 (с, 1 Н : =СН в 3). Пример 3. Раствор 3,28 г D-фукозы и 6,31 л формиата аммония в 12 см 3 воды кипятят с обратным холодильником в течение 2 ч, после чего раствору дают охладиться до комнатной температуры. Смесь упаривают при пониженном давлении(2,7 кПа) и температуре 55 С. Пастообразный остаток поглощают 70 см 3 этанола, растирают,фильтруют и промывают нерастворимую фракцию этанолом (повторяя операцию три раза). Фильтрат упаривают при пониженном давлении(2,7 кПа) и температуре, близкой к 50 С, получая бурое масло (1,8 г), которое очищают хроматографией на колонке с силикагелем (0,0200,045 мм), элюируя смесью хлороформ/ метанол/водно-аммиачный раствор (12/6/1 по объему) и собирая фракции объемом 50 см 3. Фракции, содержащие искомый продукт, объединяют, упаривают при пониженном давлении(2,7 кПа) и температуре 50 С. Полученную бурую пастообразную массу хроматографируют второй раз в тех же условиях. Фракции, содержащие искомый продукт, объединяют, упаривают при пониженном давлении (2,7 кПа) и температуре 50 С. Полученное при этом масло поглощают 8 см 3 дистиллированной воды, раствор фильтруют и лиофилизуют, получая 0,25 г 1-[6-(2R,3R-дигидроксибутил)пиразин-2-ил]бутан-1R,2S,3R-триола в виде бежевого цвета твердого вещества [Спектр ЯМР 1H (400 МГц,(CD3)2SO d6, при температуре 353 Кв м.д.): 1,14 (д, J = 7 Гц, 3H : СН 3 6); 1,16 (д, J = 7 Гц,3H : СН 3 2); 2,82 и 2,97 (2 дд, соответственно, J(мт, 1 Н : СН 6); 3,88 (мт, 1 Н : СН 2); от 3,90 до 4,30 (mf, 4 Н : ОН), 4,67 (д, J = 7 Гц, 1 Н : СН 2); 5,18 (mf, 1 Н : ОН); 8,41 (с, 1 Н : =СН в 5); 8,52 (с, 1 Н : =СН в 3)]. Соединения формулы I обладают ценными фармакологическими свойствами, являясь гипогликемическими агентами. 7 Гипогликемическая активность соединений формулы I была определена по гипергликемической реакции при пероральном введении глюкозы мышам с нормальным уровнем сахара в соответствии со следующей прописью: Мышей Swiss-альбиносы весом от 22 до 26 г лишают питания в течение 2 ч. В конце этого периода измеряют уровень сахара и непосредственно после этого мышам вводят внутрь глюкозу в дозе 2 г/кг. Через 30 мин вновь измеряют уровень сахара. Отбирают мышей с гипергликемической реакцией выше 170 мг/дл с целью использования их для определения гипогликемической активности соединений изобретения. Отобранных таким образом мышей распределяют по группам, включающим, по меньшей мере, 10 животных. Отдельные группы получают один раз в день раствор от 3 до 50 мг/кг тестируемого соединения в носителе, таком как вода или метилцеллюлоза/твин и вода через желудочную трубку. Такой режим выдерживают в течение 4 дней. На четвертый день после последнего введения испытываемого соединения животные получают глюкозу в дозе 2 г/кг и спустя 20-40 мин измеряют уровень сахара. Степень ингибирования гипергликемической реакции при вводе глюкозы рассчитывают по отношению к реакции, измеряемой в группе,получающей только носитель. В этом тесте соединения изобретения показывают степень ингибирования гликемии,большую или равную 10%. Соединения общей формулы I настоящего изобретения обладают низкой токсичностью. Их летальная доза ЛД 50 при пероральном введении мышам выше 2000 мг/кг. При терапии на человеке эти соединения пригодны для профилактики и лечения диабета и, в частности, диабета типа II (диабет NID),диабета тучных, диабета пятидесятилетних, метаплеторического диабета, диабета пожилых и легкого диабета. Они могут быть использованы как дополнение к инсулинотерапии при инсулинозависимом диабете или для постепенного уменьшения дозы инсулина или же использоваться при лабильном диабете и инсулинонезависимом диабете в качестве дополнения к гипогликемическим сульфамидам, когда последние не обеспечивают достаточного снижения уровня сахара. Эти соединения могут быть также использованы при осложнениях диабета,таких как гиперлипемии, нарушения липидного метаболизма, дислипемии, ожирение. Соединения представляют также интерес для профилактики и лечения атеросклеротических нарушений и их осложнений (коронопатии, инфаркт миокарда, кардиомиопатии, переход этих осложнений в недостаточность левого желудочка сердца, различные артериопатии, артерииты нижних конечностей с хромотой и развитием язв и гангрены, цереброваскулярная недостаточность и ее осложнения, сексуальное бессилие сосуди 003642 8 стого происхождения) , диабетической ретинопатии и всех ее проявлений (увеличение капиллярной проницаемости, расширение капилляров и тромбоз, микроаневризмы, артериовенозный шунт, расширение вен, точечные и пятнистые кровотечения, экссудаты, пятнистые отеки, проявления пролиферирующей ретинопатии: неоваскуляризация, пролиферирующие ретинитные рубцы, геморрагии стекловидного тела,отслойка сетчатки) , диабетической катаракты,различных форм диабетической невропатии(периферические полиневропатии и ее проявления, такие как парестезии, гиперэстезии и боли,мононевропатии, радикулопатии, автономные невропатии, диабетические амиотрофии), проявлений диабетической стопы (язвы нижних конечностей и стопы), диабетической невропатии в ее обеих формах (диффузной и узелковой), атероматоза (повышение уровня липопротеинов высокой плотности, способствующее удалению холестерина из атеромных бляшек,снижение уровня липопротеинов низкой плотности, уменьшение отношения уровня липопротеинов низкой плотности к уровню липопротеинов высокой плотности, ингибирование окисления липопротеинов низкой плотности, уменьшение клейкости тромбоцитов), гиперлипемий и дизлипемий (гиперхолестероимии, гипертриглицеридимии, нормализация уровня жирных кислот, нормализация урикемии, нормализация апобелков А и В), катаракты, артериальной гипертензии и ее последствий. Лекарственные средства изобретения представляют собой либо одно соединение согласно изобретению или их смесь в чистом состоянии, либо композицию, в которой соединение согласно изобретению ассоциировано с каким-либо другим фармацевтически приемлемым продуктом, которое может быть либо инертным,либо физиологически активным. Лекарственные средства изобретения могут применяться перорально, парентерально, ректально или местно. Твердые композиции для перорального применения могут использоваться в виде таблеток, пилюль, порошков (желатиновые капсулы,облатки) или гранул. В этих композициях активное начало изобретения смешивают в токе аргона с несколькими инертными разбавителями, такими как крахмал, целлюлоза, сахароза,лактоза или кремнезем. Эти композиции могут также содержать отличные от разбавителей вещества, например, один или несколько смазочных агентов, таких как стеарат магния или тальк, один краситель, покрытие (для драже) или лак. Жидкие композиции для перорального применения могут использоваться в виде растворов, суспензий, эмульсий, сиропов и фармацевтически приемлемых эликсиров, содержащих инертные разбавители, такие как вода, этанол, глицерин, растительные масла или парафиновое масло. Эти композиции могут содержать отличные от разбавителей вещества, например,смачивающие агенты, мягчители, загустители,ароматизирующие добавки или стабилизаторы. Стерильные композиции для перорального применения преимущественно могут представлять собой водные или неводные растворы, суспензии или эмульсии. В качестве разбавителя или носителя может быть использована вода,пропиленгликоль, полиэтиленгликоль, растительные масла (в частности оливковое масло),пригодные для инъекций органические сложные эфиры, например этилолеат, или другие подходящие органические растворители. Композиции могут также содержать добавки, в частности увлажняющие агенты, изотонирующие добавки,эмульгаторы, диспергаторы и стабилизаторы. Стерилизация может осуществляться несколькими способами, например с помощью асептической фильтрации, путем введения специализирующих агентов, облучения или нагревания. Композиции могут быть также приготовлены в виде стерильных твердых композиций, которые могут быть растворены непосредственно перед применением в стерильной воде или любой другой, пригодной для инъекций стерильной среде. Композиции для ректального применения представляют собой ректальные свечи или капсулы, содержащие кроме активного начала инертные вещества, такие как масло какао, полусинтетические глицериды или полиэтиленгликоли. Композиции для местного применения могут, например, представлять собой кремы, лосьоны, глазные капли, полоскания, капли для носа или аэрозоли. Дозы зависят от желаемого эффекта, длительности лечения или используемого метода введения препарата. Обычно они составляют от 150 до 600 мг/сутки при пероральном применении для взрослых при разовых дозах от 50 до 200 мг активного начала. В общем случае врач определит дозировку в зависимости от возраста, веса и остальных характеризующих больного факторов. Изобретение иллюстрируют следующие примеры: Пример А. Изготовляют обычными способами желатиновые капсулы с 50 мг активного продукта,имеющие следующий состав: Активный продукт 50 мг Целлюлоза 18 мг Лактоза 55 мг Гель кремниевой кислоты 1 мг Натриевый карбоксиметилкрахмал 10 мг Тальк 10 мг Стеарат магния 1 мг Пример В. Изготовляют обычными способами таблетки с 50 мг активного продукта, имеющие следующий состав: Активный продукт 10 Лактоза 104 мг Целлюлоза 40 мг Поливинилпирролидон 10 мг Натриевый карбоксиметилкрахмал 22 мг Тальк 10мг Стеарат магния 2 мг Гель кремниевой кислоты 2 мг Смесь гидроксиметилцеллюлозы, глицерина,оксида титана (72/3,5/24,5) в количестве, достаточном для общей массы таблетки 245 мг Пример С. Приготовляют обычными способами раствор для инъекций с 50 мг активного продукта,имеющий следующий состав: Активный продукт 50 мг Бензойная кислота 80 мг Бензиловый спирт 0,06 мл Бензоат натрия 80 мг 95%-ный этанол 0,04 мл Гидроксид натрия 24 мг Пропиленгликоль 1,6 мл Вода в достаточном количестве до 4 мл Изобретение относится также к применению соединений общей формулы I, их стереоизомеров и их солей с минеральными или органическими кислотами для приготовления фармацевтических композиций, пригодных для лечения или профилактики диабета или осложнений диабета. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Лекарственное средство, содержащее в качестве активного начала, по меньшей мере,одно соединение формулы-СН 2-(СНОН)2-СН 3,или один из его стереоизомеров или одну из его солей с фармацевтически приемлемой минеральной или органической кислотой. 2. Лекарственное средство по п.1, содержащее в качестве активного начала, по меньшей мере, одно из следующих соединений: 1-[6-(2S,3S-дигидpoкcибyтил)пиpaзин-2 ил]бyтaн-1S,2R,3S-триол,1-[6-(2R,3R-дигидpoкcибyтил)пиразин-2 ил]бутан-1R,2S,3R-триол,1-[6-(2R,3S-дигидроксибутил)пиразин-2 ил]бутан-1S,2S,3S-триол,1-[5-(2R,3S-дигидроксибутил)пиразин-2 ил]бутан-1S,2S,3S-триол или, по меньшей мере, одну из их солей с фармацевтически приемлемой минеральной или органической кислотой. 3. Соединения формулы I в которой либо R2 обозначает цепь -СН 2(СНОН)2-СН 3, a R3 обозначает атом водорода,либо R2 обозначает атом водорода, a R3 обозначает цепь -СН 2-(СНОН)2-СН 3, за исключением следующих соединений: или один из их стереоизомеров, или одна из их солей с минеральной или органической кислотой. 4. Соединения формулы I по п.3, выбранные из следующих соединений: 1-[5-(2R,3S-дигидроксибутил)пиразин-2 ил]бутан-1S,2S,3S-триол,1-[6-(2S,3S-дигидроксибутил)пиразин-2 ил]бутан-1S,2R,3S-триол,1-[6-(2R,3R-дигидроксибутил)пиразин-2 ил]бутан-1R,2S,3R-тpиoл, 12 1-[6-(2S,3S-дигидроксибутил)пиразин-2 ил]бутан-1S,2S,3S-триол или соль этих соединений с минеральной или органической кислотой. 5. Способ получения соединений формулыI по п.3, отличающийся тем, что формиат аммония вводят в реакцию с одной или двумя альдозами формулы Н 3 С-(СНОН)3-СНОН-СНО(II) выделяют продукт и, при необходимости, превращают его в соль с минеральной или органической кислотой. 6. Применение соединений формулы I в которой либо R2 обозначает цепь -СН 2(СНОН)2-СН 3, a R3 обозначает атом водорода,либо R2 обозначает атом водорода, a R3 обозначает цепь -СН 2-(СНОН)2-СН 3, или одного из его стереоизомеров, или одной из его солей с минеральной или органической кислотой для приготовления фармацевтических композиций, пригодных для лечения и профилактики диабета и осложнений диабета.
МПК / Метки
МПК: C07D 241/12, A61P 3/10, A61K 31/495
Метки: лекарственные, новые, полигидроксиалкилпиразина, содержащие, средства, получение, производные
Код ссылки
<a href="https://eas.patents.su/7-3642-lekarstvennye-sredstva-soderzhashhie-proizvodnye-poligidroksialkilpirazina-novye-proizvodnye-poligidroksialkilpirazina-i-ih-poluchenie.html" rel="bookmark" title="База патентов Евразийского Союза">Лекарственные средства, содержащие производные полигидроксиалкилпиразина, новые производные полигидроксиалкилпиразина и их получение</a>
Предыдущий патент: Диарильные производные, способы их получения, применение, фармацевтическая композиция и способ лечения
Следующий патент: Композиции, содержащие лактадгерин или его варианты, и способы их использования
Случайный патент: Установка и способ обессоливания воды











