Средство, обладающее противовирусной активностью, и способ его получения
Номер патента: 7919
Опубликовано: 27.02.2007
Авторы: Прутков Лев Михайлович, Кузьмич Михаил Константинович
Формула / Реферат
1. Способ получения средства, обладающего противовирусной активностью, на основе комплекса римантадина и альгината натрия, отличающийся тем, что римантадин растворяют при температуре 55-65шС в воде, затем в охлажденный до 15-35шС раствор вводят низкомолекулярный альгинат натрия (вязкость 1% раствора в воде 9-26 мПаъс) при условии, что массовое соотношение римантадин-альгинат натрия составляет (0,56-0,64):1, оставляют набухать в течение 5-10 ч, а затем диспергируют при температуре 15-35шС в течение 30-60 мин высокоскоростной мешалкой до образования стабильного коллоидного раствора солевого комплекса с последующим введением его при температуре 60-80шС в раствор сахара, окрашенный с помощью пищевого красителя.
2. Способ получения средства по п.1, отличающийся тем, что концентрация окрашенного раствора сахара, в который вводят солевой комплекс римантадин-альгинат натрия, составляет 85-95 об.%.
3. Средство, обладающее противовирусной активностью, на основе комплекса римантадина и альгината натрия, отличающееся тем, что оно получено способом по п.1 и содержит исходные компоненты в 100 мл препарата в следующем соотношении:
| Римантадин | 0,18-0,22 г |
| Альгинат натрия | 0,30-0,34 г |
| Сахар (сахароза в виде кристаллов) | 76,9-78,5 г |
| Краситель | 0,0012-0,0014 г |
| Вода | Остальное |
Текст
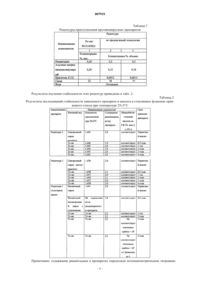
007919 Изобретение относится к медицине, более точно к фармацевтической промышленности, и может быть использовано в промышленной технологии производства препарата для профилактики и лечения вирусных заболеваний различной этиологии. Несмотря на то, что существует большое количество опубликованных статей и изобретений по этой проблеме, поиск новых способов получения таких препаратов, обладающих лучшими качествами по сравнению с известными, является актуальным. Одним из наиболее изученных противовирусных препаратов является римантадин, механизм действия которого хорошо изучен. Однако вследствие присущих этому препарату особых свойств, он имеет большой круг противопоказаний, а в РФ не разрешен для применения у детей в возрасте до 12 лет. Известна полимерная форма римантадина с полимерным носителем на основе сополимера винилового спирта с N-виниламиноянтарной кислотой (RU 2071323). Пришивка римантадина к полимеру существенно улучшает свойства препарата. Известна растворимая форма римантадина в сочетании с альгинатом натрия, которая позволяет использовать форму сахарного сиропа для приготовления препарата под названием Альгирем, который получают путем смешения римантадина, альгината натрия и сахарного сиропа 20-60% (патент RU 2185822, А 61K 31/734, 01.08.2000 г.). Это средство обладает меньшей токсичностью по сравнению с римантадином и при этом обеспечивает оказание лечебного воздействия на частоту выделения резистентных к римантадину вирусов гриппа,а также на вирусы клещевого энцефалита. Этот объект был выбран в качестве наиболее близкого аналога заявленного изобретения. Однако известный препарат нестабилен при хранении, при долговременном хранении проявляется неоднородность системы, появляются отдельные сгустки, а вязкостные свойства препарата изменяются во времени,что проявляется в изменении показателя плотности. Это связано с тем, что известный способ получения препарата Альгирем не обеспечивает получение устойчивого коллоидного раствора, стабильного во времени. Это делает предложенную технологию проблематичной для промышленного применения. Кроме того, возможно ухудшение при длительном хранении такого важного для фармации показателя, как микробиологическая чистота вследствие отсутствия в составе средства - аналога консервантов и низкой концентрации сахара (60 вес.%), которая не может гарантировать эффект консервации при длительном хранении. Задача настоящего изобретения заключается в разработке нового лекарственного средства на основе римантадина, лишенного недостатков известных средств, и способа его получения. Поставленная задача решается следующим образом. Способ получения заключается в проведении технологии в 3 этапа. На первом этапе проводят прививку к природному низкомолекулярному (вязкость 1% раствора 9,026 мПас) мукополисахариду - альгинату натрия, альфаметил-1-адамантил-метиламина гидрохлорида(римантадин) в водном растворе при соотношении римантадин:альгинат натрия (0,56-0,64):1. Для получения стабильного коллоидного раствора необходимо предварительно провести набухание мукополисахарида при температуре 15-35 С в течение 5-10 ч, после чего провести диспергирование высокоскоростной мешалкой при скорости не менее 500 об./мин в течение 30-60 мин. На втором этапе получают сахарный сироп, окрашенный подходящим красителем, например Е 122. На третьем этапе в сахарный сироп, охлажденный до температуры 60-80 С, вводят расчетное количество коллоидного раствора солевого комплекса римантадин-альгинат натрия с таким расчетом, чтобы конечная концентрация римантадина в готовом противовирусном средстве составляла 0,20,02 г в 100 мл. Техническим результатом изобретения является создание оригинальной технологии получения стабильного коллоидного раствора прочного солевого комплекса, позволяющего получить средство, обладающее противовирусной активностью за счет наличия в нем римантадина, но с лучшими характеристиками препарата при длительном (до 4 лет) хранении и сниженной токсичностью по сравнению с аналогом. Сущность предлагаемого изобретения раскрывается ниже. Альгинат натрия-гидрофильный коллоид. Когда масса альгината помещается в воду без достаточного режима перемешивания (разделения индивидуальных гранул при высокоскоростном диспергировании), то формируются комки гранул. На поверхности этих сольватированных комков образуется слой, который предотвращает смачивание внутри них, и при длительном хранении образуются сгустки. Поэтому правильно выбранный режим однородного диспергирования - важнейший этап технологии, влияющий на стабильность конечного средства. Вторым немаловажным условием получения стабильного прочного солевого комплекса является правильный выбор марки альгината натрия, которых насчитывается великое множество, и его соотношение к римантадину, так как необходимо проводить реакцию прививки при строгих стехиометрических соотношениях, не допускающих избытка римантадина в реакционной среде. Альгинаты, выделенные из различных видов водорослей и полученные по различным технологиям,обладают различными физико-химическими свойствами, что сказывается, в первую очередь, на их реологии. Так, низкомолекулярные альгинаты уже имеют вязкость 1% раствора 9-26 мПас, а вязкость 1%-1 007919 растворов высокомолекулярных альгинатов достигает 5-10 тыс. мПас, с существенным снижением текучести. При увеличении концентрации альгинатов растворы переходят в гелеобразное нетекучее состояние, вплоть до образования студней, что неприемлемо при получении лечебных сиропов. В связи с тем, что раствор солевого комплекса для получения лечебного средства вводят в заранее подготовленный сахарный сироп, для решения конечной задачи необходимо выполнить ряд условий: концентрация сахара в готовом средстве должна быть 60 мас.% для обеспечения длительного консервирующего действия; концентрация альгината должна быть максимальной, чтобы обеспечить минимальное разбавление промежуточного сахарного сиропа после введения раствора солевого комплекса; в солевом комплексе не должно быть несвязанного с полимером римантадина. В результате многочисленных экспериментов было установлено, что наиболее технологически приемлемым является низкомолекулярный альгинат натрия (НМА) (вязкость 1% раствора 9-26 мПас ), который позволяет получать текучие 2% растворы. На следующем этапе, с использованием метода гельфильтрации на колонке с сефадексом G50, было установлено, что оптимальным соотношением в таких растворах римантадин-НМА является (0,56-0,64):1. Именно при таком соотношении при элюировании хроматографической колонки с сефадексом G50 наблюдается только первый пик полимерного комплекса(М.В.=10-50 тыс.), выходящий холостым объемом колонки, и не наблюдается второй пик, характерный для низкомолекулярного римантадина (М.В.=260). Соотношение римантадин-НМА, равное 1:1, оказалось в данном случае не оптимальным, т.к. на хроматограмме выявлялся второй пик римантадина, частично не вступившего в реакцию солеобразования, возможно, также из-за не выполнения операции диспергирования. Таким образом, способ получения солевого комплекса (1 этап технологии) заключается в следующем. Сначала в 3,5 л подогретой до 55-65 С воды растворяют 0,04 кг римантадина при перемешивании в течение 30-35 мин и после полного растворения римантадина раствор охлаждают до 15-35 С. В полученный раствор вводят порошок НМА в количестве 0,065 кг и оставляют набухать при этой температуре в течение 5-10 ч, после чего проводят диспергирование высокоскоростной мешалкой при скорости не менее 500 об./мин в течение 30-60 мин до образования стабильного коллоидного раствора солевого комплекса. Этот раствор может храниться до 30 суток и использоваться частями при введении в подготовленный сахарный сироп. Отдельно проводят приготовление сахарного сиропа в воде. При температуре воды 60-80 С и перемешивании растворяют в 6,8 л воды 15,7 кг сахара (сахарозы в виде кристаллов) и после получения сиропа в него вводят расчетное количество пищевого красителя (0,2-0,23 г), предпочтительно Е 122. Объем сахарного сиропа составит 16,2-16,4 л. В полученный окрашенный сахарный сироп с температурой 50-70 С медленно (20-40 мин) вводят ранее приготовленный раствор комплекса римантадин-НМА в количестве 3,5 л и после охлаждения раствора до температуры 20-25 С объем доводят водой до 20 л. Получается окрашенный сироп сладкого вкуса с горьковатым привкусом, плотностью 1,28 г/см 3 и концентрацией римантадина 2 мг/мл, представляющий собой средство для профилактики и лечения вирусных заболеваний (сироп для детей). Объектом изобретения является средство, обладающее противовирусной активностью, на основе комплекса римантадина и альгината натрия, полученное описанным способом, при следующем содержании исходных компонентов: Римантадин 0,18-0,22 г Альгинат натрия 0,30-0,34 г Сахар (сахароза в виде кристаллов) 76,9-78,5 г Краситель 0,0012-0,0014 г Вода До 100 мл Средство имеет плотность 1,280,05 г/см 3 при температуре 202 С. По показателю биодоступности и пролонгирующему действию средство практически не отличается от аналога. Так, после приема внутрь средства с концентрацией римантадина 2 мг/мл из расчета 5 мг/кг массы тела римантадин появляется в плазме крови через 1,5-2 ч; спустя еще 4 ч в плазме (Tmax=5,5 ч) достигается максимальная концентрация римантадина 0,6-1,0 мкг/мл (Сmax), которая поддерживается на этом уровне в течение не менее 6-8 ч. В табл. 1 приведены рецептуры противовирусного средства, которые были подвергнуты исследованию на стабильность при длительном хранении.-2 007919 Таблица 1 Рецептуры приготовления противовирусных препаратов Результаты изучения стабильности этих рецептур приведены в табл. 2. Таблица 2 Результаты исследований стабильности заявленного препарата и аналога в стеклянных флаконах оранжевого стекла при температуре 255 С Примечание: содержание римантадина в препаратах определяли потенциометрическим титровани-3 007919 ем 5 мл препарата 0,01 М раствором нитрата серебра с использованием -Сl или S2- - ионселективного или серебряного индикаторного электрода. Как следует из данных табл. 2, заявленное средство, полученное по предложенной технологии, имеет лучшие показатели при длительном хранении по сравнению с аналогом, что является крайне важным при производстве и выпуске в обращении лекарственных средств. Анализировали также токсичность полученного средства в сравнении с аналогом. К сожалению,описанная в аналоге методика определения токсичности представляется недостаточно адекватной, т.к. она однозначно доказывает, что альгинат натрия, после введения в сахарный сироп, содержащий римантадин, снижает токсическое воздействие последнего на организм белых мышей, но не совсем ясно, относится ли этот результат к комплексу римантадин-альгинат натрия. Чтобы избежать этого, нами была использована специальная методика сравнительного изучения токсичности растворов комплекса римантадин-альгинат натрия в сахарном сиропе по сравнению с римантадином. Так как при пероральном способе введения не удалось добиться летального исхода, эксперименты проводили на модели внутрибрюшинной инъекции. На первом этапе был определен уровень летальной токсичности римантадина. Римантадин вводили группам мышей, изменяя дозу на порядок(1500 мг/кг; 150 мг/кг; 15 мг/кг). При максимальной дозе все животные гибли в течение 3-5 мин. При минимальной дозе все животные в группе в течение времени наблюдения (8 суток) выживали. Растянутая гибель, которую можно было разнести по времени наблюдения, регистрировалась для дозы 150 мг/кг. На втором этапе был определен диапазон летальной токсичности римантадина. Дозу вводимого препарата изменяли дробно с шагом 40 мг/кг в пределах от 20 до 160 мг/кг. Летальная токсичность наблюдалась только при использовании дозы 160 мг/кг, которая и была определена для римантадина при сравнительном изучении препаратов. На третьем этапе изучалась острая токсичность препаратов, при дозе 160 мг/кг по римантадину. Для этого был подготовлен водный раствор римантадина с концентрацией 16 мг/мл, а также 20% сахарные сиропы, содержащие комплекс римантадин-альгинат натрия с концентрацией римантадина 16 мг/мл(максимально возможная концентрация), приготовленные как рекомендовано в аналоге изобретения (1) и по предлагаемому способу (2). Сравнительные испытания проводили на группах, содержащих по 20 мышей. Полученные результаты приведены в табл. 3. Таблица 3 Сравнительные данные токсичности препаратов римантадин, аналог (1) и заявленного средства (2) при дозе 160 мг/кг римантадина Для наглядности эти результаты могут быть представлены в виде кривых выживаемости, которые построены по методу Каплана-Мейера (Доля выживших во времени мышей). Кривые выживаемости, построенные по методу Каплана-Мейера, для тестируемых препаратов различаются. По этому признаку применим логранговый критерий с нулевой статистической гипотезой об одинаковости выживаемости в группах мышей, причем в данном случае нулевая гипотеза об отсутствии различия в действии препаратов не выполняется. На этом основании можно утверждать, что препарат,полученный по патенту RU 2185822, обладает меньшей токсичностью по сравнению с римантадином, а средство, получаемое заявленным способом, обладает еще меньшей токсичностью по сравнению с аналогом. Этот фактор имеет важное значение при создании лечебных препаратов для детей младшего возраста. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ получения средства, обладающего противовирусной активностью, на основе комплекса римантадина и альгината натрия, отличающийся тем, что римантадин растворяют при температуре 5565 С в воде, затем в охлажденный до 15-35 С раствор вводят низкомолекулярный альгинат натрия (вязкость 1% раствора в воде 9-26 мПас) при условии, что массовое соотношение римантадин-альгинат натрия составляет (0,56-0,64):1, оставляют набухать в течение 5-10 ч, а затем диспергируют при температуре 15-35 С в течение 30-60 мин высокоскоростной мешалкой до образования стабильного коллоидного раствора солевого комплекса с последующим введением его при температуре 60-80 С в раствор сахара,окрашенный с помощью пищевого красителя.-4 007919 2. Способ получения средства по п.1, отличающийся тем, что концентрация окрашенного раствора сахара, в который вводят солевой комплекс римантадин-альгинат натрия, составляет 85-95 об.%. 3. Средство, обладающее противовирусной активностью, на основе комплекса римантадина и альгината натрия, отличающееся тем, что оно получено способом по п.1 и содержит исходные компоненты в 100 мл препарата в следующем соотношении: Римантадин 0,18-0,22 г Альгинат натрия 0,30-0,34 г Сахар (сахароза в виде кристаллов) 76,9-78,5 г Краситель 0,0012-0,0014 г Вода Остальное
МПК / Метки
МПК: A61K 36/02, A61K 31/13, A61K 31/734, A61K 31/12
Метки: противовирусной, способ, средство, обладающее, получения, активностью
Код ссылки
<a href="https://eas.patents.su/6-7919-sredstvo-obladayushhee-protivovirusnojj-aktivnostyu-i-sposob-ego-polucheniya.html" rel="bookmark" title="База патентов Евразийского Союза">Средство, обладающее противовирусной активностью, и способ его получения</a>
Предыдущий патент: Пептидные производные – ингибиторы слияния при вич-инфекции
Следующий патент: Дипиридодиазепиноны в качестве ингибиторов обратной транскриптазы
Случайный патент: Способ эксплуатации транспортного средства