Способ получения ( е )-5-(2-бромвинил )-2′-дезоксиуридина
Номер патента: 6156
Опубликовано: 27.10.2005
Авторы: Туроцци Дамиано, Салимбени Альдо, Мандзини Стефано, Магги Карло Альберто
Формула / Реферат
1. Способ получения (E)-5-(2-бромвинил)-2'-b-дезоксиуридина формулы
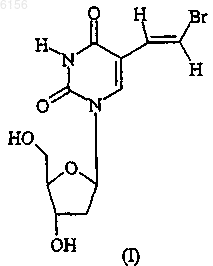
включающий
а) реакцию взаимодействия соединения формулы II
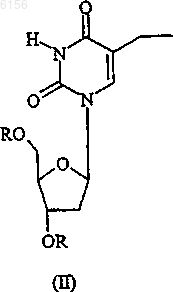
где R представляет собой алканоильную C1-C8 группу, бензоильную группу или бензоильную группу, замещенную в параположении C1-C4 алкильной группой или атомом галогена, с бромирующим агентом в присутствии радикального инициатора, в растворителе, свободном от галогенов, выбранном из сложного алкильного эфира или циклического простого эфира;
б) дегидробромирование полученного соединения формулы (III)
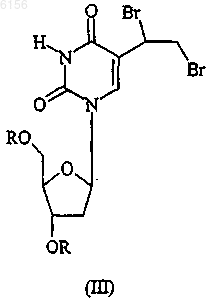
где R имеет вышеуказанное значение, с основаниями или без оснований, в растворителе, свободном от галогенов, с получением промежуточного соединения формулы (IV)
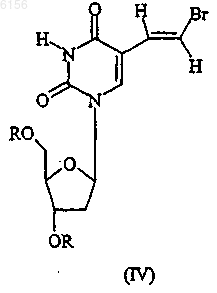
где R имеет вышеуказанное значение;
в) снятие защиты с промежуточного соединения формулы (IV).
2. Способ по п.1, при котором реакцию бромирования на стадии (а) осуществляют в растворителе, свободном от галогенов, выбранном из группы, состоящей из метила, этила, н-пропила, изопропила, н-бутила, изобутилацетата, 1,4-диоксана.
3. Способ по п.1 или 2, который включает реакцию соединения формулы II, где R представляет собой группу 4-ClC6H4CO.
4. Способ по п.1 или 2, в котором реакцию осуществляют с молекулярным бромом в присутствии радикального инициатора.
5. Способ по п.1 или 2, в котором реакцию осуществляют с N-бромсукцинимидом в присутствии радикального инициатора.
6. Способ по п.1 или 2, в котором реакцию осуществляют с N-бромсукцинимидом в присутствии 2,2'-азобисизобутиронитрила (AIBN) в этилацетате при температуре кипения растворителя.
7. Способ по п.1 или 2, в котором реакцию осуществляют с N-бромсукцинимидом в присутствии AIBN в 1,4-диоксане при температуре в интервале от 70 до 90шC.
8. Способ по любому из пп.1-7, при котором дегидробромирование на стадии (б) осуществляют в этилацетате, либо N,N-диметилформамиде, либо N,N-диметилацетамиде.
Текст
006156 В настоящем изобретении описан способ получения (Е)-5-(2-бромвинил)-2'-дезоксиуридина (Бривудина), при котором свободные от галогена растворители используют в самом способе, и в частности на первой стадии бромирования 5-этил-2'-дезоксиуридина диацилата. Область техники(Е)-5-(2-бромвинил)-2'-дезоксиуридин (Бривудин) формулы I представляет собой соединение, обладающее сильной противовирусной активностью, особенно полезное для лечения инфекций вируса опоясывающего герпеса. Первый способ синтеза описан в DE 2915254 и включает алкилирование (Е)-5-(2 бромвинил)урацила 1-хлор-2-дезокси-3,5-ди-O-п-толилD-эритропентафуранозой и последующее деацилирование с получением соединения формулы I. Недостатком этого способа является то, что синтез (Е)-5-(2-бромвинил)урацила является трудным и дает низкие выходы. Более того, соединение формулы I, полученное таким способом, не является чистым, а представляет собой смесь альфа и бета изомеров. Только последний из них обладает практической ценностью и необходимостью быть выделенным путем хроматографического разделения. Альтернативный способ описан в GB 2125399 (соответствует DE 3328238) и включает бромирование соединений формулы II где R представляет собой алканоильную С 1-С 8 группу, бензоильную группу или бензоильную группу,замещенную в пара-положении С 1-С 4 алкильной группой или атомом галогена бромом в галогенированном углеводородном растворителе, таком как 1,2-дихлорэтан, метиленхлорид, хлороформ, тетрахлорид углерода, в присутствии света, с получением дибромпроизводного формулы III, где R определен как выше. Указанное соединение III затем дегидробромируют в галогенированном углеводородном растворителе, в присутствии третичного основания, с получением нуклеозида формулы IV, где R имеет те же самые значения, указанные для соединений формулы II, с выходом 62-69%, после удаления защитных групп (Е)-5-(2-бромвинил)-2'-дезоксиуридин формулы I получают с выходом примерно 93%. В течение последних лет бромхлорметан стал в промышленной практике выбранным растворителем в радикальных реакциях, стимулируемых термическими инициаторами, вследствие его относительно высокой точки кипения (68 С) и его более низкой токсичности по сравнению с другими галогенированными растворителями, такими как, например хлороформ, тетрахлорид углерода, 1,2-дихлорэтан. Тем не менее, применение этого растворителя было недавно запрещено из-за риска, связанного с уменьшением озонового слоя (см. правило СЕЕ 2037/2000 европейского парламента).-1 006156 Описание изобретения В данном изобретении было обнаружено, что бривудин может быть с успехом получен путем реакции соединений формулы II и III, как определено выше, в растворителе, выбранном из сложных алкильных эфиров или простых циклических эфиров. Применение указанных растворителей, свободных от галогенов, является преимуществом по сравнению с применением галогенированных растворителей, поскольку первые имеют более низкую токсичность, удовлетворяют европейским положениям, касающимся защиты окружающей среды, и позволяет уменьшить примерно на 50% промышленные расходные затраты. Следовательно, в изобретении предложен способ, включающий а) радикальное бромирование соединений формулы II, в которой R такой, как определено выше, посредством бромирующего агента в растворителе, свободном от галогенов, выбранном из сложных алкильных эфиров и циклических простых эфиров, в присутствии радикального инициатора, с получением соединений формулы (III), в которой R имеет вышеуказанное значение; б) дегидробромирование в растворителе, свободном от галогенов, с основаниями или без оснований, с получением соединений формулы IV, в которой R имеет вышеуказанное значение; в) снятие защиты с получением соединения формулы (I). Предпочтительной R группой является пара-хлорбензоил. Бромирующий агент, который может представлять собой бром или N-бромсукцинимид, N-бромфталимид, 1,3-дибром-5,5-диметилидантоин,N-бромацетамид, N-броммалеимид, N-бромсульфонамид, используют в молярном избытке в интервале от 2 до 3 раз по сравнению с соединением II. Бром и N-бромсукцинимид являются особенно предпочтительными. Примеры растворителей, свободных от галогена, для стадии (а) включают алкилацетаты, такие как метил, этил, н-пропил, изопропил, н-бутил, изобутилацетат, либо циклический алифатический простой эфир, такой как 1,4-диоксан, предпочтительно в соотношении в интервале от 3:1 до 12:1, в сравнении с соединением II. Этилацетат и 1,4-диоксан являются особо предпочтительными. Растворителем, используемым для дегидробромирования (стадия б), является диметилформамид или диметилацетамид, либо он может быть таким же, как тот, что используется на стадии бромирования. Этилацетат и N,N-диметилформамид являются особенно предпочтительными. 2,2'-Азобисизобутиронитрил (AIBN), 2,2'-азобис(2,4-диметилвалеронитрил), 2,2'-азобис(2-метилбутиронитрил), азобисизовалеронитрил, 1,1'-азобис-(циклогексанкарбонитрил), 2,2'-азобис(2-амидинопропан)гидрохлорид, диметил-2,2'-азобисизобутиррат могут быть использованы в качестве радикальных инициаторов. Азобисизонитрилы предпочтительны, особенно AIBN. Указанные соединения используют в молярных процентах в интервале от 1 до 6% (3 и 6% дляAIBN) по отношению к соединению II. Температура реакции находится в интервале от комнатной температуры до точки кипения растворителя, а время реакции составляет от 15 мин до 4 ч. Предпочтительные условия включают реакцию с Nбромсукцинимидом в присутствии 2,2'-азобисизобутиронитрила (AIBN) в этилацетате при температуре кипения растворителя, или реакцию с N-бромсукцинимидом в присутствии AIBN в 1,4-диоксане при температуре в интервале от 70 до 90 С. Дополнительно к экономическим преимуществам, вытекающим из более низких расходных затрат,более низкой токсичности и соответствия правилам, касающимся защиты окружающей среды, как обсуждалось выше, способ по изобретению также отличается особо высокими выходами. Это особенно удивительно, поскольку из химической литературы известно, что большинство реакций радикального бромирования обычно осуществляют в галогенированных растворителях; например в уже цитированном GB 2125399 описано только применение хлорированных растворителей для синтеза бривудина в соответствии с общей информацией, доступной в данной области техники. Более того, не все растворители, свободные от галогенов, могут быть с успехом использованы в способе синтеза и только некоторые из них обеспечивают удовлетворительные результаты. Например, в способе получения бривудина, описанном в DE 2915254, бромирование (Е)-5-винилурацила происходит в безводном диметилформамиде. Тем не менее, когда диметилформамид используют в настоящем способе на стадии бромирования соединений формулы II, конверсионные выходы удивительно низкие и образуется ряд неточно идентифицируемых побочных продуктов. Еще одним растворителем, свободным от галогенов, иногда используемым в радикальном бромировании, является ацетонитрил (J.A.C.S. (Журнал Американского Химического Общества) 1969 (91) 7398-740; J.A.C.S. 1971 (93) 5846-5850; J.A.C.S. 1974 (96) 5616-5617), но этот растворитель также не дал удовлетворительных результатов в бромировании соединений формулы II. Одинаково неприемлемые результаты получены также с эфиро-подобными растворителями, такими как 1,2-диметоксиэтан или метилцеллозольв. Способ по изобретению дополнительно проиллюстрирован следующими примерами. Исходные промежуточные соединения формулы II (где R такой, как определено выше) получают известным способом, как это описано в GB 2125399.-2 006156 Пример 1. 10,0 г (18,7 ммоль) 3',5'-ди-О-пара-хлорбензоил-5-этил-2'дезоксиуридина формулы II, где R = 4 СlC6 Н 4 СО, и 175 мг (1,1 ммоль) ,'-азоизобутиронитрила (AIBN) добавляют к 60 мл этилацетата, и данную смесь кипятят с обратным холодильником. 2,05 мл (6,33 г; 39,6 ммоль) брома в 8 мл этилацетата добавляют по каплям в смесь в зависимости от потребления галогенирующего агента (можно наблюдать обесцвечивание смеси). Раствор, полученный в конце добавления, нагревают в течение дополнительных 15 мин до тех пор, пока флегма не станет бесцветной. Растворитель выпаривают при пониженном давлении. Остаток, состоящий из дибромпроизводного формулы III, где R = 4-СlС 6 Н 4 СО, дегидробромируют аналогично тому, как описано в GB 2125399, используя ДМФ в качестве растворителя. Получают 8,0 г 3',5'-ди-О-пара-хлорбензоил-(Е)-5-(2-бромвинил)-2'дезоксиуридина формулы IV,где R = 4-ClC6H4CO (выход 70%), который затем деацилируют известным способом, как, например, описано в GB 2125399. Получают 4,1 г (Е)-5-(2-бромвинил)-2'дезоксиуридина формулы I (выход 94%). Пример 2. 10,0 г (18,7 ммоль) 3',5'-ди-О-пара-хлорбензоил-5-этил-2'дезоксиуридина формулы II, где R = 4 СlС 6 Н 4 СО, и 175 мг (1,1 ммоль) ,'-азоизобутиронитрила (AIBN) добавляют к 60 мл этилацетата и кипятят с обратным холодильником. 7,85 г (44,1 ммоль) N-бромсукцинимида добавляют к смеси в соответствии со скоростью реакции(примерно 25 мин). В конце добавления смесь нагревают в течение дополнительных 15 мин, до тех пор,пока она не станет прозрачной. Остаток, состоящий из дибромпроизводного формулы III, где R = 4 СlC6 Н 4 СО, растворяют в 60 мл горячего AcOEt и 3,3 мл (23,6 ммоль) триэтиламина по каплям добавляют в раствор. Осадок фильтруют и обрабатывают 80% ЕtOН. Нерастворившийся материал, состоящий из соединения формулы IV, где R = 4-СlC6 Н 4 СО, фильтруют, промывают ЕtOН и сушат при пониженном давлении. Получают 9,4 г соединения формулы IV, где R = 4-СlC6 Н 4 СО, (выход 82%) и затем деацилируют известным способом, как например описано в GB 2125399. Получают 4,8 г соединения формулы I(выход 94%). Пример 3. Бромирование осуществляют в соответствии с примером 1 при 80 С, используя изобутилацетат в качестве растворителя. Добавление раствора брома в изобутилацетате осуществляют в течение 20 мин. В конце добавления раствор нагревают в течение дополнительных 15 мин до тех пор, пока он не станет бесцветным, после чего реакцию осуществляют, как описано в примере 2. Получают 8,6 г соединения формулы IV, где R = 4-СlC6 Н 4 СО (выход 75%), и затем деацилируют известным способом, как, например, описано в GB 2125399. Получают 4,4 г (выход 94%) соединения формулы I (выход 94%). Пример 4. Бромирование осуществляют в соответствии с примером 2 при 80 С, используя изобутилацетат в качестве растворителя. Продолжая следовать процедуре, приведенной в примере 2, получают 9,0 г соединения формулыIV, где R = 4-ClC6H4CO (выход 79%), и затем деацилируют известным способом, как, например, описано в GB 2125399. Получают 4,6 г соединения формулы I (выход 94%). Пример 5. 10,0 г (18,7 ммоль) 3',5'-ди-О-пара-хлорбензоил-5-этил-2'-дезоксиуридина формулы II, где R = 4-СlС 6 Н 4 СО,и 175 мг (1,1 ммоль) ,'-азоизобутиронитрила (AIBN) добавляют к 25 мл 1,4-диоксана. Данную смесь нагревают при 80 С и затем раствор 8,5 г (47,7 ммоль) N-бромсукцинимида в 35 мл 1,4-диоксана добавляют по каплям в соответствии со скоростью реакции (примерно 30 мин). После завершения добавления раствор нагревают в течение дополнительных 15 мин до тех пор, пока он не станет бесцветным. Реакцию продолжают, как описано в примере 1; получают 8,8 г соединения формулы IV, где R = 4-СlС 6 Н 4 СО, (выход 77%), и затем деацилируют известным способом, как, например, описано в GB 2125399. Получают 4,5 г соединения формулы I (выход 94%). Пример 6. Следуя процедуре, описанной в примере 2, и используя этилацетат в качестве растворителя и 1,1'бис(циклогексанкарбонитрил) (270 мг, 1,1 ммоль) в качестве радикального инициатора, получают 8,1 г(71%) соединения формулы IV, где R = 4-СlC6 Н 4 СО, и затем деацилируют известным способом, как например описано в GB 2125399. Получают 4,2 г соединения формулы I (выход 95%). ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ получения (Е)-5-(2-бромвинил)-2'-b-дезоксиуридина формулы включающий а) реакцию взаимодействия соединения формулы II где R представляет собой алканоильную С 1-С 8 группу, бензоильную группу или бензоильную группу, замещенную в параположении С 1-С 4 алкильной группой или атомом галогена, с бромирующим агентом в присутствии радикального инициатора, в растворителе, свободном от галогенов, выбранном из сложного алкильного эфира или циклического простого эфира; б) дегидробромирование полученного соединения формулы (III) где R имеет вышеуказанное значение, с основаниями или без оснований, в растворителе, свободном от галогенов, с получением промежуточного соединения формулы (IV) где R имеет вышеуказанное значение; в) снятие защиты с промежуточного соединения формулы (IV). 2. Способ по п.1, при котором реакцию бромирования на стадии (а) осуществляют в растворителе,свободном от галогенов, выбранном из группы, состоящей из метила, этила, н-пропила, изопропила, нбутила, изобутилацетата, 1,4-диоксана. 3. Способ по п.1 или 2, который включает реакцию соединения формулы II, где R представляет собой группу 4-ClC6H4CO. 4. Способ по п.1 или 2, в котором реакцию осуществляют с молекулярным бромом в присутствии радикального инициатора. 5. Способ по п.1 или 2, в котором реакцию осуществляют с N-бромсукцинимидом в присутствии радикального инициатора. 6. Способ по п.1 или 2, в котором реакцию осуществляют с N-бромсукцинимидом в присутствии 2,2'-азобисизобутиронитрила (AIBN) в этилацетате при температуре кипения растворителя.-4 006156 7. Способ по п.1 или 2, в котором реакцию осуществляют с N-бромсукцинимидом в присутствииAIBN в 1,4-диоксане при температуре в интервале от 70 до 90 С. 8. Способ по любому из пп.1-7, при котором дегидробромирование на стадии (б) осуществляют в этилацетате, либо N,N-диметилформамиде, либо N,N-диметилацетамиде.
МПК / Метки
МПК: C07H 19/06
Метки: получения, способ, 2'-дезоксиуридина, 5-(2-бромвинил
Код ссылки
<a href="https://eas.patents.su/6-6156-sposob-polucheniya-e-5-2-bromvinil-2-dezoksiuridina.html" rel="bookmark" title="База патентов Евразийского Союза">Способ получения ( е )-5-(2-бромвинил )-2′-дезоксиуридина</a>
Предыдущий патент: 4-,5-, 6-и 7-индольные производные, полезные при лечении заболеваний центральной нервной системы
Следующий патент: Лекарственная форма силимарина и способ ее получения
Случайный патент: Способ определения долговечности керамических изделий










