Пестицидные сернистые соединения
Номер патента: 645
Опубликовано: 29.12.1999
Авторы: Лоудер Патрик Дойл, Филлипс Дженнифер Лантц, Меннинг Девид Тридвей, Пилато Майкл Томас, Ву Тай-Те
Формула / Реферат
1. Серосодержащие производные гетероциклических соединений
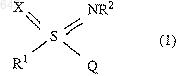
в которой =Х представляет собой группу = NR3, =О или электронную пару, R1 представляет собой алкил C1-C6, циклоалкил С3-C6 или (циклоалкил)алкил C4-C8, каждый из которых возможно замещен одним или несколькими атомами галогена,
R2 и R3 независимо выбирают из атома водорода, алкила C1-C6, галоидалкила C1-C6, COR4, S(O)pR4, циано-, нитро-, COOR4, CONR4R5, -C(O)SR4, -C(S)OR4, -SO2NR4R5, -P(O)qR4R5, -P(O)q(OR4)R5, -P(O)q(OR4)(OR5), C=(NR4)NR5R6, CH=NR4, C=(NR4)(OR5), C(S)N(R4)(R5), C(O)C(O)R4, C(O)C(O)OR4, C(O)C(O)NR4R5 и CONR4SO2R5;
p равно 0, 1 или 2,
q равно 0 или 1,
R4, R5 и R6 независимо выбирают из атома водорода, нитро-, циано-, группы CHO, R14; фенила, возможно замещенного одной или несколькими группами R14, атомом галогена, нитро-, циано-, OR14, SR14, COR14, COOR14 или OR14 атома галогена, СОR14, COOR14 группой СНО и гидроксилом,
Q представляет собой Q-1, Q-2 или Q-3, которые приведены ниже,
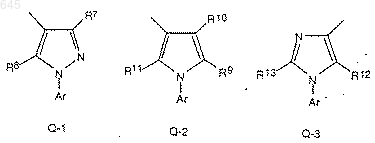
R7 представляет собой атом водорода, циано-, нитро-, алкил C1-C4, галоидалкил С1-С4, атом галогена, СНО или СОR20;
R8 является атомом водорода, атомом галогена, циано-, S(O)pR14, OR4, NR16R17, N(R16)CON(R17)(R18), N3 или NH(C1-C5)алкилом, замещенным одной или несколькими группами гидроксила, циано-, нитро-, OR14, S(O)pR14, COOR14 или CON(R16)(R17);
R9 и R11 независимо выбирают из атома водорода, атома галогена, OR14, SR14 и R14
R10 является цианогруппой,
R12 представляет собой атом водорода, атом галогена, R14, OR14, S(O)pR14 или
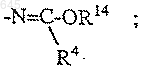
R13 представляет собой атом водорода, атом галогена или R14,
Ar представляет собой фенил, возможно содержащий один или несколько заместителей, выбранных из группы, состоящей из атома галогена, R15, OR15, SF5 и S(O)pR15; или Аr представляет собой 2-пиридил, возможно содержащий один или несколько заместителей, выбранных из группы, состоящей из атома галогена, R15, OR15, SF5 и S(О)рR14,
R14 и R19 независимо выбирают из алкила C1-C6, циклоалкила С3-С6 и (циклоалкил)алкила С4-С8, каждый из которых возможно замещен одним или несколькими атомами галогена,
R15 является алкилом C1-C6, возможно замещенным одним или несколькими атомами галогена,
R16, R17 и R18 независимо выбирают из атома водорода, нитро-, циано-, группы СНО, R19, СOR19 и COOR19,
R20 выбирают из алкилов C1-C6 возможно, замещенных одним или несколькими атомами галогена.
2. Соединение по п.1, в котором R1 является возможно галоидированным алкилом C1-C6, предпочтительно метилом или этилом.
3. Соединение по п.1, в котором R2 представляет собой атом водорода, COOR4, S(О)pR4, циано-, CONR4R5, -COR4, Р(O)qR4R5 или P(O)q(OR4)(OR5).
4. Соединение по п.3, где R2 представляет собой атом водорода, или циано, или группу СООR4, в которой R4 является алкилом С1-С6.
5. Соединение по п.4, где R2 является группой S(O)pR4, в которой р равно 2 и R4 является алкилом C1-C6 или возможно замещенным фенилом.
6. Соединение по п.4, где R2 представляет собой группу CONR4R5, в которой R4 является атомом водорода или алкилом С1-С6, a R5 является алкилом C1-C6, или в котором R4 является Н, а R5 является группой COR14, в которой R14 является возможно галоидированным алкилом C1-C6.
7. Соединение по п.4, где R2 представляет собой группу COR4, в которой R4 является атомом водорода или алкилом C1-C6, или R2 представляет собой группу Р(O)q R4R5 или Р(O)q(OR4)(OR5), в котором q =1, R4 и R5 каждый является алкилом C1-C6.
8. Соединение по п.1, в котором Q представляет собой Q-1, предпочтительно, в котором R7 является цианогруппой или атомом водорода, или алкилом С1-С4, и/или R8 - это группа NR16R17.
9. Соединение по п.8, в котором R8 является аминогруппой.
10. Соединение по п.1, в котором Аr представляет собой фенил, замещенный в положениях -2 и -6 атомом галогена, а в положении -4 галоидированным алкилом C1-C6, или группой SF5 или OR15, предпочтительно, когда Аr представляет собой 2,6-дихлор-4-трифторметилфенил, или Аr представляет собой 2-пиридил, замещенный в положении -3 атомом галогена и в положении -5 галоидированным алкилом C1-C6 или OR15, или SF5, предпочтительно, когда Аr представляет собой 3-хлор-5-трифторметилпирид-2-ил.
11. Соединение по п.1, которое представляет собой
S-((5-амино-3-циано-1-(2,6-дихлор-4-трифторметил)-фенил)-4-(1H-пиразолил))-S-этил-N-(трет-бутоксикарбонил)-сульфилимин,
S-((5-амино-3-циано-1-(2,6-дихлор-4-трифторметил)-фенил)-4-(1Н-пиразолил))-S-этил-N-ацетилсульфилимин,
S-((5-амино-3-циано-1-(2,6-дихлор-4-трифторметил)-фенил)-4-(1H-пиразолил))-S-этил-N-(метоксикарбонил)сульфилимин,
S-((5-амино-3-циано-1-(2,6-дихлор-4-трифторметил)-фенил)-4-(1H-пиразолил))-S-этил-N-(метилсульфонил)сульфилимин,
S-(5-амино-3-циано-1-(2,6-дихлор-4-трифторметил)-фенил)-4-(1H-пиразолил))-S-этил-N-(метилкарбамоил)сульфилимин,
S-((5-амино-3-циано-1-(2,6-дихлор-4-трифторметил)-фенил)-4-(1H-пиразолил))-S-этил-N-(циано)сульфилимин,
S-((5-амино-3-циано-1-(2,6-дихлор-4-трифторметил)-фенил)-4-(1H-пиразолил))-S-этил-N-(формил)сульфилимин,
S-((5-амино-3-циано-1-(2,6-дихлор-4-трифторметил)-фенил)-4-(1H-пиразолил))-S-метил-N-ацетилсульфилимин,
S-((5-амино-3-циано-1-(2,6-дихлор-4-трифторметил)-фенил)-4-(1H-пиразолил))-S-этил-N-(диэтилфосфорил)сульфилимин,
S-((5-амино-3-циано-1-(2,6-дихлор-4-трифторметил)-фенил)-4-(1H-пиразолил))-S-этил-N-(диметилкарбамоил)сульфилимин,
S-((5-амино-3-циано-1-(2,6-дихлор-4-трифторметил)-фенил)-4-(1H-пиразолил))-S-этил-N-(диметилфосфинил)сульфилимин,
S-((5-амино-3-циано-1-(2,6-дихлор-4-трифторметил)-фенил)-4-(1H-пиразолил))-S-этил-N-((трихлорацетиламино)-карбонил)-сульфилимин,
S-((5-амино-3-циано-1-(2,6-дихлор-4-трифторметил)-фенил)-4-(1H-пиразолил))-S-этил-N-((хлорацетиламино)карбонил)сульфилимин,
S-((5-амино-3-циано-1-(2,6-дихлор-4-трифторметил)-фенил)-4-(1H-пиразолил))-S-этил-N-(метилтиокарбамоил)сульфилимин,
S-((5-амино-3-циано-1-(2,6-дихлор-4-трифторметил)-фенил)-4-(1H-пиразолил))-S-этил-N-((этоксикарбонилметил)-аминокарбонил)сульфилимин,
S-((5-амино-3-циано-1-(2,6-дихлор-4-трифторметил)-фенил)-4-(1H-пиразолил))-S-метил-N-(метилтиокарбамоил)сульфилимин,
S-((5-амино-3-циано-1-(2,6-дихлор-4-трифторметил)-фенил)-4-(1H-пиразолил))-S-этил-N-(этоксикарбониламинокарбонил)сульфилимин,
S-((5-амино-3-циано-1-(2,6-дихлор-4-трифторметил)-фенил)-4-(1H-пиразолил))-S-метил-N-(формил)сульфилимин,
S-((5-амино-3-циано-1-(2,6-дихлор-4-трифторметил)-фенил)-4-(1H-пиразолил))-S-метил-N-(циано)сульфилимин,
S-((5-амино-3-циано-1-(2,6-дихлор-4-трифторметил)-фенил)-4-(1H-пиразолил))-S-метил-N-(1,2-диоксопропил)сульфилимин,
S-((5-амино-3-циано-1-(2,6-дихлор-4-трифторметил)-фенил)-4-(1H-пиразолил))-S-метил-N-(трет-бутоксикарбонил)-сульфилимин,
S-((5-амино-1-(2,6-дихлор-4-трифторметил)фенил)-4-(1H-пиразолил))-S-метил-N-(формил)сульфилимин,
S-((5-амино-1-(2,6-дихлор-4-трифторметил)фенил)-4-(1Н-пиразолил))-S-метил-N-(ацетил)сульфилимин,
S-((5-амино-1-(2,6-дихлор-4-трифторметил)фенил)-4-(1H-пиразолил))-3-метил-N-(циано)сульфилимин,
S-((5-амино-1-(2,6-дихлор-4-трифторметил)фенил-3-метил)-4-(1H-пиразолил))-S-этил-N-(формил)сульфилимин,
S-((5-амино-1-(2,6-дихлор-4-трифторметил)фенил-3-метил)-4-(1H-пиразолил))-3-этил-N-(циано)сульфилимин,
S-((5-амино-1-(2,6-дихлор-4-трифторметил)фенил-3-этил)-4-(1H-пиразолил))-S-этил-N-(формил)сульфилимин,
S-((5-амино-1-(2,6-дихлор-4-трифторметил)фенил-3-этил)-4-(1H-пиразолил))-S-этил-N-(циано)сульфилимин,
N-(трет-бутоксикарбонил)-S-4-(5-амино-3-циано-1-(2,6-дихлор-4-трифторметил)фенилпиразолил)-S-этилсульфоксимин,
N-ацетил-S-4-(5-амино-3-циано-1-(2,6-дихлор-4-трифторметил)фенилпиразолил))-S-этилсульфоксимин,
S-4-(5-амино-3-циано-1-(2,6-дихлор-4-трифторметил)-фенилпиразолил)-S-этил-сульфоксимин,
S-(5-амино-3-циано-1-(2,6-дихлор-4-трифторметил)фенил)-4-(1H-пиразолил))-S-метил-N-((4-метилфенил)сульфонилсульфимин,
S-4-(5-амино-3-циано-1-(2-(З-хлор-5-трифторметил)пиридил)пиразолил)-S-этилсульфоксид.
12. Серосодержащие производные гетероциклических соединений формулы (II)

R1 представляет собой алкил С1-C6, циклоалкил С3-C6 или (циклоалкил)алкил C4-C8, каждый из которых возможно замещен одним или несколькими атомами галогена,
m равно 1 или 2,
Q представляет собой Q-1, Q-2 или Q-3, которые приведены ниже,
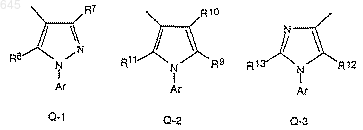
R7 представляет собой атом водорода, циано-, нитро-, алкил С1-С4, галоидалкил С1-С4, атом галогена, СНО или COR20,
R8 является атомом водорода, атомом галогена, циано-, S(O)pR14, OR4, NR16R17, N(R16)CON(R17)(R18), N3 или NH(C1-C5)алкилом, замещенным одной или несколькими группами гидроксила, циано-, нитро-, OR14, S(O)pR14, COOR14 или CON(R16)(R17);
R9 и R11 независимо выбирают из атома водорода, атома галогена, OR14, SR14 и R14;
R10 является цианогруппой,
R12 представляет собой атом водорода, атом галогена, R14, OR14, S(O)pR14 или
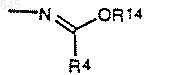
R13 представляет собой атом водорода, атом галогена или R14,
Аr представляет собой фенил, возможно содержащий один или несколько заместителей, выбранных из группы, состоящей из атома галогена, R15, OR15, SFs и S(O)pR15; или Аr представляет собой 2-пиридил, необязательно содержащий один или несколько заместителей, выбранных из группы, состоящей из атома галогена, R15, OR15, SF5 и S(O)pR14;
R14 и R19 независимо выбирают из алкила C1-C6, циклоалкила C1-C6 и (циклоалкил)алкила С4-С8, каждый из которых возможно замещен одним или несколькими атомами галогена,
R15 является алкилом C1-C6, возможно замещенным одним или несколькими атомами галогена,
R16, R17 и R18 независимо выбирают из атома водорода, нитро-, циано-, группы СНО, R19, COR19 или COOR19,
R20 выбирают из алкилов C1-C6, возможно замещенных одним или несколькими атомами галогена, и
Z является анионным противоионом, таким как ион хлора, брома, иода, фтора, -OSO2R4, -OCOR4, BF4-, SbF6-, перхлората, сульфита или гидросульфата, анион фосфата или гидрофосфата или другой сельскохозяйственно приемлемый анион.
13. Соединение по п.12, в котором R1 является возможно галоидированным алкилом C1-C6, предпочтительно метилом или этилом.
14. Соединение по п.12, в котором Q представляет собой Q-1, предпочтительно, в котором R7 является цианогруппой или атомом водорода, или алкилом С1-С4, и/или R8 - это группа NR16R17.
15. Соединение по п.14, в котором R8 является аминогруппой.
16. Соединение по п.1, в котором Аr представляет собой фенил, замещенный в положениях -2 и -6 атомом галогена, а в положении -4 галоидированным алкилом C1-C6, или группой SF5 или OR15, предпочтительно, когда Аr представляет собой 2,6-дихлор-4-трифторметилфенил, или Аr представляет собой 2-пиридил, замещенный в положении -3 атомом галогена и в положении -5 галоидированным алкилом C1-C6 или OR15, или SF5, предпочтительно, когда Аr представляет собой 3-хлор-5-трифторметилпирид-2-ил.
17. Соединение по п.12 которое представляет собой
соединение 2,4,6-триметилбензолсульфокислоты с S-4-(5-амино-3-циано-1-(2,6-дихлор-4-трифторметил)фенил)пиразолил-S-этилсульфилимином,
соединение 2,4,6-триметилбензолсульфокислоты с S-4-(5-амино-3-циано-1-(2,6-дихлор-4-трифторметил)фенил)пиразолил-S-метилсульфилимином,
соединение 2,4,6-триметилбензолсульфокислоты с S-4-(5-амино-1-(2,6-дихлор-4-трифторметил)фенил)пиразолил-S-метилсульфилимином,
соединение 2,4,6-триметилбензолсульфокислоты с S-4-(5-амино-1-(2,6-дихлор-4-трифторметил)фенил-3-метил)пиразолил-3-этилсульфилимином,
соединение 2,4,6-триметилбензолсульфокислоты с S-4-(5-амино-1-(2,6-дихлор-4-трифторметил)фенил-3-этил)пиразолил-S-этилсульфилимином,
18. Пестицидная композиция, содержащая пестицидно эффективное количество вещества в соответствии с любым одним из пп.1-8 и сельскохозяйственно приемлемый инертный носитель.
19. Способ борьбы с членистоногими, нематодами, гельминтами или простейшими вредителями на местности, отличающийся тем, что он включает внесение на указанной местности пестицидно эффективного количества вещества в соответствии с любым одним из пп.1-9.
Текст
1 Настоящее изобретение относится к новым сернистым соединениям, включая их сульфилиминовые и сульфоксиминовые промежуточные соединения и к способам получения таких соединений. Кроме того, это изобретение относится к композициям упомянутых соединений и к способам использования этих соединений для борьбы с членистоногими, нематодными, гельминтными или простейшими вредителями. В частности изобретение относится к применению соединений или их композиций в сельском хозяйстве, в особенности в качестве пестицидов. В настоящем описании термин сульфилимин используется для веществ, содержащих группу S=N-. В настоящем описании термин сульфоксимин используется для веществ, содержащих группу S(О)=N-. Были описаны различные пестицидные пиразолы, пирролы и имидазолы. В патентных публикациях: Европатент 418016, Европатент 403309, патент США 5104994, Европатент 352944, патент США 5079370, патент США 5047550, патент США 5232940, патент США 4810720, патент США 4804675,патент США 5306694, патент США 4614533, публикации WPO93/06089 и публикации WPO94/21606 описаны пестицидные (4-пиразолил)сульфиды, сульфоксиды и сульфоны. В патенте США 5187185 описаны(4-пирролил)сульфиды, сульфоксиды и сульфоны. В патенте США 5223525 описаны пестицидные 4-имидазолилсульфиды, сульфоксиды и сульфоны. В связи с большим разнообразием существующих вредителей и культур, а также условий воздействия вредителей на культуры, существует дополнительная потребность в новых пестицидных соединениях. В одном аспекте настоящее изобретение предоставляет вещества, которые используются для подавления членистоногих, нематодных,гельминтных или простейших вредителей, причем эти вещества имеют общую формулу: в которой =Х представляет собой группу =NR3,=O или электронную пару, в этом случае в формуле (1) группа =Х отсутствует,R1 представляет собой алкил C1-C6, циклоалкил С 3-С 6 или (циклоалкил)-алкил С 4-С 8, каждый из которых необязательно замещен одним или несколькими атомами галогена;R2 и R3 независимо выбирают из атома водорода, алкила C1-С 6, галоидалкила C1-С 6, 000645R4, R5 и R6 независимо выбирают из атома водорода, нитро-, циано-, группы -СНО, R14; фенила, необязательно замещенного одной или несколькими группами R14, атомом галогена,нитро-, циано-, -OR14, -SR14, -COR14, -COOR14 или -OR14; атома галогена, -COR14, -COOR14,группой -СНО и гидроксилом;R7 представляет собой атом водорода, циано-, нитро-, алкил С 1-С 4, галоидалкил C1-C4,атом галогена, -СНО или -COR20;R8 является атомом водорода, атомом галогена, циано-, -S(O)pR14, -OR4, -NR16R17,-N(R16)CON(R17)(R18), -N3 или -NH(C1-C5) алкилом, замещенным одной или несколькими группами гидроксила, циано-, нитро-, -OR14,-S(O)pR14, -COOR14 или -CON(R16) (R17);R9 и R11 независимо выбирают из атома водорода, атома галогена, -OR14, -SR14 и R14;R12 представляет собой атом водорода,атом галогена, R14, -OR14, -S(O)pR14 илиR13 представляет собой атом водорода,атом галогена или R14; Аr представляет собой фенил, необязательно содержащий один или несколько заместителей, выбранных из группы, состоящей из атома галогена, R15, -OR15, -SF5 и -S(O)pR15; или Аr представляет собой 2-пиридил, необязательно содержащий один или несколько заместителей, выбранных из группы, состоящей из атома галогена, R15, -OR15, -SF5 и -S(O)pR14;R14 и R19 независимо выбирают из алкила С 1-С 6, циклоалкила С 3-С 6 и (циклоалкил)алкилаC4-C8, каждый из которых необязательно замещен одним или несколькими атомами галогена;R15 является алкилом C1-C6, необязательно замещенным одним или несколькими атомами галогена;R16, R17 и R18 независимо выбирают из атома водорода, нитро-, циано-, группы -СНО,R19 -COR19 и -COOR19;R20 выбирают из алкилов C1-C6, необязательно замещенных одним или несколькими атомами галогена; иZ является анионным противоионом, таким как ион хлора, брома, иода, фтора, OSO2R4-,ClO4-, OCOR4-, BF4-, SbF6-, перхлората, сульфита или гидросульфата, анион фосфата, или гидрофосфата, или другой сельскохозяйственно приемлемый анион. В это изобретение также входят стереоизомеры, например диастереоизомеры и оптические изомеры, имеющие формулы (1) или (2). Предпочтительные вещества настоящего изобретения имеют один или несколько следующих признаков: 1) R1 является необязательно галоидированным алкилом С 1-С 6, предпочтительно метилом или этилом, и/или 2) R2 представляет собой атом водорода,-COOR4 -S(O)pR4 -CONR4R5, циано-, -COR4 P(O)qR4R5, или P(O)q(OR4)(OR5); более предпочтительно, R2 представляет собой атом водорода,или циано-, или группу -COOR4 (в которой R4 является алкилом C1-С 6) ; или R2 является группой -S(O)pR4 (в которой р равно 2 и R4 является алкилом C1-C6 или необязательно замещенным фенилом); или R2 представляет собой группуCONR4R5 (в которой R4 является атомом водорода или алкилом C1-С 6, а R5 является алкиломR14 является необязательно галоидированным алкилом C1-C6); или R2 представляет собой группу -COR4 (в которой R4 является атомом водорода или алкилом C1-С 6); или R2 представляет собой группу-Р(О)qR4R5 или 4 5 Р(О)q(OR )(OR ) (в которой q равно 1, а R4 и R5 каждый является алкилом C1-С 6) и/или 3) Q представляет собой Q-1, предпочтительно, в котором R7 является цианогруппой,или атомом водорода, или алкилом C1-C4, и/или когда R8 - это группа NR16R17, наиболее предпочтительно, когда R8 является аминогруппой и/или 4) Аr представляет собой фенил, замещенный в положениях -2 и -6 атомом галогена, а в положении -4 галоидированным алкилом C1-C6,или группой -SF5 или -OR15 , предпочтительно,когда Аr представляет собой 2,6-дихлор-4 трифторметилфенил; или Аr представляет собой 2-пиридил, замещенный в положении -3 атомом галогена и в положении -5 галоидированным алкилом C1-C6 или -OR15, или -SF5, предпочтительно, когда Аr представляет собой 3-хлор-5 трифторметилпирид-2-ил. В другом аспекте настоящее изобретение предоставляет пестицидную композицию (то есть, композицию против членистоногих, нематодных, гельминтных или простейших), содержащую пестицидно эффективное количество (то есть, количество, эффективное для подавления членистоногих, нематодных, гельминтных или 4 простейших вредителей) вещества формулы (1) или формулы (2) и сельскохозяйственно приемлемый инертный носитель. Выражение "вещество формулы (1) или (2)", используемое здесь и во всей этой заявке, включает в себя различные стереоизомерные формы веществ формулы (1) или (2), и их соли. В еще одном аспекте изобретение предоставляет способ борьбы с членистоногими, нематодами, гельминтами или простейшими вредителями в местах их распространения; этот способ включает внесение на указанной местности пестицидно эффективного количества (то есть,количество, эффективное для подавления членистоногих, нематодных, гельминтных или простейших вредителей) вещества формулы (1) или(2), или указанной выше пестицидной композиции. Вещества формулы (1), в которой Х является атомом кислорода и R2 не является атомом водорода, получают из веществ формулы (1), в которой Х является электронной парой и R2 не является атомом водорода (такие вещества также представляют собой часть изобретения) посредством окисления атома серы в сульфоксиминовую группу в соответствии с любым способом, по-существу, известным специалистам в этой области техники. Такие превращения могут быть осуществлены с помощью различных окисляющих агентов, включающих (но не ограниченных) перманганат калия, периодат калия и тетроксид рутения. Это превращение может происходить в обычных растворителях, таких как вода, простые эфиры, например диоксан,нитрилы, например ацетонитрил, или галоидуглеводороды, такие как дихлорметан, хлороформ, четыреххлористый углерод и тому подобные, при температурах примерно между -100 и 100 С, предпочтительно примерно между 0 и 50 С. Такое химическое превращение может быть подобным описанному в журнале Tetrahedron, 1975, т. 31, с. 505. Вещества формулы (1), в которой Х является электронной парой и R2 отличается от атома водорода, могут быть получены из веществ формулы (2) путем взаимодействия подходящего электрофильного соединения R2-L в присутствии основания. Радикал R2 имеет указанное выше значение, за исключением того, что он не является атомом водорода, и L является отщепляемой группой. Примерами отщепляемой группы L являются галогенидная, ацетатная,фенилсульфонатная, алкилсульфонатная и феноксигруппы. Примерами оснований, которые могут применяться в этой реакции, являются гидрид натрия, триэтиламин и трет-бутоксид калия. Такие превращения могут происходить во множестве обычных растворителей, таких как(но не ограниченных ими) простые эфиры, такие как тетрагидрофуран или диоксан; вода,галоидуглеводороды, такие как дихлорметан 5 или хлороформ, нитрилы, такие как ацетонитрил, и тому подобные. Такие реакции могут протекать при температурах примерно между-100 и 100 С, но предпочтительно примерно между 0 С и температурой кипения растворителя. Вещества формулы (1), в которой Х является электронной парой и R2 является атомом водорода, могут быть получены из соответствующих веществ формулы (1), в которой R2 представляет собой эфирную группу -COOR14, путем традиционного гидролиза. Вещества формулы (2) могут быть получены из веществ формулы (3) путем аминирования в соответствии с реакцией, по-существу,известной специалистам в этой области техники. Такое химическое превращение может происходить при смешивании сульфида формулы (3) с аминирующим реагентом, таким как (но не ограниченным) O-бензоилгидроксиламин,например О-(2,4,6-триметилбензоил) гидроксиламин или О-(3-хлорбензоил)гидроксиламин; Oсульфонилгидроксиламином, таким как (но не ограниченным) гидроксиламин-сульфокислота или О-(2,4,6-триизопропилбензолсульфонил) гидроксиламин; или O-фосфиновый гидроксиламин, такой как O-(дифенилфосфинил) гидроксиламин. Превращение может протекать во множестве обычных растворителей, включающих (но не ограниченных) воду, галоидированные углеводороды, такие как дихлорметан, дихлорэтан, хлороформ, и т.п.; и ароматические растворители, такие как бензол, толуол, ксилолы, и тому подобные, и реакция может протекать при температуре примерно между -100 и 100 С, предпочтительно примерно между 0 С и температурой кипения растворителя. Такое химическое превращение может быть подобным описанному в журнале Aldrichimica Acta, 1980,т. 13,1, с. 3. Вещества формулы (1), в которой Х является группой =NН и R2 представляет собой атом водорода, могут быть получены из веществ формулы (3) путем взаимодействия с хлорамином (Tetrahedron, 1970, т. 51, с. 4449). Такая реакция может протекать в аммиаке, при температуре примерно между -100 и -33 С. Вещества формулы (1), в которой =Х является группой =NR3 (в которой R3 такой, как указано выше, за исключением того, что он не является атомом водорода), и R2 представляет собой атом водорода, могут быть получены из веществ формулы (1), в которой =X является группой =NH и R2 представляет собой атом водорода, путем взаимодействия подходящего электрофильного соединения R3-L в присутствии основания. Радикал R3 имеет указанное выше значение, за исключением того, что он не является атомом водорода, и L является отщеп 000645 6 ляемой группой. Примерами отщепляемой группы L являются галогенидная, ацетатная,фенилсульфонатная, алкилсульфонатная и феноксигруппы. Примерами оснований, которые могут применяться в этой реакции, являются гидрид натрия, триэтиламин и трет-бутоксид калия. Такие превращения могут происходить во множестве обычных растворителей, таких как(но не ограниченных ими) простые эфиры, такие как тетрагидрофуран или диоксан; вода,галоидуглеводороды, такие как дихлорметан или хлороформ; нитрилы, такие как ацетонитрил, и тому подобные. Такие реакции могут протекать при температурах примерно между-100 и 100 С, но предпочтительно примерно между 0 С и температурой кипения растворителя. Аналогичные реакции описаны в журналеChem. Ber., 1984, т. 117, с. 2779. Вещества формулы (1), в которой =Х является группой =NR3, в которой R2 и R3 являются одинаковыми и не являются атомами водорода,могут быть получены из веществ формулы (1), в которой =Х является группой =NH и R2 представляет собой атом водорода, путем взаимодействия по меньшей мере двух эквивалентов подходящего электрофильного соединения R3-L,в присутствии основания. Радикал R3 имеет указанное выше значение, за исключением того,что он не является атомом водорода, и L является отщепляемой группой. Примерами отщепляемой группы L являются галогенидная, ацетатная, фенилсульфонатная, алкилсульфонатная и феноксигруппы. Примерами оснований, которые могут применяться в этой реакции, являются гидрид натрия,триэтиламин и трет-бутоксид калия. Такие превращения могут происходить во множестве обычных растворителей, таких как(но не ограниченных ими) простые эфиры, такие как тетрагидрофуран или диоксан; вода,галоидуглеводороды, такие как дихлорметан или хлороформ; нитрилы, такие как ацетонитрил, и тому подобные. Такие реакции могут протекать при температурах примерно между 100 и 100 С, но предпочтительно примерно между 0 С и температурой кипения растворителя. Аналогичные реакции описаны в журнале Lieb.Ann. Chem., 1972, т. 759, с. 107. Вещества формулы (3) известны из уровня техники. Например те вещества, в которых Q это Q-1, описаны в публикациях Европатента 418016, Европатента 403309, патента США 5104994, Европатента 352944, патента США 5079370, патента США 5047550,патента США 5232940, патента США 4810720, патента США 4804675, патента США 5306694, патента США 4614533,публикации WPO93/06089 и публикации 7 5187185. Вещества формулы (3), в которых Q это Q-3, описаны в патенте США 5223525. Во многих описанных выше превращениях является очевидным, что выбранные заместители иногда могут мешать рассмотренным реакциям. Такие нежелательные эффекты могут быть исключены за счет использования соответствующих защитных групп, чтобы предотвратить нежелательные побочные реакции. Кроме того, возможно использование реагентов, которые не влияют на функциональные группы, отличающиеся от тех, которые желательно изменить. Конкретный выбор подходящих защитных групп и реагентов будет вполне ясен специалистам в этой области техники. Предполагается использование реферативного журнала ChemicalAbstracts, что рассматривается как часть знаний специалиста в этой области техники. Для того чтобы дополнительно проиллюстрировать настоящее изобретение и его преимущества, приведены следующие ниже конкретные примеры. Следует понимать, что эти примеры приведены только с целью иллюстрации, и никоим образом не ограничивают объем изобретения. Пример 1. Соединение 2,4,6-триметилбензолсульфокислоты с S-4-[5-амино-3-циано-1-(2,6-дихлор 4-трифторметил)фенил)пиразолил-5-этилсульфилимином. Этиловый эфир-O-мезитиленсульфонилацетогидроксамовой кислоты (10 г, 35 ммоль) растворяют в 10 мл диоксана и охлаждают до 0 С. Добавляют 70%-ную перхлорную кислоту(3,3 мл, 38 ммоль), и смесь перемешивают в течение 10 мин. Добавляют 200 мл воды и отфильтровывают оставшееся твердое вещество; промывают его водой, затем растворяют в 50 мл хлористого метилена и выделяют из водной фазы. 5-Амино-3-циано-1-(2,6-дихлор-4-трифторметил)фенил-4-этилтиопиразол (10,7 г, 28 ммоль) растворяют в 50 мл хлористого метилена и охлаждают до 0 С. Добавляют полученный выше раствор. После перемешивания в течение 1 ч при 0 С и затем при комнатной температуре,хлористый метилен удаляют и добавляют 200 мл диэтилового эфира. Образовавшееся твердое вещество отфильтровывают, получая указанное в заголовке соединение в виде белого твердого вещества (12,45 г, 75%), температура плавления(Т.пл.) около 193 С. Аналогичным образом были получены следующие вещества: соединение 2,4,6-триметилбензолсульфокислоты с S-4-(5-амино-3-циано-1-(2,6-дихлор 4-трифторметил)фенил)пиразолил-3-метилсульфилимином, Т.пл. около 180 С, в последующем известное как вещество примера 1 а; соединение 2,4,6-триметилбензолсульфокислоты с S-4-(5-амино-1-(2,6-дихлор-4-трифторметил)-фенил)пиразолил-8-метилсульфи 000645 8 лимином, Т.пл. около 187 С, в последующем известное как вещество примера 1b. Два следующих соединения также были получены указанным выше способом, но не были выделены и использованы как таковые в примере 2: соединение 2,4,6-триметилбензолсульфокислоты с S-4-(5-амино-1-(2,6-дихлор-4-трифторметил)фенил-3-метил)пиразолил-S-этилсульфилимином и соединение 2,4,6-триметилбензолсульфокислоты с S-4-(5-амино-1-(2,6-дихлор-4 трифтор-метил)фенил-3-этил)пиразолил-S-этилсульфилимином. Пример 2.S-5-Амино-3-циано-1-(2,6-дихлор-4 трифторметил)фенил)-4-(1H-пиразолил-Sэтил-N-(трет-бутоксикарбонил)сульфилимин. Продукт примера 1 (1,0 г, 1,7 ммоль) перемешивают в 10 мл хлористого метилена, охлаждают до 0 С и добавляют 1,2 мл (8,5 ммоль) триэтиламина. Добавляют 0,6 мл (2,6 ммоль) дитрет-бутилдикарбоната, и реакционную смесь перемешивают 50 мин. Смесь разбавляют диэтиловым эфиром и промывают водой (3 раза по 50 мл) и насыщенным водным раствором хлористого натрия (75 мл). Органический слой сушат, фильтруют и концентрируют. Образовавшееся масло смешивают с холодным пентаном и отфильтровывают осадок. Твердое вещество вновь объединяют с фильтратом, и растворитель удаляют: масло фильтруют через силикагель,используя в качестве элюента смесь 2:3 этилацетата и гексана. После удаления растворителя,осаждение из смеси диэтилового эфира и пентана дает указанное в заголовке соединение в виде белого твердого вещества (0,36 г, 43%), Т.пл. около 191 С. Аналогичным образом были получены следующие ниже вещества (таблица 1).(12,4 ммоль) метапериодата натрия в виде водного раствора (19 мл). Добавляют 20 мг гидрата трихлорида рутения (используют, чтобы получить тетрооксид in situ) и 25 мл ацетонитрила. Спустя 2 ч добавляют еще 1,8 г (8,2 ммоль) периодата натрия и 15 мг гидрата трихлорида рутения (образующего тетрооксид in situ), и реакционную смесь перемешивают 30 мин. Затем последовательно добавляют 100 мл воды, 100 мл диэтилового эфира и 2 мл изопропанола и перемешивают. Органическую фазу выделяют и затем промывают водой (100 мл) и насыщенным водным раствором хлористого натрия (100 мл). После высушивания над сульфатом магния смесь фильтруют, и удаляют растворитель, по 000645 10 лучая маслянистый остаток, который растирают с холодным диэтиловым эфиром и хлористым метиленом. Получают указанное в заголовке соединение в виде коричневого, смолистого твердого вещества (0,94 г, 60%). В спектре протонного магнитного резонанса, записанного в дейтерохлороформе, имеются следующие химические сдвиги: 7,81 (мультиплет, 2 Н); 5,57 (широкий синглет, 2 Н); 3,7-3,5 (мультиплет, 2 Н); 1,44 (с, 9 Н); 1,39 (триплет, 3 Н). Аналогичным образом был получен N-ацетил-S-4-(5-амино-3 циано-1-(2,6-дихлор-4-трифторметил)фенилпиразолил-S-этилсульфоксимин, Т.пл. около 217 С, в последующем известный как вещество примера 30 а. Пример 31.(0,46 ммоль) йодистого натрия и 0,06 мл (0,46 ммоль) хлортриметилсилана в 2 мл ацетонитрила, и к смеси добавляют полученный выше раствор. Спустя 25 мин смесь разбавляют диэтиловым эфиром (7 мл) и последовательно промывают водой, 10%-ной соляной кислотой и насыщенным водным раствором хлористого натрия. Органическую фазу сушат над сульфатом натрия, фильтруют и концентрируют при пониженном давлении. Остаточное масло растирают с холодным пентаном и хлористым метиленом,получая целевой продукт в виде желтого твердого вещества (46 мг), имеющего Т.пл. около 86 С. Пример 32.S-(5-Амино-3-циано-1-(2,6-дихлор-4 трифторметил)фенил)-4-(1H-пиразолил-Sметил-N-4-метилфенил)сульфонил)сульфимин. В перемешиваемый раствор 5-амино-1(2,6-дихлор-4-трифторметил)-фенил-4-метилтио-1 Н-пиразол-3-карбонитрила (990 мг, 2,7 ммоль) в 25 мл ацетонитрила добавляют 610 мг(2,7 ммоль) водного раствора натриевой соли гидрата N-хлор-п-толуолсульфонамида (Хлорамин-Т) в 5 мл воды, в течение 2-минутного интервала. Перемешивание в условиях окружающей среды продолжается примерно в течение 2 ч, и затем смесь нагревают до кипения на паровой бане в течение 1 ч. Летучие вещества удаляются при пониженном давлении, и остаток очищают хроматографически на силикагеле,элюируемом смесью 3:1 этилацетата и гексана. Получают 810 мг указанного в заголовке соединения в виде твердого вещества, имеющего Т.пл. около 197 С. Пример 33. 11 Этиловый эфир-O-мезитиленсульфонилацетогидроксамовой кислоты (470 мг, 1,64 ммоль) растворяют в 1 мл диоксана и охлаждают до 0 С. Добавляют 70%-ную перхлорную кислоту (0,5 мл, 38 ммоль), и смесь перемешивают в течение 10 мин. Добавляют воду, и отфильтровывают оставшееся твердое вещество; промывают его водой, затем растворяют в хлористом метилене и выделяют из водной фазы. 5-Амино-3-циано-1-(2-(3-хлор-5-трифторметил)пиридил-4-этилсульфинил-пиразол (0,5 г,1,37 ммоль) растворяют в 25 мл хлористого метилена и полученный раствор охлаждают до 0 С. Добавляют полученный выше раствор. Спустя 1 месяц смесь концентрируют досуха и повторно промывают до полного удаления исходного пиразола. При этом получают указанное в заголовке соединение в виде белого твердого вещества, температура плавления около 193 С. Дополнительные примеры конкретных веществ изобретения приведены ниже в таблицах 2 - 5. В тексте этих таблиц для указания неподеленной электронной пары используется обозначение " ". В таблицах 2 -5 используются следующие сокращения заместителей:
МПК / Метки
МПК: A01N 43/56, C07D 231/44
Метки: соединения, пестицидные, сернистые
Код ссылки
<a href="https://eas.patents.su/30-645-pesticidnye-sernistye-soedineniya.html" rel="bookmark" title="База патентов Евразийского Союза">Пестицидные сернистые соединения</a>
Предыдущий патент: Состав для метатезисной полимеризации
Следующий патент: Антиокислители, содержащие группы фенола и группы ароматического амина
Случайный патент: Триазолопиридины