Разветвленные производные 3-фенилпропионовой кислоты и их применение
Номер патента: 23990
Опубликовано: 31.08.2016
Авторы: Беккер-Пельстер Эва-Мария, Штолль Фридерикке, Вольтеринг Элизабет, Вундер Франк, Ли Фолькхарт Миньцзянь, Лампе Томас, Шташ Иоганнес-Петер, Хан Михаэль, Шлеммер Карл-Хайнц, Кнорр Андреас
Формула / Реферат
1. Соединение формулы (I)
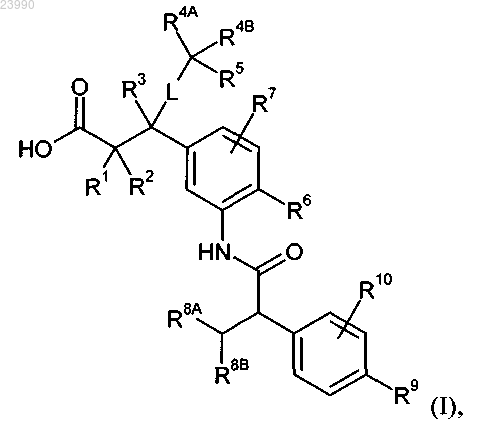
в которой R1, R2 и R3 независимо друг от друга означают водород или метил;
L означает связь или -СН2-;
R4A и R4B независимо друг от друга означают метил, трифторметил или этил, или
R4A и R4B вместе с атомом углерода, к которому они присоединены, образуют циклопропильное или циклобутильное кольцо, которое может быть замещено до двух раз фтором;
R5 означает водород, фтор, метил или метокси;
R6 означает водород, фтор, хлор, бром, циано, метил, трифторметил, этил, метокси или трифторметокси;
R7 означает водород, фтор, хлор или метил;
R8A означает метил или этил;
R8B означает трифторметил, или
R8A и R8B вместе с атомом углерода, к которому они присоединены, образуют необязательно дифторзамещенное циклопентильное кольцо формулы
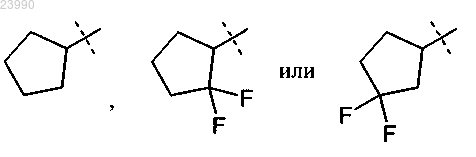
R9 означает фтор, хлор, бром, циано, (С1-С4)алкил, (С2-С4)алкенил, циклопропил или циклобутил, где
(С1-С4)алкил и (С2-С4)алкенил могут быть замещены до трех раз фтором и
циклопропил и циклобутил могут быть замещены до двух раз фтором;
R10 означает водород, фтор, хлор, метил, трифторметил, этил или метокси,
и его физиологически приемлемые соли.
2. Соединение формулы (I) по п.1, в которой
R1 означает водород или метил;
R2 означает водород;
R3 означает водород или метил;
L означает связь или -СН2-;
R4A и R4B оба означают метил или вместе с атомом углерода, к которому они присоединены, образуют циклопропильное или циклобутильное кольцо, которое может быть замещено до двух раз фтором;
R5 означает водород, фтор, метил или метокси;
R6 означает фтор, хлор, метил или этил;
R7 означает водород или фтор;
R8A означает метил;
R8B означает трифторметил, или
R8A и R8B вместе с атомом углерода, к которому они присоединены, образуют дифторзамещенное циклопентильное кольцо формулы
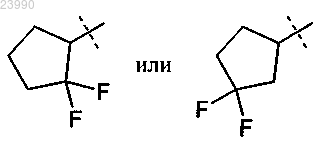
R9 означает фтор, хлор, (С1-С4)алкил, (С2-С3)алкенил, циклопропил или циклобутил, где
(С1-С4)алкил и (С2-С3)алкенил могут быть замещены до трех раз фтором и
циклопропил и циклобутил могут быть замещены до двух раз фтором;
R10 означает водород, фтор, хлор, метил или метокси,
и его физиологически приемлемые соли.
3. Соединение формулы (I) по п.1 или 2, в которой
R1 и R2 оба означают водород;
R3 означает водород или метил;
L означает связь или -СН2-;
R4A и R4B оба означают метил или вместе с атомом углерода, к которому они присоединены, образуют циклопропильное или циклобутильное кольцо, которое может быть замещено до двух раз фтором;
R5 означает водород, фтор или метил;
R6 означает хлор;
R7 означает водород;
R8A означает метил;
R8B означает трифторметил;
R9 означает фтор, хлор, метил, трифторметил, этил, 2,2,2-трифторэтил, изопропил, трет-бутил, циклопропил или 2,2-дифторциклопропил;
R10 означает водород, фтор, метил или метокси,
и его физиологически приемлемые соли.
4. Соединение следующей формулы:

и его физиологически приемлемые соли.
5. Способ получения соединения формулы (I) по любому из пп.1-4, отличающийся тем, что карбоновую кислоту формулы (II)
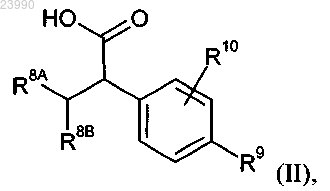
в которой R8A, R8B, R9 и R10 имеют значения, приведенные в любом из пп.1-4,
сочетают с амином формулы (III)
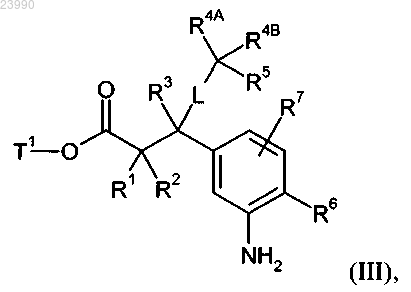
в которой L, R1, R2, R3, R4A, R4B, R5, R6 и R7 имеют значения, приведенные в пп.1-4, и Т1 означает (С1-С4)алкил или бензил,
в инертном растворителе в присутствии конденсирующего агента или через промежуточное образование соответствующего карбонилхлорида, в присутствии основания, с получением карбоксамида формулы (IV)
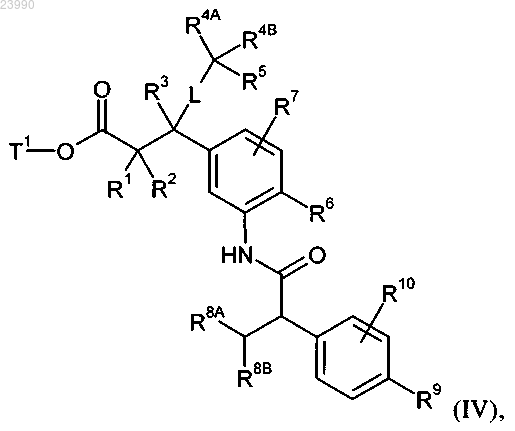
в которой L, R1, R2, R3, R4A, R4B, R5, R6, R7, R8A, R8B, R9, R10 и Т1 имеют значения, приведенные выше,
и сложноэфирный радикал Т1 затем удаляют путем основного или кислотного сольволиза или, в случае, когда Т1 означает бензил, путем гидрогенолиза с получением карбоновой кислоты формулы (I),
и соединения формулы (I) необязательно разделяют на их энантиомеры и/или диастереомеры и/или подвергают реакции с подходящими (i) растворителями и/или (ii) основаниями с получением их физиологически приемлемых солей.
6. Применение соединения по любому из пп.1-4 для лечения и/или предотвращения сердечной недостаточности, стенокардии, гипертензии, легочной гипертензии, тромбоэмболических нарушений, ишемий, сосудистых нарушений, нарушений микроциркуляции, почечной недостаточности, фиброзных нарушений и артериосклероза.
7. Применение соединения по любому из пп.1-4 для изготовления лекарственного средства для лечения и/или предотвращения сердечной недостаточности, стенокардии, гипертензии, легочной гипертензии, тромбоэмболических нарушений, ишемий, сосудистых нарушений, нарушений микроциркуляции, почечной недостаточности, фиброзных нарушений и артериосклероза.
8. Лекарственное средство для лечения и/или предотвращения сердечной недостаточности, стенокардии, гипертензии, легочной гипертензии, тромбоэмболических нарушений, ишемий, сосудистых нарушений, нарушений микроциркуляции, почечной недостаточности, фиброзных нарушений и артериосклероза, содержащее эффективное количество соединения по любому из пп.1-4 в комбинации с одним или несколькими инертными, нетоксичными, фармацевтически пригодными наполнителями.
9. Применение лекарственного средства по п.8 для лечения и/или предотвращения сердечной недостаточности, стенокардии, гипертензии, легочной гипертензии, тромбоэмболических нарушений, ишемий, сосудистых нарушений, нарушений микроциркуляции, почечной недостаточности, фиброзных нарушений и артериосклероза.
Текст
Изобретение относится к новым производным 3-фенилпропионовой кислоты, которые несут разветвленный или циклический алкильный заместитель в 3-м положении, к способам их получения, к их применению для лечения и/или предотвращения заболеваний и к их применению для изготовления лекарственных средств для лечения и/или предотвращения заболеваний, в частности для лечения и/или предотвращения сердечно-сосудистых заболеваний, а именно к соединениям формулы (I)(71)(73) Заявитель и патентовладелец: БАЙЕР ИНТЕЛЛЕКТЧУАЛ ПРОПЕРТИ ГМБХ (DE) Изобретение относится к новым производным 3-фенилпропионовой кислоты, которые несут разветвленный или циклический алкильный заместитель в 3-м положении, к способам их получения, к их применению для лечения и/или предотвращения заболеваний и к их применению для изготовления лекарственных средств для лечения и/или предотвращения заболеваний, в частности для лечения и/или предотвращения сердечно-сосудистых заболеваний. Одна из важнейших клеточных систем передачи сигналов в клетках млекопитающих представлена циклическим гуанозинмонофосфатом (цГМФ). Вместе с монооксидом азота (NO), который высвобождается из эндотелия и передает гормональные и механические сигналы, он образует NO/цГМФ систему. Гуанилатциклазы катализируют биосинтез цГМФ из гуанозинтрифосфата (ГТФ). Раскрытые до настоящего времени представители этого семейства могут быть разделены на две группы, исходя как из структурных признаков, так и типа лигандов: специфические гуанилатциклазы, которые могут стимулироваться натрийуретическими пептидами, и растворимые гуанилатциклазы, которые могут стимулироваться с помощью NO. Растворимые гуанилатциклазы состоят из двух субъединиц и вероятнее всего содержат на гетеродимер один гем, который представляет собой часть регуляторного участка. Последний имеет центральное значение в механизме активации. NO может связываться с атомом железа гема и таким образом значительно повышать активность фермента. В отличие от этого гем-свободные препараты не могут стимулироваться с помощью NO. Монооксид углерода (СО) также может присоединяться к центральному атому железа в геме, но стимуляция с помощью СО заметно слабее, чем стимуляция с помощью NO. Благодаря выработке цГМФ и вызываемой им регуляции фосфодиэстераз, ионных каналов и протеинкиназ, гуанилатциклаза играет ключевую роль в различных физиологических процессах, в частности в расслаблении и в пролиферации клеток гладкой мускулатуры, в агрегации и адгезии тромбоцитов и в нейрональной передаче сигналов, и в заболеваниях, вызванных искажением представленных выше процессов. В патофизиологических условиях NO/цГМФ система может быть угнетена, что может привести,например, к высокому кровяному давлению, активации тромбоцитов, усилению пролиферации клеток,эндотелиальной дисфункции, атеросклерозу, стенокардии, сердечной недостаточности, тромбозам, удару и инфаркту миокарда. Возможный путь лечения таких нарушений, который является независимым от NO и нацелен на влияние на цГМФ сигнальный путь в организмах, представляет собой перспективный подход, ввиду его ожидаемой высокой эффективности и незначительности побочных действий. До настоящего времени для терапевтической стимуляции растворимой гуанилатциклазы применялись исключительно соединения, такие как органические нитраты, чье действие основано на NO. NO вырабатывается путем биоконверсии и активирует растворимую гуанилатциклазу путем присоединения к центральному атому железа в геме. Наряду с побочными эффектами, развитие переносимости является одним из ключевых неудобств этого способа лечения [O.V. Evgenov и др., Nature Rev. Drug Disc. 5(2006), 755]. В последние годы были выявлены вещества, которые непосредственно стимулируют растворимую гуанилатциклазу, т.е. в отсутствие предшествующего высвобождения NO. Производное индазола YC-1 было первым описанным NO-независимым, но гем-зависимым рГЦ стимулятором [Evgenov и др., ibid.]. На основе YC-1 были выявлены дальнейшие вещества, которые являются более мощным, чем YC-1, и не показывают значимого ингибирования фосфодиэстеразы (ФДЭ). Это привело к идентификации пиразолопиридиновых производных BAY 41-2272, BAY 41-8543 и BAY 63-2521. Вместе с недавно опубликованными структурно различными веществами CMF-1571 и А-350619, эти соединения образуют новый класс рГЦ стимуляторов [Evgenov и др., ibid.]. Общей особенностью этого класса веществ является NOнезависимая и селективная активация гем-содержащей рГЦ. Кроме того, рГЦ стимуляторы в комбинации с NO обладают синергическим действием на рГЦ активацию на основе стабилизации комплекса нитрозил-гем. Точный сайт связывания рГЦ стимуляторов на рГЦ все еще обсуждается. Если из растворимой гуанилатциклазы удаляют группу гема, фермент все еще обладает обнаруживаемой каталитической базальной активностью, т.е. цГМФ все еще образуется. Остающаяся каталитическая базальная активность гем-свободного фермента не может стимулироваться с помощью какого-либо из стимуляторов, упомянутых выше [Evgenov и др., ibid.]. Кроме того, были выявлены NO- и гем-независимые активаторы рГЦ, с BAY 58-2667 в качестве прототипа этого класса. Общей характеристикой этих веществ является то, что в комбинации с NO они проявляют только аддитивное действие на активацию фермента, и что активация окисленного или гемсвободного фермента значительно выше, чем в случае гем-содержащего фермента [Evgenov и др., ibid.;J.P. Stasch и др., Br. J. Pharmacol. 136 (2002), 773; J.P. Stasch и др., J. Clin. Invest. 116 (2006), 2552]. Спектроскопические исследования показывают, что BAY 58-2667 смещает окисленную группу гема, которая,в результате ослабления связи железо-гистидин, присоединена к рГЦ очень слабо. Кроме того, было показано, что типичный, связывающий гем рГЦ мотив Tyr-x-Ser-x-Arg, является абсолютно необходимым как для взаимодействия отрицательно заряженных пропионовых кислот группы гема, так и для действияBAY 58-2667. С учетом этого, предполагается, что сайт связывания BAY 58-2667 на рГЦ является идентичным сайту связывания группы гема [J.P. Stasch и др., J. Clin. Invest. 116 (2006), 2552]. Соединения, описанные в настоящем изобретении, подобным образом способны активировать гем-1 023990 свободную форму растворимой гуанилатциклазы. Это также подтверждается фактом, что эти новые активаторы, во-первых, не обладают синергетическим действием с NO на гем-содержащий фермент и, вовторых, их действие не может быть заблокировано гем-зависимым ингибитором растворимой гуанилатциклазы, 1H-1,2,4-оксадиазоло[4,3-а]хиноксалин-1-оном (ODQ), напротив, оно даже усиливается этим ингибитором [ср. O.V. Evgenov и др., Nature Rev. Drug Disc. 5 (2006), 755; J.P. Stasch и др., J. Clin. Invest. 116 (2006), 2552]. Таким образом, целью настоящего изобретения является обеспечение новых соединений, которые действуют в качестве активаторов растворимой гуанилатциклазы описанным выше способом, и могут использоваться как таковые, в частности, для лечения и предотвращения сердечно-сосудистых нарушений.WO 00/64888-А 1, ЕР 1216980-А 1, ЕР 1285908-А 1, ЕР 1348698-А 1, ЕР 1375472-А 1, ЕР 1452521-А 1,US 2005/0187266-А 1 и US 2005/0234066-A1 описывают различные производные арилалканкарбоновых кислот в качестве агонистов PPAR для лечения диабета, дислипидемии, артериосклероза, ожирения и других нарушений. ЕР 1312601-А 1 и ЕР 1431267-А 1 раскрывают замещенные арилалканкарбоновые кислоты в качестве антагонистов рецептора PGE2 для лечения, например, болевых состояний, урологических нарушений, болезни Альцгеймера и рака. Кроме того, в WO 2005/086661-А 2 заявлены арилалканкарбоновые кислоты в качестве модуляторов GPR40 для лечения диабета и дислипидемии, aWO 2004/099170-А 2, WO 2006/050097-A1 и WO 2006/055625-A2 описывают фенилзамещенные карбоновые кислоты в качестве ингибиторов РТР-1 В для лечения диабета, рака и нейродегенеративных нарушений. Кроме того, отдельные фенилацетамидо-замещенные фенилалканкарбоновые кислоты, которые, в виде нековалентных смесей улучшают доставку активных пептидных соединений в организме, известны из WO 96/12473-A1 и WO 96/30036-A1. В WO 2009/067493-A2 заявлены производные 3,5-дизамещенной фенилуксусной кислоты для лечения болезни Альцгеймера. WO 2009/127338-A1 и WO 2010/ 102717-А 1 раскрывают производные оксогетероциклически замещенной карбоновой кислоты, которые действуют в качестве активаторов растворимой гуанилатциклазы. Настоящее изобретение обеспечивает соединения общей формулы (I) в которой R1, R2 и R3 независимо друг от друга означают водород или метил;L означает связь или -СН 2-;R4A и R4B независимо друг от друга означают метил, трифторметил или этил, илиR4A и R4B вместе с атомом углерода, к которому они присоединены, образуют циклопропильное или циклобутильное кольцо, которое может быть замещено до двух раз фтором;R8A означает метил или этил;R8A и R8B вместе с атомом углерода, к которому они присоединены, образуют необязательно дифторзамещенное циклопентильное кольцо формулы(С 1-С 4)алкил и (С 2-С 4)алкенил могут быть замещены до трех раз фтором и циклопропил и циклобутил могут быть замещены до двух раз фтором;R10 означает водород, фтор, хлор, метил, трифторметил, этил или метокси,и их физиологически приемлемые соли. Соединения в соответствии с изобретением представляют собой соединения формулы (I) и их физиологически приемлемые соли, соединения, включенные в формулу (I), описываемые формулами, упоминаемыми далее, и их физиологически приемлемые соли, и соединения, включенные в формулу (I) и описываемые далее в качестве примеров вариантов осуществления и их физиологически приемлемые соли, если только соединения, включенные в формулу (I) и описываемые далее, уже не являются солями,сольватами и сольватами солей. Также включены соли, которые сами не являются пригодными для фармацевтических применений,но могут применяться, например, для выделения, очистки или хранения соединений в соответствии с изобретением. Физиологически приемлемые соли соединений в соответствии с изобретением включают, в частности, соли обычных оснований, такие как, в качестве примера и предпочтительно, соли щелочных металлов (например, соли натрия и калия), соли щелочно-земельных металлов (например, соли кальция и магния) и соли аммония, полученные из аммиака или органических аминов, содержащих от 1 до 16 атомов С, таких как, в качестве примера и предпочтительно, этиламин, диэтиламин, триэтиламин, N,Nдиизопропилэтиламин, моноэтаноламин, диэтаноламин, триэтаноламин, диметиламиноэтанол, диэтиламиноэтанол, прокаин, дициклогексиламин, дибензиламин, N-метилпиперидин, N-метилморфолин, аргинин, лизин и 1,2-этилендиамин. Соединения в соответствии с изобретением, в зависимости от их структуры, могут существовать в различных стереоизомерных формах, т.е. в виде конфигурационных изомеров или, если уместно, также в виде конформационных изомеров (энантиомеров и/или диастереомеров, включая такие в случае атропоизомеров). Вследствие этого, настоящее изобретение охватывает энантиомеры или диастереомеры и их соответствующие смеси. Стереоизомерно однородные компоненты могут быть выделены из таких смесей энантиомеров и/или диастереомеров известным путем; для этого предпочтительно используют хроматографические способы, в частности ВЭЖХ хроматографию на ахиральной или хиральной фазе. Когда соединения в соответствии с изобретением могут встречаться в таутомерных формах, настоящее изобретение охватывает все таутомерные формы. Настоящее изобретение также охватывает все пригодные изотопные варианты соединений в соответствии с изобретением. Изотопный вариант соединения в соответствии с изобретением в данном документе понимают в значении соединения, у которого по меньшей мере один атом в рамках соединения в соответствии с изобретением заменен на другой атом того же атомного номера, но с атомной массой,иной, чем атомная масса, которая обычно или преимущественно встречается в природе. Примерами изотопов, которые могут быть включены в соединение в соответствии с изобретением, являются изотопы водорода, углерода, азота, кислорода, фосфора, серы, фтора, хлора, брома и йода, такие как 2 Н (дейтерий), 3 Н (тритий), 13 С, 14 С, 15N, 17 О, 18 О, 32 Р, 33 Р, 33S, 34S, 35S, 36S, 18F, 36Cl, 82Br, 123I, 124I, 129I и 131I. Отдельные изотопные варианты соединения в соответствии с изобретением, особенно варианты, в которые включены один или несколько радиоактивных изотопов, могут быть полезными, например, для исследования механизма действия или распространения активного соединения в организме; благодаря сравнительной легкости получения и обнаружения, для этой цели являются особенно пригодными соединения,меченные изотопами 3 Н или 14 С. Кроме того, введение изотопов, например дейтерия, может приводить к особенным терапевтическим выгодам в результате большей метаболической стабильности соединения,например, удлинению периода полураспада в организме или снижению необходимой активной дозы; такие модификации соединений в соответствии с изобретением могут вследствие этого в некоторых случаях также составлять предпочтительный вариант осуществления настоящего изобретения. Изотопные варианты соединений в соответствии с изобретением могут быть получены обычно используемыми способами, известными специалистам в данной области техники, например с помощью методов, описанных ниже, и методов, описанных в рабочих примерах, при использовании в них соответствующих изотопных модификаций отдельных реагентов и/или исходных соединений. Кроме того, настоящее изобретение также включает пролекарства соединений в соответствии с изобретением. Термин "пролекарства" в данном случае обозначает соединения, которые сами могут быть биологически активными или неактивными, но которые превращаются (например, метаболически или гидролитически) в соединения в соответствии с изобретением во время их пребывания в организме. В качестве пролекарств, настоящее изобретение, в частности, включает гидролизуемые сложноэфирные производные карбоновых кислот формулы (I) в соответствии с изобретением. Такие производные следует понимать в значении сложных эфиров, которые могут быть гидролизованы до свободных карбоновых кислот, в качестве соединений, которые преимущественно являются активными биологически, в физиологических средах, в условиях биологических исследований, описанных далее, и, в частности, in vivo ферментативными или химическими путями. (С 1-С 4)алкиловые сложные эфиры, в которых алкильные группы могут иметь нормальную или разветвленную цепь, являются предпочтительными в качестве таких сложных эфиров. Особое предпочтение отдают метиловым, этиловым или третбутиловым сложным эфирам. В рамках настоящего изобретения заместители имеют следующее значение, если не указано иное.(С 1-С 4)алкил в рамках изобретения означает алкильный радикал с нормальной или разветвленной цепью, содержащий от 1 до 4 атомов углерода. Следующие радикалы могут быть приведены в качестве примера и с целью предпочтения: метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил и трет-бутил.(С 2-С 4)алкенил и (С 2-С 3)алкенил в рамках изобретения означают алкенильный радикал с нормальной или разветвленной цепью, содержащий двойную связь и от 2 до 4 и 2 или 3 атома углерода соответственно. Алкенильный радикал с нормальной или разветвленной цепью, содержащий 2 или 3 атома углерода, является предпочтительным. Следующие радикалы могут быть приведены в качестве примера и с целью предпочтения: винил, аллил, н-проп-1-ен-1-ил, изопропенил, н-бут-1-ен-1-ил, н-бут-2-ен-1-ил, нбут-3-ен-1-ил, 2-метилпроп-1-ен-1-ил и 2-метилпроп-2-ен-1-ил. В рамках настоящего изобретения, все радикалы, которые встречаются более чем один раз, определяются независимо друг от друга. Если радикалы в соединениях в соответствии с изобретением являются замещенными, такие радикалы, если не указано иное, могут быть моно- или полизамещенными. Замещение одним, двумя или тремя одинаковыми или разными заместителями является предпочтительным. Особое предпочтение отдают замещению одним или двумя одинаковыми или разными заместителями. В рамках настоящего изобретения предпочтение отдают соединениям формулы (I), в которойR1 означает водород или метил;R3 означает водород или метил;L означает связь или -СН 2-;R4A и R4B оба означают метил или вместе с атомом углерода, к которому они присоединены, образуют циклопропильное или циклобутильное кольцо, которое может быть замещено до двух раз фтором;R7 означает водород или фтор;R8A и R8B вместе с атомом углерода, к которому они присоединены, образуют дифторзамещенное циклопентильное кольцо формулы(С 1-С 4)алкил и (С 2-С 3)алкенил могут быть замещены до трех раз фтором и циклопропил и циклобутил могут быть замещены до двух раз фтором;R10 означает водород, фтор, хлор, метил или метокси,и их физиологически приемлемым солям. Отдельный вариант осуществления настоящего изобретения включает соединения формулы (I), в которойR1 и R2 оба означают водород,и их физиологически приемлемым солям. Дополнительный отдельный вариант осуществления настоящего изобретения включает соединения формулы (I), в которойR3 означает водород или метил иL означает связь,и их физиологически приемлемые соли. Дополнительный отдельный вариант осуществления настоящего изобретения включает соединения формулы (I), в которойL означает -СН 2-,и их физиологически приемлемые соли. Дополнительный отдельный вариант осуществления настоящего изобретения включает соединения формулы (I), в которойR4A и R4B оба означают метил иR5 означает водород,и их физиологически приемлемые соли. Дополнительный отдельный вариант осуществления настоящего изобретения включает соединения формулы (I), в которойR4A и R4B вместе с атомом углерода, к которому они присоединены, образуют циклопропильное или циклобутильное кольцо, которое может быть замещено до двух раз фтором; и их физиологически приемлемые соли. Дополнительный отдельный вариант осуществления настоящего изобретения включает соединения формулы (I), в которойR7 означает водород,и их физиологически приемлемые соли. Дополнительный отдельный вариант осуществления настоящего изобретения включает соединения формулы (I), в которойR8B означает трифторметил,и их физиологически приемлемые соли. Дополнительный отдельный вариант осуществления настоящего изобретения включает соединения формулы (I), в которойR8A и R8B вместе с атомом углерода, к которому они присоединены, образуют дифторзамещенное циклопентильное кольцо формулы и их физиологически приемлемые соли. Дополнительный отдельный вариант осуществления настоящего изобретения включает соединения формулы (I), в которойR9 означает фтор, хлор, (С 1-С 4)алкил или циклопропил, где (С 1-С 4)алкил может быть замещен до трех раз фтором, и циклопропил может быть замещен до двух раз фтором,и их физиологически приемлемые соли. Дополнительный отдельный вариант осуществления настоящего изобретения включает соединения формулы (I), в которойR10 означает водород, фтор, хлор, метил или метокси,и их физиологически приемлемые соли. Особенное предпочтение в рамках настоящего изобретения отдают соединениям формулы (I), в которойR3 означает водород или метил;L означает связь или означает -СН 2-;R4A и R4B оба означают метил или вместе с атомом углерода, к которому они присоединены, образуют циклопропильное или циклобутильное кольцо, которое может быть замещено до двух раз фтором;R10 означает водород, фтор, метил или метокси,и их физиологически приемлемым солям. Особенно важными в рамках настоящего изобретения являются соединения формулы (I-A) в которой атом углерода фенилацетамидной группы, помеченный , имеет показанную Sконфигурацию и-5 023990 каждый из радикалов R3, R4A, R4B, R5, R6, R8A, R8B, R9 и R10 и L имеет значения, приведенные выше,и их физиологически приемлемые соли. Определения радикалов, указанные особым образом в соответствующих комбинациях или предпочтительных комбинациях радикалов, заменяют при желании, независимо от конкретных комбинаций, указанных для радикалов, также определениями радикалов других комбинаций. Комбинации из двух или нескольких указанных выше предпочтительных диапазонов, являются особенно предпочтительными. Кроме того, изобретение обеспечивает способ получения соединений формулы (I) в соответствии с изобретением, отличающийся тем, что карбоновую кислоту формулы (II) в которой L, R1, R2, R3, R4A, R4B, R5, R6 и R7 имеют значения, приведенные выше, и Т 1 означает (С 1-С 4)алкил или бензил,в инертном растворителе в присутствии конденсирующего агента или через промежуточное образование соответствующего карбонилхлорида, в присутствии основания, с получением карбоксамида формулы (IV) в которой L, R1, R2, R3, R4A, R4B, R5, R6, R7, R8A, R8B, R9, R10 и Т 1 имеют значения, приведенные выше,и сложноэфирный радикал Т 1 затем удаляют путем основного или кислотного сольволиза или, в случае, когда Т 1 означает бензил, путем гидрогенолиза с получением карбоновой кислоты формулы (I), и соединения формулы (I) необязательно разделяют на их энантиомеры и/или диастереомеры и/или подвергают реакции с подходящими (i) растворителями и/или (ii) основаниями с получением их физиологически приемлемых солей. Инертными растворителями для стадии способа (II) + (III)(IV) [амидное сочетание] являются,например, эфиры, такие как диэтиловый эфир, трет-бутил-метиловый эфир, тетрагидрофуран, 1,4 диоксан, диметиловый эфир гликоля или диметиловый эфир диэтиленгликоля, углеводороды, такие как бензол, толуол, ксилол, гексан, циклогексан или фракции минерального масла, галогенированные углеводороды, такие как дихлорметан, трихлорметан, четыреххлористый углерод, 1,2-дихлорэтан, трихлорэтилен или хлорбензол, или другие растворители, такие как ацетон, ацетонитрил, этилацетат, пиридин,диметилсульфоксид (ДМСО), N,N-диметилформамид (ДМФА), N,N'-диметилпропиленмочевина (DMPU) или N-метилпирролидинон (NMP). Также возможно использование смесей упомянутых растворителей. Предпочтение отдают использованию дихлорметана, тетрагидрофурана, диметилформамида или смесей этих растворителей. Пригодными конденсирующими агентами для этих реакций сочетания являются, например, карбодиимиды, такие как N,N'-диэтил-, N,N'-дипропил-, N,N'-диизопропил-, N,N'-дициклогексилкарбодиимид такие как N,N'-карбонилдиимидазол (CDI) или изобутил хлорформиат, соединения 1,2-оксазолия, такие как 3-сульфат 2-этил-5-фенил-1,2-оксазолия или перхлорат 2-трет-бутил 5-метилизоксазолия, ациламиносоединения, такие как 2-этокси-1-этоксикарбонил-1,2-дигидрохинолин, -хлоренамины, такие как 1 хлор-2-метил-1-диметиламино-1-пропен, соединения фосфора, такие как ангидрид пропанфосфоновой кислоты, диэтилцианофосфонат, бис-(2-оксо-3-оксазолидинил)фосфорил хлорид, гексафторфосфат бензотриазол-1-илокси-трис(диметиламино)фосфония или гексафторфосфат бензотриазол-1-илокситрис(пирролидино)фосфония (РуВОР), или соединения урония, такие как тетрафторборат О(бензотриазол-1-ил)-N,N,N',N'-тетраметилурония (TBTU), гексафторфосфат O-(бензотриазол-1-ил)N,N,N',N'-тетраметилурония(HATU) или тетрафторборат О-(1H-6-хлорбензотриазол-1-ил)-1,1,3,3-тетраметилурония (TCTU), если уместно, в комбинации с дополнительными вспомогательными средствами, такими как 1 гидроксибензотриазол (HOBt) или N-гидроксисукцинимид (HOSu), и, в качестве оснований, карбонатами щелочных металлов, например, карбонатом натрия или карбонатом калия, или основаниями-третичными аминами, такими как триэтиламин, N-метилморфолин, N-метилпиперидин, N,N-диизопропилэтиламин,пиридин или 4-N,N-диметиламинопиридин. Предпочтение отдают использованию гексафторфосфата O(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилурония (HATU) в комбинации с пиридином или N,Nдиизопропилэтиламином, или гидрохлорида N-(3-диметиламинопропил)-N'-этилкарбодиимида (EDC) в комбинации с 1-гидроксибензотриазолом (HOBt) и триэтиламином, или 1-хлор-2-метил-1 диметиламино-1-пропена вместе с пиридином. Реакцию (II) + (III)(IV) обычно проводят в температурном диапазоне от 0 до 60 С, предпочтительно от 10 до 40 С. Если используют карбонилхлорид, соответствующий соединению (II), сочетание с аминным компонентом (III) проводят в присутствии обычного органического вспомогательного основания, такого как триэтиламин, N-метилморфолин, N-метилпиперидин, N,N-диизопропилэтиламин, пиридин, 4-N,Nдиметиламинопиридин, 1,8-диазабицикло[5.4.0]ундец-7-ен (DBU) или 1,5-диазабицикло[4.3.0]нон-5-ен(DBN). Предпочтение отдают использованию триэтиламина или N,N-диизопропилэтиламина. Реакцию амина (III) с карбонилхлоридом обычно проводят в температурном диапазоне от -20 до 60 С, предпочтительно в диапазоне от -10 до 30 С. В свою очередь, получение карбонилхлоридов проводят обычным образом путем обработки карбоновой кислоты (II) тионилхлоридом или оксалилхлоридом. Удаление сложноэфирной группы Т 1 на стадии способа (IV)(I) проводят обычными методами путем обработки сложного эфира в инертных растворителях кислотами или основаниями, причем в последнем варианте первоначально образовавшуюся соль превращают путем обработки кислотой в свободную карбоновую кислоту. В случае трет-бутиловых эфиров, расщепление сложного эфира предпочтительно проводят с использованием кислот. Сложные бензиловые эфиры предпочтительно расщепляют путем гидрогенолиза (гидрирования) в присутствии пригодного катализатора, такого как, например, палладий на активированном угле. Пригодными инертными растворителями для этих реакций являются вода или органические растворители, обычные для реакций расщепления сложного эфира. Такие растворители предпочтительно включают спирты, такие как метанол, этанол, н-пропанол, изопропанол, н-бутанол или трет-бутанол, или эфиры, такие как диэтиловый эфир, тетрагидрофуран, диоксан или диметиловый эфир гликоля, или другие растворители, такие как ацетон, дихлорметан, диметилформамид или диметилсульфоксид. Также возможно использование смесей упомянутых выше растворителей. В случае гидролиза сложного эфира основанием, предпочтение отдают использованию смесей воды с диоксаном, тетрагидрофураном, метанолом и/или этанолом. В случае реакции с трифторуксусной кислотой, предпочтение отдают использованию дихлорметана, а в случае реакции с хлороводородом, предпочтение отдают использованию тетрагидрофурана, диэтилового эфира, диоксана или воды. Пригодными основаниями являются обычные неорганические основания. Такие основания включают, в частности, гидроксиды щелочных или щелочно-земельных металлов, такие как, например, гидроксид лития, гидроксид натрия, гидроксид калия или гидроксид бария, или карбонаты щелочных или щелочно-земельных металлов, такие как, карбонат натрия, карбонат калия или карбонат кальция. Предпочтение отдают гидроксиду лития, гидроксиду натрия или гидроксиду калия. Пригодными кислотами для расщепления сложного эфира являются, в общем, серная кислота, хлороводород/соляная кислота, бромоводород/бромисто-водородная кислота, фосфорная кислота, уксусная кислота, трифторуксусная кислота, толуолсульфоновая кислота, метансульфоновая кислота или трифторметансульфоновая кислота или их смеси, если уместно, с добавлением воды. Предпочтение отдают хлороводороду или трифторуксусной кислоте в случае трет-бутиловых эфиров, и соляной кислоте в случае сложных метиловых эфиров. Расщепление сложного эфира обычно проводят в температурном диапазоне от -20 до 100 С, предпочтительно от 0 до 60 С. Промежуточные соединения формулы (II) могут быть получены, например, путем:[А] первоначального депротонирования карбоновой кислоты формулы (V) в которой R8A и R8B имеют значения, приведенные выше, и Т 2 означает (С 1-С 4)алкил или бензил,в инертном растворителе с помощью основания, и затем арилирования в присутствии пригодного палладиевого катализатора фенилбромидом формулы (VI) в которой R9 и R10 имеют значения, приведенные выше,с получением соединения формулы (VII)[Б] алкилирования сложного эфира фенилуксусной кислоты формулы (VIII) в которой R9 и R10 имеют значения, приведенные выше, и Т 2 означает (С 1-С 4)алкил или бензил,в инертном растворителе в присутствии основания соединением формулы (IX)X1 означает пригодную уходящую группу, такую как, например, бром или йод,с получением соединения формулы (VII) в которой R8A, R8B, R9, R10 и Т 2 имеют значения, приведенные выше, и затем, в каждом случае, удаления сложноэфирного радикала Т 2 путем основного или кислотного сольволиза или, в случае, если Т означает бензил, также путем гидрогенолиза, с получением карбоновой кислоты (II). Реакцию арилирования на стадии способа (V) + (VI)(VII) предпочтительно проводят в толуоле или смесях толуол/тетрагидрофуран в температурном диапазоне от 20 до 100 С. В данном случае основание, используемое для депротонирования сложного эфира (V), предпочтительно представляет собой бис-(триметилсилил)амид лития. Пригодными палладиевыми катализаторами являются, например, ацетат палладия(II) или трис-(дибензилиденацетон)дипалладий, в каждом случае в комбинации с богатым электронами фосфиновым лигандом, накладывающим стерические ограничения на структуру рецептора,таким как 2-дициклогексилфосфино-2'-(N,N-диметиламино)бифенил или 2-ди-трет-бутилфосфино-2'(N,N-диметиламино)бифенил [ср., например, W.A. Moradi, S.L. Buchwald, J. Am. Chem. Soc. 123, 79968002 (2001)]. Инертными растворителями для реакции алкилирования (VIII) + (IX)(VII) являются, например,эфиры, такие как диэтиловый эфир, метил-трет-бутиловый эфир, диоксан, тетрагидрофуран, диметиловый эфир гликоля или диметиловый эфир диэтиленгликоля, углеводороды, такие как бензол, толуол,ксилол, гексан, циклогексан или фракции минерального масла, или диполярные апротонные растворители,такие как(ДМСО),N,N'диметилпропиленмочевина (DMPU) или N-метилпирролидинон (NMP). Также возможно использование смесей упомянутых растворителей. Предпочтение отдают использованию тетрагидрофурана, диметилформамида или их смесей. Пригодными основаниями для стадии способа (VIII) + (IX)(VII) являются обычные сильные неорганические или органические основания. Такие основания включают, в частности, алкоголяты щелочных металлов, такие как метилат натрия или метилат калия, этилат натрия или этилат калия или третбутилат натрия или трет-бутилат калия, гидриды щелочных металлов, такие как гидрид натрия или гидрид калия, или амиды, такие как бис-(триметилсилил)амид лития, бис-(триметилсилил)амид натрия или бис-(триметилсилил)амид калия или диизопропиламид лития. Предпочтение отдают использованию трет-бутилата калия, гидрида натрия или диизопропиламида лития. Реакцию (VIII) + (IX)(VII) обычно проводят в температурном диапазоне от -80 до 40 С, предпочтительно от -20 до 20 С. Удаление сложноэфирной группы Т 2 на стадии способа (VII)(II) проводят путем, аналогичным описанному выше для сложноэфирного радикала Т 1. Альтернативно, промежуточные соединения формулы (II-А) в которой R9 и R10 имеют значения, приведенные выше,также могут быть получены путем первоначального превращения сложного эфира фенилуксусной кислоты формулы (VIII) в которой R9, R10 и Т 2 имеют значения, приведенные выше, посредством индуцированного основанием присоединения к 2-циклопентен-1-ону, в соединение формулы (X) в которой R9, R1 и Т 2 имеют значения, приведенные выше,затем фторирования этого соединения 1,1'-[(трифтор-4-сульфанил)имино]-бис-(2-метоксиэтаном) при катализе трифторидом бора с получением соединения формулы (VII-A) в которой R9, R10 и Т 2 имеют значения, приведенные выше, и впоследствии удаления сложноэфирной группы Т 2, снова с получением карбоновой кислоты (II-А). На стадии способа (VIII)(X), для депротонирования сложного эфира (VIII), предпочтение отдают использованию амидного основания, такого как диизопропиламид лития или бис(триметилсилил)амид лития. Для деоксифторирования в превращении (X)(VII-А), взамен 1,1'[(трифтор-4-сульфанил)имино]-бис-(2-метоксиэтана) ("дезоксофтор"), упомянутого выше, также возможно, если уместно, использовать другие известные агенты фторирования, такие как трифторид диэти-9 023990 ламиносеры (DAST) или трифторид морфолиносеры (морфо-DAST) [для последовательности реакций(VIII)(X)(VII-A), ср., например, Т. Mase и др., J. Org. Chem. 66 (20), 6775-6786 (2001)]. Промежуточные соединения формулы (III), в зависимости от их схемы замещения, могут быть получены, например, путем либо[В-1] реакции сложного эфира фосфоноуксусной кислоты формулы (XI)R11 означает (С 1-С 4)алкил,в инертном растворителе, в индуцированной основанием реакции олефинирования, с 3 нитробензоильным соединением формулы (XII) в которой L, R4A, R4B, R5, R6 и R7 имеют значения, приведенные выше,с получением соединения формулы (XIII) в которой L, R1, R4A, R4B, R5, R6, R7 и Т 1 имеют значения, приведенные выше, и затем гидрогенизования этого соединения в присутствии пригодного палладиевого или платинового катализатора с получением сложного эфира 3-(3-аминофенил)пропионовой кислоты формулы (III-А)[В-2] реакции сложного эфира фосфоноуксусной кислоты формулы (XI)R11 означает (С 1-С 4)алкил,в инертном растворителе, в индуцированной основанием реакции олефинирования, с защищенным 3-аминобензоильным соединением формулы (XIV)PG означает бензил или 4-метоксибензил в качестве инертной аминозащитной группы,с получением соединения формулы (XV)(i) восстановления этого соединения магнием в метаноле с получением соединения формулы (XVI) в которой L, PG, R1, R4A, R4B, R5, R6, R7 и Т 1 имеют значения, приведенные выше,с получением после удаления аминозащитных групп PG в соответствии с обычными методами, путем гидрогенолиза или окисления, сложного эфира 3-(3-аминофенил)пропионовой кислоты формулы(ii) превращения соединения формулы (XV) в одностадийном способе путем гидрирования в присутствии пригодного палладиевого или платинового катализатора в сложный эфир 3-(3 аминофенил)пропионовой кислоты формулы (III-А), или[Г] сочетания производного сложного эфира акриловой кислоты формулы (XVII) в инертном растворителе при катализе палладием с 3-амино- или 3-нитрофенилбромидом формулыR12 означает амино или нитро,с получением соединения формулы (XIX) в которой L, R1, R4A, R4B, R5, R6, R7, R12 и Т 1 имеют значения, приведенные выше, и затем восстановления этого соединения водородом в присутствии пригодного палладиевого или платинового катализатора или, в случае, если R12 означает амино, альтернативно, магнием в метаноле с получением сложного эфира 3-(3-аминофенил)пропионовой кислоты формулы (III-А)[Д-1] превращения фенилйодида формулы (XX) в которой R6 и R7 имеют значения, приведенные выше,в инертном растворителе реакцией с изопропилмагнийхлоридом в присутствии хлорида лития с получением соответствующего соединения фенилмагния, затем сочетания этого соединения in situ при катализе медью(I) со сложным эфиром алкилиденмалоновой кислоты формулы (XXI) в которой L, R3, R4A, R4B и R5 имеют значения, приведенные выше, и Т 3 означает метил или этил,с получением соединения формулы (XXII)- 12023990 в которой L, R3, R4A, R4B, R5, R6, R7 и Т 3 имеют значения, приведенные выше, затем удаления одной из двух сложноэфирных групп путем нагревания с хлоридом лития в смеси ДМСО/вода, затем превращения полученного сложного эфира 3-фенилпропионовой кислоты формулы (XXIII) в которой L, R3, R4A, R4B, R5, R6, R7 и Т 3 имеют значения, приведенные выше, и в заключение, гидрогенизования в присутствии пригодного палладиевого или платинового катализатора с получением сложного эфира 3-(3-аминофенил)пропионовой кислоты формулы (III-В)PG означает бензил или 4-метоксибензил в качестве инертной аминозащитной группы,в инертном растворителе, реакцией с изопропилмагнийхлоридом в присутствии хлорида лития в соответствующее фенилмагниевое соединение, затем сочетания этого соединения in situ при катализе медью(I) со сложным эфиром алкилиденмалоновой кислоты формулы (XXI) в которой L, R3, R4A, R4B и R5 имеют значения, приведенные выше, и Т 3 означает метил или этил,с получением соединения формулы (XXVI) в которой L, PG, R3, R4A, R4B, R5, R6, R7 и Т 3 имеют значения, приведенные выше,затем снятия зашиты с этого соединения путем гидрогенолиза или путем обработки пригодным окислителем, таким как, например, 2,3-дихлор-5,6-дициано-1,4-бензохинон (DDQ), с получением соединения формулы (XXVII) в которой L, R3, R4A, R4B, R5, R6, R7 и Т 3 имеют значения, приведенные выше, и затем удаления одной из двух сложноэфирных групп путем нагревания с хлоридом лития в смеси ДМСО/вода, с получением 3-(3-аминофенил)пропионовой кислоты формулы (III-В)[Е] алкилирования сложного эфира карбоновой кислоты формулы (XXVIII)X2 означает пригодную уходящую группу, такую как хлор, бром, йод, мезилат, трифлат или тозилат,с получением соединения формулы (XXX) в которой L, R1, R2, R4A, R4B, R5, R6, R7 и Т 1 имеют значения, приведенные выше,затем реакции с бензиламином в присутствии основания и палладиевого катализатора с получением соединения формулы (XXXI) в которой L, R1, R2, R4A, R4B, R5, R6, R7 и Т 1 имеют значения, приведенные выше,и затем удаления N-бензильной группы путем гидрогенолиза, с получением сложного эфира 3-(3 аминофенил)пропионовой кислоты формулы (III-С) в которой L, R1, R2, R4A, R4B, R5, R6, R7 и Т 1 имеют значения, приведенные выше. Пригодными для депротонирования сложного фосфоноэфира (XI) в реакциях олефинирования(XI) + (XII)(XIII) и (XI) + (XIV)(XV) являются, в частности, ненуклеофильные сильные основания,такие как, например, гидрид натрия или гидрид калия, бис-(триметилсилил)амид лития, бис(триметилсилил)амид натрия или бис-(триметилсилил)амид калия или диизопропиламид лития; предпочтение отдают использованию гидрида натрия. Гидрирование в стадиях способа (XIII)(III-А), (XV)(III-А), (XIX)(III-А) и (XXIV)(IIIВ) обычно проводят в стационарной атмосфере водорода при атмосферном или повышенном давлении. Предпочтительно используемый катализатор представляет собой палладий или платину на активированном угле (в качестве подложки катализатора). Удаление аминозащитной группы(групп) в превращениях(XVI)(III-А), (XXVI)(XXVII) и (XXXI)(III-С) обычно проводят путем гидрогенолиза согласно такой же методики; если PG в (XVI) или (XXVI) означает n-метоксибензил, снятие защиты альтернативно также можно провести путем окисления, например с помощью 2,3-дихлор-5,6-дициано-1,4 бензохинона (DDQ) или нитрата аммония-церия(IV). Предпочтительным для применения в качестве палладиевого катализатора для реакции (XVII) +[реакция Хека] является ацетат палладия(II) или трис(дибензилиденацетон)дипалладий(0), в каждом случае в комбинации с фосфиновым лигандом, таким как,например, три-трет-бутилфосфин, трифенилфосфин или три-2-толилфосфин. Превращение фенилйодида (XX) в соответствующее фенилмагниевое соединение и его опосредованное медью(I) 1,4-присоединение к алкилиденмалонату (XXI) с получением продукта формулы (XXII) проводят обычным методом, известным из литературы [см., например, P. Knochel и др., Tetrahedron 56,2727-2731 (2000), и литературу, цитированную там]; это также относится и к аналогичной реакции Особенно пригодными для -депротонирования сложных эфиров карбоновых кислот (XXVIII) в реакциях алкилирования (XXVIII) + (XXIX)(XXX) являются ненуклеофильные сильные основания, такие как, например, трет-бутилат натрия или трет-бутилат калия, гидрид натрия или гидрид калия, диизопропиламид лития или бис-(триметилсилил)амид лития; бис-(триметилсилил)амид натрия или бис(триметилсилил)амид калия; предпочтение отдают использованию диизопропиламида лития. Предпочтительными инертными растворителями для этой реакции являются эфиры, такие как диэтиловый эфир,диизопропиловый эфир, метил трет-бутиловый эфир, тетрагидрофуран, диметиловый эфир гликоля или диметиловый эфир диэтиленгликоля. Реакцию обычно проводят в температурном диапазоне от -80 до 25 С. Для превращения (XXX)(XXXI) [сочетание Бухвальда-Хартвига с бензиламином], предпочтительным катализатором является трис-(дибензилиденацетон)дипалладий(0) в комбинации с -2,2'-бис(дифенилфосфино)-1,1'-бинафтилом в качестве фосфинового лиганда, и предпочтительным основанием является трет-бутилат натрия или трет-бутилат калия [ср., например, J.P. Wolfe и S.L. Buchwald, OrganicSyntheses, Coll. т. 10, 423 (2004), т. 78, 23 (2002)]. Реакции, описанные выше, можно проводить при атмосферном давлении, при повышенном давлении или при пониженном давлении (например, в диапазоне от 0.5 до 5 бар); как правило, указанные реакции в каждом случае проводят при атмосферном давлении. Разделение соединений в соответствии с изобретением на соответствующие энантиомеры и/или диастереомеры может осуществляться в случае необходимости, в зависимости от целесообразности, уже на стадии соединений (II), (III), (IV), (VII), (XVI), (XXII), (XXIII), (XXIV), (XXVI), (XXVII), (XXX) или(XXXI), которые затем вводят в дальнейшую реакцию в разделенном виде в соответствии с описанными выше последовательностями способа. Такое разделение изомеров можно проводить обычными методами, известными специалисту в данной области техники. В рамках настоящего изобретения, предпочтение отдают использованию хроматографических методов на ахиральных или хиральных разделительных фазах; в случае карбоновых кислот в качестве промежуточных соединений или конечных продуктов, разделение альтернативно также можно осуществлять через диастереомерные соли. Соединения формул (V), (VI), (VIII), (IX), (XI), (XII), (XIV), (XVII), (XVIII), (XX), (XXI), (XXV),(XXVIII) и (XXIX) являются либо доступными для приобретения, либо описаны как таковые в литературе, либо они могут быть получены способом, очевидным для специалиста в данной области техники,аналогично методам, опубликованным в литературе. Многочисленные подробные методики и ссылки на литературу, описывающие получение исходных веществ, также можно найти в экспериментальной части в разделе, касающемся получения исходных веществ и промежуточных соединений. Получение соединений в соответствии с изобретением может быть проиллюстрировано с помощью схем реакций, приведенных в качестве примеров ниже: Схема 1 Соединения в соответствии с изобретением обладают ценными фармакологическими свойствами и могут применяться для предотвращения и лечения нарушений у людей и животных. Соединения в соответствии с изобретением являются сильными активаторами растворимой гуанилатциклазы. Они приводят к расширению сосудов, ингибированию агрегации тромбоцитов и снижению кровяного давления и увеличению коронарного кровотока. Эти эффекты опосредуются через прямую гем-независимую активацию растворимой гуанилатциклазы и увеличение внутриклеточного цГМФ. Кроме того, соединения в соответствии с изобретением обладают выгодными фармакокинетическими свойствами, в частности, что касается их биодоступности и/или продолжительности действия после внутривенного или перорального введения. Соединения в соответствии с изобретением являются особенно пригодными для лечения и/или предотвращения сердечно-сосудистых, легочных, тромбоэмболических и фиброзных нарушений. Соответственно, соединения в соответствии с изобретением могут применяться в лекарственных средствах для лечения и/или предотвращения сердечно-сосудистых нарушений, таких как, например,высокое кровяное давление (гипертензия), сердечная недостаточность, коронарная болезнь сердца, стабильная и нестабильная стенокардия, легочная артериальная гипертензия (РАН) и другие формы легочной гипертензии (РН), почечная гипертензия, периферические и сердечно-сосудистые нарушения, аритмии, предсердные и желудочковые аритмии и нарушения проводимости, такие как, например, предсердно-желудочковая блокада I-III степени, наджелудочковая тахиаритмия, фибрилляция предсердий, трепетание предсердий, фибрилляция желудочков, трепетание желудочков, желудочковая тахиаритмия, двунаправленная желудочковая тахикардия, предсердная и желудочковая экстрасистолии, ПЖ-узловая экстрасистолия, синдром слабости синусного узла, обморок, ПЖ-узловая реципрокная тахикардия, синдром Вольфа-Паркинсона-Уайта, острый коронарный синдром (ACS), аутоиммунные нарушения со стороны сердца (перикардит, эндокардит, вальвулит, аортит, кардиомиопатии), кардиомиопатия боксеров, аневризмы, шок, такой как кардиогенный шок, септический шок и анафилактический шок, кроме того для лечения и/или предотвращения тромбоэмболических осложнений и ишемий, таких как миокардиальная ишемия, инфаркт миокарда, удар, гипертрофия сердца, транзиторные и ишемические атаки, преэклампсия, воспалительные сердечно-сосудистые нарушения, спазмы коронарных артерий и периферических артерий, образование отеков, таких как, например, отек легких, отек головного мозга, отек почек или отек, вызванный сердечной недостаточностью, периферическими нарушениями кровообращения, реперфузионными повреждениями, артериальным и венозным тромбозом, микроальбуминурией, миокардиальной недостаточностью, эндотелиальной дисфункцией, микрососудистым и макрососудистым повреждением (васкулит), а также для предотвращения рестенозов, например, после тромболизисной терапии,чрескожной транслюминальной ангиопластики (РТА), чрескожной транслюминальной коронарной ангиопластики (РТСА), пересадок сердца и операций с его отключением. В рамках настоящего изобретения термин "сердечная недостаточность" включает как острое, так и хроническое проявление сердечной недостаточности, а также более специфические или связанные типы заболеваний, такие как острая декомпенсированная сердечная недостаточность, правосторонняя сердечная недостаточность, левосторонняя сердечная недостаточность, глобальная сердечная недостаточность,- 20023990 ишемическая кардиомиопатия, дилатационная кардиомиопатия, гипертрофическая кардиомиопатия,идиопатическая кардиомиопатия, врожденные пороки сердца, пороки клапана сердца, сердечная недостаточность, связанная с пороками клапана сердца, стеноз митральных клапанов, митральная недостаточность, аортальный стеноз, аортальная недостаточность, трикуспидальный стеноз, трикуспидальная недостаточность, стеноз легочного ствола, недостаточность легочного ствола, комбинированные пороки клапана сердца, воспаление миокарда (миокардит), хронический миокардит, острый миокардит, вирусный миокардит, сердечная недостаточность при сахарном диабете, алкогольная кардиомиопатия, "болезни накопления" сердца, и диастолическая и систолическая сердечная недостаточность. Кроме того, соединения в соответствии с изобретением также можно применять для лечения и/или предотвращения артериосклероза, нарушения липидного обмена, гиполипопротеинемий, дислипидемий,гипертриглицеридемий, гиперлипидемий, комбинированных гиперлипидемий, гиперхолестеринемий,абеталипопротеинемий, ситостеролемии, ксантоматоза, танжерской болезни, тучности, ожирения и метаболического синдрома. Кроме того, соединения в соответствии с изобретением можно применять для лечения и/или предотвращения первичного и вторичного феномена Рейно, нарушений микроциркуляции, перемежающейся хромоты, шума в ушах, периферической и вегетативной невропатии, диабетической микроангиопатии,диабетической ретинопатии, диабетических язв на конечностях, гангрены, CREST-синдрома, эритематоза, онихомикоза и ревматических нарушений. Кроме того, соединения в соответствии с изобретением можно применять для предотвращения связанных с ишемией и/или реперфузией повреждений органов или тканей, а также в качестве добавок в растворы для перфузии и консервирования органов, частей органов, тканей или частей тканей человека или животных, в частности при оперативном вмешательстве или в области трансплантационной медицины. Соединения в соответствии с изобретением, кроме того, являются пригодными для лечения и/или предотвращения нарушений почек, в частности почечной недостаточности и отказа почек. В рамках настоящего изобретения, термины почечная недостаточность и отказ почки включают и острое и хроническое проявление таковых, а также первопричинные или связанные заболевания почек, такие как почечная гипоперфузия, интрадиализная гипотензия, обструктивная уропатия, гломерулопатия, гломерулонефрит, острый гломерулонефрит, гломерулосклероз, тубулоинтерстициальные заболевания, нефропатические заболевания, такие как первичное и врожденное заболевание почек, нефрит, иммунологические заболевания почек, такие как отторжение трансплантата почки и вызванные иммунным комплексом заболевания почек, нефропатия, вызванная токсичными веществами, нефропатия, вызванная контрастными веществами, диабетическая и недиабетическая нефропатия, пиелонефрит, кисты почки, нефросклероз,гипертонический нефросклероз и нефротический синдром, который можно охарактеризовать диагностически, например, аномально сниженным(ой) креатинином и/или экскрецией воды, аномально повышенными концентрациями в крови мочевины, азота, калия и/или креатинина, измененной активностью почечных ферментов, таких как, например, глутамилсинтетаза, измененной(ым) осмолярностью мочи или объемом мочи, повышенным содержанием микроальбумина, макроальбумина в моче, поражением клубочков и артериол, тубулярной дилатацией, гиперфосфатемией и/или потребностью в диализе. Настоящее изобретение также включает применение соединений в соответствии с изобретением для лечения и/или предотвращения осложнений почечной недостаточности, таких как, например, гипертензия, отек легких, сердечная недостаточность, уремия, анемия, электролитные нарушения (например, гиперкалиемия, гипонатриемия) и нарушения обмена веществ в костной ткани и углеводного обмена. Кроме того, соединения в соответствии с изобретением пригодны для лечения и/или предотвращения нарушений мочеполовой системы, таких как, например, доброкачественный синдром предстательной железы (BPS), доброкачественная гиперплазия предстательной железы (ВРН), доброкачественное увеличение предстательной железы (ВРЕ), обструкция выходного отверстия мочевого пузыря (BOO), синдром нижних мочевыводящих путей (LUTS), нейрогенный гиперактивный мочевой пузырь (ОАВ), недержание, такое как, например, смешанное, ургентное, недержание при напряжении или вследствие переполнения мочевого пузыря (MUI, UUI, SUI, OUI), тазовая боль, и также эректильная дисфункция и женская сексуальная дисфункция. Соединения в соответствии с изобретением также являются пригодными для лечения и/или предотвращения астматических нарушений, хронического обструктивного заболевания легких (ХОЗЛ), острого респираторного дистресс-синдрома (ARDS) и острого повреждения легких (ALI), альфа- 1 антитрипсиновой недостаточности (AATD), фиброза легких, эмфиземы легких (например, эмфиземы легких, вызванной сигаретным дымом) и фиброзно-кистозной дегенерации (CF), а также легочной артериальной гипертензии (РАН) и других форм легочной гипертензия (РН), в том числе болезней левого отдела сердца, ВИЧ, серповидно-клеточной анемии, тромбоэмболии, саркоидоза, ХОЗЛ или ассоциированной с фиброзом легких легочной гипертензии. Соединения, описанные в настоящем изобретении, также являются активными соединениями для борьбы с заболеваниями центральной нервной системы, характеризующимися нарушениями NO/цГМФ системы. Они являются пригодными, в частности, для улучшения восприятия, концентрации внимания,- 21023990 обучения или памяти после когнитивных нарушений, подобных тем, которые встречаются, в частности, в связи с состояниями/заболеваниями/синдромами, такими как умеренные когнитивные нарушения, связанные с возрастом нарушения обучения и памяти, связанная с возрастом потеря памяти, сосудистая деменция, черепно-мозговая травма, удар, деменция, возникающая после ударов (постударная деменция),посттравматическое состояние, связанное с черепно-мозговой травмой, общие нарушения концентрации внимания, нарушения концентрации внимания у детей с проблемами обучения и памяти, болезнь Альцгеймера, деменция с тельцами Леви, деменция с дегенерацией лобных долей, включая синдром Пика,болезнь Паркинсона, прогрессирующий ядерный паралич, деменция с кортикобазальной дегенерацией,амиолатеральный склероз (ALS), болезнь Хантингтона, демиелинизация, рассеянный склероз, таламическая дегенерация, деменция Крейтцфельда-Якоба, деменция при ВИЧ, шизофрения с деменцией или психоз Корсакова. Такие соединения также являются пригодными для лечения и/или предотвращения нарушений центральной нервной системы, таких как состояния страха, напряжения и депрессии, связанные с ЦНС сексуальные дисфункции и нарушения сна, а также для борьбы с патологическими нарушениями приема пищи, стимуляторов и веществ, вызывающих привыкание. Соединения в соответствии с изобретением, кроме того, также являются пригодными для контролирования церебрального кровотока и, таким образом, представляют эффективные средства для борьбы с мигренью. Они также являются пригодными для профилактики и борьбы с осложнениями церебрального инфаркта (Apoplexia cerebri), например, удара, церебральной ишемии и черепно-мозговой травмы. Соединения в соответствии с изобретением также могут применяться для борьбы с болевыми состояниями. Кроме того, соединения в соответствии с изобретением обладают противовоспалительным действием и вследствие этого могут применяться в качестве противовоспалительных средств для лечения и/или предотвращения сепсиса (SIRS), полиорганной недостаточности (MODS, MOF), воспалительных заболеваний почек, хронического воспаления кишечника (IBS, болезнь Крона, неспецифический язвенный колит), панкреатита, перитонита, ревматоидных нарушений, воспалительных кожных заболеваний и воспалительных болезней глаз. Соединения в соответствии с изобретением, кроме того, являются пригодными для лечения и/или предотвращения фиброзных нарушений внутренних органов, таких как, например, легкое, сердце, почка,костный мозг и, в частности, печень, а также фиброзов кожи и фиброзных болезней глаз. В рамках настоящего изобретения, термин фиброзные нарушения включает, в частности, следующие нарушения: фиброз печени, цирроз печени, фиброз легких, эндомиокардиальный фиброз, нефропатия, гломерулонефрит, интерстициальный фиброз почек, фиброзные повреждения, вызванные диабетом, фиброз костного мозга и подобные фиброзные нарушения, склеродермия, кольцевидная склеродермия, келоиды, гипертрофированные рубцы, невусы, диабетическая ретинопатия, пролиферативная витреоретинопатия и нарушения соединительной ткани (например, саркоидоз). Соединения в соответствии с изобретением также можно применять для стимулирования заживления ран, для борьбы с послеоперационными рубцами, например в результате операций по поводу глаукомы, и косметически для стареющей и кератинизированной кожи. Благодаря своему профилю активности, соединения в соответствии с изобретением являются особенно пригодными для лечения и/или предотвращения сердечно-сосудистых нарушений, таких как сердечная недостаточность, стенокардия, гипертензия и легочная гипертензия, а также тромбоэмболических осложнений и ишемий, сосудистых нарушений, нарушений микроциркуляции, почечной недостаточности, фиброзных нарушений и артериосклероза. Настоящее изобретение, кроме того, относится к применению соединений в соответствии с изобретением для лечения и/или предотвращения нарушений, особенно указанных выше нарушений. Настоящее изобретение, кроме того, относится к применению соединений в соответствии с изобретением для изготовления лекарственного средства для лечения и/или предотвращения нарушений, особенно указанных выше нарушений. Настоящее изобретение, кроме того, относится к применению соединений в соответствии с изобретением в способе лечения и/или предотвращения нарушений, особенно указанных выше нарушений. Настоящее изобретение дополнительно обеспечивает лекарственные средства, которые включают по меньшей мере одно из соединений в соответствии с изобретением, типично вместе с одним или несколькими инертными, нетоксичными, фармацевтически пригодными вспомогательными веществами, и их применение для вышеуказанных целей. Соединения в соответствии с изобретением могут действовать системно и/или местно. Для этой цели, они могут быть введены пригодным образом, например, пероральным, парентеральным, пульмональным, назальным, сублингвальным, лингвальным, буккальным, ректальным, дермальным, трансдермальным, конъюнктивальным, ушным путем или в виде имплантата или стента. Соединения в соответствии с изобретением можно вводить в лекарственных формах, пригодных для этих путей введения. Пригодными лекарственными формами для перорального введения являются формы, которые используются в соответствии с известным уровнем техники, которые высвобождают соединения в соответствии с изобретением быстро и/или модифицированным образом и которые содержат соединения в соот- 22023990 ветствии с изобретением в кристаллической и/или аморфизированной и/или растворенной форме, например, таблетки (непокрытые или покрытые оболочкой таблетки, например с устойчивым к желудочному соку или обеспечивающим замедленное растворение, или нерастворимым покрытиями, которые контролируют высвобождение соединений в соответствии с изобретением), таблетки или пленки/облатки, которые быстро распадаются в ротовой полости, пленки/лиофилизаты или капсулы (например, твердые или мягкие желатиновые капсулы), таблетки с сахарным покрытием, гранулы, пеллеты,порошки, эмульсии, суспензии, аэрозоли или растворы. Парентеральное введение может позволить обойти стадию абсорбции (например, внутривенное,внутриартериальное, внутрисердечное, интраспинальное или интралюмбальное введение) или включает абсорбцию (например, внутримышечное, подкожное, внутрикожное, чрескожное или внутрибрюшинное введение). Лекарственные формы, пригодные для парентерального введения, включают препараты для инъекции и инфузии в форме растворов, суспензий, эмульсий, лиофилизатов или стерильных порошков. Для других путей введения, пригодными примерами являются ингалируемые лекарственные формы(включая применение порошковых ингаляторов, аэрозольных ингаляторов), капли в нос, растворы или жидкости для распыления, таблетки, пленки/облатки или капсулы для лингвального, сублингвального или буккального введения, суппозитории, препараты для введения в уши или в глаза, вагинальные капсулы, водные суспензии (смеси, требующие встряхивания), липофильные суспензии, мази, кремы, трансдермальные терапевтические системы (например, пластыри), молочко, пасты, пены, порошки для опудривания, имплантаты или стенты. Пероральное или парентеральное введение является предпочтительным, особенно пероральное и внутривенное введение. Соединения в соответствии с изобретением могут быть переведены в упомянутые лекарственные формы. Это может быть выполнено способом, известным per se, путем смешивания с инертными, нетоксичными, фармацевтически пригодными наполнителями. Эти наполнители включают носители (например, микрокристаллическую целлюлозу, лактозу, маннит), растворители (например, жидкие полиэтиленгликоли), эмульгаторы и диспергаторы или смачивающие вещества (например, додецилсульфат натрия, полиоксисорбитанолеат), связующие вещества (например, поливинилпирролидон), синтетические и природные полимеры (например, альбумин), стабилизаторы (например, антиоксиданты, например аскорбиновую кислоту), красители (например, неорганические пигменты, например, оксиды железа) и добавки для коррекции вкуса и/или запаха. В общем, было обнаружено, что в случае парентерального введения для достижения эффективных результатов выгодно вводить соединения в количествах приблизительно от 0.001 до 1 мг/кг, предпочтительно приблизительно от 0.01 до 0.5 мг/кг массы тела. В случае перорального введения дозировка составляет приблизительно от 0.01 до 100 мг/кг, предпочтительно приблизительно от 0.01 до 20 мг/кг и наиболее предпочтительно от 0.1 до 10 мг/кг массы тела. Однако, когда это целесообразно, может существовать необходимость в отклонении от указанных количеств, а именно в зависимости от массы тела, пути введения, индивидуального ответа на активное соединение, природы препарата и времени или интервала, в течение которого осуществляют введение. Например, в некоторых случаях, может быть достаточно количества, меньшего, чем вышеупомянутое минимальное количество, в то время как в других случаях упомянутый верхний предел должен быть превышен. При введении относительно больших количеств, может быть целесообразным разделять их на несколько отдельных доз, вводимых в течение дня. Рабочие примеры, которые следуют ниже, иллюстрируют изобретение. Изобретение не ограничивается примерами. Процентные отношения, указанные в исследованиях и примерах, которые следуют ниже, являются,если не указано иное, процентными отношения по массе; части являются частями по массе. Отношения растворителей, степени разбавления и данные концентраций для растворов жидкость/жидкость в каждом случае относятся к объемам.Thermo Hypersil GOLD 3 мк 20 мм 4 мм; подвижная фаза А: 1 л воды + 0.5 мл муравьиной кислоты 50%ной концентрации, подвижная фаза Б: 1 л ацетонитрила + 0.5 мл муравьиной кислоты 50%-ной концентрации; градиент: 0.0 мин 100% А 3.0 мин 10% А 4.0 мин 10% А 4.01 мин 100% А (скорость потока 2.5 мл/мин)5.00 мин 100% А; печь: 50 С; скорость потока: 2 мл/мин; УФ-детектирование: 210 нм. Метод 3 (ЖХ-МС). Тип МС прибора: Micromass ZQ; тип ВЭЖХ прибора: HP 1100 Series; УФ ДДМ; колонка: Phenomenex Gemini 3 мк 30 мм 3.00 мм; подвижная фаза А: 1 л воды + 0.5 мл муравьиной кислоты 50%-ной концентрации, подвижная фаза Б: 1 л ацетонитрила + 0.5 мл муравьиной кислоты 50%-ной концентрации; градиент: 0.0 мин. 90% А 2.5 мин 30% А 3.0 мин 5% А 4.5 мин 5% А; скорость потока: 0.0 мин 1 мл/мин 2.5 мин/3.0 мин/4.5 мин 2 мл/мин; печь: 50 С; УФ-детектирование: 210 нм. Метод 4 (ЖХ-МС). Прибор: Micromass Quattro Premier с Waters UPLC Acquity; колонка: Thermo Hypersil GOLD 1.9 мк 50 мм 1 мм; подвижная фаза А: 1 л воды + 0.5 мл муравьиной кислоты 50%-ной концентрации, подвижная фаза Б: 1 л ацетонитрила + 0.5 мл муравьиной кислоты 50%-ной концентрации; градиент: 0.0 мин 90% А 0.1 мин 90% А 1.5 мин 10% А 2.2 мин 10% А; скорость потока: 0.33 мл/мин; печь: 50 С; УФ-детектирование: 210 нм. Метод 5 (ЖХ-МС). Прибор: Waters Acquity SQD UPLC System; колонка: Waters Acquity UPLC HSS T3 1.8 мк, 50 мм 1 мм; подвижная фаза А: 1 л воды + 0.25 мл муравьиной кислоты 99%-ной концентрации, подвижная фаза Б: 1 л ацетонитрила + 0.25 мл муравьиной кислоты 99%-ной концентрации; градиент: 0.0 мин 90% А 1.2 мин 5% А 2.0 мин 5% А; скорость потока: 0.40 мл/мин; печь: 50 С; УФ-детектирование: 210-400 нм. Метод 6 (ГХ-МС). Прибор: Thermo DFS, Trace GC Ultra; колонка: Restek RTX-35, 15 м 200 мкм 0.33 мкм; постоянный поток гелия: 1.20 мл/мин; печь: 60 С; вход: 220 С; градиент: 60 С, 30 С/мин 300 С (поддерживаемый в течение 3.33 мин). Метод 7 (ЖХ-МС). Прибор: Waters Acquity SQD UPLC System; колонка: Waters Acquity UPLC HSS T3 1.8 мк, 30 мм 2 мм; подвижная фаза А: 1 л воды + 0.25 мл муравьиной кислоты 99%-ной концентрации, подвижная фаза Б: 1 л ацетонитрила + 0.25 мл муравьиной кислоты 99%-ной концентрации; градиент: 0.0 мин 90% А 1.2 мин 5% А 2.0 мин 5% А; скорость потока: 0.60 мл/мин; печь: 50 С; УФ-детектирование: 208-400 нм. Метод 8 (ЖХ-МС). Прибор: Micromass Quattro Premier with Waters UPLC Acquity; колонка: Thermo Hypersil GOLD 1.9 мк 50 мм 1 мм; подвижная фаза А: 1 л воды + 0.5 мл муравьиной кислоты 50%-ной концентрации, подвижная фаза Б: 1 л ацетонитрила + 0.5 мл муравьиной кислоты 50%-ной концентрации; градиент: 0.0 мин 97% А 0.5 мин 97% А 3.2 мин 5% А 4.0 мин 5% А; скорость потока: 0.3 мл/мин; печь: 50 С; УФ-детектирование: 210 нм. Исходные вещества и промежуточные соединения Пример 1 А. трет-Бутил (2E/Z)-4-метокси-4-метилпент-2-еноат При -70 С и в атмосфере аргона 6.8 мл (96 ммоль) ДМСО в 10 мл дихлорметана по каплям добавляли к смеси 24 мл (48 ммоль) 2 М раствора оксалилхлорида в дихлорметане и дополнительных 100 мл дихлорметана и смесь перемешивали в течение 15 мин. Затем по каплям добавляли 5.2 мл (48 ммоль) 2 метокси-2-метилпропан-1-ола [Н. Garcia и др, Chem Eur J. 16 (28), 8530-8536 (2010)], растворенного в 15 мл дихлорметана, и смесь перемешивали при -70 С в течение других 15 мин. Медленно добавляли 22.1 мл (158 ммоль) триэтиламина, реакционную смесь затем перемешивали в течение других 15 мин и потом медленно нагревали до комнатной температуры. Затем добавляли 22 г (58 ммоль) трет-бутил (трифенил 5-фосфанилиден)ацетата и реакционную смесь перемешивали при комнатной температуре в течение ночи. Затем реакционный раствор медленно добавляли к 100 мл воды со льдом и полученные фазы разделяли. Органическую фазу два раза промывали, в каждом случае, 100 мл воды, сушили над сульфатом магния и концентрировали при пониженном давлении на роторном испарителе (температура водяной бани 40 С, давление не ниже 150 мбар). Полученный остаток переносили в приблизительно 100 мл диэтилового эфира и оставляли стоять в холодильнике при 3 С в течение 2 дней. Осажденный трифенилфосфиноксид отфильтровывали и фильтрат концентрировали при пониженном давлении. Полученный остаток очищали с помощью хроматографии на силикагеле (подвижная фаза циклогексан/этилацетат 100:150:1). Это давало 7.06 г (73% от теории) указанного в заголовке соединения в виде бесцветной жидкости. ГХ-МС (метод 6): Rt = 3.32 мин, m/z = 218 (M+NH4)+. Два соединения, приведенные ниже, получали аналогично примеру синтеза 1 А: Пример 4 А и пример 5 А. Метил (2E/Z)-3-(3-амино-4-хлорфенил)-4-метилпент-2-еноат и метил 3-(3-амино-4-хлорфенил)-4-метилпент-3-еноат. В атмосфере аргона смесь 3.22 г (15.6 ммоль) 5-бром-2-хлоранилина, 3.0 г (23.4 ммоль) метил-(2E)4-метилпент-2-еноата, 143 мг (0.16 ммоль) трис-(дибензилиденацетон)дипалладия, 63 мг (0.31 ммоль) три-трет-бутилфосфина и 3.64 мл (17.2 ммоль) N,N-дициклогексилметиламина в 30 мл диоксана нагревали до 120 С и перемешивали при этой температуре в течение трех дней. Как и после первого, так и после второго дня реакции к реакционной смеси добавляли такое же количество палладиевого катализатора и фосфинового лиганда. Реакционную смесь затем фильтровали через целит и фильтрат концентрировали при пониженном давлении. Остаток разделяли на его компоненты с помощью хроматографии на силикагеле (подвижная фаза циклогексан/этилацетат 50:1). Это давало 1.52 г метил (2E/Z)-3-(3-амино-4 хлорфенил)-4-метилпент-2-еноата (38% от теории) и 906 мг метил 3-(3-амино-4-хлорфенил)-4 метилпент-3-еноата (22% от теории). Пример 4 А. Метил (2E/Z)-3-(3-амино-4-хлорфенил)-4-метилпент-2-еноат Следующее соединение получали аналогично примеру синтеза 4 А/5 А: Стадия 1. Раствор 11.1 мл (116.1 ммоль) оксалилхлорида в 50 мл абс. дихлорметана охлаждали до -78 С и по каплям добавляли раствор 16.5 мл (232.2 ммоль) ДМСО в 50 мл абс. дихлорметана, поддерживая температуру ниже -50 С. Спустя 5 мин по каплям добавляли раствор 10.0 г (116.1 ммоль) циклобутанметанола в 20 мл абс. дихлорметана. Спустя дополнительные 15 мин перемешивания при -78 С добавляли 80.9 мл(580.5 ммоль) триэтиламина. Спустя 5 мин охлаждение удаляли, смесь медленно нагревали до к.т. и реакционную смесь затем добавляли к воде. Смесь насыщали хлоридом натрия и отделенную органическую фазу два раза промывали насыщенным раствором хлорида натрия, три раза 1 н. соляной кислотой и три раза рН буферным раствором, сушили над сульфатом натрия и концентрировали при пониженном давлении (500 мбар). Это давало 6.28 г циклобутанкарбальдегида в виде сырого продукта, который непосредственно вводили в реакцию далее. Стадия 2. 6.4 мл (27.3 ммоль) трет-бутил (диэтоксифосфорил)ацетата по каплям добавляли к охлажденной до 0 С суспензии 1.05 г (60% в минеральном масле, 26.2 ммоль) гидрида натрия в смеси 22 мл ТГФ и 22 мл ДМФА. Спустя 30 мин смесь охлаждали до -10 С и несколькими порциями добавляли 2.0 г (сырого,приблизительно 23.8 ммоль) циклобутанкарбальдегида. Реакционную смесь перемешивали при 0 С в течение 5 ч, затем медленно нагревали до к.т. в течение ночи, потом добавляли к воде и экстрагировали три раза этилацетатом. Органические фазы объединяли и концентрировали при пониженном давлении. Остаток очищали с помощью хроматографии на силикагеле (подвижная фаза циклогексан/этилацетат 50:1). Это давало 1.21 г целевого продукта (приблизительно 28% от теории). ГХ-МС (метод 1): Rt = 3.26 мин; m/z = 126 (М-С 4 Н 8)+. 1 Н-ЯМР (400 МГц, ДМСО-d6):[м.д.] = 1.42 (s, 9H), 1.74-1.96 (m, 4H), 2.05-2.17 (m, 2 Н), 3.03-3.16(m, 1 Н), 5.66 (dd, 1H), 6.86 (dd, 1H). Пример 8 А и пример 9 А. трет-Бутил 3-(3-амино-4-хлорфенил)-3-циклобутилакрилат и трет-бутил 3-(3-амино-4-хлорфенил)-3-циклобутилиденпропаноат 0.78 мл (5.60 ммоль) триэтиламина добавляли к смеси 385.2 мг (1.87 ммоль) 5-бром-2-хлоранилина и 510 мг (2.80 ммоль) трет-бутил (2 Е)-3-циклобутилакрилата в 2.8 мл ДМФА. Смесь три раза вакуумировали и в каждом случае вентилировали аргоном. После добавления 41.9 мг (0.187 ммоль) ацетата палладия(II) и 113.6 мг (0.373 ммоль) три-2-толилфосфина, реакционную смесь вакуумировали еще два раза, в каждом случае вентилировали аргоном и затем перемешивали при 150 С в течение 3 ч. Затем добавляли дополнительные 193 мг 5-бром-2-хлоранилина и реакционную смесь перемешивали при 150 С в течение другого 1 ч. После охлаждения реакционную смесь фильтровали через целит и остаток на фильтре два раза промывали с помощью ДМФА. Объединенный фильтрат концентрировали в высоком вакууме и с помощью хроматографии на силикагеле (подвижная фаза циклогексан/этилацетат 60:1) из остатка выделяли два изомерных целевых продукта. Это давало 203 мг трет-бутил 3-(3-амино-4-хлорфенил)-3 циклобутилакрилата (35.4% от теории) и 137 мг трет-бутил 3-(3-амино-4-хлорфенил)-3 циклобутилиденпропаноата (23.8% от теории). ЖХ-МС (метод 5): Rt = 1.27 мин, m/z = 252 (М+Н-С 4 Н 8)+. Н-ЯМР (400 МГц, ДМСО-d6):[м.д.] = 1.31 (s, 9H), 1.93 (quin, 2H), 2.72-2.86 (m, 4H), 3.12 (s, 2H),5.18-5.24 (m, 2H), 6.42 (dd, 1H), 6.69 (d, 1H), 7.06-7.11 (m, 1 Н). Следующие соединения получали аналогично примеру синтеза 8 А/9 А: 1
МПК / Метки
МПК: A61P 9/00, A61K 31/195, C07C 233/55
Метки: производные, разветвленные, кислоты, применение, 3-фенилпропионовой
Код ссылки
<a href="https://eas.patents.su/30-23990-razvetvlennye-proizvodnye-3-fenilpropionovojj-kisloty-i-ih-primenenie.html" rel="bookmark" title="База патентов Евразийского Союза">Разветвленные производные 3-фенилпропионовой кислоты и их применение</a>
Предыдущий патент: Способ кислотно-катализируемой деполимеризации целлюлозы
Следующий патент: Способ получения интермедиатов эстетрола
Случайный патент: Лечение заболеваний, связанных с гиперпроницаемостью сосудов












