Композиции и способы ингибирования экспрессии гена pcsk9
Номер патента: 15676
Опубликовано: 31.10.2011
Авторы: Акинк Акин, Брамлаге Биргит, Тан Памела, Франк-Каменетски Мария, Фитцжеральд Кевин, Котелянски Виктор Е.
Формула / Реферат
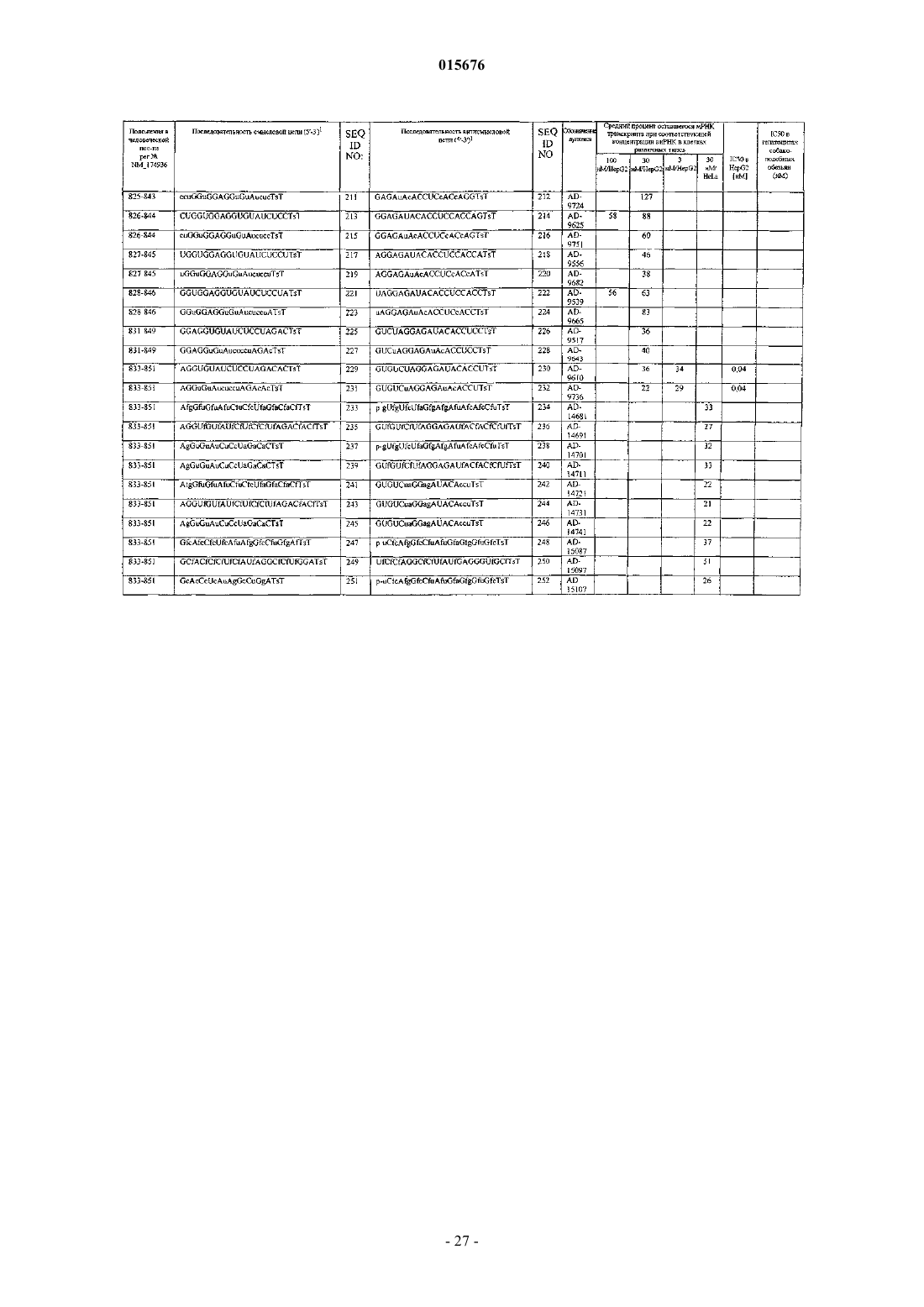
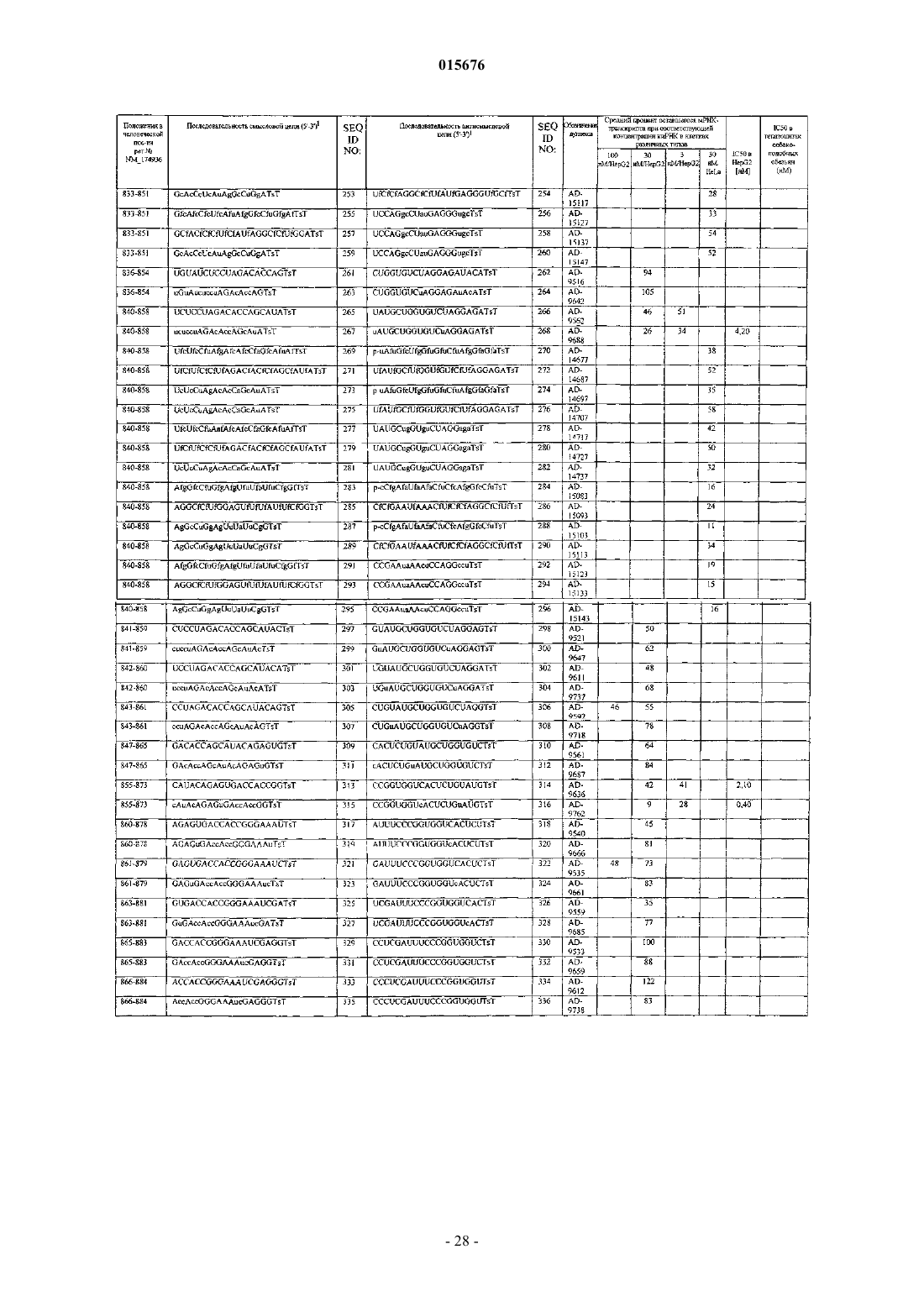
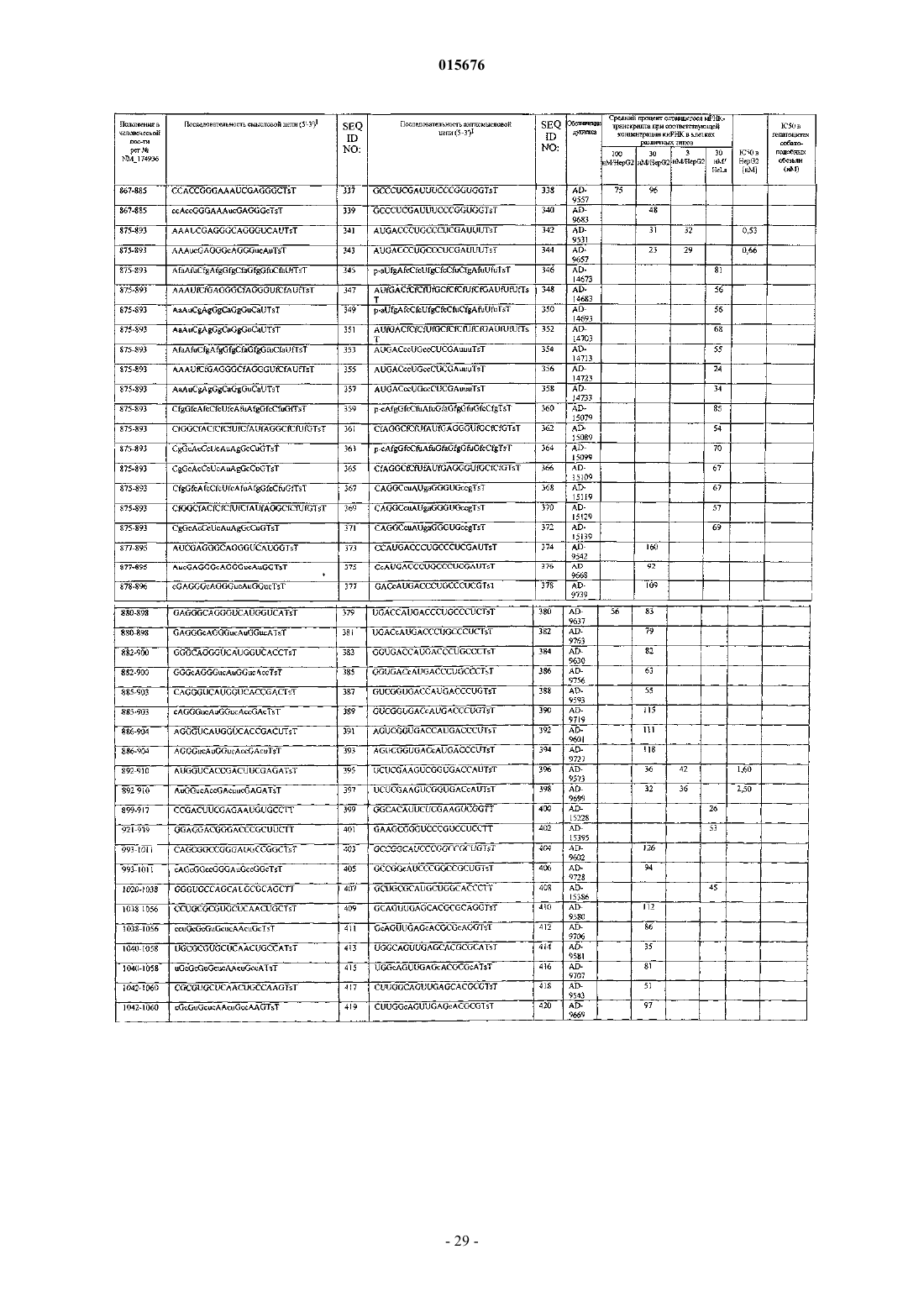
1. Двухцепочечная рибонуклеиновая кислота (дцРНК), ингибирующая экспрессию человеческого гена PCSK9 в клетке, где указанная дцРНК содержит по меньшей мере две последовательности, комплементарные друг другу, где смысловая цепь содержит первую последовательность, а антисмысловая цепь содержит вторую последовательность, включающую в себя область комплементарности, которая, по существу, комплементарна по меньшей мере части мРНК, кодирующей PCSK9, где указанная область комплементарности составляет в длину менее 30 нуклеотидов, где указанная первая последовательность содержит SEQ ID NO: 1229 и указанная вторая последовательность содержит SEQ ID NO: 1230 и где указанная дцРНК в результате ее контактирования с клеткой, экспрессирующей указанную PCSK9, ингибирует экспрессию указанного гена PCSK9.
2. дцРНК по п.1, где указанная дцРНК содержит по меньшей мере один модифицированный нуклеотид.
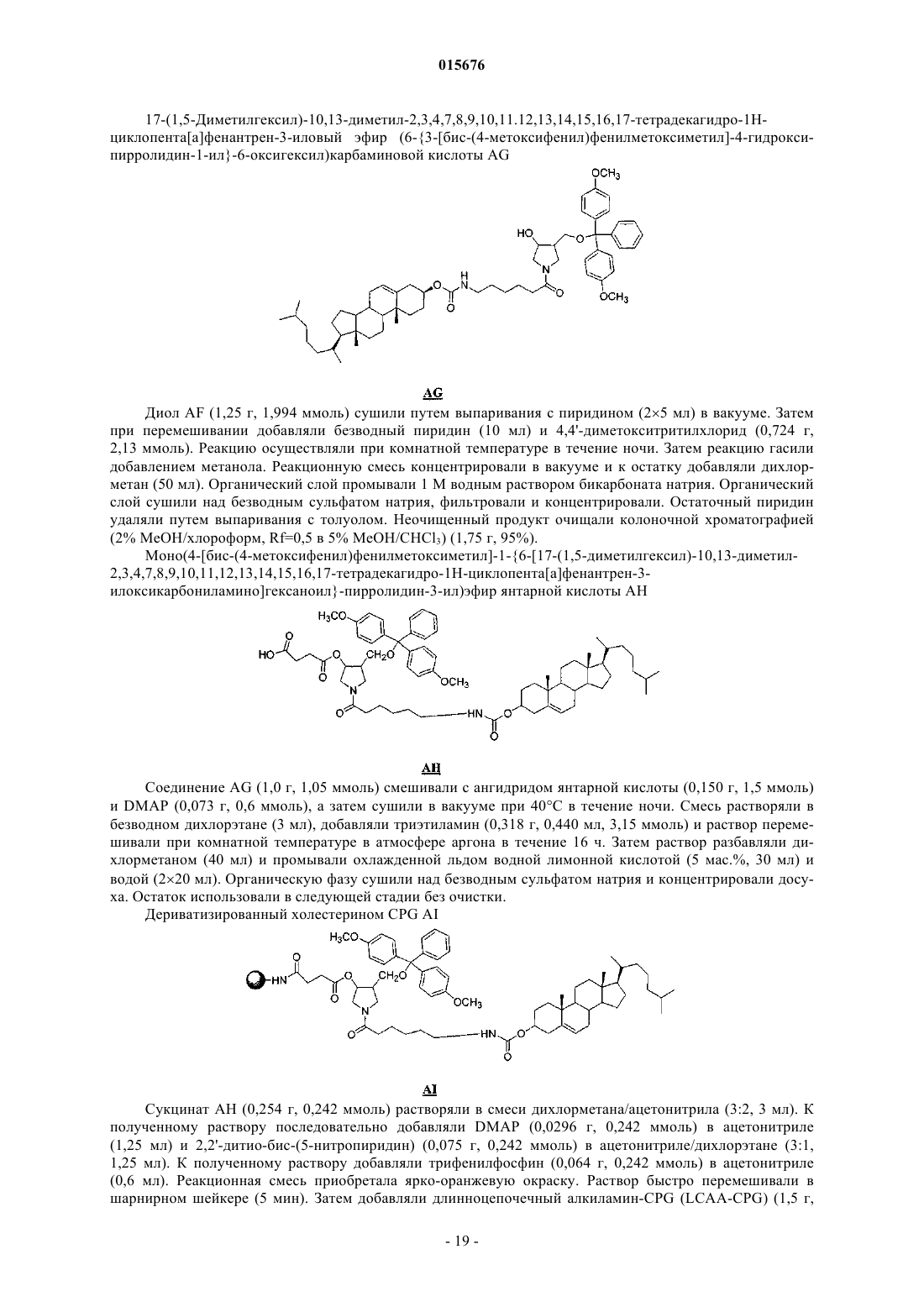
3. дцРНК по п.2, где указанный модифицированный нуклеотид выбран из группы, состоящей из 2'-O-метилмодифицированного нуклеотида; нуклеотида, содержащего 5'-фосфортиоатную группу, и концевого нуклеотида, присоединенного к холестериловому производному или бисдециламидной группе додекановой кислоты, 2'-дезокси-2'-фтормодифицированного нуклеотида, 2'-дезоксимодифицированного нуклеотида, блокированного нуклеотида, неосновного нуклеотида, 2'-аминомодифицированного нуклеотида, 2'-алкилмодифицированного нуклеотида, морфолинонуклеотида, фосфорамидата и нуклеотида, содержащего неприродное основание.
4. дцРНК по п.1, где указанная первая последовательность состоит из SEQ ID NO: 1229, а указанная вторая последовательность состоит из SEQ ID NO: 1230.
5. дцРНК по п.1, где указанная дцРНК способна вызвать снижение уровня липидов в сыворотке.
6. Фармацевтическая композиция для ингибирования экспрессии гена PCSK9 в организме, содержащая дцРНК и фармацевтически приемлемый носитель, где указанная дцРНК содержит по меньшей мере две последовательности, комплементарные друг другу, где смысловая цепь содержит первую последовательность, а антисмысловая цепь содержит вторую последовательность, включающую в себя область комплементарности, которая, по существу, комплементарна по меньшей мере части мРНК, кодирующей PCSK9, где указанная область комплементарности составляет в длину менее 30 нуклеотидов, где указанная первая последовательность содержит SEQ ID NO: 1229 и указанная вторая последовательность содержит SEQ ID NO: 1230 и где указанная дцРНК в результате ее контактирования с клеткой, экспрессирующей указанный PCSK9, ингибирует экспрессию указанного гена PCSK9.
7. Фармацевтическая композиция по п.6, где указанная первая последовательность состоит из SEQ ID NO: 1229, а указанная вторая последовательность состоит из SEQ ID NO: 1230.
8. Фармацевтическая композиция по п.6, где указанная дцРНК способна вызвать снижение уровня липидов в сыворотке.
9. Способ in vitro ингибирования экспрессии гена PCSK9 в клетке, предусматривающий:
(a) введение в клетку двухцепочечной рибонуклеиновой кислоты (дцРНК) по п.1 и
(b) поддержание клетки, продуцированной на стадии (а), в течение периода, достаточного для разрушения мРНК-транскрипта гена PCSK9 и тем самым ингибирования экспрессии гена PCSK9 в указанной клетке.
10. Способ лечения, профилактики или контролирования патологических состояний, которые могут быть опосредованы понижающей регуляцией экспрессии гена PCSK9, предусматривающий введение пациенту, в случае необходимости такого лечения, профилактики или контролирования патологического состояния, терапевтически или профилактически эффективного количества дцРНК по п.1.
11. Вектор для ингибирования экспрессии гена PCSK9 в клетке, где указанный вектор содержит регуляторную последовательность, функционально присоединенную к нуклеотидной последовательности, кодирующей по меньшей мере одну цепь дцРНК по п.1.
Текст
Дата публикации и выдачи патента Номер заявки КОМПОЗИЦИИ И СПОСОБЫ ИНГИБИРОВАНИЯ ЭКСПРЕССИИ ГЕНА PCSK9 Настоящее изобретение относится к двухцепочечной рибонуклеиновой кислоте (дцРНК) для ингибирования экспрессии гена пропротеин-конвертазы субтилизин-кексина 9 (PCSK9),где указанная дцРНК включает в себя антисмысловую цепь, имеющую нуклеотидную последовательность длиной менее чем в 30 нуклеотидов, обычно 19-25 нуклеотидов, и, по существу, комплементарную по меньшей мере части гена PCSK9. Настоящее изобретение относится также к фармацевтической композиции, содержащей дцРНК в комбинации с фармацевтически приемлемым носителем, и к способам лечения заболеваний, вызываемых экспрессией гена PCSK9, с использованием указанной фармацевтической композиции. 015676 Перекрестная ссылка на родственные заявки В заявке на данный патент испрашивается приоритет предварительной заявки на патент США 60/799458, поданной 11 мая 2006 г.; предварительной заявки на патент США 60/817203, поданной 27 июня 2006 г.; предварительной заявки на патент США 60/840089, поданной 25 августа 2006 г.; предварительной заявки на патент США 60/829914, поданной 18 октября 2006 г., и предварительной заявки на патент США 60/901134, поданной 13 февраля 2007 г. Содержание всех указанных предварительных заявок во всей своей полноте вводится в настоящее описание посредством ссылки. Область, к которой относится изобретение Настоящее изобретение относится к двухцепочечной рибонуклеиновой кислоте (дцРНК) и к ее применению в опосредовании интерференции РНК для ингибирования экспрессии гена PCSK9, а также к применению дцРНК для лечения патологических состояний, которые могут быть модулированы посредством ингибирования PCSK9, таких как гиперлипидемия. Предшествующий уровень техники Пропротеин-конвертаза субтилизин-кексин 9 (PCSK9) является членом семейства сериновых протеаз субтилизинов. Другие восемь субтилизиновых протеаз, PCSK1-PCSK8 (также называемых PC1/3,PC2, фурин, PC4, PC5/6, PACE4, PC7 и S1P/SKI-1), представляют собой пропротеин-конвертазы, которые направляют белки широкого ряда на секреторный путь и играют определенную роль в различных биологических процессах (Bergeron, F. (2000), J. Mol. Endocrinol. 24, 1-22, Gensberg, K. (1998), Semin. Cell Dev.Zhou, A. (1999), J. Biol. Chem. 274, 20745-20748). Было высказано предположение, что PCSK9 играет определенную роль в метаболизме холестерина. Экспрессия мРНК PCSK9 ингибировалась после кормления мышей холестеринсодержащей пищей (Maxwell, K.N. (2003), J. Lipid Res. 44, 2109-2119), активируется статинами в клетках HepG2 (Dubuc, G. (2004), Arterioscler. Thromb. Vase. Biol. 24, 1454-1459) и активируется белком, связывающимся со стеролрегулирующим элементом у трансгенных мышей (SREBF)(Horton, J.D. (2003), Proc. Natl. Acad. Sci. USA 100, 12027-12032), аналогично действию ферментов биосинтеза холестерина и рецептора липопротеина низкой плотности (LDL-R). Кроме того, было обнаружено, что миссценс-мутации PCSK9 ассоциируются с гиперхолестеринемией, наследуемой по аутосомнодоминантному типу (Hchola3) (Abifadel, M., et al. (2003), Nat. Genet, 34, 154-156, Timms, K.M. (2004),Hum. Genet 114, 349-353, Leren, T.P. (2004), Clin. Genet. 65, 419-422). PCSK9 может также имеет важное значение в определении уровней холестерина ЛНП у всего населения, поскольку, как наблюдалось у населения Японии, полиморфизм в один нуклеотид (SNP) обычно влияет на уровни холестерина (Shioji, K.(2004), J. Hum. Genet. 49, 109-114). Аутосомно-доминантная гиперхолистеринемия (ADH) представляет собой моногенное заболевание,при котором у пациентов наблюдается повышение уровня общего холестерина и холестерина ЛНП и развитие ксантом сухожилий, а также наблюдается атеросклероз у недоношенных новорожденных(Rader, D.J. (2003), J. Clin. Invest. 111, 1795-1803). Патогенез ADH и его рецессивной формы, аутосомнорецессивной гиперхолистеринемии (ARH) (Cohen, J.C. (2003), Curr. Opin. Lipidol. 14, 121-127), обусловлен нарушением поглощения ЛНП печенью. ADH может быть вызвана мутациями ЛНПР, которые препятствуют поглощению ЛНП, или мутациями в белке, присутствующем на ЛНП, а именно на аполипопротеине В, который связывается с ЛНПР. ARH вызывается мутациями в белке ARH, который необходим для осуществления эндоцитоза комплекса "ЛНПР-ЛНП" посредством его взаимодействия с клатрином. Поэтому если мутации PCSK9 являются этиологическим фактором заболеваний группы Hchola3, то очевидно, что PCSK9 играет определенную роль в опосредуемом рецептором поглощении ЛНП. Исследования сверхэкспрессии показали, что PCSK9 играет определенную роль в регуляции уровней ЛНПР, а следовательно, и в поглощении ЛНП печенью (Maxwell K.N. (2004), Proc. Natl. Acad. Sci.Chem. 279, 50630-50638). У мышей опосредуемая аденовирусом сверхэкспрессия мышиного или человеческого PCSK9, наблюдаемая в течение 3 или 4 дней, приводит к повышению уровней общего холестерина и холестерина ЛНП; при этом такой эффект не наблюдается у животных, не содержащих ЛНПРPCSK9 приводит к значительному снижению уровня белка ЛНПР в печени, но не влияет на уровни мРНК ЛНПР, уровни белка SREBP или на отношение ядерного белка SREBP к цитоплазматическому белкуSREBP. Полученные результаты показали, что PCSK9 прямо или опосредованно снижает уровни белка ЛНПР по посттрансляционному механизму. Мутации, приводящие к потере функций в PCSK9, были смоделированы на мышах (Rashid et al.(2005), PNAS, 102, 5374-5379) и идентифицированы у человека (Cohen et al. (2005), Nature Genetics. 37.161-165). В обоих случаях потеря функции PCSK9 приводит к снижению уровней общего холестерина и холестерина ЛНП. Результаты ретроспективных исследований, проводимых в течение 15 лет, показали,что утрата одной копии PCSK9 приводит к снижению уровня ЛНП и к увеличению степени защиты от развития сердечно-сосудистых заболеваний (Cohen et al. 2006, N. Engl. J. Med., 354, 1264-1272). В настоящее время имеются неопровержимые данные, которые указывают на то, что снижение уровнейPCSK9 приводит к снижению уровней ЛНП. Недавно было показано, что молекулы двухцепочечной РНК (дцРНК) блокируют экспрессию генов по высококонсервативному регуляторному механизму, известному как интерференция РНК (РНКи). ВWO 99/32619 (Fire et al.) описано применение дцРНК длиной по меньшей мере 25 нуклеотидов для ингибирования экспрессии генов у C. elegans. Было также показано, что дцРНК разрушает РНК-мишень в других организмах, включая растения (см., например, WO 99/53050, Waterhouse et al.; WO 99/61631,Heifetz et al.), дрозофилу (Drosophila) (см., например, Yang, D., et al., Curr. Biol. (2000), 10:1191-1200) и млекопитающих (см. WO 00/44895, Limmer; DE 10100586.5, Kreutzer et al.). Такой природный механизм был положен в основу разработки нового класса фармацевтических средств для лечения расстройств,вызываемых нарушением регуляции гена или нежелательной регуляцией гена. Несмотря на значительные успехи в области исследования интерференции РНК (РНКи) и успехи в лечении патологичесих состояний, которые могут быть модулированы негативной регуляцией экспрессии гена PCSK9, необходимость в разработке средств, которые могут ингибировать экспрессию генаPCSK9 и которые могут быть применены для лечения заболеваний, ассоциированных с экспрессией генаPCSK9, таких как гиперлипидемия, остается актуальной. Описание сущности изобретения Настоящее изобретение относится к решению проблемы, связанной с лечением заболеваний, которые могут быть модулированы путем ингибирования пропротеин-конвертазы субтилизин-кексина 9(PCSK9) с использованием двухцепочечной рибонуклеиновой кислоты (дцРНК) для подавления экспрессии PCSK9. Настоящее изобретение относится к двухцепочечной рибонуклеиновой кислоте (дцРНК), а также к композициям и к способам, применяемым в целях ингибирования экспрессии гена PCSK9 в клетках или у млекопитающих с использованием такой дцРНК. Настоящее изобретение также относится к композициям и к способам, применяемым для лечения патологических состояний, которые могут быть модулированы путем ингибирования экспрессии гена PCSK9, таких как гиперлипидемия. дцРНК согласно изобретению содержит цепь РНК (антисмысловую цепь), имеющую область длиной менее чем 30 нуклеотидов, а обычно 19-24 нуклеотидов, и является в основном комплементарной по меньшей мере части мРНК-транскрипта гена PCSK9. В одном из своих вариантов настоящее изобретение относится к молекулам двухцепочечной рибонуклеиновой кислоты (дцРНК), ингибирующим экспрессию гена PCSK9. дцРНК содержит по меньшей мере две последовательности, комплементарные друг другу. дцРНК содержит смысловую цепь, включающую первую последовательность, и антисмысловую цепь, включающую вторую последовательность. Антисмысловая цепь содержит нуклеотидную последовательность, в основном комплементарную по меньшей мере части мРНК, кодирующей PCSK9, где указанная область комплементарности имеет длину менее чем 30 нуклеотидов, а обычно 19-24 нуклеотидов. дцРНК после ее контактирования с клеткой,экспрессирующей PCSK9, ингибирует экспрессию гена PCSK9 по меньшей мере на 40%. Так, например, молекулы дцРНК согласно изобретению могут состоять из первой последовательности дцРНК, выбранной из группы, состоящей из смысловых последовательностей, представленных в табл. 1 и 2, и из второй последовательности, выбранной из группы, состоящей из антисмысловых последовательностей, представленных в табл. 1 и 2. Молекулы дцРНК согласно изобретению могут состоять из природных нуклеотидов, либо они могут состоять по меньшей мере из одного модифицированного нуклеотида, такого как 2'-O-метилмодифицированный нуклеотид; нуклеотид, содержащий 5'-фосфортиоатную группу, и концевой нуклеотид, присоединенный к холестериловому производному. Альтернативно, модифицированный нуклеотид может быть выбран из группы, состоящей из 2'-дезокси 2'-фтормодифицированного нуклеотида, 2'-дезоксимодифицированного нуклеотида, блокированного нуклеотида,неосновного нуклеотида,2'-аминомодифицированного нуклеотида,2'-алкилмодифицированного нуклеотида, морфолинонуклеотида, фосфорамидата и нуклеотида, содержащего неприродное основание. Обычно такую модифицированную последовательность получают на основе первой последовательности указанной дцРНК, выбранной из группы, состоящей из смысловых последовательностей, представленных в табл. 1 и 2, и второй последовательности, выбранной из группы, состоящей из антисмысловых последовательностей, представленных в табл. 1 и 2. В другом своем варианте настоящее изобретение относится к клетке, содержащей одну из дцРНК согласно изобретению. Такой клеткой обычно является клетка млекопитающего, такая как человеческая клетка. В другом своем варианте настоящее изобретение относится к фармацевтической композиции, предназначенной для ингибирования экспрессии гена PCSK9 в организме, обычно в организме человека, где указанная композиция содержит одну или несколько дцРНК согласно изобретению и фармацевтически примемлемый носитель или носитель для доставки. В другом своем варианте настоящее изобретение относится к способу ингибирования экспрессии гена PCSK9 в клетке, где указанный способ включает следующие стадии:(a) введение в клетку двухцепочечной рибонуклеиновой кислоты (дцРНК), где указанная дцРНК содержит по меньшей мере две последовательности, комплементарные друг другу. дцРНК содержит-2 015676 смысловую цепь, включающую первую последовательность, и антисмысловую цепь, включающую вторую последовательность. Антисмысловая цепь содержит область комплементарности, которая в основном комплементарна по меньшей мере части мРНК, кодирующей PCSK9, где указанная комплементарная область имеет длину менее чем 30 нуклеотидов, а обычно 19-24 нуклеотидов, и где указанная дцРНК после ее контактирования с клеткой, экспрессирующей PCSK9, ингибирует экспрессию гена PCSK9 по меньшей мере на 40%; и(b) поддержание клетки, продуцированной в стадии (a), в течение определенного периода времени,достаточного для разрушения мРНК-транскрипта гена PCSK9 и тем самым ингибирования экспрессии гена PCSK9 в указанной клетке. В другом своем варианте настоящее изобретение относится к способам лечения, предупреждения или подавления патологических состояний, которые могут быть модулированы путем ингибирования экспрессии гена PCSK9, например гиперлипидемии, где указанные способы включают введение пациенту, нуждающемуся в таком лечении, предупреждении или подавлении, терапевтически или профилактически эффективного количества одной или нескольких дцРНК согласно изобретению. В другом своем варианте настоящее изобретение относится к векторам для ингибирования экспрессии гена PCSK9 в клетке, где указанные векторы содержат регуляторную последовательность, функционально присоединенную к нуклеотидной последовательности, кодирующей по меньшей мере одну цепь одной из дцРНК согласно изобретению. В другом своем варианте настоящее изобретение относится к клетке, содержащей вектор для ингибирования экспрессии гена PCSK9 в клетке. Указанный вектор содержит регуляторную последовательность, функционально присоединенную к нуклеотидной последовательности, кодирующей по меньшей мере одну цепь одной из дцРНК согласно изобретению. Краткое описание графического материала На фиг. 1 представлена структура липида ND-98. На фиг. 2 представлены результаты in vivo скрининга 16 киРНК, специфических к мышиномуPCSK9 (AL-DP-9327-AL-DP-9342), направленных против различных областей OPC мРНК PCSK9(имеющих первый нуклеотид, соответствующий положению ОРС, как показано на графике), у мышейC57/BL6 (5 животных/группу). Отношение мРНК PCSK9 к мРНК GAPDH в лизатах печени усредняли для каждой группы обработки и сравнивали с контрольной группой, обработанной PBS, или с контрольной группой, обработанной неродственной киРНК (фактора свертывания крови VII). На фиг. 3 представлены результаты in vivo скрининга 16 человеческих/мышиных/крысиных перекрестно-реактивных PCSK9-специфических киРНК (AL-DP-9311-AL-DP-9326), направленных против различных областей OPC мРНК PCSK9 (имеющих первый нуклеотид, соответствующий положению ОРС, как показано на графике) у мышей C57/BL6 (5 животных/группу). Отношение мРНК PCSK9 к мРНК GAPDH в лизатах печени усредняли для каждой группы обработки и сравнивали с контрольной группой, обработанной PBS, или с контрольной группой, обработанной неродственной киРНК (фактора свертывания крови VII). Сайленсинг мРНК PCSK9 приводил к снижению общего уровня холестерина в сыворотке. Наибольшая эффективность в ингибировании киРНК-транскрипта PCSK9 выражается в наиболее заметном снижении уровня холестерина (примерно на 20-30%). На фиг. 4 представлены результаты in vivo скрининга 16 киРНК, специфических к мышиномуPCSK9 (AL-DP-9327-AL-DP-9342) у мышей C57/BL6 (5 животных/группу). Общие уровни холестерина в сыворотке усредняли для каждой группы обработки и сравнивали с контрольной группой, обработаннойPBS, или с контрольной группой, обработанной неродственной киРНК (фактора свертывания крови VII). На фиг. 5 представлены результаты in vivo скрининга 16 человеческих/мышиных/крысиных перекрестно-реактивных PCSK9-специфических киРНК (AL-DP-9311-AL-DP-9326) у мышей C57/BL6 (5 животных/группу). Общие уровни холестерина в сыворотке усредняли для каждой группы обработки и сравнивали с контрольной группой, обработанной PBS, или с контрольной группой, обработанной неродственной киРНК (фактора свертывания крови VII). На фиг. 6 проиллюстрировано сравнение результатов in vitro и in vivo, полученных для сайленсингаPCSK9. На фиг. 7A и 7B представлены результаты, полученные in vitro для сайленсинга PCSK9 с использованием первичных гепатоцитов обезьян. На фиг. 8 проиллюстрирована in vivo активность киРНК, полученных в виде липосомных препаратов LNP-01 и направленных против pcsk-9. На фиг. 9 проиллюстрирована in vivo активность препаратов LNP-01, содержащих химически модифицированные родительские молекулы 9314 и 10792 в различные периоды времени. Было выявлено,что модифицированные варианты 10792 обнаруживают активность в сайленсинге in vivo.-3 015676 Подробное описание изобретения Настоящее изобретение относится к решению проблемы, связанной с лечением заболеваний, которые могут быть модулированы путем ингибирования гена PCSK9 с использованием двухцепочечной рибонуклеиновой кислоты (дцРНК) для подавления экспрессии гена PCSK9 и тем самым для лечения таких заболеваний, как гиперлипидемия. Настоящее изобретение относится к двухцепочечной рибонуклеиновой кислоте (дцРНК), а также к композициям и к способам, применяемым для ингибирования экспрессии гена PCSK9 в клетках или у млекопитающих с использованием такой дцРНК. Настоящее изобретение также относится к композициям и к способам, применяемым для лечения патологических состояний и заболевания, которые могут быть модулированы путем ингибирования экспрессии гена PCSK9. дцРНК регулирует последовательность-специфическое разрушение мРНК по механизму, известному как интерференция РНК (РНКи). дцРНК согласно изобретению включает цепь РНК (антисмысловую цепь), которая имеет область длиной менее чем 30 нуклеотидов, а обычно 19-24 нуклеотидов, и в основном комплементарна по меньшей мере части мРНК-транскрипта гена PCSK9. Применение таких дцРНК позволяет осуществлять направленное разрушение мРНК, которое приводит к транспорту натрия. С помощью клеточных анализов и анализов,проводимых на животных, авторами настоящего изобретения было продемонстрировано, что очень низкие дозы этих дцРНК могут специфически и эффективно опосредовать РНКи, что будет приводить к значительному ингибированию экспрессии гена PCSK9. Таким образом, указанные способы и композиции согласно изобретению, в которых используются эти дцРНК, могут быть применены для лечения патологических состояний, которые могут быть модулированы путем ингибирования PCSK9, например, для лечения гиперлипидемии. Ниже подробно описан способ получения и использования дцРНК и композиций, содержащих дцРНК, для ингибирования экспрессии гена-мишени PCSK9, а также описаны композиции и способы,применяемые для лечения заболеваний, которые могут быть модулированы путем ингибирования экспрессии PCSK9, таких как гиперлипидемия. Фармацевтические композиции согласно изобретению включают дцРНК, имеющую антисмысловую цепь, которая содержит область комплементарности длиной менее чем 30 нуклеотидов, а обычно 19-24 нуклеотидов, и является в основном комплементарной по меньшей мере части мРНК-транскрипта гена PCSK9, в комбинации с фармацевтически приемлемым носителем. В соответствии с этим в некоторых своих аспектах настоящее изобретение относится к фармацевтическим композициям, содержащим дцРНК согласно изобретению в комбинации с фармацевтически приемлемым носителем; к способам применения таких композиций для ингибирования экспрессии генаPCSK9 и к способам применения фармацевтических композиций для лечения заболеваний, которые могут быть модулированы путем ингибирования экспрессии PCSK9.I. Определения. Для удобства ниже приводятся значения некоторых терминов и выражений, используемых в настоящем описании, в примерах и в прилагаемой формуле изобретения. Если имеется значительное различие между употреблением данного термина в других разделах настоящего описания и его определением, приводимым в этом разделе, то следует отдать предпочтение определению данного термина в этом разделе. Каждый из "G", "C", "A" и "U" обычно означает нуклеотид, который содержит гуаниновое, цитозиновое, адениновое и урациловое основания соответственно. Однако при этом следует отметить, что термин "рибонуклеотид" или "нуклеотид" также может означать модифицированный нуклеотид, как будет подробно описано ниже, или молекулу-аналог, имеющую замену. Специалисту в данной области хорошо известно, что гуанин, цитозин, аденин и урацил могут быть заменены другими молекулами без какоголибо значительного изменения свойств спаривания оснований олигонуклеотида, включающего нуклеотид, имеющий такую замененную молекулу. Так, например, нуклеотид, содержащий инозин в качестве основания, может спариваться с нуклеотидами, содержащими аденин, цитозин или урацил и т.п. Следовательно, в нуклеотидных последовательностях согласно изобретению нуклеотиды, содержащие урацил,гуанин или аденин, могут быть заменены нуклеотидом, содержащим, например, инозин. Последовательности, содержащие такие замененные молекулы, являются вариантами настоящего изобретения. Используемый здесь термин "PCSK9" означает ген полипротеин-конвертазы субтилизин-кексина 9 или его белок (также известный как FH3, HCHOLA3, NARC-1, NARC1). Последовательности мРНК, нацеленные на PCSK9, представляют собой человеческую последовательность: NM 174936; мышиную последовательность: NM153565 и крысиную последовательность: NM199253. Используемый здесь термин "последовательность-мишень" означает непрерывную часть нуклеотидной последовательности молекулы мРНК, образованную в процессе транскрипции гена PCSK9,включая мРНК, которая является продуктом РНК-процессинга первичного продукта транскрипции. Используемый здесь термин "цепь, содержащая последовательность" означает олигонуклеотид, содержащий цепь нуклеотидов, последовательность которой описана в соответствии со стандартной номенклатурой нуклеотидов.-4 015676 Используемый здесь термин "комплементарный", если это не оговорено особо и если он используется для описания первой нуклеотидной последовательности по сравнению со второй нуклеотидной последовательностью, означает способность олигонуклеотида или полинуклеотида, содержащего первую нуклеотидную последовательность, гибридизоваться и образовывать дуплексную структуру в определенных условиях с олигонуклеотидом или полинуклеотидом, содержащим вторую нуклеотидную последовательность, как хорошо известно специалистам. Такими условиями могут быть, например, жесткие условия, где указанные жесткие условия могут включать обработку 400 мМ NaCl, 40 мМ PIPES, pH 6,4,1 мМ EDTA, при 50 или 70C в течение 12-16 ч с последующей промывкой. Могут быть применены и другие условия, такие как физиологически релевантные условия, которые могут возникать внутри организма. Специалист в данной области может самостоятельно определить ряд условий, наиболее подходящих для оценки комплементарности двух последовательностей в зависимости от целей применения гибридизованных нуклеотидов. Это определение включает спаривание оснований олигонуклеотида или полинуклеотида, содержащего первую нуклеотидную последовательность, с олигонуклеотидом или полинуклеотидом, содержащим вторую нуклеотидную последовательность, по всей длине первой и второй нуклеотидных последовательностей. Такие последовательности могут называться "полностью комплементарными" друг другу. Однако если первую последовательность определяют как "в основном комплементарную" второй описанной здесь последовательности, то эти две последовательности могут быть полностью комплементарными, либо они могут образовывать одну или более, но в основном не более чем 4, 3 или 2 несоответствующих пар оснований после гибридизации, и при этом сохранять свою способность гибридизоваться в условиях, наиболее подходящих для их конечного применения. Однако если после гибридизации два олигонуклеотида образуют один или несколько одноцепочечных выступающих концов, то такие концы не должны рассматриваться как несоответствия при определении комплементарности. Так, например,дцРНК, содержащая один олигонуклеотид длиной в 21 нуклеотид и другой олигонуклеотид длиной в 23 нуклеотидов, где более длинный олигонуклеотид содержит последовательность из 21 нуклеотида, которая является полностью комплементарной более короткому олигонуклеотиду, может также называться"полностью комплементарной" с точки зрения цели применения настоящего изобретения. Используемый здесь термин "комплементарные" последовательности может также включать пары оснований, не спаренные в соответствии с правилами Уотсона-Крика, или полностью состоять из таких пар оснований, и/или они могут включать пары оснований, образованные неприродными и модифицированными нуклеотидами в зависимости от того, насколько удовлетворяются вышеуказанные требования к их способности к гибридизации. Используемые здесь термины "комплементарный", "полностью комплементарный" и "в основном комплементарный" могут употребляться по отношению к спариванию основания смысловой цепи и антисмысловой цепи дцРНК или антисмысловой цепи дцРНК и последовательности-мишени, как будет очевидно исходя из целей их применения. Используемый здесь термин полинуклеотид, который является, "по существу, комплементарным по меньшей мере части" матричной РНК (мРНК), означает полинуклеотид, в основном комплементарный непрерывной части представляющей интерес мРНК (например, кодирующей PCSK9). Так, например,полинуклеотид является комплементарным по меньшей мере части мРНК PCSK9, если его последовательность, по существу, комплементарна непрерывной части мРНК, кодирующей PCSK9. Используемый здесь термин "двухцепочечная РНК" или "дцРНК" означает комплекс молекул рибонуклеиновой кислоты, имеющий дуплексную структуру, содержащую две антипараллельные и, по существу, комплементарные, как определено выше, цепи нуклеиновой кислоты. Две цепи, образующие дуплексную структуру, могут представлять собой различные части одной более крупной молекулы РНК,либо они могут представлять собой отдельные молекулы РНК. В случае отдельных молекул РНК такая дцРНК часто называется в литературе киРНК ("короткой интерферирующей РНК"). Если две цепи являются частью одной более крупной молекулы, а поэтому между 3'-концом одной цепи и 5'-концом соответствующей другой цепи они соединены друг с другом непрерывной цепью нуклеотидов, образующих дуплексную структуру, то такая соединяющая цепь РНК называется "шпилечной петлей", "короткой шпилечной РНК" или "кшРНК". Если две цепи между 3'-концом одной цепи и 5'-концом соответствующей другой цепи, ковалентно связанные друг с другом посредством другой цепи, т.е. цепи, не являющейся непрерывной цепью нуклеотидов, образующей дуплексную структуру, то такая соединяющая структура называется "линкером". Цепи РНК могут иметь одинаковые или различные количества нуклеотидов. Максимальным числом пар оснований является число нуклеотидов в самой короткой цепи дцРНК минус какие-либо выступающие концы, присутствующие в этом дуплексе. Помимо дуплексной структуры дцРНК может содержать один или несколько выступающих нуклеотидов. Кроме того, используемый в настоящем описании термин "дцРНК" может включать химические модификации рибонуклеотидов, включая основные модификации во многих положениях нуклеотидов и все типы модификаций, описанные в настоящем изобретении или известные специалистам. Все такие модификации, присутствующие в молекуле типа киРНК, входят в объем термина "дцРНК", определяемого в настоящем описании и в формуле изобретения.-5 015676 Используемый здесь термин "выступающий нуклеотид" означает неспаренный нуклеотид или нуклеотиды, которые выступают из дуплексной структуры дцРНК, если 3'-конец одной цепи дцРНК находится за пределами 5'-конца другой цепи или наоборот. Термины "тупой" или "тупой конец" означают,что на конце дцРНК отсутствуют неспаренные нуклеотиды, т.е. отсутствует выступающий нуклеотид."Затупленная по концам дцРНК" представляет собой дцРНК, которая является двухцепочечной по всей ее длине, т.е. у любого конца этой молекулы отсутствуют выступающие нуклеотиды. Для ясности следует отметить, что при определении наличия у киРНК выступающего конца или тупого конца не рассматриваются химические "кэпы" или ненуклеотидные химические молекулы, конъюгированные с 3'-концом или с 5'-концом киРНК. Термин "антисмысловая цепь" означает цепь дцРНК, которая включает область, по существу, комплементарную последовательности-мишени. Используемый здесь термин "область комплементарности" означает область на антисмысловой цепи, которая, по существу, комплементарна последовательности,например последовательности-мишени, определенной в настоящем изобретении. Если область комплементарности не полностью комплементарна последовательности-мишени, то такие несоответствия являются наиболее приемлемыми в концевых областях, а если они и присутствуют, то, главным образом, в концевой области или в концевых областях, например в положениях 6, 5, 4, 3 или 2 нуклеотида 5'- и/или 3'-концов. Используемый здесь термин "смысловая цепь" означает цепь дцРНК, включающую область, по существу, комплементарную области антисмысловой цепи. Термин "введение в клетку", если он относится к дцРНК, означает облегчение поглощения или абсорбции в клетке, как это очевидно для специалиста в данной области. Абсорбция или поглощение дцРНК может происходить посредством природных диффузных или активных клеточных процессов,либо оно может быть осуществлено с помощью вспомогательных средств или устройств. Значения этого термина не ограничиваются клетками in vitro; при этом, дцРНК может быть также "введена в клетку",которая является частью живого организма. В таком случае, термин "введение в клетку" также включает доставку в организм. Так, например, для доставки in vivo, дцРНК может быть инъецирована в конкретный участок, или она может быть введена системно. Введение in vitro в клетку осуществляют методами,известными специалистам, такими как электропорация и липофекция. Используемые здесь термины "сайленсинг" и "ингибирование экспрессии", если они относятся к гену PCSK9, означают, по меньшей мере, частичное подавление экспрессии гена PCSK9, на что указывает снижение количества мРНК, транскрибируемого из гена PCSK9, который может быть выделен из первой клетки или группы клеток, в которой (в которых) транскрибируется ген PCSK9 и которая (которые) были обработаны так, чтобы происходило ингибирование экспрессии гена PCSK9, по сравнению со второй клеткой или группой клеток, по существу, идентичной (или идентичных) первой клетке или группе клеток, которая (или которые) не была (не были) обработана(ы) указанным способом (контрольными клетками). Степень ингибирования обычно выражают математической формулой Альтернативно, степень ингибирования может быть определена как уменьшение значения параметра, которое функционально связано с транскрипцией гена PCSK9, например количества белка, кодируемого геном PCSK9, и секретируемого клеткой, или числа клеток, представляющих определенный фенотип, например подверженных апоптозу. В принципе, сайленсинг гена PCSK9 может быть обнаружен в любой клетке, экспрессирующей мишень, либо конститутивно, либо с помощью генной инженерии, а также с помощью любого подходящего анализа. Однако если необходимо определить, ингибирует ли данная дцРНК экспрессию гена PCSK9 в определенной степени, а следовательно, такое определение входит в объем настоящего изобретения, то для осуществления такого определения рекомендуется проводить анализ, описанный ниже в разделе "Примеры". Так, например, в некоторых случаях экспрессию гена PCSK9 подавляют по меньшей мере примерно на 20, 25, 35 или 50% путем введения двухцепочечного олигонуклеотида согласно изобретению. В некоторых вариантах изобретения ген PCSK9 ингибируется по меньшей мере примерно на 60, 70 или 80% путем введения двухцепочечного олигонуклеотида согласно изобретению. В некоторых вариантах изобретения ген PCSK9 ингибируется по меньшей мере примерно на 85, 90 или 95% путем введения двухцепочечного олигонуклеотида согласно изобретению. В табл. 1 и 2 приводится широкий ряд величин для ингибирования экспрессии, полученных с помощью анализа in vitro, проводимого с использованием различных молекул дцРНК PCSK9 в различных концентрациях. Термины "лечить", "лечение" и т.п., используемые здесь с точки зрения экспрессии PCSK9, означают ослабление или облегчение тяжести патологических состояний, которые могут быть модулированы посредством ингибирования гена PCSK9. В контексте настоящего изобретения термины "лечить", "лечение" и т.п., если они относятся к любым другим описанным ниже состояниям (а не к патологическим состояниям, которые могут быть модулированы посредством ингибирования гена PCSK9), означают облегчение или ослабление по меньшей мере одного симптома, ассоциированного с таким состоянием, ли-6 015676 бо его реверсию. Так, например, если термин "лечение" относится к гиперлипидемии, то он включает снижение уровней липидов в сыворотке. Используемые здесь термины "терапевтически эффективное количество" и "профилактически эффективное количество" означают количество, которое дает терапевтический эффект при лечении, предупреждении или ослаблении патологических состояний или явно выраженного симптома таких патологических состояний, которые могут быть модулированы посредством ингибирования гена PCSK9. Конкретное количество, которое является терапевтически эффективным, может быть легко определено практикующим врачом и может широко варьироваться в зависимости от факторов, известных специалистам,таких как тип патологических состояний, которые могут быть модулированы посредством ингибирования гена PCSK9, история болезни данного пациента и его возраст, стадия развития патологических состояний, которые могут быть модулированы посредством ингибирования PCSK9, и способа введения других средств для подавления патологий, которые могут быть модулированы посредством ингибирования гена PCSK9. Используемая здесь "фармацевтическая композиция" включает фармакологически эффективное количество дцРНК и фармацевтически приемлемый носитель. Используемый здесь термин "фармакологически эффективное количество", "терапевтически эффективное количество" или просто "эффективное количество" означает количество РНК, эффективное для достижения нужного фармакологического, терапевтического или превентивного эффекта. Так, например, если эффективным лечением заболевания считается по меньшей мере 25% снижение величины измеряемого параметра, ассоциированного с данным заболеванием или расстройством, то терапевтически эффективное количество лекарственного средства для лечения данного заболевания или расстройства представляет собой количество, необходимое для достижения по меньшей мере 25% снижения величины данного параметра. Термин "фармацевтически приемлемый носитель" означает носитель для введения терапевтического средства. Такими носителями являются, но не ограничиваются ими, физиологический раствор, забуференный физиологический раствор, декстроза, вода, глицерин, этанол и их комбинации, и такие носители более подробно описаны ниже. Данный термин, в частности, исключает среду для культивирования клеток. Используемый здесь термин "трансформированная клетка" означает клетку, в которую был введен вектор, способный экспрессировать молекулу дцРНК.II. Двухцепочечная рибонуклеиновая кислота (дцРНК). В одном из своих вариантов настоящее изобретение относится к молекулам двухцепочечной рибонуклеиновой кислоты (дцРНК), используемый для ингибирования экспрессии гена PCSK9 в клетках или у млекопитающих, где указанная дцРНК содержит антисмысловую цепь, включающую область комплементарности, которая является комплементарной по меньшей мере части мРНК, образованной в результате экспрессии гена PCSK9, где указанная область комплементарности имеет длину менее чем 30 нуклеотидов, а обычно 19-24 нуклеотидов, и где указанная дцРНК, после ее контактирования с клеткой, экспрессирующей указанный ген PCSK9, ингибирует экспрессию указанного гена PCSK9 по меньшей мере на 40%. Указанная дцРНК содержит две цепи РНК, которые являются достаточно комплементарными для гибридизации с образованием дуплексной структуры. Одна цепь дцРНК (антисмысловая цепь) содержит область комплементарности, которая, по существу, комплементарна, а обычно полностью комплементарна последовательности-мишени, происходящей от последовательности мРНК, образованной в процессе экспрессии гена PCSK9, а другая цепь (смысловая цепь) содержит область, которая является комплементарной антисмысловой цепи, в результате чего эти две цепи гибридизуются и, при их объединении в подходящих условиях, образуют дуплексную структуру. Обычно дуплексная структура имеет длину 15-30, чаще 18-25, еще чаще 19-24, а чаще всего 19-21 пар оснований. Аналогичным образом, область, комплементарная последовательности-мишени, имеет длину 15-30, чаще 18-25, еще чаще 19-24, а чаще всего 19-21 пар оснований. дцРНК согласно изобретению может также включать один или несколько выступающих одноцелочечных нуклеотидов. дцРНК может быть синтезирована стандартными методами, известными специалистам и подробно обсуждаемыми ниже, например с применением автоматического синтезатора ДНК, например, такого как синтезатор, поставляемый компанией Biosearch, AppliedBiosystems, Inc. В предпочтительном варианте изобретения геном PCSK9 является человеческий генPCSK9. В конкретных вариантах изобретения антисмысловая цепь дцРНК включает цепь, выбранную из смысловых последовательностей, представленных в табл. 1 и 2, и вторую последовательность, выбранную из группы, состоящей из антисмысловых последовательностей, представленных в табл. 1 и 2. Альтернативные антисмысловые агенты, нацеленные на последовательность-мишень, представленную в табл. 1 и 2, могут быть легко определены с использованием последовательности-мишени и фланкирующей последовательности PCSK9. В других вариантах изобретения дцРНК содержит по меньшей мере одну нуклеотидную последовательность, выбранную из группы последовательностей, представленных в табл. 1 и 2. В других вариантах изобретения дцРНК содержит по меньшей мере две последовательности, выбранные из этой группы, где одна из по меньшей мере двух последовательностей комплементарна другой последовательности по меньшей мере из двух последовательностей, а одна по меньшей мере из двух последовательностей, поPCSK9. Обычно дцРНК содержит два олигонуклеотида, где один олигонуклеотид описан в табл. 1 и 2 как смысловая цепь, а второй олигонуклеотид описан в табл. 1 и 2 как антисмысловая цепь. Специалистам в данной области хорошо известно, что дцРНК, содержащие дуплексную структуру из 20-23 пар оснований, а в частности из 21 пары оснований, является особенно эффективной в индуцировании интерференции РНК (Elbashir et al., EMBO 2001, 20:6877-6888). Однако другими исследователями было также обнаружено, что могут оказаться эффективными и более короткие или более длинные дцРНК. В описанных выше вариантах дцРНК согласно изобретению могут содержать по меньшей мере одну цепь длиной минимум 21 нуклеотид, что обусловлено природой олигонуклеотидных последовательностей, представленных в табл. 1 и 2. Разумно предположить, что более короткие дцРНК, содержащие одну из последовательностей, представленных в табл. 1 и 2, только без нескольких нуклеотидов у одного или обоих концов, могут быть также эффективными по сравнению с дцРНК, описанными выше. Следовательно, в настоящем изобретении рассматриваются дцРНК, содержащие неполную последовательность по меньшей мере из 15, 16, 17, 18, 19, 20 или более смежных нуклеотидов одной из последовательностей, представленных в табл. 1 и 2, и отличающиеся по своей способности ингибировать экспрессию гена PCSK9 в FACS-анализе, описанном ниже, не более чем на 5, 10, 15, 20, 25 или 30% по сравнению с дцРНК, содержащей полноразмерную последовательность. Другие дцРНК, которые расщепляются в последовательности-мишени, представленной в табл. 1 и 2, могут быть легко получены с использованием описанной здесь последовательности PCSK9 и последовательности-мишени. Кроме того, РНКи-агенты, представленные в табл. 1 и 2, идентифицируют сайт в мРНК PCSK9,восприимчивый к РНКи-расщеплению. Настоящее изобретение также относится к РНКи-агентам, нацеленным на последовательность, на которую нацелен один из агентов согласно изобретению. Считается,что используемый здесь второй РНКи-агент нацелен на последовательность первого РНКи-агента, если указанный второй РНКи-агент расщепляет транскрипт в любом участке мРНК, который является комплементарным антисмысловой цепи первого РНКи-агента. Такой второй агент, по существу, состоит по меньшей мере из 15 смежных нуклеотидов, происходящих от одной из последовательностей, представленных в табл. 1 и 2 и присоединенных к дополнительным нуклеотидным последовательностям, происходящим от области, смежной с выбранной последовательностью в гене PCSK9. Так, например, по меньшей мере 15 нуклеотидов SEQ ID NO: 1 (минус добавленные последовательности AA), объединенные со следующими 6 нуклеотидами от гена-мишени PCSK9, продуцируют одноцепочечный агент из 21 нуклеотида на основе одной из последовательностей, представленных в табл. 1 и 2. дцРНК согласно изобретению может содержать одно или несколько несоответствий по отношению к последовательности-мишени. В предпочтительном варианте изобретения дцРНК согласно изобретению содержит не более чем 3 несоответствия. Если антисмысловая цепь дцРНК содержит несоответствия по отношению к последовательности-мишени, то предпочтительно, чтобы область несоответствий не находилась в центре области комплементарности. Если антисмысловая цепь дцРНК содержит несоответствия по отношению к последовательности-мишени, то предпочтительно, чтобы такое несоответствие ограничивалось 5 нуклеотидами, расположенными у любого конца, например 5, 4, 3, 2 или 1 нуклеотидом, присутствующими у 5'- или 3'-конца области комплементарности. Так, например, в случае цепи дцРНК из 23 нуклеотидов, которая комплементарна области гена PCSK9, эта дцРНК обычно не содержит каких-либо несоответствий в центральной области, состоящей из 13 нуклеотидов. Для того чтобы определить, является ли дцРНК, содержащая несоответствия по отношению к последовательности-мишени, эффективной в ингибировании экспрессии гена PCSK9, могут быть применены способы, описанные в настоящем изобретении. Очень важно, чтобы дцРНК с несоответствиями эффективно ингибировали экспрессию генаPCSK9, особенно если известно, что конкретная область комплементарности в гене PCSK9 имеет модификацию полиморфной последовательности в пределах данной популяции. В одном из вариантов изобретения по меньшей мере на одном конце дцРНК присутствуют 1-4, а обычно 1-2 выступающих одноцепочечных нуклеотида. Было неожиданно обнаружено, что дцРНК,имеющие по меньшей мере один выступающий нуклеотид, обладают превосходными ингибирующими свойствами по сравнению со свойствами их аналогов, имеющих тупые концы. Кроме того, авторами настоящего изобретения было обнаружено, что присутствие лишь одного выступающего нуклеотида усиливает интерферирующую активность дцРНК, не оказывая при этом какого-либо влияния на ее общую стабильность. Было подтверждено, что дцРНК, имеющая только один выступающий конец, является особенно стабильной и эффективной in vivo, а также в различных клетках, в средах для культивирования клеток, в крови и сыворотке. Вообще говоря, одноцепочечный выступающий конец расположен у 3'-конца антисмысловой цепи или, альтернативно, у 3'-конца смысловой цепи. дцРНК может также иметь тупой конец, обычно расположенный у 5'-конца антисмысловой цепи. Такие дцРНК обладают повышенной стабильностью и ингибирующей активностью, что позволяет вводить эти дцРНК в низких дозах, т.е. в дозах, составляющих менее чем 5 мг/кг массы тела реципиента в день. Обычно антисмысловая цепь дцРНК имеет выступающие нуклеотиды у 3'-конца, а 5'-конец является тупым. В другом варианте изобретения один или несколько нуклеотидов в выступающем конце заменены нуклеозид-тиофосфатом. В еще одном варианте изобретения дцРНК химически модифицируют для повышения стабильно-8 015676 сти. Нуклеиновые кислоты согласно изобретению могут быть синтезированы и/или модифицированы методами, хорошо известными специалистам, например, как описано в публикации "Current protocols innucleic acid chemistry". Beaucage, S.L. et. al. (Edrs.), John WileySons, Inc., New York, N.Y., USA, которая вводится в настоящее описание посредством ссылки. Химическими модификациями могут быть, но не ограничиваются ими, 2'-модификации; модификации в других положениях сахаров или оснований олигонуклеотида; введение неприродных оснований в олигонуклеотидную цепь; ковалентное связывание с лигандом или химической молекулой, и замена межнуклеотидных фосфатных связей другими связями,такими как тиофосфатные связи. При этом могут быть использованы более чем одна такая модификация. Химическое связывание двух отдельных цепей дцРНК может быть достигнуто с применением любых различных хорошо известных методов, например путем введения ковалентных, ионных или водородных связей; посредством гидрофобных взаимодействий, ван-дер-ваальсовых взаимодействий или стэкинг-взаимодействий; посредством введения координационных связей "металл-ион" или с использованием пуриновых аналогов. В основном химическими группами, которые могут быть использованы для модификации дцРНК, являются, но не ограничиваются ими, метиленовый синий; бифункциональные группы, обычно бис-(2-хлорэтил)амин; N-ацетил-N'-(п-глиоксилбензоил)цистамин; 4-тиоурацил и псорален. В одном из вариантов изобретения указанным линкером является гексаэтиленгликолевый линкер. В этом случае дцРНК продуцируют посредством твердофазного синтеза, а гексаэтиленгликолевый линкер вводят в соответствии со стандартными методами (см. Williams, D.J. and K.B. Hail, Biochem. (1996),35:14665-14670). В конкретном варианте изобретения 5'-конец антисмысловой цепи и 3'-конец смысловой цепи химически связаны посредством гексаэтиленгликолевого линкера. В другом варианте изобретения по меньшей мере один нуклеотид дцРНК содержит фосфортиоатные или фосфордитиоатные группы. Химическая связь у концов дцРНК обычно образована трехспиральными связями. В табл. 1 и 2 приводятся примеры модифицированных РНКи-агентов согласно изобретению. В еще одном варианте изобретения нуклеотиды у одной или обеих двух одиночных цепей могут быть модифицированы так, чтобы они предотвращали или ингибировали расщепляющую активность клеточных ферментов, например, таких как некоторые нуклеазы и т.п. Методы ингибирования расщепляющей активности клеточных ферментов, направленной против нуклеиновых кислот, известны специалистам, и такими методами являются, но не ограничиваются ими, 2'-амино-модификации, 2'-аминомодификации сахаров, 2'-F-модификации сахаров, 2'-F-модификации, 2'-алкил-модификации сахаров,модификации незаряженного остова, морфолиномодификации, 2'-O-метил-модификации и фосфорамидатные модификации (см., например, Wagner, Nat. Med. (1995), 1:1116-8). Таким образом, по меньшей мере одна 2'-гидроксильная группа нуклеотидов на дцРНК заменена химической группой, обычно 2'амино- или 2'-метильной группой. Кроме того, по меньшей мере один нуклеотид может быть модифицирован так, чтобы он образовывал блокированный нуклеотид. Такой блокированный нуклеотид содержит метиленовый мостик, соединяющий 2'-кислород рибозы с 4'-углеродом рибозы. Олигонуклеотиды, содержащие указанный блокированный нуклеотид, описаны в публикации Koshkin, A.A., et al., Tetrahedron(1998), 54: 3607-3630 и Obika, S. et al. Tetrahedron Lett. (1998), 39; 5401-5404. Введение блокированного нуклеотида в олигонуклеотид приводит к повышению аффинности по отношению к комплементарным последовательностям и увеличению температуры плавления на несколько градусов (Braasch, D.A. and D.R. Corey, Chem. Biol. (2001), 8:1-7). Конъюгирование лиганда с дцРНК может усиливать ее абсорбцию в клетки, а также ее нацеливание на конкретную ткань или поглощение клетками конкретных типов, такими как клетки печени. В некоторых случаях гидрофобный лиганд конъюгируют с дцРНК для облегчения прямого прохождения через клеточную мембрану или поглощения клетками печени. Альтернативно, лиганд, конъюгированный с дцРНК, представляет собой субстрат для опосредуемого рецептором эндоцитоза. Такие подходы были применены для облегчения проникновения в клетку антисмысловых олигонуклеотидов, а также дцРНКагентов. Так, например, холестерин был конъюгирован с различными антисмысловыми олигонуклеотидами с получением соединений, которые являются в основном более активными, чем их неконъюгированные аналоги. См. M. Manoharan AntisenseNucleic Acid Drug Development 2002, 12, 103. Другими липофильными соединениями, которые были конъюгированы с олигонуклеотидами, являются 1-пиренмасляная кислота, 1,3-бис-O-(гексадецил)глицерин и ментол. Одним из примеров лиганда для опосредуемого рецептором эндоцитоза является фолиевая кислота. Фолиевая кислота поступает в клетку благодаря эндоцитозу, опосредуемому фолатным рецептором. Соединения дцРНК, несущие фолиевую кислоту, могут эффективно транспортироваться в клетку посредством эндоцитоза, опосредуемого фолатным рецептором. Li и сотрудники сообщают, что присоединение фолиевой кислоты к 3'-концу олигонуклеотида приводит к 8-кратному повышению уровня поглощения олигонуклеотида клетками. Li, S.;Deshmukh, H.M.; Huang, L. Pharm. Res. 1998, 15, 1540. Другими лигандами, которые были конъюгированы с олигонуклеотидами, являются полиэтиленгликоли, углеводные кластеры, перекрестносвязывающие агенты, конъюгаты порфирина, пептиды для доставки и липиды, такие как холестерин. В некоторых случаях конъюгирование катионного лиганда с олигонуклеотидами приводит к повышению резистентности к нуклеазам. Репрезентативными примерами катионных лигандов являются пропиламмоний и диметилпропиламмоний. Интересно отметить, что антисмысловые олигонуклеотиды, как-9 015676 сообщалось, сохраняют свою высокую аффинность связывания с мРНК в том случае, если катионный лиганд распределен по всему олигонуклеотиду. См. публикацию M. Manoharan AntisenseNucleic AcidDrug Development, 2002, 22, 103 и цитируемые в ней работы. Конъюгированная с лигандом дцРНК согласно изобретению может быть синтезирована с использованием дцРНК, содержащей боковую реакционноспособную функциональную группу, такую как группа,образующаяся в результате присоединения линкерной молекулы к дцРНК. Этот реакционноспособный олигонуклеотид может непосредственно взаимодействовать с коммерчески доступными лигандами; с синтезированными лигандами, содержащими любую из различных защитных групп; или с лигандами,имеющими присоединенную к ним линкерную группу. Способы согласно изобретению облегчают синтез конъюгированной с лигандом дцРНК с использованием в некоторых предпочтительных вариантах изобретения нуклеозидных мономеров, которые были соответствующим образом конъюгированы с лигандами и которые могут быть также присоединены к твердому носителю. Такие конъюгаты "лиганднуклеозид", присоединенные, но необязательно, к твердому носителю, получают в соответствии с некоторыми предпочтительными вариантами способов согласно изобретению посредством взаимодействия выбранного связывающегося с сывороткой лиганда с линкерной группой, присутствующей в 5'положении нуклеозида или олигонуклеотида. В некоторых случаях дцРНК, несущую аралкильный лиганд, присоединенный к 3'-концу дцРНК, получают, главным образом, посредством ковалентного присоединения мономерного структурного блока к стеклянному носителю с регулируемым размером пор через длинноцепочечную аминоалкильную группу. Затем нуклеотиды присоединяют к мономерному структурному блоку, связанному с твердым носителем, стандартными методами твердофазного синтеза. Таким мономерным структурным блоком может быть нуклеозид или другое органическое соединение,совместимое с твердофазным синтезом. дцРНК, используемая в конъюгатах согласно изобретению, может быть получена подходящим и рутинным способом с применением хорошо известного метода твердофазного синтеза. Оборудование для такого синтеза поставляется несколькими компаниями, включая, например, Applied Biosystems(Foster City, CA.). Дополнительно или альтернативно могут быть применены любые другие методы такого синтеза, известные специалистам. Для получения других олигонуклеотидов, таких как фосфортиоаты и их алкилированные призводные, могут быть применены аналогичные методы, также известные специалистам. Описание синтеза конкретных модифицированных олигонуклеотидов можно найти в следующих патентах США: в патентах США 5138045 и 5218105, относящихся к олигонуклеотидам, конъюгированным с полиаминами; в патенте США 5212295, относящемся к мономерам, используемым для получения олигонуклеотидов, имеющих хиральные фосфорные связи; в патентах США 5378825 и 5541307, относящихся к олигонуклеотидам, имеющим модифицированные остовы; в патенте США 5386023, относящемся к олигонуклеотидам с модифицированным остовом и к их получению посредством восстановительного связывания; в патенте США 5457191, относящемся к модифицированным нуклеотидным основаниям, полученным на основе 3-деазапуриновой кольцевой системы и к методам их синтеза; в патенте США 5459255, относящемся к модифицированным нуклеотидным основаниям, полученным на основе N-2-замещенных пуринов; в патенте США 5521302, относящемся к способам получения олигонуклеотидов, имеющих хиральные фосфорные связи; в патенте США 5539082, относящемся к нуклеиновым кислотам, связанным с пептидами; в патенте США 5554746, относящемся к олигонуклеотидам, имеющим -лактамовые остовы; в патенте США 5571902, относящемся к методам и материалам для синтеза олигонуклеотидов; в патенте США 5578718, относящемся к нуклеозидам,имеющим алкилтиогруппы, где указанные группы могут быть использованы в качестве линкеров или других групп, присоединенных в любом из различных положений нуклеозида; в патентах США 5587361 и 5599797, относящихся к олигонуклеотидам, имеющим фосфортиоатные связи с высокой хиральной чистотой; в патенте США 5506351, относящемся к способам получения 2'-Oалкилгуанозиновых и родственных соединений, включая 2,6-диаминопуриновые соединения; в патенте США 5587469, относящемся к олигонуклеотидам, имеющим N-2-замещенные пурины; в патенте США 5587470, относящемся к олигонуклеотидам, имеющим 3-деазапурины; в патентах США 5223168 и 5608046, относящихся к конъюгированным 4'-десметил-нуклеозидным аналогам; в патентах США 5602240 и 5610289, относящихся к олигонуклеотидным аналогам с модифицированным остовом; и в патентах США 6262241 и 5459255, относящихся, inter alia, к методам синтеза 2'-фторолигонуклеотидов. В конъюгированной с лигандом дцРНК и в молекуле лиганда, несущей последовательностьспецифические связанные нуклеозиды согласно изобретению, олигонуклеотиды и олигонуклеозиды могут быть сконструированы на подходящем синтезаторе ДНК с использованием стандартных нуклеотидных или нуклеозидных предшественников или предшественников нуклеотидных или нуклеозидных конъюгатов, которые уже несут линкерную группу, предшественников конъюгатов лиганд-нуклеотид или лиганд-нуклеозид, которые уже несут молекулу лиганда, или структурных блоков, несущих ненуклеозидный лиганд. При использовании предшественников нуклеотидных конъюгатов, уже несущих линкерную группу,- 10015676 обычно осуществляют синтез последовательность-специфических связанных нуклеозидов, а затем молекулу лиганда подвергают взаимодействию с линкерной группой, в результате чего образуется конъюгированный с лигандом олигонуклеотид. Олигонуклеотидные конъюгаты, несущие различные молекулы,такие как стероиды, витамины, липиды и репортерные молекулы, уже были описаны в литературе(см. заявку PCT WO 93/07883, Manoharan et al.). В предпочтительном варианте изобретения олигонуклеотиды или связанные нуклеозиды согласно изобретению синтезируют на автоматическом синтезаторе с использованием фосфорамидитов, происходящих от конъюгатов "лиганд-нуклеозид", помимо стандартных фосфорамидитов и нестандартных фосфорамидитов, которые являются коммерчески доступными и обычно используются в синтезе олигонуклеотидов. Введение 2'-O-метильной группы, 2'-O-этильной группы, 2'-O-пропильной группы, 2'-O-аллильной группы, 2'-O-аминоалкильной группы или 2'-дезокси-2'-фтор-группы в нуклеозиды олигонуклеотида придает такому олигонуклеотиду повышенную способность к гибридизации. Кроме того, олигонуклеотиды, содержащие фосфортиоатные остовы, обладают повышенной стабильностью к нуклеазе. Таким образом, функционализированные связанные нуклеозиды согласно изобретению могут быть увеличены по своему размеру за счет включения любых из следующих компонентов: фосфортиоатного остова или 2'-O-метильной группы, 2'-O-этильной группы, 2'-O-пропильной группы, 2'-O-аминоалкильной группы,2'-O-аллильной группы или 2'-дезокси-2'-фтор-группы. Краткий список некоторых олигонуклеотидных модификаций, известных специалистам, можно найти, например, в публикации заявки PCTWO 200370918. В некоторых вариантах изобретения функционализированные нуклеозидные последовательности согласно изобретению, имеющие аминогруппу у 5'-конца, получают с использованием синтезатора ДНК,а затем их подвергают взаимодействию с активным сложноэфирным производным выбранного лиганда. Активные производные сложных эфиров хорошо известны специалистам в данной области. Репрезентативными активными сложными эфирами являются N-гидроксисукцинимидоэфиры, сложные эфиры тетрафторфенола, сложные эфиры пентафторфенола и сложные эфиры пентахлорфенола. В результате взаимодействия аминогруппы и активного сложного эфира образуется олигонуклеотид, в котором выбранный лиганд присоединен к 5'-положению посредством линкерной группы. Аминогруппа у 5'-конца может быть введена с использованием 5'-амино-модификатора C6. В одном из вариантов изобретения,молекулы лиганда могут быть конъюгированы с олигонуклеотидами в 5'-положении с использованием конъюгата "лиганд-нуклеозид-фосфорамидит", где указанный лиганд прямо или опосредованно присоединен к 5'-гидрокси-группе посредством линкера. Такие конъюгаты "лиганд-нуклеозид-фосфорамидиты" обычно вводят по окончании автоматизированной процедуры синтеза, в результате чего получают конъюгированный с лигандом олигонуклеотид, содержащий лиганд у 5'-конца. Примерами модифицированных межнуклеозидных связей или остовов являются, например, фосфортиоаты, хиральные фосфортиоаты, фосфордитиоаты, фосфотриэфиры, аминоалкилфосфотриэфиры,метилфосфонаты и другие алкилфосфонаты, включая 3'-алкиленфосфонаты и хиральные фосфонаты,фосфинаты, фосфорамидаты, включая 3'-аминофосфорамидат и аминоалкилфосфорамидаты, тионофосфорамидаты, тионоалкилфосфонаты, тионоалкилфосфотриэфиры и боранофосфаты, имеющие нормальные 3'-5'-связи, 2'-5'-связанные аналоги этих соединений и аналоги, имеющие обратную полярность, где смежные пары нуклеозидных остатков имеют 3'-5'-5'-3'- или 2'-5'-5'-2'-связи. Могут быть также включены различные соли, смешанные соли и свободные кислоты. Репрезентативными патентами США, относящимися к получению вышеописанных связей, содержащих атом фосфора, являются, но не ограничиваются ими, патенты США 3687808; 4469863; 4476301; 5023243; 5177196; 5188897; 5264423; 5276019; 5278302; 5286717; 5321131; 5399676; 5405939; 5453496; 5455233; 5466677; 5476925; 5519126; 5536821; 5541306; 5550111; 5563253; 5571799; 5587361; 5625050 и 5697248, каждый из которых вводится в настоящее описание посредством ссылки. Примерами модифицированных межнуклеозидных связей или остовов, не включающих атом фосфора (т.е. олигонуклеозидов), являются связи или остовы, образованные короткоцепочечным алкильными или циклоалкильными межсахарными связями, смешанным гетероатомом и алкильными или циклоалкильными межсахарными связями или одной или несколькими короткоцепочечными гетероатомными или гетероциклическими межсахарными связями. Такими молекулами являются молекулы, имеющие морфолино-связи (частично образованные из сахарной части нуклеозида); силоксановые остовы; сульфидные, сульфоксидные и сульфоновые остовы; формацетильные и тиоформацетильные остовы; метиленформацетильные и тиоформацетильные остовы; алкенсодержащие остовы; сульфаматные остовы; метилениминовые и метиленгидразиновые остовы; сульфонатные и сульфонамидные остовы; амидные остовы и другие остовы, имеющие смешанные группы N, O, S и CH2. Репрезентативными патентами США, относящимися к получению вышеописанных олигонуклеозидов, являются, но не ограничиваются ими, патенты США 5034506; 5166315; 5185444; 5214134; 5216141; 5235033; 5264562; 1264564; 5405938; 5434257; 5466677; 5470967; 5489677; 5541307; 5561225; 5596086; 5602240; 5610289; 5602240; 5608046; 5610289; 5618704; 5623070; 5663312; 5633360; 5677437 и 5677439, каждый и которых вводится в настоящее описание посредством ссылки. В некоторых случаях олигонуклеотид может быть модифицирован нелигандной группой. Различ- 11015676 ные нелигандные молекулы были конъюгированы с олигонуклеотидами для повышения их активности,улучшения распределения в клетках или усиления их поглощения клетками, и процедуры получения таких конъюгатов описаны в научной литературе. Указанными нелигандными молекулами являются липидные молекулы, такие как холестерин (Letsinger et al., Proc. Natl. Acad. Sci. USA, 1989, 86:6553), холевая кислота (Manoharan et al., Bioorg. Med. Chem. Lett., 1994, 4:1053), тиоэфир, например гексил-Sтритилтиол (Manoharan et al., Ann. N.Y. Acad. Sci., 1992, 660:306; Manoharan et al., Bioorg. Med. Chem.Let, 1993, 3:2765), тиохолестерин (Oberhauser et al., Nucl. Acids Res., 1992, 20:533), алифатическая цепь,например додекандиол или ундециловые остатки (Saison-Behmoaras et al., EMBO J., 1991, 10:111;(Manoharan et al. Tetrahedron Lett., 1995, 36:3651; Shea et al., Nucl. Acids Res., 1990, 18:3777), полиаминовая или полиэтиленгликолевая цепь (Manoharan et al., NucleosidesNucleotides, 1995, 14:969) или адамантануксусная кислота (Manoharan et al. Tetrahedron Lett., 1995, 36:3651), пальмитиловая группа (Mishraet al. Biochim. Biophys. Acta, 1995, 1264:229) или октадециламиновая или гексиламино-карбонилоксихолестериновая молекула (Crooks et al., J. Pharmacol Exp. Ther., 1996, 277:923). Репрезентативные патенты США, в которых описано получение таких олигонуклеотидных конъюгатов, перечислены выше. Типичные протоколы конъюгирования включают синтез олигонуклеотидов, несущих аминолинкер в одном или нескольких положениях последовательности. Затем аминогруппу подвергают взаимодействию с молекулой, конъюгированной с использованием соответствующих связывающих или активирующих реагентов. Реакция конъюгирования может быть проведена либо с олигонуклеотидом, еще связанным с твердым носителем, либо уже отщепленным в жидкой фазе. После очистки олигонуклеотидного конъюгата с помощью ВЭЖХ обычно получают чистый конъюгат. Использование холестеринового конъюгата является особенно предпочтительным, поскольку такая молекула может улучшать доставку в клетки печени, т.е. в место, где происходит экспрессия PCSK9. Кодируемые вектором РНКи-агенты. дцРНК согласно изобретению могут также экспрессироваться из рекомбинантных вирусных векторов внутри клеток in vivo. Рекомбинантные вирусные векторы согласно изобретению включают последовательности, кодирующие дцРНК согласно изобретению, и любой подходящий промотор для экспрессии последовательностей дцРНК. Подходящими промоторами являются, например, последовательности промоторов РНК U6 или H1 pol III и промотор цитомегаловируса. Выбор других подходящих промоторов может быть осуществлен самим специалистом в данной области. Рекомбинантные вирусные векторы согласно изобретению могут также содержать индуцибельные или регуляторные промоторы для экспрессии дцРНК в конкретной ткани или в конкретной внутриклеточной среде. Использование рекомбинантных вирусных векторов для доставки дцРНК согласно изобретению в клетки in vivo более подробно обсуждается ниже. дцРНК согласно изобретению может экспрессироваться из рекомбинантого вирусного вектора в виде двух отдельных комплементарных молекул РНК или в виде одной молекулы РНК с двумя комплементарными областями. При этом может быть использован любой вирусный вектор, способный включать кодирующие последовательности экспрессируемой(ых) молекулы(молекул) дцРНК, например векторы, происходящие от аденовируса (AV); аденоассоциированного вируса (AAV); ретровирусов (например, лентивирусов (LV),рабдовирусов, вируса мышиного лейкоза); вируса герпеса и т.п. Тропизм вирусных векторов может быть модифицирован путем псевдотипирования векторов оболочечными белками или другими поверхностными антигенами, происходящими от других вирусов, или путем замены, если это необходимо, различных вирусных капсидных белков. Так, например, лентивирусные векторы согласно изобретению могут быть псевдотипированы поверхностными белками, происходящими от вируса везикулярного стоматита (VSV), вируса бешенства,вируса Эбола, вируса Мокола и т.п. AAV-векторы согласно изобретению могут быть получены для нацеливания на различные клетки путем конструирования векторов, экспрессирующих капсидные белки различных серотипов. Так, например, AAV-вектор, экспрессирующий капсид серотипа 2 на геноме серотипа 2, обозначается AAV 2/2. Такой ген капсида серотипа 2 в векторе AAV 2/2 может быть заменен геном капсида серотипа 5 с получением вектора AAV 2/5. Методы конструирования AAV-векторов, которые экспрессируют капсидные белки различных серотипов, известны специалистам, см., например, публикацию Rabinowitz J. E. et al. (2002), J. Virol. 76:791-801, которая во всей своей полноте вводится в настоящее описание посредством ссылки. Методы отбора рекомбинантных вирусных векторов, подходящих для применения в настоящем изобретении, методы встраивания последовательностей нуклеиновой кислоты для экспрессии дцРНК в векторе и методы доставки вирусного вектора в представляющие интерес клетки известны специалистам. См., например, публикации Dornburg R. (1995), Gene Therap. 2: 301-310; Eglitis M.A. (1988), Biotechniques 6: 608-614; Miller A.D. (1990), Hum Gene Therap. 1: 5-14; Anderson W.F. (1998), Nature 392; 25-30 иRubinson D.A. et al., Wat. Genet. 33: 401-406, которые во всей своей полноте вводятся в настоящее описание посредством ссылки.- 12015676 Предпочтительными вирусными векторами являются векторы, происходящие от AV и AAV. В особенно предпочтительном варианте изобретения дцРНК согласно изобретению экспрессируются как две отдельные комплементарные одноцепочечные молекулы РНК из рекомбинантного AAV-вектора, содержащего, например, либо промоторы РНК U6 или H1, либо промотор цитомегаловируса (CMV).AV-вектор, подходящий для экспрессии дцРНК согласно изобретению, метод конструирования рекомбинантного AV-вектора и метод доставки вектора в клетки-мишени описаны в публикации Xia H. etal. (2002), Nat. Biotech, 20; 1006-1010. Подходящие AAV-векторы для экспрессии дцРНК согласно изобретению, методы конструирования рекомбинантного AV-вектора и методы доставки векторов в клетки-мишени описаны в публикацияхet al. (1989), J. Virol. 63: 3822-3826; в патенте США 5252479; в патенте США 5139941; в международной патентной заявке WO 94/13788; и в международной патентной заявке WO 93/24641, содержание которых во всей своей полноте вводится в настоящее описание посредством ссылки.III. Фармацевтические композиции, содержащие дцРНК. В одном из своих вариантов настоящее изобретение относится к фармацевтическим композициям,содержащим дцРНК, описанную в настоящем изобретении, и фармацевтически приемлемый носитель. Фармацевтическая композиция, содержащая дцРНК, может быть использована для лечения заболеваний или расстройств, ассоциированных с экспрессией или активностью гена PCSK9, таких как патологические состояния, которые могут быть модулированы посредством ингибирования экспрессии гена PCSK9,например, гиперлипидемия. Такие фармацевтические композиции получают исходя из способа доставки. Одним из примеров являются композиции, приготовленные для доставки в печень путем парентерального введения. Фармацевтические композиции согласно изобретению вводят в дозах, достаточных для ингибирования экспрессии гена PCSK9. Авторами настоящего изобретения было обнаружено, что благодаря своей высокой эффективности, композиции, содержащие дцРНК согласно изобретению, могут быть введены в поразительно низких дозах. Доза в 5 мг дцРНК на килограмм массы тела реципиента в день является достаточной для ингибирования или подавления экспрессии гена PCSK9 и может быть системно введена данному пациенту. В общих чертах, подходящая доза дцРНК составляет в пределах от 0,01 до 5,0 мг на 1 кг массы тела реципиента в день, а обычно в пределах от 1 мкг до 1 мг на 1 кг массы тела в день. Фармацевтическая композиция может быть введена один раз в день, либо дцРНК может быть введена в виде двух, трех или более субдоз через определенные интервалы времени в течение дня или даже путем непрерывного вливания или доставки с помощью препарата с регулируемым высвобождением. В этом случае для достижения общей суточной дозы количество дцРНК, содержащееся в каждой субдозе, должно быть соответствующим образом снижено. Унифицированная лекарственная форма может быть также приготовлена для доставки в течение нескольких дней, например, с использованием стандартного препарата с пролонгируемым высвобождением, который обеспечивает пролонгированное высвобождение дцРНК в течение нескольких дней. Препараты с пролонгированным высвобождением хорошо известны специалистам. Специалисту в данной области совершенно очевидно, что на выбор дозы и времени, требуемых для эффективного лечения индивидуума, могут влиять некоторые факторы, включая, но не ограничиваясь ими, тяжесть заболевания или расстройства, предварительное лечение, общее состояние здоровья и/или возраст индивидуума, а также наличие других заболеваний. Кроме того, лечение индивидуума терапевтически эффективным количеством композиции может включать один или несколько курсов лечения. Оценка эффективности доз и времени полужизни in vivo отдельных дцРНК согласно изобретению может быть осуществлена с применением стандартных методик или на основе in vivo тестирования с использованием соответствующего животного-модели, как описано в настоящем изобретении. Прогресс в области генетических исследований на мышах позволяет создать ряд мышиных моделей для исследования различных заболеваний человека, таких как патологические состояния, которые могут быть модулированы путем ингибирования экспрессии гена PCSK9. Указанные модели используются дляin vivo анализа дцРНК, а также для определения терапевтически эффективной дозы. Для введения дцРНК согласно изобретению млекопитающему может быть применен любой метод. Так, например, таким методом введения может быть прямое введение; пероральное введение или парентеральное введение (например, подкожное введение, интравентрикулярное введение, внутримышечное введение, внутрибрюшинное введение или внутривенное вливание). Введение может быть осуществлено сразу (например, путем инъекции) или в течение определенного периода времени (например, путем пролонгированного вливания или введения препаратов с пролонгированным высвобождением). Обычно при лечении млекопитающего с гиперлипидемией, молекулы дцРНК вводят системно путем парентеральной доставки. Так, например, пациенту могут быть внутривенно введены дцРНК, которые могут быть конъюгированы или не конъюгированы, либо приготовлены в виде липосом или без использования липосом. Для этого молекула дцРНК может быть приготовлена в виде композиций, таких как стерильные и нестерильные водные растворы, безводные растворы в стандартных растворителях,таких как спирты, или растворы в жидких или твердых масляных основах. Такие растворы могут также- 13015676 содержать буферы, разбавители и другие подходящие добавки. Для парентерального, интратекального или интравентрикулярного введения, молекула дцРНК может быть приготовлена в виде композиций,таких как стерильные водные растворы, которые могут также содержать буферы, разбавители и другие подходящие добавки (например, усилители пенетрации, соединения-носители и другие фармацевтически приемлемые носители). Кроме того, молекулы дцРНК могут быть введены млекопитающему биологическими или небиологическими методами, описанными, например, в патенте США 6271359. Небиологическая доставка может быть осуществлена различными методами, включая, но не ограничиваясь ими, (1) загрузку липосом молекулой дцРНК, описанной в настоящем изобретении и (2) образование комплекса молекулы дцРНК с липидами или липосомами с получением комплексов "нуклеиновая кислота - липид" или "нуклеиновая кислота - липосома". Липосома может состоять из катионных и нейтральных липидов, обычно используемых для трансфецирования клеток in vitro. Катионные липиды могут подвергаться реакции комплексообразования (например, с переносом заряда) с отрицательно заряженными нуклеиновыми кислотами с образованием липосом. Примерами катионных липосом являются, но не ограничиваются ими,липофектин, липофектамин, липофектак и DOTAP. Методы получения липосом хорошо известны специалистам. Липосомные композиции могут быть получены, например, из фосфатидилхолина, димиристоилфосфатидилхолина, дипальмитоилфосфатидилхолина, димиристоилфосфатидилглицерина или диолеилфосфатидилэтаноламина. Многие липофильные агенты являются коммерчески доступными,включая липофектин (Invitrogen/Life Technologies, Carlsbad, Calif.) и эффектин (Qiagen, Valencia,Calif.). Кроме того, методы системной доставки могут быть оптимизированы с использованием коммерчески доступных катионных липидов, таких как DDAB или DOTAP, каждый из которых может быть смешан с нейтральным липидом, таким как DOPE или холестерин. В некоторых случаях могут быть использованы липосомы, например, описанные в публикации Templeton et al. (Nature Biotechnology, 15: 647-652 (1997. В других вариантах изобретения для доставки in vivo и ex vivo могут быть использованы поликатионы, такие как полиэтиленимин (Boletta et al., J. Am. Soc. Nephrol. 7: 1728 (1996. Дополнительную информацию, относящуюся к использованию липосом для доставки нуклеиновых кислот, можно найти в патенте США 6271359, в публикации заявки PCT WO 96/40964 и в публикацииMorrissey, D. et al. 2005, Nat. Biotechnol. 23(8): 1002-7. Биологическая доставка может быть осуществлена различными методами, включая, но не ограничиваясь ими, использование вирусных векторов. Так, например, вирусные векторы (например, аденовирусные и герпесвирусные векторы) могут быть использованы для доставки молекул дцРНК в клетки печени. Стандартные методы молекулярной биологии могут быть применены для введения одной или нескольких описанных здесь дцРНК в один из множества различных вирусных векторов, предварительно полученных для доставки нуклеиновой кислоты в клетки. Такие вирусные векторы могут быть использованы для доставки одной или нескольких дцРНК в клетки, например, путем инфицирования. дцРНК согласно изобретению могут быть приготовлены в фармацевтически приемлемом носителе или разбавителе. Термин "фармацевтически приемлемый носитель" (также называемый здесь "наполнителем") означает фармацевтически приемлемый растворитель, суспендирующий агент или любой другой фармакологически инертный носитель. Фармацевтически приемлемые носители могут быть жидкими или твердыми и могут быть выбраны в зависимости от выбранного метода введения с учетом желаемого объема, нужной консистенции и другого подходящего способа доставки, а также от химических свойств. Типичными фармацевтически приемлемыми носителями являются, например, но не ограничиваются ими, вода; физиологический раствор; связующие агенты (например, поливинилпирролидон или гидроксипропилметилцеллюлоза); наполнители (например, лактоза и другие сахара, желатин или сульфат кальция); замасливатели (например, крахмал, полиэтиленгликоль или ацетат натрия); дезинтегрирующие агенты (например, крахмал или натрийсодержащий гликолят крахмала) и смачивающие агенты (например, лаурилсульфат натрия). Кроме того, дцРНК, нацеленная на ген PCSK9, может быть приготовлена в виде композиций, содержащих дцРНК, смешанную, инкапсулированную, конъюгированную или как-либо иначе ассоциированную с другими молекулами, молекулярными структурами или смесями нуклеиновых кислот. Так, например, композиция, содержащая один или несколько дцРНК-агентов, нацеленных на ген PCSK9, может содержать другие терапевтические средства, например средства, снижающие уровни липидов (например,статины). Способы лечения заболеваний, которые могут быть модулированы путем ингибирования экспрессии PCSK9. Описанные здесь способы и композиции могут быть использованы для лечения заболеваний и состояний, которые могут быть модулированы путем ингибирования экспрессии гена PCSK9. Так, например, описанные здесь композиции могут быть использованы для лечения гиперлипидемии и других форм нарушений липидного обмена, таких как гиперхолистеринемия, гипертриглицеридемия, а также патологических состояний, ассоциированных с этими расстройствами, таких как болезни сердца и крови. Способы ингибирования экспрессии гена PCSK9. В еще одном своем аспекте настоящее изобретение относится к способу ингибирования экспрессии- 14015676 гена PCSK9 у млекопитающего. Такой способ включает введение композиции согласно изобретению млекопитающему для ингибирования экспрессии гена-мишени PCSK9. Благодаря своей высокой специфичности, дцРНК согласно изобретению специфически нацелены на РНК (первичные или процессированные) гена-мишени PCSK9. Композиции и способы для ингибирования экспрессии этих генов PCSK9 с использованием дцРНК могут быть применены, как описано в настоящем патенте. В одном из вариантов изобретения указанный способ включает введение композиции, содержащей дцРНК, где указанная дцРНК содержит нуклеотидную последовательность, комплементарную по меньшей мере части РНК-транскрипта гена PCSK9 у млекопитающего, подвергаемого лечению. Если подвергаемым лечению организмом является организм млекопитающего, такого как человек, то композиция может быть введена любыми методами, известными специалистам, включая, но не ограничиваясь ими,пероральное или парентеральное введение, включая внутривенное введение, внутримышечное введение,подкожное введение, чрескожное введение и введение в дыхательные пути (с помощью аэрозоля). В предпочтительных вариантах изобретения указанные композиции вводят путем внутривенного вливания или внутривенной инъекции. Если это не оговорено особо, то все технические и научные термины, используемые в настоящем описании, имеют общепринятые значения, понятные среднему специалисту в области, к которой относится настоящее изобретение. Хотя для осуществления настоящего изобретения или для анализов, проводимых в соответствии с настоящим изобретением, могут быть использованы методы и материалы,аналогичные или эквивалентные описанным здесь методам и материалам, однако предпочтительными являются методы и материалы, описанные ниже. Все публикации, патентные заявки, патенты и другие упомянутые здесь работы во всей своей полноте вводятся в настоящее описание посредством ссылки. В случае возникновения противоречий они могут быть урегулированы в соответствии с представленным описанием, включая определения. Кроме того, материалы, методы и примеры приводятся лишь в иллюстративных целях и не должны рассматриваться как ограничение настоящего изобретения. Примеры Прогулка по геному гена PCSK9. Конструирование киРНК осуществляли для ее идентификации в двух отдельных процедурах отбора:a) киРНК, нацеленных на мРНК человеческого и мышиного или крысиного PCSK9, иb) всех человеческих реактивных киРНК с предсказанной специфичностью к гену-мишени PCSK9. Были использованы последовательности мРНК для человеческого, мышиного и крысиного PCSK9: человеческая последовательность NM 174936.2 была использована в качестве эталонной последовательности в процессе осуществления процедуры отбора киРНК. 19-мерные фрагменты, которые являются консервативными для последовательностей мРНК, человеческих и мышиных и человеческих и крысиных PCSK9 были идентифицированы в первой стадии, в результате чего были отобраны киРНК, которые перекрестно реагируют с человеческими и мышиными мишенями, и киРНК, которые перекрестно реагируют с человеческими и крысиными мишенями. Во второй процедуре отбора были идентифицированы киРНК, специфически нацеленные на человеческий PCSK9. Все возможные 19-мерные последовательности человеческого PCSK9 были экстрагированы и определены как кандидаты на последовательности-мишени. Последовательности, перекрестно реагирующие с человеческими и обезьяньими мишенями и с мышиными, крысиными, человеческими и обезьяньими мишенями, перечислены в табл. 1 и 2. Химически модифицированные варианты этих последовательностей и их активность в анализах in vitro и in vivo также перечислены в табл. 1 и 2 и в примерах, представленных на фиг. 2-8. Для ранговой оценки кандидатов последовательностей-мишеней и их соответствующих киРНК и для отбора подходящих последовательностей, их предсказанный потенциал взаимодействия с нерелевантными мишенями (off-target potential) был взят за ранговый параметр. киРНК с низким потенциалом нерелевантного взаимодействия были определены как предпочтительные и было сделано предположение, что они являются специфичными in vivo. Для предсказания киРНК-специфического потенциала нерелевантного взаимодействия были сделаны следующие предположения, что: 1) положения 2-9 (в направлении 5'3') цепи (уникальная область) могут вносить более важный вклад в потенциал нерелевантного взаимодействия, чем остальная последовательность (область за пределами уникальной области и область сайта расщепления); 2) положения 10 и 11 (в направлении 5'3') цепи (область сайта расщепления) могут вносить более важный вклад в потенциал нерелевантного взаимодействия, чем область за пределами уникальной области; 3) положения 1 и 19 каждой цепи не являются подходящими для нерелевантных взаимодействий; 4) показатель нерелевантности может быть вычислен для каждого гена и для каждой цепи исходя из комплементарности последовательности цепи киРНК к последовательности данного гена и из положения несоответствия; 5) число предсказанных нерелевантных мишеней, а также наиболее высокий показатель нерелевантности должен рассматриваться как потенциальная нерелевантность;- 15015676 6) показатели нерелевантности являются более достоверными для оценки потенциала нерелевантности, чем число нерелевантных мишеней; 7) если принять во внимание возможное нарушение активности смысловой цепи в результате введения внутренних модификаций, то следует рассматривать только потенциал нерелевантных взаимодействий антисмысловой цепи. Для идентификации потенциальных нерелевантных генов 19-мерные последовательностикандидаты были подвергнуты скринингу на гомологию с известными человеческими последовательностями мРНК. Для вычисления показателя нерелевантности были выявлены следующие нерелевантные свойства для каждой 19-мерной исходной последовательности каждого нерелевантного гена: число несоответствий в неуникальной области; число несоответствий в уникальной области; число несоответствий в области сайта расщепления. Показатель нерелевантности вычисляли исходя из предположений 1-3 по следующей формуле: Показатель нерелевантности=число несоответствий в уникальной области 10+число несоответствий в сайте расщепления 1,2+число несоответствий в неуникальной области 1. Самый нерелевантный ген для каждой киРНК, соответствующей исходной 19-мерной последовательности, был определен как ген с наиболее низким показателем нерелевантности. В соответствии с этим наиболее низкий показатель нерелевантности был определен как наиболее достоверная оценка нерелевантности для каждой киРНК. Синтез дцРНК. Источник реагентов. Если источник реагентов конкретно не указан в настоящем изобретении, то это означает, что такой реагент может быть получен от любого поставщика реагентов для исследований в области молекулярной биологии в соответствии со стандартами качества/чистоты, установленными для применения в молекулярной биологии. Синтез киРНК. Одноцепочечные РНК были получены методом твердофазного синтеза в масштабе 1 мкмоль на синтезаторе Expedite 8909 (Applied Biosystems, Applera Deutschland GmbH, Darmstadt, Germany) с использованием стекла с регулируемым размером пор (CPG, 500 A, Proligo Biochemie GmbH, Hamburg,Germany) в качестве твердого носителя. РНК и РНК, содержащую 2'-O-метил-нуклеотиды, получали методом твердофазного синтеза с применением соответствующих фосфорамидитов и 2'-Oметилфосфорамидитов соответственно (Proligo Biochemie GmbH, Hamburg, Germany). Эти структурные блоки были введены в выбранные сайты последовательности олигорибонуклеотидной цепи стандартным химическим нуклеозид-фосфорамидитным методом, описанным в современных протоколах по химии нуклеиновых кислот, Beaucage, S.L. et al. (Edrs.), John WileySons, Inc., New York, N.Y., USA. Фосфортиоатные связи были введены путем замены раствора йодного окислителя раствором реагента Бокажа(Chruachem Ltd, Glasgow, UK) в ацетонитриле (1%). Дополнительные вспомогательные реагенты были получены от компании Mallinckrodt Baker (Griesheim, Germany). Снятие защиты и очистку неочищенных олигорибонуклеотидов с помощью анионообменной ВЭЖХ проводили в соответствии со стандартными процедурами. Выходы и концентрации определяли по УФ-поглощению раствора соответствующей РНК на длине волны 260 нм с помощью спектрофотометра (DU 640B, Beckman Coulter GmbH, Unterschleiheim, Germany). Двухцепочечную РНК получали путем смешивания эквимолярного раствора комплементарных цепей в буфере для отжига (20 мМ фосфат натрия, pH 6,8; 100 мМ хлорид натрия), а затем нагревали на водяной бане при 85-90C в течение 3 мин и охлаждали до комнатной температуры в течение 3-4 ч. Раствор гибридизованной РНК хранили при -20C вплоть до ее использования. Для синтеза киРНК, конъюгированных с холестерином в 3'-положении (также обозначаемых здесьChol-3'), использовали соответствующим образом модифицированный твердый носитель. Модифицированный твердый носитель получала следующим образом. Диэтил-2-азабутан-1,4-дикарбоксилат АА 4,7 М водный раствор гидроксида натрия (50 мл) добавляли в перемешиваемый охлажденный льдом раствор гидрохлорида этилглицината (32,19 г, 0,23 моль) в воде (50 мл). Затем добавляли этилакрилат (23,1 г, 0,23 моль) и смесь перемешивали при комнатной температуре до завершения реакции, на что указывала ТСХ. Через 19 ч раствор распределяли с дихлорметаном (3100 мл). Органический слой сушили безводным сульфатом натрия, фильтровали и упаривали. Остаток подвергали перегонке с получением AA (28,8 г, 61%).Fmoc-6-аминогексановую кислоту (9,12 г, 25,83 ммоль) растворяли в дихлорметане (50 мл) и охлаждали на льду. К полученному раствору добавляли диизопропилкарбодиимид (3,25 г, 3,99 мл,25,83 ммоль) при 0C. Затем добавляли диэтилазабутан-1,4-дикарбоксилат (5 г, 24,6 ммоль) и диметиламинопиридин (0,305 г, 2,5 ммоль). Раствор доводили до комнатной температуры и перемешивали еще 6 ч. Завершение реакции определяли с помощью ТСХ. Реакционную смесь концентрировали в вакууме и добавляли этилацетат для осаждения диизопропилмочевины. Суспензию фильтровали. Фильтрат промывали 5% водной соляной кислотой, 5% бикарбонатом натрия и водой. Объединенный органический слой сушили над сульфатом натрия и концентрировали с получением неочищенного продукта, который затем очищали с помощью колоночной хроматографии (50% EtOAC/гексан), в результате чего получали 11,87 г (88%) AB. Этиловый эфир 3-[(6-аминогексаноил)этоксикарбонилметиламино]пропионовой кислоты АС Этиловый эфир 3-этоксикарбонилметил-[6-(9H-флуорен-9-илметоксикарбониламино)гексаноил]аминопропионовой кислоты AB (11,5 г, 21,3 ммоль) растворяли в 20% пиперидине в диметилформамиде при 0C. Раствор перемешивали в течение 1 ч. Реакционную смесь концентрировали в вакууме, а затем к остатку добавляли воду и продукт экстрагировали этилацетатом. Неочищенный продукт очищали путем его превращения в гидрохлоридную соль. Этиловый эфир 3-(6-[17-(1,5-диметилгексил)-10,13-диметил-2,3,4,7,8,9,10,11,12,13,14,15,16,17 тетрадекагидро-1H-циклопента[a]фенантрен-3-илоксикарбониламино]гексаноилэтоксикарбонилметиламино)пропионовой кислоты AD Гидрохлоридную соль этилового эфира 3-[(6-аминогексаноил)этоксикарбонилметиламино]пропионовой кислоты AC (4,7 г, 14,8 ммоль) растворяли в дихлорметане. Суспензию охлаждали до 0C на льду. К этой суспензии добавляли диизопропилэтиламин (3,87 г, 5,2 мл, 30 ммоль). К полученному раствору добавляли холестерилхлорформиат (6,675 г, 14,8 ммоль). Реакционную смесь перемешивали в течение ночи. Затем реакционную смесь разбавляли дихлорметаном и промывали 10% соляной кислотой. Полученный продукт очищали флэш-хроматографией (10,3 г, 92%). трет-Бутоксид калия (1,1 г, 9,8 ммоль) суспендировали в 30 мл сухого толуола. Смесь охлаждали до 0C на льду и медленно добавляли 5 г (6,6 ммоль) диэфира AD при перемешивании в течение 20 мин. В процессе добавления температуру поддерживали ниже 5C. Перемешивание продолжали в течение 30 мин при 0C и добавляли 1 мл ледяной уксусной кислоты, а затем сразу добавляли 4 г NaH2PO4H2O в 40 мл воды. Полученную смесь два раза экстрагировали 100 мл дихлорметана и объединенные органические экстракты два раза промывали 10 мл фосфатного буфера, а затем сушили и упаривали досуха. Остаток растворяли в 60 мл толуола, охлаждали до 0C и экстрагировали тремя 50-миллилитровыми порциями холодного карбонатного буфера, pH 9,5. Водные экстракты доводили до pH 3 добавлением фосфорной кислоты и экстрагировали пятью 40-миллилитровыми порциями хлороформа, которые затем объединяли, сушили и упаривали досуха. Остаток очищали колоночной хроматографией с использованием 25% этилацетата/гексана, в результате чего получали 1,9 г b-кетоэфира (39%). 17-(1,5-Диметилгексил)-10,13-диметил-2,3,4,7,8,9,10,11,12,13,14,15,16,17-тетрадекагидро-1Hциклопента[a]фенантрен-3-иловый эфир В кипящую смесь b-кетоэфира AE (L,5 г, 2,2 ммоль) и борогидрида натрия (0,226 г, 6 ммоль) в тетрагидрофуране (10 мл) по каплям в течение 1 ч добавляли метанол (2 мл). Перемешивание продолжали при температуре флегмы в течение 1 ч. После охлаждения до комнатной температуры добавляли 1 н. HCl(12,5 мл) и смесь экстрагировали этилацетатом (340 мл). Объединенный этилацетатный слой сушили над безводным сульфатом натрия и концентрировали в вакууме с получением продукта, который очищали колоночной хроматографией (10% MeOH/CHCl3) (89%). Диол AF (1,25 г, 1,994 ммоль) сушили путем выпаривания с пиридином (25 мл) в вакууме. Затем при перемешивании добавляли безводный пиридин (10 мл) и 4,4'-диметокситритилхлорид (0,724 г,2,13 ммоль). Реакцию осуществляли при комнатной температуре в течение ночи. Затем реакцию гасили добавлением метанола. Реакционную смесь концентрировали в вакууме и к остатку добавляли дихлорметан (50 мл). Органический слой промывали 1 М водным раствором бикарбоната натрия. Органический слой сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаточный пиридин удаляли путем выпаривания с толуолом. Неочищенный продукт очищали колоночной хроматографией Соединение AG (1,0 г, 1,05 ммоль) смешивали с ангидридом янтарной кислоты (0,150 г, 1,5 ммоль) и DMAP (0,073 г, 0,6 ммоль), а затем сушили в вакууме при 40C в течение ночи. Смесь растворяли в безводном дихлорэтане (3 мл), добавляли триэтиламин (0,318 г, 0,440 мл, 3,15 ммоль) и раствор перемешивали при комнатной температуре в атмосфере аргона в течение 16 ч. Затем раствор разбавляли дихлорметаном (40 мл) и промывали охлажденной льдом водной лимонной кислотой (5 мас.%, 30 мл) и водой (220 мл). Органическую фазу сушили над безводным сульфатом натрия и концентрировали досуха. Остаток использовали в следующей стадии без очистки. Дериватизированный холестерином CPG AI Сукцинат AH (0,254 г, 0,242 ммоль) растворяли в смеси дихлорметана/ацетонитрила (3:2, 3 мл). К полученному раствору последовательно добавляли DMAP (0,0296 г, 0,242 ммоль) в ацетонитриле(1,25 мл) и 2,2'-дитио-бис-(5-нитропиридин) (0,075 г, 0,242 ммоль) в ацетонитриле/дихлорэтане (3:1,1,25 мл). К полученному раствору добавляли трифенилфосфин (0,064 г, 0,242 ммоль) в ацетонитриле(0,6 мл). Реакционная смесь приобретала ярко-оранжевую окраску. Раствор быстро перемешивали в шарнирном шейкере (5 мин). Затем добавляли длинноцепочечный алкиламин-CPG (LCAA-CPG) (1,5 г,- 19015676 61 мМ). Суспензию перемешивали в течение 2 ч. CPG фильтровали через воронку из спеченного стекла и последовательно промывали ацетонитрилом, дихлорметаном и эфиром. Непрореагировавшие аминогруппы маскировали с использованием ангидрида уксусной кислоты/пиридина. Конечную загрузку CPG определяли по интенсивности УФ-излучения (37 мМ/г). Синтез киРНК, несущих группу бис-дециламида 5'-12-додекановой кислоты (обозначаемую здесь"5'-C32-") или группу 5'-холестерилового производного (обозначаемую здесь "5"-Chol-"), проводили как описано в WO 2004/065601, за исключением того, что в случае холестерилового производного, для введения фосфортиоатной связи у 5'-конца олигомера нуклеиновой кислоты проводили стадию окисления с использованием реагента Бокажа. Последовательности нуклеиновой кислоты представлены ниже в соответствии со стандартной номенклатурой и имеют конкретные аббревиатуры, указанные в табл. 1-1. Таблица 1-1 Аббревиатуры нуклеотидных мономеров, используемых в репрезентативных последовательностях нуклеиновой кислоты. Следует отметить, что эти мономеры, если они присутствуют в олигонуклеотиде, связаны друг с другом 5'-3'-фосфордиэфирными связями. Заглавные буквы означают 2'-дезоксирибонуклеотиды (ДНК),строчные группы означают рибонуклеиды (РНК). Скрининг киРНК PCSK9 в клетках HuH7, HepG2, Hela и в первичных гепатоцитах обезьян выявил в высокой степени активные последовательности. Клетки HuH-7 были получены из банка клеток JCRB (Японская коллекция биологических источников для исследований) (Shinjuku, Japan, cat.JCRB0403). Клетки культивировали в среде MEM Дульбекко (Biochrom AG, Berlin, Germany, cat.F0435), в которую были добавлены 10% фетальная телячья сыворотка (FCS) (Biochrom AG, Berlin, Germany, cat.S0115), 100 ед/мл пенициллина, 100 мкг/мл стрептомицина (Biochrom AG, Berlin, Germany, cat. No, A2213) и 2 мМ L-глутамина (Biochrom AG,Berlin, Germany, cat. No K0282), при 37C в атмосфере с 5% CO2 в инкубаторе с повышенной влажностью(Heraeus HERAcell, Kendro Laboratory Products, Langenselbold, Germany). Клетки HepG2 и клетки Hela получали из Американской коллекции типовых культур (Rockville, Md., cat. No, HB-8065) и культивировали в MEM (Gibco Invitrogen, Karlsruhe, Germany, cat. No, 21090-022), в которую были добавлены 10% фетальная телячья сыворотка (FCS) (Biochrom AG, Berlin, Germany, cat.S0115), 100 ед/мл пенициллина, 100 мкг/мл стрептомицина (Biochrom AG, Berlin, Germany, cat. No, A2213), 1 заменимых аминокислот (Biochrom AG, Berlin, Germany, cat.K-0293) и 1 мМ пирувата натрия (Biochrom AG, Berlin, Germany, cat.L-0473), при 37C в атмосфере с 5% CO2 в инкубаторе с повышенной влажностью (HeraeusHERAcell, Kendro Laboratory Products, Langenselbold, Germany). Для киРНК-трансфекции, клетки HuH7, HepG2 или Hela высевали в 96-луночные планшеты при плотности 2,0104 клеток/лунку и сразу трансфецировали. киРНК-трансфекцию (30 нМ для скрининга одной дозы) осуществляли с использованием липофектамина 2000 (Invitrogen GmbH, Karlsruhe, Germany,cat.11668-019), как описано производителем.- 20015676 Через 24 ч после трансфекции клетки HuH7 и HepG2 подвергали лизису и уровни мРНК PCSK9 оценивали с использованием набора Quantigene Explore Kit (Genosprectra, Dumbarton Circle Fremont,USA, cat.QG-000-02) в соответствии с протоколом. Уровни мРНК PCSK9 нормализовали по мРНКGAP-DH. Для каждой киРНК получали восемь независимых результатов. В качестве контроля использовали киРНК-дуплексы, не являющиеся родственными гену PCSK9. Активность данного PCSK9 специфического киРНК-дуплекса выражали как процент концентрации мРНК PCSK9 в обработанных клетках по отношению к концентрации мРНК PCSK9 в клетках, обработанных контрольным киРНКдуплексом. Первичные гепатоциты собакоподобных обезьян (криоконсервированные) получали от компании InMedium (cat No Z99029) при 37C в атмосфере с 5% CO2 в инкубаторе с повышенной влажностью. Для киРНК-трансфекции первичные клетки собакоподобных обезьян высевали на покрытые коллагеном 96-луночные планшеты (Fisher Scientific, cat.08-774-5) при плотности 3,5104 клеток на лунку и сразу трансфецировали. киРНК-трансфекцию (восемь 2-кратных серийных разведений начиная с 30 нМ) осуществляли в дубликатах с использованием липофектамина 2000 (Invitrogen GmbH, Karlsruhe,Germany, cat.11668-019), как описано производителем. Через 16 ч после трансфекции среду заменяли свежей средой In VitroGRO CP, содержащей смесь антибиотиков Torpedo Antibiotic Mix (In vitro Technologies, Inc, cat. No Z99000). Через 24 ч после замены среды первичные клетки собакоподобных обезьян подвергали лизису и уровни мРНК PCSK9 оценивали с использованием набора Quantigene Explore Kit (Genosprectra, Dumbarton Circle Fremont, USA, cat.QG-000-02) в соответствии с протоколом. Уровни мРНК PCSK9 нормализовали по мРНК GAPDH. Затем нормализованные отношения PCSK9/GAPDH сравнивали с отношениемPCSK9/GAPDH для контрольных клеток, обработанных только липофектамином 2000. В табл. 1, 2 (и на фиг. 6) систематизированы результаты и приводятся примеры in vitro скрининга в различных клеточных линиях при различных дозах. Сайленсинг транскрипта PCSK9 выражали как процент от остального транскрипта, присутствующего в данной дозе. В высокой степени активными последовательностями являются последовательности, в которых присутствовало менее чем 70% остаточного транскрипта после обработки данной киРНК в дозе, равной 100 нМ или менее. Очень активными последовательностями являются последовательности, в которых присутствовало менее чем 60% остаточного транскрипта после обработки данной киРНК в дозе, равной 100 нМ или менее. Активными последовательностями являются последовательности, в которых присутствовало менее чем 85% остаточного транскрипта после обработки высокой дозой (100 нМ). Репрезентативные активные киРНК, полученные в виде липидоидных препаратов, описанных ниже, были также скринированы у мышей in vivo. Последовательности, которые были активными in vitro, также обычно обнаруживали активность in vivo (см., например, фиг. 6). Скрининг in vivo эффективности киРНК PCSK9. Процедура получения препаратов. Для получения наночастиц "липид-киРНК" использовали липидоид LNP-01-4HCl (MW 1487)(фиг. 1), холестерин (Sigma-Aldrich) и ПЭГ-церамид C16 (Avanti Polar Lipids). Были получены маточные этаноловые растворы каждого из следующих компонентов: LNP-01 - 133 мг/мл; холестерина - 25 мг/мл,ПЭГ-церамида C16 - 100 мг/мл. Затем маточные растворы LNP-01, холестерина и ПЭГ-церамида C16 объединяли в молярном отношении 42:48:10. Объединенный липидный раствор быстро смешивали с водной киРНК (в ацетате натрия, pH 5) так, чтобы конечная концентрация этанола составляла 35-45%, а конечная концентрации ацетата натрия составляла 100-300 мМ. Наночастицы "липид-киРНК" спонтанно образовывались после смешивания. В зависимости от нужного распределения частиц по размеру полученную смесь наночастиц в некоторых случаях подвергали экструзии через поликарбонатную мембрану(с отсечкой 100 нМ) на поршневом термоэкструдере (Lipex Extruder, Northern Lipids, Inc). В других случаях стадию экструзии не проводили. Затем этанол удаляли и одновременно проводили замену буфера либо путем диализа, либо путем фильтрации в тангенциальном потоке. Буфер заменяли забуференным фосфатом физиологическим раствором (PBS), pH 7,2. Характеризация препаратов. Препараты, полученные либо стандартным методом, либо неэкструзионным методом, охарактеризовывали аналогичным образом. Препараты сначала охарактеризовывали путем визуального наблюдения. Эти препараты представляли собой беловатые прозрачные растворы, не содержащие агрегированных включений или осадка. Размер частиц и гранулометрический состав липидных наночастиц измеряли по динамическому рассеянию света с использованием Malvern Zetasizer Nano ZS (Malvern, USA). Частицы должны иметь размер 20-300 нм, а в идеальном случае 40-100 нм. Распределение частиц по размеру должно быть унимодальным. Общую концентрацию киРНК в данном препарате, а также наличие иммобилизованной фракции оценивали с помощью анализа на вытеснение метки-красителя. Образец препарата киРНК инкубировали с РНК-связывающим красителем Ribogreen (Molecular Probes) в присутствии или в отсутствие поверхностно-активного вещества, разрушающего препарат, 0,5% тритона-100. Общее- 21015676 количество киРНК в данном препарате определяли по сигналу, передаваемому от образца, содержащего поверхностно-активное вещество, в соответствии со стандартной кривой. Иммобилизованную фракцию определяли путем вычитания содержания "свободной" киРНК (измеренного по сигналу в отсутствие поверхностно-активного вещества) из общего содержания киРНК. Процент иммобилизованной киРНК обычно составляет 85%. Ударная доза. Мышам C57/BL6 (5 мышей на группу, в возрасте 8-10 недель, Charles River Laboratories, MA) в хвостовую вену иглой 27G инъецировали ударную дозу препарата киРНК. киРНК приготавливали в LNP-01(а затем диализовали против PBS) при концентрации 0,5 мг/мл, что позволяло вводить дозу 5 мг/кг в объеме 10 мкл/г массы тела. Перед введением дозы мышей помещали под инфракрасную лампу приблизительно на 3 мин для облегчения инъекции. Через 48 ч после введения дозы мышей умерщвляли путем CO2-асфиксии. Затем из ретроорбитальной области брали 0,2 мл крови, после чего печень собирали и замораживали в жидком азоте. Сыворотку и печень хранили при -80C. Замороженную печень измельчали с использованием холодильника 6850/криогенной мельницы(SPEX CentriPrep, Inc) и порошок хранили при -80C до проведения анализа. Уровни мРНК PCSK9 определяли методом продуцирования разветвленных ДНК с использованием набора, поставляемого QuantiGene Reagent System (Genospectra), в соответствии с протоколом. 10-20 мг порошка замороженной печени подвергали лизису в 600 мкл 0,16 мкг/мл протеиназы K (Epicentre,MPRK092) в растворе для лизиса ткани и клеток (Epicentre, MTC096H) при 65C в течение 3 ч. Затем к 90 мкл рабочего реагента для лизиса добавляли 10 мкл лизатов (1 объем маточной смеси для лизиса в двух объемах воды) и смесь инкубировали при 52C в течение ночи на планшетах для иммобилизацииGenospectra с наборами зондов, специфичных к мышиному PCSK9 и мышиному GAPDH или циклофилину В. Последовательности нуклеиновой кислоты для активатора захвата (CE), активатора метки (LE) и блокирующих (BL) зондов отбирали из последовательностей нуклеиновой кислоты PCSK9, GAPDH и циклофиллина В с помощью компьютерной программы QuantiGene ProbeDesigner 2.0 (Genospectra, Fremont, Calif., USA, cat.QG-002-02). Хемолюминесценцию считывали на устройстве Victor2-Light(Perkin Elmer) в относительных единицах силы света. Отношение мРНК PCSK9 к мРНК GAPDH или циклофилина В в лизатах печени усредняли для каждой группы обработки и сравнивали с отношением для контрольной группы, обработанной PBS, или контрольной группы, обработанной неродственной киРНК (фактора свертывания крови VII). Общий уровень холестерина в сыворотке мышей измеряли с использованием набора StanBio Cholesterol LiquiColor (StanBio Laboratory, Boerne, Tex., USA) в соответствии с инструкциями производителей. Измерения проводили на счетчике Victor2 1420 Multilabel Counter (Perkin Elmer) на 495 нм. Примеры 32 киРНК PCSK9, приготовленных в липосомах LNP-01, тестировали in vivo в мышиной модели. Этот эксперимент проводили при дозе киРНК 5 мг/кг, и по меньшей мере 10 киРНК PCSK9 обнаруживали более чем 40% разрушенной мРНК PCSK9 по сравнению с контрольной группой, обработанной PBS,a контрольная группа, обработанная неродственной киРНК (фактора свертывания крови VII), не обнаруживала какого-либо эффекта (фиг. 2-5). Сайленсинг транскрипта PCSK9 также коррелировал со снижением уровня холестерина у этих животных (фиг. 4-5). Кроме того, между молекулами, которые были активны in vitro и in vivo, наблюдалась значительная корреляция (фиг. 6). Последовательности, содержащие различные химические модификации, также скринировали in vitro (табл. 1 и 2) и in vivo. Так, например, последовательности 9314 и 9318 с меньшим числом модификаций, и варианты последовательностей 9314-(10792, 10793 и 10796); 9318-(10794, 10795, 10797) с большим числом модификаций тестировали invitro (в первичных гепатоцитах обезьян) или in vivo (9314 и 10792) в препарате LNP-01. На фиг. 7 (см. также табл. 1 и 2) показано, что все родительские молекулы 9314 и 9318 и их модифицированные варианты являются активными in vitro. На фиг. 8 в качестве примера показано, что родительская последовательность 9314 и последовательность 10792 с большим числом модификаций являются активными invivo, на что указывает 50-60% сайленсинг эндогенного PCSK9 у мышей. На фиг. 9 также проиллюстрирована активность других химически модифицированных вариантов родительских последовательностей 9314 и 10792. дцРНК-экспрессирующие векторы. В другом аспекте изобретения PCSK9-специфические молекулы дцРНК, которые модулируют активность экспрессии гена PCSK9, экспрессируются от транскрипционных единиц, встроенных в ДНКили РНК-векторы (см., например, Couture, A. et al., TIG. (1996), 12:5-10; Skillern, A., et al., публикацию международной заявки PCT WO 00/22113, Conrad, публикацию международной заявки PCTWO 00/22114, Conrad, и патент США 6054299). Эти трансгены могут быть введены в виде линейной конструкции, кольцевой плазмиды или вирусного вектора, которые могут быть включены в геном хозяина и могут наследоваться как интегрированный трансген. Этот трансген может быть также сконструирован так, чтобы он наследовался как внехромосомная плазмида (Gassmann, et al., Proc. Natl. Acad. Sci. USA(1995), 92:1292). Отдельные цепи дцРНК могут транскрибироваться промоторами на двух отдельных экспрессионных векторах и котрансфецироваться в клетку-мишень. Альтернативно, каждая отдельная цепь дцРНК может транскрибироваться промоторами, которые присутствуют на одной и той же экспрессионной плазмиде. В предпочтительном варианте изобретения дцРНК экспрессируется как инвертированный повтор, связанный посредством линкерной полинуклеотидной последовательности, в результате чего дцРНК имеет структуру типа "стебля" и "петли". Рекомбинантными дцРНК-экспрессирующими векторами обычно являются плазмидные ДНК или вирусные векторы. дцРНК-экспрессирующие вирусные векторы могут быть сконструированы на основе вирусов, таких как, но не ограничивающихся ими, аденоассоциированный вирус (обзор см., например,Muzyczka, et al., Curr. Topics Micro. Immunol. (1992), 158:97-129); аденовирус (см., например, Berkner, etal., BioTechniques (1998), 6:616, Rosenfeld et al. (1991, Science 252:431-434) и Rosenfeld et al. (1992), Cell 68:143-155); или альфавирус, а также другие вирусы, известные специалистам. Ретровирусы были использованы для введения различных генов в различные клетки многих типов, включая эпителиальные клетки in vitro или in vivo (см., например, Eglitis, et al., Science (1985), 230:1395-1398; Danos and Mulligan,Proc. Natl. Acad. Sci. USA (1998), 85:6460-6464; Wilson et al., 1988, Proc. Natl. Acad. Sci. USA 85:30143018; Armentano et al., 1990, Proc. Natl. Acad. Sci. USA. 87:61416145; Huber et al., 1991, Proc. Natl. Acad.WO 89/07136; заявку PCT WO 89/02468; заявку PCT WO 89/05345 и заявку PCT WO 92/07573). Рекомбинантные ретровирусные векторы, способные переносить и экспрессировать гены, встроенные в геном клетки, могут быть продуцированы путем трансфекции рекомбинантного ретровирусного генома в подходящие упаковывающие клеточные линии, такие как РА 317 и Psi-CRIP (Comette et al., 1991, HumanGene Therapy 2:5-10; Cone et al., 1984, Proc. Natl. Acad. Sci, USA 81:6349). Рекомбинантные аденовирусные векторы могут быть использованы для инфицирования клеток и тканей широкого ряда у восприимчивых хозяев (например, крыс, хомячков, собак и шимпанзе) (Hsu et al., 1992. J. Infectious Disease,166:769), а также они имеют то преимущество, что для их инфицирования не требуются митотически активные клетки. Промотором, регулирующим экспрессию дцРНК в плазмидной ДНК или в вирусном векторе согласно изобретению, может быть промотор гена эукариотической РНК-полимеразы I (например, промотор рибосомной РНК), промотор РНК-полимеразы II (например, ранний промотор CMV или промотор актина или промотор мяРНК U1) или обычно промотор РНК-полимеразы III (например, промотор мяРНКU6 или РНК 7SK) или прокариотический промотор, например промотор T7, при условии, что экспрессионная плазмида также кодирует РНК-полимеразу T7, необходимую для транскрипции с промотора T7. Промотор может также направлять экспрессию трансгена в поджелудочную железу (например, последовательность, регулирующая поступление инсулина в поджелудочную железу (Bucchim et al., 1986, Proc.Natl. Acad. Sci. USA 83:2511-2515. Кроме того, экспрессия трансгена может соответствующим образом регулироваться, например, с использованием индуцибельной регуляторной последовательности и экспрессионных систем, таких как регуляторная последовательность, восприимчивая к некоторым физиологическим регуляторам, например уровням глюкозы в крови или гормонам (Docherty et al., 1994, FASEB J. 8:20-24). Такими индуцибельными экспрессионными системами, подходящими для регуляции экспрессии трансгенов в клетках или у млекопитающих, являются системы регуляции под действием экдизонов, эстрогена, прогестерона, тетрациклина, химических индукторов димеризации и изопропил-бета-D1-тиогалактопиранозида (EPTG). Специалист в данной области может самостоятельно выбрать соответствующую регуляторную/промоторную последовательность в зависимости от целей использования дцРНК-трансгена. Обычно доставку рекомбинантных векторов, способных экспрессировать молекулы дцРНК, осуществляют, как описано ниже, и после этого они интегрируются в клетках-мишенях. Альтернативно, могут быть использованы вирусные векторы, обеспечивающие временную экспрессию молекул дцРНК. Такие векторы, при необходимости, могут быть введены повторно. После экспрессии дцРНК связываются с РНК-мишенью и модулируют ее функцию или экспрессиию. Доставка дцРНК-экспрессирующих векторов может быть системной, например, она может быть осуществлена путем внутривенного или внутримышечного введения, или путем введения в клетки-мишени, эксплантированные у пациента, с последующим введением этих клеток снова пациенту, или любыми другими методами, позволяющими осуществлять введение в нужные клетки-мишени. дцРНК-экспрессирующие ДНК-плазмиды обычно трансфецируют в клетки-мишени в виде комплекса с катионными липидными носителями (например, олигофектамином) или с некатионными липидными носителями (например, Transit-TKO). В настоящем изобретении также рассматриваются множественные липидные трансфекции для дцРНК-опосредуемого подавления различных областеймишеней одного гена PCSK9 или множества генов PCSK9 в течение одной недели или более. Успешное- 23015676 введение векторов согласно изобретению в клетки-хозяева может быть оценено различными известными методами. Так, например, временная трансфекция может быть выявлена по сигналу репортера, такого как флуоресцентный маркер, например белок, флуоресцирующий в зеленом диапазоне спектра (GFP). Стабильная трансфекция клеток ex vivo может быть обеспечена с использованием маркеров, которые сообщают трансфецированным клеткам резистентность к конкретным внешним факторам (например, к антибиотикам и лекарственным средствам), такую как резистентность к гигромицину В.PCSK9-специфические молекулы дцРНК могут быть также встроены в векторы и использованы в качестве векторов, применяемых в генотерапии для лечения человека. Векторы для генотерапии могут быть доставлены индивидууму, например, путем внутривенной инъекции, местного введения (см. патент США 5328470) или стереотаксической инъекции (см., например, Chen et al. (1994), Proc. Natl. Acad.Sci. USA 91:3054-3057). Фармацевтический препарат векторов, применяемый в генотерапии, может включать вектор для генотерапии в приемлемом разбавителе, либо он может содержать матрицу с пролонгированным высвобождением, в которую может быть введен носитель для доставки генов. Альтернативно, если вектор для доставки полноразмерного гена, например ретровирусный вектор, может быть получен в интактной форме из рекомбинантных клеток, то такой фармацевтический препарат может включать одну или несколько клеток, продуцирующих систему доставки гена. Специалистам в данной области очевидно, что помимо методов и композиций, конкретно описанных в настоящем изобретении, существуют и другие методы и композиции, которые могут быть применены для осуществления настоящего изобретения, полный объем которого определен в прилагаемой формуле изобретения. Таблица 1
МПК / Метки
МПК: A61K 31/07, A01N 43/04, C07H 21/04, C12Q 1/68
Метки: экспрессии, pcsk9, способы, гена, ингибирования, композиции
Код ссылки
<a href="https://eas.patents.su/30-15676-kompozicii-i-sposoby-ingibirovaniya-ekspressii-gena-pcsk9.html" rel="bookmark" title="База патентов Евразийского Союза">Композиции и способы ингибирования экспрессии гена pcsk9</a>
Предыдущий патент: Производные циклогексилпиразол-лактама в качестве ингибиторов 11-бета-гидроксистероиддегидрогеназы 1
Следующий патент: Соли и кристаллические формы 2-метил-2-[4-(3-метил-2-оксо-8-хинолин-3-ил-2,3-дигидроимидазо[4,5-c]хинолин-1-ил)фенил]пропионитрила
Случайный патент: Способ защиты финансовых транзакций