Пиримидиниламидные соединения (варианты), включающая их фармацевтическая композиция и способ лечения заболевания, опосредованного a4-интегринами
Номер патента: 15388
Опубликовано: 31.08.2011
Авторы: Фукуда Джури И., Сюй Ин-Цзы, Росситер Кассандра Инес, Конрэди Андрей В., Смит Дженифер Ли, Сэмкоу Кристофер Майкл, Стэпэнбэк Фрэнк
Формула / Реферат
1. Пиримидиниламидные соединения общей формулы I
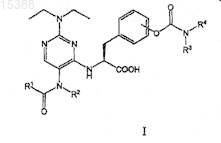
где R1выбран из группы, включающей C1-C4-алкил, C1-C4-галогеналкил, гетероарил- и -NR5R6, где R5и R6 независимо выбраны из группы, включающей водород и C1-C4-алкил, или R5 и R6совместно с атомом азота, с которым они связаны, формируют гетероцикл;
R2 представляет собой C1-C4-алкил;
R3 и R4совместно с атомом азота, с которым они связаны, образуют гетероцикл;
или их фармацевтически приемлемые соли или сложные эфиры.
2. Соединения по п.1, у которых группа -OC(O)NR3R4находится в пара-положении фенильного цикла.
3. Соединения по п.2, у которых R3 и R4совместно с атомом азота, с которым они связаны, образуют пирролидинил.
4. Соединения по п.3, у которых R2 представляет собой этил.
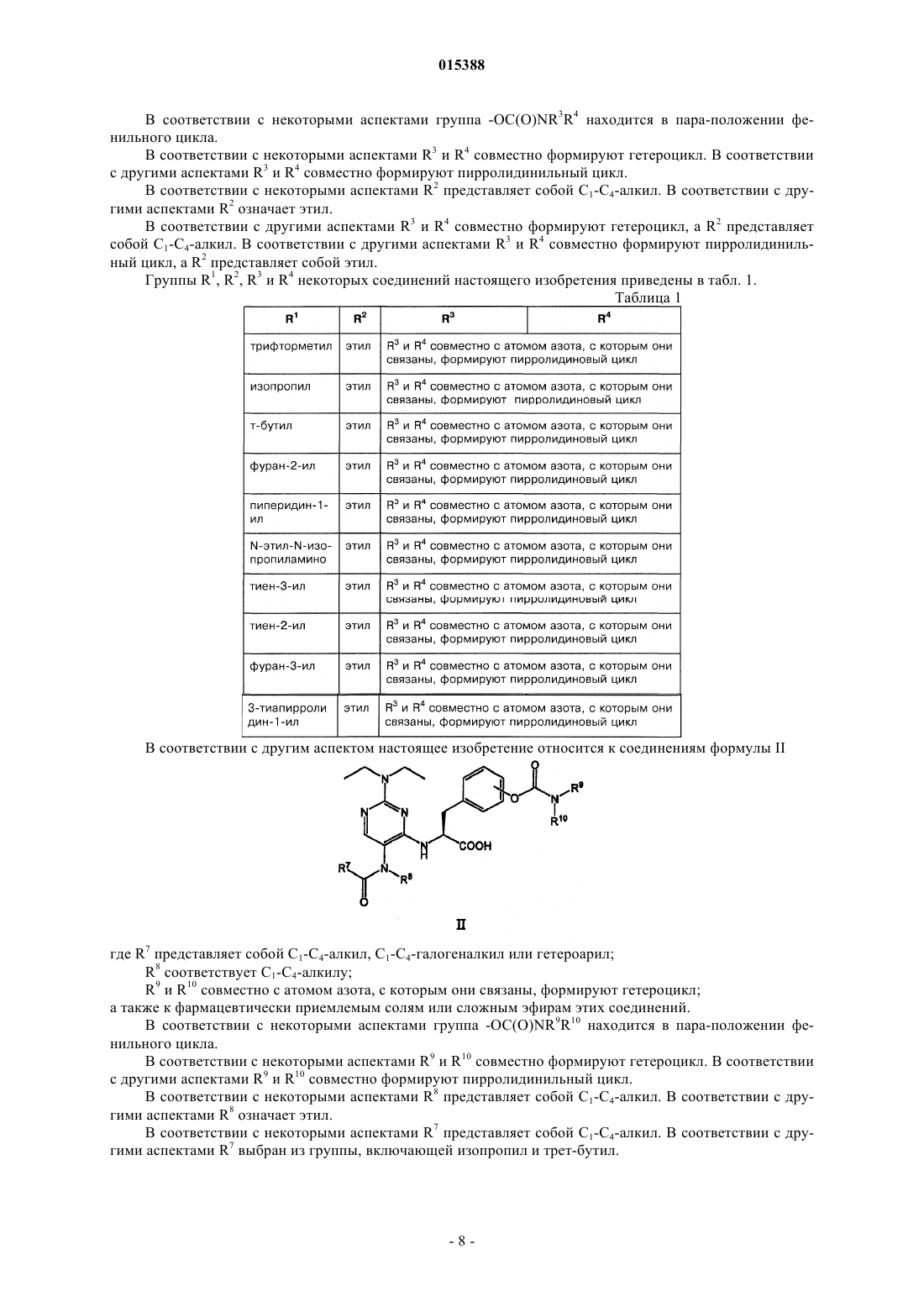
5. Пиримидиниламидные соединения общей формулы II
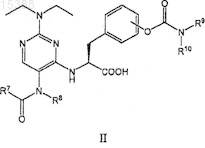
где R7выбран из группы, включающей C1-C4-алкил, C1-C4-галогеналкил и гетероарил;
R8 представляет собой C1-C4-алкил;
R9 и R10 совместно с атомом азота, с которым они связаны, образуют гетероцикл;
или их фармацевтически приемлемые соли или сложные эфиры.
6. Соединения по п.5, у которых группа -OC(O)NR9R10 находится в пара-положении фенильного цикла.
7. Соединения по п.6, у которых R9 и R10 совместно с атомом азота, с которым они связаны, образуют пирролидинил.
8. Соединения по п.7, у которых R8 представляет собой этил.
9. Соединения по п.8, у которых R7 представляет собой C1-C4-алкил.
10. Соединения по п.9, у которых R7 выбран из группы, включающей изопропил и трет-бутил.
11. Соединения по п.8, у которых R7 представляет собой C1-C4-галогеналкил.
12. Соединения по п.11, у которых R7 представляет собой трифторметил.
13. Соединения по п.8, у которых R7 представляет собой гетероарил.
14. Соединения по п.13, у которых R7 выбран из группы, включающей фуран-2-ил, фуран-3-ил, тиен-2-ил и тиен-3-ил.
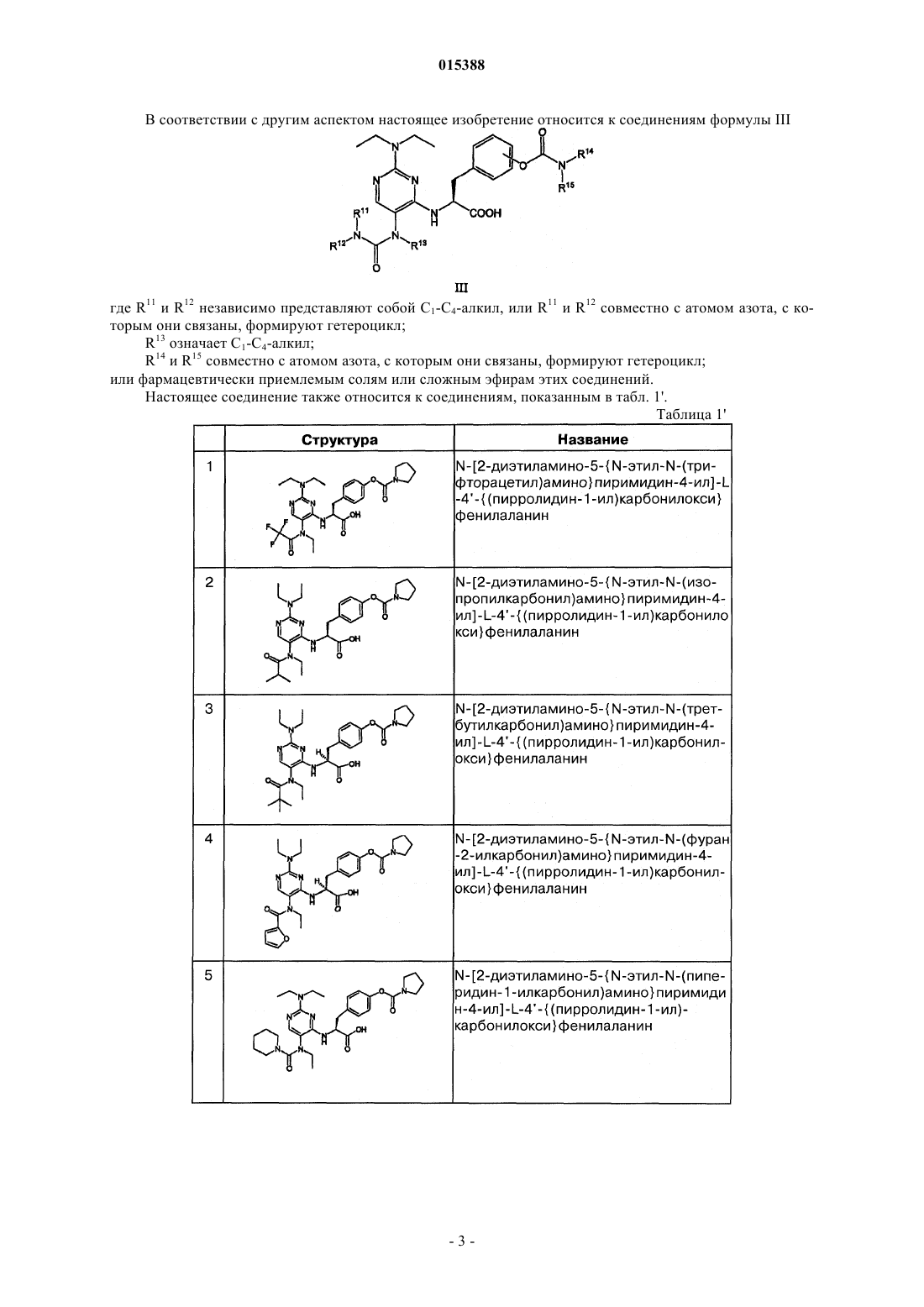
15. Пиримидиниламидные соединения общей формулы III
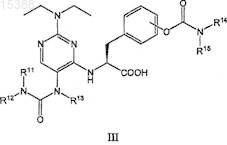
где R11 и R12 независимо представляют собой C1-C4-алкил или R11 и R12 совместно с атомом азота, с которым они связаны, образуют гетероцикл;
R13 представляет собой C1-C4-алкил;
R14 и R15 совместно с атомом азота, с которым они связаны, образуют гетероцикл;
или их фармацевтически приемлемые соли или сложные эфиры.
16. Соединения по п.15, у которых группа -OC(O)NR14R15 находится в пара-положении фенильного цикла.
17. Соединения по п.16, у которых R14 и R15 совместно с атомом азота, с которым они связаны, образуют пирролидинил.
18. Соединения по п.17, у которых R13 представляет собой этил.
19. Соединения по п.18, у которых R11 и R12 независимо представляют собой C1-C4-алкил.
20. Соединения по п.19, у которых R11 представляет собой этил, a R12 - изопропил.
21. Соединения по п.18, у которых R11 и R12 совместно с атомом азота, с которым они связаны, образуют гетероцикл.
22. Соединения по п.21, у которых указанный гетероцикл выбран из группы, включающей пиперидин-1-ил и 3-тиапирролидин-1-ил.
23. Пиримидиниламидные соединения, представляющие собой соединения, выбранные из группы, включающей
N-[2-диэтиламино-5-{N-этил-N-(трифторацетил)амино}пиримидин-4-ил]-L-4'-{(пирролидин-1-ил)карбонилокси}фенилаланин;
N-[2-диэтиламино-5-{N-этил-N-(изопропилкарбонил)амино}пиримидин-4-ил]-L-4'-{(пирролидин-1-ил)карбонилокси}фенилаланин;
N-[2-диэтиламино-5-{N-этил-N-(трет-бутилкарбонил)амино}пиримидин-4-ил]-L-4'-{(пирролидин-1-ил)карбонилокси}фенилаланин;
N-[2-диэтиламино-5-{N-этил-N-(фуран-2-илкарбонил)амино}пиримидин-4-ил]-L-4'-{(пирролидин-1-ил)карбонилокси}фенилаланин;
N-[2-диэтиламино-5-{N-этил-N-(пиперидин-1-илкарбонил)амино}пиримидин-4-ил]-L-4'-{(пирролидин-1-ил)карбонилокси}фенилаланин;
N-[2-диэтиламино-5-{N-этил-N-(N-этил-N-изопропиламинокарбонил)амино}пиримидин-4-ил]-L-4'-{(пирролидин-1-ил)карбонилокси}фенилаланин;
N-[2-диэтиламино-5-{N-этил-N-(тиен-3-илкарбонил)амино}пиримидин-4-ил]-L-4'-{(пирролидин-1-ил)карбонилокси}фенилаланин;
N-[2-диэтиламино-5-{N-этил-N-(тиен-2-илкарбонил)амино}пиримидин-4-ил]-L-4'-{(пирролидин-1-ил)карбонилокси}фенилаланин;
N-[2-диэтиламино-5-{N-этил-N-(фуран-3-илкарбонил)амино}пиримидин-4-ил]-L-4'-{(пирролидин-1-ил)карбонилокси}фенилаланин;
N-[2-диэтиламино-5-{N-этил-N-(3-тиапирролидин-1-илкарбонил)амино}пиримидин-4-ил]-L-4'-{(пирролидин-1-ил)карбонилокси}фенилаланин;
N-[2-диэтиламино-5-{N-этил-N-(тиен-2-илкарбонил)амино}пиримидин-4-ил]-L-4'-{(пирролидин-1-ил)карбонилокси}фенилаланина трет-бутиловый эфир;
N-[2-диэтиламино-5-{N-этил-N-(трифторметилкарбонил)амино}пиримидин-4-ил]-L-4'-{(пирролидин-1-ил)карбонилокси}фенилаланина трет-бутиловый эфир;
N-[2-диэтиламино-5-{N-этил-N-(трет-бутилкарбонил)амино}пиримидин-4-ил]-L-4'-{(пирролидин-1-ил)карбонилокси}фенилаланина трет-бутиловый эфир и
N-[2-диэтиламино-5-{N-этил-N-(фуран-3-илкарбонил)амино}пиримидин-4-ил]-L-4'-{(пирролидин-1-ил)карбонилокси}фенилаланина трет-бутиловый эфир,
или их фармацевтически приемлемые соли или сложные эфиры.
24. Фармацевтическая композиция, включающая фармацевтически приемлемый носитель и терапевтически эффективное количество по меньшей мере одного соединения по пп.1-23.
25. Способ лечения заболевания у людей или животных, опосредованного a4-интегринами, который включает введение человеку или животному фармацевтической композиции по п.24.
26. Способ по п.25, в котором a4-интегрины представляют собой VLA-4.
27. Способ по п.25, в котором указанное заболевание выбрано из группы, включающей астму, болезнь Альцгеймера, атеросклероз, вызванную СПИДом деменцию, диабет, острый ювенильный приступ диабета, воспалительное заболевание кишечника, язвенные колиты, болезнь Крона, рассеянный склероз, артрит, ревматоидный артрит, последствия трансплантации тканей, метастазы опухолей, менингит, энцефалит, инсульт, травмы мозга, нефрит, ретинит, атопический дерматит, псориаз, миокардиальная ишемия, острое опосредованное лейкоцитами повреждение легких и синдром дыхательной недостаточности у взрослых.
28. Способ по п.25, в котором указанное заболевание представляет собой воспалительное заболевание.
29. Способ по п.28, в котором воспалительное заболевание выбрано из группы, включающей узловатую эритему, аллергические конъюктивиты, оптический неврит, увеит, аллергический ринит, анкилозирующий спондилоартрит, псориатический артрит, васкулит, синдром Рейтера, системную красную волчанку, прогрессирующий системный склероз, полимиозит, дерматомиозит, грануломатоз Вегнера, аортит, саркоидоз, лимфоцитопению, темпоральный артериит, перикардит, миокардит, застойную сердечную недостаточность, узловатый полиартериит, синдромы гиперчувствительности, аллергию, синдромы гиперэозинофилии, синдром Чурга-Страусса, хроническое обструктивное заболевание легких, пневмониты с гиперчувствительностью, хронический активный гепатит, интерстициальный цистит, аутоиммунную эндокринную недостаточность, первичный цирроз желчного пузыря, аутоиммунную апластическую анемию, стойкий хронический гепатит и тироидит.
Текст
ПИРИМИДИНИЛАМИДНЫЕ СОЕДИНЕНИЯ (ВАРИАНТЫ), ВКЛЮЧАЮЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЯ,ОПОСРЕДОВАННОГО 4-ИНТЕГРИНАМИ Настоящее изобретение относится к соединениям, которые связывают VLA-4. Некоторые из этих соединений ингибируют также адгезию лейкоцитов, в частности адгезию лейкоцитов, опосредованнуюVLA-4. Такие соединения можно использовать для лечения воспалительных заболеваний у человека и животных, опосредованных 4-интегринами, таких как астма, болезнь Альцгеймера, атеросклероз,вызванная СПИДом деменция, диабет, воспалительное заболевание кишечника, ревматоидный артрит,последствия трансплантации тканей, метастазы опухолей и миокардиальная ишемия. Соединения могут назначаться также для лечения воспалительных заболеваний мозга, например рассеянного склероза 015388 Область техники, к которой относится изобретение Настоящее изобретение относится к соединениям, ингибирующим адгезию лейкоцитов, в частности адгезию лейкоцитов, опосредованную 4-интегринами, где 4-интегрин предпочтительно представляет собой VLA-4. Настоящее изобретение относится также к фармацевтическим композициям, содержащим вышеуказанные соединения, а также к способам лечения, например, воспалительных заболеваний, в которых используются соединения или фармацевтические композиции настоящего изобретения. Сведения о предшествующем уровне техники Следующие публикации указаны в настоящем патенте надстрочным индексом. 1. Hemler and Takada, European Patent Application Publication No. 330506, опубликована 30 августа,1989. 2. Elices, et al., Cell, 60:577, 584 (1990). 3. Springer, Nature, 346:425, 434 (1990). 4. Osborn, Cell, 62:3, 6 (1990). 5. Vedder, et al., Surgery, 106:509 (1989). 6. Pretolani, et al., J. Exp. Med., 180:795 (1994). 7. Abraham, et al., J. Clin. Invest., 93:776 (1994). 8. Mulligan, et al., J. Immunology, 150:2407 (1993). 9. Cybulsky, et al., Science, 251:788 (1991). 10. Li, et al., Arterioscler. Thromb., 13:197 (1993). 11. Sasseville, et al., Am. J. Path., 144:27 (1994). 12. Yang, et al., Proc. Nat. Acad. Science (USA), 90: 10494 (1993). 13. Burldy, et al., Diabetes, 43:529 (1994). 14. Baron, et al., J. Clin. Invest, 93:1700 (1994). 15. Hamann, et al., J. Immunology, 152:3238 (1994). 16. Yednock, et al., Nature, 356:63 (1992). 17. Baron, et al., J. Exp. Med., 177:57 (1993). 18. van Dinther-Janssen, et al., J. Immunology, 147:4207 (1991). 19. van Dinther-Janssen, et al., Annals. Rheumatic Dis., 52:672 (1993). 20. Elices, et al., J. Clin. Invest, 93:405 (1994). 21. Postigo, et al., J. Clin. Invest., 89:1445 (1991). 22. Paul, et al., Transpl. Proceed., 25:813 (1993). 23. Okarhara, et al., Can. Res., 54:3233 (1994). 24. Paavonen, et al., Int. J. Can., 58:298 (1994). 25. Schadendorf, et al., J. Path., 170:429 (1993). 26. Bao, et al., Diff., 52:239 (1993). 27. Lauri, et al., British J. Cancer, 68:862 (1993). 28. Kawaguchi, et al., Japanese J. Cancer Res., 83:1304 (1992). 29. Konradi, et al., PCT/US00/01686, filed, January 21, 2000. Все вышеуказанные публикации включены в данный текст описания по ссылке по всей своей полноте, как если бы о каждой из них в отдельности было сказано, что она включена по ссылке по всей своей полноте.VLA-4 (также называемый 41-интегрином и CD49d/CD29) был впервые упомянут в работеHemler and Takada1, он представлен в составе семейства 1-интегринов рецепторов клеточной поверхности, каждый из членов которого содержит две субъединицы, называемые -цепь и -цепь. VLA-4 содержит 4- и 1-цепи. Существует по меньшей мере девять 1-интегринов, у всех из них одинаковая 1 цепь и разные -цепи. Эти девять рецепторов связывают различные комплементы разнообразных молекул матрикса клетки, такие как фибронектин, ламинин и коллаген. Например, VLA-4 связывает фибронектин. Кроме того, VLA-4 связывает молекулы, не входящие в матрикс, которые экспрессируются в эндотелиальных и других клетках. Эти нематриксные молекулы включают VCAM-1, который экспрессируется в цитокин-активируемых эндотелиальных клетках пупочной вены в культуре. За связывание с фибронектином и VCAM-1 отвечают различные эпитопы VLA-4, при этом показано, что каждый вид связывания ингибируется независимо 2. Внутриклеточная адгезия, опосредованная VLA-4 и другими рецепторами клеточной поверхности,связана с разнообразными воспалительными ответами. В месте повреждения или действия других воспалительных стимулов активированные эндотелиальные клетки кровеносных сосудов экспрессируют молекулы, которые являются адгезивными для лейкоцитов. Механизм адгезии лейкоцитов к эндотелиальным клеткам включает, помимо прочего, узнавание и связывание рецепторов клеточной поверхности лейкоцитов с соответствующими молекулами клеточной поверхности эндотелиальных клеток. После связывания лейкоциты проходят через стенку кровеносного сосуда и попадают в область повреждения,где выделяют химические медиаторы, противодействующие инфекции. Обзоры рецепторов адгезии иммунной системы содержатся, например, в работах Springer3 и Osborn4.-1 015388 Такие воспалительные заболевания мозга, как экспериментальный аллергический энцефаломиелит(ЭАЭ), рассеянный склероз (PC) и менингит, являются примерами расстройств центральной нервной системы, при которых адгезия лейкоцитов к эндотелию приводит к разрушению в остальном здоровой ткани мозга. У субъектов, страдающих такими воспалительными заболеваниями, через гематоэнцефалический барьер (ГЭБ) проходит большое количество лейкоцитов. Эти лейкоциты выделяют токсические медиаторы, вызывающие значительные повреждения тканей, приводящие к нарушению нервной проводимости и параличу. В других системах органов повреждения тканей также происходят посредством адгезии, приводящей к миграции или активации лейкоцитов. Например, показано, что первичный инсульт, сопровождающий миокардиальную ишемию ткани сердца, может осложняться миграцией лейкоцитов в поврежденную ткань, что вызывает вторичный инсульт (Vedder, et al.)5. Другие воспалительные или патологические состояния, опосредованные механизмом адгезии, включают, например, астму 6-8, болезнь Альцгеймера, атеросклероз 9-10, вызванную СПИДом деменцию 1, диабет 12-14 (включая острый ювенильный приступ диабета), воспалительное заболевание кишечника 15 (включая язвенные колиты и болезнь Крона), рассеянный склероз 16-17, ревматоидный артрит 18-21, последствия трансплантации тканей 22, метастазы опухолей 23"28, менингит, энцефалит, инсульт и другие повреждения мозга, нефриты, ретиниты, атопический дерматит, псориаз, миокардиальную ишемию и острое опосредованное лейкоцитами повреждение легких, такое как бывает при синдроме дыхательной недостаточности у взрослых. Известно, что замещенные аминопиримидины, как класс, ингибируют связывание VLA-4 с VCAM1 и соответственно демонстрируют противовоспалительные свойства 29. Хотя эти соединения и являются антагонистами подобного связывания, улучшение их биодоступности повысило бы их эффективность еще больше. Сущность изобретения Настоящее изобретение относится к соединениям, их фармацевтически приемлемым солям, их композициям, способам их получения и способам лечения заболеваний, опосредованных VLA-4. В соответствии с одним аспектом настоящее изобретение относится к соединениям формулы I где R1 выбран из группы, включающей C1-C4-алкил, C1-C4-галогеналкил, гетероарил и -N(R5)(R6), где R5 и R6 независимо выбраны из группы, включающей водород, C1-C4-алкил, или R5 и R6 совместно с атомом азота, с которым они связаны, формируют гетероцикл;R3 и R4 совместно с атомом азота, с которым они связаны, формируют гетероцикл; или фармацевтически приемлемым солям или сложным эфирам этих соединений. В соответствии с другим аспектом настоящее изобретение относится к соединениям формулы IIR9 и R10 совместно с атомом азота, с которым они связаны, формируют гетероцикл; или фармацевтически приемлемым солям или сложным эфирам этих соединений.-2 015388 В соответствии с другим аспектом настоящее изобретение относится к соединениям формулы III где R11 и R12 независимо представляют собой C1-C4-алкил, или R11 и R12 совместно с атомом азота, с которым они связаны, формируют гетероцикл;R14 и R15 совместно с атомом азота, с которым они связаны, формируют гетероцикл; или фармацевтически приемлемым солям или сложным эфирам этих соединений. Настоящее соединение также относится к соединениям, показанным в табл. 1'. Таблица 1' Сведения, подтверждающие возможность осуществления изобретения Как уже упоминалось, настоящее изобретение относится к соединениям, ингибирующим адгезию лейкоцитов, в частности адгезию лейкоцитов, по меньшей мере, частично опосредованную 4 интегринами, предпочтительно VLA-4. Однако прежде чем приступить к более подробному описанию настоящего изобретения, необходимо дать определение следующим терминам. Определения. Если не указано иначе, следующие термины, встречающиеся в тексте настоящего описания и формуле изобретения, соответствуют приведенным ниже значениям. В соответствии с настоящим изобретением, если не указано иначе, термин "алкил" означает прямые, разветвленные и циклические алкильные группы, содержащие от 1 до 4 атомов углерода, более предпочтительно от 1 до 3 атомов углерода. В качестве примеров подобных групп можно привести метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, циклопропил, циклобутил и метилен-циклопропил. Термин "алкенил" означает прямые и разветвленные алкенильные группы, содержащие от 2 до 4 атомов углерода, предпочтительно от 2 до 3 атомов углерода, а также по меньшей мере один, предпочтительно один, сайт алкенильной ненасыщенности. Примеры алкенильных групп включают винил(-СН=СН 2), аллил (-СН 2 СН=СН 2), н-пропен-1-ил (-СН=СНСН 3), н-бутен-2-ил (-СН 2 СН=СНСН 3) и подобные им. Термин охватывает цис- и транс-изомеры, а также смеси этих изомеров. Термин "алкинил" означает прямые и разветвленные алкинильные группы, содержащие от 2 до 4 атомов углерода, предпочтительно от 2 до 3 атомов углерода, а также по меньшей мере один, предпочтительно один, сайт алкинильной ненасыщенности. Примеры таких алкинильных групп включают ацетиленил (-ССН), пропаргил (-CH2CCH), н-пропин-1-ил (-СНСНСН 3) и подобные им. Термин "арил" или "Ar" означает одновалентную ароматическую карбоциклическую группу из 6-14 атомов углерода, содержащую один цикл (например, фенил) или несколько конденсированных циклов (например, нафтил или антрил), при этом конденсированные циклы могут быть ароматическими (например, 2-бензоксазолин, 2 Н-1,4-бензоксазин-3(4 Н)-он-7-ил и подобные им), причем точка прикрепления этой группы представляет собой ароматический атом углерода. Предпочтительные арилы включают фенил и нафтил.-5 015388 Термир "замещенный арил" означает арильные группы, содержащие от 1 до 3 заместителей, предпочтительно от 1 до 2 заместителей, выбранных из группы, включающей гидроксил, ацил, ациламино,ацилокси, алкил, замещенный алкил, алкокси, замещенный алкокси, алкенил, замещенный алкенил, алкинил, замещенный алкинил, амино, замещенный амино, аминоацил, арил, замещенный арил, арилокси,замещенный арилокси, карбоксил, карбоксильный сложные эфиры, циано, тиол, тиоалкил, замещенный тиоалкил, тиоарил, замещенный тиоарил, тиогетероарил, замещенный тиогетероарил, тиоциклоалкил,замещенный тиоциклоалкил, тиогетероциклил, замещенный тиогетероциклил, циклоалкил, замещенный циклоалкил, галоген, нитро, гетероарил, замещенный гетероарил, гетероциклил, замещенный гетероциклил, гетероарилокси, замещенный гетероарилокси, гетероциклилокси, замещенный гетероциклилокси,амино-сульфонил- (NH2-SO2-) и замещенный аминосульфонил. Термины "гало" или "галоген" означают фтор, хлор, бром и йод, предпочтительно либо фтор, либо хлор. Термин "галогеналкил" означает алкильные группы, содержащие от 1 до 5 галогрупп. Предпочтительно, чтобы такие группы содержали от 1 до 3 галогрупп и от 1 до 2 атомов углерода. Особо предпочтительные галогеналкильные группы включают тригалогенметил (например, трифторметил) и тригалогенэтил (например, 2,2,2-трифторэт-1-ил). Термин "гетероарил" означает ароматическую карбоциклическую группу, содержащую в цикле от 2 до 10 атомов углерода и от 1 до 4 гетероатомов, выбранных из числа кислорода, азота и серы. Такие гетероарильные группы могут содержать один цикл (например, пиридил или фурил) или несколько конденсированных циклов, причем каждый конденсированный цикл может быть арилом или гетероарилом. Примеры подобных гетероарилов включают, например, фуран-2-ил, фуран-3-ил, тиен-2-ил, тиен-3-ил,пиррол-2-ил, пиррол-3-ил, пиридил (2-, 3- и 4-пиридилы) и подобные им. В соответствии с одним аспектом атомы серы и/или азота гетероарила могут быть окислены (т.е. находиться в форме -S(O)-, или-S(O)2-, и/или N-оксидов). Термин "гетероцикл" или "гетероциклический" означает насыщенную или ненасыщенную негетероароматическую группу, содержащую один цикл или несколько конденсированных циклов, от 1 до 10 атомов углерода и от 1 до 4 гетероатомов в цикле, выбранных из числа азота, серы или кислорода,причем, в случае конденсированной системы, один или несколько циклов могут представлять собой арил или гетероарил. В соответствии с одним аспектом атомы серы и/или азота гетероцикла могут быть окислены (т.е. находиться в форме -S(O)-, или -S(O)2-, и/или N-оксидов). Термин "фармацевтически приемлемый носитель" означает носитель, пригодный для приготовления фармацевтической композиции, в целом безопасный, нетоксичный и не проявляющий биологических или других нежелательных свойств. Такие носители включают применимые в ветеринарии или при лечении людей. При использовании в настоящем описании или формуле изобретения термин "фармацевтически приемлемый носитель" включает как один, так и несколько таких носителей. Термин "фармацевтически приемлемая соль" относится к солям, сохраняющим биологическую эффективность и свойства соединений настоящего изобретения и не проявляющим биологических или иных нежелательных свойств. Часто соединения настоящего изобретения могут образовывать кислые и/или основные соли в присутствии амино- и/или карбоксильных групп или подобных им. Фармацевтически приемлемые соли присоединения оснований готовят из неорганических и органических оснований. К первой категории относятся, например, натриевые, калиевые, литиевые, аммонийные, кальциевые и магниевые соли. Примеры солей, полученных с участием органических оснований, включают, но не ограничиваются, соли первичных, вторичных и третичных аминов, такие как алкиламины, диалкиламины, триалкиламины, замещенные алкиламины, ди(замещенные алкил)амины,три(замещенные алкил)амины, алкениламины, диалкениламины, триалкениламины, замещенные алкениламины, ди(замещенные алкенил)амины, три(замещенные алкенил)амины, циклоалкиламины,ди(циклоалкил)амины, три(циклоалкил)амины, замещенные циклоалкиламины, дизамещенные циклоалкиламины,тризамещенные циклоалкиламины,циклоалкениламины,ди(циклоалкенил)амины,три(циклоалкенил)амины, замещенные циклоалкениламины, дизамещенные циклоалкениламины, тризамещенные циклоалкениламины, ариламины, диариламины, триариламины, гетероариламины, дигетероариламины, тригетероариламины, гетероциклиламины, дигетероциклиламины, тригетероциклиламины,смешанные ди- и триамины, где по меньшей мере два заместителя на амине отличаются друг от друга и выбраны из группы, включающей алкил, замещенный алкил, алкенил, замещенный алкенил, циклоалкил,замещенный циклоалкил, циклоалкенил, замещенный циклоалкенил, арил, гетероарил, гетероциклил и подобные им. К указанной категории относятся также амины, два или три заместителя которых совместно с атомом азота амина формируют гетероциклильную или гетероарильную группу. К числу подходящих аминов относятся, например, изопропиламин, триметиламин, диэтиламин,три(изопропил)амин, три(н-пропил)амин, этаноламин, 2-диметиламиноэтанол, трометамин, лизин, аргинин, гистидин, кафеин, прокаин, гидрабамин, холин, бетаин, этилендиамин, глюкозамин, Nалкилглюкамины, теобромин, пурины, пиперазин, пиперидин, морфолин, N-этилпиперидин и подобные им. Следует также понимать, что в практике настоящего изобретения могут быть пригодны другие производные карбоновых кислот, например амиды карбоновых кислот, включая карбоксамиды, низшие ал-6 015388 килкарбоксамиды, диалкилкарбоксамиды и подобные им. Фармацевтически приемлемые соли присоединения кислот можно получить из неорганических и органических кислот. К первой категории относятся соли соляной, бромоводородной, серной, азотной,фосфорной кислот и подобные им. Соли органических кислот включают соли уксусной, пропионовой,гликолевой, пировиноградной, щавелевой, яблочной, малоновой, янтарной, малеиновой, фумаровой, винной, лимонной, бензойной, циннамовой, манделовой, метансульфоновой, этансульфоновой, паратолуолсульфоновой, салициловой кислоты и подобных им. Термин "фармацевтически приемлемый катион" означает катион фармацевтически приемлемой соли. Следует понимать, что для всех описанных здесь заместителей в объем настоящего изобретения не входят полимеры, полученные при определении заместителей, содержащих другие заместители, которые также содержат другие заместители (например, замещенный арил с замещенным арилом в качестве заместителя, который также содержит замещенную арильную группу и т.д.). Максимальное количество подобных заместителей составляет три. Это накладывает ограничение на каждое приведенное выше определение. Например, замещенные арильные группы ограничены конструкцией - замещенный арил(замещенный арил)-(замещенный арил). Термин "лечение заболевания" включает:(1) профилактику заболевания, т.е. предупреждение развития клинических симптомов заболевания у млекопитающих, которые могут заразиться или предрасположены к заболеванию, но у которых симптомы заболевания еще не появились.(2) ингибирование заболевания, т.е. замедление или ослабление развития заболевания или его клинических симптомов, а также(3) облегчение заболевания, т.е. регрессия заболевания или его клинических симптомов."Терапевтически эффективным количеством" называют такое количество соединения, которого при введении млекопитающему для лечения заболевания достаточно для такого лечения. Терапевтически эффективное количество зависит от соединения, заболевания и его интенсивности, а также возраста, веса и т.д. млекопитающего, подлежащего лечению. Термин "фармацевтически приемлемая соль" означает фармацевтически приемлемые соли соединения формулы I, полученные с помощью хорошо известных разнообразных органических и неорганических противоионов, и включает, например, натриевые, калиевые, кальциевые, магниевые, аммонийные,тетраалкиламмонийные и подобные соли; а если молекула содержит основную функциональность, то соли органических или неорганических кислот, таких как гидрохлориды, гидробромиды, тартраты, мезилаты, ацетаты, малеаты, оксалаты и подобные им. Интегрины представляют собой большое семейство гомологичных протеинов с трансмембранными линкерами, являющихся в клетках животных основными рецепторами связывания большинства внеклеточных матриксных протеинов, таких как коллаген, фибронектин и ламинин. Интегрины представляют собой гетеродимеры, содержащие - и -цепи. К настоящему времени обнаружено двадцать различных гетеродимеров интегринов, они содержат 9 различныхсубъединиц и 14 различныхсубъединиц. Термин "4-интегрины" означает класс гетеродимерных связанных с ферментами рецепторов клеточной поверхности, содержащих 4-субъединицу, сопряженную с любой изсубъединиц. Примером 4 интегрина является VLA-4, который представляет собой гетеродимер, содержащий 4 и 1 субъединицы, его также называют 41-интегрином. Настоящее изобретение относится к соединениям, их фармацевтически приемлемым солям, композициям, их получению и способам лечения заболеваний, опосредованных VLA-4. В соответствии с одним аспектом настоящее изобретение относится к соединениям формулы I где R1 выбран из группы, включающей C1-C4-алкил, C1-C4-галогеналкил, гетероарил и -N(R5)(R6), где R5 и R6 независимо выбраны из группы, включающей водород, C1-C4-алкил, или R5 и R6 совместно с атомом азота, с которым они связаны, формируют гетероцикл;R3 и R4 совместно с атомом азота, с которым они связаны, формируют гетероцикл; а также к фармацевтически приемлемым солям или сложным эфирам этих соединений.-7 015388 В соответствии с некоторыми аспектами группа -OC(O)NR3R4 находится в пара-положении фенильного цикла. В соответствии с некоторыми аспектами R3 и R4 совместно формируют гетероцикл. В соответствии с другими аспектами R3 и R4 совместно формируют пирролидинильный цикл. В соответствии с некоторыми аспектами R2 представляет собой C1-C4-алкил. В соответствии с другими аспектами R2 означает этил. В соответствии с другими аспектами R3 и R4 совместно формируют гетероцикл, a R2 представляет собой C1-C4-алкил. В соответствии с другими аспектами R3 и R4 совместно формируют пирролидинильный цикл, a R2 представляет собой этил. Группы R1, R2, R3 и R4 некоторых соединений настоящего изобретения приведены в табл. 1. Таблица 1 В соответствии с другим аспектом настоящее изобретение относится к соединениям формулы IIR9 и R10 совместно с атомом азота, с которым они связаны, формируют гетероцикл; а также к фармацевтически приемлемым солям или сложным эфирам этих соединений. В соответствии с некоторыми аспектами группа -OC(O)NR9R10 находится в пара-положении фенильного цикла. В соответствии с некоторыми аспектами R9 и R10 совместно формируют гетероцикл. В соответствии с другими аспектами R9 и R10 совместно формируют пирролидинильный цикл. В соответствии с некоторыми аспектами R8 представляет собой C1-C4-алкил. В соответствии с другими аспектами R8 означает этил. В соответствии с некоторыми аспектами R7 представляет собой C1-C4-алкил. В соответствии с другими аспектами R7 выбран из группы, включающей изопропил и трет-бутил.-8 015388 В соответствии с некоторыми аспектами R7 представляет собой C1-C4-галогеналкил. В соответствии с другими аспектами R7 соответствует трифторметилу. В соответствии с некоторыми аспектами R7 означает гетероарил. В соответствии с другими аспектами R7 выбран из группы, включающей фуран-2-ил, фуран-3-ил, тиен-2-ил и тиен-3-ил. В соответствии с некоторыми аспектами R9 и R10 совместно формируют гетероцикл, R8 представляет собой C1-C4-алкил и R7 соответствует гетероарилу. В соответствии с другими аспектами R9 и R10 совместно с атомом азота, с которым они связаны, формируют пирролидинильный цикл, R8 представляет собой этил и R7 - гетероарил. В соответствии с некоторыми аспектами R9 и R10 совместно формируют гетероцикл, R8 представляет собой C1-C4-алкил и R7 соответствует алкилу. В соответствии с другими аспектами R9 и R10 совместно с атомом азота, с которым они связаны, формируют пирролидинильный цикл, R8 представляет собой этил и R7 означает алкил. Настоящее изобретение относится также к соединениям формулы II, группы R7, R8, R9 и R10 которых описаны в табл. 2. Таблица 2 В соответствии с другим аспектом настоящее изобретение относится к соединениям формулы III где R11 и R12 независимо представляют собой C1-C4-алкил, или R11 и R12 совместно с атомом азота, с которым они связаны, формируют гетероцикл;R14 и R15 совместно с атомом азота, с которым они связаны, формируют гетероцикл; а также к фармацевтически приемлемым солям или сложным эфирам этих соединений. В соответствии с некоторыми аспектами группа -OC(O)NR14R15 находится в пара-положении фенильного цикла. В соответствии с некоторыми аспектами R14 и R15 совместно формируют гетероцикл. В соответствии с другими аспектами R14 и R15 совместно формируют пирролидинильный цикл. В соответствии с некоторыми аспектами R13 представляет собой C1-C4-алкил. В соответствии с другими аспектами R13 - этил. В соответствии с некоторыми аспектами R11 и R12 независимо представляют собой C1-C4-алкил. В соответствии с другими аспектами R11 - этил и R12 - изопропил.-9 015388 В соответствии с некоторыми аспектами R11 и R12 совместно с атомом азота, с которым они связаны, формируют гетероцикл. В соответствии с другими аспектами гетероцикл выбран из группы, включающей пиперидин-1-ил и 3-тиапирролидин-1-ил. В соответствии с дополнительными аспектами R14 и R15 совместно формируют гетероцикл, R13 соответствует C1-C4-алкилу, a R11 и R12 совместно с атомом азота, с которым они связаны, также формируют гетероцикл. Настоящее изобретение относится также к соединениям формулы III, группы R11, R12, R13, R14 и R15 которых описаны в табл. 3. Таблица 3 В соответствии с некоторыми аспектами настоящее изобретение относится к соединениям формулI-III, содержащим следующие карбамильные заместители: причем эти группы присоединены к фенильному циклу в пара-положении. В соответствии с другими аспектами соединения из табл. 1-3 содержат карбамильные заместители, присоединенные также в параположении. В соответствии с некоторыми аспектами настоящее изобретение относится также к соединениям формул I-III, включая указанные в табл. 1-3, причем карбамильные заместители присоединены в них в орто- или мета-положениях. Настоящее изобретение относится также к соединениям, указанным в табл. 4. Таблица 4 В соответствии с другим аспектом настоящее изобретение относится к фармацевтическим композициям, содержащим фармацевтически приемлемый носитель и терапевтически эффективное количество одного или более описанных здесь соединений. В соответствии с одним из своих методических аспектов настоящее изобретение относится к способу лечения заболеваний, опосредованных по меньшей мере частично 4-интегрином, предпочтительноVLA-4, у пациента, причем указанный способ предполагает введение фармацевтической композиции,- 12015388 содержащей фармацевтически приемлемый носитель и терапевтически эффективное количество одного или более соединений настоящего изобретения. В соответствии с другим аспектом настоящее изобретение относится к использованию фармацевтической композиции, содержащей соединения настоящего изобретение, для получения лекарственного средства для лечения 4-интегрин-опосредованного заболевания. Соединения и фармацевтические композиции настоящего изобретения пригодны для лечения патологических состояний, опосредованных, по крайней мере частично, 4-интегринами, где 4-интегрин предпочтительно представляет собой VLA-4, а также адгезией лейкоцитов. Такие патологические состояния включают, например, астму, болезнь Альцгеймера, атеросклероз, вызванную СПИДом деменцию, диабет (включая острый ювенильный приступ диабета), воспалительное заболевание кишечника(включая язвенные колиты и болезнь Крона), рассеянный склероз, ревматоидный артрит, последствия трансплантации тканей, метастазы опухолей, менингит, энцефалит, инсульт и другие травмы мозга, нефриты, ретиниты, атопический дерматит, псориаз, миокардиальную ишемию и острое опосредованное лейкоцитами повреждение легких, такое как бывает при синдроме дыхательной недостаточности у взрослых. Другие заболевания включают, но не ограничиваются ими, воспалительные состояния, такие как узловатая эритема, аллергические конъюктивиты, ретробульбарный неврит, увеит, аллергический ринит,анкилозирующий спондилоартрит, псориатический артрит, васкулит, синдром Рейтера, системная красная волчанка, прогрессирующий системный склероз, полимиозит, дерматомиозит, грануломатоз Вегнера,аортит, саркоидоз, лимфоцитопения, темпоральный артериит, перикардит, миокардит, застойная сердечная недостаточность, узловатый полиартериит, синдромы гиперчувствительности, аллергия, синдромы гиперэозинофилии, синдром Чурга-Страусса, хронические обструктивное заболевание легких, пневмонит с гиперчувствительностью, хронический активный гепатит, внутритканевый цистит, аутоиммунная эндокринная недостаточность, первичный цирроз желчного пузыря, аутоиммунная апластическая анемия, стойкий хронический гепатит и тиреоидит. В соответствии с предпочтительным аспектом патологическое состояние, опосредованное 4 интегрином, представляет собой воспалительное заболевание. Соединения настоящего изобретения включают, например, следующие:N-[2-диэтиламино-5-N-этил-N-(фуран-3-илкарбонил)аминопиримидин-4-ил]-L-4'-(пирролидин 1-ил)карбонилоксифенилаланина трет-бутиловый эфир; а также фармацевтически приемлемые соли или сложные эфиры указанных соединений.- 13015388 Получение соединений. Соединения настоящего изобретения можно получить из легкодоступных исходных материалов с использованием следующих общих методов и процедур. Необходимо понимать, что в случае, если приведены типичные или предпочтительные условия протекания процесса (т.е. температура реакции, время,мольное соотношение реагентов, растворители, давление и т.д.), можно использовать и другие условия,если только не указано иначе. Оптимальные условия реакции могут варьировать в зависимости от конкретных используемых реагентов и растворителей, но такие условия компетентный специалист сможет определить рутинными процедурами оптимизации. Кроме того, компетентному специалисту должно быть очевидно, что для предотвращения нежелательных реакций с участием некоторых функциональных групп может появиться необходимость во введении обычных защитных групп. В литературе хорошо известны и описаны подходящие защитные группы для различных функциональных групп и подходящие условия для введения и снятия защиты. Например, разнообразные защитные группы описаны в работе Т.W. Greene and G.M. Wuts, Protecting Groups inOrganic Synthesis, Second Edition, Wiley, New York, 1991, а также в приведенных там ссылках. Кроме того, как правило, соединения настоящего изобретения содержат один или несколько хиральных центров. Это означает, что при необходимости такие соединения можно получить или выделить в виде чистых стереоизомеров, т.е. индивидуальных энантиомеров или диастереомеров, а также в виде смесей, обогащенных одним из стереоизомеров. Все такие стереоизомеры (и обогащенные смеси) включены в объем настоящего изобретения, если не указано иначе. Чистые стереоизомеры (или обогащенные смеси) можно приготовить с помощью, например, оптически активных исходных материалов или стереоселективных реагентов, хорошо известных в соответствующей области. Альтернативно, рацемические смеси таких соединений можно разделить с помощью, например, хиральной колоночной хроматографии, хиральных расщепляющих агентов и т.д. В соответствии с одним аспектом соединения настоящего изобретения можно получить, как показано ниже на схеме. Схема где группы R1, R2, R3, R4, R5 и R6 описаны выше, а Pg представляет собой карбоксильную защитную группу, такую как бензил, трет-бутил и подобные им. Исходное 5-аминопиримидиновое промежуточное соединение на схеме, соединение 1.1, подробно описано в публикации WO 03/099809 и для иллюстративных целей показано в виде 4-замещенного фе- 14015388 нилаланинового производного. Разумеется, 2- и 3-замещенные фенилаланиновые производные вступают в такие же реакции. Конкретно, как показано на схеме, соединение 1.1, 5-амино-2-диэтиламино-4-замещенный пиримидин (полученный из соответствующего 5-нитропиримидина восстановлением на 5% Pd/C или 5% PtO2 по весу), конвертируется в соответствующий трифторацетамид, соединение 1.2, обычными методами. Например, небольшой избыток трифторуксусного ангидрида смешивают с соединением 1.1 в подходящем инертном разбавителе, таком как тетрагидрофуран, метиленхлорид, пиридин и подобные им. Реакцию проводят при температуре приблизительно от 0 до 30 С до фактического завершения, что обычно происходит через 0,5-24 ч. По завершении реакции соединение 1.2 выделяют традиционными методами, включая нейтрализацию, упаривание, экстракцию, осаждение, хроматографию, фильтрование и подобные им,или, альтернативно, используют на следующем этапе без очистки и/или выделения. Превращение соединения 1.2 в соответствующий N(R2),N-трифторацетамидопиримидин, соединение 1.3, также осуществляется традиционными методами. Например, избыток галогенида, R2-I, смешивают с соединением 1.2 в подходящем инертном разбавителе, таком как ДМФ, в присутствии избытка подходящего основания, например, карбоната калия. В соответствии с предпочтительным аспектом используют приблизительно два эквивалента R2-I и карбоната калия. Реакция протекает при температуре окружающей среды в закупоренном контейнере до своего фактического завершения, что происходит обычно через 20-72 ч. По завершении реакции соединение 1.3 выделяют традиционными методами,включая нейтрализацию, упаривание, экстракцию, осаждение, хроматографию, фильтрование и подобные им, или, альтернативно, используют на следующем этапе без очистки и/или выделения. Карбоксильную защитную группу соединения 1.3 можно удалить в традиционных условиях, получив соединение формулы I (не показано). В соответствии с одним аспектом трет-бутильную защитную группу можно удалить действием муравьиной кислоты. В соответствии с другим аспектом бензильную защитную группу можно удалить действием водорода в присутствии катализатора палладий на углероде,как правило, в протонном растворителе, таком как метанол, в условиях повышенного давления водорода. Альтернативно, трифторацетильную группу можно удалить, получив соответствующий амин, соединение 1.4. В соответствии с этим аспектом трифторацетильная группа действует как аминозащитная группа. Как и в предыдущих реакциях, это вещество обычно получают, например, смешивая соединение 1.3 с большим избытком подходящего основания, такого как карбонат калия, в смеси воды и протонного растворителя, например метанола. Реакцию проводят при повышенной температуре, например, от 40 до 60 С до ее фактического завершения. По завершении реакции соединение 1.4 выделяют традиционными методами, включая нейтрализацию, упаривание, экстракцию, осаждение, хроматографию, фильтрование и подобные им, или, альтернативно, используют на следующем этапе без очистки и/или выделения. В соответствии со схемой соединение 1.4 может быть использовано для получения либо производных мочевины, где R1=-NR5R6, либо ациламино-производных, если R1 представляет собой C1-C4-алкил,C1-C4-галогеналкил или гетероарил, связанный с карбонильной группой, но не через атом азота, с которым они связаны. В первом случае производные мочевины получают традиционными методами, включающими получение на первом этапе амидохлорида, соединения 1.7. Для этого соединение 1.4 вводят в реакцию с избытком фосгена в присутствии подходящего основания, такого как карбонат калия, бикарбонат калия, карбонат натрия и подобные им. По завершении реакции соединение 1.7 выделяют традиционными методами, включая нейтрализацию, упаривание, экстракцию, осаждение, хроматографию,фильтрование и подобные им, но предпочтительно используют на следующем этапе без очистки и/или выделения. Полученный аминохлорид, соединение 1.7, затем конвертируют в соответствующее производное мочевины, соединение 1.8, путем его взаимодействия с подходящим амином, R5R6NH, в обычных условиях. Предпочтительно, если при этом эквимолярное количество или избыток амина взаимодействует с соединением 1.7 в подходящем растворителе, например тетрагидрофуране, диоксане, хлорформе и подобных им. По завершении реакции соединение 1.8 выделяют традиционными методами, включая нейтрализацию, упаривание, экстракцию, осаждение, хроматографию, фильтрование и подобные им, или,альтернативно, используют на следующем этапе без очистки и/или выделения. Карбоксильную защитную группу соединения 1.8 можно удалить в обычных условиях с получением соединения 1.9, соответствующего формуле I. В соответствии с одним аспектом трет-бутильную защитную группу удаляют, воздействуя муравьиной кислотой. В соответствии с другим аспектом это делают, действуя водородом в присутствии катализатора палладий на углероде, как правило, в протонном растворителе, таком как метанол, в атмосфере водорода при повышенном давлении. По завершении реакции соединение 1.8 выделяют традиционными методами, включая нейтрализацию, упаривание, экстракцию, осаждение, хроматографию, фильтрование и подобные им. В соответствии со вторым аспектом ациламино-производные, соединение 1.5, получают, смешивая соединение 1.4 с небольшим избытком ацил галогенида в присутствии подходящего основания, такого как триэтиламин, диизопропилэтиламин и подобные им (оно требуется для перехвата образующейся кислоты). Обычно реакцию проводят в подходящем инертном растворителе, таком как тетрагидрофуран,диоксан, хлорформ и подобные им. Предпочтительно реакцию проводят при температуре от 0 до 30 С до- 15015388 ее фактического завершения, что происходит, как правило, через 2-48 ч. По завершении реакции соединение 1.8 выделяют традиционными методами, включая нейтрализацию, упаривание, экстракцию, осаждение, хроматографию, фильтрование и подобные им, или, альтернативно, используют на следующем этапе без очистки и/или выделения. Карбоксильную защитную группу соединения 1.5 можно удалить в обычных условиях с получением соединения 1.6, соответствующего формуле I. В соответствии с одним аспектом трет-бутильную защитную группу удаляют, воздействуя муравьиной кислотой. В соответствии с другим аспектом бензильную защитную группу удаляют, действуя водородом в присутствии катализатора палладий на углероде,как правило, в протонном растворителе, таком как метанол, в атмосфере водорода при повышенном давлении. По завершении реакции соединение 1.6 выделяют традиционными методами, включая нейтрализацию, упаривание, экстракцию, осаждение, хроматографию, фильтрование и подобные им. Фармацевтические составы. Если соединения настоящего изобретения используют в качестве лекарственных препаратов, то их обычно вводят в форме фармацевтических композиций. Эти соединения можно вводить по различным маршрутам, включая пероральный, ректальный, трансдермальный, подкожный, внутривенный, внутримышечный и интраназальный маршруты. Соединения эффективны при использовании в составе как пероральных составов, так и вводимых в виде инъекций. Подобные композиции готовятся с использованием методов, хорошо известных в фармацевтике, и содержат по меньшей мере одно активное соединение. Настоящее изобретение включает также фармацевтические композиции, содержащие в качестве активного ингредиента одно или более соединений, охватываемых формулами I-III, и фармацевтически приемлемые носители. При получении композиций по настоящему изобретению активный ингредиент обычно смешивают с наполнителем, разбавляют им или помещают внутрь специального носителя, который может представлять собой капсулы, таблетки, пакетики, бумажные упаковки или другие контейнеры. Используемый наполнитель, как правило, должен быть удобен для введения людям или другим млекопитающим. Если наполнитель используется как разбавитель, то он может быть твердым, полутвердым или жидким веществом, являясь при этом носителем или средой для активного ингредиента. Таким образом, композиции могут принимать форму таблеток, пилюль, порошков, ромбовидных таблеток, пакетиков, облаток, эликсиров, суспензий, эмульсий, растворов, сиропов, аэрозолей (в твердой или жидкой среде), мазей, содержащих, например, до 10 мас.% активного соединения, мягких и твердых желатиновых капсул, суппозиториев, стерильных растворов для инъекций и стерильных упакованных порошков. В процессе приготовления состава может потребоваться размолоть активный ингредиент для получения частиц соответствующих размеров и только потом смешивать его с другими ингредиентами. Если активное соединение практически нерастворимо, то обычно его размалывают до размера частиц менее 200 меш (проходящих через сито с плотностью ячеек 200 на дюйм). Если активное соединение в значительной степени растворимо в воде, то размер частиц обычно делают таким, чтобы обеспечить их равномерное распределение в препарате, например, около 40 меш. В качестве примеров подходящих наполнителей можно привести лактозу, декстрозу, сахарозу, сорбит, манит, крахмалы, аравийскую камедь, фосфат кальция, альгинаты, трагакант, желатин, силикат кальция, микрокристаллическую целлюлозу, поливинилпирролидон, целлюлозу, воду, патоку и метилцеллюлозу. Составы могут также содержать смазочные вещества, такие как тальк, стеарат магния и минеральное масло; увлажняющие агенты; эмульсификаторы и суспендирующие агенты; консерванты, такие как метил- и полигидроксипропилбензоаты; подсластители и вкусовые добавки. Композиции настоящего изобретения можно получить таким образом, чтобы обеспечить быстрое, отложенное или замедленное высвобождение активного ингредиента после введения пациенту; для этого используются методы, хорошо известные в фармацевтике. Внутривенное введение терапевтических агентов хорошо известно в фармацевтике. Составы для внутривенного введения должны обладать определенными свойствами, а не просто представлять собой композицию, терапевтический агент в которой растворим в воде. Например, состав должен усиливать общую стабильность активных ингредиентов, кроме того, его производство должно быть достаточно экономичным. Все эти факторы в совокупности и определяют общий успех и эффективность препарата для внутривенного введения. В фармацевтическую композицию с участием соединений настоящего изобретения можно включать и другие вспомогательные добавки, например растворители: этанол, глицерин,пропиленгликоль; стабилизаторы: этилендиаминтетрауксусную кислоту (ЭДТА), лимонную кислоту; антимикробные консерванты: бензиловый спирт, метилпарабен, пропилпарабен; агенты буферизации: лимонная кислота/цитрат натрия, гидротартрат калия, гидротартрат натрия, уксусная кислота/ацетат натрия, малеиновая кислота/малеат натрия, гидрофталат натрия; а также модификаторы ионной силы (осмотического давления): хлорид натрия, маннит, декстроза. Для поддержания рН в диапазоне от 4 до 8 и более предпочтительно приблизительно от 4 до 6, может потребоваться буфер. Обычно буферная система представляет собой смесь слабой кислоты и ее растворимой соли, например цитрата натрия/лимонной кислоты; или моно и дисолей двухосновной кислоты, например, гидротартрат калия; гидротартрат натрия, фосфорная кислота/дигидрофосфат калия и фосфорная кислота/гидрофосфат калия.- 16015388 Количество используемой буферной системы зависит (1) от желаемого значения рН и (2) от количества лекарства. В общем случае, мольное соотношение буфер:лекарство (где число молей буфера определяется как суммарное число молей его ингредиентов, например, цитрата натрия и лимонной кислоты) находится в интервале от 0,5:1 до 50:1 для поддержания рН в диапазоне от 4 до 8 и обычно используется отношение от 1:1 до 10:1. Примером пригодного для настоящего изобретения буфера является система цитрата натрия/лимонной кислоты состава от 5 до 50 мг на 1 мл цитрата натрия и от 1 до 15 мг на 1 мл лимонной кислоты, этого достаточно для поддержания рН композиции в интервале от 4 до 6. Агент буферизации вводят также, чтобы не допустить осаждения лекарства. При этом он образует растворимые комплексы с ионами металлов, например Ca, Mg, Fe, Al, Ba, которые могут попадать в раствор из стеклянных контейнеров или резиновых пробок или присутствовать в обычной питьевой воде. Агент может выступать в роли агента комплексообразования, конкурирующего с лекарством, и образовывать растворимые комплексы металлов, которые иначе привели бы к появлению нежелательных частиц. Кроме того, наличие в системе агента, например хлорида натрия, в количестве приблизительно 1-8 мг/мл, позволяет довести осмотическое давление до тех значений, которые соответствуют человеческой крови, и, тем самым не допустить распухания или сжимания эритроцитов при внутривенном введении состава, что может привести к нежелательным побочным эффектам, таким как рвота или диарея, а также, возможно, к связанным заболеваниям крови. В общем случае, осмотическое давление состава соответствует человеческой крови, которая имеет осмолярность в интервале от 282 до 288 мОсм/кг. Обычно осмолярность состава равна 285 мОсм/кг, что эквивалентно осмотическому давлению 0,9% раствора хлорида натрия. Внутривенные составы можно вводить прямой инъекцией, в виде внутривенного болюса, а можно путем инфузии. При этом его добавляют в соответствующий раствор для инфузии, такой как 0,9% раствор хлорида натрия или в другой совместимый раствор. Предпочтительно готовить композиции в виде форм единичной дозированной лекарственной формы, каждая доза содержит приблизительно от 5 до 100 мг, обычно от 10 до 30 мг активного ингредиента. Термин "единичная дозированная лекарственная форма" означает физически дискретную единицу, подходящую в качестве единичной дозы для людей и других млекопитающих, каждая такая единица содержит заранее заданное количество активного вещества, рассчитанное так, чтобы оно вызывало желательный терапевтический эффект, в сочетании с подходящим фармацевтическим наполнителем. Активное соединение эффективно в широком диапазоне концентраций и его, как правило, вводят в фармацевтически эффективном количестве. Необходимо понимать, однако, что фактически назначаемая доза соединения определяется врачом с учетом сопутствующих обстоятельств, включая заболевание,выбранный маршрут введения, фактическое вводимое соединение, возраст, вес и реакцию конкретного пациента, тяжесть его симптомов и т.д. Для приготовления твердых композиций, таких как таблетки, основной активный ингредиент смешивают с фармацевтическим наполнителем, получая твердую предварительную композицию, содержащую гомогенную смесь соединений настоящего изобретения. Под гомогенностью этих предварительных составов понимается то, что активный ингредиент равномерно распределен по композиции, так что ее можно легко разделить на одинаково эффективные единичные дозированные лекарственные формы, такие как таблетки, пилюли и капсулы. Этот твердый предварительный состав затем делят на единичные дозированные лекарственные формы описанного типа, содержащего, например, приблизительно от 0,1 до 500 мг активного ингредиента настоящего изобретения. Таблетки или пилюли настоящего изобретения могут быть покрыты оболочкой или иным способом приготовлены, чтобы обеспечить пролонгированное действие. Например, таблетка или пилюля может содержать один компонент внутри, а другой снаружи, причем последний представляет собой оболочку вокруг первого. Компоненты могут быть разделены слоем, защищающим внутренний компонент от распада в желудке, так чтобы он мог пройти в двенадцатиперстную кишку, или чтобы его высвобождение было замедленным. Для таких слоев или покрытий можно использовать множество веществ, включая большое количество полимерных кислот и смесей полимерных кислот с такими материалами, как шеллак, цетиловый спирт и ацетат целлюлозы. Жидкие формы, содержащие композиции настоящего изобретения и пригодные для введения перорально или в виде инъекций, включают водные растворы сиропов приятного вкуса, водные или масляные суспензии, а также приятные на вкус эмульсии, содержащие такие пригодные в пищу масла, такие как хлопковое, кунжутное, кокосовое или арахисовое, а также эликсиры и аналогичные фармацевтические носители. Композиции для ингаляции или вдувания включают растворы и суспензии в фармацевтически приемлемых, водных или органических растворителях и их смесях, а также порошки. Жидкие или твердые композиции могут содержать подходящие фармацевтически приемлемые наполнители, как описано в настоящем описании. Предпочтительно для получения местного или системного эффекта вводят композиции по пероральному или назальному дыхательному маршруту. Композиции в предпочтительных фар- 17015388 мацевтически приемлемых растворителях можно распылять действием инертных газов. Распыляемые растворы вдыхают непосредственно из приборов для распыления (небулайзеров), либо последние можно соединить со специальной лицевой маской или промежуточным дыхательным устройством, создающим повышенное давление. Растворы, суспензии или порошковые композиции можно вводить, предпочтительно перорально или назально, из устройств, доставляющих состав соответствующим способом. Приведенные ниже примеры фармацевтических составов иллюстрируют фармацевтические композиции настоящего изобретения. Пример 1. Состав. Готовят твердые желатиновые капсулы, содержащие следующие ингредиенты. Указанные ингредиенты смешивают и помещают в твердую желатиновую капсулу в количестве 340 мг. Пример 2. Состав. Таблетка готовится из следующих ингредиентов. Компоненты перемешивают и уплотняют в таблетки весом 240 мг каждая. Пример 3. Состав. Сухой порошок для ингаляции готовят из следующих компонентов. Активный ингредиент смешивают с лактозой и смесь помещают в устройство для ингаляции сухого порошка. Пример 4. Состав. Таблетки, содержащие по 30 мг активного ингредиента, готовят следующим образом. Активный ингредиент, крахмал и целлюлозу пропускают через сито с ячейками 20 меш (1 меш число отверстий на 1 линейный дюйм (24,5 см и тщательно перемешивают. Раствор поливинилпирролидона смешивают с полученным порошком, после чего пропускают через сито размером 16 меш. Полученные таким способом гранулы высушивают при температуре 50-60 С и пропускают через сито 16 меш. Карбоксиметил-крахмал натрия, стеарат магния и тальк пропускают через сито 30 меш, а затем добавляют к гранулам, которые после перемешивания прессуют в таблетки весом 120 мг каждая. Пример 5. Состав. Капсулы, содержащие по 40 мг лекарственного средства, готовят следующим образом. Активный ингредиент, крахмал и стеарат магния смешивают, пропускают через сито размером 20 меш и заполняют им твердые желатиновые капсулы по 150 мг. Активный ингредиент пропускают через сито размером 60 меш и суспендируют в насыщенных глицеридах жирных кислот, предварительно расплавленных при минимально возможной температуре. Смесь затем выливают в форму для суппозиториев емкостью 2,0 г и позволяют остыть. Пример 7. Состав. Суспензии, содержащие 50 мг лекарственного средства на дозу объемом 5,0 мл, готовят следующим образом. Активный ингредиент, сахарозу и ксантановую камедь смешивают, пропускают через сито размером 10 меш, после чего перемешивают с заранее приготовленным раствором микрокристаллической целлюлозы и карбоксиматилцеллюлозы натрия в воде. Бензоат натрия, вкусовые добавки и краситель разбавляют небольшим количеством воды и добавляют в систему при перемешивании. Затем систему доводят водой до требуемого объема. Пример 8. Состав. Активный ингредиент, крахмал и стеарат магния перемешивают, пропускают через сито размером 20 меш и помещают в желатиновую капсулу в количестве 425 мг. Пример 9. Состав. Состав для подкожного введения можно приготовить следующим образом. Пример 10. Состав. Состав для местного применения можно приготовить следующим образом. Белый мягкий парафин нагревают до плавления. В него добавляют жидкий парафин и воскэмульсификатор, после чего перемешивают систему до их растворения. Затем туда же вводят активный ингредиент и продолжают перемешивание до полного диспергирования. Смесь охлаждают до твердого состояния.- 19015388 Пример 11. Состав. Состав для внутривенного введения можно приготовить следующим образом. Еще один предпочтительный состав, реализованный в способах по настоящему изобретению, предполагает использование приспособлений для трансдермальной доставки ("пластыри"). Такие трансдермальные пластыри обеспечивают непрерывную или прерывистую инфузию соединений настоящего изобретения в контролируемых количествах. Конструкция и использование трансдермальных пластырей для доставки фармацевтических агентов хорошо известны в фармацевтике, см., например, PatentUS 5023252, утвержденный 11 июня 1991 г. и включенный сюда по ссылке. Можно получить пластыри,обеспечивающие непрерывное, пульсирующее введение фармацевтических агентов или их доставку "по требованию". Часто бывает желательно или необходимо прямо или опосредованно ввести фармацевтическую композицию в мозг. Прямые технологии обычно предполагают помещение катетера по доставке лекарственного средства в вентрикулярную систему хозяина, что позволяет обойти гематоэнцефалический барьер. Одна из таких имплантируемых систем доставки, используемая для транспорта биологических факторов в специфические анатомические области тела, описана в патенте US 5011472, который включен сюда по ссылке. Обычно предпочтительны непрямые способы, они, как правило, предполагают такую форму композиции, чтобы обеспечить перевод лекарственного средства в латентное состояние путем превращения гидрофильных лекарственных средств в форму, растворимую в липидах. Обычно такая латенциация осуществляется путем блокирования гидроксильных, карбонильных, сульфатных и первичных аминогрупп лекарственного средства, которое делает его более растворимым в липидах и способным преодолеть гематоэнцефалический барьер. Альтернативно, доставку гидрофильных лекарственных средств можно усилить внутри артериальной инфузией гипертонических растворов, которые временно открывают гематоэнцефалический барьер. Другие составы, пригодные для использования в настоящем изобретении можно найти в руководстве Remington's Pharmaceutical Sciences, Mace Publishing Company, Philadelphia, PA, 17th ed. (1985). Как уже отмечалось выше, описанные соединения удобны для использования в разнообразных системах доставки лекарственных средств, описанных выше. Кроме того, чтобы увеличить период полувыведения вводимых соединений из сыворотки, их можно инкапсулировать, заключив в полость липосомы,приготовить в виде коллоидного раствора или использовать другие традиционные методы, позволяющие увеличить период полувыведения соединений. Большое количество методов приготовления липосом описано в работе, например, Szoka, et al., U.S. Patent4235871, 4501728 и 4837028, каждая из которых включена сюда по ссылке. Конъюгаты настоящего изобретения представляют собой антагонисты VLA-4 и предполагается, что они обеспечивают большее удержание in vivo, по сравнению с неконъюгированными соединениями. Такое улучшенное удержание конъюгата в организме приводит к меньшей необходимой дозировке лекарственного средства, что, в свою очередь, приводит к меньшим побочным эффектам и уменьшению токсичности. Кроме того, это позволяет реже вводить лекарственные препараты пациенту, достигая того же или улучшенного терапевтического эффекта. Предполагается, что конъюгаты настоящего изобретения демонстрируют in vivo ингибирование адгезии лейкоцитов к эндотелиальным клеткам, опосредованной VLA-4, путем конкуретного связывания сVLA-4. Предпочтительно использовать соединения настоящего изобретения в составах для внутривенного введения с целью лечения заболеваний, опосредованных VLA-4 или адгезией лейкоцитов. Такие заболевания включают воспалительные заболевания у млекопитающих, например астму, болезнь Альцгеймера, атеросклероз, вызванную СПИДом деменцию, диабет (включая острый ювенильный приступ диабета), воспалительное заболевание кишечника (включая язвенные колиты и болезнь Крона), рассеянный склероз, ревматоидный артрит, последствия трансплантации тканей, метастазы опухолей, менингит, энцефалит, инсульт и другие травмы мозга, нефриты, ретиниты, атопический дерматит, псориаз, миокардиальную ишемию и острое опосредованное лейкоцитами повреждение легких, такое как бывает при синдроме дыхательной недостаточности у взрослых. Особенно эффективны соединения настоящего изобретения для лечения множественного склероза и ревматоидного артрита. Подходящие in vivo модели для демонстрации эффективности при лечении воспалительных заболеваний включают экспериментальный аллергический энцефаломиелит (ЭАЭ) у мышей, крыс, морских свинок или приматов, а также и другие воспалительные модели, зависимые от 4-интегринов. Воспалительное заболевание кишечника представляет собой обобщенный термин, обозначающий две похожие болезни, называемые болезнью Крона и ульцеративным (язвенным) колитом. Болезнь Крона - идиопатическое хроническое язвенно-сократительное заболевание, характеризующееся- 20015388 четко оформленным и, как правило, трансмуральным вовлечением всех слоев стенки желудочнокишечного тракта в грануломатозный воспалительный процесс. Участвовать в этом процессе может любой сегмент желудочно-кишечного тракта, от рта до ануса, но чаще всего болезнь поражает терминальную часть подвздошной или толстую кишку. Ульцеративный (язвенный) колит представляет собой воспалительный ответ, ограниченный в основном слизистой или подслизистой оболочкой подвздошной или толстой кишки. В вызванных воспалительными заболеваниями повреждениях кишечника встречается много лимфоцитов и макрофагов, они вносят свой вклад в эти повреждения. Астма - болезнь, характеризующаяся повышенной реакцией трахеобронхиального дерева на различные стимулы, усиливающие пароксизмальные сокращения бронхиальных дыхательных путей. Стимулы вызывают высвобождение различных медиаторов воспаления из покрытых IgE тучных клеток,включая гистамин, эозинофильные и нейтрофильные хемотактические факторы, лейкотриены, простагландины и фактор активации тромбоцитов. Высвобождение этих факторов рекрутирует базофилы, эозинофилы и нейтрофилы, что вызывает воспалительное повреждение. Атеросклероз - заболевание артерий (например, коронарной, сонной, аорты и подвздошной). Основное повреждение при этом, атерома, представляет собой фокальную бляшку на внутренней стенке сосуда (интиме) с липидным ядром и закрывающей шляпкой из фиброзной ткани. Атеромы мешают артериальному кровотоку и ослабляют пораженные артерии. Основным последствием данного заболевания являются миокардиальные и церебральные инфаркты. В атеромах рекрутируются макрофаги и лейкоциты, они вносят свой вклад в воспалительное повреждение. Ревматоидный артрит представляет собой хроническое рецидивирующее воспалительное заболевание, вызывающее, прежде всего, нарушение в работе и повреждения суставов. Обычно сначала ревматоидные артриты влияют на небольшие связки ладоней и ступней, но впоследствии могут распространяться на запястья, локти, лодыжки и колени. Артрит возникает в результате действия лейкоцитов на синовиальные клетки, причем лейкоциты проникают в синовиальную жидкость из кровотока, см., например,Paul, Immunology (3d ed., Raven Press, 1993). Еще одним показанием для использования соединений настоящего изобретения является лечение отторжения органов или трансплантатов, опосредованного VLA-4. За последнее время эффективность хирургических методов трансплантации тканей и органов, таких как кожа, почка, печень, сердце, легкое,поджелудочная железа и костный мозг, значительно возросла. Возможно, основной проблемой теперь является отсутствие удовлетворительных агентов, вызывающих у реципиента иммунотолерантность к пересаженному органу или аллотрансплантату. Когда хозяину пересаживают аллогенные клетки или органы (т.е. донор и реципиент представляют собой различных индивидуумов того же вида), то, скорее всего, иммунная система хозяина вызовет иммунный ответ на внешние антигены трансплантата (хозяин против трансплантата) с последующим разрушением пересаженной ткани. В отторжении пересаженных тканей принимают участие клетки CD8+, CD4 и моноциты. Соединения настоящего изобретения, которые связывают 4-интегрин, эффективны, помимо прочего, для блокирования аллоантигениндуцированного иммунного ответа реципиента, что не позволяет этим клеткам участвовать в разрушении пересаженной ткани или органа, см., например, Paul et al., Transplant International 9, 420-425 (1996);Yang et al., Transplantation 60, 71-76 (1995); Anderson et al., APMIS 102, 23-27 (1994). Похожее использование связывающих VLA-4 соединений настоящего изобретения - модулирование иммунного ответа, принимающего участие в заболевании "трансплантат против хозяина" (GVHD),см., например, Schlegel et al., J. Immunol. 155, 3856-3865 (1995). GVHD представляет собой потенциально фатальное заболевание, возникающее, когда аллогенному реципиенту пересаживают иммунокомпетентные клетки. В такой ситуации эти клетки донора могут атаковать ткани реципиента. Распространенными мишенями являются ткани кожи, эпителия кишечника и печени, в ходе GVHD они могут быть разрушены. Особенно серьезные проблемы возникают, если пересаживается иммунная ткань, например костный мозг; менее интенсивное GVHD отмечено и в других случаях, включая пересадку сердца и печени. Терапевтические агенты настоящего изобретения эффективны, помимо прочего, для блокирования активации донорных Т-клеток, что уменьшает их способность лизировать клетки-мишени хозяина. Еще одним вариантом применения соединений настоящего изобретения является ингибирование метастазирования опухолей. Сообщалось, что некоторые опухолевые клетки экспрессируют VLA-4 и соединения, которые связываются с VLA-4, блокируют адгезию таких клеток к эндотелиальным клеткам.Steinbacket al., Urol. Res. 23, 175-83 (1995); Orosz et al., Int. J. Cancer 60, 867-71 (1995); Freedman et al.,Leuk. Lymphoma 13, 47-52 (1994); Okahara et al., Cancer Res. 54, 3233-6 (1994). Обладающие требуемой биологической активностью соединения можно модифицировать, чтобы получить желаемые свойства, например улучшить фармакологические свойства (такие как стабильностьin vivo или биодоступность) или так изменить соединение, чтобы его можно было обнаружить в диагностических методах. Стабильность проверяют различными способами, такими как определение полураспада протеинов при инкубации с пептидазами или сывороткой или плазмой крови человека. Большое количество подобных анализов стабильности протеинов описано, например, в работе Verhoef et al., Eur.- 21015388 Еще одним вариантом применения соединений настоящего изобретения является лечение рассеянного склероза. Рассеянный склероз представляет собой прогрессирующее неврологическое аутоиммунное заболевание, которым страдает приблизительно 250000-350000 человек в Соединенных Штатах. Полагают, что рассеянный склероз является результатом специфической аутоиммунной реакции, в которой определенные лейкоциты атакуют миелин, образующий изолирующее покрытие нервных волокон, и инициируют его разрушение. На животных моделях множественного склероза показано, что мышиные моноклинальные антитела против VLA-4 блокируют адгезию лейкоцитов к эндотелию и тем самым предотвращают воспаление центральной нервной системы и последующий паралич у животных 16. Фармацевтические композиции изобретения подходят для использования в различных системах доставки лекарств. Подходящие для настоящего изобретения составы описаны в Remington's Pharmaceutical Sciences, Mace Publishing Company, Philadelphia, PA, 17th ed. (1985). Вводимая пациенту доза зависит от того, что именно вводят, от цели введения, например профилактика или лечение, от состояния пациента, от способа введения и т.д. В терапевтических вариантах использования композицию вводят пациенту, уже страдающему от заболевания, в количестве, эффективном для лечения или, хотя бы, частичного прекращения симптомов заболевания и его осложнений. Количество лекарственного средства, адекватное для достижения этой цели, называют "терапевтически эффективной дозой". Эффективное в таком контексте количество зависит от состояния заболевания, которое предстоит лечить, и от мнения лечащего врача, на которое влияют такие факторы, как интенсивность воспалительного процесса, возраст, вес и общее состояние здоровья пациента, и подобные факторы. При этом необходимо учитывать данные, полученные на животных моделях, такие как представлены в настоящем описании. Методы оценки дозировки для людей, основанные на указанной информации,хорошо известны в фармацевтике (см., например, Wagner, J.G. Pharmacokinetics for the PharmaceuticalScientist. Technomic, Inc., Lancaster, PA 1993). Вводимые пациенту композиции находятся в форме описанных здесь фармацевтических композиций. Их можно стерилизовать известными методами стерилизации, а можно стерильно отфильтровать. Полученные водные растворы можно "упаковать" для использования как они есть, а можно лиофилизировать, после чего смешать лиофилизированный препарат со стерильным водным раствором перед введением. Терапевтическое дозирование соединений настоящего изобретения зависит, например, от конкретного применения, от режима введения соединения, от состояния здоровья пациента и от мнения лечащего врача. Например, в случае внутривенного введения доза, как правило, находится в интервале приблизительно от 20 до 2000 мкг на 1 кг веса тела, предпочтительно приблизительно от 20 до 500 мкг, более предпочтительно приблизительно от 100 до 300 мкг на 1 кг веса тела. Для интраназального введения предпочтительный интервал доз составляет, в общем случае, приблизительно от 0,1 пг до 1 мг на 1 кг веса тела. Эффективные дозы можно экстраполировать из кривых зависимости доза-ответ, полученных в тестовых системах in vitro или на животных моделях. Соединения настоящего изобретения способны также связываться или проявлять антагонизм по отношению к 61-, 91-, 47-, d2-, e7-интегринам (хотя в настоящем изобретении предпочтительны 41- и 91-интегрины). Соответственно соединения изобретения эффективны также для профилактики или изменения симптомов, расстройств или заболеваний, индуцируемых связыванием этих интегринов с их соответствующими лигандами. Например, международная публикация WO 98/53817, опубликованная 3 декабря 1998 г. (содержание которого включено сюда по ссылке во всей своей полноте), и процитированные в ней работы описывают расстройства, опосредованные 47. В этих ссылках описан также анализ определения антагонизма 47-зависимого связывания с протеином сшивания VCAM-Ig. Кроме того, соединения, связывающие d2- и e7-интегрины, особенно эффективны для лечения астмы и связанных с ней заболеваний легких, см., например, работу М.Н. Grayson et al., J. Exp. Med. 1998, 188(11), 2187-2191. Соединения, ингибирующие e7-интегрин, эффективны также для лечения системной красной волчанки (см., например, Arthritis Rheum. 1998, 41(8), 1456-1463); болезни Крона,язвенного колита и воспалительного заболевания кишечника (IBD) (см., например, D. Elewaut et al.,Scand J. Gastroenterol. 1998, 33(1) 743-748); синдрома Сьоргена (см., например, U. Kroneld et al., Scand J.Gastroenterol. 1998, 27(3), 215-218); и ревматоидного артрита (см., например, Scand J. Gastroenterol. 1996,44(3), 293-298). Связывающие 61 соединения могут быть эффективны также для профилактики фертилизации (см., например, Н. Chen et al., Chem. Biol. 1999, 6, 1-10). В соответствии с другим аспектом изобретения описанные здесь соединения и композиции можно использовать для ингибирования миграции иммунных клеток из кровотока в центральную нервную систему в случае, например, множественного склероза, или в области, которые приводят к воспалительному разрушению миелина. Предпочтительно, чтобы эти реагенты ингибировали также миграцию иммунных клеток так, чтобы при этом ингибировалось разрушение миелинового слоя и усиливалась ремиелинизация. Реагенты могут также не допускать разрушение миелинового слоя и стимулировать ремиелинизацию центральной нервной системы для врожденных метаболических расстройств, при которых инфильт- 22015388 рация иммунных клеток влияет на развитие миелиновой оболочки в основном в ЦНС. Предпочтительно,чтобы реагенты уменьшали также паралич при введении субъекту, страдающему от паралича, индуцированного связанным с демиелинизацией заболеванием или состоянием. Воспалительные заболевания, показанные для лечения описанными здесь композициями, соединениями и способами, включают общие состояния, относящиеся к демиелинизации. Гистологически, миелиновые нарушения бывают либо демиелинизирующими, либо дисмиелинизирующими. Димиелинизация означает разрушение миелина. Дисмиелинизация означает дефективное образование или поддержание миелина, вызванное дисфункцией олигодендроцитов. Предпочтительно, чтобы описанные здесь композиции и методы обеспечивали лечение заболеваний и состояний, связанных с демиелинизацией, и помощь при дисмиелинизации. Другие заболевания или состояния, показанные для лечения, включают менингит, энцефалит, повреждения спинного мозга и состояния, которые в общем индуцируют димиелинизацию в результате развития воспалительного ответа. Описанные здесь композиции, соединения и коктейли предназначены для лечения состояний и заболеваний, связанных с демиелинизацией. Такие заболевания и состояния включают, но не ограничиваются, рассеянный склероз, врожденные метаболические расстройства (например, фенилкетонурия, болезнь Тея-Сакса, болезнь Ниманна-Пика, болезнь Гоше, болезнь Гурлера, болезнь Краббе и другие лейкодистрофии), невропатии с ненормальной миелинизацией (например, болезнь Гийена-Барре, хроническая иммунная демиелинизирующая полиневропатия (CIDP), мультифокальная CIDP, синдром антиMAG, синдром GALOP, синдром анти-сульфатидных антител, синдром анти-GM2 антител, синдром POEMS, периневрит, синдром антител IgM анти-GD1b), связанную с действием лекарств демиелинизацию(например, вызванную введением хлорквина, FK506, пергексилина, прокаинамида и зимелдина), другие наследственные связанные с демиелинизацией состояния (например, углевод-дефицитный гликопротеин,синдром Коккейна, врожденная гипомиелинизация, врожденная мышечная дистрофия, болезнь Фарбера,синдром Маринеско-Шегрена, метахроматическая лейкодистрофия, болезнь Пелицеуса-Мерцбахера,болезнь Рефсума, состояния, связанные с прионами и болезнь Салла), а также другие связанные с демиелинизацией состояния (например, менингит, энцефалит или повреждения спинного мозга) или заболевания. Для исследования этих заболеваний in vivo существует множество моделей. Например, животные модели включают, но не ограничиваются, следующие. Рассеянный склероз. Наиболее распространенным демиелинизирующим заболеванием является рассеянный склероз, но к дефициту или нарушениям миелинизации приводит и множество других метаболических и воспалительных заболеваний. Рассеянный склероз (PC) представляет собой хроническое неврологическое заболевание, проявляющееся в ранней юности и с течением времени часто приводящее к инвалидности. Только в Соединенных Штатах насчитывается около 350000 случаев PC. Если не считать травм, то PC является наиболее частой причиной неврологической инвалидности у взрослых людей. Причину PC еще предстоит определить. Заболевание характеризуется хроническим воспалением,демиелинизацией и глиозисом (рубцевание). Демиелинизация может приводить как к негативным, так и к позитивным эффектам на проводимость аксонов. Негативные нарушения проводимости включают замедленную проводимость аксонов, временную блокаду проводимости в присутствии высоко- но не низкочастотных последовательностей импульсов, а также полную блокаду проводимости. Позитивные нарушения включают эктопическую генерацию импульсов, спонтанную или после механического напряжения, а также ненормальные "коммуникации" между демиелинизованными экзонами. Показано, что Т-клетки, реактивные против миелиновых белков, либо основного белка миелина(ОБМ), либо миелинового протеолипидного белка (ПЛП), опосредуют воспаление ЦНС в экспериментальном аллергическом энцефаломиелите. У пациентов также наблюдался повышенный уровень иммуноглобулина (Ig) в ЦНС. Возможно также, что некоторые повреждения тканей, наблюдаемые при PC,опосредованы выработкой цитокинов активированными Т-клетками, макрофагами и астроцитами. В настоящее время 80% пациентов с диагнозом PC живут еще 20 лет после начала болезни. Методы терапии, позволяющие взять ее под контроль, включают (1) лечение, направленное на модификацию хода болезни, включая лечение острого обострения, а также на долгосрочное подавление болезни;(2) лечение симптомов PC; (3) профилактика и лечение медицинских осложнений и (4) обслуживание сопровождающего персонала и решение социальных проблем.- 23015388 Начало PC может протекать драматично, а может быть таким незаметным, что пациент даже не обращается за медицинской помощью. Самые распространенные симптомы включают слабость в конечностях, вызванное невритом оптического нерва затуманивание зрения, сенсорные нарушения, диплопию и атаксию. В дальнейшем заболевание может протекать по трем общим направлениям: (1) рецидивирующий PC, (2) хронический прогрессирующий PC и (3) неактивный PC. Рецидивирующий PC характеризуется повторяющимися приступами неврологической дисфункции. Обычно они продолжаются несколько дней или недель, после чего может наступить полное, частичное восстановление или восстановления не происходит. Промежутки между приступами могут продолжаться от нескольких недель до месяцев между максимальными проявлениями симптомов, хотя в редких случаях продолжительность ремиссии может достигать двух или более лет. Хронический прогрессирующий PC протекает как постоянное прогрессирующее ухудшение состояния без периодов стабилизации или ремиссии. Такая форма развивается у пациентов, страдавших рецидивирующим PC, хотя у 20% таких больных рецидивов не было никогда. Острые рецидивы могут возникать также в ходе прогрессирующего ухудшения. Третья форма представляет собой неактивный PC. Эта форма характеризуется фиксированным неврологическим дефицитом переменной степени выраженности. У большинства больных неактивным PC в прошлом имел место рецидивирующий PC. Течение заболевания зависит также от возраста пациента. Например, к числу благоприятных прогностических факторов относятся раннее начало заболевания (исключая детство), рецидивирующий характер и незначительная остаточная инвалидность спустя 5 лет после начала болезни. Напротив, плохой прогноз связывают с поздним началом заболевания (т.е. в 40 лет или старше) и с его прогрессирующим развитием. Эти переменные взаимозависимы, и хронический прогрессирующий PC часто начинается в более позднем возрасте, чем рецидивирующий PC. Вызванная хроническим прогрессирующим PC инвалидность обычно связана с прогрессирующей параплегией или квадриплегией (параличом) и пациентов. В соответствии с одним аспектом настоящего изобретения пациентов следует предпочтительно лечить в состоянии ремиссии, а не во время рецидива болезни. Одним специфическим терапевтическим средством лечения пациентов с острым приступом PC является кратковременное применение адренокортикотропных гормонов или пероральных кортикостероидов (например, пероральное введение преднизолона или внутривенное введение метил преднизолона). Более новые методы лечения PC включают лечение пациентов интерфероном бета-Ib, интерфероном бета-Ia и копаксоном (Copaxone, ранее назывался сополимером 1). Показано, что эти три лекарственных средства значительно снижают вероятность рецидива заболевания. Пациент самостоятельно вводит их внутримышечно или подкожно. Однако ни один из существующих методов лечения не ингибирует демиелинизация, не говоря уже о стимулировании или поддержке спонтанного ремиелинирования или уменьшения паралича. Один из аспектов настоящего изобретения включает лечение PC описанными здесь агентами самостоятельно или совместно с другими стандартными методами лечения. Врожденные метаболические расстройства. Врожденные метаболические расстройства включают фенилкетонурию (PKU) и другие аминоацидурии, болезнь Тея-Сакса, болезнь Ниманна-Пика, болезнь Гоше, болезнь Гурлера, болезнь Краббе и другие лейкодистрофии, влияющие на развитие изолирующей оболочки вокруг нервных волокон, как более подробно описано ниже.PKU представляет собой наследственное нарушение метаболизма, вызванное дефицитом фермента фенилаланингидроксилазы. Недостаток фермента приводит к задержке умственного развития, повреждению органов, необычной осанке и может, если PKU наследуется от матери, сильно осложнить беременность. На мышах разработана модель исследования PKU. Предпочтительно, чтобы младенцы с диагнозом PKU находились на диете без фенилаланина (или обедненной этой аминокислотой). Один аспект настоящего изобретения заключается в комбинировании такой диеты с описанными здесь соединениями и композициями с целью профилактики демиелинизации и ремиелинизации клеток, поврежденных заболеванием. Классическая болезнь Тея-Сакса проявляется приблизительно в возрасте 6 месяцев и приводит к смерти пациента в возрасте около 5 лет. Заболевание вызвано отсутствием фермента гексоаминидазы A(hex A), который необходим для разложения некоторых содержащихся в жирах веществ в мозге и нервных клетках. В отсутствие фермента эта вещества накапливаются и ведут к разрушению нервных клеток. Еще одна форма дефицита фермента hex А проявляется позже и называется ювенильной, хронической и взрослой формой этого заболевания. Симптомы болезни напоминают те, что характеризуют классическую болезнь Тея-Сакса. Иногда дефицит фермента проявляется и у взрослых. В настоящее время лечения заболевания/дефицита не существует, практикуется только превентивная мера внутриматочного тестирования зародыша на предмет наличия болезни. Так, описываемые здесь соединения и композиции могут быть эффективны для смягчения или профилактики процесса разрушения нервных клеток у таких пациентов. Обычно болезнь Ниманна-Пика бывает трех типов: острая инфантильная форма, тип В (менее распространенная, хроническая, не неврологическая форма) и тип С (биохимически и генетически отли- 24015388 чающаяся форма заболевания). У нормального человека холестерин клеток поступает в лизосомы для обработки, после чего выделяется из клеток. Показано, что в клетках людей, больных болезнью Ниманна-Пика, вывобождение холестерина из лизосом нарушено. Это ведет к избыточному накоплению холестерина в лизосомах, в результате чего процесс его обработки также нарушается. Показано, что NPC1 содержит определенные стерол-чувствительные участки, общие с другими протеинами, что наводит на мысль об их роли в регулировании обмена холестерина. Для типов А и С болезни Ниманна-Пика успешного лечения не существует. Больным формой С рекомендуют следовать низкохолестериновой диете. Таким образом, описанные здесь соединения и композиции могут быть эффективны для ослабления или профилактики процесса разрушения клеток. Болезнь Гоше представляет собой наследственное заболевание, вызванное генетической мутацией. Обычно этот ген отвечает за фермент глюкоцереброзидазу, расщепляющий в организме жир глюкоцереброзид. У больных болезнью Гоше организм не может правильно генерировать этот фермент, и жир не разрушается. Как и в случае синдрома Тея-Сакса, болезнь Гоше значительно более распространена среди потомков евреев из Восточной Европы (Ашкенази), хотя может поражать представителей любой этнической группы. Среди популяции евреев Ашкенази болезнь Гоше является наиболее распространенным генетическим расстройством и наблюдается у одного человека из 450. В целом эта болезнь поражает приблизительно одного человека из 100000. Впервые эффективное лечение болезни Гоше стало доступно в 1991 году с появлением заместительной терапии ферментами. Лечение представляет собой внутривенное введение модифицированной формы фермента глюкоцереброзидазы. Предполагается, что описанные здесь композиции и соединения можно использовать самостоятельно или, более предпочтительно, совместно с введением глюкоцереброзидазы, для лечения заболевания у страдающего им субъекта. Синдром Гурлера, называемый также мукополисахаридозом типа I, включает целый класс похожих заболеваний. Общей характеристикой всех этих заболеваний является накопление мукополисахаридов в фибробластах клеток. Генетически эти заболевания неразличимы. Трансплантация фибробластов и костного мозга не помогает, так что необходимы соединения и композиции, способные ослабить тяжесть заболевания и его развитие. С этой целью субъекту можно вводить описанные здесь соединения и композиции соединений настоящего изобретения. Болезнь Краббе (называемая также лейкодистрофией глобоидных клеток) представляет собой аутосомальное рецессивное состояние, вызванное дефицитом галактозилцерамидазы (или галактоцереброзидазы), лизосомального фермента, катаболизирующего основной липидный компонент миелина. Во Франции вероятность такого заболевания составляет приблизительно один случай на 150000 рождений. Заболевание приводит к демиелинизации центральной и периферической нервной системы. Обычно болезнь начинается в течение первого года жизни, после чего быстро прогрессирует, но сообщалось также и о детской, юношеской и взрослой формах заболевания с менее интенсивным развитием. Диагноз ставится по результатам ферментативного анализа (дефицит галактозилцерамидазы). Имеется несколько при родных животных моделей заболевания (мышь, собака, обезьяна). Как и у всех лейкодистрофий, у болезни Краббе не существует эффективных методов лечения. Один из аспектов настоящего изобретения связан с использованием описанных здесь соединений и композиций для лечения или ослабления болезни Краббе и других лейкодистрофий. Лейкодистрофии представляют собой группу наследственных прогрессирующих заболеваний, затрагивающих головной, спинной мозг и периферическую нервную систему. Они включают адренолейкодистрофию (ALD), адреномиелонефропатию (AMN), синдром Айкарди-Гутье, болезнь Александера,САСН (т.е. детскую атаксию с гипермиелинизацией центральной нервной системы и утратой белого вещества), CADASIL (т.е. церебральную аутосомальную доминантную артериопатию с субкортикальными инфарктами и лейкоэнцефалопатией), болезнь Канавана (дегенерацию губчатого тела), церебральносухожильный ксантоматоз (СТХ), болезнь Краббе (обсуждалась ранее), метахроматическую лейкодистрофию (МЛД), неонатальную адренолейкодистрофию, синдром овариолейкодистрофии, болезнь Пелицеуса-Мерцбахера (Х-связанную спастическую паралгию), болезнь Рефсума, синдром Ван дер Кнаапа(вакулирующая лейкодистрофия с субкортикальными кистами) и синдром Целлвегера. Не существует эффективного лечения ни для одного из перечисленных заболеваний, не говоря уже о полном выздоровлении. Таким образом, имеется выраженная потребность в средствах для лечения или облегчения симптомов заболевания, таких как описываемые здесь композиции и соединения.- 25015388 Невропатии с ненормальной миелинизацией. Существует множество хронических иммунных полиневропатий, приводящих к демиелинированию у пациентов. Возраст начала заболевания зависит от его конкретного типа. Существует стандартное лечение указанных болезней, его можно сочетать с рассматриваемыми здесь композициями и соединениями. Альтернативно, рассматриваемые здесь композиции и соединения можно использовать самостоятельно. Существующие стандартные методы лечения включают следующие. Таблица 5 Демиелинизация, индуцированная лекарственными средствами и облучением. Некоторые лекарственные средства и облучение могут вызывать демиелинизацию у субъектов. Лекарства, приводящие к демиелинизации, включают, но не ограничиваются, хлорквин, FK506, пергексилин, прокаинамид и зимелдин. Облучение также может индуцировать демиелинизацию. Полагают, что обусловленный радиацией вред для центральной нервной системы вызван (1) повреждением структуры сосудов, (2) уничтожением предшественников олигодендроцит-2 астроцитов и взрослых олигодендроцитов, (3) гибелью популяции нервных стволовых клеток в гиппокампе, мозжечке и коре головного мозга, а также распространенными изменениями экспрессии цитокинов. Чаще всего вред от облучения связан с лучевой терапией, применяемой при лечении некоторых видов рака, см. обзор в работе Belka et al., 2001, Br, J. Cancer 85: 1233-9. Однако значительному облучению могут подвергаться также астронавты (Hopewell, 1994, Adv. Space- 26015388 Пациенты, принимающие лекарственные средства, а также случайно или намеренно подвергающиеся действию радиации, могут с пользой для себя принимать одно из соединений или композиций,раскрытых в настоящем изобретении, чтобы не допустить демиелинизацию или вызвать ремиелинизацию. Состояния с участием демиелинизации. Дополнительные наследственные синдромы/заболевания, которые приводят к демиелинизации,включают синдром Кокейна, врожденную гипомиелинизацию, болезнь Фабера, метахроматическую лейкодистрофию, болезнь Пелицеуса-Мерцбахера, болезнь Рефсума, состояния, связанные с действием прионов, а также болезнь Салла. Синдром Кокейна (CS) представляет собой редкое наследственное заболевание, при котором люди оказываются чувствительны к солнечному свету, характеризуются маленьким ростом и проявляют признаки преждевременного старения. В классической форме синдрома Кокейна (типа I) симптомы прогрессируют и, как правило, становятся заметны в возрасте одного года. Синдром типа II характеризуется ранним началом, его признаки видны уже при рождении. Интересно, что в отличие от других связанных с повреждением ДНК заболеваний синдром Кокейна не связан с раком. CS представляет собой мультисистемное расстройство, вызывающее глубокое нарушение роста тела и мозга, а также прогрессирующую кахексию, ретинальную, кохлеарную и неврологическую денегерацию, а также лейкодистрофию и демиелирующую невропатию без развития рака. После действия ультафиолетового излучения (например, солнечного света) больные синдромом Кокейна не способны на восстановление, сопряженное с транскрипцией. На данный момент идентифицированы два гена, дефективные при синдроме Кокейна, CSA и CSB. Ген CSA содержится в хромосоме 5. Оба гена кодируют протеины, взаимодействующие с компонентами механизма транскрипции и с протеинами, обеспечивающие восстановление ДНК. В настоящее время не существует лечения или эффективной терапии больных этим синдромом. Таким образом, одним из аспектов настоящего изобретения является лечение указанного заболевания описанными здесь соединениями и композициями. Врожденная гипомиелинизация имеет несколько названий, в том числе, врожденная дисмиелинизирующая невропатия, врожденная гипомиелинизирующая полиневропатия, врожденная гипомиелинизация (луковая головка), полиневропатия, врожденная невропатия, вызванная гипомиелинизацией, гипомиелинизирующая невропатия и CHN. Наследственные периферические невропатии находятся в ряду наиболее распространенных генетических нарушений у людей и представляют собой сложную, клинически и генетически гетерогенную группу заболеваний, приводящих к прогрессирующему разрушению периферической нервной системы. Врожденная гипомиелинизация - только одно заболевание из этой группы. В целом оно включает наследственную невропатию с предрасположенностью к компрессионному параличу, наследственную невральную амиотрофию, синдром Дежерина-Сотта и врожденную гипомиелинизирующую невропатию. Для этих заболеваний не известно способов терапии или эффективного лечения. Болезнь Фарбера также имеет несколько названий, включая липогрануломатоз Фарбера, дефицит церамидазы, дефицит кислой церамидазы, дефицит АС, дефицит N-лаурилсфингозиндеацилазы и Nацилсфингозинамидогидролазы. Как видно из названий, заболевание вызвано дефицитом кислой церамидазы (называемой также N-ацилсфингозинамидогидролазой, ASAH). Отсутствие фермента приводит к накоплению несульфонированного кислого мукополисахарида в нейронах и глиальных клетках. Больные этим заболеванием обычно умирают, не дожив до двух лет. Метахроматическая лейкодистрофия (МЛД) - наследственное заболевание, вызванное дефицитом фермента арилсульфотазы А. Оно входит в группу наследственных заболеваний, называемых лейкодистрофиями, которые влияют на развитие миелиновой оболочки. Существует три формы МЛД: поздняя младенческая, детская и взрослая. В наиболее распространенной поздней младенческой (инфантильной) форме симптомы проявляются в возрасте от 6 месяцев до 2 лет. При рождении младенец обычно выглядит нормальным, но затем утрачивает первоначально приобретенные способности. Симптомы включают гипотонию (низкий мышечный тонус), нарушения речи, утрату умственных способностей, слепоту, ригидность (т.е. неконтролируемое напряжение мышц), конвульсии, нарушения глотания, паралич и деменцию. Симптомы детской формы проявляются в возрасте от 4 до 14 лет и включают ухудшение успеваемости в школе, ухудшение умственных способностей, атаксию, судороги и деменцию. В случае взрослой формы симптомы проявляются после 16 лет, они включают нарушения способности сосредотачиваться, депрессию, психические расстройства, атаксию, тремор и деменцию. Во взрослой форме могут быть и судороги, но они менее распространены, чем в других формах. Во всех формах первым признаком обычно бывают ментальные нарушения. Болезнь Пелицеуса-Мерцбахера (называемая также перинатальной суданофильной лейкодистрофией) представляет собой Х-связанное наследственное заболевание, вызывающее нарушения в строении протеолипидного протеина. Нарушения приводят к смерти младенца в возрасте приблизительно до года. Известных способов лечения заболевания не существует. Болезнь Рефсума (также называемая дефицитом оксидазы фитановой кислоты, heredopathia atacticapolyneuritiformis или наследственной моторной и сенсорной невропатией IV, HPCN IV) вызвана мута- 27015388 циями гена, кодирующего фитаноил-СоА гидроксилазу (РАНХ или PHYH). Основными клиническими проявлениями является пигментная дегенерация сетчатки, хроническая полиневропатия и признаки повреждения мозжечка. Фитановая кислота представляет собой необычную разветвленную жирную кислоту (3,7,11,15-тетраметилгексадекановую кислоту), накапливающуюся в тканях и жидкостях организма пациентов вследствие невозможности ее метаболизма (из-за отсутствия РАНХ). Выполняемый один или два раза в месяц плазмафорез эффективно выводит кислоту из организма, что позволяет ослабить жесткие требования к диете пациентов, направленные на ограничение потребления фитановой кислоты. Связанные с прионами состояния включают болезнь Герштмана-Штраусслера (GSD), болезнь Крейцфелдта-Якоба (CJD), семейную фатальную бессонницу и аберрантные изоформы прионов, которые могут функционировать как инфекционные агенты в таких расстройствах, как куру и почесуха (болезнь овец). Термин "прион" означает "протеиновый инфекционный агент" (Prusiner, Science, 216: 136-44,1982). Связанный с прионами протеин (PRP) подвергается протеолитическому расщеплению с получением амилоидогенного пептида, который полимеризуется с образованием нерастворимых фибрилл. Болезнь Салла и сиалурии других типов представляют собой заболевания, связанные с нарушениями в хранении сиаловой кислоты. Это аутосомальные рецессивные аутодегенеративные заболевания,протекающие в тяжелых формах в младенческом возрасте (инфантильные формы, т.е. ISSD), а также в виде слабо прогрессирующей формы у взрослых в основном в Финляндии (т.е. болезнь Салла). Основными симптомами являются гипотония, атаксия мозжечка и задержка умственного развития. Эти состояния и заболевания поддаются паллиативному (направленному на смягчение состояния) или мелиаративному лечению (направленному на улучшение состояния). Другие приводящие к димиелинизации состояния включают постинфекционный энцефалит (называемый также острым диссеменирующим энцефаломиелитом, ADEM), менингит и повреждения спинного мозга. Описанные здесь соединения и композиции могут также использоваться для лечения и этих демиелинизирующих состояний. Приведенные ниже примеры, демонстрирующие получение и биологические свойства соединений,предназначены для иллюстрации настоящего изобретения и никоим образом не ограничивают его объема. Если не указано иначе, все температуры выражены в градусах по Цельсию. Примеры В приведенных ниже примерах использованы следующие сокращения. Если сокращение не определено явным образом, используется общепринятое значение.- ангестремы;TLC - thin layer chromatography (тонкослойная хроматография); УФ - ультрафиолетовое излучение; вес./вес. - отношение веса к весу; вес./об. - отношение веса к объему; мкг - микрограммы; мкм - микрометры; мкМ - микромолярная концентрация. Общие методы. Флэш-хроматографию проводили на приборе Biotage Flash 75L с использованием 800 г KP-Sil кремнеземовые картриджи (32-63 мкМ, 60 , 500-550 м 2/г). Для аналитической TLC приводятся значенияRf, при этом использовались платы 250 мкМ ЕМ Sciences Silica Gel 60 F(254) толщиной 240 мкм для нормальной фазы. Спектры ЯМР получили на спектрометре Varian Gemini 300 МГц (300 МГц для спектров 1 Н и 75 МГц для спектров 13 С). Аналитическую ВЭЖХ проводили на хроматографе Agilent 1100Series HPLC с колонкой Phenomenex Luna, 3 мкм, С-18, 304,6 мм и с УФ-детекцией при длине волны 210 нм. При этом использовали растворители 0,1% ТФУ в воде и 0,1% ТФУ в ацетонитриле. Стандартная скорость потока составляла 1,5 мл/мин; в соответствии со стандартным способом градиент растворителя менялся от 20% CH3CN до 70% CH3CN за 2,33 мин. В соответствии с альтернативным способом скорость потока составляла 2 мл/мин, градиент менялся от 20% CH3CN до 70% CH3CN за 1,75 мин. В соответствии с третьим способом скорость потока составляла 1,5 мл/мин, состав растворителя менялся от 20%CH3CN до 70% CH3CN за 10 мин, затем 2 мин удерживался на уровне 70%, за 1 мин поднимался до 95% и удерживался на этом уровне еще 2 мин. LC/PC проводили на приборе Agilent 1100 Series HPLC с детектором Series 1100 PCD с ионизацией электрораспылением (если не указано, что была химическая ионизация). Колонка и условия соответствовали требованиям ВЭЖХ. Спектры 1 Н ЯМР амидов, как правило, показывают наличие ротамеров, объединение нескольких пиков отображено в виде дробных значений протонов.
МПК / Метки
МПК: C07D 409/12, A61K 31/506, C07D 417/12, C07D 239/50, C07D 405/12, C07D 401/12, A61P 29/00
Метки: заболевания, пиримидиниламидные, композиция, включающая, a4-интегринами, лечения, соединения, способ, опосредованного, фармацевтическая, варианты
Код ссылки
<a href="https://eas.patents.su/30-15388-pirimidinilamidnye-soedineniya-varianty-vklyuchayushhaya-ih-farmacevticheskaya-kompoziciya-i-sposob-lecheniya-zabolevaniya-oposredovannogo-a4-integrinami.html" rel="bookmark" title="База патентов Евразийского Союза">Пиримидиниламидные соединения (варианты), включающая их фармацевтическая композиция и способ лечения заболевания, опосредованного a4-интегринами</a>
Предыдущий патент: Способ и устройство очистки низкокачественного кремнийсодержащего материала
Следующий патент: Тригидрохлорид производного дигидроптеридиона и способ его получения
Случайный патент: Способ и колонна для отгонки изобутена