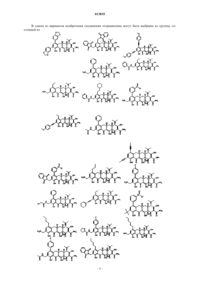
Замещенные соединения тетрациклина (варианты), фармацевтическая композиция и способ лечения чувствительного к тетрациклину состояния субъекта
Номер патента: 13835
Опубликовано: 30.08.2010
Авторы: Измаил Мохамед, Шихэн Пол, Фречетт Роджер, Нельсон Марк Л., Уорчол Тэд, Баузер Тодд, Редди Лаксма, Макинтайр Лора, Бхатиа Бина, Стэплетон Карен, Хокинс Пол, Виски Питер
Формула / Реферат
1. 7,9-Замещенные соединения тетрациклина формулы (I)
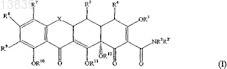
где X означает CR6'R6;
R2, R2', R4' и R4'', каждый независимо, означают водород или C1-C-4алкил;
R4 означает NR4'R4'';
R3, R8, R10, R11 и R12, каждый, означают водород;
R5 означает гидроксил или водород;
R6 и R6', каждый, означают водород или C1-C4-алкил;
R7 означает C2-C6-алкенил, C2-C6-алкинил, C5-C10-арил, C5-C10-арил-C2-C6-алкенил, C5-C10-арил-C2-C6-алкинил или C1-C6-ацил;
R9 означает нитро, C1-C4-алкил, C2-C6-алкенил, C2-C6-алкинил, C5-C10-арил, C5-C10-арил-C1-C4-алкил, амино, C5-C10-арил-C2-C6-алкенил, C5-C10-арил-C2-C4-алкинил, C1-C6-ацил или -(CH2)1-3NR9cC(=Z')ZR9a;
Z означает CR9dR9e, S, NR9b или О;
Z' означает О, S или NR9f;
R9a, R9b, R9c, R9d, R9e и R9f, каждый независимо, означают водород, C1-C6-ацил, C1-C4-алкил, C2-C6-алкенил, C2-C6-алкинил, C1-C4-алкокси, C1-C4-алкилтио, C1-C4-алкилсульфинил, C1-C4-алкилсульфонил, C1-C4-алкиламино, C5-C10-арил-C1-C4-алкил, C5-C10-арил, гетероциклический остаток, содержащий 5- или 6-членный цикл и 1-2 гетероатома, выбранных из N и О, или гетероароматический остаток, включающий один или два 5- или 6-членных цикла и 1-2 гетероатома, выбранных из N и О;
или их фармацевтически приемлемые соли при условии, что R7и R9, оба, не означают незамещенный фенил.
2. Соединения тетрациклина по п.1, отличающиеся тем, что R2, R2', R6 и R6', каждый, означают водород; R4' и R4'' означают C1-C4-алкил; a R5 означает гидроксил или водород.
3. Соединения тетрациклина по п.2, отличающиеся тем, что R4' и R4'', каждый, означают метил, a R5означает водород.
4. Соединения тетрациклина по любому из пп.1-3, отличающиеся тем, что R7 означает C5-C10-арил.
5. Соединения тетрациклина по п.4, отличающиеся тем, что R7 означает замещенный или незамещенный фенил.
6. Соединения тетрациклина по п.5, отличающиеся тем, что указанный замещенный фенил замещен по меньшей мере одним заместителем, выбранным из группы, содержащей C1-C4-алкил, C2-C6-алкенил, галоген, гидроксил, C1-C4-алкокси, C1-C4-алкилоксикарбонил, C1-C4-алкилкарбонил, C1-C4-алкиламинокарбонил, C5-C10-арилкарбонил, амино-C1-C4-алкил, аминокарбонил, амино, C1-C6-ациламино и нитро.
7. Соединения тетрациклина по п.6, отличающиеся тем, что указанный заместитель означает замещенный или незамещенный C1-C4-алкил, нитро, галоген, амино или C1-C4-алкокси.
8. Соединения тетрациклина по п.7, отличающиеся тем, что указанный галоген представлен фтором.
9. Соединения тетрациклина по п.7, отличающиеся тем, что указанный алкокси представлен метилендиокси или метоксигруппой.
10. Соединения тетрациклина по п.7, отличающиеся тем, что указанный амино представлен диалкиламиногруппой.
11. Соединения тетрациклина по п.5, отличающиеся тем, что R7 означает незамещенный фенил.
12. Соединения тетрациклина по п.62, отличающиеся тем, что R7 означает замещенный или незамещенный C1-C10-алкил.
13. Соединения тетрациклина по п.12, отличающиеся тем, что указанный алкил представлен незамещенным алкилом.
14. Соединения тетрациклина по п.13, отличающиеся тем, что указанный алкил выбран из группы, содержащей метил, этил, пропил, бутил, пентил и гексил.
15. Соединения тетрациклина по п.12, отличающиеся тем, что указанный алкил содержит цикл.
16. Соединения тетрациклина по п.15, отличающиеся тем, что указанный цикл представлен циклогексилом.
17. Соединения тетрациклина по п.12, отличающиеся тем, что указанный замещенный алкил замещен по меньшей мере одним заместителем, выбранным из группы, содержащей C5-C10-арилкарбониламино, C1-C4-алкоксикарбониламино, карбоксилат, C1-C4-алкилкарбонил, C1-C4-алкиламинокарбонил, амино, C1-C6-ациламино, амидо, гетероциклил, содержащий один или два 5- или 6-членных цикла и 1-2 гетероатома, выбранных из N и О, C5-C10-арил и гетероарил, содержащий один или два 5- или 6-членных цикла и 1-2 гетероатома, выбранных из N и О.
18. Соединения тетрациклина по п.17, отличающиеся тем, что указанным гетероциклическим заместителем является изоиндол-[1,3]-дион.
19. Соединения тетрациклина по п.17, отличающиеся тем, что указанным заместителем является C5-C10-арилкарбониламино.
20. Соединения тетрациклина по п.19, отличающиеся тем, что указанный арилкарбониламино представлен гетероарилкарбониламино.
21. Соединения тетрациклина по п.17, отличающиеся тем, что заместителем является амино или карбоксилат.
22. Соединения тетрациклина по любому из пп.1-3, отличающиеся тем, что R7 означает С1-С6-ацил.
23. Соединения тетрациклина по п.22, отличающиеся тем, что указанный ацил представлен ацетилом.
24. Соединения тетрациклина по любому из пп.1-3, отличающиеся тем, что R7 означает замещенный или незамещенный C2-C6-алкинил.
25. Соединения тетрациклина по п.24, отличающиеся тем, что указанный замещенный C2-C6-алкинил замещен по меньшей мере одним заместителем, выбранным из группы, содержащей C1-C4-алкил, амино-C1-C4-алкил, амино и C5-C10-арил.
26. Соединения тетрациклина по п.25, отличающиеся тем, что указанный алкил представлен метилом.
27. Соединения тетрациклина по п.25, отличающиеся тем, что указанный арил представлен замещенным или незамещенным фенилом.
28. Соединения тетрациклина по п.27, отличающиеся тем, что указанный замещенный фенил замещен C1-C4-алкокси.
29. Соединения тетрациклина по любому из пп.1-28 или 62, отличающиеся тем, что R9 означает замещенный или незамещенный C5-C10-арил.
30. Соединения тетрациклина по п.29, отличающиеся тем, что R9 означает замещенный или незамещенный фенил.
31. Соединения тетрациклина по п.30, отличающиеся тем, что указанный замещенный фенил замещен по меньшей мере одним заместителем, выбранным из группы, содержащей C1-C4-алкил, галоген, гидроксил, C1-C4-алкокси, амино и нитро.
32. Соединения тетрациклина по п.31, отличающиеся тем, что указанный заместитель выбран из группы, содержащей замещенный или незамещенный C1-C4-алкил, нитро, галоген, амино и C1-C4-алкокси.
33. Соединения тетрациклина по п.32, отличающиеся тем, что указанный алкокси представлен метилендиокси.
34. Соединения тетрациклина по п.30, отличающиеся тем, что R9 означает незамещенный фенил.
35. Соединения тетрациклина по любому из пп.1-3, отличающиеся тем, что R9 означает замещенный или незамещенный C1-C4-алкил.
36. Соединения тетрациклина по п.35, отличающиеся тем, что указанный алкил представлен незамещенным алкилом.
37. Соединения тетрациклина по п.36, отличающиеся тем, что указанный алкил выбран из группы, содержащей метил, этил, изопропил, н-пропил, изобутил, трет-бутил, н-бутил, пентил и гексил.
38. Соединения тетрациклина по п.35, отличающиеся тем, что указанный замещенный алкил замещен по меньшей мере одним заместителем, выбранным из группы, содержащей C5-C10-арилкарбониламино, C1-C4-алкоксикарбониламино, C1-C4-алкилкарбониламино, амино, C1-C6-ациламино, амидо, гетероциклил, содержащий один или два 5- или 6-членных цикла и 1-2 гетероатома, выбранных из N и О, C5-C10-арил и гетероарил, содержащий один или два 5- или 6-членных цикла и 1-2 гетероатома, выбранных из N и О.
39. Соединения тетрациклина по п.38, отличающиеся тем, что указанный заместитель представлен незамещенной аминогруппой.
40. Соединения тетрациклина по п.38, отличающиеся тем, что указанный заместитель представлен C1-C10-арилкарбониламиногруппой или C1-C4-алкилкарбониламиногруппой.
41. Соединения тетрациклина по п.40, отличающиеся тем, что указанная арилкарбониламиногруппа является гетероарилкарбониламиногруппой.
42. Соединения тетрациклина по п.38, отличающиеся тем, что указанным гетероциклическим заместителем является изоиндол-[1,3]-дион.
43. Соединения тетрациклина по любому из пп.1-28 или 62, отличающиеся тем, что R9 означает C1-C6-ацил.
44. Соединения тетрациклина по п.43, отличающиеся тем, что указанный ацил представлен ацетилом.
45. Соединения тетрациклина по любому из пп.1-28 или 62, отличающиеся тем, что R9 означает замещенный или незамещенный C2-C6-алкинил.
46. Соединения тетрациклина по п.45, отличающиеся тем, что указанный замещенный C2-C6-алкинил замещен по меньшей мере одним заместителем, выбранным из группы, содержащей C1-C4-алкил, C2-C6-алкенил и C5-C10-арил.
47. Соединения тетрациклина по п.46, отличающиеся тем, что указанный алкил представлен метилом.
48. Соединения тетрациклина по п.46, отличающиеся тем, что указанный арил представлен замещенным или незамещенным фенилом.
49. Соединения тетрациклина по п.48, отличающиеся тем, что указанный замещенный фенил замещен C1-C4-алкокси.
50. Соединения тетрациклина по п.46, отличающиеся тем, что указанный заместитель представлен C2-C6-алкенилом.
51. Соединение тетрациклина, выбранное из группы, состоящей из
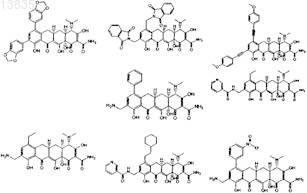
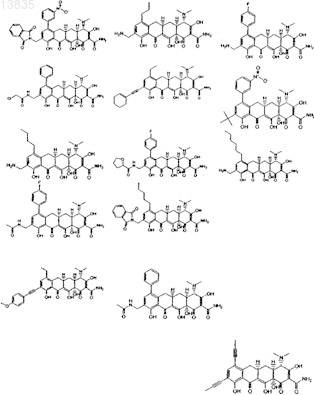
52. Способ лечения чувствительного к тетрациклину состояния субъекта, отличающийся тем, что субъекту вводят соединение тетрациклина по одному из пп.1-51 или 62 и осуществляют лечение субъекта.
53. Способ по п.52, отличающийся тем, что чувствительное к тетрациклину состояние представлено бактериальной инфекцией.
54. Способ по п.53, отличающийся тем, что бактериальная инфекция ассоциирована с Е.coli.
55. Способ по п.53, отличающийся тем, что бактериальная инфекция ассоциирована с S.aureus.
56. Способ по п.53, отличающийся тем, что бактериальная инфекция ассоциирована с Е.faecalis.
57. Способ по п.53, отличающийся тем, что бактериальная инфекция устойчива к другим тетрациклиновым антибиотикам.
58. Способ по п.52, отличающийся тем, что соединение тетрациклина вводят совместно с фармацевтически приемлемым носителем.
59. Способ по п.52, отличающийся тем, что субъектом является человек.
60. Соединение тетрациклина, выбранное из группы соединений, приведенных в табл. 2.
61. Фармацевтическая композиция для лечения чувствительного к тетрациклину состояния субъекта, отличающаяся тем, что она содержит терапевтически эффективное количество соединения тетрациклина по одному из пп.1-51 или 62 и фармацевтически приемлемый носитель.
62. 7,9-Замещенные соединения тетрациклина формулы (I)
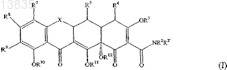
где X означает CR6'R6;
R2, R2', R4' и R4'', каждый независимо, означают водород или C1-C4-алкил;
R4 означает NR4'R4'';
R3, R8, R10, R11 и R12, каждый, означают водород;
R5 означает гидроксил или водород;
R6 и R6', каждый, означают водород или C1-C4-алкил;
R7 означает C1-C10-алкил, C5-C10-арил-C1-C4-алкил или -(СН2)1-3NR7cC(=W')WR7a;
R9 означает C2-C6-алкинил, C5-C10-арил, C5-C10-арил-C1-C4-алкил, C5-C10-арил-C2-C6-алкенил, C5-C10-арил-C2-C4-алкинил, C1-C6-ацил или -(СН2)1-3NR9cC(=Z')ZR9a;
Z означает CR9dR9e, S, NR9b или О;
Z' означает О, S или NR9f;
W означает CR7dR7e, S, NR7b или О;
W означает О, NR7fили S;
R7a, R7b, R7c, R7d, R7e, R7f, R9a, R9b, R9c, R9d, R9e и R9f, каждый независимо, означают водород, C1-C6-ацил, C1-C4-алкил, C2-C6-алкенил, C2-C6-алкинил, C1-C4-алкокси, C1-C4-алкилтио, C1-C4-алкилсульфинил, C1-C4-алкилсульфонил, C1-C4-алкиламино, C5-C10-арил-C1-C4-алкил, C5-C10-арил, гетероциклический остаток, содержащий 5- или 6-членный цикл и 1-2 гетероатома, выбранных из N и О, или гетероароматический остаток, включающий один или два 5- или 6-членных цикла и 1-2 гетероатома, выбранных из N и О;
или их фармацевтически приемлемые соли.
Текст
ЗАМЕЩЕННЫЕ СОЕДИНЕНИЯ ТЕТРАЦИКЛИНА (ВАРИАНТЫ), ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ ЧУВСТВИТЕЛЬНОГО К ТЕТРАЦИКЛИНУ СОСТОЯНИЯ СУБЪЕКТА Настоящее изобретение касается новых 7,9-замещенных тетрациклиновых соединений. Данные тетрациклиновые соединения могут быть использованы для лечения множества состояний, чувствительных к тетрациклиновым соединениям, таких как бактериальные инфекции и новообразования, а также в других известных областях применения миноциклиновых соединений в целом,таких как блокирование тетрациклинового эффлюкса и модуляции экспрессии генов. 013835 Область техники, к которой относится изобретение Изобретение относится к области медицинской химии, более конкретно - к химии антибиотиков, и,в частности, касается новых 7,9-замещенных соединений тетрациклина и их использованию для лечения множества состояний, чувствительных к тетрациклиновым соединениям, в частности бактериальных инфекций и новообразований. Уровень техники Разработка тетрациклиновых антибиотиков является прямым результатом систематического анализа бактериального состава образцов почв, собранных в различных частях земного шара, с целью обнаружения микроорганизмов, способных продуцировать бактерицидные и/или бактериостатические композиции. Первым из таких новых соединений в 1948 г. был обнаружен антибиотик под названием хлортетрациклин. Двумя годами позже был обнаружен окситетрациклин. Изучение химической структуры таких соединений подтвердило сходство их свойств и в 1952 г. явилось аналитической основой для получения третьего представителя этой группы - тетрациклина. Новое семейство соединений тетрациклина, не содержащих присоединенной к кольцу метильной группы, которая присутствовала в предыдущих препаратах тетрациклина, было получено в 1957 г. и получило широкое распространение в 1967 г., а миноциклин используется с 1972 г. Позднее исследования были сфокусированы на разработке новых композиций на основе тетрациклиновых антибиотиков, эффективных при лечении различных состояний с использованием различных способов введения. Были исследованы также новые аналоги тетрациклина с равным или более эффективным действием по сравнению с первыми соединениями тетрациклина. Примеры включают в себя патенты США 2980584, 2990331, 3062717, 3165531, 3454697, 3557280, 3674859, 3957980, 4018889,4024272 и 4126680. В этих патентах представлен широкий спектр фармацевтически активных композиций на основе тетрациклина и аналогов тетрациклина. Позднее, сразу же после их открытия и внедрения, было показано, что тетрациклины обладают чрезвычайно высокой фармакологической эффективностью в отношении риккетсий, ряда грамположительных и грамотрицательных бактерий и агентов, вызывающих венерическую лимфогранулему,конъюктивиты с включениями и пситтакоз. В связи с этим тетрациклины стали известны как антибиотики "широкого спектра". В связи с последующим исследованием их антимикробной активности in vitro,эффективности по отношению к экспериментальным инфекциям и фармакологических свойств класс тетрациклинов быстро получил широкое распространение в терапии. Однако указанное широко распространенное использование тетрациклинов для лечения как серьезных, так и неопасных заболеваний и расстройств привело к развитию устойчивости к этим антибиотикам даже среди высокочувствительных бактериальных штаммов, как симбиотических, так и патогенных (например, Pneumococci и Salmonella). Появление устойчивых к тетрациклину организмов привело к общему отказу от использования композиций на основе тетрациклина и аналогов тетрациклина. Сущность изобретения Изобретение относится к 7,9-замещенным соединениям тетрациклина формулы (I)R2, R2', R4' и R4, каждый независимо, означают водород или С 1-С 4-алкил;R5 означает гидроксил или водород;R6 и R6', каждый, означают водород или C1-C4-алкил;R9a, R9b, R9c, R9d, R9e и R9f, каждый независимо, означают водород, C1-C6-ацил, C1-C4-алкил, C2-C6 алкенил, C2-C6-алкинил, C1-C4-алкокси, С 1-С 4-алкилтио, C1-C4-алкилсульфинил, C1-C4-алкилсульфонил,C1-C4-алкиламино, C5-C10-арил-C1-C4-алкил, C5-C10-арил, гетероциклический остаток, содержащий 5- или 6-членный цикл и 1-2 гетероатома, выбранных из N и О, или гетероароматический остаток, включающий один или два 5- или 6-членных цикла и 1-2 гетероатома, выбранных из N и О; или их фармацевтически приемлемым солям при условии, что R7 и R9, оба, не означают незамещен-1 013835 ный фенил. В одном воплощении для вышеуказанных 7,9-замещенных соединений тетрациклина R2, R2', R6 и 6'R , каждый, означают водород; R4' и R4 означают C1-C4-алкил; a R5 означает гидроксил или водород. В другом воплощении для вышеуказанных 7,9-замещенных соединений тетрациклина R4' и R4, каждый, означают метил, a R5 означает водород. В другом воплощении для вышеуказанных 7,9-замещенных соединений тетрациклина R7 означаетC5-C10-арил. Согласно настоящему изобретению для вышеуказанных 7,9-замещенных соединений R7 может означать замещенный или незамещенный фенил. Кроме того, указанный замещенный фенил замещен по меньшей мере одним заместителем, выбранным из группы, содержащей C1-C4-алкил, C2-C6-алкенил,галоген,гидроксил,C1-C4-алкокси,C1-C4-алкилоксикарбонил,C1-C4-алкилкарбонил,C1-C4-алкиламинокарбонил, C5-C10-арилкарбонил, амино-C1-C4-алкил, аминокарбонил, амино,C1-C6-ациламино и нитро. Соединения тетрациклина согласно настоящему изобретению могут содержать указанный заместитель, означающий замещенный или незамещенный C1-C4-алкил, нитро, галоген, амино илиC1-C4-алкокси. Также соединения тетрациклина по настоящему изобретению могут содержать указанный галоген, представленный фтором. Соединения тетрациклина по настоящему изобретению могут содержать метилендиокси или метоксигруппу. Соединения тетрациклина по настоящему изобретению могут содержать указанный амино, представленный диалкиламиногруппой. В другом воплощении соединения тетрациклина по настоящему изобретению могут содержать R7,означающий незамещенный фенил, замещенный или незамещенный C1-C10-алкил. При этом указанный алкил может быть представлен незамещенным алкилом или выбран из группы, содержащей метил, этил,пропил, бутил, пентил и гексил. Кроме того, указанный алкил может содержать цикл, который может быть представлен циклогексилом. Также указанный замещенный алкил может быть замещен по меньшей мере одним заместителем,выбранным из группы, содержащей C5-C10-арилкарбониламино, C1-C4-алкоксикарбониламино, карбоксилат, C1-C4-алкилкарбонил, C1-C4-алкиламинокарбонил, амино, C1-C6-ациламино, амидо, гетероциклил,содержащий один или два 5- или 6-членных цикла и 1-2 гетероатома, выбранных из N и О, C5-C10-арил и гетероарил, содержащий один или два 5- или 6-членных цикла и 1-2 гетероатома, выбранных из N и О. При этом указанным гетероциклическим заместителем может являться изоиндол-[1,3]-дион илиC5-C10-арилкарбониламино, который может быть представлен гетероарилкарбониламино. В одном из вариантов изобретения R7 означает C1-C6-ацил, который может быть представлен ацетилом, замещенный или незамещенный C2-C6-алкинил, который необязательно замещен по меньшей мере одним заместителем, выбранным из группы, содержащей C1-C4-алкил, амино-C1-C4-алкил, амино иC5-C10-арил. При этом указанный алкил может быть представлен метилом, указанный арил может быть представлен замещенным или незамещенным фенилом, указанный замещенный фенил может быть замещен C1-C4-алкокси. В другом варианте настоящего изобретения R9 означает замещенный или незамещенныйC5-C10-арил, замещенный или незамещенный фенил, который необязательно замещен по меньшей мере одним заместителем, выбранным из группы, содержащей C1-C4-алкил, галоген, гидроксил,C1-C4-алкокси, амино и нитро. При этом указанный заместитель выбран из группы, содержащей замещенный или незамещенный C1-C4-алкил, нитро, галоген, амино и C1-C4-алкокси, который может быть представлен метилендиокси. Также согласно настоящему изобретению R9 может означать незамещенный фенил, замещенный или незамещенный C1-C4-алкил, который может быть представлен незамещенным алкилом, который может быть выбран из группы, содержащей метил, этил, изопропил, н-пропил, изобутил, трет-бутил,н-бутил, пентил и гексил или может быть замещен по меньшей мере одним заместителем, выбранным из группы, содержащей C5-C10-арилкарбониламино, C1-C4-алкоксикарбониламино, C1-C4-алкилкарбониламино, амино, C1-C6-ациламино, амидо, гетероциклил, содержащий один или два 5- или 6-членных цикла и 1-2 гетероатома, выбранных из N и О, C5-C10-арил и гетероарил, содержащий один или два 5- или 6 членных цикла и 1-2 гетероатома, выбранных из N и О, незамещенную аминогруппу. При этом указанная арилкарбониламиногруппа может являться гетероарилкарбониламиногруппой, а указанным гетероциклическим заместителем может являться изоиндол-[1,3]-дион. В одном воплощении изобретения R9 может означать C1-C6-ацил, необязательно представленный ацетилом, замещенный или незамещенный C2-C6-алкинил, который необязательно замещен по меньшей мере одним заместителем, выбранным из группы, содержащей C1-C4-алкил, C2-C6-алкенил и C5-C10-арил. При этом указанный алкил может быть представлен метилом, а указанный арил может быть представлен замещенным или незамещенным фенилом, который может быть замещен C1-C4-алкокси.-2 013835 В одном из вариантов изобретения соединения тетрациклина могут быть выбраны из группы, состоящей из-3 013835 В другом варианте настоящее изобретение включает способ лечения чувствительного к тетрациклину состояния субъекта, который необязательно является человеком, включающий введение соединений тетрациклина согласно настоящему изобретению. В одном из вариантов изобретения чувствительное к тетрациклину состояние представлено бактериальной инфекцией, которая может быть ассоциирована с Е.coli, S.aureus, E.faecalis. При этом бактериальная инфекция может быть устойчива к другим тетрациклиновым антибиотикам. В одном из вариантов изобретения соединение тетрациклина вводят совместно с фармацевтически приемлемым носителем. В другом варианте настоящее изобретение включает соединение тетрациклина, выбранное из группы соединений, приведенных в табл. 2. Кроме того, настоящее изобретение включает фармацевтическую композицию для лечения чувствительного к тетрациклину состояния субъекта, содержащую терапевтически эффективное количество соединения тетрациклина по настоящему изобретению и фармацевтически приемлемый носитель. В другом варианте настоящее изобретение включает 7,9-замещенные соединения тетрациклина формулы (I)R2, R2', R4' и R4, каждый независимо, означают водород или C1-C4-алкил;R5 означает гидроксил или водород;R6 и R6', каждый, означают водород или C1-C4-алкил;R7a, R7b, R7c, R7d, R7e, R7f, R9a, R9b, R9c, R9d, R9e и R9f, каждый независимо, означают водород,C1-C6-ацил, C1-C4-алкил, C2-C6-алкенил, C2-C6-алкинил, C1-C4-алкокси, C1-C4-алкилтио, C1-C4-алкилсульфинил, C1-C4-алкилсульфонил, C1-C4-алкиламино, C5-C10-арил-C1-C4-алкил, C5-C10-арил, гетероциклический остаток, содержащий 5- или 6-членный цикл и 1-2 гетероатома, выбранных из N и О, или гетероароматический остаток, включающий один или два 5- или 6-членных цикла и 1-2 гетероатома, выбранных из N и О; или их фармацевтически приемлемые соли. Изобретение относится также к способу лечения у субъекта состояния, чувствительного к соединениям тетрациклина, посредством введения субъекту соединения тетрациклина, соответствующего изобретению (например, соединения формулы I), таким образом, что чувствительное к тетрациклину состояние излечивается. Сведения, подтверждающие возможность осуществления изобретения Настоящее изобретение относится, по крайней мере частично, к новым 7,9-замещенным соединениям тетерациклина. Эти соединения могут быть использованы для лечения многочисленных чувствительных к тетрациклину состояний, таких как бактериальные инфекции и новообразования, наряду с другими известными областями применений соединений миноциклина и тетрациклина, например в качестве блокаторов тетрациклинового эффлюкса (оттока тетрациклина) и модуляции экспрессии генов. Термин "соединение тетрациклина" включает в себя множество соединений с кольцевой структурой, сходной со структурой тетрациклина. Примеры соединений тетрациклина включают в себя тетрациклин, хлортетрациклин, окситетрациклин, демеклоциклин, метациклин, санциклин, доксициклин и миноциклин. Примеры включают также другие производные и аналоги, содержащие аналогичную четырехкольцевую структуру. В табл. 1 представлены тетрациклины и несколько известных тетрациклиновых производных. Термин "7,9-замещенные соединения тетрациклина" включает в себя соединения тетрациклина, содержащие заместители в положениях 7 и 9. В одном из вариантов воплощения настоящего изобретения заместители в положениях 7 и 9 увеличивают способность соединения тетрациклина выполнять его основную предназначенную функцию, например способность лечения чувствительных к тетрациклину состояний. В варианте воплощения настоящего изобретения 7,9-замещенное соединение тетрациклина означает 7,9-замещенный тетрациклин (например, в котором R4 означает NR4'R4 , a R4' и R4 означают метил, R5 означает водород и X означает CR6R6', где R6 означает метил и R6' означает гидрокси); 7,9 замещенный доксициклин (например, в котором R4 означает NR4'R4, a R4' и R4 означают метил, R5 означает гидроксил и X означает CR6R6', где R6 означает метил и R6' означает водород) или 7,9-замещенный санциклин (в котором R4 означает NR4'R4 , a R4' и R4 означают метил, R5 означает водород и X означаетCR6R6', где R6 и R6' означают атомы водорода). В одном варианте воплощения изобретения заместитель в положении 7 в 7,9-замещенном соединении тетрациклина не относится к хлору или триметиламиногруппе. В одном варианте воплощения изобретения R4 означает водород. Изобретение включает в себя 7,9-замещенные соединения тетрациклина формулы (I)R2, R2', R4' и R4, каждый независимо, означают водород, алкил, алкенил, алкинил, алкокси, алкилтио, алкилсульфинил, алкилсульфонил, алкиламино, арилалкил, арил, гетероциклический, гетероароматический остаток или остаток пролекарства;R2', R3, R10, R11 и R12, каждый, означают водород или остаток пролекарства;R7a, R7b, R7c, R7d, R7e, R9a, R9b, R9c, R9d и R9e, каждый независимо, означают водород, ацил, алкил, алкенил, алкинил, алкокси, алкилтио, алкилсульфинил, алкилсульфонил, алкиламино, арилалкил, арил,гетероциклический, гетероароматический остаток или остаток пролекарства;R13 означает водород, гидрокси, алкил, алкенил, алкинил, алкокси, алкилтио, алкилсульфинил, алкилсульфонил, алкиламино или арилалкил иY' и Y, каждый независимо, означают водород, галоген, гидроксил, циано, сульфгидрил, амино, алкил, алкенил, алкинил, алкокси, алкилтио, алкилсульфинил, алкилсульфонил, алкиламино или арилалкил,и их фармацевтически приемлемые соли. Соединения тетрациклина, соответствующие изобретению, включают в себя, например, соединения, где X представлено CR6R6'; R4-NR4'R4; каждое из R2, R2', R6, R6', R8, R10, R11 и R12 представлено водородом; R4' и R4 представлены низшим алкилом и R5 - гидроксигруппой или водородом. В одном из вариантов осуществления каждое из R4' и R4 представлено метилом и R5 - водородом. Тетрациклиновые соединения, соответствующие изобретению, включают каждую из возможных комбинаций заместителейR7 и R9, обсуждаемых ниже. В одном из вариантов воплощения изобретения R7 представлено арилом (например, гетероарилом или замещенным или незамещенным фенилом). Фенильная группа R7 может быть замещена одним или более заместителями. Примеры заместителей фенильных групп R7 включают в себя алкил, алкенил, галоген, гидроксил, алкокси, алкилкарбонилокси, алкилоксикарбонил, арилкарбонилокси, алкоксикарбониламино, алкоксикарбонилокси, арилоксикарбонилокси, карбоксилат, алкилкарбонил, алкиламинокарбонил, арилалкиламинокарбонил, алкениламинокарбонил, арилкарбонил, аминоалкил, арилалкилкарбонил, алкенилкарбонил, алкоксикарбонил,силил, аминокарбонил, алкилтиокарбонил, фосфат, аралкил, фосфонатную группу, фосфинатную группу,циано, амино, ациламино, амидо, имино, сульгидрил, алкилтио, сульфат, арилтио, тиокарбоксилат, алкилсульфинил, сульфонатную группу, сульфамоил, сульфонамидную группу, нитро, азидную группу,гетероциклил, алкиларил, арил и гетероарил. В ряде вариантов осуществления заместитель представляет собой замещенный или незамещенный алкил (например, метил, этил, пропил, бутил и т.п.), нитро, галоген (например, фтор, бром, хлор, йод), аминогруппу (например, незамещенную аминогруппу, алкиламино, диалкиламиногруппу (например, диметиламиногруппу) или алкоксигруппу (метилендиоксигруппу или метоксигруппу).R7 может быть также замещенным или незамещенным алкилом (например, метилом, этилом, изопропилом, н-пропилом трет-бутилом, изобутилом, н-бутилом, пентилом, н-пентилом, н-гексилом или гексилом). Алкил может иметь разветвленную или неразветвленную цепь и может содержать циклическую структуру, например циклоалкильное кольцо, например циклогексильное кольцо. Алкильная группа R7 может быть замещена любым из заместителей, который позволяет тетрациклиновому соединению выполнять предназначенную ему функцию. Примеры заместителей включают в себя, но без ограничения перечисленным, алкенил, галоген (например, фтор, хлор, бром, йод), гидроксил,алкоксигруппу (например, метокси, этокси, перхлорметокси, перфторметоксигруппу и т.п.), алкилкарбонилокси, алкилоксикарбонил, арилкарбонилокси, арилкарбониламино, алкоксикарбониламино, алкоксикарбонилокси, арилоксикарбонилокси, карбоксилат, алкил карбонил, алкиламинокарбонил, арилалкиламинокарбонил, алкениламинокарбонил, арилкарбонил, аминоалкил, арилалкилкарбонил, алкенилкарбонил, алкоксикарбонил, силил, аминокарбонил, алкилтиокарбонил, фосфат, аралкил, фосфонатную группу, фосфинатную группу, циано, амино, ациламино, амидо, имино, сульфгидрил, алкилтио, сульфат,арилтио, тиокарбоксилат, алкилсульфинил, сульфонатную группу, сульфамоил, сульфонамидную группу, нитро, азидную группу, гетероциклил, алкиларил, арил и гетероарил. Примеры гетероциклических заместителей включают в себя N-изоиндол-[1,3]-дион (например, фталимид). В одном из вариантов осуществления заместитель представляет собой арилкарбониламино, например гетероарилкарбониламиногруппу. Например, гетероарильная группа может быть представлена пиридинилом. Другие примеры заместителей включают аминогруппу или карбоксилат. В другом варианте осуществления изобретения R7 представлено ацилом, например ацетилом. Еще в одном варианте осуществления R7 представляет собой замещенный или незамещенный алкинил. Примеры заместителей включают в себя заместители, которые позволяют тетрациклиновому соединению выполнять предназначенную ему функцию. Примеры заместителей включают в себя, но без ограничения перечисленным, алкил (например, метил, этил, пропил, бутил и т.п.), алкенил, галоген, гидроксил, алкокси, алкилкарбонилокси, алкилоксикарбонил, арилкарбонилокси, арилкарбониламино,алкоксикарбониламино, алкоксикарбонилокси, арилоксикарбонилокси, карбоксилат, алкилкарбонил,алкиламинокарбонил, арилалкиламинокарбонил, алкениламинокарбонил, арилкарбонил, аминоалкил,арилалкилкарбонил, алкенилкарбонил, алкоксикарбонил, силил, аминокарбонил, алкилтиокарбонил,фосфат, аралкил, фосфонатную группу, фосфинатную группу, циано, амино, ациламино, амидную группу, имино, сульфгидрил, алкилтио, сульфат, арилтио, тиокарбоксилат, алкилсульфинил, сульфонатную группу, сульфамоил, сульфонамидную группу, нитро, азидную группу, гетероциклил, алкиларил, арил и гетероарил. В следующем варианте осуществления арильный заместитель представляет собой замещенный или незамещенный фенил. Фенил может быть также дальше замещен одним или более заместителями, которые позволяют тетрациклиновому соединению выполнять предназначенную ему функцию. Примеры заместителей включают в себя, но без ограничения перечисленным, алкоксигруппу (например, метоксигруппу).-6 013835 Тетрациклиновые соединения, соответствующие изобретению, включают соединения, в которых R9 представляет собой замещенный или незамещенный арил (например, карбоциклическое соединение или гетероарил). В одном из вариантов изобретения R9 - замещенный или незамещенный фенил. Замещенная фенильная группа может быть замещена любым заместителем или комбинацией заместителей, которые позволяют тетрациклиновому соединению выполнять предназначенную ему функцию. Примеры заместителей включают в себя, но без ограничения перечисленным, алкил, алкенил, галоген, гидроксил, алкокси, алкилкарбонилокси, алкилоксикарбонил, арилкарбонилокси, алкоксикарбониламино, алкоксикарбонилокси, арилоксикарбонилокси, карбоксилат, алкилкарбонил, алкиламинокарбонил, арилалкиламинокарбонил, алкениламинокарбонил, арилкарбонил, аминоалкил, арилалкилкарбонил, алкенилкарбонил,алкоксикарбонил, силил, аминокарбонил, алкилтиокарбонил, фосфат, аралкил, фосфонатную группу,фосфинатную группу, циано, амино, ациламино, амидную группу, имино, сульфгидрил, алкилтио, сульфат, арилтио, тиокарбоксилат, алкилсульфинил, сульфонатную группу, сульфамоил, сульфонамидную группу, нитро, азидную группу, гетероциклил, алкиларил, арил и гетероарил. В следующем варианте изобретения фенильный заместитель R9 представляет собой замещенный или незамещенный алкил, нитро, галоген, аминогруппу или алкоксигруппу (например, метилендиоксигруппу). Изобретение включает в себя также соединения, в которых R9 представляет собой замещенный или незамещенный алкил (например, метил, этил, изопропил, н-пропил, изобутил, трет-бутил, н-бутил, пентил, гексил и т.п.). Алкильная группа может быть замещена любым заместителем, который позволяет тетрациклиновому соединению выполнять предназначенную ему функцию. Примеры заместителей включают в себя, но без ограничения перечисленным, алкенил, галоген, гидроксил, алкокси, алкилкарбонилокси, алкилоксикарбонил, арилкарбонилокси, арилкарбониламино, алкоксикарбониламино, алкоксикарбонилокси, арилоксикарбонилокси, алкилкарбониламино, карбоксилат, алкилкарбонил, алкиламинокарбонил, арилалкиламинокарбонил, алкениламинокарбонил, арилкарбонил, аминоалкил, арилалкилкарбонил, алкенилкарбонил, алкоксикарбонил, силил, аминокарбонил, алкилтиокарбонил, фосфат, аралкил, фосфонатную группу, фосфинатную группу, циано, амино, ациламино, амидную группу, имино,сульфгидрил, алкилтио, сульфат, арилтио, тиокарбоксилат, алкилсульфинил, сульфонатную группу,сульфамоил, сульфонамидную группу, нитро, азидную группу, гетероциклил, алкиларил, арил и гетероарил. Предложен вариант изобретения, в котором данный заместитель представляет собой незамещенную аминогруппу. В следующем варианте изобретения группа R9 является аминометилом. В другом варианте алкильная группа R9 замещена арилкарбониламиногруппой (например, гетероарилкарбониламиногруппой, в частности пиридинилкарбониламиногруппой) или алкилкарбониламиногруппой. В еще одном варианте изобретения алкильная группа R9 замещена гетероциклическим заместителем, таким как изоиндол-[1,3]-дион (например, фталимид). В одном из вариантов изобретения R9 представляет собой ацил, например ацетил. В еще одном варианте изобретения R9 представляет собой замещенный или незамещенный алкинил. Алкинильная группа R9 может быть замещена любым заместителем, который позволяет тетрациклиновому соединению, соответствующему изобретению, выполнять предназначенную ему функцию. Примеры заместителей включают в себя, но без ограничения перечисленным, алкил (например,метил, этил, пропил, бутил, пентил, гексил, гептил и т.п.), алкенил, галоген, гидроксил, алкокси, алкилкарбонилокси, алкилоксикарбонил, арилкарбонилокси, арилкарбониламино, алкоксикарбониламино, алкоксикарбонилокси, арилоксикарбонилокси, карбоксилат, алкилкарбонил, алкиламинокарбонил, арилалкиламинокарбонил, алкениламинокарбонил, арилкарбонил, аминоалкил, арилалкилкарбонил, алкенилкарбонил, алкоксикарбонил, силил, аминокарбонил, алкилтиокарбонил, фосфат, аралкил, фосфонатную группу, фосфинатную группу, циано, амино, ациламино, амидную группу, имино, сульфгидрил, алкилтио, сульфат, арилтио, тиокарбоксилат, алкилсульфинил, сульфонатную группу, сульфамоил, сульфонамидную группу, нитро, азидную группу, гетероциклил, алкиларил, арил и гетероарил. В следующем варианте осуществления арилзамещенная алкинильная группа R9, например, представляет собой замещенный или незамещенный фенил. Фенил может быть замещен, например, алкоксигруппой, в частности метоксигруппой. Примеры алкенильных заместителей включают циклоалкены, такие как циклогексен. В одном из вариантов изобретения R9 не является незамещенным фенилом, когда R7 является незамещенным фенилом. Примеры 7,9-замещенных соединений тетрациклина, соответствующих изобретению, включают в себя соединения, представленные ниже, а также в табл. 2.-8 013835 Изобретение также относится к каждому из 7,9-замещенных соединений тетрациклина, перечисленных в табл. 2, а также к их фармацевтически приемлемым солям. Соединения 7,9-замещенного тетрациклина, соответствующие настоящему изобретению, могут быть синтезированы с использованием методик, представленных на схемах синтез 1-5. Некоторые 7,9-замещенные соединения тетрациклина могут быть синтезированы способом, представленным на схеме синтез 1. Несмотря на то что в каждой схеме в качестве соединения тетрациклина используют санциклин, специалисту в данной области техники представляется очевидным, что данную методику можно использовать также для других соединений тетрациклина, таких как тетрациклин и доксициклин. Более того, для 7-замещенных соединений представлены некоторые из следующих методов синтеза. Для получения соединений, замещенных в положении 9, можно следовать аналогичным методикам. Синтез 1 В основном 7,9-замещенные соединения тетрациклина могут быть синтезированы, как показано на схеме синтез 1, для получения санциклина. Санциклин (1 А) обрабатывают серной кислотой и нитратом натрия. Полученный продукт представляет собой 7,9-нитросанциклин (1 В). Затем соединение нитросанциклина обрабатывают газообразным водородом в присутствии платинового катализатора, при этом получают соединение 7,9-аминосанциклина (1 С). Чтобы синтезировать 7,9-производные,7,9-аминосанциклин обрабатывают HONO, при этом получают соль диазония (1D). Полученную соль можно потом обрабатывать множеством соединений, содержащих алкеновую функциональную группу или функциональную группу с -связью, таких как алкены, арилы и алкинилы (например, RBr), с получением 7,9-замещенного соединения санциклина (1 Е). Синтез 2 Как показано на схеме синтез 2, соединения тетрациклина по настоящему изобретению, в которыхR7 означает карбамат или производное мочевины, могут быть синтезированы по следующей методике. Санциклин (2 А) обрабатывают NaNO2 в кислотных условиях, при этом образуется 7-нитросанциклин(2 В) в смеси с изомерами в положении 9. Затем 7-нитросанциклин (2 В) обрабатывают газообразным водородом в присутствии платинового катализатора, при этом получают производное 7-аминосанциклина(2 С). Для получения производного мочевины (2 Е) проводят реакцию взаимодействия изоцианата (2D) с производным 7-аминосанциклина (2 С). Для получения карбамата (2G) проводят реакцию взаимодействия соответствующего эфира хлоругольной кислоты (2F) с производным 2 С. Синтез 3 7- и 9-Алкинилсанциклины (3 А и 3D соответственно) и 7- и 9-алкенилсанциклины (3 В и 3 Е) можно гидрировать с образованием 7- и 9-алкилзамещенных санциклиновых соединений (3 С и 3F). На схеме синтез 4 представлено избирательное гидрирование двойной и тройной связи по 7- и 9-положениям в насыщенном растворе хлористо-водородной кислоты в метаноле. Для получения продукта реакцию проводят под давлением с использованием катализатора палладия на угле. Данную реакцию можно также проводить одновременно по обоим положениям 7 и 9 с целью получения диалкилтетрациклинового соединения. Синтез 4 На схеме синтез 4 представлена общая схема синтеза производных, содержащих арил в положении 7. Показано связывание по реакции Сузуки арилбороновой кислоты с йодсанциклиновым соединением. Йодсанциклиновое соединение (4 В) может быть синтезировано из санциклина путем обработки санциклина (4 А) по меньшей мере одним эквивалентом N-йодсукцинимида (NIS) в кислых условиях. Реакцию останавливают, после чего полученный 7-йодсанциклин (4 В) может быть очищен с использованием стандартных методик, известных в области техники. Для получения арильного производного 7-йодсанциклин (4 В) обрабатывают бороновой кислотой (4 С) с добавлением водного раствора карбоната натрия и катализируют реакцию палладием. Продукт (4D) может быть очищен способами, известными в области техники, такими как ВЭЖХ (высокоэффективная жидкостная хроматография). При использовании аналогичных методик могут быть синтезированы другие 7-арил- и алкинилтетрациклиновые соединения. 7,9-Замещенные соединения тетрациклина по настоящему изобретению могут быть также синтезированы с использованием реакции перекрестного взаимодействия по Стиллу. Реакцию перекрестного взаимодействия по Стиллу можно проводить с использованием соответствующего соединения олова (например, R-SnBu3) и галогенированного соединения тетрациклина (например, 7-йодсанциклина). Соединение олова и соединение йодсанциклина могут быть обработаны в присутствии катализатора на основе палладия (например, Pd(PPh3)2Cl2 или Pd(AsPh3)2Cl2) и, при необходимости, в присутствии дополнительной соли меди, например, CuI. Полученное соединение может быть очищено методами, известными в Соединения, соответствующие изобретению, могут быть также синтезированы с использованием реакций перекрестного связывания Хек-типа. Как показано на схеме синтез 5, перекрестные связывания Хек-типа можно осуществить при использовании галогенированного тетрациклинового соединения (например, 7-йодсанциклина, 5 А), реакционноспособного алкена (5 В) или алкина (5D) и соответствующего палладиевого катализатора или катализатора, представленного другим переходным металлом. Затем полученное 7-замещенное алкенил- (5 С) или 7-замещенное алкинил- (5 Е) тетрациклиновое соединение может быть очищено методиками, известными в уровне техники. Другие замещенные тетрациклиновые соединения, соответствующие изобретению, могут быть синтезированы с использованием одного или более из следующих способов синтеза по положению либо 7-,либо 9 с последующим применением таких же или других химических способов по другому положению. Например, если группа находится в положении 7, можно использовать любой из вышеприведенных способов проведения реакции для дальнейшей дериватизации положения 9, как показано в примере 1. Термин "алкил" включает в себя насыщенные алифатические группы, включая линейные алкильные группы (например, метил, этил, пропил, бутил, пентил, гексил, гептил, октил, нонил, децил и т.п.), разветвленные алкильные группы (изопропил, трет-бутил, изобутил и т.п.), циклоалкильные (алициклические) группы (циклопропил, циклопентил, циклогексил, циклогептил, циклооктил), алкилзамещенные циклоалкильные группы и циклоалкилзамещенные алкильные группы. Термин "алкил" включает в себя,кроме того, алкильные группы, которые могут содержать атомы кислорода, азота, серы или фосфора,замещающие по меньшей мере один атом в углеводородной цепи. В одном из вариантов воплощения настоящего изобретения линейный или разветвленный алкил включает в себя 6 или менее атомов углерода в цепи (например, C1-C6 для линейной цепи, C3-C6 для разветвленной цепи) и более предпочтительно 4 или менее. Аналогичным образом, предпочтительные циклоалкилы содержат 3-8 атомов углерода в кольце и более предпочтительно 5 или 6 атомов углерода в кольце. Термин C1-C6 включает в себя алкильные группы, содержащие от 1 до 6 атомов углерода. Более того, термин "алкил" включает в себя оба понятия "незамещенные алкилы" и "замещенные алкилы", последний из которых относится к алкильным группам, содержащим заместители, замещающие водород по меньшей мере у одного атома углерода в углеводородной цепи. Такие заместители могут включать в себя, например, алкил, алкенил, алкинил, галоген, гидроксил, алкилкарбонилокси, арилкарбонилокси, алкоксикарбонилокси, арилоксикарбонилокси, карбоксилат, алкилкарбонил, арилкарбонил,алкоксикарбонил, аминокарбонил, алкиламинокарбонил, диалкиламинокарбонил, алкилтиокарбонил,алкоксил, фосфат, фосфонато, фосфинато, циано, амино (включая алкиламино, диалкиламино, ариламино, диариламино и алкилариламино), ациламино (включая алкилкарбониламино, арилкарбониламино,карбамоил и уреидо), амидино, имино, сульфгидрил, алкилтио, арилтио, тиокарбоксилат, сульфаты, алкилсульфинил, сульфонато, сульфамоил, сульфонамидо, нитро, трифторметил, азидо, гетероциклил, алкиларил или ароматический или гетероароматический остаток. Циклоалкилы могут быть также замещены, например, заместителями, описанными выше. Остаток "алкиларил" или "аралкил" означает алкил,замещенный арилом (например, фенилметил (бензил. Термин "алкил" включает в себя также боковые цепи природных и неприродных аминокислот. Термин "арил" включает в себя группы, содержащие 5- и 6-членные моноциклические ароматические группы, которые могут включать от 0 до 4 гетероатомов, например бензол, фенил, пиррол, фуран,тиофен, тиазол, изотиазол, имидазол, триазол, тетразол, пиразол, оксазол, изооксазол, пиридин, пиразин,пиридазин, пиримидин и т.п. Более того, арильные группы включают также полициклические арильные группы, например трициклические, бициклические, такие как нафталин, бензоксазол, бензодиоксазол,- 11013835 бензотиазол, бензоимидазол, бензотиофен, метилендиоксифенол, хинолин, изохинолин, нафтиридин,индол, бензофуран, пурин, деазапурин или индолизин. Такие арильные группы, содержащие в кольце гетероатомы, могут также называться "арилгетероциклами", "гетероарилами" или "гетероароматическими соединениями". Ароматическое кольцо может быть замещено по меньшей мере в одном положении кольца заместителями, описанными выше, такими как, например, галоген, гидроксил, алкокси,алкилкарбонилокси, арилкарбонилокси, алкоксикарбонилокси, арилоксикарбонилокси, карбоксилат, алкилкарбонил, алкиламинокарбонил, аралкиламинокарбонил, алкениламинокарбонил, арилкарбонил,аралкилкарбонил, алкенилкарбонил, алкоксикарбонил, аминокарбонил, алкилтиокарбонил, фосфат, фосфонато, фосфинато, циано, амино (включая алкиламино, диалкиламино, ариламино, диариламино и алкилариламино), ациламино (включая алкилкарбониламино, арилкарбониламино, карбамоил и уреидо),амидино, имино, сульфгидрил, алкилтио, арилтио, тиокарбоксилат, сульфаты, алкилсульфинил, сульфонато, сульфамоил, сульфонамидо, нитро, трифторметил, азидо, гетероциклил, алкиларил или ароматический или гетероароматический остаток. Арильные группы могут быть также конденсированными или соединены мостиковыми группами с алициклическими или гетероциклическими кольцами, которые не являются ароматическими, с образованием полициклической системы (например, тетралин). Термин "алкенил" включает в себя ненасыщенные алифатические группы, по длине и положениям возможного замещения аналогичные описанным выше алкилам, но содержащие по крайней мере одну двойную связь. Термин "алкенил" включает в себя, например, линейные алкенильные группы, (например, этенил,пропенил, бутенил, пентенил, гексенил, гептенил, октенил, ноненил, деценил и т.п.), разветвленные алкенильные группы, циклоалкенильные (алициклические) группы (циклопропенил, циклопентенил, циклогексенил, циклогептенил, циклооктенил), алкил- или алкенилзамещенные циклоалкенильные группы и циклоалкил- или циклоалкенилзамещенные алкенильные группы. Термин "алкенил", кроме того, включает в себя алкенильные группы, содержащие атомы кислорода, азота, серы или фосфора, замещающие по меньшей мере один атом углерода в углеводородной цепи. В одном из вариантов воплощения настоящего изобретения линейный или разветвленный алкенил включает в себя 6 или менее атомов углерода в цепи (например, C2-C6 для линейной цепи, C3-C6 для разветвленной цепи). Аналогичным образом,циклоалкенильные группы содержат 3-8 атомов углерода в кольце и более предпочтительно 5 или 6 атомов углерода в кольце. Термин "C2-C6" включает в себя алкенильные группы, содержащие от 2 до 6 атомов углерода. Более того, термин "алкенил" включает в себя оба понятия: "незамещенные алкенилы" и "замещенные алкенилы", последний из которых относится к алкенильным группам, содержащим заместители, замещающие водород по меньшей мере у одного атома углерода в углеводородной цепи. Такие заместители могут включать, например, алкил, алкинил, галоген, гидроксил, алкилкарбонилокси, арилкарбонилокси, алкоксикарбонилокси, арилоксикарбонилокси, карбоксилат, алкилкарбонил, арилкарбонил, алкоксикарбонил, аминокарбонил, алкиламинокарбонил, диалкиламинокарбонил, алкилтиокарбонил, алкоксил,фосфат, фосфонато, фосфинато, циано, амино (включая алкиламино, диалкиламино, ариламино,диариламино и алкилариламино), ациламино (включая алкилкарбониламино, арилкарбониламино, карбамоил и уреидо), амидино, имино, сульфгидрил, алкилтио, арилтио, тиокарбоксилат, сульфаты, алкилсульфинил, сульфонато, сульфамоил, сульфонамидо, нитро, трифторметил, азидо, гетероциклил,алкиларил или ароматический или гетероароматический остаток. Термин "алкинил" включает в себя ненасыщенные алифатические группы, которые по длине и положениям возможного замещения аналогичны описанным выше алкилам, но содержат по крайней мере одну тройную связь. Например, термин "алкинил" включает в себя линейные алкинильные группы, (например, этинил,пропинил, бутинил, пентинил, гексинил, гептинил, октинил, нонинил, децинил и т.п.), разветвленные алкинильные группы и циклоалкил- или циклоалкенилзамещенные алкинильные группы. Термин "алкенил" включает в себя также алкинильные группы, которые содержат атомы кислорода, азота, серы или фосфора, замещающие по меньшей мере один атом углерода в углеводородной цепи. В одном из вариантов воплощения настоящего изобретения линейный или разветвленный алкинил включает в себя 6 или менее атомов углерода в цепи (например, C2-C6 для линейной цепи, C3-C6 для разветвленной цепи). Термин "C2-C6" включает в себя алкинильные группы, содержащие от 2 до 6 атомов углерода. Более того, термин "алкинил" включает в себя оба понятия: "незамещенные алкинилы" и "замещенные алкинилы", последний из которых относится к алкинильным группам, содержащим заместители,замещающие водород по меньшей мере у одного атома углерода в углеводородной цепи. Такие заместители могут включать, например, алкил, алкинил, галоген, гидроксил, алкилкарбонилокси, арилкарбонилокси, алкоксикарбонилокси, арилоксикарбонилокси, карбоксилат, алкилкарбонил, арилкарбонил, алкоксикарбонил, аминокарбонил, алкиламинокарбонил, диалкиламинокарбонил, алкилтиокарбонил, алкоксил, фосфат, фосфонато, фосфинато, циано, амино (включая алкиламино, диалкиламино, ариламино,диариламино и алкилариламино), ациламино (включая алкилкарбониламино, арилкарбониламино, карбамоил и уреидо), амидино, имино, сульфгидрил, алкилтио, арилтио, тиокарбоксилат, сульфаты,алкилсульфинил, сульфонато, сульфамоил, сульфонамидо, нитро, трифторметил, азидо, гетероциклил,- 12013835 алкиларил или ароматический или гетероароматический остаток. Если количество атомов углерода особо не указано, термин "низший алкил", используемый в настоящем описании, означает алкильную группу, определенную выше, но содержащую в основной цепи от 1 до 5 атомов углерода. Аналогично, "низший алкенил" и "низший алкинил" имеют аналогичную длину цепи, например, содержащую от 2 до 5 атомов углерода. Термин "ацил" включает в себя соединения и остатки, содержащие ацильный радикал (СН 3 СО-) или карбонильную группу. Термин "замещенный ацил" включает в себя ацильные группы, в которых по меньшей мере один атом водорода замещен и содержит, например, такие заместители, как алкил, алкинил, галоген, гидроксил, алкилкарбонилокси, арилкарбонилокси, алкоксикарбонилокси, арилоксикарбонилокси, карбоксилат, алкилкарбонил, арилкарбонил, алкоксикарбонил, аминокарбонил, алкиламинокарбонил, диалкиламинокарбонил, алкилтиокарбонил, алкоксил, фосфат, фосфонато, фосфинато, циано,амино (включая алкиламино, диалкиламино, ариламино, диариламино и алкилариламино), ациламино(включая алкилкарбониламино, арилкарбониламино, карбамоил и уреидо), амидино, имино, сульфгидрил, алкилтио, арилтио, тиокарбоксилат, сульфаты, алкилсульфинил, сульфонато, сульфамоил, сульфонамидо, нитро, трифторметил, азидо, гетероциклил, алкиларил или ароматический или гетероароматический остаток. Термин "ациламино" включает в себя остатки, в которых ацильный остаток присоединен к аминогруппе. Например, ациламино включает в себя следующие группы: алкилкарбониламино, арилкарбониламино, карбамоил и уреидо. Термин "ароил" включает в себя соединения и остатки, в которых арильный или гетероароматический остаток присоединен к карбонильной группе. Примеры ароильных групп включают фенилкарбокси,нафтилкарбокси и т.п. Термины "алкоксиалкил", "алкиламиноалкил" и "тиоалкоксиалкил" включают в себя алкильные группы, описанные выше, но содержащие атомы кислорода, азота или серы, замещающие по меньшей мере один атом углерода в углеводородной цепи, например атомы кислорода, азота или серы. Термин "алкокси" включает в себя замещенные или незамещенные алкильные, алкенильные и алкинильные группы, ковалентно связанные с атомом кислорода. Примеры алкоксигрупп включают метокси, этокси, изопропокси, пропокси, бутокси и пентокси. Примеры замещенных алкоксигрупп включают галогенированные алкоксигруппы. Алкоксигруппы могут быть замещены следующими группами: алкенил, алкинил, галоген, гидроксил, алкилкарбонилокси, арилкарбонилокси, алкоксикарбонилокси, арилоксикарбонилокси, карбоксилат, алкилкарбонил, арилкарбонил, алкоксикарбонил, аминокарбонил, алкиламинокарбонил, диалкиламинокарбонил, алкилтиокарбонил, алкоксил, фосфат, фосфонато, фосфинато, циано, амино (включая алкиламино, диалкиламино, ариламино, диариламино и алкилариламино),ациламино (включая алкилкарбониламино, арилкарбониламино, карбамоил и уреидо), амидино, имино,сульфгидрил, алкилтио, арилтио, тиокарбоксилат, сульфаты, алкилсульфинил, сульфонато, сульфамоил,сульфонамидо, нитро, трифторметил, азидо, гетероциклил, алкиларил или ароматический или гетероароматический остаток. Примеры галогенированных алкоксигрупп включают в себя, но без ограничения перечисленным, фторметокси, дифторметокси, трифторметокси, хлорметокси, дихлорметокси, трихлорметокси и т.п. Термин "амин" или "амино" включает в себя соединения, в которых атом азота ковалентно связан по крайней мере с одним атомом углерода или гетероатомом. Термин "алкиламино" включает в себя группы и соединения, в которых атом азота связан по крайней мере с одной дополнительной алкильной группой. Термин "диалкиламино" включает в себя группы, в которых атом азота связан по крайней мере с двумя дополнительными алкильными группами. Термин "ариламино" и "диариламино" включает в себя группы, в которых атом азота связан по крайней мере с одной или двумя арильными группами соответственно. Термин "алкилариламино", "алкиламиноарил" или "ариламиноалкил" означает аминогруппу, которая связана по крайней мере с одной алкильной группой и по крайней мере с одной арильной группой. Термин "алкаминоалкил" означает алкильную, алкенильную или алкинильную группу, связанную с атомом азота, который связан также с алкильной группой. Термин "амид" или "аминокарбонил" включает в себя соединения или остатки, которые содержат атом азота, связанный с атомом углерода карбонильной или тиокарбонильной группы. Термин включает в себя "алкаминокарбонил" или "алкиламинокарбонил", которые содержат следующие группы: алкил,алкенил, арил или алкинил, связанные с аминогруппой, которая связана с карбонильной группой. Указанные группы включают в себя ариламинокарбонильные группы, которые включают остатки арила или гетероарила, связанные с аминогруппой, связанной с углеродом карбонильной или тиокарбонильной группы. Термины"арилкарбониламино" включают в себя термин "амид". Амиды также включают группы мочевины (аминокарбониламино) и карбаматы (оксикарбониламино).- 13013835 Термин "карбонил" или "карбокси" включает в себя соединения или остатки, которые содержат атом углерода, связанный двойной связью с атомом кислорода. Карбонил, кроме того, может быть замещен любым остатком, который обеспечивает выполнение соединением по изобретению его предназначенную функцию. Например, остатки карбонила могут содержать следующие заместители: алкилы, алкенилы, алкинилы, арилы, алкокси, амино и т.п Примеры остатков, содержащих карбонильную группу,включают в себя альдегиды, кетоны, карбоновые кислоты, амиды, сложные эфиры, ангидриды и т.п. Термин "тиокарбонил" или "тиокарбокси" включает в себя соединения и остатки, которые содержат атом углерода, присоединенный двойной связью к атому серы. Термин "простой эфир" включает в себя соединения или остатки, которые содержат атом кислорода, присоединенный к двум различным атомам углерода или гетероатомам. Например, термин включает в себя "алкоксиалкил", который означает алкильную, алкенильную или алкинильную группу, ковалентно связанную с атомом кислорода, который ковалентно связан с другой алкильной группой. Термин "сложный эфир" включает в себя соединения или остатки, которые содержат атом углерода или гетероатом, присоединенный к атому кислорода, который соединен с атомом углерода карбонильной группы. Термин "сложный эфир" включает в себя алкоксикарбоксигруппы, такие как метоксикарбонил,этоксикарбонил, пропоксикарбонил, бутоксикарбонил, пентоксикарбонил и т.п. Алкильные, алкенильные или алкинильные группы имеют значения, определенные выше. Термин "тиоэфир" включает в себя соединения или остатки, которые содержат атом серы, присоединенный к двум различным атомам углерода или гетероатомам. Примеры тиоэфиров включают в себя,без ограничения перечисленным, алктиоалкилы, алктиоалкенилы и алктиоалкинилы. Термин "алктиоалкилы" включает в себя соединения, которые содержат алкильную, алкенильную или алкинильную группу, связанную с атомом серы, соединенным с алкильной группой. Аналогичным способом термины "алктиоалкенилы" и "алктиоалкинилы" означают соединения или остатки, которые содержат алкильную, алкенильную или алкинильную группу, связанную с атомом серы, ковалентно соединенным с алкильной группой. Термин "гидрокси" или "гидроксил" включает в себя группы, содержащие -ОН или -О-. Термин "галоген" включает в себя фтор, бром, хлор, йод. Термин "пергалогенированный" в основном означает остаток, в котором все атомы водорода заменены на атомы галогена. Термины "полициклический" или "полициклический радикал" означают два или более циклических кольца (например, циклоалкилов, циклоалкенилов, циклоалкинилов, арилов и/или гетероциклилов), в которых 2 или более атомов углерода одновременно принадлежат двум соседним кольцам, например кольца являются "конденсированными". Кольца, соединенные не через соседние атомы, называются"мостиковыми" кольцами. Каждое из колец полицикла может быть замещено заместителями, такими как описано выше, например галоген, гидроксил, алкилкарбонилокси, арилкарбонилокси, алкоксикарбонилокси, арилоксикарбонилокси, карбоксилат, алкилкарбонил, алкоксикарбонил, алкиламинокарбонил,арилакиламинокарбонил, алкениламинокарбонил, арилкарбонил, арилалкилкарбонил, алкенилкарбонил,аминокарбонил, алкилтиокарбонил, алкоксил, фосфат, фосфонато, фосфинато, циано, амино (включая алкиламино, диалкиламино, ариламино, диариламино и алкилариламино), ациламино (включая алкилкарбониламино, арилкарбониламино, карбамоил и уреидо), амидино, имино, сульфгидрил, алкилтио,арилтио, тиокарбоксилат, сульфаты, алкилсульфинил, сульфонато, сульфамоил, сульфонамидо, нитро,трифторметил, азидо, гетероциклил, алкил, алкиларил или ароматический или гетероароматический остаток. Термин "гетероатом" включает в себя любой элемент, отличный от атомов углерода или водорода. Предпочтительными гетероатомами являются азот, кислород, сера и фосфор. Термин "остаток пролекарства" включает в себя остатки, которые могут метаболизироваться in vivo с образованием гидроксильной группы, или остатки, которые предпочтительно могут оставаться этерифицированными in vivo. Остатки пролекарств предпочтительно могут метаболизироваться in vivo эстеразами или по другому механизму до гидроксильных групп или других требуемых групп. Примеры пролекарств и их использования хорошо известны в данной области техники (см., например, в статье Berge etal. (1997), "Pharmaceutical salts" ("Фармацевтические соли"), J. Pharm. Sci., v. 66, p. 1-19). Некоторые пролекарства могут быть получены in situ в процессе конечного выделения и очистки соединений или отдельным взаимодействием очищенного соединения в форме свободной кислоты или гидроксила с подходящим этерифицирующим агентом. Гидроксильные группы, например, могут быть превращены в сложные эфиры путем обработки карбоновой кислотой. Примеры остатков пролекарства включают замещенные и незамещенные, разветвленные или неразветвленные низшие алкильные сложноэфирные остатки(например, сложные эфиры пропионовой кислоты), сложные эфиры низших алкенилов, сложные эфиры ди(низш.)алкиламинонизших алкилов (например, диметиламиноэтиловый сложный эфир), ациламинонизшие алкильные эфиры (например, ацетилоксиметиловый эфир), ацилокси(низш.)алкильные сложные эфиры (например, пивалоилоксиметиловый эфир), арильные сложные эфиры (фенильный сложный эфир), арил(низш.)алкиловые сложные эфиры (например, бензиловый эфир), замещенные (например,группами метил, галоген или метокси) арильные и арил(низш.)алкильные сложные эфиры, амиды,- 14013835(низш.)алкиламиды, ди(низш.)алкиламиды и гидроксиамиды. Предпочтительными остатками пролекарства являются сложные эфиры пропионовой кислоты и ацильные сложные эфиры. Следует отметить, что структуры некоторых соединений тетрациклина по настоящему изобретению включают в себя асимметрические атомы углерода. Соответственно следует понимать, что изомеры, образующиеся в связи с такой асимметрией (например, все энантиомеры и диастереомеры), включены в объем настоящего изобретения, если не указано иное. Такие изомеры могут быть получены практически полностью в очищенной форме с использованием классических методов выделения и методов стереохимического синтеза. Кроме того, структуры и другие соединения и остатки, описанные в настоящем описании, также включают в себя все их таутомеры. Изобретение относится также к способу лечения чувствительных к тетрациклину состояний у субъектов посредством введения субъекту эффективного количества 7-замещенного соединения тетрациклина по настоящему изобретению (например, соединения формулы (I) или представленного в табл. 1), способного вылечить указанное чувствительное к тетрациклину состояние. Термин "чувствительное к соединению тетрациклина состояние" включает в себя состояние, которое можно вылечить, провести его профилактику или уменьшить интенсивность его симптомов путем введения соединения тетрациклина по настоящему изобретению. Чувствительные к соединению тетрациклина состояния включают в себя бактериальные инфекции (включая состояния, устойчивые к другим соединениям тетрациклина), онкологические заболевания, диабет и другие состояния, для которых показано, что в этом случае соединения тетрациклина действенны (см., например, патенты США 5789395,5834450 и 5532227). Соединения по настоящему изобретению могут быть использованы для профилактики или борьбы с наиболее распространенными заболеваниями млекопитающих и животных, такими как диарея, инфекции мочевых путей, инфекции кожи и структуры кожи, инфекции уха, горла и носа,инфекции в ранах, маститы и т.п. Кроме того, в изобретение включены способы лечения новообразований с использованием соединений тетрациклина по настоящему изобретению (см. статью van der Bozert et al., Cancer Res., 48:66866690 (1988. Бактериальные инфекции могут быть вызваны широким спектром грамположительных и грамотрицательных бактерий. Соединения по настоящему изобретению используют в качестве антибиотиков против организмов, устойчивых к другим соединениям тетрациклина. Антибиотическую активность соединений тетрациклина по настоящему изобретению можно определить с использованием способа, который описан в примере 2, или с использованием стандартного способа разведения питательной среды in vitro,который описан в документе Waitz J.A., National Commission for Clinical Laboratory Standarts (Стандарты национальной комиссии по клиническим лабораторным методам), Document M7-A2, v. 10, No 8, p. 13-20,2nd ed., Villanova, PA (1990). Соединения тетрациклина могут быть также использованы для лечения инфекций, которые обычно лечат соединениями тетрациклина, таких как риккетсии, ряд грамположительных и грамотрицательных бактерий, а также агенты, вызывающие венерическую лимфогранулему, конъюктивиты с включениями,пситтакоз. Соединения тетрациклина могут быть использованы для лечения инфекций, например, таких как K.pneumoniae, Salmonella, E.hirae, A.baumanii, В.catarrhalis, H.influenzae, P.aeruginosa, E.faecium,E.coli, S.aureus или Е.faecalis. Согласно варианту воплощения настоящего изобретения соединение тетрациклина используют для лечения бактериальной инфекции, устойчивой к другим тетрациклиновым антибиотикам. Соединение тетрациклина по настоящему изобретению можно вводить в смеси с фармацевтически приемлемым носителем. Термин "эффективное количество" соединения означает количество, необходимое или достаточное для лечения или профилактики состояния, чувствительного к соединению тетрациклина. Эффективное количество может варьировать в зависимости от факторов, таких как размер и масса субъекта, тип заболевания или конкретное соединение тетрациклина. Например, выбор соединения тетрациклина может влиять на величину "эффективного количества". Специалист в данной области техники способен оценить вышеупомянутые факторы и сделать выводы относительно эффективного количества соединения миноциклина без дополнительных экспериментов. Изобретение относится также к способу лечения инфекций, вызванных микроорганизмами и связанных с ними заболеваний. Способы включают в себя введение субъекту эффективного количества по меньшей мере одного соединения тетрациклина.Субъектом может являться растение или предпочтительно животное, например млекопитающее, например человек. Согласно терапевтическим способам по настоящему изобретению по меньшей мере одно соединение тетрациклина по настоящему изобретению может быть введено субъекту отдельно или в более типичном случае соединение по настоящему изобретению вводят в виде компонента в составе фармацевтической композиции в смеси со стандартным наполнителем, т.е. с фармацевтически приемлемыми органическими или неорганическими веществами-носителями, подходящими для парентерального, перорального или другого требуемого способа введения, и которые не оказывают отрицательного действия посредством взаимодействия с активными соединениями, а также не оказывают отрицательного действия на реципиента.- 15013835 Изобретение относится также к фармацевтическим композициям, содержащим терапевтически эффективное количество соединения тетрациклина (например, соединение формулы (I), табл. 2 или другого соединения, описанного в данном контексте) и необязательно фармацевтически приемлемый носитель. Термин "фармацевтически приемлемый носитель" включает в себя вещества, которые могут быть введены совместно с соединением (соединениями) тетрациклина и которые обеспечивают осуществление функций соединений, т.е. лечение или профилактику состояния, чувствительного к тетрациклину. Подходящие фармацевтически приемлемые носители включают в себя, без ограничения перечисленным,воду, солевые растворы, спирт, растительные масла, полиэтиленгликоли, желатин, лактозу, амилозу,стеарат магния, тальк, кремниевую кислоту, вязкий парафин, ароматическое масло, моноглицериды жирных кислот и диглицериды, петролейные эфиры жирных кислот, гидроксиметилцеллюлозу, поливинилпирролидон и т.п. Фармацевтические препараты могут быть стерилизованы и, при необходимости,смешаны со вспомогательными агентами, например, такими как замасливатели, консерванты, стабилизаторы, увлажнители, эмульгаторы, соли для регулировки осмотического давления, буферные вещества,красители, вкусовые добавки и/или ароматические вещества и т.п., которые не оказывают отрицательного воздействия посредством взаимодействия с активными соединениями по настоящему изобретению. Соединения тетрациклина по настоящему изобретению по своей природе являются основаниями и могут образовывать множество солей с различными неорганическими и органическими кислотами. К кислотам, которые могут быть использованы для получения фармацевтически приемлемых кислотноаддитивных солей с основными по природе соединениями тетрациклина по настоящему изобретению,относятся кислоты, которые образуют нетоксичные кислотно-аддитивные соли, т.е. соли, содержащие фармацевтически приемлемые анионы, такие как гидрохлорид, гидробромид, гидройодид, нитрат, сульфат, бисульфат, фосфат, кислый фосфат, изоникотинат, ацетат, лактат, салицилат, цитрат, кислый цитрат,тартрат, пантотенат, битартрат, аскорбат, сукцинат, малеат, гентизинат, фумарат, глюконат, глюкаронат,сахарат, формиат, бензоат, глутамат, метансульфонат, этансульфонат, бензолсульфонат, птолуолсульфонат и пальмоат (т.е. 1,1'-метилен-бис-(2-гидрокси-3-нафтоат. Несмотря на то что такие соли должны быть фармацевтически приемлемыми для введения субъекту, например млекопитающему,на практике часто требуется выделять соединение тетрациклина по настоящему изобретению из реакционной смеси в виде фармацевтически неприемлемой соли, а затем просто превращать последнюю в свободное основание путем обработки щелочным реагентом с последующим превращением упомянутого свободного основания в фармацевтически приемлемую кислотно-аддитивную соль. Кислотноаддитивные соли основных соединений по настоящему изобретению легко получить путем обработки основного соединения эквивалентным количеством выбранной неорганической или органической кислоты в среде водного растворителя или в подходящем органическом растворителе, таком как метанол или этанол. После осторожного упаривания растворителя легко получить требуемую твердую соль. Получение других соединений тетрациклина по настоящему изобретению, которое подробно не описано выше в экспериментальной части, можно осуществить с использованием комбинации реакций,описанных выше и известных для специалиста в данной области техники. Соединения тетрациклина по настоящему изобретению, которые имеют кислотную природу, могут образовывать множество солей с основаниями. К химическим основаниям, которые могут быть использованы в качестве реагентов для получения фармацевтически приемлемых основных солей таких соединений тетрациклина по изобретению, которые имеют кислотную природу, относятся основания, которые образуют нетоксические основные соли таких соединений. Такие нетоксические основные соли включают в себя, без ограничения перечисленным, соли, содержащие фармацевтически приемлемые катионы,такие как катионы щелочных металлов (например, калия и натрия) и щелочно-земельных металлов (например, кальция и магния), аммония или воднорастворимые аминоаддитивные соли, такие какN-метилглюкамин-(меглюмин), а также низший алканоламмоний и другие основные соли фармацевтически приемлемых органических аминов. Фармацевтически приемлемые основно-аддитивные соли соединений тетрациклина по изобретению, которые имеют кислотную природу, могут быть получены с фармацевтически приемлемыми катионами с использованием стандартных способов. Таким образом, эти соли могут быть легко получены путем обработки соединения тетрациклина по изобретению водным раствором требуемого фармацевтически приемлемого катиона и упаривания полученного раствора досуха предпочтительно при пониженном давлении. В другом варианте раствор замещенного соединения тетрациклина по изобретению в низшем алкиловом спирте может быть смешан с алкоксидом требуемого металла и затем раствор упаривают досуха. Получение других соединений тетрациклина, соответствующих изобретению, которое не описано подробно в следующих далее экспериментах, может быть осуществлено с использованием комбинаций вышеописанных реакций, которые являются очевидными для специалистов в данной области. Соединения тетрациклина по изобретению и их фармацевтически приемлемые соли могут быть введены с помощью перорального, парентерального или местного способов введения. В основном наиболее предпочтительно вводить эти соединения в эффективных дозах в зависимости от массы и состояния субъекта, подлежащего лечению, от конкретного выбранного пути введения. Возможны варианты в зависимости от вида субъекта, подлежащего лечению, и от его индивидуальной чувствительности к упо- 16013835 мянутому лекарственному средству, а также от типа выбранного фармацевтического состава, от периода времени и интервала, через который осуществляют введение. Фармацевтические композиции по настоящему изобретению могут быть введены отдельно или в комбинации с другими известными композициями для лечения чувствительных к тетрациклину состояний у млекопитающих. Предпочтительные млекопитающие включают в себя домашних животных (например, кошки, собаки, хорьки и т.п.), сельскохозяйственный скот (крупный рогатый скот, овцы, свиньи,лошади, козы и т.п.), лабораторных животных (крысы, мыши, обезьяны и т.п.) и приматов (шимпанзе,человекообразные, гориллы). Термин "в комбинации с" известной композицией включает в себя одновременное введение композиции по изобретению и известной композиции, введение сначала композиции по изобретению с последующим введением известной композиции и введение сначала известной композиции с последующим введением композиции по изобретению. Согласно способам по настоящему изобретению может быть использована любая терапевтическая композиция, известная в данной области техники для лечения чувствительных к тетрациклину состояний. Соединения тетрациклина по настоящему изобретению могут быть введены отдельно или в комбинации с фармацевтически приемлемыми носителями или разбавителями любым из ранее упомянутых способов, и введение осуществляют в виде однократной или многократной дозы. Например, новые терапевтические агенты по настоящему изобретению могут быть эффективно введены в виде широкого спектра различных лекарственных форм, т.е. они могут быть смешаны с различными фармацевтически приемлемыми инертными носителями в форме таблеток, капсул, лепешек, пастилок, твердых капсул, порошков, спреев, кремов, бальзамов, суппозиториев, желе, гелей, паст, лосьонов, мазей, водных суспензий, растворов для инъекций, эликсиров, сиропов и т.п. Такие носители включают в себя твердые разбавители или наполнители, стерильные водные среды и различные нетоксичные органические растворители и т.п. Более того, в пероральные фармацевтические композиции могут быть добавлены подходящие подсластители и/или ароматизаторы. В основном в таких формах терапевтически эффективные соединения по настоящему изобретению содержатся при концентрации в диапазоне от приблизительно 5,0 до приблизительно 70 мас.%. Для перорального введения могут быть использованы таблетки, содержащие различные носители,такие как микрокристаллическая целлюлоза, цитрат натрия, карбонат кальция, кислый фосфат кальция и глицин, наряду с различными дезинтегрирующими агентами, такими как крахмал (предпочтительно кукурузный, картофельный крахмал или крахмал из тапиоки), альгиновая кислота и определенные комплексные силикаты в смеси со связующими гранул, такими как поливинилпирролидон, сахароза, желатин и аравийская камедь. Кроме того, для формирования таблеток в большинстве случаев используют замасливатели, такие как стеарат магния, лаурилсульфат натрия и тальк. В качестве наполнителей в желатиновых капсулах используют также твердые композиции аналогичного типа, причем предпочтительные материалы в этом случае включают также лактозу или молочный сахар, а также высокомолекулярные полиэтиленгликоли. Если требуются водные суспензии и/или эликсиры для перорального введения,активный компонент может быть смешан с различными подсластителями или ароматизаторами, красителями или пигментами и, при необходимости, с эмульгаторами и/или суспендирующими агентами наряду с разбавителями, такими как вода, этанол, пропиленгликоль, глицерин и другие их аналогичные комбинации. Для парентерального введения (включая внутрибрюшинное, подкожное, внутривенное, чрескожное или внутримышечное введение) могут быть использованы растворы терапевтического соединения по изобретению в кунжутном или арахисовом масле или в водном пропиленгликоле. В водных растворах при необходимости следует использовать буферные вещества (предпочтительно при рН выше 8) и жидкий разбавитель, который в первую очередь придает изотонические свойства. Такие водные растворы подходят для внутривенной инъекции. Масляные растворы подходят для внутрисуставной, внутримышечной и подкожной инъекциям. Получение всех таких растворов в стерильных условиях с использованием стандартных фармацевтических методов известны специалистам в данной области техники. Примеры подходящих препаратов для парентерального применения включают в себя растворы, предпочтительно масляные или водные, а также суспензии, эмульсии или имплантаты, включая суппозитории. Терапевтические соединения могут быть переработаны в стерильную форму, содержащую многократную или однократную дозу, например, в виде дисперсии в жидком носителе, таком как стерильный физиологический солевой раствор или 5%-ный солевой раствор декстрозы, которые обычно используют в составах для инъекции. Кроме того, возможно также введение соединений по настоящему изобретению местным способом при лечении воспалительных процессов на коже. Примеры способов местного введения включают чрескожный, буккальный или подъязычный. Для местного введения подходящим способом может быть смешивание терапевтических соединений в фармацевтически инертном носителе для местного введения,таком как гель, мазь, лосьон или крем. Такие носители для местного введения включают в себя воду,глицерин, спирт, пропиленгликоль, жирные спирты, триглицериды, сложные эфиры жирных кислот или минеральные масла. Другими возможными носителями для местного введения являются жидкий вазелин, изопропилпальмитат, полиэтиленгликоль, 95%-ный этанол, 5%-ный монолаурат полиоксиэтилена в- 17013835 воде, 5%-ный лаурилсульфат натрия в воде и т.п. Кроме того, при необходимости могут быть добавлены материалы, такие как антиоксиданты, увлажнители, стабилизаторы вязкости и т.п. Для энтерального введения, подходящими являются, прежде всего, таблетки, драже или капсулы,содержащие тальк и/или углеводный связующий носитель или аналогичный материал, причем в качестве носителя предпочтительно используют лактозу, и/или кукурузный крахмал, и/или картофельный крахмал. Могут быть также использованы сироп, эликсир и т.п., в которые добавляют подсластитель в качестве носителя. Могут быть получены композиции пролонгированного действия, в которых активный компонент защищен дифференциально разрушаемыми покрытиями, например, с помощью микроинкапсуляции, многокомпонентных покрытий и т.д. Кроме лечения человека, терапевтические способы лечения по настоящему изобретению имеют большое значение в ветеринарной практике, например при лечении сельскохозяйственного скота, такого как крупный рогатый скот, овцы, козы, коровы, свиньи и т.п., домашней птицы, такой как куры, утки,гуси, индейки и т.п., лошадей и домашних животных, таких как собаки и кошки. Соединения по изобретению могут быть также использованы для лечения объектов неживотного мира, таких как растения. Следует понимать, что действительные предпочтительные количества активных соединений, используемых для данного лечения, могут различаться в зависимости от конкретного используемого соединения,от конкретных полученных композиций, способа применения, специфического участка введения и т.д. Оптимальная частота введения для данной схемы введения может быть легко определена специалистами в данной области техники с использованием обычного тестирования для определения дозировки, которое осуществляют в соответствии с вышеупомянутыми рекомендациями. В основном соединения по настоящему изобретению, предназначенные для лечения, могут быть введены субъекту в дозировках, которые использовали в предшествующей практике лечения тетрациклином. См., например, издание "Physicians' Desk Reference" (Настольные рекомендации для терапевтов). Например, подходящая эффективная доза по меньшей мере одного соединения по настоящему изобретению изменяется от 0,01 до 100 мг/кг массы тела реципиента в сутки, предпочтительно от 0,1 до 50 мг/кг массы тела реципиента в сутки, более предпочтительно от 1 до 20 мг/кг массы тела реципиента в сутки. Требуемую дозу вводят один раз в сутки или в виде нескольких разделенных доз, например от 2 до 5 разделенных доз, причем введение осуществляют через определенные интервалы в течение суток или по другой соответствующей схеме введения. Следует также понимать, что с целью обеспечения эффективности введенных соединений в нормальных условиях применения необходимо принимать стандартные известные меры предосторожности при введении тетрациклинов. Прежде всего, при использовании для терапевтического лечения человека и животных in vivo, практикующий врач должен принимать все разумные меры предосторожности, чтобы исключить известные обычные отрицательные действия и токсичные эффекты. Таким образом, следует надлежащим образом учитывать определяемые обычным способом неблагоприятные реакции с учетом заболеваний желудочно-кишечного тракта и воспалительных процессов, нефротоксичности, гиперчувствительности, изменений состава крови и ухудшения всасываемости, связанного с ионами алюминия, кальция и магния. Кроме того, настоящее изобретение относится также к использованию соединения тетрациклина формулы (I) для получения лекарственных средств. Лекарственное средство может содержать фармацевтически приемлемый носитель и соединение тетрациклина в эффективном количестве, например эффективном для лечения чувствительного к тетрациклину состояния. Примеры Соединения по настоящему изобретению могут быть получены, как описано ниже, причем возможны модификации описанных ниже методик, которые очевидны для специалистов в данной области техники. Пример 1. Синтез соединений, соответствующих изобретению. 7,9-Дийодсанциклин 30,0 мл концентрированной серной кислоты при перемешивании добавляют к 1,00 г санциклина гидрохлорида полугидрата и охлаждают раствор до 0 С; 1,09 г N-йодсукцинимида порциями добавляют в раствор в течение 1 ч и мониторируют реакционную смесь с помощью ВЭЖХ и ТСХ (тонкослойной хроматографии). Реакционную смесь выливают в 250 мл ледяной воды, три раза экстрагируют н-бутанолом и удаляют растворитель при пониженном давлении. Неочищенный остаток очищают препаративной ВЭЖХ, получая 787 мг (61%) 7-йодсанциклина и 291 мг (22%) 7,9-дийодсанциклина в виде желтых и темно-желтых кристаллов соответственно. 577 мг (0,74 ммоль) 7,9-дийодсанциклина (6 С) и 8,3 мг (0,37 ммоль) ацетата палладия растворяют в 25 мл метанола в атмосфере азота. Раствор нагревают до 60 С. После перемешивания в течение 10 мин добавляют 234 мг (2,22 ммоль) карбоната натрия, а затем 246 мг (1,48 ммоль) 3,4-метилендиоксифенилбороновой кислоты (6 В). Реакция завершается через 4 ч. Реакционную смесь фильтруют через слой целита и концентрируют при пониженном давлении. Данный продукт-сырец очищают с помощью препаративной жидкостной хроматографии при использовании С 18-стационарной фазы с элюентом А: 0,1% ТФУ (трифторуксусная кислота) в воде и элюентом В: 0,1% ТФУ в ацетонитриле. Выделяют 60 мг очищенного продукта (6 С). 7-Йодсанциклин 1 г санциклина растворяют в 25 мл ТФУ, охлажденной до 0 С (на льду). В реакционную смесь вводят 1,2 экв. N-йодсукцинимида (NIS) и проводят реакцию в течение 40 мин. Реакцию снимают с ледяной бани и продолжают при комнатной температуре в течение дополнительных 5 ч. Затем смесь анализируют с помощью ВЭЖХ и ТСХ и доводят до окончания постепенным добавлением NIS. После завершения реакции ТФУ удаляют под вакуумом и добавляют 3 мл метанола, чтобы растворить остаток. Метанольный раствор медленно вводят в быстро перемешиваемый раствор диэтилового эфира с образованием зеленовато-коричневого осадка. 7-Йодизомер санциклина очищают обработкой 7-йодпродукта активированным углем, фильтрацией через целит с последующим удалением растворителя под вакуумом для получения соединения 7-изомера в виде очищенного твердого вещества желтого цвета с выходом 75%. К раствору 6,54 г (10 ммоль) трифторацетата 7-йодсанциклина добавляют 500 мг тетракистрифенилфосфинопалладата, 500 мг йодида меди (I), 100 мг ацетата палладия, 30 мл триэтиламина и 3 мл триметилсилилацетилена. Реакционную смесь перемешивают при комнатной температуре в течение 2 ч,затем фильтруют через слой целита и концентрируют. Сухой материал собирают в метаноле, нерастворимые вещества отфильтровывают. Раствор концентрируют для выделения 6,8 г продукта (7 В). 7-Тетраметилсилилэтинилсанциклин (7 В) растворяют в 300 мл метанола и перемешивают при 40 С с 6,8 г карбоната калия. Когда исходный материал перестает определяться с помощью ВЭЖХ (примерно через 3 ч), реакционную смесь охлаждают на ледяной/водяной бане и удаляют твердые вещества с помощью фильтрации. Структуру алкина (8 В) подтверждают с использованием LC (жидкостной хроматографии) и MS. Соединение 8 В используют на следующей стадии в неочищенном виде. 7-Этилсанциклин Синтез 9 10% палладиевый катализатор на угле (1 г) добавляют к 7-этинилсанциклину (8 В) в растворителе в виде метанола, насыщенного хлористо-водородной кислотой. Реакционную смесь помещают в гидрогенизатор под давлением водорода 344,75 кН/м 2. Реакцию завершают приблизительно через 8 ч. Катализатор отфильтровывают и концентрируют полученный раствор. Продукт-сырец очищают с помощью препаративной жидкостной хроматографии, используя С 18-стационарную фазу с элюентом А: 0,1% ТФУ в воде и элюентом В: 0,1% ТФУ в ацетонитриле. Объединенные очищенные фракции концентрируют и добавляют изопропанол, насыщенный хлористо-водородной кислотой. Очищенный продукт осаждают добавлением диэтилового эфира и отфильтровывают. После сушки при пониженном давлении выделяют 3,2 г 7-этилсанциклина (9 В). 7-Этил-9-йодсанциклин Синтез 10 7-Этилсанциклин (9 В, 6,7 ммоль, 3,2 г) растворяют в 75 мл метансульфоновой кислоты при комнатной температуре. N-Йодсукцинимид (10 В, 13,5 ммоль, 3,05 г) добавляют в течение 2 ч в шести порциях. Через 2 ч добавляют диэтиловый эфир, отфильтровывают осадок и высушивают его. Продукт-сырец очищают с помощью препаративной жидкостной хроматографии, используя С 18-стационарную фазу с элюентом А: 0,1% ТФУ в воде и элюентом В: 0,1% ТФУ в ацетонитриле. Выделяют 1,5 г очищенного продукта (10 С). Соединение НО (7-этил-9-циклогексенилэтинилсанциклин) Синтез 11- 20013835 К раствору 7-этилсанциклина (500 мг, 1,13 ммоль) добавляют 50 мг тетракистрифенилфосфинопалладата, 50 мг йодида меди (I), 10 мг ацетата палладия, 3 мл триэтиламина и 0,1 мл циклогексинилацетилена. Реакционную смесь перемешивают при 60 С в течение 1 ч, фильтруют через слой целита и концентрируют. Сухой материал растворяют в метаноле и фильтруют. Затем раствор концентрируют и очищают, используя препаративную жидкостную хроматографию. При проведении препаративной жидкостной хроматографии используют С 18-стационарную фазу с элюентом А: 0,1% ТФУ в воде и элюентом В: 0,1% ТФУ в ацетонитриле. Выделяют 100 мг соединения НО. 7-Йод-9-трет-бутилсанциклин Синтез 12(0,448 г, 2 ммоль). N-Йодсукцинимид (12 В) добавляют при комнатной температуре в течение 1 ч в четырех порциях. Продукт (12 С) осаждают диэтиловым эфиром, отфильтровывают и используют в другой реакции без дальнейшей очистки. Соединение ID [(7-(2-метокси-5-диметиламинометилфенил)-9-трет-бутилсанциклин)] Синтез 13 7-Йод-9-трет-бутилсанциклин (12 В, 710 мг, 1,0 ммоль) и ацетат палладия (22,4 мг, 0,1 ммоль) растворяют в 25 мл метанола в атмосфере азота. Добавляют карбонат цезия (3,25 г, 10 ммоль) и 2-метокси-5 диметиламинометилфенилбороновую кислоту (13 В, 0,435 г, 0,15 ммоль). Реакционную смесь перемешивают при 60 С в течение 2 ч, а затем фильтруют через слой целита и концентрируют при пониженном давлении. Продукт-сырец очищают препаративной жидкостной хроматографией, используя С 18-стационарную фазу с элюентом А: 0,1% ТФУ в воде и элюентом В: 0,1% ТФУ в ацетонитриле. Выделяют 210 мг соединения ID (13C). Пример 2. Определение минимальной ингибирующей концентрации (МИК) in vitro. Следующий анализ используют для определения эффективности соединений тетрациклина по отношению к распространенным бактериям. По 2 мг каждого соединения растворяют в 100 мкл ДМСО. Затем раствор добавляют в питательную среду Mueller Hinton, сбалансированную по катионам(САМНВ), до конечной концентрации соединения 200 мкг/мл. Растворы соединений тетрациклина разбавляют до 50 мкл, при этом концентрация исследуемого соединения составляет 0,098 мкг/мл. Оптическую плотность (ОП) определяют относительно свежеприготовленных культур в логарифмической фазе роста исследуемых штаммов. Готовят разбавления, в которых конечная плотность клеток составляет приблизительно 1106 КОЕ (колониеобразующих единиц)/мл. Если ОП=1, то плотность клеток для различных видов бактерий приблизительно составляет: В каждую лунку микропланшета для титрования добавляют по 50 мкл клеточной суспензии. Конечная плотность клеток составляет приблизительно 5105 КОЕ/мл. Эти планшеты инкубируют при 35 С в атмосфере окружающей среды в инкубаторе в течение приблизительно 18 ч. Планшеты считывают с использованием ридера для микропланшет и при необходимости наблюдают визуально. Величину МИК определяют в виде наименьшей концентрации соединения тетрациклина, при которой наблюдается ингибирование роста. Соединения по настоящему изобретению проявляют достаточно высокую ингибирующую активность в отношении роста бактерий.- 21013835 В табл. 3 соединения, обладающие удовлетворительным ингибированием роста конкретного штамма бактерии, обозначены знаком ; соединения, обладающие высоким ингибированием роста конкретного штамма бактерии, обозначены знаком ; соединения, обладающие чрезвычайно высоким ингибированием роста конкретного штамма бактерии, обозначены знаком . Таблица 3 Эквивалентные решения. Специалисты в данной области техники знают или способны выявить с использованием простых стандартных экспериментов множество эквивалентов специфических методов, описанных в данном контексте. Такие эквивалентные решения включены в объем притязаний настоящего изобретения и определены в формуле изобретения. Содержание всех ссылок, патентов и заявок на выдачу патентов, цитированных в данном описании, полностью включены в изобретение в качестве ссылок. Для настоящего изобретения и вариантов его воплощения могут быть выбраны соответствующие компоненты, процессы и способы, описанные в указанных патентах, заявках и других документах. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. 7,9-Замещенные соединения тетрациклина формулы (I)R2, R2', R4' и R4, каждый независимо, означают водород или C1-C-4 алкил;R5 означает гидроксил или водород;R6 и R6', каждый, означают водород или C1-C4-алкил;R9a, R9b, R9c, R9d, R9e и R9f, каждый независимо, означают водород, C1-C6-ацил, C1-C4-алкил,C2-C6-алкенил, C2-C6-алкинил, C1-C4-алкокси, C1-C4-алкилтио, C1-C4-алкилсульфинил, C1-C4-алкилсульфонил, C1-C4-алкиламино, C5-C10-арил-C1-C4-алкил, C5-C10-арил, гетероциклический остаток, содержащий 5- или 6-членный цикл и 1-2 гетероатома, выбранных из N и О, или гетероароматический остаток,включающий один или два 5- или 6-членных цикла и 1-2 гетероатома, выбранных из N и О; или их фармацевтически приемлемые соли при условии, что R7 и R9, оба, не означают незамещенный фенил. 2. Соединения тетрациклина по п.1, отличающиеся тем, что R2, R2', R6 и R6', каждый, означают водород; R4' и R4 означают C1-C4-алкил; a R5 означает гидроксил или водород. 3. Соединения тетрациклина по п.2, отличающиеся тем, что R4' и R4, каждый, означают метил, a R5 означает водород. 4. Соединения тетрациклина по любому из пп.1-3, отличающиеся тем, что R7 означает C5-C10-арил. 5. Соединения тетрациклина по п.4, отличающиеся тем, что R7 означает замещенный или незамещенный фенил. 6. Соединения тетрациклина по п.5, отличающиеся тем, что указанный замещенный фенил
МПК / Метки
МПК: C07C 237/26, A61P 31/00, A61K 31/65
Метки: замещенные, варианты, способ, состояния, чувствительного, субъекта, тетрациклину, фармацевтическая, композиция, соединения, тетрациклина, лечения
Код ссылки
<a href="https://eas.patents.su/30-13835-zameshhennye-soedineniya-tetraciklina-varianty-farmacevticheskaya-kompoziciya-i-sposob-lecheniya-chuvstvitelnogo-k-tetraciklinu-sostoyaniya-subekta.html" rel="bookmark" title="База патентов Евразийского Союза">Замещенные соединения тетрациклина (варианты), фармацевтическая композиция и способ лечения чувствительного к тетрациклину состояния субъекта</a>
Предыдущий патент: Устройство для сохранения равновесия крыльев на многосекционной жатке
Следующий патент: Способ лечения послеоперационной тошноты и рвоты
Случайный патент: Ротационное устройство с несколькими направляющими и способ ротационной штамповки