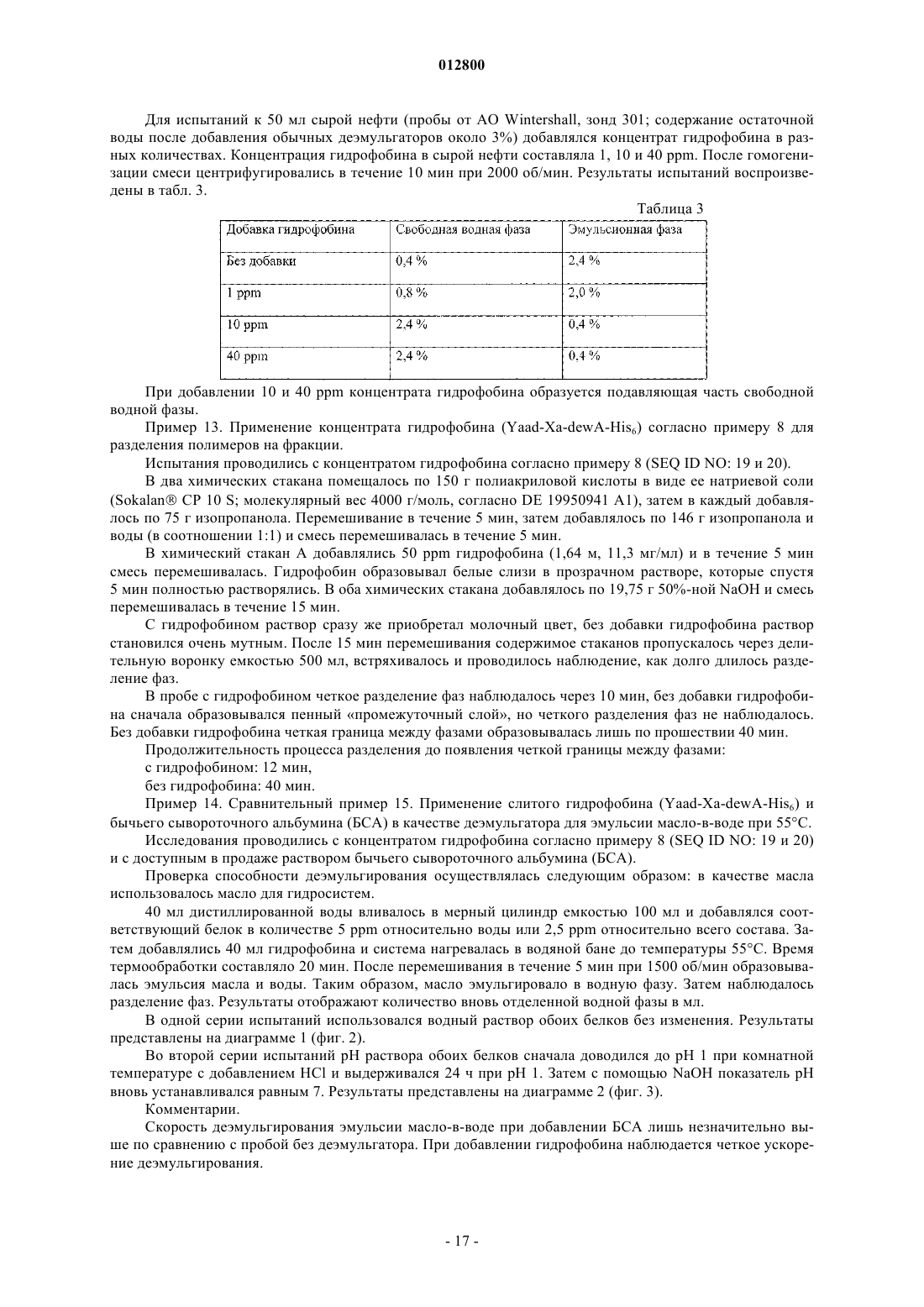
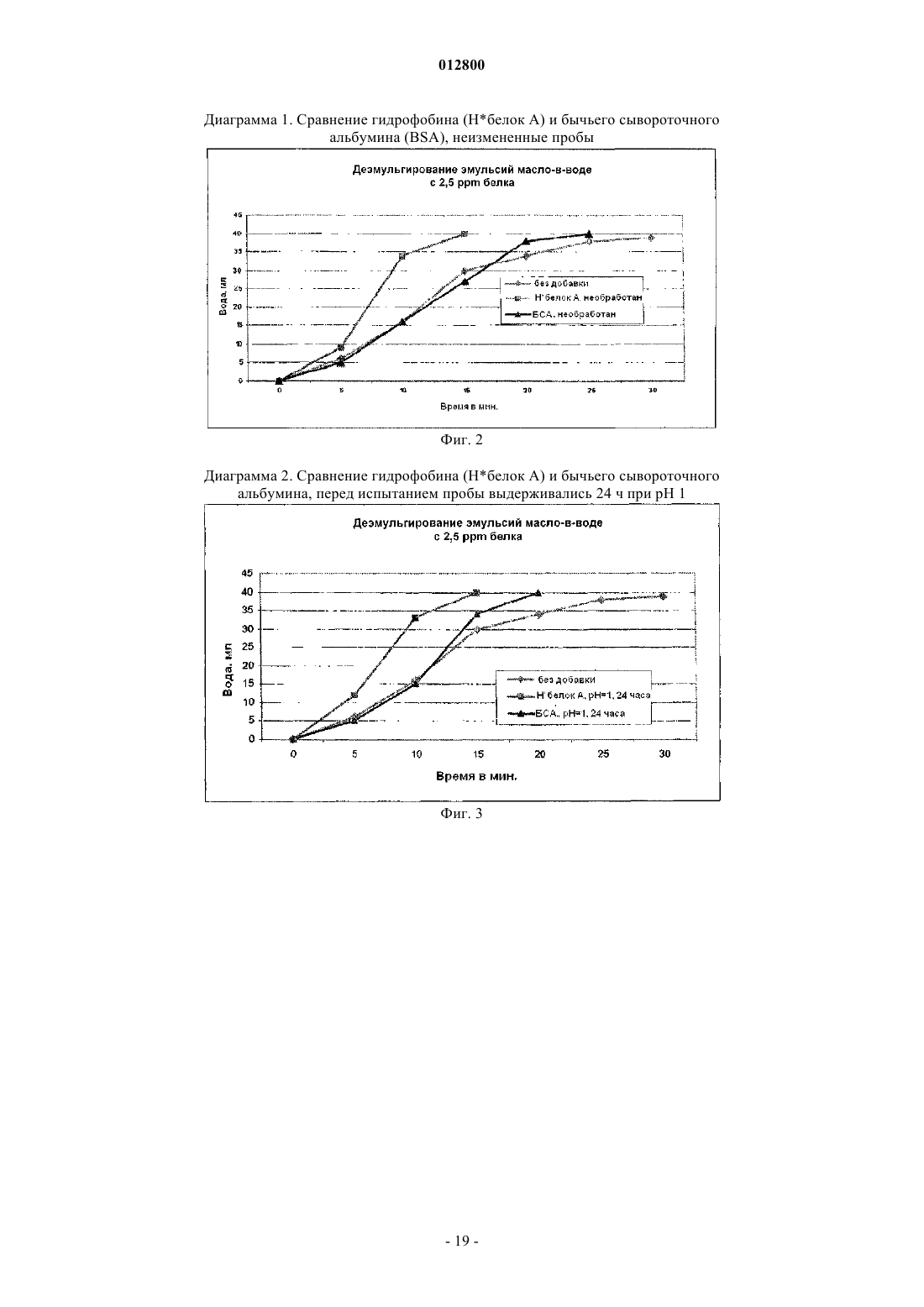
Применение белков в качестве деэмульгаторов
Номер патента: 12800
Опубликовано: 30.12.2009
Авторы: Баус Ульф, Корманн Клаудиус, Карос Марвин, Шмитт Вернер, Болльшвайлер Клаус, Зубовски Томас, Гуцманн Маркус, Кифер Матиас, Лемэр Ханс-Георг, Поссельт Дитмар
Формула / Реферат
1. Применение по меньшей мере одного гидрофобина для улучшения разделения фаз в составах, содержащих по меньшей мере две жидкие фазы.
2. Применение по п.1, причем по меньшей мере один гидрофобин является слитым гидрофобином.
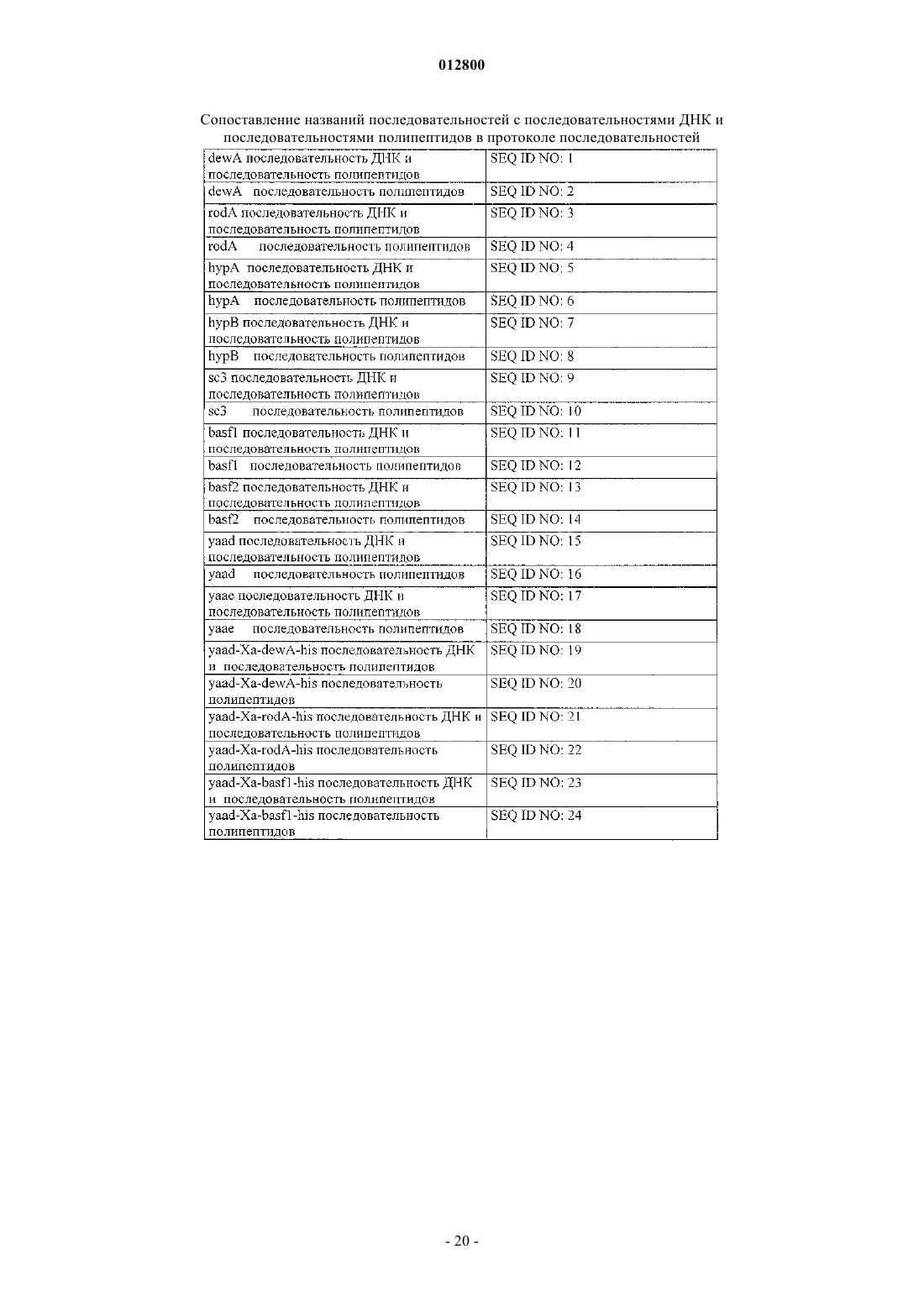
3. Применение по п.2, отличающееся тем, что для слитого гидрофобина речь идет по крайней мере об одном выбранном из группы (SEQ ID NO: 20), (SEQ ID NO: 22) или (SEQ ID NO: 24) гидрофобине.
4. Применение по одному из пп.1-3, причем состав, содержащий по меньшей мере две жидкие фазы, выбран из группы, состоящей из
составов, содержащих масло и воду;
составов, содержащих горючее или топливо и воду;
реакционных смесей, содержащих по меньшей мере две жидкие фазы.
5. Применение по одному из пп.1-4, причем используется по крайней мере один гидрофобин в количестве от 0,0001 до 1000 ppm относительно всего состава.
6. Способ разделения по крайней мере двух жидких фаз в составе, содержащем по крайней мере две жидкие фазы, включающий добавление к составу по крайней мере одного гидрофобина.
7. Способ по п.6, причем используется по крайней мере один гидрофобин в количестве от 0,0001 до 1000 ppm относительно всего состава.
8. Композиция, содержащая по крайней мере одно соединение, выбранное из группы, состоящей из горючих, топлив или растворимых в воде или в масле полимерных растворов, и по меньшей мере одного гидрофобина, причем гидрофобин содержится в композиции в количестве от 0,0001 до 1000 ppm относительно всей композиции.
9. Композиция по п.8, причем композиция содержит, по крайней мере, топливо или горючее, и гидрофобин содержится в композиции в количестве от 0,001 до 0,5 ppm относительно всей композиции.
10. Композиция по одному из пп.8 или 9, причем белок является слитым гидрофобином.
Текст
012800 Настоящее изобретение касается применения по крайней мере одного гидрофобина или, по крайней мере, его производного для улучшения фазового разделения в составах, содержащих по крайней мере две жидкие фазы, способа разделения по крайней мере двух жидких фаз в составах, состоящих по крайней мере из двух жидких фаз, а также композиций, содержащих по крайней мере одно соединение из группы,состоящей из горючего, топлива, сырой нефти или растворов полимеров, растворимых в воде или в масле, и по крайней мере одного гидрофобина или его производного. Гидрофобины - это низкомолекулярные белки из 100-500 аминокислот, характерные для нитевидных грибов, например Schizophyllum commune. Во всех случаях они имеют 8 фрагментов цистеина. Гидрофобины имеют ярко выраженное свойство разделения поверхностей раздела и поэтому годятся для покрытия поверхностей, чтобы изменить их раздел путем образования обволакивающих пленок. Таким образом, можно, например, нанести покрытие на тефлон с помощью гидрофобинов для получения гидрофильной поверхности. Гидрофобины могут быть выделены из природных источников. Известны также способы получения гидрофобинов и их производных. Например, в DE 102005007480.4 опубликованы способы получения гидрофобинов и их производных. Современный уровень техники предлагает использование гидрофобинов для различных применений.WO 96/41882 предлагает использование гидрофобинов в качестве эмульгаторов, поверхностноактивных веществ, для придания гидрофильных свойств гидрофобным поверхностям, для улучшения водостойкости гидрофильных подложек, для изготовления эмульсий масло-в-воде или вода-в-масле. Предлагаются также применения в фармакологии, например для приготовления мазей или кремов, а также в косметике как средства для защиты кожи или для изготовления шампуней или лосьонов для волос.WO 96/41882 описывает составы, содержащие гидрофобины, в особенности составы для фармацевтических применений. В патенте ЕР-А 1252516 показано покрытие окон, контактных линз, биодатчиков, медицинских приспособлений, емкостей для проведения опытов или для их хранения, корабельных корпусов, твердых частиц или рам и кузовов легковых автомобилей раствором, содержащим гидрофобины, при температуре от 30 до 80 С. В WO 03/53383 показано применение гидрофобина для обработки кератиновых материалов в косметических целях. В WO 03/10331 показано, что гидрофобины обладают поверхностно-активными свойствами. Так,показан покрытый гидрофобином датчик, например измерительный электрод, с которым связаны не ковалентно другие вещества, например электроактивные вещества, антитела или энзимы. В WO 2004/000880 также показано покрытие поверхностей гидрофобином или аналогичными ему веществами. Кроме того, показано, что даже такие эмульсии, как масло-в-воде или вода-в-масле, могут быть стабилизированы путем добавки гидрофобинов. В патенте WO 01/74864 рассматриваются также подобные гидрофинам белки и показано, что они могут использоваться для стабилизации дисперсий и эмульсий. Применение белков для разделения фаз, в принципе, известно. В GB 195876 показан способ расслоения эмульсии вода-в-масле с применением коллоидов. В качестве коллоидов приведены характерные белки, такие как желатин, казеин, альбумин, или полисахариды,такие как гуммиарабик или трагакантовая камедь. В JP-A 11-169177 показано применение белков с липазной активностью для расслоения эмульсий. В WO 01/60916 показано применение не содержащих поверхностно-активных веществ смесей по меньшей мере из одного водорастворимого белка, по меньшей мере одного водорастворимого полисахарида и по меньшей мере одного водорастворимого полимера, как, например, окиси полиэтилена для различных использований, среди прочего и для деэмульгирования сырой нефти. Ни одна из приведенных работ не указывает на применение гидрофобинов для разделения фаз. Преимущество применения белков состоит в том, что речь идет о веществах природного происхождения, которые способны к биологическому расщеплению и поэтому не загрязняют окружающую среду. Для многих операций в крупных масштабах, например для разделения эмульсий неочищенная нефть-в-воде, требуется возможно быстрое разделение фаз. Задачей изобретения было получение улучшенного способа разделения фаз с использованием белков. Согласно изобретению эта задача решается путем применения по меньшей мере одного гидрофобина для улучшения разделения фаз в составах, содержащих как минимум две жидкие фазы. При этом гидрофобин согласно изобретению может добавляться, в принципе, в любых количествах,пока не будет удостоверено, что улучшено разделение фаз в составах, содержащих как минимум две жидкие фазы. Под термином улучшение разделения фаз в рамках данного изобретения понимается, что разделение двух жидких фаз при добавлении какого-либо вещества к смеси осуществляется быстрее, чем без добавления вещества к этой же смеси, или что разделение двух жидких фаз вообще возможно только путем добавления этого вещества.-1 012800 Понятие гидрофобин в рамках данного изобретения включает также его производные, а также модифицированный гидрофобин. Относительно модифицированного и дериватизированного гидрофобинов речь может идти, например, о смеси белков с гидрофобином или о белках с аминокислотной последовательностью, которая идентична последовательности гидрофобина как минимум на 60%, например не менее 70%, лучше не менее 80%, особенно предпочтительно не менее 90%, а наиболее предпочтительно не менее 95%, и которая до 50%, например до 60%, лучше до 70% и особенно предпочтительно до 80% удовлетворяет биологическим свойствам гидрофобина, в особенности свойству, которое путем нанесения этих белков так изменяет поверхностные свойства, что увеличение краевого угла смачивания водной капли перед нанесением белка и после его нанесения на стеклянную поверхность составляет не менее 20, предпочтительно не менее 25, особенно предпочтительно не менее 30. Неожиданно было найдено, что гидрофобины или их производные улучшают разделение как минимум двух жидких фаз. Это имеет особенное преимущество, когда должно быть осуществлено быстрое разделение фаз или для предотвращения образования эмульсии. При этом уже небольшие количества действуют чрезвычайно эффективно. Это свойство может быть также использовано, если необходимо разрушить уже образовавшуюся эмульсию. Соединения, которые разрушают эмульсию, называются деэмульгаторами. Поэтому данное изобретение касается по меньшей мере одного гидрофобина или по меньшей мере одного производного гидрофобина для описанного выше применения, причем по меньшей мере один гидрофобин или по меньше мере одно производное гидрофобина используется в качестве деэмульгатора. Для определения гидрофобинов решающим является специфичность структуры, а не последовательности. Аминокислотная последовательность природных гидрофобинов очень различная, однако они все имеют очень характерный участок из 8 постоянно присутствующих цистеиновых остатков. Эти остатки образуют четыре внутримолекулярных дисульфидных мостика.N-конец и С-конец являются вариабельными в широком диапазоне. Здесь с помощью известных специалисту методов молекулярной биологии могут быть присоединены белки партнеров слияния с длиной от 10 до 500 аминокислот. Исходя из этого, под понятием гидрофобины и их производные следует понимать в смысле данного изобретения белки с аналогичной структурой и функциональной эквивалентностью. Под понятием гидрофобины в смысле данного изобретения следует понимать в дальнейшем полипептиды общей структурной формулы (I) причем X может представлять любую из 20 аминокислот природного происхождения (Phe, Leu, Ser, Tyr,Cys, Trp, Pro, His, Gln, Arg, lle Met, Thr, Asn, Lys, Val, Ala, Asp, Glu, Gly). При этом Х могут быть одинаковыми или разными. Индексы, стоящие при X, представляют собой соответственно количество аминокислот, С представляет собой цистеин, аланин, серин, глицин, метионин или треонин, причем по меньшей мере четыре из названных С групп представляют цистеины, а индексы n и m независимо друг от друга представляют собой натуральные числа от 0 до 500, предпочтительно от 15 до 300. Полипептиды согласно формулы (I) характеризуются тем свойством, что после нанесения их на стеклянную поверхность при комнатной температуре наблюдается увеличение краевого угла смачивания водной капли по меньшей мере на 20, предпочтительно не менее 25, а особенно предпочтительно на 30, по сравнению с краевым углом водной капли такого же размера на непокрытой стеклянной поверхности. Обозначенные С 1-С 8 аминокислоты являются предпочтительно цистеинами, но они могут быть заменены и другими аминокислотами подобной плотности упаковки, предпочтительно аланином, серином,треонином, метионином или глицином. Во всяком случае, по крайней мере 4, предпочтительно не менее 5, особенно предпочтительно не менее 6, а наиболее предпочтительно не менее 7 позиций от С 1 до С 8 должны быть цистеинами. Цистеины в белках согласно изобретению могут быть либо редуцированными,либо образовывать друг с другом дисульфидные мостики. Особенно предпочтительно внутримолекулярное образование С-С мостиков, в особенности по крайней мере с 1 дисульфидным мостиком, предпочтительно с 2, особенно предпочтительно с 3, и наиболее предпочтительно с 4 внутримолекулярными дисульфидными мостиками. При описанном выше замещении цистеинов аминокислотами с аналогичным объемом попарно заменяются предпочтительно такие С-позиции, которые могут образовывать между собой внутримолекулярные дисульфидные мостики. Если в позициях, обозначенных X, используются цистеины, серины, аланины, метионины или треонины, то нумерация отдельных С-позиций в общих формулах может соответствующим образом изменяться. Для реализации данного изобретения предпочтительно применялись гидрофобины общей формулы(II) где X, С и стоящие при X и С индексы имеют описанные выше значения, индексы n и m представляют-2 012800 собой числа от 0 до 300, белки выгодно характеризуются упомянутым выше свойством изменения краевого угла смачивания и по меньшей мере для 6 обозначенных С остатков речь идет о цистеине. Особенно предпочтительно наличие цистеина во всех остатках С. Особенно предпочтительно применение гидрофобинов общей формулы (III) где X, С и стоящие при X и С индексы имеют описанные выше значения, индексы n и m представляют числа от 0 до 200, белки выгодно характеризуются упомянутым выше свойством изменения краевого угла смачивания и по меньшей мере для 6 обозначенных С остатков речь идет о цистеине. Особенно предпочтительно наличие цистеина во всех остатках С. В случае остатков Xn и Xm речь может идти о последовательностях пептидов, которые также соединены естественно с гидрофобином. Однако в случае одного или обоих остатков может идти речь также о последовательностях пептидов, которые не соединены естественно с гидрофобином. Под такими остатками следует понимать остатки Xn и/или Xm, у которых встречающиеся в природе в гидрофобине последовательности пептидов удлиняются последовательностями пептидов, не встречающимися в гидрофобине в природе. В случае, если для Xn и/или Xm речь идет о не соединенных естественно в гидрофобине последовательностях пептидов, такого рода последовательности имеют, как правило, длину не менее 20, предпочтительно не менее 35, особенно предпочтительно не менее 50 и наиболее предпочтительно не менее 100 аминокислот. Такой остаток, не соединенный естественно с гидрофобином, в дальнейшем будет обозначаться также как партнер слияния. Этим будет выражаться то, что белки могут состоять по меньшей мере из гидрофобиновой части и части партнера слияния, которые в природе в таком виде вместе не существуют. Часть - партнер слияния может быть выбрана из множества белков. С гидрофобиновой частью могут также соединяться несколько партнеров слияния, например, у аминного конца (Xn) и у карбоксиконца (Xm) гидрофобиновой части. Однако с позициями (Xn или Xm) белка согласно данному изобретению могут соединяться также, например, два партнера слияния. Наиболее подходящими партнерами слияния являются белки, которые в природе встречаются в микроорганизмах, например в E.coli или Bacillus subtilis. Примерами таких партнеров слияния являются последовательности yaad (SEQ ID NO: 15 и 16), уаае (SEQ ID NO: 17 и 18) и тиоредоксин. Подходят также фрагменты или производные этих вышеназванных последовательностей, которые охватывают только часть, например 70-99%, предпочтительно 5-50% и наиболее предпочтительно 10-40% названных последовательностей, или у которых отдельные аминокислоты или, точнее говоря, нуклеотиды изменены по сравнению с названной последовательностью, причем процентные данные соответственно относятся к числу аминокислот. В другом предпочтительном варианте осуществления фузионный гидрофобин имеет кроме партнера слияния в качестве группы Xn или Xm еще так называемые домены сродства (affinity tag/affinity tail). При этом речь идет, в принципе, об известных якорных группах, которые могут взаимодействовать с некоторыми комплементарными группами и предназначаться для облегчения обработки и очистки белков. Примерами таких доменов сродства служат (His)k-, (Arg)k-, (Asp)k-, (Phe)k- или (Cys)k-группы, причем k означает в общем случае натуральное число от 1 до 10. Предпочтительно может идти речь о (His)kгруппе, причем k означает 4-6. Согласно изобретению белки, используемые в качестве гидрофобинов или производных гидрофобинов, могут также быть модифицированными в их полипептидной последовательности, например, путем гликозирования, ацетилирования или также за счет химической сшивки, например, глутаровым альдегидом. Свойством используемых согласно изобретению гидрофобинов или их производных является изменение свойств поверхностей, если поверхности покрываются белками. Изменение поверхностных свойств можно определить экспериментально, например, измеряя краевой угол капли воды до нанесения покрытия и после нанесения покрытия с белками на поверхность и определяя разницу между этими двумя измерениями. Метод измерения краевых углов в принципе известен специалисту. Измерения проводятся при комнатной температуре на капле воды в 5 мкл при использовании в качестве субстрата стеклянных пластинок. Точные экспериментальные условия пригодного метода измерения краевого угла указаны в экспериментальной части. При названных там условиях используемые согласно данному изобретению слитые белки обладают свойством увеличивать краевой угол капли воды не менее чем на 20, предпочтительно не менее чем на 25, наиболее предпочтительно не менее чем на 30, соответственно, по сравнению с краевым углом равной по величине капли воды на стеклянной поверхности без покрытия. Наиболее предпочтительными гидрофобинами для осуществления данного изобретения являются гидрофобины типа dewA, rodA, hypA, hypB, sc3, basf1, basf2, которые структурно охарактеризованы в нижеследующем протоколе последовательностей. Однако речь может идти только о части или производном. Также несколько гидрофобиновых частей, предпочтительно 2 или 3, с одинаковой или различной-3 012800 структурой могут соединяться друг с другом и с соответствующей подходящей последовательностью полипептидов, которая не связана естественно с гидрофобином. Наиболее подходящими для данного изобретения являются слитые белки yaad-Xa-dewA-his (SEQID NO: 20), yaad-Xa-rodA-his (SEQ ID NO: 22) или yaad-Xa-basf1-his (SEQ ID NO: 24) с указанными в скобках последовательностями полипептидов, а также кодирующими для них последовательностями нуклеиновых кислот, в особенности последовательности в соответствии с SEQ ID NO: 19, 21, 23. Наиболее предпочтительные варианты осуществления представляют собой также белки, которые получаются,исходя из представленных в SEQ ID NO: 20, 22 или 24 последовательностей полипептидов, путем замещения, вставки или делеции по меньшей мере одной аминокислоты, до 10, предпочтительно 5, в особенности 5% всех аминокислот, и которые обладают биологическими свойствами исходного белка еще по меньшей мере на 50%. Под биологическими свойствами белков следует понимать уже описанное изменение краевого угла по меньшей мере на 20. Наиболее подходящими для осуществления изобретения производными являются yaad-Xa-dewA-his(SEQ ID NO: 20), yaad-Xa-rodA-his (SEQ ID NO: 22) или yaad-Xa-basfl-his (SEQ ID NO: 24) за счет сокращения остатка, имеющего происхождение от yaad-партнера слияния. Вместо полного yaad-партнера слияния (SEQ ID NO: 16) с 294 аминокислотами с успехом может использоваться укороченный yaadостаток. Но укороченный остаток должен включать по меньшей мере 20, предпочтительно не менее 35 аминокислот. Например, может использоваться укороченный остаток с 20-293, предпочтительно с 25250, особенно предпочтительно с 35-150 и наиболее предпочтительно с 35-100 аминокислотами. Место разрыва между гидрофобином и партнером слияния или слитыми партнерами может использоваться для того, чтобы высвободить чистый гидрофобин в неизмененном виде (например, путем BrCNрасщепления у метионина, расщепления фактором Ха, расщепления энтерокиназой, тромбинового расщепления, TEV-расщепления и т.п.). Далее, можно получать поочередно слитые белки из партнера слияния, например yaad или уаае, и нескольких гидрофобинов также с различными последовательностями, например, DewA-RodA или Sc3DewA, Sc3-RodA). Также можно использовать гидрофобиновые фрагменты (например, укороченные с Nили С-концов) или мутеины, которые имеют до 70% гомологии. Выбор оптимальных конструктов происходит в расчете на соответствующее использование, т.е. применительно к разделяемым жидким фазам. Используемые согласно данному изобретению гидрофобины, иначе гидрофобины, содержащиеся в композициях согласно данному изобретению, можно получать химическим путем с помощью известных методов синтеза пептидов, например твердофазным синтезом по Меррифилду. Встречающиеся в природе гидрофобины можно выделить из природных источников с помощью подходящих методов. Сошлемся, например, на работу Wsten et al., Eur. J Cell Bio. 63, 122-129 (1994) илиWO 96/41882. Получение слитых белков предпочтительно может осуществляться методами генной инженерии,при которых последовательности нуклеиновых кислот, кодирующие для партнера слияния и для гидрофобиновой части, в частности последовательности ДНК, комбинируются таким образом, что в организме хозяина путем экспрессии генов комбинированной последовательности нуклеиновых кислот получается желаемый белок. Такой метод получения описан, например, в DE 102005007480.4. Подходящими организмами-хозяевами для названного метода получения могут быть при этом прокариоты (включая Archaea) или эукариоты, особенно бактерии, включая галобактерии и метанококки,грибы, клетки насекомых, растений и млекопитающих, наиболее предпочтительны Escherichia coli, Bacillus subtilis, Bacillus megaterium, Aspergillus oryzea, Aspergillus nidulans, Aspergillus niger, Pichia pastoris,Pseudomonas spec., Lactobacillen, Hansenula polymorpha, Trichoderma reesei, SF9 (или родственные клетки) и др. Кроме того, предметом изобретения является применение экспрессионных конструктов, содержащих кодирующую последовательность нуклеиновых кислот для используемого согласно изобретению полипептида, находящихся под генетическим контролем регуляторных последовательностей нуклеиновых кислот, а также векторы, включающие хотя бы один из таких экспрессионных конструктов. Используемые конструкты предпочтительно охватывают выше 5'-конца от соответствующей промоторной кодирующей последовательности и ниже 3'-конца терминаторной последовательности, а также при необходимости другие обычные регуляторные элементы, а именно соответственно оперативно соединенные с кодирующей последовательностью. Под понятием оперативное соединение в рамках данного изобретения понимают последовательное расположение промотора, кодирующей последовательности, терминатора и при необходимости других регуляторных элементов таким образом, что каждый из регуляторных элементов может выполнять по назначению свои функции при экспрессии кодирующей последовательности. Примерами оперативно соединяемых последовательностей являются целевые последовательности,а также энханцеры, сигналы полиаденилирования и т.п. Другие регуляторные элементы включают способные к отбору маркеры, амплификационные сигналы, начала репликации и т.п. Подходящие регуляторные последовательности, например, описаны в книге Goeddel, Gene Expression Technology: Methods in-4 012800 В дополнение к этим регуляторным последовательностям может еще иметь место естественная регуляция этих последовательностей от собственных структурных генов и при необходимости генетически она может быть изменена так, чтобы естественная регуляция исключалась и усиливалась экспрессия генов. Предпочитаемый конструкт из нуклеиновых кислот предпочтительно содержит также один или несколько так называемых энханцер-последовательностей, функционально соединенных с промотором,которые дают возможность усиленной экспрессии последовательности нуклеиновых кислот. Также у 3'конца последовательности ДНК могут помещаться дополнительные полезные последовательности, такие как другие регуляторные элементы и терминаторы. Нуклеиновые кислоты могут содержаться в конструкте в одной или нескольких копиях. В конструкте могут еще содержаться другие маркеры, такие как гены, комплементирующие устойчивость к антибиотикам или ауксотрофии, при необходимости для селекции на конструкте. Предпочитаемые регулирующие последовательности для получения содержатся, например, в промоторах, таких как cos-, tac-, trp-, tet-, trp-tet-, Ipp-, lac-, Ipp-lac-, laclq-T7-, T5-, T3-, gal-, trc-, ara-,rhaP(rhaPBAD) SP6-, лямбда-PR- или в лямбда-Р-промоторе, которые находят применение в грамотрицательных бактериях. Другие предпочтительные регулирующие последовательности содержатся, например, в грамположительных промоторах amy и SP02, в дрожжевых или грибковых промоторах ADC1, MFальфа, АС, Р-60, CYC1, GAPDH, TEF, rp28, ADH. Для регуляции могут использоваться также искусственные промоторы. Конструкт нуклеиновых кислот вставляется для экспрессии в организме хозяина предпочтительно в вектор, такой как, например, плазмида или фаг, который позволяет осуществлять оптимальную экспрессию генов в хозяине. Под векторами следует понимать кроме плазмид и фагов также все другие известные специалисту векторы, такие как, например, SV40, CMV, бакуловирус и аденовирус, транспозоны, ISэлементы, фазмиды, космиды, и линейные или кольцевые ДНК, а также системы агробактерий. Эти векторы могут быть реплицированы в организм хозяина автономно или хромосомно. Подходящими плазмидами являются, например, в E.coli pLG338, pACYC184, pBR322, pUC18, pUC19, pKC30,pRep4, pHS1, pKK223-3, pDHE19.2, pHS2, pPLc236, pMBL24, pLG200, pUR290, pIN-III"3-Bl, tgt11 илиpBdCI, в Streptomyces plJ101, pIJ364, plJ702 или plJ361, в Bacillus pUB110, pC194 или pBD214, в Corynebacterium pSA77 или pAJ667, в грибах pALS1, plL2 или рВВ 116, в дрожжах 2 альфа, pAG-1, YEp6, YEp13 или pEMBLYe23 или в растениях pLGV23, pGHlac+, pBIN19, pAK2004 или pDH51. Названные плазмиды представляют собой небольшую выборку из возможных плазмид. Другие плазмиды известны специалисту и могут быть взяты из книги Cloning Vectors (Eds. Pouwels P. H. et al. Elsevier, Amsterdam-New YorkOxford, 1985, ISBN 0444904018). Предпочтительно конструкт из нуклеиновых кислот для экспрессии других содержащихся генов содержит еще 3'- и/или 5'-терминальные регуляторные последовательности для усиления экспрессии,которые выбираются для оптимальной экспрессии в зависимости от выбранного организма-хозяина и гена или генов. Эти регуляторные последовательности должны давать возможность целенаправленной экспрессии генов и экспрессии белков. Это, например, в зависимости от организма-хозяина может означать то, что ген экспримируется или суперэкспримируется только после индукции, или что он экспримируется и/или суперэкспримируется немедленно. Регуляторные последовательности или факторы при этом могут преимущественно оказывать положительное влияние на экспрессию внедренного гена и тем самым усиливать е. Так, усиление регуляторных элементов может происходить благоприятным образом на транскрипционном участке, тем что применяются сильные транскрипционные сигналы, такие как промоторы и/или энханцеры. Наряду с этим возможно также усиление трансляции, тем что, например, улучшается стабильность мРНК. В другом варианте вектора содержащий конструкт из нуклеиновых кислот или нуклеиновые кислоты вектор также вводится в микроорганизмы предпочтительно в форме линейной ДНК и интегрируется в геном организма-хозяина через гетерологичную или гомологичную рекомбинацию. Эта линейная ДНК может состоять из линеаризованного вектора, такого как плазмида, или только из конструкта нуклеиновых кислот или из нуклеиновых кислот. Для оптимальной экспрессии чужеродных генов в организмы предпочтительно следует изменять последовательности нуклеиновых кислот в соответствии с применяемым в организме специфическим синонимическим кодоном (codon usage). Синонимический кодон (Codon usage) можно легко определить, пользуясь компьютерной оценкой других, известных генов данного организма. Получение экспрессионной кассеты происходит путем соединения подходящего промотора с подходящей кодирующей последовательностью нуклеотидов, а также сигналом терминатора или сигналом полиаденилирования. Для этого применяют общеупотребительные приемы рекомбинации и клонирования, какие описаны, например, Т. Maniatis, E.F. Fritsch и J. Sambrook, Molecular Cloning: A LaboratoryInterscience (1987). Рекомбинантный конструкт нуклеиновых кислот или генный конструкт вводится для экспрессии в подходящий организм хозяина, предпочтительно в характерный для хозяина вектор, который дает возможность осуществления оптимальной экспрессии генов в хозяине. Векторы хорошо известны специалисту и могут быть взяты из "Cloning Vectors" (Pouwels P. H. et al., Hrsg, Elsevier, Amsterdam-New YorkOxford, 1985). С помощью векторов получаются рекомбинантные микроорганизмы, которые, например, трансформированы минимум одним вектором и могут использоваться для получения применяемого согласно изобретению гидрофобина или его производных. Вышеописанные рекомбинантные конструкты преимущественно вводятся с подходящую систему-хозяин и экспримируются. При этом используются преимущественно известные специалисту привычные методы клонирования и трансфекции, такие как соосаждение, слияние протопластов, электропорация, ретровиральная трансфекция и т.п., чтобы довести до экспрессии названные нуклеиновые кислоты в соответствующей экспрессионной системе. Подходящие системы описаны, например, в Current Protocols in Molecular Biology, F. Ausubel et al., Hrsg., Wiley Interscience, New York 1997, или Sambrook et al. Molecular Cloning : A Laboratory Manual. 2. Aufl., Cold SpringHarbor Laboratory, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, NY, 1989. Можно также получать гомологичные рекомбинированные микроорганизмы. Для этого получают вектор, который содержит, по меньшей мере, участок используемого гена или кодирующей последовательности, в котором при необходимости для изменения последовательности, по меньшей мере, осуществлено удаление, присоединение или замещение аминокислоты, например функционального разрыва(нокаутирующий вектор). Введенная последовательность может, например, также быть гомологом из родственного микроорганизма или происходить из клеток млекопитающего, дрожжевых клеток или клеток насекомого. Вектору, применяемому для гомологичной рекомбинации, альтернативно может быть придан такой вид, чтобы эндогенный ген при гомологичной рекомбинации был мутирован или был изменен иным путем, но еще был способен кодировать функциональный белок (например, расположенная выше регуляторная область может изменяться таким образом, что вследствие этого изменяется экспрессия эндогенного белка). Измененный участок использованного согласно изобретению гена находится в гомологичном рекомбинантном векторе. Конструкция подходящих векторов для гомологичной рекомбинации описана, например, в работе Thomas, K.R. и Capecchi, M.R. (1987) Cell 51: 503. В качестве рекомбинантных организмов-хозяев для такого рода нуклеиновых кислот или такого рода конструктов из нуклеиновых кислот подходят, в принципе, все организмы, как прокариоты, так и эукариоты. Предпочтительно в качестве организмов-хозяев используются такие микроорганизмы, как бактерии, грибы или дрожжи. Преимущественно применяются грамположительные и грамотрицательные бактерии, предпочтительно бактерии семейств Enterobacteriaceae, Pseudomonadaceae, Rhizobiaceae, Streptomycetaceae или Nocardiaceae, наиболее предпочтительны бактерии родов Escherichia, Pseudomonas,Streptomyces, Nocardia, Burkholderia, Salmonella, Agrobacterium или Rhodococcus. Организмы, применяемые в описанных выше способах получения слитых белков, разводятся или выращиваются известными специалисту способами в зависимости от организма-хозяина. Микроорганизмы, как правило, выращиваются в жидкой среде, которая содержит источник углерода, чаще всего в форме сахаров, источник азота, чаще всего в форме источника органического азота, такого как экстракт дрожжей, или соли, такие как сульфат аммония, микроэлементы, такие как соли железа, марганца и магния, а также при необходимости витамины, при температуре от 0 до 100 С, предпочтительно от 10 до 60 С при насыщении кислородом. При этом величина рН в питательной жидкости может поддерживаться на постоянном значении, т.е. во время выращивания регулируется или не регулируется. Выращивание может происходить периодическим способом, полупериодическим способом или непрерывным способом. Питательные вещества могут загружаться полностью к началу ферментации или подаваться полупериодически или непрерывно. Энзимы могут выделяться из организмов в соответствии со способами,описанными в примерах, или могут применяться в реакции в виде неочищенного экстракта. Применяемые согласно изобретению гидрофобины или функциональные, биологически активные их фрагменты могут формироваться способом рекомбинантного получения, при этом культивируют микроорганизм, продуцирующий полипептиды, при необходимости индуцируют экспрессию белков и выделяют их из культуры. Белки таким способом могут производиться в промышленном масштабе, если это будет желательно. Рекомбинантные микроорганизмы могут культивироваться и ферментироваться по известным методикам. Бактерии могут размножаться, например, в ТВ- или LB-среде при температуре от 20 до 40 С и величине рН от 6 до 9. В подробностях подходящие условия культивирования описаны, например, в книге Т. Maniatis, E.F. Fritsch и J. Sambrook, Molecular Cloning: A Laboratory Manual, ColdSpring Harbor Laboratory, Cold Spring Harbor, NY (1989). Затем клетки, если белки не выделяются в питательную среду, подвергаются лизированию и продукт получается из лизата известными способами выделения белков. По выбору клетки могут переводиться в удобное для переработки состояние высокочастотным ультразвуком, высоким давлением, таким как, например, в работающей под давлением ячейке (French-Druckzelle), осмолизом, воздействием детер-6 012800 гентов, литических энзимов или органических растворителей, с помощью гомогенизаторов или комбинацией нескольких из перечисленных способов. Очистка белков может достигаться с помощью известных хроматографических методов, таких как хроматография на молекулярных ситах (гель-фильтрация), хроматография на Q-сефарозе, ионообменная хроматография и гидрофобная хроматография, а также с использованием других обычных способов, таких как ультрафильтрация, кристаллизация, высаливание, диализ и естественный гель-электрофорез. Подходящие способы описаны, например, в книгах Cooper, F.G., Biochemische Arbeitsmethoden, VerlagWater de Gruyter, Berlin, New York или Scopes, R., Protein Purification, Springer Verlag, New York, Heidelberg, Berlin. Особенно выгодным может быть, если для облегчения выделения и очистки снабдить слитый гидрофобин специальными якорными группами, которые могут привязываться к соответствующим комплементарным группам твердых носителей, в частности подходящих полимеров. Такого рода твердые носители могут использоваться, например, в качестве наполнителей для хроматографических колонок, и таким способом можно, как правило, заметно повысить эффективность разделения. Такие способы разделения также известны как аффинная хроматография. Для встраивания якорных групп можно использовать при получении белков векторные системы или олигонуклеотиды, которые удлиняют кДНК на определенную последовательность нуклеотидов и тем самым кодируют измененные белки или слитые белки. Для более легкой очистки модифицированные белки включают действующие в качестве якоря так называемые таги ("Tags") (метки), например, известные модификации в виде гексагистидиновых якорей. Модифицированные гистидиновыми якорями слитые гидрофобины можно, например, очищать хроматографически при использовании никель-сефарозы в качестве заполнителя для колонки. После чего слитый гидрофобин с помощью подходящих средств для элюирования, таких как, например, раствор имидазола,снова вымывается с колонки. В упрощенном способе очистки можно отказаться от хроматографической очистки. Для этого клетки сначала с помощью подходящего метода выделяются из ферментативного бульона, например путем микрофильтрации или центрифугированием. Затем клетки с помощью подходящих методов, например с использованием уже упомянутых выше методов, переводят в удобное для переработки состояние и фрагменты разрушенных клеток отделяются от телец включений. Последнее удобно осуществлять путем центрифугирования. Наконец, тельца включений в принципе можно обычным путем переводить в удобное для переработки состояние, чтобы высвободить слитый гидрофобин. Это может, например, происходить с помощью кислот, оснований и/или детергентов. Тельца включений с использованным согласно изобретению слитым гидрофобином, как правило, могут полностью растворяться уже при использовании 0,1 М раствора NaOH в течение примерно 1 ч. Чистота полученного этим упрощенным способом слитого гидрофобина, как правило, составляет 60-80 вес.% по сравнению с количеством всех белков. Растворы,полученные описанным упрощенным способом очистки, могут использоваться без дальнейшей очистки для осуществления этого изобретения. Гидрофобины, полученные, как описано, могут применяться как непосредственно в качестве слитых белков, так и после отщепления и отделения партнера слияния как чистые гидрофобины. Если предусмотрено отделение партнера слияния, рекомендуется вводить потенциальное место расщепления в слитом белке (особенное место распознавания для протеаз) между гидрофобиновой частью и частью партнера слияния. В качестве мест расщепления пригодны, в частности, такие последовательности пептидов, которые не встречаются ни в гидрофобиновой части, ни в части партнера слияния,что легко можно определить с помощью биоинформационных технологий. Наиболее подходящими являются, например, BrCN-расщепление у метионина, или расщепление при посредничестве протеазы с фактором Ха-, расщепление энтерокиназой, тромбином, TEV-расщепление (протеаза Tobacca etch virus). Согласно изобретению гидрофобины и их производные могут применяться в составах, имеющих по крайней мере две жидкие фазы, для улучшения разделения фаз. При этом речь идет о любых составах,если они содержат не менее двух жидких фаз. В частности, речь может идти также о составах, которые до добавки по меньшей мере одного гидрофобина или его производного представляют собой эмульсию. При этом состав в рамках данного изобретения может иметь больше двух жидких фаз. Если речь идет о минимум двух жидких фазах, то имеются в виду две жидкие фазы разной плотности, например масло и вода, два водных раствора разной плотности, два органических раствора разной плотности, горючее и вода, топливо и вода или растворитель и вода. При этом под водным раствором в рамках данного изобретения понимаются растворы, содержащие воду, в некоторых случаях в комбинации с еще одним растворителем. В рамках данного изобретения каждая жидкая фаза может при этом содержать дополнительные вещества. Согласно изобретению речь идет о масле, преимущественно о сырой нефти. Подходящими растворителями являются все жидкости, образующие с водой двухфазную смесь, в частности органические растворители, например простые эфиры, ароматические соединения как толуол или бензол, спирты, алканы, алкены, циклоалканы, циклоалкены, сложные эфиры, кетоны, нафтены или галогенированные углеводороды.-7 012800 Согласно следующей форме исполнения данное изобретение затрагивает поэтому описанное ранее применение по меньшей мере одного гидрофобина или по меньшей мере одного его производного, причем состав, содержащий не менее двух жидких фаз, выбирается из группы, состоящей из составов, содержащих масло, предпочтительно сырую нефть, и воду,составов, содержащих горючее или топливо и воду,реакционных смесей, содержащих не менее двух жидких фаз. В рамках данного изобретения соединение может содержать больше фаз, например твердую или жидкую фазу, в частности твердую фазу. Гидрофобин или его производные могут использоваться во всех известных специалисту применениях. В частности, в рамках данного изобретения следует назвать применение в качестве деэмульгатора в смесях автомобильный бензин/вода, в качестве деэмульгатора в смесях воды с другими видами горючего или топлива, разделение фаз при химических реакциях, особенно в промышленных процессах, расщепление эмульсии на сырую нефть и воду при нефтедобыче или нефтепереработке, а также обессоливание сырой нефти путем экстракции сырой нефти с водой и последующее разделение полученной эмульсии. В качестве промышленных химических процессов рассматриваются все процессы, для которых должна привлекаться операция разделения фаз, например гидрокомпозиция полиизобутена с катализаторами из кобальта, причем отделение катализатора осуществляется в воде. Гидрофобин или его производные согласно изобретению применяются также для улучшения разделения фаз составов, содержащих не менее двух жидких фаз, возникающих при протекании реакции, т.е. которые образуются в ходе реакции или появляются в результате добавки растворителя или компонента. Благодаря применению гидрофобина или их производных согласно изобретению достигается сокращение времени разделения фаз, что позволяет уменьшить потери ценных материалов. Согласно изобретению возможно также улучшить разделение фаз составов, содержащих две водные фазы разной плотности, причем под водной фазой подразумевается фаза, содержащая воду, в некоторых случаях в комбинации с другим растворителем. Гидрофобины или их производные согласно изобретению применяются для улучшения разделения фаз при фракционировании полимеров в водных системах. При этом, в частности, перегоняются водорастворимые полимеры. Вообще следует назвать все известные специалисту растворимые в воде и в масле полимеры, в особенности полиакрилаты и их сополимеры, которые по условиям их изготовления получаются с молекулярно-массовым распределением или полидисперсностью больше чем 1,1. Благодаря добавке деэмульгаторов эмульсии могут быть разрушены. Так, например, добываемая нефть представляет собой, как правило, относительно стабильную эмульсию вода-в-масле, которая в зависимости от месторождения может содержать до 90 вес.% воды. При обработке и очистке сырой нефти после отделения большой части воды в сырой нефти все еще остается около 2-3 вес.% воды. Она образует с нефтью стабильную эмульсию, которая не разделяется полностью даже путем центрифугирования и добавлением обычных деэмульгаторов. Проблема заключается в том, что, во-первых, вода содержит соль и приводит к коррозии, а во-вторых, остаток воды увеличивает объем предназначенного для транспортировки и хранения продукта, что повышает его стоимость. Согласно изобретению было найдено, что применение гидрофобинов или их производных особенно выгодно для улучшения разделения фаз в таких составах. Достигается очень быстрое разделение. При этом деэмульгатор должен быть ориентирован на вид образовавших эмульсию масел или жиров, а также на содержащиеся в некоторых случаях эмульгаторы и поверхностно-активные вещества,чтобы обеспечить оптимальную эффективность. Разрушение эмульсий может дополнительно поддерживаться повышенной температурой, например температурой от 0 до 100 С или от 10 до 80 С, в особенности от 20 до 60 С. Следующие применения согласно изобретению охватывают, например, деэмульгаторы пропиточных эмульсий в текстильной промышленности и при изготовлении древесно-стружечных плит, а также для лекарственных эмульсий. Следующим применением является расщепление эмульсий сточных вод после органической обработки, например промышленные сточные воды, в особенности с предприятий металлообработки, например смазочно-охлаждающие жидкости после обработки металлов, кожевенных заводов и нефтеочистительных установок, а также хозяйственных источников, имеющих дело с эмульсиями из масла и воды. Такие сточные воды появляются, например, при переработке нефти в очистительных и нефтехимических установках. Прежде чем эти сточные воды подать к очистным сооружениям,необходимо отделить остатки масла, которые в большинстве случаев представляют собой эмульсию. Следующим применением согласно изобретению является расщепление эмульсии в составах маслов-воде или вода-в-масле, например эмульсий, которые должны использоваться и в качестве смазочноохлаждающих материалов и должны быть вторично возвращены в производство. Смесь воды с маслом образуется также на борту морских судов в виде трюмной воды. Для этого требуется разделение эмульсий, чтобы можно было отделить воду и уменьшить объем предназначенного для утилизации растворителя. Количество используемого гидрофобина или его производного может варьироваться в больших-8 012800 пределах, причем приемлемое количество подбирается в соответствии с составом или, при необходимости, с компонентами, входящими в состав. Если, например, состав содержит вещества, которые задерживают или ухудшают разделение по крайней мере двух жидких фаз, к примеру, поверхностно-активные вещества или эмульгаторы, то следует добавлять большее количество гидрофобина или его производного. Поскольку масло, в особенности сырая нефть, состоит из смеси многих химических соединений, то из-за отличающейся химической ее структуры, процента содержания воды и солей, а также в зависимости от конкретных условий расщепления эмульсии, как температура и длительность процесса расщепления, требуется подбирать способ подмешивания и химического взаимодействия с другими компонентами смеси и вид деэмульгатора в соответствии с конкретными условиями. Неожиданно было найдено, что уже небольшие количества гидрофобина или его производного приводят к улучшению разделения фаз. Согласно изобретению по меньшей мере один гидрофобин или его производное может быть добавлен в любом приемлемом количестве. Как правило, гидрофобин или его производное добавляется в количестве не менее 0,0001-1000 ppm относительно всего состава; предпочтительно в количестве от 0,001 до 500 ppm, особенно предпочтительно от 0,01 до 200 ppm или от 0,01 до 100 ppm, а наиболее предпочтительно 0,1-50 ppm. В рамках данного описания данные в ppm означают мг на кг. Поэтому данное изобретение в соответствии со следующей формой исполнения касается описанного ранее применения, причем используется по меньшей мере один гидрофобин или по меньшей мере одно его производное в количестве от 0,0001 до 1000 ppm относительно всего состава. Концентрация устанавливается специалистом в зависимости от вида предназначенного для деэмульгирования состава. Если речь идет о составе, содержащем горючее или топливо и воду, то гидрофобин или его производное применяются обыкновенно в количестве от 0,001 до 10 ppm, предпочтительно 0,005-2 ppm, лучше 0,01-1 ppm, особенно предпочтительно 0,05-0,5 ppm, а еще предпочтительней 0,01-0,1 ppm. Если речь идет о составе, содержащем сырую нефть и воду, то гидрофобин или его производное применяются обыкновенно в количестве от 1 до 1000 ppm, предпочтительно от 1 до 800 ppm, лучше от 5 до 500 ppm,особенно предпочтительно от 10 до 200 ppm, а еще предпочтительней от 15 до 100 ppm, к примеру 2050 ppm. Если речь идет о составе, содержащем две водные фазы различной плотности, которые могут возникнуть, например, при разделении на фракции растворимых в воде полимеров, то гидрофобин или его производное применяются обыкновенно в количестве от 1 до 1000 ppm, предпочтительно от 1 до 500 ppm, лучше от 5 до 250 ppm, особенно предпочтительно от 10 до 200 ppm, а еще предпочтительней от 15 до 100 ppm. Согласно изобретению возможно также, что состав кроме гидрофобина или его производного содержит другие соединения, которые улучшают разделение фаз. При этом речь может идти обо всех соединениях, известных специалисту для такого рода применений. Например, подходящими дополнительными соединениями для улучшения разделения фаз, особенно в качестве деэмульгаторов для нефтепродуктов, являются оксиалкилированная фенол-формальдегидная смола, ЕО/РО-сополимеры в виде блоков, сшитые диэпоксиды, полиамиды и их алкоксильные группы, соли сульфоновых кислот, этоксилированные алифатические амины, сукцинаты, а также соединения, приведенные для таких применений в патенте DE 102005006030.7. Поэтому данное изобретение в соответствии со следующей формой исполнения касается описанного ранее применения, причем помимо гидрофобина или его производного используется по меньшей мере одно дополнительное соединение, которое улучшает разделение фаз. В соответствии со следующим аспектом данное изобретение касается также способа разделения по меньшей мере двух жидких фаз в составе, содержащем не менее двух жидких фаз, включающего добавление к составу по меньшей мере одного гидрофобина или его производного. При этом речь для состава может идти об описанном ранее составе, включающем не менее двух жидких фаз. В соответствии с предпочтительной формой исполнения данное изобретение касается поэтому такого рода способа, при котором состав, содержащий по меньшей мере две жидкие фазы, выбирается из группы, состоящей из составов, содержащих масло, предпочтительно сырую нефть, и воду,составов, содержащих горючее или топливо и воду,реакционных смесей, содержащих не менее двух жидких фаз. В принципе, в рамках данного изобретения гидрофобины или их производные могут применяться в любых количествах,пока не будет достигнуто улучшение фазового разделения. В особенности пригодно применение гидрофобина или его производного в количестве от 0,0001 до 1000 ppm относительно всего состава. Данное изобретение касается также описанного ранее способа, причем по меньшей мере один гидрофобин или его производное применяются в количестве от 0,0001 до 1000 ppm относительно всего со-9 012800 става. Предпочтительные количества для соответствующих систем уже были названы. Способ согласно изобретению может включать дополнительные этапы, например, такие, которые улучшают разделение фаз или разрушение эмульсий. При этом речь может идти, например, о повышении температуры или о центрифугировании. Такого рода этап может выполняться до добавления по меньшей мере одного гидрофобина или его производного во время этого действия или после него. В соответствии со следующей формой исполнения данное изобретение касается поэтому описанного ранее способа, причем способ включает повышение температуры состава, содержащего не менее двух жидких фаз, до или после добавления по меньшей мере одного гидрофобина или по меньшей мере одного его производного. Согласно изобретению могут добавляться гидрофобины или их производные, например, к композициям, содержащим горючее или топливо. При контакте композиции с водой это обеспечивает быстрое расслоение смеси и предотвращает образование эмульсий. Образование эмульсий, например, в складских резервуарах сделало бы необходимыми дорогостоящие операции по очистке композиции. В такой же степени полезно добавлять гидрофобины или их производные к сырой нефти, чтобы предотвратить, например, образование эмульсии. При этом композиция, содержащая горючее или топливо, в рамках данного изобретения может содержать другие добавки, которые обычно содержатся в такого рода композициях. Подходящие добавки названы, например, в патенте WO 2004/087808. Данное изобретение касается поэтому также композиции, содержащей по меньшей мере одно соединение, выбранное из группы, состоящей из горючего, топлива, сырой нефти или растворов полимеров в воде или в масле, и по крайней мере одного гидрофобина или его производного. Количество применяемого гидрофобина или его производного можно варьировать в зависимости от других добавок, пока не будет обеспечено улучшение разделения фаз при контакте композиции с водой. Согласно изобретению количество применяемого гидрофобина или его производного лежит преимущественно в области между 0,0001 и 1000 ppm, предпочтительно от 0,001 до 500 ppm, особенно предпочтительно от 0,01 до 100 ppm. Поэтому данное изобретение касается также описанной ранее композиции, причем гидрофобин или его производное содержится в композиции в количестве от 0,0001 до 1000 ppm по отношению ко всей композиции. Если для композиции речь идет о смеси, содержащей сырую нефть, то количество добавляемого к такой композиции гидрофобина или его производного составляет, как правило, от 1 до 1000 ppm, предпочтительно от 10 до 800 ppm, особенно предпочтительно от 10 до 500 ppm. Если для композиции речь идет о смеси, содержащей горючее или топливо, то количество добавляемого к такой композиции гидрофобина или его производного составляет, как правило, от 0,001 до 0,5 ppm, предпочтительно от 0,005 до 0,3 ppm, особенно предпочтительно от 0,01 до 0,2 ppm. Поэтому настоящее изобретение в соответствии со следующей формой исполнения касается описанной ранее композиции, причем композиция содержит по крайней мере одно горючее или топливо, и в композиции содержится гидрофобин или его производное в количестве от 0,001 до 0,5 ppm относительно всей композиции. В рамках данного изобретения под топливом понимаются, например, легкие, средние или тяжелые мазуты. В рамках данного изобретения под горючим понимаются, например, автомобильные бензины, дизельное или газотурбинное топливо. Особенно предпочтительно речь идет о бензинах. Горючее может содержать дополнительные присадки. Обычные присадки в основном известны специалисту. Подходящие присадки и растворители названы, например, в патенте WO 2004/087808. Например, согласно изобретению пригодными в качестве дополнительных компонентов являются присадки с моющим действием и/или препятствующие износу седла клапана (называемые в дальнейшем моющие присадки). Такая моющая присадка содержит по крайней мере один гидрофобный углеводородный остаток со среднечисленным молекулярным весом Mn от 85 до 20000 г/моль и по крайней мере одну полярную группировку, выбранную из:(a) моно- или полиаминогрупп с атомами азота до 6, причем по крайней мере один атом азота имеет свойства основания;(c) гидроксильных групп в комбинации с моно- или полиаминогруппами, причем по крайней мере один атом азота имеет свойства основания;(d) карбоксильных групп или их солей щелочных или щелочно-земельных металлов;(e) сульфогрупп или их солей щелочных или щелочно-земельных металлов;(f) полиокси-С 2-С 4-алкиловых группировок, которые оканчиваются гидроксильными группами, моно- или полиаминогруппами, причем по крайней мере один атом азота имеет свойства основания, или карбаматными группами;(g) групп эфиров карбоновой кислоты;(h) группировок, производных от ангидрида янтарной кислоты, с гидрокси-, и/или амино-, и/или(i) группировок, полученных реакцией обмена Манниха замещенных фенолов с альдегидами и моно- или полиаминами. Гидрофобный углеводородный остаток в упомянутых выше моющих присадках, предназначенный для достаточной растворимости в горючем, имеет среднечисленный молекулярный вес (Mn) от 800 до 20000, в особенности от 113 до 10000, лучше всего от 300 до 5000. В качестве типичного гидрофобного углеводородного остатка, в особенности в соединении с полярными группировками (а), (с), (h) и (i), рассматриваются полипропиленовый остаток, полибутениловый остаток и полиизобутениловый остаток сMn=300-5000, особенно 500-2500, лучше всего 700-2300. В качестве примеров указанных выше групп моющих присадок можно назвать следующие. Присадки, содержащие моно- или полиаминогруппы (а), являются преимущественно полиалкенмоно- или полиалкенполиаминами на основе полипропена или обычного (т.е. с двойными связями, расположенными преимущественно не на конце) полибутена или полиизобутена с Mn от 300 до 5000 г/моль. При изготовлении присадок на основе полибутена или полиизобутена с преимущественной срединной двойной связью (в большинстве случаев в бета- или гамма-позиции) предлагается способ хлорирования с последующим аминированием или окисление двойной связи кислородом воздуха или озоном до карбонилкарбоксилсоединения с последующием аминированием при восстанавливающих (гидрирующих) условиях. Для аминирования здесь могут использоваться амины, например аммиак, моноамины или полиамины, как диметиламинопропиламин, этилендиамин, диэтилентриамин, триэтилентетрамин или тетраэтиленпентамин. Соответствующие присадки на основе полипропена описаны, в частности, в патентеWO 94/24231. Следующие предпочтительные присадки, содержащие моноаминогруппы (а), являются продуктами гидрирования продуктов реакции обмена из полиизобутенов со средней степенью полимеризации Р=5100 с оксидами азота или смесями из оксидов азота и кислорода, как это, в частности, описано в патентеWO 97/03946. Следующие предпочтительные присадки, содержащие моноаминогруппы (а), являются соединениями, полученными из полиизобутенэпоксидов реакцией обмена с аминами и с последующей дегидратацией и восстановлением аминоспиртов, как это, в частности, описано в патенте DE-A 19620262. Присадки, содержащие нитрогруппы (b), в некоторых случаях в комбинации с гидроксилгруппами являются преимущественно продуктами реакции обмена из полиизобутенов средней степени полимеризации Р=5-100 или 10-100 с оксидами азота или смесями из оксидов азота и кислорода, как это, в частности, описано в патентах WO 96/03367 и WO 96/03479. Эти продукты обмена представляют собой, как правило, смеси из чистых нитрополиизобутенов (например, альфа-, бета-динитрополиизобутены) и смешанных гидроксинитрополиизобутенов (например, альфа-нитро-бета-гидроксиполиизобутены). Присадки, содержащие нитрогруппы (b) в комбинации с моно- или полиаминогруппами (с), являются, в основном, продуктами обмена полиизобутенэпоксидов, полученных из полиизобутенов преимущественно с концевыми двойными связями и Mn=300-5000, с аммиаком, моно- или полиаминами, как это, в частности, описано в патенте ЕР-А 0476485. Присадки, содержащие карбоксильные группы или их соли щелочных или щелочно-земельных металлов (d), являются преимущественно сополимерами С 2-С 40-олефинов с малеиновым ангидридом общей молярной массой от 500 до 20000, карбоксильные группы которых полностью или частично превращаются в соли щелочных или щелочно-земельных металлов, а остаток карбоксильных групп реагирует со спиртами или аминами. Такие присадки известны, в частности, из ЕР-А 0307815. Такого рода присадки служат, в основном, для предотвращения износа седла клапана и могут, как описано в WO 87/01126, с пользой использоваться в комбинации с обычными топливными присадками, как поли(изо)бутенамины или полиэфирамины. Присадки, содержащие сульфогруппы или их соли щелочных или щелочно-земельных металлов (е),являются преимущественно солями щелочных или щелочно-земельных металлов алкилового эфира сульфоянтарной кислоты, как это, в частности, описано в патенте ЕР-А 0639632. Такого рода присадки служат, в основном, для предотвращения износа седла клапана и могут с пользой использоваться в комбинации с обычными топливными присадками, как поли(изо)бутенамины или полиэфирамины. Присадки, содержащие полиокси-С 2-С 4-алкиловые группировки, являются преимущественно полиэфирами или полиэфираминами, которые можно получить путем реакции обмена С 2-С 60-алканолов, С 6 С 30-алкандиолов, моно- или ди-С 2-С 30-алкиламинов, C1-С 30-алкилциклогексанолов или С 1-С 30 алкилфенолов с 1-30 моль этиленоксида, и/или пропиленоксида, и/или бутиленоксида на каждую гидроксильную группу или аминогруппу и, в случае полиэфираминов путем последующего восстановительного аминирования аммиаком, моноаминами или полиаминами. Такого рода продукты описаны, в частности, в патентах ЕР-А 0310875, ЕР-А 0356725, ЕР-А 0700985 и US 4877416. В случае полиэфиров такие продукты удовлетворяют также свойствам масла-носителя. Типичными примерами этому являются тридеканол- или изотридеканолбутоксилаты, изононилфенолбутоксилаты, а также полиизобутенолбутоксилаты и -пропоксилаты и соответствующие продукты реакции обмена с аммиаком.- 11012800 Присадки, содержащие группы эфиров карбоновой кислоты (g), являются преимущественно сложными эфирами из моно-, ди- или трикарбоновых кислот с длинноцепочечными алканолами или полиолами, в особенности со средней вязкостью 2 мм 2/с при 100 С, как описано, в частности, в патенте DE-A 3838918. В качестве моно-, ди- или трикарбоновых кислот могут использоваться алифатические или ароматические кислоты, в качестве сложных эфиров оксикислоты или многоатомных спиртов, прежде всего,пригодны длинноцепные представители, например, с 6-24 атомами углерода. Типичными представителями сложных эфиров являются адипинаты, фталаты, изофталаты, терефталаты и тримеллитаты изооктанола, изононанола, изодеканола и изотридеканола. Такого рода продукты удовлетворяют также свойствам масла-носителя. Присадки, содержащие группировки, производные от ангидрида янтарной кислоты, с гидрокси-,и/или амино-, и/или амидо-, и/или имидогруппами (h), являются преимущественно соответствующими производными ангидрида полиизобутенил-янтарной кислоты, которые получаются реакцией обмена нормального или высокоактивного полиизобутена с Mn=300-5000 с ангидридом малеиновой кислоты при нагревании или через хлорированный полиизобутен. Особый интерес представляют также производные с алифатическими полиаминами, как этилендиамин, диэтилентриамин, триэтилентетрамин. Такого типа топливные присадки описаны, в частности, в патенте US 4849572. Присадки, содержащие группировки, полученные реакцией обмена Манниха замещенных фенолов с альдегидами и моно- или полиаминами (i), являются преимущественно продуктами реакций обмена полиизобутензамещенных фенолов с формальдегидом и моно- или полиаминами, например этилендиамином, диэтилентриамином, триэтилентетрамином, тетраэтиленпентамином или диметиламинопропиламином. Полиизобутенилзамещенные фенолы могут получаться из нормального или высокоактивного полиизобутена с Mn=300-5000. Такого типа полиизобутеновые основания Манниха описаны, в частности, в патенте ЕР-А 0831141. Для более точного определения отдельных приведенных топливных присадок здесь сделаны ссылки на публикации названных выше современных трудов. Названные присадки применяются в количествах, которые определяются специалистом как пригодные для конкретного использования. Кроме того, композиции согласно изобретению могут комбинироваться и с другими обычными компонентами и добавками. Здесь следует указать масла-носители без выраженного моющего действия. Подходящими минеральными маслами-носителями являются получаемые при нефтепереработке фракции, например, брайтсток или базовые масла с вязкостью, например, класса SN 500-2000; а также ароматические углеводороды, парафиновые углеводороды и алкоксиалканолы. Согласно изобретению пригодна также фракция, известная как гидрокрекинговое масло ("hydrocrack oil") и получаемая при рафинировании минерального масла (этап вакуумной дистилляции с температурой кипения от 360 до 500 С, получение из каталитически гидрогенизированного и изомеризованного при высоком давлении, а также депарафинированного натурального минерального масла). Также пригодны смеси названных выше масел-носителей. Примеры применимых согласно изобретению синтетических масел-носителей можно выбрать из полиолефинов (полиальфаолефин или полиинтерналолефин), сложных полиэфиров, (поли)алкоксилатов,простых полиэфиров, алифатических аминов простых полиэфиров, инициированных алкилфенолом простых полиэфиров, аминов инициированных алкилфенолом простых полиэфиров и эфиры карбоновых кислот с длинноцепочечными алканолами. Примерами для подходящего полиолефина являются полимеризаты олефина с Mn=400-1800, прежде всего на основе полибутена или полиизобутена (гидрированного или не гидрированного). Примерами подходящих простых полиэфиров или аминов простых полиэфиров предпочтительно являются соединения, содержащие группировки полиокси-С 2-С 4-алкиленов, которые получаются реакцией обмена С 2-С 60-алканолов, С 6-С 30-алкандиолов, моно- или ди-С 1-С 30-алкиламинов, C1-С 30 алкилциклогексанолов или C1-С 30-алкилфенолов с 1-30 моль этиленоксида и/или пропиленоксида и/или бутиленоксида на каждую гидроксильную или аминогруппу, а в случае аминов простых полиэфиров путем последующего восстановительного аминирования аммиаком, моноаминами или полиаминами. Такие продукты описаны, в частности, в патентах ЕР-А 0310875, ЕР-А 0356725, ЕР-А 0700985 иUS 4877416. Например, в качестве аминов простых полиэфиров могут применяться поли-С 2-С 6 алкиленоксидамины или их функциональные производные. Типичными примерами этому являются тридеканол- или изотридеканолбутоксилаты, изононилфенолбутоксилаты, полиизобутенолбутоксилаты и-пропоксилаты, а также соответствующие продукты реакции обмена с аммиаком. Примерами эфиров карбоновой кислоты с длинноцепными алканолами являются, в частности,сложные эфиры из моно-, ди- или трикарбоновых кислот с длинноцепными алканолами или полиолами,что описано, в частности, в патенте DE-А 3838918. В качестве моно-, ди- или трикарбоновых кислот могут использоваться алифатические или ароматические кислоты, в качестве сложных эфиров оксикислот пригодны, в первую очередь, длинноцепочечные представители, например с от 6 до 24 атомов углерода. Типичными представителями сложных эфиров являются адипаты, фталаты, изофталаты, терефталаты и- 12012800 тримеллитаты изооктанола, изононанола, изодеканола и изотридеканола, как, например, ди(н- или изотридецил)фталат. Другие пригодные системы масел-носителей описаны, например, в патентах DE-A 3826608, DE-A 4142241, DE-A 4309074, ЕР-А 0452328 и ЕР-А 0548617. Примерами наиболее подходящих синтетических масел-носителей являются инициированные спиртами простые полиэфиры с 5-35 или, например, 5-30 фрагментами С 3-С 6-алкиленоксидов, выбранных, например, из группы фрагментов пропиленоксида, n-бутиленоксида и i-бутиленоксида или их смесей. Неограниченными примерами подходящих спиртов инициации являются длинноцепочечные спирты или фенолы, замещенные длинноцепочечными алкилами, причем длинноцепочечный алкильный остаток стоит за неразветвленным или разветвленным С 6-С 18-алкильным остатком. В качестве предпочтительных примеров следует назвать тридеканол и нонилфенол. Другими пригодными синтетическими маслами-носителями являются алкоксилированные алкилфенолы, которые описаны в патенте DE-A 10102913.6. Названные масла-присадки применяются в количествах, которые определяются специалистом как пригодные для конкретного использования. Следующими общеупотребительными добавками являются ингибиторы коррозии, например, на основе склонных к образованию пленок солей аммония органических карбоновых кислот или гетероароматических соединений для защиты от коррозии цветных металлов; антиокислители или стабилизаторы,например, на основе таких аминов, как р-фенилендиамин, дициклогексиламин или их производных, или таких производных фенола, как 2,4-ди-трет-бутилфенол, или пропионовые кислоты 3,5-ди-трет-бутил-4 гидроксифенила; другие употребительные деэмульгаторы; антистатические средства; органические соединения с атомом металла, как ферроцен; метилциклопентадиенилмангантрикарбонил; такие присадки,повышающие смазывающую способность, как определенные кислоты жирного ряда, алкениловый эфир янтарной кислоты, бис-(гидроксиалкил)амины жирного ряда, гидроксиацетамиды или касторовое масло; а также красители (маркеры). В некоторых случаях используются также амины для уменьшения рНпоказателя горючего. Названные моющие присадки с полярными группировками (а)-(i) добавляются к горючему обычно в количестве от 10 до 5000 ppm по весу, в особенности от 50 до 1000 ppm по весу. Другие названные компоненты добавляются в принятых для них количествах. В качестве горючего или топлива пригодны все известные специалисту марки, например топливо для карбюраторных двигателей, марки которого описаны, например, в Ullmann's Encyclopedia of IndustrialChemistry, 5.Aufl. 1990, Band A16, S. 719ff. Подходящими типами топлива согласно изобретению являются также дизельное топливо, керосин и реактивное топливо. Особенно пригодно топливо для карбюраторных двигателей с максимальным содержанием ароматических соединений 60 об.%, например не более 43 об.%, и максимальным содержанием серы 2000 ppm по весу, например не более 150 ppm по весу. Содержание ароматических соединений в топливе для карбюраторных двигателей составляет, к примеру, 10-50 или 30-43 об.%, в особенности 32-40 об.%. Содержание серы в топливе для карбюраторных двигателей составляет, к примеру, 2-500 или 5-150 ppm по весу или от 10 до 100 ppm по весу. Кроме того, подходящее топливо для карбюраторных двигателей может содержать олефины в количестве до 50 об.%, например от 6 до 21 об.%, в особенности 7-18 об.%; бензол в количестве до 5 об.%,например 0,5-1,0 об.%, в особенности 0,6-0,9 об.%, и/или серу в количестве до 25 вес.%, например до 10 вес.% или 1,0-2,7 вес.%, в особенности от 1,2 до 2,0 вес.%. В частности, можно назвать такие сорта топлива для карбюраторных двигателей, которые одновременно содержат максимум 38 об.% ароматических соединений, максимум 21 об.% олефинов, максимум 50 ppm по весу серы, максимум 1,0 об.% бензола и кислород от 1,0 до 2,7 вес.%. Содержание спиртов и эфиров в топливе для карбюраторных двигателей может варьироваться в широком диапазоне. Например, типичные максимальные содержания составляют для метанола 15 об.%,для этилового спирта - 65 об.%, для изопропилового спирта - 20 об.%, для третичного бутилового спирта - 15 об.%, для изобутилового спирта - 20 об.% и для эфиров с 5 или более атомами углерода в молекуле - 30 об.%. Давление пара летом над подходящим согласно изобретению топливом для карбюраторных двигателей составляет обычно не более 70 кПа, особенно 60 кПа (соответственно при 37 С). Определенное по исследовательскому методу октановое число (ROZ) топлива для карбюраторных двигателей составляет, как правило, 75-105. Принятый диапазон для соответствующего октанового числа, определенного по моторному методу (MOZ), равен от 65 до 95. Названные спецификации определяются обычными способами (DIN EN 228). Более подробно изобретение объясняется на примерах. Примеры Пример 1. Подготовительные работы для клонирования yaad-His6/yaaE-His6. С помощью олигонуклеотидов Hal570 и Hal571 (Hal 572/Hal 573) была выполнена полимеразная цепная реакция. В качестве матрицы ДНК была использована геномная ДНК бактерии Bacillus subtilis.- 13012800 Полученный фрагмент ПЦР содержит кодирующую последовательность гена yaaD/yaaE из Bacillus subtilis и на концах по одной рестрикционной нуклеазе NcoI и BglII. Фрагмент ПЦР очищали и разрезали с помощью рестрикционных эндонуклеаз NcoI и BglII. Этот фрагмент ДНК использовали как вставку, и клонировали в ранее линеаризированный с помощью рестрикционных эндонуклеаз NcoI и BglII векторpQE60 фирмы Qiagen. Созданные таким образом векторы pQE60YAAD2/pQE60YaaE5 могут применяться для экспрессии белков, состоящих из YAADHIS6 или YAAEHIS6.Hal573: gcagatcttacaagtgccttttgcttatattcc Пример 2. Клонирование yaad-гидрофобина DewA-His6. С помощью олигонуклеотидов KaM 416 и KaM 417 осуществляли цепную реакцию полимеразы. В качестве исходного образца ДНК использовали геномную ДНК плесневого грибка Aspergillus nidulans. Полученный фрагмент ПЦР содержал кодирующую последовательность гена гидрофобина dewA и Nконцевое место расщепления фактора Ха протеиназы. Фрагмент ПЦР очищали и разрезали с помощью рестрикционной эндонуклеазы BamHI. Этот фрагмент ДНК использовали как вставку и клонировали в ранее линеаризированный с помощью рестрикционной эндонуклеазы BglII вектор pQE60YAAD2. Созданный таким образом вектор 508 может применяться для экспрессии слитого белка, состоящего из YAADXadewAHIS6.KaM417: CCCGTAGCTAGTGGATCCATTGAAGGCCGCATGAAGTTCTCCGTCTCCGC Пример 3. Клонирование yaad-гидрофобина RodA-His6. Клонирование плазмиды 513 осуществляется аналогично плазмиде 508 при использовании олигонуклеотидов KaM 434 и KaM 435.KaM435: CCAATGGGGATCCGAGGATGGAGCCAAGGG Пример 4. Клонирование yaad-гидрофобина BASF1-His6. Клонирование плазмиды 507 осуществляется аналогично плазмиде 508 при использовании олигонуклеотидов KaM 417 и KaM 418. В качестве исходной ДНК использовали искусственно синтезированную последовательность ДНКгидрофобин BASF1 (см. дополнение, SEQ ID NO: 11 и 12).KaM418: CTGCCATTCAGGGGATCCCATATGGAGGAGGGAGACAG Пример 5. Клонирование yaad-гидрофобина BASF2-His6. Клонирование плазмиды 506 осуществляется аналогично плазмиде 508 при использовании олигонуклеотидов KaM 417 и KaM 418. В качестве исходной ДНК использовалась искусственно синтезированная последовательность ДНКгидрофобин BASF2 (см. приложение, SEQ ID NO: 13 и 14).KaM418: CTGCCATTCAGGGGATCCCATATGGAGGAGGGAGACAG Пример 6. Клонирование yaad-гидрофобина SC3-His6. Клонирование плазмиды 526 осуществляется аналогично плазмиде 508 при использовании олигонуклеотидов KaM 464 и KaM 465. В качестве исходной ДНК использовалась кДНК Schyzophyllum commune (см. приложение, SEQ IDKaM465: GCTAACAGATCTATGTTCGCCCGTCTCCCCGTCGT Пример 7. Ферментация рекомбинантного штамма E.coli yaad-гидрофобин DewA-His6. Инокуляция 3 мл жидкой LB-среды с экспримирующим штаммом E.coli yaad-гидрофобин DewAHis6 в сосуде Грайнера на 15 мл. Инкубация 8 ч при 37 С на мешалке с 200 об/мин. По две колбы Эрленмейера емкостью 1 л с дефлектором и 250 мл LB-среды (+100 мкг/мл ампициллина) засевали 1 мл соответствующей предварительной культуры и инкубировали 9 ч при 37 С на качалке с 200 об/мин. 13,5 л LB-среды (+100 мкг/мл ампициллина) засевали в 20 л ферментере 0,5 л предварительной культуры (OD600nm 1:10 измерено по сравнению с Н 2 О). При OD60nm 3,5 добавление 140 мл 100 мМIPTG. Через 3 ч ферментер охлаждали до 10 С и ферментативный бульон центрифугировали. Клеточный осадок использовали для последующей очистки. Пример 8. Очистка рекомбинантного гидрофобин-слитого белка.(Janke und Kunkel; IKA-Labortechnik) в течение 10 мин и затем инкубировали в течение 1 ч при комнат- 14012800 ной температуре с 500 единицами бензоназы (Merck, Darmstadt; Best.-Nr. 1.01697.0001) для расщепления нуклеиновых кислот. Перед переведением клеток в удобное для переработки состояние фильтровали с помощью стеклянного фильтрующего элемента (Р 1). Для перевода клеток в удобное для переработки состояние и для разрезания остаточных геномных ДНК осуществляли две операции по гомогенизации при 1,500 бар (Microfluidizer M-110EH; Microiluidics Corp.). Гомогенизат центрифугировали (Sorvall RC5B, GSA-Rotor, сосуд для центрифуги емкостью 250 мл, 60 мин, 4 С, 12.000 об/мин, 23.000 g), жидкость сверху поставили на лед, а осадок после центрифугирования ресуспендировали в 100 мл натрийфосфатного буфера, рН 7,5. Центрифугирование и ресуспендирование повторяли трижды, причем натрийфосфатный буфер при третьем повторе содержал 1% SDS (=додецилсульфат натрия). После ресуспендирования перемешивали 1 ч и осуществляли заключительное центрифугирование (Sorvall RC-5B, GSA-Rotor,сосуд для центрифуги емкостью 250 мл, 60 мин, 4 С, 12.000 об/мин, 23.000 g). В соответствии с SDSPAGE-аиализом гидрофобин после заключительного центрифугирования содержится в жидкости(фиг. 1). Опыты показали, что гидрофобин, по-видимому, содержится в форме телец включений в соответствующих клетках E.coli. 50 мл жидкости, содержащей гидрофобин, наносили на колонку с 50 мл никель-сефарозы высокого качества 17-5268-02 (Amersham), которая приведена к равновесию с помощью 50 мМ буфера Tris-Cl рН 8,0. Колонку промывали 50 мМ буфера Tris-Cl рН 8,0 и гидрофобин элюировали затем с помощью 50 мМ буфера Tris-Cl рН 8,0, содержащего 200 мМ имидазола. Для удаления имидазола раствор подвергали диализу против 50 мМ буфера Tris-Cl рН 8,0. На фиг. 1 показана очистка полученного гидрофобина. След А: нанесенный на колонку слой никель-сефарозы (1:10 разбавление). След В: протекание=элюат стадии промывки. Следы С-Е: OD 280 максимумы фракций элюирования (WP1, WP2, WP3). След F отображает нанесенный маркер. Гидрофобин на фиг. 1 имеет молекулярный вес около 53 кД. Более мелкие полосы представляют отчасти продукты разложения гидрофобина. Пример 9. Технологические испытания; характеристика гидрофобина с помощью изменения краевого угла капли воды на стекле. Субстрат: стекло (оконное стекло, Sddeutsche Glas, Mannheim). Использовали очищенный в соответствии с примером 8 гидрофобин. Концентрация гидрофобина в растворе: 100 мкг/мл, раствор содержит еще 50 мМ натрийацетатного буфера, а также 0,1% полиоксиэтилен(20)-сорбит-монолаурата (Tween 20), величина рН раствора: 4. Погружение стеклянной пластинки в этот раствор на ночь (температура 80 С). После чего покрытая гидрофобином стеклянная пластинка извлекается из раствора и промывается дистиллированной водой. После этого инкубация 10 мин/80 С/1% раствор SDS (=додецилсульфата натрия) в дистиллированной воде. Повторное промывание в дистиллированной воде. Образцы сушили на воздухе и определяли краевой угол (в градусах) между каплей воды в 5 мкл и обработанной стеклянной поверхностью при комнатной температуре. Измерение краевого угла осуществляли на приборе Dataphysics Contact Angle System OCA 15+,Software SCA 20.2.0. (November 2002). Измерение происходило в соответствии с данными изготовителя. Необработанное стекло давало краевой угол 305. Стеклянная пластинка, покрытая гидрофобином в соответствии с примером 8 (yaad-dewA-his6), давала краевой угол 755.Увеличение краевого угла: 45. Пример 10. Применение концентрата гидрофобина (yaad-Xa-dewA-His6) в качестве присадки к горючему. Принцип исследования. Современное горючее содержит обычно ряд различных присадок (так называемый пакет присадок). Если на этапе изготовления или эксплуатации в горючее попадет вода, то эти присадки могут проявить эмульгирующее действие и привести к образованию нежелательной эмульсии из горючего и воды. Для предотвращения этого эффекта к горючему добавляются деэмульгаторы. Испытания деэмульгатора проводились с концентратом гидрофобина согласно примеру 8 (SEQ IDNO: 19 и 20). Концентрат гидрофобина разбавлялся этиловым спиртом и добавлялся к стандартному в Европе высокосортному топливу (согласно стандарту EN 228), в котором уже содержалось 725 мг/кг специального эффективного пакета присадок А. Этот пакет присадок состоит из полиизобутенамина KerocomPIBA, смесей масел-носителей, растворителя, ингибитора коррозии и модификатора трения. Приготовлялись пробы топлива с гидрофобином в количествах 0,01, 0,03, 0,05, 0,07, 0,14 и 0,28 мг/кг. В качестве сравнительного образца (10-V1) служило топливо с пакетом присадок А без гид- 15012800 рофобина. В следующем сравнительном испытании (10-V2) использовался принятый в торговле деэмульгатор D на основе фенольных полимеров (ADX 606, фирмы Lubrizol) в количестве 1,45 мг/кг. С каждой пробой топлива были проведены эмульсионные тесты согласно стандарту DIN 51415. Для этого интенсивно перемешивались по 80 мл топлива и 20 мл воды. Затем наблюдался процесс расслоения смеси в зависимости от времени. Результаты оценивались на основании заданных в стандарте норм, причем 1 оценивалось очень хорошее расслоение, а большими цифрами - худшее расслоение. Детали приведены в указанном стандарте DIN. В табл. 1 представлены результаты испытаний. Приведены оценки слоев фазового разделения после 1, 5, 30 и 60 мин. Как правило, результат 1 или 1b получался после 5 мин. Таблица 1 Комментарии. Без добавки деэмульгатора наблюдается лишь очень медленное разрушение эмульсии. Оценка 4 неприемлема, речь идет о стабильной эмульсии. Гидрофобины уже в крайне малых количествах оказывают очень хорошее деэмульгирующее действие. Всего 0,01 ppm гидрофобина в течение 1 мин приводит к приемлемому результату. Такой же эффект, как с 0,07 мг/кг гидрофобина, получается при добавлении к топливу 1,45 мг/кг принятого в торговле деэмульгатора на основе фенольных полимеров. При применении гидрофобина достаточно 1/20 количества традиционного деэмульгатора для получения такого же эффекта. Сравнительный пример 11. Применение других белков в качестве присадки к топливу. Аналогично примеру 10 исследовались белки, кроме гидрофобина, для применения в горючем. Испытания проводились с бычьим сывороточным альбумином (БСА) и казеином. Эти белки доступны в торговой сети. Далее использовался yaad согласно SEQ ID NO 15 и 16, поскольку это партнер слияния, не связанный самостоятельно с гидрофобином. Соответствующий белок в концентрации 0,07 мг/кг добавлялся к высококачественному топливу торговой марки (согласно EN 228), которое уже содержало упомянутый выше пакет присадок А. Для сопоставления служило топливо только с пакетом присадок А без белка. Тестирование эмульсий выполнялось согласно стандарту DIN 51415, как описано выше. Результаты испытаний приведены в табл. 2. Таблица 2 Комментарии. Расслоение эмульсии без добавки деэмульгатора протекает также медленно, как в примере 10. Оценка 4 неприемлема, речь идет о стабильной эмульсии. Применяемые белки способствовали разрушению эмульсии, но скорость деэмульгирования была ниже, чем при применении гидрофобинов. Пример 12. Применение концентрата гидрофобина (Yaad-Xa-dewA-His6) в качестве деэмульгатора для сырой нефти. Испытания проводились с концентратом гидрофобина согласно примеру 8 (SEQ ID NO: 19 и 20).- 16012800 Для испытаний к 50 мл сырой нефти (пробы от АО Wintershall, зонд 301; содержание остаточной воды после добавления обычных деэмульгаторов около 3%) добавлялся концентрат гидрофобина в разных количествах. Концентрация гидрофобина в сырой нефти составляла 1, 10 и 40 ppm. После гомогенизации смеси центрифугировались в течение 10 мин при 2000 об/мин. Результаты испытаний воспроизведены в табл. 3. Таблица 3 При добавлении 10 и 40 ppm концентрата гидрофобина образуется подавляющая часть свободной водной фазы. Пример 13. Применение концентрата гидрофобина (Yaad-Xa-dewA-His6) согласно примеру 8 для разделения полимеров на фракции. Испытания проводились с концентратом гидрофобина согласно примеру 8 (SEQ ID NO: 19 и 20). В два химических стакана помещалось по 150 г полиакриловой кислоты в виде ее натриевой соли(Sokalan CP 10 S; молекулярный вес 4000 г/моль, согласно DE 19950941 А 1), затем в каждый добавлялось по 75 г изопропанола. Перемешивание в течение 5 мин, затем добавлялось по 146 г изопропанола и воды (в соотношении 1:1) и смесь перемешивалась в течение 5 мин. В химический стакан А добавлялись 50 ppm гидрофобина (1,64 м, 11,3 мг/мл) и в течение 5 мин смесь перемешивалась. Гидрофобин образовывал белые слизи в прозрачном растворе, которые спустя 5 мин полностью растворялись. В оба химических стакана добавлялось по 19,75 г 50%-ной NaOH и смесь перемешивалась в течение 15 мин. С гидрофобином раствор сразу же приобретал молочный цвет, без добавки гидрофобина раствор становился очень мутным. После 15 мин перемешивания содержимое стаканов пропускалось через делительную воронку емкостью 500 мл, встряхивалось и проводилось наблюдение, как долго длилось разделение фаз. В пробе с гидрофобином четкое разделение фаз наблюдалось через 10 мин, без добавки гидрофобина сначала образовывался пенный промежуточный слой, но четкого разделения фаз не наблюдалось. Без добавки гидрофобина четкая граница между фазами образовывалась лишь по прошествии 40 мин. Продолжительность процесса разделения до появления четкой границы между фазами: с гидрофобином: 12 мин,без гидрофобина: 40 мин. Пример 14. Сравнительный пример 15. Применение слитого гидрофобина (Yaad-Xa-dewA-His6) и бычьего сывороточного альбумина (БСА) в качестве деэмульгатора для эмульсии масло-в-воде при 55 С. Исследования проводились с концентратом гидрофобина согласно примеру 8 (SEQ ID NO: 19 и 20) и с доступным в продаже раствором бычьего сывороточного альбумина (БСА). Проверка способности деэмульгирования осуществлялась следующим образом: в качестве масла использовалось масло для гидросистем. 40 мл дистиллированной воды вливалось в мерный цилиндр емкостью 100 мл и добавлялся соответствующий белок в количестве 5 ppm относительно воды или 2,5 ppm относительно всего состава. Затем добавлялись 40 мл гидрофобина и система нагревалась в водяной бане до температуры 55 С. Время термообработки составляло 20 мин. После перемешивания в течение 5 мин при 1500 об/мин образовывалась эмульсия масла и воды. Таким образом, масло эмульгировало в водную фазу. Затем наблюдалось разделение фаз. Результаты отображают количество вновь отделенной водной фазы в мл. В одной серии испытаний использовался водный раствор обоих белков без изменения. Результаты представлены на диаграмме 1 (фиг. 2). Во второй серии испытаний рН раствора обоих белков сначала доводился до рН 1 при комнатной температуре с добавлением HCl и выдерживался 24 ч при рН 1. Затем с помощью NaOH показатель рН вновь устанавливался равным 7. Результаты представлены на диаграмме 2 (фиг. 3). Комментарии. Скорость деэмульгирования эмульсии масло-в-воде при добавлении БСА лишь незначительно выше по сравнению с пробой без деэмульгатора. При добавлении гидрофобина наблюдается четкое ускорение деэмульгирования.- 17012800 ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Применение по меньшей мере одного гидрофобина для улучшения разделения фаз в составах,содержащих по меньшей мере две жидкие фазы. 2. Применение по п.1, причем по меньшей мере один гидрофобин является слитым гидрофобином. 3. Применение по п.2, отличающееся тем, что для слитого гидрофобина речь идет по крайней мере об одном выбранном из группы (SEQ ID NO: 20), (SEQ ID NO: 22) или (SEQ ID NO: 24) гидрофобине. 4. Применение по одному из пп.1-3, причем состав, содержащий по меньшей мере две жидкие фазы,выбран из группы, состоящей из составов, содержащих масло и воду; составов, содержащих горючее или топливо и воду; реакционных смесей, содержащих по меньшей мере две жидкие фазы. 5. Применение по одному из пп.1-4, причем используется по крайней мере один гидрофобин в количестве от 0,0001 до 1000 ppm относительно всего состава. 6. Способ разделения по крайней мере двух жидких фаз в составе, содержащем по крайней мере две жидкие фазы, включающий добавление к составу по крайней мере одного гидрофобина. 7. Способ по п.6, причем используется по крайней мере один гидрофобин в количестве от 0,0001 до 1000 ppm относительно всего состава. 8. Композиция, содержащая по крайней мере одно соединение, выбранное из группы, состоящей из горючих, топлив или растворимых в воде или в масле полимерных растворов, и по меньшей мере одного гидрофобина, причем гидрофобин содержится в композиции в количестве от 0,0001 до 1000 ppm относительно всей композиции. 9. Композиция по п.8, причем композиция содержит, по крайней мере, топливо или горючее, и гидрофобин содержится в композиции в количестве от 0,001 до 0,5 ppm относительно всей композиции. 10. Композиция по одному из пп.8 или 9, причем белок является слитым гидрофобином.- 18012800 Диаграмма 1. Сравнение гидрофобина (Hбелок А) и бычьего сывороточного альбумина (BSA), неизмененные пробы Фиг. 2 Диаграмма 2. Сравнение гидрофобина (Нбелок А) и бычьего сывороточного альбумина, перед испытанием пробы выдерживались 24 ч при рН 1- 19012800 Сопоставление названий последовательностей с последовательностями ДНК и последовательностями полипептидов в протоколе последовательностей
МПК / Метки
МПК: C10L 1/26, B01D 17/05, C10G 33/04, B01D 17/04, C10L 1/22, C07K 14/375, C10L 1/24
Метки: деэмульгаторов, белков, применение, качестве
Код ссылки
<a href="https://eas.patents.su/30-12800-primenenie-belkov-v-kachestve-deemulgatorov.html" rel="bookmark" title="База патентов Евразийского Союза">Применение белков в качестве деэмульгаторов</a>
Предыдущий патент: Терапевтические применения ингибиторов rtp801
Следующий патент: Самобуферирующиеся композиции белков
Случайный патент: Таблетка с насечкой, обладающая превосходной фотостабильностью