Имидазопиридины и способы их получения и применения
Номер патента: 10426
Опубликовано: 29.08.2008
Авторы: Сунь Лихун, БОРИАК-CЙОДИН Паула, Чои Майкл Дж., Ли Вен-Чернг, Чуацюй Клаудио, Сингх Джусвиндер, Картер Мэри Бет
Формула / Реферат
1. Соединение формулы I
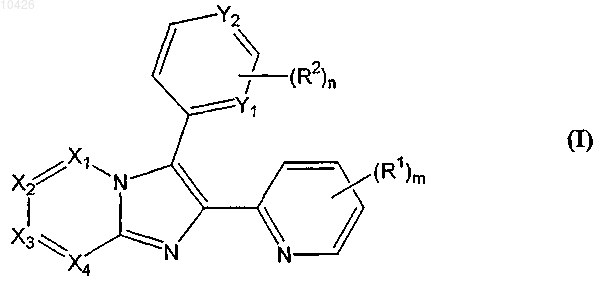
где каждый из X1, X2 и Х3 независимо выбирают из CRX или N; Х4 представляет CRX; при условии, что только два из X1, X2 и Х3 могут представлять N одновременно;
каждый из Y1 и Y2 независимо выбирают из CRY или N; при условии, что по меньшей мере один из Y1 и Y2 должен представлять N;
каждый R1 независимо выбирают из алкила, алкенила, алкинила, галогена, циклоалкила или гетероциклоалкила;
каждый из R2 независимо выбирают из алкила, алкенила, алкинила, ацила, галогена, гидрокси,
-NH2, -NH(алкила), -N(алкила)2, -NH(циклоалкила), -N(алкил)(циклоалкила), -NH(гетероциклоалкила),
-NH(гетероарила), -NH-алкилгетероциклоалкила, -NH-алкилгетероарила, -NH(аралкила), циклоалкила, (циклоалкил)алкила, арила, аралкила, ароила, гетероциклоалкила, (гетероциклоалкил)алкила, гетероарила, гетероаралкила, гетероароила, циано, гуанидино, амидино, карбокси, сульфо, меркапто, алкокси, циклоалкилокси, (циклоалкил)алкокси, арилокси, арилалкокси, гетероциклоалкилокси, (гетероциклоалкил) алкокси, гетероарилокси, гетероарилалкокси, алкилсульфанила, циклоалкилсульфанила, (циклоалкил) алкилсульфанила, арилсульфанила, аралкилсульфанила, гетероциклоалкилсульфанила, (гетероциклоалкил)алкилсульфанила, гетероарилсульфанила, гетероарилалкилсульфанила, алкилсульфинила, алкилсульфонила, аминокарбонила, аминосульфонила, алкилкарбониламино, циклоалкилкарбониламино, (циклоалкил)алкилкарбониламино, арилкарбониламино, аралкилкарбониламино, (гетероциклоалкил) карбониламино, (гетероциклоалкил)алкилкарбониламино, гетероарилкарбониламино, гетероаралкилкарбониламино, алкоксикарбониламиноалкиламино, (гетероарил)арилкарбониламиноалкиламино, гетероаралкилкарбониламиноалкиламино, (гетероарил)арилсульфониламиноалкилкарбониламиноалкиламино, арилсульфониламиноалкиламино, алкоксикарбонила, алкилкарбонилокси, мочевины, тиомочевины, сульфамоила, сульфамида или карбамоила;
m выбирают из 0, 1 или 2; при условии, что, если m равно 2, две соседние R1 группы могут объединяться с образованием 4-8-членного необязательно замещенного циклического фрагмента;
n выбирают из 0, 1, 2 или 3; при условии, что если n_2, две соседние R2 группы могут объединяться с образованием 4-8-членного необязательно замещенного циклического фрагмента;
каждый из RX и RY независимо выбирают из водорода, алкила, алкенила, алкинила, алкокси, ацила, галогена, гидрокси, амино, нитро, циано, гуанидино, амидино, карбокси, сульфо, меркапто, алкилсульфанила, алкилсульфинила, алкилсульфонила, циклоалкилкарбонила, (циклоалкил)алкилкарбонила, ароила, аралкилкарбонила, гетероциклоалкилкарбонила, (гетероциклоалкил)ацила, гетероароила, (гетероарил)ацила, аминокарбонил, алкилкарбониламино, (амино)аминокарбонила, алкилсульфониламинокарбонила, алкилсульфониламино, циклоалкилкарбониламино, циклоалкилсульфониламино, (циклоалкил) алкилкарбониламино, (циклоалкил)алкилсульфониламино, арилкарбониламино, арилсульфониламино, аралкилкарбониламино, аралкилсульфониламино, (гетероциклоалкил)карбониламино, (гетероциклоалкил)сульфониламино, (гетероциклоалкил)алкилкарбониламино, (гетероциклоалкил)алкилсульфониламино, гетероарилкарбониламино, гетероарилсульфониламино, гетероаралкилкарбониламино, гетероаралкилсульфониламино, алкоксикарбонила, алкилкарбонилокси, мочевины, тиомочевины, сульфамоила, сульфамида, карбамоила, циклоалкила, циклоалкилокси, циклоалкилсульфанила, (циклоалкил)алкила, (циклоалкил)алкокси, (циклоалкил)алкилсульфаниал, гетероциклоалкила, гетероциклоалкилокси, гетероциклоалкилсульфанила, (гетероциклоалкил)алкила, (гетероциклоалкил)алкокси, (гетероциклоалкил) алкилсульфанила, арила, арилокси, арилсульфанила, аралкила, аралкилокси, аралкилсульфанила, арилалкенила, арилалкинила, гетероарила, гетероарилокси, гетероарилсульфанила, гетероаралкила, (гетероарил)алкокси или (гетероарил)алкилсульфанила;
где термин "алкил", как группа или как часть других групп, относится к насыщенной алифатической углеводородной группе, которая может быть неразветвленной или разветвленной и содержит 1-8 атомов углерода, алкильная группа может быть необязательно замещена одним или более заместителями, такими как алкокси, циклоалкилокси, гетероциклоалкилокси, арилокси, гетероарилокси, аралкилокси, гетероарилалкокси, амино, нитро, карбокси, циано, галоген, гидрокси, сульфо, меркапто, алкилсульфанил, алкилсульфинил, алкилсульфонил, аминокарбонил, алкилкарбониламино, циклоалкилкарбониламино, циклоалкилалкилкарбониламино, арилкарбониламино, аралкилкарбониламино, гетероциклоалкилкарбониламино, гетероциклоалкилалкилкарбониламино, гетероарилкарбониламино, гетероаралкилкарбониламино, мочевина, тиомочевина, сульфамоил, сульфамид, алкоксикарбонил или алкилкарбонилокси;
термин "алкенил", как группа или как часть других групп, относится к алифатической углеводородной группе, которая может быть неразветвленной или разветвленной и содержит 2-8 атомов углерода и по меньшей мере одну двойную связь, алкенильная группа может быть необязательно замещена одним или более заместителями, такими как алкокси, циклоалкилокси, гетероциклоалкилокси, арилокси, гетероарилокси, аралкилокси, гетероарилалкокси, амино, нитро, карбокси, циано, галоген, гидрокси, сульфо, меркапто, алкилсульфанил, алкилсульфинил, алкилсульфонил, аминокарбонил, алкилкарбониламино, циклоалкилкарбониламино, циклоалкилалкилкарбониламино, арилкарбониламино, аралкилкарбониламино, гетероциклоалкилкарбониламино, гетероциклоалкилалкилкарбониламино, гетероарилкарбониламино, гетероаралкилкарбониламино, мочевина, тиомочевина, сульфамоил, сульфамид, алкоксикарбонил,или алкилкарбонилокси; т
ермин "алкинил", как группа или как часть других групп, относится к алифатической углеводородной группе, которая может быть неразветвленной или разветвленной и содержит 2-8 атомов углерода и по меньшей мере одну тройную связь, алкинильная группа может быть необязательно замещена одним или более заместителями, такими как алкокси, циклоалкилокси, гетероциклоалкилокси, арилокси, гетероарилокси, аралкилокси, гетероарилалкокси, амино, нитро, карбокси, циано, галоген, гидрокси, сульфо, меркапто, алкилсульфанил, алкилсульфинил, алкилсульфонил, аминокарбонил, алкилкарбониламино, циклоалкилкарбониламино, циклоалкилалкилкарбониламино, арилкарбониламино, аралкилкарбониламино, гетероциклоалкилкарбониламино, гетероциклоалкилалкилкарбониламино, гетероарилкарбониламино, гетероаралкилкарбониламино, мочевина, тиомочевина, сульфамоил, сульфамид, алкоксикарбонил или алкилкарбонилокси;
термин "циклоалкильная" группа относится к алифатическому карбоциклическому кольцу, состоящему из 3-10 атомов углерода, которая может быть необязательно замещена одним или более заместителями, такими как алкил (включая карбоксиалкил, гидроксиалкил и галогеноалкил, такой как трифторметил), алкенил, алкинил, циклоалкил, (циклоалкил)алкил, гетероциклоалкил, (гетероциклоалкил)алкил, арил, гетероарил, алкокси, циклоалкилокси, гетероциклоалкилокси, арилокси, гетероарилокси, аралкилокси, гетероаралкилокси, ароил, гетероароил, амино, нитро, карбокси, алкоксикарбонил, алкилкарбонилокси, аминокарбонил, алкилкарбониламино, циклоалкилкарбониламино, (циклоалкил)алкилкарбониламино, арилкарбониламино, аралкилкарбониламино, гетероциклоалкилкарбониламино, (гетероциклоалкил)алкилкарбониламино, гетероарилкарбониламино, гетероаралкилкарбониламино, циано, галоген, гидрокси, ацил, меркапто, алкилсульфанил, сульфокси, мочевина, тиомочевина, сульфамоил, сульфамид, оксо или карбамоил;
термин "гетероциклоалкильная" группа относится к 3-10-членной насыщенной кольцевой структуре, в которой один или более атомов кольца являются гетероатомом, таким как N, О или S, которая необязательно может быть замещена одним или более заместителями, такими как алкил (включая карбоксиалкил, гидроксиалкил и галогеноалкил, такой как трифторметил), алкенил, алкиншы, циклоалкил, (циклоалкил)алкил, гетероциклоалкил, (гетероциклоалкил)алкил, арил, гетероарил, алкокси, циклоалкилокси, гетероциклоалкилокси, арилокси, гетероарилокси, аралкилокси, гетероаралкилокси, ароил, гетероароил, амино, нитро, карбокси, алкоксикарбонил, алкилкарбонилокси, аминокарбонил, алкилкарбониламино, циклоалкилкарбониламино, (циклоалкил)алкилкарбониламино, арилкарбониламино, аралкилкарбониламино, гетероциклоалкилкарбониламино, (гетероциклоалкил)алкилкарбониламино, гетероарилкарбониламино, гетероаралкилкарбониламино, циано, галоген, гидрокси, ацил, меркапто, алкилсульфанил, сульфокси, мочевина, тиомочевина, сульфамоил, сульфамид, оксо или карбамоил;
термин "гетероарильная" группа относится к моноциклической, бициклической или трициклической кольцевой структуре, содержащей 5-15 атомов кольца, где один или более атомов кольца являются гетероатомом, таким как N, О, S или В, и где одно или более колец бициклической или трициклической кольцевой структуры являются ароматическими, гетероарил может быть необязательно замещен одним или более заместителями, такими как алкил (включая карбоксиалкил, гидроксиалкил, и галогеноалкил, такой как трифторметил), алкенил, алкинил, циклоалкил, (циклоалкил)алкил, гетероциклоалкил, (гетероциклоалкил)алкил, арил, гетероарил, алкокси, циклоалкилокси, гетероциклоалкилокси, арилокси, гетероарилокси, аралкилокси, гетероаралкилокси, ароил, гетероароил, амино, нитро, карбокси, алкоксикарбонил, алкилкарбонилокси, аминокарбонил, алкилкарбониламино, циклоалкилкарбониламино, (циклоалкил)алкилкарбониламино, арилкарбониламино, аралкилкарбониламино, гетероциклоалкилкарбониламино, (гетероциклоалкил)алкилкарбониламино, гетероарилкарбониламино, гетероаралкилкарбониламино, циано, галоген, гидрокси, ацил, меркапто, алкилсульфанил, сульфокси, мочевина, тиомочевина, сульфамоил, сульфамид, оксо или карбамоил;
термин "арильная" группа относится к фенильной, нафтильной или бензоконденсированной группе, содержащей от 2 до 3 колец, арил может быть необязательно замещен одним или более заместителями, такими как алкил (включая карбоксиалкил, гидроксиалкил и галогеноалкил, такой как трифторметил), алкенил, алкинил, циклоалкил, (циклоалкил)алкил, гетероциклоалкил, (гетероциклоалкил)алкил, арил, гетероарил, алкокси, циклоалкилокси, гетероциклоалкилокси, арилокси, гетероарилокси, аралкилокси, гетероаралкилокси, ароил, гетероароил, амино, нитро, карбокси, алкоксикарбонил, алкилкарбонилокси, аминокарбонил, алкилкарбониламино, циклоалкилкарбониламино, (циклоалкил)алкилкарбониламино, арилкарбониламино, аралкилкарбониламино, (гетероциклоалкил)карбониламино, (гетероциклоалкил) алкилкарбониламино, гетероарилкарбониламино, гетероаралкилкарбониламино, циано, галоген, гидрокси, ацил, меркапто, алкилсульфанил, сульфокси, мочевина, тиомочевина, сульфамоил, сульфамид, оксо или карбамоил;
термин "аминогруппа" относится к -NRXRY, где каждый из RX и RY независимо представляет водород, гидроксил, алкил, алкокси, циклоалкил, (циклоалкил)алкил, арил, аралкил, гетероциклоалкил, (гетероциклоалкил)алкил, гетероарил или гетероаралкил, причем если термин "амино" относится не к концевой группе, он представлен как -NRX-, где RX имеет указанные выше значения;
термин "ацильная" группа относится к формильной группе или к группе алкил-С(=O)-, где "алкил" имеет указанные выше значения; термин "карбамоильная" группа относится к группе, структура которой представлена -O-CO-NRXRY или -NRX-CO-O-RZ, где RX и RY имеют указанные выше значения и RZ представляет алкил, циклоалкил, (циклоалкил)алкил, арил, аралкил, гетероциклоалкил, (гетероциклоалкил)алкил, гетероарил или гетероаралкил;
термин "сульфокси" группа относится к -O-SO-RX или -SO-O-RX группам, где RX имеет указанные выше значения; термин "сульфамоильная" группа относится к группе -S(O)2-NRXRY или -NRX-S(О)2-RZ, где RX, RY и RZ имеют указанные выше значения; термин "сульфамидная" группа относится к группе
-NRX-S(О)2-NRYRZ где RX, RY и RZ имеют указанные выше значения; термин "мочевина" относится к группе -NRX-CO-NRYRZ и термин "тиомочевина" относится к группе -NRX-CS-NRYRZ, где RX, RY и RZ имеют указанные выше значения; термин "циклический фрагмент" включает циклоалкил, гетероциклоалкил, циклоалкенил, гетероциклоалкенил, арил или гетероарил, каждый из которых имеет указанные выше значения.
2. Соединение по п.1, где каждый из X1, Х2, и Х3 представляет CRX.
3. Соединение по п.2, где каждый RX независимо выбирают из водорода, незамещенного алкила, гидроксиалкила, галогеноалкила, аминоалкила, арилоксиалкила, гетероаралкилоксиалкила, алкокси, галогена, гидрокси, карбокси, циано, гуанидино, амидино, амино, карбокси, (гетероарил)ацила, алкоксикарбонила, аминокарбонила, алкилкарбониламино, циклоалкилкарбониламино, гетероарилкарбониламино, (гетероциклоалкил)алкокси, (гетероарил)алкокси, (гетероарил)алкилсульфанила, гетероциклоалкила, (гетероциклоалкил)алкила, гетероарила или гетероаралкила.
4. Соединение по п.2, где каждый RX независимо выбирают из водорода, незамещенного алкила, гидроксиалкила, трифторметила, алкокси, галогена, гидрокси, циано, гуанидино, амидино, -NH2,
-NH(незамещенного алкила), -NH(гидроксиалкила), -NH(алкоксиалкила), -NH(карбоксиалкила),
-N(незамещенного алкила)2, -NH(гетероциклоалкила), -NH(гетероарила), -NH(гетероциклоалкилалкила), -NH(аралкила), -NH(гетероаралкила), -NH-CO-алкила, -NH-CO-гетероарила, аминокарбонила, гетероциклоалкила или гетероарила.
5. Соединение по п.2, где каждый RX представляет водород, метил, этил, -NH2, -NH-CO-метил, -NH-CO-этил, -NH-CO-пиридил или -CO-NH(OH).
6. Соединение по п.2, где каждый из Х2, Х3 и Х4 независимо выбирают из -СН-, -С(СН3)-, -С(ОН)-,
-C(NH2)-, -C(CO-NH2), -С(CO-NHOH)-, -С(NH(незамещенного алкила))-, -С(NH(арила))-,
-С(NH(аралкила))-, -С(NH(гетероарила))-, -С(NH(гетероарилалкила))-, -С(NH-CO-(незамещенного алкила))-, -С(NH-CO-(арила))-, -С(NH-CO-(гетероарила))-, -С(NH-CO-(аралкила))-, -С(NH-CO-(гетероарилалкила))-, -С(NH-SO2-(незамещенного алкила))-, -С(NH-SO2-(арила))-, -C(NH-SO2-гетероарила))-, -С(NH-SO2-(аралкила))-, -С(NH-SO2-(гетероарилалкила))-, -С(NH-SO-NH(незамещенного алкила))-, -С(NH-SO2-NH(арила))-, -С(NH-SO2-NH(гетероарила))-, -С(NH-SO2-NH(аралкила))-, -С(NH-SO2-NH(гетероарилалкила))-, -С(гидроксиалкила)- или -С(карбокси)- и X1 представляет -СН-.
7. Соединение по п.2, где каждый из Х1 и Х2 представляет -СН-; и Х3 представляет -C(NH2)-,
-С(NH(незамещенный алкил))-, -С(NH(арил))-, -С(NH(аралкил))-, -С(NH(гетероарил))-,
-С(NH(гетероарилалкил))-, -С(NH-CO-(незамещенный алкил))-, -С(NH-CO-(арил))-, -С(NH-CO-(гетероарил))-, -С(NH-CO-(аралкил))-, -С(NH-CO-(гетероарилалкил))-, -С(NH-SO2-(незамещенный алкил))-, -С(NH-SO2-(арил))-, -C(NH-SO2-гетероарил))-, -С(NH-SO2-(аралкил))-, -С(NH-SO2-(гетероарилалкил))-, -С(NH-SO2-NH(незамещенный алкил))-, -С(NH-SO2-NH(арил))-, -С(NH-SO2-NH (гетероарил))-, -С(NH-SO2-NH (аралкил))- или -С(NH-SO2-NH(гетероарилалкил))-.
8. Соединение по п.2, где каждый R1 независимо выбирают из незамещенного алкила, гидроксиалкила, галогеноалкила, аминоалкила, арилоксиалкила, гетероаралкилоксиалкила, незамещенного алкенила, галогена, циклоалкила, гетероциклоалкила, (гетероциклоалкил)алкила или гетероаралкила.
9. Соединеэшх по п.2, где m=1 и R1 выбирают из 6-алкила, 6-алкенила, 6-циклоалкила или 6-галогена.
10. Соединение по п.2, где оба Y1 и Y2 представляют N.
11. Соединение по п.10, где n выбирают из 1 или 2 и каждый R2 независимо выбирают из незамещенного алкила, гидроксиалкила, галогеноалкила, аминоалкила, арилоксиалкила, гетероаралкилоксиалкила, алкокси, ацила, галогена, гидрокси, карбокси, циано, гуанидино, амидино, -NH2, моноалкиламино, диалкиламино, моноциклоалкиламино, моногетероциклоалкиламино, моногетероариламино, моно((гетероциклоалкил)алкил)амино, моно(гетероаралкил)амино, N(алкил)(циклоалкила), меркапто, алкилсульфанила, алкилсульфинила, алкилсульфонила, -CO-NH2, -CO-NH(алкила), -CO-N(алкила)2, -NH-CO-алкила, -N(алкил)-СО-алкила, -СО2-алкила, -О-СО-алкила, -SO2-NH2, -SO2-NH(алкила), -SO2-N (алкила)2, -NH-SO2-алкила, -N(алкил)-SO2-алкила, -NH-CO-NH(алкила), -N(алкил)-CO-NH(алкила), -NH-алкил-NH-СО-алкилгетероарила, -NH-алкил-NH-СО-арилгетероарила, -NH-алкил-NH-CO-алкил-NH-SO2-арилгетероарила, -NH-алкил-NH-SO2-арила, -NH-SO2-NH(алкила), -N(алкил)-SO2-NH(алкила), гетероциклоалкила или гетероарила.
12. Соединение по п.11, где R2 замещен в 3 положении группой, выбранной из гуанидино, амидино, -NH2, моноалкиламино, диалкиламино, моноциклоалкиламино, моногетероциклоалкиламино, моногетероариламино, моно((гетероциклоалкил)алкил)амино, моно(гетероаралкил)амино, -NH-CO-NH(алкила),
-N(алкил)-CO-NH(алкила), -NH-алкил-NH-СО-алкилгетероарила, -NH-алкил-NH-СО-арилгетероарила,
-NH-алкил-NH-СО-алкил-NH-SO2-арилгетероарила, -NH-алкил-NH-SO2-арила, -NH-SO2-NH (алкила),
-N(алкил)-SO2-NH(алкила), гетероциклоалкила или гетероарила.
13. Соединение по п.12, где m=1 и R1 выбирают из 6-метила, 6-этила, 6-пропила, 6-хлоро, 6-трифторметила, 6-винила или 6-циклопропила.
14. Соединение по п.1, где R1 замещен в 5 положении или в 6 положении.
15. Соединение по п.14, где R1 представляет С1-4алкил или галоген.
16. Соединение по п.1, где каждый R1 независимо выбирают из незамещенного алкила, гидроксиалкила, галогеноалкила, аминоалкила, арилоксиалкила, гетероаралкилоксиалкила, незамещенного алкенила, галогена, циклоалкила или гетероциклоалкила.
17. Соединение по п.16, где m=1 и R1 выбирают из 6-метила, 6-этила, 6-пропила, 6-хлоро, 6-трифторметила, 6-винила или 6-циклопропила.
18. Соединение по п.1, где оба Y1 и Y2 представляют N.
19. Соединение по п.18, где n выбирают из 1 или 2 и каждый R2 независимо выбирают из незамещенного алкила, гидроксиалкила, галогеноалкила, аминоалкила, арилоксиалкила, гетероаралкилоксиалкила, алкокси, ацила, галогена, гидрокси, карбокси, циано, гуанидино, амидино, -NH2, моноалкиламино, диалкиламино, моноциклоалкиламино, моногетероциклоалкиламино, моногетероариламино, моно((гетероциклоалкил)алкил)амино, моно(гетероаралкил)амино, N(алкил)(циклоалкила), меркапто, алкилсульфанила, алкилсульфинила, алкилсульфонила, -CONH2, -CONH(алкила), -CO-N(алкила)2, -NH-CO-алкила, -N(алкил)-СО-алкила, -СО2-алкила, -O-СО-алкила, -SO2-NH2, -SO2-NH(алкила), -SO2-N(алкила)2, -NH-SO2-алкила, -N(алкил)-SO2-алкила, -NH-CO-NH(алкила), -N(алкил)-CO-NH(алкила), -NH-SO2-NH(алкила), -N(алкил)-SO2-NH (алкила), -NH-алкил-NH-СО-алкилгетероарила, -NH-алкил-NH-СО-арилгетероарила, -NH-алкил-NH-СО-алкил-NH-SO2-арилгетероарила, -NH-алкил-NH-SO2-арила, гетероциклоалкила или гетероарила.
20. Соединение по п.19, где n=1 и каждый R2 независимо выбирают из гуанидино, амидино, -NH2, моноалкиламино, диалкиламино, моноциклоалкиламино, моногетероциклоалкиламино, моногетероариламино, моно((гетероциклоалкил)алкила)амино, моно(гетероаралкил)амино, -NH-CO-NH(алкила),
-N(алкил)-CO-NH(алкила), -NH-SO2-NH(алкила), -N(алкил)-SO2-NH(алкила), -NH-алкил-NH-СО-алкилгетероарила, -NH-алкил-NH-СО-арилгетероарила, -NH-алкил-NH-СО-алкил-NH-SO2-арилгетероарила, -NH-алкил-NH-SO2-арила, гетероциклоалкила или гетероарила.
21. Соединение по п.20, где R2 замещен в 3 положении.
22. Соединение по п.1, где каждый из Х2, Х3 и Х4 независимо выбирают из -СН-, -С(ОН)-, -C(NH2)-, -С(NH(незамещенного алкила))-, -С(NH(арила))-, -С(NH(аралкила))-, -С(NH(гетероарила))-,
-С(NH(гетероарилалкила))-, -С(NH-CO-(незамещенного алкила))-, -С(NH-CO-(арила))-, -С(NH-CO-(гетероарила))-, -С(NH-CO-(аралкила))-, -С(NH-CO-(гетероарилалкила))-, -С(NH-SO2-(незамещенного алкила))-, -С(NH-SO2-(арила))-, -С(NH-SO2-гетероарила))-, -С(NH-SO2-(аралкила))-, -С(NH-SO2-(гетероарилалкила))-, -С(NH-SO2-NH(незамещенного алкила))-, -С(NH-SO2-NH(арила))-, -С(NH-SO2-NH (гетероарила))-, -С(NH-SO2-NH (аралкила))-, -С(NH-SO2-NH(гетероарилалкила))-, -С(гидроксиалкила)- или -С(карбокси)-; или каждый из Х2 и Х3 независимо представляет N.
23. Соединение по п.1, где X1 представляет -СН-.
24. Соединение по п.1, где X1 представляет N.
25. Соединение по п.1, где Х2 представляет N.
26. Соединение по п.1, где Х3 представляет N.
27. Соединение по п.1, выбранное из группы, включающей
(2-метоксиэтил)-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
трет-бутиловый эфир (3-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламино}пропил)карбаминовой кислоты;
(3-имидазол-1-илпропил)-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
(4-метоксибензил)-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
[2-(6-метилпиридин-2-ил)-3-(2-метилсульфанилпиримидин-4-ил)имидазо[1,2-а]пиридин-6-ил]метанол;
3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин;
трет-бутиловый эфир (4-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламино}бутил)карбаминовой кислоты;
(4-аминобензил)-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
трет-бутиловый эфир (5-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламино}пентил)карбаминовой кислоты;
[3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-ил]метанол;
[3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-7-ил]метанол;
[3-(2-аминопиримидин-4-ил)-6-метил-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-8-ил]-(2-морфолин-4-илэтил)амин;
[3-(2-аминопиримидин-4-ил)-6-метил-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-8-ил]-(2-пиридин-2-илэтил)амин;
[3-(2-аминопиримидин-4-ил)-6-метил-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-8-ил]-(2-пиридин-3-илэтил)амин;
[3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-ил]метанол;
[3-(2-аминопиримидин-4-ил)-6-метил-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-8-ил]-(2-пиридин-4-илэтил)амин;
[3-(2-аминопиримидин-4-ил)-6-метил-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-8-ил]-(3-морфолин-4-илпропил)амин;
[3-(4-метилпиперазин-1-ил)пропил]-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
[3-(4-метилпиперидин-1-ил)пропил]-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
[4-(2-пиридин-2-илимидазо[1,2-а]пиридин-3-ил)пиримидин-2-ил]пиридин-3-илметиламин;
{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}-((R)-1-фенилэтил)амин;
{4-[2-(6-метилпиридин-2-ил)имидазю[1,2-а]пиридин-3-ил]пиримидин-2-ил}-((S)-1-фенилэтил)амин;
{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}-(1Н-тетразол-5-ил)амин;
{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}-(2Н-пиразол-3-ил)амин;
{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}-(2-морфолин-4-илэтил)амин;
{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3ил]пиримидин-2-ил}-(2-пиридин-2-илэтил)амин;
{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}-(2-пиридин-3-илэтил)амин;
{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}-(2-пиридин-4-илэтил)амин;
{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}-(3-морфолин-4-илпропил)амин;
{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3ил]пиримидин-2-ил}-(3-пиперидин-1-илпропил)амин;
{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}-[1,3,4]тиадиазол-2-иламин;
2-(6-метилпиридин-2-ил)-3-(2-метилсульфанилпиримидин-4-ил)имидазо[1,2-а]пиридин;
метиловый эфир 2-(6-метилпиридин-2-ил)-3-(2-метилсульфанилпиримидин-4-ил)имидазо[1,2-а]пиридин-6-карбоновой кислоты;
этиловый эфир 2-(6-метилпиридин-2-ил)-3-(2-метилсульфанилпиримидин-4-ил)имидазо[1,2-а]пиридин-7-карбоновой кислоты;
2-(6-метилпиридин-2-ил)-3-(2-метилсульфанилпиримидин-4-ил)имидазо[1,2-а]пиримидин-7-иламин;
{7,7-диметил-8-[5-(4-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламино}бутилкарбамоил)пентил]-2-оксо-4-трифторметил-7,8-дигидро-2Н-1-окса-8-азаантрацен-5-ил}метансульфоновая кислота;
2-(2,7-дифтор-6-гидрокси-3-оксо-9,9а-дигидро-3Н-ксантен-9-ил)-3,5,6-трифтор-4-[(4-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламино}бутилкарбамоил)метилсульфанил]бензойная кислота;
2-(6-метилпиридин-2-ил)-3-(2-морфолин-4-илпиримидин-4-ил)имидазо[1,2-а]пиридин;
2-(6-метилпиридин-2-ил)-3-(2-пиперидин-1-илпиримидин-4-ил)имидазо[1,2-а]пиридин;,
2-(6-метилпиридин-2-ил)-3-(2-пирролидин-1-илпиримидин-4-ил)имидазо[1,2-а]пиридин;
2-(6-метилпиридин-2-ил)-3-[2-(1Н-тетразол-5-ил)пиримидин-4-ил]имидазо[1,2-а]пиридин;
2-(6-метилпиридин-2-ил)-3-пиримидин-4-илимидазо[1,2-а]пиридин;
2-(6-метилпиридин-2-ил)-3-пиримидин-4-илимидазо[1,2-а]пиримидин-7-иламин;
3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-8-иламин;
3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбонитрил;
3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбоновая кислота;
([1,4]диоксан-2-илметил)амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а] пиридин-6-карбоновой кислоты;
([1,4]диоксан-2-илметил)амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а] пиридин-6-карбоновой кислоты;
(2-диметиламиноэтил)амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а] пиридин-6-карбоновой кислоты;
(2-метоксиэтил)амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбоновой кислоты;
(2-тиофен-2-илэтил)амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбоновой кислоты;
[3-(4-метилпиперазин-1-ил)пропил]амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил) имидазо[1,2-а]пиридин-6-карбоновой кислоты;
амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбоновой кислоты;
циклопропиламид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбоновой кислоты;
этиламид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбоновой кислоты;
гидроксиамид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбоновой кислоты;
метоксиамид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбоновой кислоты;
метиловый эфир 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбоновой кислоты;
3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-7-карбоновая кислота;
([1,4]диоксан-2-илметил)амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а] пиридин-7-карбоновой кислоты;
(2-аминоэтил)амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-7-карбоновой кислоты;
(2-диметиламиноэтил)амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а] пиридин-7-карбоновой кислоты;
(2-гидроксиэтил)амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-7-карбоновой кислоты;
(2-оксо-2-пиридин-3-илэтил)амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо [1,2-а]пиридин-7-карбоновой кислоты;
(2-тиофен-2-илэтил)амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-7-карбоновой кислоты;
(пиперидин-3-илметил)амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а] пиридин-7-карбоновой кислоты;
2,2-диметилгидразид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-7-карбоновой кислоты;
амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-7-карбоновой кислоты;
циклопропиламид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-7-карбоновой кислоты;
этиловый эфир 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-7-карбоновой кислоты;
этиламид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-7-карбоновой кислоты;
гидроксиамид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-7-карбоновой кислоты;
метоксиамид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-7-карбоновой кислоты;
3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиримидин-7-иламин;
3-(2-азетидин-1-илпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин;
этиловый эфир 3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-7-карбоновой кислоты;
метиловый эфир 3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбоновой кислоты;
3-(2-метансульфонилпиримидин-4-ил)-7-метил-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин;
3-(2-метансульфонилпиримидин-4-ил)-8-метил-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин;
3,3-диметил-N-[2-(6-метилпиридин-2-ил)-3-(2-метилсульфанилпиримидин-4-ил)имидазо[1,2-а]пиримидин-7-ил]бутирамид;
3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбонитрил;
3-(2-метилсульфанилпиримидин-4-ил)-2-пиридин-2-илимидазо[1,2-а]пиридин;
3,6-дихлор-N-(4-4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламино-бутил)-2-(2,4,5,7-тетрахлор-6-гидрокси-3-оксо-9,9а-дигидро-3Н-ксантен-9-ил)терефталамовая кислота;
3-[2-(2-метилазиридин-1-ил)пиримидин-4-ил]-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин;
3-[2-(4-метилпиперазин-1-ил)пиримидин-4-ил]-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин;
метиловый эфир 3-{[3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбонил]амино}пропионовой кислоты;
метиловый эфир 3-{[3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-7-карбонил]амино}пропионовой кислоты;
3-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламино}фенол;
4-(2-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламино}этил)бензолсульфонамид;
4-(2-пиридин-2-илимидазо[1,2-а]пиридин-3-ил)пиримидин-2-иламин;
4-[2-(6-хлорпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламин;
4-[2-(6-метилпиридин-2-ил)-7-трифторметилимидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламин;
4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламин;
4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-карбонитрил;
амид 4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3ил]пиримидин-2-карбоновой кислоты;
4-[6-бром-2-(6-метилпиридин-2-ил)имидазю[1,2-а]пиридин-3-ил]пиримидин-2-иламин;
4-[6-хлор-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил ]пиримидин-2-иламин;
4-[6-фтор-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламин;
4-[6-метил-2-(6-метилпиридин-2-ил)-8-(2-морфолин-4-илэтиламино)имидазо[1,2-а]пиридин-3-ил] пиримидин-2-ол;
4-[6-метил-2-(6-метилпиридин-2-ил)-8-(2-пиридин-2-илэтиламино)имидазо[1,2-а]пиримидин-3-ил] пиримидин-2-ол;
4-[6-метил-2-(6-метилпиридин-2-ил)-8-(2-пиридин-3-илэтиламино)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ол;
4-[6-метил-2-(6-метилпиридин-2-ил)-8-(2-пиридин-4-илэтиламино)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ол;
4-[6-метил-2-(6-метилпиридин-2-ил)-8-морфолин-4-илимидазо[1,2-а]пиридин-3-ил]пиримидин-2-ол;
4-[6-метил-2-(6-метилпиридин-2-ил)-8-морфолин-4-илимидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламин;
4-[6-метил-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламин;
4-[7-аминометил-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламин;
4-[7-метил-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил ]пиримидин-2-иламин;
4-[8-бензилокси-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ол;
4-[8-бензилокси-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламин;
4-[8-бром-6-метил-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ол;
4-[8-метил-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламин;
6-хлор-3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин;
(4-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламино}бутил)амид 5-диметиламинонафталин-1-сульфоновой кислоты;
6-(2,7-дифтор-6-гидрокси-3-оксо-3Н-ксантен-9-ил)-N-(4-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламино}бутил)изофталамовая кислота;
6-амино-9-[2-карбокси-5-(4-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламино}бутилкарбамоил)фенил]ксантен-3-илиденаммоний;
6-бром-2-(6-метилпиридин-2-ил)-3-(2-метилсульфанилпиримидин-4-ил)имидазо[1,2-а]пиридин;
6-фтор-2-(6-метилпиридин-2-ил)-3-(2-метилсульфанилпиримидин-4-ил)имидазо[1,2-а]пиридин;
7-амино-4-метил-3-[(4-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-
иламино}бутилкарбамоил)метил]-2-оксо-2Н-хромен-6-сульфоновая кислота;
циклобутил{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
циклопентил{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
циклопропил{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
циклопропилметил{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
диметил{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
изопропил{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
метил{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
N-(2-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламино}этил)ацетамид;
N-(4-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламино}бутил)ацетамид;
N,N-диметил-N'-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}этан-1,2-диамин;
N-[2-(6-метилпиридин-2-ил)-3-(2-метилсульфанилпиримидин-4-ил)имидазо[1,2-а]пиримидин-7-ил]-3-пиридин-3-илпропионамиц;
N-[2-(6-метилпиридин-2-ил)-3-(2-метилсульфанилпиримидин-4-ил)имидазо[1,2-а]пиримидин-7-ил]никотинамид;
N-[2-(6-метилпиридин-2-ил)-3-(2-метилсульфанилпиримидин-4-ил)имидазо[1,2-а]пиримидин-7-ил]пропионамид;
N-[3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбонил]метансульфонамид;
N-[3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-7-карбонил]метансульфонамид;
N-[3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиримидин-7-ил]-2-(3-метоксифенил)ацетамид;
N-[3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиримидин-7-ил]-3,3-диметилбутирамид;
N-[3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиримидин-7-ил]-3-пиридин-3-илпропионамид;
N-[3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиримидин-7-ил]ацетамид;
N-[3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиримидин-7-ил]никотинамид;
N-[3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиримидин-7-ил]-2-(3-метоксифенил)ацетамид;
N-[3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиримидин-7-ил]-3,3-диметилбутирамид;
N-[3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиримидин-7-ил]-3-пиридин-3-илпропионамид;
N-[3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиримидин-7-ил]никотинамид;
N-[3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиримидин-7-ил]пропионамид;
N-[3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиримидин-7-ил]пропионамид;
N-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3ил] пиримидин-2-ил}ацетамид;
N1-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3ил] пиримидин-2-ил}бутан-1,4-диамин;
N1-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}пропан-1,3-диамин;
N-(4-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламино}бутил)-(BODIPY FL)амид и
N-(4-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламино}бутил)-(Texas Red-X)амид
или их фармацевтически приемлемые соли или N-оксиды.
28. Соединение по п.1, выбранное из группы, включающей
(2-метоксиэтил)-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
трет-бутиловый эфир (3-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламино}пропил)карбаминовой кислоты;
(3-имидазол-1-илпропил)-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
(4-аминобензил)-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
трет-бутиловый эфир (5-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламино}пентил)карбаминовой кислоты;
[3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-ил]метанол;
[3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-7-ил]метанол;
[3-(2-аминопиримидин-4-ил)-6-метил-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-8-ил]-(2-пиридин-2-илэтил)амин;
[3-(4-метилпиперазин-1-ил)пропил]-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
[3-(4-метилпиперидин-1-ил)пропил]-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
[3-(4-метилпиперазин-1-ил)пропил]-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3ил]пиримидин-2-ил}-(2Н-пиразол-3-ил)амин;
{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3ил]пиримидин-2-ил}-(2-морфолин-4-илэтил)амин;
{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3ил]пиримидин-2-ил}-(2-пиридин-2-илэтил) амин;
{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3ил]пиримидин-2-ил}-(2-пиридин-3-илэтил) амин;
{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}-(2-пиридин-4-илэтил) амин;
{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}-(3-морфолин-4-илпропил)амин;
{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}-(3-пиперидин-1-илпропил)амин;
{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}-[1,3,4]тиадиазол-2-иламин;
2-(6-метилпиридин-2-ил)-3-пиримидин-4-илимидазо[1,2-а]пиримидин-7-иламин;
3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбонитрил;
(2-метоксиэтил)амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбоновой кислоты;
аьшф 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбоновой кислоты;
циклопропиламид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбоновой кислоты;
этиламид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбоновой кислоты;
гидроксиамид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбоновой кислоты;
метоксиамид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбоновой кислоты;
(2-тиофен-2-илэтил)амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-7-карбоновой кислоты;
амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-7-карбоновой кислоты;
циклопропиламид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-7-карбоновой кислоты;
этиламид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-7-карбоновой кислоты;
метоксиамид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-7-карбоновой кислоты;
3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-7-иламин;
3-(2-азетидин-1-илпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин;
3-[2-(2-метилазиридин-1-ил)пиримидин-4-ил]-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин;
метиловый эфир 3-{[3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-7-карбонил]амино}пропионовой кислоты;
4-(2-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3ил]пиримидин-2-иламино}этил)бензолсульфонамид;
4-[2-(6-хлорпиридин-2-ил)имидазо[1,2-а]пиридин-3ил] пиримидин-2-иламин;
4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламин;
4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-карбонитрил;
4-[6-бром-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3ил]пиримидин-2-иламин;
4-[6-хлор-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламин;
4-[6-фтор-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3ил]пиримидин-2-иламин;
4-[6-метил-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3ил]пиримидин-2-иламин;
4-[7-аминометил-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламин;
4-[7-метил-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3ил]пиримидин-2-иламин;
4-[8-метил-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3ил]пиримидин-2-иламин;
6-(2,7-дифтор-6-гидрокси-3-оксо-3Н-ксантен-9-ил)-N-(4-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а] пиридин-3-ил]пиримидин-2-иламино}бутил)изофталамовая кислота;
7-амино-4-метил-3-[(4-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламино}бутилкарбамоил)метил]-2-оксо-2Н-хромен-6-сульфоновая кислота;
циклобутил{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
циклопентил{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
циклопропил{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
циклопропилметил{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
диметил{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
изопропил{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
метил{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
N-(2-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламино}этил)ацетамид;
N-(4-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридил-3-ил]пиримидин-2-иламино}бутил)ацетамид;
N-[3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиримидин-7-ил]-2-(3-метоксифенил)ацетамлд;
N-[3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиримидин-7-ил]-3,3-диметилбутирамид;
N-[3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиримидин-7-ил]-3-пиридин-3-илпропионамид;
N-[3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиримидин-7-ил]ацетамид;
N-[3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиримидин-7-ил]никотинамид;
N-[3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиримидин-7-ил]пропионамид;
N-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}ацетамид;
N1-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}бутан-1,4-диамин;
трет-бутиловый эфир (4-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламино}бутил)карбаминовой кислоты;
[3-(2-аминопиримидин-4-ил)-6-метил-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-8-ил]-(2-морфолин-4-илэтил)амин;
[3-(2-аминопиримидин-4-ил)-6-метил-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-8-ил]-(2-пиридин-3-илэтил)амин;
[3-(2-аминопиримидин-4-ил)-6-метил-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-8-ил]-(2-пиридин-4-илэтил)амин;
[3-(2-аминопиримидин-4-ил)-6-метил-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-8-ил]-(3-морфолин-4-илпропил)амин;
[4-(2-пиридин-2-илимидазо[1,2-а]пиридин-3-ил)пиримидин-2-ил]пиридин-3-илметиламин;
{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3ил]пиримидин-2-ил}-((R)-1-фенилэтил)амин;
{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}-((S)-1-фенилэтил)амин;
{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}-(1Н-тетразол-5-ил) амин;
{7,7-диметил-8-[5-(4-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламино}бутилкарбамоил)пентил]-2-оксо-4-трифторметил-7,8-дигидро-2Н-1-окса-8-азаантрацен-5-ил} метансульфоновая кислоты;
2-(6-метилпиридин-2-ил)-3-(2-морфолин-4-илпиримидин-4-ил)имидазо[1,2-а]пиридин;
2-(6-метилпиридин-2-ил)-3-(2-пиперидин-1-илпиримидин-4-ил)имидазо[1,2-а]пиридин;
2-(6-метилпиридин-2-ил)-3-(2-пирролидин-1-илпиримидин-4-ил)имидазо[1,2-а]пиридин;
2-(6-метилпиридин-2-ил)-3-пиримидин-4-илимидазо[1,2-а]пиридин;
3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-8-иламин;
3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбоновая кислота;
([1,4]диоксан-2-илметил)амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а] пиридин-6-карбоновой кислоты;
([1,4]диоксан-2-илметил)амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а] пиримидин-6-карбоновой кислоты;
(2-диметиламиноэтил)амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а] пиридин-6-карбоновой кислоты;
(2-тиофен-2-илэтил)амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбоновой кислоты;
метиловый эфир 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбоновой кислоты;
([1,4]диоксан-2-илметил)амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а] пиридин-7-карбоновой кислоты;
(2-диметиламиноэтил)амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а] пиридин-7-карбоновой кислоты;
(2-гидроксиэтил)амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-7-карбоновой кислоты;
(2-оксо-2-пиридин-3-илэтил)амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо [1,2-а]пиридин-7-карбоновой кислоты;
(пиперидин-3-илметил)амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а] пиридин-7-карбоновой кислоты;
этиловый эфир 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-7-карбоновой кислоты;
3-(2-метилсульфанилпиримидин-4-ил)-2-пиридин-2-илимидазо[1,2-а]пиридин;
3-[2-(4-метилпиперазин-1-ил)пиримидин-4-ил]-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин;
метиловый эфир 3-{[3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбонил]амино}пропионовой кислоты;
4-(2-пиридин-2-илимидазо[1,2-а]пиридин-3-ил)пиримидин-2-иламин;
4-[2-(6-метилпиридин-2-ил)-7-трифторметилимидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламин;
амид 4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-карбоновой кислоты;
4-[6-метил-2-(6-метилпиридин-2-ил)-8-(2-морфолин-4-илэтиламино)имидазо[1,2-а]пиридин-3-ил] пиримидин-2-ол;
4-[6-метил-2-(6-метилпиридин-2-ил)-8-морфолин-4-илимидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламин;
4-[8-бензилокси-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ол;
4-[8-бензилокси-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламин;
4-[8-бром-6-метил-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ол;
(4-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламино}бутил)амид 5-диметиламинонафталин-1-сульфоновой кислоты;
6-амино-9-[2-карбокси-5-(4-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламино}бутилкарбамоил)фенил]ксантен-3-илиденаммоний;
6-бром-2-(6-метилпиридин-2-ил)-3-(2-метилсульфанилпиримидин-4-ил)имидазо[1,2-а]пиридин;
6-фтор-2-(6-метилпиридин-2-ил)-3-(2-метилсульфанилпиримидин-4-ил)имидазо[1,2-а]пиридин;
N,N-диметил-N'-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}этан-1,2-диамин;
N1-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}пропан-1,3-диамин;
N-(4-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламино}бутил)-(BODIPY FL) амид;
N-(4-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3ил]пиримидин-2-иламино}бутил)-(Texas Red-X) амид
или их фармацевтически приемлемые соли или их N-оксиды.
29. Соединение по п.1, выбранное из группы, включающей
(2-метоксиэтил)-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
трет-бутиловый эфир (3-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламино}пропил)карбаминовой кислоты;
(3-имидазол-1-илпропил)-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
(4-аминобензил)-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
трет-бутиловый эфир (5-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламино}пентил)карбаминовой кислоты;
[3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-ил]метанол;
[3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-7-ил]метанол;
[3-(2-аминопиримидин-4-ил)-6-метил-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-8-ил]-(2-пиридин-2-илэтил)амин;
[3-(4-метилпиперазин-1-ил)пропил]-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
[3-(4-метилпиперидин-1-ил)пропил]-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}-(2Н-пиразол-3-ил)амин;
{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}-(2-морфолин-4-илэтил) амин;
{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}-(2-пиридин-2-илэтил) амин;
{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}-(2-пиридин-3-илэтил) амин;
{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}-(2-пиридин-4-илэтил) амин;
{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}-(3-морфолин-4-илпропил)амин;
{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}-(3-пиперидин-1-илпропил)амин;
{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}[1,3,4]тиадиазол-2-иламин;
2-(6-метилпиридин-2-ил)-3-пиримидин-4-илимидазо[1,2-а]пиримидин-7-иламин;
3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбонитрил;
(2-метоксиэтил)амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбоновой кислоты;
амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбоновой кислоты;
циклопропиламид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбоновой кислоты;
этиламид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбоновой кислоты;
гидроксиамид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбоновой кислоты;
метоксиамид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбоновой кислоты;
(2-тиофен-2-илэтил)амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-7-карбоновой кислоты;
амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-7-карбоновой кислоты;
циклопропиламид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-7-карбоновой кислоты;
этиламид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-7-карбоновой кислоты;
метоксиамид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-7-карбоновой кислоты;
3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиримидин-7-иламин;
3-(2-азетидин-1-илпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин;
3-[2-(2-метилазиридин-1-ил)пиримидин-4-ил]-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин;
метиловый эфир 3-{[3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-7-карбонил]амино}пропионовой кислоты;
4-(2-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламино}этил)бензолсульфонамид;
4-[2-(6-хлорпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламин;
4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламин;
4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-карбонитрил;
4-[6-бром-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламин;
4-[6-хлор-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламин;
4-[6-фтор-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламин,
4-[6-метил-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламин;
4-[7-аминометил-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламин;
4-[7-метил-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламин;
4-[8-метил-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламин;
6-(2,7-дифтор-6-гидрокси-3-оксо-3Н-ксантен-9-ил)-N-(4-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а] пиридин-3-ил]пиримидин-2-иламино}бутил)изофталамовая кислота;
7-амино-4-метил-3-[(4-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламино}бутилкарбамоил)метил]-2-оксо-2Н-хроман-6-сульфоновая кислота;
циклобутил{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
циклопентил{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
циклопропил{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламин;
циклопропилметил{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
диметил{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
изопропил{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
метил{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}амин;
N-(2-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламино}этил)ацетамид;
N-(4-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламино}бутил)ацетамид;
N-[3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиримидин-7-ил]-2-(3-метоксифенил)ацетамид;
N-[3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиримидин-7-ил]-3,3-диметилбутирамид;
N-[3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиримидин-7-ил]-3-пиридин-3-илпропионамид;
N-[3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиримидин-7-ил]ацетамид;
N-[3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиримидин-7-ил]никотинамид;
N-[3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиримидин-7-ил]пропионамид;
N-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}ацетамид;
N-{4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил}бутан-1,4-диамин
или их фармацевтически приемлемые соли или N-оксиды.
30. Фармацевтическая композиция, содержащая по меньшей мере одно соединение по п.1 и фармацевтически приемлемый носитель.
31. Фармацевтическая композиция, содержащая по меньшей мере одно соединение по п.27 и фармацевтически приемлемый носитель.
32. Способ ингибирования сигнального пути TGFb у субъекта, который включает введение указанному субъекту эффективного количества по меньшей мере одного соединения по п.1.
33. Способ ингибирования сигнального пути TGFb у субъекта, который включает введение указанному субъекту эффективного количества по меньшей мере одного соединения по п.27.
34. Способ ингибирования рецептора TGFb типа I в клетке, который включает контактирование указанной клетки с эффективным количеством по меньшей мере одного соединения по п.1.
35. Способ ингибирования рецептора TGFb типа I в клетке, который включает контактирование указанной клетки с эффективным количеством по меньшей мере одного соединения по п.27.
36. Способ уменьшения накопления избытка внеклеточного матрикса, индуцируемого TGFb, у субъекта, который включает введение указанному субъекту эффективного количества по меньшей мере одного соединения по п.1.
37. Способ уменьшения накопления избытка внеклеточного матрикса, индуцируемого TGFb, у субъекта, который включает введение указанному субъекту эффективного количества по меньшей мере одного соединения по п.27.
38. Способ лечения или профилактики фиброзных состояний у субъекта, включающий введение указанному субъекту эффективного количества по меньшей мере одного соединения по п.1.
39. Способ лечения или профилактики фиброзных состояний у субъекта, включающий введение указанному субъекту эффективного количества по меньшей мере одного соединения по п.27.
40. Способ по пп.38 или 39, где фиброзное состояние выбирают из склеродермы, волчаночного нефрита, заболевания соединительных тканей, заживления ран, рубцов после хирургических операций, поражений спинного мозга, поражений ЦНС, острых поражений легких, идиопатического фиброза легких, хронических обструктивных заболеваний легких, респираторного дистресса-синдрома у взрослых, острого поражения легких, поражения легких, вызванного лекарствами, гломерулонефрита, диабетической нефропатии, нефропатии, вызванной гипертонией, фиброза печени или желчного пузыря, почечного фиброза, цирроза печени, первичного цирроза желчного пузыря, болезни ожирения печени, первичного склерозирующего холангита, рестеноза, фиброза сердца, образования бельма, фибросклероза, фиброзных раковых заболеваний, фиброидов, фибромы, фиброаденом, фибросарком, трансплантатной артериопатии, фиброза, вызванного облучением при лечении, фиброза, вызванного химиотерапией и келоидов.
41. Способ ингибирования метастазов опухолевых клеток у субъекта, включающий введение указанному субъекту эффективного количества, по меньшей мере, одного соединения по п.1.
42. Способ ингибирования метастазов опухолевых клеток у субъекта, включающий введение указанному субъекту эффективного количества по меньшей мере одного соединения по п.27.
43. Способ лечения заболеваний или нарушений, опосредствованных сверхэкспрессией TGFp, включающий введение указанному субъекту эффективного количества по меньшей мере одного соединения по п.1.
44. Способ лечения заболеваний или нарушений, опосредствованных сверхэкспрессией TGFb, включающий введение указанному субъекту эффективного количества по меньшей мере одного соединения по п.27.
45. Способ по пп.43 или 44, где указанные заболевания или нарушения выбирают из группы, состоящей из демиелинизации нейронов при рассеянном склерозе, болезни Алцгеймера, церебральной ангиопатии, плоскоклеточной карциномы, множественной миеломы, меланомы, глиомы, глиобластомы, лейкемии и карциномы легких, молочной железы, яичников, шейки матки, печени, желчных путей, желудочно-кишечного тракта, поджелудочной железы, простаты и головы и шеи
Текст
TGF (трансформирующий фактор роста ) является членом большого семейства димерных полипептидных факторов роста, которые включают активины, ингибины, костные морфогенетические белки(BMP), факторы роста и дифференциации (GDF) и ингибирующее вещество муллериана (mullerian)(MIS). TGF существует в трех изоформах (TGF1, TGF2 и TGF3) и присутствует в большинстве клеток, наряду со своими рецепторами. Каждая изоформа экспрессируется как тканеспецифическим, так и регулируемым в процессе развития образом. Каждая TGF изоформа синтезируется как белокпредшественник, который расщепляется внутриклеточно на С-концевой участок (латентноассоциированный белок (LAP и N-концевой участок, известный как зрелый или активный TGF. LAP обычно не ковалентно ассоциирован со зрелым TGF, прежде чем он секретируется из клетки. КомплексLAP-TGF не способен связываться с TGF рецепторами и не является биологически активным. TGF обычно высвобождается (и активируется) из комплекса за счет различных механизмов, включая взаимодействие с тромбоспондином-1 или плазмином. После активации TGF связывается с высокой аффинностью с рецептором типа II (TGFRII), конститутивно активной серин/треонинкиназой. Связанный с лигандом рецептор типа II фосфорилирует рецептор TGF типа I (Alk 5) в обогащенный глицин/серином домен, что позволяет рецептору типа I привлекать и фосфорилировать далее сигнальные молекулы, Smad2 или 3mad3. См., например, Huse, M.et al., Mol. Cell. 8: 671-682 (2001). Фосфорилированные Smad2 или Smad3 могут затем образовывать комплекс с Smad4, и этот гетеро-Smad комплекс целиком перемещается в ядра и регулирует транскрипцию различных TGF-быстрореагирующих генов. См., например, Massague, J. Ann. Rev. Biochem. Med. 67: 773 (1998). Активины также являются членами надсемейства TGF, которые отличаются от TGF тем, что они являются гомо- или гетеродимерами активина а или b. Активины подают сигналы таким же образом,как и TGF, то есть путем связывания с конститутивным серин-треонин рецептором киназы, рецептором активина типа II (ActRIIB), и активирования серин-треонинового рецептора типа I, Alk 4, чтобы фосфорилировать Smad2 или Smad3. Последующее образование гетеро-Smad комплекса с Smad4 также приводит к индуцируемому активином регулированию генной транскрипции. Действительно, TGF и родственные факторы, такие как активин, регулируют обширную совокупность клеточных процессов, например остановку клеточного цикла в эпителиальных и гематопоэтических клетках, контролируют мезенхимную клеточную пролиферацию и дифференциацию, увеличение численности воспалительных клеток, иммуносупрессию, заживление ран и продуцирование внеклеточного матрикса. См., например, Massague, J. Ami Rev. Cell. Biol. 6: 594-641 (1990); Roberts, A.B. and Sporn(1995). Гиперактивность сигнального пути TGF лежит в основе многих нарушений в организме человека (например, избыточное отложение внеклеточного матрикса, ненормально высокие уровни воспалительных реакций, фиброзные нарушения и прогрессирующие раковые заболевания). Аналогично, подача сигналов активином и сверхэкспрессия активина связаны с патологическими нарушениями, которые включают избыточное накопление внеклеточного матрикса и фиброзы (См., например, Matsuse, Т. et al,Am. J. Respir. Cell. Mol. Biol. 13: 17-24 (1995); Inoue, S. et al., Biochem. Biophys, Res. Comm. 205: 441-448(1998); Munz, B. et al., EMBO J. 18: 5205-5215 (1999 и воспалительные реакции (См., например, Rosendahl, A. et al., Am. J. Repir. Cell. Mol. Biol. 25: 60-68 (2001. Исследования показали, что TGF и активин могут действовать синергически для индуцирования внеклеточного матрикса (См., например, Sugiyama,М. et al., Gastroenterology 114: 550-558, (1998. Поэтому желательно создать модуляторы (например, антагонисты) для компонентов сигнального пути семейства TGF для профилактики/лечения нарушений,связанных с нарушениями этого сигнального пути. Сущность изобретения Соединения формулы (I) неожиданно оказались эффективными антагонистами рецепторов семейства TGF типа I, Alk5 и/или Alk4. Поэтому соединения формулы (I) можно использовать для профилактики и/или лечения заболеваний, таких как фиброз (например, почечный фиброз, фиброз легких и фиброз печени), прогрессирующих раковых заболеваний или других заболеваний, для которых желательно снижение сигнальной активности семейства TGF. В одном из аспектов настоящее изобретение представляет соединение формулы I: Каждый из X1, X2, Х 3 и Х 4 независимо представляет CRX или N; при условии, что только два из X1,X2, Х 3 и Х 4 могут представлять N одновременно. Каждый из Y1 и Y2 независимо представляет CRy или N; при условии, что по меньшей мере один из Y1 и Y2 должен представлять N. Каждый R1 независимо представляет алкил, алкенил, алкинил, алкокси, ацил, галоген, гидрокси, амино, нитро, циано, гуанидино,амидино, карбокси, сульфо, меркапто, алкилсульфанил, алкилсульфинил, алкилсульфонил, аминокарбонил, алкилкарбониламино, алкилсульфониламино, алкоксикарбонил, алкилкарбонилокси, мочевину,тиомочевину, сульфамоил, сульфамид, карбамоил, циклоалкил, циклоалкилокси, циклоалкилсульфанил,гетероциклоалкил, гетероциклоалкилокси, гетероциклоалкилсульфанил, арил, арилокси, арилсульфанил,ароил, гетероарил, гетероарилокси, гетероарилсульфанил или гетероароил. Каждый из R2 независимо представляет алкил, алкенил, алкинил, ацил, галоген, гидрокси, -NH2, -NH(алкил), -N(алкил)2,-NH(циклоалкил), -N(алкил)(циклоалкил), -NH(гетероциклоалкил), -NH(гетероарил), -NH-алкилгетероциклоалкил, -NH-алкилгетероарил, -NH(аралкил), циклоалкил, (циклоалкил)алкил, арил, аралкил, ароил, гетероциклоалкил, (гетероциклоалкил)алкил, гетероарил, гетероаралкил, гетероароил, нитро, циано,гуанидино, амидино, карбокси, сульфо, меркапто, алкокси, циклоалкилокси, (циклоалкил)алкокси, арилокси, арилалкокси, гетероциклоалкилокси, (гетероциклоалкил)алкокси, гетероарилокси, гетероарилалкокси, алкилсульфанил, циклоалкилсульфанил, (циклоалкил)алкилсульфанил, арилсульфанил, аралкилсульфанил, гетероциклоалкилсульфанил, (гетероциклоалкил)алкилсульфанил, гетероарилсульфанил,гетероарилалкилсульфанил, алкилсульфинил, алкилсульфонил, аминокарбонил, аминосульфонил, алкилкарбониламино, циклоалкилкарбониламино, (циклоалкил)алкилкарбониламино, арилкарбониламино,аралкилкарбониламино, (гетероциклоалкил)карбониламино, (гетероциклоалкил)алкилкарбониламино,гетероарилкарбониламино, гетероаралкилкарбониламино, алкоксикарбониламиноалкиламино, (гетероарил)арилкарбониламиноалкиламино,гетероаралкилкарбониламиноалкиламино,(гетероарил)арилсульфониламиноалкилкарбониламиноалкиламино, арилсульфониламиноалкиламино, алкоксикарбонил,алкилкарбонилокси, мочевину, тиомочевину, сульфамоил, сульфамид или карбамоил, m равен 0, 1, 2, 3 или 4; при условии, что если m2, две соседние R1 группы могут объединиться с образованием 4-8 членного необязательно замещенного циклического фрагмента, n равен 0, 1, 2 или 3; при условии, что если n2, две соседние R2 группы могут объединиться с образованием 4-8-членного необязательно замещенного циклического фрагмента. Каждый из RX и RY независимо представляет водород, алкил, алкенил,алкинил, алкокси, ацил, галоген, гидрокси, амино, нитро, циано, гуанидино, амидино, карбокси, сульфо,меркапто, алкилсульфанил, алкилсульфинил, алкилсульфонил, циклоалкилкарбонил, (циклоалкил)алкилкарбонил, ароил, аралкилкарбонил, гетероциклоалкилкарбонил, (гетероциклоалкил)ацил, гетероароил, (гетероарил)ацил, аминокарбонил, алкилкарбониламино, (амино)аминокарбонил, алкилсульфониламинокарбонил, алкилсульфониламино, циклоалкилкарбониламино, циклоалкилсульфониламино,(циклоалкил)алкилкарбониламино, (циклоалкил)алкилсульфониламино, арилкарбониламино, арилсульфониламино, аралкилкарбониламино, аралкилсульфониламино, (гетероциклоалкил)карбониламино, (гетероциклоалкил)сульфониламино, (гетероциклоалкил)алкилкарбониламино, (гетероциклоалкил)алкилсульфониламино, гетероарилкарбониламино, гетероарилсульфониламино, гетероаралкилкарбониламино,гетероаралкилсульфониламино, (гетероарил)арилкарбониламиноалкиламино, гетероаралкилкарбониламиноалкиламино, (гетероарил)арилсульфониламиноалкилкарбониламиноалкиламино, арилсульфониламиноалкиламино, алкоксикарбонил, алкилкарбонилокси, мочевину, тиомочевину, сульфамоил, сульфамид, карбамоил, циклоалкил, циклоалкилокси, циклоалкилсульфанил, (циклоалкил)алкил, (циклоалкил)алкокси, (циклоалкил)алкилсульфанил, гетероциклоалкил, гетероциклоалкилокси, гетероциклоалкилсульфанил, (гетероциклоалкил)алкил, (гетероциклоалкил)алкокси, (гетероциклоалкил)алкилсульфанил, арил, арилокси, арилсульфанил, аралкил, аралкилокси, аралкилсульфанил, арилалкенил, арилалкинил, гетероарил, гетероарилокси, гетероарилсульфанил, гетероаралкил, (гетероарил)алкокси или (гетероарил)алкилсульфанил. Как было указано выше, если m2, две соседние R1 группы могут объединяться с образованием 4-8 членного необязательно замещенного циклического фрагмента. То есть 2-пиридильное кольцо может конденсироваться с 4-8-членным циклическим фрагментом с образованием такого фрагмента, как 7 Н[1]пиридинил, 6,7-дигидро-5 Н-[1]пиридинил, 5,6,7,8-тетрагидрохинолинил, 5,7-дигидрофуро[3,4-b]пиридинил или 3,4-дигидро-1 Н-тиопирано[4,3-c]пиридинил. Конденсированный кольцевой фрагмент может быть необязательно замещен одним или более заместителями, такими как алкил (включая карбоксиалкил, гидроксиалкил и галогеноалкил, такой как трифторметил; см. определение "алкил" ниже), алкенил, алкинил, циклоалкил, гетероциклоалкил, алкокси, арил, гетероарил, арилокси, гетероарилокси,аралкилокси, гетероарилалкокси, ароил, гетероароил, амино, нитро, карбокси, алкоксикарбонил, алкил-2 010426 карбонилокси, аминокарбонил, алкилкарбониламино, циклоалкилкарбониламино, циклоалкилалкилкарбониламино, арилкарбониламино, аралкилкарбониламино, гетероциклоалкилкарбониламино, гетероциклоалкилалкилкарбониламино, гетероарилкарбониламино, гетероаралкилкарбониламино, циано, галоген,гидрокси, ацил, меркапто, алкилсульфанил, сульфокси, мочевина, тиомочевина, сульфамоил, сульфамид,оксо или карбамоил. Аналогично, если n2, две соседние R2 группы могут объединяться с образованием 4-8-членного необязательно замещенного циклического фрагмента, тем самым образуя кольцо, конденсированное с пиридильной или пиримидинильной группой. Некоторые примеры таких фрагментов представлены ниже: 4-8-членный циклический фрагмент, образованный двумя соседними R2 группами, может быть необязательно замещен заместителями, такими как алкил (включая карбоксиалкил, гидроксиалкил и галогеноалкил, такой как трифторметил; см. определение термина "алкил" ниже), алкенил, алкинил, циклоалкил, гетероциклоалкил, алкокси, арил, гетероарил, арилокси, гетероарилокси, аралкилокси, гетероарилалкокси, ароил, гетероароил, амино, нитро, карбокси, алкоксикарбонил, алкилкарбонилокси, аминокарбонил, алкилкарбониламино, циклоалкилкарбониламино, циклоалкилалкилкарбониламино, арилкарбониламино, аралкилкарбониламино, гетероциклоалкилкарбониламино, гетероциклоалкилалкилкарбониламино, гетероарилкарбониламино, гетероаралкилкарбониламино, циано, галоген, гидрокси, ацил, меркапто, алкилсульфанил, сульфокси, мочевина, тиомочевина, сульфамоил, сульфамид, оксо или карбамоил. В одном из вариантов каждый из X1, X2 и Х 3 представляет CRX. В одном из вариантов, каждый из Х 2, Х 3 и Х 4 независимо представляет -СН-, -С(СН 3)-, -С (ОН)-, -C(NH2)-, -С (CO-NH2)-, -C(CO-NHOH),-С(NH(незамещенный алкил-, -С(NH(арил-, -С(NH(аралкил-, -С(NH(гетероарил-, -С(NH(гетероарилалкил-, -С(NH-CO-(незамещенный алкил-, -С(NH-CO-(арил-, -С(NH-CO-(гетероарил-, -С(NHCO-(аралкил)-, -С(NH-CO-(гетероарилалкил-, -С(NH-SO2-(незамещенный алкил-, -С(NH-SO2-(арил-,-С(NH-SO2-(гетероарил-, -С(NH-SO2-(аралкил-, -С(NH-SO2-(гетероарилалкил-, -С(NH-SO2-NH (незамещенный алкил-, -С(NH-SO2-NH(арил-, -С(NH-SO2-NH(гетероарил-, -С(NH-SO2-NH(аралкил-,-C(NH-SO2-NH(гетероарилалкил-, -С(гидроксиалкил)- или -С(карбокси)- и X представляет -СН-. В одном из вариантов, каждый из X1 и Х 2 представляет -СН-; Х 4 представляет N и Х 3 представляет C(NH2)-, -С(NH(незамещенный алкил-, -С(NH(арил-, -С(NH(аралкил-, -С(NH(гетероарил-,-С(NH(гетероарилалкил-, -С(NH-CO-(незамещенный алкил-, -С(NH-CO-(арил-, -С(NH-CO(гетероарил-, -С(NH-CO-(аралкил-, -С(NH-CO-(гетероарилалкил-, -С(NH-SO2-(незамещенный алкил-,-С(NH-SO2-(арил-,-С(NH-SO2-(гетероарил-,-С(NH-SO2-(аралкил-,-С(NH-SO2(гетероарилалкил-, -С(NH-SO2-NH(незамещенный алкил-, -С(NH-SO2-NH(арил-, -С(NH-SO2NH(гетероарил-, -С(NH-SO2-NH(аралкил- или -С(NH-SO2-NH(гетероарилалкил-. В одном из вариантов оба Y1 и Y2 представляют N. В одном из вариантов m равен 0, 1 или 2 (например, m=1). В одном из вариантов, R1 замещен в 5 положении или 6-положении (т.е. R1 может быть монозамещен в любом из 5-положенияили 6 положения, или R1 может быть дизамещен в обоих 5- и 6-положениях). В одном из вариантов, R1 представляет C1-4 алкил, С 1-4 алкокси, С 1-4 алкилтио, галоген, амино, аминокарбонил или алкоксикарбонил. В одном из вариантов n равен 1 или 2 (например, n=1). В одном из вариантов, каждый R1 независимо представляет незамещенный алкил (например, 6 метил, 6-этил, 6-н-пропил или 6-изопропил), гидроксиалкил, галогеноалкил (например, 6-трифторметил),аминоалкил, арилоксиалкил, гетероаралкилоксиалкил, незамещенный алкенил (например, 6-винил), алкокси, ацил, галоген, гидрокси, карбокси, циано, гуанидино, амидино, амино (например, -NH2, моноалкиламино,диалкиламино,моногетероциклоалкиламино,моногетероариламино,моно(гетероциклилалкил)амино, моно(аралкил)амино или моно(гетероаралкил)амино), карбокси, меркапто,алкилсульфанил, алкилсульфинил, алкилсульфонил, аминокарбонил (например, -CONH2, -CONH(алкил) или -CO-N(алкил)2), алкилкарбониламино (например, -NH-CO-алкил или -N(алкил)-СО-алкил), алкоксикарбонил, алкилкарбонилокси, алкилсульфонил, сульфамоил (например, -SO2-NH2, -SO2-NH (алкил) или-SO2-N(алкил)2), циклоалкил (например, 6-циклопропил), гетероциклоалкил, (гетероциклоалкил)алкил,гетероарил или гетероаралкил. В одном из вариантов, каждый R2 независимо представляет незамещенный алкил, гидроксиалкил,галогеноалкил, аминоалкил (например, аминометил), арилоксиалкил, гетероаралкилоксиалкил, алкокси,ацил, галоген, гидрокси, карбокси, циано, гуанидино, амидино, -NH2, моноалкиламино, диалкиламино,моноциклоалкиламино, моногетероциклоалкиламино (например, -NH-пиперидинил или -NH-морфолино), моногетероариламино (например, -NH-тетразолил, -NH-пиразолил или -NH-имидазолил), моно(алкил), -N(алкил)-CO-NH (алкил), -NH-SO2-NH (алкил), -N(алкил)-SO2-NH(алкил), гетероциклоалкил или гетероарил (например, имидазолил, пиразолил, тетразолил или пиридил). Например, R2 замещен в 3 положении и представляет гуанидино, амидино, -NH2, моноалкиламино, диалкиламино, моноциклоалкиламино, моногетероциклоалкиламино, моногетероариламино, моногетероциклоалкил)алкил)амино,моно(гетероаралкил)амино, -NH-CO-NH(алкил), -N(алкил)-CO-NH(алкил), -NH-SO2-NH(алкил), -N(алкил)-SO2-NH(алкил), гетероциклоалкил или гетероарил. В одном из вариантов, каждый Rx независимо представляет водород, незамещенный алкил, гидроксиалкил (например, гидрокси-С 1-4 алкил, такой как гидроксиэтил), галогеноалкил (например, трифторметил), аминоалкил, арилоксиалкил, гетероаралкилоксиалкил, алкокси (например, С 1-4 алкокси, такой как метокси или С 1-4 галогеналкокси, такой как -OCF3), галоген (например, хлор или бром), гидрокси, карбокси, циано, гуанидино, амидино, амино (например, -NH2, -NH(алкил), -N(алкил)2, -NH(гетероциклоалкил),-NH(гетероарил), -NH(гетероциклоалкилалкил), -NH(аралкил) или -NH(гетероаралкил, карбокси, (гетероарил)ацил, аминокарбонил (например, -CO-NH2, -CO-NH-(СН 2)0-3-СООН, -CO-NH-(СН 2)0-3-ОН, -CONH-(СН 2)0-3-гетероарил (например, -CO-NH-(СН 2)0-3-тетразолил, -CO-NH-(СН 2)0-3-пиразолил или -CONH-(СН 2)0-3-имидазолил), -CO-NH-(СН 2)0-3-гетероциклоалкил (например, -CO-NH-(СН 2)0-3-пиперидинил или -CO-NH-(СН 2)0-3-морфолино) или -CO-NH-(СН 2)0-3-арил (например, -CO-NH-(СН 2)0-3-фенил), гетероарилкарбониламино, (гетероциклоалкил)алкокси, (гетероарил)алкокси, (гетероарил)алкилсульфанил,гетероциклоалкил (например, морфолино, пиразинил или пиперидинил), (гетероциклоалкил)алкил (например, морфолино-С 1-4 алкил, пиразинил-С 1-4 алкил или пиперидинил-С 1-4 алкил), гетероарил (например,имидазолил, пиразолил, тетразолил или пиридил) или гетероаралкил (например, имидазолил-С 1-4 алкил,пиразолил-С 1-4 алкил, тетразолил-С 1-4 алкил или пиридил-С 1-4 алкил). Некоторыми примерами группы-NH(алкил) служат -NH(галогеноалкил) (например, -NHCF3), -NH(карбоксиалкил) (например,-NH(CH2)1-3COOH) и -NH (гидроксиалкил) (например, -NH(СН 2)1-3-ОН). Некоторыми примерами группы -NH(гетероарил) служат -NH(тетразолил), -NH(пиразолил) и-NH(имидазолил). Некоторыми примерами группы -NH(гетероциклоалкилалкил) служат NH(пиперазинилалкил) (например, -NH(СН 2)1-3-пиперазин) и -NH(морфолиноалкил) (например, -NH(СН 2)1-3 морфолин). Некоторыми примерами группы -NH(гетероаралкил) служат -NH(тетразолилалкил) (например, -NH(СН 2)1-3-тетразол), -NH(пиразолилалкил) (например, -NH(СН 2)0-3-пиразол) и -NH(имидазолилалкил) (например, -NH (СН 2)0-3-имидазол). В одном из вариантов, RY представляет водород, незамещенный алкил, гидроксиалкил, галогеноалкил (например, трифторметил), аминоалкил, арилоксиалкил, гетероаралкилоксиалкил, алкокси, галоген,гидрокси, карбокси, циано, гуанидино, амидино, амино (например, -NH2, -NH(алкил), -N(алкил)2,-NH(циклоалкил), -NH(гетероциклоалкил), -NH(гетероарил), -NH(гетероциклоалкилалкил), -NH(аралкил) или -NH(гетероаралкил, карбокси, (гетероарил)ацил, аминокарбонил, гетероарилкарбониламино, (гетероциклоалкил)алкокси, (гетероарил)алкокси, (гетероарил)алкилсульфанил, гетероциклоалкил, (гетероциклоалкил)алкил, гетероарил или гетероаралкил. В одном из вариантов Х 1 представляет N. Например, X1 представляет N и каждый из Х 2, Х 3 и Х 4 независимо представляет CRX. В одном из вариантов Х 2 представляет N. Например, Х 2 представляет N и каждый из X1 X3, и Х 4 независимо представляет CRX. В одном из вариантов Х 3 представляет N. Например, Х 3 представляет N и каждый из X1, Х 2 и Х 4 независимо представляет CRX. В одном из вариантов Х 4 представляет N. Например, Х 4 представляет N и каждый из X1, X2 и Х 3 независимо представляет CRX. Некоторыми примерами соединений формулы (I) являются:N-оксидные производные или фармацевтически приемлемые соли каждого из соединений формулы(I) также включены в объем настоящего изобретения. Например, атом азота кольца центрального имидазольного кольца или азотсодержащего гетероциклического заместителя может образовывать оксид в присутствии подходящего окисляющего агента, такого как м-хлорпербензойная кислота или Н 2 О 2. Соединение формулы (I), которое является кислым по своей природе (например, содержащее карбоксильную или фенольную гидроксильную группу), может образовывать фармацевтически приемлемую соль, такую как соль натрия, калия, кальция или золота. В объем настоящего изобретения включены также соли, образованные с фармацевтически приемлемыми аминами, такими как аммиак, алкиламины, гидроксиалкиламины и N-метилглюкамин. Соединение формулы (I) можно обработать кислотой, получая соли присоединения. Примеры таких кислот включают хлористо-водородную кислоту, бромисто-водородную кислоту, йодисто-водородную кислоту, серную кислоту, метансульфоновую кислоту, фосфорную кислоту, п-бромфенилсульфоновую кислоту, карбоновую кислоту, янтарную кислоту, лимонную кислоту, бензойную кислоту, щавелевую кислоту, малоновую кислоту, салициловую кислоту, яблочную кислоту, фумаровую кислоту, аскорбиновую кислоту, малеиновую кислоту, уксусную кислоту и другие минеральные и органические кислоты, хорошо известные специалистам в данной области. Соли присоединения кислот можно получить, обрабатывая соединения формулы (I) в форме свободных оснований достаточным количеством кислоты (например, хлористо-водородной кислоты) до получения солей присоединения кислот (например, гидрохлоридной соли). Соль присоединения кислоты можно снова пре-8 010426 вратить в ее свободную форму, обрабатывая соль соответствующим образом разбавленным водным щелочным раствором (например, гидроксидом натрия, бикарбонатом натрия, карбонатом калия или аммиаком). Соединения формулы (I) могут быть также, например, в форме ахиральных соединений, рацемических смесей, оптически активных соединений, чистых диастереоизомеров или смеси диастереоизомеров. Соединения формулы (I) демонстрируют неожиданно высокую аффинность к рецепторам TGF семейства типа I, Alk 5 и/или Alk 4, например, с величиной ИК 50 менее чем 10 мкМ в условиях, раскрытых в примерах 7 и 8, ниже. Некоторые соединения формулы (I) демонстрируют величину ИК 50 менее чем 0,1 мкМ. Соединения формулы (I) можно также модифицировать, добавляя соответствующие функциональные группы для усиления селективных биологических характеристик. Некоторые модификации известны в данной области и включают такие, которые повышают биологическое проникновение в рассматриваемую биологическую систему (например, кровь, лимфатическую систему, центральную нервную систему), повышают доступность при пероральном введении, повышают растворимость, чтобы обеспечить возможность введения путем инъекций, изменяют метаболизм и/или изменяют скорость выведения. Примеры таких модификаций включают, но ими не ограничиваются, этерификацию полиэтиленгликолями, получение производных, используя в качестве заместителей пиволаты или жирные кислоты, превращение в карбаматы, гидроксилирование ароматических колец и замещение гетероатомами в ароматических кольцах. Настоящее изобретение характеризуется также фармацевтической композицией, содержащей соединение формулы (I) (или комбинацию двух или более соединений формулы (I и фармацевтически приемлемый носитель. В объем настоящего изобретения включены также лекарственные композиции,включающие любые из соединений формулы (I), отдельно или в комбинации, вместе с подходящим эксципиентом. Настоящее изобретение характеризуется также способом ингибирования рецепторов семействаTGF типа I, Alk 5 и/или Alk 4 (например, с величиной ИК 50 менее чем 10 пМ; предпочтительно менее чем 1 мкМ; более предпочтительно менее чем 0,1 мкМ) в клетке, включающим стадию контактирования клетки с эффективным количеством одного или более из соединений формулы (I). B объем настоящего изобретения включен также способ ингибирования сигнального пути TGF и/или активина в клетке или в организме субъекта (например, млекопитающего, такого как человек), включающий стадию контактирования клетки с эффективным количеством одного или более из соединений формулы (I) или стадию введения субъекту эффективного количества одного или более из соединений формулы (I). В объем настоящего изобретения входит также способ лечения субъекта или профилактики субъекта, у которого наблюдается состояние, характеризующееся повышенным уровнем активности TGF и/или активина или возникшее из-за повышенного уровня активности TGF и/или активина (например,из-за сверхэкспрессии TGF). Способ включает стадию введения субъекту эффективного количества одного или более из соединений формулы (I). Состояния включают накопление избытка внеклеточного матрикса; фиброзные состояния (например, склеродерму, волчаночный нефрит, заболевания соединительных тканей, заживление ран, рубцы после хирургических операций, поражения спинного мозга, поражения ЦНС, острые поражения легких,идиопатический фиброз легких, хронические обструктивные заболевания легких, респираторный дистресс-синдром у взрослых, острые поражения легких, поражения легких, вызванные лекарствами, гломерулонефрит, диабетическую нефропатию, нефропатию, вызванную гипертонией, фиброз печени или желчного пузыря, цирроз печени, первичный цирроз желчного пузыря, болезни ожирения печени, первичный склерозирующий холангит, рестеноз, фиброз сердца, образование бельма, фибросклероз, фиброзные раковые заболевания, фиброиды, фиброму, фиброаденомы, фибросаркомы, трансплантантную артериопатию и келоиды); демиелинизацию нейронов при рассеянном склерозе, болезнь Алцгеймера,церебральную ангиопатию и индуцированные TGF метастазы опухолевых клеток и карциномы (например, плоскоклеточная карцинома, множественная миелома, меланома, глиома, глиобластома, лейкемия и карциномы легких, молочной железы, яичников, шейки матки, печени, желчных путей, желудочнокишечного тракта, поджелудочной железы, простаты и головы и шеи. В том смысле, как использовано в данном описании, термин "алкильная" группа относится к насыщенной алифатической углеводородной группе, содержащей 1-8 (например, 1-6 или 1-4) атомов углерода. Алкильная группа может быть неразветвленной или разветвленной. Примеры алкильных групп включают, но ими не ограничиваются, метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил, третбутил, н-пентил, н-гептил и 2-этилгексил. Алкильная группа может быть необязательно замещена одним или более заместителями, такими как алкокси, циклоалкилокси, гетероциклоалкилокси, арилокси, гетероарилокси, аралкилокси, гетероарилалкокси, амино, нитро, карбокси, циано, галоген, гидрокси, сульфо,меркапто, алкилсульфанил, алкилсульфинил, алкилсульфонил, аминокарбонил, алкилкарбониламино,циклоалкилкарбониламино, циклоалкилалкилкарбониламино, арилкарбониламино, аралкилкарбониламино, гетероциклоалкилкарбониламино, гетероциклоалкилалкилкарбониламино, гетероарилкарбониламино, гетероаралкилкарбониламино, мочевина, тиомочевина, сульфамоил, сульфамид, алкоксикарбонил,-9 010426 или алкилкарбонилокси. В том смысле, как использовано в данном описании, термин "алкенильная" группа относится к алифатической углеводородной группе, которая содержит 2-8 (например, 2-6 или 2-4) атомов углерода и по меньшей мере одну двойную связь. Подобно алкильной группе, алкенильная группа может быть неразветвленной или разветвленной. Примеры алкенильных групп включают, но ими не ограничиваются,аллил, изопропенил, 2-бутенил и 2-гексенил. Алкенильная группа может быть необязательно замещена одним или более заместителями, такими как алкокси, циклоалкилокси, гетероциклоалкилокси, арилокси,гетероарилокси, аралкилокси, гетероарилалкокси, амино, нитро, карбокси, циано, галоген, гидрокси,сульфо, меркапто, алкилсульфанил, алкилсульфинил, алкилсульфонил, аминокарбонил, алкилкарбониламино, циклоалкилкарбониламино, циклоалкилалкилкарбониламино, арилкарбониламино, аралкилкарбониламино, гетероциклоалкилкарбониламино, гетероциклоалкилалкилкарбониламино, гетероарилкарбониламино, гетероаралкилкарбониламино, мочевина, тиомочевина, сульфамоил, сульфамид, алкоксикарбонил или алкилкарбонилокси. В том смысле, как использовано в данном описании, термин "алкинильная" группа относится к алифатической углеводородной группе, которая содержит 2-8 (например, 2-6 или 2-4) атомов углерода и содержит по меньшей мере одну тройную связь. Алкинильная группа может быть неразветвленной или разветвленной. Примеры алкинильных групп включают, но ими не ограничиваются, пропаргил и бутинил. Алкинильная группа может быть необязательно замещена одним или более заместителями, такими как алкокси, циклоалкилокси, гетероциклоалкилокси, арилокси, гетероарилокси, аралкилокси, гетероарилалкокси, амино, нитро, карбокси, циано, галоген, гидрокси, сульфо, меркапто, алкилсульфанил, алкилсульфинил, алкилсульфонил, аминокарбонил, алкилкарбониламино, циклоалкилкарбониламино, циклоалкилалкилкарбониламино, арилкарбониламино, аралкилкарбониламино, гетероциклоалкилкарбониламино, гетероциклоалкилалкилкарбониламино, гетероарилкарбониламино, гетероаралкилкарбониламино, мочевина, тиомочевина, сульфамоил, сульфамид, алкоксикарбонил или алкилкарбонилокси. В том смысле, как использовано в данном описании, термин "аминогруппа относится к -NRXRY, где каждый из RX и RY независимо представляет водород, гидроксил, алкил, алкокси, циклоалкил, (циклоалкил)алкил, арил, аралкил, гетероциклоалкил, (гетероциклоалкил)алкил, гетероарил, или гетероаралкил. Если термин "амино" относится не к концевой группе (например, алкилкарбониламино), он представлен как -NRX-. RX имеет указанные выше значения. В том смысле, как использовано в данном описании, термин "арильная" группа относится к фенильной, нафтильной или бензоконденсированной группе, содержащей от 2 до 3 колец. Например, бензоконденсированные группы включают фенил, конденсированный с одним или двумя С 4-8 карбоциклическими фрагментами, например, такими как 1,2,3,4-тетрагидронафтил, инданил или флуоренил. Арил может быть необязательно замещен одним или более заместителями, такими как алкил (включая карбоксиалкил, гидроксиалкил и галогеноалкил, такой как трифторметил), алкенил, алкинил, циклоалкил, (циклоалкил)алкил, гетероциклоалкил, (гетероциклоалкил)алкил, арил, гетероарил, алкокси, циклоалкилокси, гетероциклоалкилокси, арилокси, гетероарилокси, аралкилокси, гетероаралкилокси, ароил,гетероароил, амино, нитро, карбокси, алкоксикарбонил, алкилкарбонилокси, аминокарбонил, алкилкарбониламино, циклоалкилкарбониламино, (циклоалкил)алкилкарбониламино, арилкарбониламино, аралкилкарбониламино, (гетероциклоалкил)карбониламино, (гетероциклоалкил)алкилкарбониламино, гетероарилкарбониламино, гетероаралкилкарбониламино, циано, галоген, гидрокси, ацил, меркапто, алкилсульфанил, сульфокси, мочевина, тиомочевина, сульфамоил, сульфамид, оксо или карбамоил. В том смысле, как использовано в данном описании, термин "аралкильная" группа относится к алкильной группе (например, С 1-4 алкильная группа), которая замещена арильной группой. Как "алкил", так и "арил" имеют указанные выше значения. Примером аралкильных групп является бензил. В том смысле, как использовано в данном описании, термин "циклоалкильная" группа относится к алифатическому карбоциклическому кольцу, состоящему из 3-10 (например, 4-8) атомов углерода. Примеры циклоалкильных групп включают циклопропил, циклопентил, циклогексил, циклогептил, адамантил, норборнил, кубил, октагидроинденил, декагидронафтил, бицикло[3.2.1]октил, бицикло[2.2.2]октил,бицикло[3.3.1]нонил и бицикло[3.2.3]нонил. Термин "циклоалкенильная группа, в том смысле, как использовано в данном описании, относится к неароматическому карбоциклическому кольцу, состоящему из 3-10 (например, 4-8) атомов углерода и содержащему одну или более двойных связей. Примеры циклоалкенильных групп включают циклопентенил, 1,4-циклогексадиенил, циклогептенил, циклооктенил, гексагидроинденил, октагидронафтил, бицикло[2.2.2]октенил и бицикло[3.3.1]ноненил. Циклоалкильная или циклоалкенильная группы могут быть необязательно замещены одним или более заместителями, такими как алкил (включая карбоксиалкил, гидроксиалкил и галогеноалкил, такой как трифторметил), алкенил, алкинил, циклоалкил, (циклоалкил)алкил, гетероциклоалкил, (гетероциклоалкил)алкил, арил, гетероарил, алкокси, циклоалкилокси, гетероциклоалкилокси, арилокси, гетероарилокси, аралкилокси, гетероаралкилокси, ароил, гетероароил,амино, нитро, карбокси, алкоксикарбонил, алкилкарбонилокси, аминокарбонил, алкилкарбониламино,циклоалкилкарбониламино, (циклоалкил)алкилкарбониламино, арилкарбониламино, аралкилкарбониламино, гетероциклоалкилкарбониламино, (гетероциклоалкил)алкилкарбониламино, гетероарилкарбони- 10010426 ламино, гетероаралкилкарбониламино, циано, галоген, гидрокси, ацил, меркапто, алкилсульфанил, сульфокси, мочевина, тиомочевина, сульфамоил, сульфамид, оксо или карбамоил. В том смысле, как использовано в данном описании, термин "гетероциклоалкильная" группа относится к 3-10-членной (например, 4-8-членной) насыщенной кольцевой структуре, в которой один или более атомов кольца являются гетероатомом, например N, О или S. Примеры гетероциклоалкильных групп включают пиперидинил, пиперазинил, тетрагидропиранил, тетрагидрофурил, диоксоланил, оксазолидинил, изооксазолидинил, морфолинил, октагидробензофурил, октагидрохроманил, октагидротиохроменил, октагидроиндолил, октагидропиридинил, декагидрохинолинил, октагидробензо[b]тиофенил,2-оксабицикло[2.2.2]октил, 1-азабицикло[2.2.2]октил, 3-азабицикло[3.2.1]октил и 2,6-диоксатрицикло[3.3.1.03,7]нонил. Термин "гетероциклоалкенильная" группа, в том смысле, как использовано в данном описании, относится к 3-10-членной (например, 4-8-членной) неароматической кольцевой структуре,содержащей одну или более двойных связей, и в которой один или более атомов кольца представляют гетероатом, например N, О или S. Гетероциклоалкильная или гетероциклоалкенильная группа необязательно может быть замещена одним или более заместителями, такими как алкил (включая карбоксиалкил, гидроксиалкил и галогеноалкил, такой как трифторметил), алкенил, алкинил, циклоалкил, (циклоалкил)алкил, гетероциклоалкил, (гетероциклоалкил)алкил, арил, гетероарил, алкокси, циклоалкилокси, гетероциклоалкилокси, арилокси, гетероарилокси, аралкилокси, гетероаралкилокси, ароил, гетероароил,амино, нитро, карбокси, алкоксикарбонил, алкилкарбонилокси, аминокарбонил, алкилкарбониламино,циклоалкилкарбониламино, (циклоалкил)алкилкарбониламино, арилкарбониламино, аралкилкарбониламино, гетероциклоалкилкарбониламино, (гетероциклоалкил)алкилкарбониламино, гетероарилкарбониламино, гетероаралкилкарбониламино, циано, галоген, гидрокси, ацил, меркапто, алкилсульфанил, сульфокси, мочевина, тиомочевина, сульфамоил, сульфамид, оксо или карбамоил. Термин "гетероарильная" группа, в том смысле, как использовано в данном описании, относится к моноциклической, бициклической или трициклической кольцевой структуре, содержащей 5-15 атомов кольца, где один или более атомов кольца являются гетероатомом, например N, О, S или В, и где одно или более колец бициклической или трициклической кольцевой структуры являются ароматическим. Некоторыми примерами гетероарильных групп служат пиридил, фурил, пирролил, тиенил, тиазолил,оксазолил, имидазолил, индолил, тетразолил, бензофурил, бензтиазолил, ксантен, тиоксантен, фенотиазин, дигидроиндол и бензо[1,3]диоксол. Гетероарил может быть необязательно замещен одним или более заместителями, такими как алкил (включая карбоксиалкил, гидроксиалкил и галогеноалкил, такой как трифторметил), алкенил, алкинил, циклоалкил, (циклоалкил)алкил, гетероциклоалкил, (гетероциклоалкил)алкил, арил, гетероарил, алкокси, циклоалкилокси, гетероциклоалкилокси, арилокси, гетероарилокси, аралкилокси, гетероаралкилокси, ароил, гетероароил, амино, нитро, карбокси, алкоксикарбонил, алкилкарбонилокси, аминокарбонил, алкилкарбониламино, циклоалкилкарбониламино, (циклоалкил)алкилкарбониламино, арилкарбониламино, аралкилкарбониламино, гетероциклоалкилкарбониламино, (гетероциклоалкил)алкилкарбониламино, гетероарилкарбониламино, гетероаралкилкарбониламино, циано,галоген, гидрокси, ацил, меркапто, алкилсульфанил, сульфокси, мочевина, тиомочевина, сульфамоил,сульфамид, оксо или карбамоил. Термин "гетероаралкильная группа", в том смысле, как использовано в данном описании, относится к алкильной группе (например, С 1-4 алкильной группе), которая замещена гетероарильной группой. Оба термина "алкил" и "гетероарил" имеют указанные выше значения. В том смысле, как использовано в данном описании, термин "циклический фрагмент" включает циклоалкил, гетероциклоалкил, циклоалкенил, гетероциклоалкенил, арил или гетероарил, каждый из которых имеет указанные выше значения. В том смысле, как использовано в данном описании, термин "ацильная" группа относится к формильной группе или к группе алкил-С(=О)-, где "алкил" имеет указанные выше значения. Примерами ацильных групп служат ацетил и пивалоил. В том смысле, как использовано в данном описании, термин "карбамоильная" группа относится к группе, структура которой представлена -O-CO-NRXRY или -NRX-CO-O-RZ, где RX и RY имеют указанные выше значения и RZ представляет алкил, циклоалкил, (циклоалкил)алкил, арил, аралкил, гетероциклоалкил, (гетероциклоалкил)алкил, гетероарил или гетероаралкил. В том смысле, как использовано в данном описании, термины "карбоксигруппа" и "сульфогруппа",они относятся к группам -СООН и -SO3H соответственно. В том смысле, как использовано в данном описании, термин "алкоксигруппа" относится к алкил-Oгруппе, где "алкил" имеет указанные выше значения. В том смысле, как использовано в данном описании, термин "сульфоксигруппа" относится к -O-SORX или -SO-O-RX группам, где RX имеет указанные выше значения. В тем смысле, как использовано в данном описании, термин "галоген" или "гало" относится к фтору, хлору, брому или йоду. В том смысле, как использовано в данном описании, термин "сульфамоильная" группа относится к группе -S(O)2-NRXRY или -NRX-S(О)2-RZ, где RX, RY и RZ имеют указанные выше значения. В том смысле, как использовано в данном описании, термин "сульфамидная" группа относится к группе -NRX-S(О)2-NRYRZ, где RX, RY и RZ имеют указанные выше значения.- 11010426 В том смысле, как использовано в данном описании, термин "мочевина" относится к группе -NRXCO-NRYRZ и термин "тиомочевина" относится к группе -NRX-CS-NRYRZ, где RX, RY и RZ имеют указанные выше значения. В том смысле, как использовано в данном описании, термин эффективное количество определен как количество, которое необходимо для обеспечения терапевтического эффекта для подлежащего лечению пациента, и его обычно определяют исходя из возраста, площади поверхности тела, массы и состояния пациента. Взаимоотношение доз для животных и людей (в расчете на миллиграмм на квадратный метр поверхности тела) раскрыто у Freireich et al, Cancer Chemother. Rep., 50: 219 (1966). Площадь поверхности тела можно приблизительно определить, исходя из роста и массы пациента. См., например,Scientific Tables, Geigy Pharmaceuticals, Ardsley, New York, 537 (1970). В том смысле, как использовано в данном описании, термин "пациент" относится к млекопитающим, включая человека. Антагонистом является молекула, которая связывается с рецептором без активации рецептора. Он конкурирует с эндогенным лигандом(лигандами) или субстратом(субстратами) за сайт(сайты) связывания у рецептора и тем самым ингибирует способность рецептора преобразовывать внутриклеточный сигнал в реакцию на связывание с эндогенным лигандом. Так как соединения формулы (I) являются антагонистами TGF рецептора типа I (Alk5) и/или рецептора активина типа I (Alk4), эти соединения можно использовать для ингибирования результатов преобразования сигналов TGF и/или активина, таких как продуцирование внеклеточного матрикса (например, коллагена и фибронектина), дифференциацию клеток стромы в миофибробласты и стимуляцию миграции воспалительных клеток. Таким образом, соединения формулы (I) ингибируют патологические воспалительные и фиброзные реакции и обладают терапевтической применимостью для лечения и/или профилактики нарушений или заболеваний, при которых желательно снижение активности TGF и/или активина (например, при различного типа фиброзах или при прогрессирующих раковых заболеваниях). Если нет других указаний, все использованные в данном описании технические и научные термины имеют те же значения, которые обычно подразумевают специалисты в данной области, к которой и относится рассматриваемое изобретение. Все указанные публикации, заявки, патенты и другие ссылки включены в данное описание посредством ссылки во всей их полноте. Кроме того, материалы, способы и примеры являются лишь иллюстративными, и их не следует рассматривать как ограничивающие. Другие характеристики и преимущества рассматриваемого изобретения будут очевидны из следующего подробного описания и формулы изобретения. Подробное описание изобретения В целом, отличительной особенностью настоящего изобретения являются соединения формулы (I),которые демонстрируют неожиданно высокую аффинность к рецепторам семейства TGF типа I, Alk 5 и/или Alk 4. Получение соединений формулы (I). Соединения формулы (I) можно получить рядом известных способов из коммерчески доступных или известных исходных веществ. В одном из способов соединения формулы (I) получают в соответствии со схемой 1, представленной ниже. Более конкретно, исходное соединение формулы (II) (где R2 было выбрано выше) можно метилировать в присутствии метилиодида в щелочных условиях (например, водн.NaOH), получая соединение формулы (III), которое можно депротонировать в соответствующих условиях (например, используя гексаметилдисилазан натрия (NaHMDS) в ТГФ). Реакция депротонирования соединения формулы (III) с использованием соединения формулы (IV) (где R1 был выбран выше) приводит к образованию аддукта соединения формулы (V). Затем аддукт бромируют и затем циклизуют, используя аминозамещенный гетероцикл формулы (VI), получая соединение формулы (I). Схема 1 Ссылаясь на схему 2, ниже, то тиоэфирзамещенное соединение формулы (I) (см. конечный продукт на схеме 1) можно далее модифицировать, получая другое соединение формулы (I). Следует обратить внимание, что каждый из RA и RB представляет водород, алкил, циклоалкил, (циклоалкил)алкил, арил,аралкил, гетероциклоалкил, (гетероциклоалкил)алкил, гетероарил или гетероаралкил. Альтернативно, соединения формулы (I) можно получить в соответствии со схемой 3, ниже. Более конкретно, соединение формулы (VII) можно циклизовать, используя аминозамещенный гетероцикл формулы (VI), получая соединение формулы (VIII), которое можно бромировать, получая соединение формулы (IX). Соединения формулы (IX) и формулы (X) можно подвергнуть реакции сочетания Сузуки,получая соединение формулы (I), которое можно далее модифицировать, получая другие соединения формулы (I). См. реакцию аминирования, представленную на последней стадии на схеме 3 (каждый изRA и RB имеет указанные выше значения). Для получения соединения формулы (X), см. WO 02/16359. Альтернативно, бромзамещенное соединение формулы (I) можно модифицировать, получая другие соединения формулы (I) в соответствии со схемой 4, ниже. Схема 4 Альтернативно, аминозамещенное соединение формулы (I) можно модифицировать, получая другие соединения формулы (I) в соответствии со схемой 5, ниже, где Rc представляет алкил, циклоалкил,(циклоалкил)алкил, арил, аралкил, гетероциклоалкил, (гетероциклоалкил)алкил, гетероарил или гетероаралкил. Схема 5 Следует отметить, что способы, проиллюстрированные выше на схемах, являются просто примерами. Специалисты в данной области могут легко модифицировать эти способы, чтобы получить соединения формулы (I), отличающиеся от соединений, представленных на этих схемах. Например, можно заменить моно(метилсульфанил)-замещенное соединение формулы (III) на схеме 1 ди(метилсульфанил)замещенным производным (например, 4-метил-2,6-бисметилсульфанилпиримидином, который можно получить, например, в соответствии с Aust. J. Chem. 34:172 9 (1981), Syn. Commun. 10:791 (1980), илиSynthesis 70-72 (1988, получая в итоге различные дизамещенные соединения формулы (I) (т.е. дизамещенные производные соединения формулы (I), как представлено на схемах 1 и 2). В одном из вариантов изобретения молекулярная масса соединения настоящего изобретения не превышает 1200. В другом варианте изобретения молекулярная масса не превышает 1000. Как должно быть очевидно специалисту в данной области, некоторые промежуточные соединения- 14010426 могут нуждаться в защите до осуществления раскрытых выше стадий синтеза. Для выбора подходящих защитных групп см., например, Т. W. Greene, Protective Groups in Organic Synthesis, John WileySons,Inc., New York (1981). Применение соединений формулы (I). Как было раскрыто выше, гиперактивность сигнальных путей семейства TGF может привести к избыточному отложению внеклеточного матрикса и к усиленным воспалительным реакциям, которые затем приводят к фиброзу тканей и органов (например, легких, почек и печени), что в итоге приводит к поражению органов. См., например, Border, W.A. and Ruoslahti E.J. Clin. Invest. 90: 1-7 (1992) и Border,W.A. и Noble, N.A. N. Engl. J. Med 331: 1286-1292 (1994). Исследования показали, что экспрессия TGF и/или мРНК активина и уровни TGF и/или активина увеличиваются у пациентов с различными фиброзными заболеваниями, например фиброзным заболеванием почек, фиброзом, вызванным алкоголем и аутоиммунным фиброзом печени, миелофиброзом, фиброзом легких, вызванным блеомицином, и идиопатическим фиброзом легких. Соединения формулы (I), которые являются антагонистами рецепторов TGF семейства типа I, Alk 5 и/или Alk 4 и ингибируют сигнальный путь TGF и/или активина, являются полезными для лечения и/или профилактики фиброзных нарушений или заболеваний, опосредствованных повышенными уровнями активности TGF и/или активина. Как использовано в данном описании, соединение ингибирует сигнальный путь TGF семейства, если оно связывается (например, с величиной ИК 50 менее чем 10 мкМ; предпочтительно менее чем 1 мкМ; более предпочтительно менее чем 0,1 мкМ) с рецептором этого пути(например, Alk 5 и/или Alk 4), тем самым конкурируя с эндогенным лигандом(лигандами) или субстратом(субстратами) за сайт(сайты) связывания на рецепторе, и уменьшает способность рецептора преобразовывать внутриклеточный сигнал в реакцию на связывание с эндогенным лигандом или субстратом. Вышеуказанные нарушения или заболевания включают любые состояния (а), характеризующиеся ненормально высокими уровнями TGF и/или активина; и/или (b) избыточным накоплением внеклеточного матрикса; и/или (с) увеличенным количеством и повышенной активностью синтеза миофибробластов. Эти нарушения и заболевания включают, но ими не ограничиваются, фиброзные состояния, такие как склеродерма, идиопатический фиброз легких, гломерулонефрит, диабетическая нефропатия, волчаночный нефрит, вызванная нефропатией гипертензия, фиброзные образования в глазу или на роговице, фиброз печени или желчных путей, острое поражение легких, фиброз легких, фиброз сердца после инфаркта,фибросклероз, фиброзные раковые заболевания, фиброиды, фиброма, фиброаденома и фибросаркома. Другие фиброзные нарушения, профилактическое лечение которых соединениями формулы (I) может иметь терапевтическую применимость, включают фиброз, вызванный облучением в процессе лечения,фиброз, вызванный химиотерапией, рубцы после хирургических операций, включая спайки после операций, ламинэктомию и коронарный рестеноз. Обнаружено также, что повышенная активность TGF проявляется у пациентов с прогрессирующими раковыми заболеваниями. Исследования показали, что на поздних стадиях раковых заболеваний как опухолевые клетки, так и стромальные клетки внутри опухоли обычно сверхэкспрессируют TGF. Это ведет к стимуляции ангиогенеза и подвижности клеток, подавлению иммунной системы и к усиленному взаимодействию опухолевых клеток с внеклеточным матриксом. См., например, Hojo, M. et al., Nature 397: 530-534 (1999). В результате опухолевые клетки становятся более инвазивными и образуют метастазы в отдаленных органах. См., например, Maehara, Y. et al., J. Clin. Oncol. 17: 607-614 (1999) и Picon,A. et al., Cancer Epidemiol. Biomarkers Prev. 7: 497-504 (1998). Таким образом, соединения формулы (I),которые являются антагонистами рецепторов TGF типа I и ингибируют сигнальный путь TGF, можно также использовать для лечения и/или профилактики различных поздних стадий раковых заболеваний,при которых наблюдается сверхэкспрессия TGF. Такие поздние стадии раковых заболеваний включают карциному легких, молочной железы, печени, желчных путей, желудочно-кишечного тракта, головы и шеи, поджелудочной железы, простаты, шейки матки, также как множественную миелому, меланомы,глиомы и глиобластомы. Важно подчеркнуть, что благодаря хроническому и в некоторых случаях локализованному характеру нарушений или заболеваний, опосредствованных сверхэкспрессией TGF и/или активина (например,фиброза или ракового заболевания), лечение малыми молекулами (таким лечением, которое раскрыто в настоящем изобретении) благоприятно для длительного лечения. Соединения формулы (I) полезны не только для лечения нарушений или заболеваний, опосредствованных высокими уровнями активностиTGF и/или активина, но эти соединения можно также использовать для профилактики тех же нарушений или заболеваний. Известно, что полиморфизм, приводящий к усиленному продуцированию TGF и/или активина, связывали с фиброзом и гипертензией. Действительно, высокие уровни TGF в сыворотке коррелируют с развитием фиброза у пациентов с раком молочной железы, подвергнутых радиационной терапии, у пациентов с хронической несовместимостью хозяина с трансплантатом (трансплантатпротив хозяина), идиопатической интерстициальной пневмонией, заболеванием, связанным с окклюзией вен у реципиентов трансплантатов, и брюшинным фиброзом у пациентов, подвергающихся непрерывному амбулаторному брюшинному диализу. Таким образом, уровни TGF и/или активина в сыворотке и- 15010426 мРНК TGF и/или активина в тканях могут быть измерены и использованы в качестве диагностических или прогнозирующих маркеров нарушений или заболеваний, опосредствованных сверхэкспрессиейTGF и/или активина, и полиморфизм в гене TGF, который определяет продуцирование TGFp и/или активина также можно использовать для прогнозирования предрасположенности к нарушениям или заболеваниям. См., например, Blobe, G.C. et al., N. Engl. J. Med. 342(18): 1350-1358 (2000); Matsuse, T. et al.,Am. J. Respir. Cell Mol. Biol. 13: 17-24 (1995); Inoue, S. et al., Biochem. Biophys. Res. Comm. 205: 441-448Pawlowski, Т.Е., et al., J. Clin. Invest. 100: 639-648 (1997); and Sugiyama, M. et al., Gastroenterology 114: 550-558 (1998). Введение соединений формулы (I). Как было указано выше, эффективным количеством является такое количество, которое необходимо для создания терапевтического эффекта у подлежащего лечению пациента. Для соединений формулы(I) эффективное количество может составлять интервал от около 1 мг/кг до около 150 мг/кг (например, от около 1 мг/кг до около 100 мг/кг). Эффективные дозы также будут изменяться, как известно специалистам в данной области, в зависимости от способа введения, используемого эксципиента и возможности совместного применения других терапевтических способов лечения, включая использование других терапевтических средств и/или радиационной терапии. Соединения формулы (I) можно вводить любым из подходящих способов введения фармацевтических соединений, включая, но ими не ограничиваясь, пилюли, таблетки, капсулы, аэрозоли, суппозитории, жидкие композиции для приема внутрь или для инъекций, или для использования в качестве глазных или ушных капель, пищевых добавок и препаратов для наружного использования. Фармацевтически приемлемые композиции включают водные растворы активных агентов в изотоническом солевом растворе, в 5% глюкозе или в других хорошо известных фармацевтически приемлемых эксципиентах. Способствующие растворению агенты, такие как циклодекстрины, или другие способствующие растворению агенты, хорошо известные в данной области, можно использовать в качестве фармацевтических эксципиентов для доставки терапевтических соединений. Что касается способов введения, то композиции можно вводить перорально, интраназально, чрезкожно, интрадермально, вагинально, интрааурально,интраокулярно, буккально, ректально, через слизистую или с помощью ингаляции, имплантации (например, используя хирургические методы) или внутривенно. Композиции можно вводить животным (например, млекопитающим, таким как человек, отличным от человека приматам, лошадям, собакам, коровам, свиньям, овцам, козам, кошкам, мышам, крысам, морским свинкам, кроликам, хомякам, песчанкам,хорькам, ящерицам, рептилиям или птицам). Необязательно, соединения формулы (I) можно вводить вместе с одним или более другими средствами, которые ингибируют сигнальный путь TGF или лечат соответствующие патологические нарушения (например, фиброз или прогрессирующие раковые заболевания) за счет различных других механизмов действия. Примеры таких средств включают ингибиторы ангиотензин-конвертирующего фермента,нестероидные, стероидные противовоспалительные средства и химиотерапевтические средства и радиационные методики, а также средства, которые антагонизируют связывание с лигандом или активациюTGF рецепторов, например антитела против TGF, против TGF рецепторов или антагонисты рецепторов TGF типа II. Далее настоящее изобретение будет раскрыто в следующих примерах, которые не ограничивают объем изобретения, заявленный в формуле изобретения. Пример 1. 2-(6-Метилпиридин-2-ил)-3-(2-метилсульфанилпиримидин-4-ил)имидазо[1,2-а]пиридин. Получение указанного в заголовке соединения раскрыто в частях (а)-(с) ниже.(а) 4-Метил-2-метилсульфанилпиримидин. Измельченный гидроксид натрия (272,7 ммоль) добавляют к суспензии гидрохлорида 2-меркапто-4 метилпиримидина (122,8 ммоль) в воде (175 мл) при комнатной температуре. Через 15 мин к темнокоричневому раствору по каплям добавляют йодометан (134,9 ммоль), при этом происходит образование осадка оранжевого цвета. Суспензию перемешивают при комнатной температуре в течение 3,5 ч и затем экстрагируют метиленхлоридом (360 мл). Объединенные органические фазы сушат (Na2SO4) и концентрируют в вакууме, получая 17,141 г масла темно-коричневого цвета, идентифицированного как 4-метил 2-метилсульфанилпиримидин. 1 Н ЯМР (CDCl3, 300 МГц): 2,41 (с, 3 Н), 2,52 (с, 3 Н), 6,77 (д, J=5,06 Гц, 1 Н), 8,32 (д, J=5,12 Гц, 1 Н).(b) 1-(6-Метилпиридин-2-ил)-2-(2-метилсульфанилпиримидин-4-ил)этанон. Смесь натрий бис(триметилсилил)амид/ТГФ (1,0 М, 7 4 ммоль) по каплям добавляют к раствору 4 метил-2-метилсульфанилпиримидина (36,89 ммоль) и этилового эфира 6-метилпиридин-2-карбоновой кислоты (36,80 ммоль) в безводном ТГФ (74 мл) в атмосфере азота на бане с водой комнатной температуры. После перемешивания в течение 3 ч реакционную смесь гасят насыщенным NH4Cl (110 мл) и органическую и водную фазы разделяют. Водную фазу экстрагируют этилацетатом (2100 мл). Объединенные органические фазы промывают водой (100 мл) и насыщенным раствором соли (100 мл), сушат(MgSO4) и концентрируют в вакууме, получая твердое вещество темно-оранжевого цвета, которое затем суспендируют в эфире при комнатной температуре в течение 1 ч, охлаждают при 0 С в течение ночи,фильтруют и сушат на воздухе, получая 4,85 г твердого вещества темно-коричневого цвета, идентифицированного как енол 1-(6-метилпиридин-2-ил)-2-(2-метилсульфанилпиримидин-4-ил)этанона. 1 Н ЯМР (CDCl3, 300 МГц): 2,60 (с, 6 Н), 6,73 (с, 1 Н), 6,76 (д, J=5,35 Гц, 1 Н), 7,17 (д, J=7,54 Гц, 1 Н),7,67 (дд, J=7,72, 7,72 Гц, 1 Н), 7,75 (д, J=7,72 Гц, 1 Н), 8,33 (д, J=5,37 Гц, 1 Н), 14,30 (с, 1 Н).MC(ESP+) 260,16 (М+1). Эфирный раствор концентрируют в вакууме, растворяют в этилацетате, обрабатывают обесцвечивающим углем, фильтруют и концентрируют в вакууме, получая твердое вещество, которое суспендируют в эфире при комнатной температуре в течение 1 ч, охлаждают при 0 С в течение ночи, фильтруют и сушат на воздухе, получая 0,63 г твердого вещества светло-коричневого цвета, идентифицированного как смесь 4:1 кетон/енольной формы 1-(6-метилпиридин-2-ил)-2-(2-метилсульфанилпиримидин-4 ил)этанона.(1,21 ммоль) добавляют к раствору 1-(6-метилпиридин-2-ил)-2-(2-метилсульфанилпиримидин-4 ил)этанона (0,89 ммоль) и каталитического количества ВНТ в ледяной уксусной кислоте (4 мл) при комнатной температуре до образования осадка. После 1 ч перемешивания реакционную смесь разбавляют до 50 мл эфиром, фильтруют, промывают эфиром, быстро сушат на воздухе и затем растворяют в этаноле (6 мл). Этанольный раствор по каплям добавляют к раствору 2-аминопиридина (0,965 ммоль) и диизопропилэтиламина (2,67 ммоль) в этаноле (1 мл) при 67 С. После перемешивания в течение 3,5 ч реакционную смесь концентрируют в вакууме и распределяют между эфиром (20 мл) и 1 М HCl (10 мл). Водную фазу промывают эфиром (210 мл), охлаждают на бане со льдом и добавляют твердый бикарбонат натрия до тех пор, пока раствор не становится нейтральным. Суспензию охлаждают при 0 С, фильтруют и сушат на воздухе, получая 0,18 г твердого вещества коричневого цвета, которое идентифицируют как указанное в заголовке соединение, 2-(6-метилпиридин-2-ил)-3-(2-метилсульфанилпиримидин-4 ил)имидазо[1,2-а]пиридин. 1 Н ЯМР (CDCl3, 300 МГц): 2,53 (с, 3 Н), 2,62 (с, 3 Н), 6,94 (дд, J=7,18, 6,73 Гц, 1 Н), 7,14 (д, J=5,42 Гц,1 Н),7,18 (д, J=4,49 Гц, 1 Н), 7,36 (дд, J=7,44, 8,35 Гц, 1 Н), 7,67 (д, J=4,43 Гц, 1 Н), 7,71 (дд, J=8,96 Гц, 2 Н),8,33 (д, J=5,38 Гц, 1 Н), 9,49 (д, J=7,09 Гц, 1 Н). MC(ESP+) 334,15 (М+1). Пример 2. 3-(2-Метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин. Серную кислоту (4,0 н, 0,04 ммоль), каталитическое количество дигидрата вольфрамата натрия и 30 мас.% перекиси водорода (1,01 ммоль) добавляют к суспензии 2-(6-метилпиридин-2-ил)-3-(2-метилсульфанилпиримидин-4-ил)имидазо[1,2-а]пиридина (0,31 ммоль; см. пример 1 для его получения) в метаноле(2 мл) при 55 С. Вся твердая часть растворяется в начале реакции, затем образуется осадок. После 3 ч перемешивания реакционную смесь разбавляют водой (2 мл) и нагревают при 55 С дополнительно в течение 0,5 ч. Затем реакционную смесь охлаждают до комнатной температуры, гасят насыщенным тиосульфатом натрия и концентрируют в вакууме. Твердую часть распределяют между этилацетатом (20 мл) и водой (10 мл). Органическую фазу промывают 2 М раствором карбоната натрия (7 мл) и насыщенным раствором соли (7 мл), сушат (Na2SO4) и концентрируют в вакууме, получая 0,10 г твердого вещества желтого цвета, идентифицированного как указанное в заголовке соединение, 3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин. 1 Н ЯМР (CDCl3, 400 МГц): 2,54 (с, 3 Н), 3,39 (с, 3 Н), 7,12 (дд, J=6,93, 7,76 Гц, 1 Н), 7,25 (д, J=7,61 Гц,1 Н), 7,50 (дд, J=7,32, 7,67 Гц, 1 Н), 7,77 (дд, J=7,73, 7,73 Гц, 1 Н), 7,83 (д, J=8,91 Гц, 1 Н), 7,89 (д, J=9,02 Гц,1 Н), 7,90 (д, J=5, 58 Гц, 1 Н), 8,66 (д, J=5,55 Гц, 1 Н), 9,74 (д, J=7,08 Гц, 1 Н).MC(ESP+) 366,09 (М+1). Пример 3. (4-Метоксибензил)-4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламин. Суспензию 4-метоксибензиламина (0,54 ммоль) и 3-(2-метансульфонилпиримидин-4-ил)-2-(6 метилпиридин-2-ил)имидазо[1,2-а]пиридина (0,27 ммоль; см. пример 2 для его получения) в ацетонитриле (1 мл) нагревают до кипения с обратным холодильником. После 20 ч кипячения с обратным холодильником добавляют 4-метоксибензиламин (0,27 ммоль). После кипячения с обратным холодильником в течение дополнительных 4,5 ч реакционной смеси дают остыть до комнатной температуры и концентрируют в вакууме, получая твердое вещество желтого цвета. Это твердое вещество растворяют в хлороформе (20 мл), промывают 5% лимонной кислотой (6 мл), 10% бикарбонатом натрия (6 мл) и насыщенным раствором соли (7 мл), сушат (Na2SO4) и концентрируют в вакууме, получая 0,11 г воскообразного вещества желтого цвета, которое идентифицируют как указанное в заголовке соединение, (4-метоксибензил)-4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламин. 1 Н ЯМР (CDCl3, 300 МГц): 2,57 (с, 3 Н), 3,82 (с, 3 Н), 4,65 (д, J=5,9 Гц, 2 Н), 6,65 (д, J=5,3 Гц, 1 Н), 6,66,71 (ушир.м, 1 Н), 6,89-6,94 (м, 2 Н), 7,18 (ушир.д, J=5,3 Гц, 1 Н), 7,25-7,28 (м, 2 Н), 7,31-7,36 (м, 2 Н), 7,89MC(ESP+) 423,20 (М+1); MC(ESP-) 421,21 (М-1). Пример 4. 4-[2-(6-Метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламин. Раствор (4-метоксибензил)-4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2 иламина (0, 2 627 ммоль; см. пример 3 для его получения) в смеси 1:1 диоксан/5 н. HCl (4 мл) нагревают при 100 С в течение 2 дней. Затем полученный раствор концентрируют в вакууме и очищают, используя ВЭЖХ с обращенной фазой (ацетонитрил/вода градиент с 0,1% TFA), получая 0,02 г твердого вещества желтого цвета, которое идентифицируют как TFA соль указанного в заголовке соединения, 4-[2-(6 метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламин. 1 Н ЯМР (d6-ДМСО, 400 МГц): 2,48 (с, 3 Н), 6,75 (д, J=5,9 Гц, 1 Н), 7,20 (ддд, J=1,1, 6,9, 6,9 Гц, 1 Н),7,39 (д, J=7,7 Гц, 1 Н), 7,62 (ддд, J=1,1, 6,9, 6,9 Гц, 1 Н), 7,77 (д, J=7,7 Гц, 1 Н), 7,83 (д, J=8,9 Гц, 1 Н), 7,89MC(ESP+) 303,11 (М+1). Пример 5. 3-(2-Аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиримидин-7 иламин. Раствор 3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиримидин 7-иламина (0,0718 ммоль; получен по способу примера 2) и 28 мас.% гидроксида аммония (4,34 ммоль) в диоксане (2 мл) нагревают при 100 С в запаянной ампуле. Через 19,5 ч реакционную смесь концентрируют в вакууме и очищают, используя ВЭЖХ с обращенной фазой (градиент ацетонитрил/вода с 0,1%TFA), получая 0,0200 г твердого вещества желтого цвета, идентифицированного как TFA соль указанного в заголовке соединения, 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиримидин-7-иламина. 1 Н ЯМР (ДМСО-d6, 400 МГц): 2,49 (с, 1,5 Н), 2,50 (с, 1,5 Н), 6,54 (д, J=5,37 Гц, 1 Н), 6,64 (д, J=7,71 Гц,1 Н), 7,15 (ушир.с, 2 Н), 7,40 (д, J=7,75 Гц, 1 Н), 7,55 (д, J=7,74 Гц, 1 Н), 7,84 (дд, J=7,79, 7,17 Гц, 1 Н), 8,17(0,121 ммоль; см. пример 2 для его получения) и 4-аминоморфолина (0,38 ммоль) в безводном ацетонитриле (1 мл) нагревают при 100 С в запаянной ампуле. Через 3 дня добавляют 4-аминоморфолин (0,76 ммоль) и реакционную смесь нагревают при 100 С в течение дополнительного дня. Затем полученный раствор концентрируют в вакууме и очищают, используя ВЭЖХ с обращенной фазой (градиент вода/ ацетонитрил с 0,1% TFA), получая 0,0258 г твердого вещества оранжевого цвета, идентифицированного как TFA соль указанного в заголовке соединения, 2-(6-метилпиридин-2-ил)-3-(2-морфолин-4-илпиримидин-4-ил)имидазо[1,2-а]пиридина. 1 Н ЯМР (ДМСО-d6, 400 МГц): 2,43 (с, 3 Н), 3,60-3,71 (м, 4 Н), 6,75 (д, J=6,75 Гц, 1 Н), 7,16 (дд, J=6,19,7,11 Гц, 1 Н), 7,37 (д, J=7,70 Гц, 1 Н), 7,57 (дд, J=7,57, 8,26 Гц, 1 Н), 7,70 (д, J=7,75 Гц, 1 Н), 7,77 (д, J=9,01 Гц, 1 Н), 7,86 (дд, J=7,74, 7,78 Гц, 1 Н), 8,35 (д, J=5,12 Гц, 1 Н), 9,13 (д, J=7,01 Гц, 1 Н).MC(ESP+) 373,19 (M+1). Пример 7. (4-Аминобензил)-4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин 2-иламин. В запаянной ампуле раствор 3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридина (0,147 ммоль; см. пример 2 для его получения) и 4-аминометилфениламина (0,443 ммоль) в CH3CN (2 мл) нагревают при кипении с обратным холодильником в течение ночи. Затем полученный раствор концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (545%MC(ESP+) 408,2 (М+1). Пример 8. 4-[2-(6-Метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил-(2-морфолин-4-илэтил)амин. В запаянной ампуле раствор 3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридина (0,147 ммоль; см. пример 2 для его получения и 2-морфолин-4-илэтиламина (0,443 ммоль) в CH3CN (2 мл) нагревают при кипении с обратным холодильником в течение ночи. Реакционную смесь концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (550% CH3CN/H2O с 0,1% TFA), получая 34 мг 4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил(2-морфолин-4-илэтил)амина в виде соли TFA. 1 Н ЯМР (d6-ДМСО, 400 МГц): 2,53 (с, 3 Н), 3,40 (м, 2 Н), 3,42 (м, 4 Н), 3,75 (м, 2 Н), 3,91 (т, 4 Н), 6,85(д, 1 Н, J=7,5 Гц), 7,91 (дд, 1 Н, J=7,6, 7,6 Гц), 8,37 (д, 1 Н, J=4,8 Гц). MC(ESP+) 416,3 (M+1). Пример 9. N,N-диметил-N'-4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2 илэтан-1,2-диамин. В запаянной ампуле раствор 3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридина (0,192 ммоль; см. пример 2 для его получения) и N,N-диметилэтилдиамина (0,574 ммоль) в CH3CN (2 мл) нагревают при кипении с обратным холодильником в течение ночи. Реакционную смесь концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (550% CH3CN/H2O с 0,1% TFA), получая 10 мг N,N-диметил-N'-4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил] пиримидин-2-илэтан-1,2-диамина в виде соли TFA. 1 Н ЯМР (d6-ДМСО, 400 МГц): 2,51 (с, 3 Н), 2,89 (д, 63, 3,6 Гц), 3,35 (ддд, 2 Н, J=6,0, 5,7, 5,7 Гц), 3,72MC(ESP+) 374,2 (М+1). Пример 10. N-(2-4-[2-(6-Метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламино этил)ацетамид. В запаянной ампуле раствор 3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридина (0,192 ммоль; см. пример 2 для го получения) и N-(2-аминоэтил)ацетамида (0,689 ммоль) в CH3CN (2 мл) нагревают при кипении с обратным холодильником в течение ночи. Реакционную смесь концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (550%MC(ESP+) 388,2 (M+1). Пример 11. N-(4-4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламино бутил)ацетамид. В запаянной ампуле суспензию 3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил) имидазо[1, 2-а]пиридина (0,171 ммоль; см. пример 2 для его получения), гидрохлората Nацетилпутрицина (0,546 ммоль) и CS2CO3 (0,683 ммоль) в CH3CN (2 мл) нагревают при кипении с обратным холодильником в течение ночи. Реакционную смесь концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (550% CH3CN/H2O с 0,1% TFA), получая 12 мг N-(4-4-[2-(6-метилпиридин-2-ил)имидаао[1,2-а]пиридин-3-ил]пиримидин-2-иламинобутил)ацетамида в виде соли TFA. 1 Н ЯМР (d6-ДМСО, 400 МГц): 1,51 (квинтет, 2 Н, J=6,7 Гц), 1,51 (квинтет, 2 Н, J=6,7 Гц), 1,82 (с, 3 Н),2,58 (с, 3 Н), 3,10 (кв., 2 Н, 6,5 Гц), 3,39 (ушир.м, 2 Н), 6,75 (ушир.с, 1 Н), 7,30 (ушир.м, 1 Н), 7,49 (д, 1 Н,J=7,1 Гц), 7,71 (дд, 1 Н, J=7,7 Гц), 7,81 (д, 1 Н, J=8 Гц), 7,86 (м, 1 Н), 7,90 (д, 1 Н, J=9 Гц), 7,99 (дд, 1 Н, J=8,0,8,0 Гц), 8,30 (д, 1 Н, J=5,6 Гц).MC(ESP+) 416,2 (М+1). Пример 12. 4-[2-(6-Метилпиридин-2-ил)имидазо[1,2-а]пиридин-3 ил]пиримидин-2-ил-(2-пиридин 3-илэтил)амин. В запаянной ампуле раствор 3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридина (0,171 ммоль; см. пример 2 для его получения) и пиридин-3-илэтиламина (0,565 ммоль) в CH3CN (2 мл) нагревают при кипении с обратным холодильником в течение ночи. Реакционную смесь концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (550% CH3CN/H2O с 0,1% TFA), получая 40 мг (4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил(2-пиридин-3-илэтил)амина в виде соли TFA. 1 Н ЯМР (d6-ДМСО, 400 МГц): 2,54 (с, 3 Н), 3,10 (т, 2 Н, J=6,5 Гц), 3,71 (м, 2 Н), 6,76 (ушир.с, 1 Н),7,23 (дд, 1 Н, J=6,8, 6,8 Гц), 7,44 (д, 1 Н, J=7,8 Гц), 7,65 (дд, 1 Н, J=7,8 Гц)3 7,72 (ушир.м, 1 Н), 7,78 (д, 1 Н,J=7,3 Гц)3 7,83 (ушир.м, 1 Н), 7,87 (д, 1 Н, 9,4 Гц), 7,95 (дд, 1 Н, J=8,3, 8,3 Гц), 8,31 (д, 1H,J=5,7 Гц), 8,71 (д,1 Н, J=6,2 Гц), 8,79 (ушир.с, 1 Н).MC(ESP+) 408,2 (М+1). Пример 13. 4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3 ил]пиримидин-2-ил-(2-пиридин 4-илэтил)амин. В запаянной ампуле раствор 3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридина (0,171 ммоль; см. пример 2 для его получения) и пиридин-4-илэтиламина (0,565 ммоль) в CH3CN (2 мл) нагревают при кипении с обратным холодильником в течение ночи. Реакционную смесь концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (550%MC(ESP+) 408,2 (М+1). Пример 14. трет-Бутиловый эфир (4-4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламинобутил)карбаминовой кислоты. В запаянной ампуле раствор 3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридина (0,191 ммоль; см. пример 2 для его получения) и трет-бутилового эфира (4 аминобутил)карбаминовой кислоты (0,611 ммоль) в CH3CN (2 мл) нагревают при кипении с обратным холодильником в течение ночи. Реакционную смесь концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (550% CH3CN/H2O), получая 44 мг трет-бутилового сложного эфира (4-4-[2(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламинобутил)карбаминовой кислоты. 1 Н ЯМР (d6-ДМСО, 400 МГц): 1,39 (с, 9 Н), 1,50 (квинтет, 2 Н, J=6,8 Гц), 1,58 (квинтет, 2 Н, J=6,8 Гц),2,53 (с, 3 Н), 2,98 (кв., 2 Н, J=6,6 Гц), 3,35 (м, 2 Н), 6,60 (ушир.с, 1 Н), 6,81 (дд, 1 Н, J=5,3, 5,3 Гц), 7,09 (дд,1 Н, J=6,4, 6,4 Гц), 7,28 (д, 1 Н, J=7,4 Гц), 7,32 (м, 1 Н), 7,47 (ддд, 1 Н, J=1,1, 6,8, 6,8 Гц), 7,73 (дд, 1 Н, J=7,7,7,7 Гц), 7,81 (дд, 1 Н, J=7,7, 7,7 Гц), 8,19 (д, 1 Н, 5,5 Гц), 9,45 (ушир.с, 1 Н).CH2Cl2/TFA (2 мл) оставляют при перемешивании на 30 мин, затем сушат в вакууме, получая 12 мг N14-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3 ил]пиримидин-2-илбутан-1,4-диамина в виде соли три-TFA. 1 Н ЯМР (d6-ДМСО, 400 МГц): 1,67 (м, 4 Н), 2,56 (с, 3 Н), 2,87 (м, 2 Н), 3,42 (м, 2 Н), 6,76 (ушир.с, 1 Н),7,28 (дд, 1 Н, J=6,9, 6,9 Гц), 7,47 (д, 1 Н, J=7,9 Гц), 7,69 (м, 1 Н), 7,74 (ушир.с, 2 Н), 7,81 (д, 1 Н, J=7,8 Гц),7,90 (д, 1 Н, J=9,0 Гц), 7,97 (дд, 1 Н, J=7,9, 7,9 Гц), 8,31 (д, 1 Н, J=5,4 Гц), 9,49 (ушир.с, 1 Н).MC(ESP+) 374,3 (М+1). Пример 16. трет-Бутиловый эфир (3-4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламинопропил)карбаминовой кислоты. В запаянной ампуле раствор 3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридина (0,191 ммоль; см. пример 2 для его получения) и трет-бутиловый эфир (3-аминопропил)карбаминовой кислоты (0,602 ммоль) в CH3CN (2 мл) нагревают при кипении с обратным холодильником в течение ночи. Реакционную смесь концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (550% CH3CN/H2O), получая 27 мг трет-бутилового эфира (3-4-[2-(6-метилпиридин-2 ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламинопропил)карбаминовой кислоты. 1 Н ЯМР (d6-ДМСО, 400 МГц): 1,40 (с, 9 Н), 1,73 (квинтет, 2 Н, J=6,7 Гц), 2,53 (с, 3 Н), 3,05 (кв., 2 Н,J=6,2 Гц), 3,36 (м, 2 Н), 6,63 (ушир.с, 1 Н), 6,87 (дд, 1 Н, J=5,6, 5,6 Гц), 7,12 (дд, 1 Н, 6,5, 6,5 Гц), 7,30 (м,1 Н), 7,31 (д, 1 Н, J=7,7 Гц), 7,51(ддд, 1 Н, J=1,1, 6,8, 6,8 Гц), 7,77 (дд, 2 Н, 7,7 Гц), 7,84 (дд, 1 Н, J=7,1, 7,1 Гц), 8,23 (д, 1 Н, J=5,3 Гц), 9,47 (ушир.с, 1 Н).CH2Cl2/TFA (2 мл) оставляют при перемешивании при комнатной температуре в течение 30 мин, затем сушат в вакууме, получая 48 мг N1-4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин 2-илпропан-1,3-диамина в виде соли три-TFA. 1 Н ЯМР (d6-ДМСО, 400 МГц): 1,90 (квинтет, 2 Н, J=7,8 Гц), 2,55 (с, 3 Н), 2,93 (септет, 2 Н, J=6,7 Гц),3,45 (кв., 2 Н, J=5,4 Гц), 6,76 (ушир.с, 1 Н), 7,23 (дд, 1 Н, J=7,0, 7,0 Гц), 7,43 (д, 1 Н, J=7,4 Гц), 7,67 (м, 4 Н),7,80 (д, 1 Н, J=7,9 Гц), 7,36 (д, 1 Н, J=9,l Гц), 7,95 (дд, 1 Н, J=7,9, 7,9 Гц), 8,32 (д, 1 Н, J=5,3 Гц), 9,44MC(ESP+) 360,2 (М+1). Пример 18. 4-[2-(6-Метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил-(3-морфолин-4-илпропил)амин. В запаянной ампуле раствор 3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридина (0,205 ммоль; см. пример 2 для его получения) и 3-пропиламиноморфолина (0,670 ммоль) в CH3CN (2 мл) нагревают при кипении с обратным холодильником в течение ночи. Реакционную смесь концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (550% CH3CN/H2O с 0,1% TFA), получая 20 мг 4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил(3-морфолин-4-илпропил)амина в виде соли TFA.MC(ESP+) 430,2 (М+1). Пример 19. 4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил-(2-пиридин 2-илэтил)амин. В запаянной ампуле раствор 3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2 ил)имидазо[1,2-а]пиридина (0,193 ммоль; см. пример 2 для его получения) и 2-пиридин-2-илэтиламина(0,641 ммоль) в CH3CN (2 мл) нагревают при кипении с обратным холодильником в течение ночи. Реакционную смесь концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (550%MC(ESP+) 408,1 (M+1). Пример 20. 4-(2-4-[2-(6-Метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2 иламиноэтил)бензолсульфонамид. В запаянной ампуле раствор 3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридина (0,193 ммоль; см. пример 2 для его получения) и 4-(2-аминоэтил)бензолсульфонамида (0,639 ммоль) в ДМФА(2 мл) нагревают при кипении с обратным холодильником в течение ночи. Реакционную смесь концентрируют в вакууме и очищают, используя препаративную ВЭЖХMC(ESP+) 486,0 (М+1). Пример 21. Метил 4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламин. В запаянной ампуле раствор 3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил) имидазо[1,2-а]пиридина (0,137 ммоль; см. пример 2 для его получения) и 2,00 М метиламин/ТГФ (1,00 ммоль) в CH3CN (2 мл) нагревают при кипении с обратным холодильником в течение ночи. Реакционную смесь концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (550%MC(ESP+) 317,2 (M+1). Пример 22. Диметил 4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2 иламин. В запаянной ампуле раствор 3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридина (0,136 ммоль; см. пример 2 для его получения) и 2,0 М диметиламин/ТГФ (1 ммоль) в CH3CN (2 мл) нагревают при кипении с обратным холодильником в течение ночи. Реакционную смесь концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (550% CH3CN/H2O), получая 17 мг диметил 4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламина. 1 Н ЯМР (d6-ДМСО, 400 МГц): 2,46 (с, 3 Н), 3,24 (с, 6 Н), 6,70 (д, 1 Н, J=5,0 Гц), 7,14 (дд, 1 Н, J=6,8, 6,8 Гц), 7,32 (д, 1 Н, J=7,3 Гц), 7,52 (дд, 1 Н, J=8,0, 8,0 Гц), 7,79 (м, 2 Н), 7,85 (д, 1 Н, J=7,8, 7,8 Гц), 8,33 (д, 1 Н,J=5,4, 5,4 Гц), 9,39 (д, 1 Н, J=7,2 Гц).MC(ESP+) 331,2 (М+1). Пример 23. (3-имидазол-1-илпропил)-4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламин. В запаянной ампуле раствор 3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридина (0,273 ммоль; см. пример 2 для его получения) и имидазол-1-илпропиламина (0,905 ммоль) в CH3CN (4 мл) нагревают при кипении с обратным холодильником в течение ночи. Реакционную смесь концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (550% CH3CN/H2O с 0,1% TFA), получая 8 мг (3-имидазол-1-илпропил)-4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин 3-ил]пиримидин-2-иламина в виде соли TFA. 1 Н ЯМР (d6-ДМСО, 400 МГц): 2,12 (п, 2 Н, J=6, 8 Гц), 2,45 (с, 3 Н), 3,37 (м, 2 Н), 4,23 (т, 2 Н, J=7,1 Гц),6,70 (ушир.с, 1 Н), 7,11 (дд, 1 Н, J=6,9, 6,9 Гц), 7,31 (д, 1 Н, J=7,6), 7,34 (ушир.с, 1 Н), 7,50 (м, 2 Н), 7,57(ушир.с, 1 Н), 7,78 (м, 2 Н), 7,85 (дд, 1 Н, J=8,0, 8,0 Гц), 8,26 (д, 1 Н, 5,3 Гц), 8,46 (ушир.с, 1 Н), 9,38 (ушир.с,1 Н). MC(ESP+) 411,2 (M+1). Пример 24. 3-4-[2-(6-Метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламино фенол. В запаянной ампуле перемешивают суспензию твердого KHMDS (0,501 ммоль) и 3-аминофенола(0,458 ммоль) в безводном диоксане (2 мл) в течение 1 ч. К реакционной смеси добавляют 3-(2 метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин (0,137 ммоль; см. пример 2 для его получения) и смесь оставляют при перемешивании на 2 дня при 80 С. Смесь концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (550% CH3CN/H2O с 0,1% TFA), получая 12 мг 3-4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3 ил]пиримидин-2-иламинофенола в виде соли TFA. 1 Н ЯМР (d6-ДМСО, 400 МГц): 2,55 (с, 3 Н), 6,70 (м, 2 Н), 7,02 (дд, 1 Н, J=7,1, 7,1 Гц), 7,28 (м, 1 Н), 7,40MC(ESP+) 395,2 (М+1). Пример 25. 4-[2-(6-Метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил-[1,3,4]тиадиазол-2-иламин. В запаянной ампуле суспензию твердого KHMDS (0,501 ммоль) и [1,3,4]тиадиазол-2-иламина (0,454 ммоль) в безводном диоксане (2 мл) перемешивают в течение 1 ч. К реакционной смеси добавляют 3-(2 метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин (0,137 ммоль; см. пример 2 для его получения) и полученную смесь оставляют при перемешивании на 2 дня при 80 С. Смесь концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (550% CH3CN/H2O с 0,1% TFA), получая 23 мг 4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил[1,3,4]тиадиазол-2-иламина в виде соли TFA. 1 Н ЯМР (d6-ДМСО, 400 МГц): 2,51 (с, 3 Н), 7,17 (м, 2 Н), 7,37 (д, 1 Н, 7,4 Гц), 7,60 (дд, 1 Н, J=7,5, 7,5 Гц), 7,86 (м, 3 Н), 8,61 (д, 1 Н, J=5,3 Гц), 9,07 (с, 1 Н), 9,59 (ушир.с, 1 Н).MC(ESP+) 387,1 (М+1). Пример 26. Трет-бутиловый эфир (5-4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламинопентил)карбаминовой кислоты. В запаянной ампуле раствор 3-(2-метансульфонилпиркмидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридина (0,205 ммоль; см. пример 2 для его получения) и трет-бутилового эфира (5-аминопентил)карбаминовой кислоты (0,677 ммоль) в ацетонитриле (2 мл) нагревают при кипении с обратным холодильником в течение ночи. Реакционную смесь концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (550% CH3CN/H2O с 0,1% TFA), получая 65 мг трет-бутилового эфира (5-4-[2(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламинопентил)карбаминовой кислоты в виде соли TFA. 1 Н ЯМР (d6-ДМСО, 400 МГц): 1,36 (с, 9 Н), 1,40 (м, 2 Н), 1,62 (м, 2 Н), 2,58 (с, 3 Н), 2,96 (м, 2 Н), 3,37MC(ESP+) 488,2 (М+1). Пример 27. [3-(4-Метилпиперазин-1-ил)пропил]-4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламин. В запаянной ампуле раствор 3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридина (0,205 ммоль; см. пример 2 для его получения) и 3-(4-метилпиперазин-1-ил)пропиламина (0,680 ммоль) в ацетонитриле (2 мл) нагревают при кипении с обратным холодильником в течение ночи. Смесь концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (550%MC(ESP+) 443,4 (М+1). Пример 28. Циклопропил 4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2 иламин. В запаянной ампуле раствор 3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2 ил)имидазо[1,2-а]пиридина (0,205 ммоль; см. пример 2 для его получения) и циклопропиламина (14,4 ммоль) в ацетонитриле (2 мл) нагревают при кипении с обратным холодильником в течение ночи. Смесь концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (550% CH3CN/H2O с 0,1%MC(ESP+) 343,3 (М+1). Пример 29. 2-(6-Метилпиридин-2-ил)-3-(2-пирролидин-1-илпиримидин-4-ил)имидазо[1,2-а]пиридин. В запаянной ампуле раствор 3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридина (0,205 ммоль; см. пример 2 для его получения) и пирролидина (1,20 ммоль) в ацетонитриле (2 мл) нагревают при кипении с обратным холодильником в течение ночи. Смесь концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (580% CH3CN/H2O с 0,1% TFA), получая 40 мг 2-(6-метилпиридин-2-ил)-3-(2-пирролидин-1-илпиримидин-4-ил)имидазо[1,2-а]пиридина в виде соли TFA. 1 Н ЯМР (d6-ДМСО, 400 МГц): 2,00 (ушир.м, 4 Н), 2,54 (с, 3 Н), 3,60 (ушир.м, 4 Н), 6,71 (ушир.с, 1 Н),7,26 (м, 1 Н), 7,44 (д, 1 Н, 7,3 Гц), 7,68 (ушир.м, 1 Н), 7,77 (д, 1 Н, J=7,9 Гц), 7,86 (д, 1 Н, J=8,9 Гц), 7,95MC(ESP+) 357,4 (М+1). Пример 30. 2-(6-Метилпиридин-2-ил)-3-(2-пиперидин-1-илпиримидин-4-ил)имидазо[1,2-а]пиридин. В запаянной ампуле раствор 3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридина (0,205 ммоль; см. пример 2 для его получения) и пиперидина (1,01 ммоль) в ацетонитриле (2 мл) нагревают при кипении с обратным холодильником в течение ночи. Смесь концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (580% CH3CN/H2O с 0,1% TFA), получая 24 мг 2-(6-метилпиридин-2-ил)-3-(2-пиперидин-1-илпиримидин-4-ил)имидазо[1,2-а]пиридина в виде соли TFA. 1 Н ЯМР (d6-ДМСО, 400 МГц): 1,59 (м, 4 Н), 1,67 (м, 2 Н), 2,55 (с, 3 Н), 3,81 (м, 4 Н), 6,74 (д, 1 Н, J=5,0 Гц), 7,24 (ддд, 1 Н, J=0,8, 7,7, 7,7 Гц), 7,43 (д, 1 Н, 7,6 Гц), 7,63 (м, 1 Н), 7,77 (д, 1 Н, J=7,7 Гц), 7,84 (д, 1 Н,J=9,2 Гц), 7,92 (т, 1 Н, J=7,9 Гц), 8,37 (д, 1 Н, J=5,2 Гц), 9,18 (д, 1 Н, J=7,1 Гц).MC(ESP+) 371,4 (М+1). Пример 31. (2-Метоксиэтил)-4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин 2-иламин. В запаянной ампуле раствор 3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридина (0,205 ммоль; см. пример 2 для его получения) и 2-метоксиэтиламина (1,16 ммоль) в ацетонитриле (2 мл) нагревают при кипении с обратным холодильником в течение ночи. Смесь концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (580% CH3CN/H2O с 0,1% TFA), получая 42 мг (2-метоксиэтил)-4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил амина в виде соли TFA. 1 Н ЯМР (d6-ДМСО, 400 МГц): 2,58 (с, 3 Н), 3,34 (с, 3 Н), 3,57 (ушир.м, 4 Н), 6,77 (ушир.с, 1 Н), 7,28MC(ESP+) 361,4 (М+1). Пример 32. 3-[2-(4-Метилпиперазин-1-ил)пиримидин-4-ил]-2-(6-метилпиридин-2-ил)имидазо[1,2-а] пиридин. В запаянной ампуле раствор 3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридина (0,205 ммоль; см. пример 2 для его получения) и 1-метилпиперазина (0,900 ммоль) в ацетонитриле (2 мл) кипятят с обратным холодильником в течение ночи. Смесь концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (580% CH3CN/H2O с 0,1% TFA), получая 19 мг 3-[2(4-метилпиперазин-1-ил)пиримидин-4-ил]-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридина в виде солиMC(ESP+) 386,4 (М+1). Пример 33. 3-[2-(2-Метилазиридин-1-ил)пиримидин-4-ил]-2-(6-метилпирицин-2-ил)имидазо[1,2-а] пиридин. В запаянной ампуле раствор 3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридина (0,137 ммоль; см. пример 2 для его получения) и 2-метилазиридина (0,849 ммоль) в ацетонитриле (2 мл) нагревают при кипении с обратным холодильником в течение ночи. Смесь концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (550% CH3CN/H2O с 0,1% TFA), получая 11 мг 3-[2-(2-метилазиридин-1-ил)пиримидин-4-ил]-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридина в виде соли TFA. 1 Н ЯМР (d6-ДМСО, 400 МГц): 1,16 (д, 3 Н, J=5,8 Гц), 2,56 (с, 3 Н), 3,36 (м, 2 Н), 3,90 (м, 1 Н), 6,75 (м,- 23010426 1 Н), 7,16 (м, 1 Н), 7,45 (м, 1 Н), 7,72 (м, 2 Н), 7,91 (м, 1 Н), 8,20 (м, 1 Н), 9,54 (м, 1 Н).MC(ESP+) 343,2 (М+1). Пример 34. 4-[2-(6-Метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил-(2 Н-пиразол-3-ил)амин. В запаянной ампуле суспензию твердого KHMDS (0,501 ммоль) и 2 Н-пиразол-3-иламина (0,454 ммоль) в безводном диоксане (2 мл) перемешивают в течение 1 час. К реакционной смеси добавляют 3(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин (0,137 ммоль; см. пример 2 для его получения) и смесь оставляют при перемешивании на 2 дня при 80 С. Смесь пропускают через слой силикагеля, концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (58 0% CH3CN/H2O с 0,1% TFA), получая 21 мг (4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3 ил]пиримидин-2-ил-(2 Н-пиразол-3-ил)амина в виде соли TFA. 1 Н ЯМР (d6-ДМСО, 400 МГц): 2,47 (с, 3 Н), 5,94 (д, 1 Н, J=2,7 Гц), 7,22 (дд, 1 Н, J=7,0, 7,0 Гц), 7,39 (м,1 Н), 7,61 (дд, 1 Н, J=8,4, 8,4 Гц), 7,90 (м, 3 Н), 8,36 (д, 1 Н, J=2,2 Гц), 8,64 (д, 1 Н, J=4,9 Гц), 9,56 (д, 1 Н,J=7,5 Гц).(0,200 ммоль; см. пример 2 для его получения) и цианида натрия (0,671 моль) в безводном ДМФА (2 мл) нагревают при 100 С в запаянной ампуле в течение 4,5 ч. После охлаждения до комнатной температуры раствор фильтруют через слой целита и концентрируют в вакууме, получая темное твердое вещество. Твердое вещество суспендируют в смеси ДМСО/вода, охлаждают до 0 С, фильтруют, промывают холодной водой и сушат на воздухе, получая 0,0274 г твердого вещества желто-коричневого цвета, идентифицированного как 4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-карбонитрил. МС (ESP+) 313,20 (М+1). В запаянной ампуле 4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-карбонитрил (0,240 ммоль), NaN3 (1,72 ммоль) и NH4CI (1,27 ммоль) добавляют последовательно к ДМФА (3 мл). Смесь нагревают при 110 С в течение двух дней. Реакционную смесь концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (CH3CN/H2O градиент), получая 50 мг 2-(6-метилпиридин-2 ил)-3-[2-(1 Н-тетразол-5-ил)пиримидин-4-ил]имидазо[1,2-а]пиридина. 1MC(ESP-) 354,1 (М-1). Пример 36. 3-(2-Азетидин-1-илпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин. В запаянной ампуле раствор 3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридина (0,147 ммоль; см. пример 2 для его получения) и азеридина (0,297 ммоль) в CH3CN(2 мл) оставляют при перемешивании, при кипении с обратным холодильником в течение ночи. Реакционную смесь концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (590% CH3CN/MC(ESP+) 343,2 (M+1). Пример 37. Циклопентил 4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2 иламин. В запаянной ампуле раствор 3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридина (0,137 ммоль; см. пример 2 для его получения) и циклопентиламина (0,452 ммоль) вCH3CN (2 мл) оставляют при перемешивании, при кипении с обратным холодильником в течение ночи. Реакционную смесь концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (550%MC(ESP+) 371,1 (М+1). Пример 38. 4-[2-(6-Метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил-S)-1-фенилэтил)амин. В запаянной ампуле раствор 3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридина (0,137 ммоль; см. пример 2 для его получения) и (S)-бензилметиламина (1,37 ммоль) в CH3CN (2 мл) оставляют при перемешивании, при кипении с обратным холодильником в течение ночи.- 24010426 Реакционную смесь концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (550%CH3CN/H2O с 0,1% TFA), получая 11 мг 4-[2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил-S)-1-фенилэтил)амина в виде соли TFA. 1 Н ЯМР (d6-ДМСО, 400 МГц): 1,54 (д, 3 Н, J=7,0 Гц), 2,56 (с, 3 Н), 5,09 (ушир.с, 1 Н), 6,68 (д, 1 Н,J=5,2 Гц), 7,31 (м, 1 Н), 7,44 (м, 6 Н), 7,65 (м, 1 Н), 7,77 (д, 1 Н, J=7,3 Гц), 7,85 (д, 1 Н, J=7,3 Гц), 7,96 (дд, 1 Н,J=8,3, 7,3 Гц), 8,23 (м, 1 Н), 8,30 (д, 1 Н, J=5,0 Гц). МС (ESP+) 407,2 (М+1). Пример 39. 4-[2-(6-Метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-ил-R)-1 фенилэтил)амин. В запаянной ампуле раствор 3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридина (0,137 ммоль; см. пример 2 для его получения) и (R)-бензилметиламин (1,37 ммоль) в CH3CN (2 мл) оставляют при перемешивании при кипении с обратным холодильником в течение ночи. Реакционную смесь концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (550%(2,0 ммоль) добавляют к раствору 1-(6-метилпиридин-2-ил)-2-(2-метилсульфанилпиримидин-4-ил)этанона (1,54 ммоль; см. пример 1 (b) для его получения) и каталитического количества ВНТ в ледяной уксусной кислоте (10 мл) при комнатной температуре, при этом происходит образование осадка. Через 1 ч реакционную смесь разбавляют эфиром (40 мл), перемешивают в течение 30 мин, затем осадок отфильтровывают и промывают Et2O (предпринимают тщательные предосторожности, чтобы осадок не высох полностью). Осадок суспендируют в CH3CN (10 мл), добавляют к суспензии основание Хинига (4,58 ммоль) и 3-метил-2-аминопиридина (1,85 ммоль) при комнатной температуре и затем нагревают в течение ночи при 55 С. При охлаждении до комнатной температуры образуется осадок. Суспензию разбавляют водой (10 мл), фильтруют, промывают холодным CH3CN, получая 211 мг твердого вещества желтокоричневого цвета, идентифицированного как 8-метил-2-(6-метилпиридин-2-ил)-3-(2-метилсульфанилпиримидин-4-ил)имидазо[1,2-а]пиридин. Пример 41. 3-(2-Метансульфонилпиримидин-4-ил)-8-метил-2-(6-метилпиридин-2-ил)имидазо[1,2-а] пиридин. 4,0 н. серную кислоту (0,06 ммоль), каталитическое количество дигидрата вольфрамата натрия и 30 мас.% перекись водорода (1,96 ммоль) добавляют к суспензии 8-метил-2-(6-метилпиридин-2-ил)-3-(2 метилсульфанилпиримидин-4-ил)имидазо[1,2-а]пиридина (0,608 ммоль; см. пример 40 для его получения) в метаноле (4 мл) при 50 С. Через 3,5 ч реакционную смесь разбавляют водой (10 мл) и нагревают при 50 С еще 0,5 ч. Затем реакционную смесь охлаждают до комнатной температуры, гасят насыщенным тиосульфатом натрия, уровень рН доводят до 6, используя 1 М NaOH, и фильтруют, получая 0,200 г твердого вещества желто-коричневого цвета, идентифицированного как 3-(2-метансульфонилпиримидин-4 ил)-8-метил-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин. 1 Н ЯМР (d6-ДМСО, 400 МГц): 2,44 (с, 3 Н), 2,66 (с, 3 Н), 3,53 (с, 3 Н), 7,15 (дд, 1 Н, J=7,0, 7,0 Гц), 7,36MC(ESP+) 380,2 (М+1). Пример 42. 4-[8-Метил-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридия-3-ил]пиримидин-2-иламин. В запаянной ампуле суспензию 3-(2-метансульфонилпиримидин-4-ил)-8-метил-2-(6-метилпиридин 2-ил)имидазо[1,2-а]пиридина (0,263 ммоль; получен по способу примера 2) и NH4OAC (6,60 ммоль) в смеси 2:1 диоксан/вода (3 мл) нагревают при 100 С в течение 7 дней. Реакционную смесь охлаждают до комнатной температуры, разбавляют EtOAc (25 мл), промывают водой, насыщенным раствором соли,сушат (Na2SO4), концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (CH3CN/H2O градиент с 0,1% TFA), и получают 30 мг твердого вещества, идентифицированного как соль TFA 4-[8 метил-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламина. 1 Н ЯМР (d6-ДМСО, 400 МГц): 2,65 (с, 3 Н), 6,75 (д, 1 Н, J=5,8 Гц), 7,17 (дд, 1 Н, J=7,1, 7,1 Гц), 7,46 (д,1 Н, J=8,1 Гц) 7,50 (д, 1 Н, J=6,5 Гц), 7,83 (д, 1 Н, J=7,7 Гц), 7,97 (дд, 1 Н, J=7,6, 1,6 Гц), 8,20 (д, 1 Н, J=6,0 Гц), 9,57 (д, 1 Н, J=7,3 Гц).(2,0 ммоль) добавляют к раствору 1-(6-метилпиридин-2-ил)-2-(2-метилсульфанилпиримидин-4-ил)этанона (1,54 ммоль; см. пример 1(b) для его получения) и каталитического количества ВНТ в ледяной уксусной кислоте (10 мл) при комнатной температуре, при этом происходит образование осадка. Через 1 час реакционную смесь разбавляют эфиром (40 мл), перемешивают в течение 30 мин, затем выпавший осадок отфильтровывают и промывают с Et2O (предпринимают тщательные предосторожности, чтобы осадок не высох полностью). Осадок суспендируют в CH3CN, добавляют к смеси основание Хинига и 4 метил-2-аминопиридин (1,86 ммоль) при комнатной температуре и затем нагревают в течение ночи при 55 С. После охлаждения до комнатной температуры образуется осадок. Суспензию разбавляют водой (10 мл), фильтруют, промывают холодным CH3CN, получая 211 мг твердого вещества, идентифицированного как 7-метил-2-(6-метилпиридин-2-ил)-3-(2-метилсульфанилпиримидин-4-ил)имидазо[1,2-а]пиридин. 1 Н ЯМР (CDCl3, 300 МГц): 2,49 (с, 3 Н), 2,56 (с, 3 Н), 2,64 (с, 3 Н), 6,84 (м, 1 Н), 7,20 (м, 2 Н), 7,58 (м,1 Н), 7,73 (м, 2 Н), 8,35 (д, 1 Н, J=5,4 Гц), 9,41 (д, 1 Н, J=6,9 Гц).MC(ESP+) 373,3 (М+1). Пример 44. 3-(2-Метансульфонилпиримидин-4-ил)-7-метил-2-(6-метилпиридин-2-ил)имидазо[1,2 а]пиридин. 4,0 н. серную кислоту (0,02 ммоль), каталитическое количество дигидрата вольфрамата натрия и 30 мас.% перекись водорода (X ммоль) добавляют к суспензии 7-метил-2-(6-метилпиридин-2-ил)-3-(2 метилсульфанилпиримидин-4-ил)имидазо[1,2-а]пиридина (0,274 ммоль; получен по способу примера 1) в метаноле (3 мл) при 55 С. Через 3,5 ч реакционную смесь разбавляют водой (10 мл) и нагревают при 55 С еще 0,5 ч. Затем реакционную смесь охлаждают до комнатной температуры, гасят насыщенным тиосульфатом натрия, уровень рН доводят до 6, используя 1 М NaOH, и фильтруют, получая 0,070 г твердого вещества желтого цвета, идентифицированного как 3-(2-метансульфонилпиримидин-4-ил)-7-метил 2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин. 1 Н ЯМР (d6-ДМСО, 400 МГц): 2,42 (с, 3 Н), 2,46 (с, 3 Н), 3,49 (с, 3 Н), 7,11 (дд, 1 Н, J=l,6, 7,2 Гц), 7,36MC(ESP+) 380,2 (М+1). Пример 45. 4-[7-Метил-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламин. В запаянной ампуле суспензию 3-(2-метансульфонилпиримидин-4-ил)-7-метил-2-(6-метилпиридин 2-ил)имидазо[1,2-а]пиридина (0,184 ммоль; см. пример 44 для его получения) и NH4OAc (4,60 ммоль) в смеси 2:1 диоксан/вода (3 мл) нагревают при 100 С в течение 7 дней. Реакционную смесь охлаждают до комнатной температуры, разбавляют EtOAc (25 мл), промывают водой, насыщенным раствором соли,сушат (Na2SO4), концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (CH2CN/H2O градиент с 0,1% TFA), получая 22 мг твердого вещества, идентифицированного как соль TFA 4-[7-метил 2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламина. 1 Н ЯМР (d6-ДМСО, 400 МГц): 2,53 (с, 3 Н), 2,57 (с, 3 Н), 6,80 (д, 1 Н, J=6,0 Гц), 7,19 (д, 1 Н, J=7,9 Гц),7,47 (д, 1 Н, J=7,6 Гц), 7,71 (ушир.с, 1 Н), 7,78 (д, 1 Н, J=7,8 Гц), 7,96 (дд, 1 Н, J=7,6, 7,6 Гц), 8,23 (д, 1 Н,J=6,2 Гц), 9,56 (д, 1 Н, J=6,4 Гц).(2,0 ммоль) добавляют к раствору 1-(6-метилпиридин-2-ил)-2-(2-метилсульфанилпиримидин-4-ил)этанона (1,54 ммоль; см. пример 1(b) для его получения) и каталитического количества ВНТ в ледяной уксусной кислоте (10 мл) при комнатной температуре, при этом происходит образование осадка. Через 1 ч реакционную смесь разбавляют эфиром (40 мл), перемешивают в течение 30 мин, осадок затем отфильтровывают и промывают Et2O (предпринимают тщательные предосторожности, чтобы осадок не высох полностью). Осадок суспендируют в CH3CN (10 мл). К этой суспензии добавляют 4-хлор-2-аминопиридин(1,85 ммоль) и основание Хинига (4,58 ммоль) и смесь оставляют при перемешивании в течение ночи при 55 С в атмосфере азота. При охлаждении до комнатной температуры образуется осадок. Суспензию разбавляют водой (10 мл), фильтруют и промывают холодным CH3CN, получая 124 мг нечистого твердого вещества желто-коричневого цвета, идентифицированного как 6-хлор-2-(6-метилпиридин-2-ил)-3-(2 метилсульфанилпиримидин-4-ил)имидазо[1,2-а]пиридин. МС (ESP+) 368,0 (М+1). Пример 47. 6-Хлор-3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2 а]пиридин. 4,0 н. серную кислоту (0,02 ммоль), каталитическое количество дигидрата вольфрамата натрия и 30 мас.% перекись водорода (0,98 ммоль) добавляют к суспензии 6-хлор-2-(6-метилпиридин-2-ил)-3-(2 метилсульфанилпиримидин-4-ил)имидазо[1,2-а]пиридина (0,274 ммоль; см. пример 46 для его получения) в метаноле (2 мл) при 55 С. Через 3,5 ч реакционную смесь разбавляют водой (10 мл) и нагревают при 55 С в течение дополнительно 0,5 ч. Затем реакционную смесь охлаждают до комнатной температуры, гасят насыщенным тиосульфатом натрия, уровень рН доводят до 6, используя 1 М NaOH, и фильтру- 26010426 ют, получая 0,050 г твердого вещества желтого цвета, идентифицированного как нечистый 6-хлор-3-(2 метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин. МС (ESP+) 400,0 (М+1). Пример 48. 4-[6-Хлор-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-3 ил]пиримидин-2-иламин. В запаянной ампуле суспензию 6-хлор-3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2 ил)имидазо[1,2-а]пиридина (0,125 ммоль; см. пример 47 для его получения) и NH4OAc (6,60 ммоль) в смеси 1:1 диоксан/вода (2 мл) нагревают при 100 С в течение 5 дней. Реакционную смесь охлаждают до комнатной температуры, разбавляют EtOAc (25 мл), промывают Н 2 О, насыщенным раствором соли, сушат (Na2SO4), концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (CH3CN/H2O градиент с 0,1% TFA), получая 4 мг твердого вещества, идентифицированного как TFA соль 4-[6-хлор-2-(6 метилпиридин-2-ил)имидазо[1,2-а]пиридин-3-ил]пиримидин-2-иламина. 1 Н ЯМР (d6-ДМСО, 400 МГц): 2,50 (с, 3 Н), 6,84 (д, 1 Н, J=6,0 Гц), 7,45 (д, 1H,J=8,5 Гц), 7,72 (д, 1 Н,J=10,l Гц), 7,86 (д, 1 Н, J=6,9 Гц), 7,96 (м, 2 Н), 8,25 (д, 1 Н, J=6,0 Гц), 9,72 (с, 1 Н).(2,0 ммоль) добавляют к раствору 1-(6-метилпиридин-2-ил)-2-(2-метилсульфанилпиримидин-4 ил)эталона (1,54 ммоль; см. пример 1 (b) для его получения) и каталитического количества ВНТ в ледяной уксусной кислоте (10 мл) при -15 С, при этом образуется осадок. Через 0,25 ч реакционную смесь разбавляют эфиром (40 мл), перемешивают в течение 5 мин, затем осадок отфильтровывают и промывают с Et2O в токе азота (предпринимают тщательные предосторожности, чтобы осадок не высох полностью). Осадок добавляют в колбу, содержащую (6-аминопиридин-3-ил)метанол (2,06 ммоль) в атмосфере азота, суспендируют в толуоле (8 мл) и нагревают до 100 С. Медленно добавляют диизопропилэтиламин(11,4 ммоль) и реакционную смесь оставляют при перемешивании при 100 С примерно на 4 ч. При охлаждении до комнатной температуры образуется осадок. Суспензию охлаждают до 0 С, фильтруют,промывают CH3CN и сушат на воздухе, получая 345 мг твердого вещества желто-коричневого цвета,идентифицированного как [2-(6-метилпиридин-2-ил)-3-(2-метилсульфанилпиримидин-4-ил)имидазо[1,2 а]пиридин-6-ил]метанол. 1 Н ЯМР (CDCl3, 400 МГц): 2,62 (с, 3 Н), 2,63 (с, 3 Н), 4,74 (с, 2 Н), 7,01 (д, 1 Н, J=5,5 Гц), 7,24 (д, 1 Н,J=7,7 Гц), 7,29 (д, 1 Н, J=7,29 Гц), 7,59 (м, 2 Н), 7,71 (т, 1 Н, J=7,5 Гц), 8,29 (д, 1 Н, J=5,7 Гц), 9,40 (ушир.с,1 Н).MC(ESP+) 364,2 (М+1). Пример 50. [3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-ил]метанол. 4,0 н. серную кислоту (0,12 ммоль), каталитическое количество дигидрата вольфрамата натрия и 30 мас.% перекись водорода (9,8 ммоль) добавляют к суспензии [2-(6-метилпиридин-2-ил)-3-(2-метилсульфанилпиримидин-4-ил)имидазо[1,2-а]пиридин-6-ил]метанола (0,95 ммоль; см. пример 49 для его получения) в метаноле (50 мл) при 50 С. Через 3,5 ч реакционную смесь разбавляют водой (9,5 мл) и нагревают при 55 С еще 0,5 ч. Затем реакционную смесь охлаждают до комнатной температуры, гасят насыщенным тиосульфатом натрия, уровень рН доводят до 6, используя 1 М NaOH, и фильтруют, получая 0,208 г твердого вещества желто-коричневого цвета, идентифицированного как [3-(2-метансульфонилпиримидин-4 ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-ил]метанол. 1 Н ЯМР (d6-ДМСО, 400 МГц): 2,40 (с, 3 Н), 3,52 (с, 3 Н), 4,57 (д, 2 Н, J=5,4 Гц), 7,32 (д, 1 Н, J=7,3 Гц),7,54 (дд, 1 Н, J=l,3, 9,0 Гц), 7,87 (м, 3 Н), 8,05 (д, 1 Н, J=5,2 Гц), 8,98 (д, 1 Н, J=5,4 Гц), 9,31 (ушир.с, 1 Н).[3-(2-Аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6 ил]метанол. В запаянной ампуле раствор 3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-ил]метанола (0,526 ммоль; см. пример 50 для его получения) и NH4OAc (10,5 ммоль) в смеси 1:1 диоксан/вода (7 мл) нагревают при 100 С в течение 3 дней. Смесь охлаждают до комнатной температуры, концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (550%CH3CN/H2O с 0,1% TFA), получая 49,3 мг твердого вещества желтого цвета, идентифицированного как(2,48 ммоль) добавляют к раствору 1-(6-метилпиридин-2-ил)-2-(2-метилсульфанилпиримидин-4 ил)этанона (1,911 ммоль; см. пример 1(b) для его получения) и каталитического количества ВНТ в ледяной уксусной кислоте (10 мл) при комнатной температуре, при этом образуется осадок. Через 0,25 ч реакционную смесь разбавляют до 100 мл эфиром, фильтруют, промывают эфиром, быстро сушат на воздухе в токе азота и добавляют в колбу, содержащую метиловый эфир 6-аминоникотиновой кислоты(2,036 ммоль) в атмосфере азота. Добавляют безводный ацетонитрил (5 мл) и диизопропилэтиламин (7,65 ммоль) и полученный раствор нагревают до 80 С. Через 5,5 ч реакционную смесь оставляют охлаждаться до комнатной температуры, при этом образуется осадок. Суспензию фильтруют, промывают ацетонитрилом и сушат на воздухе, получая 0,4 816 г твердого вещества желто-коричневого цвета, идентифицированного как нечистый метиловый эфир 2-(6-метилпиридин-2-ил)-3-(2-метилсульфанилпиримидин-4 ил)имидазо[1,2-а]пиридин-6-карбоновой кислоты. 1 Н ЯМР (CDCl3, 400 МГц) 2,35 (с, 3 Н), 2,69 (с, 3 Н), 3,98 (с, 3 Н), 7,21 (д, J=5,26 Гц, 1 Н), 7,22 (д,J=6,81 Гц, 1 Н), 7,73 (д, J=7,31 Гц, 1 Н), 7,82 (J=9,67 Гц, 1 Н), 7,94 (дд, J=9,36, 1,54 Гц, 1 Н), 8,38 (д, J=5,33 Гц, 1 Н), 10,34 (с, 1 Н).MC(ESP+) 392,11 (М+1). Пример 53. Метиловый эфир 3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбоновой кислоты. 4,0 н. серную кислоту (0,02 ммоль), каталитическое количество дигидрата вольфрамата натрия и 30 мас.% перекись водорода (0,88 ммоль) добавляют к суспензии метилового эфира 2-(6-метилпиридин-2 ил)-3-(2-метилсульфанилпиримидин-4-ил)имидазо[1,2-а]пиридин-6-карбоновой кислоты (0,2 664 ммоль; см. пример 52 для его получения) в смеси 1:1 метанол/метиленхлорид (4 мл) при 55 С. Через 6,6 ч реакционную смесь разбавляют водой (2 мл) и нагревают при 55 С в течение 0,75 ч. Затем реакционную смесь охлаждают до комнатной температуры и нейтрализуют (I2/крахмальная бумага) насыщенным тиосульфатом натрия. Затем реакционную смесь разбавляют метиленхлоридом (20 мл) и органическую фазу промывают 10% бикарбонатом натрия (5 мл) и насыщенным раствором соли (5 мл), сушат (MgSO4) и концентрируют в вакууме, получая 0,1026 г твердого вещества желтого цвета, идентифицированного как метиловый эфир 3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин 6-карбоновой кислоты. г Н ЯМР (CDCl3, 300 МГц) 2,54 (с, 3 Н), 3,45 (с, 3 Н), 3,99 (с, 3 Н), 7,27 (д, J=6,60 Гц, 1 Н), 7,78 (д,J=9,30 Гц, 1 Н), 7,78 (дд, J=7,80, 7,80 Гц, 1 Н), 7,90 (J=8,10 Гц, 1 Н), 8,01 (дд, J=9,30, 1,50 Гц, 1 Н), 8,03 (д,J=5,40 Гц, 1 Н), 8,74 (д, J=5,40 Гц, 1 Н), 10,58 (с, 1 Н).MC(ESP+) 424,15 (М+1). Пример 54. Метиловый эфир 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а] пиридин-6-карбоновой кислоты. Раствор метилового эфира 3-(2-метансульфонилпиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбоновой кислоты (0,1717 ммоль; см. пример 53 для его получения) и ацетата аммония (3,526 ммоль) в смеси 2:1 диоксан/вода (3 мл) нагревают при 100 С в запаянной ампуле. Через 23,5 ч реакционной смеси дают остыть до комнатной температуры, фильтруют, твердую часть промывают ацетонитрилом и сушат на воздухе, получая 0,0340 г твердого вещества желто-коричневого цвета. Это твердое вещество очищают, используя ВЭЖХ с обращенной фазой (ацетонитрил/вода градиент с 0,1% TFA),получая 0,0295 г твердого вещества желтого цвета, идентифицированного как TFA соль метилового эфира 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбоновой кислоты. 1 Н ЯМР (ДМСО-d6, 400 МГц) 2,41 (с, 3 Н), 3,87 (с, 3 Н), 6,78 (д, J=5,69 Гц, 1 Н), 7,33 (д, J=7,44 Гц,1 Н), 7,4 (ушир.с, 2 Н), 7,80-7,86 (м, 4 Н)3 8,22 (д, J=5,65, 1 Н), 9,77 (с, 1 Н).MC(ESP+) 361,4 (М+1). Пример 55. 3-(2-Аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбоновая кислота. В запаянной ампуле раствор метилового эфира 3-(2-метилсульфонилпиримидин-4-ил)-2-(6 метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбоновой кислоты (2,30 ммоль; см. пример 53 для его получения) и NH4OAC (45,8 ммоль) в смеси 1:1 диоксан/вода (30 мл) нагревают при 100 С в течение 3 дней. Смесь охлаждают до комнатной температуры, что приводит к образованию осадка, который отфильтровывают и промывают водой, получая 430 мг смеси карбоновой кислоты и сложного эфира. Смесь растворяют в смеси 2:1 ТГФ/Н 2 О (15 мл), добавляют LiOHН 2 О (5,95 ммоль) и реакционную смесь перемешивают при комнатной температуре в течение 0,5 час. Реакционную смесь нейтрализуют, используя 2 М HCl, охлаждают до 0 С; фильтруют и промывают водой, получая 370 мг твердого вещества,идентифицированного как 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин 6-карбоновая кислота. 1 Н ЯМР (d6-ДМСО, 400 МГц): 2,39 (с, 3 Н), 6,75 (д, 1 Н, J=5,3 Гц), 6,79 (ушир.с, 2 Н)3 7,30 (дд, 1 Н,J=4,0, 4,3 Гц), 7,83 (м, 5 Н), 8,29 (д, 1 Н, J=5,3 Гц), 9,65 (ушир.с, 1 Н).MC(ESP+) 347,7 (М+1). Пример 56. Метоксиамид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пи- 28010426 ридин-6-карбоновой кислоты. В колбу добавляют 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6 карбоновую кислоту (0,144 ммоль; см. пример 55 для ее получения) с ДМФА(1 мл). Реакционную смесь перемешивают до тех пор, пока не растворятся все вещества. Затем добавляют HATU (0,201 ммоль) и убеждаются в том, что растворились все вещества. После этого добавляют DIEA (1,15 ммоль). Эту смесь оставляют при перемешивании в течение 10 мин. Затем добавляют гидрохлорид метоксиамина (0,173 ммоль) и реакционную смесь перемешивают в течение 2 ч, концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (550% CH3CN:H2O с 0,1% TFA), получая 28,9 мг твердого вещества,идентифицированного как TFA соль метоксиамида 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2 ил)имидазо[1,2-а]пиридин-6-карбоновой кислоты. 1 Н ЯМР (d6-ДМСО, 400 МГц): 2,52 (с, 3 Н), 3,80 (с, 3 Н), 6,92 (д, 1 Н, J=5,7 Гц), 7,45 (д, 1 Н, J=7,6 Гц),7,61 (ушир.с, 1 Н), 7,90 (м, 5 Н), 8,32 (д, 1 Н, J=5,4 Гц), 9,69 (с, 1 Н). МС 376,5 (ESP+) (М+1). Пример 57. Этиламид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин 6-карбоновой кислоты. В колбу добавляют 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6 карбоновую кислоту (0,144 ммоль; см. пример 55 для ее получения) с ДМФА (1 мл). Реакционную смесь перемешивают до тех пор, пока не растворятся все вещества. Затем добавляют HATU (0,201 ммоль) и убеждаются в том, что растворились все вещества. После этого добавляют DIEA (0,70 ммоль). Эту смесь оставляют при перемешивании на 10 мин, затем добавляют смесь 20 М этиламин/ТГФ (0,432 ммоль),реакционную смесь перемешивают в течение 2 ч, концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (540% CH3CN:H2O с 0,1% TFA), получая 41,0 мг твердого вещества, идентифицированного как TFA соль этиламида 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а] пиридин-6-карбоновой кислоты. 1 Н ЯМР (d6-ДМСО, 400 МГц): 1,17 (т, 3 Н, 7,3 Гц), 2,53 (с, 3 Н), 3,37 (м, 2 Н), 6,92 (д, 1 Н, J=5,8 Гц),7,44 (д, 1 Н, J=7,7 Гц), 7,70 (ушир.с, 1 Н), 7,93 (м, 4 Н), 8,33 (д, 1 Н, J=8,3 Гц), 8,73 (дд, 1 Н, J=5,4, 5,4 Гц),9,71 (м, 1 Н).MC(ESP+) 374,3 (М+1). Пример 58. (2-Диметиламиноэтил)амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбоновой кислоты. В колбу добавляют 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6 карбоновую кислоту (0,144 ммоль; см. пример 55 для ее получения) с ДМФА (1 мл). Реакционную смесь перемешивают до тех пор, пока не растворятся все вещества. Затем добавляютHATU (0,201 ммоль), убеждаясь, что растворились все вещества. После этого добавляют DIEA (0,720 ммоль). Эту смесь оставляют при перемешивании на 10 мин. Затем добавляют N,N-диметилэтилдиамин (0,173 ммоль) и реакционную смесь перемешивают в течение 2 ч, концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (540% CH3CN:H2O с 0,1% TFA), получая 29,9 мг твердого вещества, идентифицированного как TFA соль (2 диметиламиноэтил) амида 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин 6-карбоновой кислоты. 1 Н ЯМР (d6-ДМСО, 400 МГц): 2,50 (с, 3 Н), 2,91 (д, 6 Н, J=4,6 Гц), 3,34 (кв., 2 Н, J=5,5 Гц), 3,69 (кв.,2 Н, J=5,7 Гц), 6,90 (д, 1 Н, J=5,8 Гц), 7,41 (д, 1 Н, J=7,2 Гц), 7,51 (ушир.с, 1 Н), 7,92 (м, 4 Н), 8,33 (д, 1 Н,J=5,9 Гц), 8,96 (дд, 1 Н, J=5,7, 5,7 Гц), 9,60 (ушир.с, 1 Н), 9,78 (м, 1 Н).MC(ESP+) 417,5 (М+1). Пример 59. (2-метоксиэтил)амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2 а]пиридин-6-карбоновой кислоты. В колбу добавляют 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6 карбоновую кислоту (0,14 4 ммоль; см. пример 55 для ее получения) с ДМФА (1 мл). Реакционную смесь перемешивают до тех пор, пока не растворятся все вещества. Затем добавляют HATU (0,201 ммоль), убеждаясь, что растворились все вещества. После этого добавляют DIEA (0,720 ммоль). Эту смесь оставляют при перемешивании на 10 мин. Затем добавляют метилоксиэтиламин (0,288 ммоль) и реакционную смесь перемешивают в течение 2 ч, концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (540% CH3CN:H2O с 0,1% TFA), получая 36,1 мг твердого вещества, идентифицированного какTFA соль (2-метоксиэтил)амида 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а] пиридин-6-карбоновой кислоты. 1 Н ЯМР (d6-ДМСО, 400 МГц): 2,51 (с, 3 Н), 3,32 (с, 3 Н), 3,52 (м, 4 Н), 6,89 (д, 1 Н, J=5,6 Гц), 7,42 (д,1 Н, J=8,1 Гц), 7,45 (ушир.с, 1 Н), 7,92 (м, 4 Н), 8,33 (д, 1 Н, J=5,6 Гц), 8,81 (м, 1 Н), 9,70 (с, 1 Н). МС(ESP+) 404,7 (М+1). Пример 60. ([1,4]Диоксан-2-илметил)амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил) имидазо[1,2-а]пиридин-6-карбоновой кислоты. В колбу добавляют 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6- 29010426 карбоновую кислоту (0,14 4 ммоль; см. пример 55 для ее получения) с ДМФА(1 мл). Реакционную смесь перемешивают до тех пор, пока не растворятся все вещества. Затем добавляют HATU (0,201 ммоль), убеждаясь, что растворились все вещества. После этого добавляют DIEA (0,720 ммоль). Эту смесь оставляют при перемешивании в течение 10 мин. Затем добавляют [1,4]диоксан-2-илметиламин (0,202 ммоль) и реакционную смесь перемешивают в течение 2 час, концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (540% CH3CN:H2O с 0,1% TFA), получая 30,0 мг твердого вещества, идентифицированного как TFA соль ([1,4]диоксан-2-илметил)амида 3-(2-аминопиримидин-4-ил)-2-(6 метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбоновой кислоты. 1 Н ЯМР (d6-ДМСО, 400 МГц): 2,52 (с, 3 Н), 3,30 (м, 1 Н), 3,37 (м, 2 Н), 3,51 (м, 1 Н), 3,62 (м, 1 Н), 3,68MC(ESP+) 446,3 (М+1). Пример 61. Метиловый эфир 3-[3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2 а]пиридин-6-карбонил]аминопропионовой кислоты. В колбу добавляют 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6 карбоновую кислоту (0,144 ммоль; см. пример 55 для ее получения) с ДМФА (1 мл). Реакционную смесь перемешивают до тех пор, пока не растворятся все вещества. Затем добавляют HATU (0,201 ммоль), убеждаясь, что растворились все вещества. После этого добавляют DIEA (0,720 ммоль). Эту смесь оставляют при перемешивании на 10 мин. Затем добавляют метиловый эфир 3-аминопропионовой кислоты(0,202 ммоль), реакционную смесь перемешивают в течение 2 ч, концентрируют в вакууме и очищают,используя препаративную ВЭЖХ (540% CH3CN:H2O с 0,1% TFA), получая 27,3 мг твердого вещества,идентифицированного как TFA соль метилового эфира 3-[3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6-карбонил]аминопропионовой кислоты. 1 Н ЯМР (d6-ДМСО, 400 МГц): 2,51 (с, 3 Н), 2,68 (т, 2 Н, J=7,4 Гц), 3,57 (кв., 2 Н, J=6,8 Гц), 3,66 (с,3 Н), 6,88 (д, 1 Н, J=5,4 Гц), 7,42 (д, 1 Н, J=7,4 Гц), 7,43 (ушир.с, 1 Н), 7,91 (м, 4 Н), 8,31 (д, 1 Н, J=6,0 Гц),8,84 (дд, 1 Н, J=5,4, 5,4 Гц), 9,71 (с, 1 Н).MC(ESP+) 432,2 (М+1). Пример 62. ([1,4]диоксан-2-илметил)амид 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил) имидазо[1,2-а]пиридин-6-карбоновой кислоты. В колбу добавляют 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6 карбоновую кислоту (0,144 ммоль; см. пример 55 для ее получения) с ДМФА (1 мл). Реакционную смесь перемешивают до тех пор, пока не растворятся все вещества. Затем добавляют HATU (0,201 ммоль), убеждаясь, что растворились все вещества. После этого добавляют DIEA (0,720 ммоль). Эту смесь оставляют при перемешивании на 10 мин. Затем добавляют (не симм.)-N,N-диметилгидразин (0,202 ммоль) и реакционную смесь перемешивают в течение 2 ч, концентрируют в вакууме и очищают, используя препаративную ВЭЖХ (54 0% CH3CN:H2O с 0,1% TFA), получая 9,8 мг твердого вещества, идентифицированного как TFA соль ([1,4]диоксан-2-илметих)амида 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин 2-ил)имидазо[1,2-а]пиридин-6-карбоновой кислоты. 1 Н ЯМР (d6-ДМСО, 400 МГц): 2,52 (с, 3 Н), 2,74 (с, 6 Н), 6,92 (д, 1 Н, J=5,6 Гц), 7,43 (д, 1 Н, J=7,4 Гц),7,57 (ушир.с, 1 Н), 7,92 (м, 4 Н), 8,32 (д, 1 Н, J=5,6 Гц), 9,70 (с, 1 Н).MC(ESP+) 389,2 (М+1). Пример 63. N-[3-(2-Аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6 карбонил]метансульфонамид. В колбу добавляют 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6 карбоновую кислоту (60 мг, 0,173 ммоль; см. пример 55 для ее получения) с ДМФА(1 мл). Реакционную смесь перемешивают до тех пор, пока не растворятся все вещества. Затем добавляют HATU (92 мг, 0,242 ммоль) убеждаясь, что растворились все вещества. После этого добавляют DIEA (150 мкл, 0,865 ммоль). Эту смесь оставляют при перемешивании на 10 мин. Затем добавляют метилсульфонамин (20 мг, 0,207 ммоль), реакционную смесь перемешивают в течение 2 ч и анализируют, используя ВЭЖХ. Реакционную смесь очищают, используя препаративную ВЭЖХ (540% CH3CN:H2O с 0,1% TFA). (Примеси по данным ЯМР). 1 Н ЯМР (d6-ДМСО, 400 МГц): 2,47 (с, 3 Н), 3,45 (с, 3 Н), 6,88 (д, 1 Н, J=5,7 Гц), 7,17 (ушир.с, 1 Н), 7,36[1,2-а]пиридин-6-карбоновой кислоты. В колбу добавляют 3-(2-аминопиримидин-4-ил)-2-(6-метилпиридин-2-ил)имидазо[1,2-а]пиридин-6 карбоновую кислоту (50 мг, 0,144 ммоль; см. пример 55 для ее получения) с ДМФА(1 мл). Реакционную смесь перемешивают до тех пор, пока не растворятся все вещества. Затем добавляют HATU (77 мг, 0,201 ммоль), убеждаясь, что весь материал растворился. После этого добавляют дополнительно DIEA (180 мкл, 0,720 ммоль). Эту смесь оставляют при перемешивании на 10 мин. Затем добавляют 2-тиофен-2- 30
МПК / Метки
МПК: C07D 237/00, A01P 15/00, C07D 239/00, A61K 31/535
Метки: применения, получения, способы, имидазопиридины
Код ссылки
<a href="https://eas.patents.su/30-10426-imidazopiridiny-i-sposoby-ih-polucheniya-i-primeneniya.html" rel="bookmark" title="База патентов Евразийского Союза">Имидазопиридины и способы их получения и применения</a>
Предыдущий патент: Способ получения диарилкарбоната высокой чистоты
Следующий патент: Средство для лечения заболеваний предстательной железы
Случайный патент: Система мгновенного обмена сообщениями