Система дезактивации активного вещества в трансдермальном средстве
Формула / Реферат
1. Система дезактивации активного вещества в трансдермальном средстве доставки, включающая по меньшей мере одну подложку, на поверхность которой нанесено адгезивное покрытие, и один или более следующих компонентов, содержащихся, по меньшей мере, в адгезивном покрытии или на его поверхности, или в первой подложке или на её поверхности, или их любое сочетание:
(а) по меньшей мере один мономер и, возможно, по меньшей мере один инициатор,
(б) по меньшей мере один сшивающий агент и, возможно, по меньшей мере один инициатор,
(в) по меньшей мере один агент, дезактивирующий активное вещество.
2. Система по п.1, отличающаяся тем, что она дополнительно включает вторую подложку, которая способна приклеиваться к адгезивному покрытию на первой подложке.
3. Система по п.2, отличающаяся тем, что адгезивное покрытие расположено на одной стороне второй подложки.
4. Система по п.3, отличающаяся тем, что она дополнительно включает один или более следующих компонентов, содержащихся, по меньшей мере, в адгезивном покрытии на второй подложке или на его поверхности, или во второй подложке или на её поверхности, или любое их сочетание:
(а) по меньшей мере один мономер и, возможно, по меньшей мере один инициатор,
(б) по меньшей мере один сшивающий агент и, возможно, по меньшей мере один инициатор,
(в) по меньшей мере один агент, дезактивирующий активное вещество.
5. Система по п.3, отличающаяся тем, что по меньшей мере одна из первой и второй подложек является жёсткой.
6. Система по п.3, отличающаяся тем, что и первая, и вторая подложки являются жёсткими.
7. Система по п.5, отличающаяся тем, что по меньшей мере одна из первой и второй подложек не является плоской.
8. Система по п.6, отличающаяся тем, что и первая, и вторая подложки не являются плоскими.
9. Система по п.7, отличающаяся тем, что по меньшей мере одна из первой и второй подложек имеет углубление, конфигурация и размеры которого позволяют разместить в нём трансдермальное средство доставки.
10. Система по п.1, отличающаяся тем, что первая подложка характеризуется одним или несколькими из следующих свойств:
(а) по существу непроницаема для растворителей;
(б) по существу не набухает в растворителях;
(в) является стойкой к разрыву и
(г) является стойкой к разрезанию.
11. Система по п.1, отличающаяся тем, что содержащийся в ней компонент или компоненты включают мономер.
12. Система по п.11, отличающаяся тем, что содержащийся в ней компонент или компоненты включают по меньшей мере один сомономер.
13. Система по п.11, отличающаяся тем, что содержащиеся в ней компоненты дополнительно включают инициатор.
14. Система по п.11, отличающаяся тем, что содержащиеся в ней компоненты дополнительно включают по меньшей мере один сшивающий агент.
15. Система по п.14, отличающаяся тем, что содержащиеся в ней компоненты дополнительно включают по меньшей мере один агент, дезактивирующий активное вещество.
16. Система по п.15, отличающаяся тем, что агент, дезактивирующий активное вещество, представляет собой m -опиоидный антагонист.
17. Система по п.1, отличающаяся тем, что она дополнительно включает по меньшей мере один субстрат для адгезива, расположенный с возможностью снятия на адгезивном покрытии на первой подложке таким образом, чтобы этот субстрат для адгезива можно было легко удалить с адгезивного покрытия.
18. Набор, включающий трансдермальное средство доставки, которое содержит по меньшей мере один активный агент, и систему для дезактивации активного агента, которая включает:
(i) по меньшей мере одну подложку, на одной стороне которой имеется адгезивное покрытие, и
(ii) один или несколько из следующих компонентов, содержащихся, по меньшей мере, в адгезивном покрытии или на его поверхности, или в первой подложке или на её поверхности, или любое сочетание этих компонентов:
(а) по меньшей мере один мономер и, возможно, по меньшей мере один инициатор,
(б) по меньшей мере один сшивающий агент и, возможно, по меньшей мере один инициатор,
(в) по меньшей мере один агент, дезактивирующий активное вещество.
19. Набор по п.18, отличающийся тем, что он дополнительно включает коробку, в которой находится трансдермальное средство доставки, а трансдермальная система устранения этого средства прикреплена с возможностью снятия на наружной части коробки.
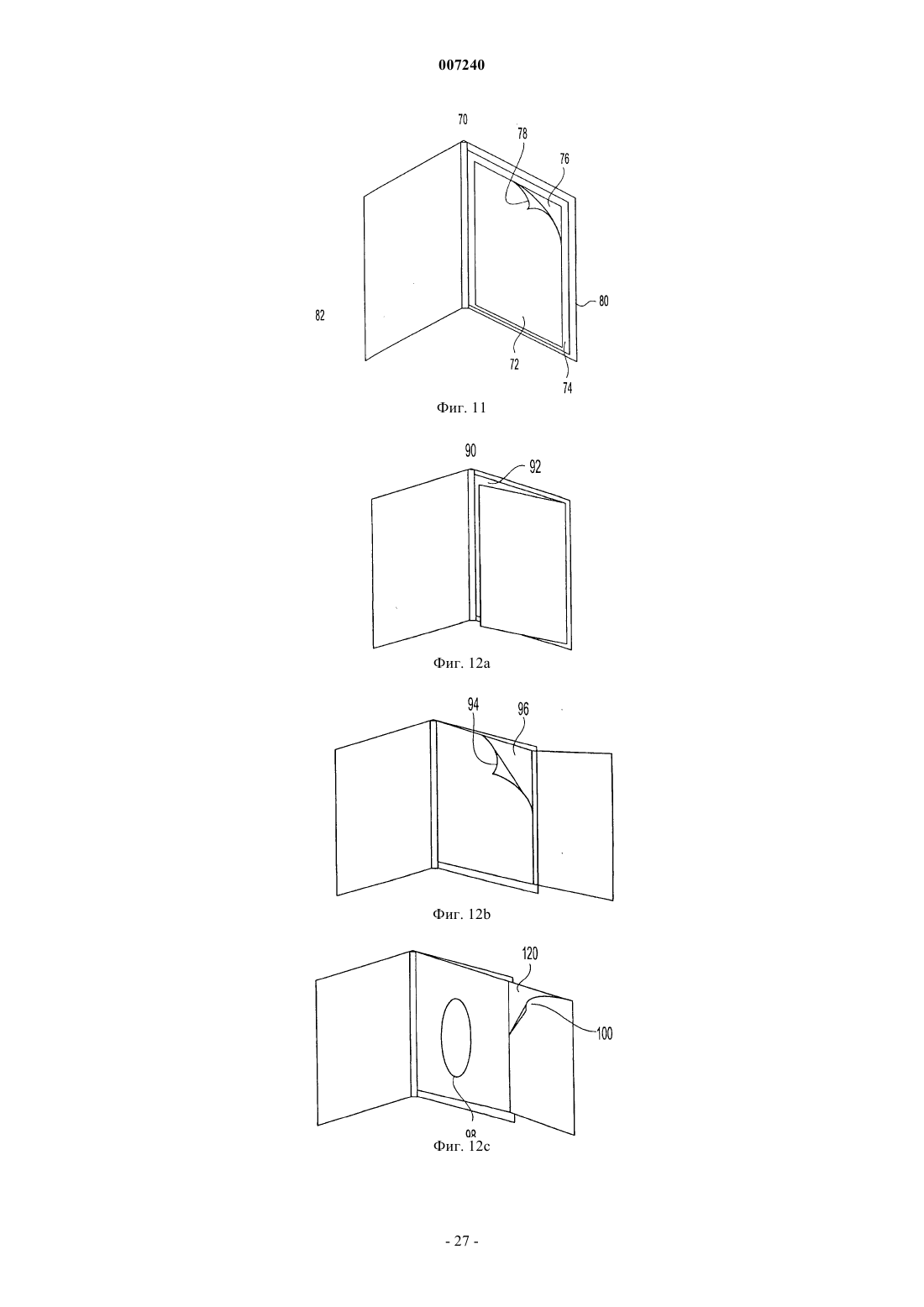
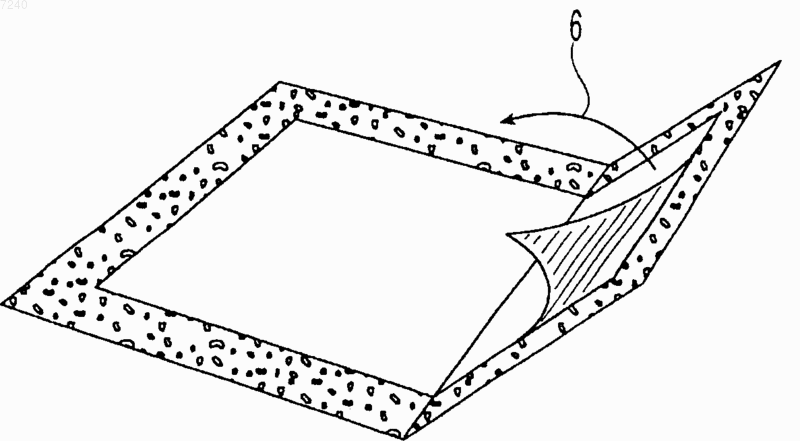
20. Набор по п.19, отличающийся тем, что один край первой подложки и один край второй подложки соединены с образованием буклета.
21. Набор по п.20, отличающийся тем, что каждая из первой и второй подложек являются жёсткими и неплоскими.
22. Набор по п.21, отличающийся тем, что по меньшей мере одна из первой и второй подложек имеет углубление для размещения в нём трансдермального средства доставки.
23. Набор по п.20, отличающийся тем, что трансдермальное средство доставки, первая подложка и вторая подложка имеют одну сторону, размер которой имеет примерно ту же величину, что и одна сторона других из этих элементов.
24. Набор, включающий трансдермальное средство доставки, содержащее по меньшей мере одно активное вещество и по меньшей мере первую жёсткую подложку, содержащую адгезивное покрытие на по меньшей мере одной стороне.
25. Набор по п.24, отличающийся тем, что он дополнительно содержит вторую жёсткую неплоскую подложку, содержащую адгезивное покрытие по меньшей мере на одной стороне.
26. Набор по п.24, отличающийся тем, что первая подложка и вторая подложка имеют каждая углубление такой конфигурации и таких размеров, которые позволяют разместить в нём трансдермальное средство доставки, причём адгезивные покрытия на первой и второй подложках расположены по меньшей мере на части первой подложки и на части второй подложки, которые ограничивают углубления.
27. Набор по п.24, отличающийся тем, что он дополнительно включает один или несколько из следующих компонентов, содержащихся по меньшей мере в первой подложке или на её поверхности, во второй подложке или на её поверхности, в адгезивном покрытии по меньшей мере на одной стороне первой подложки, в адгезивном покрытии по меньшей мере на одной стороне второй подложки или в любом сочетании этих элементов:
(а) по меньшей мере один мономер и, возможно, по меньшей мере один инициатор,
(б) по меньшей мере один сшивающий агент и, возможно, по меньшей мере один инициатор,
(в) по меньшей мере один агент, дезактивирующий активное вещество.
28. Набор, включающий трансдермальное средство доставки, содержащее бупренорфин или любую фармацевтически приемлемую форму или любое фармацевтически приемлемое производное бупренорфина и по меньшей мере одну подложку, содержащую на одной стороне адгезивное покрытие.
29. Набор, включающий трансдермальное средство доставки, содержащее фентанил или любые фармацевтически приемлемые форму или производное фентанила и по меньшей мере одну подложку, содержащую на одной стороне адгезивное покрытие.
30. Набор, включающий трансдермальное средство доставки, содержащее оксикодон или любые фармацевтически приемлемые форму или производное оксикодона и по меньшей мере одну подложку, содержащую на одной стороне адгезивное покрытие.
31. Система дезактивации активного вещества в трансдермальном средстве доставки, включающая по меньшей мере первую подложку, содержащую адгезивное покрытие на одной её стороне, причём адгезив представляет собой клей на основе силиконов.
32. Система дезактивации активного вещества в трансдермальном средстве доставки, включающая по меньшей мере первую подложку, содержащую адгезивное покрытие на одной её стороне, причём адгезив представляет собой клей на основе акрилатов.
33. Способ дезактивации активного вещества в трансдермальном средстве доставки, включающий присоединение трансдермального средства доставки к адгезивному покрытию на первой подложке системы устранения трансдермального средства доставки по п.1.
34. Способ дезактивации активного вещества в трансдермальном средстве доставки, включающий присоединеэшх трансдермального средства доставки к адгезивному покрытию на одной стороне первой подложки, причём, по меньшей мере, в адгезивном покрытии на первой подложке или на его поверхности, или в первой подложке или на её поверхности, или в любом сочетании этих элементов содержатся один или несколько из следующих компонентов:
(а) по меньшей мере один мономер и, возможно, по меньшей мере один инициатор,
(б) по меньшей мере один сшивающий агент и, возможно, по меньшей мере один инициатор,
(в) по меньшей мере один агент, дезактивирующий активное вещество,
присоединение трансдермального средства доставки к адгезивному покрытию, расположенному на одной стороне второй подложки, при этом вторая подложка способна приклеиваться к адгезивному покрытию на первой подложке, причём, по меньшей мере, в адгезивном покрытии на второй подложке или на его поверхности, или во второй подложке или на её поверхности, или в любом сочетании этих элементов содержатся один или несколько из следующих компонентов:
(а) по меньшей мере один мономер и, возможно, по меньшей мере один инициатор,
(б) по меньшей мере один сшивающий агент и, возможно, по меньшей мере один инициатор
(в) по меньшей мере один агент, дезактивирующий активное вещество.
35. Способ дезактивации активного вещества в трансдермальном средстве доставки, включающий
использование первой жёсткой неплоской подложки, содержащей по меньшей мере на одной стороне адгезивное покрытие;
использование второй жёсткой неплоской подложки, содержащей по меньшей мере на одной стороне адгезивное покрытие,
причём первая подложка и вторая подложка каждая ограничивают углубление, конфигурация и размеры которого позволяют разместить в нём трансдермальное средство для доставки, и адгезивное покрытие на первой и второй подложках расположены по меньшей мере на части первой подложки и на части второй подложки, которые ограничивают углубления;
размещение трансдермального средства доставки в углублении на первой подложке и
помещение второй подложки над первой подложкой и выравнивание углубления на второй подложке так, чтобы оно располагалось над трансдермальным средством доставки, и
присоединение первой подложки ко второй подложке с целью инкапсуляции, иммобилизации и/или изоляции трансдермального средства доставки.
36. Система дезактивации активного вещества в трансдермальном средстве доставки, включающая по меньшей мере первую подложку, содержащую адгезивное покрытие на одной стороне, и один или несколько из следующих компонентов, содержащихся, по меньшей мере, в адгезивном покрытии, на его поверхности или в первой подложке или на её поверхности, или в любом сочетании этих элементов:
(а) по меньшей мере один мономер и, возможно, по меньшей мере один инициатор,
(б) по меньшей мере один сшивающий агент и, возможно, по меньшей мере один инициатор,
(в) по меньшей мере один не m -опиоидный дезактивирующий агент.
37. Система по п.36, отличающаяся тем, что она содержит вторую подложку, способную приклеиваться к адгезивному покрытию на первой подложке.
38. Система по п.37, отличающаяся тем, что адгезивное покрытие расположено на одной стороне второй подложки.
39. Система по п.38, отличающаяся тем, что она дополнительно содержит один или несколько из следующих компонентов, содержащихся, по меньшей мере, в адгезивном покрытии на второй подложке или на его поверхности, или во второй подложке или на её поверхности, или в любом сочетании этих элементов:
(а) по меньшей мере один мономер и, возможно, по меньшей мере один инициатор,
(б) по меньшей мере один сшивающий агент и, возможно, по меньшей мере один инициатор,
(в) по меньшей мере один не m -опиоидный дезактивирующий агент.
40. Система по п.38, отличающаяся тем, что по меньшей мере одна из первой и второй подложек являются жёсткими.
41. Система по п.40, отличающаяся тем, что и первая подложка, и вторая подложка являются жёсткими.
42. Система по п.40, отличающаяся тем, что по меньшей мере одна из первой и второй подложек не являются плоскими.
43. Система по п.41, отличающаяся тем, что и первая подложка, и вторая подложка не являются плоскими.
44. Система по п.42, отличающаяся тем, что по меньшей мере одна из первой и второй подложек ограничивает углубление, конфигурация и размеры которого позволяют разместить в нём трансдермальное средство доставки.
45. Система по п.36, отличающаяся тем, что первая подложка характеризуется одним или несколькими из следующих свойств:
(а) по существу непроницаема для растворителей,
(б) по существу не набухает в растворителях,
(в) является стойкой к разрыву и
(г) является стойкой к разрезанию.
46. Система по п.36, отличающаяся тем, что содержащийся в ней компонент или компоненты включают мономер.
47. Система по п.46, отличающаяся тем, что содержащийся в ней компонент или компоненты включают по меньшей мере один сомономер.
48. Система по п.46, отличающаяся тем, что содержащиеся в ней компоненты дополнительно включают инициатор.
49. Система по п.48, отличающаяся тем, что содержащиеся в ней компоненты дополнительно включают по меньшей мере один сшивающий агент.
50. Система по п.49, отличающаяся тем, что содержащиеся в ней компоненты дополнительно включают по меньшей мере один не-m -опиоидный дезактивирующий агент.
Текст
007240 Область, к которой относится изобретение Данное изобретение относится к системе для предотвращения, ингибирования и/или уменьшения намеренного и/или непреднамеренного неправильного использования или злоупотребления трансдермальным средством доставки (TDD), содержащим активный фармацевтический агент, такой как опиоид. Данное изобретение относится к способу устранения TDD и/или предотвращения неправильного использования TDD или любого ингредиента TDD или злоупотребления TDD. Предпосылки создания изобретения Трансдермальные дозированные формы представляют собой удобные дозированные формы для доставки многих различных терапевтически активных агентов, включая, но не ограничиваясь этим, фентанил, бупренорфин, эторфины и другие высоко активные наркотики. Другие терапевтически активные агенты, которые могут быть доставлены при помощи трансдермальной системы доставки, включают, но не ограничиваются этим, противорвотные средства (скополамин), сердечно-сосудистые средства (нитраты и клонидин), гормоны (эстроген и тестостерон), никотин, витамины, диетические добавки и т.д. Наиболее распространнная трансдермальная дозированная форма является диффузионной трансдермальной системой (трансдермальный пластырь), использующей или жидкий резервуар, или матриксную систему, содержащую лекарство в клее. Другие трансдермальные дозированные формы включают,но не ограничиваются этим, топические гели, лосьоны, мази, системы и средства для доставки через слизистую оболочку и ионофоретические (электрическая диффузия) системы для доставки. Трансдермальные дозированные формы особенно пригодны для пролонгированного и непрерывного высвобождения активных агентов. Однако многие дозированные формы, и особенно формы для пролонгированного и непрерывного высвобождения активного агента(-ов), содержат большие количества активного агента(-ов), часто во много раз превышающие действительную абсорбированную дозу. Часто дозированная форма содержит избыток активного агента(-ов) или доставляет меньшее количество активного агента субъекту, чем количество этого агента, содержащееся в форме. Это приводит к тому, что большая часть активного агента остатся в дозированной форме после использования. И неиспользованная дозированная форма, и часть активного агента, которая остатся в лекарственной форме после использования, могут быть применены, хотя это запрещено, особенно, если активный агент представляет собой наркотик или контролируемое вещество. Например, использованные дозированные формы, содержащие избыток или неиспользованные опиоиды, могут быть применены при их жевании или экстракции лицом, злоупотребляющим лекарством. Даже тщательное устранение использованных дозированных форм может быть не совсем эффективным для предотвращения злоупотребления лекарством, особенно, в случаях неполного или частичного несоблюдения инструкции. Патент CШA5 804 315, Cubbage et. al., относится к системе устранения трансдермального пластыря, содержащего лекарство, такое как никотин, представляющего собой гибкую стойкую к отрыву подложку с покрытием из адгезива. Использованный трансдермальный пластырь приклеивают к подложке для того, чтобы осуществить инкапсулирование и предотвратить доступ к трансдермальному пластырю. Согласно этому патенту Cubbage предпочтительными являются адгезивы на основе каучука. Патенты США 5 149 538, Granger et. al, и 5 236 714, Lee et. al., относятся к дозированным формам для трансдермальной доставки опиоидов, которые устойчивы к неправильному использованию. В этих патентах предусмотрены соответствующие трансдермальные пластыри с опиоидным антагонистом, который предназначен для экстрагирования из пластыря, если пластырь жуют или подвергают экстракции. Опиоидный антагонист предназначен для блокирования любых проявлений эйфории, которые хотят получить при злоупотреблении дозированной формой. Непреднамеренное и/или намеренное использование и/или злоупотребление трансдермальных средств доставки представляет значительную проблему для здоровья. Таким образом, существует необходимость в системе устранения трансдермальных средств доставки, которая менее пригодна для злоупотребления ею, чем известные системы. Сущность изобретения Один вариант изобретения относится к системе TDD, содержащей, по меньшей мере, одну подложку с адгезионным покрытием на одной е поверхности и один или более следующих компонентов, содержащихся, по меньшей мере, в составе адгезионного покрытия или на его поверхности или в составе первой подложки или на е поверхности, или в любой комбинации перечисленных мест:(а) мономер и, возможно, по меньшей мере один сомономер;(б) инициатор и, возможно, по меньшей мере один соинициатор;(в) по меньшей мере один сшивающий агент и(г) по меньшей мере один агент, вызывающий деактивацию активного агента, например, опиоидный антагонист для применения в TDD, содержащем опиоидный агонист. Другой вариант изобретения относится к системе устранения TDD, дополнительно содержащей один или более следующих компонентов, содержащихся, по меньшей мере, в составе адгезионного покрытия или на его поверхности или в составе второй подложки или на е поверхности, или в любой комбинации этих мест:(а) мономер и, возможно, по меньшей мере один сомономер;(б) инициатор и, возможно, по меньшей мере один соинициатор;(в) по меньшей мере один сшивающий агент и(г) по меньшей мере один агент, деактивирующий активный агент. Дополнительный аспект данного изобретения относится к набору, содержащему трансдермальное средство доставки, включающее, по меньшей мере, один активный агент и систему для устранения TDD,причм система для устранения TDD включает:(i) по меньшей мере, первую подложку, содержащую адгезионное покрытие на одной е поверхности;(ii) один или более следующих компонентов, содержащихся, по меньшей мере, в составе адгезионного покрытия или на его поверхности, или в составе первой подложки или на е поверхности, или в любой комбинации этих мест:(а) мономер и, возможно, по меньшей мере один сомономер;(б) инициатор и, возможно, по меньшей мере один соинициатор;(в) по меньшей мере один сшивающий агент и(г) по меньшей мере один агент, деактивирующий активный агент. Согласно ещ одному аспекту система для устранения TDD содержит, по меньшей мере, один не-опиоидный деактивирующий агент, включнный в состав адгезионного покрытия или на его поверхности, или в составе первой и/или второй подложки или на их поверхности, или в любую комбинацию этих мест. Другой аспект изобретения относится к набору, включающему трансдермальное средство доставки,содержащее, по меньшей мере, один активный агент; и систему для устранения TDD, содержащую, по меньшей мере, одну жсткую неплоскую подложку, содержащую адгезионное покрытие на, по меньшей мере, одной поверхности. Ещ один аспект изобретения относится к набору, включающему трансдермальное средство доставки, содержащее бупренорфин или любую фармацевтически приемлемую форму или производное бупренорфина, и систему для устранения TDD, содержащую по меньшей мере одну подложку, имеющую адгезионное покрытие на одной е поверхности. Ещ один аспект изобретения относится к набору, включающему трансдермальное средство доставки, содержащее фентанил или любую фармацевтически приемлемую форму или производное фентанила, и систему для устранения TDD, содержащую по меньшей мере одну подложку, имеющую адгезионное покрытие на одной е поверхности. Ещ один аспект изобретения относится к набору, включающему трансдермальное средство доставки, содержащее оксикодон или любую фармацевтически приемлемую форму или производное оксикодона, и систему для устранения TDD, содержащую по меньшей мере одну подложку, имеющую адгезионное покрытие на одной е поверхности. Другой аспект данного изобретения относится к системе для устранения TDD, включающей по меньшей мере одну подложку, имеющую адгезионное покрытие на одной е поверхности, причм адгезив представляет собой клей на основе силикона. Ещ один аспект изобретения относится к системе для устранения TDD, включающей по меньшей мере одну подложку, имеющую адгезионное покрытие на одной е поверхности, причм адгезив представляет собой клей на основе акрилатов. Ещ один аспект изобретения относится к системе для устранения TDD и/или набору, включающему эту систему, причм первая подложка системы для устранения TDD обладает одним или несколькими следующими свойствами:(а) является практически непроницаемой для растворителя;(б) практически не набухает в растворителе;(в) является практически стойкой к разрыву и(г) является практически стойкой к надрезу. Краткое описание рисунков На каждой из фиг. 1A-1D показана система для устранения TDD согласно данному изобретению,имеющая участок для иммобилизации и изоляции одного TDD, такого как пластырь, или множестваTDD. На фиг. 2 А-2 С показаны TDD резервуарного типа, полимерно-матриксного типа или типа, содержащего лекарство в адгезиве, соответственно. Фиг. 3 представляет изображение системы для устранения TDD, содержащую смесь мономеров,инициатор и, возможно, сшивающий агент, а также деактивирующий агент, возможно, в смеси с агентом,вызывающим разложение, на том же участке. Фиг. 4 отображает систему для устранения TDD, содержащую деактивирующий агент, возможно, в смеси с агентом, вызывающим разложение, на первом участке и смесь мономеров, инициатор и, возможно, сшивающий агент на втором участке. На фиг. 5-10 показано количество бупренорфина (BUP), экстрагируемого из TDD, изображнного-2 007240 на фиг. 2 В и доступного для употребления путм экстракции дистиллированной водой, этилацетатом,этанолом, этиловым эфиром, ацетоном и метанолом, соответственно, TDD была иммобилизована и изолирована в системе для устранения TDD с бупренорфином, изображнной на фиг. 1B. На фиг. 11 изображена окклюзионная система для устранения TDD согласно данному изобретению,сврнутая в книгу, в форме листа или множества листьев, каждая имеет участок для иммобилизации и изоляции одного TDD, такого как пластырь, или множества TDD. На фиг. 12A-D представлена окклюзионная система для устранения TDD в соответствии с данным изобретением, сврнутая в книгу, в форме множества сложенных вдвое листьев, каждая такая система имеет участок для иммобилизации и изоляции одного TDD, такого как пластырь, или множества TDD. На фиг. 13 изображен набор согласно изобретению, включающий коробку, содержащую одно или более трансдермальных средств доставки и систему для устранения TDD в виде буклета, прикреплнного к внешней стороне коробки. На фиг. 14 показана система для устранения TDD согласно данному изобретению, содержащая две жсткие неплоские подложки. Определения Выражение трансдермальное средство доставки или TDD относится к любому средству, которое при контактировании с кожей пациента может доставлять через кожу терапевтически эффективное количество любого биологически активного агента, такого как фармакологическое соединение, например, опиоид, через кожу в большой круг кровообращения. Термин опиоид, используемый в данном описании отдельно, относится к соединению с активностью агониста -опиоидного рецептора. Используемые термины неопиоид и неопиоидный агонист относятся к активному агенту,который связывается, возможно, стереоспецифически с любым к-опиоидным рецептором, -опиоидным рецептором и/или ORL-1-опиоидным рецептором, но не с любым -опиоидным рецептором, и обеспечивает активность агониста. Используемый в данном описании термин деактивирующий агент является синонимом термина агент, вызывающий разложение и включает понятие инактивирующий агент. Используемый термин неопиоидный деактивирующий агент относится к агенту, который деактивирует или разлагает неопиоидный агонист, но который не деактивирует и не разлагает опиоидный агонист, определнный выше. Следует, конечно, иметь в виду, что, если не указано обратное, любая ссылка на любое фармацевтическое соединение в данном описании относится не только к этому фармацевтическому соединению,то есть к так называемой свободной форме этого соединения, но также и к фармацевтически приемлемым производным этого соединения, например, фармацевтически приемлемым солям этого соединения,основным формам этого соединения и их смесям, а также к смесям свободной формы и любого производного(-ых) и стереоизомеров этого соединения. Выражение фармацевтически приемлемая соль, используемое в данном описании, например, соль опиоида, относится к соли, образованной кислотой и основной азотсодержащей группой опиоида. Предпочтительные соли включают, но не ограничиваются этим, сульфаты, цитраты, ацетаты, оксалаты, хлориды, бромиды, иодиды, нитраты, бисульфаты, фосфаты, кислые фосфаты, изоникотинаты, лактаты, салицилаты, кислые цитраты, тартраты, олеинаты, таннаты, пантотенаты, битартираты, аскорбаты, сукцинаты, малеаты, гентисинаты, фумараты, глюконаты, глюкоронаты, сахараты, формиаты, бензоаты, глутаматы, метансульфонаты, этансульфонаты, бензосульфонаты, п-толуол-сульфонаты и памоаты (то есть 1,1'-метилен-бис-(2-гидрокси-3-нафтоаты. Термин основная форма, например, опиоида, относится к соли, полученной из опиоида, содержащего кислотную функциональную группу, такую как карбоксильную или сульфоновую, и фармацевтически приемлемого неорганического или органического основания. Подходящие основания включают, но не ограничиваются этим, гидроокиси щелочных металлов,таких как натрий, калий, литий; гидроокиси щлочно-земельных металлов, таких как кальций и магний,гидроокиси других металлов, таких как алюминий и цинк, гидроокись аммония и органические амины,такие как незамещнные или гидроксилзамещнные моно-, ди- или триалкиламины, дициклогексиламин,трибутиламин, пиридин, N-метил-, N-этил-амин, диэтиламин, триэтиламин, моно-, бис- или трис-(2 гидрокси-низший алкиламины), такие как моно-, бис- или трис-(2-гидроксиэтил)амин, 2-гидрокситрет.бутиламин или трис-(гидроксиметил)метиламин, N,N-ди-низший алкил-N-(гидрокси-низший алкил)амины, такие как N,N-диметил-N-(2-гидроксиэтил)амин или три-(2-гидроксиэтил)амин, N-метил-Dглюкамин, и аминокислоты, такие как аргинин, лизин и т.п. Термин по существу, используемый в данном описании, относящийся к прилагательному или определению, следующему сразу же за ним, означает, что прилагательное или определение применимо, по меньшей мере, примерно на 95%, предпочтительно, по меньшей мере, примерно на 98%, более предпочтительно, по меньшей мере, примерно на 99%, например, по меньшей мере, примерно на 99,9%, по от-3 007240 ношению к существительному или местоимению, которое модифицирует прилагательное или определение. Термин по существу может использоваться попеременно с термином полностью. Выражение по существу нет или по существу не, используемое для модификации прилагательного или определения, следующего сразу за ним, означает, что прилагательное или определение применимо не более, чем примерно на 5%, предпочтительно, не более, чем примерно на 2%, более предпочтительно, не более, чем примерно на 1%, например, не более, чем примерно на 0,1%, по отношению к существительному или местоимению, которое модифицирует прилагательное или определение. Выражение по существу не может использоваться попеременно с выражениями полностью нет или полностью не. Термин примерно, используемый в отношении численной величины или интервала, означает плюс или минус 10% от численной величины или интервала. Используемый термин сополимер включает полимер, содержащий, по меньшей мере, два разных мономерных звена. Таким образом, полимерная цепь, состоящая из трх разных мономерных звеньев(известная также как тройной сополимер), также входит в понятие сополимер, как и полимеры, содержащие более трх различных мономерных звеньев. Термин олигомер, используемый в данном описании, включает соединения, содержащие повторяющиеся мономерные звенья, как полимер или сополимер, но имеющие низкий молекулярный вес, когда соединение не считается полимерным. Подробное описание предпочтительных вариантов изобретения Система устранения по изобретению может быть использована для устранения любого типа TDD независимо от конструкции или формы этого средства и независимо от вида активного агента или агентов, содержащихся в этом средстве. Активные агенты, которые обычно вводятся при помощи TDD,включают, но не ограничиваются этим, опиоиды, неопиоиды, противорвотные средства (скополамин),сердечно-сосудистые агенты (нитраты и клонидин), гормоны (эстроген и тестостерон), никотин, витамины, диетические добавки. Для целей иллюстрации в данном описании ссылка делается прежде всего наTDD, содержащие опиоидный анальгетик в качестве фармацевтически активного агента. 1. Трансдермальные средства доставки. Типичные TDD включают фармацевтическое соединение, такое как, по меньшей мере, один опиоид, и, возможно, по меньшей мере, один антагонист опиоида в количестве, достаточном для ингибирования проявлений эйфории от прима опиоида в случае, когда опиоид и антагонист опиоида вводятся, например, перорально, внутривенно, трансбуккально, через нос, парентерально, ректально и/или вагинально млекопитающему, обычно человеку. При контакте с кожей пациента типичные TDD позволяют осуществить трансдермальное введение опиоида, но или а) позволяют трансдермально ввести только небольшое количество антагониста опиоида, которое неэффективно для ингибирования анальгетического эффекта опиоида, или б) не позволяют трансдермально ввести антагонист опиоида. Однако, если такиеTDD используют для доставки опиоида не трансдермальным путм, а, например, внутривенно, трансбуккально, через нос, перорально, парентерально, ректально и/или вагинально, тогда антагонист опиоида ослабляет или ингибирует проявления эйфории от прима опиоида. Предпочтительно, такие TDD ингибируют проявления эйфории от прима опиоида, если используются иначе, чем трансдермально, независимо от того, использовалось ли ранее это средство для лечения или профилактики боли. Хотя это не требуется, TDD могут быть устроены так, чтобы они удерживали человека, злоупотребляющего опиоидами, от или а) отделения антагониста опиоида от опиоида или б) выделения опиоида изTDD и затем прима опиоида другим путм, таким как (без ограничения) пероральный, парентеральный,назальный, внутривенный, трансбуккальный, или путм ингаляции паров, то есть таким путм, который приводит к быстрому достижению эйфории, также известным как вспышка, который предпочитают лица, злоупотребляющие наркотиками. Например, если такой человек попытается экстрагировать опиоид из TDD при помещении его в растворитель, то и антагонист опиоида также будет экстрагироваться, при этом образуется смесь опиоида и антагониста опиоида. Если смесь опиоида и антагониста опиоида вводится не трансдермальным путм, а другим, тогда антагонист опиоида будет проявлять сво антагонистическое действие по ингибированию проявлений эйфории, вызванных примом опиоида. Любое средство, известное специалистам как пригодное для трансдермальной доставки терапевтического агента пациенту, может квалифицироваться как TDD. Например, TDD может быть TDD с резервуаром, TDD полимерно-матриксного типа или TDD, содержащим лекарство в составе адгезива (см., например, H.S. Tan and W.R. Pfidter, Pressure Sensitive Adhesives for Transdermal Drag Delivery Systems,PSTT, vol.2,2, Feb. 1999, p.p. 60-69, включена в качестве ссылки). TDD устроено так, что при контакте с кожей пациента анальгетически эффективное количество опиоида вводится пациенту трансдермально. Но антагонист опиоида или остатся в TDD и не вводится пациенту, или вводится пациенту в количестве, не достаточном для ингибирования анальгетического эффекта опиоида.TDD резервуарного типа обычно содержит резервуар, обычно содержащий жидкость, расположенную между непроницаемой поддерживающей плнкой и мембраной, регулирующей скорость, которая содержит покрытие в виде слоя чувствительного к давлению адгезива, контактирующего с кожей. Резервуар, в котором может быть раствор или дисперсия, содержит опиоид и антагонист опиоида. TDD имеет-4 007240 подложку в виде непроницаемой поддерживающей плнки, а поверхность адгезива защищена снимающейся прокладкой. Для введения опиоида прокладку удаляют для освобождения чувствительного к давлению адгезива, и чувствительный к давлению адгезив контактирует с кожей. Опиоид проходит через мембрану, регулирующую скорость, проникает через не и адгезив соприкасается с кожей и проникает в кожу. Скорость доставки опиоида определяется обычно скоростью, с которой опиоид проникает через мембрану, регулирующую скорость. Предпочтительно, чтобы адгезив, чувствительный к давлению, не влиял отрицательно на скорость доставки опиоида и не вступал с ним в химическую реакцию. Скорость доставки при этом такова, что пациенту доставляется анальгетически эффективное количество опиоида. В противоположность опиоиду антагонист опиоида, который молжет быть в резервуаре, предпочтительно, не проникает через мембрану, регулирующую скорость, а если и проникает, то в количестве, которое является недостаточным для ингибирования анальгетического эффекта опиоида. На фиг. 2 А представлен пример TDD резервуарного типа. TDD 10 включает резервуар 11, обычно содержащий раствор или дисперсию 12, в которых диспергирован опиоид 13 и антагонист опиоида 14. Резервуар 11 расположен между непроницаемой поддерживающей плнкой 15, мембраной, регулирующей скорость 16 и чувствительным к давлению адгезивом 17. Снимаемая прокладка 18 нанесена на слой чувствительного к давлению адгезива 17 и перед использованием удаляется. Предпочтительно, чтобы опиоид и антагонист опиоида были диспергированы по всему объму резервуара, хотя однородная дисперсия не является необходимой. Видоизменение TDD резервуарного типа представляет собой полимер-матриксное TDD. В полимер-матриксном TDD опиоид и антагонист опиоида диспергированы в полимерной матрице, которая регулирует скорость доставки опиоида. Как и в случае средства с резервуаром, заполненным жидкостью,полимер-матриксный резервуар поддерживается непроницаемым слоем. Однако полимер-матриксное средство обычно содержит периферическое кольцо адгезива, расположенное вокруг края пластыря, а не непрерывный слой адгезива. Снимаемая прокладка защищает поверхность адгезива и поверхность полимерной матрицы. Для введения опиоида снимаемая прокладка удаляется с полимерной матрицы и кольца чувствительного к давлению адгезива и средство контактирует с кожей. Кольцо адгезива удерживает средство на коже, и полимерная матрица непосредственно контактирует с кожей. Когда полимерная матрица контактирует с кожей, опиоид диффундирует из полимерной матрицы, контактирует с кожей пациента и проникает в кожу. Скорость доставки опиоидного агониста обычно определяется скоростью диффузии опиоида из полимерной матрицы. Скорость доставки такова, что анальгетически эффективное количество опиоида доставляется пациенту. Антагонист опиоида, который может быть в любом месте полимерной матрицы, или не диффундирует из полимерной матрицы, а если диффундирует, то в количестве, которое является недостаточным для ингибирования анальгетического эффекта опиоида. На фиг. 2 В показан пример типичного TDD полимер-матриксного типа по изобретению. TDD 20 включает резервуар 21 в виде полимерной матрицы 22, в которой диспергирован опиоид 23 и антагонист опиоида 24. Предпочтительно, чтобы опиоид и антагонист опиоида были диспергированы по объму полимерной матрицы, хотя однородная дисперсия не является необходимой. Полимерная матрица 21 поддерживается непроницаемой подложкой 25 и содержит периферическое кольцо адгезива 26, расположенное по краю пластыря. Снимаемая прокладка 28 нанесена на периферическое кольцо адгезива 26 и полимерную матрицу 22 и удаляется перед использованием.TDD, содержащее лекарство в составе адгезива, содержит опиоидный агонист и антагонист опиоида, диспергированные непосредственно в чувствительной к давлению адгезивной матрице. Адгезивную матрицу поддерживает, обычно сверху, непроницаемая плнка, а на стороне, которая обращена к коже,не не наносят непроницаемую снимаемую прокладку. Для введения опиоида прокладку удаляют, высвобождая адгезивную матрицу, и средство контактирует с кожей. Адгезивная матрица прикрепляет средство к коже и обычно регулирует скорость доставки опиоида. Как и в случае средства полимерматриксного типа, средство с лекарством в адгезиве позволяет осуществить диффузию опиоида из адгезивной матрицы, который контактирует с кожей пациента и проникает в кожу. Скорость доставки опиоида обычно определяется скоростью его диффузии из адгезивной матрицы. Скорость доставки такова,что пациенту доставляется анальгетически эффективное количество опиоида. С другой стороны, антагонист опиоида, который может содержаться в любом месте адгезивной матрицы, не диффундирует из адгезивной матрицы, и, если диффундирует, то в количестве, недостаточном для ингибирования анальгетического эффекта опиоида. На фиг. 2 С показано TDD, содержащее лекарство в адгезиве, по изобретению. TDD 30 включает адгезивную матрицу 31, в которой диспергирован опиоид 32 и антагонист опиоида 33. Предпочтительно,чтобы опиоид и антагонист опиоида были диспергированы по всей адгезивной матрице, хотя однородная дисперсия не является необходимой. Адгезивная матрица 31 поддерживается непроницаемым слоем 34 и имеет непроницаемую снимаемую прокладку 35 со стороны, которая обращена к коже и удаляется перед применением.TDD резервуарного типа, полимер-матриксного типа и TDD, содержащее лекарство в составе адгезива, хорошо известны специалистам (см., например, H.S. Tan and W.R. Pfister, Pressure SensitiveAdhesives for Transdermal Drag Delivery Systems, PSTT, vol.2, February 1999, включена в качестве ссылки). Согласно одному предпочтительному варианту система для устранения TDD по изобретению иммобилизует и изолирует TDD полимер-матриксного типа и/или TDD, содержащее лекарство в адгезиве, для того, чтобы предотвратить, контролировать или ингибировать неправильное использование и/или злоупотребление активным агентом, содержащимся в TDD. В TDD по изобретению может быть использована любая мембрана, регулирующая скорость, известная специалистам. Предпочтительно выбирать мембрану, которая не позволяет сколько-нибудь заметному количеству антагониста опиоида пройти через не, особенно в тех случаях, когда антагонист опиоида может проникнуть в кожу пациента. Подходящие материалы для мембран, регулирующих скорость, включают, без ограничения, полиэтилен, полипропилен, сополимеры этилена с пропиленом, сополимеры этилена с этилакрилатом, сополимеры этилена с винилацетатом, полиакрилаты, полиметакрилаты, силиконовые эластомеры, медицинские полидиметилсилоксаны, неопреновый каучук, полиизобутилен, хлорированный полиэтилен, поливинилхлорид, сополимер винилхлорида с винилацетатом, полиметакрилат (гидрогель), поливинилиденхлорид, полиэтилентерефталат, бутилкаучук, эпихлоргидринные каучуки, сополимер этилена с виниловым спиртом, сополимеры этилена с вилилоксиэтанолом, силиконовые сополимеры, например, полисилоксан-поликарбонатные сополимеры, сополимеры полисилоксана с полиэтиленоксидом, сополимеры полисилоксана с полиметакрилатом, полисилоксан-алкиленовые сополимеры (например, сополимеры этилена с полисилоксаном), сополимеры алкиленсилана с полисилоксаном (например, сополимеры полисилоксана с этиленсиланом) и т.п., целлюлозы, например, метил- или этилцеллюлоза, гидроксипропилметил-целлюлоза и сложные эфиры целлюлозы, поликарбонаты, политетрафторэтилен, крахмалы, желатин, натуральные и синтетические смолы, любой другой природный или синтетический полимер или волокно и их сочетания. Поддерживающий слой может быть любым подходящим материалом, который является непроницаемым для содержимого резервуара, полимерной матрицы или адгезивной матрицы. Подходящие материалы для таких плнок хорошо известны специалистам и включают, но не ограничиваются этим, окклюзионные полимеры, такие как полиуретан, сложные полиэфиры, такие как полиэтиленфталат, полиэфирамид, сополиэфир, полиизобутилен, полиэтилен высокой и низкой плотности, полипропилен, поливинилхлорид, металлическую фольгу и ламинаты на основе металлической фольги и подходящих полимерных плнок. Подходящие материалы для полимерной матрицы хорошо известны специалистам и включают, но не ограничиваясь этим, полиэтилен, полипропилен, сополимеры этилена с пропиленом, сополимеры этилена с этилакрилатом, сополимеры этилена с винилацетатом, силиконовые эластомеры, особенно медицинские полидиметилсилоксаны, неопреновый каучук, полиизобутилен, хлорированный полиэтилен,поливинилхлорид, сополимер винилхлорида с винилацетатом, полиметакрилат (гидрогель), поливинилиденхлорид, полиэтилентерефталат, бутилкаучук, эпихлоргидринные каучуки, сополимер этилена с виниловым спиртом, сополимеры этилена с вилилоксиэтанолом, силиконовые сополимеры, например полисилоксан-поликарбонатные сополимеры, сополимеры полисилоксана с полиэтиленоксидом, сополимеры полисилоксана с полиметакрилатом, полисилоксан-алкиленовые сополимеры (например, сополимеры этилена с полисилоксаном), сополимеры алкиленсилана с полисилоксаном (например, сополимеры полисилоксана с этиленсиланом) и т.п., целлюлозы, например, метил- или этилцеллюлоза, гидроксипропилметилцеллюлоза и сложные эфиры целлюлозы, поликарбонаты, политетрафторэтилен и их сочетания. Предпочтительно, чтобы полимерная матрица имела температуру стеклования ниже комнатной температуры. Полимер может, но необязательно, иметь ненулевую степень кристалличности при комнатной температуре. Полимеры могут содержать сшивающие мономерные звенья или сайты. Например, сшивающие мономеры могут быть введены в полиакрилаты. Сшивающие мономеры обеспечивают сайты для сшивки полимерной матрицы после микродиспергирования опиоида и антагониста опиоида в полимере. Известные сшивающие мономеры для полиакрилатов включают, но не ограничиваются этим, полиметакриловые эфиры полиолов, такие как бутилендиакрилат и диметакрилат, триметилолпропантриметакрилат и т.п. Другие мономеры, обеспечивающие сшивающие сайты, включают аллилакрилат, аллилметакрилат,диаллилмалеинат и т.п. Предпочтительно выбирать такую полимерную матрицу, которая вообще не позволяла антагонисту опиоида диффундировать из не или же не позволяла диффундировать заметному количеству этого антагониста, особенно, в тех случаях, когда антагонист опиоида может проникать в кожу пациента. Подходящие материалы для чувствительной к давлению адгезивной матрицы хорошо известны из уровня техники и включают, но не ограничиваются этим, полиизобутилены, полисилоксаны и полиакрилатные сополимеры (полиакриловые эфиры), клеи на основе натурального каучука/смолы карайя, гидрогели, гидрофильные полимеры и полиуретаны, такие как описаны в работе H. Tan and W. Pfister, PressureSensitive Adhesives for Transdermal Drag Delivery Systems, PSTT, vol.2, February 1999, включенной в данное описание в качестве ссылки. Адгезив может также включать модифицирующие мономеры, добавки,повышающие клейкость, пластификаторы, наполнители, воски, масла, другие добавки для придания же-6 007240 лательных адгезионных свойств (см. там же). Предпочтительно выбирать чувствительную к давлению адгезивную матрицу таким образом, чтобы она вообще не позволяла антагонисту опиоида диффундировать из не или же не позволяла диффундировать заметному количеству этого антагониста, особенно, в тех случаях, когда антагонист опиоида может проникать в кожу пациента. Размер средства, предпочтительно, меняется от примерно 1 см 2 до более 200 см 2 и обычно составляет примерно 5-50 см 2 . Способы изготовления TDD хорошо известны специалистам. Примеры средств для трансдермальной доставки включают, но не ограничиваются этим, средства,описанные в патентах США 4,806,341, 5,069,909, 5,236,714, 5,240,711, 5,718,914, 5,902,603,5,969,547, 6,162,456 и 6,344,212, которые включены в данное описание в качестве ссылок.TDD может включать один или более агентов, улучшающих проницаемость, которые повышают скорость, с которой опиоид проникает через кожу пациента. Предпочтительно, чтобы такой агент не увеличивал проникновение антагониста опиоида через кожу. Агент, повышающий проницаемость, должен проникать через мембрану, регулирующую скорость,или диффундировать из полимерной матрицы или адгезивной матрицы таким образом, чтобы он мог контактировать с кожей пациента и повышать проникновение опиоида через кожу пациента. Подходящие агенты, повышающие проницаемость, используемые в TDD и способах по изобретению, включают,но не ограничиваются этим, С 2-С 4-спирты, такие как этанол и изопропанол, монолаурат полиэтиленгликоля, полиэтилен-гликоль-3-лаурамид, триолеат сорбита, жирные кислоты, эфиры жирных кислот, содержащие от примерно 10 до примерно 20 атомов углерода, моноглицериды или смеси моноглицеридов жирных кислот, содержащие моноэфиры в количестве, по меньшей мере, 51%, где моноэфиры содержат от 10 до 20 атомов углерода, и смеси моно-, ди- и триглицеридов жирных кислот. Подходящие жирные кислоты включают, но не ограничиваются этим, лауриновую кислоту, миристиновую кислоту, стеариновую кислоту, олеиновую кислоту, линолевую кислоту и пальмитиновую кислоту. Моноглицеридные повысители проницаемости включают, например, моноолеат глицерина, монолаурат глицерина, монолинолеат глицерина. Примеры повысителей проницаемости, используемых в способах по изобретению включают, но не ограничиваются этим, вещества, описанные в патентах 3,472,931; 3,527,864; 3,896,238; 3,903,256; 3,952,099; 3,989,816; 4,046,886; 4,130,643; 4,130,667; 4,299,826; 4,335,115; 4,343,798; 4,379,454; 4,405,616; 4,746,515; 4,316,893; 4,405,616; 4,060,084; 4,379,454; 4,560,553; 4,863,952; 4,863,970; 4,879,275; 4,940,586; 4,960,771; 4,973,968; 5,066,648; 5,164,406; 5,227,169; 5,229,130; 5,238,933; 5,308,625; 4,326,566; 5,378,730; 5,420,106; 5,641,504; 5,716,638; 5,750,137; 5,785,991; 5,837,289; 5,834,468; 5,882,676; 5,912,009; 5,952,000; 6,004,578 и Idson, Percutaneous Absorption, J. Pharm. Sci. Vol. 64, no. Ъ 6, June 1975, pp. 901-924, которые включены в данное описание в качестве ссылок.TDD могут также содержать другие добавки, обычно используемые в терапевтических продуктах. Например, TDD может также включать один или более консервантов или бактериостатических агентов,например, метилгидроксибензоат, пропилгидроксибензоат, хлоркрезол, бензалконийхлориды и т.п., или другие активные ингредиенты, такие как антимикробные агенты, в частности, антибиотики, анестетики,другие анальгетики и противозудные средства. В TDD может содержаться любой опиоид или неопиоид, его фармацевтически приемлемая соль,его основная форма или смесь любого сочетания таких опиоидов и/или их производных, известные из уровня техники. Полагают, что опиоиды имеют, по меньшей мере в некоторой степени, активность агониста -опиоидного рецептора (и возможно, по меньшей мере в некоторой степени, также активность агониста одного или нескольких к-опиоидного рецептора, -опиоидного рецептора и ORL-1-рецептора),они включают, но не ограничиваются этим, алфентанил, аллилпродин, альфапродин, анилеридин, бензилморфин, бензитрамид, бупренорфин, буторфанол, клонитазин, кодеин, дезоморфин, декстроморамид,дезоцин, диампромид, диаморфон, дигидрокодеин, дигидроморфин, дигидроморфон, дигидроизоморфин,дименоксадол, димефептанол, диметилтиамбутен, диоксафетилбутират, дипипанон, эптазоцин, этогептазин, этилметилтиамбутен, этилморфин, этонитазен, эторфин, дигидроэторфин, фентанил, героин, гидрокодон, гидроморфон, гидроморфодон, гидроксипетидин, изометадон, кетобемидон, леворфанол, левофенацилморфан, лофентанил, меперидин, мептазинол, метазоцин, метадон, метопон, морфин, мирофин,нарцеин, никоморфин, норлеворфанол, норметадон, налорфин, налбуфен, норморфин, норпитанон, опий,оксикодон, оксиморфон, пантопон, папаверетум, парегорик, пентазоцин, фенадоксон, фендиметразин,фендиметразон, феноморфан, феназоцин, феноперидин, пиминодин, пиритрамид, профептазин, промедол, проперидин, пропоксифен, пропилгекседрин, суфентанил, тимидин, трамадол и их смеси. Не-опиоиды включают, но не ограничиваются этим, опиоидные агонисты, специфические по отношению кORL-1, такие как ноцицептин, делторфин и т.п. и их смеси. Согласно предпочтительному варианту опиоид включает бупренорфин, его фармацевтически приемлемые соли, его основные формы, фентанил,его фармацевтически приемлемые соли, его основные формы, оксикодон, его фармацевтически приемлемые соли, его основные формы и любое сочетание этих опиоидов и/или их производных. Согласно некоторым предпочтительным вариантам опиоидный агонист включает гидрокодон, морфин, гидроморфон, оксикодон, кодеин, леворфанол, меперидин, метадон, оксиморфон, бупренорфин,фентанил, дипипанон, героин, трамадол, эторфин, дигидроэторфин, буторфанол, леворфанол, их фарма-7 007240 цевтически приемлемые соли, основные формы и любые их смеси. Более предпочтительно, опиоидный агонист включает оксикодон, гидрокодон, фентанил, бупренорфин, их фармацевтически приемлемые соли, основные формы и смеси любых или всех этих веществ. Наиболее предпочтительно, опиоидный агонист включает бупренорфин, его фармацевтически приемлемые соли, его основные формы, фентанил,его фармацевтически приемлемые соли, его основные формы и любую комбинацию таких опиоидов и/или их производных. Предпочтительно, особенно в случае пассивных пластырей, опиоид представляет собой свободную форму, то есть не фармацевтически приемлемую соль опиоида. Однако для пластырей,которые используют ионофорез для облегчения проникновения опиоида через кожу, предпочтительны фармацевтически приемлемые соли опиоида. Кроме того, вместо опиоидного агониста или в добавление к нему TDD может содержать фармакологически активный агент, который способен вызвать желательный биологический или фармакологический эффект, который может включать, но не ограничивается этим, (1) влияние на жизненные процессы,(2) профилактический эффект для пациента и предотвращение нежелательного эффекта, например, профилактика инфекции, (3) облегчение состояния, вызванного каким-либо заболеванием, или симптома этого заболевания, например, облегчение боли или уменьшение воспаления, (4) или облегчение, уменьшение или полное излечивание болезни, состояния или симптомов у пациента. Действие активного агента может быть локальным, например, обеспечение анестетического эффекта, или оно может быть системным или сочетанием того и другого. Согласно одному из вариантов классы таких соединений включают, но не ограничиваются этим, ингибиторы АСЕ, аденогипофизные гормоны, агенты, блокирующие адренергические нейроны, адренокортикальные стероиды, ингибиторы биосинтеза адренокортикальных стероидов, альфа-адренергические агонисты, альфа-адренергические антагонисты, селективные альфадва-адренергические агонисты, андрогены, агенты против привыкания, антиандрогены, противоинфекционные средства, такие как антибиотики, антимикробные агенты, противовирусные агенты, анальгетики и комбинации анальгетиков, средства, повышающие аппетит, антигельминтные средства, противоартритные средства, антиастматические агенты, противосудорожные средства, антидепрессанты, антидиабетические средства, средства против диареи, противорвотные и прокинетические агенты, антиэпилептические агенты, антиэстрогены, противогрибковые средства, антигистаминные средства, противовоспалительные средства, препараты против мигрени, антимускариновые агенты, средства против тошноты,антинеопластические агенты, антипаразитические агенты, средства для лечения болезни Паркинсона,агенты, снижающие образование тромбоцитов, антипрогестины, противозудные средства, антипсихотические средства, жаропонижающие средства, спазмолитические средства, антихолинергические средства,средства для щитовидной железы, противокашлевые средства, азаспиродекандионы, симпатомиметики,производные ксантина, сердечно-сосудистые препараты, включая блокаторы калиевых и кальциевых каналов, альфа-блокаторы, бета-блокаторы и противаритмические средства, средства, снижающие давление, диуретики и антидиуретики, сосудорасширяющие средства, включающие средства для коронарных периферических и церебральных сосудов, стимулянты центральной нервной системы, вазоконстрикаторы, препараты против кашля и простуды, включая противоотчные средства, гормоны, такие как эстрадиол и другие стероиды, включая кортикостероиды, гипнотические средства, иммуносупрессивные средства, миорелаксанты, парасимпатолитики, психостимулянты, успокоительные средства, транквилизаторы, никотин и его кислые соли, бензодиазепины, барбитураты, бензотиадиазиды, бетаадренергические агонисты, бета-адренергические антагонисты, селективные бета-один-адренергические антагонисты, селективные бета-два-адренергические антагонисты, соли желчи, агенты, влияющие на объм и состав жидкостей в организме, бутирофеноны, агенты, влияющие на кальцификацию, кетехоламины, холинергические агонисты, реактиваторы холинэстеразы, дерматологические агенты, дифенилбутилпиперидины, эргоалкалоиды, ганглиозные блокирующие агенты, гидантоины, агенты для контроля кислотности желудочного сока и лечения пептических язв, гематопоетические агенты, гистамины, антагонисты 5 гидрокситриптамина, лекарственные вещества для лечения гиперлипепротеинемии, слабительные средства, метилксантины, ингибиторы монкаминоксидазы, нервно-мышечные блокирующие агенты, органические нитраты, панкреатические ферменты, фенотиазины, простагландины, ретиноиды, агенты для мышечной спастичности и острых мышечных спазм, сукцинимиды, тиоксантины, тромболитические агенты, тироидные агенты, ингибиторы транспорта органических соединений по канальцам, лекарства,влияющие на подвижность матки, витамины и т.п. или их сочетание. Кроме того, вместо опиоидного агониста или в добавление к нему TDD может содержать активный компонент, который может включать, но не ограничивается этим, флуорогестонацетат, гидроксипрогестерон, гидроксипрогестеронацетат, гидроксипрогестеронкапроат, медроксипрогестеронацетат, норетиндрон, норетиндронацетат, норетистерон, норетинодрел, дезогестрел, 3-кетодезогестрел, гестаден, левоноргестрел, эстрадиол, эстрадиолбензоат, эстрадиолвалериат, эстрадиолциприонат, эстрадиолдеканоат,эстрадиолацетат, этинилэстрадиол, эстриол, эстрон, местранол, бетаметазон, бетаметазонацетат, кортизон, гидрокортизон, гидрокортизонацетат, кортикостерон, флуоцинолонацетонид, преднизолон, преднизон, триамцинолон, алдостерон, андростерон, тестостерон, метилтестостерон или их сочетание. Кроме того, вместо опиоидного агониста или в добавление к нему TDD может содержать активный компонент, который может включать, но не ограничивается этим, а) кортикостероиды, например, корти-8 007240 зон, гидрокортизон, преднизолон, беклометазона пропионат, дексаметазон, бетаметазон, флюметазон,триамцинолон, триамцинолона ацетонид, флуоцинолон, флуоцинолона ацетонид, клобетазола пропионат и т.п. или их сочетание; б) анальгетические противовоспалительные агенты, например, ацетаминофен,мефенамовую кислоту, флуфенамовую кислоту, гендометацин, диклофенак, натриевую соль диклофенака, аклофенак, ибуфенак, оксифенбутазон, фенилбутазон, ибупрофен, флурбипрофен, кетопрофен, салициловую кислоту, метилсалицилат, ацетилсалициловую кислоту, 1-ментол, камфору, слиндак, натриевую соль толмедина, напроксен, фенбуфен и т.п. или их сочетание; в) гипнотические седативные средства,например, фенобарбитал, амобарбитал, циклобарбетал, лоразепам, галоперидол и т.п. или их сочетание; г) транквилизаторы, например, фулфеназин, тиоридазин, диазепам, флуразепам, хлорпромазин и т.п. или их сочетание; д) средства, снижающие давление, например, клонидин, клонидина гидрохлорид, бопинидол, тимолол, пиндолол, пропранолол, пропранолола гидрохлорид, бупранолол, генденолол, букумолол,нифедипин, бунитролол и т.п. или их сочетание; е) гипотензивные диуретики, например, бендрофлуметиазид, политиазид, метилхлортиазид, трихлорметиазид, циклопентиазид, бензилгидрохлортиазид, гидрохлортиазид, буметанид и т.п. или их сочетание; ж) антибиотики, например, пенициллин, тектрациклин,окситетрациклин, метациклин, доксициклин, миноциклин, фрадиомицина сульфат, эритромицин, хлорамфеникол и т.п. или их сочетание; з) анестезирующие средства, например, лидокаин, бензокаин, этиламинобензоат и т.п. или их сочетание; и) антимикробные агенты, например, бензалкония хлорид, нитрофуразон, нистатин, сульфацетамид, клотримазол и т.п. или их сочетание; к) противогрибковые агенты,например, пентамицин, амфотерицин В, пирролнитрин, клотримазол и т.п. или их сочетание; л) витамины, например, витамин А, эргокальциферол, холекальциферол, октотриамин, эфир масляной кислоты и рибофлавина и т.п. или их сочетание; м) противоэпилептические средства, например, нитразепам, мепробамат, клоназепам и т.п. или их сочетание; н) антигистаминные средства, например, дифенгидрамина гидрохлорид, хлорфенирамин, дифенилимидазол и т.п. или их сочетание; о) противокашлевые средства,например, декстрометорфан, тербуталин, эфедрин, эфедрина гидрохлорид и т.п. или их сочетание; п) половые гормоны, например, прогестерон, эстрадиол, эстрол, эстрон и т.п. или их сочетание; р) антидепрессанты, например, доксетин; с) вазодилаторные средства, например, нитроглицерин, изосорбида нитрат, нитрогликоль, пентаэритрита тетранитрат, дипиридамол и т.п. или их сочетание; т) другие лекарственные вещества, например, 5-флуорацил, дигидроэрготамин, десмопрессин, дигоксин, метоклопрамид,домперидон, скополамин, скополамина гидрохлорид и т.п. или их сочетание. Эффективное количество активного агента, содержащегося в TDD, будет зависеть от конкретного вида этого агента, типа средства, вида материалов, используемых для изготовления средства, промежутка времени, в течение которого активный агент должен быть доставлен пациенту. Когда активным агентом является опиоид анальгетически эффективное количество опиоида, содержащегося в TDD, обычно составляет от примерно 0,1 до примерно 500 мг, предпочтительно, от примерно 1 до примерно 100 мг, более предпочтительно, от примерно 1 до примерно 50 мг. Специалист легко может определить анальгетически эффективное количество опиоида или неопиоида, необходимое для назначения пациенту. 2. Система устранения TDD. Системы устранения TDD согласно изобретению предпочтительно содержат, по меньшей мере, одну подложку, на которой имеется покрытие на основе адгезива. Может быть по меньшей мере одна подложка, которая может быть гибкой (то есть способной складываться, по существу, без потери своей механической целостности) или жсткой (то есть такой, которая может или механически, или физически сопротивляться складыванию или же не складывается без потери своей механической целостности при складывании вручную или механическими средствами). Гибкие подложки могут быть такими, как представлены, например, на фиг. 1B (для системы устранения одного TDD) или на фиг. 1D (для системы устранения многих TDD). Жесткие подложки могут быть такими, как показаны, например, на фиг. 1A (для системы устранения одного TDD) и на фиг. 1 С (для системы устранения многих TDD). На гибкость или жсткость, по меньшей мере, одной подложки по изобретению может влиять не только химическая природа материала подложки, но также, наряду с другими факторами, размеры (толщина, длина и/или ширина) подложки. Как показано на фиг. 1A, система устранения TDD согласно изобретению включает внешний слой(1) и внутренний слой (4), которые соединены при помощи адгезива (3), покрывающего первую часть внутреннего слоя. Сочетание внутреннего и внешнего слоев образует замкнутый участок (2) иммобилизации и/или герметизации, между внешним слоем, обращенным к стороне внутреннего слоя, и внутренним слоем, обращенным к стороне внешнего слоя. Как показано далее на Фиг. 1B, внутренний и внешний слои, предпочтительно, соединены таким образом, что они образуют герметичное отверстие между двумя слоями. Как показано на фиг. 1B, отверстие, предпочтительно, герметизируется клапаном (6), содержащим адгезив (3), который покрывает, по меньшей мере, часть клапана, которая используется для герметизации отверстия. Фиг. 1 С и 1D представляют аналоги системы устранения TDD с одной подложкой, показанной на фиг. 1A и 1B, содержащие много подложек и имеющие вид буклета. Если имеется только одна подложка, на которую нанесн адгезив, предпочтительно, чтобы она была гибкой и способной складываться для иммобилизации и изоляции помещнного TDD. Или же, если-9 007240 имеется только одна подложка, на которую нанесено покрытие, может иметься вторая дополнительная подложка, причм вторая подложка, предпочтительно, должна быть способна необратимо присоединяться с помощью адгезива к, по меньшей мере, одной подложке с адгезивным покрытием. В этом случае подложка с адгезивным покрытием и вторая дополнительная подложка могут быть гибкими или жсткими, как описано выше. Согласно некоторым вариантам изобретения подложка или подложки могут быть достаточно жсткими, чтобы сделать подложку неспособной складываться без повреждения или растрескивания подложки. В соответствии с этими вариантами система устранения может включать одну или несколько жстких подложек, которые могут быть или плоскими, или неплоскими. Как показано на фиг. 14 А и 14 В, неплоские подложки могут иметь такие конфигурацию и размеры, чтобы обеспечить углубление 50 на одной стороне для помещения TDD. В зависимости от толщины подложки и глубины углубления, сторона подложки, которая является противоположной углублению, может быть плоской или неплоской. Как показано на фиг. 14 А, подложка может иметь углубление на одной стороне и соответствующую выпуклую поверхность на противоположной стороне. Предпочтительно, чтобы адгезивное покрытие и любые возможные компоненты располагаемые, по меньшей мере, в или на подложке в углублении, как и над другой частью стороны подложки. Кроме того, могут быть предусмотрены две подложки, каждая из которых имеет углубление. При использовании TDD может быть помещено в углубление на первой подложке, а вторая подложка может быть выровнена и приведена в контакт с первой подложкой так, чтобы углубление на второй подложке располагалось над TDD, и TDD, первая подложка и вторая подложка необратимо соединились друг с другом. Углубление 50 может иметь глубину, которая меньше, равна или больше толщины TDD. Предпочтительно, чтобы в случае одной подложки глубина углубления была примерно равна или превышала толщину TDD. Если есть две подложки, или одна, или обе могут иметь углубления. В таких случаях общая глубина углубления или углублений может быть меньше, равна или больше толщины TDD, предпочтительно, примерно равна толщине TDD. Согласно другим вариантам изобретения подложки могут дополнительно включать один или несколько выступающих элементов, которые являются достаточно жсткими и/или острыми, чтобы проникнуть в TDD, помещнное в систему. Эти варианты особенно предпочтительны для прокалывания резервуара в TDD резервуарного типа, чтобы обеспечить более лгкий выход активного агента из резервуара и его взаимодействие с подложкой, адгезивами и другими компонентами, которые могут содержаться. На фиг. 3 показан альтернативный вариант данного изобретения. Изделие представляет собой систему устранения TDD, содержащую один или более инициаторов (и, возможно, соинициаторов), мономеров (и, возможно, сомономеров), сшивающих агентов и деактивирующих агентов (для активного компонента(-ов) TDD), расположенных на участке иммобилизации и/или герметизации системы устраненияTDD. Конкретно, система устранения TDD согласно изобретению включает слой адгезива (возможно,содержащий один или несколько дополнительных компонентов) (41), имеющий переводную сторону и противоположную сторону. Изделие включает также внешний слой (43) со стороной, обращенной к слою адгезива, и противоположной стороной, причм слой адгезива соединн с внешним слоем с образованием участка иммобилизации и/или герметизации (44) между противоположной стороной слоя адгезива и стороной внешнего слоя, обращенной к слою адгезива. Предпочтительно, чтобы каждый из слоев системы устранения TDD по изобретению был стойким к отрыву. Фиг. 4 отражает ещ один вариант системы устранения TDD по изобретению, имеющей переводную сторону и противоположную сторону и, возможно, адгезив (61), расположенный по периметру переводной стороны. Переводная сторона включает первый (62) и второй (63) участки, которые могут быть отделены друг от друга мембраной или непроницаемым барьером (64). Первый участок или второй участок или оба содержат, по меньшей мере, один из вышеупомянутых компонентов. Предпочтительно, если оба участка содержат, по меньшей мере, один из вышеупомянутых компонентов, то этот содержащийся компонент(-ы) не является одинаковым. Система устранения TDD может также включать снимаемый слой, покрывающий адгезив, и этот снимаемый слой может быть отстающим. Подложка(-и), которые включены в систему устранения TDD согласно изобретению, могут предпочтительно включать, не ограничиваясь этим, прочные, стойкие к разрыву (со)полимеры и композиты на основе (со)полимеров. (Со)полимеры, используемые для изготовления подложек, могут быть аморфными или, преимущественно, могут быть ориентированы способом, включающим, но не ограничивающимся этим, одноосную вытяжку, биаксиальную вытяжку, мультиаксиальную вытяжку, образование плоскостной структуры, кристаллической структуры со сложенными цепями, кристаллической структуры с вытянутыми цепями, некристаллической структуры с вытянутыми цепями, жидкокристаллической структуры, фибриллярной, ламеллярной, сферулитической структуры и т.п. или сочетания этих структур. Примеры полимеров для подложек, используемых в системе устранения TDD согласно изобретению,включают, но не ограничиваются этим, сложные полиэфиры, например, полиэтилентерефталат, полибутилентерефталат, сополимеры сложных и простых полиэфиров, сополимеры полиэфирамидов и т.п.; поликарбонаты, полиуретаны, например, полиэфируретаны на основе сложных полиэфиров, полиэфируретаны на основе простых полиэфиров, полиэфируретанмочевины на основе простых полиэфиров, поли- 10007240 эфируретанмочевины на основе сложных полиэфиров, полиэфирмочевины на основе простых полиэфиров, полиэфирмочевины на основе сложных полиэфиров, полисилоксануретаны, поликарбонатуретаны и т.п.; поли(мет)акрилаты, например, полиметилакрилат, сополимеры этилена с метакрилатами, частично нейтрализованные металлические соли поли(мет)акриловых кислот, частично омыленные поли(мет)акриловые кислоты и т.п.; поли(мет)акриловые кислоты, поливинилацетаты, такие как сополимеры этилена с винилацетатом, полиамиды, например, нейлоны, арамидные волокна, такие как Kevlar, сополимеры полиэфирамидов на основе сложных полиэфиров, сополимеры полиэфирамидов на основе простых полиэфиров и т.п.; простые полиэфиры, например, полиэфирэфиркетоны, полиэфиркетонкетоны, сополимеры простых и сложных полиэфиров, сополимеры простых полиэфиров и полиамидов и т.п.; полиимиды, композиты на основе углеродных волокон, полимер-керамические композиты, полимерметаллические (сплавы) композиты; полимеры, описанные в патентах США 4 588 580, 5 573 778 или 5 750 134, которые включены в данное описание в качестве ссылок; или сочетания указанных полимеров. Особенно в случае наличия одной или нескольких жстких подложек подложка может включать любой полимер или полимерный композит, имеющий достаточные толщину и жсткость для предотвращения складывания подложки без повреждения или растрескивания. В добавление к вышеуказанным полимерам и полимерным композитам, перечисленным выше, такие жсткие подложки могут включать любые стекловолокно, металлы и/или керамику и/или композиты, содержащие один или несколько из этих компонентов с любым полимером. Например, такие жсткие подложки могут включать металлы,такие как алюминий, титан, сталь, нержавеющую сталь, а также металлокерамические композиты, содержащие такие металлы. В то время как толщина подложки (подложек) особенно не ограничивается, гибкие подложки,предпочтительно, тоньше, чем жсткие подложки. Кроме того, толщина подложки (подложек) зависит,наряду с другими факторами, от е (их) барьерных свойств для предотвращения, ингибирования или уменьшения неправильного применения или злоупотребления, например, опиоидным агонистом (то есть чем лучшие барьерные свойства имеет материал подложки, например, по отношению к потенциальным экстрагирующим растворителям, тем менее толстой должна быть подложка). Например, гибкие подложки, преимущественно, имеют толщину от примерно 0,0005 дюйма (13 мкм) до примерно 0,01 дюйма (250 мкм), предпочтительно, от примерно 0,001 дюйма (25 мкм) до примерно 0,005 дюйма (130 мкм), в то время как жсткие подложки предпочтительно имеют толщину более примерно 0,005 дюйма (130 мкм),более предпочтительно имеют толщину от примерно 0,01 дюйма (250 мкм) до примерно 1 дюйм (25 мм). Хотя длина и ширина подложки (подложек) особенно не ограничивается, подложки (и, особенно, та часть, на которой имеется адгезивное покрытие, если это покрытие имеется не на всей поверхности подложки), имеющие сторону с площадью поверхности, приближающейся к площади поверхности TDD,имеют, предпочтительно, форму буклета, то есть являются системами для устранения TDD с множеством подложек по изобретению, в то время как обычно только необходимо, чтобы подложки (и, особенно, та часть, на которой имеется адгезивное покрытие, если это покрытие имеется не на всей поверхности подложки) имели площадь поперечного сечения, достаточную для того, чтобы покрыть или содержать TDD или активный компонент(-ы), содержащиеся в нм, и предотвратить от неправильного употребления или злоупотребления ими. То есть желательные длина и ширина подложки (подложек) (и, особенно, та часть,на которой имеется адгезивное покрытие, если это покрытие имеется не на всей поверхности подложки) может зависеть, наряду с другими факторами, от относительной необратимости адгезии к TDD и/или способности к изоляции и герметизации TDD или активного компонента(-ов) в нм для предотвращения,ингибирования или уменьшения неправильного использования или злоупотребления, например, опиоидным агонистом, то есть, чем лучше соединяется подложка с нанеснным адгезивом с TDD и/или чем лучше барьерные свойства соединнных подложки и TDD по отношению, например, к экстракции растворителями, тем меньше должны быть длина и/или ширина подложки, особенно, та часть, на которой имеется адгезивное покрытие, если это покрытие имеется не на всей поверхности подложки. Согласно одному варианту площадь поперечного сечения поверхности подложки (и, особенно, та часть, на которой имеется адгезивное покрытие, если это покрытие имеется не на всей поверхности подложки) не более, чем на 10% больше, чем TDD, к которому она должна присоединиться, или не более,чем на 5% больше, чем TDD, например, их площади примерно одинаковы. Подложка может быть снабжена соответствующей инструкцией для пользователя, помещнной на этикетке. Кроме того, подложка может быть цветной, например, красной, для контраста с цветом обычного TDD. Адгезивное покрытие на подложке (подложках) в системе устранения TDD по изобретению может быть преимущественно похожим на покрытия, используемые в TDD, и описанные ранее, или же может быть таким же. Дополнительно или альтернативно адгезивное покрытие на подложке (подложках) может включать, но не ограничиваясь этим, эпоксидные смолы, полиимиды, полиамиды, силиконы, акриловые полимеры, полимеры, включающие повторяющиеся звенья, содержащие замещнные или незамещнные фенольные группы и т.п., или сополимеры или их комбинации. Особенно предпочтительные адгезивы,которые могут быть использованы для нанесения на подложку (подложки), включают, но не ограничива- 11007240 ясь этим, клеи на основе эпоксидных смол, такие как поставляемые Durapowes, и чувствительные к давлению клеи, такие как клеи на основе акрилатов 387-2051 и 387-3054, поставляемые National Starch, и клеи на основе силиконов 7-4102, 7-4202, 7-4302, 7-4402, 7-4502 и 7-4602, поставляемые Dow Silicones.He ограничиваясь какой-либо теорией, полагают, что, по меньшей мере, на жстких подложках адгезива на основе силиконов имеют преимущества в отношении изоляции активного соединения (соединений)TDD, соединившихся с адгезивом и тем самым предотвращению, ингибирования или уменьшения их неправильного использования или злоупотребления ими, по меньшей мере, по сравнению с другими адгезивами на основе каучуков, например, такими, которые перечислены в патенте США 5,804,215. Кроме того, полагают, что могут быть предпочтительными и адгезивы на основе акрилатов. Хотя толщина адгезивного покрытия (покрытий) конкретно не ограничивается, предпочтительно,чтобы она была достаточной, чтобы по существу присоединить подложку с расположенным на ней адгезивным покрытием к TDD или к части, по меньшей мере, одной подложки, не содержащей адгезивного покрытия, или ко второй подложке, если она имеется. Например, адгезивное покрытие может, преимущественно, иметь толщину от примерно 0,0005 дюйма (13 мкм) до примерно 0,1 дюйма (2,5 мм), предпочтительно, от примерно 0,001 дюйма (25 мкм) до примерно 0,01 дюйма (250 мкм), более предпочтительно, от примерно 0,002 дюйма (50 мкм) до примерно 0,004 дюйма (100 мкм). Согласно предпочтительному варианту толщина адгезивного покрытия является достаточной, чтобы, по существу, осуществить герметизацию TDD на участках иммобилизации и изоляции и для того, чтобы, по существу необратимо, присоединить подложку с нанеснным адгезивом к самой себе, к части, по меньшей мере, одной подложки, не содержащей адгезивного покрытия, или ко второй подложке, если она имеется. Возможно и предпочтительно, система устранения TDD по изобретению содержит субстрат для адгезива, такой как снимающаяся подложка или слой, который был превращен в снимающуюся подложку путм нанесения снимающегося покрытия, расположенного на адгезивном покрытии подложки, таким образом, что субстрат может быть легко удалн с адгезивного покрытия, например, снят, когда желательно, чтобы адгезивный слой практически соединился с TDD, с самим собой, с частью, по меньшей мере, одной подложки, не содержащей адгезивного покрытия, и/или со второй подложкой, когда она имеется. Согласно одному предпочтительному варианту изобретения система устранения TDD может, преимущественно, содержать множество подложек, каждая из которых имеет адгезивное покрытие, на котором предпочтительно с возможностью удаления, расположен субстрат для адгезива или снимающееся покрытие, которое может быть легко удалено с адгезивного покрытия, например, снятием, когда желательно, чтобы адгезивный слой практически соединился с TDD, с самим собой, с частью по меньшей мере одной подложки, не содержащей адгезивного покрытия, и/или со второй подложкой, когда она имеется. Эти многочисленные подложки могут каждая соединяться, осуществлять иммобилизацию, изоляцию TDD и/или предотвращать, ингибировать или уменьшать неправильное использование одного или нескольких TDD или злоупотребление ими. Согласно другому предпочтительному варианту изобретения система устранения TDD содержит множество подложек, на каждой из которых нанесн слой адгезива, а также может содержать множество субстратов для адгезивов, каждый из которых расположен с возможностью снятия на одном из адгезивных покрытий на множестве подложек, причм множество подложек соединены вместе с образованием системы в виде буклета. Этот вариант изображн на фиг. 11. Отдельные листы, например (72) и (74), каждый включающий систему устранения TDD, соединены в форме буклета (70). Как описано подробно выше, каждый отдельный лист выполнен по меньшей мере из одной подложки с адгезивным покрытием,например (76), причм лист может содержать следующий компонент (компоненты): мономер, возможно по меньшей мере один сомономер, инициатор, возможно по меньшей мере один соинициатор, по меньшей мере один сшивающий агент, по меньшей мере один агент, деактивирующий опиоидный агонист,например, опиоидный антагонист, и их смеси. В примере, показанном на фиг. 11, защитный субстрат для адгезива, такой как снимающийся слой (78), показанный на фигуре, удаляется с каждого листа перед использованием этого листа для устранения, по меньшей мере, одного TDD. Буклет, здесь имеющий обложки (80) и (82), используется соответствующим образом, например, каждый лист применяется для устранения TDD. Если желательно, система может быть снабжена инструкцией, например, в виде слоя,снимающегося субстрата. Согласно ещ одному предпочтительному варианту система устранения TDD по изобретению содержит множество сложенных вдвое подложек, на каждой из которых нанесн адгезив, и может содержать множество субстратов для адгезива, каждый из которых расположен с возможностью удаления на одном из адгезивных покрытий на множестве подложек, причм множество подложек соединены друг с другом в форме буклета. Этот вариант показан на фиг. 12 А. Отдельные сложенные листы (для простоты показан только один из них (92, каждый из которых включает систему устранения TDD, соединены в форме буклета (90). Как подробно описано выше, каждый сложенный вдвое лист имеет, по меньшей мере, одну подложку с нанеснным на не адгезивом, причм этот лист может содержать следующий компонент (компоненты): мономер и, возможно, по меньшей мере, один сомономер, инициатор и, возможно,по меньшей мере, один соинициатор, по меньшей мере, один сшивающий агент, по меньшей мере, один- 12007240 агент, деактивирующий опиоидный агонист и их смеси. Система устранения TDD в виде буклета, содержащая множество сложенных пополам листов, используется следующим образом. На фиг. 12 В показано удаление части защитного субстрата для адгезива,такого как снимающийся слой (94), показанный на этой Фигуре, с листа, таким образом, что, по меньшей мере, одно TDD, например, использованное TDD, снятое у пациента, могло соединиться с освобожднным от субстрата адгезивным покрытием (96) листа. Предпочтительно, чтобы поверхность TDD с нанеснным адгезивным покрытием контактировала с адгезивным покрытием листа. Удалнный слой субстрата после удаления используется соответствующим образом. На фиг. 12 С показаны TDD (98) на месте адгезива листа и удаление с листа другой части защитного субстрата для адгезива, такого как снимающийся слой (100), показанный на этой фигуре. Удалнный слой субстрата после удаления используется соответствующим образом. На фиг. 12D показана часть сложенного пополам листа с адгезивом (102),причм лист сложен над TDD так, чтобы практически изолировать это TDD. Буклет после применения используется соответствующим образом, например, каждый лист был использован для устранения TDD. Этот вид системы устранения легко адаптируется для включения в предпочтительную упаковку и удовлетворяет в то же время потребность в уменьшении возможного злоупотребления. Если желательно, эта система устранения TDD может быть снабжена инструкцией, например, на подложке или на снимающемся слое. Как показано на фиг. 13, в некоторых вариантах изобретения предусмотрен набор, включающий коробку 52 для одного или нескольких пластырей и систему устранения TDD в виде буклета 54, содержащего множество подложек 56. Согласно ещ одному предпочтительному варианту система устранения TDD по изобретению имеет одно или несколько следующих свойств: практически непроницаема для растворителей, практически не набухает в растворителях, устойчива на разрыв, устойчива к разрезанию, практически герметична по отношению к участку (участкам) иммобилизации и изоляции TDD, содержащихся в системе, когда TDD содержатся в системе; практически необратимо соединена, когда подложка с нанеснным адгезивом практически приклеивается к себе самой, к части, по меньшей мере, одной подложки без адгезива, например, при складывании, или ко второй подложке, если она есть; практически является препятствием для экстракции активного вещества, например опиоидного агониста, содержащегося в TDD, или т.п. Система устранения TDD по изобретению, предпочтительно, может включать один или более (альтернативно) следующие компоненты: мономер (и возможно, сомономеры) для осуществления полимеризации, инициатор (и возможно, соинициаторы) для инициирования полимеризации, предпочтительно,при активации энергией, например УФ - видимым светом, или видимым светом, и/или термической энергией (или ИК- радиацией), по меньшей мере, один сшивающий агент для сшивки (со)полимера, по меньшей мере один агент, деактивирующий опиоидный агонист, такой как опиоидный антагонист, для противодействия, ингибирования, уменьшения или остановки проявлений эйфории от введения опиоидного агониста (агонистов), содержащихся в TDD, в случае попытки не правильно использовать или злоупотребить опиоидным агонистом (агонистами), содержащимися в TDD, или для того, чтобы сделать опиоидный агонист недоступным путм деактивации, бионедоступности, физической недоступности, потери желания ввести активное вещество лицу, злоупотребляющему им, и т.п. или сочетания этих примов; по меньшей мере, один агент, деактивирующий опиоидный агонист для химического изменения, разложения и/или деактивации опиоидного агониста (агонистов), содержащегося в TDD, для того, чтобы в случае неправильного использования или злоупотребления, проявления эйфории в результате действия опиоидного агониста (агонистов), содержащихся в TDD, по меньшей мере, временно (и предпочтительно, постоянно) в их изменнном, разложившемся и/или деактивированном виде, ингибировались,уменьшались или прекращались in vivo и т.п. Согласно ещ одному варианту система устранения TDD по изобретению может включать неопиоидный деактивирующий агент. Если эти возможные компоненты содержатся, они могут быть включены в любую часть системы устранения TDD по изобретению таким образом, чтобы эти возможные компоненты могли контактировать с TDD, как только TDD окажется в системе устранения TDD по изобретению. Согласно одному предпочтительному варианту эти возможные компоненты растворены или диспергированы в адгезивном покрытии, находящемся, по меньшей мере, на одной подложке. Дополнительно или альтернативно, эти возможные компоненты могут содержаться во второй подложке, если она есть, и/или на е поверхности. Согласно одному варианту по меньшей мере один из возможных компонентов находится на первом участке адгезивного покрытия, на по меньшей мере одной подложке и/или на второй подложке, если она есть, в то время как другой из возможных компонентов находится на втором участке адгезивного покрытия на по меньшей мере одной подложке и/или на второй подложке, если она есть. Согласно другому варианту все возможные компоненты, которые содержатся в системе, расположены на одном и том же участке адгезивного покрытия на по меньшей мере одной подложке и/или на второй подложке, если она есть. Мономер и/или сомономер (сомономеры), если они содержатся, которые могут быть в система устранения TDD согласно изобретению, могут включать любой мономер и/или сомономер (сомономеры),которые могут быть применены для получения, например, адгезивного слоя (покрытия) в системе устра- 13007240 нения TDD и/или в TDD, мембраны, регулирующей скорость, в TDD, материала по меньшей мере одной из подложек и т.п., или смесь (со)мономеров. Примеры мономеров/сомономеров включают, но не ограничиваясь этим, диизоцианаты, диолы, дикислоты (предпочтительно, карбоксильные), диэфиры, диамины, эпоксидные соединения, диэпоксидные соединения, цианакрилаты, (мет)акриловую кислоту, соли одновалентных металлов и (мет)акрилатов, органические (мет)акрилаты, винилацетат, предшественники винилового спирта, мономеры/ олигомеры целлюлозы (например, ацетат целлюлозы, пропионат целлюлозы, бутират целлюлозы, ацетатпропионат целлюлозы, ацетатбутират целлюлозы, пропионатбутират целлюлозы, нитрат целлюлозы, метилцеллюлозу, этилцеллюлозу, карбоксиметилцеллюлозу, карбоксиэтилцеллюлозу, соли целлюлозы и сочетания их сополимеров, которые могут быть модифицированы,например, частично или полностью этерифицированы, частично или полностью регенерированы, частично или полностью модифицированы введением групп простых эфиров, частично или полностью подкислены, частично или полностью нейтрализованы по кислотным группам и т.п.), стабильные при комнатной температуре -олефины, силиконсодержащие мономеры (например, органосиланы, силоксаны и т.п. или их сочетание), фосфазены и т.п. и любые сочетания этих мономеров. Инициатор и/или (со)инициатор (соинициаторы), если они есть, которые могут быть включены в систему устранения TDD по изобретению, включают любые инициаторы/(со)инициаторы, известные из уровня техники, для инициирования (со)полимеризации мономера (и/или (со)мономера (сомономеров,имеющихся в системе устранения TDD по изобретению и, предпочтительно, подбираются для конкретного мономера/сомономера (сомономеров). Специалист может легко осуществить такой выбор, осуществив ограниченное число обычных экспериментов, если это требуется. Примеры инициаторов/ соинициаторов включают, не ограничиваясь этим, моноамины (например, для инициирования полимеризации эпоксидных соединений), соединения, образующие свободные радикалы (например, перекиси, бисазосоединения и т.п., такие как для инициирования полимеризации -олефинов, (мет)акриловых кислот или их металлических солей, (мет)акрилатов и т.п.), особенно, те соединения, которые активируются при помощи УФ, фото- или термически и т.п., и любые их сочетания. Многие типы свободно-радикальных инициаторов пригодны для инициирования сшивки, например, азо- и диазосоединения, такие как азо-бис-изобутиронитрил (AIBN), органические перекиси, гидроперекиси, персульфаты и гидроперсульфаты, такие как перекись бензоила, неорганические перекиси,персульфаты, такие как перекисно-восстановительные системы, углерод-углеродные инициаторы, такие как гексазамещнные этаны, и фотоинициаторы; многочисленные примеры известны из уровня техникиand Sons, New York, 1995, vol. 14, p.p. 431-460, включена в данное описание в качестве ссылки). Подходящие анионные инициаторы для инициирования сшивки известны из уровня техники и включают ароматические радикальные анионы, такие как натриевая соль нафталина, алкиллитиевые соединения, например трет.бутиллитий, флуорениловые карбанионы, 1,1-дифенилметилкарбанионы, кумил калия и инициаторы, описанные Quirk et. al., Initiators (Anionic) in Kirk-Othmer Encyc. of Chem. Technol., 4th Ed.,John Wiley and Sons, New York, 1995, vol. 14, p.p. 461-476, включено в данное описание в качестве ссылки. Подходящие катионные инициаторы для инициирования сшивки также известны из уровня техники и включают протоновые кислоты, системы донор катионов (инициатор)/кислоты Фриделя-Крафтса (соинициатор), стабильные соли катионов и инициаторы, описанные Faust, Initiators (Cationic) in KirkOthmer Encyc. of Chem. Technol., 4th Ed., John Wiley and Sons, New York, 1995, vol. 14, p.p. 476-482, включено в данное описание в качестве ссылки. Свободно-радикальный, анионный или катионный инициатор может подвергаться распаду любыми известными средствами, например, термически или фотолитически, когда это требуется для инициирования полимеризации и/или сшивки. В частности, можно назвать фотоинициаторы, такие как описанные в McGinniss Radiation Curing в Kirk-Othmer Encyc. of Chem. Technol., 4th Ed., John Wiley and Sons, NewYork, 1996, vol. 20, p.p. 848-850, также включено в данное описание в качестве ссылки. Например, соединения, образующие свободные радикалы, могут включать, никоим образом не ограничиваясь этим, перекись дикумила (коммерчески доступную под маркой PEROXEMON DC 400KEP в Elf Atochem N. А., и как ESPERAL 115 G в Witco), 1,1-ди(трет.бутилперокси)-3,3,5-триметилциклогексан (например, коммерчески доступный как VAROX 231XL в R.T. Vanderbilt и как LUPERCO 231 КЕ в Elf Atochem N. А.), ,'-бис(трет.бутилперокси)-диизопропилбензол (например, коммерчески доступный как RETILOX F40KEP в Elf Atochem N. А.), 2,5-диметил-2,5-ди (трет.бутилперокси)гексан(например, коммерчески доступный как VAROX DBPH-50 в R. T. Vanderbilt и как LUPERCO 101-XL в Elf Atochem N. А.), ди(трет.бутил)перекись (например, коммерчески доступная в Witco), 2,5-диметил 2,5-ди(трет.бутилперокси)-3-гексин, перекись трет.бутилкумила, н-бутил-(4,4-дитрет.бутилперокси)валерат, трет.амилпероксибензоат, 4,4-азобис-(4-циановалерьяновая кислота), 1,1'-азобис(циклогексанкарбонитрил), 2,2'-азобисизобутилтиронитрил, перекись бензоила, 2,2-бис-(трет. бутилперокси)бутан, 1,1 бис(трет.бутилперокси)циклогексан, 2,5-бис-(трет.бутилперокси)-2,5-диметилгексан, бис[1-(трет.бутилперокси)-1-метилэтил]бензол, гидроперекись трет.бутила, трет.бутилперацетат, трет.бутилпероксиизопропилкарбонат, перекись трет.бутила, трет.бутилпербензоат, гидроперекись кумила, гидроперекись- 14007240 циклогексанона, гидроперекись лаурила, гидроперекись стеарата, перекись 2,4-пентандиона, перуксусную кислоту и т.п. или любое их сочетание. Полимеризацию и/или сшивку можно, конечно, осуществлять при помощи источников ионизирующего облучения высокой энергии. Например, сшивка может быть осуществлена путм облучения полимера (полимеров) и мономера (мономеров), особенно, мономера (мономеров) со средней функциональностью более 2, пучком электронов, УФ-светом, обычно в присутствии фотоинициатора, и ионизирующим облучением высокой энергии, например, гамма-облучением 60 Со и 137Cs, -частицами, -частицами, быстрыми нейтронами и Х-лучами (рентген). Каждый из этих методов может вызвать образование свободных радикалов и/или ионов, которые, в свою очередь, инициируют полимеризацию и/или сшивку (см. Sanchez et. al., Initiators (Free-Radical), p.p. 454-457;York, 1981, vol. 13, p.p.367-370, включены в данное описание в качестве ссылок). Из уровня техники хорошо известны, по меньшей мере, три следующих метода радиационной сшивки или прививки: (1) предварительное облучение, когда полимер облучается до взаимодействия с мономером (мономерами); (2) взаимное облучение, когда полимер и мономер (мономеры) находятся в контакте, когда осуществляется облучение; и (3) перекисный метод, когда полимер облучают в присутствии воздуха или кислорода до взаимодействия с мономером (мономерами) (см. Stannett et al.,Polymerization by High-Energy Radiation в Comprehensive Polymer Science, Pergamon Press, Oxford, 1989,vol. 4, Eastmond et al., Eds., p. 327-334, включено в качестве ссылки в данное описание). Таким образом, свободно-радикальными инициирующими средствами для сшивки и/или полимеризации, которые могут действовать путм термической и/или фотолитической диссоциации, могут быть инициаторы, выбранные из группы, состоящей из азосоединений, диазосоединений, органических перекисей, органических гидроперекисей, органических персульфатов, органических гидроперсульфатов,неорганических перекисей, неорганических персульфатов, окислительно-восстановительных систем,углерод-углеродных инициаторов, фотоинициаторов и их смесей. Сшивающий агент (агенты), если они есть, который может быть включн в систему устраненияTDD по изобретению, может, преимущественно, включать любой сшивающий агент, известный из уровня техники для химической или физической сшивки мономера (и/или сомономера (сомономеров или олигомеров и/или (со)полимеров, образующихся из них в системе устранения TDD по изобретению, и,предпочтительно, выбирается для конкретных (со)мономеров/ олигомеров/(со)полимеров. Специалист способен сделать такой выбор путм осуществления ряда рутинных экспериментов, если это требуется. Сшивающие агенты, предпочтительно, содержат или (а) функциональную группу(группы), способную реагировать со многими функциональными группами, содержащимися в полимере или являющимися боковыми уже образовавшихся олигомера или (со)полимера, или (б) полимеризующуюся группу (группы), способную реагировать со многими концами цепей олигомера или (со)полимера, образуя тем самым сшивки между цепями олигомера или (со)полимера. Примеры сшивающих агентов включают, но не ограничиваются этим, соединения, имеющие в среднем один или несколько следующих фрагментов: более двух изоцианатных функциональных групп,более двух гидроксильных функциональных групп, более двух сложноэфирных групп (например, для реакций переэтерификации или этерификации), более двух кислотных (предпочтительно, карбоксильных) функциональных групп, более двух функциональных аминогрупп (то есть каждая имеет, по меньшей мере, один реакционноспособный сайт), одну или несколько эпоксидных функциональных групп,более одной способной к полимеризации ненасыщенной группы, более двух групп карбоксилата одновалентного металла и т.п. или комбинацию перечисленных функциональных групп. Сшивающие агенты могут также реагировать с ранее неактивным сайтом в уже образовавшемся олигомере или (со)полимере с целью его активации. Затем этот активный сайт может сам реагировать с реакционноспособным или до того неактивным сайтом в цепи другого уже образовавшегося олигомера или (со)полимера. Или же этот реакционноспособный сайт может реагировать с другими соединениями,содержащимися в системе устранения TDD по изобретению, например, мономерами/сомономерами, перечисленными выше, которые могут взаимодействовать с реакционноспособным или ранее неактивным сайтом в цепи другого уже образовавшегося олигомера или (со)полимера. Согласно изобретению в систему устранения TDD по изобретению может быть включн, по меньшей мере, один агент, деактивирующий активное вещество. Например, может быть любой агент, деактивирующий опиоидный агонист, который при этом химически изменяет, разлагает и/или деактивирует опиоидный агонист (агонисты), содержащийся в TDD, с тем, чтобы в случае неправильного использования или злоупотребления проявления эйфории от опиоидного агониста (агонистов), содержащегося вTDD, по меньшей мере, временно (предпочтительно, постоянно в его изменнном, разложившемся или деактивированном виде) ингибировались, уменьшались или прекращались in vivo. Агент, деактивирующий опиоидный агонист, если он содержится, предпочтительно, выбирается конкретно для конкретного опиоидного агониста (агонистов), содержащихся в TDD, хотя определнные агенты, деактивирующие опиоидный агонист, вызывают химическое изменение, разложение и/или деактивацию многих обычных опиоидных агонистов. Специалист в данной области сможет сделать конкретный вывод путм проведения ограниченного числа рутинных экспериментов, если это потребуется.- 15007240 Примеры агентов, деактивирующих активное вещество, включают, но не ограничиваются этим,сильно окисляющиеся соединения и очень реакционноспособные соединения, образующие свободные радикалы, например, такие как перекиси, надкислоты, пер(окиси металлов), пер(окиси неметаллов), азосоединения, перечисленные в качестве инициаторов (и/или соинициаторов) выше или их сочетание. Дополнительно или альтернативно, деактивирующие агенты могут включать, но не ограничиваясь этим,перекись водорода, пер(окислы неметаллов) кислоты, такие как периодная кислота и т.п. или их сочетание. Другим примером агента, деактивирующего активное вещество, который может содержаться, является опиоидный антагонист. По меньшей мере один агент, деактивирующий опиоидный агонист, который может быть включн в систему устранения TDD по изобретению, может являться любым агентом,деактивирующим опиоидный агонист, известным из уровня техники, таким как опиоидный антагонист,противодействующим, ингибирующим, уменьшающим или прекращающим проявления эйфории in vivo,вызванные опиоидным агонистом (агонистами), содержащимся в TDD, в случае попытки неправильно использовать или злоупотребить опиоидным агонистом (агонистами), содержащмися в TDD. Агент, деактивирующий опиоидный агонист, если он содержится, предпочтительно, подбирается для конкретного опиоидного агониста (агонистов), содержащегося в TDD, хотя некоторые деактивирующие агенты противодействуют проявлениям эйфории, вызванным многими обычными опиоидными агонистами. Специалист в данной области сможет сделать такой выбор путм проведения ограниченного числа экспериментов, если это потребуется. Агенты, деактивирующие опиоидные агонисты, могут сделать активный агент недоступным за счт инактивации, такой как, например, химическая инактивация, изменение сайта опиоидного агониста, связывающего рецептор, механическая инактивация или изменение сайта опиоидного агониста, связывающего рецептор; бионедоступности, физической недоступности; потери стремления лица, злоупотребляющего активным веществом, принять опиоидный агонист, например, деактивирующий агент создат непереносимо плохой вкус и непереносимую реакцию, например, сильную тошноту или т.п., что-нибудь похожее и любую комбинацию таких реакций. Например, для опиоидного агониста в трансдермальном пластыре или другом средстве для доставки, которое нужно устранить путм помещения его в систему устранения TDD по изобретению деактивирующим агентом может быть химический или денатурирующий агент, который приведт к изменению остаточных молекул опиоида в дозированной форме и сделает их неактивными. Деактивирующий агент альтернативно или дополнительно может быть опиоидным рецептором, который связывает остаточный опиоид с образованием комплекса нерастворимый лиганд - рецептор. Деактивирующий агент альтернативно или дополнительно может быть антагонистом опиоидного рецептора, предпочтительно, с большей специфичностью и/или сродством к рецептору, чем опиоид, который будет изолирован или доставлен с остаточным опиоидом при неправильном использовании/злоупотреблении с целью соревнования с остаточным опиоидом за опиоидный рецептор, тем самым сводится на нет неправильное использование или злоупотреблении опиоидом. Деактивирующий агент альтернативно или дополнительно может физически захватить остаточный опиоидный агонист, например, в непроницаемой микросфере или в постоянно связанной матрице. Точно также деактивирующий агент может альтернативно или дополнительно являться неопиоидным с неприятными и дисфорическими свойствами, когда он абсорбируется, что делает неправильное употребление/ злоупотребление нежелательным. Примеры деактивирующих агентов включают, никоим образом не ограничиваясь этим, -опиоидный рецептор крысы или человека, антитела, нейтрализующие опиоид, опиоидные/наркотические антагонисты, такие как налоксан, налтрексон, налмефен, циклазацин, циклазоцин, налорфин, налбуфин, леваллорфан, буторфанол, пентазоцин и т.п. или их сочетание; дисфорические или раздражающие агенты,такие как скополамин, кетамин, атропин, горчичные масла и т.п. или их сочетание. Согласно одному варианту система устранения TDD по изобретению может включать не-опиоидный деактивирующий агент, который может представлять собой, не ограничиваясь этим, копиоидный рецептор крысы или человека, -опиоидный рецептор крысы или человека; налтриндол, норбиналторфимин, J-113397 (описанный Ozaki et al., (2000) Eur. J. Pharmacol., 402:45); JTC-801 (описанныйet al., (2002) Br. J. Pharmacol., 136:303) и их сочетание. Другие подходящие неопиоидные деактивирующие агенты хорошо известны специалистам. Следует отметить, что некоторые компоненты могут преимущественно выбираться с целью выполнения нескольких функций в трансдермальных системах устранения средств доставки по изобретению. Например, при введении перекиси в систему, эта перекись может действовать как деактивирующий агент для фармацевтического соединения (соединений) в TDD, такого как опиоидный агонист, а также действовать как инициатор и/или соинициатор (соинициаторы), если он содержится, для инициированияTDD. Если мономер содержится в системе устранения TDD по изобретению, то общее количество моно- 16007240 мера (включая сомономеры) может составлять от примерно 0,01% до примерно 15%, предпочтительно от примерно 0,1% до примерно 10% или же от примерно 0,1% до примерно 5% по весу в расчте на общий вес слоя, в котором или на поверхности которого содержится мономер. Если в системе устранения TDD по изобретению содержится инициатор, то общее количество инициатора (включая соинициаторы) может составлять от примерно 0,01% до примерно 15%, предпочтительно от примерно 0,1% до примерно 10% или же от примерно 0,1% до примерно 5% по весу в расчте на общий вес слоя, в котором или на поверхности которого содержится инициатор. Если в системе устранения TDD по изобретению содержится сшивающий агент, то общее количество сшивающего агента может составлять от примерно 0,1% до примерно 20%, предпочтительно от примерно 0,5% до примерно 10% или же от примерно 1% до примерно 5% по весу в расчте на общий вес слоя, в котором или на поверхности которого содержится сшивающий агент. Если в системе устранения TDD по изобретению содержится деактивирующий агент, то общее количество деактивирующего агента может составлять от примерно 0,001% до примерно 25%, предпочтительно от примерно 0,01% до примерно 15% или же от примерно 0,1% до примерно 5% по весу в расчте на общий вес слоя, в котором или на поверхности которого содержится деактивирующий агент. Если в системе устранения TDD по изобретению содержится деактивирующий агент, то общее количество деактивирующего агента может составлять от примерно 0,001% до примерно 15%, предпочтительно от примерно 0,01% до примерно 10% или же от примерно 0,1% до примерно 5% по весу в расчте на общий вес слоя, в котором или на поверхности которого содержится деактивирующий агент. Кроме того, или альтернативно, некоторые аспекты системы устранения TDD по изобретению или любых е компонентов описаны в сопутствующей заявкеPCT/US02/12920, США, поданной 23 апреля 2002 года и в предварительных заявках США 60/285,862 и 60/292,601, поданных, соответственно, 23 апреля 2001 года и 22 мая 2001 года, на приоритет которых претендует данная заявка PCT. Соответственно вышеуказанные заявки PCT и предварительная заявка включены в данное описание в качестве ссылок. Другой аспект данного изобретения относится к способу устранения TDD и/или предотвращения неправильного использования или злоупотребления компонентом TDD (например, опиоидным агонистом). Способ включает получение системы устранения TDD по изобретению, включающей, по меньшей мере, одну подложку, на которую нанесено адгезивное покрытие. Если имеется только одна подложка,на которую нанесн адгезив, она, предпочтительно, является гибкой, для того, чтобы она была способна складываться для иммобилизации и изоляции TDD, помещнного в систему. Или же, если есть только одна подложка, на которую нанесн адгезив, может иметься вторая дополнительная подложка, причм вторая подложка, предпочтительно, способна необратимо соединяться с, по меньшей мере, одной подложкой с адгезивным покрытием. Согласно этому альтернативному варианту подложка, на которую нанесн адгезив, и вторая дополнительная подложка могут быть гибкими или жсткими, если это желательно. Подложки и адгезивы, преимущественно такие, какие описаны выше. Может быть, и это предпочтительно, предусмотрен субстрат для адгезива или снимающееся покрытие, расположенное с возможностью снятия на адгезивном покрытии на подложке, этот субстрат может быть легко удалн с адгезивного покрытия, например, снят, когда желательно, чтобы адгезивный слой практически приклеивался к самому себе, к части по меньшей мере одной подложки, на которой не содержится адгезивного покрытия, или ко второй подложке, если она есть. Способ далее включает помещение TDD на участок адгезивного покрытия и по существу закрытиеTDD на этом участке с целью иммобилизации и изоляции на нм TDD, или за счт складывания подложки таким образом, чтобы адгезивный слой практически приклеивался к самому себе, к части, по меньшей мере, одной подложки, на которой не содержится адгезивного покрытия, или при контактировании адгезивного покрытия на подложке со второй подложкой с тем, чтобы адгезивное покрытие практически приклеилось ко второй подложке. Дополнительно или альтернативно способ может также включать практически необратимое соединение TDD по меньшей мере с одним участком адгезивного покрытия или по меньшей мере с одной подложкой для иммобилизации и изоляции TDD и затем образования области иммобилизации и изоляции, в которой может содержаться TDD. Возможно и предпочтительно, способ может также включать введение одного или нескольких следующих компонентов в систему устранения TDD по изобретению: мономера (и возможно, сомономеров), который полимеризуется с получением (со)полимера; инициатора (и возможно, соинициаторов) для инициирования полимеризации (со)мономеров, предпочтительно, путм активации энергией, например УФ-светом, УФ-видимым светом или видимым светом и/или термической энергией (или инфракрасным облучением); по меньшей мере, одного сшивающего агента для сшивки (со)полимера; по меньшей мере,одного агента, деактивирующего опиоидный агонист, для противодействия, ингибирования, уменьшения или прекращения проявлений эйфории, вызванных опиоидным агонистом (агонистами), содержащимся вTDD, или для того, чтобы сделать опиоидный агонист недоступным за счт инактивации, бионедоступности, физической недоступности, потери стремления лица, злоупотребляющего активным веществом,употребить последнее и т.п. или для сочетания этих механизмов; по меньшей мере, одного агента, деактивирующего опиоидный агонист, для химического изменения, разложения и/или деактивации опиоид- 17007240 ного агониста (агонистов), содержащегося в TDD, с тем, чтобы в случае неправильного использования или злоупотребления проявления эйфории, вызванные опиоидным агонистом (агонистами), содержащимся в TDD, по меньшей мере, временно (предпочтительно, постоянно в его изменнном, разложившемся и/или деактивированном виде), ингибировались, уменьшались или прекращались in vivo и т.п. Если эти возможные компоненты содержатся, они могут находиться внутри или на поверхности любого участка системы устранения TDD по изобретению для того, чтобы эти возможные компоненты могли войти в контакт с TDD, как только TDD будет помещено в систему устранения по изобретению. Согласно одному предпочтительному варианту эти возможные компоненты растворены или диспергированы в адгезивном покрытии, содержащемся по меньшей мере на одной подложке. Согласно другому предпочтительному варианту эти возможные компоненты растворены или диспергированы в, по меньшей мере, одной подложке. Дополнительно или альтернативно, эти возможные компоненты могут быть предусмотрены в и/или на поверхности второй подложки, если она есть. Согласно одному предпочтительному варианту способ предусматривает многочисленные подложки, каждая из которых имеет слой адгезивного покрытия, на котором, предпочтительно с возможностью снятия, расположены субстрат для адгезивного покрытия или снимающееся покрытие, такое, которое может быть легко удалено с поверхности адгезивного покрытия, например, снято, когда желательно,чтобы слой адгезива практически соединился с TDD, с самим собой, с частью, по меньшей мере, одной подложки, которая не содержит адгезивного покрытия, или со второй подложкой, если она есть. Эти многочисленные подложки могут, преимущественно каждая, соединиться с TDD для иммобилизации,изоляции и/или предотвращения, ингибирования или уменьшения неправильного использования или злоупотребления одним или более TDD. Согласно другому предпочтительному варианту способ предусматривает систему устранения TDD,включающую множество подложек, на каждую из которых нанесено адгезивное покрытие, которая может также включать множество субстратов для адгезивных слоев, каждый из которых с возможностью снятия расположен на одном из адгезивных покрытий на многих подложках, причм множественные подложки соединены друг с другом в виде буклета. Эти множественные подложки буклета могут каждая присоединяться к TDD для иммобилизации, изоляции и/или предотвращения, ингибирования или уменьшения неправильного использования или злоупотребления одним или более TDD. Примеры Нижеследующие примеры служат для иллюстрации изобретения, не ограничивая его объм. Пример 1. В примере 1 трансдермальное средство доставки, показанное на фиг. 2 В, содержало бупренорфин (BUP). Конкретное TDD с BUP, используемое в примере 1, по составу похоже на средства,продаваемые в Европе Graenenthal of Switzerland под маркой TRANSTEC, но содержало только 20 мг общей дозы BUP (и, следовательно, площадь поверхности отличалась от коммерчески доступных TDD).TDD, содержащее BUP, затем иммобилизовали и изолировали в системе устранения TDD, показанной на фиг. 1B. Затем определяли количество BUP, экстрагируемое из TDD (и тем самым потенциально доступное для злоупотребления им) и содержащееся в системе устранения TDD, путм экстракции с применением следующих растворителей: дистиллированной воды, водопроводной воды, 0,026 М-ного водного раствора соды, 5%-ного уксуса, ацетона, метанола, этанола, этилацетата или этилового эфира. Экстракцию осуществляли при следующих условиях экстракции: через 5 мин, 60 мин и 120 мин после выдержки в растворителе при комнатной температуре, около 25 С. При применении для экстракции каждого растворителя TDD находилось в следующем состоянии изоляции: (1) без складывания подложки TDD (открытая поверхность), (2) со сложенной подложкой, приклеенной к самой себе (сложенная сверху), (3) с подложкой, сложенной и приклеенной к себе самой и затем разрезанной примерно на 10 и примерно на 50 частей (сложенная и разрезанная) и (4) без складывания подложки, причм подложка TDD приклеена к слою адгезива в системе устранения TDD (средство прикреплено стороной с адгезивом, расположенной внизу) (покрыто плнкой адгезива). Система устранения TDD состояла из плнки полиэтилентерефталата/сополимера этилена с винилацетатом толщиной примерно 46 мкм, полученной из 3 М Company (9733), на которой нанесено чувствительное к давлению силиконовое адгизивное покрытие, поставляемое Dow Silicones ( 7-4302), толщиной примерно 220 мкм. Для защиты адгезивного слоя на него нанесена снимающаяся полиэтилентерефталатная плнка толщиной примерно 74 мкм, поставляемая ЗМ Company (1022). Снимающуюся плнку удаляли незадолго до того, как система устранения TDD соединилась с BUP TDD. Каждая из фиг. 5-10 показывает количество BUP, экстрагируемое дистиллированной водой, этилацетатом, этанолом, этиловым эфиром, ацетоном и метанолом, соответственно, из TDD, находящегося в вышеуказанных состояниях изоляции. В табл. 1 ниже, на основании которой были построены диаграммы на фиг. 5-10, приведены данные для каждого примера экстракции. Пример 2. Для примера 2 использовали TDD, показанное на фиг. 2 В и содержащее BUP, как в примере 1. Затем осуществляли иммобилизацию и изоляцию BUP TDD в системе устранения TDD, показанной на фиг. 1 С. Затем определяли количество BUP, экстрагируемое из TDD (и тем самым потенциально доступное для злоупотребления им) и содержащееся в системе устранения TDD, путм экстракции с применением следующих растворителей: дистиллированной воды, водопроводной воды, 0,026 М-ного водного раствора соды, 5%-ного уксуса, ацетона, метанола, этанола, этилацетата или этилового эфира. Экстракцию осуществляли при следующих условиях экстракции: через 5 мин, 60 мин и 120 мин после выдержки в растворителе при комнатной температуре, около 25 С и при отгонке с обратным холодильником (то есть примерно при температуре кипения растворителя). Для каждого растворителя применялиTDD, находящееся в следующих состояниях изоляции: (1) без присоединения первой подложки (она уже приклеена к TDD) ко второй подложке (средство приклеено со слоем адгезива сверху) (открытая поверхность), (2) с TDD, расположенным и приклеенным между первой и второй подложками (сэндвич), (3) с TDD, приклеенным к первой и второй подложкам (расположенным между ними) и затем разрезанным на примерно 10 и примерно 50 частей (сложена и разрезана) и (4) без присоединения первой подложки (уже приклеенной к TDD) ко второй подложке (средство присоединено со слоем адгезива внизу) (покрыто плнкой адгезива). Система устранения TDD, используемая в этом примере, состоит из подложки-плнки из полиэтилентерефталата/сополимера этилена с винилацетатом, толщиной примерно 46 мкм, поставляемой 3 МCompany ( 9733), на которую нанесена адгезивная смесь. Эта смесь включает около 95 вес.% адгезива на основе акрилатов, поставляемого Solutia ( 2464), в сочетании с примерно 5 вес.% перекиси бензоила(в расчте на содержание тврдых веществ в смеси). Покрытие из адгезивной смеси имело толщину примерно 150-350 мкм. Для защиты слоя адгезива на него наносили снимающуюся полиэтилентерефталатную плнку толщиной около 50-100 мкм, поставляемую 3 М Company ( 1022). Эта снимающаяся плнка была удалена перед тем, как система устранения TDD была приклеена к TDD, содержащему активный агент. Объм данного изобретения не ограничен конкретными примерами, описанными в данном описании. Специалистам в данной области очевидно, что на основе данного описания и сопровождающих его фигур можно осуществить различные модификации данного изобретения. Такие модификации не выходят за рамки данного изобретения, объм которого определяется формулой изобретения. Все патенты, заявки, публикации, методы испытаний, литература и другие материалы, упомянутые в данном описании, включены в него в качестве ссылок.- 19007240 ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Система дезактивации активного вещества в трансдермальном средстве доставки, включающая по меньшей мере одну подложку, на поверхность которой нанесено адгезивное покрытие, и один или более следующих компонентов, содержащихся, по меньшей мере, в адгезивном покрытии или на его поверхности, или в первой подложке или на е поверхности, или их любое сочетание:(а) по меньшей мере один мономер и, возможно, по меньшей мере один инициатор,(б) по меньшей мере один сшивающий агент и, возможно, по меньшей мере один инициатор,(в) по меньшей мере один агент, дезактивирующий активное вещество. 2. Система по п.1, отличающаяся тем, что она дополнительно включает вторую подложку, которая способна приклеиваться к адгезивному покрытию на первой подложке. 3. Система по п.2, отличающаяся тем, что адгезивное покрытие расположено на одной стороне второй подложки. 4. Система по п.3, отличающаяся тем, что она дополнительно включает один или более следующих компонентов, содержащихся, по меньшей мере, в адгезивном покрытии на второй подложке или на его поверхности, или во второй подложке или на е поверхности, или любое их сочетание:(а) по меньшей мере один мономер и, возможно, по меньшей мере один инициатор,(б) по меньшей мере один сшивающий агент и, возможно, по меньшей мере один инициатор,(в) по меньшей мере один агент, дезактивирующий активное вещество. 5. Система по п.3, отличающаяся тем, что по меньшей мере одна из первой и второй подложек является жсткой. 6. Система по п.3, отличающаяся тем, что и первая, и вторая подложки являются жсткими. 7. Система по п.5, отличающаяся тем, что по меньшей мере одна из первой и второй подложек не является плоской. 8. Система по п.6, отличающаяся тем, что и первая, и вторая подложки не являются плоскими. 9. Система по п.7, отличающаяся тем, что по меньшей мере одна из первой и второй подложек имеет углубление, конфигурация и размеры которого позволяют разместить в нм трансдермальное средство доставки. 10. Система по п.1, отличающаяся тем, что первая подложка характеризуется одним или несколькими из следующих свойств:(а) по существу непроницаема для растворителей;(б) по существу не набухает в растворителях;(г) является стойкой к разрезанию. 11. Система по п.1, отличающаяся тем, что содержащийся в ней компонент или компоненты включают мономер. 12. Система по п.11, отличающаяся тем, что содержащийся в ней компонент или компоненты включают по меньшей мере один сомономер. 13. Система по п.11, отличающаяся тем, что содержащиеся в ней компоненты дополнительно включают инициатор. 14. Система по п.11, отличающаяся тем, что содержащиеся в ней компоненты дополнительно включают по меньшей мере один сшивающий агент. 15. Система по п.14, отличающаяся тем, что содержащиеся в ней компоненты дополнительно включают по меньшей мере один агент, дезактивирующий активное вещество. 16. Система по п.15, отличающаяся тем, что агент, дезактивирующий активное вещество, представляет собой -опиоидный антагонист. 17. Система по п.1, отличающаяся тем, что она дополнительно включает по меньшей мере один субстрат для адгезива, расположенный с возможностью снятия на адгезивном покрытии на первой подложке таким образом, чтобы этот субстрат для адгезива можно было легко удалить с адгезивного покрытия. 18. Набор, включающий трансдермальное средство доставки, которое содержит по меньшей мере один активный агент, и систему для дезактивации активного агента, которая включает:(i) по меньшей мере одну подложку, на одной стороне которой имеется адгезивное покрытие, и(ii) один или несколько из следующих компонентов, содержащихся, по меньшей мере, в адгезивном покрытии или на его поверхности, или в первой подложке или на е поверхности, или любое сочетание этих компонентов:(а) по меньшей мере один мономер и, возможно, по меньшей мере один инициатор,(б) по меньшей мере один сшивающий агент и, возможно, по меньшей мере один инициатор,(в) по меньшей мере один агент, дезактивирующий активное вещество. 19. Набор по п.18, отличающийся тем, что он дополнительно включает коробку, в которой находится трансдермальное средство доставки, а трансдермальная система устранения этого средства прикреплена с возможностью снятия на наружной части коробки.- 20007240 20. Набор по п.19, отличающийся тем, что один край первой подложки и один край второй подложки соединены с образованием буклета. 21. Набор по п.20, отличающийся тем, что каждая из первой и второй подложек являются жсткими и неплоскими. 22. Набор по п.21, отличающийся тем, что по меньшей мере одна из первой и второй подложек имеет углубление для размещения в нм трансдермального средства доставки. 23. Набор по п.20, отличающийся тем, что трансдермальное средство доставки, первая подложка и вторая подложка имеют одну сторону, размер которой имеет примерно ту же величину, что и одна сторона других из этих элементов. 24. Набор, включающий трансдермальное средство доставки, содержащее по меньшей мере одно активное вещество и по меньшей мере первую жсткую подложку, содержащую адгезивное покрытие на по меньшей мере одной стороне. 25. Набор по п.24, отличающийся тем, что он дополнительно содержит вторую жсткую неплоскую подложку, содержащую адгезивное покрытие по меньшей мере на одной стороне. 26. Набор по п.24, отличающийся тем, что первая подложка и вторая подложка имеют каждая углубление такой конфигурации и таких размеров, которые позволяют разместить в нм трансдермальное средство доставки, причм адгезивные покрытия на первой и второй подложках расположены по меньшей мере на части первой подложки и на части второй подложки, которые ограничивают углубления. 27. Набор по п.24, отличающийся тем, что он дополнительно включает один или несколько из следующих компонентов, содержащихся по меньшей мере в первой подложке или на е поверхности, во второй подложке или на е поверхности, в адгезивном покрытии по меньшей мере на одной стороне первой подложки, в адгезивном покрытии по меньшей мере на одной стороне второй подложки или в любом сочетании этих элементов:(а) по меньшей мере один мономер и, возможно, по меньшей мере один инициатор,(б) по меньшей мере один сшивающий агент и, возможно, по меньшей мере один инициатор,(в) по меньшей мере один агент, дезактивирующий активное вещество. 28. Набор, включающий трансдермальное средство доставки, содержащее бупренорфин или любую фармацевтически приемлемую форму или любое фармацевтически приемлемое производное бупренорфина и по меньшей мере одну подложку, содержащую на одной стороне адгезивное покрытие. 29. Набор, включающий трансдермальное средство доставки, содержащее фентанил или любые фармацевтически приемлемые форму или производное фентанила и по меньшей мере одну подложку,содержащую на одной стороне адгезивное покрытие. 30. Набор, включающий трансдермальное средство доставки, содержащее оксикодон или любые фармацевтически приемлемые форму или производное оксикодона и по меньшей мере одну подложку,содержащую на одной стороне адгезивное покрытие. 31. Система дезактивации активного вещества в трансдермальном средстве доставки, включающая по меньшей мере первую подложку, содержащую адгезивное покрытие на одной е стороне, причм адгезив представляет собой клей на основе силиконов. 32. Система дезактивации активного вещества в трансдермальном средстве доставки, включающая по меньшей мере первую подложку, содержащую адгезивное покрытие на одной е стороне, причм адгезив представляет собой клей на основе акрилатов. 33. Способ дезактивации активного вещества в трансдермальном средстве доставки, включающий присоединение трансдермального средства доставки к адгезивному покрытию на первой подложке системы устранения трансдермального средства доставки по п.1. 34. Способ дезактивации активного вещества в трансдермальном средстве доставки, включающий присоединение трансдермального средства доставки к адгезивному покрытию на одной стороне первой подложки, причм, по меньшей мере, в адгезивном покрытии на первой подложке или на его поверхности, или в первой подложке или на е поверхности, или в любом сочетании этих элементов содержатся один или несколько из следующих компонентов:(а) по меньшей мере один мономер и, возможно, по меньшей мере один инициатор,(б) по меньшей мере один сшивающий агент и, возможно, по меньшей мере один инициатор,(в) по меньшей мере один агент, дезактивирующий активное вещество,присоединение трансдермального средства доставки к адгезивному покрытию, расположенному на одной стороне второй подложки, при этом вторая подложка способна приклеиваться к адгезивному покрытию на первой подложке, причм, по меньшей мере, в адгезивном покрытии на второй подложке или на его поверхности, или во второй подложке или на е поверхности, или в любом сочетании этих элементов содержатся один или несколько из следующих компонентов:(а) по меньшей мере один мономер и, возможно, по меньшей мере один инициатор,(б) по меньшей мере один сшивающий агент и, возможно, по меньшей мере один инициатор(в) по меньшей мере один агент, дезактивирующий активное вещество. 35. Способ дезактивации активного вещества в трансдермальном средстве доставки, включающий использование первой жсткой неплоской подложки, содержащей по меньшей мере на одной сто- 21007240 роне адгезивное покрытие; использование второй жсткой неплоской подложки, содержащей по меньшей мере на одной стороне адгезивное покрытие,причм первая подложка и вторая подложка каждая ограничивают углубление, конфигурация и размеры которого позволяют разместить в нм трансдермальное средство для доставки, и адгезивное покрытие на первой и второй подложках расположены по меньшей мере на части первой подложки и на части второй подложки, которые ограничивают углубления; размещение трансдермального средства доставки в углублении на первой подложке и помещение второй подложки над первой подложкой и выравнивание углубления на второй подложке так, чтобы оно располагалось над трансдермальным средством доставки, и присоединение первой подложки ко второй подложке с целью инкапсуляции, иммобилизации и/или изоляции трансдермального средства доставки. 36. Система дезактивации активного вещества в трансдермальном средстве доставки, включающая по меньшей мере первую подложку, содержащую адгезивное покрытие на одной стороне, и один или несколько из следующих компонентов, содержащихся, по меньшей мере, в адгезивном покрытии, на его поверхности или в первой подложке или на е поверхности, или в любом сочетании этих элементов:(а) по меньшей мере один мономер и, возможно, по меньшей мере один инициатор,(б) по меньшей мере один сшивающий агент и, возможно, по меньшей мере один инициатор,(в) по меньшей мере один не -опиоидный дезактивирующий агент. 37. Система по п.36, отличающаяся тем, что она содержит вторую подложку, способную приклеиваться к адгезивному покрытию на первой подложке. 38. Система по п.37, отличающаяся тем, что адгезивное покрытие расположено на одной стороне второй подложки. 39. Система по п.38, отличающаяся тем, что она дополнительно содержит один или несколько из следующих компонентов, содержащихся, по меньшей мере, в адгезивном покрытии на второй подложке или на его поверхности, или во второй подложке или на е поверхности, или в любом сочетании этих элементов:(а) по меньшей мере один мономер и, возможно, по меньшей мере один инициатор,(б) по меньшей мере один сшивающий агент и, возможно, по меньшей мере один инициатор,(в) по меньшей мере один не -опиоидный дезактивирующий агент. 40. Система по п.38, отличающаяся тем, что по меньшей мере одна из первой и второй подложек являются жсткими. 41. Система по п.40, отличающаяся тем, что и первая подложка, и вторая подложка являются жсткими. 42. Система по п.40, отличающаяся тем, что по меньшей мере одна из первой и второй подложек не являются плоскими. 43. Система по п.41, отличающаяся тем, что и первая подложка, и вторая подложка не являются плоскими. 44. Система по п.42, отличающаяся тем, что по меньшей мере одна из первой и второй подложек ограничивает углубление, конфигурация и размеры которого позволяют разместить в нм трансдермальное средство доставки. 45. Система по п.36, отличающаяся тем, что первая подложка характеризуется одним или несколькими из следующих свойств:(а) по существу непроницаема для растворителей,(б) по существу не набухает в растворителях,(в) является стойкой к разрыву и(г) является стойкой к разрезанию. 46. Система по п.36, отличающаяся тем, что содержащийся в ней компонент или компоненты включают мономер. 47. Система по п.46, отличающаяся тем, что содержащийся в ней компонент или компоненты включают по меньшей мере один сомономер. 48. Система по п.46, отличающаяся тем, что содержащиеся в ней компоненты дополнительно включают инициатор. 49. Система по п.48, отличающаяся тем, что содержащиеся в ней компоненты дополнительно включают по меньшей мере один сшивающий агент. 50. Система по п.49, отличающаяся тем, что содержащиеся в ней компоненты дополнительно включают по меньшей мере один неопиоидный дезактивирующий агент.
МПК / Метки
МПК: A61K 31/445, B09B 3/00, A61F 13/00, A61K 31/485, A61K 9/70
Метки: средстве, дезактивации, вещества, трансдермальном, система, активного
Код ссылки
<a href="https://eas.patents.su/29-7240-sistema-dezaktivacii-aktivnogo-veshhestva-v-transdermalnom-sredstve.html" rel="bookmark" title="База патентов Евразийского Союза">Система дезактивации активного вещества в трансдермальном средстве</a>
Предыдущий патент: Суспензионные препараты с пропеллентом нfa, содержащие антихолинергическое средство
Следующий патент: Исполнительное устройство
Случайный патент: Фильтровальная пластина