Применение фенэтилакриламидов, новые фенэтилакриламиды, способ их получения, а также содержащие их средства
Номер патента: 5764
Опубликовано: 30.06.2005
Авторы: Гевер Маркус, Штратман Зигфрид, Аммерманн Эберхард, Лоренц Гизела, Гулльманн Оливер, Мюллер Бернд, Заутер Хуберт, Грамменос Василиос, Тормо И Бласко Хорди, Гётц Норберт, Штирль Райнхард, Фольк Торстен
Формула / Реферат
1. Применение фенэтилакриламидов формулы I
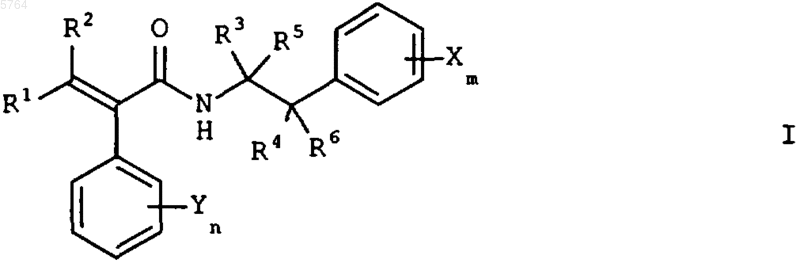
где заместители имеют следующие значения:
X означает галоген, C1-C4алкил, C1-C4галогеналкил, C1-C8алкокси, C1-C4галогеналкокси и -O-C(Ra,Rb)-Cу C-Rc;
Ra, Rb означают независимо друг от друга водород или C1-C6алкил;
Rc означает водород, C1-C8алкил, C3-C8циклоалкил и фенил, который может быть замещен галогеном, циано, нитро, CF3, C1-C4алкилом и/или C1-C4алкокси;
m равно от 1 до 4, причем остатки X могут быть различными, если m имеет значение более 1;
n равно 1 или 2, причем остатки Y могут быть различными, если n=2;
Y означает галоген, нитро, циано, C1-C4алкил, CF3, C1-C4алкокси и фенил, причем Y находится в 3-, 4- или 3,4-положении;
R1, R2 означают независимо друг от друга водород, галоген, C1-C4алкил, C1-C4алкокси, C1-C4галогеналкокси и CF3;
R3, R4, R5, R6 означают независимо друг от друга водород, C1-C4алкил и C1-C4алкокси или
R3 и R4 образуют совместно циклопропильный цикл, причем связи C-R5- и C-R6 друг с другом могут находиться в E- или Z-положении;
для борьбы с фитопатогенными грибами.
2. Фенэтилакриламиды формулы I по п.1, в которой R1 и R2 одинаковы и означают Cl, F и CH3.
3. Фенэтилакриламиды формулы I по п.1 или 2, в которой m имеет значение 1 или 2 и X находится в 3-, 4- или 3,4-положении.
4. Фенэтилакриламиды формулы I по пп.1-3, в которой X означает C1-C8алкокси и Y означает галоген.
5. Фенэтилакриламиды формулы I по пп.1-4, в которой R3 и R4 означают водород.
6. Фенэтилакриламиды формул
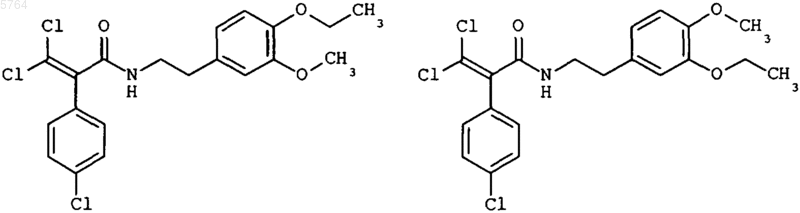
7. Способ получения соединений по пп.2-6, отличающийся тем, что сложные a-кетоэфиры формулы II

где R означает C1-C4алкил, подвергают взаимодействию с трифенилфосфином и, если R1 и R2 означают хлор, с CCl4, или, если R1 и R2 означают фтор, с натрийдифторхлорацетатом, или, если R1 и R2 означают метил, при основных условиях с изопропилтрифенилфосфонийгалогенидом с получением сложных акриловых эфиров формулы III
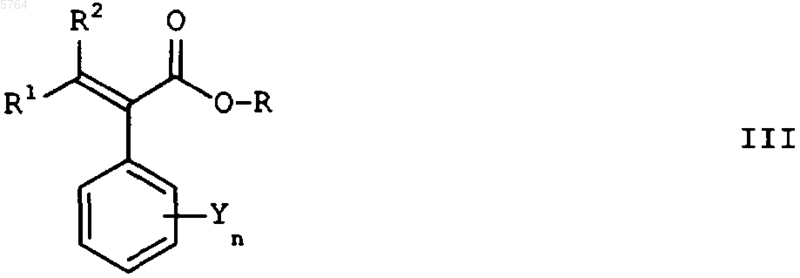
и соединение формулы III омыляют с получением карбоновых кислот формулы IV

и соединение формулы IV конденсируют фенетиламинами формулы V
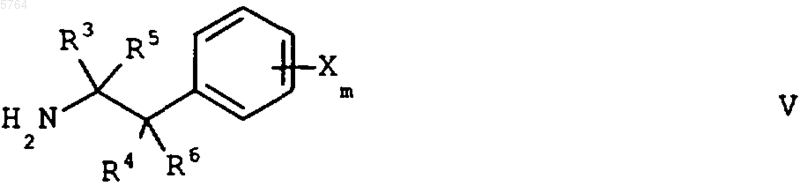
с получением соединений формулы I.
8. Средство для борьбы с фитопатогенными грибами, содержащее твердый или жидкий наполнитель и соединение формулы I по пп.2-6.
9. Применение соединений формулы I по пп.2-6 для получения пригодного для борьбы с фитопатогенными грибами средства.
10. Способ борьбы с фитопатогенными грибами, отличающийся тем, что грибы или подлежащие защите от поражения грибами материалы, растения, почву или посевной материал обрабатывают эффективным количеством соединения общей формулы I по пп.1-6.
Текст
005764 Настоящее изобретение относится к применению фенэтилакриламидов формулы I где заместители имеют следующие значения: Х означает галоген, С 1-С 4 алкил, С 1-С 4 галогеналкил, С 1-С 8 алкокси, С 1-С 4 галогеналкокси и -ОС(Ra,Rb)-СС-Rc,Ra, Rb означают независимо друг от друга водород и С 1-С 6 алкил;Rc означает водород, С 1-С 8 алкил, С 3-С 8 циклоалкил и фенил, который может быть замещен галогеном, циано, нитро, СF3, С 1-С 4 алкилом и/или С 1-С 4 алкокси;m, n независимо друг от друга имеют значение от 1 до 4, причем остатки X соответственно Y могут быть различными, если m соответственно n больше 1;R1, R2 означают независимо друг от друга водород, галоген, С 1-С 4 алкил, С 1-С 4 алкокси, С 1-С 4 галогеналкокси и CF3;R3, R4, R5, R6 означают независимо друг от друга водород, С 1-С 4 алкил и С 1-С 4 алкокси илиR3 и R4 образуют совместно циклопропильный цикл, причем связи C-R5 и C-R6 друг к другу могут быть в Е- или Z-положении; для борьбы с фитопатогенными грибами. Кроме того, изобретение относится к новым фенэтилакриламидам, к способу их получения, а также к содержащим их средствам. Различные арилакриламиды известны из публикаций ЕР-А 407217, ЕР-А 529736, WO-A 93/01523,JP-A 06/080616, US 3657340, US 3526653 и JP-А 63/154 649. Они описываются в настоящее время в качестве гербицидов. Их фунгицидное действие из уровня техники неизвестно. Ариламиды -оксиминофенилуксусной кислоты описываются в WO-A 96/17825 и WO-A 96/23763 в качестве фунгицидов. Арилакриламиды описываются в WO-А 96/17825 только в общей форме. Фунгицидное действие описываемых в вышеприведенных публикациях соединений является, однако, во многих случаях неудовлетворительным. Поэтому задачей изобретения является разработка соединений с улучшенными свойствами. В соответствии с этим разработана возможность применения фенэтилакриламидов формулы I в качестве фунгицидов, а также разработаны содержащие их средства. Фенэтилакриламиды формулы I получают описанными в публикациях ЕР-А 407217, ЕР-А 529736,WO-A 93/01523, JP-A 06/080616, US 3657340, US 3526653 и JP-A 63/154 649 методами синтеза, на которые здесь дается ссылка. Новые фенэтилакриламиды, в которых R1 и R2 одинаковы и означают Cl, F и СН 3, получают, например,исходя из сложных -кетоэфиров формулы II, в которой R означает С 1-С 4 алкил, нижеописанным методом. Соединения, в которых R1 и R2 означают хлор, получают таким образом, что сложные -кетоэфиры формулы II подвергают взаимодействию с трифенилфосфином (РРh3) и с ССl4 с получением сложных акриловых эфиров формулы IIIa. Эта реакция взаимодействия осуществляется обычно при температуре от 10 до 120 С, предпочтительно от 20 до 80 С, в инертном органическом растворителе [см. публикацию Пригодными растворителями являются такие ароматические углеводороды, как толуол, о-, м- и п-ксилол, такие галогенированные углеводороды, как метиленхлорид, хлороформ и хлорбензол, такие нитрилы,как ацетонитрил и пропионитрил, а также диметилсульфокид, диметилформамид и диметилацетамид,особенно предпочтительны ацетонитрил и пропионитрил. Могут также применяться смеси приведенных растворителей. Исходные вещества применяются, в общем, в эквимолярном количестве. Для повышения выхода может быть предпочтительным применение ССl4 и РРh3 в избыточном количестве в пересчете на соединение формулы II. Соединения, при которых R1 и R2 означают фтор, получают таким образом, что сложные -кетоэфиры формулы II подвергают взаимодействию с дифенил-1,1-дифторметилфосфином формулы VI, где Рh означает фенил, с получением сложных акриловых эфиров формулы IIIb. Эту реакцию взаимодействия-1 005764 проводят обычно при температуре от -70 до +80 С, предпочтительно от 0 до 20 С, в инертном органическом растворителе в присутствии основания [см. публикацию Tetrahedron Lett., с. 5571 и далее, 1990]. Подходящими растворителями являются такие простые эфиры, как диэтиловый эфир, диизопропиловый эфир, трет-бутилметиловый эфир, диоксан, анизол и тетрагидрофуран, особенно предпочтительны диэтиловый эфир и тетрагидрофуран. Могут также применяться и смеси приведенных растворителей. В качестве оснований пригодны, в общем, неорганические соединения, такие как гидриды щелочных и щелочно-земельных металлов, например гидрид лития, гидрид натрия, гидрид калия и гидрид кальция, такие амиды щелочных металлов, как амид лития, амид натрия и амид калия, металлорганические соединения, в частности алкилы щелочных металлов, такие как метиллитий, бутиллитий, литийдиизопропиламин и фениллитий. Особенно предпочтительны бутиллитий и литийдиизопропиламин. Основания применяются, в общем, в каталитическом количестве, однако, они могут применяться в эквимолярном количестве, в избытке или, в случае необходимости, в качестве растворителей. Исходные вещества применяются, в общем, в эквимолярном количестве. Для повышения выхода может быть предпочтительным применение ССl4 и РРh3 в избыточном количестве в пересчете на соединение формулы II. Альтернативно соединения, при которых R1 и R2 означают фтор, могут быть получены таким образом,что сложные -кетоэфиры формулы II подвергают взаимодействию с 2-хлор-2,2-дифторацетатом натрия формулы VII и трифенилфосфином (РРh3) с образованием сложных акриловых эфиров формулы IIIb. Это взаимодействие осуществляют обычно при температуре от 20 до 180 С, предпочтительно от 60 до 180 С,в инертном, органическом растворителе [см. публикацию Оrg. Synth. том V, с. 949 и след. (1973)]. Пригодными растворителями при этом являются такие ароматические углеводороды, как толуол,о-, м- и п-ксилол, такие простые эфиры, как диэтиловый эфир, диизопропиловый эфир, трет-бутилметиловый эфир, диоксан, анизол, тетрагидрофуран, этиленгликольдиметиловый эфир, диэтиленгликольдиметиловый эфир и 1,2-диэтоксиэтан, такие нитрилы, как ацетонитрил и пропионитрил, а также диметилсульфосид, диметилформамид и диметилацетамид, особенно предпочтительны тетрагидрофуран и диэтиленгликольдиметиловый эфир. Могут также применяться и смеси приведенных растворителей. Исходные вещества применяются, в общем, в эквимолярном количестве. Для выхода продукта может быть преимущественным применение соединения формулы VII в избыточном количестве в пересчете на соединение формулы II. Соединения, при которых R1 и R2 означают метил, получают таким образом, что сложные -кетоэфиры формулы II подвергают взаимодействию с галогенидом изопропилфосфония формулы VIII в смысле реакции Виттинга. В качестве галогенидов формулы VIII применяют йодиды и бромиды. В вышеприведенной схеме реакциив формуле VIII означает фосфораниловый остаток, такой как, например, трифенилфосфоранил. Реакция Виттинга осуществляется обычно при температуре от -78 до +85 С, предпочтительно отChem. 1971, с. 2143 и далее]. Пригодными растворителя при этом являются такие ароматические углеводороды, как толуол, о-, м- и п-ксилол, такие простые эфиры, как диэтиловый эфир, диизопропиловый эфир,трет-бутилметиловый эфир, диоксан, анизол, тетрагидрофуран, такие нитрилы, как ацетонитрил и пропионитрил, а также диметилсульфосид, диметилформамид и диметилацетамид, особенно предпочтительны диэтиловый эфир и тетрагидрофуран. Могут также применяться и смеси приведенных растворителей. В качестве основания пригодны, в общем, такие неорганические соединения, как гидриды щелочных и щелочно-земельных металлов, такие как гидрид лития, гидрид натрия, гидрид калия и гидрид кальция, такие амиды щелочных металлов, как амид лития, амид натрия и амид калия, металлоорганические соединения, в частности алкилы щелочных металлов, например метиллитий, бутиллитий и фениллитий, алкоголяты щелочных и щелочно-земельных металлов, такие как метанолят натрия, этанолят калия, трет-бутанолят и диметоксимагний. Особенно предпочтительны гидрид натрия и метанолят натрия.-2 005764 Основания применяются, в общем, в каталитическом количестве, однако, они могут применяться в эквимолярном количестве, в избытке или, в случае необходимости, в качестве растворителей. Исходные вещества подвергаются взаимодействию друг с другом, в общем, в эквимолярных количествах. Для повышения выхода продукта предпочтительным может быть применение соединения формулы VIII в избыточном количестве в пересчете на соединение формулы II. Сложные эфиры карбоновой кислоты формулы III, в которых R1 и R2 одинаковы и означают Cl, F и СН 3, подвергаются омылению обычными методами с получением карбоновых кислот формулы IV [см. публикацию Organikum, 16. Aufl.,с. 415 и 622, VEB Deutscher Verlag der Wissenschaften, Berlin, 1985]. Эту реакцию обычно осуществляют при температуре от 10 до 80 С, предпочтительно от 20 до 60 С, в инертном органическом растворителе в присутствии основания, такого как гидроксиды щелочного или щелочно-земельного металла, в частности гидроксида натрия или калия. Карбоновые кислоты формулы IV могут быть получены амидированием фэнетиламинами формулыV с получением соединений формулы I [см. публикацию Houben-Weyl, Methoden der Organischen Chemie,том Е 5, с. 941-972, Georg Thieme Verlag Stuttgart и New York, 1985]. Исходные вещества подвергаются взаимодействию друг с другом, в общем, в эквимолярных количествах. Для повышения выхода продукта предпочтительным может быть применение соединения формулы V в избыточном количестве в пересчете на соединение формулы IV. Альтернативно карбоновые кислоты формулы IV перед амидированием соединением формулы V сначала активируют посредством перевода в кислотные галогениды, в частности в хлорангидриды формулы IVa. Хлорирование с получением карбоновых кислот формулы IV осуществляется обычно при температуре от -20 до 100 С, предпочтительно от -10 до 80 С, в инертном органическом растворителе [см. публикацию Organikum, 16. Aufl., с. 423 и далее, VEB Deutscher Verlag derWissenschaften, Berlin, 1985]. В качестве хлорирующих средств при такой реакции взаимодействия пригодны обычные неорганические или органические хлорирующие средства, например тионилхлорид, оксалилхлорид, фосфортрихлорид, фосфорпентахлорид, фосфороксихлорид, трифенилфосфин/ССl4, предпочтительно тионилхлорид. Пригодными растворителями при этом являются алифатические углеводороды, такие как пентан,гексан, хлоргексан и петролейный эфир, ароматические углеводороды, такие как толуол, о-, м- и пксилол, галогенированные углеводороды, такие как метиленхлорид, хлороформ и хлорбензол, простые эфиры, такие как диэтиловый эфир, диизопропиловый эфир, трет-бутилметиловый эфир, диоксан, анизол и тетрагидрофуран, нитрилы, такие как ацетонитрил и пропионитрил, кетоны, такие как ацетон, метилэтилкетон, диэтилкетон и трет-бутилметилкетон, а также диметилсульфоксид, диметилформамид и диметилацетамид. Особенно предпочтительны толуол и тетрагидрофуран. Могут также применяться смеси приведенных растворителей. Хлорирующие средства применяются, в общем, по меньшей мере, в эквимолярных количествах. Для выхода может давать преимущество применение их в избыточном количестве до 10 молей на 1 моль соединения формулы IV, предпочтительно до 5 моль, в частности до 3 моль. Амидирование хлорангидридов фенэтиламидами формулы V осуществляют, как показано на примере соединения формулы IVa-3 005764 Эта реакция взаимодействия проводится обычно при температуре от 0 до 80 С, предпочтительно от 20 до 40 С, в инертном органическом растворителе в присутствии основания [см. публикацию Organikum,16. Aufl., с. 412 и далее, VEB Deutscher Veriag der Wissenschaften, Berlin, 1985]. Пригодными растворителя являются простые эфиры, такие как диэтиловый эфир, диизопропиловый эфир, трет-бутилметиловый эфир, диоксан, анизол и тетрагидрофуран, нитрилы, такие как ацетонитрил и пропионитрил, а также диметилсульфоксид, диметилформамид и диметилацетамид, особенно предпочтительны диэтиловый эфир и тетрагидрофуран. Могут также применяться смеси приведенных растворителей. В качестве оснований, в общем, пригодны такие органические соединения, как карбонаты щелочных и щелочно-земельных металлов, такие как карбонат лития, карбонат калия и карбонат кальция, а также гидрокарбонаты щелочных металлов, такие как гидрокарбонат натрия, кроме того, органические основания, например третичные амины, такие как триметиламин, триэтиламин, триизопропилэтиламин иN-метилпиперидин, пиридин, замещенные пиридины, такие как коллидин, лутидин и 4-диметиламинопиридин, а также бицикличные амины. Особенно предпочтительны триэтиламин и пиридин. Основания, в общем, применяются в каталитических количествах, они могут также применяться в эквимолярных количествах, в избытке или, в случае необходимости, в качестве растворителей. Исходные вещества подвергаются взаимодействию, в общем, в эквимолярных количествах. Для выхода может давать преимущество применение соединений формулы V в избытке в пересчете на соединение формулы IVa. Необходимые для получения соединений формулы I исходные вещества формулы II известны из литературных источников, например, они могут приобретаться на рынке или могут быть изготовлены следующим путем: Бромирование с помощью N-бромсукцинимида (NBS) или 1,3-дибром-5,5-диметилгидрантоина осуществляют обычно при температуре от 0 до 200 С, предпочтительно от 20 до 110 С, в инертном органическом растворителе в присутствии радикального инициатора [см. публикации Synthetic Reagents,Bd. 2, S. 1-63, Veriag Wiley, New York (1974); J. Heterocyclic Chem. с. 1431-1436 (1993); Synth. Commun. с. 280 и след. (1996); J. Med. Chem. с. 481 и след. (1981)]. Соединения IIb окисляют непосредственно в сложные -кетоэфиры формулы II. Окисление с помощьюN-метилморфолиноксида или п-диметиламинопиридиноксида происходит обычно при температуре от 0 до 100 С, предпочтительно от 20 до 60 С, в диметилсульфоксиде [см. Bull. Chem. Soc. Jpn., стр. 2221 (1981)]. Альтернативно сложные эфиры фенилуксусной кислоты формулы IIа могут также непосредственно окисляться в сложные -кетоэфиры формулы II. Окисление может осуществляться с помощью SeO2 или КМnO4 обычно при температуре от 20 до 180 С, предпочтительно от 20 до 120 С, в инертном органическом растворителе [см. публикации Synthesis, с. 915 (1994; Synth Commun., S. 1253 (1988); J. Gen. Chem.USSR, том 21, с. 694 и след. (1951)]. Требуемые для получения соединений формулы II сложные эфиры фенилуксусной кислоты IIа известны из различных литературных источников, соответственно могут коммерчески приобретаться. Если отдельные соединения формулы I не могут быть получены вышеприведенными методами, они могут быть получены дериватизацией других соединений формулы I. Если при синтезе возникают смеси изомеров, то, в общем, их разделения не требуется, так отдельные изомеры частично во время переработки для применения или при применении преобразуются друг в друга (например, под воздействием света, кислоты или основания). Соответствующие преобразования могут иметь место после применения, например при обработке растений, в обработанном растении или подлежащем борьбе фитопатогенном грибе или животном вредителе. Реакционные смеси перерабатываются обычным образом, например смешением с водой, разделением фаз и, в случае необходимости, хроматографической очисткой сырых продуктов. Промежуточные и конечные продукты имеются, например, в форме бесцветных или слегка коричневатых, вязких масел,которые при пониженном давлении и при соразмерно повышенной температуре освобождаются от летучих составных частей или подвергаются очистке. Если промежуточные и конечные продукты получают в качестве твердых веществ, очистку можно производить перекристаллизацией или дигидрированием. При приведенных в вышеприведенных формулах определениях символов применяются сборные понятия, которые, в общем, отражают следующие заместители: галоген означает фтор, хлор, бром и йод; алкил означает насыщенные, разветвленные или неразветвленные углеводородные остатки с 1 до 4 атомов углерода, например метил, этил, пропил, 1-метилэтил, бутил, 1-метилпропил, 2-метилпропил, 1,1 диметилэтил;-4 005764 галогеналкил означает разветвленные или неразветвленные алкильные группы с 1 до 4 атомов углерода (как приведено выше), причем в этих группах атомы водорода могут быть частично или полностью заменены атомами галогена, приведенными выше, например С 1-С 2 галогеналкил, такой как хлорметил, бромметил, дихлорметил, трихлорметил, фторметил, дифторметил, трифторметил, хлорфторметил, дихлорфторметил, хлoрдифторметил, 1-хлорэтил, 1-бромметил, 1-фторэтил, 2-фторэтил, 2,2-дифторэтил, 2,2,2-трифторэтил, 2-хлор-2-фторэтил, 2-хлор-2,2-дифторэтил, 2,2-дихлор-2-фторэтил, 2,2,2-трихлорэтил и пентафторэтил; алкокси означает разветвленные или неразветвленные алкильные группы с 1 до 8 атомов углерода(приведенными выше), которые связаны со скелетом через 1 атом кислорода (-O-); галогеналкокси означает разветвленные или неразветвленные алкильные группы с 1 до 4 атомов углерода (как приведено выше), которые связаны со скелетом через 1 атом кислорода (-O-). При учете применения согласно предназначению фенетилакриламидов формулы I особенно предпочтительны следующие значения заместителей, а именно как в отдельности, так и в комбинации. Особенно предпочтительные формы выполнения промежуточных продуктов в отношении заместителей соответствуют остаткам Xm, Yn, R1, R2, R3, R4, R5 и R6 формулы I. Особенно предпочтительны соединения формулы I, в которых R1 и R2 одинаковы и означают хлор,фтор или метил. Наряду с этим предпочтительны соединения формулы I, при которых R1 и R2 означают хлор. В той же степени предпочтительны соединения формулы I, при которых R1 и R2 означают фтор. Далее особенно предпочтительны соединения формулы I, при которых R1 и R2 означают метил. Особенно предпочтительны также соединения формулы I, в которых R1 и R2 отличны друг от друга,в частности R1 представляет собой более объемный остаток, чем остаток R2. В той же степени предпочтительны соединения формулы I, при которых R2 означает водород. Кроме того, особенно предпочтительны соединения формулы I, при которых m равно 1 или 2 и Х находится в 3-, 4- или 3,4-положении. Особенно предпочтительны соединения формулы I, при которых Хm означает 3-С 1-С 4 алкокси, 4-OC(Ra,Rb)-CC-Rc. Эти соединения соответствуют формуле I', где X' означает С 1-С 4 алкокси. В одинаковой степени предпочтительны соединения формулы I, при которых n равно 1 или 2 и Y находится в 3-, 4- или 3,4-положении. Наряду с этим особенно предпочтительны соединения формулы I, при которых Х означает C1-С 8 алкокси и Y означает галоген. Далее предпочтительны соединения формулы I, при которых Х означает метокси. Особенно предпочтительны соединения формулы I, где R3 до R6 означают водород, эти соединения описываются формулой I.1 Кроме того, особенно предпочтительны соединения формулы I, при которых R5 и R6 означают водород, эти соединения представлены формулой I.2 В такой же степени предпочтительны соединения формулы I.2, при которых R1 и R2 одинаковы и означают хлор, фтор или метил, R3 и R4 означают водород или образуют совместно циклопропиловое кольцо, Yn находится в 4-, 3,4- или 2,4-положении и означают хлор, фтор, бром, метил или этил, Х означает хлор, фтор, C1-С 3 алкил, C1-С 3 алкокси, бензилокси, аллилокси, пропаргилокси, трифторметилокси или дифторметокси и m имеет значение 1 или 2, причем если m равно 2, Х находится в 3,4-положении. В частности, предпочтительны приведенные в нижеследующих таблицах соединения формулы I при учете их применения. Приведенные в таблицах для одного заместителя группы независимо от ком-5 005764 бинации, в которой они приведены, представляют собой особенно предпочтительную форму выполнения соответствующего заместителя. Таблица 1. Соединения формулы I.1, при которых R1 и R2 означают хлор, и Yn означает хлор, и остаток Хm соответствует соединению одной строки табл. А. Таблица 2. Соединения формулы I.1, при которых R1 и R2 означают хлор, и Yn означает 3,4-дихлор, и остаток Хm соответствует соединению одной строки табл. А. Таблица 3. Соединения формулы I.1, при которых R1 и R2 означают хлор, и Yn означает 4-фтор, и остаток Хm соответствует соединению одной строки табл. А. Таблица 4. Соединения формулы I.1, при которых R1 и R2 означают хлор, и Yn означает 3,4-дифтор, и остаток Хm соответствует соединению одной строки табл. А. Таблица 5. Соединения формулы I.1, при которых R1 и R2 означают хлор, и Yn означает 4-СН 3, и остаток Хm соответствует соединению одной строки табл. А. Таблица 6. Соединения формулы I.1, при которых R1 и R2 означают хлор, и Yn означает 3,4-(СН 3)2, и остаток Хm соответствует соединению одной строки табл. А. Таблица 7. Соединения формулы I.1, при которых R1 и R2 означают хлор, и Yn означает 4-СН 2 СН 3, и остаток Хm соответствует соединению одной строки табл. А. Таблица 8. Соединения формулы I.1, при которых R1 и R2 означают хлор, и Yn означает 3,4-(СН 2 СН 3)2, и остаток Хm соответствует соединению одной строки табл. А. Таблица 9. Соединения формулы I.1, при которых R1 и R2 означают хлор, и Yn означает 4-СН(СН 3)2, и остаток Хm соответствует соединению одной строки табл. А. Таблица 10. Соединения формулы I.1, при которых R1 и R2 означают хлор, и Yn означает 4-С(СН 3)3, и остаток Хm соответствует соединению одной строки табл. А. Таблица 11. Соединения формулы I.1, при которых R1 и R2 означают хлор, и Yn означает 4-СF3, и остаток Хm соответствует соединению одной строки табл. А. Таблица 12. Соединения формулы I.1, при которых R1 и R2 означают хлор, и Yn означает 3,4-(СF3)2, и остаток Хm соответствует соединению одной строки табл. А. Таблица 13. Соединения формулы I.1, при которых R1 и R2 означают хлор, и Yn означает 4-ОСН 3, и остаток Хm соответствует соединению одной строки табл. А. Таблица 14. Соединения формулы I.1, при которых R1 и R2 означают хлор, и Yn означает 3,4-(ОСН 3)2,и остаток Хm соответствует соединению одной строки табл. А. Таблица 15. Соединения формулы I.1, при которых R1 и R2 означают хлор, и Yn означает 4-OCHF2, и остаток Хm соответствует соединению одной строки табл. А. Таблица 16. Соединения формулы I.1, при которых R1 и R2 означают хлор, и Yn означает 4-фенил, и остаток Хm соответствует соединению одной строки табл. А. Таблица 17. Соединения формулы I.1, при которых R1 и R2 означают фтор, и Yn означает 4-хлор, и остаток Хm соответствует соединению одной строки табл. А. Таблица 18. Соединения формулы I.1, при которых R1 и R2 означают фтор, и Yn означает 3,4-дихлор, и остаток Хm соответствует соединению одной строки табл. А. Таблица 19. Соединения формулы I.1, при которых R1 и R2 означают фтор, и Yn означает 4-фтор, и остаток Хm соответствует соединению одной строки табл. А. Таблица 20. Соединения формулы I.1, при которых R1 и R2 означают фтор, и Yn означает 3,4-дифтор, и остаток Хm соответствует соединению одной строки табл. А.-6 005764 Таблица 21. Соединения формулы I.1, при которых R1 и R2 означают фтор, и Yn означает 4-СН 3, и остаток Хm соответствует соединению одной строки табл. А. Таблица 22. Соединения формулы I.1, при которых R1 и R2 означают фтор и Yn означает 3,4(СН 3)2 и остаток Хm соответствует соединению одной строки табл. А. Таблица 23. Соединения формулы I.1, при которых R1 и R2 означают метил, и Yn означает 4-хлор, и остаток Хm соответствует соединению одной строки табл. А. Таблица 24. Соединения формулы I.1, при которых R1 и R2 означают метил, и Yn означает 3,4-дихлор, и остаток Хm соответствует соединению одной строки табл. А. Таблица 25. Соединения формулы I.1, при которых R1 и R2 означают метил, и Yn означает 4-фтор, и остаток Хm соответствует соединению одной строки табл. А. Таблица 26. Соединения формулы I.1, при которых R1 и R2 означают метил, и Yn означает 3,4-дифтор, и остаток Хm соответствует соединению одной строки табл. А. Таблица 27. Соединения формулы I.1, при которых R1 и R2 означают метил, и Yn означает 4-СН 3, и остаток Хm соответствует соединению одной строки табл. А. Таблица 28. Соединения формулы I.1, при которых R1 и R2 означают метил, и Yn означает 3,4-(СН 3)2, и остаток Хm соответствует соединению одной строки табл. А. Таблица 29. Соединения формулы I.1, при которых R1 означает метил, R2 означает водород и Yn означает 4-хлор и остаток Хm соответствует соединению одной строки табл. А. Таблица 30. Соединения формулы I.1, при которых R1 означает метил, R2 означает водород, и Yn означает 3,4 дихлор, и остаток Хm соответствует соединению одной строки табл. А. Таблица 31. Соединения формулы I.1, при которых R1 означает метил, R2 означает водород, и Yn означает 4 фтор, и остаток Хm соответствует соединению одной строки табл. А. Таблица 32. Соединения формулы I.1, при которых R1 означает метил, R2 означает водород, и Yn означает 3,4 дифтор, и остаток Хm соответствует соединению одной строки табл. А. Таблица 33. Соединения формулы I.1, при которых R1 означает метил, R2 означает водород, и Yn означает 4 СН 3, и остаток Хm соответствует соединению одной строки табл. А. Таблица 34. Соединения формулы I.1, при которых R1 означает метил, R2 означает водород, и Yn означает 3,4(СН 3)2, и остаток Хm соответствует соединению одной строки табл. А. Таблица 35. Соединения формулы I.1, при которых R1 означает этил, R2 означает водород, и Yn означает 4-хлор,и остаток Хm соответствует соединению одной строки табл. А. Таблица 36. Соединения формулы I.1, при которых R1 означает этил, R2 означает водород, и Yn означает 3,4 дихлор, и остаток Хm соответствует соединению одной строки табл. А. Таблица 37. Соединения формулы I.1, при которых R1 означает этил, R2 означает водород, и Yn означает 4-фтор,и остаток Хm соответствует соединению одной строки табл. А. Таблица 38. Соединения формулы I.1, при которых R1 означает этил, R2 означает водород, и Yn означает 3,4 дифтор, и остаток Хm соответствует соединению одной строки табл. А. Таблица 38. Соединения формулы I.1, при которых R1 означает этил, R2 означает водород, и Yn означает 4-СН 3,и остаток Хm соответствует соединению одной строки табл. А. Таблица 39. Соединения формулы I.1, при которых R1 означает этил, R2 означает водород, и Yn означает 3,4(СН 3)2, и остаток Хm соответствует соединению одной строки табл. А.-7 005764 Таблица 40. Соединения формулы I.1, при которых R1 означает метокси, R2 означает водород, и Yn означает 4 хлор, и остаток Хm соответствует соединению одной строки табл. А. Таблица 41. Соединения формулы I.1, при которых R1 означает метокси, R2 означает водород, и Yn означает 3,4 дихлор, и остаток Хm соответствует соединению одной строки табл. А. Таблица 42. Соединения формулы I.1, при которых R1 означает метокси, R2 означает водород, и Yn означает 4 фтор, и остаток Хm соответствует соединению одной строки табл. А. Таблица 43. Соединения формулы I.1, при которых R1 означает метокси, R2 означает водород, и Yn означает 3,4 дифтор, и остаток Хm соответствует соединению одной строки табл. А. Таблица 44. Соединения формулы I.1, при которых R1 означает метокси, R2 означает водород, и Yn означает 4 СН 3, и остаток Хm соответствует соединению одной строки табл. А. Таблица 45. Соединения формулы I.1, при которых R1 означает метокси, R2 означает водород, и Yn означает 3,4(СН 3)2, и остаток Хm соответствует соединению одной строки табл. А. Таблица 46. Соединения формулы I.1, при которых R1 означает трифторметокси, R2 означает водород, и Yn означает 4-хлор, и остаток Хm соответствует соединению одной строки табл. А. Таблица 47. Соединения формулы I.1, при которых R1 означает трифторметокси, R2 означает водород, и Yn означает 3,4-дихлор, и остаток Хm соответствует соединению одной строки табл. А. Таблица 48. Соединения формулы I.1, при которых R1 означает трифторметокси, R2 означает водород, и Yn означает 4-фтор, и остаток Хm соответствует соединению одной строки табл. А. Таблица 49. Соединения формулы I.1, при которых R1 означает трифторметокси, R2 означает водород, и Yn означает 3,4-дифтор, и остаток Хm соответствует соединению одной строки табл. А. Таблица 50. Соединения формулы I.1, при которых R1 означает трифторметокси, R2 означает водород, и Yn означает 4-СН 3, и остаток Хm соответствует соединению одной строки табл. А. Таблица 51. Соединения формулы I.1, при которых R1 означает трифторметокси, R2 означает водород, и Yn означает 3,4-(СН 3)2, и остаток Хm соответствует соединению одной строки табл. А. Таблица 52. Соединения формулы I.2, при которых R1 и R2 означают хлор и Yn означает 4-хлор, R3 и R4 образуют циклопропиловый цикл и остаток Хm соответствует соединению одной строки табл. А. Таблица 53. Соединения формулы I.2, при которых R1 и R2 означают фтор и Yn означает 4-хлор, R3 и R4 образуют циклопропиловый цикл и остаток Хm соответствует соединению одной строки табл. А. Таблица 54. Соединения формулы I.2, при которых R1 и R2 означают метил и Yn означает 4-хлор, R3 и R4 образуют циклопропиловый цикл и остаток Хm соответствует соединению одной строки табл. А. Таблица 55. Соединения формулы I.2, при которых R1 означает метил, R2 означает водород и Yn означает 4 хлор, R3 и R4 образуют циклопропиловый цикл и остаток Хm соответствует соединению одной строки табл. А. Таблица 56. Соединения формулы I.2, при которых R1 означает этил, R2 означает водород и Yn означает 4-хлор,3R и R4 образуют циклопропиловый цикл и остаток Хm соответствует соединению одной строки табл. А. Таблица 57. Соединения формулы I.2, при которых R1 означает метокси, R2 означает водород и Yn означает 4 хлор, R3 и R4 образуют циклопропиловый цикл и остаток Хm соответствует соединению одной строки табл. А. Таблица 58. Соединения формулы I.2, при которых R1 означает трифторметокси, R2 означает водород и Yn означает 4-хлор, R3 и R4 образуют циклопропиловый цикл и остаток Хm соответствует соединению одной строки табл. А. Соединения I пригодны в качестве фунгицидов. Они отличаются прекрасной активностью против широкого спектра фитопатогенных грибов, в частности, из класса аскомицетов, дейтеромицетов, фикомицетов и базидиомицетов. Они являются частично систематически активными и могут применяться при защите растений в качестве почвенных и лиственных фунгицидов. Они имеют особое значение при борьбе с множеством грибов на различных культурных растениях, таких как пшеница, рожь, ячмень,овес, рис, кукуруза, злаки, бананы, хлопчатник, соевые, кофе, сахарный тростник, виноград, плодовые и декоративные растения, и на овощных культурах, таких как огурцы, бобовые, томаты, картофель и тыквенные, а также на семенах этих растений. Особенно они пригодны для борьбы против следующих болезней растений: виды Alternaria на овощных и плодовых растениях,Botrytis cinerea (серая гниль) на клубничных, овощных, декоративных культурах и на виноградных лозах,Cercospora arachidicola на земляных орехах,Erysiphe cichoracearum и Sphaerotheca fuliginea на тыквенных,Erysiphe graminis (мучнистая роса) на зерновых культурах,виды Fusarium- и Verticillium на различных растениях,виды Helminthosporium на зерновых культурах,виды Mycosphaerella на бананах и земляных орехах,Phytophthora infestans на картофеле и томатах,Plasmopara viticola на виноградных лозах,Podosphaera leucotricha на яблоневых,Pseudocercosporella herpotrichoides на пшенице и ячмене,виды Pseudoperonospora на хмеле и огурцах,виды Puccinia на зерновых,Pyricularia oryzae на рисе,виды Rhizoctonia на хлопчатнике, рисе и дернине,Septoria nodorum на пшенице,Uncinula necator на виноградных лозьях,виды Ustilago на зерновых и сахарном тростнике, а также виды Venturia (парша) на яблоневых и грушах. Кроме того, соединения I пригодны для борьбы с патогенными грибами, такими как Paecilomycesvariotii при защите материалов (например, древесины, бумаги, дисперсий для покрытий, волокна соответственно тканей) и при защите складируемых запасов. Соединения I применяются таким образом, что грибы или подлежащие защите от поражения ими растения, материалы или почву обрабатывают фунгицидно активным количеством действующего вещества. Применение может осуществляться как перед, так и после инфекции грибами материалов, растений или семян. Фунгицидные средства содержат, в общем, между 0,1 и 95, предпочтительно между 0,5 и 90 мас.% действующего вещества.- 10005764 Нормы расхода составляют при применении для защиты растений в зависимости от желаемого эффекта между 0,01 и 2,0 кг действующего вещества на гектар. При обработке посевного зерна, в общем, требуется количества действующего вещества от 0,001 до 0,1 г, предпочтительно от 0,01 до 0,05 г на кг семян. При применении для защиты материалов соответственно защиты запасов норма расхода ориентируется на область применения и на желаемый эффект. Обычные нормы расхода при защите материалов составляют, например, от 0,001 г до 2 кг, предпочтительно от 0,005 г до 1 кг действующего вещества на 1 м 3 обрабатываемого материала. Соединения I могут быть переведены в обычные препаративные формы, например растворы, эмульсии,суспензии, тонкие порошки, порошки, пасты и грануляты. Препаративная форма зависит от цели применения,она должна, в любом случае, обеспечивать тонкое и равномерное распределение соединения по изобретению. Препаративные формы получают известным образом, например путем разбавления действующего вещества в растворителях и/или наполнителях, по желанию с применением эмульгаторов или диспергаторов, причем при применении в качестве разбавителя воды также и другие органические растворители могут применяться в качестве вспомогательных агентов. В качестве вспомогательных агентов пригодны,в основном, растворители, такие как ароматы (например, ксилол), хлорированные ароматы (например,хлорбензолы), парафины (например, фракции нефти), спирты (например, метанол, бутанол), кетоны (например, цикпогексанон), амины (например, этаноламин, диметилформамид) и вода; наполнители, такие как естественные измельченные породы (например, каолин, глинозем, тальк, мел) и синтетические измельченные породы (например, высокодисперсная кремниевая кислота, соли кремниевой кислоты); эмульгаторы, такие как неионогенные и анионные эмульгаторы (например, полиоксиэтиленовый эфир спирта жирного ряда, алкилсульфонаты и арилсульфонаты) и диспергаторы, такие как лигнинсульфитная отработанная щелочь и метилцеллюлоза. В качестве поверхностно-активных веществ применяются соли щелочных, щелочно-земельных металлов и аммониевые соли лигнинсульфокислоты, нафталинсульфокислоты, фенолсульфокислоты, дибутилнафталинсульфокислоты, алкиларилсульфонаты, алкилсульфаты, алкилсульфонаты, сульфаты спиртов жирного ряда, кислоты жирного ряда, а также их соли щелочных и щелочно-земельных металлов,соли сульфатированного гликолевого эфира жирного ряда, продукты конденсации сульфонированного нафталина и производных нафталина с формальдегидом, продукты конденсации нафталина, соответственно, нафталинсульфокислот с фенолом и формальдегидом, полиоксиэтиленоктилфенольный эфир,этоксилированный изооктилфенол, октилфенол, нонилфенол, алкилфенолполигликолевый эфир, трибутилфенилполигликолевый эфир, алкиларилполиэфирные спирты, изотридециловый спирт, продукты конденсации этиленоксида жирных спиртов, этоксилированное касторовое масло, полиоксиэтиленалкиловый эфир, этоксилированный полиоксипропилен, ацеталь поликликолевого эфира лаурилового спирта жирного ряда, сложный эфир сорбита, лигнинисульфитные отработанные щелочи и метилцеллюлоза. Для получения предназначенных для непосредственного распыления растворов, эмульсий, паст или масляных дисперсий применяются фракции минеральных масел со средней и высокой точками кипения,такие как керосин или дизельное масло, дегтярные масла растительного или животного происхождения,алифатические, циклические и ароматические углеводороды, например бензол, толуол, ксилол, парафин,тетрагидронафталин, алкилированные нафталины или их производные, метанол, этанол, пропанол, бутанол, хлороформ, тетрахлоруглерод, циклогексанол, циклогексанон, хлорбензол, изоформ, сильно полярные растворители, например диметилформамид, диэтилсульфоксид, N-метилпирролидон, вода. Порошковые препараты, препараты для опыливания и опудривания могут быть изготовлены путем смешения или совместного измельчения действующих веществ с твердым наполнителем. Гранулят, например оболочковый, импрегнированный или гомогенный гранулят, может быть получен путем связывания действующего вещества с твердыми наполнителями. Твердыми наполнителями могут быть, например, минеральные земли, такие как силикагель, кремниевые кислоты, силикаты, тальк,каолин, аттаклау, известняк, известь, мел, болюс, лесс, глина, доломит, диатомовая земля, сульфат кальция и магния, окись магния, измельченная пластмасса, удобрения, такие как сульфат аммония, фосфат аммония, нитрат аммония, мочевины и растительные продукты, такие как зерновая мука, мука древесной коры, древесная мука и мука ореховой скорлупы, порошок целлюлозы и другие твердые наполнители. Препаративные формы содержат, в общем, между 0,01 и 95 мас.%, предпочтительно между 0,1 и 90 мас.% действующего вещества. Действующие вещества имеют при этом чистоту от 90 до 100%, предпочтительно от 95 до 100% (по спектру ЯМР). Примерами препаративных форм являются следующие.I. 5 вес. долей соединения согласно изобретению хорошо перемешивают с 95 вес. долями тонкого коалина. Таким образом, получают средство опыливания, содержащее 5 мас.% действующего вещества.II. 30 вес. долей соединения согласно изобретению хорошо перемешивают с 92 вес. долями порошкового силикагеля и 8 вес. долями парафинового масла, которое напрыскивают на поверхность этого силикагеля. Таким образом, получают препаративную форму действующего вещества с хорошей адгезионной способностью (содержание действующего вещества 23 мас.%).III. 10 вес. долей соединения согласно изобретению растворяют в смеси, которая состоит из 90 вес. долей ксилола, 6 вес. долей продукта присоединения от 8 до 10 молей эиленоксида к 1 молю N-моноэтаноламида олеиновой кислоты, 2 вес. доли кальциевой соли додецилбензолсульфокислоты и 2 вес. доли продукта присоединения 40 молей этиленоксида к 1 молю касторового масла (содержание действующего вещества 9 мас.%).IV. 20 вес. долей соединения согласно изобретению растворяют в смеси, которая состоит из 60 вес. долей циклогексанона, 30 вес. долей изобутанола, 5 вес. долей продукта присоединения 7 молей этиленоксида к 1 молю изооктилфенола и 5 вес. долей продукта присоединения 40 молей этиленоксида к 1 молю касторового масла (содержание действующего вещества 16 мас.%).V. 80 вес. долей соединения согласно изобретению хорошо перемешивают с 3 вес. долями натриевой соли диизобутилнафталинсульфокислоты, 10 вес. долями натриевой соли лигнинсульфокислоты из сульфитного отработанного щелока и 7 вес. долями порошкового силикагеля и перемалывают в молотковой мельнице (содержание действующего вещества 80 мас.%).VI. Перемешивают 90 вес. долей соединения согласно изобретению с 10 вес. долями N-метил-пирролидона и получают раствор, который пригоден для применения в форме мельчайших капель (содержание действующего вещества 90 мас.%).VII. 20 вес. долей соединения согласно изобретению растворяют в смеси, состоящей из 40 вес. долей циклогексанона, 30 вес. долей изобутанола, 20 вес. долей продукта присоединения 7 молей этиленоксида к 1 молю изооктилфенола и 10 вес. долей продукта присоединения 40 молей этиленоксида к 1 молю касторового масла. Путем концентрации и тонкого распределения раствора в 100000 вес. долей воды получают водную дисперсию, содержащую 0,02 вес.% действующего вещества.VIII. 20 вес. долей соединения согласно изобретению хорошо перемешивают с 3 вес. долями натриевой соли диизобутилнафталинсульфокислоты, 17 вес. долями натриевой соли лигнинсульфокислоты из сульфитного отработанного щелока и 60 вес. долями порошкового силикагеля и перемалывают в молотковой мельнице. Путем тонкого распределения смеси в 20000 вес. долях воды получают раствор для опрыскивания, который содержит 0,1 мас.% действующего вещества. Действующие вещества могут применяться как таковые, в их препаративной форме или же в приготовленной форме применения, например в форме подлежащих непосредственному распылению растворов,порошков, суспензий или дисперсий, эмульсий, масляных дисперсий, паст, препаратов для опыливания,препаратов для опудривания, гранулятов, путем опрыскивания, мелкокапельного опрыскивания, опыливания, опудривания или полива. Используемые формы зависят от цели применения, но во всех случаях должно быть обеспечено максимально тонкое распределение действующих веществ по изобретению. Водные препаративные формы могут быть приготовлены из концентратов эмульсий, паст или смачиваемых порошков (порошков для разбрызгивания, масляных дисперсий) путем добавки воды. Для изготовления эмульсий, паст или масляных дисперсий вещества как таковые, или же растворенные в масле,могут гомогенизироваться в воде с помощью смачивающих агентов, активаторов адгезии, диспергаторов или эмульгаторов. Могут также приготовляться состоящие из действующего вещества, смачивающего агента, активатора адгезии, диспергатора или эмульгатора и, возможно, из растворителя и масла концентраты, которые можно разбавлять водой. Концентрация действующего вещества в готовых к применению препаратах может варьироваться в широких пределах. В общем, она составляет от 0,0001 до 10%, предпочтительно от 0,01 до 1%. Действующие вещества могут применяться с успехом при особенно низких нормах расхода, причем имеется возможность использовать препараты с более чем 95 мас.% действующего вещества или даже применять действующее вещество без добавок. К действующим веществам могут добавляться масла различного типа, гербицицды, фунгициды,другие средства борьбы с вредителями, бактерициды, в случае необходимости, также и непосредственно перед применением (смеси в баке). Эти средства могут примешиваться к соединениям по изобретению в весовом соотношении 1:10 до 10:1. Соединения по изобретению в форме применения как фунгициды могут применяться вместе с другими действующими веществами, например гербицидами, инсектицидами, регуляторами роста, фунгицидами или же удобрениями. При смешении соединений формулы I, соответственно содержащих их фунгицидных средств с другими фунгицидами во многих случаях обеспечивается повышение спектра фунгицидного действия. Нижеприведенный перечень фунгицидов, которые можно применять вместе с соединениями по изобретению, поясняет возможности их комбинирования, однако, не ограничивает их. К таким фунгицидам относятся следующие: сера, дитиокарбонаты и их производные, такие как ферридиметилдитиокарбамат, цинкдиметилдитиокарбамат, цинкдиметилдитиокабамат, марганецэтилен-бис-дитиокарбамат, марганеццинкэтилендиамин-бис-дитиокарбамат; тетраметилтиурамдисульфиды, аммиачный комплекс цинк(N,N-этилен-бис-дитиокарбамата), аммиачный комплекс цинк(N,N'-пропилен-бис-дитиокарбамата), полимер цинк(N,N'-пропилен-бис-дитиокарбамата), N,N'-пропилен-бис(тиокарбомоил)дисульфид;- 12005764 нитропроизводные, такие как динитро(1-метилгептил)фенилкротонат, 2-втор.-бутил-4,6-динитрофенил-3,3-диметилакрилат, 2-втор.-бутил-4,6-динитрофенилизопропилкарбонат, диизопропиловый эфир 5 нитроизофталевой кислоты; гетероциклические вещества, такие как 2-гептадецил-2-имидазолинацетат, 2,4-дихлор-6-(о-хлоранилино)-s-триазин, O,O-диэтилфталиминдофосфонотиоат, 5-амино-1-[бис-(диметиламино)фосфинил]-3-фенил-1,2,4-триазол, 2,3-дициано-1,4-дитиоантрахинон, 2-тио-1,3-дитиоло[4,5-b]хиноксалин, метиловый эфир 1-(бутилкарбамоил)-2-бензимидазолкарбаминовой кислоты, 2-метоксикарбониламинобензимидазол, 2-(фурил-(2-бензимидазол, 2-(тиазолил-(4-бензимидазол, N-(1,1,2,2-тетерахлорэтилтио)тетрагидрофталимид, N-трихлорметилтиотетрагидрофталимид, N-трихлорметилтиофталимид; диамид N-дихлорфторметилтио-N',N'-диметил-N-фенилсерной кислоты, 5-этокси-3-трихлорметил 1,2,3-тиадиазол, 2-роданметилтиобензтиазол, 1,4-дихлор-2,5-диметоксибензол, 4-(2-хлорфенилгидразоно)-3-метил-5-изоксазолон, пиридин-2-тио-1-оксид, 8-гидроксихинолин, соответственно его медная соль,2,3-дигидро-5-карбоксанилидо-6-метил-1,4-оксатиин, 2,3-дигидро-5-карбоксанилидо-6-метил-1,4-оксатиин-4,4-диоксид, анилид 2-метил-5,6-дигидро-4 Н-пиран-3-карбоновой кислоты, анилид 2-метилфуран-3 карбоновой кислоты, анилид 2,5-диметилфуран-3-карбоновой кислоты, анилид 2,4,5-триметилфуран-3 карбоновой кислоты, циклогексиламид 2,5-диметилфуран-3-карбоновой кислоты, амид N-циклогексилN-метокси-2,5-диметилфуран-3-карбоновой кислоты, 2-анилид метилбензойной кислоты, анилид 2-йодбензойной кислоты, N-формил-N-морфолин-2,2,2-трихлорэтилацеталь, пиперазин-1,4-диил-бис-1-(2,2,2 трихлорэтил)формамид, 1-(3,4-дихлоранилино)-1-формиламино-2,2,2-трихлорэтан, 2,6-диметил-N-тридецилморфолин, соответственно его соли, 2,6-диметил-N-циклододецилморфолин, соответственно его соли, N-[3-(п-трет.-бутилфенил)-2-метилпропил]-цис-2,6-диметилморфолин, N-[3-(п-трет.-бутилфенил)-2 метилпропил]пиперидин, 1-[2-(2,4-дихлорфенил)-4-этил-1,3-диоксолан-2-илэтил]-1 Н-1,2,4-триазол, 1-[2(2,4-дихлорфенил)-4-н-пропил-1,3-диоксолан-2-илэтил]-1 Н-1,2,4-триазол,N-(н-пропил)-N-(2,4,6-трихлорфеноксиэтил)-N'-имидазолилмочевина, 1-(4-хлорфенокси)-3,3-диметил-1-(1 Н-1,2,4-триазол-1-ил)-2 бутанон, 1-(4-хлорфенокси)-3,3-диметил-1-(1 Н-1,2,4-триазол-1-ил)-2-бутанол, (2RS,3RS)-1-[3-(2-хлорфенил)-2-(4-фторфенил)оксиран-2-илметил]-1 Н-1,2,4-триазол, -(2-хлорфенил)(4-хлорфенил)-5-пиримидинметанол, 5-бутил-2-диметиламино-4-гидрокси-6-метилпиримидин, бис-(п-хлорфенил)-3-пиридинметанол, 1,2-бис-(3-этоксикарбонил-2-тиоуреидо)бензол, 1,2-бис-(3-метоксикарбонил-2-тиоуреидо)бензол; стробилурины, такие как метил-Е-метоксиимино-[-(о-толилокси)-о-толил]ацетат, метил-Е-2-2-[6(2-цианофенокси)пиримидин-4-илокси]фенил-3-метоксиакрилат, метил-Е-метоксиимино-[-(2-феноксифенил)]ацетамид, метил-Е-метоксиимино-[-(2,5-диметилфенокси)-о-толил]ацетамид; анилинопиримидины, такие как N-(4,6-диметилпиримидин-2-ил)анилин, N-[4-метил-6-(1-пропинил) пиримидин-2-ил]анилин, N-[4-метил-6-циклопропилпиримидин-2-ил]анилин; фенилпирролы, такие как 4-(2,2-дифтор-1,3-бензодиоксол-4-ил)пиррод-3-карбонитрил; амиды коричной кислоты, такие как морфолид 3-(4-хлорфенил)-3-(3,4-диметоксифенил)акриловой кислоты; а также различные фунгициды, такие как додецилнуанидинацетат, 3-[3-(3,5-диметил-2-оксициклогексил)-2-гидроксиэтил]глютаримид, гексахлорбензол, DL-метил-N-(2,6-диметилфенил)-N-фуроил(2) аланинат, метиловый эфир DL-N-(2,6-диметилфенил)-N-(2'-метоксиацетил)аланина, N-(2,6-диметилфенил)-N-хлорацетил-DL-2-аминобутиролактон, метиловый эфир DL-N-(2,6-диметилфенил)-N-(фенилацетил)аланина, 5-метил-5-винил-3-(3,5-дихлорфенил)-2,4-диоксо-1,3-оксазолидин, 3-[3,5-дихлорфенил-5 метил-5-метоксиметил]-1,3-оксазолидин-2,4-дион, 3-(3,5-дихлорфенил)-1-изопропилкарбамоилгидантоин,имид N-(3,5-дихлорфенил)-1,2-диметилциклопропан-1,2-дикарбоновой кислоты, 2-циано-[N-(этиламинокарбонил)-2-метоксиимино]ацетамид, 1-[2-(2,4-дихлорфенил)пентил]-1 Н-1,2,4-триазол, 2,4-дифтор(1 Н 1,2,4-триазолил-1-метил)бензгидриловый спирт, N-(3-хлор-2,6-динитро-4-трифторметилфенил)-5-трифторметил-3-хлор-2-аминопиридин, 1-бис-(4-фторфенил)метилсилил)метил)-1 Н-1,2,4-триазол. Примеры синтеза Приведенные в нижеследующих примерах синтеза стадии при соответствующем изменении исходных соединений использовались для получения других соединений. Полученные таким образом соединения приведены в нижеследующей таблице с физическими данными. Пример 1. Получение сложного метилового эфира 2-бром-(4-хлорфенил)уксусной кислоты. К раствору из 215,3 г (1,17 моль) сложного метилового эфира 4-хлорфенилуксусной кислоты в 500 мл тетрахлорметана по порциям добавляют 116 г (0,585 моль) 1,3-дибром-5,5-диметилхинтантоина, а также 1 г азо-бис-изобутиронитрила и нагревают с обратным холодильником в течение 24 ч. После этого реакционную смесь промывают водой и 1 н натровой щелочи, водную фазу экстрагируют метиленхлоридом и органическую фазу сушат и концентрируют. Получают 260 г целевого соединения. 1H-ЯМР [, (CDCl3)]: 3,8 (s, 3H); 5,3 (s, 1H). Пример 2. Получение сложного метилового эфира (4-хлорфенил)-2-оксоуксусной кислоты. Раствор из 100 г (0,38 моль) соединения из примера 1 в 400 мл диметилсульфоксида смешивают при охлаждении льдом с 97,2 г 75%-ного водного раствора N-метилморфолин-N-оксида. После перемешивания в течение 24 ч при температуре от 20 до 25 С реакционную смесь выливают на воду и экстрагируют метил-трет.-бутиловым эфиром. Из органических фаз после сушки и отгонки растворителя и хромато- 13005764 графии на силикагеле (циклогексан/метил-трет.-бутиловый эфир [3:1]) получают 69 г целевого соединения. 1H-ЯМР [, (CDCl3)]: 4,0 (s, 3H); 7,5 (m, 2H) и 8,0 (m, 2H). Пример 3. Получение сложного метилового эфира 3,3-дихлор-2-(4-хлорфенил)акриловой кислоты. К раствору из 29,9 г (0,15 моль) сложного кетоэфира из примера 2 в 300 мл ацетонитрила после смешения с 117,9 г РРh3 (0,45 моль) прикапывают 69,3 г (0,45 моль) тетрахлоруглерода. После выдерживания в течение 4 ч при 56 С реакционную смесь концентрируют. Полученный остаток хроматографируют на силикагеле с помощью циклогексана/метил-трет.-бутилового эфира (3:1). Получают 39,2 г целевого соединения. 1H-ЯМР [, (CDCl3)]: 3,8 (s, 3H); 7,3-7,4 (m, 4H). Пример 4. Получение 3,3-дихлор-2-(4-хлорфенил)акриловой кислоты. Раствор из 17,1 г (64 ммоль) сложного эфира из примера 3 в 50 мл метанола после смешения с 193 мл 1 н раствора КОН перемешивают в течение 20 ч при температуре от 20 до 25 С. После отгонки растворителя остаток подкисляют с помощью 20%-го H2SO4 на значение рН 1 и экстрагируют этилацетатом. Из органических фаз после сушки и отгонки растворителя получают 15 г целевого соединения. 1H-ЯМР [, (CDCl3)]: 7,25 (m, 2H); 7,40 (m, 2H) и 9,5 (s, 1H). Пример 5. Получение хлорангидрида 3,3-дихлор-2-(4-хлорфенил)акриловой кислоты. К раствору из 50 г (0,199 моль) кислоты из примера 4 в 200 мл диэтилового эфира и 23,6 г (0,298 моль) пиридина прикапывают при 0 С 35,5 г (0,298 моль) тионилхлорида. Раствор перемешивают в течение 6 ч при температуре от 20 до 25 С, потом фильтруют. После отгонки растворителя получают 42,1 г продукта, который без очистки подвергают дальнейшему взаимодействию. Пример 6. Получение 3,3-дихлор-2-(4-хлорфенил)-N-[2-(3,4-диметоксифенил)этил]акриламида [I-1]. К раствору из 7,24 г (0,04 моль) гомовератриламина и 4,04 г (0,04 моль) триэтиламина в 80 мл метиленхлорида прикапывают раствор из 10,8 г (0,04 моль) полученного в примере 5 хлорангидрида в 20 мл мтеиленхлорида. Раствор перемешивают в течение 3 ч при температуре от 20 до 25 С, промывают сначала с помощью 3 н натрового щелока и потом 10 мас.%-ной соляной кислотой. Органическую фазу освобождают от растворителя, из остатка получают после хроматографии на силикагеле циклогексаном/метил-трет.-бутиловым эфиром (3:1) 13,85 г целевого соединения. 1 5 г (19,5 ммоль) 2-[4-(бензилокси)-3-метоксифенил]этиламина [ср. публикацию: Heterocycles, Vol. 28, 297-298 (1989)] в 100 мл тетрагидрофурана гидрируют после добавки 0,5 г палладия на активном угле(10%-ном) при нормальном давлении. После окончания поглощения воды реакционную смесь отфильтровывают и фильтрат освобождают от растворителя. Остаток дигенерируют диизопропиловым эфиром,отфильтровывают и сушат. К 1,25 г хлорангидрида 3,3-дихлор-2-(4-хлорфенил)акриловой кислоты в 30 мл диметилформамида добавляют 1 г 4-(2-аминоэтил)-2-метоксифенола, 2,21 г 1-бензотриазолилокси-трис(диметиламино)фосфонийгексафторфосфата, а также 1,5 г N-этилдиизопропиламина и перемешивают в течение 12 ч при температуре 23 С. Потом рационную смесь смешивают с водой, экстрагируют этилацетатом, экстракт- 14005764 промывают раствором NaCl и сушат. После удаления растворителя остаток хроматографируют на силикагеле циклогексаном/метил-трет.-бутиловым эфиром (3:1). Получают целевое соединение в форме масла. МС (m/e): M+H 400, 368, 366, 360. Пример 9. Получение 3,3-дихлор-2-(4-хлорфенил)-N-[2-(4-гидрокси-3-метоксифенил)этил]акриламида [I-53]. Раствор из 0,4 г 3,3-дихлор-2-(4-хлорфенил)-N-[2-(4-гидрокси-3-метоксифенил)этил]акриламида в 50 мл диметилформамида после добавки 0,14 г карбоната калия и 0,12 г пропаргилбромида перемешивают в течение около 12 ч. После добавки еще 0,14 г карбоната калия, а также 0,12 г пропаргилбромида и перемешивания еще в течение 6 ч реакционную смесь выливают на воду, экстрагируют метил-трет.бутиловым эфиром и экстракт промывают водой и сушат. После удаления растворителя и хроматографии на силикагеле циклогексаном/метил-трет.-бутиловым эфиром (1:1) получают целевое соединение в форме масла. 1 Примеры действия на фитопатогенные грибы Фунгицидное действие соединений общей формулы I показано на следующих опытах. Действующие вещества приготавливают отдельно или совместно в качестве 10%-ной эмульсии в смеси из 70 мас.% циклогексана, 20 мас.% Nekanil LN (Lutensol AP6, смачиватель с эмульгирующим и диспергирующим действием на базе этоксилировнных алкилфенолов) и 10 мас.% Wettol ЕМ (неионогенного эмульгатора на базе этокилированного касторового масла) и разбавляют водой в соответствии с желаемой концентрацией. Пример применения 1. Эффективность против Phytophthora infestans на томатах. Листья горшковых растений сорта "Крупные мясистые томаты St. Pierre" обильно до образования капель опрыскивают водной суспензией, приготовленной из исходного раствора, содержащего 10% действующего вещества, 63% циклогексанона и 27% эмульгатора. На следующий день листья инфицируют холодной водной суспензией спор Phytophthora infestans с плотностью спор 0,25 х 106 спор/мл. После этого растения помещали в камеру с насыщенным паром при температуре между 18 и 20 С. Через 6 дней плесень на листьях необработанных, но инфицированных контрольных растений развилась настолько сильно, что можно было визуально определить поражение в %.- 16005764 В этом опыте обработанные посредством 250 мил.дол. действующего вещества I-1, I-2, I-11, I-17, I-19,I-25, I-26, I-27, I-32, I-33, I-34, I-39, I-40, I-42, I-43, I-45, I-46 и I-49 табл. 1 растения проявляют поражение максимально на 10%, в то время как необработанные растения имели поражение в 90%. Пример применения 2. Эффективность против Plasmopara viticola. Листья выращенных в горшках виноградных лоз сорта "MuIler-Thurgau" обильно до образования капель опрыскивают композицией действующего вещества, приготовленной из исходного раствора, содержащего 10% действующего вещества, 63% циклогексанона и 27% эмульгатора. На следующий день листья инокулируют водной суспензией спор Plasmopara viticola. После этого опытные растения выдерживают сначала 48 ч в камере с насыщенный паром при 24 С и потом 5 дней в теплице при температуре между 20 и 30 С. По истечении этого времени для ускорения действия опытные растения снова помещали во влажную камеру на 16 ч. Потом визуально оценивали степень развития поражения на нижней стороне листьев. В этом опыте обработанные посредством 250 мил.дол. действующего вещества I-1, I-2, I-10, I-11, I-12,I-16, I-17, I-19, I-21 - I-27, I-29, I-30, I-32, I-33, I-34, I-39, I-40, I-42, I-43, I-45, I-46, I-48 и I-49 табл. 1 растений были поражены максимально на 10%, в то время как необработанные растения имели поражение в 90%. Сравнительный опыт. Длительная эффективность наротив Phytophthora infestans на томатах. Горшковые растения сорта "Крупные мясистые томаты St. Pierre" обильно до образования капель опрыскивают на стадии роста 4-го листа водной суспензией, приготовленной из исходного раствора, содержащего 10% действующего вещества, 63% циклогексанона и 27% эмульгатора. Для проверки длительного действия соединений через неделю после обработки листья инфицируют водной суспензией спор Phytophthora infestans. После этого растения помещают в камеру с насыщенным паром при температуре между 16 и 18 С. Через 6 дней плесень на листьях необработанных, но инфицированных контрольных растений развилась настолько сильно, что можно было визуально определить поражение в %. В качестве сравнительного действующего вещества служило известное из WO-А 96/23763 соединение следующей структуры: В этом опыте обработанные посредством 63 мил.дол. действующего вещества I-1, I-2, I-11, I-33 и I-34 табл. 1 растения имели поражение от 0 до 25%, в то время как обработанные посредством 63 мил.дол. сравнительного действующего вещества растения имели поражение до 40% и необработанные растения до 100%. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Применение фенэтилакриламидов формулы I где заместители имеют следующие значения: Х означает галоген, C1-С 4 алкил, C1-С 4 галогеналкил, C1-С 8 алкокси, C1-С 4 галогеналкокси и -OC(Ra,Rb)-CC-Rc;Ra, Rb означают независимо друг от друга водород или C1-С 6 алкил;Rc означает водород, C1-С 8 алкил, C3-С 8 циклоалкил и фенил, который может быть замещен галогеном, циано, нитро, СF3, C1-С 4 алкилом и/или C1-С 4 алкокси;m равно от 1 до 4, причем остатки Х могут быть различными, если m имеет значение более 1;R1, R2 означают независимо друг от друга водород, галоген, С 1-С 4 алкил, С 1-С 4 алкокси, С 1-С 4 галогеналкокси и CF3;RЗ, R4, R5, R6 означают независимо друг от друга водород, С 1-С 4 алкил и С 1-С 4 алкокси илиR3 и R4 образуют совместно циклопропильный цикл, причем связи С-R5- и C-R6 дpyг с другом могут находиться в Е- или Z-положении; для борьбы с фитопатогенными грибами. 2. Фенэтилакриламиды формулы I по п.1, в которой R1 и R2 одинаковы и означают Cl, F и СН 3. 3. Фенэтилакриламиды формулы I по п.1 или 2, в которой m имеет значение 1 или 2 и Х находится в 3-, 4- или 3,4-положении. 4. Фенэтилакриламиды формулы I по пп.1-3, в которой Х означает С 1-С 8 алкокси и Y означает галоген. 5. Фенэтилакриламиды формулы I по пп.1-4, в которой R3 и R4 означают водород. 6. Фенэтилакриламиды формул 7. Способ получения соединений по пп.2-6, отличающийся тем, что сложные -кетоэфиры формулы II где R означает С 1-С 4 алкил, подвергают взаимодействию с трифенилфосфином и, если R1 и R2 означают хлор, с ССl4, или, если R1 и R2 означают фтор, с натрийдифторхлорацетатом, или, если R1 и R2 означают метил, при основных условиях с изопропилтрифенилфосфонийгалогенидом с получением сложных акриловых эфиров формулы III и соединение формулы III омыляют с получением карбоновых кислот формулы IV и соединение формулы IV конденсируют фенетиламинами формулы V с получением соединений формулы I. 8. Средство для борьбы с фитопатогенными грибами, содержащее твердый или жидкий наполнитель и соединение формулы I по пп.2-6. 9. Применение соединений формулы I по пп.2-6 для получения пригодного для борьбы с фитопатогенными грибами средства. 10. Способ борьбы с фитопатогенными грибами, отличающийся тем, что грибы или подлежащие защите от поражения грибами материалы, растения, почву или посевной материал обрабатывают эффективным количеством соединения общей формулы I по пп.1-6.
МПК / Метки
МПК: A01N 37/18, C07C 233/69
Метки: новые, применение, получения, содержащие, средства, способ, фенэтилакриламиды, также, фенэтилакриламидов
Код ссылки
<a href="https://eas.patents.su/19-5764-primenenie-fenetilakrilamidov-novye-fenetilakrilamidy-sposob-ih-polucheniya-a-takzhe-soderzhashhie-ih-sredstva.html" rel="bookmark" title="База патентов Евразийского Союза">Применение фенэтилакриламидов, новые фенэтилакриламиды, способ их получения, а также содержащие их средства</a>
Предыдущий патент: Синергетические гербицидные смеси
Следующий патент: Высококонцентрированные стабильные растворы мелоксикама
Случайный патент: Способ маркировки ценных изделий