Сложный моноэфир янтарной кислоты и пробукола для лечения сердечно-сосудистых и воспалительных заболеваний
Формула / Реферат
1. Способ лечения заболевания, опосредованного VCAM-1, включающий введение млекопитающему, нуждающемуся в таком лечении, терапевтически эффективного количества сложного моноэфира янтарной кислоты и пробукола или его фармацевтически приемлемой соли.
2. Способ лечения сердечно-сосудистого заболевания, опосредованного VCAM-1, включающий введение млекопитающему, нуждающемуся в таком лечении, терапевтически эффективного количества сложного моноэфира янтарной кислоты и пробукола или его фармацевтически приемлемой соли.
3. Способ по п.2, в котором указанным заболеванием является атеросклероз.
4. Способ по п.2, в котором указанным заболеванием является рестеноз после ангиопластики.
5. Способ по п.2, в котором указанным заболеванием является заболевание, поражающее коронарную артерию.
6. Способ по п.2, в котором указанным заболеванием является стенокардия.
7. Способ по п.2, в котором указанным заболеванием является заболевание, поражающее капилляры.
8. Способ по любому из пп.1-7, который дополнительно включает использование второго агента для лечения сердечно-сосудистого заболевания.
9. Способ по п.8, в котором второй агент для лечения сердечно-сосудистого заболевания выбран из группы, состоящей из агентов, снижающих уровень липидов; ингибиторов агрегации тромбоцитов; противотромботических агентов, блокаторов кальциевых каналов; ингибиторов ангиотензин-конвертирующего фермента (АСЕ) и b-блокаторов.
10. Способ лечения воспалительного заболевания, опосредованного VCAM-1, включающий введение млекопитающему, нуждающемуся в таком лечении, терапевтически эффективного количества сложного моноэфира янтарной кислоты и пробукола или его фармацевтически приемлемой соли.
11. Способ по п.10, в котором указанное заболевание представляет собой нарушение эндотелия человека.
12. Способ по п.10, в котором указанное заболевание представляет собой астму.
13. Способ по п.10, в котором указанное заболевание представляет собой псориаз.
14. Способ по п.10, в котором указанное заболевание представляет собой экзематозный дерматит.
15. Способ по п.10, в котором указанное заболевание представляет собой саркому Капоши.
16. Способ по п.10, в котором указанное заболевание представляет собой рассеянный склероз.
17. Способ по п.10, в котором указанное заболевание представляет собой пролиферативное нарушение клеток гладких мышц.
18. Способ по п.10, в котором указанное заболевание представляет собой ревматоидный артрит.
19. Способ по п.10, в котором указанное заболевание представляет собой остеоартрит.
20. Способ по любому из пп.10-19, который дополнительно включает введение второго противовоспалительного агента.
21. Способ по п.20, в котором второй противовоспалительный агент выбран из группы, включающей ибупрофен, индометацин, фенопрофен, мефенаминовую кислоту, флуфенаминовую кислоту, сулиндак и кортикостроиды.
22. Способ по любому из пп.1-21, в котором млекопитающее является человеком.
23. Применение терапевтически эффективного количества сложного моноэфира янтарной кислоты и пробукола или его фармацевтически приемлемой соли для получения лекарственного средства для лечения заболевания, опосредованного VCAM-1.
24. Применение терапевтически эффективного количества сложного моноэфира янтарной кислоты и пробукола или его фармацевтически приемлемой соли для получения лекарственного средства для лечения сердечно-сосудистого заболевания, опосредованного VCAM-1.
25. Применение по п.24, в котором указанным заболеванием является атеросклероз.
26. Применение по п.24, в котором указанным заболеванием является рестеноз после ангиопластики.
27. Применение по п.24, в котором указанным заболеванием является заболевание, поражающее коронарную артерию.
28. Применение по п.24, в котором указанным заболеванием является стенокардия.
29. Применение по п.24, в котором указанным заболеванием является заболевание, поражающее капилляры.
30. Применение по любому из пп.23-29, в котором указанное лекарственное средство предназначено для использования в комбинации с вторым агентом для лечения сердечно-сосудистого заболевания.
31. Применение по любому из пп.23-29, в котором указанное лекарственное средство включает второй агент для лечения сердечно-сосудистого заболевания.
32. Применение по п.30 или 31, в котором второй агент для лечения сердечно-сосудистого заболевания выбран из группы, состоящей из агентов, снижающих уровень липидов; ингибиторов агрегации тромбоцитов; противотромботических агентов, блокаторов кальциевых каналов; ингибиторов ангиотензин-конвертирующего фермента (АСЕ) и b-блокаторов.
33. Применение терапевтически эффективного количества моноэфира янтарной кислоты и пробукола или его фармацевтически приемлемой соли для получения лекарственного средства для лечения воспалительного заболевания, опосредованного VCAM-1.
34. Применение по п.33, в котором указанное заболевание представляет собой нарушение эндотелия человека.
35. Применение по п.33, в котором указанное заболевание представляет собой астму.
36. Применение по п.33, в котором указанное заболевание представляет собой псориаз.
37. Применение по п.33, в котором указанное заболевание представляет собой экзематозный дерматит.
38. Применение по п.33, в котором указанное заболевание представляет собой саркому Капоши.
39. Применение по п.33, в котором указанное заболевание представляет собой рассеянный склероз.
40. Применение по п.33, в котором указанное заболевание представляет собой пролиферативное нарушение клеток гладких мышц.
41. Применение по п.33, в котором указанное заболевание представляет собой ревматоидный артрит.
42. Применение по п.33, в котором указанное заболевание представляет собой остеоартрит.
43. Применение по любому из пп.33-42, в котором указанное лекарственное средство предназначено для использования в комбинации с вторым противовоспалительным агентом.
44. Применение по любому из пп.33-42, в котором указанное лекарственное средство включает второй противовоспалительный агент.
45. Применение по п.43 или 44, в котором второй противовоспалительный агент выбран из группы, включающей ибупрофен, индометацин, фенопрофен, мефенаминовую кислоту, флуфенаминовую кислоту, сулиндак и кортикостроиды.
46. Применение по любому из пп.23-45, в котором указанное лекарственное средство подходит для перорального, местного, внутривенного, подкожного, парентерального, внутрикожного и чрезкожного введения.
47. Применение по любому из пп.23-46, в котором лекарственное средство предназначено для человека.
Текст
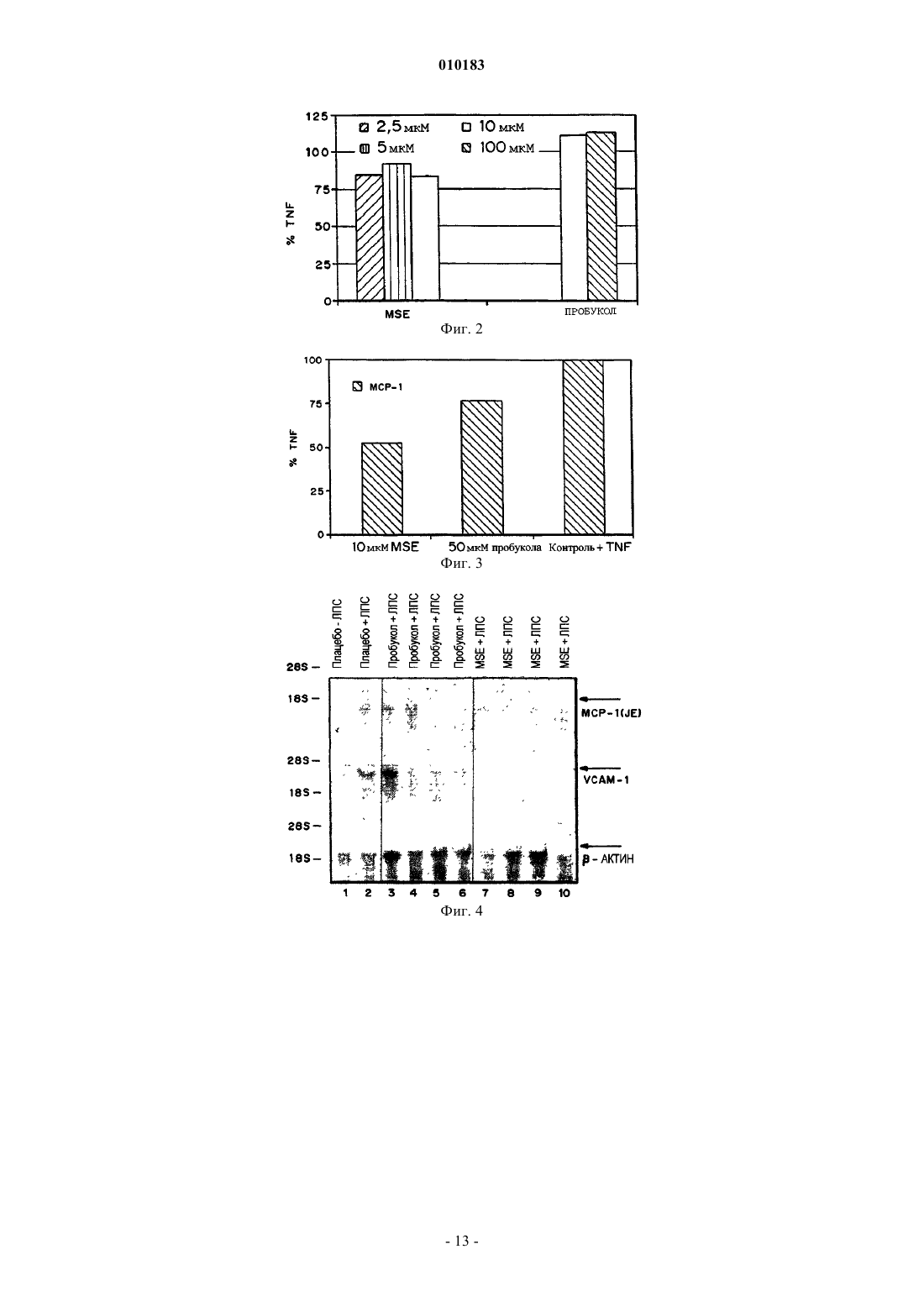
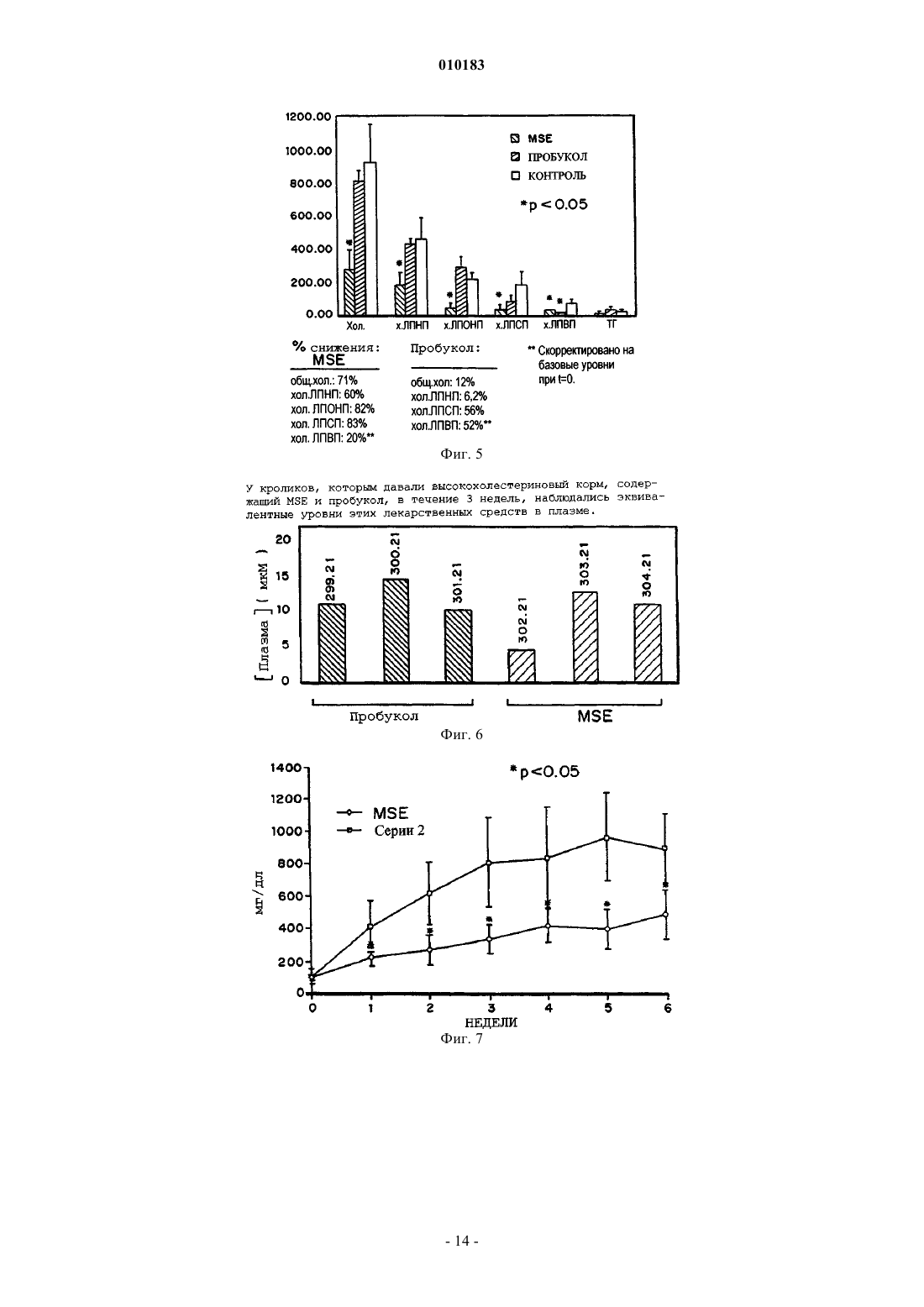
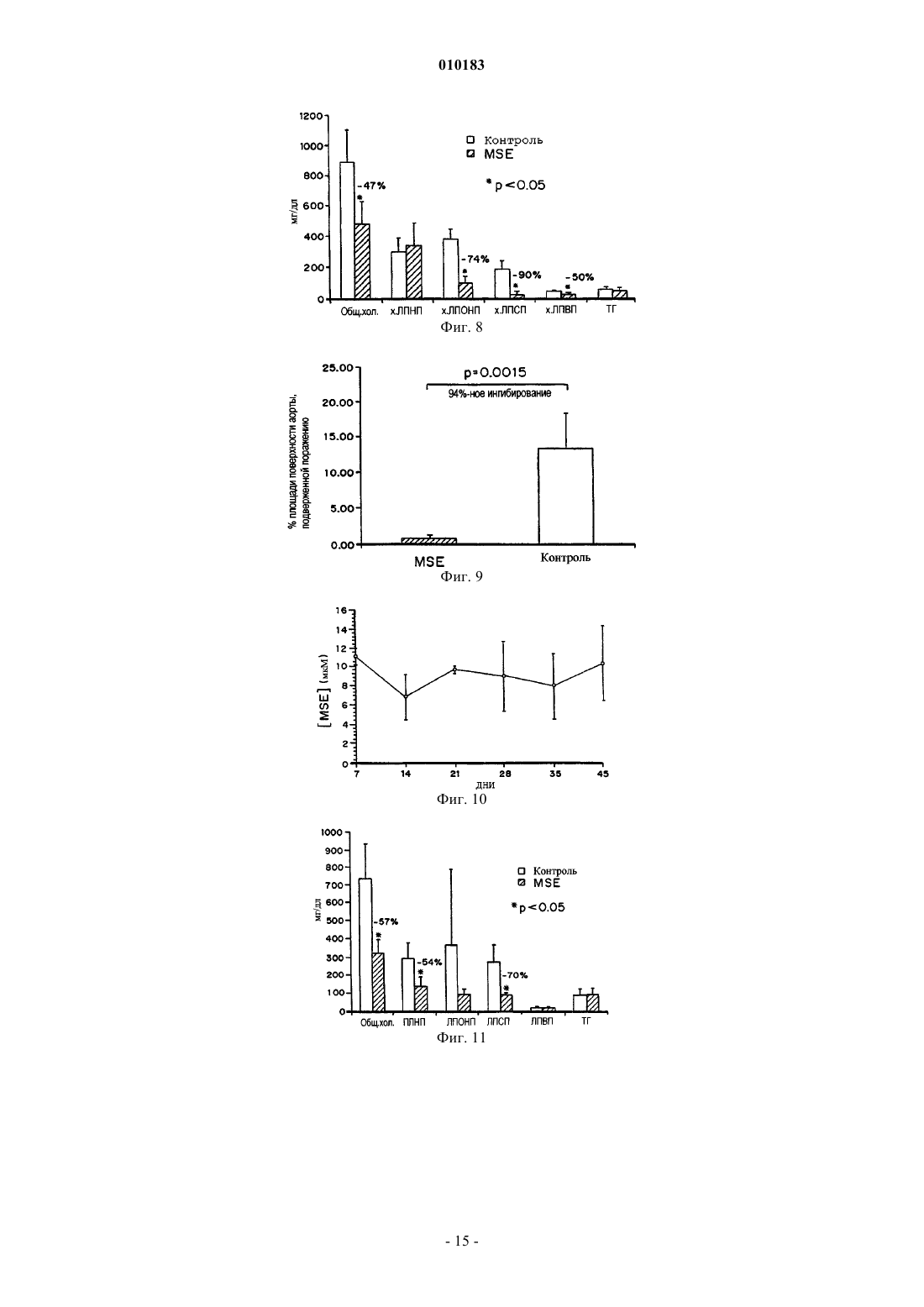
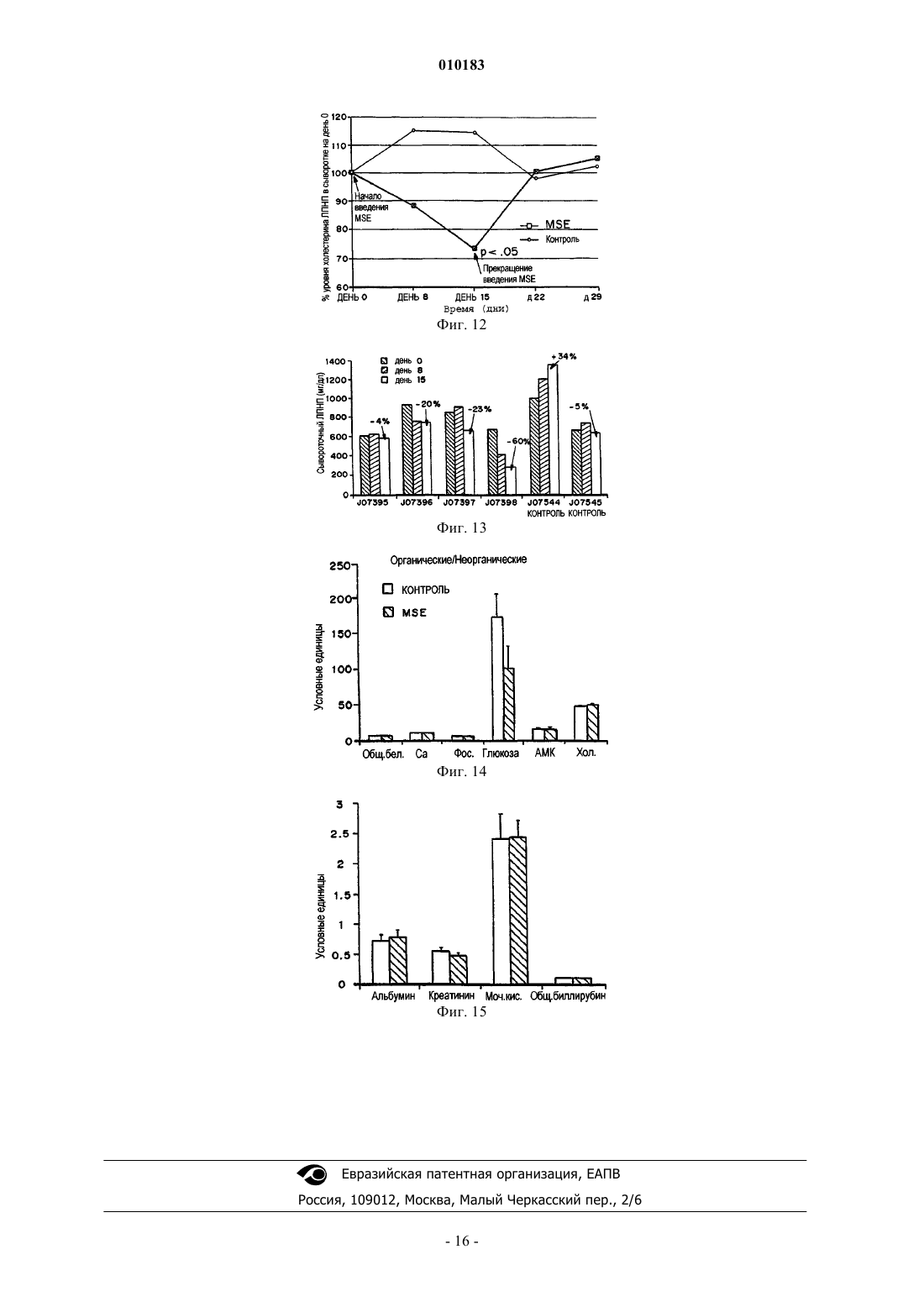
010183 Настоящее изобретение относится к способу для ингибирования адгезивной молекулы-1 клеток сосудов (VCAM-1), а, в частности, для лечения сердечно-сосудистых или воспалительных заболеваний,включая атеросклероз, где указанный способ предусматривает введение эффективного количества сложного моноэфира янтарной кислоты и пробукола. Предпосылки создания изобретения Сердечно-сосудистые заболевания остаются главной причиной смертности в Соединенных Штатах. Приблизительно девяносто процентов всех сердечно-сосудистых заболеваний в настоящее время диагностируется как атеросклероз. Сердечно-сосудистые заболевания связаны с несколькими этиологическими факторами, которые включают гиперхолестеринемию, гиперлипидемию и экспрессию VCAM-1 в эндотелиальных клетках сосудов. Гиперхолестеринемия и гиперлипидемия Гиперхолестеринемия является важным фактором риска, ассоциированным с сердечно-сосудистым заболеванием. Липопротеины сыворотки являются носителями для липицов в кровотоке. Липопротеины классифицируются по их плотности: хиломикроны, липопротеины очень низкой плотности (ЛПОНП), липопротеины низкой плотности (ЛПНП) и липопротеины высокой плотности (ЛПВП). Хиломикроны участвуют, главным образом, в транспорте пищевых триглицеридов и холестерина из кишечника в жировую ткань и печень. ЛПОНП обеспечивают доставку эндогенно синтезированных триглицеридов из печени в жировую ткань и в другие ткани. ЛПНП транспортируют холестерин в периферические ткани и регулируют уровни эндогенного холестерина в этих тканях. ЛПВП транспортируют холестерин из периферических тканей в печень. Холестерин на стенках артерий происходит почти исключительно от ЛПНП. Brownand Goldstein, Ann. Rev. Bicchem., 52, 223 (1983); Miller, Ann. Rev. Med., 31, 97 (1980). У пациентов с низкими уровнями ЛПНП атеросклероз развивается редко. Повышенные уровни холестерина ассоциируются с рядом патологических состояний, включая рестеноз, стенокардию, церебральный атеросклероз и ксантому. Желательно разработать метод снижения уровня холестерина в плазме у пациентов с развитием или с риском развития рестеноза, стенокардии,церебрального артериосклероза, ксантомы и других патологических состояний, ассоциируемых с повышенными уровнями холестерина в крови. Поскольку было определено, что гиперхолестеринемия обусловлена повышенными уровнями ЛПНП (гиперлипидемия), то были сделаны попытки снижения уровней ЛПНП посредством терапии с применением диеты. Существует несколько классов лекарственных средств, которые обычно используются для снижения уровней ЛПНП, включая вещества, усиливающие экскрецию желчных кислот, никотиновую кислоту (ниацин) и ингибиторы 3-гидрокси-3-метил-глутарилкофермент А (ГМГ-КоА)редуктазы. Пробукол и фибратные производные иногда используются в качестве вспомогательной терапии, обычно, в комбинации с другими лекарственными средствами. Было установлено, что ингибиторами ГМГ-КоА-редуктазы являются статины и вастатины. Статины, среди прочих, относятся к наиболее эффективным агентам, предлагаемым в настоящее время на фармацевтическом рынке для лечения гиперхолестеринемии, и включают правастатин (Pravchol, Bristol Myers Squibb), атровастатин (WarnerLambert/Pfizer), симвастатин (Zocor, Merck), ловастатин (Mevacor, Merck) и флувастатин (Lescol). Для многих пациентов достаточно использовать диету и один из гиполипидемических агентов. Однако пациенты с исходным уровнем холестерина ЛПНП, составляющим более 200 мг/дл, нуждаются в терапии для понижения уровней ЛПНП на 50% или более. Хотя, в некоторых случаях, такое снижение уровня ЛПНП может быть достигнуто с использованием лишь одного агента, однако в этих случаях, чаще всего наблюдается снижение лишь на 20-30%. Таким образом, для пациента с гетерозиготной врожденной гиперхолестеринемией с уровнем ЛПНП-холестерина 200-400 мг/дл, для достижения уровня ЛПНП-холестерина менее 100 мг/мл требуется использование комбинации из двух, а иногда из трех гиполипидемических лекарственных средств. Комбинация смолы, усиливающей экскрецию желчи и никотиновой кислоты, может способствовать снижению уровней ЛПНП на 45-55%, комбинация смолы и статина - приблизительно на 50-60%, комбинация никотиновой кислоты и статина - приблизительно на 50%,а терапия тремя лекарственными средствами с использованием комбинации из связывающей желчные кислоты смолы, статина и никотиновой кислоты способствует снижению указанных уровней почти на 70%. Имеющиеся данные позволяют предположить, что атерогенное действие липопротеина низкой плотности (ЛПНП) может быть частично опосредовано его окислительной модификацией. Было показано, что пробукол обладает сильнодействующими противоокислительными свойствами и блокирует окислительную модификацию ЛПНП. В соответствии с этим фактом было показано, что пробукол фактически замедляет прогрессирование атеросклероза у кроликов с дефицитом рецептора ЛПНП, как обсуждается в работе Carew et al., Proc. Natl. Acad. Sci., USA, 84:7725-7729 (1987). По всей вероятности, пробукол является эффективным благодаря своей высокой растворимости в липидах и транспортируется липопротеинами, защищая их, тем самым, от окислительного повреждения. По своей химической структуре пробукол относится к широко используемым пищевым добавкам 2,[3]-трет-бутил-4-гидроксианизолу (ВНА) и 2,6-ди-трет-бутил-4-метилфенолу (ВНТ). Пробукол имеет-1 010183 полное химическое название: 4,4'-(изопропилидендитио)-бис(2,6-ди-трет-бутилфенол). В настоящее время пробукол используется, главным образом, для снижения уровней холестерина в сыворотке у пациентов с гиперхолестеринемией. Пробукол обычно вводят в форме таблеток, выпускаемых под торговым знаком Lorelco. К сожалению, пробукол почти не растворяется в воде, а поэтому он не может быть инъецирован внутривенно. Действительно, пробукол очень плохо абсорбируется клетками in vitro из-за его плохой смешиваемости в буферах и в средах для культивирования клеток. Твердый пробукол плохо абсорбируется в кровь и выводится из организма почти в неизмененной форме. Кроме того, таблетка пробукола абсорбируется при существенно различных скоростях и в различных количествах у различных пациентов. В одном исследовании (Heeg et al., Plasma Levels of Probucol in Man AfterSingle and Repeated Oral Doses, La Nouvelle Presse Medicale, 9:2990-2994 (1980 было обнаружено, что максимальные уровни пробукола в сыворотке у различных пациентов отличаются почти в 20 раз. В другом исследовании, Kazuya et al., J. Lipid Res. 32:197-204 (1991), наблюдалось включение приблизительно менее 1 мкг пробукола на 106 клеток при инкубировании эндотелиальных клеток в течение 24 ч с 50 мкМ пробукола. В патенте США 5262439 (Parthasarathy) описаны растворимые аналоги пробукола, в которых одна или обе гидроксильные группы замещены сложноэфирными группами, что приводит к увеличению растворимости этого соединения в воде. В одном варианте это растворимое производное выбирают из группы, состоящей из сложного моно- или диэфира янтарной кислоты, глутаровой кислоты, адипиновой кислоты, субериновой кислоты, себациновой кислоты, азелаиновой кислоты или малеиновой кислоты и пробукола. В другом варианте производным пробукола является сложный моно- или диэфир, где этот сложный эфир содержит алкильную или алкенильную группу, которая включает функциональную группу, выбранную из группы, состоящей из карбоновокислотной группы, аминогруппы, соли аминогруппы,амидных групп и альдегидных групп. В ряде патентов Франции указывается, что некоторые производные пробукола представляют собой гипохолестеринемические и гиполипемические агенты: FR 2168137 (эфиры бис-4-гидроксифенилтиоалкановой кислоты); FR 2140771 (эфиры тетралинилфеноксиалкановой кислоты и пробукола); FR 2140769 (бензофурилоксиалкановокислотные производные пробукола); FR 2134810 (бис-(3-алкил-5-талкил-4-тиазол-5-карбокси)фенилтио)алканы; FR 2133024 (бис-(4-никотиноилоксифенилтио)пропаны; иFR 2130975 (бис(4-(феноксиалканоилокси)фенилтио)алканы). В патенте США 5155250 указывается, что 2,6-диалкил-4-силилфенолы являются противоатеросклеротическими агентами. В публикации РСТWO 95/15760, опубликованной 15 июня 1995, эти же самые соединения были описаны как агенты, снижающие уровни холестерина в сыворотке. В патенте США 5608095 указывается, что алкилированные 4-силилфенолы ингибируют перокисление ЛПНП,сжижают уровни холестерина в плазме и ингибируют эксгрессию VCAM-1, а поэтому они могут быть использованы для лечения атеросклероза. Экспрессия VCAM-1 Адгезия лейкоцитов к эндотелию представляет собой основной ранний результат в сердечнососудистых заболеваниях, а также в воспалительных состояниях широкого ряда, включая аутоиммунные нарушения и бактериальные и вирусные инфекции. Восстановление лейкоцитов в эндотелии начинается тогда, когда индуцируемые адгезивные молекулы-рецепторы, присутствующие на поверхности эндотелиальных клеток, взаимодействуют с контррецепторами, присутствующими на иммунных клетках. Эндотелиальные клетки сосудов определяют, какой именно тип лейкоцитов (моноцитов, лимфоцитов или нейтрофилов) восстанавливается при селективной экспрессии специфических адгезивных молекул, таких как адгезивная молекула-1 клеток сосудов (VCAM-1), молекула-1 межклеточной адгезии (ICAM-1) и Еселектин (ELAM). На самой ранней стадии атеросклеротического поражения происходит локализованная эндотелиальная экспрессия VCAM-1 и селективное восстановление мононуклеарных лейкоцитов, которые экспрессируют контррецептор интегрин VLA-4. Поскольку селективная экспрессия VLA-4 происходит на моноцитах и лимфоцитах, а не на нейтрофилах, то VCAM-1 играет важную роль в опосредовании селективной адгезии мононуклеарных лейкоцитов. VCAM-1 является медиатором хронических воспалительных заболеваний, таких как астма, ревматоидный артрит и аутоиммунный диабет. Так, например,известно, что у астматиков наблюдается повышенная экспрессия VCAM-1 и ICAM-1. Pilewski, J.M., et al.,Am. J. Respir. Cell Mol. Biol., 12:1-3 (1995); Ohkawara, Y., et al., Am. J. Respir. Cell Mol. Biol. 12:4-12(1995). Кроме того, блокирование рецепторов интегринов для VCAM-1 и ICAM-1 (VLA-4 и LFA-1, соответственно) приводит к подавлению как раннего, так и позднего ответа у овальбумин-восприимчивых экспериментальных крыс с моделью аллергической реакции дыхательных путей. Rabb, I1. A. et al., Am. J.Respir. Care Med. 149:1186-1191 (1994). Наблюдалась также повышенная экспрессия эндотелиальных адгезивных молекул, включая VCAM-1, в капиллярной сети ревматоидного синовиального слоя. Koch,A. E. et al.,. Lab. Invest. 64:313-322 (1991); Morales-Ducret, J. et al., Immunol. 149, 1421-1431 (1992). Нейтрализующие антитела, направленные против VCAM-1 или его контррецептора VLA-4, могут замедлять начало возникновения диабета у мышиной модели (у мышей NOD), у которых спонтанно развивается это заболевание. Yang, X. D. et al., Proc. Natl. Acad. Sci., USA, 90:10494-10498 (1993); Burkly, L. C. et al., Diabetes 43:523-534 (1994); Baron, J. L. et al., J. Clin. Invest. 93:1700-1708 (1994). Моноклональные антитела-2 010183 против VCAM-1 могут также оказывать благоприятное воздействие на животных с моделью отторжения аллотрансплантата, что дает основание предположить, что ингибиторы экспрессии VCAM-1 могут быть использованы для предотвращения отторжения трансплантата. Oroez, C.G et al., Immunol. Lett. 32:7-12VCAM-1 экспрессируется клетками как в мембрано-связанной форме, так и в растворимой форме. Было показано, что растворимая форма VCAM-1 индуцирует хемотаксис эндотелиальных клеток сосудовin vitro и стимулирует ангиогенный ответ в роговице крыс. Koch, A. F. et al., Nature 376:517-519 (1995). Ингибиторы экспрессии растворимого VCAM-1 обладают терапевтической ценностью для лечения заболеваний с сильным ангиогенным компонентом, включая развитие опухолей и метастазов. Folkman, J., andVCAM-1 экспрессируется в культивированных сосудистых эндотелиальных клетках человека после активации липополисахаридом (ЛПС) и цитокинами, такими как интерлейкин-1 (IL-1) и фактор некроза опухоли (TNF-). Эти факторы не являются селективными для активации экспрессии клеточноадгезивных молекул. Последующее превращение лейкоцитов в пенистные макрофаги приводит к синтезу широкого ряда воспалительных цитокинов, факторов роста и хемоаттрактантов, которые способствуют размножению лейкоцитов и восстановлению тромбоцитов, пролиферации клеток гладкой мышцы, активации эндотелиальных клеток и синтезу внеклеточного матрикса, характеризующемуся созреванием атеросклеротических бляшек. Молекулярный анализ регуляторных элементов, которые присутствуют на гене VCAM-1 человека и которые регулируют его экспрессию, дает основание предположить о важной роли ядерного фактора kB(NF-kB), фактора регуляции транскрипции или NF-kB-подобного связывающего белка в регуляции экспрессии гена VCAM-1, чувствительной к окислительно-восстановительным реакциям. Факторы транскрипции представляют собой белки, которые активируют (или подавляют) экспрессию гена в клеточных ядрах, путем связывания со специфическими ДНК-последовательностями, называемыми "энхансерными элементами", расположенными, в основном, вблизи этого гена и называемыми "промотором", с которого инициируется синтез РНК. Промоторы как для VCAM-1, так и для ICAM-1 были клонированы и охарактеризованы. Так, например, оба указанных промотора содержат множество элементов ДНК-последовательности, которые могут связываться с фактором транскрипции NF-kB. Iademarco, M. F. et al., J. Biol. Chem. 267:1632316329 (1992). Ядерный фактор-kB представляет собой фактор транскрипции широко экспрессируемой мультисубъединицы, который активируется в клетках нескольких типов различными воспалительными агентами широкого ряда, такими как TNF-, IL-1B, бактериальный эндотоксин и РНК-вирусы. Он играет ключевую роль в опосредовании воспалений и других сигналов стресса, передаваемых ядерному регуляторному аппарату клетки. Хотя биохимические сигналы, которые активируют NF-kB, точно не выяснены,однако известно, что этот фактор транскрипции может интегрироваться в общий молекулярный каскад реакций множества факторов риска и "этиологических" сигналов атеросклероза, таких как гиперлипидемия, курение, гипертензия и сахарный диабет. Активация NF-kB в сосудистых эндотелиальных клетках различными сигналами может специфически ингибироваться антиоксидантами, такими как N-ацетилцистеин и дитиокарбамат пирролидина. Это дает основание предположить, что кислородные радикалы играют важную роль в активации NF-kB посредством неясного окислительно-восстановительного механизма. Поскольку NF-kB-подобный энхансерный элемент также регулирует транскрипцию промотора гена VCAM-1 по механизму, чувствительному к окислительно-восстановительным реакциям, то было предположено, что окислительный стресс при атеросклеротическом поражении может играть определенную роль в регуляции экспрессии генаVCAM-1, опосредованной белком регуляции транскрипции, восприимчивой к окислительновосстановительным реакциям. В патенте США 5380747 (PCT/US93/10496) впервые указывается, что экспрессия VCAM-1 в сосудистых эндотелиальных клетках может быть ингибирована путем введения соединений класса дитиокарбаматов, таких как дитиокарбамат пирролидина. Поэтому эти дитиокарбаматы могут быть использованы для лечения сердечно-сосудистых заболеваний, и, как было показано, они приводят к значительному снижению уровня атеросклеротических поражений у кроликов с гиперхолестеринемией. Была высказана гипотеза, что модификация липопротеина низкой плотности (ЛПНП) в окислительно модифицированный ЛПНП (ок-ЛПНП) под действием реакционноспособных кислородных молекул является центральным событием, которое инициирует и стимулирует развитие атеросклероза. Steinberg,et al., N. Engl. J. Med. 1989; 320:915-924. Окисленный ЛПНП представляет собой комплексную структуру, состоящую, по крайней мере, из нескольких химически отличающихся окисленных соединений, каждое из которых, взятое отдельно или в комбинации друг с другом, может модулировать экспрессию генов адгезивных молекул, активированную цитокинами. Гидропероксиды жирных кислот, такие как линолеилгидропероксид (13-HPODE), продуцируются из свободных жирных кислот под действием липоксигеназ и являются важным компонентом окисленного ЛПНП.-3 010183 Было сделано предположение, что генерирование окисленных липидов инициируется под действием системы клеточных липоксигеназ, после чего эти окисленные липиды переносятся в ЛПНП. Это происходит после реакции амплификации в ЛПНП в среде, катализируемой переходными металлами и/или сульфгидрильными соединениями. Предварительные исследования показали, что модификация жирных кислот в культивированных эндотелиальных клетках может приводить к изменению их восприимчивости к окислительному повреждению. В PCT/US95/05880 указывается, что полиненасыщенные жирные кислоты и их гидропероксиды индуцируют экспрессию VCAM-1, но не ICAM-1 или Е-селектина, в эндотелиальных клетках аорты человека посредством механизма, который не опосредуется цитокинами или другими нецитокиновыми сигналами. Этот факт является фундаментальным открытием важных и ранее неизвестных каскадов биологических реакций при VCAM-1-опосредованных иммунных ответах. ВPCT/US95/05880 сообщается также, что индуцирование VCAM-1 полиненасыщенными жирными кислотами и их гидропероксидами подавляется дитиокарбаматами, включая дитиокарбамат пирролидина. Поскольку в настоящее время сердечно-сосудистые заболевания являются главной причиной смертности в Соединенных Штатах, то назрела крайняя необходимость в разработке новых способов лечения этих заболеваний. Важным этапом для достижения этой цели является получение новых агентов,которые позволили бы одновременно лечить гиперхолестеринемию, гиперлипидемию и которые ингибировали бы экспрессию VCAM-1 в эндотелиальных клетках сосудов. Следовательно, целью настоящего изобретения является обеспечение способа и композиции для подавления VCAM-1, а в частности, - способа лечения сердечно-сосудистых заболеваний. Другой целью настоящего изобретения является обеспечение способа и композиции для лечения сердечно-сосудистых заболеваний, которые могли бы одновременно использоваться для лечения гиперхолестеринемии, гиперлипидемии и для ингибирования экспрессии VCAM-1 в эндотелиальных клетках сосудов. Краткое описание изобретения Было обнаружено, что сложный моноэфир янтарной кислоты и пробукола является эффективным для одновременного снижения уровня холестерина, снижения уровней ЛПНП и ингибирования экспрессии VCAM-1, а поэтому указанное соединение может быть использовано в качестве составного агента для лечения сердечно-сосудистых заболеваний. Поскольку это соединение одновременно обладает тремя важными активностями, обеспечивающими защиту кровеносных сосудов, то для достижения того же самого эффекта пациент, вместо множества лекарственных средств, может принимать одно единственное лекарственное средство. Это повышает надежность терапии и создает удобство для пациента. Обнаружение того факта, что сложный моноэфир янтарной кислоты и пробукола ингибируетVCAM-1, было довольно неожиданным, если принять во внимание то, что сам пробукол, будучи сильным антиоксидантом, не оказывает значительного воздействия на экспрессию VCAM-1. Сложные диэфиры пробукола, как и статины, также не оказывают значительного воздействия на экспрессию VCAM1. Было также обнаружено, что у кроликов сложный моноэфир янтарной кислоты способствует снижению ЛПВП лишь в небольшой степени, тогда как у мышей и обезьян он всеобще не оказывает воздействия на ЛПВП. В противоположность этому пробукол снижает уровни ЛПНП лишь в незначительной степени и значительно снижает уровни ЛПВП. Статины снижают уровни ЛПНП и могут влиять, а могут и не влиять на уровни ЛПВП. Кроме того, было обнаружено, что моноэфир янтарной кислоты и пробукола (обозначаемый в настоящем описании "MSE"), селективно ингибирует TNF-индуцированную экспрессию генов VCAM-1 и МСР-1, но не гена ICAM-1, в эндотелиальных клетках аорты человека. MSE не оказывает воздействия на активацию NF-kB. Поскольку было обнаружено, что, моноэфир янтарной кислоты и пробукола, блокирует индуцированную экспрессию адгезивной молекулы VCAM-1 на поверхности эндотелиальных клеток, то этот сложный эфир может быть использован для лечения любого заболевания, опосредованного VCAM-1,включая атеросклероз, рестеноз после ангиопластики, заболевание, поражающее коронарную артерию,стенокардию, и другие сердечно-сосудистые заболевания, а также воспалительные заболевания, которые не относятся к сердечно-сосудистым заболеваниям, но которые опосредуются VCAM-1. Это соединение может быть также использовано для лечения отторжения трансплантата при пересадке сердца. Соединение, описанное в настоящей заявке, может быть использовано как для основного, так и для дополнительного лечения сердечно-сосудистых заболеваний. Это соединение используется для основного лечения, например, состояний при ишемической болезни сердца, включая атеросклероз, рестеноз после ангиопластики, заболевание, поражающее коронарную артерию, и стенокардию. Это соединение может быть введено для лечения заболевания, поражающего капилляры, которое не поддается лечению хирургическими методами или методами ангиопластики, или других сосудистых заболеваний, при которых не показана хирургическая операция. Это соединение может быть также использовано для стабилизации состояния пациента перед проведением терапии по реваскуляризации. Настоящее изобретение, при его надлежащем использовании, дает возможность проводить терапевтическое лечение атеросклероза путем предупреждения развития новых поражений и стимуляции об-4 010183 ратного развития уже имеющихся поражений. В альтернативном варианте осуществления изобретения описанное здесь соединение могут быть использовано для лечения воспалительных кожных заболеваний, которые опосредуются VCAM-1, а, в частности, нарушений эндотелия человека, которые опосредуются VCAM-1, и которыми являются, но не ограничиваются ими, астма, псориаз, экзематозный дерматит, саркома Капоши, рассеянный склероз, а также пролиферативные нарушения клеток гладких мышц. В другом варианте осуществления изобретения описанное здесь соединение может быть выбрано для лечения воспалительных состояний, которые опосредуются мононуклеарными лейкоцитами. Краткое описание чертежей На фиг. 1 представлена гистограмма для сравнения действия сложного моноэфира янтарной кислоты и пробукола с действием пробукола при концентрациях 2,5 мкМ, 5 мкМ, 10 мкМ и 100 мкМ на экспрессию VCAM-1 в клетках НАЕС. На фиг. 2 представлена гистограмма для сравнения действия сложного моноэфира янтарной кислоты и пробукола с действием пробукола при концентрациях 2,5 мкМ, 5 мкМ, 10 мкМ и 100 мкМ на экспрессию ICAM-1 в клетках НАЕС. На фиг. 3 представлена гистограмма для сравнения действия 10 мкМ сложного моноэфира янтарной кислоты и пробукола с действием 50 мкМ пробукола и TNF на экспрессию МСР-1 в эндотелиальных клетках аорты человека (НАЕС). На фиг. 4 проиллюстрировано действие сложного моноэфира янтарной кислоты и пробукола (10 и 25 мкМ) с действием пробукола (50 мкМ) на экспрессию гена в клетках НАЕС. На фиг. 5 представлена гистограмма для сравнения действия сложного моноэфира янтарной кислоты и пробукола с действием пробукола на уровни холестерина в плазме кроликов, которым давали пищу,содержащую липиды. На фиг. 6 представлена гистограмма для сравнения концентрации сложного моноэфира янтарной кислоты и пробукола с концентрацией пробукола в плазме кроликов через три недели после введения дозы. На фиг. 7 представлена кривая, иллюстрирующая действие сложного моноэфира янтарной кислоты и пробукола на уровни холестерина в плазме в кроличьей модели гиперхолестеринемии в течение шести недель. На фиг. 8 представлена гистограмма, иллюстрирующая действие сложного моноэфира янтарной кислоты и пробукола на уровни общего холестерина, холестерина ЛПНП, холестерина ЛПОНП, холестерина ЛПСП, холестерина ЛПВП и ТГ у кроликов через шесть недель после кормления их пищей, содержащей липиды. На фиг. 9 представлен график процента площади поверхности пораженной аорты у необработанных кроликов, принимавших жирную пищу, и у кроликов, обработанных сложным моноэфиром янтарной кислоты и пробукола. На фиг. 10 представлена кривая микромолярных уровней сложного моноэфира янтарной кислоты и пробукола в плазме в зависимости от дня обработки. На фиг. 11 представлена гистограмма уровней общего холестерина, ЛПОНП, ЛПСП, ЛПНП, ЛПВП и триглицеридов у АроЕ-КО-мышей через две недели после перорального введения этим мышам сложного моноэфира янтарной кислоты и пробукола по отношению к контролю, в мг/мл. На фиг. 12 представлен график, иллюстрирующий снижение уровня ЛПНП в сыворотке у обезьян с гиперхолестеринемией во время и после введения сложного моноэфира янтарной кислоты и пробукола. На фиг. 13 представлена гистограмма, иллюстрирующая действие сложного моноэфира янтарной кислоты и пробукола на уровень ЛПНП в сыворотке у обезьян с гиперхолестеринемией. На фиг. 14 представлена гистограмма, иллюстрирующая влияние перорального введения крысам в течение двух недель стожного моноэфира янтарной кислоты и пробукола в концентрации 1000 мг/кг/д на содержание общего белка, кальция, фосфата, глюкозы, азота мочевины крови и холестерина по отношению к контролю, в условных единицах. На фиг. 15 представлена гистограмма, иллюстрирующая влияние перорального введения крысам в течение двух недель стожного моноэфира янтарной кислоты и пробукола в концентрации 1000 мг/кг/д на содержание альбумина, креатинина, мочевой кислоты и общего биллирубина по отношению к контролю,в условных единицах. Подробное описание изобретенияI. Определения. Термин "сложный моноэфир янтарной кислоты и пробукола", используемый в настоящем описании, включает сложный моноэфир янтарной кислоты и пробукола и его соль. Для лечения атеросклероза и других сердечно-сосудистых и воспалительных заболеваний сложные моноэфиры пробукола должны быть выбраны так, чтобы они обладали нужной липофильностью для их локализации в пораженном участке. Это соединение не должно быть подвергнуто компартментализации в областях низкого метаболизма, таких как области отложения жира. В предпочтительном варианте осуществления изобретения для лечения сердечно-сосудистого заболевания фармакокинетика данного со-5 010183 единения не должна резко изменяться при застойной сердечной недостаточности или почечной недостаточности. Активное соединение вводят любым подходящим способом, включая, но не ограничиваясь системным введением, включая пероральное или внутривенное, или местное введение, включая чрескожное введение. Общий уровень доз должен составлять в пределах от 0,1 до 500 мг/кг массы тела, причем указанные дозы вводят по схеме: от одного раза через день до двух или нескольких раз в день. Продолжительность курса лечения предусматривает прием одноразовой дозы, вводимой лишь от одного до двух раз в день, в течение от двух до шести месяцев. Для терапевтического лечения сердечно-сосудистых заболеваний эти соединения могут быть также введены непосредственно в стенку сосуда с использованием перфузионных катетеров-баллонов после или вместо ангиопластики коронарной или других артерий. Так, например, 2-5 мл физиологически приемлемого раствора, который содержит приблизительно 1-500 мМ соединения или смеси соединений,вводят под давлением 1-5 атмосфер. Затем, в течение последующих шести месяцев, во время периода максимального риска рестеноза, активные соединения вводят в соответствии с другими подходящими способами и схемами лечения. Относительно короткий курс лечения указанным активным соединением проводят для уменьшения поражений при заболевании коронарной артерии, которое не поддается лечению ни посредством ангиопластики, ни посредством хирургического вмешательства. Неограничивающим примером такого кратковременного курса лечения является введение доз в интервалах от 0,5 до 500 мг/кг массы тела по схеме от одного раза через день до трех раз в день в течение от двух до шести месяцев. Более длительное лечение может быть проведено для предупреждения развития прогрессирующих поражений у пациентов с высоким риском заболевания. Длительный курс лечения может быть проведен в течение нескольких лет с использованием доз в интервале от 0,5 до 500 мг/кг массы тела по схеме введения от одного раза через день до трех раз в день. Активное соединение может быть также введено в период времени перед и после коронарной ангиопластики в целях уменьшения или предотвращения аномального пролиферативного и воспалительного ответа, который легко приводит к клинически диагностируемому рестенозу. Активное соединение может быть введено в комбинации с другими лекарственными препаратами,используемыми для лечения сердечно-сосудистых заболеваний, включая ингибиторы агрегации тромбоцитов, такие как аспирин; противотромботические агенты, такие как кумадин; блокаторы кальциевых каналов, такие как варапамил, дилтиазем и нифедипин; ингибиторы ангиотензин-конвертирующего фермента (АСЕ), такие как каптоприл и эналоприл; и -блокаторы, такие как пропаналол, тербуталол и лабеталол. Активные соединения могут быть также введены в комбинации с нестероидными противовоспалительными агентами, такими как ибупрофен, индометацин, фенопрофен, мефенаминовая кислота, флуфенаминовая кислота, сулиндак. Данное соединение может быть так же введено вместе с кортикостроидами.MSE, вводимый посредством чрескожно имплантируемых гранул (гранул с высвобождением 150 мг/кг/день активного соединения), блокирует ЛПС-индуцированную экспрессию гена VCAM-1 и МСР-1 в легких мышиной модели. Пероральное введение MSE (150 мг/кг/день) в течение шести недель снижает уровни общего АрОВ-содержащего липопротеина и уровни ЛПВП-холестерина в плазме у экспериментальных новозеландских белых кроликов. Это действие на уровни холестерина в плазме сопровождается заметным ингибированием образования атеросклеротических повреждений, аккумуляции макрофагов и экспрессииVCAM-1. Пероральное введение MSE в течение двух недель способствует селективному снижению ароВсодержащих липопротеинов у экспериментальных черных мышей С 57, которые получали холестерин с пищей, и у ароЕ-"накаченных" мышиных моделей, и не оказывает при этом какого-либо влияния на уровень ЛПВП. Пероральное введение MSE в течение двух недель собакоподобным обезьянам с моделью гиперхолестеринемии приводит к снижению общего холестерина в плазме и холестерина ЛПНП, не влияя при этом на уровень ЛПВП.MSE не является мутагеном в бактериальном тесте Ames. Пероральное введение крысам в течение двух недель MSE в концентрации 1000 мг/кг/день не приводило к их гибели и не оказывало какого-либо воздействия на сывороточный электролит и гематокритное число. Наблюдалось повышение ЛПНП, щелочной фосфатазы, ГОТС и ГПТС в сыворотке, но это повышение не имело какого-либо статистически значимого отличия по сравнению с необработанной группой и не сопровождалось какими-либо изменениями морфологии или гистопатологии печени. Для местного применения в целях лечения воспалительных поражений кожи выбранное соединение должно быть приготовлено так, чтобы оно могло абсорбироваться кожей в количестве, достаточном для достижения терапевтического эффекта в месте поражения. Сложный моноэфир пробукола должен быть физиологически приемлемым. В основном, приемлемыми являются соединения с терапевтическим индексом, составляющем, по крайней мере, 2, а предпочтительно по крайней мере 5-10. Терапевтический индекс определяют как EC50/IC50, где EC50 представляет собой концентрацию соединения, которая инги-6 010183 бирует экспрессию VCAM-1 на 50%, a IC50 представляет собой концентрацию соединения, которая обладает 50%-ной токсичностью для клеток-мишеней. Клеточная токсичность может быть измерена путем прямого подсчета клеток, путем исключения трипанового синего или путем исследований различных метаболических активностей, таких как включение 3 Н-тимидина, известных специалистам. Настоящее изобретение, кроме того, проиллюстрировано в нижеприведенных примерах, которые приводятся лишь в целях иллюстрации и не должны рассматриваться как ограничение объема изобретения. Пример 1. Экспрессия VCAM-1 в эндотелиальных клетках аорты человека. На фиг. 1 представлена гистограмма для сравнения действия сложного моноэфира янтарной кислоты и пробукола с действием пробукола при концентрациях 2,5 мкМ, 5 мкМ, 10 мкМ и 100 мкМ на экспрессию VCAM-1 в эндотелиальных клетках аорты человека in vitro как процент от экспрессии VCAM-1,индуцированной только одним TNF. Эти клетки инкубировали в течение шестнадцати часов в среде для культивирования клеток при 37 С в инкубаторе для тканевых культур. Через шестнадцать часов клетки промывали и инкубировали с антителами против VCAM-1. Количество антитела, связывающегося с клетками, определяли с помощью колориметрического ELISA-анализа с использованием конъюгирсванного с пероксидазой хрена антитела против антитела к VCAM-1. Как было указано, MSE ингибирует экспрессию VCAM-1 в тех условиях, при которых пробукол не оказывает заметного воздействия наVCAM. Пример 2. Экспрессия ICAM-1 в эндотелиальных клетках аорты человека. На фиг. 2 представлена гистограмма для сравнения действия сложного моноэфира янтарной кислоты и пробукола с действием пробукола при концентрациях 2,5 мкМ, 5 мкМ, 10 мкМ и 100 мкМ на экспрессию ICAM-1 в эндотелиальных клетках аорты человека in vitro как процент от экспрессии ICAM-1,индуцированной только одним TNF. Эти клетки инкубировали в течение шестнадцати часов в среде для культивирования клеток при 37 С в инкубаторе для тканевых культур. Через шестнадцать часов клетки промывали и инкубировали с антителами против ICAM-1. Количество антитела, связывающегося с клетками, определяли с помощью колориметрического ELISA-анализа с использованием конъюгированного с пероксидазой хрена антитела против антитела к ICAM-1. Как было указано, MSE оказывает лишь незначительное действие на экспрессию ICAM-1, которое не очень зависит от концентрации, причем пробукол вообще не оказывает какого-либо действия на экспрессию ICAM. Пример 3. Экспрессия МСР-1 в эндотелиальных клетках аорты человека. На фиг. 3 представлена гистограмма для сравнения действия 10 мкМ сложного моноэфира янтарной кислоты и пробукола с действием 50 мкМ пробукола и TNF на экспрессию МСР-1 в эндотелиальных клетках аорты человека (НАЕС). Эти клетки обрабатывали либо только TNF, либо TNF вместе с 10 мкмоль сложного моноэфира янтарной кислоты и пробукола в течение 4 ч. Культуральную клеточную среду собирали и использовали для подсчета количества МСР-1 с использованием колориметрическогоELISA-анализа. Как было проиллюстрировано, сложный моноэфир пробукола ингибировал экспрессию МСР-1 в гораздо большей степени, чем сам пробукол. МСР-1 представляет собой белок-хемоаттрактант,который способствует восстановлению моноцитов на участке атеросклеротического поражения. Пример 4. Влияние сложного моноэфира янтарной кислоты и пробукола на экспрессию гена в эндотелиальных клетках аорты человека in vitro. На фиг. 4 проиллюстрирован Нозерн-блот-анализ экспрессии генов VCAM-1 и МСР 1 из РНК, выделенной из легкого АроЕ-"накаченных" мышей, которым был введен ЛПС. Мышам подкожно вводилиMSE, пробукол и плацебо в 400 мг гранулах с пролонгированным 90-дневным высвобождением. Через одну неделю мышам внутрибрюшинно вводили 1 мг/кг ЛПС. Через два часа животных умерщвляли, и их легкие замораживали для выделения РНК. РНК фракционировали по размеру путем электрофореза в денатурирующем 1,0% агарозном геле, переносили на нейлоновую мембрану и гибридизовали с 32 Рмеченным кДНК-зондом, специфичным для мышиного JE. После этого мембрану разрезали и гибридизовали с кДНК, специфичной к мышиному VCAM-1, а затем с кДНК-зондом, специфичным к куриномуактину. Пример 5. Действие сложного моноэфира янтарной кислоты и пробукола на уровни холестерина в плазме у кроликов, которым давали пищу, содержащую липиды. На фиг. 5 представлена гистограмма для сравнения действия сложного моноэфира янтарной кислоты и пробукола с действием пробукола на уровни общего холестерина и холестерина липопротеинов в плазме кроликов, которым давали пищу, содержащую липиды. Кроликам давали корм с высоким содержанием жиров (0,5% холестерина и % кокосового масла), включающий 0,5 мас.% MSE или пробукола, в течение трех недель. Контрольным животным давали тот же самый корм, но без добавления лекарственных средств. Липопротеиновые фракции выделяли из цельной плазмы с помощью жидкостной экспрессхроматографии и анализировали на содержание холестерина. MSE приводил к статистически значимому снижению всех липопротеиновых фракций, а пробукол давал лишь снижение уровня холестерина в ЛПВП (р 0,05). Пример 6. Сравнение влияния уровней лекарственных средств MSE и пробукола в плазме кроликов,которым давали корм с высоким содержанием холестерина в течение трех недель MSE или пробукол-7 010183 вводили кроликам в течение трех недель вместе с кормом, имеющим высокое содержание жира (0,5% холестерина и 3% кокосового масла), в концентрации 0,5 мас.%. Эти лекарственные средства экстрагировали из плазмы эфиром и анализировали с помощью жидкостной хроматографии высокого давления. Как указывалось, уровни пробукола и MSE были аналогичны, хотя, как было показано в предыдущих примерах, эти соединения оказывали в значительной степени различное действие на уровни холестерина и липопротеина в плазме. Пример 7. Влияние MSE на активацию NF-kB. Эндотелиальные клетки аорты человека обрабатывали только одним TNF или TNF в комбинации с 25 мкмол MSE или PDTC в течение либо одного часа, либо двух часов, либо четырех часов. Эти клетки промывали и получали ядерные экстракты для проведения анализа на сдвиг в геле с использованием зонда для промотора VCAM-1 Было установлено, что MSE не оказывает влияния на активацию NF-kV, тогда как PDTC ингибирует активацию NF-kB. Пример 8. Влияние MSE на уровни холестерина у кроликов через шесть недель после кормления их пищей, содержащей холестерин. Новозеландским белым кроликам давали жирную пищу с высоким содержанием холестерина(0,5%) как отдельно, так и вместе с 0,5 мас.% (приблизительно 150 мг/кг/день) либо AGE-3, либо пробукол, в течение шести недель. На фиг. 8 представлена гистограмма, иллюстрирующая действие сложного моноэфира янтарной кислоты и пробукола на уровни общего холестерина, холестерина ЛПНП, холестерина ЛПОНП, холестерина ЛПСП, холестерина ЛПВП и триглицеридов (ТГ) у кроликов через шесть недель после кормления их пищей, содержащей липиды. Через шесть недель липопротеиновые фракции выделяли из цельной плазмы с помощью жидкостной экспресс-хроматографии и анализировали на содержание холестерина и триглицеридов. Как показано в примере 8, при обработке AGE-3 наблюдалось большее снижение общего холестерина, а также холестерина в ЛПОНП и ЛПСП, чем при обработке пробуколом. Пример 9. Влияние AGE-3 на прогрессирование атеросклероза при гиперхолестеринеми. Кроликов, описанных в примере 8, умерщвляли и аорты выделяли. Эти аорты окрашивали суданом 4 и анализировали на уровень окрашивания. На фиг. 9 представлен график процента площади поверхности пораженной аорты у MSE-обработанных кроликов и у необработанных кроликов, которым давали пищу, содержащую липиды. Аорты кроликов, которым вводили AGE-3, имели гораздо меньшую окраску, что указывало на снижение атеросклеротического поражения у кроликов, обработанных сложным моноэфиром янтарной кислоты и пробукола. Срезы аорт кроликов были подвергнуты иммуноокрашиванию с использованием антител противVCAM-1 или антигена Ram-11 для оценки экспрессии VCAM-1 или аккумуляции макрофагов. ОбработкаAGE-3 приводила к заметному снижению уровня экспрессии VCAM-1 и аккумуляции макрофагов (то есть приблизительно на более чем 75%). В аналогичном эксперименте пробукол, при тех же самых дозах,оказался менее эффективным (снижение экспрессии VCAM-1 и аккумуляция макрофагов составляло менее 25%). Пример 10. AGE-3 способствует обратимому снижению ЛПНП у обезьян с гиперхолестеринемией. Перед введением доз AGE-3 у собакоподобных обезьян была индуцирована гиперхолестеринемия путем их кормления жирной пищей с высоким содержанием холестерина. Затем этим обезьянам вводили пероральную дозу AGE-3 (100 мг/кг/день) в течение двух недель. За этот период процент сывороточного ЛПНП у этих обезьян снижался от 4 до 60%. После этого введение лекарственного средства прекращали и на 29-й день проверяли содержание холестерина в сыворотке. Этот уровень холестерина возвращался к значению, наблюдаемому до обработки, и оставался на этом уровне. Пример 10. На фиг. 10 представлен график микромолярных уровней сложного моноэфира янтарной кислоты и пробукола в плазме в зависимости от дня обработки. Как было показано, уровень MSE в плазме оставался почти постоянным. Пример 11. На фиг. 11 представлена гистограмма уровней общего холестерина, ЛПОНП, ЛПСП,ЛПНП, ЛПВП и триглицеридов у АроЕ-КО-мышей через две недели после перорального введения этим мышам сложного моноэфира янтарной кислоты и пробукола (150 мг/кг/день) по отношению к контролю,в мг/мл. Пример 12. На фиг. 12 представлен график, иллюстрирующий снижение уровня ЛПНП у обезьян с гиперхолестеринемией во время и после введения сложного моноэфира янтарной кислоты и пробукола. Пример 13. На фиг. 13 представлена гистограмма, иллюстрирующая влияние сложного моноэфира янтарной кислоты и пробукола на уровень ЛПНП в сыворотке у обезьян с гиперхолестеринемией. Пример 14. На фиг. 14 представлена гистограмма, иллюстрирующая влияние перорального введения крысам в течение двух недель сложного моноэфира янтарной кислоты и пробукола в концентрации 1000 мг/кг/д на содержание общего белка, кальция, фосфата, глюкозы, азота мочевины крови и холестерина по отношению к контролю, в условных единицах. Пример 15. На фиг. 15 представлена гистограмма, иллюстрирующая влияние перорального введения крысам в течение двух недель сложного эфира янтарной кислоты и пробукола в концентрации 1000 мг/кг/д на содержание альбумина, креатинина, мочевой кислоты и общего биллирубина по отношению к-8 010183 контролю, в условных единицах. Было отмечено различие в действии MSE и пробукола у мышей, по сравнению с кроликами и обезьянами с точки зрения влияния на уровень общего холестерина и ЛПНП. MSE является значительно более эффективным в снижении как уровня холестерина, так и уровня ЛПНП у кроликов и обезьян, чем у мышей. Очевидно, что у мышей, MSE оказывает то же самое действие, что и пробукол, то есть минимальное действие, если он вообще оказывает какое-либо действие на эти два фактора. Однако MSE ингибирует экспрессию VCAM-1 у всех исследованных видов животных.III. Фармацевтические композиции. Человек, лошади, собаки, коровы и другие животные, а в частности, млекопитающие, страдающие любыми из вышеописанных состояний, включая сердечно-сосудистые расстройства и воспалительные состояния, опосредованные VCAM-1, могут быть подвергнуты лечению путем введения пациенту эффективного количества сложного моноэфира янтарной кислоты и пробукола или его фармацевтически приемлемой соли в фармацевтически приемлемом носителе или разбавителе. Активное соединение может быть введено любыми подходящими способами, например перорально, парентерально, внутривенно,внутрикожно, подкожно или местно. Используемый в настоящем описании термин "фармацевтически приемлемые соли" означает соли,которые сохраняют желаемую биологическую активность вышеупомянутых соединений и обладают минимальным нежелательным токсическим действием. Неограничивающими примерами таких солей являются (а) кислотно-аддитивные соли, образованные неорганическими кислотами (например, хлористо-водородной кислотой, бромисто-водородной кислотой, серной кислотой, фосфорной кислотой, азотной кислотой и т.п.), и соли, образованные органическими кислотами, такими как уксусная кислота, щавелевая кислота, винная кислота, янтарная кислота,яблочная кислота, аскорбиновая кислота, бензойная кислота, дубильная кислота, памовая кислота, альгиновая кислота, полиглутаминовая кислота, нафталинсульфоновая кислота, нафталиндисульфоновая кислота и полигалактуроновая кислота; (b) основно-аддитивные соли, образованные катионами поливалентных металлов, таких как цинк, кальций, висмут, барий, магний, алюминий, медь, кобальт, никель,кадмий, натрий, калий и т.п., или органическими катионами, образованными из N,Nдибензилэтилендиамина, D-глюкозамина, аммония, тетраэтиламмония или этилендиамина; или (с) комбинации соединений (а) и (b), например, таннатная соль цинка или т.п. Активное соединение вводят в фармацевтически приемлемый носитель или разбавитель в количестве, достаточном для доставки в организм пациента терапевтически эффективного количества активного соединения, и не оказывающем серьезного токсического действия на организм пациента, подвергающегося лечению. Предпочтительная доза активного соединения для всех вышеупомянутых состояний составляет в пределах от около 0,1 до 500 мг/кг, а предпочтительно 1-100 мг/кг/день. Интервал эффективных доз фармацевтически приемлемых производных может быть определен на основании массы исходного соединения, необходимого для доставки. Если это производное само обладает активностью, то эффективная доза может быть определена, как указано выше, исходя из массы производного, или другими способами, известными специалистам. Для системного введения это соединение обычно вводят в любой подходящей унифицированной лекарственной форме, включая лекарственную форму, но не ограничиваясь ею, содержащую 1-3000 мг, а предпочтительно 5-500 мг активного ингредиента на унифицированную лекарственную форму. Пероральная доза обычно составляет 25-250 мг активного соединения. Активный ингредиент должен быть введен так, чтобы его максимальная концентрация в плазме достигала от около 0,1 до 100 мМ, а предпочтительно около 1-10 мМ. Это может быть достигнуто, например, путем внутривенной инъекции раствора или композиции активного ингредиента, необязательно, в физиологическом растворе или в водной среде, либо путем введения в виде болюса, содержащего активный ингредиент. Концентрация активного соединения в лекарственной композиции зависит от скорости абсорбции,распределения, инактивации и выведения лекарственного средства, а также от других факторов, известных специалистам. При этом следует отметить, что значения доз могут также варьироваться в зависимости от тяжести состояния, подвергаемого лечению. Кроме того, следует отметить, что для любого конкретного индивидуума конкретный интервал доз должен быть скорректирован в соответствии с периодом времени, индивидуальной потребностью и профессиональной оценкой специалиста, осуществляющего назначение по введению композиций или наблюдение за введением данных композиций; и что интервал доз, указанный в данном описании, приводится лишь в качестве примера и не должен рассматриваться как ограничение объема или применения заявленной композиции. Активный ингредиент может быть введен в виде разовой дозы, либо он может быть разделен на несколько дробных доз, которые могут быть введены через различные интервалы времени. Пероральные композиции, в основном, включают инертный разбавитель или пищевой носитель. Они могут быть включены в желатиновые капсулы или спрессованы в таблетки. Для перорального введения в терапевтических целях активное соединение может быть введено вместе с носителями и использовано в форме таблеток, пастилок или капсул. В данную композицию, в качестве ее составной части,могут быть включены фармацевтически приемлемые связующие агенты и/или добавки.-9 010183 Таблетки, пилюли, капсулы, пастилки и т.п. могут содержать любой из нижеследующих ингредиентов или соединений аналогичной природы, а именно: связующее вещество, такое как микрокристаллическая целлюлоза, трагакантовая камедь или желатин; носитель, такой как крахмал или лактоза; дезинтегрирующий агент, такой как альгиновая кислота, примогель или кукурузный крахмал; смазывающее вещество, такое как стеарат магния или стероты; вещество, увеличивающее скольжение, такое как коллоидный диоксид кремния; подслащивающий агент, такой как сахароза или сахарин; или отдушка, такая как перечная мята, метил-салицилат или апельсиновая отдушка. Если унифицированной лекарственной формой является капсула, то, помимо ингредиентов вышеуказанного типа, она может содержать жидкий носитель, такой как жирное масло. Кроме того, унифицированные лекарственные формы могут содержать различные другие вещества, которые модифицируют физическую форму разовой лекарственной формы, на пример, оболочку из сахара, шеллака или других энтеросолюбильных агентов. Активное соединение или его фармацевтически приемлемая соль могут быть введены в виде компонента элексира, суспензии, сиропа, облатки, жевательной резинки или т.п. Помимо активных соединений сироп может содержать сахарозу в качестве подслащивающего агента, а также он может содержать консерванты, красители и окрашивающие вещества, и отдушки. Активное соединение или его фармацевтически приемлемые соли могут быть введены вместе с другими активными соединениями, не обладающими нежелательным действием, или вместе с другими веществами, дополняющими желаемый эффект, такими как антибиотики, противогрибковые агенты,противовоспалительные агенты или противовирусные соединения. Активное соединение может быть введено вместе с другими соединениями, снижающими уровень липидов, такими как пробукол и никотиновая кислота; ингибиторами агрегации тромбоцитов, такими как аспирин; противотромботическими агентами, такими как кумадин; блокаторами кальциевых каналов, такими как варапамил, дилтиазем и нифедипин; ингибиторами ангиотензин-конвертирующего фермента (АСЕ), такими как каптоприл и эналоприл; и -блокаторами, такими как пропаналол, тербуталол и лабеталол. Эти соединения могут быть также введены в комбинации с нестероидными противовоспалительными агентами, такими как ибупрофен, индометацин, аспирин, фенопрофен, мефенаминовая кислота, флуфенаминовая кислота, сулиндак. Данное соединение может быть также введено в сочетании с кортикостероидами. Растворы или суспензии, используемые для парентерального, чрескожного, подкожного или местного введения, могут включать в себя следующие компоненты: стерильный разбавитель, такой как вода для инъекций, физиологический раствор, жирные масла, полиэтиленгликоли, глицерин, пропиленгликоль или другие синтетические растворители; антибактериальные агенты, такие как бензиловый спирт или метилпарабены; антиоксиданты, такие как аскорбиновая кислота или бисульфит натрия; хелатообразующие агенты, такие как этилендиаминотетрауксусная кислота; буферы, такие как ацетаты, цитраты или фосфаты; и агенты для коррекции тоничности раствора, такие как хлорид натрия или декстроза. Препарат для парентерального введения может быть включен в ампулы, одноразовые шприцы или в стеклянные или пластиковые флаконы для многократных доз. Подходящие наполнители или носители для местного применения хорошо известны, и ими являются лосьоны, суспензии, мази, кремы, гели, тинктуры, спреи, порошки, пасты, пластыри пролонгированного действия для чрескожного введения, аэрозоли для лечения астмы и суппозитории для ректального,вагинального, интраназального введения или для перорального введения через слизистую оболочку. При изготовлении композиций для местного применения могут быть использованы загустители,мягчители и стабилизаторы. В качестве примеров могут служить загустители, такие как вазилин, пчелиный воск, ксантановая камедь или полиэтиленгликоль; увлажнители, такие как сорбит; мягчители, такие как минеральное масло, ланолин и их производные, или сквален. Некоторые из этих растворов и мазей являются коммерчески доступными. Для улучшения вкуса препаратов для местного применения путем нанесения на поверхность слизистой оболочки могут быть добавлены натуральные или синтетические отдушки или подслащивающие агенты. В частности, в случае использования препаратов, предназначенных для нанесения на слизистую оболочку рта, в эти препараты могут быть добавлены инертные красители или подкрашивающие агенты. Активное соединение может быть приготовлено в виде смеси с носителями, защищающими это соединение от быстрого высвобождения, например в виде композиции с регулируемым высвобождением,включая имплантаты и системы доставки в форме микрокапсул. Могут быть использованы биологически разлагаемые и биологически совместимые полимеры, такие как этиленвинилацетат, полиангидриды, полигликолевая кислота, коллаген, сложные полиортоэфиры и полимолочная кислота. Многие методы получения таких композиций запатентованы или, в общих чертах, известны специалистам. Для внутривенного введения предпочтительными носителями являются физиологический раствор или забуференный фосфатом физиологический раствор (PBS). Активное соединение может быть также введено с помощью пластыря для чрескожного введения. Методы получения таких пластырей для чрескожного введения хорошо известны специалистам. См.,например, работу Brown, L., and Langer, R., Transdermal Delivery of Drugs, Annual Review of Medicine, 39: 221-229 (1988), которая включена в настоящее описание в качестве ссылки. В другом варианте осуществления изобретения активное соединение приготавливают в виде гото- 10010183 вой препаративной формы с использованием носителей, которые предохраняют данное соединение от быстрого выведения из организма, такой как готовая препаративная форма с регулируемым высвобождением, включая имплантаты и системы доставки в виде микрокапсул. Могут быть использованы биологически разлагаемые и биологически совместимые полимеры, такие как этиленвинилацетат, полиангидриды, полигликолевая кислота, коллаген, сложные полиортоэфиры и полимолочная кислота. Методы получения таких композиций известны специалистам. Указанные материалы могут быть также закуплены у фирм Alza Corporation и Nova Pharmaceuticals, Inc. В качестве фармацевтически приемлемых носителей также могут использоваться липосомные суспензии. Они могут быть получены методами, известными специалистам, например методами, описанными в патенте США 4522811 (который полностью включен в настоящее описание в качестве ссылки). Так, например, липосомные препараты могут быть получены путем растворения соответствующих липидов (таких как стеароилфосфатидилэтаноламин,стеароилфосфатидилхолин, арахадоилфосфатидилхолин и холестерин) в неорганическом растворителе,который затем выпаривают, в результате чего остается тонкая пленка осушенного липида на поверхности контейнера. После этого в этот контейнер вводят водный раствор активного соединения или его монофосфатных, дифосфатных и/или трифосфатных производных. Затем этот контейнер взбалтывают вручную для отделения липидного материала от стенок контейнера и для диспергирования липидных скоплений, в результате чего образуется липосомная суспензия. Исходя из вышеуказанного подробного описания изобретения, для каждого специалиста очевидно,что в него могут быть внесены различные модификации и изменения. Все эти варианты воплощения рассматриваются как включенные в объем данного изобретения. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ лечения заболевания, опосредованного VCAM-1, включающий введение млекопитающему, нуждающемуся в таком лечении, терапевтически эффективного количества сложного моноэфира янтарной кислоты и пробукола или его фармацевтически приемлемой соли. 2. Способ лечения сердечно-сосудистого заболевания, опосредованного VCAM-1, включающий введение млекопитающему, нуждающемуся в таком лечении, терапевтически эффективного количества сложного моноэфира янтарной кислоты и пробукола или его фармацевтически приемлемой соли. 3. Способ по п.2, в котором указанным заболеванием является атеросклероз. 4. Способ по п.2, в котором указанным заболеванием является рестеноз после ангиопластики. 5. Способ по п.2, в котором указанным заболеванием является заболевание, поражающее коронарную артерию. 6. Способ по п.2, в котором указанным заболеванием является стенокардия. 7. Способ по п.2, в котором указанным заболеванием является заболевание, поражающее капилляры. 8. Способ по любому из пп.1-7, который дополнительно включает использование второго агента для лечения сердечно-сосудистого заболевания. 9. Способ по п.8, в котором второй агент для лечения сердечно-сосудистого заболевания выбран из группы, состоящей из агентов, снижающих уровень липидов; ингибиторов агрегации тромбоцитов; противотромботических агентов, блокаторов кальциевых каналов; ингибиторов ангиотензин-конвертирующего фермента (АСЕ) и -блокаторов. 10. Способ лечения воспалительного заболевания, опосредованного VCAM-1, включающий введение млекопитающему, нуждающемуся в таком лечении, терапевтически эффективного количества сложного моноэфира янтарной кислоты и пробукола или его фармацевтически приемлемой соли. 11. Способ по п.10, в котором указанное заболевание представляет собой нарушение эндотелия человека. 12. Способ по п.10, в котором указанное заболевание представляет собой астму. 13. Способ по п.10, в котором указанное заболевание представляет собой псориаз. 14. Способ по п.10, в котором указанное заболевание представляет собой экзематозный дерматит. 15. Способ по п.10, в котором указанное заболевание представляет собой саркому Капоши. 16. Способ по п.10, в котором указанное заболевание представляет собой рассеянный склероз. 17. Способ по п.10, в котором указанное заболевание представляет собой пролиферативное нарушение клеток гладких мышц. 18. Способ по п.10, в котором указанное заболевание представляет собой ревматоидный артрит. 19. Способ по п.10, в котором указанное заболевание представляет собой остеоартрит. 20. Способ по любому из пп.10-19, который дополнительно включает введение второго противовоспалительного агента. 21. Способ по п.20, в котором второй противовоспалительный агент выбран из группы, включающей ибупрофен, индометацин, фенопрофен, мефенаминовую кислоту, флуфенаминовую кислоту, сулиндак и кортикостроиды. 22. Способ по любому из пп.1-21, в котором млекопитающее является человеком.- 11010183 23. Применение терапевтически эффективного количества сложного моноэфира янтарной кислоты и пробукола или его фармацевтически приемлемой соли для получения лекарственного средства для лечения заболевания, опосредованного VCAM-1. 24. Применение терапевтически эффективного количества сложного моноэфира янтарной кислоты и пробукола или его фармацевтически приемлемой соли для получения лекарственного средства для лечения сердечно-сосудистого заболевания, опосредованного VCAM-1. 25. Применение по п.24, в котором указанным заболеванием является атеросклероз. 26. Применение по п.24, в котором указанным заболеванием является рестеноз после ангиопластики. 27. Применение по п.24, в котором указанным заболеванием является заболевание, поражающее коронарную артерию. 28. Применение по п.24, в котором указанным заболеванием является стенокардия. 29. Применение по п.24, в котором указанным заболеванием является заболевание, поражающее капилляры. 30. Применение по любому из пп.23-29, в котором указанное лекарственное средство предназначено для использования в комбинации с вторым агентом для лечения сердечно-сосудистого заболевания. 31. Применение по любому из пп.23-29, в котором указанное лекарственное средство включает второй агент для лечения сердечно-сосудистого заболевания. 32. Применение по п.30 или 31, в котором второй агент для лечения сердечно-сосудистого заболевания выбран из группы, состоящей из агентов, снижающих уровень липидов; ингибиторов агрегации тромбоцитов; противотромботических агентов, блокаторов кальциевых каналов; ингибиторов ангиотензин-конвертирующего фермента (АСЕ) и -блокаторов. 33. Применение терапевтически эффективного количества моноэфира янтарной кислоты и пробукола или его фармацевтически приемлемой соли для получения лекарственного средства для лечения воспалительного заболевания, опосредованного VCAM-1. 34. Применение по п.33, в котором указанное заболевание представляет собой нарушение эндотелия человека. 35. Применение по п.33, в котором указанное заболевание представляет собой астму. 36. Применение по п.33, в котором указанное заболевание представляет собой псориаз. 37. Применение по п.33, в котором указанное заболевание представляет собой экзематозный дерматит. 38. Применение по п.33, в котором указанное заболевание представляет собой саркому Капоши. 39. Применение по п.33, в котором указанное заболевание представляет собой рассеянный склероз. 40. Применение по п.33, в котором указанное заболевание представляет собой пролиферативное нарушение клеток гладких мышц. 41. Применение по п.33, в котором указанное заболевание представляет собой ревматоидный артрит. 42. Применение по п.33, в котором указанное заболевание представляет собой остеоартрит. 43. Применение по любому из пп.33-42, в котором указанное лекарственное средство предназначено для использования в комбинации с вторым противовоспалительным агентом. 44. Применение по любому из пп.33-42, в котором указанное лекарственное средство включает второй противовоспалительный агент. 45. Применение по п.43 или 44, в котором второй противовоспалительный агент выбран из группы,включающей ибупрофен, индометацин, фенопрофен, мефенаминовую кислоту, флуфенаминовую кислоту, сулиндак и кортикостроиды. 46. Применение по любому из пп.23-45, в котором указанное лекарственное средство подходит для перорального, местного, внутривенного, подкожного, парентерального, внутрикожного и чрезкожного введения. 47. Применение по любому из пп.23-46, в котором лекарственное средство предназначено для человека.
МПК / Метки
МПК: C07C 323/20, A61P 9/10, A61P 29/00, A61P 9/00, A61K 31/225
Метки: моноэфир, сложный, сердечно-сосудистых, воспалительных, заболеваний, янтарной, кислоты, лечения, пробукола
Код ссылки
<a href="https://eas.patents.su/17-10183-slozhnyjj-monoefir-yantarnojj-kisloty-i-probukola-dlya-lecheniya-serdechno-sosudistyh-i-vospalitelnyh-zabolevanijj.html" rel="bookmark" title="База патентов Евразийского Союза">Сложный моноэфир янтарной кислоты и пробукола для лечения сердечно-сосудистых и воспалительных заболеваний</a>