Производные замещённого 8-перфторалкил-6, 7, 8, 9-тетрагидропиримидо[1,2-а]пиримидин-4-она
Номер патента: 9198
Опубликовано: 28.12.2007
Авторы: Саади Мурад, Локхид Алистер, Йеш Филипп, Словински Франк
Формула / Реферат
1. Производное замещенного пиримидона, представленное формулой (I)
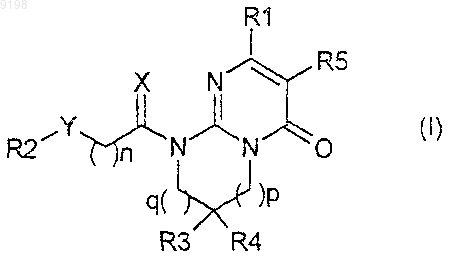
или его соль, или его сольват, или его гидрат,
где X представляет собой два атома водорода, атом серы, атом кислорода или С1-2алкильную группу и атом водорода;
Y представляет собой связь, карбонильную группу, метиленовую группу, возможно замещенную одной или двумя группами, выбранными из C1-6алкильной группы, гидроксильной группы, С1-4алкоксигруппы, С1-2пергалогенированной алкильной группы или аминогруппы;
R1 представляет собой 2-, 3- или 4-пиридиновое кольцо либо 2-, 4- или 5-пиримидиновое кольцо, причем эти кольца возможно замещены С1-4алкильной группой, С1-4алкоксигруппой или атомом галогена;
R2 представляет собой фенильную группу или нафталиновое кольцо, причем фенильная группа и нафталиновое кольцо возможно замещены 1-4 заместителями, выбранными из С1-6алкильной группы, фенильной группы, метилендиоксигруппы, атома галогена, С1-2пергалогенированной алкильной группы, C1-3галогенированной алкильной группы, гидроксильной группы, С1-4алкоксигруппы, нитро, циано, амино, С1-5моноалкиламиногруппы или С2-10диалкиламиногруппы;
R3 представляет собой атом водорода или С1-6алкильную группу;
R4 представляет собой С1-2пергалогенированную алкильную группу или C1-3галогенированную алкильную группу;
R5 представляет собой водород, С1-6алкильную группу или атом галогена;
n представляет собой число от 0 до 3; и
р+q=от 0 до 3.
2. Производное замещенного пиримидона, или его соль, или его сольват, или его гидрат по п.1, где R4 представляет собой С1-2пергалогенированную алкильную группу.
3. Производное замещенного пиримидона, или его соль, или его сольват, или его гидрат по п.1 или 2,
где R1 представляет собой незамещенное 4-пиридиновое кольцо или 4-пиримидиновое кольцо;
R2 представляет собой фенильную группу, возможно замещенную 1-4 заместителями, выбранными из C1-3алкильной группы, фенильной группы, атома галогена, гидроксильной группы, циано или С1-2 алкоксигруппы, либо альтернативно R2 представляет собой фенильную группу, возможно замещенную 1-4 заместителями, выбранными из С1-3алкильной группы, атома галогена, гидроксильной группы или
С1-2алкоксигруппы;
R3 представляет собой атом водорода;
R4 представляет собой трифторметильную группу;
R5 представляет собой атом водорода или фтора либо альтернативно R5 представляет собой атом водорода;
X представляет собой два атома водорода;
Y представляет собой карбонильную группу или метиленовую группу, возможно замещенную гидроксильной группой;
n, р и q равны 0, 2 и 0 соответственно.
4. Производное замещенного пиримидона, выбранное из группы, состоящей из
9-(2-оксо-2-фенилэтил)-2-(4-пиридинил)-8-(трифторметил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2-а]пиримидин-4-она,
9-[(2S)-2-гидрокси-2-фенилэтил]-2-(4-пиридинил)-8-(трифторметил)-6,7,8,9-тетрагидро-4Н-пиримидо[1,2-а]пиримидин-4-она,
9-[2-(3-бромфенил)-2-оксоэтил]-2-(4-пиридинил)-8-(трифторметил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2-а]пиримидин-4-она,
9-[2-(3-бромфенил)-2-гидроксиэтил]-2-(4-пиридинил)-8-(трифторметил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2-а]пиримидин-4-она,
9-[2-оксо-2-фенилэтил]-2-(4-пиримидинил)-8-(трифторметил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2-а]пиримидин-4-она,
(-)-9-(2-оксо-2-фенилэтил)-2-(4-пиридинил)-8-(трифторметил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2-а]пиримидин-4-она,
(+)-9-(2-оксо-2-фенилэтил)-2-(4-пиридинил)-8-(трифторметил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2-а]пиримидин-4-она,
(+)-9-[2-оксо-2-фенилэтил]-2-(4-пиримидинил)-8-(трифторметил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2-а]пиримидин-4-она,
(-)-9-[2-оксо-2-фенилэтил]-2-(4-пиримидинил)-8-(трифторметил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2-а]пиримидин-4-она,
3-фтор-9-(2-оксо-2-фенилэтил)-2-пиридин-4-ил-8-(трифторметил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2-а]пиримидин-4-она,
9-(фенилметил)-2-пиримидин-4-ил-8-(трифторметил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2-а]пиримидин-4-она,
9-(2-фенилэтил)-2-пиримидин-4-ил-8-(трифторметил)-6,7,8,9-тетрагидро-4Н-пиримидо[1,2-а]пиримидин-4-она,
9-[2-(3-бромфенил)-2-оксоэтил]-2-пиримидин-4-ил-8-(трифторметил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2-а]пиримидин-4-она,
9-[2-(3-фторфенил)-2-оксоэтил]-2-пиримидин-4-ил-8-(трифторметил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2-а]пиримидин-4-она,
9-[2-(4-метилфенил)-2-оксоэтил]-2-пиримидин-4-ил-8-(трифторметил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2-а]пиримидин-4-она,
9-[2-(4-фторфенил)-2-оксоэтил]-2-пиримидин-4-ил-8-(трифторметил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2-а]пиримидин-4-она,
9-[2-(4-цианофенил)-2-оксоэтил]-2-пиримидин-4-ил-8-(трифторметил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2-а]пиримидин-4-она,
9-(2-бифенил-4-ил-2-оксоэтил)-2-пиримидин-4-ил-8-(трифторметил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2-а]пиримидин-4-она,
или его соль, или его сольват, или его гидрат.
5. Соединение формулы (III)
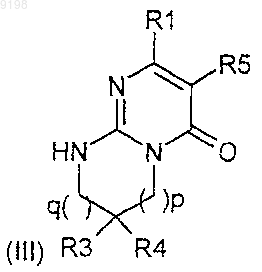
где R1, R3, R4, R5, р и q такие, как определено для соединения формулы (I) по п.1.
6. Лекарство, содержащее в качестве активного ингредиента вещество, выбранное из группы, состоящей из производного замещенного пиримидона, представленного формулой (I), или его соли, или его сольвата, или его гидрата по п.1.
7. Ингибитор GSK3b (киназы-3b гликогенсинтазы), выбранный из группы, состоящей из производного замещенного пиримидона, представленного формулой (I), или его соли, или его сольвата, или его гидрата по п.1.
8. Применение соединения по любому из пп.1-4 для изготовления лекарства для профилактического и/или терапевтического лечения заболевания, вызванного аномальной активностью GSK3b.
9. Применение соединения по любому из пп.1-4 для изготовления лекарства для профилактического и/или терапевтического лечения нейродегенеративного заболевания.
10. Применение соединения по п.9, где нейродегенеративное заболевание выбрано из группы, состоящей из болезни Альцгеймера, болезни Паркинсона, тауопатий, сосудистой деменции; острого инсульта, травматических повреждений; церебрально-васкулярных повреждений, травмы головного мозга, травмы спинного мозга; периферических невропатий; ретинопатий или глаукомы.
11. Применение соединения по любому из пп.1-4 для изготовления лекарства для профилактического и/или терапевтического лечения инсулиннезависимого диабета, ожирения, маниакально-депрессивного заболевания, шизофрении, алопеции или рака.
12. Применение по п.11, где рак представляет собой рак молочной железы, немелкоклеточный рак легкого, рак щитовидной железы, Т- или В-клеточную лейкемию или опухоли, вызванные вирусами.
Текст
009198 Область изобретения Настоящее изобретение относится к соединениям, которые полезны в качестве активного ингредиента лекарства для профилактического и/или терапевтического лечения нейродегенеративных заболеваний, вызванных аномальной активностью GSK3. Предшествующий уровень техникиGSK3 (киназа-3 гликогенсинтазы) представляет собой регулируемую пролином серин-, треонинкиназу, которая играет важную роль в регуляции метаболизма, дифференциации и выживания. Первоначально она была идентифицирована как фермент, способный фосфорилировать и, следовательно, ингибировать гликогенсинтазу. Позднее было признано, что GSK3 идентична тау-протеинкиназе 1 (ТРК 1),ферменту, который фосфорилирует тау-протеин в эпитопах, которые, как также было обнаружено, гиперфосфорилированы при болезни Альцгеймера и при некоторых таупатиях. Интересно, что фосфорилирование GSK3 протеинкиназой В (АКТ) приводит к потере ее киназной активности, и предполагалось,что такое ингибирование может опосредовать некоторые воздействия нейротрофических факторов. Кроме того, фосфорилирование посредством GSK3 -катенина, белка, вовлеченного в выживание клетки,приводит к его деградации зависимым от убиквитинилирования протеасомным путем. Таким образом, очевидно, что следствием ингибирования активности GSK3 может являться нейротрофическая активность. Действительно, существует доказательство, что литий, неконкурентный ингибитор GSK3, усиливает нейритогенез в некоторых моделях, а также увеличивает выживание нейронов посредством индукции факторов выживания, таких как Bcl-2, и ингибирования экспрессии проапоптотических факторов, таких как Р 53 и Вах. Недавние исследования показали, что -амилоид увеличивает активность GSK3 и фосфорилирование тау-протеина. Кроме того, такое гиперфосфорилирование, также как нейротоксичные воздействия-амилоида блокируются хлоридом лития и антисмысловой мРНК GSK3. Эти наблюдения уверенно свидетельствуют, что GSK3 может являться связующим звеном между двумя основными патологическими процессами при болезни Альцгеймера: аномальным процессингом АРР (белка-предшественника амилоида) и гиперфосфорилированием тау-протеина. Хотя тау-гиперфосфорилирование приводит к дестабилизации нейронального цитоскелета, патологические последствия аномальной активности GSK3, наиболее вероятно, являются не только следствием патологического фосфорилирования тау-протеина, поскольку, как упоминалось выше, избыточная активность данной киназы может негативно влиять на выживание посредством модуляции экспрессии апоптотических и антиапоптотических факторов. Кроме того, было показано, что индуцированное амилоидом увеличение активности GSK3 приводит к фосфорилированию и, следовательно, ингибированию пируватдегидрогеназы, основного фермента в производстве энергии и синтезе ацетилхолина. В совокупности эти экспериментальные наблюдения указывают на то, что GSK3 может найти применение в лечении нейропатологических последствий и дефицитах когнитивных функции и внимания, связанных с болезнью Альцгеймера, а также других острых и хронических нейродегенеративных заболеваний. Последние включают в себя, без ограничения, болезнь Паркинсона, тауопатии (например лобно-височно-теменную деменцию, кортикобазальную дегенерацию, болезнь Пика, прогрессирующий супрануклеарный паралич) и другие деменции, включая сосудистую деменцию; острый инсульт и другие травматические повреждения; церебрально-васкулярные повреждения (например возрастную дегенерацию желтого пятна); травму головного и спинного мозга; периферические нейропатии; ретинопатии и глаукому. Кроме того, GSK3 может найти применение в лечении других заболеваний, таких как инсулиннезависимый диабет (такой как диабет типа II) и ожирение; маниакально-депрессивное заболевание; шизофрения; алопеция; рак, такой как рак молочной железы, немелкоклеточная карцинома легкого, рак щитовидной железы, Т- или В-клеточная лейкемия и некоторые опухоли, вызванные вирусами. Наиболее близкий аналог данного изобретения раскрыт в WO 02/18386, где описано лечение нейродегенеративного заболевания, вызванного аномальной активностью GSK3, такого как болезнь Альцгеймера, с помощью производных тетрагидропиримидо[1,2 а]пиримидин-4-она. В отличие от соединений по данному изобретению, в которых заместитель тетрагидропиримидо-кольца R4 представляет собой С 1-2 пергалогенированную группу или C1-3 галогенированную группу, в соединениях, известных из уровня техники, данный заместитель отсутствует. Описание изобретения Задачей настоящего изобретения является предложение соединений, полезных в качестве активного ингредиента лекарства для профилактического и/или терапевтического лечения заболевания, вызванного аномальной активностью GSK3, более конкретно нейродегенеративных заболеваний. Более конкретно,задачей настоящего изобретения является предложение новых соединений, полезных в качестве активного ингредиента лекарства, которое обеспечивает возможность предупреждения и/или лечения нейродегенеративных заболеваний, таких как болезнь Альцгеймера. Таким образом, авторы настоящего изобретения идентифицировали соединения, обладающие инги-1 009198 биторной активностью в отношении GSK3. В результате они обнаружили, что соединения, представленные следующей ниже формулой (I), обладали нужной активностью и были полезны в качестве активного ингредиента лекарства для профилактического и/или терапевтического лечения вышеуказанных заболеваний. В настоящем изобретении, таким образом, предложены производные замещенного пиримидона,представленные формулой (I), или их соли, их сольваты, или их гидраты где X представляет собой два атома водорода, атом серы, атом кислорода или С 1-2 алкильную группу и атом водорода;Y представляет собой связь, карбонильную группу, метиленовую группу, возможно замещенную одной или двумя группами, выбранными из С 1-6 алкильной группы, гидроксильной группы, С 1-4 алкоксигруппы, С 1-2 пергалогенированной алкильной группы или аминогруппы;R1 представляет собой 2, 3 или 4-пиридиновое кольцо либо 2, 4 или 5-пиримидиновое кольцо, причем эти кольца возможно замещены С 1-4 алкильной группой, С 1-4 алкоксигруппой или атомом галогена;R2 представляет собой фенильную группу или нафталиновое кольцо, причем фенильная группа и нафталиновое кольцо возможно замещены заместителями в количестве от 1 до 4, выбранными из С 1-6 алкильной группы, фенильной группы, метилендиоксигруппы, атома галогена, С 1-2 пергалогенированной алкильной группы, С 1-3 галогенированной алкильной группы, гидроксильной группы, С 1-4 алкоксигруппы,нитро, циано, амино, С 1-5 моноалкиламиногруппы или С 2-10 диалкиламиногруппы;R3 представляет собой атом водорода или C1-6 алкильную группу;R4 представляет собой С 1-2 пергалогенированную алкильную группу или C1-3 галогенированную алкильную группу;R5 представляет собой водород, C1-6 алкильную группу или атом галогена;n равно от 0 до 3; и р + q равно от 0 до 3. В соответствии с другим аспектом настоящего изобретения предложено лекарство, содержащее в качестве активного ингредиента вещество, выбранное из группы, состоящей из производных пиримидона, представленных формулой (I), и их физиологически приемлемых солей, и их сольватов, и их гидратов. В качестве предпочтительных воплощений лекарств предложено вышеуказанное лекарство, которое используется для профилактического и/или терапевтического лечения заболеваний, вызванных аномальной активностью GSK3, и вышеуказанное лекарство, которое используется для профилактического и/или терапевтического лечения нейродегенеративных заболеваний и кроме того других заболеваний,таких как инсулиннезависимый диабет (такой как диабет типа II) и ожирение; маниакально-депрессивное заболевание; шизофрения; алопеция; рак, такой как рак молочной железы, немелкоклеточный рак легкого, рак щитовидной железы, Т- или В-клеточная лейкемия и некоторые опухоли, вызванные вирусами. В качестве дополнительных предпочтительных воплощений настоящего изобретения предложено вышеуказанное лекарство, причем заболевания представляют собой нейродегенеративные заболевания и выбраны из группы, состоящей из болезни Альцгеймера, болезни Паркинсона, тауопатий (например лобно-височно-теменного слабоумия, кортикобазальной дегенерации, болезни Пика, прогрессирующего супрануклеарного паралича) и других деменций, включая сосудистую деменцию; острого инсульта и других травматических повреждений; церебрально-васкулярных повреждений (например возрастной дегенерации желтого пятна); травмы головного и спинного мозга; периферических невропатий; ретинопатий и глаукомы; и вышеуказанное лекарство находится в форме фармацевтической композиции, содержащей в качестве активного ингредиента вышеуказанное вещество вместе с одной или более фармацевтическими вспомогательными веществами. В настоящем изобретении дополнительно предложен ингибитор GSK3-активности, содержащий в качестве активного ингредиента вещество, выбранное из группы, состоящей из производных замещенного пиримидона формулы (I) и их солей, и их сольватов, и их гидратов. В соответствии с дополнительными аспектами настоящего изобретения предложен способ профилактического и/или терапевтического лечения нейродегенеративных заболеваний, вызванных аномальной активностью GSK3, включающий стадию введения пациенту профилактически и/или терапевтически эффективного количества вещества, выбранного из группы, состоящей из производных замещенного пиримидона формулы (I), и их физиологически приемлемых солей, и их сольватов, и их гидратов; и применение вещества, выбранного из группы, состоящей из производных замещенного пиримидона формулы (I), и их физиологически приемлемых солей, и их сольватов, и их гидратов для изготовления вышеуказанного лекарства.-2 009198 При использовании здесь, С 1-6 алкильная группа представляет собой прямую или разветвленную алкильную группу, имеющую от 1 до 6 атомов углерода, например метильную группу, этильную группу, нпропильную группу, изопропильную группу, н-бутильную группу, изобутильную группу, вторбутильную группу, трет-бутильную группу, н-пентильную группу, изопентильную группу, неопентильную группу, 1,1-диметилпропильную группу, н-гексильную группу, изогексильную группу и подобное. С 1-4 алкоксигруппа представляет собой алкилоксигруппу, имеющую от 1 до 4 атомов углерода, например метоксигруппу, этоксигруппу, пропоксигруппу, изопропоксигруппу, бутоксигруппу, изобутоксигруппу, втор-бутоксигруппу, трет-бутоксигруппу и подобное. Атом галогена представляет собой атом фтора, хлора, брома или иода. С 1-2 пергалогенированная алкильная группа представляет собой алкильную группу, в которой все водороды замещены атомами галогена, например CF3 или C2F5;C1-3 галогенированная алкильная группа представляет собой алкильную группу, в которой по меньшей мере один водород не замещен атомом галогена. С 1-5 моноалкиламиногруппа представляет собой аминогруппу, замещенную одной C1-6 алкильной группой, например метиламиногруппу, этиламиногруппу, пропиламиногруппу, изопропиламиногруппу,бутиламиногруппу, изобутиламиногруппу, трет-бутиламиногруппу, пентиламиногруппу и изопентиламиногруппу. С 2-10 диалкиламиногруппа представляет собой аминогруппу, замещенную двумя С 1-5 алкильными группами, например диметиламиногруппу, этилметиламиногруппу, диэтиламиногруппу, метилпропиламиногруппу и диизопропиламиногруппу. Уходящая группа L представляет собой группу, которая может быть легко отщеплена и замещена,такая группа может представлять собой, например, тозил, мезил, бромид и подобное. Р + q = от 0 до 3 указывает на то, что при сложении р и q получается 0, 1, 2 или 3. Соединения, представленные вышеуказанной формулой (I), могут образовывать соль. Примеры соли включают, при наличии кислотной группы, соли щелочных и щелочно-земельных металлов, таких как литий, натрий, калий, магний и кальций; соли аммония и аминов, таких как метиламин, диметиламин,триметиламин, дициклогексиламин, трис(гидроксиметил)аминометан, N,N-бис(гидроксиэтил)пиперазин,2-амино-2-метил-1-пропанол, этаноламин, N-метилглюкамин и L-глюкамин; или соли с основными аминокислотами, тикими как лизин, -гидроксилизин и аргинин. Соли присоединения оснований к кислым соединениям получают стандартными способами, хорошо известными в данной области. При наличии основной группы, примеры включают соли с минеральными кислотами, такими как соляная кислота, бромисто-водородная кислота, серная кислота, азотная кислота, фосфорная кислота,соли с органическими кислотами, такими как метансульфоновая кислота, бензолсульфоновая кислота,паратолуолсульфоновая кислота, уксусная кислота, пропионовая кислота, винная кислота, фумаровая кислота, малеиновая кислота, яблочная кислота, щавелевая кислота, янтарная кислота, лимонная кислота,бензойная кислота, миндальная кислота, коричная кислота, молочная кислота, гликолевая кислота, глюкуроновая кислота, аскорбиновая кислота, никотиновая кислота и салициловая кислота; либо соли с кислыми аминокислотами, такими как аспарагиновая кислота и глутаминовая кислота. Соли присоединения кислоты к основным соединениям получают стандартными способами, хорошо известными в данной области, которые включают, но не ограничены ими, растворение свободного основания в водном спиртовом растворе, содержащем соответствующую кислоту, и выделение соли путем упаривания раствора либо путем взаимодействия свободного основания и кислоты в органическом растворителе, причем в этом случае соль выделяется непосредственно, либо ее осаждают вторым органическим растворителем, либо она может быть получена посредством концентрирования раствора. Кислоты, которые можно использовать для получения солей присоединения кислоты, предпочтительно включают те, которые при объединении со свободным основанием образуют фармацевтически приемлемые соли, то есть соли, анионы которых относительно безвредны для животного организма в фармацевтических дозах этих солей, так что полезные свойства, присущие свободному основанию, не ухудшаются побочными эффектами, приписываемыми анионам. Хотя предпочтительными являются приемлемые с медицинской точки зрения соли основных соединений, все соли присоединения кислоты входят в объем настоящего изобретения. В дополнение к производным замещенного пиримидона, представленным вышеуказанной формулой (I), и их солям, их сольваты и гидраты также входят в объем настоящего изобретения. Производные замещенного пиримидона, представленные вышеуказанной формулой (I), могут иметь один или более асимметрический атом углерода. Что касается стереохимии таких асимметрических атомов углерода, они могут независимо находиться либо в (R)-, либо в (S)-конфигурации, и производное может существовать в виде стереоизомеров, таких как оптические изомеры или диастереоизомеры. Любые стереоизомеры в чистой форме, любые смеси стереоизомеров, рацематы и подобное входят в объем настоящего изобретения. Примеры соединений по настоящему изобретению представлены ниже в таблице. Однако, объем настоящего изобретения не ограничен этими соединениями. Одно из воплощений настоящего изобретения включает также соединения, представленные форму-3 009198 лой (I), где R1, R3, R4, R5, X, Y, n, p и q такие, как определено выше, и R2 представляет собой фенильную группу или нафталиновое кольцо, причем фенильная группа и нафталиновое кольцо возможно замещены 1-4 заместителями, выбранными из С 1-6 алкильной группы, метилендиоксигруппы, атома галогена, С 1-2 пергалогенированной алкильной группы, C1-3 галогенированной алкильной группы, гидроксильной группы, С 1-4 алкоксигруппы, нитро, циано, амино, С 1-5 моноалкиламиногруппы или С 2-10 диалкиламиногруппы. Еще одно воплощение настоящего изобретения включает соединения, представленные формулой(I), где R1, R2, R3, R5, X, Y, n, p и q такие, как определено выше, и R4 представляет собой С 1-2 пергалогенированную алкильную группу. Еще одно воплощение настоящего изобретения включает соединения, представленные формулойR1 представляет собой 3- или 4-пиридиновое кольцо, и более предпочтительно 4-пиридиновое кольцо или 4- или 5-пиримидиновое кольцо, и более предпочтительно 4-пиримидиновое кольцо, которое может быть замещено С 1-2 алкильной группой, С 1-2 алкоксигруппой или атомом галогена;R2 представляет собой фенильную группу или нафталиновое кольцо, причем фенильная группа и нафталиновое кольцо возможно замещены 1-4 заместителями, выбранными из C1-3 алкильной группы,фенильной группы, атома галогена, циано, гидроксильной группы или С 1-2 алкоксигруппы, либо альтернативно R2 представляет собой фенильную группу или нафталиновое кольцо, причем фенильная группа и нафталиновое кольцо возможно замещены 1-4 заместителями, выбранными из C1-3 алкильной группы,атома галогена, гидроксильной группы или С 1-2 алкоксигруппы;R3 представляет собой атом водорода;R4 представляет собой С 1-2 пергалогенированную алкильную группу и более предпочтительно перфторалкильную группу;R5 представляет собой атом водорода или атом галогена, либо альтернативно R5 представляет собой атом водорода;X представляет собой два атома водорода;Y представляет собой связь, карбонильную группу или метиленовую группу, возможно замещенную одной или двумя группами, выбранными из C1-3 алкильной группы, гидроксильной группы, С 1-4 алкоксигруппы, С 1-2 пергалогенированной алкильной группы, аминогруппы, или альтернативно Y представляет собой карбонильную группу или метиленовую группу, возможно замещенную одной или двумя группами, выбранными из C1-3 алкильной группы, гидроксильной группы, С 1-4 алкоксигруппы, С 1-2 пергалогенированной алкильной группы, аминогруппы;n, р и q равны 0, 2 и 0 соответственно. Еще одно воплощение настоящего изобретения включает соединения, представленные формулой(I), где R1, R2, R3, R4, R5, X, Y, n, p и q такие, как определено здесь ниже:R1 представляет собой незамещенное 4-пиридиновое кольцо или 4-пиримидиновое кольцо;R2 представляет собой фенильную группу, возможно замещенную 1-4 заместителями, выбранными из С 1-3 алкильной группы, фенильной группы, атома галогена, гидроксильной группы, циано или С 1-2 алкоксигруппы, либо альтернативно R2 представляет собой фенильную группу, возможно замещенную 1-4 заместителями, выбранными из C1-3 алкильной группы, атома галогена, гидроксильной группы или С 1-2 алкоксигруппы;R3 представляет собой атом водорода;R4 представляет собой трифторметильную группу;R5 представляет собой атом водорода или фтора либо альтернативно R5 представляет собой атом водорода;X представляет собой два атома водорода;Y представляет собой карбонильную группу или метиленовую группу, возможно замещенную гидроксильной группой;n, р и q равны 0, 2 и 0 соответственно. Конкретные соединения по настоящему изобретению, представленные формулой (I), где R4 представляет собой трифторметильную группу, включают соединения: 1) 9-(2-оксо-2-фенилэтил)-2-(4-пиридинил)-8-(трифторметил)-6,7,8,9-тетрагидро-4 Н-пиримидо [1,2 а]пиримидин-4-он; 2) 9-[(2S)-2-гидрокси-2-фенилэтил]-2-(4-пиридинил)-8-(трифторметил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2-а]пиримидин-4-он; 3) 9-[2-(3-бромфенил)-2-оксоэтил]-2-(4-пиридинил)-8-(трифторметил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2-а]пиримидин-4-он; 4) 9-[2-(3-бромфенил)-2-гидроксиэтил]-2-(4-пиридинил)-8-(трифторметил)-6,7,8,9-тетрагидро-4Hпиримидо[1,2-а]пиримидин-4-он; 5) 9-[2-оксо-2-фенилэтил]-2-(4-пиримидинил)-8-(трифторметил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2-а]пиримидин-4-он; 8) (+)-9-[2-оксо-2-фенилэтил]-2-(4-пиримидинил)-8-(трифторметил)-6,7,8,9-тетрагидро-4 Н-пиримидо[1,2-а]пиримидин-4-он; 9) (-)-9-[2-оксо-2-фенилэтил]-2-(4-пиримидинил)-8-(трифторметил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2-а]пиримидин-4-он; 10) 3-фтор-9-(2-оксо-2-фенилэтил)-2-пиридин-4-ил-8-(трифторметил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2-а]пиримидин-4-он; 11) 9-(фенилметил)-2-пиримидин-4-ил-8-(трифторметил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2-а] пиримидин-4-он; 12) 9-(2-фенилэтил)-2-пиримидин-4-ил-8-(трифторметил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2-а] пиримидин-4-он; 13) 9-[2-(3-бромфенил)-2-оксоэтил]-2-пиримидин-4-ил-8-(трифторметил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2-а]пиримидин-4-он; 14) 9-[2-(3-фторфенил)-2-оксоэтил]-2-пиримидин-4-ил-8-(трифторметил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2-а]пиримидин-4-он; 15) 9-[2-(4-метилфенил)-2-оксоэтил]-2-пиримидин-4-ил-8-(трифторметил)-6,7,8,9-тетрагидро-4 Нпиримидо[1,2-а]пиримидин-4-он; 16) 9-[2-(4-фторфенил)-2-оксоэтил]-2-пиримидин-4-ил-8-(трифторметил)-6,7,8,9-тетрагидро-4 Н-пиримидо[1,2-а]пиримидин-4-он; 17) 9-[2-(4-цианофенил)-2-оксоэтил]-2-пиримидин-4-ил-8-(трифторметил)-6,7,8,9-тетрагидро-4Hпиримидо[1,2-а]пиримидин-4-он; 18) 9-(2-бифенил-4-ил-2-оксоэтил)-2-пиримидин-4-ил-8-(трифторметил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2-а]пиримидин-4-он. В качестве дополнительного объекта настоящее изобретение касается также способов получения замещенных пиримидоновых соединений, представленных вышеуказанной формулой (I). Эти соединения могут быть получены, например, в соответствии со способами, раскрытыми ниже. Способ получения Замещенные пиримидоновые соединения, представленные вышеуказанной формулой (I), могут быть получены в соответствии со способом, показанным на схеме 1. Схема 1 Согласно этому способу для получения соединения указанной выше формулы (I) обеспечивают взаимодействие пиримидинонового производного, представленного указанной выше формулой (III), гдеR1, R3, R4, R5, p и q такие, как определено для соединения формулы (I), с основанием, таким как гидрид натрия, карбонат натрия или карбонат калия, в растворителе, таком как N,N-диметилформамид, Nметилпирролидон, N,N-диметилацетамид или хлороформ, при подходящей температуре в интервале от 0 до 130 С, в атмосфере обычного воздуха, а затем с соединением формулы (II), где R2, X, Y и n такие, как определено для соединения формулы (I), и L представляет собой уходящую группу, предпочтительно бромидную или мезильную группу. Альтернативно, соединения формулы (I), где Y представляет собой карбонильную группу, могут быть получены путем окисления соединения формулы (I), где Y представляет собой метиленовую группу, замещенную гидроксильной группой, способами, хорошо известными специалисту в данной области. Соединение формулы (II) имеется в продаже или может быть синтезировано способами, хорошо известными специалисту в данной области. Соединение формулы (III) может быть получено в соответствии со способом, показанным на схеме 2.-5 009198 Согласно этому способу обеспечивают взаимодействие 3-кетоэфира формулы (IV), где R1 и R5 такие, как определено для соединения формулы (I), и R представляет собой алкильную группу, такую как,например метил или этил, с соединением формулы (V), где R3, R4, p и q такие, как определено для соединения формулы (I). Это взаимодействие можно осуществлять в присутствии основания, такого как карбонат калия, в спиртовом растворителе, таком как метанол, этанол и подобное, либо без него, при подходящей температуре в интервале от 25 до 140 С в атмосфере обычного воздуха. Альтернативно, соединение формулы (III), где R5 представляет собой атом водорода, можно галогенировать для получения соединений формулы (III), где R5 представляет собой атом галогена, такой как атом брома или атом хлора. Реакцию можно осуществлять в кислой среде, такой как уксусная кислота или пропионовая кислота, в присутствии бромсукцинимида, или хлорсукцинимида, или брома. Кроме того, соединения формулы (III), где R5 представляет собой атом фтора, могут быть получены по аналогии со способом, описанным в Tetrahedron Letters, Vol. 30, 45, рр 6113-6116, 1989. Соединение формулы (IV) имеется в продаже или может быть синтезировано способами, хорошо известными специалисту в данной области. Например, соединения формулы (IV), где R1 представляет собой пиридиновое кольцо или пиримидиновое кольцо, возможно замещенное С 1-4 алкильной группой, С 1-4 алкоксигруппой или атомом галогена,могут быть получены путем взаимодействия, соответственно, изоникотиновой кислоты или пиримидинкарбоновой кислоты, возможно замещенной С 1-4 алкильной группой, С 1-4 алкоксигруппой или галогеном,с соответствующим моноэфиром малоновой кислоты. Реакцию можно проводить, используя способы,хорошо известные специалисту в данной области, например, в присутствии агента сочетания, такого как 1,1'-карбонилбис-1H-имидазол, в растворителе, таком как тетрагидрофуран, при температуре в интервале от 20 до 70 С. В вышеуказанных реакциях иногда может требоваться защита или удаление защиты функциональных групп. Подходящая защитная группа Pg может быть выбрана в зависимости от типа функциональной группы и может быть использован способ, описанный в литературе. Примеры защитных групп, способы защиты и удаления защиты приведены, например, в Protective groups in Organic Synthesis. Greene etal., 2nd Ed. (John WileySons, Inc., New York). Соединение формулы (V) имеется в продаже или может быть синтезировано способами, хорошо известными специалисту в данной области. Альтернативно, соединение формулы (V), где p равно 2, a q равно 0, можно получить в соответствии со способом, показанным на схеме 3.(На приведенной выше схеме Pg представляет собой защитную группу аминогруппы, a L представляет собой уходящую группу, предпочтительно бромидную группу или мезильную группу). Согласно этому способу соединение формулы (VI), где R4 такой, как определен для соединения формулы (I), может быть получено различными путями, в зависимости от R3. 3-Аминокислота формулы (VI), где R3 представляет собой атом водорода, может быть синтезирована по аналогии со способом, описанным в Tetrahedron Letters, Vol. 43, 11, рр 1977-1981, 2002. 3-Аминокислота формулы (VI), где R3 представляет собой С 1-6 алкильную группу, может быть синтезирована по аналогии со способом, описанным в Journal of Organic Chemistry, Vol. 56, 1, pp 4-6, 1991. В обоих случаях необходима защитная группа аминогруппы. Примеры способов защиты и удаления защиты приведены, например, в Protective groups in Organic Synthesis Greene et al., 2nd Ed. (John WileySons, Inc., New York). По аналогии с этими способами соединения формул (VII) и (VIII) могут быть получены путем защиты аминогруппы, а соединение формулы (IX) может быть получено путем удаления защиты. Затем, соединение формулы (V) может быть получено путем циклизации, способами, хорошо из-6 009198 вестными специалисту в данной области. Альтернативно, если R3 представляет собой H, соединение формулы (V) может быть получено путем гидрирования соединения формулы (X) способами, хорошо известными специалисту в данной области. Соединение формулы (X) имеется в продаже, либо может быть синтезировано способами, хорошо известными специалисту в данной области. В качестве дополнительного объекта настоящее изобретение касается также соединения формулы(III) в качестве промежуточного соединения для получения соединений формулы (I). Соединения по настоящему изобретению обладают ингибиторной активностью в отношенииGSK3. Соответственно, соединения по настоящему изобретению полезны в качестве активного ингредиента для изготовления лекарства, которое обеспечивает возможность профилактического и/или терапевтического лечения заболевания, вызванного аномальной активностью GSK3, и более конкретно нейродегенеративных заболеваний, таких как болезнь Альцгеймера. Кроме того, соединения по настоящему изобретению также полезны в качестве активного ингредиента для изготовления лекарства для профилактического и/или терапевтического лечения нейродегенеративных заболеваний, таких как болезнь Паркинсона, тауопатии (например лобно-височно-теменная деменция, кортикобазальная дегенерация,болезнь Пика, прогрессирующий супрануклеарный паралич) и другие деменции, включая сосудистую деменцию; острый инсульт и другие травматические повреждения; церебрально-васкулярные повреждения (например возрастная дегенерация желтого пятна); травма головного и спинного мозга; периферические невропатии; ретинопатии и глаукома; и других заболеваний, таких как инсулиннезависимый диабет(такой как диабет типа II) и ожирение; маниакально-депрессивное заболевание; шизофрения; алопеция; рак, такой как рак молочной железы, немелкоклеточный рак легкого, рак щитовидной железы, Т- или Вклеточная лейкемия и некоторые опухоли, вызванные вирусами. Настоящее изобретение кроме того относится к способу лечения нейродегенеративных заболеваний, вызванных аномальной активностью GSK3P, и вышеуказанных заболеваний, включающему введение в организм млекопитающего, нуждающегося в лечении, эффективного количества соединения формулы (I). В качестве активного ингредиента лекарства по настоящему изобретению можно использовать вещество, которое выбрано из группы, состоящей из соединения, представленного вышеуказанной формулой (I), и его фармакологически приемлемых солей, его сольватов и его гидратов. Данное вещество как таковое можно вводить в качестве лекарственного средства по настоящему изобретению, однако желательно вводить лекарственное средство в форме фармацевтической композиции, которая содержит вышеуказанное вещество, в качестве активного ингредиента, и одно или более чем одно дополнительное вещество. В качестве активного ингредиента лекарственного средства по настоящему изобретению может быть использована комбинация двух или более вышеуказанных веществ. Вышеуказанная фармацевтическая композиция может быть дополнена активным ингредиентом другого лекарственного средства для лечения вышеуказанных заболеваний. Тип фармацевтической композиции конкретно не ограничен, и данная композиция может быть представлена в виде любого препарата для перорального или парентерального введения. К примеру, фармацевтическая композиция может быть приготовлена например в форме фармацевтических композиций для перорального введения, таких как гранулы, мелкие гранулы,порошки, твердые капсулы, мягкие капсулы, сиропы, эмульсии, суспензии, растворы и подобное, или в форме фармацевтических композиций для парентерального введения, таких как инъекции для внутривенного, внутримышечного или подкожного введения, капельные инфузии, чрескожные препараты, препараты для введения через слизистую оболочку, назальные капли, ингаляционные препараты, суппозитории и подобное. Инъекции или капельные инфузии могут быть приготовлены в виде порошковых препаратов, например в форме лиофилизированных препаратов, и их можно применять путем растворения непосредственно перед применением в подходящей водной среде, такой как физиологический раствор. Препараты с замедленным высвобождением, например покрытые полимерной оболочкой, можно вводить непосредственно интрацеребрально. Типы фармацевтических дополнительных веществ, используемых для изготовления фармацевтической композиции, процентные отношения фармацевтических дополнительных веществ к активному ингредиенту и способы получения фармацевтической композиции могут быть соответствующим образом выбраны специалистами в данной области. Неорганические или органические вещества, либо твердые или жидкие вещества могут быть использованы в качестве фармацевтических дополнительных веществ. В общем случае, фармацевтические дополнительные вещества могут входить в состав композиции в отношении в интервале от 1 до 90 мас.%, исходя из массы активного ингредиента. Примеры эксципиентов, используемых для получения твердых фармацевтических композиций,включают в себя, например, лактозу, сахарозу, крахмал, тальк, целлюлозу, декстрин, каолин, карбонат кальция и подобные. Для получения жидких композиций для перорального введения можно использовать традиционный инертный разбавитель, такой как вода или растительное масло. Жидкая композиция может содержать, кроме инертного разбавителя, вспомогательные вещества, такие как увлажняющие-7 009198 агенты, вспомогательные средства для суспендирования, подсластители, ароматизаторы, красители и консерванты. Жидкой композицией можно заполнять капсулы, изготовленные из рассасывающегося материала, такого как желатин. Примеры растворителей или суспензионных сред, используемых для получения композиций для парентерального введения, например инъекций, суппозиториев, включают в себя воду, пропиленгликоль, попиэтиленгликоль, бензиловый спирт, этилолеат, лецитин и подобное. Примеры основных материалов, используемых для суппозиториев, включают в себя, например, какао-масло,эмульгированное какао-масло, лауриновый липид, витепсол. Доза и частота введения лекарственного средства по настоящему изобретению конкретно не ограничены и могут быть соответствующим образом выбраны в зависимости от условий, таких как цель профилактического и/или терапевтического лечения, тип заболевания, масса тела или возраст пациента, тяжесть заболевания и подобное. В общем случае суточная доза для перорального введения взрослому человеку может составлять от 0,01 до 1000 мг (масса активного ингредиента), и эту дозу можно вводить один раз в сутки или несколько раз в сутки в виде разделенных порций или один раз в несколько суток. При применении лекарственного средства в виде инъекции введения можно предпочтительно осуществлять взрослому человеку непрерывно или с перерывами в суточной дозе от 0,001 до 100 мг (масса активного ингредиента). Химические примеры Настоящее изобретение более конкретно будет пояснено следующими примерами общего характера, однако объем настоящего изобретения не ограничен данными примерами. Пример 1 (соединение 1 таблицы). 9-(2-Оксо-2-фенилэтил)-2-(4-пиридинил)-8-(трифторметил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2-а] пиримидин-4-она гидрохлорид (1:1). 1.1 6-(Трифторметил)-1,4,5,6-тетрагидро-2-пиримидинамина гидрохлорид (1:2). К раствору 10 г (45,11 ммоль) 4-трифторметилпиримидин-2-иламина и 0,065 г палладия в виде 10 мас.% на активированном угле в 5 мл изопропанола добавляли 45 мл раствора соляной кислоты в изопропаноле (5-6 н.). Смесь встряхивали при 40 С при давлении водорода 4 атмосферы (0,4 МПа) до тех пор, пока не прекращалось поглощение водорода. Катализатор удаляли фильтрацией и промывали изопропанолом. Фильтрат упаривали досуха с получением 12,14 г чистого продукта в виде белого твердого вещества. Т. пл. (температура плавления): 138-140 С. 1.2 2-(4-Пиридинил)-8-(трифторметил)-6,7,8,9-тетрагидро-4 Н-пиримидо[1,2-а]пиримидин-4-он. Смесь 5,62 г (29,09 ммоль) этил-3-(пиридин-4-ил)-3-оксопропионата, 7 г (29,09 ммоль) 6(трифторметил)-1,4,5,6-тетрагидро-2-пиримидинамина гидрохлорида (1:2) и 10,05 г (72,72 ммоль) карбоната калия в 50 мл этанола нагревали с обратным холодильником в течение 12 ч. Охлажденный раствор упаривали для удаления растворителя, остаток обрабатывали водой и осадок фильтровали с получением 4,82 г продукта в виде желтого порошка. Т. пл.: 302-304 С. 1.3 9-(2-Оксо-2-фенилэтил)-2-(4-пиридинил)-8-(трифторметил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2-а]пиримидин-4-она гидрохлорид (1:1). К раствору 0,45 г (1,52 ммоль) 2-(4-пиридинил)-8-(трифторметил)-6,7,8,9-тетрагидро-4Hпиримидо[1,2-а]пиримидин-4-она в 10 мл безводного диметилформамида добавляли 0,079 г (1,98 ммоль) гидрида натрия (60%-ная суспензия в минеральном масле). Смесь оставляли перемешиваться при 40 С в течение 15 мин и охлаждали при 0 С. Затем добавляли 0,363 г (1,82 ммоль) 2-бром-1-фенилэтанона и смесь оставляли перемешиваться при комнатной температуре в течение 16 ч. Добавляли воду и смесь экстрагировали дихлорметаном. Экстракты промывали насыщенным водным раствором хлорида натрия,сушили и упаривали с получением неочищенного продукта. После очистки посредством хроматографии на силикагеле, элюируя смесью дихлорметан/метанол/аммиак в соотношении 95/5/0,5 получали свободное основание, которое превращали в солянокислую соль обычным способом с получением 0,358 г продукта в виде белого твердого вещества. Т. пл.: 247-249 С. ЯМР 1 Н (200 МГц; DMSO-d6):8.7 (d, 2H), 8.21 (m, 4H), 7.7 (m, 3 Н), 6.8 (s, 1 Н), 5.8 (d, 1H), 4.95 (d,1H), 4.85 (m, 1H), 4.45 (m, 1H), 3.5 (m, 1H), 2.7-2.2 (m, 2 Н). Пример 2 (соединение 2 таблицы). 9-[(2S)-2-Гидрокси-2-фенилэтил]-2-(4-пиридинил)-8-(трифторметил)-6,7,8,9-тетрагидро-4 Н-пиримидо[1,2-а]пиримидин-4-она гидрохлорид (1:1). Первая и вторая стадии данного способа такие же, как описано в примере 1. Третья стадия может быть подробно изложена следующим образом. К раствору 0,4 г (1,35 ммоль) 2-(4-пиридинил)-8-(трифторметил)-6,7,8,9-тетрагидро-4 Н-пиримидо[1,2-а]пиримидин-4-она в 8 мл безводного диметилформамида добавляли 0,12 г (2,97 ммоль) гидрида натрия (60%-ная суспензия в минеральном масле). Смесь оставляли перемешиваться при 50 С в течение 15 мин. Затем добавляли 0,28 г (1,76 ммоль) (1-S)-2-хлор-1-фенилэтанона и смесь оставляли перемешиваться при 110 С в течение 16 ч.-8 009198 Добавляли воду и смесь экстрагировали этилацетатом. Экстракты промывали насыщенным водным раствором хлорида натрия, сушили и упаривали с получением неочищенного продукта. После очистки посредством хроматографии на силикагеле, элюируя смесью этилдихлорметан/метанол в соотношениях от 100/0 до 95/5, получали соединение в форме свободного основания. Это основание превращали в его солянокислую соль с получением 0,10 г чистого продукта. Т. пл.: 220-222 С. ЯМР 1 Н (200 МГц; DMSO-d6):8.9 (d, 2H), 8.4 (d, 2H), 7.6-7.2 (m, 5H), 6.8 (s, 1 Н), 5.2-4.7 (m, 2 Н),4.6-4.1 (m, 2 Н), 3.6-3.2 (m, 2 Н), 2.5-2.3 (m, 1 Н), 1.9-1.6 (m, 1 Н). Пример 3 (соединение 3 таблицы). 9-[2-(3-Бромфенил)-2-оксоэтил]-2-(4-пиридинил)-8-(трифторметил)-6,7,8,9-тетрагидро-4 Н-пиримидо[1,2-а]пиримидин-4-она гидрохлорид (1:1). Данный продукт получали по аналогии со способом, описанным в примере 1, но заменяя 2-бром-1 фенилэтанон на третьей стадии 2-бром-1-[(3-бром)фенил]этаноном. Т. пл.: 292-294 С. ЯМР 1 Н (200 МГц; DMSO-d6):8.7 (d, 2H), 8.1 (m, 5H), 7.95 (m, 1H), 6.75 (s, 1H), 5.8 (d, 1H), 5.1 (d,1H), 4.8 (m, 1H), 4.6 (m, 1H), 3.5 (m, 1H), 2.7-2.2 (m, 2H). Пример 4 (соединение 4 таблицы). 9-[2-(3-Бромфенил)-2-гидроксиэтил]-2-(4-пиридинил)-8-(трифторметил)-6,7,8,9-тетрагидро-4 Н-пиримидо[1,2-а]пиримидин-4-он. Данный продукт получали по аналогии со способом, описанным в примере 2, но заменяя (1-S)-2 хлор-1-фенилэтанол на третьей стадии 2-хлор-1-[(3-бром)фенил]этанолом. Т. пл.: 113-115 С. ЯМР 1 Н (200 МГц; CDCl3):8.9 (d, 2H), 8.4 (d, 2H), 7.6-7.2 (m, 5H), 6.5 (s, 1 Н), 5.3 (m, 1H), 5.0 (m,1H), 4.5 (m, 1H), 3.9 (m, 1H), 3.5 (m, 2H), 2.45 (m, 1H), 1.9 (m,1H). Пример 5 (соединение 5 таблицы). 9-[2-Оксо-2-фенилэтил]-2-(4-пиримидинил)-8-(трифторметил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2 а]пиримидин-4-он. Данный продукт получали по аналогии со способом, описанным в примере 1, но заменяя этил-3(пиридин-4-ил)-3-оксопропионат на второй стадии этил-3-(пиримидин-4-ил)-3-оксопропионатом. Т. пл.: 247-249 С. ЯМР 1 Н (200 МГц; CDCl3):9.3 (s, 1H), 8.5 (d, 1H), 8.1 (s, 1H), 7.8-7.4 (m, 4 Н), 7.1 (s, 1H), 6.1 (d,1H), 4.9-4.7 (m, 1H), 4.5 (d, 1H), 4.2 (m, 1H), 3.8-3.6 (m, 1H), 2.5 (m, 2H). Пример 6 (соединение 6 таблицы).[1,2-а]пиримидин-4-она гидрохлорид (1:1). 4,0 г (9,6 ммоль) 9-(2-оксо-2-фенилэтил)-2-(4-пиридинил)-8-(трифторметил)-6,7,8,9-тетрагидро-4 Нпиримидо[1,2-а]пиримидин-4-она (соединение 1) разделяли посредством хиральной препаративной ВЭЖХ (CHIRALPAK AD), элюируя смесью н-гептан/изопропанол в соотношении 80/20, с получением 1,43 г чистого продукта в форме свободного основания. tR(время удерживания): 20 мин. Основание переводили в его солянокислую соль с получением 1,52 г чистого продукта. Т. пл.: 233-235 С. []D20 = -85,1 (с = 0,994, CH3OH). ЯМР 1 Н (200 МГц; DMSO-d6):8.7 (d, 2H), 8.21 (m, 4H), 7.7 (m, 3 Н), 6.8 (s, 1 Н), 5.8 (d, 1H), 4.95 (d,1H), 4.85 (m, 1H), 4.45 (m, 1H), 3.5 (m, 1H), 2.7-2.2 (m, 2 Н). Пример 7 (соединение 7 таблицы).[1,2-а]пиримидин-4-она гидрохлорид (1:1). 4,0 г (9,6 ммоль) 9-(2-оксо-2-фенилэтил)-2-(4-пиридинил)-8-(трифторметил)-6,7,8,9-тетрагидро-4Hпиримидо[1,2-а]пиримидин-4-она (соединение 1) разделяли посредством хиральной препаративной ВЭЖХ (CHIRALPAK AD), элюируя смесью н-гептан/изопропанол в соотношении 80/20, с получением 1,47 г чистого продукта в форме свободного основания. tR: 32 мин. Основание переводили в его солянокислую соль с получением 1,56 г чистого продукта. Т. пл.: 233-235 С. [ ]D20 = +86,2 (с = 0,994, CH3OH). ЯМР 1 Н (200 МГц; DMSO-d6):8.7 (d, 2H), 8.21 (m, 4H), 7.7 (m, 3 Н), 6.8 (s, 1 Н), 5.8 (d, 1H), 4.95 (d,1H), 4.85 (m, 1H), 4.45 (m, 1H), 3.5 (m, 1H), 2.7-2.2 (m, 2 Н). Пример 8 (соединение 8 таблицы).[1,2-а]пиримидин-4-он. 200 мг (0,48 ммоль) 9-[2-оксо-2-фенилэтил]-2-(4-пиримидинил)-8-(трифторметил)-6,7,8,9 тетрагидро-4H-пиримидо[1,2-а]пиримидин-4-она (соединение 5) разделяли посредством хиральной препаративной ВЭЖХ (CHIRALPAK AD), элюируя смесью н-гептан/изопропанол в соотношении 80/20,с получением 0,095 г чистого продукта в форме свободного основания. tR: 17 мин.[1,2-а]пиримидин-4-он. 200 мг (0,48 ммоль) 9-[2-оксо-2-фенилэтил]-2-(4-пиримидинил)-8-(трифторметил)-6,7,8,9 тетрагидро-4H-пиримидо[1,2-а]пиримидин-4-она (соединение 5) разделяли посредством хиральной препаративной ВЭЖХ (CHIRALPAK AD), элюируя смесью н-гептан/изопропанол в соотношении 80/20,с получением 0,099 г чистого продукта в форме свободного основания. tR 30 мин. Т. пл.: 237-238. []D20 = -110,8 (с = 0,445, DMSO). ЯМР 1 Н (200 МГц; CDCl3):9.3 (s, 1H), 8.5 (d, 1H), 8.1 (s, 1H), 7.8-7.4 (m, 4 Н), 7.1 (s, 1H), 6.1 (d,1H), 4.9-4.7 (m, 1H), 4.5 (d, 1H), 4.2 (m, 1H), 3.8-3.6 (m, 1H), 2.5(m, 2H). Химические структуры и физические данные соединений вышеуказанной формулы (I), иллюстрирующих настоящее изобретение, приведены в таблице. Соединения получали в соответствии со способами, приведенными в примерах. В таблице р равно 2, q равно 0, Ph представляет собой фенильную группу; (+), (-) указывают соответственно право- и левовращающие изомеры; (S), (R) или (Рац.) указывает в колонке Y или R4 стереохимию атома углерода: (рац.) обозначает рацемическую смесь, (R) означает абсолютную R-конфигурацию, (S) обозначает абсолютную S- конфигурацию. Пример испытания: ингибирующая активность лекарственного средства по настоящему изобретению в отношении GSK3. Могут быть использованы два разных протокола. По первому протоколу: 7,5 мкМ предварительно фосфорилированного GS1 пептида и 10 мкМ АТФ(аденозинтрифосфата) (содержащего 300000 имп/мин 33 Р-АТФ) инкубировали в 25 мМ Tris-HCl, pH 7,5; 0,6 мМ DTT(дитиотеитол), 6 мМ MgCl2; 0,6 мМ EGTA (этиленбис(оксиэтиленнитрило)тетрауксусная кислота); 0,05 мг/мл BSA буфере в течение 1 ч при комнатной температуре в присутствии GSK3 (общий реакционный объем 100 мкл). По второму протоколу: 4,1 мкМ предварительно фосфорилированного GS1 пептида и 42 мкМ АТФ(содержащего 260000 имп/мин 33 Р-АТФ) инкубировали в 80 мМ Mes-NaOH, pH 6,5; 1 мМ ацетата магния, 0,5 мМ EGTA; 5 мМ 2-меркаптоэтанола, 0,02% Tween 20, 10%-ном глицериновом буфере в течение 2 ч при комнатной температуре в присутствии GSK3. Ингибиторы растворяли в DMSO (конечная концентрация растворителя в реакционной среде 1%). Реакцию останавливали 100 мкл раствора, приготовленного из 25 г полифосфорной кислоты (85%P2O5), 126 мл 85%-ной H3PO4 и H2O до 500 мл, а затем перед использованием разбавляли до 1:100. Аликвоту реакционной смеси затем переносили на Whatman P81 катионообменные фильтры и промывали раствором, описанным выше. Инкорпорированную 33 Р радиоактивность определяли посредством жидкостной сцинтилляционной спектрометрии. Фосфорилированный GS-1 пептид имел следующую последовательность:CSK3-ингибирующую активность соединений по настоящему изобретению выражают в виде значения IC50 (концентрации, вызывающей 50%-ное ингибирование), и, в качестве примера, интервал значений IC50 для соединений, представленных в таблице, соответствует концентрациям от 1 нмоль до 1 мкмоль. Например, соединение 6 таблицы демонстрирует IC50 равную 3 нМ. Примеры препаратов(1) Таблетки Ингредиенты, указанные ниже, смешивали обычным способом и прессовали, используя стандартные устройства, мг:(2) Мягкие капсулы Ингредиенты, указанные ниже, смешивали обычным способом и помещали в мягкие капсулы, мг: Соединение примера 1 30 Оливковое масло 300 Лецитин 20(1) Парентеральные препараты Ингредиенты, указанные ниже, смешивали обычным способом для приготовления инъекционных препаратов, помещенных в 1 мл ампулу, мг: Соединение примера 1 3 Хлорид натрия 4 Дистиллированная вода для 1 инъекций Промышленная применимость Соединения по настоящему изобретению обладают ингибирующей активностью в отношенииGSK3 и полезны в качестве активного ингредиента лекарства для профилактического и/или терапевтического лечения заболеваний, вызванных аномальной активностью GSK3, и более конкретно нейродегенеративных заболеваний. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Производное замещенного пиримидона, представленное формулой (I) или его соль, или его сольват, или его гидрат,где X представляет собой два атома водорода, атом серы, атом кислорода или С 1-2 алкильную группу и атом водорода;Y представляет собой связь, карбонильную группу, метиленовую группу, возможно замещенную одной или двумя группами, выбранными из C1-6 алкильной группы, гидроксильной группы, С 1-4 алкоксигруппы, С 1-2 пергалогенированной алкильной группы или аминогруппы;R1 представляет собой 2-, 3- или 4-пиридиновое кольцо либо 2-, 4- или 5-пиримидиновое кольцо,причем эти кольца возможно замещены С 1-4 алкильной группой, С 1-4 алкоксигруппой или атомом галогена;R2 представляет собой фенильную группу или нафталиновое кольцо, причем фенильная группа и нафталиновое кольцо возможно замещены 1-4 заместителями, выбранными из С 1-6 алкильной группы,фенильной группы, метилендиоксигруппы, атома галогена, С 1-2 пергалогенированной алкильной группы,C1-3 галогенированной алкильной группы, гидроксильной группы, С 1-4 алкоксигруппы, нитро, циано, амино, С 1-5 моноалкиламиногруппы или С 2-10 диалкиламиногруппы;R3 представляет собой атом водорода или С 1-6 алкильную группу;R4 представляет собой С 1-2 пергалогенированную алкильную группу или C1-3 галогенированную алкильную группу;R5 представляет собой водород, С 1-6 алкильную группу или атом галогена;n представляет собой число от 0 до 3; и р+q=от 0 до 3. 2. Производное замещенного пиримидона, или его соль, или его сольват, или его гидрат по п.1, гдеR4 представляет собой С 1-2 пергалогенированную алкильную группу. 3. Производное замещенного пиримидона, или его соль, или его сольват, или его гидрат по п.1 или 2,где R1 представляет собой незамещенное 4-пиридиновое кольцо или 4-пиримидиновое кольцо;R2 представляет собой фенильную группу, возможно замещенную 1-4 заместителями, выбранными из C1-3 алкильной группы, фенильной группы, атома галогена, гидроксильной группы, циано или С 1-2 алкоксигруппы, либо альтернативно R2 представляет собой фенильную группу, возможно замещенную 1-4 заместителями, выбранными из С 1-3 алкильной группы, атома галогена, гидроксильной группы илиR3 представляет собой атом водорода;R4 представляет собой трифторметильную группу;R5 представляет собой атом водорода или фтора либо альтернативно R5 представляет собой атом водорода;X представляет собой два атома водорода;Y представляет собой карбонильную группу или метиленовую группу, возможно замещенную гидроксильной группой; где R1, R3, R4, R5, р и q такие, как определено для соединения формулы (I) по п.1. 6. Лекарство, содержащее в качестве активного ингредиента вещество, выбранное из группы, состоящей из производного замещенного пиримидона, представленного формулой (I), или его соли, или его сольвата, или его гидрата по п.1. 7. Ингибитор GSK3 (киназы-3 гликогенсинтазы), выбранный из группы, состоящей из производного замещенного пиримидона, представленного формулой (I), или его соли, или его сольвата, или его- 13009198 гидрата по п.1. 8. Применение соединения по любому из пп.1-4 для изготовления лекарства для профилактического и/или терапевтического лечения заболевания, вызванного аномальной активностью GSK3. 9. Применение соединения по любому из пп.1-4 для изготовления лекарства для профилактического и/или терапевтического лечения нейродегенеративного заболевания. 10. Применение соединения по п.9, где нейродегенеративное заболевание выбрано из группы, состоящей из болезни Альцгеймера, болезни Паркинсона, тауопатий, сосудистой деменции; острого инсульта, травматических повреждений; церебрально-васкулярных повреждений, травмы головного мозга,травмы спинного мозга; периферических невропатий; ретинопатий или глаукомы. 11. Применение соединения по любому из пп.1-4 для изготовления лекарства для профилактического и/или терапевтического лечения инсулиннезависимого диабета, ожирения, маниакальнодепрессивного заболевания, шизофрении, алопеции или рака. 12. Применение по п.11, где рак представляет собой рак молочной железы, немелкоклеточный рак легкого, рак щитовидной железы, Т- или В-клеточную лейкемию или опухоли, вызванные вирусами.
МПК / Метки
МПК: C07D 487/04
Метки: замещённого, производные, 9-тетрагидропиримидо[1,2-а]пиримидин-4-она, 8-перфторалкил-6
Код ссылки
<a href="https://eas.patents.su/15-9198-proizvodnye-zameshhyonnogo-8-perftoralkil-6-7-8-9-tetragidropirimido12-apirimidin-4-ona.html" rel="bookmark" title="База патентов Евразийского Союза">Производные замещённого 8-перфторалкил-6, 7, 8, 9-тетрагидропиримидо[1,2-а]пиримидин-4-она</a>
Предыдущий патент: 8 – замещённые производные 6, 7, 8, 9-тетрагидропиримидо[1, 2-a] пиримидин-4-она
Следующий патент: N-мостиковые селективные модуляторы андрогенных рецепторов и способы их применения
Случайный патент: Способы и системы для ослабления колебаний при бурении



















