Предрасположенность к инфекции, связанная с интенсивными физическими упражнениями или другим стрессом
Формула / Реферат
1. Способ оценки потенциальной восприимчивости к инфекции у субъекта, подверженного воздействию фактора или факторов стресса, включающий
(a) определение уровня иммуноглобулина А (IgA) у субъекта на фазе тренировки и
(b) прогноз восприимчивости субъекта к инфекции сравнением уровня IgA на фазе тренировки с заданной пороговой величиной.
2. Способ оценки потенциальной восприимчивости к инфекции у субъекта, подверженного воздействию фактора или факторов стресса, включающий
(a) определение уровня иммуноглобулина A1 (IgA1) у субъекта и
(b) прогноз восприимчивости субъекта к инфекции сравнением уровня IgA1 с заданной пороговой величиной.
3. Способ по п.1 или 2, в котором уровень иммуноглобулина определяется на ранней фазе тренировки.
4. Способ по любому из пп.1-3, в котором инфекция представляет собой инфекцию слизистой оболочки.
5. Способ по п.4, в котором инфекция представляет собой респираторную инфекцию.
6. Способ по любому из пп.1-5, в котором пороговая величина представляет собой пороговую величину у здоровой популяции.
7. Способ по любому из пп.1-5, в котором пороговая величина представляет собой внутреннюю личную пороговую величину.
8. Способ по любому из пп.1-7, в котором иммуноглобулин представляет собой секреторный иммуноглобулин.
9. Способ по п.8, в котором секреторный иммуноглобулин представляет собой иммуно-
глобулин слюны.
10. Способ по п.9, в котором иммуноглобулин слюны получен из образца цельной, не стимулированной слюны.
11. Способ по п.10, в котором у субъекта слюна берется не натощак.
12. Способ по любому из пп.1-11, в котором субъект представляет собой спортсмена.
13. Способ по п.12, в котором спортсмен является профессиональным пловцом.
14. Способ по любому из пп.1-13, в котором фактор стресса достоверно влияет на эффективность иммунной системы.
15. Способ по любому из пп.1-13, в котором субъект подвержен воздействию физического и/или психологического фактора стресса.
16. Способ по п.15, в котором физический и/или психологический фактор стресса представляет собой длительную физическую тренировку или избыточную тренировку.
17. Способ по любому из пп.1-16, в котором уровень иммуноглобулина определяется радиальной иммунодиффузией.
18. Способ по любому из пп.1-16, в котором уровень иммуноглобулина определяется иммуноферментным анализом.
19. Способ по любому из пп.1-18, в котором уровень иммуноглобулина определяется быстрым количественным анализом около субъекта.
20. Способ по любому из пп.1-19, в котором анализ слюны на содержание иммуноглобулина производится in situ контактированием устройства или системы для анализа со слюной субъекта.
21. Способ по любому из пп.1-20, в котором количественный анализ представляет собой самостоятельный тест, выполняемый субъектом.
22. Способ мониторинга динамики состояния субъекта после инвазивного лечения, включающий
(a) определение уровня IgA1 у субъекта и
(b) мониторинг динамики состояния субъекта сравнением указанного уровня IgA1 с заданной пороговой величиной.
23. Способ по п.22, в котором уровень IgA1 оценивается в образце слюны субъекта.
24. Способ оценки воздействия фактора или факторов стресса на определенные здесь функциональную способность и/или степень усталости, включающий
(a) определение уровня IgA1 в слюне субъекта и
(b) оценку воздействия фактора или факторов стресса на функциональную способность и/или степень усталости субъекта сравнением указанного уровня IgA1 с заданной пороговой величиной.
25. Способ по п.24, в котором субъект представляет собой спортсмена.
26. Способ по п.25, в котором спортсмен представляет собой профессионального пловца.
27. Способ оценки потенциальной восприимчивости к респираторной инфекции у профессионального пловца, включающий
(a) определение уровня иммуноглобулина A (IgA) в слюне пловца на ранней фазе тренировки и
(b) прогноз потенциальной восприимчивости пловца к респираторной инфекции сравнением уровня IgA на ранней фазе тренировки с заданной пороговой величиной.
28. Способ оценки потенциальной восприимчивости к респираторной инфекции у профессионального пловца, включающий
(a) определение уровня иммуноглобулина A1 (IgA1) в слюне пловца на ранней фазе тренировки и
(b) прогноз потенциальной восприимчивости пловца к респираторной инфекции сравнением уровня IgA1 на ранней фазе тренировки с заданной пороговой величиной.
29. Способ по п.28, в котором пороговая величина представляет собой пороговую величину у здоровой популяции.
30. Способ по п.28, в котором пороговая величина представляет собой внутреннюю личную пороговую величину.
31. Способ оценки потенциальной восприимчивости субъекта к инфекции, включающий
(a) определение уровня иммуноглобулина А (IgA) у субъекта после воздействия фактора или факторов стресса;
(b) предоставление периода восстановления, как здесь определено;
(c) определение уровня IgA у субъекта после периода восстановления;
(d) прогноз потенциальной восприимчивости субъекта к инфекции сравнением уровня IgA на указанном выше этапе (a) с уровнем IgA на указанном выше этапе (с).
32. Способ оценки потенциальной восприимчивости субъекта к инфекции, включающий
(a) определение уровня иммуноглобулина A1 (IgA1) у субъекта после воздействия фактора или факторов стресса;
(b) предоставление периода восстановления, как здесь определено;
(c) определение уровня IgA1 у субъекта после периода восстановления;
(d) прогноз потенциальной восприимчивости субъекта к инфекции сравнением уровня IgA1 на указанном выше этапе (a) с уровнем IgA1 на указанном выше этапе (c).
33. Способ по п.31 или 32, в котором инфекция представляет собой инфекцию слизистой оболочки.
34. Способ по п.33, в котором инфекция представляет собой респираторную инфекцию.
35. Способ по любому из пп.31-34, в котором иммуноглобулин представляет собой секреторный иммуноглобулин.
36. Способ по п.35, в котором секреторный иммуноглобулин представляет собой иммуно-
глобулин слюны.
37. Способ по п.36, в котором иммуноглобулин слюны получен из образца цельной, не стимулированной слюны.
38. Способ по п.37, в котором у субъекта слюна берется не натощак.
39. Способ по любому из пп.31-38, в котором субъект представляет собой спортсмена.
40. Способ по п.39, в котором спортсмен является профессиональным пловцом.
41. Способ по любому из пп.31-40, в котором фактор стресса достоверно влияет на эффективность иммунной системы.
42. Способ по любому из пп.31-40, в котором субъект подвержен воздействию физического и/или психологического фактора стресса.
43. Способ по п.42, в котором физический и/или психологический фактор стресса представляет собой длительную физическую тренировку или избыточную тренировку.
44. Способ по любому из пп.31-43, в котором уровень иммуноглобулина определяется радиальной иммунодиффузией.
45. Способ по любому из пп.31-43, в котором уровень иммуноглобулина определяется иммуноферментным анализом.
46. Способ по любому из пп.31-45, в котором уровень иммуноглобулина определяется быстрым количественным анализом около субъекта.
47. Способ по любому из пп.31-46, в котором анализ слюны на содержание иммуноглобулина производится in situ контактированием устройства или системы для анализа со слюной субъекта.
48. Способ по любому из пп.31-47, в котором количественный анализ представляет собой самостоятельный тест, выполняемый субъектом.
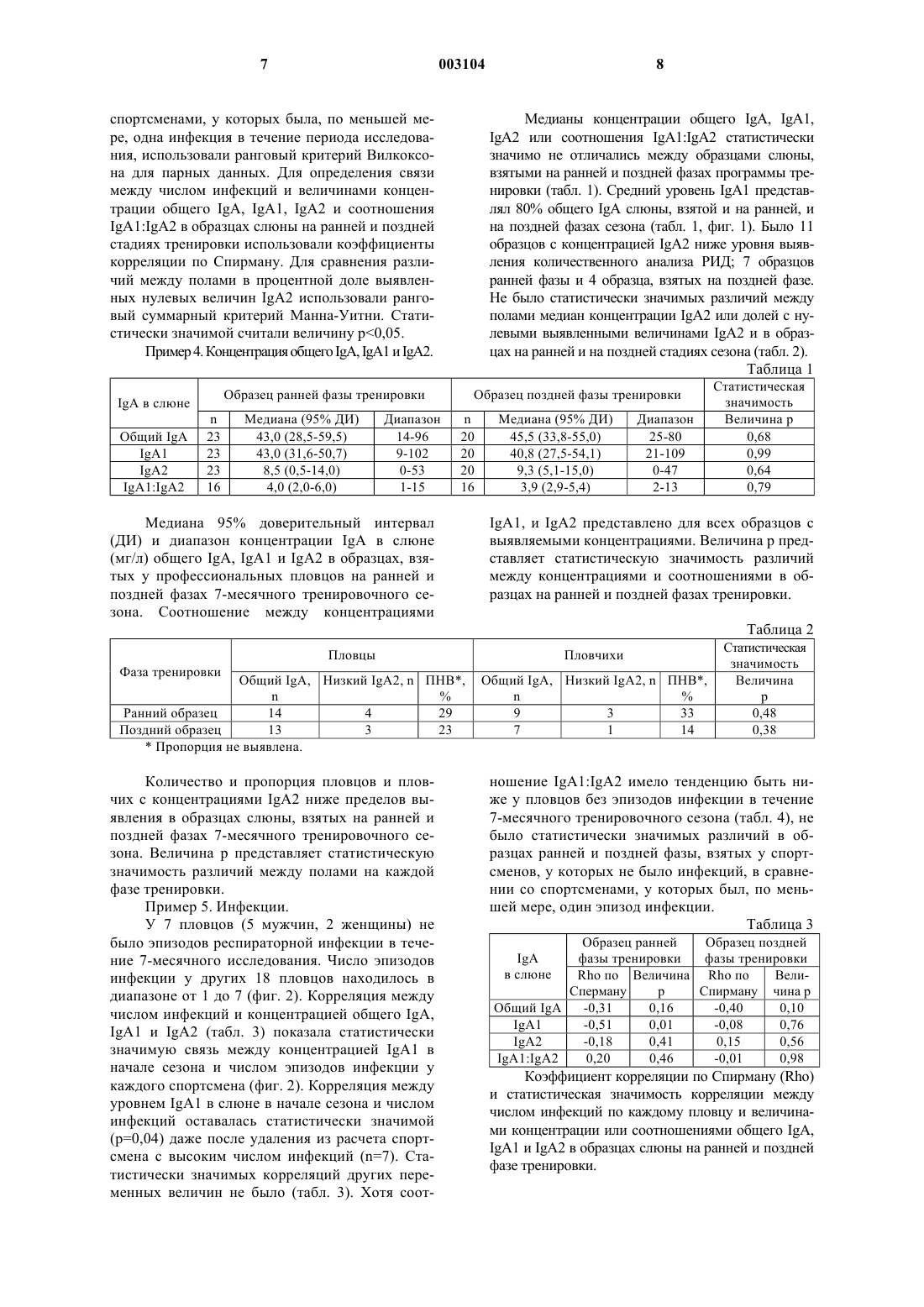
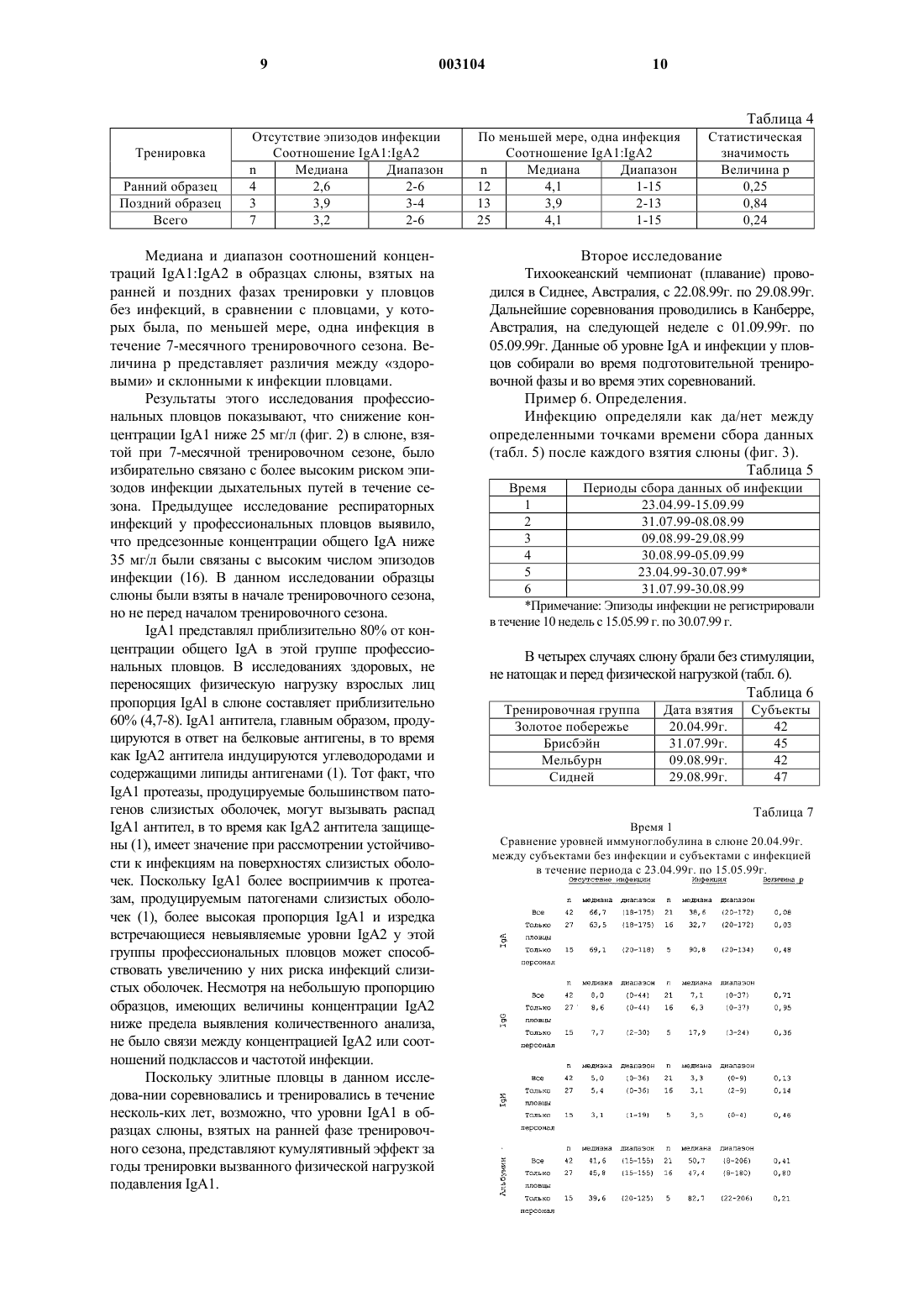
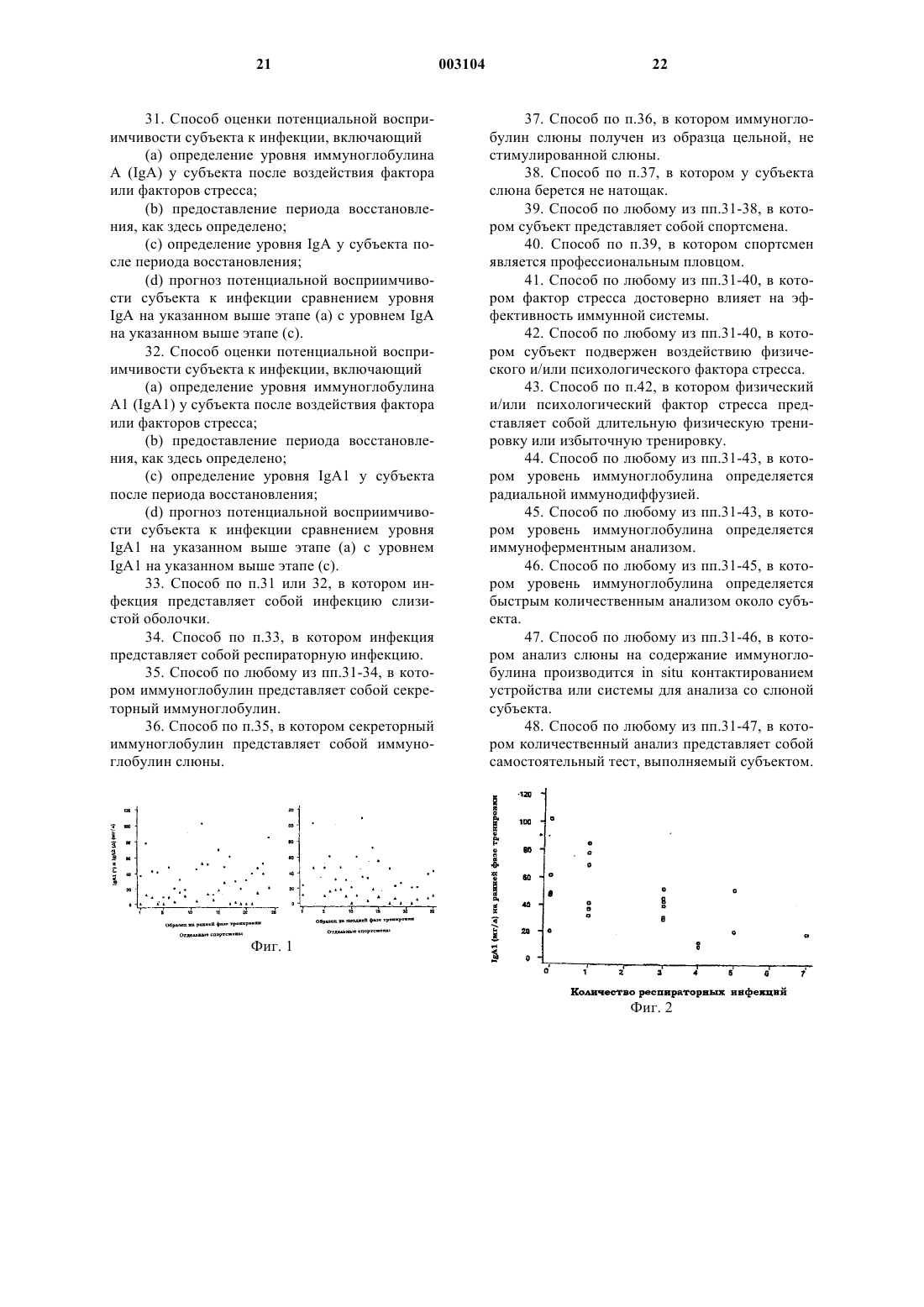
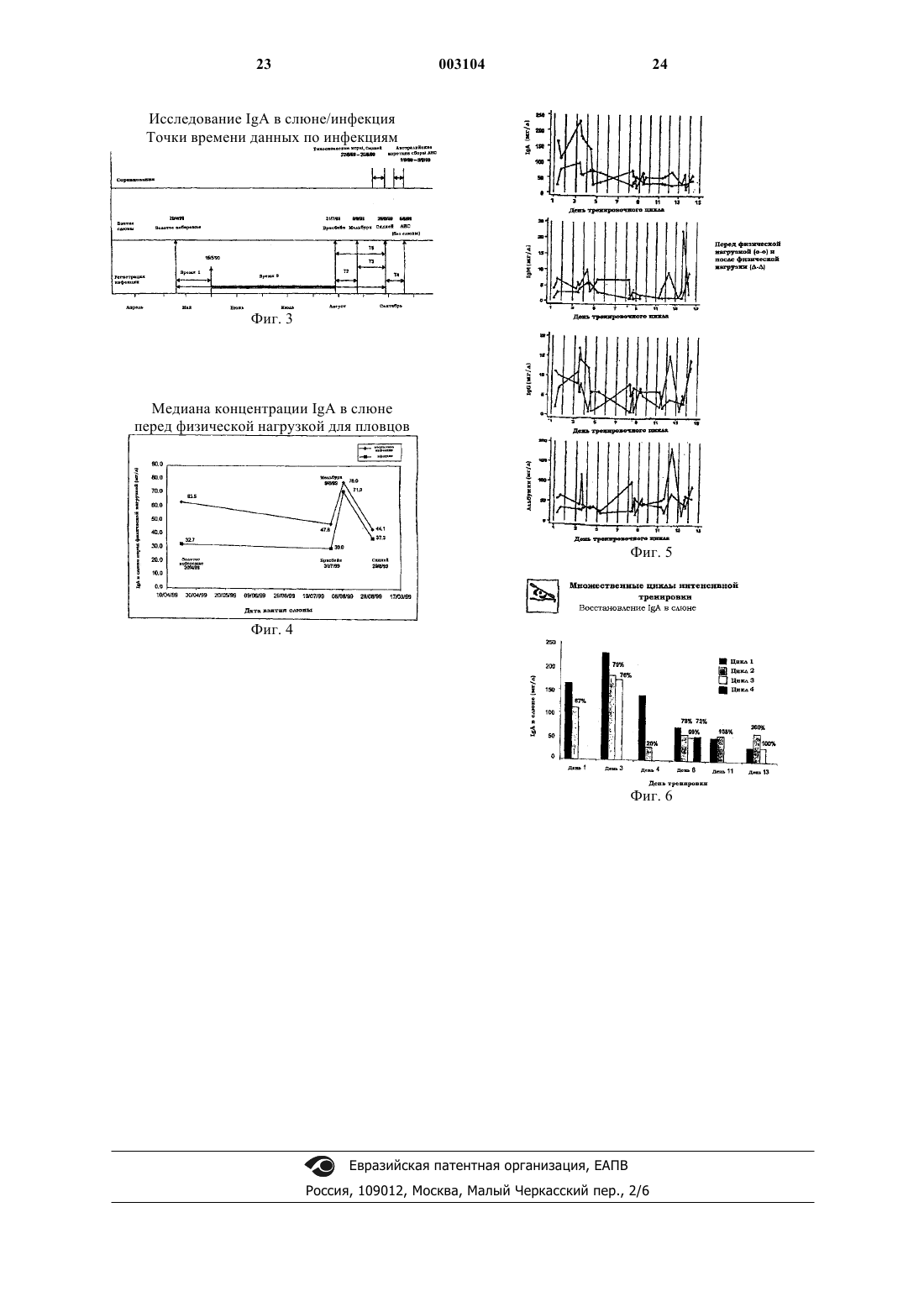
Текст
1 Область техники Настоящее изобретение относится к способам определения предрасположенности к инфекции у субъекта, подверженного действию факторов стресса. В частности, настоящее изобретение относится к способам оценки риска восприимчивости к инфекции у субъекта мониторингом уровней IgA и IgA1. Предшествующий уровень техники Секреторный IgA (SIgA) представляет преобладающую форму антитела, которое опосредует специфическую иммунологическую защиту на поверхностях слизистых оболочек (1). Защита обеспечивается несколькими признанными механизмами: вмешательством в адгезию микроба к поверхностям слизистых оболочек,ингибированием проникновения антигенов через эпителиальную мембрану, комплексообразования с антигенами на базолатеральной поверхности эпителия слизистой оболочки для облегчения элиминации экзоцитозом в просвет слизистой оболочки и механизмами спасения на внутриклеточном и интерстициальном уровнях (2). У людей иммуноглобулин А (IgA) встречается в виде двух подклассов, которые отличаются аминокислотными последовательностями и гликозилированием тяжелой цепи альфа (3). IgA1 преобладает (приблизительно 90%) в сыворотке, в то время как IgA2 преобладает в большинстве секретов слизистой оболочки (4). Пропорции двух подклассов варьируют между участками слизистой оболочки вследствие различий распределения иммуноцитов, продуцирующих иммуноглобулин(1,5-6). В слюне здоровых людей содержится приблизительно 60% IgAl (4,7-8). Исследование содержания IgA в слюне популяций, занимающихся физическими упражнениями, привлекло значительное внимание благодаря сообщениям о высоком распространении респираторных инфекций у профессиональных спортсменов (9-12). Связи между изменениями концентрации IgA в слюне при физических упражнениях сложны и зависят от интенсивности, длительности и периодичности тренировок и степени физической подготовки спортсмена (13-14). Было показано, что концентрация IgA в слюне снижается после интенсивной физической нагрузки у профессиональных спортсменов, тренирующихся в различных видах спорта на выносливость (14-19). Единственным сообщением о влиянии физической нагрузки на подклассы IgA было исследование влияния максимальной физической нагрузки на общий уровень IgA и подклассов IgA в женском молоке(20). После изнурительной физической нагрузки в женском молоке снизилась общая концентрация IgA и IgA1, но не IgA2, с восстановлением до исходного уровня в пределах 60 мин (20). Недавно сообщалось, что низкая концентрация IgA в слюне профессиональных пловцов и группы с умеренной физической нагрузкой была связана с повышенным риском респира 003104 2 торной инфекции (16). Продольные исследования профессиональных пловцов также показали статистически значимое снижение концентрации IgA в слюне в течение 7-месячного периода(сезона) тренировок (15-16). Однако не все пловцы, участвовавшие в программе тренировок, были восприимчивы к инфекции. Остается необходимость в подходящем и своевременном тесте для прогноза восприимчивости к инфекции у лиц, подверженных воздействию физического или другого стресса. Задачей настоящего изобретения является преодоление или уменьшение, по меньшей мере, некоторых недостатков предшествующего уровня техники или предоставление полезной альтернативы. Сущность изобретения Как упоминалось выше, IgA включает два подкласса, IgA1 и IgA2. Неожиданно было обнаружено, что из этих двух подклассов уровеньIgAl у субъекта, подверженного действию фактора стресса, является лучшим показателем восприимчивости к инфекции. Было также неожиданно обнаружено, что наилучшие прогностические результаты при использовании общегоIgA в качестве показателя чувствительности к инфекции получаются, когда уровень IgA измеряется на ранней фазе тренировки. Кроме того,было также показано, что если уровень IgA,снижение которого происходит после воздействия фактора стресса, быстро не восстанавливается, то это приводит к длительному снижению уровня IgA. Как упомянуто выше, сниженный уровень IgA является показателем восприимчивости к инфекции. Таким образом, скорость восстановления уровня IgA также является хорошим показателем восприимчивости к инфекции. В соответствии с первым аспектом изобретение предоставляет способ оценки потенциальной восприимчивости к инфекции у субъекта, подверженного воздействию фактора или факторов стресса, включающий(a) определение уровня иммуноглобулина А (IgA) у субъекта на фазе тренировки и(b) прогноз восприимчивости субъекта к инфекции сравнением уровня IgA на фазе тренировки с заданной пороговой величиной. В соответствии со вторым аспектом изобретение предоставляет способ оценки потенциальной восприимчивости к инфекции у субъекта, подверженного воздействию фактора или факторов стресса, включающий(b) прогноз восприимчивости субъекта к инфекции сравнением уровня IgA1 на фазе тренировки с заданной пороговой величиной. В соответствии с третьим аспектом изобретение предоставляет способ мониторинга изменения состояния субъекта после лечебного вмешательства, включающий(b) мониторинг изменения состояния субъекта сравнением указанного уровня IgA1 с заданной пороговой величиной. В соответствии с четвертым аспектом изобретение предоставляет способ оценки воздействия фактора или факторов стресса на функциональное состояние субъекта и/или степень усталости, как определено здесь, включающий(b) оценку воздействия фактора или факторов стресса на функциональное состояние субъекта и/или степень усталости сравнением указанного уровня IgA1 с заданной пороговой величиной. В соответствии с пятым аспектом изобретение предоставляет способ оценки потенциальной восприимчивости к респираторной инфекции у профессионального пловца, включающий(a) определение уровня иммуноглобулина A(IgA) в слюне пловца на ранней фазе тренировки и(b) прогноз потенциальной восприимчивости пловца к респираторной инфекции сравнением уровня IgA на ранней фазе тренировки с заданной пороговой величиной. В соответствии с шестым аспектом изобретение предоставляет способ оценки потенциальной восприимчивости к респираторной инфекции у профессионального пловца, включающий(a) определение уровня иммуноглобулина А 1(IgA1) в слюне пловца на ранней фазе тренировки и(b) прогноз потенциальной восприимчивости пловца к респираторной инфекции сравнением уровня IgA1 на ранней фазе тренировки с заданной пороговой величиной. В соответствии с седьмым аспектом изобретение предоставляет способ оценки потенциальной восприимчивости субъекта к инфекции, включающий(a) определение уровня иммуноглобулина А (IgA) у субъекта после воздействия фактора или факторов стресса;(c) определение уровня IgA у субъекта после периода восстановления;(d) прогноз потенциальной восприимчивости субъекта к инфекции сравнением уровняIgA на указанном выше этапе (а) с уровнем IgA на указанном выше этапе (с). В соответствии с восьмым аспектом изобретение предоставляет способ оценки потенциальной восприимчивости субъекта к инфекции, включающийA1 (IgA1) у субъекта после воздействия фактора или факторов стресса;(c) определение уровня IgA1 у субъекта после периода восстановления;(d) прогнозирование потенциальной восприимчивости субъекта к инфекции сравнением 4 уровня IgA1 на указанном выше этапе (а) с уровнем IgA1 на указанном выше этапе (с). Предпочтительно уровень иммуноглобулина определяется на ранней фазе тренировки. Предпочтительно инфекция представляет собой инфекцию слизистых оболочек и наиболее предпочтительно инфекция представляет собой респираторную инфекцию. Предпочтительно пороговая величина представляет пороговую величину у здоровой популяции. Однако в определенных случаях может быть более целесообразным использование внутренней персональной пороговой величины. Предпочтительно иммуноглобулин представляет собой секреторный иммуноглобулин. Предпочтительно секреторный иммуноглобулин представляет собой слюнной иммуноглобулин. Предпочтительно слюнной иммуноглобулин получен из образца цельной нестимулированной слюны, а наиболее предпочтительно субъект не голодает при сборе слюны. Предпочтительно субъект является спортсменом. Предпочтительно спортсмен является профессиональным пловцом. Предпочтительно, что фактор стресса достоверно влияет на эффективность иммунной системы. Предпочтительно субъект подвергается воздействию физического и/или психологического фактора стресса. Предпочтительно физическим и/или психологическим фактором стресса является длительная физическая тренировка или избыточная тренировка. Предпочтительно уровень иммуноглобулина определяется радиальной иммунодиффузией или иммуноферментным методом (ELISA). Предпочтительно уровень иммуноглобулина определяется с помощью быстрого анализа в присутствии пациента. Предпочтительно анализ слюны производится на содержание иммуноглобулина insitu контактированием анализирующего устройства или системы со слюной субъекта. Предпочтительно анализ представляет собой самостоятельное исследование, выполняемое субъектом. В контексте настоящего изобретения слово фактор стресса включает в себя значение физических, физиологических, психологических и питательных факторов стресса, которые включают усталость, но не ограничивается ими. В контексте настоящего изобретения слово функциональное состояние включает в себя значение функционального состояния в отношении других субъектов или функциональное состояние в отношении к личному уровню функционального состояния. Аналогичным образом термин усталость включает в себя значение усталости в отношении других субъектов или усталости в отношении к личному уровню усталости. В контексте настоящего изобретения слово предсезонный следует понимать специалистам в данной области как обозначающее перед возобновлением тренировок. 5 В контексте настоящего изобретения слова ранняя тренировочная фаза следует понимать специалистам в данной области как обозначающие первый микроцикл тренировки после периода отдыха. В контексте настоящего изобретения слова поздняя тренировочная фаза следует понимать специалистам в данной области как обозначающие микроцикл тренировки перед соревнованием. Хотя настоящее изобретение было проиллюстрировано примерами, относящимися к спортсменам, подверженным действию физического фактора стресса, специалистам в данной области будет ясно, что аналогичная оценка восприимчивости к инфекции будет применима к другим профессиям и видам деятельности,связанным со стрессом, например к профессиям,связанным с медициной и уходом за пациентами, командировочным и профессиональным путешественникам, где факторы стресса могут быть физическими и/или не физическими факторами стресса, включая физиологические и психологические факторы стресса и им подобные. Кроме того, настоящее изобретение будет также применимо к пациентам, подверженным действию стресса лечебного вмешательства. В контексте настоящего изобретения термин лечебное вмешательство включает инвазивные/агрессивные методы медицинского лечения/процедуры, включая хирургические и не хирургические вмешательства и им подобные. В контексте настоящего изобретения термин период восстановления включает период отдыха после воздействия фактора стресса или факторов стресса. Соответствующая длительность времени восстановления будет определяться опытным адресатом и будет варьировать в зависимости от типа фактора стресса и субъекта, подвергнутого действию стресса. Хотя настоящее изобретение было описано преимущественно в контексте восприимчивости к инфекции, включая реактивацию латентной инфекции, специалистам в данной области будет понятно, что аналогичные принципы могут применяться к оценке нарушенного функционального состояния и усталости. Краткое описание чертежей Фиг. 1 - концентрация (мг/л) IgA1 иIg2 в образцах слюны, собранных у 25 профессиональных пловцов во время ранней и поздней фаз 7-месячного тренировочного сезона; фиг. 2 - концентрация IgA1 (мг/л) на ранней фазе тренировки у каждого пловца и количество эпизодов инфекции, зарегистрированное в течение 7-месячного тренировочного сезона; фиг. 3 - точки времени сбора данных по инфекции в исследовании слюны в отношенииIgA/инфекции в тихоокеанском регионе; фиг. 4 - медиана концентрации IgA в слюне у пловцов перед физической нагрузкой; фиг. 5 - концентрация иммуноглобулина и альбумина (мг/л) перед физической нагрузкой и после физической нагрузкив слюне для каждого тренировочного цикла в течение 14-дневного периода исследования; фиг. 6 - процентное восстановление уровняIgA в слюне перед циклом физической нагрузки по отношению к исходному уровню на день(100%) в дни с множественными циклами физической нагрузки. Описание предпочтительного варианта реализации Концентрация IgA1 в образце, взятом у субъекта, подлежащего исследованию, определяется радиальной иммунодиффузией (РИД) с использованием полученных в промышленных условиях планшет РИД низкого уровня и калибраторов, иммуноферментным анализом (ELISA) или другими технологиями, применимыми для быстрого тестирования около субъекта. Настоящие результаты показывают, что сниженные концентрации IgA1 особенно связаны с более высоким риском инфекции. Первое исследование Пример 1. Субъекты и структура исследования. Образцы цельной нестимулированной слюны брали у 25 профессиональных пловцов (16 мужчин, 9 женщин) в течение ранней (с апреля по июнь) и поздней (с августа по октябрь) фаз 7 месячной программы тренировки (15). Среднее время между взятием образцов у отдельных спортсменов составляло 4 месяца. Образцы слюны брали до первого цикла физической нагрузки в день взятия и, по меньшей мере, через 18 ч после предыдущего цикла физической нагрузки. Пловцы в возрасте от 16 до 24 лет проводили в бассейне тренировку длительностью 20-25 ч и 5 ч тренировки на суше в 1 неделю. Каждый эпизод респираторной инфекции регистрировали во время исследования, и он верифицировался врачом (16). Исследование проводили по информированному согласию команды пловцов Австралийского Института Спорта (АИС), и оно было утверждено комитетом по этике Австралийской Спортивной Комиссии. Пример 2. Определение общего IgA, IgA1 и IgA2. Концентрацию общего IgА в цельной нестимулированной слюне измеряли электроиммунодиффузией (21). Концентрацию IgA1 и IgA2 определяли радиальной иммунодиффузией (РИД) с использованием одного номера серии полученных в промышленных условиях планшет РИД низкого уровня и калибраторов (The Binding Site,Birmingham, UK). Предел выявления количественных анализов составил 4,0 мг/л для общегоIgA, 8,3 мг/л для IgA1 и 7,5 мг/л для IgA2. Коэффициент вариации между циклами составил 3,5% для общего IgA, 4,1% для IgA1 и 3,0% для IgA2. Пример 3. Статистический анализ. В целях этого исследования спортсменов классифицировали или как не имеющих инфекций ("здоровых") или, по меньшей мере, имевших один эпизод инфекции в течение периода исследования. Для сравнения величин соотношения между "здоровыми" спортсменами и Медианы концентрации общего IgA, IgA1,IgA2 или соотношения IgA1:IgA2 статистически значимо не отличались между образцами слюны,взятыми на ранней и поздней фазах программы тренировки (табл. 1). Средний уровень IgA1 представлял 80% общего IgA слюны, взятой и на ранней, и на поздней фазах сезона (табл. 1, фиг. 1). Было 11 образцов с концентрацией IgA2 ниже уровня выявления количественного анализа РИД; 7 образцов ранней фазы и 4 образца, взятых на поздней фазе. Не было статистически значимых различий между полами медиан концентрации IgA2 или долей с нулевыми выявленными величинами IgA2 и в образцах на ранней и на поздней стадиях сезона (табл. 2). Таблица 1 спортсменами, у которых была, по меньшей мере, одна инфекция в течение периода исследования, использовали ранговый критерий Вилкоксона для парных данных. Для определения связи между числом инфекций и величинами концентрации общего IgA, IgA1, IgA2 и соотношенияIgA1:IgA2 в образцах слюны на ранней и поздней стадиях тренировки использовали коэффициенты корреляции по Спирману. Для сравнения различий между полами в процентной доле выявленных нулевых величин IgA2 использовали ранговый суммарный критерий Манна-Уитни. Статистически значимой считали величину р 0,05. Пример 4. Концентрация общего IgA, IgA1 и IgA2. Образец ранней фазы тренировки Образец поздней фазы тренировки(мг/л) общего IgA, IgA1 и IgA2 в образцах, взятых у профессиональных пловцов на ранней и поздней фазах 7-месячного тренировочного сезона. Соотношение между концентрациями Статистическая значимость Величина p 0,68 0,99 0,64 0,79IgA1, и IgA2 представлено для всех образцов с выявляемыми концентрациями. Величина р представляет статистическую значимость различий между концентрациями и соотношениями в образцах на ранней и поздней фазах тренировки. Таблица 2 Количество и пропорция пловцов и пловчих с концентрациями IgА 2 ниже пределов выявления в образцах слюны, взятых на ранней и поздней фазах 7-месячного тренировочного сезона. Величина р представляет статистическую значимость различий между полами на каждой фазе тренировки. Пример 5. Инфекции. У 7 пловцов (5 мужчин, 2 женщины) не было эпизодов респираторной инфекции в течение 7-месячного исследования. Число эпизодов инфекции у других 18 пловцов находилось в диапазоне от 1 до 7 (фиг. 2). Корреляция между числом инфекций и концентрацией общего IgA,IgA1 и IgA2 (табл. 3) показала статистически значимую связь между концентрацией IgA1 в начале сезона и числом эпизодов инфекции у каждого спортсмена (фиг. 2). Корреляция между уровнем IgA1 в слюне в начале сезона и числом инфекций оставалась статистически значимой(р=0,04) даже после удаления из расчета спортсмена с высоким числом инфекций (n=7). Статистически значимых корреляций других переменных величин не было (табл. 3). Хотя соот Пловчихи Общий IgA, Низкий IgA2, n ПНВ,n ношение IgA1:IgA2 имело тенденцию быть ниже у пловцов без эпизодов инфекции в течение 7-месячного тренировочного сезона (табл. 4), не было статистически значимых различий в образцах ранней и поздней фазы, взятых у спортсменов, у которых не было инфекций, в сравнении со спортсменами, у которых был, по меньшей мере, один эпизод инфекции. Таблица 3 Образец ранней Образец поздней фазы тренировки фазы тренировки Коэффициент корреляции по Спирману (Rho) и статистическая значимость корреляции между числом инфекций по каждому пловцу и величинами концентрации или соотношениями общего IgA,IgA1 и IgA2 в образцах слюны на ранней и поздней фазе тренировки. Тренировка Ранний образец Поздний образец Всего Отсутствие эпизодов инфекции Соотношение IgA1:IgA2 Медиана и диапазон соотношений концентраций IgA1:IgA2 в образцах слюны, взятых на ранней и поздних фазах тренировки у пловцов без инфекций, в сравнении с пловцами, у которых была, по меньшей мере, одна инфекция в течение 7-месячного тренировочного сезона. Величина р представляет различия между здоровыми и склонными к инфекции пловцами. Результаты этого исследования профессиональных пловцов показывают, что снижение концентрации IgA1 ниже 25 мг/л (фиг. 2) в слюне, взятой при 7-месячной тренировочном сезоне, было избирательно связано с более высоким риском эпизодов инфекции дыхательных путей в течение сезона. Предыдущее исследование респираторных инфекций у профессиональных пловцов выявило,что предсезонные концентрации общего IgA ниже 35 мг/л были связаны с высоким числом эпизодов инфекции (16). В данном исследовании образцы слюны были взяты в начале тренировочного сезона,но не перед началом тренировочного сезона.IgA1 представлял приблизительно 80% от концентрации общего IgA в этой группе профессиональных пловцов. В исследованиях здоровых, не переносящих физическую нагрузку взрослых лиц пропорция IgAl в слюне составляет приблизительно 60% (4,7-8). IgA1 антитела, главным образом, продуцируются в ответ на белковые антигены, в то время как IgA2 антитела индуцируются углеводородами и содержащими липиды антигенами (1). Тот факт, чтоIgA1 протеазы, продуцируемые большинством патогенов слизистых оболочек, могут вызывать распадIgA1 антител, в то время как IgA2 антитела защищены (1), имеет значение при рассмотрении устойчивости к инфекциям на поверхностях слизистых оболочек. Поскольку IgA1 более восприимчив к протеазам, продуцируемым патогенами слизистых оболочек (1), более высокая пропорция IgA1 и изредка встречающиеся невыявляемые уровни IgA2 у этой группы профессиональных пловцов может способствовать увеличению у них риска инфекций слизистых оболочек. Несмотря на небольшую пропорцию образцов, имеющих величины концентрации IgA2 ниже предела выявления количественного анализа,не было связи между концентрацией IgA2 или соотношений подклассов и частотой инфекции. Поскольку элитные пловцы в данном исследова-нии соревновались и тренировались в течение несколь-ких лет, возможно, что уровни IgA1 в образцах слюны, взятых на ранней фазе тренировочного сезона, представляют кумулятивный эффект за годы тренировки вызванного физической нагрузкой подавления IgA1. По меньшей мере, одна инфекция Соотношение IgA1:IgA2 Статистическая значимость Величина р 0,25 0,84 0,24 Второе исследование Тихоокеанский чемпионат (плавание) проводился в Сиднее, Австралия, с 22.08.99 г. по 29.08.99 г. Дальнейшие соревнования проводились в Канберре,Австралия, на следующей неделе с 01.09.99 г. по 05.09.99 г. Данные об уровне IgA и инфекции у пловцов собирали во время подготовительной тренировочной фазы и во время этих соревнований. Пример 6. Определения. Инфекцию определяли как да/нет между определенными точками времени сбора данных(табл. 5) после каждого взятия слюны (фиг. 3). Таблица 5 Время Периоды сбора данных об инфекции 1 23.04.99-15.09.99 2 31.07.99-08.08.99 3 09.08.99-29.08.99 4 30.08.99-05.09.99 5 23.04.99-30.07.99 6 31.07.99-30.08.99 Примечание: Эпизоды инфекции не регистрировали в течение 10 недель с 15.05.99 г. по 30.07.99 г. В четырех случаях слюну брали без стимуляции,не натощак и перед физической нагрузкой (табл. 6). Таблица 6 Тренировочная группа Золотое побережье Брисбэйн Мельбурн Сидней Время 1 Сравнение уровней иммуноглобулина в слюне 20.04.99 г. между субъектами без инфекции и субъектами с инфекцией в течение периода с 23.04.99 г. по 15.05.99 г. Время 2 Сравнение уровней иммуноглобулина в слюне 31.07.99 г. между субъектами без инфекции и субъектами с инфекцией в течение периода с 31.07.99 г. по 09.08.99 г. Время 4 Сравнение уровней иммуноглобулина в слюне 29.08.99 г. между субъектами без инфекции и субъектами с инфекцией в течение периода с 30.08.99 г. по 05.09.99 г. Таблица 9 Время 3 Сравнение уровней иммуноглобулина в слюне 09.08.99 г. между субъектами без инфекции и субъектами с инфекцией в течение периода с 09.08.99 г. по 30.08.99 г. Таблица 11 Время 5 Сравнение уровней иммуноглобулина в слюне 20.04.99 г. между субъектами без инфекции и субъектами с инфекцией в течение периода с 23.04.99 г. по 30.08.99 г. Время 6 Сравнение уровней иммуноглобулина в слюне 31.07.99 г. между субъектами без инфекции и субъектами с инфекцией в течение периода с 31.07.99 г. по 30.08.99 г. Период регистрации инфекции 23.04.99 г.-15.05.99 г. 23.04.99 г.-30.08.99 г. Эти данные свидетельствуют о том, что концентрация IgA в слюне раннего тренировочного лагерного сезона является самым лучшим прогностическим показателем возникающей позднее инфекции (инфекций) во время тренировок непосредственно перед основными соревнованиями. Медиана концентрации у пловцов, не сообщавших о респираторной инфекции верхних дыхательных путей после каждой точки времени, снизилась в течение 4-х месячного периода(с 63,5 до 44,1 мг/л), в то время как у пловцов с инфекциями выявлено небольшое изменение (с 32,7 до 37,3 мг/л) (фиг. 4). Это свидетельствует о том, что у пловцов, которые восприимчивы к инфекциям, уровень IgA в слюне может быть уже ниже критического в начале сезона, и у них мало запаса возможности для дальнейшего снижения по мере тренировки. Увеличение содержания IgA в образцах слюны, взятых 09.08.99 г., может происходить вследствие того, что после этого взятия слюны не было вспышки желудочно-кишечных заболеваний в тренировочном лагере, что может отражать стимуляцию слизистой оболочки при возросшем уровне IgA в слюне, даже перед возникновением симптомов желудочно-кишечной инфекции. Третье исследование Это исследование случая представляет данные по применению мониторинга иммуноглобулина в слюне при ведении одного профессионального спортсмена-байдарочника, который 14 Число субъектов в исследовании варьировало в каждую точку времени (см. выше) вследствие недоступности субъектов в день взятия слюны, или исключения образцов по различным причинам после анализа, или недоступности регистрации эпизодов инфекции. Не было связи между IgG, IgM или альбумином в слюне и инфекцией в любой из изученных точек времени. Была тенденция у пловцов с инфекцией иметь более низкую концентрацию IgA в слюне,чем у пловцов без инфекции (табл. с 7 по 12), и в двух точках времени концентрации IgA в слюне перед физической нагрузкой были статистически значимо ниже у пловцов с инфекцией был склонен к рецидивирующему, ослабляющему респираторному заболеванию, которое помешало тренировке и подготовке к соревнованиям. Пример 7. Анамнез заболевания Мужчина, профессиональный спортсмен в возрасте 25 лет, участвовал в соревнованиях на международном уровне в течение 10 лет. За 5 лет до данного исследования он был инфицирован вирусом Эпштейна-Барра (EBV) с последующими двумя эпизодами заболевания верхних дыхательных путей (ЗВДП). За прошедшие годы среднее число ЭВДП возросло до 5-6 эпизодов в год и было связано с усталостью. Медицинское обследование исключило все признанные клинические причины рецидивирующего заболевания и связанной с ним усталости. Структура исследования Образцы слюны спортсмен брал стандартизированным способом (27) не натощак и без стимуляции до и еще непосредственно после каждого цикла физической нагрузки в течение 14-дневного периода. С помощью иммуноферментого анализа (ELISA) в стационаре измеряли концентрацию IgA, IgG и IgM, а концентрацию альбумина измеряли нефелометрией с использованием анализатора Beckman ARRAY (Beckman. Brae, CA). Спортсмен использовал программу PEATS (24), адаптацию способа, описанного Sharp (27), для расчета интенсивности каждого цикла физической нагрузки. 15 Статистические методы Для сравнения величин белка перед и после цикла физической нагрузки использовали ранговый критерий Вилкоксона для парных данных. Для сравнения величин между двумя отобранными периодами времени использовалиU критерий Манна-Уитни. Для оценки связи между величинами белка и днем тренировки и временем дня цикла использовали коэффициенты корреляции по Спирману. Иммуноглобулины и альбумин в слюне Величины концентрации белка в слюне были в среднем выше в образцах в цикл перед физической нагрузкой, в сравнении с образцами в цикл после физической нагрузки (фиг. 5). Медианы различий были статистически значимы(табл. 14). Величины концентрации IgA в слюне значительно упали в течение двухнедельного исследования (коэффициент корреляции (rs)=-0,55,р=0,0002) и для величин концентрации перед физической нагрузкой (rs=-0,61, р=0,003), и после физической нагрузки (rs=-0,52, р=0,02). Со временем не было статистически значимых изменений других белков в слюне. Величина изменения за цикл (уровень до физической нагрузки минус уровень после физической нагрузки) для величин концентрации IgA в слюне также статистически значимо снизились со временем (rs=-0,56, р=0,01), но это не было статистически значимо для других белков слюны. Величина изменения в течение цикла величин концентрации IgA в слюне, но не других белков, положительно коррелировала с интенсивностью цикла физической нагрузки (rs=0,53,р=0,02). Интенсивность каждого цикла физической нагрузки в течение двухнедельного периода исследования уменьшалась (rs=-0,45, р=0,03) и была значительно выше (р=0,05) в первые 4 дня (медиана в баллах=165, диапазон=80-217), в сравнении с последующими 10 днями тренировки (медиана в баллах=110, диапазон=56-185). Величины концентрации IgA в образцах и перед физической нагрузкой, и после физической нагрузки были статистически значимо выше (р=0,009) в течение первых 4 дней (медиана=164 мг/л, диапазон=28-228 мг/л) в сравнении с последними 10 днями (медиана=51 мг/л, диапазон=30-72 мг/л). Величина изменения концентрации IgA в слюне за цикл статистически значимо выше(р=0,02) в первые 4 дня (медиана=115 мг/л, диапазон=-44-137 мг/л) в сравнении со следующими 10 днями (медиана=20 мг/л, диапазон=-30-47 мг/л), будучи почти в 6 раз выше. Это было вы 003104 16 звано, главным образом, падением концентрации IgA в слюне перед циклом физической нагрузки в течение четвертого дня тренировки и отсутствием последующего восстановления(фиг. 5). В течение некоторых дней тренировки были предприняты множественные циклы физической нагрузки. Среднее восстановление в процентах исходной величины IgA в течение первых 3 дней составило 74% (фиг. 6). На четвертый день восстановление за второй цикл физической нагрузки составило только 20%. Как только исходные величины концентрации IgA падали ниже 50 мг/л (8-13 дни) концентрацияIgA проявляла небольшое изменение при дополнительной тренировке в течение дня (фиг. 5 и 6). Обсуждение Адекватный уровень иммунной защиты на поверхностях слизистых оболочек важен для устойчивости к инфекции (23). Низкие уровниIgA в слюне были связаны с риском инфекции верхних дыхательных путей у групп профессиональных спортсменов (16, 26, 18, 28). Мониторинг каждого эпизода тренировки в этом исследовании случаев позволило выявить точный цикл физической нагрузки, который привел к статистически значимому подавлению концентрации IgA в слюне без последующего восстановления (четвертый день). Важным было выявление связи между ранней высокоинтенсивной физической нагрузкой и величиной последующего иммунного подавления слизистых оболочек, отражаемого более низкими уровнямиIgA в слюне после периода интенсивной физической нагрузки. Данное исследование подчеркивает выгоду для спортсмена и тренера быстрого получения результатов анализов исследования концентрации IgA в слюне. Без преимущества знания о подавлении иммунитета слизистых оболочек спортсмен продолжал интенсивные тренировки до тех пор, пока не наступало ограничение в виде еще одного эпизода респираторного заболевания. У отдельных спортсменов, которые склонны к инфекции или у которых происходило снижение физических возможностей, обширный мониторинг тренировочной программы спортсмена может помочь выявить факторы тренировки, которые способствуют подавлению иммунитета слизистых оболочек и потенциальному риску инфекции. Таблица 14 Медиана и диапазон и различие медиан концентрации иммуноглобулинов и альбумина в слюне (мг/л) при циклах перед тренировкой и после тренировки в течение двухнедельного исследования Белок слюны Перед тренировкой После тренировки Различие по циклам Статистическая значимость Медиана, Диапазон, Медиана, Диапазон,Различие медиан Величина р мг/л мг/л мг/л мг/л мг/л 95% ДИ Хотя изобретение было описано со ссылкой на определенные примеры, специалистам в данной области будет понятно, что изобретение может быть реализовано во многих других формах. Библиография 1. Brandtzaeg P. Humoral immune responseJ Appl Physiol 1990; 60:61-64. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ оценки потенциальной восприимчивости к инфекции у субъекта, подвержен 19 ного воздействию фактора или факторов стресса, включающий(a) определение уровня иммуноглобулина А (IgA) у субъекта на фазе тренировки и(b) прогноз восприимчивости субъекта к инфекции сравнением уровня IgA на фазе тренировки с заданной пороговой величиной. 2. Способ оценки потенциальной восприимчивости к инфекции у субъекта, подверженного воздействию фактора или факторов стресса, включающий(b) прогноз восприимчивости субъекта к инфекции сравнением уровня IgA1 с заданной пороговой величиной. 3. Способ по п.1 или 2, в котором уровень иммуноглобулина определяется на ранней фазе тренировки. 4. Способ по любому из пп.1-3, в котором инфекция представляет собой инфекцию слизистой оболочки. 5. Способ по п.4, в котором инфекция представляет собой респираторную инфекцию. 6. Способ по любому из пп.1-5, в котором пороговая величина представляет собой пороговую величину у здоровой популяции. 7. Способ по любому из пп.1-5, в котором пороговая величина представляет собой внутреннюю личную пороговую величину. 8. Способ по любому из пп.1-7, в котором иммуноглобулин представляет собой секреторный иммуноглобулин. 9. Способ по п.8, в котором секреторный иммуноглобулин представляет собой иммуноглобулин слюны. 10. Способ по п.9, в котором иммуноглобулин слюны получен из образца цельной, не стимулированной слюны. 11. Способ по п.10, в котором у субъекта слюна берется не натощак. 12. Способ по любому из пп.1-11, в котором субъект представляет собой спортсмена. 13. Способ по п.12, в котором спортсмен является профессиональным пловцом. 14. Способ по любому из пп.1-13, в котором фактор стресса достоверно влияет на эффективность иммунной системы. 15. Способ по любому из пп.1-13, в котором субъект подвержен воздействию физического и/или психологического фактора стресса. 16. Способ по п.15, в котором физический и/или психологический фактор стресса представляет собой длительную физическую тренировку или избыточную тренировку. 17. Способ по любому из пп.1-16, в котором уровень иммуноглобулина определяется радиальной иммунодиффузией. 18. Способ по любому из пп.1-16, в котором уровень иммуноглобулина определяется иммуноферментным анализом. 20 19. Способ по любому из пп.1-18, в котором уровень иммуноглобулина определяется быстрым количественным анализом около субъекта. 20. Способ по любому из пп.1-19, в котором анализ слюны на содержание иммуноглобулина производится in situ контактированием устройства или системы для анализа со слюной субъекта. 21. Способ по любому из пп.1-20, в котором количественный анализ представляет собой самостоятельный тест, выполняемый субъектом. 22. Способ мониторинга динамики состояния субъекта после инвазивного лечения, включающий(b) мониторинг динамики состояния субъекта сравнением указанного уровня IgA1 с заданной пороговой величиной. 23. Способ по п.22, в котором уровеньIgA1 оценивается в образце слюны субъекта. 24. Способ оценки воздействия фактора или факторов стресса на определенные здесь функциональную способность и/или степень усталости, включающий(b) оценку воздействия фактора или факторов стресса на функциональную способность и/или степень усталости субъекта сравнением указанного уровня IgA1 с заданной пороговой величиной. 25. Способ по п.24, в котором субъект представляет собой спортсмена. 26. Способ по п.25, в котором спортсмен представляет собой профессионального пловца. 27. Способ оценки потенциальной восприимчивости к респираторной инфекции у профессионального пловца, включающийA (IgA) в слюне пловца на ранней фазе тренировки и(b) прогноз потенциальной восприимчивости пловца к респираторной инфекции сравнением уровня IgA на ранней фазе тренировки с заданной пороговой величиной. 28. Способ оценки потенциальной восприимчивости к респираторной инфекции у профессионального пловца, включающий(a) определение уровня иммуноглобулина А 1 (IgA1) в слюне пловца на ранней фазе тренировки и(b) прогноз потенциальной восприимчивости пловца к респираторной инфекции сравнением уровня IgA1 на ранней фазе тренировки с заданной пороговой величиной. 29. Способ по п.28, в котором пороговая величина представляет собой пороговую величину у здоровой популяции. 30. Способ по п.28, в котором пороговая величина представляет собой внутреннюю личную пороговую величину. 21 31. Способ оценки потенциальной восприимчивости субъекта к инфекции, включающий(a) определение уровня иммуноглобулина А (IgA) у субъекта после воздействия фактора или факторов стресса;(c) определение уровня IgA у субъекта после периода восстановления;(d) прогноз потенциальной восприимчивости субъекта к инфекции сравнением уровняIgA на указанном выше этапе (а) с уровнем IgA на указанном выше этапе (с). 32. Способ оценки потенциальной восприимчивости субъекта к инфекции, включающийA1 (IgA1) у субъекта после воздействия фактора или факторов стресса;(c) определение уровня IgA1 у субъекта после периода восстановления;(d) прогноз потенциальной восприимчивости субъекта к инфекции сравнением уровняIgA1 на указанном выше этапе (а) с уровнемIgA1 на указанном выше этапе (с). 33. Способ по п.31 или 32, в котором инфекция представляет собой инфекцию слизистой оболочки. 34. Способ по п.33, в котором инфекция представляет собой респираторную инфекцию. 35. Способ по любому из пп.31-34, в котором иммуноглобулин представляет собой секреторный иммуноглобулин. 36. Способ по п.35, в котором секреторный иммуноглобулин представляет собой иммуноглобулин слюны. 22 37. Способ по п.36, в котором иммуноглобулин слюны получен из образца цельной, не стимулированной слюны. 38. Способ по п.37, в котором у субъекта слюна берется не натощак. 39. Способ по любому из пп.31-38, в котором субъект представляет собой спортсмена. 40. Способ по п.39, в котором спортсмен является профессиональным пловцом. 41. Способ по любому из пп.31-40, в котором фактор стресса достоверно влияет на эффективность иммунной системы. 42. Способ по любому из пп.31-40, в котором субъект подвержен воздействию физического и/или психологического фактора стресса. 43. Способ по п.42, в котором физический и/или психологический фактор стресса представляет собой длительную физическую тренировку или избыточную тренировку. 44. Способ по любому из пп.31-43, в котором уровень иммуноглобулина определяется радиальной иммунодиффузией. 45. Способ по любому из пп.31-43, в котором уровень иммуноглобулина определяется иммуноферментным анализом. 46. Способ по любому из пп.31-45, в котором уровень иммуноглобулина определяется быстрым количественным анализом около субъекта. 47. Способ по любому из пп.31-46, в котором анализ слюны на содержание иммуноглобулина производится in situ контактированием устройства или системы для анализа со слюной субъекта. 48. Способ по любому из пп.31-47, в котором количественный анализ представляет собой самостоятельный тест, выполняемый субъектом. Исследование IgA в слюне/инфекция Точки времени данных по инфекциям Медиана концентрации IgA в слюне перед физической нагрузкой для пловцов
МПК / Метки
МПК: G01N 33/68
Метки: инфекции, связанная, другим, физическими, интенсивными, стрессом, предрасположенность, упражнениями
Код ссылки
<a href="https://eas.patents.su/13-3104-predraspolozhennost-k-infekcii-svyazannaya-s-intensivnymi-fizicheskimi-uprazhneniyami-ili-drugim-stressom.html" rel="bookmark" title="База патентов Евразийского Союза">Предрасположенность к инфекции, связанная с интенсивными физическими упражнениями или другим стрессом</a>
Предыдущий патент: Винтовая крышка с прокладочной шайбой
Следующий патент: Многоосная турбина (варианты)
Случайный патент: Никелевый катализатор, способ получения катализатора и способ селективного гидрирования