Способ лечения заболеваний, связанных с фактором роста сосудистого эндотелия
Номер патента: 1779
Опубликовано: 27.08.2001
Авторы: Виньяти Луис, Вэйс Дуглас Кирк, Аиелло Ллойд П., Кинг Джордж Л., Джироусек Майкл Р.
Формула / Реферат
1. Способ лечения неоплазии, который включает введение нуждающемуся в таком лечении млекопитающему терапевтически эффективного количества (S)-3,4-[N,N'-1,1'-((2''-этокси)-3'''-(O)-4'''-(N,N-диметиламино)бутан)-бис-(3,3'-индолил)]-1(Н)-пиррол-2,5-диона или его фармацевтически приемлемой соли.
2. Способ по п.1, отличающийся тем, что неоплазия выбрана из группы, состоящей из капиллярной гемангиобластомы, рака молочной железы, саркомы Капоши, глиобластомы, ангиоматозных заболеваний, гемангиомы младенческого возраста, рака толстой и прямой кишки, медуллобластомы, карциномы желудка, аденокарцином желудочно-кишечного тракта, злокачественной меланомы, рака яичников, не мелкоклеточного рака легких, рака предстательной железы, злокачественных выпотов, отека вокруг опухолей, карциномы мочевого пузыря, синдрома von Hippel Lindau, почечно-клеточной карциномы, рака кожи, злокачественных заболеваний щитовидной железы, рака шейки матки, печеночно-клеточной карциномы, рабдомиосаркомы и лейкомиосаркомы.
3. Способ по п.1, отличающийся тем, что неоплазия выбрана из группы, состоящей из капиллярной гемангиобластомы, рака молочной железы, саркомы Капоши, глиобластомы, ангиоматозных заболеваний, гемангиомы младенческого возраста, рака толстой и прямой кишки, злокачественной меланомы, рака яичников, не мелкоклеточного рака легких, рака предстательной железы, злокачественных выпотов, отека вокруг опухолей, карциномы мочевого пузыря.
4. Способ лечения ревматоидного артрита, включающий введение нуждающемуся в таком лечении млекопитающему терапевтически эффективного количества (S)-3,4-[N,N'-1,1''-(2''-этокси)-3'''-(O)-4'''-(N,N-диметиламино)бутан)-бис-(3,3'-индолил)]-1(Н)-пиррол-2,5-диона или его фармацевтически приемлемой соли.
5. Способ лечения отека легких, включающий введение нуждающемуся в таком лечении млекопитающему терапевтически эффективного количества (S)-3,4-[N,N'-1,1'-(2''-этокси)-3'''-(O)-4'''-(N,N-диметиламино)бутан)-бис-(3,3'-индолил]-1(Н)-пиррол-2,5-диона или его фармацевтически приемлемой соли.
6. Способ ингибирования капиллярной проницаемости, стимулированной фактором роста сосудистого эндотелия, связанной с отеком лёгких, включающий введение нуждающемуся в таком лечении млекопитающему терапевтически эффективного количества (S)-3,4-[N,N'-1,1'-(2''-этокси)-3'''-(O)-4'''-(N,N-диметиламино)бутан)-бис-(3,3'-индолил)]-1(Н)-пиррол-2,5-диона или его фармацевтически приемлемой соли.
7. Способ лечения келоида, включающий введение нуждающемуся в таком лечении млекопитающему терапевтически эффективного количества (S)-3,4-[N,N'-1,1'-(2''-этокси)-3'''-(O)-4'''-(N,N-диметиламино)бутан)-бис-(3,3'-индолил)]-1(Н)-пиррол-2,5-диона или его фармацевтически приемлемой соли.
8. Способ лечения запястного синдрома, включающий введение нуждающемуся в лечении млекопитающему терапевтически эффективного количества (S)-3,4-[N,N'-1,1'-(2''-этокси)-3'''-(O)-4'''-(N,N-диметиламино)бутан)-бис-(3,3'-индолил)]-1(Н)-пиррол-2,5-диона или его фармацевтически приемлемой соли.
Текст
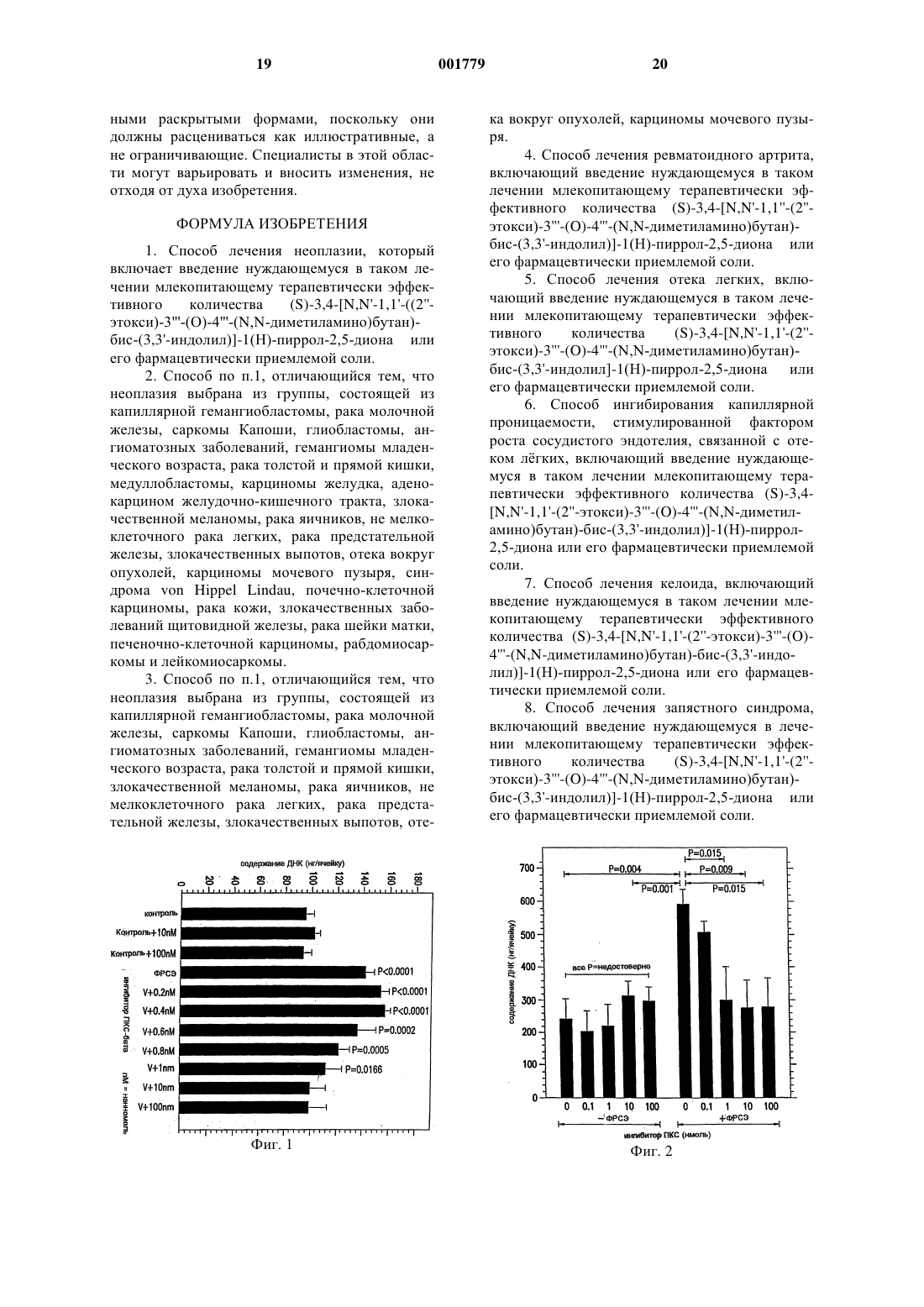
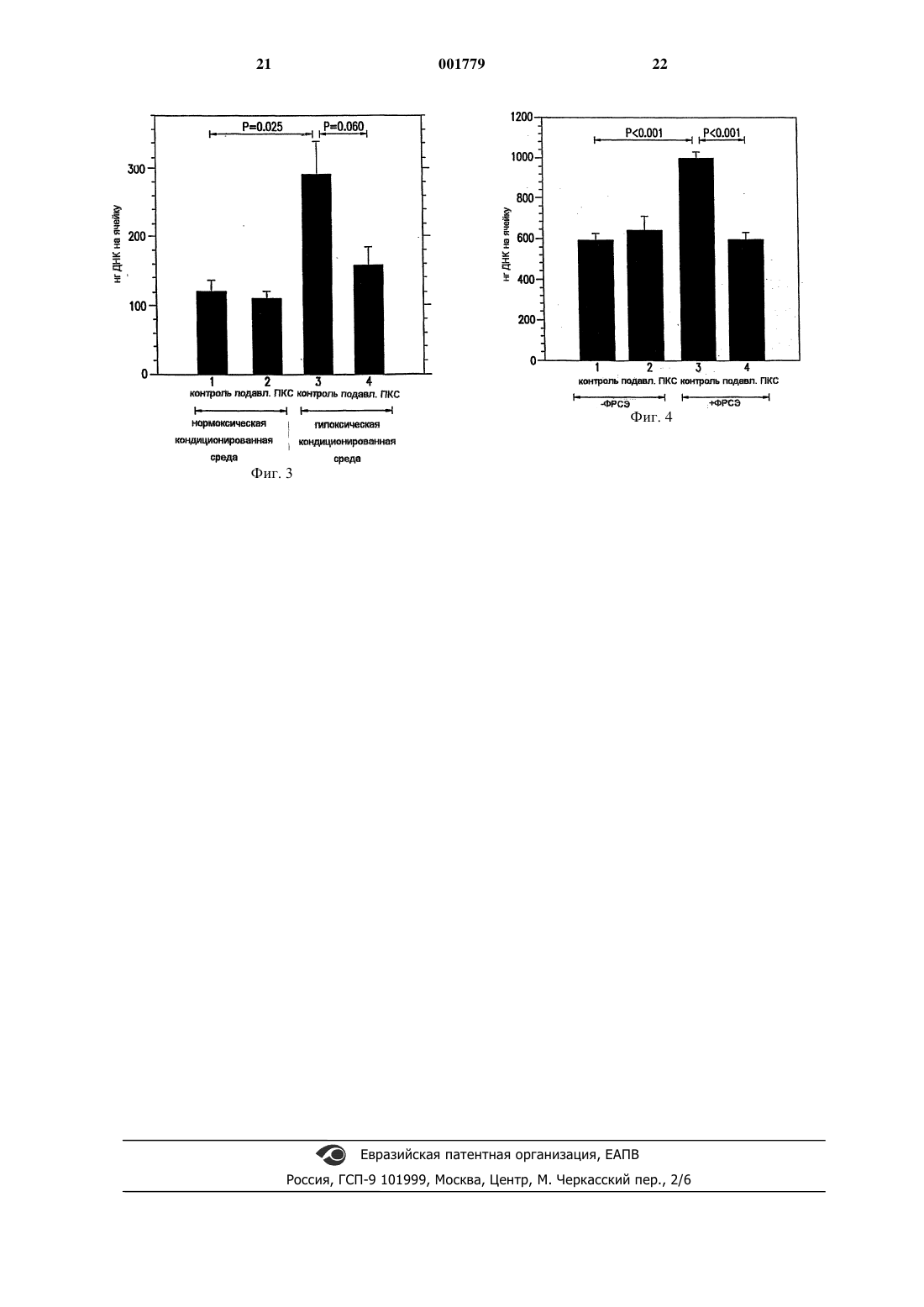
1 Предпосылки изобретения Область изобретения Настоящее изобретение относится к способу подавления роста эндотелиальных клеток и капиллярной проницаемости, связанных с фактором роста сосудистого эндотелия (ФРСЭ),например, возросшего клеточного роста и проницаемости, вызванных (ФРСЭ) с использованием ингибитора изоферментапротеинкиназы С (ПКС). Состояние, вызванное ФРСЭ, тесно связано с новообразованиями у млекопитающих и другими заболеваниями, включая отек легких. Настоящее изобретение, в частности, относится к применению ингибитора изоферментапротеинкиназы С (ПКС) для лечения опухолевых заболеваний, включая капиллярную гемангиобластому, рак молочной железы, саркому Капоши, глиобластому, ангиоматозные заболевания, рак толстой и прямой кишки, медуллобластому, карциному желудка, аденокарциномы желудочно-кишечного тракта, злокачественную меланому, рак яичников, немелкоклеточный рак легких, рак предстательной железы, злокачественные выпоты, отек вокруг опухоли, например,внутримозговой отек и кисты, связанные с опухолью мозга, карциному мочевого пузыря, синдром von Hippel Lindau, почечно-клеточную карциному, рак кожи, злокачественные заболевания щитовидной железы, рак шейки матки,печеночно-клеточную карциному, рабдомиоскаркому и лейомиосаркому и родственных заболеваний, связанные с ФРСЭ. Описание предшествующего уровня техники ФСП/ФРСЭ представляет собой гликолизированный, многофункциональный цитокин. Избыточная экспрессия ФСП/ФРСЭ связана с неоплазией и несколькими другими патологическими состояниями. ФСП/ФРСЭ вызывает пролиферацию эндотелиальных клеток, избыточную проницаемость посредством активации транспорта, опосредованного пузырьково-вакуолярными органеллами, миграции и реорганизации актина с изменениями формы и ундуляцией. Он изменяет экспрессию гена эндотелиальной клетки, вызывая повышенную выработку тканевого фактора и нескольких протеаз, включая интерстициальную коллагеназу и как урокиназоподобного активатора, так и активатора тканевого плазминогена. Большинство этих генов индуцированы активацией ПКС, стимулированной форбол миристат ацетатом (ФМА). ФСП/ФРСЭ обильно экспрессирован и секретируется большинством исследованных к настоящему времени опухолей человека и животных. ФСП/ФРСЭ может непосредственно воздействовать на опухолевые клетки, например, опухолевые клетки глиобластомы, а также играть важную роль в индуцировании опухолевого ангиогенеза (Claffey et al. Cancer Research 56, 172-181 (1996) и приведенные там ссылки). 2 Ангиогенный потенциал ФРСЭ вероятно,усиливается синергической активностью фактора роста фибробластов, высвобождаемого вследствие разрыва или гибели клеток [Pepper et(1992); Muthukrishman et al., J. Cell Physiol.,148:1-16 (1991)]. Рост и метастазирование опухолей тесно связаны с усиленной экспрессией ФРСЭ. Химический сигнал от опухолевых клеток может произвести сдвиг покоящихся эндотелиальных клеток в фазу быстрого роста. Из двенадцати известных ангиогенных белков, наиболее часто обнаруживаемыми в опухолях, представляются основной фактор роста фибробластов (ОФРФ) и фактор роста сосудистого эндотелия (ФРСЭ),известный также как фактор сосудистой проницаемости (ФСП) [Folkman, J. New England J. ofMedicine., Vol 999 (26):1757-1763 (1995) и приведенные в ней ссылки]. Осознание того, что рост опухоли требует новых кровеносных сосудов, и выявление химических факторов, которые опосредуют неоваскуляризацию или ангиогенез, расширили понимание патологических процессов и открыли новые пути к лечению этих заболеваний. В настоящее время на 1 или 2 фазах клинических испытаний исследуются девять различных ингибиторов ангиогенеза для лечения широкого спектра твердых опухолей, включая рак молочной железы, толстой кишки, легких и предстательной железы, а также саркому КапошиSaunders, 1995:206-232). Один из этих препаратов. TNP-170, синтетический аналог фумагиллина (Denekamp J., Br J Radiol 66:181-196, 1993) был одобрен FDA для 1 фазы исследования у многих пациентов с твердыми опухолями. Другие ингибиторы ангиогенеза, клинические испытания которых проводятся в настоящее время у пациентов с запущенным раком, включают тромбоцитарный фактор 4; карбоксиаминотриазол; ВВ-94 и ВВ-2516; ингибиторы металлопротеиназы; сульфатированный полисахарид текогалан (DS-152); талидомид, интерлейкин-12 и линомид (Flier et al., The New England Journal ofMedicine, vol 333 pp 1757-1763, 1995 и приведенные в ней ссылки). Ингибиторы ПКС также были предложены для лечения рака (см. патент США 5 552 396). Однако эффективность ингибиторов изоферментаПКС при определенных опухолевых заболеваниях была неизвестна. Учитывая роль,которую ФРСЭ играет при определенных опухолевых и других заболеваниях, необходимо выявить дополнительные препараты, особо нацеленные на функцию ФРСЭ. Сущность изобретения Целью изобретения является предоставление способа лечения новообразований. 3 Еще одной целью изобретения является предоставление способа лечения ревматоидного артрита. Еще одной целью изобретения является предоставление способа лечения келоида. Еще одной целью изобретения является предоставление способа лечения состояний,связанных с отеком легких, таких как респираторный дистресс-синдром у взрослых (РДСВ). Еще одной целью изобретения является предоставление способа лечения запястного синдрома. Эти и другие цели изобретения обеспечиваются с помощью одного или более описанных ниже вариантов реализации. В одном варианте реализации изобретения предоставляется способ лечения неоплазии, который включает введение указанному млекопитающему терапевтически эффективного количества ингибитора изоферментапротеинкиназы С. Еще в одном варианте реализации изобретения предоставляется способ лечения ревматоидного артрита, который включает введение указанному млекопитающему терапевтически эффективного количества ингибитора изоферментапротеинкиназы С. В другом варианте реализации изобретения предоставляется способ лечения келоидных рубцов, который включает введение указанному млекопитающему терапевтически эффективного количества ингибитора изоферментапротеинкиназы С. Еще в одном варианте реализации изобретения предоставляется способ лечения отека легких, который включает введение указанному млекопитающему терапевтически эффективного количества ингибитора изоферментапротеинкиназы С. Настоящее изобретение предоставляет способ с указанием соединений, которые являются профилактическими и эффективными в лечении неоплазии и других заболеваний, связанных с фактором роста сосудистого эндотелия(ФРСЭ). Краткое описание фигур На фиг. 1 показано подавляющее действие ингибитора ПКС, (S)-3,4-[N,N'-1,1'-2-этoкcи)3(O)-4-(N,N-димeтилaминo)-бутан)-бис-(3,3'индолил)]-1(Н)-пиррол-2,5-диона, на рост клеток эндотелия, стимулированных рекомбинантным ФРСЭ человека; на фиг. 2 дополнительно показано подавляющее действие ингибитора ПКС, (S)-3,4[N,N'-1,1'-2"-этокси-3(О)-4-(N,N-диметиламино)-бутан)-бис-(3,3'-индолил)]-1(Н)-пиррол 2,5-диона на рост клеток эндотелия, стимулированный рекомбинантным ФРСЭ человека; на фиг. 3 показано воздействие ингибитора ПКС на активность эндогенного ФРСЭ, экс 001779 4 прессируемого после культивирования перицитов сетчатки в условиях гипоксии; на фиг. 4 дополнительно показано подавляющее влияние ингибитора ПКС на рост клеток эндотелия, стимулированный рекомбинантным ФРСЭ человека. Подробное описание изобретения Открытием настоящего изобретения является то, что терапевтическое применение определенного класса ингибиторов протеинкиназы С, а именно, ингибиторов изоферментапротеинкиназы С и, особенно, избирательных ингибиторов изоферментапротеинкиназы С,противодействует воздействиям ФРСЭ. В частности, открытием настоящего изобретения является то, что применение этого определенного класса ингибиторов протеинкиназы С противодействует росту клеток эндотелия и капиллярной проницаемости, особенно, росту клеток эндотелия и капиллярной проницаемости, стимулированным фактором роста ФРСЭ. Следовательно, такие соединения могут применяться терапевтически для лечения заболеваний, связанных с ФРСЭ, таких как новообразования и другие патологические состояния, которые связаны с ФРСЭ. В способе этого изобретения предпочтительно используются те ингибиторы протеинкиназы С, которые эффективно подавляют изофермент . Одна подходящая группа соединений в целом описана в предшествующем уровне техники как бис-индолилмалеимиды или макроциклические бис-индолилмалеимиды. Бисиндолилмалеимиды, хорошо известные в предшествующем уровне техники, включают соединения, которые описаны в патентах США 5621098, 5552396, 5545636, 5481003, 5491242 и 5057614, и все включены сюда в виде ссылки. Макроциклические бис-индолилмалеимиды, в частности, представлены соединениями формулы I. Эти соединения и способы их получения были раскрыты в патенте США 5 552 396, который включен сюда в виде ссылки. Эти соединения вводятся в терапевтически эффективном количестве млекопитающему для подавления роста клеток эндотелия и капиллярной проницаемости, связанных с ФРСЭ, для подавления воздействий ФРСЭ, связанных с новообразованиями и другими патологическими состояниями, такими как ревматоидный артрит, келоид,синдром канала запястья и отека легких. Эти соединения можно также вводить пациентам с риском упомянутых выше патологических состояний в качестве профилактических средств. Предпочтительным соединением для применения в способе изобретения является (S)-3,4[N,N'-1,1'-2"-этокси)-3-(O)-4-(N,N-диметиламино)бутан)-бис-(3,3'-индолил)]-1(Н)-пиррол 2,5-диона или его фармацевтически приемлемая соль. 5 Кислоты, обычно используемые для образования таких солей, включают неорганические кислоты, такие как хлористо-водородная, бромисто-водородная, иодисто-водородная, серная и фосфорная кислота, а также органические кислоты, такие как паратолуолсульфоновая, метансульфоновая, щавелевая, парабромфенилсульфоновая, карбоновая, янтарная, лимонная,бензойная, уксусная кислота и родственные неорганические и органические кислоты. Такие фармацевтически приемлемые соли, таким образом, включают сульфат, пиросульфат, бисульфат, сульфит, бисульфит, фосфат, моногидрофосфат, дигидрофосфат, метафосфат, пирофосфат, хлорид, бромид, иодид, ацетат, пропионат, деканоат, каприлат, акрилат, формат, изобутират, гептаноат, пропиолат, оксалат, малонат, сукцинат, суберат, себакат, фумарат, малеат, 2-бутин-1,4-диоат, 3-гексин-2,5-диоат, бензоат, хлорбензоат, гидроксибензоат, метоксибензоат, фталат, ксилолсульфонат, фенилацетат,фенилпропионат, фенилбутират, цитрат, лактат,гиппурат, -гидроксибутират, гликолат, малеат,тартрат, метансульфонат, пропансульфонат,нафталин-1-сульфонат, нафталин-2-сульфонат,манделат и им подобные. Особенно применяются хлористо-водородная соль и мезилат. В дополнение к фармацевтически приемлемым солям могут также существовать другие соли. Они могут служить в качестве промежуточных продуктов при очистке соединений, при получении других солей или при идентификации и характеристике соединений промежуточных продуктов. Фармацевтически приемлемые соли вышеуказанного соединения могут также существовать в виде различных сольватов, таких как с водой, метанолом, этанолом, диметилформамидом, этилацетатом и им подобными. Могут также быть получены смеси таких сольватов. Источником такого сольвата может быть растворитель кристаллизации, растворитель получения или кристаллизации, или дополнительным к такому растворителю. Синтез различных производных бисиндол-N-малеимида описан в патенте США 5 057 614, выданном Davis et al., а синтез предпочтительного соединения, подходящего для использования в этом изобретении, описан в ранее указанном патенте США 5 552 396 и в публикации ЕР 0 657 411 Al, Faul et al., которые включены в описание в виде ссылок. Особенно предпочтительным ингибитором протеинкиназы С для использования в способе этого изобретения является соединение, описанное в примере 5g (хлористо-водородная соль(S)-3,4-[N,N'-1,1'-2"-этокси)-3(O)-4-(N,Nдиметиламино)бутан)-бис-(3,3'-индолил)]-1(Н)пиррол-2,5-диона), упомянутого выше патента США 5 552 396. Это соединение является мощным ингибитором протеинкиназы С. Оно более избирательно по отношению протеинкиназы С, 001779 6 в сравнении с другими киназами и является высоко избирательным к изоферменту, т.е. оно избирательно к бета-1 и бета-2 изоферментам. Пригодны также другие соли этого соединения,особенно, мезилатные соли. Предпочтительная мезилатная соль может быть получена с помощью вступления в реакцию соединения формулы II с метансульфоновой кислотой в нереакционном органическом растворителе, предпочтительно смеси органического растворителя и воды, и наиболее предпочтительно воды-ацетона. Могут применяться другие растворители, такие как метанол, ацетон, этилацетат и их смеси. Отношение растворителя к воде не имеет принципиального значения и в целом определяется растворимостью реагентов. Предпочтительные соотношения растворителя к воде в целом составляют отношение растворителя к воде от 0,1:1 до 100:1 по объему. Предпочтительно соотношение составляет от 1:1 до 20:1 и наиболее предпочтительно от 5:1 до 10:1. Оптимальное соотношение зависит от выбранного растворителя и представляет собой предпочтительно ацетон при соотношении растворителя к воде 9:1. В реакции обычно участвуют эквимолярные количества двух реагентов, хотя могут применяться другие соотношения, особенно те,при которых имеется избыток метансульфоновой кислоты. Скорость добавления метансульфоновой кислоты не имеет принципиального значения для реакции, и она может добавляться быстро (5 мин) или медленно в течение 6 ч или более. Реакция проводится при температурах в диапазоне от 0 С до температуры флегмы. Реакционная смесь перемешивается до завершения образования соли по данным рентгеновской дифракции порошка и может занимать от 5 мин до 12 ч. Соли настоящего изобретения предпочтительно и легко получаются в кристаллической форме. Тригидратную форму соли можно легко превратить в моногидрат после высушивания или воздействия относительной влажности от 20 до 60%. Соль является по существу кристаллической, проявляющей определенную точку плавления, двойное лучепреломление и характер рентгеновской дифракции. В целом, кристаллы имеют менее чем 10% аморфного твердого вещества, а предпочтительно менее чем 5% и наиболее предпочтительно менее чем 1% аморфного твердого вещества. 7 Мезилатная соль выделяется с помощью фильтрации или других признанных в этой области техники методик разделения непосредственно из реакционной смеси с выходом в диапазоне от 50 до 100%. При желании для дальнейшей очистки могут применяться повторная кристаллизация и другие методики очистки, известные в этой области техники. Эндотелиальные клетки в тканевой культуре, стимулированные фактором роста, таким как ФРСЭ, проявляют более высокую скорость роста, чем исходная скорость клеточного роста. Эксперименты, выполненные настоящем изобретении, показали, что при введении in vitro в концентрации приблизительно от 0,1 до 100 нмоль, ингибитор протеинкиназы С кислотная соль(S)-3,4-[N,N'-1,1'-2"-этокси)-3(O)-4(N,N-диметиламино)бутан)-бис-(3,3'-индолил)]1(Н)-пиррол-2,5-диона значительно подавляет рост небазальных клеток, стимулированный фактором роста (таким как ФРСЭ). Важно, что другие исследования показали,что рост нормальных эндотелиальных клеток в тканевой культуре не подавляется этим соединением, что показано отсутствием подавления роста эндотелиальных клеток без стимуляции ФРСЭ в нормоксических кондиционированных средах. В гипоксических кондиционированных средах скорость клеточного роста возрастает вследствие увеличения содержания эндогенного фактора роста, ФРСЭ, вырабатываемого гипоксическими клетками. И снова -изоферментный избирательный ингибитор протеинкиназы С,кислотная соль (S)-3,4-[N,N'-1,1'-2"-этокси)3(О)-4-(N,N-диметиламино)бутан)-бис-(3,3'индолил)]-1(Н)-пиррол-2,5-диона, нормализует клеточный рост, вызванный такими гипоксическими условиями. Эксперименты, предоставленные в настоящем изобретении, показывают, что факторы роста, такие как ФРСЭ, также воздействуют на капиллярную проницаемость. Исследования показали, что в экспериментальной модели на животном ФРСЭ значительно увеличивает капиллярную проницаемость, причем увеличение достигает трехкратного. Это зависимое от ФРСЭ возрастание капиллярной проницаемости также является дозозависимым. В соответствии с исследованиями на животных in vivo, введение ингибитора протеинкиназы С в концентрации приблизительно 25 мг/кг/сутки перед провокационной пробой с введением ФРСЭ значительно подавляло капиллярную проницаемость,вызванную ФРСЭ. Особенно предпочтительно применение концентраций от 1 нмоль до 5 ммоль и предпочтительно от 1 до 500 нмоль. Подавление может достигать 80% и в целом специфично для капиллярной проницаемости,вызванной фактором роста. Капиллярную проницаемость можно определить с помощью ангиографии с флюоресцеином. Ингибиторы ПКС- настоящего изобретения могут применяться для лечения патологических состояний, связанных с ростом эндотелиальных клеток и капиллярной проницаемостью,особенно, новообразований и других заболеваний, связанных с ФРСЭ. Отек легких также можно лечить с помощью соединений настоящего изобретения. Отек легких характеризуется увеличением содержания интерстициальной жидкости в легких вследствие возросшей капиллярной проницаемости. Отек легких может быть связан с несколькими патологическими состояниями,включая респираторный дистресс-синдром у взрослых (РДСВ). Он, вероятно, в первую очередь, связан с разрывом мембран альвеолярных капилляров, который может вызвать гипоксию и последующее возрастание содержания ФРСЭ. Такой разрыв может также активировать ПКС. Поэтому соединения, идентифицированные в настоящем изобретении, могут препятствовать стимуляции капиллярной проницаемости посредством факторов роста и/или ПКС- и облегчать состояния, которые приводят к отеку легких. Ингибиторы ПКС настоящего изобретения могут также применяться для лечения новообразований и других заболеваний, связанных с ФРСЭ, у млекопитающего. Путь передачи сигнала ФРСЭ оказывает непосредственные воздействия на опухолевые клетки, а также опосредует различные формы эндогенной активности в широком диапазоне опухолевых и неопухолевых патологических состояний. Экспрессия ФРСЭ была продемонстрирована в различных опухолях человека, таких как капиллярная гемангиобластома, рак молочной железы, саркома Капоши, глиобластома, ангиоматозные заболевания, рак толстой и прямой кишки, медуллобластома, рак желудка, аденокарциномы желудочно-кишечного тракта, рак яичников, немелкоклеточный рак легких, рак предстательной железы, рак мочевого пузыря, синдром von Hippel Lindau, почечно-клеточная карцинома, рак кожи, злокачественные поражения щитовидной железы, рак шейки матки, печеночно-клеточная карцинома, рабдомиосаркома и лейомиосаркома. Неблагоприятный прогноз опухоли часто связан со степенью насыщения опухоли кровеносными сосудами, связанной с экспрессией ФРСЭ. Рост опухоли без сосудистого снабжения ограничен. Поэтому применение антиангиогенного средства или средства против ФРСЭ может предотвратить дальнейший рост и вызвать обратное развитие опухолей путем ограничения сосудистого снабжения. Средства против ФРСЭ могут также оказывать непосредственное воздействие на опухолевые клетки, например,ФРСЭ оказывает непосредственное воздействие на клетки злокачественной меланомы. 9 Экспрессия ФРСЭ регулируется посредством множества механизмов. Выработка ФРСЭ может положительно модулироваться посредством гипоксии, определенных онкогенов и различных цитокинов, включая трансформирующий фактор роста-бета (ТФР-), тромбоцитарный фактор роста. В предпочтительном варианте реализации ингибиторы ПКС- могут применяться в терапии против ФРСЭ для лечения человека с новообразованием. На любой рост новообразований,экспрессирующих ФРСЭ, например, перечисленные выше опухоли, можно воздействовать ингибиторами ПКС- настоящего изобретения. Терапия против ФРСЭ особенно предпочтительна для лечения человека с неоперабельными первичными опухолями, первичными опухолями, которые не полностью удалены с помощью хирургических или радиационно-терапевтических методик, первичными опухолями, которые лечили соответствующим образом, но имеющими высокий риск последующего развития метастатического заболевания, и опухоли с установленным метастатическим заболеванием. Группы опухолей, имеющих самый неблагоприятный прогноз ввиду высокой степени сосудистого снабжения, например, рак молочной железы,рак предстательной железы, рак толстой кишки,меланоматозный рак, немелкоклеточный рак легких и/или карцинома головы/шеи, являются хорошими кандидатами на терапию против ФРСЭ или лечение ингибитором ПКС- изобретения. Гемангиома младенческого возраста встречается у 10-12% белых младенцев. В целом, это не угрожающее жизни заболевание, но в некоторых случаях или вследствие размера,или анатомического расположения может вызвать высокую частоту осложнений и смертности. ФРСЭ вовлечен в рост этих опухолей. В настоящее время -2 а интерферон применяется для индуцирования обратного развития этой опухоли. Учитывая ангиогенную природу этой опухоли, терапия против ФРСЭ с применением ингибиторов ПКС- должна быть такой же эффективной как интерферон -2 а, или может расцениваться как терапия по жизненным показаниям для применения после несостоятельности интерферона -2 а. Ингибиторы ПКС- или терапия против ФРСЭ могут также применяться для лечения вызванного опухолью асцита, злокачественных плевральных выпотов и отека вокруг опухоли. Учитывая, что содержание ФРСЭ возрастает в асцитной жидкости женщин, имеющих синдром гиперстимуляции яичников после индукции овуляции, ингибитор ПКС- мог бы применяться при этом состоянии. ФРСЭ представляет собой фактор проницаемости с высокой активностью, например, в 50000 раз выше, чем у гистамина. Концентрация ФРСЭ повышена в жидко 001779 10 сти, удаленной у пациентов с плевральными и внутрибрюшными выпотами вследствие злокачественных процессов. Внубрюшинная инъекция опухолевых клеток безволосым мышам приводит к накоплению асцитной жидкости,которое по времени коррелирует с увеличением секреции ФРСЭ в брюшную полость. Отек вокруг опухоли, встречающийся в новообразованиях центральной нервной системы, таких как гиобластома, связан с высоким уровнем ФРСЭ. Терапия против ФРСЭ уменьшит асцит и плевральные выпоты, связанные со злокачественными процессами, и синдром гиперстимуляции яичников. Такая терапия снизит потребность в повторном парацентезе/торакоцентезе и частоту сопутствующих осложнений, связанных с этими процедурами, например, инфекции, белкового истощения, легочного ателектаза и т.д. Такая терапия особенно предпочтительна для подавления отека вокруг опухоли, встречающегося в закрытых анатомических зонах, таких как центральная нервная система. Ингибиторы ПКС-, применяемые в настоящем изобретении, могут также использоваться в способах терапии против ФРСЭ для лечения других заболеваний, связанных с экспрессией ФРСЭ. Ревматоидный артрит характеризуется гиперпластическим синовиальным паннусом с высокой степенью сосудистого снабжения, который внедряется и разрушает нормальную архитектуру сустава. Кроме того, эксудативная природа синовиальной жидкости свидетельствует о повышенной степени капиллярной проницаемости. ФРСЭ может стимулировать экспрессию коллагеназы и вызвать дальнейшее ухудшение деструктивного процесса. Уровни ФРСЭ значительно повышены, в синовиальной жидкости, полученной у пациентов с ревматоидным артритом, в сравнении с пациентами с остеоартритом. Локализация выработки ФРСЭ также была отнесена к инфильтрирующим макрофагам. Поэтому ревматоидный артрит можно лечить введением ингибитора ПКС- в терапии против ФРСЭ. Келоид характеризуется избыточным образованием грануляционной ткани во время заживления ран, что приводит к гипертрофическому рубцеванию. Это расстройство обычно наблюдается у чернокожих пациентов и имеет тенденцию быть рецидивирующим заболеванием. Местное нанесение ингибиторов ПКС на гипертрофическую грануляционную ткань может снизить ангиогенез и уменьшить последующее oбразование рубца. Синдром канала запястья, называемый также нейропатией вследствие ущемления, характеризуется сдавлением нервов, которое может привести к сенсорным изменениям, мышечной слабости и мышечной атрофии. Он вызывается давлением на срединный нерв при его про 11 хождении через пространство, образованное костями запястья и поперечной запястной связкой. Синдром канала запястья встречается или как синдром, связанный с диабетом, или у популяций, не страдающих диабетом. Усиленная гидратация нерва при синдроме канала запястья может быть вызвана повышенным уровнем ФРСЭ. Повышенные уровни ФРСЭ в тканях, окружающих нерв, может вызвать ущемление нерва, вызывая повышение сосудистой проницаемости и выходящий поток жидкости в окружающие нерв ткани. Изменение синтеза и/или распад коллагена при синдроме канала запястья может быть вызван высоким уровнем выработки ТФР-. Повышенная экспрессия ТФР- может усилить внеклеточный синтез белка, включая коллаген, и снизить его распад, которые приводит к увеличенному отложению внеклеточной матрицы в тканях, окружающих нерв. Было показано, что активация ПКС вызывает транскрипцию ТФР- путем стимуляции активности активатора белка-1. Поэтому ингибиторы ТФР- настоящего изобретения могут применяться для противодействия ФРСЭ и/или активности ТФР- при синдроме канала запястья. Специалисту в этой области будет понятно, что терапевтически эффективное количество ингибиторов протеинкиназы С-, применяемых в соответствии с настоящим изобретением,представляет собой количество, достаточное для подавления роста эндотелиальных клеток или развития проницаемости капилляров путем подавления ФРСЭ и что это количество варьирует, наряду с другими, в зависимости от размера пораженной ткани, концентрации соединения в терапевтической композиции и массы тела пациента. В целом, обсужденное выше количество ингибитора протеинкиназы С, которое предстоит ввести в качестве терапевтического средства для лечения новообразований и других заболеваний, связанных с ФРСЭ, будет определяться от случая к случаю лечащим врачом. В качестве руководства при установлении соответствующей дозы будут рассматриваться степень неоваскуляризации, масса тела и возраст пациента. В целом, подходящей дозой является доза,которая приводит к концентрации ингибитора протеинкиназы С в участке лечения, в диапазоне от 0,5 нмоль до 200 мкмоль, а более обычно от 0,5 до 200 нмоль. Ожидается, что в большинстве случаев должна быть достаточной сывороточная концентрация от 0,5 до 100 нмоль. Для получения этих лечебных концентраций нуждающемуся в лечении пациенту, вероятно, будет введено приблизительно от 0,001 мг в сутки на 1 кг массы тела до 50,0 мг в сутки на 1 кг. Обычно потребуется не более чем приблизительно от 1,0 до 10,0 мг в сутки на 1 кг массы тела ингибитора протеинкиназы С-. Как отме 001779 12 чено выше, указанные выше количества могут варьировать от случая к случаю. Композиции соединений формулы I и предпочтительные соединения формулы Iа и Ib предпочтительно составляются перед введением. Подходящие фармацевтические композиции получают с помощью известных способов с использованием хорошо известных и легко доступных ингредиентов. При приготовлении композиций, пригодных для применения в способе настоящего изобретения, активный ингредиент будет обычно смешиваться с носителем или растворяться носителем, или помещаться внутрь носителя, который может быть в форме капсулы, бумаги или другого контейнера. Когда носитель служит в качестве растворителя, он может быть твердым, полутвердым или жидким материалом, который действует в качестве носителя, наполнителя или среды для активного ингредиента. Таким образом, композиции могут быть в форме таблеток, пилюль, порошков, лепешек, саше, каше, эликсиров, суспензий,эмульсий, растворов, сиропов, аэрозоля (как твердое вещество или в жидкой среде), в мягких и твердых желатиновых капсулах, в форме свечей, стерильных растворов для инъекций и стерильных упакованных порошков или для орального, или для местного применения. Некоторые примеры подходящих носителей, наполнителей и растворителей включают лактозу, декстрозу, сахарозный сорбит, маннит,крахмалы, смолу акации, фосфаты кальция, альгинат, трагакант, желатин, силикат кальция,микрокристаллическую целлюлозу, поливинилпирролидон, целлюлозу, водный сироп метилцеллюлозу, метил и пропилгидроксибензоаты,тальк, стеарат магния и минеральное масло. Композиции могут дополнительно включать смазывающие средства, увлажняющие средства,эмульгирующие и суспензирующие средства,консервирующие средства, подслащивающие средства или корригенты. Композиции изобретения могут составляться так, чтобы обеспечить быстрое, длительное или отсроченное высвобождение активного ингредиента после введения пациенту. Композиции предпочтительно составлены в форме стандартной лекарственной формы, причем каждая лекарственная форма содержит приблизительно от 0,05 мг до 3 г, более обычно приблизительно 750 мг активного ингредиента. Однако следует понимать, что введенная терапевтическая доза будет определяться врачом в свете соответствующих обстоятельств, включая тяжесть подлежащего лечению состояния, выбор подлежащего введению соединения и выбранный путь введения. Поэтому указанные выше диапазоны дозировки никоим образом не предназначены для ограничения объема притязаний изобретения. Термин "стандартная лекарственная форма" относится к физически дискретным единицам, подходящим в качестве стандартных доз для людей и других 13 млекопитающих, причем каждая единица содержит предварительно определенное количество активного материала, рассчитанное с целью вызывать желательный терапевтический эффект, в сочетании с подходящим фармацевтическим носителем. В дополнение к указанным выше композициям, большинство из которых может вводиться орально, соединения, применяемые в способе настоящего изобретения, могут также применяться местно. Композиции для местного применения включают мази, кремы и гели. Мази в целом получают с использованием или (1) маслянистой основы, т.е. основы, состоящей из фиксированных масел или углеводородов, таких как белый вазелин или минеральное масло, или (2) абсорбирующей основы,т.е. основы, состоящей из безводного вещества или веществ, которые могут поглощать воду,например безводный ланолин. Обычно после образования основы, маслянистой или абсорбирующей, добавляется активный ингредиент (соединение) в количестве, обеспечивающем желаемую концентрацию. Кремы представляют собой эмульсию масло/вода. Они состоят из масляной фазы (внутренней фазы), обычно включающей фиксированные масла, углеводороды и им подобные,такие как воски, вазелин, минеральное масло и им подобные, и водную фазу (непрерывная фаза), включающие воду и любые водорастворимые вещества, такие как соли присоединения. Эти две фазы стабилизируются с помощью применения эмульгирующего средства, например, поверхностно-активного вещества, такого как натрийлаурилсульфат; гидрофильные коллоиды, такие как коллоидные глины акации,veegum и им подобные. После составления композиции эмульсии обычно добавляется активный ингредиент (соединение) в количестве, необходимом для достижения желаемой концентрации. Гели включают основу, выбранную из маслянистой основы, воды или эмульсионносуспензионной основы. В основу добавляется средство, образующее гель, которое формирует в основе матрицу, увеличивая ее вязкость. Примерами средств, образующих гель, являются гидроксипропилцеллюлоза, полимеры акриловой кислоты и им подобные. Обычно активный ингредиент (соединения) добавляется в композицию в желаемой концентрации в момент,предшествующий добавлению средства, образующего гель. Количество соединения, включенного в композицию для местного применения, не имеет принципиального значения; концентрация должна быть в диапазоне, достаточном для обеспечения возможности быстрого нанесения композиции на область пораженной ткани в количестве, которое доставит желаемое количество соединения к участку лечения. 14 Обычное количество композиции для местного применения, которое предполагается нанести на пораженную ткань, будет зависеть от размера пораженной ткани и концентрации соединения в композиции. В целом, композиция будет наноситься на пораженную ткань в количестве, обеспечивающем приблизительно от 1 до 500 мкг соединения на 1 см 2 пораженной ткани. Предпочтительно нанесенное количество соединения будет находиться в диапазоне приблизительно от 30 до приблизительно 300 мкг/см 2, более предпочтительно приблизительно от 50 до 200 мкг/см 2 и наиболее предпочтительно приблизительно от 60 до 100 мкг/см 2. Следующие примеры композиции являются только иллюстративными и ни коим образом не предназначены для ограничения объема притязаний изобретения. Готовая форма (препарат) 1. Твердые желатиновые капсулы изготовлены с использованием следующих ингредиентов: Активное средство Крахмал, высушенный Стеарат магния Всего Указанные выше ингредиенты смешивают,и смесью в количестве 460 мг заполняют твердые желатиновые капсулы. Готовая форма (препарат) 2. Таблетка изготавливается с использованием указанных ниже ингредиентов: Активное средство Целлюлоза, микрокристаллическая Двуокись кремния, мелкодисперсная Стеариновая кислота Всего Компоненты смешивают и прессуют для образования таблеток, масса каждой из которых составляет 665 мг. Готовая форма (препарат) 3. Таблетки, каждая из которых содержит 60 мг активного ингредиента, изготавливаются следующим образом: Активное средство Крахмал Микрокристаллическая целлюлоза Поливинилпирролидон (в виде 10% раствора в воде) Натрий карбоксиметилкрахмал Стеарат магния Тальк Всего Активный ингредиент, крахмал и целлюлозу пропускают через сито 45 стандарта 15 США и тщательно смешивают. Раствор поливинилпирролидона смешивают с полученными в результате порошками, которые пропускают через сито 14 стандарта США. Полученные таким образом гранулы высушивают при 50 С и пропускают через сито 18 стандарта США. Натрий карбоксиметил крахмал, стеарат магния и тальк, ранее пропущенные через сито 60 стандарта США, затем добавляют в гранулы,которые после смешивания прессуют на таблетировочной машине для получения таблеток,каждая из которых имеет массу 150 мг. Примеры Все эти примеры демонстрируют использование хлористо-водородной соли (S)-3,4[N,N'-1,1'-2"-этокси)-3(O)-4-(N,N-диметиламино)бутан)-бис-(3,3'-индолил)]-1(Н)-пиррол 2,5-диона для подавления in vitro роста эндотелиальных клеток и увеличения in vivo капиллярной проницаемости,стимулированной ФРСЭ. Пример 1. В этом примере подавляющее воздействие указанного соединения на рост эндотелиальных клеток, стимулированный ФРСЭ, исследуют с использованием рекомбинантного человеческого ФРСЭ. Бычьи эндотелиальные клетки сетчатки выделяют из свежих глаз телят гомогенизацией несколькими стадиями фильтрации. Первичные культуры эндотелиальных клеток выращивают в покрытых фибронектином (NYBen Reagents,New York Blood Center) чашках (Costar), содержащих модифицированную среду Dulbecco'sEagle's (DMEM) с 5,5 ммоль глюкозы, 10% полученной из плазмы лошадиной сыворотки(Wheaton, Scientific), 50 мг гепарина на 1 л и 50 единиц фактора роста эндотелиальных клеток на 1 л (Boehringer Mannheim). После того как клетки достигнут слияния, среду меняют для включения 5% сыворотки плода теленка (HyClonc). Среду меняют 1 раз в 3 дня. Гомогенность эндотелиальных клеток подтверждают с помощью антител против фактора VIII. Влияние указанного ингибитора ПКС на действие ФРСЭ in vitro оценивают путем использования высеянных с низкой плотностью на чашки культур микрососудистых эндотелиальных клеток бычьей сетчатки, которые подвергаются стимуляции роста после добавления ФРСЭ. Эндотелиальные клетки бычьей сетчатки высевают с низкой плотностью ( 2500 клеток на 1 ячейку) на 24-ячеечные чашки (Costar), инкубируемые в течение ночи в DMEM, содержащей 10% телячью сыворотку (GIBCO). Среду меняют на следующий день. Для исследования воздействия указанного ингибитора ПКС на рост эндотелиальных клеток, проводят одну серию экспериментов, в которой рост клеток в отсутствие какого-либо средства служит в качестве контроля, а затем исследуют воздействие добавления указанного 16 ингибитора ПКС и в присутствии ФРСЭ (25 нг/мл; Genentech), и в отсутствие ФРСЭ. После инкубации при 37 С в течение 4 дней клетки лизируют в 0,1% натрия додецилсульфате(НДС) и измеряют содержание ДНК с использованием красителя Hoechst 33258 и флюориметра(модель ТКО-100; Hoefer). Все определения выполняют, по меньшей мере, трижды, и эксперименты повторяют минимум три раза. Результаты выражают в виде среднихстандартное отклонение по всем экспериментам. Анализ результатов in vitro выполняют с помощью непарного t критерия Student. Величину Р, составляющую 0,050, считают статистически достоверной. На фиг. 1 показаны результаты, полученные с пользованием рекомбинантного ФРСЭ. Как показано тремя самыми левыми столбиками на фигуре, добавление указанного ингибитора ПКС в культуру эндотелиальных клеток по существу не оказывало воздействие на исходную скорость роста (первый столбик). Скорость роста существенно возросла после добавления ФРСЭ (четвертый столбик). Эта скорость роста значительно уменьшается после добавления 0,5 нмоль указанного ингибитора ПКС (четыре самых правых столбика). Пример 2. Этот пример аналогичен работе, представленной на фиг. 1, и дополнительно иллюстрирует подавляющее влияние указанного ингибитора ПКС на рост клеток, стимулированный ФРСЭ, с использованием рекомбинантного человеческого ФРСЭ. Используя процедуры примера 1, выделяют и выращивают бычьи эндотелиальные клетки сетчатки; затем получают высеянные с низкой плотностью на чашки культуры. Опять же,используя процедуру примера 1, проводят эксперименты, в которых исследуют влияние указанного ингибитора ПКС на рост эндотелиальных клеток и в присутствии ФРСЭ (25 нг/мл;Genentech), и в отсутствие ФРСЭ. После инкубации при 37 С в течение 4 дней клетки лизируют в 0,1% натрия додецилсульфате (НДС) и измеряют содержание ДНК с использованием красителя Hoechst 33258 и флюориметра (модель ТКО-100; Hoefer). На фиг. 2 показаны результаты этой работы. Как показано столбиками над подписью-ФРСЭ, добавление указанного ингибитора ПКС в культуру эндотелиальных клеток при концентрации от 0,1 нмоль до 100 нмоль по существу не оказывало воздействие на исходную скорость роста клеток. Стимуляция эндотелиальных клеток рекомбинантным человеческим ФРСЭ (25 нг/мл) вызывала достоверное увеличение содержания клеточной ДНК через 4 дня, что указывает на увеличение скорости роста, в сравнении с не стимулированными клетками (сравните-ФРСЭ при 0 +ФРСЭ при 0). Эта скорость роста значительно уменьшается после добавления 17 указанного ингибитора ПКС (четыре самых правых столбика над надписью +ФРСЭ). В частности, стимулирующая способность ФРСЭ слегка снижалась в присутствии 0,1 нмоль ингибитора ПКС и по существу полностью устранялась одновременным добавлением ингибитора ПКС в концентрации 1 нмоль и выше. Пример 3. В этом примере исследуют воздействие указанного ингибитора ПКС на активность эндогенного ФРСЭ, экспрессируемую после культивации перицитов сетчатки в условиях гипоксии. Бычьи эндотелиальные клетки сетчатки и перициты сетчатки выделяют из свежих глаз телят с помощью гомогенизации и серии этапов фильтрации. Используя процедуры примера 1,бычьи эндотелиальные клетки выращивают и культивируют с низкой плотностью на чашках,используя процедуры примера 1. Используя аналогичные методики, перициты бычьей сетчатки культивируют в DMEM/5,5 ммоль глюкозы с 20% сыворотки плода теленка. Гипоксическую кондиционированную среду для экспрессии эндогенного ФРСЭ и нормоксическую кондиционированную контрольную среду соответственно готовят, выполняя следующие процедуры. Слившиеся монослои перицитов сетчатки подвергают воздействию в течение 24 ч 2% О 2/5% СO2/93% N2 с использованием контролируемого компьютером инкубатора СО 2 Lab-Line Instruments с инфракрасной водяной рубашкой и контролем пониженного содержания кислорода (модель 480). Все клетки сохранялись при 37 С, и при световой микроскопии в них не было морфологических изменений, они исключали краситель трипан синий(98%) и в последующем их можно было нормально пересевать. Клетки, инкубированные в нормоксических условиях (95% воздуха/5% СО 2) из той же партии и пересева используют в качестве контролей. Среду затем собирают и перед использованием фильтруют (Nalgene, 0,22 мкм). В этом примере проводят эксперименты, в которых исследуют воздействие указанного ингибитора ПКС на рост эндотелиальных клеток в присутствии или нормоксической кондиционированной среды или гипоксической кондиционированной среды. Как и в предыдущих экспериментах, после инкубации при 37 С в течение 4 дней клетки лизируют в 0,1% натрия додецилсульфате (НДС) и измеряют содержание ДНК с использованием красителя Hoechst 33258 и флюориметра (модель ТКО-100; Hoefer). В исследованиях, представленных на фиг. 3, указанный ингибитор ПКС используют в концентрации 10 нмоль. Как показано на фиг. 3,рост эндотелиальных клеток сетчатки стимулируется кондиционированной средой из перицитов сетчатки, культивированных в гипоксических условиях, которые, как известно, вызыва 001779 18 ют экспрессию ФРСЭ (сравните столбик 1 со столбиком 3 на фиг. 3). Эта стимуляция роста подавляется (нормализуется) в присутствии соли хлористо-водородной кислоты (S)-3,4-[N,N'1,1'-2"-этoкcи)-3(O)-4-(N,N-димeтилaминo)бутан)-бис-(3,3'-индолил)]-1(Н)-пиррол-2,5 диона ингибитора ПКС (сравните столбик 3 со столбиком 4). Пример 4. Этот пример аналогичен работе, представленной на фиг. 1 и 2, и дополнительно иллюстрирует подавляющее влияние указанного ингибитора ПКС на рост клеток, стимулированный ФРСЭ, с использованием рекомбинантного человеческого ФРСЭ. Используя процедуры примера 1, выделяют и выращивают бычьи эндотелиальные клетки сетчатки, затем получают высеянные с низкой плотностью на чашки культуры. Опять же,используя процедуру примера 1, проводят эксперименты, в которых исследуют влияние указанного ингибитора ПКС на рост эндотелиальных клеток и в присутствии (+ФРСЭ) (25 нг/мл;Genentech), и в отсутствие ФРСЭ (-ФРСЭ). Как указано выше, после инкубации при 37 С в течение 4 дней клетки лизируют в 0,1% натрия додецилсульфате (НДС) и измеряют содержание ДНК с использованием красителя Hoechst 33258 и флюориметра (модель ТКО-100; Hoefer). На фиг. 4 показаны результаты этой работы. Как показано столбиками над подписью-ФРСЭ, добавление указанного ингибитора ПКС в культуру эндотелиальных клеток при концентрации 10 нмоль по существу не оказывало воздействия на исходную скорость роста клеток. Стимуляция эндотелиальных клеток рекомбинантным человеческим ФРСЭ (25 нг/мл) вызывала достоверное увеличение содержания клеточной ДНК, что указывает на увеличение скорости роста, в сравнении с не стимулированными клетками (сравните -ФРСЭ контроль с+ФРСЭ контролем). Эта скорость роста значительно уменьшается после добавления указанного ингибитора ПКС в концентрации 10 нмоль. Эти результаты показывают, что раскрытый класс ингибиторов ПКС и, в частности, (S)3,4-[N,N'-1,1'-2-этокси)-3(О)-4-(N,N-диметиламино)бутан)-бис-(3,3'-индолил)]-1(Н)-пиррол-2,5-дион предотвращает стимуляцию in vitro роста эндотелиальных клеток и экзогенным,и индуцированным гипоксией ФРСЭ. Поскольку экспрессия ФРСЭ была тесно связана с неоваскуляризацией, связанной с дегенерацией желтого пятна, эти результаты подтверждают использование ингибиторов ПКС в качестве терапии для лечения дегенерации желтого пятна. Принципы, предпочтительные варианты реализации и виды практического применения были раскрыты в описании. Однако изобретение, защита которого предполагается, не должно рассматриваться как ограниченное конкрет 19 1. Способ лечения неоплазии, который включает введение нуждающемуся в таком лечении млекопитающему терапевтически эффективного количества(S)-3,4-[N,N'-1,1'-2 этокси)-3-(O)-4-(N,N-диметиламино)бутан)бис-(3,3'-индолил)]-1(Н)-пиррол-2,5-диона или его фармацевтически приемлемой соли. 2. Способ по п.1, отличающийся тем, что неоплазия выбрана из группы, состоящей из капиллярной гемангиобластомы, рака молочной железы, саркомы Капоши, глиобластомы, ангиоматозных заболеваний, гемангиомы младенческого возраста, рака толстой и прямой кишки,медуллобластомы, карциномы желудка, аденокарцином желудочно-кишечного тракта, злокачественной меланомы, рака яичников, не мелкоклеточного рака легких, рака предстательной железы, злокачественных выпотов, отека вокруг опухолей, карциномы мочевого пузыря, синдрома von Hippel Lindau, почечно-клеточной карциномы, рака кожи, злокачественных заболеваний щитовидной железы, рака шейки матки,печеночно-клеточной карциномы, рабдомиосаркомы и лейкомиосаркомы. 3. Способ по п.1, отличающийся тем, что неоплазия выбрана из группы, состоящей из капиллярной гемангиобластомы, рака молочной железы, саркомы Капоши, глиобластомы, ангиоматозных заболеваний, гемангиомы младенческого возраста, рака толстой и прямой кишки,злокачественной меланомы, рака яичников, не мелкоклеточного рака легких, рака предстательной железы, злокачественных выпотов, оте ка вокруг опухолей, карциномы мочевого пузыря. 4. Способ лечения ревматоидного артрита,включающий введение нуждающемуся в таком лечении млекопитающему терапевтически эффективного количества (S)-3,4-[N,N'-1,1-(2 этокси)-3-(O)-4-(N,N-диметиламино)бутан)бис-(3,3'-индолил)]-1(Н)-пиррол-2,5-диона или его фармацевтически приемлемой соли. 5. Способ лечения отека легких, включающий введение нуждающемуся в таком лечении млекопитающему терапевтически эффективного количества(S)-3,4-[N,N'-1,1'-(2 этокси)-3-(O)-4-(N,N-диметиламино)бутан)бис-(3,3'-индолил]-1(Н)-пиррол-2,5-диона или его фармацевтически приемлемой соли. 6. Способ ингибирования капиллярной проницаемости, стимулированной фактором роста сосудистого эндотелия, связанной с отеком лгких, включающий введение нуждающемуся в таком лечении млекопитающему терапевтически эффективного количества (S)-3,4[N,N'-1,1'-(2-этокси)-3-(O)-4-(N,N-диметиламино)бутан)-бис-(3,3'-индолил)]-1(Н)-пиррол 2,5-диона или его фармацевтически приемлемой соли. 7. Способ лечения келоида, включающий введение нуждающемуся в таком лечении млекопитающему терапевтически эффективного количества (S)-3,4-[N,N'-1,1'-(2-этокси)-3-(O)4-(N,N-диметиламино)бутан)-бис-(3,3'-индолил)]-1(Н)-пиррол-2,5-диона или его фармацевтически приемлемой соли. 8. Способ лечения запястного синдрома,включающий введение нуждающемуся в лечении млекопитающему терапевтически эффективного количества(S)-3,4-[N,N'-1,1'-(2 этокси)-3-(O)-4-(N,N-диметиламино)бутан)бис-(3,3'-индолил)]-1(Н)-пиррол-2,5-диона или его фармацевтически приемлемой соли. ными раскрытыми формами, поскольку они должны расцениваться как иллюстративные, а не ограничивающие. Специалисты в этой области могут варьировать и вносить изменения, не отходя от духа изобретения. ФОРМУЛА ИЗОБРЕТЕНИЯ
МПК / Метки
МПК: A61P 35/00, A61K 31/404
Метки: сосудистого, фактором, связанных, роста, способ, заболеваний, лечения, эндотелия
Код ссылки
<a href="https://eas.patents.su/12-1779-sposob-lecheniya-zabolevanijj-svyazannyh-s-faktorom-rosta-sosudistogo-endoteliya.html" rel="bookmark" title="База патентов Евразийского Союза">Способ лечения заболеваний, связанных с фактором роста сосудистого эндотелия</a>
Предыдущий патент: Косметическая композиция в аэрозольной упаковке и способ косметической обработки кератиновых волокон
Следующий патент: Производные пиридилкарбамоилиндолинов в качестве антагонистов 5-нт2с-рецепторов
Случайный патент: Конденсатор и способ получения серной кислоты