Фармацевтические композиции, предназначенные для направленного восполнения дефицита эстрогена в центральной нервной системе
Номер патента: 2707
Опубликовано: 29.08.2002
Авторы: Шварц Зигфрид, Пачев Владимир, Рёмер Вольфганг, Ёттель Михаэль, Тиме Ина
Формула / Реферат
1. Применение стероидов общей формулы I
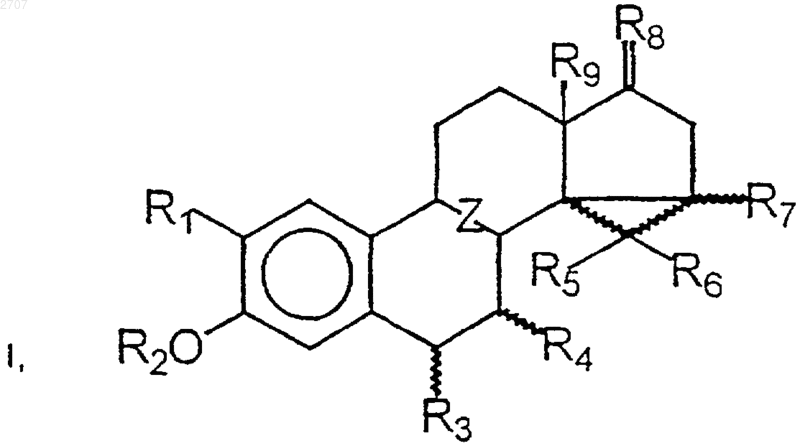
где R1 означает атом водорода, гидроксильную группу или алкилоксигруппу, имеющую 1-5 атомов углерода,
R2 означает атом водорода, алкильную группу, имеющую 1-5 атомов углерода, ацильную группу, имеющую 1-5 атомов углерода, группу общей формулы SO2NR10R11, где R10 и R11 независимо друг от друга обозначают атом водорода, алкильную группу, имеющую 1-5 атомов углерода, или вместе с атомом азота образуют пирролидино-, пиперидино- или морфолиногруппу,
R3 означает атом водорода или гидроксильную группу,
R4 означает атом водорода, гидроксильную группу или алкильную группу, имеющую до 5 атомов углерода,
R5 и R6 независимо друг от друга означают атом водорода или атом галогена,
R7 означает атом водорода или метильную группу,
R8 означает атом водорода и гидроксильную группу, оксогруппу или группу общей формулы CR12R13, где R12 и R13 независимо друг от друга означают атом водорода или атом галогена,
R9 означает метильную или этильную группу,
Z означает двойную связь С=С или замещенное либо незамещенное циклопропановое кольцо, и
группа >CR5R6 находится либо в a-, либо в b-положении, причем R7 находится в b-положении, если группа >СR5R6 находится в a-положении, и наоборот,
для приготовления фармацевтических композиций, предназначенных для направленного восполнения дефицита эстрогена в центральной нервной системе (ЦНС) без воздействия на другие органы или системы.
2. Применение стероидов по п.1, которые представляют собой соединения, выбранные из группы, включающей
15bН,3'Н-циклопроп[14,15]эстра-1,3,5(10),8-тетраен-3,17a-диол,
15bН,3'Н-циклопроп[14,15]-18а-гомоэстра-1,3,5(10),8-тетраен-3,17a-диол,
17a-гидрокси-15bН,3'Н-циклопроп[14,15]эстра-1,3,5(10),8-тетраен-3-илпентаноат,
17-метилен-15bН,3'Н-циклопроп[14,15]эстра-1,3,5(10),8-тетраен-3-ол,
15bН,3'Н-3',3'-дифторциклопроп[14,15]эстра-1,3,5(10),8-тетраен-3,17a-диол,
17-метилен-15bН,3'Н-циклопроп[14,15]эстра-1,3,5(10),8-тетраен-3-илсульфамат,
17-дифторметилен-15bН,3'Н-циклопроп[14,15]эстра-1,3,5(10),8-тетраен-3-ол,
3-метокси-15b-метил-3'Н-циклопроп[14,15]эстра-1,3,5(10),8-тетраен-3-ол,
15a-метил-3'Н-циклопроп[14,15]эстра-1,3,5(10),8-тетраен-3,17a-диол,
17-дифторметилен-15bН,3'Н-циклопроп[14,15]эстра-1,3,5(10),8-тетраен-3-ил(тетраметиленимино)сульфонат,
17-метилен-3'Н-циклопроп[8,9]-15bН,3'Н-циклопроп[14,15]эстра-1,3,5(10)-триен-3-ол.
3. Применение стероидов по п.1 или 2 для приготовления фармацевтических композиций, предназначенных для профилактики и терапии зависящего от возраста снижения познавательной способности, возрастной и перименопаузальной дисфории, предменструального синдрома, невроза и неврастении, состояний страха и невротических состояний, приступов жара (приливов) вследствие дефицита эстрогена (менопауза, гонадоэктомия, лечение с использованием аналогов GnRH), психогенных подавлений сексуального поведения.
Текст
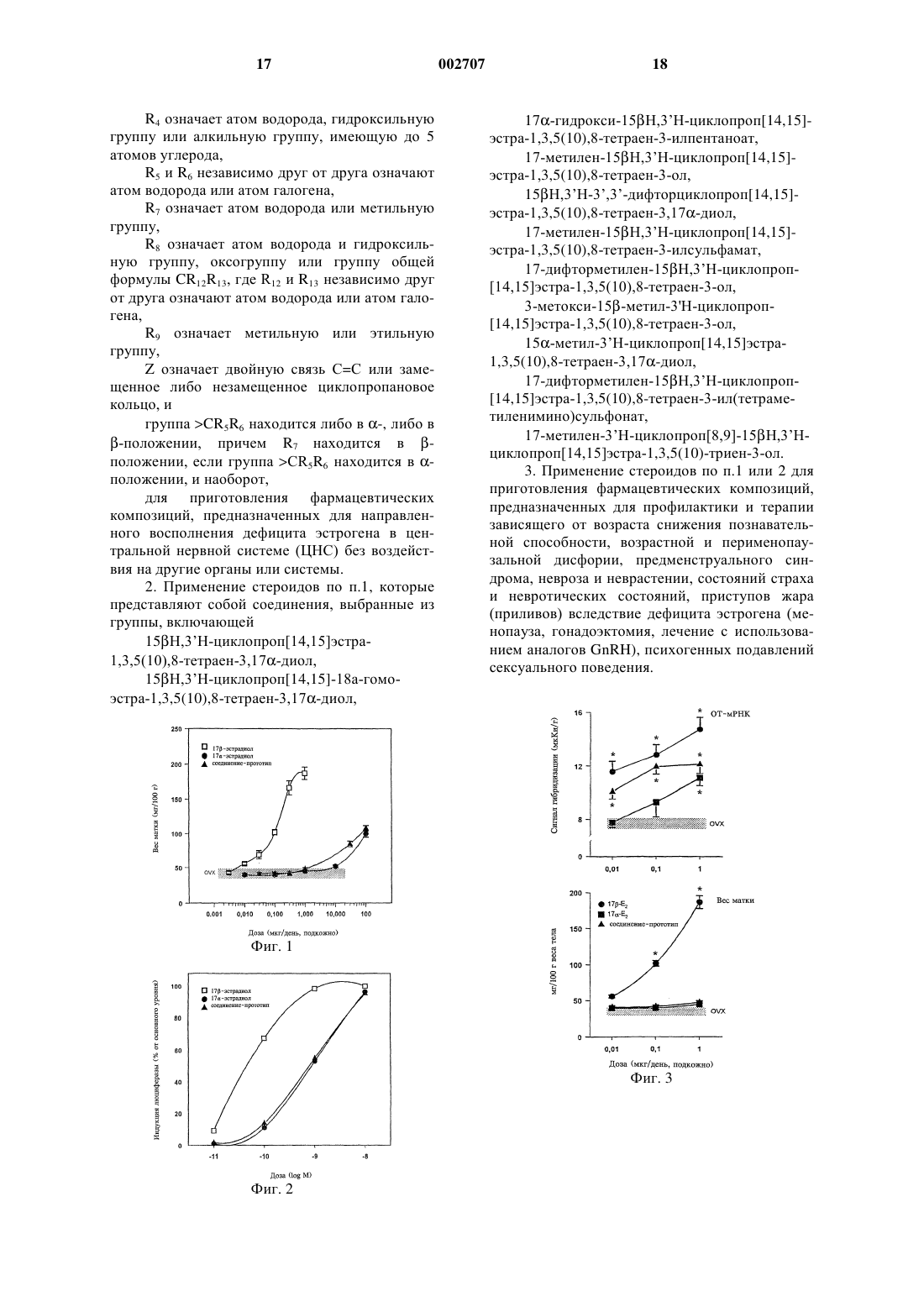
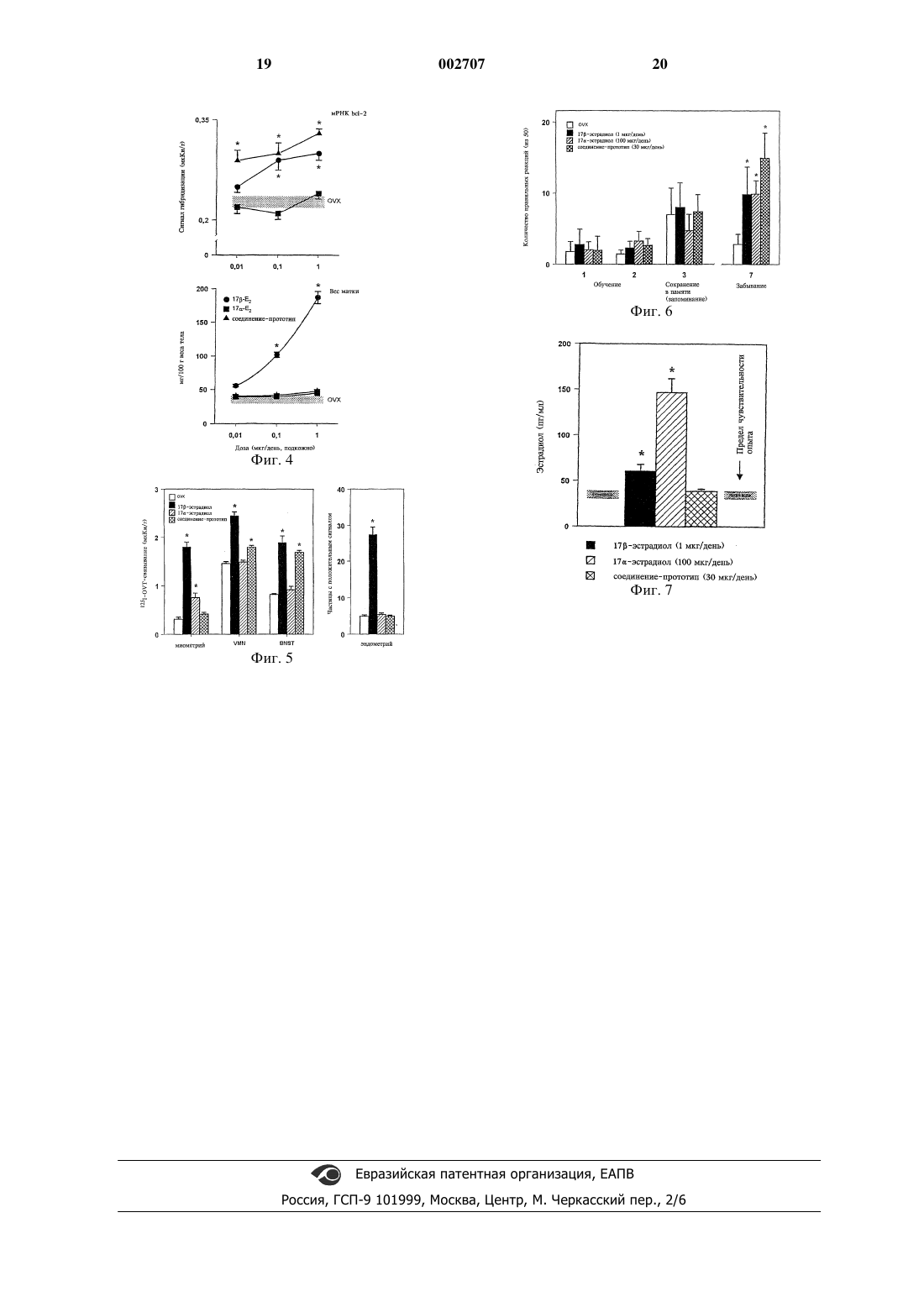
1 Настоящее изобретение относится к применению определенных стероидов для приготовления фармацевтических композиций, предназначенных для направленного восполнения дефицита эстрогена в центральной нервной системе (ЦНС) без воздействия на другие органы или системы. Эти стероиды характеризуются тем, что в отличие от обладающих системным действием природных и синтетических эстрогенов, включая 17-эстрадиол, они обладают избирательным нейротропным транскрипционным действием, сходным с действием эстрогена. Эти стероиды представляют собой соединения общей формулы IR1 означает атом водорода, гидроксильную группу или алкилоксигруппу, имеющую 1-5 атомов углерода,R2 означает атом водорода, алкильную группу, имеющую 1-5 атомов углерода, ацильную группу, имеющую 1-5 атомов углерода,группу общей формулы SO2NR10R11, где R10 иR11 независимо друг от друга означают атом водорода, алкильную группу, имеющую 1-5 атомов углерода, или вместе с атомом азота образуют пирролидино-, пиперидино- или морфолиногруппу,R3 означает атом водорода или гидроксильную группу,R4 означает атом водорода, гидроксильную группу или алкильную группу, имеющую до 5 атомов углерода,R5 и R6 независимо друг от друга означают атом водорода или атом галогена,R7 означает атом водорода или метильную группу,R8 означает атом водорода и гидроксильную группу, оксогруппу или группу общей формулы CR12R13, где R12 и R13 независимо друг от друга обозначают атом водорода или атом галогена,R9 означает метильную или этильную группу,Z означает двойную связь С=С или замещенное либо незамещенное циклопропановое кольцо, и группа CR5R6 находится либо в -, либо в-положении, причем R7 находится в положении, если группа CR5R6 находится в положении, и наоборот. Резкое или постепенное понижение концентрации эстрогена в организме может происходить как у женщин, так и у мужчин при определенных физиологических (пожилой возраст,менопауза) и патологических состояниях (гонадоэктомия, применение аналогов GnRH (гор 002707 2 мон, высвобождающий гонадотропин) в качестве дополнительной терапии при лечении рака). К наиболее известным клиническим симптомам дефицита эстрогена относятся нарушения терморегуляции в виде приступов жара(приливов), остеопороз и повышенная предрасположенность к заболеваниям сердечнососудистой системы (Netter A., The menopause,под ред. Thibault С., Levasseur М.С., Hunterphysical and psychsocial well-being in elderly men,The aging Male 1 (Suppl. 1), 54, 1998) однозначно доказывают снижение уровня эстрогена в сыворотке с увеличением возраста мужчин. При этом подчеркивается наличие "синдрома дефицита эстрогена" и его связь с патофизиологией у стареющего мужчины. Головной мозг представляет собой очень важный орган, являющийся объектом (мишенью) действия эстрогена. Эстрогены оказывают решающее физиологическое влияние на многие нейробиологические процессы. В целом их воздействия можно подразделить на две основные группы: организующие (контролирующие) и активирующие (McEwen B.S. и др., Steroid hormones as mediators of neural plasticity, J. SteroidBiochem. Mol. Biol. 39: 223-232, 1991). Воздействия первой группы касаются прежде всего специфической в отношении пола организации нейронных субстратов на стадии раннего онтогенеза. Вторая группа включает специфические изменения функции нервной регулирующей системы в зависимости от концентраций эстрогена, обусловленных связанной с физиологическим состоянием секрецией гонад после полового созревания. Активирующее воздействие эстрогенов на ЦНС проявляется среди прочего в таких физиологических процессах, как специфическое в отношении пола регулирование секреции гонадотропина (Fink G., Gonadotropin secretion and its control, под ред. Knobil E., Neil J.D., The Physiology of Reproduction,изд-во Raven Press, New York, 1349-1376, 1988),управление сексуальным поведениемand receptivity in female primates. Arch. Sex. Behav. 6: 173-192, 1977),регулирование нейроэндокринной реакционной способности на стресс (Viau V., Meaneyin the rat, Endocrinology 129: 2503-2511, 1991),обучение и запоминание стереотипов поведения со способностью к адаптации (O'NealM.F. и др., Estrogen affects performance of ovariectomized rats in a two-choice water-escape working memory task, Psychneuroendocrinology 21:5165,1996), 3 сохранение реакционной способности нейрохимических механизмов, ответственных за внимание и адекватную обработку информацииmemory, Cell Mol. Neurobiol. 16: 325-344, 1996),динамические изменения плотности межнейронных контактов в структурах головного мозга, имеющих решающее значение для познавательных способностей и эмоционального статуса (Wooley C.S., McEwen B.S., Estradiol mediates fluctuations in hippocampal synapse densityduring the estrous cycle in the adult rat, J. Neurosci. 12: 2549-2554, 1992). Очень высокий нейротропный потенциал эстрогенов обусловливает их способность индуцировать экспрессию целого ряда ЦНС-специфических генов, продукты которых имеют решающее значение для жизнеспособности нервных клеток (Miranda R.C., Sohrabji F.,Toran-Allerand C.D., Presumptive estrogen targetdevelopment interactions of estrogen with the neurotrophins, Mol. Cell Neurosci. 4: 510-525, 1993),обеспечивать многообразие и необходимое качество переноса сигналов в ЦНС (Luine V.N.,Estradiol increases choline acetyltransferase activity in specific basal forebrain nuclei and projectionreceptors by estradiol: a clue for CNS changes occuring at menopause. Cell Mol. Neurobiol, 16: 199212, 1996) и повышать устойчивость нервных клеток в отношении патологических воздействийneurons, J. Neurochem. 6: 1836-1844, 1996). Клинические испытания позволили установить, что дефицит эстрогена является причинным фактором патогенеза болезни Альцгеймера, и показали, что путем восполнения дефицита эстрогена можно приостановить клиническое проявление, соответственно прогрессивное развитие этой болезни (Henderson V.W. и др.,Estrogen replacement therapy in older women:controls, Arch. Neurol. 51: 896-900, 1994); Paganini-Hill A., Henderson V.W., Estrogen deficiency and risk of Alzheimer's disease. Am. J. Epidemiol. 140: 256-261, 1994). Целый ряд нейропептидов, на транскрипцию генов которых оказывают влияние физиологические количества эстрогена (например окситоцин и аргининвазопрессин), играют важную роль в управлении компонентами эмоционального поведенияthyroid hormone, Progr. Brain Res. 92: 127-136,1992). Из научных публикаций известно, что дефицит эстрогена коррелирует с выраженным ослаблением способности организма выводить реакционноспособные разновидности кислорода и свободные радикалы (Niki E., Nakano М., Estrogens as antioxidants, Methods Enzymol. 186: 330-333, 1990); (Lacort M. и др., Protective effectsof estrogens and catecholestrogens against peroxidative membrane damage in vitro, Lipids, 30: 141146, 1995). Избыток свободных радикалов участвует в механизме повреждения клеток в многочисленных органах и системах и связан с патогенезом нейродегенеративных заболеванийinsights from an animal model of Parkinsonism,под ред. Fiskum G., Neurodegenerative Diseases,изд-во Plenum Press, New York, 37-46, 1996). Вследствие этого восполнение дефицита эстрогена играет определенную роль в поддержании уровня и повышении эндогенной антиокислительной способности (Behl С. и др., 17Estradiol protects neurons from oxidative stressinduced cell death in vitro, Biochem. Biophys. Res.Commun. 216: 473-482, 1995). В настоящее время восполнение дефицита эстрогена осуществляют с помощью природных и синтетических эстрогенов, которые действуют на все органы и системы, имеющие рецепторы эстрогена, т.е. практически на весь организм. Поскольку эти эстрогены уже в небольших фармакологических дозах оказывают сильное влияние на пролиферацию клеток в тканях женской половой системы (эндометрий) и в эпителии молочной железы, в конечном итоге приводящую к карциногенной дедифференцировке,их применение для лечения симптомов дефицита эстрогена в ЦНС ограничено многими противопоказаниями (Bernstein B.A., Ross R.K.,Henderson B.E., Relationship of hormone use tocancer risk, J. Natl. Cancer Inst. Monograph. 12: 137-147, 1992). Пролиферативные воздействия эстрогенов представляют собой непосредственные факторы риска возникновения доброкачественной гиперплазии предстательной железы и/или гинекомастии у мужчин (Knabbe С., Endokrine TherapieUrbanSchwarzenberg, Mnchen, 645-651,1996). По этой причине, несмотря на имеющиеся показания, восполнение дефицита эстрогена у мужчин никогда не рассматривалось как реальная возможность. 5 Применение природных и синтетических эстрогенов, обладающих системным действием,т.е. воздействующих на все органы и системы организма, для лечения нейродегенеративных заболеваний описано в следующих патентных публикациях: US 4897389, US 5554601 и WO 95/12402, WO 97/03661, DE 4338314 C1. В US 4897389 описано применение эстрадиола, эстрона и эстриола по отдельности или в сочетании с гонадотропинами, андрогенами,анаболическими андрогенами или гормоном роста человека для лечения старческой деменции, болезни Паркинсона, церебральной атрофии, болезни Альцгеймера, мозжечковой атрофии, старческого или эссенциального тремора. В US 5554601 и WO 95/12402 описано применение эстрогенных веществ, включая вещества, обладающие слабым влиянием на "сексуальную активность", для защиты нервных клеток от прогрессирующего повреждения и гибели и для лечения нейродегенеративных заболеваний. Примером вещества, обладающего умеренным влиянием на "сексуальную активность" и нейрозащитным действием, является 17 - эстрадиол. В WO 97/03661 описано применение неэстрогенных веществ, в структуре которых имеются, по крайней мере, две кольцевые системы,причем, по крайней мере, одна из них представляет собой концевое фенольное кольцо, и молекулярная масса которых составляет менее 1000 Да, для обеспечения защиты нейронов. В DE 4338314 С 1 описаны имеющие фенольную А-кольцевую структуру стероиды,свойства которых в отношении связывания с радикалами и антиокислительная активность не зависят от уровня эстрогенподобной активности. Эти соединения могут применяться для профилактики и терапии вызванных радикалами повреждений клеток. Во всех этих публикациях основой терапевтической и нейрозащитной эффективности полученных соединений являются одно или несколько из следующих конечных воздействий: стимулирование биосинтеза природных нейронных факторов роста,стимулирование активности ацетилхолинсинтезирующих ферментов, соответственно поглощения субстрата для синтеза ацетилхолина,непосредственное цитозащитное действие в результате повышения устойчивости нервных клеток к дефициту питательных субстратов,соответственно факторов роста,снижение чувствительности нервных клеток к свободным радикалам и реакционноспособным разновидностям кислорода, которые высвобождаются вследствие травмы, соответственно нейротоксического воздействия. Однако ни в одной из указанных публикаций не описаны стероиды с избирательными нейротропными воздействиями в отношении транскрипции, сходными с воздействием эстро 002707 6 гена, т.е. такие, которые при введении in vivo, не оказывая заметного биологического влияния на репродуктивную систему, воздействуют на транскрипцию в ЦНС генов, зависящих от эстрогена, сходным с действием эстрогена образом. Следует особо подчеркнуть, что описанное в US 5554601 и WO 95/12402 действие 17 эстрадиола, т.е. вещества, обладающего пониженной эстрогенностью в половой системеSteroid Biochem. 16: 323-328, 1982), основано только на защите культивируемых нервных клеток от индуцируемой дефицитом питательной среды их гибели, при этом относительная активность 17-эстрадиола не оценена в сравнении с активностью 17-эстрадиола. Из этого можно сделать вывод о том, что в опубликованных к настоящему времени исследованиях и патентных публикациях отсутствуют сведения об избирательном нейротропном действии 17 эстрадиола, соответственно его производных,тогда как известно, что 17-эстрадиол не обладает избирательным действием в отношении ЦНС и поэтому сопоставим с эстрогеном системного действия. В WO 97/03661 и DE 4338314 С 1 цитозащитное действие эстрогенов интерпретируется как следствие способностей их концевых фенольных А-колец присоединять радикалы. Диссоциированное нейротропное действие 17-эстрадиола, основанное на воздействии на транскрипцию чувствительных к эстрогену генов, не описано ни в патентной, ни в научной литературе. Исходя из вышеизложенного, в основу настоящего изобретения была положена задача разработать такие фармацевтические композиции, которые позволяли бы направленно восполнять дефицит эстрогена в центральной нервной системе (ЦНС) без воздействия на другие органы или системы. Согласно изобретению указанная задача решается благодаря тому, что для приготовления фармацевтических композиций применяют определенные стероиды, которые обеспечивают восполнение дефицита эстрогена в центральной нервной системе (ЦНС) без воздействия на другой орган или систему. Эти стероиды характеризуются тем, что в отличие от природных или синтетических эстрогенов системного действия, включая 17 эстрадиол, они обладают избирательным нейротропным воздействием на транскрипцию, сходным с действием эстрогена. При создании изобретения неожиданно было установлено, что определенные стероиды при их применении согласно изобретению оказывают избирательное действие на транскрипцию зависящих от эстрогена генов в 7 ЦНС и вызывают изменения соответствующих физиологических параметров,обладают специфичными в отношении ЦНС действиями на транскрипцию при применении в таких дозах, которые не оказывают биологических воздействий на ткани репродуктивной системы,обладают специфичными в отношении ЦНС действиями на транскрипцию при применении в таких дозах, в которых ни 17 эстрадиол, ни 17-эстрадиол не обладают эффективностью, и вызываемое ими воздействие на транскрипцию зависящих от эстрогена генов в ЦНС не является результатом действия вторично образовавшегося 17-эстрадиола. Эти стероиды представляют собой соединения общей формулы IR1 означает атом водорода, гидроксильную группу или алкилоксигруппу, имеющую 1-5 атомов углерода,R2 означает атом водорода, алкильную группу, имеющую 1-5 атомов углерода, ацильную группу, имеющую 1-5 атомов углерода,группу общей формулы SO2NR10R11, где R10 иR11 независимо друг от друга обозначают атом водорода, алкильную группу, имеющую 1-5 атомов углерода, или вместе с атомом азота образуют пирролидино-, пиперидино- или морфолиногруппу,R3 означает атом водорода или гидроксильную группу,R4 означает атом водорода, гидроксильную группу или алкильную группу, имеющую до 5 атомов углерода,R5 и R6 независимо друг от друга означают атом водорода или атом галогена,R7 означает атом водорода или метильную группу,R8 означает атом водорода и гидроксильную группу, оксогруппу или группу общей формулы CR12R13, где R12 и R13 независимо друг от друга обозначают атом водорода или атом галогена,R9 означает метильную или этильную группу,Z означает двойную связь С = С или замещенное либо незамещенное циклопропановое кольцо, и группа CR5R6 находится либо в -, либо в-положении, причем R7 находится в положении, если группа CR5R6 находится в положении, и наоборот. Предпочтительными соединениями являются следующие:(10),8-тетраен-3,17-диол,15 Н,3'Н-циклопроп[14,15]-18 а-гомоэстра 1,3,5(10),8-тетраен-3,17-диол,17-гидрокси-15 Н,3'Н-циклопроп[14,15]эстра-1,3,5(10), 8-тетраен-3-илпентаноат,17-метилен-15H,3'Н-циклопроп[14,15]эстра-1,3,5(10),8-тетраен-3-ол,15 Н,3'Н-3',3'-дифторциклопроп[14,15]эстра-1,3,5(10),8-тетраен-3,17-диол,17-метилен-15 Н,3'Н-циклопроп[14,15]эстра-1,3,5(10),8-тетраен-3-илсульфамат,17-дифторметилен-15 Н,3'Н-циклопроп[14,15]эстра-1,3,5(10),8-тетраен-3-ол,3-метокси-15-метил-3'Н-циклопроп[14,15]эстра-1,3,5(10),8-тетраен-3-ол,15-метил-3'Н-циклопроп[14,15]эстра 1,3,5(10),8-тетраен-3,17-диол,17-дифторметилен-15 Н,3'Н-циклопроп[14,15]эстра-1,3,5(10),8-тетраен-3 ил(тетраметиленимино)сульфонат,17-метилен-3'Н-циклопроп[8,9]-15 Н,3'Нциклопроп[14,15]эстра-1,3,5(10)-триен-3-ол. В предпочтительном варианте соединения применяют согласно изобретению для приготовления фармацевтических композиций, предназначенных для профилактики и терапии зависящего от возраста снижения познавательных способностей, возрастной и перименопаузальной дисфории, предменструального синдрома,невроза и неврастении, состояний страха и неврозных состояний, приступов жара в результате дефицита эстрогена (менопауза, гонадоэктомия,лечение с использованием аналогов GnRH) и психогенного подавления сексуального поведения. Было установлено, что при этом риск неблагоприятного воздействия на чувствительные к гормону ткани репродуктивной системы (эндометрий, миометрий, предстательная железа,молочная железа) в отношении неконтролируемой пролиферации и карциногенеза практически исключен. Объектом настоящего изобретения являются также фармацевтические композиции для орального и парентерального, в том числе для местного, ректального, подкожного, внутривенного, внутримышечного, внутрибрюшинного,интраназального, внутриматочного, интрабуккального или подъязычного применения, которые наряду с обычными носителями и разбавителями содержат в качестве действующего вещества указанное выше соединение. В качестве фармацевтических композиций могут применяться таблетки или драже по 0,1-2 мг для ежедневного введения оральным путем,ампулы по 0,1-2 мг для ежедневного введения в виде подкожной инъекции,пластыри для ежедневного трансдермального высвобождения от 0,05 до 2 мг, 9 подкожные имплантаты с ежедневным высвобождением 0,05-2 мг,гели и кремы для трансдермального высвобождения от 0,05 до 2 мг в день,системы для буккального применения с ежедневным высвобождением 0,1-1 мг. Лекарственные средства по изобретению приготавливают известным способом с использованием общепринятых твердых или жидких носителей или разбавителей и обычно применяемых в фармацевтике вспомогательных веществ, соответствующих требуемой форме введения с включением соответствующей дозы действующего вещества. На примере 15 Н,3'Н-циклопроп[14,15]эстра-1,3,5(10),8-тетраен-3,17-диола(соединение общей формулы I, где R1, R2, R3, R4, R5,R6 и R7 означают Н, R8 означает -ОН, -Н, R9 означает СН 3, Z означает двойную связь С = С), который далее на чертежах обозначен как соединениепрототип, экспериментальным путем продемонстрировано его избирательное действие по изобретению, сходное с действием эстрогена в сравнении с 17-эстрадиолом и 17-эстрадиолом. Пример 1. Влияние хронического подкожного введения in vivo на массу матки. Половозрелых (возраст 3 месяца, вес 25030 г) самок крыс линии Wistar (виварийSchnwalde GmbH, Германия) подвергали овариэктомии под наркозом с использованием кетамина. Через 14 дней животным имплантировали подкожно осмотические мининасосы(фирма Alzett, США), которые высвобождали в течение 7 дней ежедневные дозы по 0,01, 0,1,0,3, 1, 3, 30 и 100 мкг исследуемых веществ(15 Н,3'Н-циклопроп[14,15]эстра-1,3,5(10),8 тетраен-3,17-диол, 17-эстрадиол и 17 эстрадиол). Животным контрольной группы вводили носитель (пропиленгликоль) в соответствующих объемах. На седьмой день после обработки животных умерщвляли и определяли сырой вес матки (в пересчете на 100 г веса тела животного). На фиг. 1 приведены данные об утеротропном действии различных доз 17 эстрадиола (прямоугольники), 17-эстрадиола(кружки) и 15 Н,3'Н-циклопроп[14,15]эстра 1,3,5(10),8-тетраен-3,17-диола (треугольники) на подвергнутых овариэктомии крыс. Каждая точка представляет собой среднее значениестандартное отклонение (хСКО) для 7-10 подопытных животных; заштрихованная область характеризует диапазон разброса этих параметров для обработанных плацебо животных(OVX). Очевидно, что при обработке 17 эстрадиолом существенное увеличение матки проявляется уже при суточной дозе 0,03-0,1 мкг. Для достижения сопоставимого утеротропного действия требуются суточные дозы, составляющие для 17-эстрадиола 100 мкг, для 15 Н,3'Н 002707 10 циклопроп[14,15]эстра-1,3,5(10),8-тетраен 3,17-диола 30 мкг соответственно. Эти результаты свидетельствуют о том,что действие 15 Н,3'Н-циклопроп[14,15]эстра 1,3,5(10),8-тетраен-3,17-диола на женскую половую систему приблизительно в 1000 раз меньше, чем действие 17-эстрадиола, и сопоставимо с действием 17-эстрадиола. Пример 2. Активация транскрипции in vitro репортерного гена, зависящего от рецептора аэстрогена. Клетки рака молочной железы линии MCF7/2A, экспрессирующие альфа-изоформу рецептора эстрогена (ERa), стабильно трансформировали репортерной плазмидой EREwtcLUC. Репортер содержал чувствительный к действию эстрогена элемент (ERE) вителлогенина, промотор тимидинкиназы и ген, кодирующий люциферазу из Photinuspyralis. Культуру клеток выращивали в течение 7 дней до начала эксперимента в среде, не содержащей стероидов, и затем инкубировали в течение 48 ч с 17-эстрадиолом, 17-эстрадиолом и 15 Н,3'Нциклопроп[14,15]эстра-1,3,5(10),8-тетраен-3,17 диолом, взятых в четырех различных концентрациях (10-11, 10-10, 10-9 - и 10-8M). Клетки лизировали и определяли транскрипцию репортерного гена люциферазы путем оценки люциферазной активности с помощью обладающего специфичной активностью соединения для тестирования (фирмаServa/Promega, Германия). На фиг. 2 представлены данные по индукции транскрипции стабильно трансформированного,зависящего от эстрогена репортерного гена (люциферазы) в экспрессирующих рецептор эстрогена клетках рака молочной железы линии MCF-7/2A после 48-часовой обработки различными дозами 17-эстрадиола (прямоугольники), 17-эстрадиола(треугольники). Данные на чертеже представляют собой средние значения по двум независимым опытам. Очевидно, что тестируемые соединения стимулировали транскрипцию репортера в зависимости от дозы. Эффективность 15H,3'Нциклопроп[14,15]эстра-1,3,5(10),8-тетраен-3,17 диола и 17-эстрадиола на порядок (т.е., примерно в 10 раз) ниже эффективности 17-эстрадиола. Эти результаты свидетельствуют о том, что 5H,3'Н-циклопроп[14,15]эстра-1,3,5(10),8-тетраен 3,17-диол оказывал в несколько раз меньшее эстрогенное воздействие на ткани рака молочной железы. Пример 3. Стимулирование транскрипции гена окситодина в головном мозге после хронической обработки in vivo дозами, не оказывающими воздействия на матку. Половозрелых (возраст 3 месяца, вес 250 30 г) самок крыс линии Wistar (виварийSchnwalde GmbH, Германия) подвергали овариэктомии под наркозом с использованием кетамина. Через 14 дней животным имплантиро 11 вали подкожно осмотические мининасосы(фирма Alzett, США), которые высвобождали в течение 7 дней ежедневные дозы по 0,01, 0,1 и 1 мкг исследуемых веществ(15H,3'Нциклопроп[14,15]эстра-1,3,5(10),8-тетраен 3,17-диол, 17-эстрадиол и 17-эстрадиол); животным контрольной группы вводили носитель (пропиленгликоль) в соответствующих объемах. Сразу после умерщвления животных определяли сырой вес матки (в пересчете на 100 г веса тела животного). Матричную рибонуклеиновую кислоту(мРНК), кодирующую биосинтез окситоцина,выявляли в паравентрикулярных ядрах (PVN) гипоталамуса путем гибридизации in-situ со специфичным несущим радиоактивную метку олигодезоксинуклеотидным зондом по известному методу (Fischer D. и др., Lactation as aClin. Invest., 96: 1208-1215, 1995). Обусловленные обработкой изменения транскрипции гена окситоцина количественно оценивали с помощью денситометрических измерений специфичных сигналов гибридизации в определенных анатомических структурах. На фиг. 3 представлены данные по индукции кодирующих окситоцин транскриптов (ОТмРНК; верхний график) в паравентрикулярных ядрах гипоталамуса подвергнутых овариэктомии крыс после хронической обработки путем подкожного введения 17-эстрадиола (кружки),17-эстрадиола (прямоугольники) и 15 Н,3'Нциклопроп[14,15]эстра-1,3,5(10),8-тетраен 3,17-диола (треугольники) в трех различных дозах. На нижнем графике показано воздействие тестируемых соединений на вес матки. Каждая точка представляет собой хСКО по 5-7 отдельным опытам. Заштрихованной областью показан диапазон разброса соответствующих параметров у крыс, обработанных носителем. Звездочками обозначены достоверные различия(OVX). Результаты свидетельствуют о том, что 15 Н,3'Н-циклопроп[14,15]эстра-1,3,5(10),8 тетраен-3,17-диол стимулировал транскрипцию гена окситоцина в PVN в зависимости от дозы, при этом стимулирующее действие очень схоже с действием, обусловленным 17 эстрадиолом. Однако нейротропное воздействие 15 Н,3'Н-циклопроп[14,15]эстра-1,3,5(10),8 тетраен-3,17-диола на транскрипцию в отличие от 17-эстрадиола не сопровождалось увеличением матки. При применении в указанных дозах 17-эстрадиол не оказывал влияния на концентрацию окситоцин-мРНК в PVN гипоталамуса. Эти результаты свидетельствуют об избирательном действии 15 Н,3'Н-циклопроп 002707[14,15]эстра-1,3,5(10),8-тетраен-3,17-диола,сходном с действием эстрогена, на головной мозг самок крыс. Пример 4. Стимулирование транскрипции антиапоптозного гена bcl-2 в гиппокампе после хронической обработки in vivo дозами, которые не оказывают утеротропного действия. Материал для опытов получали с использованием животных, которых обрабатывали аналогично эксперименту, описанному в примере 3. Ген bcl-2 кодирует синтез протеина, участвующего в каскаде клеточной пролиферации, и противодействует запрограммированной гибели клеток (апоптозу) (Merry D.E., Korsmeyer SJ.,Bcl-2 gene family in the nervous system, Ann. Rev.Neurosci. 20:245-267, 1997). Транскрипция этого гена стимулируется эстрогеном (Kandouz М. и др., Antagonism between estradiol and progestin onBcl-2 expression in breast cancer cells. Int. J. Cancer 68: 120-125, 1996). Зубчатая извилина (Gyrus dentatus) представляет собой составную часть гиппокампа, в которой у крыс даже во взрослом возрасте происходит нейрогенез (Gould E. и др ProliferationAcad. Sci. USA 96: 3168-3170, 1998) и происходит экспрессия bcl-2. bcl-2-Транскрипты в срезах головного мозга выявляли путем гибридизации in-situ со специфичным олигонуклеотидным зондом (Clark R.S.B. и др., Apoptosis-supressorrats, J. Neurosci. 17: 9172-9182, 1997) и оценивали количественно денситометрическим путем согласно описанному в примере 3 методу. На фиг. 4 показано влияние трех различных доз 17-эстрадиола (кружки), 17 эстрадиола (прямоугольники) и 15 Н,3'Нциклопроп[14,15]эстра-1,3,5(10),8-тетраен 3,17-диола (треугольники) на экспрессию bcl-2 в Gyrus dentatus гиппокампа крыс, подвергнутых овариэктомии (обозначения и сокращения те же, что и на фиг. 3). Обработка 15 Н,3'Н-циклопроп[14,15]эстра-1,3,5(10),8-тетраен-3,17-диолом вызывала зависящую от дозы стимуляцию экспрессии bcl2 в зубчатой извилине. Воздействие было идентичным тому, которое вызывалось такой же дозой 17-эстрадиола. Как следует из представленных на фиг. 4 данных, 17-эстрадиол при применении в указанных дозах не оказывал влияния на транскрипцию bcl-2. Эти результаты свидетельствуют о том,что при применении в указанных дозах 15 Н,3'Н-циклопроп[14,15]эстра-1,3,5(10),8-тетраен-3,17-диол влиял на транскрипцию антиапоптозного гена bcl-2 в ЦНС сходным с действием эстрогена образом, не оказывая при этом влияния на матку. 13 Пример 5. Диссоциированная индукция рецепторов окситоцина в головном мозге и в миометрии. В миометрии и в ЦНС присутствуют сайты связывания пептидного гормона окситозина,имеющие одинаковые биохимические характеристики. В обоих органах острая или хроническая обработка эстрогеном вызывает увеличение количества (плотности) рецепторов окситоцина. Структурами головного мозга, в которых указанный параметр наиболее восприимчив к действию эстрогена, являются интерстициальное ядро концевой полоски (Nucleus interstitialis striae terminalis), вентромедиальное ядро (Nucleus ventromedialis) и миндалевидный ядерный комплекс. Обусловленная действием эстрогена индукция рецепторов окситоцина в этих структурах связана с проявлением целого ряда просоциальных стереотипов поведения, включая сексуальное поведение (Insel T.R., Oxitocin - аneuropeptide for affiliation: evidence from behavioral,receptor autoradiographic, and comparative studies,Psychoneuroendocrinology 17: 3-35, 1992). Определение плотности рецепторов окситоцина в определенных анатомических структурах проводили методом, основанным на получении авторадиографического изображения с помощью связывания несущих радиоактивную метку антагонистов рецептора окситоцина d(CH2)5-Tyr(Me)2,Thr4, Оrn8-[125I]Туr9 вазотоцин (125I-OVTA) (Kremarikthe rat, J. Соmр. Neurol. 333: 343-359, 1993). Замороженные срезы головного мозга и матки подвергнутых овариэктомии крыс, которым на протяжении 7 дней ежедневно вводили подкожно в дозе 1 мкг 15 Н,3'Н-циклопроп[14,15]эстра 1,3,5(10),8-тетраен-3,17-диол, 17-эстрадиол, соответственно 17-эстрадиол (ср. пример 3), инкубировали с 125I-OVTA (фирма NEN DuPont, Германия) в концентрации 50 пМ. Затем получали авторадиограммы на пленке, которые использовали для денситометрического определения сайтов связывания окситоцина согласно известному методу(Patchev V.K. и др., Oxytocin binding sites in rat limbic and hypothalamic structures:site-specific modulation by adrenal and gonadal steroids, Neuroscience, 57: 537-543, 1993). На фиг. 5 представлены данные, характеризующие специфичное связывание 125I-меченых лигандов рецептора окситоцина (125I-OVT) в миометрии и в двух чувствительных к эстрогену структурах головного мозга, а именно, в вентромедиальном ядре гипоталамуса (VMN) и в интерстициальном ядре концевой полоски (BNST), после обработки в течение 7 дней суточными дозами по 1 мкг 17 эстрадиола (черные столбики), 17-эстрадиола (заштрихованные стоблики) и 15 Н,3'Нциклопроп[14,15]эстра-1,3,5(10),8-тетраен-3,17 диола (серые столбики). Звездочками обозначены достоверные различия (р 0,05) по сравнению с подвергнутыми овариэктомии крысами, обрабо 002707 14 танными плацебо (OVX). На правом графике показано воздействие тестируемого соединения на пролиферацию эндометрия. Каждый столбик представляет собой хСКО по 4-5 отдельным опытам. Результаты этого опыта также представлены на фиг. 5. Обработка 17-эстрадиолом и 15H,3'Нциклопроп[14,15]эстра-1,3,5(10),8-те-траен-3,17 диолом приводила к существенному увеличению плотности рецепторов окситоцина во всех исследованных структурах головного мозга, при этом 15 Н,3'Н-цикло-проп[14,15]эстра-1,3,5(10),8 тетраен-3,17-диол оказывал меньшее воздействие на VMN, чем 17-эстрадиол. 17-эстрадиол, использованный в рассматриваемых дозах, оказался неэффективным во всех структурах головного мозга. В миометрии 17-эстрадиол вызывал сильную индукцию сайтов связывания окситоцина, тогда как 17-эстрадиол и 15 Н,3'Н-циклопроп-[14,15]эстра 1,3,5(10),8-тетраен-3,17-диол оказывали существенно меньшее действие. Измерение с использованием компьютера толщины эндометрия в препаратах матки показало, что 17-эстрадиол в суточной дозе 1 мкг вызывал значительную пролиферацию эндометрия, в то время как 17-эстрадиол и 15 Н,3'Н-циклопроп[14,15]эстра-1,3,5(10),8-тетраен-3,17-диол в эквивалентных дозах не оказывали влияния на толщину эндометрия. В целом результаты, приведенные в примере 5, свидетельствуют о том, что 15H,3'Нциклопроп[14,15]эстра-1,3,5(10),8-тетраен-3,17 диол оказывает влияние на такой биохимический параметр, как рецептор окситоцина, который характерен как для репродуктивной системы (миометрий), так и для ЦНС, преимущественно в центральной нервной системе и благодаря такому нейротропному воздействию качественно отличается от 17-эстрадиола и 17-эстрадиола, являющихся природными эстрогенами. Пример 6. Воздействие хронической обработки на познавательные способности. Известно, что снижение концентрации эстрогена коррелирует с понижением способности к обучению и запоминанию (Кореrа Н., Estrogens andRes. 2: 118-133, 1973). Корреляция между уровнем эстрогена в сыворотке и познавательными способностями подтверждена в опытах на модели животных (Kondodysfunction following transient brain ischemia in ovariectomized gerbils, Neurosci. Lett. 238: 45-48, 1997). Для сравнительных исследований воздействия 15 Н,3'Н-циклопроп[14,15]эстра-1,3,5(10),8 тетраен-3,17-диола, 17-эстрадиола и 17 эстрадиола на познавательные способности проводили следующий эксперимент: Половозрелых самок крыс линии Wistar (масса 24020 г) подвергали овариэктомии под наркозом с использованием нембутала. Через неделю после операции начинали обработку путем подкожного введения следующих суточных доз соеди 15 нений: 17-эстрадиол-1 мкг; 17-эстрадиол - 100 мкг; 15 Н,3'Н-циклопроп-[14,15]эстра-1,3,5(10),8 тетраен-3,17-диол - 30 мкг. Общая продолжительность обработки составляла 14 дней. На 5 и 6 день обработки проводили тренировки для обучения условному стереотипу убегания согласно известному методу (Diaz-Veliz G. и др Influence of theupon the ascquisition of conditioned avoidance responses in rats, Physiol. Behav. 46: 397-401, 1989). Во время сеанса каждого животного 50 раз подвергали воздействию комбинации из неусловного (раздражение электрическим током) и двух условных стимулов (световой и звуковой сигналы). На седьмой день обработки оценивали запоминание стереотипов поведения. После шестидневного перерыва в сеансах обучения на четырнадцатый день обработки оценивали ослабление (забывание) заученного условного стереотипа поведения. В качестве критерия оценки запоминания, соответственно забывания заученного стереотипа поведения использовали количество правильных поведенческих реакций(убегание в "безопасное" отделение устройства в течение 3 с после появления условного сигнала) в 50 последовательных опытах. На фиг. 6 показано воздействие 17 эстрадиола (черные столбики), 17-эстрадиола (заштрихованные столбики) и 15 Н,3'Н-циклопроп[14,15]эстра-1,3,5(10),8-тетраен-3,17-диола(серые столбики) на распознавание и запоминание нового стереотипа поведения у крыс, подвергнутых овариэектомии (незакрашенные столбики; OVX). Звездочками обозначены достоверные различия при сравнении с обработанными плацебо животными (OVX) в соответствующий день эксперимента. После четырнадцатидневной обработки были получены следующие данные о весе матки (хСКО;n=8-10 в соответствующим образом обработанной группе; данные выражены в мг/100 г веса тела):OVX - 532; 17-эстрадиол - 1879; 17-эстрадиол 1005; 15 Н,3'Н-циклопроп[14,15] эстра-1,3,5(10),8-тетраен-3,17-диол - 1084. Очевидно,что 15 Н,3'Н-циклопроп[14,15]эстра-1,3,5(10),8-тетраен-3,17-диол при использовании рассматриваемых доз оказывал стимулирующее действие, сходное с действием эстрогена, на запоминание заученного стереотипа поведения, при этом его утеротропное действие существенно меньше, чем соответствующее действие 17 эстрадиола при введении суточной дозы 1 мкг. Эти результаты свидетельствуют о том, что 15 Н,3'Нциклопроп[14,15]эстра-1,3,5(10),8-тетраен-3,17 диол оказывал влияние на познавательные способности, аналогичное влиянию эстрогена, при этом он оказывал слабое пролиферативное воздействие на репродуктивные органы. Пример 7. Биотрансформация 15H,3'Нциклопроп[14,15]эстра-1,3,5(10),8-тетраен-3,17 диола и 17-эстрадиола в 17-эстрадиол. 16 Подвергнутым овариэктомии крысам в течение 7 дней (ср. пример 6) вводили подкожно 17 эстрадиол в суточной дозе 100 мкг, 15 Н,3'Нциклопроп[14,15]эстра-1,3,5(10),8-тетраен-3,17 диол в суточной дозе 30 мкг, соответственно 17 эстрадиол в суточной дозе 1 мкг. В последний день обработки определяли концентрации 17 эстрадиола в сыворотке в трех группах подопытных животных и сравнивали их с данными, полученными для обработанных носителем контрольных животных. На фиг. 7 представлены уровни 17 эстрадиола в сыворотке после обработки подвергнутых овариэктомии крыс в течение 7 дней путем подкожного введения в указанных дозах 17 эстрадиола (черные столбики), 17-эстрадиола (заштрихованные столбики) и 15H,3'Нциклопроп[14,15]эстра-1,3,5(10),8-тетраен-3,17 диола (серые столбики). Звездочками обозначены достоверные различия по сравнению с величинами,полученными для обработанных плацебо животных; эти величины находились ниже порога чувствительности метода; каждая обрабатываемая группа состояла из 7 животных. Очевидно, что после введения в указанных дозах 17-эстрадиола и 17-эстрадиола зарегистрированы заметные концентрации 17-эстрадиола в сыворотке. Хроническая обработка путем подкожного введения 15 Н,3'Н-циклопроп[14,15]эстра 1,3,5(10),8-тетраен-3,17-диола не приводила к возрастанию эндогенного уровня 17-эстрадиола. Эти результаты свидетельствуют о том, что наблюдаемые фармакологические воздействия после введения 15H,3'Н-циклопроп[14,15]эстра-1,3,5(10),8 тетраен-3,17-диола не связаны с биотрансформацией соединения в 17-эстрадиол. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Применение стероидов общей формулы IR1 означает атом водорода, гидроксильную группу или алкилоксигруппу, имеющую 1-5 атомов углерода,R2 означает атом водорода, алкильную группу, имеющую 1-5 атомов углерода, ацильную группу, имеющую 1-5 атомов углерода,группу общей формулы SO2NR10R11, где R10 иR11 независимо друг от друга обозначают атом водорода, алкильную группу, имеющую 1-5 атомов углерода, или вместе с атомом азота образуют пирролидино-, пиперидино- или морфолиногруппу,R3 означает атом водорода или гидроксильную группу, 17R4 означает атом водорода, гидроксильную группу или алкильную группу, имеющую до 5 атомов углерода,R5 и R6 независимо друг от друга означают атом водорода или атом галогена,R7 означает атом водорода или метильную группу,R8 означает атом водорода и гидроксильную группу, оксогруппу или группу общей формулы CR12R13, где R12 и R13 независимо друг от друга означают атом водорода или атом галогена,R9 означает метильную или этильную группу,Z означает двойную связь С=С или замещенное либо незамещенное циклопропановое кольцо, и группа CR5R6 находится либо в -, либо в-положении, причем R7 находится в положении, если группа СR5R6 находится в положении, и наоборот,для приготовления фармацевтических композиций, предназначенных для направленного восполнения дефицита эстрогена в центральной нервной системе (ЦНС) без воздействия на другие органы или системы. 2. Применение стероидов по п.1, которые представляют собой соединения, выбранные из группы, включающей 15 Н,3 Н-циклопроп[14,15]эстра 1,3,5(10),8-тетраен-3,17-диол,15 Н,3 Н-циклопроп[14,15]-18 а-гомоэстра-1,3,5(10),8-тетраен-3,17-диол, 002707 17-гидрокси-15 Н,3 Н-циклопроп[14,15]эстра-1,3,5(10),8-тетраен-3-илпентаноат,17-метилен-15 Н,3 Н-циклопроп[14,15]эстра-1,3,5(10),8-тетраен-3-ол,15 Н,3 Н-3,3-дифторциклопроп[14,15]эстра-1,3,5(10),8-тетраен-3,17-диол,17-метилен-15 Н,3 Н-циклопроп[14,15]эстра-1,3,5(10),8-тетраен-3-илсульфамат,17-дифторметилен-15 Н,3 Н-циклопроп[14,15]эстра-1,3,5(10),8-тетраен-3-ол,3-метокси-15-метил-3'Н-циклопроп[14,15]эстра-1,3,5(10),8-тетраен-3-ол,15-метил-3 Н-циклопроп[14,15]эстра 1,3,5(10),8-тетраен-3,17-диол,17-дифторметилен-15 Н,3 Н-циклопроп[14,15]эстра-1,3,5(10),8-тетраен-3-ил(тетраметиленимино)сульфонат,17-метилен-3 Н-циклопроп[8,9]-15 Н,3 Нциклопроп[14,15]эстра-1,3,5(10)-триен-3-ол. 3. Применение стероидов по п.1 или 2 для приготовления фармацевтических композиций,предназначенных для профилактики и терапии зависящего от возраста снижения познавательной способности, возрастной и перименопаузальной дисфории, предменструального синдрома, невроза и неврастении, состояний страха и невротических состояний, приступов жара(приливов) вследствие дефицита эстрогена (менопауза, гонадоэктомия, лечение с использованием аналогов GnRH), психогенных подавлений сексуального поведения.
МПК / Метки
МПК: A61K 31/565, A61P 15/12
Метки: нервной, центральной, фармацевтические, эстрогена, восполнения, предназначенные, направленного, композиции, системе, дефицита
Код ссылки
<a href="https://eas.patents.su/11-2707-farmacevticheskie-kompozicii-prednaznachennye-dlya-napravlennogo-vospolneniya-deficita-estrogena-v-centralnojj-nervnojj-sisteme.html" rel="bookmark" title="База патентов Евразийского Союза">Фармацевтические композиции, предназначенные для направленного восполнения дефицита эстрогена в центральной нервной системе</a>
Предыдущий патент: Производные эхинокандина, способ их получения и их применение в качестве противогрибковых средств
Следующий патент: Опорное средство для защитного устройства
Случайный патент: Разветвленные иономеры и способ их получения