Кристаллическая форма vii агомелатина, способ ее получения, применение и содержащая ее фармацевтическая композиция
Номер патента: 23297
Опубликовано: 31.05.2016
Авторы: Тон Лин, Хуан Ю, Чжу Сюйянь, Юань Чжэдун, Ю Сюй, Шань Ханьбинь
Формула / Реферат
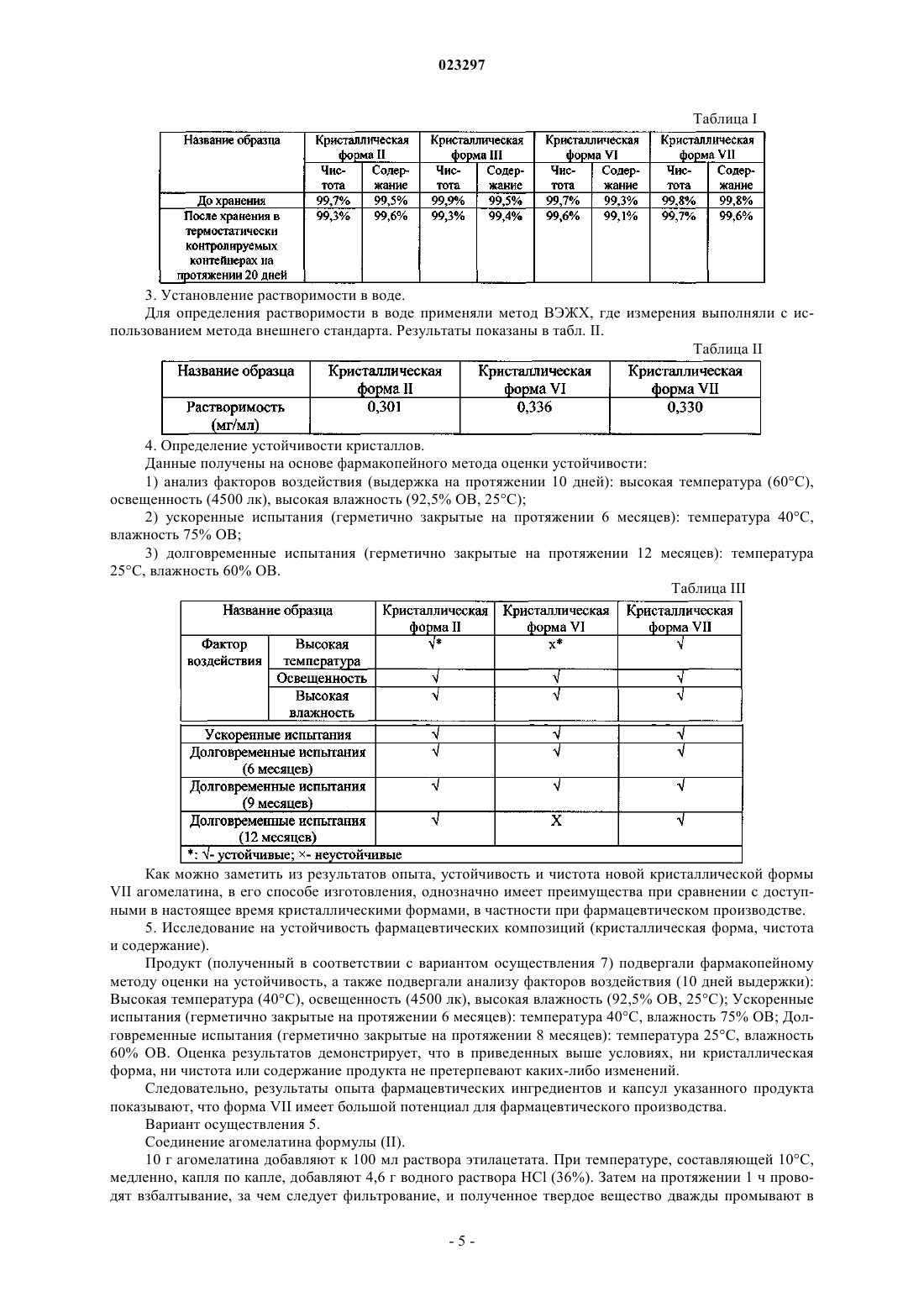
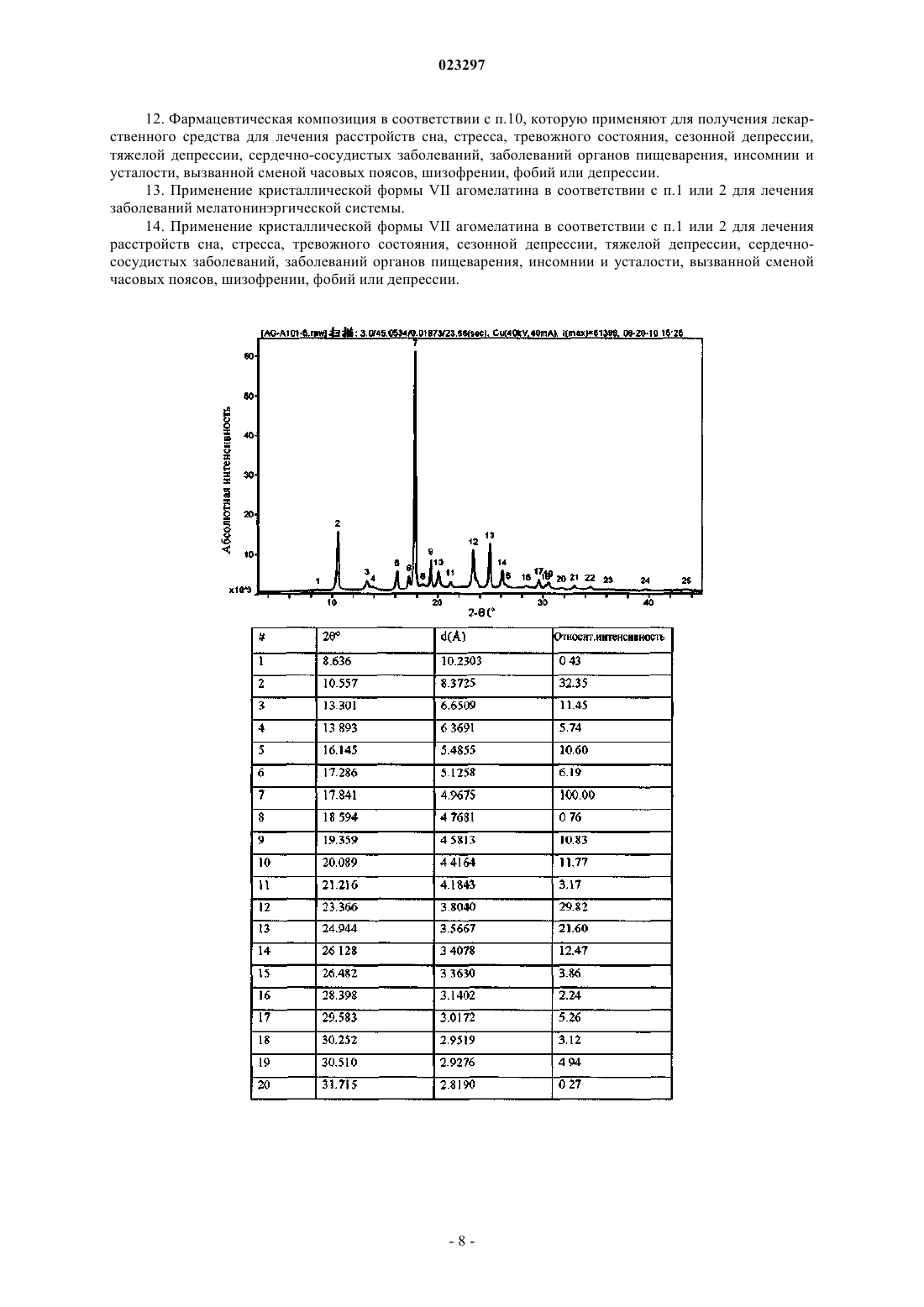
1. Кристаллическая форма VII агомелатина, имеющая следующие значения брэгговского угла 2θ:
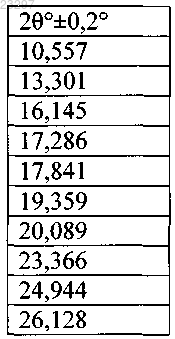
2. Кристаллическая форма VII агомелатина в соответствии с п.1, имеющая следующие значения межплоскостного расстояния кристалла d, брэгговского угла 2θ и относительной интенсивности:
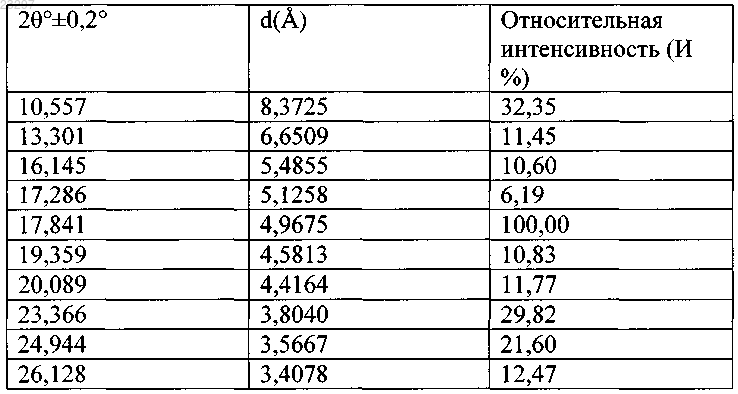
3. Способ получения кристаллической формы VII агомелатина в соответствии с п.1 или 2, где соединения агомелатина формулы (II) или (III) растворяют в уксусной кислоте, к которой затем добавляют ацетат, за чем следует добавление к указанной реакционной смеси капля по капле воды, затем смесь взбалтывают при температуре, составляющей 17-23°C, для того, чтобы вызвать кристаллизацию, и кристаллы отделяют от раствора
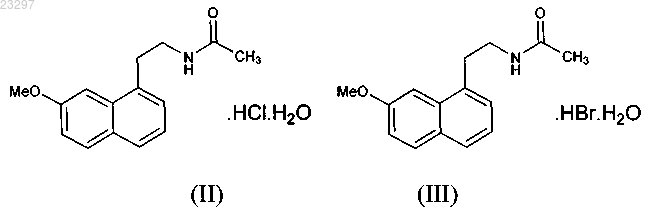
4. Способ получения в соответствии с п.3, где молярное соотношение соединений агомелатина формулы (II) или (III) и ацетата составляет 1:1-1,5, наиболее оптимально 1:1-1,1.
5. Способ получения в соответствии с п.3 или 4, где соотношение объема уксусной кислоты к воде составляет 1:10-30.
6. Способ получения в соответствии с любым из пп.3-5, где указанный ацетат представляет собой ацетат калия или ацетат аммония.
7. Способ получения в соответствии с любым из пп.3-6, в котором, когда температура полученной реакционной смеси достигает 19-25°C, и в частности, когда достигает приблизительно 22 или 23°C, капля по капле добавляют воду для того, чтобы вызвать кристаллизацию.
8. Способ получения в соответствии с любым из пп.3-7, где воду добавляют капля по капле к полученной реакционной смеси, которую затем взбалтывают при температуре 20°C для того, чтобы вызвать кристаллизацию.
9. Способ получения в соответствии с любым из пп.3-8, где после добавления ацетата, реакционную смесь нагревают до температуры 30-50°C, что приводит к получению прозрачного раствора; при этом указанный раствор затем оставляют охлаждаться сам по себе, и капля по капле добавляют воду для того, чтобы вызвать кристаллизацию.
10. Фармацевтическая композиция, обладающая активностью агониста рецепторов мелатонинергической системы и антагониста 5HT2C рецептора, включающая кристаллическую форму VII агомелатина в соответствии с п.1 или 2 и фармацевтически приемлемые адъюванты или вспомогательные вещества.
11. Фармацевтическая композиция в соответствии с п.10, которую применяют для получения лекарственного средства для лечения заболеваний мелатонинэргической системы.
12. Фармацевтическая композиция в соответствии с п.10, которую применяют для получения лекарственного средства для лечения расстройств сна, стресса, тревожного состояния, сезонной депрессии, тяжелой депрессии, сердечно-сосудистых заболеваний, заболеваний органов пищеварения, инсомнии и усталости, вызванной сменой часовых поясов, шизофрении, фобий или депрессии.
13. Применение кристаллической формы VII агомелатина в соответствии с п.1 или 2 для лечения заболеваний мелатонинэргической системы.
14. Применение кристаллической формы VII агомелатина в соответствии с п.1 или 2 для лечения расстройств сна, стресса, тревожного состояния, сезонной депрессии, тяжелой депрессии, сердечно-сосудистых заболеваний, заболеваний органов пищеварения, инсомнии и усталости, вызванной сменой часовых поясов, шизофрении, фобий, или депрессии.
Текст
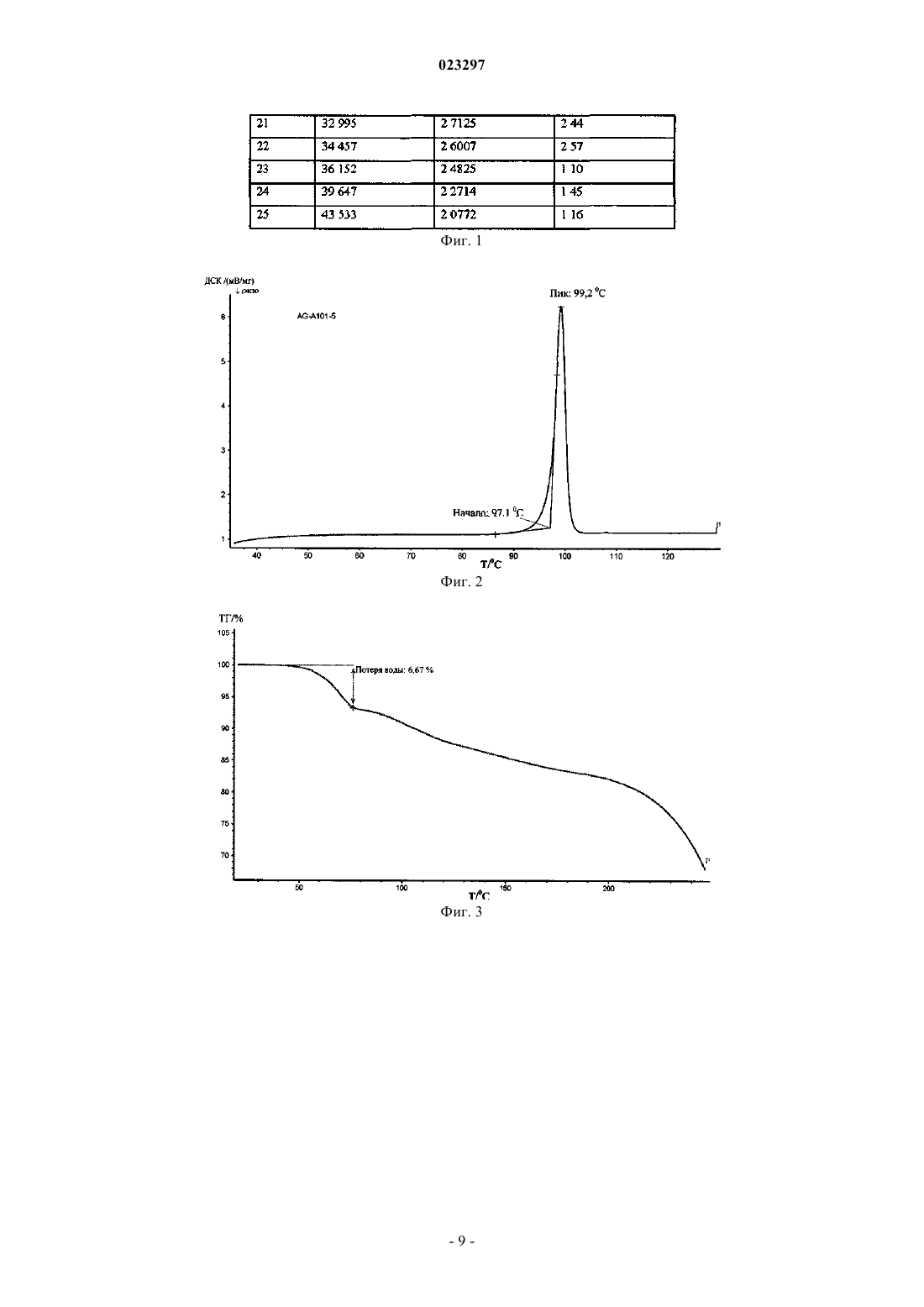
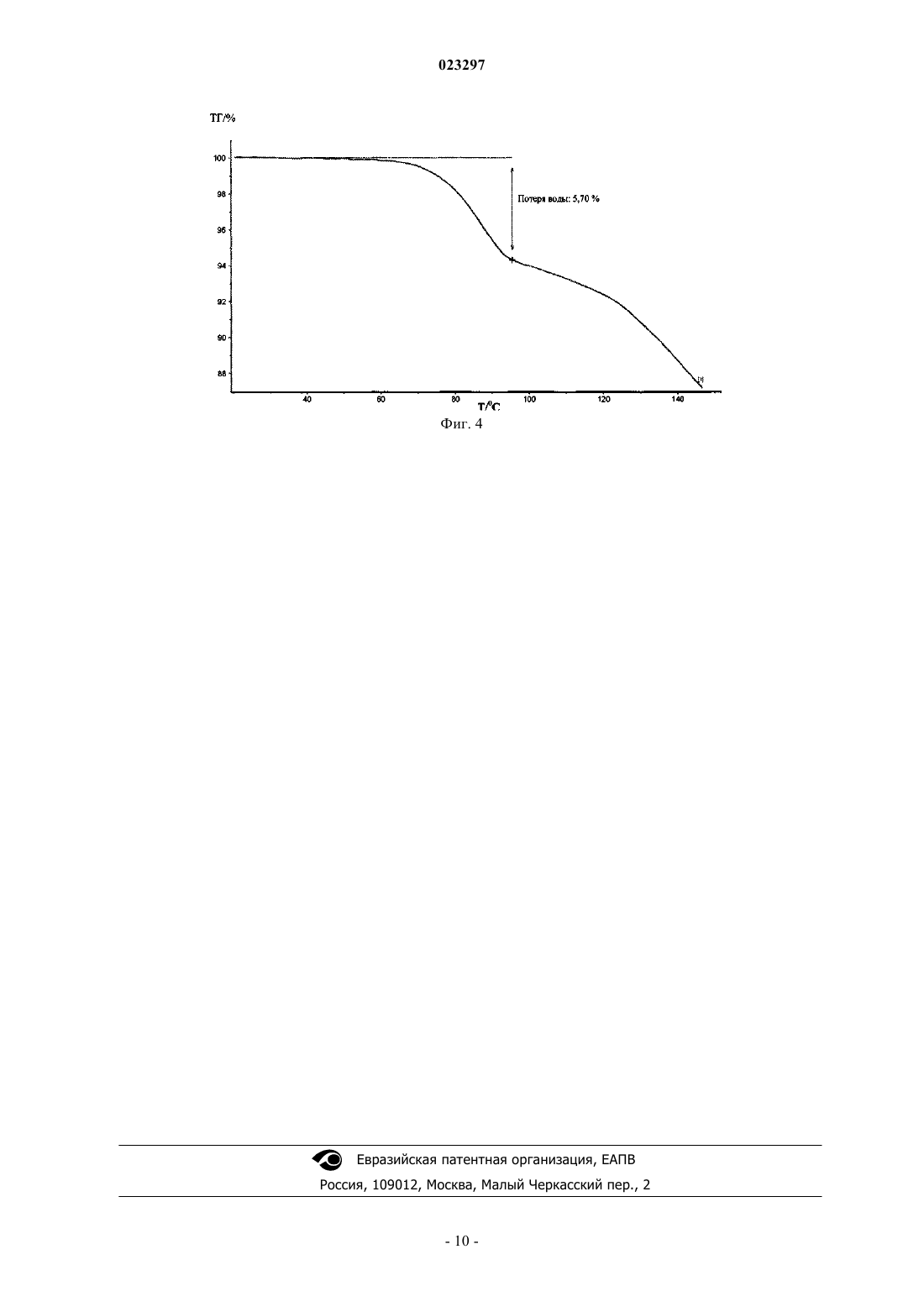
КРИСТАЛЛИЧЕСКАЯ ФОРМА VII АГОМЕЛАТИНА, СПОСОБ ЕЕ ПОЛУЧЕНИЯ,ПРИМЕНЕНИЕ И СОДЕРЖАЩАЯ ЕЕ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ Настоящее изобретение обеспечивает новую кристаллическую форму VII агомелатина, способ ее изготовления, применение и фармацевтическую композицию. Указанная новая кристаллическая форма характеризуется высокой чистотой, устойчивой кристаллической структурой и хорошей воспроизводимостью, при этом способ ее изготовления хорошо пригоден для массового производства. Что касается устойчивости и чистоты, то они превосходят множество кристаллических форм, которые были описаны до настоящего времени. Таким образом,кристаллическая форма VII в соответствии с настоящим изобретением обладает преимуществами для применения в фармацевтическом препарате.(71)(73) Заявитель и патентовладелец: ШАНХАЙ ИНСТИТЬЮТ ОФ ФАРМАСЬЮТИКЛ ИНДАСТРИ(CN); ЛЕ ЛАБОРАТУАР СЕРВЬЕ (FR) Область техники Настоящее изобретение относится к новой кристаллической форме агомелатина, N-[2-(7-метокси-1 нафтил)этил]ацетамиду, к способу его изготовления, к применению и к фармацевтическим композициям. Предшествующий уровень техники Агомелатин, с химическим названием N-[2-(7-метокси-1-нафтил)этил]ацетамид и торговым названием Валдоксан, имеет следующую химическую структуру (I): Он имеет двойное действие, действуя не только как агонист рецепторов мелатонинэргической системы, но также как антагонист 5 НТ 2 С рецептора. Его свойства означают, что он является активным в центральной нервной системе, особенно при лечении тяжелой депрессии, сезонной депрессии, расстройств сна, сердечно-сосудистых заболеваний, заболеваний органов пищеварения, инсомнии и усталости, вызванной сменой часовых поясов, расстройства прима пищи и ожирения. Агомелатин является первым мелатонинэргическим антидепрессантом, а также он является эффективным при лечении депрессии и для улучшения параметров сна, не влияя при этом на сексуальную функцию. Изготовление и терапевтическое применение агомелатина было описано в Европейском патентеEP 0447285. С точки зрения фармацевтического достоинства указанного соединения, является важным получить высокочистую, устойчивую кристаллическую форму с хорошей воспроизводимостью для того, чтобы соединение было предпочтительным в качестве применения в фармацевтическом препарате и было достаточно устойчивым при длительном хранении без предъявления особых требований в отношении условий температуры, освещенности, влажности или уровня кислорода. Китайские патенты CN 200510071611.6, CN 200610108396.7, CN 200610108394.8,CN 200610108395.2, CN 200910047329.2, CN 200910245029.5 сделали публично доступными различные кристаллические формы агомелатина, также как и способы его изготовления. Среди указанных способов кристаллическую форму II изготавливают с помощью вторичной кристаллизации из этанола и воды. Кристаллическую форму III изготавливают с помощью нагрева агомелатина до температуры 110C до тех пор, пока не произойдет полное расплавление, и после этого медленно охлаждают до тех пор, пока происходит кристаллизация. Кристаллическую форму IV изготавливают с помощью нагрева агомелатина до температуры 110C до тех пор, пока не произойдет полное расплавление, а также затем быстро охлаждают до температуры 50-70C и поддерживают температуру, составляющую 70C, на протяжении приблизительно 5 ч до тех пор, пока произойдет кристаллизация; кристаллическую форму V изготавливают посредством так называемого "высокоинтенсивного" механического измельчения агомелатина, при этом кристаллическую форму VI получают в результате вторичной кристаллизации из уксусной кислоты и воды. Хорошо известно, что химические соединения могут демонстрировать различные расположения молекул, а также иметь различные твердые формы, т.е. существует много кристаллических форм того же соединения. В фармацевтических препаратах различные кристаллические формы могут приводить к различиям в растворимости и биодоступности. По этой причине при разработке фармацевтического препарата является особенно важным найти кристаллические структуры, которые являются высокочистыми,обладают хорошей воспроизводимостью, являются легко изготовимыми и применимыми, а также обладают превосходной растворимостью и биодоступностью. Объем изобретения Целью настоящего изобретения является обеспечение новой кристаллической формы агомелатина,т.е. кристаллической формы VII, и вместе с тем также обеспечение способа изготовления кристаллической формы агомелатина. При сравнении с кристаллической формой II доступного в настоящее время Валдоксана, указанная новая кристаллическая форма обеспечивает ценные свойства и способ изготовления, обладающий хорошей воспроизводимостью. Кристаллическая форма VII агомелатина в настоящем изобретении может быть применена при лечении заболеваний мелатонинэргической системы, расстройств сна, стресса, тревожного состояния, сезонной депрессии, тяжелой депрессии, сердечно-сосудистых заболеваний, заболеваний органов пищеварения, инсомнии и усталости, вызванной сменой часовых поясов, шизофрении, фобий, а также депрессии. Настоящее изобретение также ставит своей целью обеспечение способа изготовления кристаллической формы VII агомелатина, который является простым в исполнении и обеспечивает хорошую воспроизводимость. Дополнительная цель настоящего изобретения состоит в обеспечении фармацевтической композиции, которая включает кристаллическую форму VII агомелатина в соответствии с указанным изобретением, также как и фармацевтически приемлемые адъюванты или вспомогательные вещества. Указанная фармацевтическая композиция может быть приспособлена для того, чтобы применяться посредством разных способов применения, в частности для перорального применения или для введения посредством инъекции. В соответствии с природой и серьезностью заболевания, лечение может быть проведено посредством дозировки, отрегулированной в зависимости от возраста и массы пациента. Дозировка может варьироваться в пределах между 0,1 мг и 1 г в день, которую при этом вводят только один или несколько раз. Следующие примеры рентгеновских дифрактограмм кристаллической формы агомелатина в соответствии с настоящим изобретением, с применением брэгговского угла 2, межплоскостных расстояний кристалла d и относительной интенсивности, показывают: Когда используют рентгеновскую дифракцию для анализа кристаллизации в соответствии с настоящим изобретением, иногда, в зависимости от измерительного оборудования или условий опыта, установленные пики показывают небольшие отклонения в значениях измерений; в частности, например,может существовать отклонение в измерении значения 2, которое составляет приблизительно 0,2; даже если применяют очень точное оборудование, отклонение, составляющее приблизительно 0,1 может наблюдаться. В итоге, указанное отклонение необходимо принимать во внимание при определении каждой кристаллической структуры. Условия РД анализа. Модель аппарата: рентгеновский дифрактометр Bruker D8 ADVANCE. Параметры исследования. Детектор: детектор LynxEye. Источник излучения: CuK 40 кВ 40 мА. Монохроматор: Ni фильтрующий диск. Щель расходимости: 1.DivH.L.Slit: 1,0 мм. Зонд: зонд LynxEye. Метод сканирования: - непрерывное сканирование. Диапазон сканирования: 345. Длина шага: 0,02. Скорость сканирования: 8,0/мин. Время сканирования: 5 мин. Температура сканирования: комнатная температура. Условия анализа ДСК. Модель аппарата: NETZSCH DSC 204F1. Условия исследования. Тип тигля: стандартный алюминиевый тигель (перфорированный). Продувочный газ: азот высокой чистоты 20 мл/мин; защитный газ: азот высокой чистоты 60 мл/мин. Диапазон температуры: комнатная температура - 140C. Скорость нагрева: 10C/мин. Условия анализа ТГА. Модель аппарата: NETZSCH TG 209F1. Условия исследования. Тип тигля: Al2O3. Продувочный газ: N2 20 мл/мин; защитный газ: N2 10 мл/мин. Диапазон температуры: комнатная температура - 300C. Скорость нагрева: 10C/мин. Способ изготовления кристаллической формы VII в соответствии с настоящим изобретением включает растворение соединений агомелатина формулы (II) или (III) в уксусной кислоте, к которой затем добав-2 023297 ляют ацетат (предпочтительно ацетат калия или ацетат аммония). Затем к указанной реакционной смеси капля по капле добавляют воду и взбалтывают при температуре, составляющей 17-23C, для того, чтобы вызвать кристаллизацию, где кристаллы затем отделяют от раствора В настоящем изобретении, как описано, нет специальных требований в отношении количества уксусной кислоты, которая должна быть добавлена, при условии, что применяют достаточное количество для растворения исходных материалов, тогда как нагрев также может быть соответствующим образом применен для того, чтобы способствовать растворимости. Молярное соотношение соединений агомелатина формы (II) или (III) и ацетата предпочтительно представляет собой 1 : 1-1.5, наиболее оптимально 1 : 1-1.1. Указанный ацетат включает ацетат калия и ацетат аммония. В способе изготовления в соответствии с настоящим изобретением, как описано, соотношение объема уксусной кислоты к воде составляет 1:10-30. В предпочтительном варианте осуществления способа изготовления кристаллической формы VII в настоящем изобретении, когда температура полученной реакционной смеси достигает 19-25C, а также в частности, когда температура полученной реакционной смеси достигает приблизительно 22C или 23C,то для того, чтобы вызвать кристаллизацию, воду добавляют капля по капле. В дополнительном предпочтительном варианте осуществления, когда к полученной реакционной смеси воду добавляют капля по капле, тогда взбалтывание проводят при температуре, составляющей приблизительно 20C. Указанное может происходить на протяжении периода, который составляет приблизительно 2 ч, для появления кристаллизации. В другом предпочтительном варианте осуществления, вслед за добавлением ацетата, реакционную смесь нагревают до температуры 30-50C, в результате чего получают прозрачный раствор; при этом указанный раствор затем оставляют охлаждаться сам по себе, а также капля по капле добавляют воду для того, чтобы вызвать кристаллизацию. Настоящее изобретение приводит к получению новой кристаллической формы VII агомелатина, с высокой чистотой, при этом устойчивая кристаллическая форма и хорошая воспроизводимость являются подходящими для массового производства, таким образом, дает преимущества при производстве. При сравнении с доступными в настоящее время кристаллическими формами, указанная кристаллическая форма обладает качествами хорошей устойчивости и растворимости. В соответствии с заявками на получение китайского патента CN 201010126254.X иCN 201010126263.9, соединения агомелатина формулы (II) или (III), как описано ранее, могут быть получены посредством следующего способа изготовления, где указанный способ изготовления включает вступление агомелатина в реакцию с различными формами HCl или HBr для того, чтобы образовать гидрат. Два способа представляют собой следующее: агомелатин сначала растворяют в содержащем воду органическом растворителе, после чего добавляют либо HCl, либо газ HBr, твердые кристаллы промывают и затем сушат; или же агомелатин добавляют к растворителю, который содержит HCl или HBr, и твердые кристаллы затем промывают и сушат. Если применяют первый способ, то избыток HCl или HBr может приводить к уменьшению выхода, в то время как во втором способе количество HCl и HBr, которое присутствует в растворителе, легко контролируется. По этой причине второй способ является предпочтительным. В частности, агомелатин может быть добавлен к содержащему воду органическому растворителю,за чем следует добавление капля по капле растворителя, который содержит HCl или HBr. Твердые кристаллы затем промывают и после этого сушат. Подобным образом, также является возможным добавлять агомелатин к органическому растворителю, за чем следует добавление капля по капле водного раствора, который содержит HCl или HBr. Твердые кристаллы затем промывают и после этого сушат. Полное содержание документов ссылки, либо процитированных либо упомянутых в указанной заявке, были приведены в качестве ссылки. Описание графических материалов Фиг. 1 показывает рентгеновскую дифракцию кристаллической формы VII в варианте осуществления 1 в соответствии с настоящим изобретением; фиг. 2 показывает ДСК изменение в тепловой абсорбции кристаллической формы VII в варианте осуществления 1 в соответствии с настоящим изобретением; фиг. 3 показывает кривую термогравиметрического анализа ТГА продукта в варианте осуществления 5 в соответствии с настоящим изобретением; фиг. 4 показывает кривую термогравиметрического анализа ТГА продукта в варианте осуществления 6 в соответствии с настоящим изобретением. Подробное описание вариантов осуществления Следующие варианты осуществления далее описывают настоящее изобретение, но не ограничивают его объем. Вариант осуществления 1. 7,6 г соединения агомелатина формулы (III) растворяют в 19 мл AcOH, к которой добавляют 3,5 гKOAc; смесь затем нагревают до температуры 40C, что приводит к получению прозрачного раствора; указанный раствор затем оставляют охлаждаться сам по себе, при этом он постепенно становится мутным. Когда температура достигает 22C, капля по капле добавляют 250 мл воды. При температуре, составляющей 20C, проводят взбалтывание на протяжении 2 ч, за чем следует фильтрование, затем промывание и сушка отфильтрованного осадка при температуре 50C в вакууме до тех пор, пока не будет достигнута постоянная масса, что приводит к получению 4,5 г твердого вещества белого цвета, чистота: 99,8%, температура плавления: 98-100C. Вариант осуществления 2. 2 г соединения агомелатина формулы (II) растворяют в 5 мл AcOH, к которой затем добавляют 0,57 г NH4OAc; смесь затем нагревают до температуры 40C, что приводит к получению прозрачного раствора; указанный раствор затем оставляют охлаждаться сам по себе, при этом он постепенно становится мутным; когда температура достигает 22C, капля по капле добавляют 150 мл воды, а также при температуре, составляющей 20C, проводят взбалтывание на протяжении 2 ч, за чем следует фильтрование, затем промывание и сушка отфильтрованного осадка при температуре 50C в вакууме до тех пор,пока не будет достигнута постоянная масса, что приводит к получению 1,4 г твердого вещества белого цвета, чистота: 99,7%, температура плавления: 98-100C. Вариант осуществления 3. 40 г соединения агомелатина формулы (III) растворяют в 130 мл AcOH, к которой затем добавляют 10 г NH4OAc; смесь затем нагревают до температуры 40C, что приводит к получению прозрачного раствора; указанный раствор затем оставляют охлаждаться сам по себе, при этом он постепенно становится мутным; когда температура достигает 23C, капля по капле добавляют 2,6 л воды, а также при температуре 20C, проводят взбалтывание на протяжении 2 ч, за чем следует фильтрование, затем промывание и сушка отфильтрованного осадка при температуре 50C в вакууме до тех пор, пока не будет достигнута постоянная масса, что приводит к получению 25 г твердого вещества белого цвета, чистота: 99,8%, температура плавления: 98-100C. Вариант осуществления 4. Каждую из кристаллических форм II, III, VI и VII (полученных в результате варианта осуществления 3) помещают в термостатические контейнеры при температуре, составляющей 40C, и хранят на протяжении 20 дней, где устойчивость указанных кристаллических образцов исследуют с использованием метода высокоэффективной жидкостной хроматографии. 1. Определение чистоты образца. Параметры хроматографирования: силикагель, химически связанный с октадецилсиланом, применяют в качестве наполнителя; смешанный раствор, состоящий из 10 ммоль/л фосфатного буфера (доведенного до pH 7,0 с использованием гидроксида натрия) и ацетонитрила в соотношение 2:7 от объема,действует в качестве подвижной фазы; температура колонки 40 С; и длина волны детектирования составляет 220 нм. Чистоту устанавливали с использованием метода внутреннего стандарта. В подвижной фазе, кристаллические формы II, III, VI и VII распределены в 1 мг/мл растворов,10 мкл каждого из которых затем превращают в жидкостном хроматографе, где регистрируют их хроматограммы. 2. Количественный анализ образца. Применяли метод определения чистоты с использованием контрольного образца, где измерения выполняли с использованием метода внешнего стандарта, результаты показаны в табл. I. 3. Установление растворимости в воде. Для определения растворимости в воде применяли метод ВЭЖХ, где измерения выполняли с использованием метода внешнего стандарта. Результаты показаны в табл. II. Таблица II 4. Определение устойчивости кристаллов. Данные получены на основе фармакопейного метода оценки устойчивости: 1) анализ факторов воздействия (выдержка на протяжении 10 дней): высокая температура (60C),освещенность (4500 лк), высокая влажность (92,5% ОВ, 25C); 2) ускоренные испытания (герметично закрытые на протяжении 6 месяцев): температура 40C,влажность 75% ОВ; 3) долговременные испытания (герметично закрытые на протяжении 12 месяцев): температура 25C, влажность 60% ОВ. Таблица III Как можно заметить из результатов опыта, устойчивость и чистота новой кристаллической формыVII агомелатина, в его способе изготовления, однозначно имеет преимущества при сравнении с доступными в настоящее время кристаллическими формами, в частности при фармацевтическом производстве. 5. Исследование на устойчивость фармацевтических композиций (кристаллическая форма, чистота и содержание). Продукт (полученный в соответствии с вариантом осуществления 7) подвергали фармакопейному методу оценки на устойчивость, а также подвергали анализу факторов воздействия (10 дней выдержки): Высокая температура (40C), освещенность (4500 лк), высокая влажность (92,5% ОВ, 25C); Ускоренные испытания (герметично закрытые на протяжении 6 месяцев): температура 40C, влажность 75% ОВ; Долговременные испытания (герметично закрытые на протяжении 8 месяцев): температура 25C, влажность 60% ОВ. Оценка результатов демонстрирует, что в приведенных выше условиях, ни кристаллическая форма, ни чистота или содержание продукта не претерпевают каких-либо изменений. Следовательно, результаты опыта фармацевтических ингредиентов и капсул указанного продукта показывают, что форма VII имеет большой потенциал для фармацевтического производства. Вариант осуществления 5. Соединение агомелатина формулы (II). 10 г агомелатина добавляют к 100 мл раствора этилацетата. При температуре, составляющей 10C,медленно, капля по капле, добавляют 4,6 г водного раствора HCl (36%). Затем на протяжении 1 ч проводят взбалтывание, за чем следует фильтрование, и полученное твердое вещество дважды промывают в 10 мл этилацетата, затем сушат при температуре, составляющей 40C, в результате чего получают 10,2 г формы II твердого вещества белого цвета; чистота: 99,8%, выход: 88,7%. Элементный анализ Cl: Теоретически вычисленное значение: содержание Cl 11,91 мас.% Установленное значение: содержание Cl 11,86 мас.% Определение содержания воды в кристаллах соединения агомелатина формулы (II): Вычисленное теоретическое содержание воды в кристаллах C15H17NO2HClH2O составляет 6,06 мас.%. 5.1 Метод Фишера (Китайская Фармакопея издание 2010 года, приложение VIII M). Продукт, полученный в соответствии с вариантом осуществления 5, анализировали в соответствии с методом Фишера, как упомянуто выше, и при этом содержание воды в кристаллах было зафиксировано как: 6,15 мас.%. 5.2 Термогравиметрический анализ (Китайская Фармакопея издание 2010 года, приложение VIII Q). Продукт, полученный в соответствии с вариантом осуществления 5, анализировали в соответствии с термогравиметрическим анализом, как упомянуто выше, и при этом потеря воды в кристаллах было зафиксировано как: 6,67 мас.%, т.е. содержание воды в кристаллах исходного продукта составляло 6,67 мас.%. Кривую ТГА, пожалуйста, см. на фиг. 3. Вариант осуществления 6: Соединение агомелатина формулы (III). 100 г агомелатина размешивают и растворяют в 800 мл этилацетата. Водный раствор HBr (8,32 г,40%), при низкой температуре, добавляют капля по капле и затем взбалтывают на протяжении 1 ч перед тем, как подвергнуть фильтрации. Полученное твердое вещество затем промывают дважды в 100 мл этилацетата, затем сушат при температуре, составляющей 40C, в результате чего получают 120 г твердого вещества белого цвета; чистота: 99,9%, выход: 85,3%. Анализ результатов (C15H17NO2HBrH2O)Вычисленное значение:% Br (23,35%). Установленное значение:% Br (23,29%). Определение содержания воды в кристаллах соединения агомелатина формулы (III): Вычисленное теоретическое содержание воды в кристаллах C15H17NO2HBrH2O составляет 5,26 мас.%. 6.1 Метод Фишера (Китайская Фармакопея издания 2010 года, приложение VIII M). Продукт, полученный в соответствии с вариантом осуществления 6, анализировали в соответствии с методом Фишера, как упомянуто выше, и при этом содержание воды в кристаллах было зафиксировано как: 5,10 мас.%. 6.2 Термогравиметрический анализ (Китайская Фармакопея издания 2010 года, приложение VIII Q) Продукт, полученной в соответствии с вариантом осуществления 6, анализировали в соответствии с термогравиметрическим анализом, как упомянуто выше, и при этом потеря воды в кристаллах была зафиксирована как: 5,70 мас.%, т.е. содержание воды в кристаллах исходного продукта составляло 5,70 мас.%. Кривую ТГА, пожалуйста, см. на фиг. 4. Вариант осуществления 7: Изготовление фармацевтической композиции ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Кристаллическая форма VII агомелатина, имеющая следующие значения брэгговского угла 2: 2. Кристаллическая форма VII агомелатина в соответствии с п.1, имеющая следующие значения межплоскостного расстояния кристалла d, брэгговского угла 2 и относительной интенсивности: 3. Способ получения кристаллической формы VII агомелатина в соответствии с п.1 или 2, где соединения агомелатина формулы (II)или (III) растворяют в уксусной кислоте, к которой затем добавляют ацетат, за чем следует добавление к указанной реакционной смеси капля по капле воды, затем смесь взбалтывают при температуре, составляющей 17-23C, для того, чтобы вызвать кристаллизацию, и кристаллы отделяют от раствора 4. Способ получения в соответствии с п.3, где молярное соотношение соединений агомелатина формулы (II) или (III) и ацетата составляет 1:1-1,5, наиболее оптимально 1:1-1,1. 5. Способ получения в соответствии с п.3 или 4, где соотношение объема уксусной кислоты к воде составляет 1:10-30. 6. Способ получения в соответствии с любым из пп.3-5, где указанный ацетат представляет собой ацетат калия или ацетат аммония. 7. Способ получения в соответствии с любым из пп.3-6, в котором, когда температура полученной реакционной смеси достигает 19-25C, и в частности, когда достигает приблизительно 22 или 23C, капля по капле добавляют воду для того, чтобы вызвать кристаллизацию. 8. Способ получения в соответствии с любым из пп.3-7, где воду добавляют капля по капле к полученной реакционной смеси, которую затем взбалтывают при температуре 20C для того, чтобы вызвать кристаллизацию. 9. Способ получения в соответствии с любым из пп.3-8, где после добавления ацетата, реакционную смесь нагревают до температуры 30-50C, что приводит к получению прозрачного раствора; при этом указанный раствор затем оставляют охлаждаться сам по себе, и капля по капле добавляют воду для того,чтобы вызвать кристаллизацию. 10. Фармацевтическая композиция, обладающая активностью агониста рецепторов мелатонинергической системы и антагониста 5HT2C рецептора, включающая кристаллическую форму VII агомелатина в соответствии с п.1 или 2 и фармацевтически приемлемые адъюванты или вспомогательные вещества. 11. Фармацевтическая композиция в соответствии с п.10, которую применяют для получения лекарственного средства для лечения заболеваний мелатонинэргической системы. 12. Фармацевтическая композиция в соответствии с п.10, которую применяют для получения лекарственного средства для лечения расстройств сна, стресса, тревожного состояния, сезонной депрессии,тяжелой депрессии, сердечно-сосудистых заболеваний, заболеваний органов пищеварения, инсомнии и усталости, вызванной сменой часовых поясов, шизофрении, фобий или депрессии. 13. Применение кристаллической формы VII агомелатина в соответствии с п.1 или 2 для лечения заболеваний мелатонинэргической системы. 14. Применение кристаллической формы VII агомелатина в соответствии с п.1 или 2 для лечения расстройств сна, стресса, тревожного состояния, сезонной депрессии, тяжелой депрессии, сердечнососудистых заболеваний, заболеваний органов пищеварения, инсомнии и усталости, вызванной сменой часовых поясов, шизофрении, фобий или депрессии.
МПК / Метки
МПК: C07C 231/24, A61P 25/22, C07C 233/18, A61P 25/00, A61P 25/20, A61P 1/00, A61K 31/165, A61P 25/24, A61P 9/00
Метки: форма, композиция, фармацевтическая, способ, применение, содержащая, получения, агомелатина, кристаллическая
Код ссылки
<a href="https://eas.patents.su/11-23297-kristallicheskaya-forma-vii-agomelatina-sposob-ee-polucheniya-primenenie-i-soderzhashhaya-ee-farmacevticheskaya-kompoziciya.html" rel="bookmark" title="База патентов Евразийского Союза">Кристаллическая форма vii агомелатина, способ ее получения, применение и содержащая ее фармацевтическая композиция</a>
Предыдущий патент: Бытовой прибор с генератором озона (варианты)
Следующий патент: Оксазольные и изоксазольные производные в качестве модуляторов crac