Фармацевтическая композиция, содержащая дротаверин
Номер патента: 22944
Опубликовано: 31.03.2016
Авторы: Джайсваль Нилеш, Прасад Кум, Бадабхагни Судхакара Рао, Кхуллар Правин
Формула / Реферат
1. Фармацевтическая композиция для перорального введения, включающая
5-30% (м/м) дротаверина гидрохлорида;
не менее 60% (м/м) жидкой смеси по меньшей мере одного неионного гидрофильного поверхностно-активного вещества и по меньшей мере одного неионного гидрофобного поверхностно-активного вещества.
2. Фармацевтическая композиция по п.1, в которой общее количество поверхностно-активного вещества находится в диапазоне от 75 до 90%.
3. Фармацевтическая композиция по п.1, в которой неионное гидрофобное поверхностно-активное вещество имеет значение HLB от 4 до 6.
4. Фармацевтическая композиция по п.1, в которой неионное гидрофобное поверхностно-активное вещество представляет собой пропиленгликоля монокаприлат.
5. Фармацевтическая композиция по п.1, в которой гидрофобное поверхностно-активное вещество представлено в количествах от 60 до 90% от массы композиции.
6. Фармацевтическая композиция по п.1, в которой неионное гидрофильное поверхностно-активное вещество имеет значение HLB от 11 до 16.
7. Фармацевтическая композиция по п.1, в которой неионное гидрофильное поверхностно-активное вещество представляет собой полисорбат 80.
8. Фармацевтическая композиция по п.1, в которой неионное гидрофильное поверхностно-активное вещество представлено в количествах от 3 до 7% от массы композиции.
9. Фармацевтическая композиция по п.1, в которой неионное гидрофобное поверхностно-активное вещество представляет собой пропиленгликоля монокаприлат и неионное гидрофильное поверхностно-активное вещество представляет собой полисорбат 80.
10. Фармацевтическая композиция по п.1, в которой массовое соотношение дротаверина гидрохлорида к жидкой смеси поверхностно-активных веществ составляет от 1:3 до 1:7.
11. Фармацевтическая композиция по любому из пп.1-10, в которой конечное значение pH композиции находится между 4 и 6.
12. Фармацевтическая композиция по любому из пп.1-11 в форме мягкой капсулы.
13. Способ получения фармацевтической композиции по любому из пп.1-12, включающий следующие последовательные стадии: растворение дротаверина гидрохлорида в жидкой смеси по меньшей мере одного неионного гидрофильного поверхностно-активного вещества и по меньшей мере одного неионного гидрофобного поверхностно-активного вещества при перемешивании для получения гомогенной смеси; и затем установление pH между 4 и 6, используя обычный буфер.
14. Применение композиции, заявленной в любом из пп.1-12, для получения лекарственного средства для лечения спазмов и острых болей.
Текст
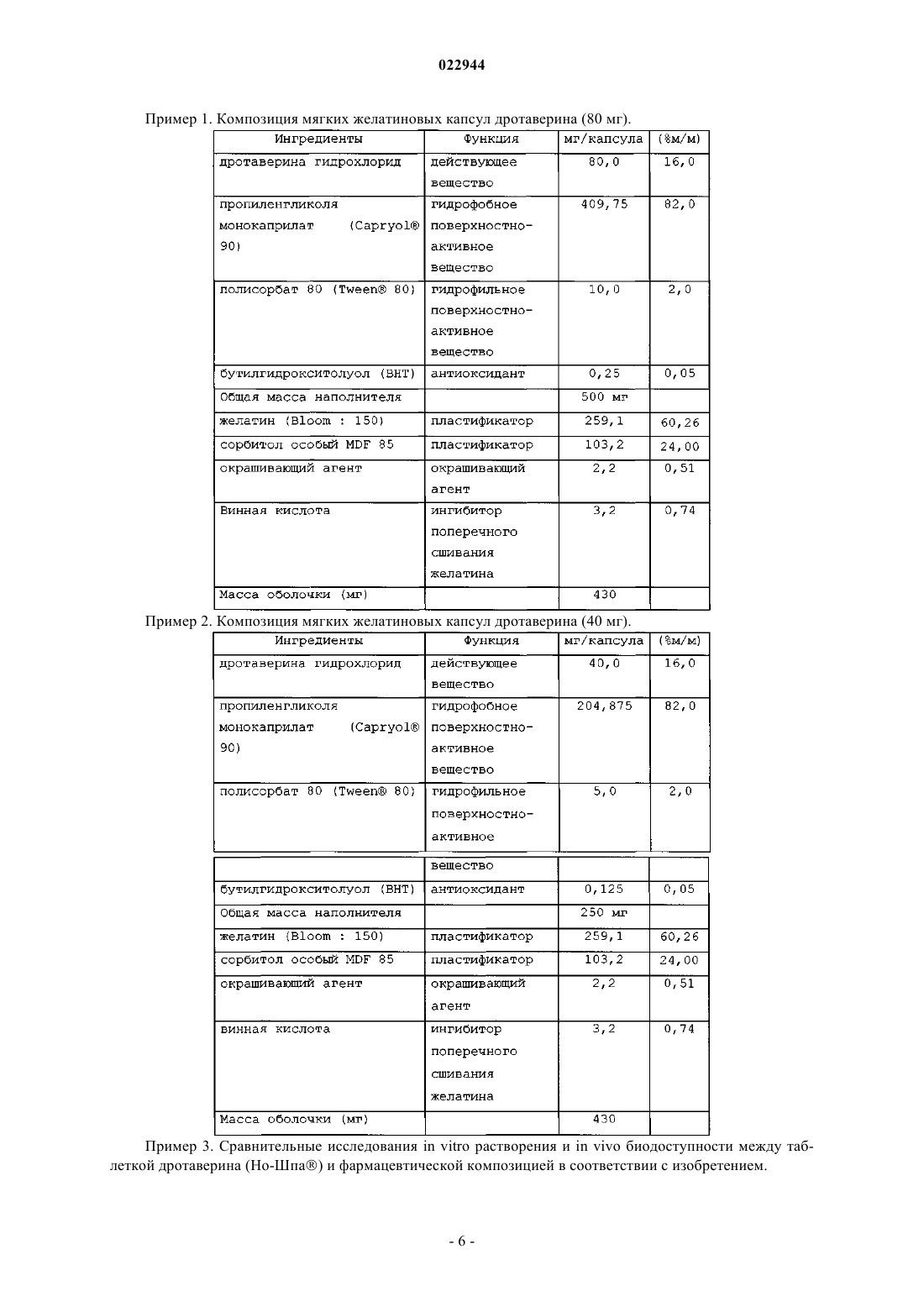
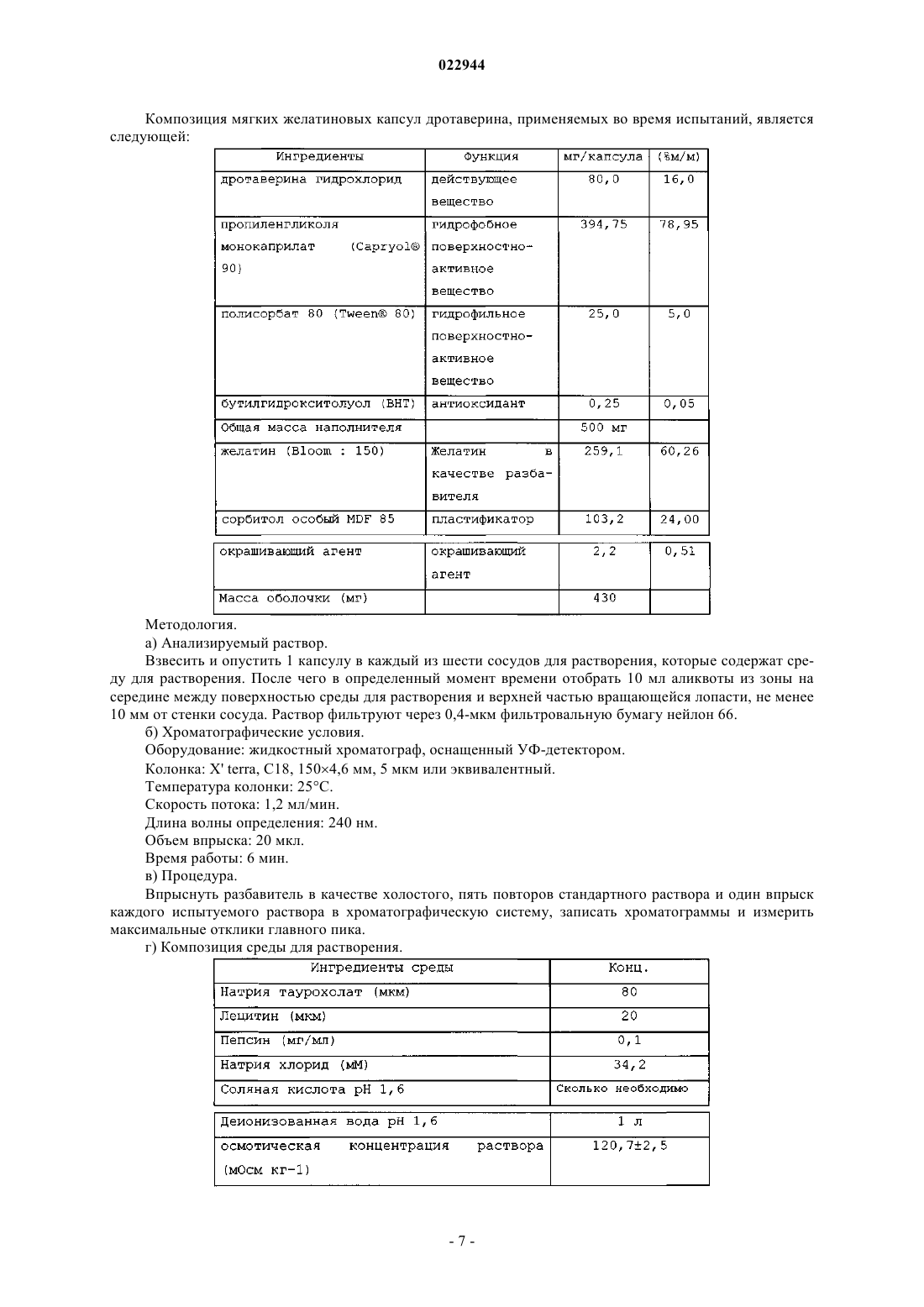
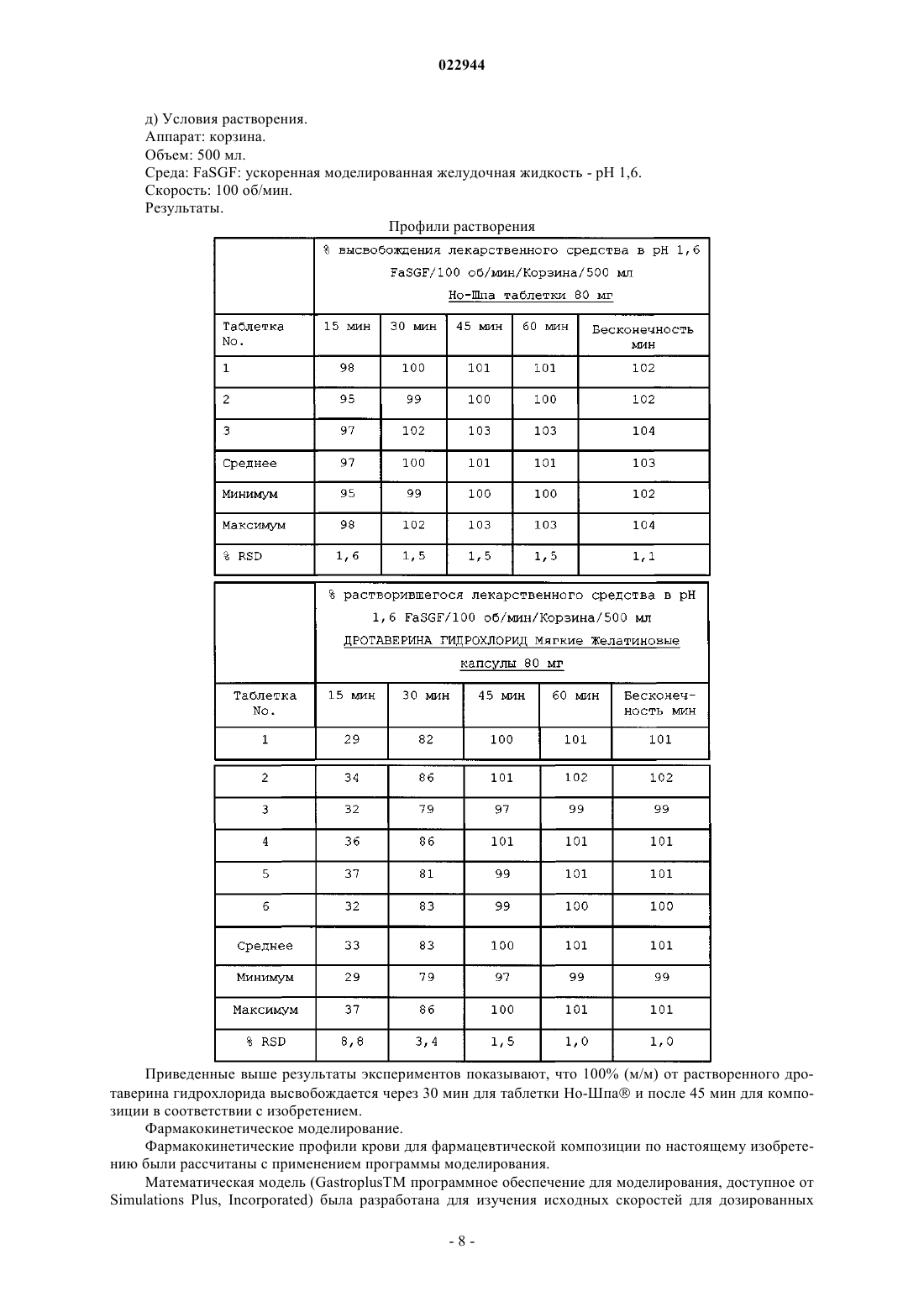
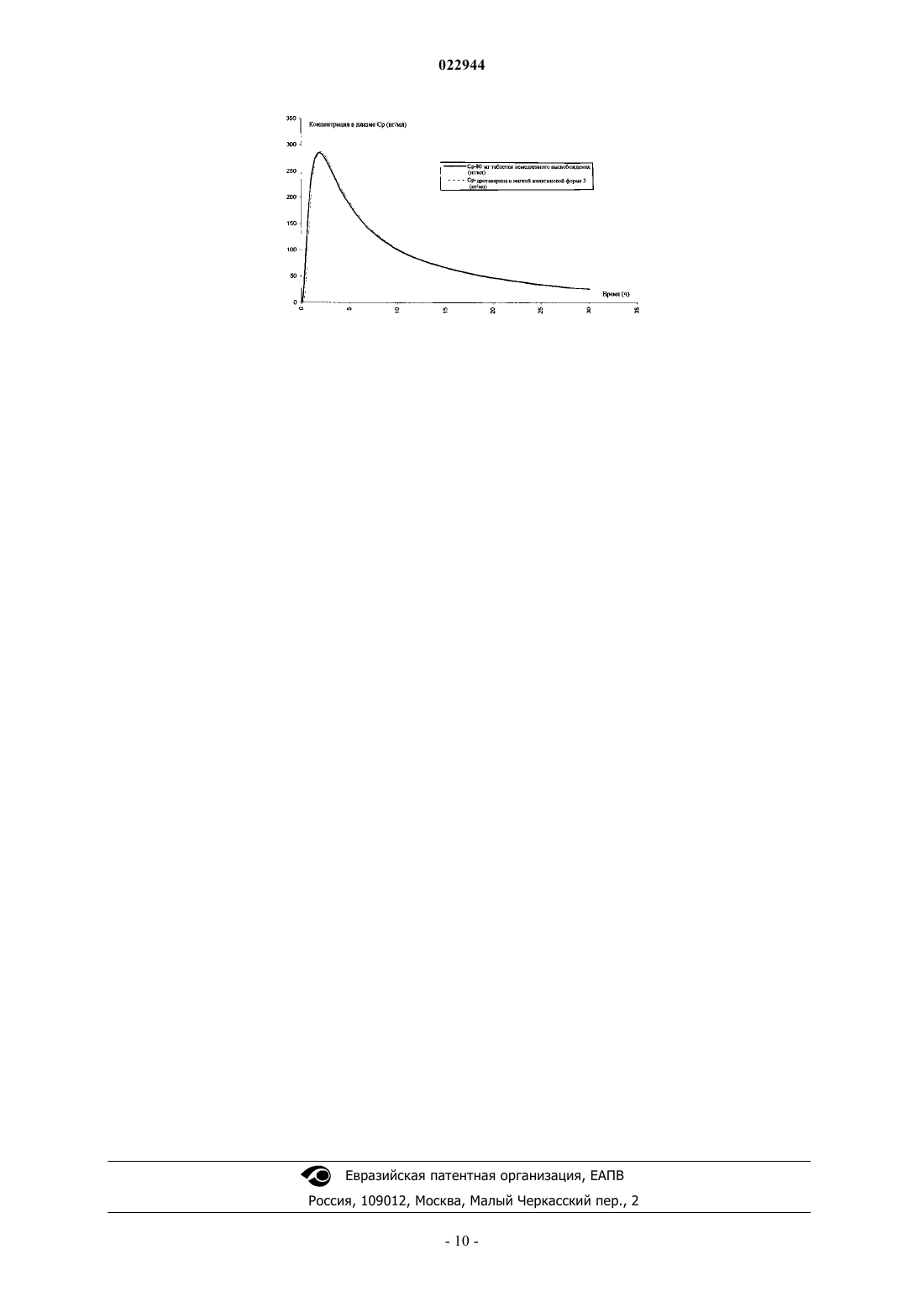
Изобретение относится к фармацевтической композиции дротаверина гидрохлорида в системе растворителя, пригодной в качестве жидкой композиции наполнения. В другом аспекте изобретение также относится к способу получения указанной фармацевтической композиции и к применению указанной композиции для получения лекарственного средства, предназначенного для лечения спазмов и острых болей.(71)(73) Заявитель и патентовладелец: ХИНОИН ПРАЙВИТ КО ЛТД. (HU) Область техники, к которой относится изобретение Настоящее изобретение относится к стабильной фармацевтической композиции дротаверина гидрохлорида для перорального введения. В частности, изобретение относится к композиции, содержащей дротаверина гидрохлорид в подходящей системе растворителя, необязательно заключенной в капсуле. Кроме того, настоящее изобретение также относится к способу получения такой фармацевтической композиции и применения указанной композиции для изготовления лекарственного средства для лечения спазмов и острых болей. Уровень техники изобретения Дротаверин (1-(3,4-диэтоксибензилиден)-6,7-диэтокси-1,2,3,4-тетрагидроизохинолин) принадлежит к классу лекарств, известных как гидроизохинолоны, со следующей формулой: Он относится к фармакологической группе холинергических мускариновых антагонистов на основании механизма действия и также классифицирован в фармакологической группе спазмолитических агентов. Молекулярная масса дротаверина составляет 397,50. Считается, что дротаверин имеет свойства релаксанта гладких мышц. Их эффект зависит от примененной концентрации. Это неантихолинергический спазмолитик, который селективно ингибирует фосфодиэстеразу IV, и это сопровождается умеренным эффектом блокирования кальциевых каналов. Он находится в продаже в форме таблеток под товарным знаком Но-Шпа преимущественно в некоторых странах Восточной и Центральной Европы и в Африке южнее Сахары. Дротаверин, в первую очередь, назначается при таких состояниях, как холангит,холецистит, холецистолитиаз, цистит, нефролитиаз, папиллит, спазм гладких мышц, образование камней,уретеролитиазе, уролитиазе, тенезма мочевого пузыря. Сложностью в составе дротаверина в пероральных фармацевтических композициях является его неприятный, сильный и горький вкус и послевкусие, что привело к недостаточности и даже не соблюдению лечения и, таким образом, имело негативное влияние на эффективность лечения. Кроме того, исследования фармакокинетики и биодоступности, проведенные для пероральной дозы дротаверина гидрохлорида на здоровых людях, показали, что абсолютная биодоступность была непостоянна и изменялась в диапазоне от 24,5 до 91% со средним значением от 58,2 до 18,2% (среднее SD) (European Journal of Drug Metabolism and Pharmacokinetics, vol. 21, Issue: 3, р. 217-221). Предположено, что высокая изменчивость в биодоступности дротаверина гидрохлорида после перорального введения может иметь следствием значительные межиндивидуальные различия в терапевтическом ответе. Объектом настоящего изобретения является предоставление препаратов, таких как мягкая капсула,позволяющих получить фармакокинетические параметры, биоэквивалентные полученным для таблеток дротаверина гидрохлорида в существенно эквивалентной дозе, которая доступна под товарным знаком Но-Шпа. Другим аспектом изобретения является предоставление способа получения пероральной фармацевтической композиции по изобретению, включающего растворение лекарственного средства в подходящем количестве жидкого носителя и приведение pH к приемлемому диапазону, посредством чего достигается устойчивость при хранении и срок годности состава. Другим объектом изобретения является предоставление перорального состава дротаверина гидрохлорида с уменьшенным горьким вкусом. Заявители обнаружили, что эти объекты могут быть получены путем предоставления жидкой композиции, содержащей дротаверина гидрохлорид в жидкой смеси по меньшей мере одного неионного гидрофильного поверхностно-активного вещества и по меньшей мере одного неионного гидрофобного поверхностно-активного вещества. Сущность изобретения Настоящее изобретение предоставляет фармацевтическую композицию дротаверина гидрохлорида для перорального введения, включающую дротаверина гидрохлорид и жидкую смесь по меньшей мере одного неионного гидрофильного поверхностно-активного вещества и по меньшей мере одного неионного гидрофобного поверхностно-активного вещества; фармацевтическая композиция может необязательно содержать допустимые фармацевтически приемлемые эксципиенты. Еще одним объектом настоящего изобретения является предоставление фармацевтической композиции, например мягкой капсулы, твердой капсулы, капсулы из двух частей или таблетки, включающей композицию по настоящему изобретению. В другом аспекте изобретения предоставлен способ получения фармацевтической композиции по изобретению, включающий растворение лекарства в подходящем количестве системы растворителя. Изобретение также относится к применению пероральной фармацевтической композиции изобретения для получения лекарственного средства для лечения спазмов и острых болей. Эти и другие аспекты, признаки и преимущества настоящего изобретения станут более понятны со ссылкой на последующие описание и формулу изобретения. Описание Несколько экспериментов было проведено настоящими авторами для того, чтобы получить жидкую фармацевтическую композицию дротаверина, имеющую биодоступность, сравнимую с полученной для таблетки Но-Шпа, где было неожиданно выявлено, что дротаверин в системе растворителя выполнял главную роль в пероральной биодоступности. Было обнаружено, что дротаверин в жидкой смеси по меньшей мере одного неионного гидрофильного поверхностно-активного вещества и по меньшей мере одного неионного гидрофобного поверхностно-активного вещества позволяет получить биодоступность,эквивалентную полученной для таблетки Но-Шпа."Биоэквивалентный" здесь используется в значении, что если фармацевтическая композиция в соответствии с изобретением проверена в исследовании посредством сравнения с эталонным товарным продуктом, средняя площадь под кривой (AUC) и/или Cmax для каждого лекарственного средства составляет не менее 80% от (соответственной) наблюдаемых средней AUC и/или Cmax. Согласно изобретению стабильный состав означает состав, который, в частности, проявляет высокую устойчивость к разложению дротаверина гидрохлорида. Таким образом, при хранении в течение 1 месяца при 40C и влажности 75% фармацевтическая композиция в соответствии с настоящим изобретением содержит в себе по меньшей мере 99% (м/м) исходного дротаверина гидрохлорида и не проявляет какого-либо признака высокого уровня разложения, т.е. уровень общего количества примесей составляет менее 1% от массы в пересчете на дротаверина гидрохлорид (о чем свидетельствует анализ ВЭЖХ). Дротаверина гидрохлорид взят в терапевтически эффективных количествах. "Терапевтически эффективное количество" следует понимать как значение дозы лекарственного средства, эффективной в проявлении терапевтического эффекта. Для перорального введения изобретения термин "терапевтически эффективное количество" означает дозу лекарственного средства, которая после всасывания в тело через стенки желудочно-кишечного тракта дает концентрацию лекарственного средства в крови, эффективную в проявлении терапевтического эффекта на орган-мишень. Специалисты в данной области техники поймут, что количества лекарственного средства, представленные в композиции, меняются в зависимости от конкретной ситуации, включая, но не ограничиваясь, путь введения, размер, возраст и состояние пациента и тому подобное. Кроме того, эти эффективные количества могут быть легко определены врачом без дополнительного экспериментирования. В композиции по настоящему изобретению дротаверина гидрохлорид представлен в количествах от 5 до 30% от массы композиции. В предпочтительном варианте исполнения дротаверина гидрохлорид представлен в количествах от 10 до 30% от массы композиции. В одном варианте осуществления фармацевтическая композиция содержит смесь по меньшей мере одного неионного гидрофильного поверхностно-активного вещества, которое относится к поверхностноактивным веществам, имеющим значение гидрофильно-липофильного баланса (HLB) от 10 до 18, предпочтительно от 11 до 16; и по меньшей мере одного гидрофобного поверхностно-активного вещества,которое относится к поверхностно-активным веществам, имеющим значение HLB от 4 до 10, предпочтительно от 4 до 6. Система HLB (Fiedler, H.B., Encyclopedia of Excipients, 5th ed., Aulendorf: ECV-EditioCantor-Verlag (2002 присваивает численные значения поверхностно-активным веществам, причем липофильные вещества получают меньшие значения HLB, a гидрофильные вещества получают большие значения HLB. Общее количество поверхностно-активного вещества составляет по меньшей мере 60% и предпочтительно от 60 до 95% от массы, основанной на общей массе композиции. Более предпочтительно, чтобы общее количество поверхностно-активного вещества составляло от 75 до 90% от массы композиции. Предпочтительным поверхностно-активным веществом, используемым в контексте настоящего изобретения, является пропиленгликоль монокаприлат (каприол-90), который имеет значение HLB, равное 6. В композиции по настоящему изобретению является предпочтительным, что гидрофобное поверхностно-активное вещество присутствует в количествах от 60 до 90% от массы композиции. Более предпочтительно, когда гидрофобное поверхностно-активное вещество присутствует в количествах от 80 до 85% от массы композиции. Наиболее предпочтительным гидрофильным поверхностно-активным веществом для включения в фармацевтическую композицию является полисорбат 80 (полиоксиэтилен сорбитан моноолеат; Tween 80), который имеет значение HLB, равное 15. В композиции по настоящему изобретению является предпочтительным, что гидрофильное поверхностно-активное вещество присутствует в количествах от 1 до 10% от массы композиции. Более пред-2 022944 почтительно, когда гидрофильное поверхностно-активное вещество присутствует в количествах от 3 до 7% от массы композиции. В наиболее предпочтительном варианте осуществления по изобретению фармацевтическая композиция является смесью пропиленгликоль монокаприлата (каприол-90) (неионное гидрофобное поверхностно-активное вещество) и полисорбата 80 (неионное гидрофильное поверхностно-активное вещество). В еще одном аспекте настоящее изобретение относится к перорально вводимому составу, содержащему дротаверина гидрохлорид и жидкую смесь по меньшей мере одного неионного гидрофильного поверхностно-активного вещества и по меньшей мере одного неионного гидрофобного поверхностноактивного вещества, в котором массовое соотношение дротаверина гидрохлорида к жидкой смеси поверхностно-активного вещества составляет от 1:2 до 1:10. В предпочтительном варианте осуществления по изобретению массовое соотношение дротаверина гидрохлорида к жидкой смеси составляет от 1:3 до 1:7. Композиция дротаверина в соответствии с настоящим изобретением может дополнительно содержать модификатор вязкости и, необязательно, консервант. Модификаторы вязкости, применяемые в настоящем изобретении, могут быть любыми из известных в данной области, такими как производные целлюлозы, набухающие полимеры, смолы, сополимеры полиоксиэтилена и им подобные. Консерванты, применяемые в настоящем изобретении, могут быть любыми из известных в данной области, такими как натрия метабисульфит, натрия сульфит, натрия бензоат, бензойная кислота, ЭДТА динатриевый, альфа-токоферол, пропилгаллат, бутилированный гидроксианизол и бутилированный гидрокситолуол, аскорбиновая кислота и им подобные. В предпочтительном варианте осуществления pH системы растворителя поддерживается от 4 до 6. Более конкретно, pH находится в диапазоне 4,5-5,8. Наиболее предпочтительно, чтобы pH поддерживался на уровне 4,5. pH системы растворителя может быть отрегулирован с помощью любого обычного буфера. Предпочтительным буфером для применения является ацетатный буфер. Изобретение также относится к способу получения фармацевтического препарата, содержащего 530% от массы композиции дротаверина гидрохлорида, 60-95% от массы композиции жидкой смеси по меньшей мере одного неионного гидрофильного поверхностно-активного вещества и по меньшей мере одного неионного гидрофобного поверхностно-активного вещества. Этот метод содержит следующие стадии: растворение дротаверина гидрохлорида в жидкой смеси по меньшей мере одного неионного гидрофильного поверхностно-активного вещества и по меньшей мере одного неионного гидрофобного поверхностно-активного вещества при перемешивании для получения гомогенной смеси; и затем установление pH между 4 и 6, используя обычный буфер. Один аспект изобретения предоставляет мягкие желатиновые капсулы, которые включают оболочку капсулы, содержащую желатин и/или пластификаторы и, при желании или необходимости, другие вспомогательные материалы. При разработке мягкой желатиновой капсулы для композиции дротаверина в соответствии с настоящим изобретением должно быть очевидно, что капсула является системой, содержащей композицию дротаверина и желатиновую оболочку, применяемую для капсулирования композиции дротаверина. Таким образом, не только наполненная композиция дротаверина предпочтительна для получения желаемых характеристик пероральной биодоступности, но и состав желатиновой оболочки также является предпочтительным, так как он должен быть совместим с композицией дротаверина. Специалист в данной области техники знает о потенциальных взаимодействиях наполнителя и оболочки, которые могут привести как к физической, так и к химической нестабильности капсулы. Соответственно композиция желатиновой оболочки, используемая для формирования капсулы для композиции дротаверина, также является предпочтительной и значимой для настоящего изобретения. В общем, композиция желатиновой оболочки капсулы для мягких желатиновых капсул состоит из необработанного желатина и одного или нескольких ингредиентов, которые добавляются для пластификации желатина с получением капсулы подходящей твердости в соответствии с требованиями проекта или предпочтениями. Типичные пластификаторы включают глицерин и сорбитол. Также ангидриды сорбитана и маннитол тоже могут быть использованы. Кроме того, другие нетрадиционные ингредиенты также могут быть использованы для пластификации желатина. Главной проблемой в композициях на основе желатина является видимое снижение растворения при старении, что связано с поперечным сшиванием желатинсодержащих продуктов. Поперечное сшивание является причиной образования разбухшей, очень тонкой, тугой, резиноподобной, нерастворимой в воде мембраны, также известной как тонкая пленка. Тонкая пленка действует как барьер и ограничивает высвобождение лекарственного средства. Лекарственные средства наподобие дротаверина или его фармацевтически приемлемых солей или гидратов имеют тенденцию реагировать с желатином и индуцировать поперечное сшивание, из-за чего возможность снижения растворения в течение исследований стабильности является высокой. Авторы настоящего изобретения обнаружили, что такое поперечное сшивание желатина неожиданно преодолевается путем добавления некоторых слабых кислот в сочетании с глицином. В конкретном варианте осуществления по изобретению слабой кислотой, используемой в настоящем изобретении, является винная кислота, лимонная кислота или их комбинации. Слабая кислота может присутствовать в количестве от примерно 0,1 до 1,0% на массу основы состава желатиновой оболочки. Как таковые, композиции желатина, подходящие для применения с композицией дротаверина по настоящему изобретению, обеспечивают требуемую необходимую физическую и химическую стабильность. Предпочтительная композиция желатина для применения при создании мягких желатиновых капсул для применения с композицией дротаверина по настоящему изобретению включает в себя желатин и пластификатор. Такой пластификатор, который хорошо известен в области техники фармацевтической композиции, включает, например, пропиленгликоль и сорбитол. Подходящие пластификаторы для применения с предпочтительной композицией капсулы включают сорбитол, такой как Special MDF 85 отSPI Pharma. Композиции капсульные могут также включать другие подходящие добавки, такие как консерванты и/или окрашивающие агенты, которые используются, чтобы стабилизировать капсулу и/или придать определенную характеристику, такую как цвет или внешний вид капсулы. Фармацевтически приемлемые консерванты могут включать, например, метил- и пропилпарабены. Цвет может быть придан желатиновой оболочке при применении FDC и/или DC красителей. Примерные красители включают, но не ограничиваются ими, тартразин желтый, азура красный и тому подобные. Замутнители, такие как диоксид титана и/или оксиды железа, могут быть использованы для того, чтобы окрасить и/или сделать капсулу непрозрачной. Изобретение предполагает использование покрывающих агентов, которые могут включать как нефункциональные, так и кишечнорастворимые покрывающие агенты, например полимеры на основе целлюлозы, пленочные покрывающие агенты или другие покрывающие агенты, известные специалистам в данной области техники. Настоящее изобретение также предусматривает применение других фармацевтических вспомогательных веществ, таких как буферные агенты, подкислители, подщелачиватели, связующие вещества,разрыхлители, разбавители, смазывающие вещества, пластификаторы, усилители проницаемости и растворители, известных специалисту в данной области техники. Другие добавки, обычно применяемые в фармацевтических композициях, могут быть включены, и эти добавки хорошо известны в данной области техники. Такие добавки включают антиоксиданты, такие как бутилгидрокситолуол (ВНТ), консерванты, хелатирующие агенты, комплексообразующие агенты,модификаторы вязкости, тонизаторы, ароматизаторы, пигменты, отдушки, замутнители, суспендирующие агенты, связующие вещества и их смеси. Количества таких добавок могут быть легко определены специалистом в данной области техники в зависимости от конкретных желаемых свойств. Точная доза активного агента и конкретной композиции для введения зависят от ряда факторов, например от состояния, подлежащего лечению, требуемой продолжительности лечения и скорости высвобождения активного агента. Например, количество требуемого активного агента и скорость высвобождения вследствие этого могут быть определены на основе известных in vitro или in vivo методик, определяющих, как долго концентрация конкретного действующего вещества в плазме крови остается на приемлемом уровне для терапевтического эффекта. Как только основные принципы реализации фармацевтических композиций в соответствии с настоящим изобретением в форме мягких желатиновых капсул становятся понятны, эксперту по фармацевтическим композициям не составит никакой сложности в адаптации критериев способа под конкретные нужды. Еще одним аспектом настоящего изобретения является создание способа введения фармацевтически активного ингредиента пациенту с учетом изменчивости в биодоступности фармацевтически активного агента дротаверина, который содержит стадии а) предоставления стабильной желатиновой композиции по изобретению для перорального введения и б) введения указанной композиции в указанный организм для приема внутрь. В дополнительном варианте осуществления активный агент содержит приблизительно 40-80 мг основной композиции. Основные ингредиенты типичной композиции в соответствии с настоящим изобретением могут содержать приблизительно 5-30% (м/м) активного агента, предпочтительно соль дротаверина или гидраты,по меньшей мере 60% (м/м) жидкой смеси по меньшей мере одного неионного гидрофильного поверхностно-активного вещества и по меньшей мере одного неионного гидрофобного поверхностноактивного вещества. Буферный агент, применяемый в настоящем изобретении, может быть любым из известных в данной области техники, таким как уксусная кислота, фосфорная кислота, фосфат калия, щавелевая кислота,угольная кислота, натрия карбонат, натрия ацетат, натрия цитрат, лития оксалат, аммония гидроксид,аммония нитрат, лимонная кислота, натрия бикарбонат, глицин и т.д. и/или их комбинации. Подщелачиватель, применяемый в настоящем изобретении, может быть выбран из кальция карбо-4 022944 ната, магния гидроксида, аравийской камеди, дикальцийфосфата, калия гидроксида, аскорбиновой кислоты и т.д. и/или их комбинаций. Подкислитель, применяемый в настоящем изобретении, может быть выбран из молочной кислоты,аскорбиновой кислоты, лимонной кислоты, фосфорной кислоты, кальция хлорида и т.д. и/или их комбинаций. Ингредиенты желатиновой оболочки типичной композиции в соответствии с настоящим изобретением могут содержать 35-52% (м/м), более предпочтительно 40-44% желатина,15-35% (м/м), более предпочтительно 15-25% сорбитола и/или глицерина,0,1-10% (м/м) окрашивающих агентов,0,1-10% (м/м) винной кислоты. В другом предпочтительном варианте осуществления активный наполнитель (основной состав) по изобретению заключен в мягкую желатиновую капсулу круглой/овальной формы. В еще одном аспекте настоящего изобретения предложен способ получения фармацевтической композиции. Способ содержит включение активного ингредиента дротаверина или его фармацевтически приемлемой соли или их гидратов в липофильный и/или гидрофильный носитель. Дополнительно, при необходимости, подходящие фармацевтические эксципиенты добавляются, чтобы образовать эмульсию лекарственного средства. В предпочтительном варианте осуществления подходящий носитель непрерывно перемешивают с активным ингредиентом. Эксципиенты затем смешивают. Мягкие желатиновые капсулы получены с применением способа роторной штамповки, используя желатин в обычном способе. Гранулы сухого желатина соединяют с водой и подходящими пластификаторами, и эту комбинацию затем смешивают и нагревают под вакуумом, чтобы сформировать расплавленную массу желатина. Массу желатина поддерживают в расплавленном состоянии, пока она формуется или отливается в пленки или ленты на отливочных колесах или барабанах. Пленки или ленты подают под клин и между роторными штампами для капсулирования. Внутри штампов для капсулирования капсулы одновременно образуются в углублениях штампов из пленок или лент. Композицией, содержащей дротаверин, наполняют мягкие желатиновые капсулы, применяя любой традиционный способ. Капсулу затем вырезают и запаивают. Запайки формируются посредством сочетания давления и нагрева, как только капсула заполнена и вырезана. Настоящее изобретение дополнительно определено в последующих примерах. Следует понимать,что эти примеры, показывающие предпочтительные варианты осуществления по изобретению, даются только в качестве иллюстрации. Из приведенного выше обсуждения и этих примеров специалист в данной области техники может выяснить основные характеристики настоящего изобретения и без отклонения от сущности и объема изобретения может делать различные изменения и модификации изобретения,чтобы адаптировать его к различным применениям и условиям. Примеры Хотя изобретение было описано в связи с конкретными вариантами осуществления, несомненно,что многие альтернативы и варианты будут очевидны специалистам в данной области техники в свете приведенного выше описания. Соответственно настоящее изобретение предназначено, чтобы охватить все альтернативы и варианты, которые попадают в пределы сущности и объема изобретения. Пример 1. Композиция мягких желатиновых капсул дротаверина (80 мг). Пример 2. Композиция мягких желатиновых капсул дротаверина (40 мг). Пример 3. Сравнительные исследования in vitro растворения и in vivo биодоступности между таблеткой дротаверина (Но-Шпа) и фармацевтической композицией в соответствии с изобретением. Композиция мягких желатиновых капсул дротаверина, применяемых во время испытаний, является следующей: Методология. а) Анализируемый раствор. Взвесить и опустить 1 капсулу в каждый из шести сосудов для растворения, которые содержат среду для растворения. После чего в определенный момент времени отобрать 10 мл аликвоты из зоны на середине между поверхностью среды для растворения и верхней частью вращающейся лопасти, не менее 10 мм от стенки сосуда. Раствор фильтруют через 0,4-мкм фильтровальную бумагу нейлон 66. б) Хроматографические условия. Оборудование: жидкостный хроматограф, оснащенный УФ-детектором. Колонка: X' terra, C18, 1504,6 мм, 5 мкм или эквивалентный. Температура колонки: 25C. Скорость потока: 1,2 мл/мин. Длина волны определения: 240 нм. Объем впрыска: 20 мкл. Время работы: 6 мин. в) Процедура. Впрыснуть разбавитель в качестве холостого, пять повторов стандартного раствора и один впрыск каждого испытуемого раствора в хроматографическую систему, записать хроматограммы и измерить максимальные отклики главного пика. г) Композиция среды для растворения. д) Условия растворения. Аппарат: корзина. Объем: 500 мл. Среда: FaSGF: ускоренная моделированная желудочная жидкость - pH 1,6. Скорость: 100 об/мин. Результаты. Профили растворения Приведенные выше результаты экспериментов показывают, что 100% (м/м) от растворенного дротаверина гидрохлорида высвобождается через 30 мин для таблетки Но-Шпа и после 45 мин для композиции в соответствии с изобретением. Фармакокинетическое моделирование. Фармакокинетические профили крови для фармацевтической композиции по настоящему изобретению были рассчитаны с применением программы моделирования. Математическая модель (GastroplusTM программное обеспечение для моделирования, доступное отSimulations Plus, Incorporated) была разработана для изучения исходных скоростей для дозированных лекарственных форм дротаверина, которые отвечали бы конкретным мишеням высвобождения in vivo.Gastroplus представляет собой компьютерную программу, которая моделирует всасывание и фармакокинетику для перорально дозированных лекарственных средств. Базовой моделью является модель Улучшенного Блочного Всасывания и Передачи (АСАТ) - расширение работы, изначально сделаннойGastroplus был применен для моделирования всасывания и фармакокинетики эталонных и анализируемых составов. Профили растворения in vitro составов дротаверина гидрохлорида (описанных выше) были применены в качестве исходных функций для моделирования всасывания и фармакокинетики эталонных (находящихся в продаже таблеток Но-Шпа 80 мг) и анализируемых составов. На чертеже показаны результаты применения модели для моделирования биодоступности in vivo таблеток Но-Шпа 80 мг и фармацевтической композиции в соответствии с изобретением, содержащей 80 мг дротаверина гидрохлорида. Эта модель была применена, чтобы оценить степень эффективности дозированных форм по изобретению. Эти данные показывают, что дозированные формы по настоящему изобретению будут эффективны. Было обнаружено, что отношения AUC и Cmax сопоставимы для состава мягкого геля и таблетки дротаверина гидрохлорида на 80 мг, применяя программное обеспечение Gastro Plus. Предшествующие обсуждение и описание являются иллюстративными для некоторых вариантов осуществления по настоящему изобретению, но не предназначены, чтобы быть ограничениями на этой практике. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Фармацевтическая композиция для перорального введения, включающая 5-30% (м/м) дротаверина гидрохлорида; не менее 60% (м/м) жидкой смеси по меньшей мере одного неионного гидрофильного поверхностно-активного вещества и по меньшей мере одного неионного гидрофобного поверхностно-активного вещества. 2. Фармацевтическая композиция по п.1, в которой общее количество поверхностно-активного вещества находится в диапазоне от 75 до 90%. 3. Фармацевтическая композиция по п.1, в которой неионное гидрофобное поверхностно-активное вещество имеет значение HLB от 4 до 6. 4. Фармацевтическая композиция по п.1, в которой неионное гидрофобное поверхностно-активное вещество представляет собой пропиленгликоля монокаприлат. 5. Фармацевтическая композиция по п.1, в которой гидрофобное поверхностно-активное вещество представлено в количествах от 60 до 90% от массы композиции. 6. Фармацевтическая композиция по п.1, в которой неионное гидрофильное поверхностно-активное вещество имеет значение HLB от 11 до 16. 7. Фармацевтическая композиция по п.1, в которой неионное гидрофильное поверхностно-активное вещество представляет собой полисорбат 80. 8. Фармацевтическая композиция по п.1, в которой неионное гидрофильное поверхностно-активное вещество представлено в количествах от 3 до 7% от массы композиции. 9. Фармацевтическая композиция по п.1, в которой неионное гидрофобное поверхностно-активное вещество представляет собой пропиленгликоля монокаприлат и неионное гидрофильное поверхностноактивное вещество представляет собой полисорбат 80. 10. Фармацевтическая композиция по п.1, в которой массовое соотношение дротаверина гидрохлорида к жидкой смеси поверхностно-активных веществ составляет от 1:3 до 1:7. 11. Фармацевтическая композиция по любому из пп.1-10, в которой конечное значение pH композиции находится между 4 и 6. 12. Фармацевтическая композиция по любому из пп.1-11 в форме мягкой капсулы. 13. Способ получения фармацевтической композиции по любому из пп.1-12, включающий следующие последовательные стадии: растворение дротаверина гидрохлорида в жидкой смеси по меньшей мере одного неионного гидрофильного поверхностно-активного вещества и по меньшей мере одного неионного гидрофобного поверхностно-активного вещества при перемешивании для получения гомогенной смеси; и затем установление pH между 4 и 6, используя обычный буфер. 14. Применение композиции, заявленной в любом из пп.1-12, для получения лекарственного средства для лечения спазмов и острых болей.
МПК / Метки
МПК: A61K 31/485, A61K 31/47, A61K 9/48
Метки: композиция, фармацевтическая, дротаверин, содержащая
Код ссылки
<a href="https://eas.patents.su/11-22944-farmacevticheskaya-kompoziciya-soderzhashhaya-drotaverin.html" rel="bookmark" title="База патентов Евразийского Союза">Фармацевтическая композиция, содержащая дротаверин</a>
Предыдущий патент: Антагонисты рецепторов trpm8
Следующий патент: Способ формирования термочувствительных нанокомпозиционных фотонных кристаллов
Случайный патент: Способ снижения содержания цветного металла в шлаке при получении цветного металла в печи взвешенной плавки