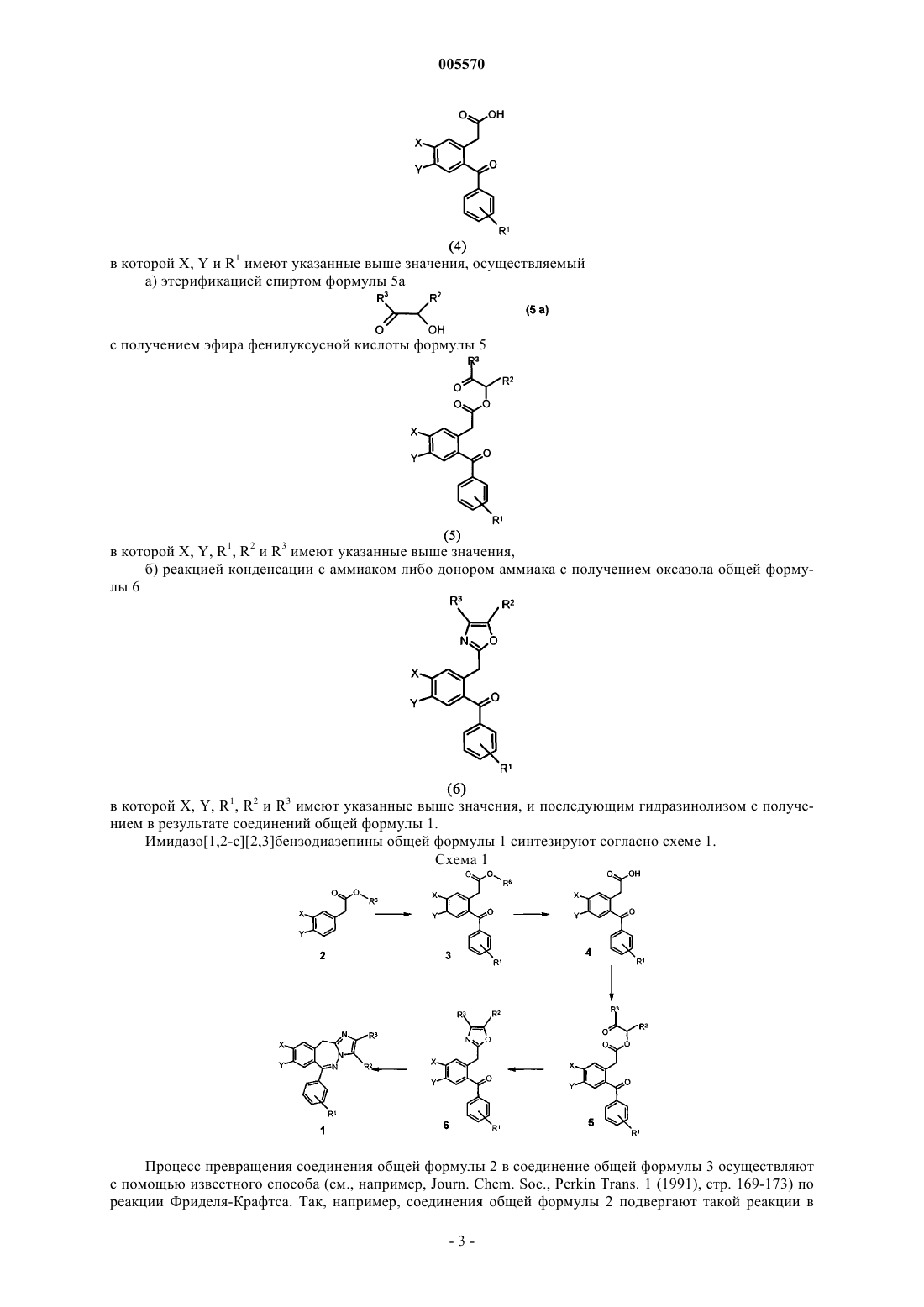
Способ получения имидазо[1,2-c][2,3]бензодиазепинов и получаемые по этому способу промежуточные продукты
Формула / Реферат
1. Способ получения имидазо[1,2-c][2,3]бензодиазепинов общей формулы 1
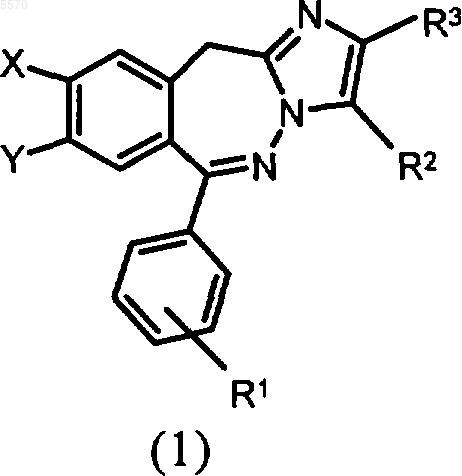
в которой
R1 обозначает водород, C1-C6алкил, нитрогруппу, галоген, цианогруппу, C1-C4алкоксигруппу, -CF3, гидроксигруппу или C1-C6алканоилоксигруппу,
R2 и R3 имеют идентичные или разные значения и обозначают водород, галоген, C1-C6алкоксигруппу, гидроксигруппу, цианогруппу, C1-C6алканоил, C2-C6алкинил, C2-C6алкенил, необязательно замещенный галогеном, гидроксигруппой либо C1-C6алкоксигруппой C1-C6алкил, C3-C7циклоалкил или необязательно замещенный галогеном, C1-C4алкоксигруппой либо C1-C4алкилом арил или гетероарил,
X обозначает водород или галоген,
Y обозначает C1-C6алкоксигруппу или
X и Y вместе обозначают -O-(CH2)n-O-, где
n обозначает 1, 2 или 3,
из фенилуксусных кислот общей формулы 4
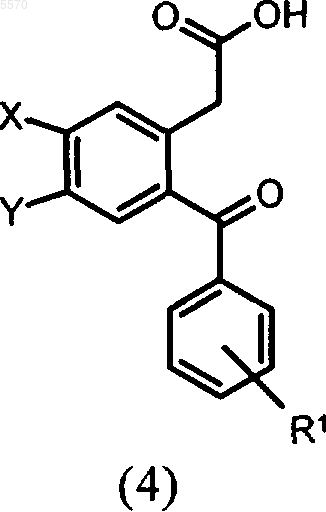
в которой X, Y и R1 имеют указанные выше значения, заключающийся в том, что осуществляют
а) этерификацию спиртом формулы 5а
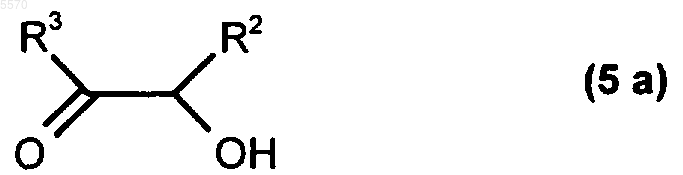
с получением эфира фенилуксусной кислоты формулы 5

в которой X, Y, R1, R2 и R3 имеют указанные выше значения,
б) реакцию конденсации с аммиаком либо донором аммиака с получением оксазола общей формулы 6
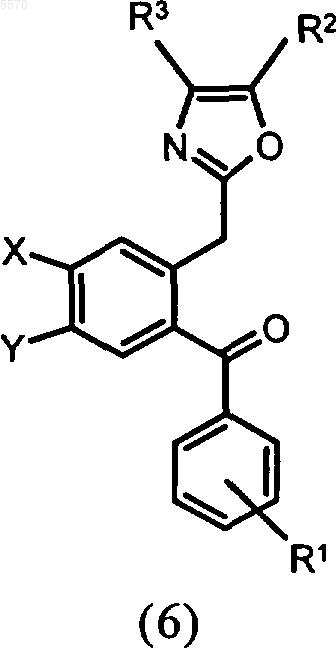
в которой X, Y, R1, R2 и R3 имеют указанные выше значения, и последующий гидразинолиз с получением в результате соединений общей формулы 1
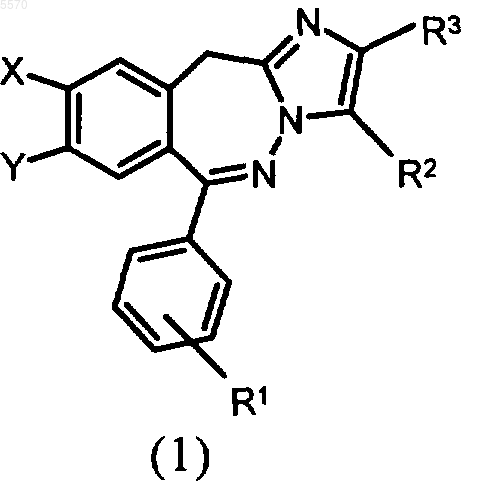
в которой X, Y, R1, R2 и R3 имеют указанные выше значения.
2. Способ по п.1, в котором соединения общей формулы 5 по реакции получения в одном аппарате взаимодействием с ацетатом аммония и аммиаком либо донором аммиака при температуре в интервале от 0 до 150шC в растворителе или смеси растворителей, а затем взаимодействием с гидразином при температуре в интервале от 0 до 200шC, необязательно в автоклаве, превращают в соединения общей формулы 1.
3. Способ по п.1 или 2, предназначенный для получения
2,3-диметил-6-фенил-(12H)-[1,3]диоксоло[4,5-h]имидазо[1,2-c][2,3]бензодиазепина,
2,3-диметил-6-(4-хлорфенил)-(12H)-[1,3]диоксоло[4,5-h]имидазо[1,2-c][2,3]бензодиазепина,
2,3-диметил-6-(4-нитрофенил)-(12H)-[1,3]диоксоло[4,5-h]имидазо[1,2-c][2,3]бензодиазепина,
2,3-диметил-6-(4-метоксифенил)-(12H)-[1,3]диоксоло[4,5-h]имидазо[1,2-c][2,3]бензодиазепина,
2,3-диэтил-6-фенил-(12H)-[1,3]диоксоло[4,5-h]имидазо[1,2-c][2,3]бензодиазепина,
2,3-дифенил-6-фенил-(12H)-[1,3]диоксоло[4,5-h]имидазо[1,2-c][2,3]бензодиазепина.
4. Эфиры фенилуксусных кислот общей формулы 5
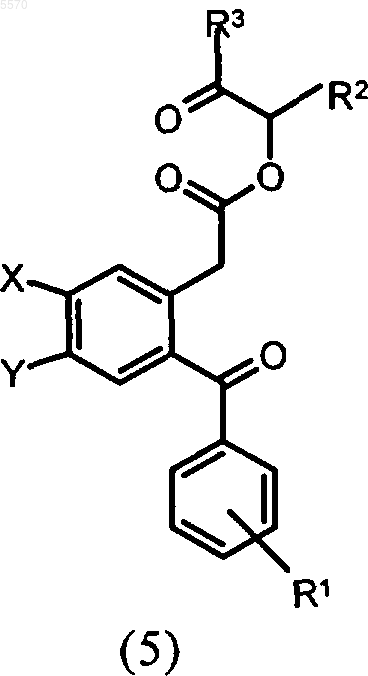
в которой
R1 обозначает водород, C1-C6алкил, нитрогруппу, галоген, цианогруппу, C1-C4алкоксигруппу, -CF3, гидроксигруппу или C1-C6алканоилоксигруппу,
R2 и R3 имеют идентичные или разные значения и обозначают водород, галоген, C1-C6алкоксигруппу, гидроксигруппу, цианогруппу, C1-C6алканоил, C2-C6алкинил, C2-C6алкенил, необязательно замещенный галогеном, гидроксигруппой либо C1-C6алкоксигруппой C1-C6алкил, C3-C7циклоалкил или необязательно замещенный галогеном, C1-C4алкоксигруппой либо C1-C4алкилом арил или гетероарил,
X обозначает водород или галоген,
Y обозначает C1-C6алкоксигруппу или
X и Y вместе обозначают -O-(CH2)n-O-, где
n обозначает 1, 2 или 3.
5. Оксазольные производные общей формулы 6
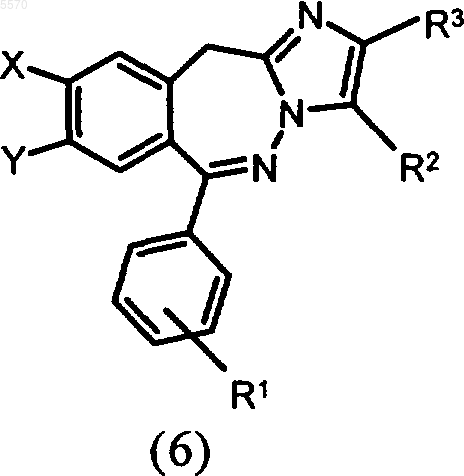
в которой
R1 обозначает водород, C1-C6алкил, нитрогруппу, галоген, цианогруппу, C1-C4алкоксигруппу, -CF3, гидроксигруппу или C1-C6алканоилоксигруппу,
R2 и R3 имеют идентичные или разные значения и обозначают водород, галоген, C1-C6алкоксигруппу, гидроксигруппу, цианогруппу, C1-C6алканоил, C2-C6алкинил, C2-C6алкенил, необязательно замещенный галогеном, гидроксигруппой либо C1-C6алкоксигруппой C1-C6алкил, C3-C7циклоалкил или необязательно замещенный галогеном, C1-C4алкоксигруппой либо C1-C4алкилом арил или гетероарил,
X обозначает водород или галоген,
Y обозначает C1-C6алкоксигруппу или X и Y вместе обозначают -O-(CH2)n-O-, где
n обозначает 1, 2 или 3.
Текст
005570 Настоящее изобретение относится к новому способу получения имидазо[1,2-с][2,3]бензодиазепинов приведенной ниже общей формулы (1), а также к новым промежуточным продуктам, получаемым по этому способуR1 обозначает водород, C1-С 6 алкил, нитрогруппу, галоген, цианогруппу, С 1-С 4 алкоксигруппу, -CF3,гидроксигруппу или C1-С 6 алканоилоксигруппу,R2 и R3 имеют идентичные или разные значения и обозначают водород, галоген, С 1 С 6 алкоксигруппу, гидроксигруппу, цианогруппу, С 1-С 6 алканоил, С 2-С 6 алкинил, С 2-С 6 алкенил, необязательно замещенный галогеном, гидроксигруппой либо С 1-С 6 алкоксигруппой С 1-С 6 алкил, С 3 С 7 циклоалкил или необязательно замещенный галогеном, С 1-С 4 алкоксигруппой либо С 1-С 4 алкилом арил или гетероарил,X обозначает водород или галоген,Y обозначает С 1-С 6 алкоксигруппу илиn обозначает 1, 2 или 3. Изобретение относится также к новым промежуточным продуктам для получения обладающих фармакологическим действием соединений - производным фенилуксусной кислоты общей формулы 5R1 обозначает водород, С 1-С 6 алкил, нитрогруппу, галоген, цианогруппу, С 1-С 4 алкоксигруппу, -CF3,гидроксигруппу или С 1-С 6 алканоилоксигруппу,R2 и R3 имеют идентичные или разные значения и обозначают водород, галоген, С 1 С 6 алкоксигруппу, гидроксигруппу, цианогруппу, С 1-С 6 алканоил, С 2-С 6 алкинил, С 2-С 6 алкенил, необязательно замещенный галогеном, гидроксигруппой либо С 1-С 6 алкоксигруппой С 1-С 6 алкил, С 3 С 7 циклоалкил или необязательно замещенный галогеном, С 1-С 4 алкоксигруппой либо С 1-С 4 алкилом арил или гетероарил,X обозначает водород или галоген,Y обозначает С 1-С 6 алкоксигруппу илиn обозначает 1, 2 или 3,и к оксазольным производным общей формулы 6R1 обозначает водород, С 1-С 6 алкил, нитрогруппу, галоген, цианогруппу, С 1-С 4 алкоксигруппу, -CF3,гидроксигруппу или С 1-С 6 алканоилоксигруппу,R2 и R3 имеют идентичные или разные значения и обозначают водород, галоген, С 1 С 6 алкоксигруппу, гидроксигруппу, цианогруппу, С 1-С 6 алканоил, С 2-С 6 алкинил, С 2-С 6 алкенил, необязательно замещенный галогеном, гидроксигруппой либо С 1-С 6 алкоксигруппой С 1-С 6 алкил, С 3 С 7 циклоалкил или необязательно замещенный галогеном, С 1-С 4 алкоксигруппой либо С 1-С 4 алкилом арил или гетероарил,X обозначает водород или галоген,Y обозначает C1-С 6 алкоксигруппу илиn обозначает 1, 2 или 3. Радикалы в указанных общих формулах имеют следующие значения. Под С 1-С 6 алкилом имеется в виду соответственно прямоцепочечный либо разветвленный алкил, такой, например, как метил, этил, пропил, изопропил, бутил, изобутил, втор-бутип, пентил, изопентил или гексил.R2 и R3 при их значении С 2-С 6 алкенил содержат соответственно по меньшей мере одну двойную связь, при этом в качестве примера можно назвать винил, пропенил, бутен-1-ил, изобутенил, пентен-1 ил, 2,2-диметилбутен-1-ил, 3-метилбутен-1-ил или гексен-1-ил. Если R2 и R3 обозначают С 1-С 6 алкинил, то они содержат соответственно по меньшей мере одну тройную связь, при этом в качестве примера можно назвать этинил, пропинил, бутин-1-ил, бутин-2-ил,пентин-1-ил, пентин-2-ил, 3-метилбутин-1-ил или гексин-1-ил. Вышеописанные алкенильные и алкинильные радикалы необязательно могут быть также замещены атомами галогена. В случае галогенированного алкильного радикала последний может быть галогенирован одно- либо многократно, вместе с тем он может быть полностью галогенирован, например -CF3. Под галогеном как заместителем вышеуказанных радикалов имеются в виду соответственно фтор,хлор, бром и иод. Если R2 и R3 обозначают арил или гетероарил, то они могут быть одно-, дву- или трехкратно замещены галогеном, С 1-С 4 алкоксигруппой либо С 1-С 4 алкилом; при этом возможны любые перестановки. Арил и гетероарил могут быть представлены в виде моно- или бицикла и содержать в цикле 5-12,предпочтительно 5-9 атомов, в качестве арила можно назвать, например, фенил, бифенил, нафтил или иденил, а в качестве гетероарила, содержащего 1-3 гетероатома, таких, например, как сера, кислород и/или азот, можно назвать среди прочих тиенил, фурил, пиранил, пирролил, пиразолил, пиридил, пиримидил, пиридазинил, оксазолил, изооксазолил, тиазолил, изотиазолил, 1,3,4-оксадиазол-2-ил, 1,2,4 оксадиазол-5-ил, 1,2,4-оксадиазол-3-ил, хинолил, изохинолил, бензо[1]тиенил и бензофуранил. Предпочтительными являются 2-тиенил, 3-тиенил, пиридин-2-ил, пиридин-3-ил, придин-4-ил и фенил. Если R2 и R3 обозначают С 3-С 7 циклоалкил, то под этим понятием подразумеваются, например, циклопропил, циклобутил, циклопентил, циклогексил и циклогептил. В качестве С 1-С 6 алканоила приемлемы соответственно прямоцепочечные или разветвленные алифатические карбоновокислотные остатки, такие, например, как формил, ацетил, пропионил, бутаноил,изопропилкарбонил, капроил, валероил или триметилацетил. Предпочтительно R1 обозначает водород, хлор, нитрогруппу или метоксигруппу; R2 и R3 обозначают водород, С 1-С 4 алкил или фенил; X и Y обозначают вместе -О-СН 2-О-. Способы получения соединений общей формулы 1 описаны в заявке WO 97/28163. В основу настоящего изобретения была положена задача разработать новый способ синтеза соединений общей формулы 1. Объектом настоящего изобретения являются также новые, не известные до настоящего времени промежуточные продукты общих формул 5 и 6, которые получают при осуществлении указанного синтеза и которые могут использоваться как таковые либо в виде производных в качестве исходных материалов для синтеза других целевых молекул. Указанную задачу удается решить благодаря объекту изобретения, признаки которого раскрыты в формуле изобретения. Предлагаемый в изобретении способ отличается меньшим числом промежуточных стадий по сравнению с синтезом, известным из уровня техники, заметным снижением количества операций по очистке и повышением общего выхода продуктов. Способ по изобретению позволяет получать соединения формулы 1 в промышленном масштабе. В соответствии с вышеизложенным объектом изобретения является способ получения имидазо[1,2 с][2,3]бензодиазепинов общей формулы 1, в которой R1, R2 и R3 , а также X и Y имеют указанные выше значения, из фенилуксусных кислот общей формулы 4 в которой X, Y и R1 имеют указанные выше значения, осуществляемый а) этерификацией спиртом формулы 5 а с получением эфира фенилуксусной кислоты формулы 5 в которой X, Y, R1, R2 и R3 имеют указанные выше значения,б) реакцией конденсации с аммиаком либо донором аммиака с получением оксазола общей формулы 6 в которой X, Y, R1, R2 и R3 имеют указанные выше значения, и последующим гидразинолизом с получением в результате соединений общей формулы 1. Имидазо[1,2-с][2,3]бензодиазепины общей формулы 1 синтезируют согласно схеме 1. Схема 1 Процесс превращения соединения общей формулы 2 в соединение общей формулы 3 осуществляют с помощью известного способа (см., например, Journ. Chem. Soc., Perkin Trans. 1 (1991), стр. 169-173) по реакции Фриделя-Крафтса. Так, например, соединения общей формулы 2 подвергают такой реакции в-3 005570 присутствии кислот Льюиса, таких, например, как тетрахлорид олова, трихлорид алюминия, тетрахлорид титана, и ацилирующего агента, такого, например, как бензоилхлорид, ангидрид бензойной кислоты или какого-либо иного активированного производного карбоновой кислоты. Существенного повышения выхода удается достичь в тех случаях, когда к реакционной смеси дополнительно добавляютN,N=диметилацетамид. В качестве растворителей могут служить галогенированные углеводороды, такие, например, как метиленхлорид или этиленхлорид либо их смеси. Реакцию проводят при температурах в интервале от -30 до +50 С, предпочтительно, однако, в интервале от 0 до 25 С. Процесс превращения соединения общей формулы 3 в соединение общей формулы 4 осуществляют с помощью известного способа, используемого при реакции омыления. Так, например, соединение общей формулы 3 нагревают в присутствии основания, такого как гидроксид щелочного металла, предпочтительно гидроксида натрия, в растворителе, таком как низший, предпочтительно первичным спиртом,или в воде либо в их смесях. Реакцию проводят при температурах в интервале от 25 до 150 С, предпочтительно, однако, в интервале от 70 до 110 С. Процесс превращения соединения общей формулы 4 в соединение формулы 5 осуществляют с помощью известного способа этерификации. Так, например, соединение общей формулы 4 подвергают такой реакции в присутствии активирующего агента, такого как карбонилдиимидазол, и спирта формулы 5 а такого как 3-гидрокси-ц-бутанон. В качестве растворителей могут служить галогенированные углеводороды, такие, например, как метиленхлорид или этиленхлорид, а также ТГФ и их смеси. Реакцию проводят при температурах в интервале от -20 до +100 С, предпочтительно, однако, в интервале от 0 до 25 С. Для специалистов в данной области очевидно, что значения R2 и R3 в соединениях общей формулы 5 могут варьироваться по стандартным методам. Так, в частности, это можно осуществлять за счет использования при этерификации других спиртов, равно как и путем переэтерификации уже имеющегося сложного эфира. С учетом вышеизложенного R2 и R3 могут обозначать водород, галоген, алкоксигруппу,гидроксигруппу, цианогруппу, алканоил, необязательно замещенный алкинил, необязательно замещенный алкенил, необязательно замещенный галогеном, гидроксигруппой либо алкоксигруппой алкил, циклоалкил или необязательно замещенный арил либо гетероарил. При превращении соединения общей формулы 5 в соединение общей формулы 6 используют известный способ получения оксазолов, осуществляемый реакцией конденсации двух карбонильных групп с аммиаком. Так, в частности, соединение общей формулы 5 подвергают взаимодействию с ацетатом аммония, аммиаком, раствором аммиака или с каким-либо иным донором аммиака, таким, например, как ацетамид или формамид, в присутствии уксусной кислоты. В качестве растворителей могут служить галогенированные углеводороды, такие, например, как метиленхлорид или этиленхлорид, органические кислоты, такие, например, как муравьиная кислота или уксусная кислота, низшие спирты, такие, например, как метанол или этанол, а также этиленгликоль и их смеси. Реакцию проводят при температурах в интервале от 0 до 150 С, предпочтительно, однако, в интервале от 50 до 100 С. Процесс превращения соединения общей формулы 6 в соединение общей формулы 1 осуществляют с помощью известного способа путем гидразинолиза, соответственно образования гидразона. Так, в частности, соединение общей формулы 6 подвергают обменной реакции с гидразином либо гидратом гидразина. В качестве растворителей могут служить галогенированные углеводороды, такие, например, как метиленхлорид или этиленхлорид, органические кислоты, такие, например, как муравьиная кислота или уксусная кислота, низшие спирты, такие, например, как метанол или этанол, а также этиленгликоль и их смеси. Реакцию проводят при температурах в интервале от 0 до 200 С, предпочтительно, однако, в интервале от 80 до 120 С. Реакцию можно проводить в автоклаве. Процесс превращения соединения общей формулы 5 в соединение общей формулы 1 также осуществляют по так называемому методу получения в одном аппарате. Так, в частности, соединение общей формулы 5 подвергают взаимодействию с ацетатом аммония, аммиаком, раствором аммиака или с каким-либо иным донором аммиака, таким, например, как ацетамид или формамид, в присутствии уксусной кислоты. В качестве растворителей могут служить галогенированные углеводороды, такие, например, как метиленхлорид или этиленхлорид, органические кислоты, такие, например, как муравьиная кислота или уксусная кислота, низшие спирты, такие, например, как метанол или этанол, а также этиленгликоль и их смеси. Реакцию проводят при температурах в интервале от 0 до 150 С, предпочтительно,однако, в интервале от 50 до 100 С. По завершении реакции к реакционной смеси добавляют гидразин либо гидрат гидразина. Реакцию проводят при температурах в интервале от 0 до 200 С, предпочтительно, однако, в интервале от 80 до 120 С. Реакцию можно проводить в автоклаве. Если в описании не указывается, каким образом получают исходные соединения, то это означает,что они либо известны, либо их можно получать по известным или описанным в данной заявке методам.-4 005570 Ниже предлагаемый в изобретении способ более подробно поясняется на примерах. Примеры Метиловый эфир 2-бензоил-4,5-(метилендиокси)фенилуксусной кислоты (соединение 3). 79 мл тетрахлорида олова и 25 мл N,N'-диметилацетамида в 270 мл метиленхлорида смешивают при комнатной температуре с 39 мл бензоилхлорида. Затем к этой смеси при 0 С добавляют по каплям 44 г метилового эфира 4,5-(метилендиокси)фенилуксусной кислоты (2) и раствор в течение 12 ч перемешивают при комнатной температуре. Для последующей переработки добавляют при -15 С 660 мл воды и водную фазу экстрагируют метиленхлоридом. Объединенные органические фракции промывают 6 н. водным NaOH и досуха концентрируют с помощью роторного испарителя. Сырой продукт 3 (74 г) кристаллизуют из этанола. 1 Н-ЯМР (CDCl3):= 3,61 (s, 3H, ОМе), 3,80 (s, 2H, бензил, СН 2), 6,03 (s, 2 Н, ОСН 2 О), 6,84 и 6,88 (2s по 1 Н, 3- и 6-Н арил), 7,43-7,80 (m, 5H, PhCO).tпл: 74-76 С. Анализ сжиганием: рассч.: С 68,45, Н 4,73; обнар.: С 68,53, Н 4,59. Аналогичным путем получают следующие соединения: метиловый эфир 2-(4-хлорбензоил)-4,5-(метилендиокси)фенилуксусной кислоты,метиловый эфир 2-(4-нитробензоил)-4,5-(метилендиокси)фенилуксусной кислоты,метиловый эфир 2-(4-метоксибензоил)-4,5-(метилендиокси)фенилуксусной кислоты,метиловый эфир 2-(4-метилбензоил)-4,5-(метилендиокси)фенилуксусной кислоты,метиловый эфир 2-(4-цианобензоил)-4,5-(метилендиокси)фенилуксусной кислоты. 2-Бензоил-4,5-(метилендиокси)фенилуксусная кислота (соединение 4). Суспензию из 10 г соединения 2 в 50 мл 1 н. водного NaOH в течение 2 ч нагревают с обратным холодильником. Затем добавляют 10 мл 1 н. водной серной кислоты, выпавшее в осадок твердое вещество отфильтровывают и промывают водой. Полученный продукт 4 (8,3 г) сушат под вакуумом и без дальнейшей очистки используют на следующей стадии. 1 Н-ЯМР (ДМСО):= 3,68 (s, 2H, бензил, СН 2), 6,12 (s, 2H, ОСН 2 О), 6,86 и 7,03 (2s по 1 Н, 3- и 6-Н арил), 7,50-7,73 (m, 5H, PhCO), 12,18 (шир. s, 1H, СООН).tпл: 185-189 С. Анализ сжиганием: рассч.: С 67,60, Н 4,25; обнар.: С 67,66, Н 4,20. Аналогичным путем получают следующие соединения: 2-(4-хлорбензоил)-4,5-(метилендиокси)фенилуксусную кислоту,2-(4-нитробензоил)-4,5-(метилендиокси)фенилуксусную кислоту,2-(4-метоксибензоил)-4,5-(метилендиокси)фенилуксусную кислоту,2-(4-метилбензоил)-4,5-(метилендиокси)фенилуксусную кислоту,2-(4-цианобензоил)-4,5-(метилендиокси)фенилуксусную кислоту. 3-Оксобут-2-иловый эфир 2-бензоил-4,5-(метилендиокси)фенилуксусной кислоты (соединение 5). 50 г соединения 4, 19 г 3-гидрокси-2-бутанона и 32 г N,N'-карбонилдиимидазола растворяют при комнатной температуре в 500 мл метиленхлорида и перемешивают в течение 3 дней. Для последующей переработки смешивают с 200 мл полностью деминерализованной воды и затем экстрагируют метиленхлоридом. Объединенные органические фракции концентрируют с помощью роторного испарителя. Сырой продукт двукратно кристаллизуют из метанола и в результате получают 45 г соединения 5. 1 Н-ЯМР (CDCl3):= 1,32 (d, 3 Н, J= 6.9, CH3C-O), 2,11 (s, 3 Н, СН 3 С=О), 3,88 (s, 2H, бензил, СН 2),5,03 (q, 1H, J = 6.9, СН-О), 6,04 (s, 2H, ОСН 2 О), 6,87 и 6,90 (2s a 1H, 3- и 6-Н арил), 7,42-7,74 (m, 5H,PhCO).tпл: 81-83 С. Анализ сжиганием: рассч.: С 67,79, Н 5,12; обнар.: С 67,83, Н 5,04. Аналогичным путем получают следующие соединения: 3-оксобут-2-иловый эфир 2-(4-хлорбензоил)-4,5-(метилендиокси)фенилуксусной кислоты,3-оксобут-2-иловый эфир 2-(4-нитробензоил)-4,5-(метилендиокси)фенилуксусной кислоты,3-оксобут-2-иловый эфир 2-(4-метоксибензоил)-4,5-(метилендиокси)фенилуксусной кислоты,4-оксогекс-3-иловый эфир 2-бензоил-4,5-(метилендиокси)фенилуксусной кислоты,2-оксо-1,2-дифенилэт-1-иловый эфир 2-бензоил-4,5-(метилендиокси)фенилуксусной кислоты. 2-Бензоил-4,5-(метилендиокси)бензил-4,5-диметилоксазол (соединение 6). К 10 г соединения 5 и 19 г ацетата аммония в 200 мл 1,2-дихлорэтана добавляют 14 мл концентрированной уксусной кислоты и смесь в течение 6 ч нагревают с обратным холодильником. Затем добав-5 005570 ляют 100 мл 1 н. водного NaOH и экстрагируют метиленхлоридом. Объединенные органические экстракты упаривают с помощью роторного испарителя и сырой продукт фильтруют через силикагель (гексан: этиловый эфир уксусной кислоты в соотношении от 9:1 до 8:2). В результате получают 6,9 г чистого соединения 6 (вязкое масло). 1 Н-ЯМР (CDCl3):= 1,94 и 2,03 (2s3H, 2 СН 3), 4,13 (s, 2H, бензил, СН 2), 6,01 (s, 2H, ОСН 2 О), 6,83 и 6,86 (2s1H, 3- и 6-Н арил), 7,41-7,80 (m, 5H, PhCO). Анализ сжиганием: рассч.: С 71,63, Н 5,11, N 4,18; обнар.: С 71,47, Н 5,04, N 3,94. Аналогичным путем получают следующие соединения: 2-(4-хлорбензоил)-4,5-(метилендиокси)бензил-4,5-диметилоксазол,2-(4-нитробензоил)-4,5-(метилендиокси)бензил-4,5-диметилоксазол,2-(4-метоксибензоил)-4,5-(метилендиокси)бензил-4,5-диметилоксазол,2-бензоил-4,5-(метилендиокси)бензил-4,5-диэтилоксазол,2-бензоил-4,5-(метилендиокси)бензил-4,5-дифенилоксазол. 2,3-Диметил-6-фенил-(12 Н)-[1,3]диоксоло[4,5-h]имидазо[1,2-с][2,3]бензодиазепин (соединение 1). В автоклаве к 2 г соединения 6, растворенных в 18 мл этиленгликоля и 2 мл концентрированной уксусной кислоты, добавляют 0,5 мл гидрата гидразина. После этого в течение 12 ч нагревают до 120 С и затем реакционную смесь смешивают при комнатной температуре с 2 н. водным NaOH. Далее несколько раз экстрагируют этиловым эфиром уксусной кислоты и объединенные органические фазы концентрируют досуха с помощью роторного испарителя. В завершение сырой продукт очищают хроматографией на колонке (гексан:этиловый эфир уксусной кислоты в соотношении от 9:1 до 8:2). Выход чистого соединения 1 составляет 1,2 г. 1 Н-ЯМР (ДМСО):= 2,01 и 2,20 (2s3H, 2 СН 3), 3,82 (шир. s, 2H, бензил. СН 2), 6,08 (s, 2H,ОСН 2 О), 6,55 и 7,15 (2s1H, 2 арил-Н), 7,48-7,72 (m, 5H, PhCO).tпл: 177 С. Анализ сжиганием: рассч.: С 72,49, Н 5,18, N 12,88; обнар.: С 72,33, Н 5,31, N 12,46. Аналогичным путем получают следующие соединения: 2,3-диметил-6-(4-хлорфенил)-(12 Н)-[1,3]диоксоло[4,5-h]имидазо[1,2-с][2,3]бензодиазепин,2,3-диметил-6-(4-нитрофенил)-(12 Н)-[1,3]диоксоло[4,5-h]имидазо[1,2-с][2,3]бензодиазепин,2,3-диметил-6-(4-метоксифенил)-(12 Н)-[1,3]диоксоло[4,5-h]имидазо[1,2-с][2,3]бензодиазепин,2,3-диэтил-6-фенил-(12 Н)-[1,3]диоксоло[4,5-h]имидазо[1,2-с][2,3]бензодиазепин,2,3-дифенил-6-фенил-(12 Н)-[1,3]диоксоло[4,5-h]имидазо[1,2-с][2,3]бензодиазепин. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ получения имидазо[1,2-с][2,3]бензодиазепинов общей формулы 1R1 обозначает водород, C1-С 6 алкил, нитрогруппу, галоген, цианогруппу, С 1-С 4 алкоксигруппу, -CF3,гидроксигруппу или C1-С 6 алканоилоксигруппу,R2 и R3 имеют идентичные или разные значения и обозначают водород, галоген, C1 С 6 алкоксигруппу, гидроксигруппу, цианогруппу, C1-С 6 алканоил, C2-С 6 алкинил, C2-С 6 алкенил, необязательно замещенный галогеном, гидроксигруппой либо C1-С 6 алкоксигруппой C1-С 6 алкил, С 3 С 7 циклоалкил или необязательно замещенный галогеном, С 1-С 4 алкоксигруппой либо С 1-С 4 алкилом арил или гетероарил,X обозначает водород или галоген,Y обозначает C1-С 6 алкоксигруппу илиn обозначает 1, 2 или 3,из фенилуксусных кислот общей формулы 4 в которой X, Y и R1 имеют указанные выше значения, заключающийся в том, что осуществляют а) этерификацию спиртом формулы 5 а с получением эфира фенилуксусной кислоты формулы 5 в которой X, Y, R1, R2 и R3 имеют указанные выше значения,б) реакцию конденсации с аммиаком либо донором аммиака с получением оксазола общей формулы 6 в которой X, Y, R1, R2 и R3 имеют указанные выше значения, и последующий гидразинолиз с получением в результате соединений общей формулы 1 в которой X, Y, R1, R2 и R3 имеют указанные выше значения. 2. Способ по п.1, в котором соединения общей формулы 5 по реакции получения в одном аппарате взаимодействием с ацетатом аммония и аммиаком либо донором аммиака при температуре в интервале от 0 до 150 С в растворителе или смеси растворителей, а затем взаимодействием с гидразином при температуре в интервале от 0 до 200 С, необязательно в автоклаве, превращают в соединения общей формулы 1. 3. Способ по п.1 или 2, предназначенный для получения 2,3-диметил-6-фенил-(12 Н)-[1,3]диоксоло[4,5-h]имидазо[1,2-с][2,3]бензодиазепина,2,3-диметил-6-(4-хлорфенил)-(12 Н)-[1,3]диоксоло[4,5-h]имидазо[1,2-с][2,3]бензодиазепина,2,3-диметил-6-(4-нитрофенил)-(12 Н)-[1,3]диоксоло[4,5-h]имидазо[1,2-с][2,3]бензодиазепина,2,3-диметил-6-(4-метоксифенил)-(12 Н)-[1,3]диоксоло[4,5-h]имидазо[1,2-с][2,3]бензодиазепина,2,3-диэтил-6-фенил-(12 Н)-[1,3]диоксоло[4,5-h]имидазо[1,2-с][2,3]бензодиазепина,2,3-дифенил-6-фенил-(12 Н)-[1,3]диоксоло[4,5-h]имидазо[1,2-с][2,3]бензодиазепина.-7 005570 4. Эфиры фенилуксусных кислот общей формулы 5R1 обозначает водород, C1-С 6 алкил, нитрогруппу, галоген, цианогруппу, С 1-С 4 алкоксигруппу, -CF3,гидроксигруппу или C1-С 6 алканоилоксигруппу,R2 и R3 имеют идентичные или разные значения и обозначают водород, галоген, C1 С 6 алкоксигруппу, гидроксигруппу, цианогруппу, C1-С 6 алканоил, C2-С 6 алкинил, C2-С 6 алкенил, необязательно замещенный галогеном, гидроксигруппой либо C1-С 6 алкоксигруппой C1-С 6 алкил, С 3 С 7 циклоалкил или необязательно замещенный галогеном, С 1-С 4 алкоксигруппой либо С 1-С 4 алкилом арил или гетероарил,X обозначает водород или галоген,Y обозначает C1-С 6 алкоксигруппу илиn обозначает 1, 2 или 3. 5. Оксазольные производные общей формулы 6R1 обозначает водород, C1-С 6 алкил, нитрогруппу, галоген, цианогруппу, С 1-С 4 алкоксигруппу, -CF3,гидроксигруппу или C1-С 6 алканоилоксигруппу,R2 и R3 имеют идентичные или разные значения и обозначают водород, галоген, C1 С 6 алкоксигруппу, гидроксигруппу, цианогруппу, C1-С 6 алканоил, C2-С 6 алкинил, C2-С 6 алкенил, необязательно замещенный галогеном, гидроксигруппой либо C1-С 6 алкоксигруппой C1-С 6 алкил, С 3 С 7 циклоалкил или необязательно замещенный галогеном, С 1-С 4 алкоксигруппой либо С 1-С 4 алкилом арил или гетероарил,X обозначает водород или галоген,Y обозначает C1-С 6 алкоксигруппу или
МПК / Метки
МПК: C07D 487/04, C07C 69/614, C07D 491/14
Метки: способ, промежуточные, способу, получаемые, этому, получения, продукты, имидазо[1,2-c][2,3]бензодиазепинов
Код ссылки
<a href="https://eas.patents.su/9-5570-sposob-polucheniya-imidazo12-c23benzodiazepinov-i-poluchaemye-po-etomu-sposobu-promezhutochnye-produkty.html" rel="bookmark" title="База патентов Евразийского Союза">Способ получения имидазо[1,2-c][2,3]бензодиазепинов и получаемые по этому способу промежуточные продукты</a>
Предыдущий патент: Топливная присадка улучшенного состава и способ ее применения
Следующий патент: Система для транспорта активных веществ в биологической системе
Случайный патент: Устройство и способ оптического воспроизведения изображения особенностей на поверхности руки