Композиции n-(метилэтиламинокарбонил)-4-(3-метилфениламино)-3-пиридилсульфонамида и циклических олигосахаридов
Номер патента: 5111
Опубликовано: 28.10.2004
Авторы: Думич Миленко, Даниловски Александар, Филич Дарко, Клепич Божена, Тудья Мариян
Формула / Реферат
1. Физические смеси, отличающиеся тем, что они содержат торасемид и циклодекстрины или производные циклодекстринов.
2. Физические смеси по п.1, отличающиеся тем, что торасемид выбирают из группы, состоящей из модификаций I, II, III, IV и V или любой их смеси.
3. Физические смеси по п.1, отличающиеся тем, что циклодекстрин выбирают из группы, состоящей из a -, b - и g -циклодекстрина.
4. Физические смеси по п.1, отличающиеся тем, что производные циклодекстрина выбирают из группы простых эфиров или смешанных простых эфиров a -, b - и g -циклодекстринов, имеющих одну или несколько групп из ангидроглюкозных частей циклодекстрина, замещенных C1-6алкилом, предпочтительно метилом, этилом или изопропилом; гидроксиC1-6алкилом, предпочтительно гидроксиэтилом, или гидроксипропилом, или гидроксибутилом; карбоксиC1-6алкилом, предпочтительно карбоксиметилом или карбоксиэтилом; C1-6алкилкарбонилом, предпочтительно ацетилом, C1-6алкоксикарбонилC1-6алкилом или карбоксиC1-6алкоксиC1-6алкилом, предпочтительно карбоксиметоксипропилом или карбоксиэтоксипропилом; C1-6алкоксикарбонилоксиC1-6алкилом, предпочтительно 2-ацетилоксипропилом.
5. Физические смеси по п.1, отличающиеся тем, что производные циклодекстрина выбирают из группы, состоящей из 2-гидроксипропил-a -циклодекстрина, 2-гидроксипропил-b -циклодекстрина, 2-гидроксипропил-g -циклодекстрина, 2-гидроксиэтил-b -циклодекстрина, 2-гидроксиэтил-g -циклодекстрина, 2,6-диметил-b -циклодекстрина и (2-карбоксиметокси)пропил-b -циклодекстрина.
6. Физические смеси по п.1, отличающиеся тем, что торасемид и циклодекстрины или производные циклодекстринов находятся в мольном отношении от 1:0,1 до 1:5.
7. Способ получения физических смесей по п.1, отличающийся тем, что торасемид и циклодекстрины или производные циклодекстринов гомогенизируют.
8. Способ получения физических смесей по п.7, отличающийся тем, что указанную гомогенизацию осуществляют в ступке или смесителях.
9. Способ получения физических смесей по п.7, отличающийся тем, что указанное смешивание осуществляют при температуре от 10 до 100шC.
10. Способ получения физических смесей по п.7, отличающийся тем, что указанное смешивание проводят в течение от 0,1 до 24 ч.
11. Применение физических смесей по п.1 в качестве диуретика и в качестве средства для профилактики поражения сердца или повреждения ткани сердца, вызванных метаболическими или ионными нарушениями, связанными с ишемией, при лечении тромбоза, стенокардии, астмы, гипертензии, отека почек, отека легких, первичного и вторичного альдостеронизма, синдрома Баттера, опухолей, глаукомы, снижения внутриглазного давления, острого или хронического бронхита, при лечении отека мозга, вызванного травмой, ишемией, сотрясением мозга, метастазами или эпилептическими припадками, и при лечении назальных инфекций, вызванных аллергенами.
12. Лекарственная форма, отличающаяся тем, что она содержит физические смеси по п.1 в качестве активного вещества в сочетании с одной или несколькими фармацевтическими добавками, такими как сахар, крахмал, производные крахмала, целлюлоза, производные целлюлозы, средства, задающие режим выделения, и антиадгезивные средства и, необязательно, средства регуляции текучести.
13. Лекарственная форма по п.12, отличающаяся тем, что она является таблеткой, капсулой, формой для инъекций или аэрозолем.
14. Комплексы включения, отличающиеся тем, что они содержат торасемид и циклодекстрины или производные циклодекстринов.
15. Комплексы включения по п.14, отличающиеся тем, что циклодекстрин выбирают из группы, состоящей из a -, b - и g -циклодекстрина.
16. Комплексы включения по п.14, отличающиеся тем, что производные циклодекстринов выбирают из группы простых эфиров или смешанных простых эфиров a -, b - и g -циклодекстринов, имеющих одну или несколько групп из ангидроглюкозных частей циклодекстрина, замещенных C1-6алкилом, предпочтительно метилом, этилом или изопропилом; гидроксиC1-6алкилом, предпочтительно гидроксиэтилом, или гидроксипропилом, или гидроксибутилом; карбоксиC1-6алкилом, предпочтительно карбоксиметилом или карбоксиэтилом; C1-6алкилкарбонилом, предпочтительно ацетилом, C1-6алкоксикарбонилC1-6алкилом или карбоксиC1-6алкоксиC1-6алкилом, предпочтительно карбоксиметоксипропилом или карбоксиэтоксипропилом; C1-6алкоксикарбонилоксиC1-6алкилом, предпочтительно 2-ацетилоксипропилом.
17. Комплексы включения по п.14, отличающиеся тем, что производные циклодекстринов выбирают из группы, состоящей из 2-гидроксипропил-a -циклодекстрина, 2-гидроксипропил-b -циклодекстрина, 2-гидроксипропил-g -циклодекстрина, 2-гидроксиэтил-b -циклодекстрина, 2-гидроксиэтил-g -циклодекстрина, 2,6-диметил-b -циклодекстрина и (2-карбоксиметокси)пропил-b -циклодекстрина.
18. Комплексы включения по п.14, отличающиеся тем, что торасемид и циклодекстрины или производные циклодекстринов находятся в мольном отношении от 1:0,1 до 1:5.
19. Способ получения комплексов включения по п.14, отличающийся тем, что торасемид и циклодекстрины или производные циклодекстринов взаимодействуют в воде с водным раствором основания или без него.
20. Способ получения комплексов включения по п.19, отличающийся тем, что в качестве водного раствора основания используют водный раствор аммиака.
21. Способ получения комплексов включения по п.19, отличающийся тем, что его осуществляют при температуре от 10 до 100шC.
22. Способ получения комплексов включения по п.19, отличающийся тем, что его осуществляют в течение от 0,1 ч до 7 дней.
23. Способ получения комплексов включения по п.19, отличающийся тем, что после образования указанного комплекса воду и основание удаляют сушкой.
24. Способ получения комплексов включения по п.23, отличающийся тем, что указанную сушку осуществляют лиофилизацией, распылительной сушкой, вакуумным выпариванием или вакуумной сушкой.
25. Применение комплексов по п.14 в качестве диуретика и в качестве средства для профилактики поражения сердца или повреждения ткани сердца, вызванных метаболическими или ионными нарушениями, связанными с ишемией, при лечении тромбоза, стенокардии, астмы, гипертензии, отека почек, отека легких, первичного и вторичного альдостеронизма, синдрома Баттера, опухолей, глаукомы, снижения внутриглазного давления, острого или хронического бронхита, при лечении отека мозга, вызванного травмой, ишемией, сотрясением мозга, метастазами или эпилептическими припадками, и при лечении назальных инфекций, вызванных аллергенами.
26. Лекарственная форма, отличающаяся тем, что она содержит комплексы включения по п.14 в качестве активного вещества в сочетании с одной или несколькими фармацевтическими добавками, такими как сахар, крахмал, производные крахмала, целлюлоза, производные целлюлозы, определяющие высвобождение средства и антиадгезивные средства и, необязательно, средства регуляции текучести.
27. Лекарственная форма по п.26, отличающаяся тем, что она является таблеткой, капсулой, формой для инъекций или аэрозолем.
Текст
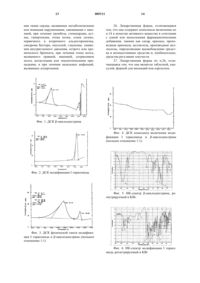
1 Данное изобретение относится к композициям N-(1-метилэтиламинокарбонил)-4-(3-метилфениламино)-3-пиридилсульфонамида (далее в тексте называемого его непатентованным видовым названием торасемид) и циклических олигосахаридов с повышенным выделением, к методам их получения, к лекарственным формам, содержащим их, а также к их применению. Торасемид является новым сильным диуретиком в группе так называемых петлевых диуретиков, который описан в примере 71 патента DE 2515025. Структурно он совершенно отличается от диуретиков той же группы, таких как фуросемид, буметанид и азосемид. В дополнение к диуретическим свойствам он также обладает антигипертензивными свойствами. Как диуретик, действующий на уровне петли Генле, он интересен в качестве средства предупреждения повреждений сердца или ткани сердца, вызываемых метаболическими нарушениями или ионными нарушениями (нарушениями электролитного баланса), связанными с ишемией, при лечении тромбоза, стенокардии,астмы, гипертензии, отека почек, отека легких,первичного и вторичного альдостеронизма,синдрома Баттера, опухолей, глаукомы, снижении внутриглазного давления, острого и хронического бронхита, при лечении отека мозга, вызванного травмой, ишемии, сотрясении мозга,метастазах или эпилептических припадках и при лечении назальных инфекций, вызванных аллергенами. Хорошо известно, что торасемид может существовать в четырех кристаллических модификациях: полиморф I [Acta Cryst. B34 (1978),1304-1310], полиморф II [Acta Cryst. B34 (1978) 2659-2662], полиморф III (PCT/WO 00/20395) и полиморф V (HR патентная заявкаР 20000328 А) и в одной аморфной модификации(HR патентная заявкаР 20000162 А). Модификации торасемида (полиморфы IV) очень гидрофобны и практически нерастворимы в воде. Очень плохая растворимость в воде и смачиваемость торасемида представляет одну из проблем при изготовлении фармацевтических препаратов с хорошим растворением и стабильной биодоступностью. Проблема повышения степени растворения активных веществ, которые плохо растворимы в воде, имеет место во многих областях, в диапазоне препаратов от фитофармацевтических до пестицидов, и, в основном, со всеми теми областями, где используются биологически активные вещества. Степень растворения определяется физико-химическими свойствами активного вещества и особенно его растворимостью в воде. Таким образом, степень растворения активного вещества является ограничивающим фактором в процессе всасывания и для терапевтической активности данного вещества. Кроме того, про 005111 2 дукты распада активного вещества, образовавшиеся в фармацевтических препаратах, могут также вызывать различные побочные эффекты. Поэтому повышенная растворимость и стабильность, достигаемая изготовлением соответствующего лекарственного препарата, дает в результате повышенную эффективность активного вещества. В фармацевтической промышленности проблема увеличения степени растворения и стабильности плохо растворимых активных веществ решалась разными способами, например микронизацией (измельчением до микронных размеров), получением аморфных форм, клатратов, химическими модификациями, регулировкой рН и очень часто изготовлением твердых композиций активного вещества с физиологически подходящими добавками, делающими возможной желаемую физико-химическую трансформацию активного вещества, например улучшение степени растворения и смачиваемости активного вещества. В качестве физиологически подходящих добавок обычно используются, например, поливинилпирролидон, карбоксиметилцеллюлоза, гидроксипропилцеллюлоза и,со все увеличивающейся частотой применения,циклодекстрины, доступные для приобретения циклические олигосахариды, состоящие из 6, 7 и 8 связанных глюкопиранозных единиц (-, и -циклодекстрины и их производные). Твердые композиции активное вещество/физиологически подходящая добавка могут быть получены смешиванием, размолом, осаждением, выпариванием, лиофилизацией, распылительной сушкой и плавлением. Свойства циклодекстринов хорошо известны и были описаны подробно в обзорах в периодических изданиях [Szejtli J., CyclodextrinIndustry, Angew. Chem. Int. Ed. Engl. 19 (1980) 344]. Циклодекстрины характеризуются формой их молекулы в виде цилиндра. Внутри цилиндра существует внутримолекулярная полость, которая является гидрофобной, тогда как наружная сторона является гидрофильной. Гидрофобный характер внутримолекулярной полости обеспечивает возможность другим молекулам или частям молекул, известным как гостевые молекулы, проникать в молекулу-хозяина с образованием тем самым комплексов включения. Комплекс включения может быть стабилизирован многими силами, включая силы притяжения Ван дер Ваальса и водородные связи. Комплексообразование с включением соответ 3 ствующей "гостевой молекулы" с циклодекстринами может давать в результате многочисленные изменения физико-химических свойств"гостевой молекулы". Изменяется температура плавления, ИК-спектр и порошковая рентгенограмма комплекса относительно отличаются от данных для чистой "гостевой" молекулы или простой (без образования комплекса) смеси молекулы-"хозяина" и "гостевой" молекулы. С помощью циклодекстринового комплекса включения нерастворимые в воде гостевые молекулы становятся более растворимыми. Во многих случаях химически нестабильные соединения стабилизируются за счет комплексообразования включения. Указанные изменения физикохимических свойств гостевой молекулы, происходящие в результате комплексообразования включения с циклодекстринами, представляют доказательство того, что циклодекстриновый комплекс включения представляет уникальную форму твердого состояния "гостевой" молекулы. Хотя при изготовлении твердых композиций активное вещество/физиологически подходящая добавка была отмечена повышенная степень растворения для большого числа плохо растворимых фармацевтически активных веществ, это не может быть принято за правило. А именно, для каждого активного вещества и физиологически подходящей добавки должно быть установлено, какие метод изготовления, физиологически активная добавка и мольное отношение активного вещества/физиологически подходящей добавки, растворитель, время, температура изготовления и т.д. будут давать твердую композицию, делающую возможной желаемую степень растворения активного вещества. Твердые композиции циклодекстрина с разными фармацевтически интересными активными веществами были известны из патентов, а также из литературы, и несколько примеров приведено здесь. Так, М. I. La Rotonda et al. сравнили твердые композиции нестероидного противовоспалительного средства нимесулида и циклодекстрина (мольное отношение 1:1), изготовленные физическим смешиванием, выпариванием, лиофилизацией, распылительной сушкой и замешиванием, и сообщили, что степень растворения зависит от физико-химических свойств каждой твердой композиции. По сравнению с одним только нимесулидом растворение нимесулида из твердых композиций было значительно ускорено, и, как было показано, твердые композиции, полученные лиофилизацией и распылительной сушкой являются формами с наиболее быстрым растворением нимесулида [S.T.P.P.R. Vavia et al. также сравнили твердые композиции нимесулида с -циклодекстрином и НРциклодекстрином в мольном отношении 4 1:1 (физические смеси и лиофилизаты). Как установлено авторами, в противоположность физическим смесям комплексы включения, полученные лиофилизацией, увеличивали растворение нимесулида, и особенно с помощью комплекса включения нимесулид/НРциклодекстрин достигалось значительно более высокое растворение [Drug Develop. Ind. Pharm. 25J.R. Mayano et al. получали физическим смешиванием, распылительной сушкой и замешиванием твердые композиции лекарственного средства оксазепама с -циклодекстрином в мольном отношении 1:1 и 1:2, и все твердые композиции ускоряли растворение оксазепама по сравнению с одним оксазепамом. В случае физических смесей оба мольных отношения оксазепама к -циклодекстрину продемонстрировали одинаковое влияние на растворение оксазепама, тогда как твердые композиции, полученные замешиванием и распылительной сушкой с мольным отношением 1:2, значительно ускоряли растворение оксазепама по сравнению с растворением комплекса с мольным отношением 1:1 [Int. J. Pharm. 114 (1995) 95]. Кроме того, М. Guyot et al. получали физические смеси и комплексы включения лекарственного средства норфлоксацина с -циклодекстрином и НРциклодекстрином в мольных отношениях 1:1 и 1:2. Физические смеси, а также комплексы включения значительно повышали растворение по сравнению с одним норфлоксацином. Никакого влияния мольного соотношения на растворение не отмечено [Int. J. Pharm. 123 (1995) 53]. Кроме того, М. Pedersen et al. установили,что физические смеси антимикотического средства миконазола и -циклодекстрина в мольном отношении 1:2 проявляют более быстрое растворение по сравнению с комплексом включения с -циклодекстрином [Drug Develop. Ind.Pharm. 25 (1999) 1241]. В патенте США 5849329 авторы защитили способ получения фармацевтических композиций с регулируемым растворением, полученных размолом или сухим перемешиванием активных веществ также, среди прочего, и с -, -, - иHPциклодекстринами и их производными. В качестве активных веществ приведены нафтазон, терфенадин, карбамазепин, гликазид, глибенкламид, бифоназол, а также нифедипин, диазепам и кетопрофен. В патенте США 5449521 авторы защитили фармацевтические композиции, содержащие гризеофульвин, пироксикам, диацереин, дилтиазем, мегестрола ацетат, нифедипин, ницерголин,кетопрофен, напроксен, диклофенак, ибупрофен, лоразепам, оксазепам в качестве активного вещества и, среди прочего, структурированный полимерный циклодекстрин. Приведенные фармацевтические композиции были получены 5 размолом активного вещества и подходящей добавки в мельницах, насыщенных парами растворителя или смеси растворителей. Кроме того, в патенте США 5010064 авторы защитили комплекс включения дипиридамола и -циклодекстрина (мольное отношение от 1:1 до 1:12), тогда как в патенте США 5019563 защищен комплекс натриевой соли ибупрофена и -циклодекстрина (мольное отношение от 1:0,2 до 1:0,75). Кроме того, в патенте США 5674854 авторы описали и защитили получение и комплекс включения фармацевтически приемлемых солей диклофенака и -циклодекстрина (мольное отношение 1:1), а в патенте США 5744165 авторы защитили комплексы включения солей щелочных металлов и солей щелочно-земельных металлов нимесулида с -, - и -циклодекстринами и их производными. В патентной публикации WO 93/00097 авторы заявили стабильные фармацевтические препараты, содержащие торасемид или его соли и добавки, такие как гидроксипропилцеллюлозу,поливинилпирролидон,натрий-кроскармеллозу, крос-повидон, кальцийкарбоксиметилцеллюлозу, низшую замещенную гидроксипропилцеллюлозу, модифицированный крахмал и т.д. Циклодекстрины в ней не приведены. В дополнительном исследовании в области торасемида неожиданно обнаружено, что физические смеси модификаций I-V торасемида с циклодекстринами или производными циклодекстринов отличаются более быстрым растворением торасемида. Кроме того, было неожиданно обнаружено, что комплексы включения модификаций I-V торасемида с циклодекстринами или производными циклодекстринов отличаются более быстрым растворением торасемида. В первую очередь данное изобретение относится к физиологически приемлемым физическим смесям модификаций I, II, III, IV или V торасемида с циклодекстринами или производными циклодекстринов или к любой смеси модификаций I, II, III, IV и V торасемида и циклодекстринов или производных циклодекстринов. Циклодекстрины, содержащиеся в физических смесях представляют собой -, - и -циклодекстрины и их производные. Подходящими производными -, - и -циклодекстринов являются их простые эфиры и смешанные простые эфиры, имеющие одну или несколько групп из ангидроглюкозных частей циклодекстрина, замещенных C1-6 алкилом, предпочтительно метилом, этилом или изопропилом; гидроксиC1-6 алкилом, предпочтительно гидроксиэтилом, или гидроксипропилом, или гидроксибутилом; карбоксиC1-6 алкилом, предпочтительно карбоксиметилом или карбоксиэтилом; C1-6 алкилкарбонилом, предпочтительно ацетилом, C1-6 алкоксикарбонилC1-6 алкилом или карбокси-C1-6 ал 005111 6 коксиC1-6 алкилом, предпочтительно карбоксиметоксипропилом или карбоксиэтоксипропилом; С 1-6 алкоксикарбонилоксиC1-6 алкилом,предпочтительно 2-ацетилоксипропилом. Особенно важными циклодекстринами или их производными являются -, - и -циклодекстрины,2-гидроксипропилциклодекстрин, 2-гидроксипропилциклодекстрин,2-гидроксипропилциклодекстрин, 2-гидроксиэтилциклодекстрин, 2-гидроксиэтилциклодекстрин, 2,6 диметилциклодекстрин и (2-карбоксиметокси)пропилциклодекстрин. В основном в физических смесях данного изобретения мольное отношение модификацийI-V торасемида к циклодекстринам или производным циклодекстринов может изменяться в интервале от 1:0,1 до 1:5. Кроме того, данное изобретение относится к способу получения вышеназванных физических смесей модификаций I-V торасемида и циклодекстринов и производных циклодекстринов. На практике данный способ может осуществляться в соответствии со следующим ниже методом. Модификации I, II, III, IV или V торасемида и циклодекстрины или производные циклодекстринов или любую смесь модификаций I, II,III, IV или V торасемида и циклодекстринов или производных циклодекстринов соединяют в конкретном мольном отношении, гомогенизируют в ступке или смесителях, обычно используемых в фармацевтической промышленности,при температуре и в течение срока, необходимых для получения смеси с желаемой скоростью растворения торасемида. В соответствии с первой целью изобретения данное изобретение относится также к физиологически приемлемым комплексам включения модификаций I, II, III, IV или V торасемида с циклодекстринами или производными циклодекстринов или любой смеси модификаций I, II,III, IV или V торасемида и циклодекстринов или производных циклодекстринов. Циклодекстринами, содержащимися в комплексах включения, являются -, - и циклодекстрины и их производные. Подходящими производными -, - и -циклодекстринов являются их простые эфиры или смешанные простые эфиры, имеющие одну или несколько групп из ангидроглюкозных частей циклодекстрина, замещенных C1-6 алкилом, предпочтительно метилом, этилом или изопропилом; гидроксиC1-6 алкилом, предпочтительно гидроксиэтилом,или гидроксипропилом, или гидроксибутилом; карбоксиC1-6 алкилом, предпочтительно карбоксиметилом или карбоксиэтилом; C1-6 алкилкарбонилом, предпочтительно ацетилом; C1-6 алкоксикарбонилC1-6 алкилом или карбокси-C1-6 алкокси-C1-6 алкилом, предпочтительно карбоксиметоксипропилом или карбоксиэтоксипропилом;C1-6 алкоксикарбонилоксиC1-6 алкилом, предпоч 7 тительно 2-ацетилоксипропилом. Особенно важными циклодекстринами или их производными являются -, - и -циклодекстрины, 2 гидроксипропилциклодекстрин, 2-гидроксипропилциклодекстрин, 2-гидроксипропил-циклодекстрин, 2-гидроксиэтилциклодекстрин, 2-гидроксиэтилциклодекстрин, 2,6-диметилциклодекстрин и (2-карбоксиметокси) пропилциклодекстрин. В основном, в комплексах включения данного изобретения мольное отношение модификаций I-V торасемида и циклодекстринов или производных декстринов может изменяться в интервале от 1:0,1 до 1:5. Кроме того, настоящее изобретение относится к способу получения вышеупомянутых комплексов включения модификаций I-V торасемида и циклодекстринов или производных циклодекстрина. На практике данный способ может быть осуществлен по следующему ниже методу. Модификацию I, II, III, IV или V торасемида или любую смесь модификаций I, II, III, IV или V торасемида добавляют в водный раствор циклодекстринов или производных декстринов и с добавлением или без добавления водного раствора аммиака эту смесь перемешивают при температуре и в течение срока, необходимых для образования комплекса включения. После того, как комплекс включения образовался, воду удаляют лиофилизацией, распылительной сушкой, вакуумным выпариванием при низких температурах или любым другим способом, известным в области фармацевтической технологии. Физические смеси модификаций I-V торасемида и циклодекстринов или производных циклодекстринов, а также комплексы включения модификаций I-V торасемида и циклодекстринов или производных циклодекстринов, полученные по способам данного изобретения,могут, в качестве подходящей формы торасемида, использоваться как диуретик или средство профилактики поражений сердца или поражений ткани сердца, вызываемых метаболическими нарушениями или нарушениями электролитного баланса, связанными с ишемией, при лечении тромбоза, стенокардии, астмы, гипертензии,отека почек, отека сердца, первичного или вторичного альдостеронизма, синдрома Баттера,опухолей, глаукомы, снижения внутриглазного давления, острого или хронического бронхита,при лечении отека мозга, вызванного травмой,ишемией, сотрясением мозга, метастазами или эпилептическими припадками, и при лечении назальных инфекций, вызванных аллергенами. Данное изобретение относится также к лекарственным формам, таким как таблетки, капсулы, инъекции или аэрозольные препараты,содержащим физические смеси или комплексы включения модификаций I, II, III, IV или V торасемида и циклодекстринов, или производных 8 циклодекстринов, или любую смесь модификаций I, II, III, IV или V торасемида с циклодекстринами или производными циклодекстринов, в качестве активного ингредиента, без каких-либо добавок или в сочетании с одной или несколькими из фармацевтически приемлемых добавок,таких как сахар, крахмал, производные крахмала, целлюлоза, производные целлюлозы, средства, задающие режим выделения, и антиадгезивные средства и, необязательно, средства для регуляции текучести. Фиг. 1 представляет кривую ДСК -циклодекстрина. Фиг. 2 представляет кривую ДСК модификации I торасемида. Фиг. 3 представляет кривую ДСК физической смеси модификации I торасемида и циклодекстрина (мольное отношение 1:1). Фиг. 4 представляет кривую ДСК комплекса включения модификации I торасемида и-циклодекстрина (мольное отношение 1:1). Фиг. 5 представляет ИК-спектр -циклодекстрина, регистрируемый в KВr. Фиг. 6 представляет ИК-спектр модификации I торасемида, регистрируемый в KВr. Фиг. 7 представляет ИК-спектр физической смеси модификации I торасемида и -циклодекстрина (мольное отношение 1:1), регистрируемый в KВr. Фиг. 8 представляет ИК-спектр комплекса включения модификации I торасемида и -циклодекстрина (мольное отношение 1:1), регистрируемый в KВr. Фиг. 9 представляет вид рентгенограммы порошка -циклодекстрина. Фиг. 10 представляет вид рентгенограммы порошка модификации I торасемида. Фиг. 11 представляет вид рентгенограммы порошка физической смеси модификации I торасемида и -циклодекстрина (мольное отношение 1:1). Фиг. 12 представляет вид рентгенограммы порошка комплекса включения модификации I торасемида и -циклодекстрина (мольное отношение 1:1). Данное изобретение иллюстрируется, но не ограничивается следующими примерами. Пример 1. Модификацию I торасемида поPCT/WO 00/20395 (0,50 г) и эквимолярное количество -циклодекстрина гомогенизировали в миксере в течение 24 ч. Кривая дифференциальной сканирующей калориметрии (ДСК), представленная на фиг. 3,содержит экзотермические пики модификации I торасемида и -циклодекстрина. Анализ ДСК выполняли на аппарате Perkin-Elmer, модельDSC7 при скорости нагревания 25 С/мин. ИК-спектр, представленный на фиг. 7, содержит характерные пики модификации I торасемида и -циклодекстрина. ИК-спектр регист 9 рировали на ИК-спектрофотометре Nicolet, модель Magna 760, в интервале от 4000 до 600 см-1. Характерный вид рентгенограммы порошка представлен на фиг. 11 и зарегистрирован на диффрактометре PHILIPS, модель PW 3710 в интервале 2=5-40 с использованием лучей СuK=1,541 . Шаг регистрации составлял 0,029, и время регистрации составляло 1 с на шаг. Пример 2. Физическую смесь модификации I торасемида и -циклодекстрина, полученную в соответствии с примером 1 данного изобретения, подвергали испытанию на высвобождение активного вещества в воду при температуре 37 С (USP 24 - Фармакопея США 24), и результаты представлены в табл. 1. Таблица 1. Высвобождение торасемида из физической смеси модификации I торасемида и-циклодекстрина (мольное отношение 1:1) в воду (USP 24) (37 С, 50 об./мин, 1000 мл) Время, Высвобожденный торасемид, % мин модификация I физическая торасемида смесь 0 0 0 15 0,7 32,2 30 20,3 57,1 45 38,5 70,2 60 51,8 80,6 90 68,5 89,1 120 78,7 93,8 Пример 3. -Циклодекстрин (1,81 г) растворяли в 50 мл деминерализованной воды и добавляли 10 капель водного раствора аммиака. Затем к раствору добавляли эквимолярное количество модификации I торасемида, полученной по PCT/WO 00/20395, его энергично перемешивали в течение 24 ч и затем фильтровали и удаляли воду лиофилизацией. Образование комплекса включения торасемида и -циклодекстрина было доказано данными, полученными дифференциальной сканирующей калориметрией, ИК-анализом и по рентгенограмме порошка. Кривая дифференциальной сканирующей калориметрии (ДСК), представленная на фиг. 4,не содержит значительных пиков, характерных для модификации I торасемида и -циклодекстрина. ИК-спектр, представленный на фиг. 8,сильно отличается от ИК-спектра модификацииI торасемида и от ИК-спектра -циклодекстрина, представленных на фиг. 5 и 6. Рентгенограмма порошка, представленная на фиг. 12, сильно отличается от рентгенограммы порошка модификации I торасемида и рентгенограммы порошка -циклодекстрина, представленных на фиг. 10 и 11. Пример 4. -Циклодекстрин (0,28 г) растворяли в 50 мл деминерализованной воды, раствор нагревали до 80 С при энергичном пере 005111 10 мешивании, его перемешивали в течение 60 мин и затем добавляли эквимолярное количество модификации I торасемида, полученной в соответствии с PCT/WO 00/20395, в течение 90 мин. Затем горячий раствор фильтровали, охлаждали до комнатной температуры, после чего воду удаляли лиофилизацией. ИК-спектр полученного таким образом образца был идентичен ИК-спектру образца, полученного по примеру 3 данного изобретения. Пример 5. Комплекс включения модификации I торасемида и -циклодекстрина, полученный в соответствии с примером 3 данного изобретения, подвергали испытанию на высвобождение активного вещества в воду при температуре 37 С (USP 24), и результаты представлены в табл. 2. Таблица 2. Высвобождение торасемида из комплекса включения модификации I торасемида и -циклодекстрина (мольное отношение 1:1) в воду (USP 24) (37 С, 50 об./мин, 1000 мл) Время, Высвобожденный торасемид, % мин модификация комплекс включеI торасемида ния 0 0 0 15 0,7 95,8 30 20,3 98,2 45 38,5 97, 9 60 51,8 98,3 90 68,5 98,8 120 78,7 98,5 ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Физические смеси, отличающиеся тем,что они содержат торасемид и циклодекстрины или производные циклодекстринов. 2. Физические смеси по п.1, отличающиеся тем, что торасемид выбирают из группы, состоящей из модификаций I, II, III, IV и V или любой их смеси. 3. Физические смеси по п.1, отличающиеся тем, что циклодекстрин выбирают из группы,состоящей из -, - и -циклодекстрина. 4. Физические смеси по п.1, отличающиеся тем, что производные циклодекстрина выбирают из группы простых эфиров или смешанных простых эфиров -, - и -циклодекстринов,имеющих одну или несколько групп из ангидроглюкозных частей циклодекстрина, замещенных C1-6 алкилом, предпочтительно метилом,этилом или изопропилом; гидроксиC1-6 алкилом,предпочтительно гидроксиэтилом, или гидроксипропилом, или гидроксибутилом; карбоксиC1-6 алкилом, предпочтительно карбоксиметилом или карбоксиэтилом; C1-6 алкилкарбонилом,предпочтительно ацетилом, C1-6 алкоксикарбонилC1-6 алкилом или карбоксиC1-6 алкоксиC1-6 алкилом, предпочтительно карбоксиметоксипропилом или карбоксиэтоксипропилом; C1-6 11 алкоксикарбонилоксиC1-6 алкилом, предпочтительно 2-ацетилоксипропилом. 5. Физические смеси по п.1, отличающиеся тем, что производные циклодекстрина выбирают из группы, состоящей из 2-гидроксипропил-циклодекстрина, 2-гидроксипропилциклодекстрина, 2-гидроксипропилциклодекстрина, 2-гидроксиэтилциклодекстрина, 2-гидроксиэтилциклодекстрина,2,6-диметилциклодекстрина и (2-карбоксиметокси)пропил-циклодекстрина. 6. Физические смеси по п.1, отличающиеся тем, что торасемид и циклодекстрины или производные циклодекстринов находятся в мольном отношении от 1:0,1 до 1:5. 7. Способ получения физических смесей по п.1, отличающийся тем, что торасемид и циклодекстрины или производные циклодекстринов гомогенизируют. 8. Способ получения физических смесей по п.7, отличающийся тем, что указанную гомогенизацию осуществляют в ступке или смесителях. 9. Способ получения физических смесей по п.7, отличающийся тем, что указанное смешивание осуществляют при температуре от 10 до 100 С. 10. Способ получения физических смесей по п.7, отличающийся тем, что указанное смешивание проводят в течение от 0,1 до 24 ч. 11. Применение физических смесей по п.1 в качестве диуретика и в качестве средства для профилактики поражения сердца или повреждения ткани сердца, вызванных метаболическими или ионными нарушениями, связанными с ишемией, при лечении тромбоза, стенокардии, астмы, гипертензии, отека почек, отека легких,первичного и вторичного альдостеронизма,синдрома Баттера, опухолей, глаукомы, снижения внутриглазного давления, острого или хронического бронхита, при лечении отека мозга,вызванного травмой, ишемией, сотрясением мозга, метастазами или эпилептическими припадками, и при лечении назальных инфекций,вызванных аллергенами. 12. Лекарственная форма, отличающаяся тем, что она содержит физические смеси по п.1 в качестве активного вещества в сочетании с одной или несколькими фармацевтическими добавками, такими как сахар, крахмал, производные крахмала, целлюлоза, производные целлюлозы, средства, задающие режим выделения,и антиадгезивные средства и, необязательно,средства регуляции текучести. 13. Лекарственная форма по п.12, отличающаяся тем, что она является таблеткой, капсулой, формой для инъекций или аэрозолем. 14. Комплексы включения, отличающиеся тем, что они содержат торасемид и циклодекстрины или производные циклодекстринов. 12 15. Комплексы включения по п.14, отличающиеся тем, что циклодекстрин выбирают из группы, состоящей из -, - и -циклодекстрина. 16. Комплексы включения по п.14, отличающиеся тем, что производные циклодекстринов выбирают из группы простых эфиров или смешанных простых эфиров -, - и -циклодекстринов, имеющих одну или несколько групп из ангидроглюкозных частей циклодекстрина, замещенных C1-6 алкилом, предпочтительно метилом, этилом или изопропилом; гидроксиC1-6 алкилом, предпочтительно гидроксиэтилом, или гидроксипропилом, или гидроксибутилом; карбоксиC1-6 алкилом, предпочтительно карбоксиметилом или карбоксиэтилом;C1-6 алкилкарбонилом, предпочтительно ацетилом, C1-6 алкоксикарбонилC1-6 алкилом или карбоксиC1-6 алкоксиC1-6 алкилом, предпочтительно карбоксиметоксипропилом или карбоксиэтоксипропилом; C1-6 алкоксикарбонилоксиC1-6 алкилом, предпочтительно 2-ацетилоксипропилом. 17. Комплексы включения по п.14, отличающиеся тем, что производные циклодекстринов выбирают из группы, состоящей из 2-гидроксипропилциклодекстрина, 2-гидроксипропилциклодекстрина, 2-гидроксипропилциклодекстрина, 2-гидроксиэтилциклодекстрина, 2-гидроксиэтилциклодекстрина, 2,6-диметилциклодекстрина и (2-карбоксиметокси) пропилциклодекстрина. 18. Комплексы включения по п.14, отличающиеся тем, что торасемид и циклодекстрины или производные циклодекстринов находятся в мольном отношении от 1:0,1 до 1:5. 19. Способ получения комплексов включения по п.14, отличающийся тем, что торасемид и циклодекстрины или производные циклодекстринов взаимодействуют в воде с водным раствором основания или без него. 20. Способ получения комплексов включения по п.19, отличающийся тем, что в качестве водного раствора основания используют водный раствор аммиака. 21. Способ получения комплексов включения по п.19, отличающийся тем, что его осуществляют при температуре от 10 до 100 С. 22. Способ получения комплексов включения по п.19, отличающийся тем, что его осуществляют в течение от 0,1 ч до 7 дней. 23. Способ получения комплексов включения по п.19, отличающийся тем, что после образования указанного комплекса воду и основание удаляют сушкой. 24. Способ получения комплексов включения по п.23, отличающийся тем, что указанную сушку осуществляют лиофилизацией, распылительной сушкой, вакуумным выпариванием или вакуумной сушкой. 25. Применение комплексов по п.14 в качестве диуретика и в качестве средства для профилактики поражения сердца или поврежде 13 ния ткани сердца, вызванных метаболическими или ионными нарушениями, связанными с ишемией, при лечении тромбоза, стенокардии, астмы, гипертензии, отека почек, отека легких,первичного и вторичного альдостеронизма,синдрома Баттера, опухолей, глаукомы, снижения внутриглазного давления, острого или хронического бронхита, при лечении отека мозга,вызванного травмой, ишемией, сотрясением мозга, метастазами или эпилептическими припадками, и при лечении назальных инфекций,вызванных аллергенами. 14 26. Лекарственная форма, отличающаяся тем, что она содержит комплексы включения по п.14 в качестве активного вещества в сочетании с одной или несколькими фармацевтическими добавками, такими как сахар, крахмал, производные крахмала, целлюлоза, производные целлюлозы, определяющие высвобождение средства и антиадгезивные средства и, необязательно,средства регуляции текучести. 27. Лекарственная форма по п.26, отличающаяся тем, что она является таблеткой, капсулой, формой для инъекций или аэрозолем. Фиг. 1. ДСК -циклодекстрина Фиг. 4. ДСК комплекса включения модификации I торасемида и -циклодекстрина Фиг. 3. ДСК физической смеси модификации I торасемида и -циклодекстрина (мольное отношение 1:1) Фиг. 6. ИК-спектр модификации I торасемида, регистрируемый в KВr Фиг. 7. ИК-спектр физической смеси модификации I торасемида и -циклодекстрина Фиг. 8. ИК-спектр комплекса включения модификации I торасемида и -циклодекстрина Фиг. 10. Рентгенограмма порошка модификации I торасемида Фиг. 11. Рентгенограмма порошка физической смеси модификации I торасемида и -циклодекстрина (мольное отношение 1:1) Фиг. 12. Рентгенограмма порошка комплекса включения модификации I торасемида и циклодекстрина (мольное отношение 1:1).
МПК / Метки
МПК: A61K 47/40, A61P 9/00
Метки: n-(метилэтиламинокарбонил)-4-(3-метилфениламино)-3-пиридилсульфонамида, циклических, композиции, олигосахаридов
Код ссылки
<a href="https://eas.patents.su/9-5111-kompozicii-n-metiletilaminokarbonil-4-3-metilfenilamino-3-piridilsulfonamida-i-ciklicheskih-oligosaharidov.html" rel="bookmark" title="База патентов Евразийского Союза">Композиции n-(метилэтиламинокарбонил)-4-(3-метилфениламино)-3-пиридилсульфонамида и циклических олигосахаридов</a>
Предыдущий патент: Калийная соль 5-[4-[2-(n-метил-n-(2-пиридил)амино)этокси]бензил]тиазолидин-2,4-диона и ее применение в качестве противодиабетического лекарственного средства
Следующий патент: Сополимеры этилена и пленки из них
Случайный патент: Векторы и конструкции для доставки гриппозного антигена