Способ синтеза перфторсульфонамидов, перфторсульфонимидов и их солей, а также агент сульфонирования
Формула / Реферат
1. Способ перфторсульфонирования, заключающийся в том, что он включает стадию контактирования нуклеофильного соединения, у которого нуклеофильным атомом является атом азота, с реагентом, содержащим вводимые одновременно или последовательно сульфонилхлорид и неалкоилированное и одновременно жирорастворимое органическое основание, выбираемое из пространственно затрудненных диалкоилфосфинов, триалкоилфосфинов, гидроксидов фосфония, пространственно затрудненных диалкоиламинов, триалкоиламинов, гидроксидов аммония, причем органическая часть упомянутого сульфонилхлорида является перфторированной по атому углерода, связанному с атомом серы, а количество основания, по меньшей мере, равно стехиометрически необходимому для нейтрализации выделяемой в процессе реакции хлористо-водородной кислоты или взято в избытке, равном самое большее количеству, стехиометрически необходимому для нейтрализации выделяющейся хлористо-водородной кислоты.
2. Способ по п.1, отличающийся тем, что нуклеофильное соединение в нейтральной или анионной форме имеет в качестве ассоциированной кислоты кислоту, рКа которой самое большее равно приблизительно 7, преимущественно 6, предпочтительно 5.
3. Способ по пп.1 и 2, отличающийся тем, что азот нуклеофильного соединения связан с электроноакцепторной группой, преимущественно с сульфонильной, причем нуклеофильное соединение выбирают преимущественно из сульфамидов сульфоновых кислот, в которых сера связана с арилом, или из сульфамидов сульфоновых кислот, в которых сера связана с алифатическим радикалом, включая алкильные радикалы предпочтительно из сульфамидов сульфоновых кислот, в которых сера связана с алифатическим радикалом, перфторированных по атому углерода, находящемуся рядом с серой.
4. Способ по пп.1-3, отличающийся тем, что нуклеофильное соединение представляет собой соль сульфонамида (сульфамида) и неалкоилированного органического основания.
5. Способ по пп.1-4, отличающийся тем, что нуклеофильное соединение представляет собой сульфонамид (сульфамид) в форме жирорастворимой соли с упомянутым неалкоилированным и одновременно жирорастворимым органическим основанием.
6. Способ по пп.1-5, отличающийся тем, что упомянутое неалкоилированное органическое основание выбирают из пространственно затрудненных диалкоилфосфинов, триалкоилфосфинов, гидроксидов фосфония, пространственно затрудненных диалкоиламинов, триалкоиламинов, гидроксидов аммония.
7. Способ по пп.1-6, отличающийся тем, что упомянутое неалкоилированное и одновременно жирорастворимое основание имеет, по меньшей мере, значительную растворимость в бензоле (символ "s" согласно справочнику по химии и физике), преимущественно высокую растворимость в бензоле (символ "v" согласно справочнику по химии и физике).
8. Способ по пп.1-7, отличающийся тем, что упомянутое органическое основание имеет, по меньшей мере, значительную растворимость (символ "s" согласно справочнику по химии и физике), преимущественно высокую растворимость (символ "v" согласно справочнику по химии и физике).
9. Способ по пп.1-8, отличающийся тем, что рКа кислоты, ассоциированной с упомянутым органическим основанием, выше или равно рКа упомянутого сульфонамида.
10. Способ по пп.1-9, отличающийся тем, что рКа кислоты, ассоциированной с неалкоилированным и жирорастворимым основанием выше или равно рКа вышеупомянутого сульфонамида.
11. Способ по пп.1-10, отличающийся тем, что если нуклеофильным соединением является соль сульфонамида (сульфамида) и неалкоилированного органического основания, то указанное неалкоилированное органическое основание и указанное неалкоилированное и одновременно жирорастворимое основание являются идентичными.
12. Способ по пп.1-11, отличающийся тем, что контактирование осуществляют в органическом растворителе, преимущественно в слабополярном, предпочтительно мало смешивающемся с водой (не более 10 мас.%, преимущественно не более 5 мас.%, предпочтительно не более 2 мас.%).
13. Способ по пп.1-12, отличающийся тем, что контактирование осуществляют в органическом растворителе, который выбирают таким образом, чтобы упомянутая соль была растворима в нем преимущественно в концентрации по меньшей мере 0,05 М, предпочтительно по меньшей мере 0,2 М.
14. Способ по пп.1-13, отличающийся тем, что органическая часть сульфонилхлорида одинакова с органической частью сульфонамида.
15. Способ по пп.1-14, отличающийся тем, что органические части, одинаковые или разные, сульфонилхлорида и сульфонамида выбирают из радикалов формулы (Rf)
-(CX2)p-GEA,
где X, одинаковые или разные, обозначают фтор или радикал формулы CnF2n+1, где n - целое число, самое большее, равное 5, предпочтительно 2;
p обозначает целое число, самое большее, равное 2;
GEA обозначает электроноакцепторную группу, в которой возможные функциональные группы инертны в условиях реакции, преимущественно атом фтора или перфторированный радикал формулы CnF2n+1, где n - целое число, самое большее, равное 8, преимущественно 5, причем общее число атомов углерода в Rf составляет преимущественно от 1 до 15, предпочтительно от 1 до 10.
16. Способ по пп.1-15, отличающийся тем, что нуклеофильное соединение, нуклеофильным атомом которого является азот, представляет собой соль сульфонамида (сульфамида) и неалкоилированного органического основания, причем вышеупомянутый способ содержит после возможной стадии очистки и/или выделения стадию обработки гидроксидом или основной солью лития.
17. Реагент для осуществления способа по пп.1-16, характеризующийся тем, что он содержит вводимые одновременно или последовательно тяжелый сульфонилгалогенид (с атомным номером галогена, по меньшей мере равным атомному номеру хлора), преимущественно сульфонилхлорид, и неалкоилированное и одновременно жирорастворимое органическое основание, выбираемое из пространственно затрудненных диалкоилфосфинов, триалкоилфосфинов, гидроксидов фосфония, пространственно затрудненных диалкоиламинов, триалкоиламинов, гидроксидов аммония, и слабополярный растворитель, причем органическая часть упомянутого сульфонилгалогенида является перфторированной по атому углерода, связанному с атомом серы.
18. Реагент по п.17, отличающийся тем, что слабополярный растворитель, включая смесь растворителей, выбирают среди растворителей, имеющих низкую растворимость в воде и не содержащих хлорированной алифатической цепочки.
19. Реагент по пп.17 и 18, отличающийся тем, что слабополярный растворитель выбирают среди тех растворителей, полярность которых (Eft, выраженная в ккал/моль) самое большее равна 40 (преимущественно две значащие цифры).
20. Реагент по пп.17-19, отличающийся тем, что слабополярный растворитель выбирают среди кислородсодержащих органических соединений (в частности, простых эфиров, сложных эфиров и даже кетонов), углеводородов (включая нефтяные фракции), ароматических углеводородов, галогенированных в ядре.
21. Реагент по пп.17-20, отличающийся тем, что слабополярный растворитель выбирают из замещенных бензолов и углеводородов, галогенированных в ядре.
Текст
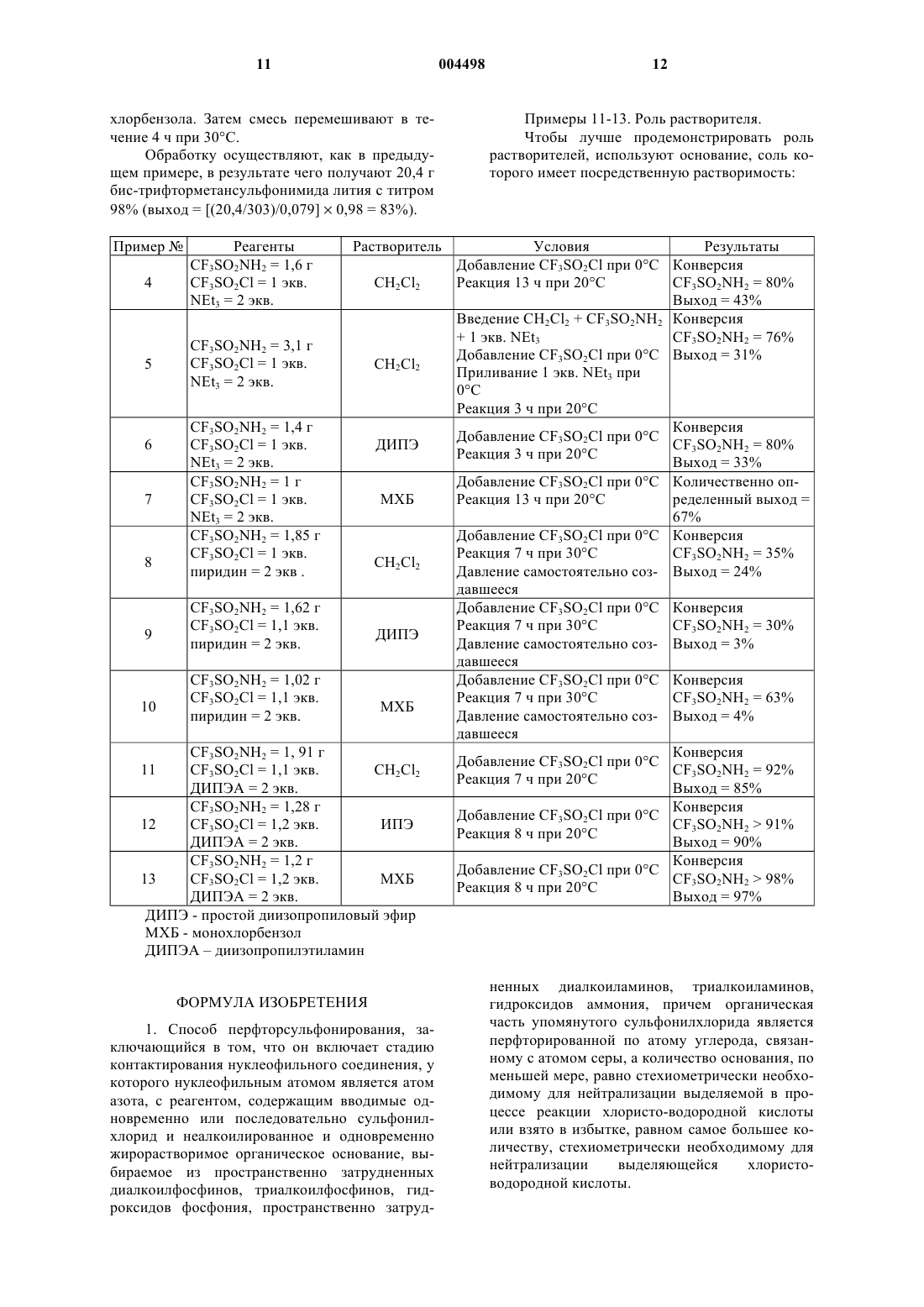
1 Настоящее изобретение относится к способу синтеза перфторсульфонамидов и перфторсульфонимидов, а также их солей. Настоящее изобретение относится также к агенту перфторсульфонирования. Более конкретно, оно касается реакции сульфонирования азотсодержащей функциональной группы, несущей электроноакцепторный радикал. В частности, оно касается сульфонирования сульфонамида, в частности, фторсодержащего сульфонамида. Синтез сульфамидов предусматривает в особенности тот случай, когда сульфамид получают с целью последующего сульфонирования (на втором этапе, в том же самом реакторе, или одновременно in situ). Фторсодержащие производные сульфонимидов все больше и больше используются в электротехнике, особенно для создания батарей,а также в связи с их каталитическими свойствами. Наиболее часто используемым производным этих сульфонимидов является литийсодержащее производное, т.е. соль этого имида, имида, который сам по себе является очень кислым. Синтез этих сульфонимидов уже был осуществлен, но с использованием очень тонких и сложных в осуществлении способов. В международной заявке на патент WO 97/23448 описан способ, в котором, как во всех ранее описанных способах (например, во французской заявке на патент 2724380), используют перфторалкансульфонилфториды, реакционная способность которых очень специфична и побочным продуктом которых является фторидион, который требует применения материалов,устойчивых по отношению к нему, и, следовательно, дорогих, а также полного удаления его перед выбросом эффлюентов. Очень высокая летучесть и условия осуществления способа приводят, как правило, к необходимости работать при относительно высоких давлениях. Как следует из указанного документа, чувствительность перфторалкансульфонилфторидов к воде особенно высока. Некоторые опыты были осуществлены с сульфонилгалогенидами, но они привели к неудаче (проблемы, связанные с их получением,изложены в международной заявке на патентWO 90/11999, см., например, стр. 2, строки с 30 по 35 и др.). Наиболее трудно осуществим оказался синтез бис-трифторметилсульфинимида,исходя из трифторметансульфонилхлорида. Поэтому одной из целей настоящего изобретения является разработка способа, который позволил бы получать фторсодержащие имиды описанного выше типа, используя тяжелые сульфонилгалогениды (т.е. галогениды, соответствующие галогену с атомным номером, по меньшей мере равным атомному номеру хлора). По экономическим соображениям предпочитают использовать сульфонилхлориды. Эта цель, а также другие сопутствующие цели достигаются с помощью способа, который 2 содержит стадию контактирования нуклеофила,нуклеофильным атомом которого является азот,с реагентом, имеющим в своем составе для последовательного или одновременного введения тяжелый галогенид (т.е. атомный номер,по меньшей мере, равен атомному номеру хлора) сульфонила, преимущественно хлорид сульфонила, и органическое основание, являющееся одновременно неалкоилируемым и жирорастворимым; при условии, что если нуклеофильный атом азота субстрата не несет сульфонильной группы, в которой углерод, соседний с серой,является перфторированным, то органическая часть вышеупомянутого тяжелого сульфонилгалогенида содержит перфторированный углерод,связанный с серой. Таким образом, способ особенно интересен тогда, когда органическая часть вышеупомянутого тяжелого сульфонилгалогенида имеет перфторированный углерод, который связан с серой. Настоящее изобретение относится к способу получения перфторсульфонамидов и перфторсульфонимидов, которые содержат по меньшей мере одну, преимущественно две сульфонильные группы, атом углерода которой,соединенный с атомом серы, является перфторированным. Соли этих имидов получают известным способом, исходя из самих имидов. Способ согласно настоящему изобретению может включать в себя стадию получения этих солей (как в примерах). Понятие органическое основание, являющееся одновременно неалкоилированным и жирорастворимым, разъясняется ниже. Вышеупомянутый азот нуклеофильной группы является преимущественно носителем водорода или отрицательного заряда (анион). Предпочтительно, чтобы вышеупомянутый азот нуклеофильной группы был носителем 2 атомов водорода (и даже 3, для частного случая аммиака или гидроксида аммония, который позволяет синтезировать предпочтительную категорию субстратов, а именно сульфамиды, предпочтительно перфторированные по углероду,связанному с серой, предпочтительно отвечающие определению Rf) или носителем водорода и отрицательного заряда (анион). В частности, нуклеофилом может быть сульфонамид (сульфамид), в частности, в форме соли преимущественно с неалкоилированным органическим основанием. Способ приемлем даже тогда, когда органическая часть вышеупомянутого сульфонамида (сульфамида) перфторирована по углероду, связанному с серой. Используемые сульфамиды (соответствующие неперфторированным сульфоновым кислотам, таким как Ar-SО 3 Н, где Ar представляет собой арил, и RSO3H, где R представляет 3 собой алкоил), нецелесообразно иметь в форме соли, которую к тому же трудно получить с предпочтительными основаниями согласно изобретению. В настоящем описании термин АЛКО-ил используют в его этимологическом значении: получаемый от углеводородного остатка АЛКО-ол после удаления функциональной группы спирта (или окончания "ол"). Нуклеофильный субстрат содержит, таким образом, в качестве нуклеофильной группы группу, выбираемую преимущественно из сульфамидов сульфоновых кислот, атом серы которых связан с арильным радикалом или алифатическим радикалом, включая алкоильные радикалы предпочтительно с алифатическим радикалом, перфторированным по углероду, находящемуся рядом с серой. Обычно число атомов углерода нуклеофильного субстрата изменяется в интервале от 1 до 15 и даже от 1 до 10. Итак, исходя из изложенного выше и из исследований, которые привели к настоящему изобретению, следует, что нуклеофилами (в нейтральной форме или особенно анионной форме), сложные проблемы с которыми особенно хорошо решаются настоящим изобретением,являются такие соединения, в которых ассоциированная кислота имеет рKа, самое большее,равное приблизительно 7, преимущественно 6 и предпочтительно 5. Аммиак представляет собой особенный случай и может, в случае аммиака, приводить к имиду в результате двух последовательных конденсаций in situ. Конденсация тяжелых сульфонилгалогенидов, согласно изобретению, с аммиаком или с гидроксидом аммония может представлятьсобой предварительную стадию конденсации амидов. В настоящем описании термин "приблизительно" применяют для того, чтобы подчеркнуть, что величины, которые указаны этим термином, соответствуют математически округленным величинам и, особенно, когда одна или более самая правая цифра от числа представляют собой нули, эти нули являются нулями положения, а не значащими цифрами, за исключением, разумеется, случаев, когда оговорено иное. Преимущественно вышеупомянутое неалкоилированное органическое основание выбирают среди пространственно затрудненных диалкоилфосфинов, триалкоилфосфинов, гидроксидов фосфония, пространственно затрудненных диалкоиламинов, триалкоиламинов, гидроксидов аммония. Равным образом, можно назвать фосфорсодержащие и азотсодержащие циклы, имеющие соответствующую основность(см. ниже). Например, кольца пиридинового типа, согласно настоящему изобретению и вопреки известному, эти основные функциональные группы ароматических гетероциклов не являются предпочтительными основаниями. 4 Желательно, чтобы вышеупомянутое основание, одновременно неалкоилированное и жирорастворимое, было выбрано среди пространственно затрудненных диалкоилфосфинов, триалкоилфосфинов, гидроксидов фосфония, пространственно затрудненных диалкоиламинов,триалкоиламинов, гидроксидов аммония. Рекомендуется, чтобы вышеупомянутое основание, одновременно неалкоилируемое и жирорастворимое, имело, по меньшей мере,определенную растворимость в бензоле (символ"s" в справочнике по химии и физике), преимущественно (символ "v" в справочнике по химии и физике) высокую. Рекомендуется, чтобы субстрат имел, по меньшей мере, определенную растворимость в бензоле (символ "s" в справочнике по химии и физике), преимущественно (символ "v" в справочнике по химии и физике) высокую. Также согласно настоящему изобретению предпочтительно, чтобы нуклеофильный субстрат находился в форме соли с неалкоилированным органическим основанием, это возможное солевое соединение между органическим основанием и вышеупомянутым субстратом (когда он кислый, как в случае перфторсульфонамида) имеет, по меньшей мере,определенную растворимость в бензоле (символ"s" в справочнике по химии и физике), преимущественно (символ "v" в справочнике по химии и физике) высокую. В указанных случаях особенно предпочтительно, чтобы растворимость была такой, чтобы бензол и основания, указанные выше, смешивались друг с другом в любом соотношении (символ "х" в справочнике по химии и физике). Чтобы выбрать основание, следует соблюдать требование основности, а также желательно, чтобы рKа кислоты, ассоциированной с вышеупомянутым органическим основанием (образующей возможную соль с нуклеофилом) было больше или близко к рKа вышеупомянутого нуклеофила (например, сульфонамида, который в основном является носителем двух атомов водорода на азоте). Также желательно, чтобы рKа кислоты, ассоциированной с вышеупомянутым неалкоилированным и жирорастворимым основанием, было равно и предпочтительно больше рKа вышеупомянутого сульфонамида. Когда имеется неравенство, то желательно,чтобы разность между величинами рKа ассоциированных кислот и величиной рKа вышеупомянутого нуклеофила была, по меньшей мере, равна 1, преимущественно 2 и предпочтительно 3. Хотя это не является предпочтительным,основания могут представлять собой смеси оснований, при условии, что смесь отвечает требованиям, оговоренным выше. Можно уточнить, что когда вышеупомянутый нуклеофил представляет собой сульфамид, 5 по причинам простоты в обращении предпочтительно, чтобы вышеупомянутое неалкоилированное органическое основание и вышеупомянутое основание, одновременно неалкоилированное и жирорастворимое, были идентичны. Реакция может быть проведена в растворителе, особенно, когда органические основания выбраны среди предпочтительных, т.е., в частности, жирорастворимых и слабополярных (например и особенно, триалкоиламинов, содержащих больше 6 атомов углерода; триалкоиламинов, содержащих меньше 7 атомов углерода,но содержащих по меньшей мере один вторичный или третичный радикал, преимущественно два, или пространственно затрудненного диалкоиламина). Благоприятные условия осуществления вышеупомянутой стадии заключаются в контактировании реагентов в органическом растворителе, составляющем преимущественно не более 5 мас.%, предпочтительно не более 2 мас.%. Температура реакции преимущественно,по меньшей мере, равна конечной температуре плавления (за исключением нерастворимых и, в частности, солей [галогенгидратов]) реакционной смеси и преимущественно не больше 100 С(преимущественно две значащие цифры, предпочтительно 3), преимущественно самое большее равной 50 С, предпочтительно 40 С и преимущественно, по меньшей мере, равна 0 С. Таким образом, температура реакции преимущественно находится в интервале, ограниченном конечной температурой плавления и 100 С. Предпочтительно в интервале от 0 до 50 С, более предпочтительно в интервале от 0 до 40 С. Хотя реакция может быть проведена при разном давлении, ее легче проводить при атмосферном давлении. В этом случае целесообразно выбрать растворители таким образом, чтобы было возможно кипятить с обратным холодильником при температуре, выбранной в вышеуказанных интервалах температур. Чтобы обеспечить хорошую кинетику реакции, рекомендуется осуществлять вышеупомянутое контактирование в органическом растворителе, который выбирают таким образом,чтобы, когда вышеупомянутым нуклеофилом является соль сульфамида, вышеупомянутая соль была бы в нем растворима преимущественно в концентрации по меньшей мере 0,05 М,предпочтительно по меньшей мере 0,2 М. Чтобы добиться этой растворимости, можно варьировать вышеупомянутое неалкоилируемое органическое основание. Равным образом, можно варьировать растворитель и органическое основание одновременно. Основания, используемые в настоящем изобретении, содержат преимущественно от 3 до приблизительно 40 атомов углерода, предпочтительно от 6 до приблизительно 30 атомов углерода, более предпочтительно от 8 до 25 атомов углерода. В частности, когда число ато 004498 6 мов углевода низкое (т.е. меньше 7), предпочтительно, чтобы по меньшей мере один из заместителей основного атома был бы, по меньшей мере, вторичным. По экономическим соображениям эти основания представляют собой, в основном, амины. Основаниями также могут быть полифункциональные основания (например, замещенные этилендиамины и, в частности, тетраметилэтилендиамин), в этом случае вышеуказанное ограничение должно быть приведено к числу используемых основных функциональных групп. Наиболее пригодными растворителями являются относительно слабополярные растворители типа хлорсодержащих растворителей или ароматических растворителей при предпочтительном условии, что возможная вышеупомянутая соль будет в нем достаточно растворима. Вышеупомянутый слабополярный растворитель, который может представлять собой смесь, выбирают, преимущественно, из тех растворителей, полярность которых (Eft, выраженная в ккал/моль), самое большее равна 40 (преимущественно две значащие цифры). Однако из соображений гигиены труда и защиты окружающей среды [некоторые отныне запрещены], следует избегать использовать в качестве растворителя неароматические хлорсодержащие производные, особенно алифатические (такие как метиленхлорид; хлороформ) или алкеновые (например, трихлорэтилен). Кроме того, хотя они дают хорошие результаты, эти растворители не представляют собой группу,дающую наилучшие результаты (так, растворимость в воде метиленхлорида составляет порядка 2 об.% или 2,6 мас.%). Принимая во внимание вышеизложенное,вышеупомянутый слабополярный растворитель выбирают среди кислородсодержащих органических соединений (в частности, простых эфиров, сложных эфиров и даже кетонов), углеводородов (включая нефтяные фракции), ароматических углеводородов, галогенированных в ядре. Предпочтительно можно выбрать вышеупомянутый слабополярный растворитель среди замещенных бензолов и углеводородов, галогенированных в ядре. Желательно соблюдать стехиометрию реакции между сульфонилгалогенидом и сульфонамидом (сульфамидом). Отклонение плюс или минус 20% является приемлемым и зависит,главным образом, от соответствующей стоимости реагентов. Количество вышеупомянутого неалкоилированного и жирорастворимого основания, вводимого в реакцию, по меньшей мере, равно количеству, необходимому для нейтрализации выделяющейся галогенводородной кислоты. Когда азот субстрата несет два атома водорода (три в совершенно особенном случае 7 аммиака, который позволяет синтезировать,особенно in situ, предпочтительную категорию субстратов, а именно сульфамиды, преимущественно перфторированные по углероду, связанному с серой, предпочтительно отвечающие определению Rf; разумеется, в случае синтеза insitu надо принимать во внимание реакцию сульфонирования аммиака) и нуклеофил не находится в форме соли, целесообразно довести количество основания (или оснований), вводимого в реакцию, до величины, по меньшей мере равной двукратному количеству, необходимому для нейтрализации выделяющейся галогенводородной кислоты. Другими словами и более конкретно,предпочтительно, чтобы суммарное количество оснований (основания соли субстрата (см. выше) и неалкоилированного жирорастворимого основания) было, по меньшей мере, равно сумме кислотности, выделяющейся в форме галогенводородной кислоты и кислотности соединений, содержащих сульфогруппы (в особенности,сульфонимидов) в стадии образования. Таким образом, учитывая вышеизложенное, желательно, чтобы суммарное количество основания (или оснований) было, по меньшей мере, равно количеству, стехиометрически необходимому для нейтрализации выделяющейся галогенводородной кислоты, преимущественно,по меньшей мере, равно сумме кислотности,выделяющейся в форме галогенводородной кислоты и кислотности соединений, содержащих сульфогруппы (в особенности, сульфонимидов); более конкретно, рекомендуется использовать количество основания (выраженное в эквивалентах), по меньшей мере равное сумме кислотности сульфоновых соединений, и кислотности 1,25 кратного количества, необходимого для нейтрализации выделяющейся галогенводородной кислоты, преимущественно по меньшей мере равное сумме 1,5 кратной кислотности,выделяющейся в форме галогенводородной кислоты, и кислотности сульфоновых соединений. Также предпочтительно избегать слишком большого избытка основания(ий), поэтому желательно, чтобы суммарное количество оснований (основание соли субстрата [см. выше] и неалкоилируемое жирорастворимое основание) находилось в избытке по отношению к сумме кислотности, выделяющейся в форме галогенводородной кислоты и кислотности образующихся сульфоновых соединений, самое большее 3-х кратном, предпочтительно 2-х кратном,предпочтительно однократном количеству выделяющейся галогенводородной кислоты. Способ согласно настоящему изобретению является особенно интересным для синтеза соединений, получаемых исходя из сульфонилхлорида, органическая часть которых перфторирована (т.е. соответствует СХ 2, см. ниже) по атому углерода, связанному с серой. 8 Настоящее изобретение относится, в частности, к случаю, когда органическая часть вышеупомянутого сульфонилхлорида та же самая,что органическая часть вышеупомянутого сульфонамида. Настоящее изобретение относится также к случаю, когда органическая часть вышеупомянутого сульфонилхлорида несет, по меньшей мере временно, в форме промежуточного продукта сульфамидную группу. Это позволяет получать циклические продукты или полимерные продукты. Как это обычно хорошо известно специалисту по реакциям конденсации, циклизация или поликонденсация происходит в зависимости от числа звеньев, разделяющих две функциональные группы, в зависимости от разбавления реакционной среды (это очень известное явление, упоминаемое в заявке на патентWO 97/23448). Настоящее изобретение особенно пригодно для осуществления конденсации, когда органические части, одинаковые или разные, вышеупомянутого сульфонилгалогенида и вышеупомянутого сульфонамида выбраны из радикалов формулы (Rf)-(CX2)p-GEA где X, одинаковые или разные, обозначают фтор или радикал формулы CnF2n+1, где n - целое число не более 5, предпочтительно не более 2; р обозначает целое число, самое большее,равное 2;GEA обозначает электроноакцепторную группу, в которой возможные функциональные группы инертны в условиях реакции, преимущественно фтор или перфторированный радикал формулы CnF2n+1, где n - целое число, равное 8, преимущественно 5. Общее число атомов углерода в Rf составляет преимущественно от 1 до 15, предпочтительно от 1 до 10.GEA может представлять собой тяжелый сульфонилгалогенид или нести тяжелую сульфонилгалогенидную функциональную группу. Именно это позволяет получать in situ соединения, несущие одновременно нуклеофильную группу и тяжелую сульфонилгалогенидную группу, соединения, в которых органическая часть вышеупомянутого сульфонилхлорида несет сульфамидную группу. Это позволяет получать циклические продукты или полимерные продукты. Как было указано выше, наиболее интересными соединениями, получаемыми из имидов, синтезированных согласно настоящему изобретению, являются литиевые производные,вышеупомянутый способ содержит, дополнительно, после возможной стадии очистки и/или выделения, стадию обработки гидроксидом или основной солью лития. Согласно настоящему изобретению исходные сульфонамиды могут быть синтезированы из того же самого сульфонилгалогенида, кото 9 рый используют для синтеза имида. Этот синтез может быть осуществлен в полярных, протонных или апротонных растворителях, при условии, что они не имеют естественной склонности к алкоилированию. в частности, реакция может быть проведена в простых циклических или нециклических эфирах, симметричных или несимметричных. Другим объектом настоящего изобретения является реагент, используемый в описанных выше способах. Этот реагент содержит для последовательного или одновременного введения тяжелый сульфонилгалогенид (т.е. у которого атомный номер галогена, по меньшей мере,равен атомному номеру хлора), преимущественно сульфонилхлорид,органическое основание, одновременно неалкоилированное и жирорастворимое,преимущественно слабополярный растворитель,причем органическая часть вышеупомянутого сульфонила перфторирована по углероду,который связан с серой. Другим объектом настоящего изобретения является использование сульфонилгалогенида,перфторированного по углероду, который связан с серой, т.е. находящемуся рядом с ней, для моно- и бисульфонирования гидроксида аммония, аммиака, амида, включая сульфамид. Эта реакция протекает преимущественно в присутствии неалкоилированного и жирорастворимого органического основания. В частности, его используют в синтезах, приводящих к солям, преимущественно щелочным, имида, несущего по меньшей мере одну, предпочтительно две сульфированные группы, перфторированные по алифатическому атому углерода (т.е. в sp3 гибридизации), находящемуся рядом с серой. Одним из преимуществ использования хлорида является низкая чувствительность к побочным реакциям с водой. Для того чтобы лучше понять изобретение,можно дать для сведения типичные реакцииRf-SO2Cl + Nu-Cl- + Rf-SO2Nu и если предпочтительно Nu является по своей природе NuH (или, более точно, если рассматриваемая нуклеофильная группа Nu имеет структуру -NH- [т.е. структуру NH- или NH2]),Rf-SO2NuH + ВRf-SO2Nu-BH+ где NuH и Nu- обозначают, соответственно,нуклеофил в нейтральной и анионной форме. Наиболее интересными субстратами являются те, в которых Nu выбирают среди Ar-SO2NH-, в особенности R-SO2-NH-, включая предпочтительно Rf-SO2-NH-. Следующие примеры, не имеющие ограничительного характера, иллюстрируют изобретение. 10 Пример 1. Получение трифторметансульфонамида: CF3SO2NH2. Реакция в безводной среде. В реактор загружают 15,3 г трифторметансульфонилхлорида, растворенного в 103 г безводного простого изопропилового эфира. Среду охлаждают до 5 С и в течение 2 ч медленно добавляют аммиак. После 5 ч перемешивания при 5 С добавляют 24,8 г воды, чтобы растворить соли. Затем среду подкисляют путем добавления 20,7 г 36%-ного водного раствора соляной кислоты. После нового добавления 13 г воды фазы разделяются. Водную фазу промывают 50 г простого изопропилового эфира. Органические фазы объединяют и при пониженном давлении удаляют растворитель. Таким образом получают 10,15 г твердого белого трифторметансульфонамида. Температура плавления (по Коффлеру) = 119 С. Реакция в водной среде. Реакцию проводят аналогичным образом,используя 30%-ный водный раствор аммиака. Пример 2. Получение бис-трифторметилсульфинимида лития. В реактор загружают 1 л монохлорбензола и 164,6 г трифторметансульфонамида, полученного согласно предыдущему примеру. Затем к этой суспензии добавляют 224,6 г триэтиламина. Полученный раствор охлаждают до 5 С. Затем в течение 40 мин при температуре от 0 до 5 С добавляют раствор 187 г трифторметансульфонилхлорида в 191 г монохлорбензола. Затем доводят температуру до 28 С. После 4 ч реакции реакционную среду фильтруют. Фильтрат дегазируют путем барботирования азота, затем промывают 436 г воды. 2 нижние органические фазы выделяют и вновь промывают 507 г воды. Затем эти органические фазы обрабатывают раствором 46,7 г гидратированного гидроксида лития в 216 г воды. Полученная среда является двухфазной. Водную фазу выделяют и экстрагируют 226 г простого изопропилового эфира. Эту последнюю органическую фазу выпаривают при пониженном давлении, в результате чего получают 206 г неочищенного бистрифторметансульфонимида лития в форме твердого желтоватого вещества. Выход = 60%. ЯМР 19F = -1,8 м.д. Пример 3. Реакция в присутствии диизопропилэтиламина. В реактор загружают 11,2 г (0,079 М) амида трифторметансульфоновой кислоты в 73 г монохлорбензола. После добавления 20,7 г (0,16 М) диизопропилэтиламина при 10 С в течение 45 мин приливают раствор 14,7 г (0,087 М) трифторметансульфонилхлорида в 15 г моно 11 хлорбензола. Затем смесь перемешивают в течение 4 ч при 30 С. Обработку осуществляют, как в предыдущем примере, в результате чего получают 20,4 г бис-трифторметансульфонимида лития с титром 98% (выход = [(20,4/303)/0,079]0,98 = 83%). Пример 4CF3SO2Cl = 1,2 экв. 13 МХБ ДИПЭА = 2 экв. ДИПЭ - простой диизопропиловый эфир МХБ - монохлорбензол ДИПЭАдиизопропилэтиламин 11 ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ перфторсульфонирования, заключающийся в том, что он включает стадию контактирования нуклеофильного соединения, у которого нуклеофильным атомом является атом азота, с реагентом, содержащим вводимые одновременно или последовательно сульфонилхлорид и неалкоилированное и одновременно жирорастворимое органическое основание, выбираемое из пространственно затрудненных диалкоилфосфинов, триалкоилфосфинов, гидроксидов фосфония, пространственно затруд 12 Примеры 11-13. Роль растворителя. Чтобы лучше продемонстрировать роль растворителей, используют основание, соль которого имеет посредственную растворимость: Условия Результаты Добавление CF3SO2Cl при 0 С Конверсия Реакция 13 ч при 20 СCF3SO2NH2 = 63% Давление самостоятельно соз- Выход = 4% давшееся Конверсия Добавление CF3SO2Cl при 0 С ненных диалкоиламинов, триалкоиламинов,гидроксидов аммония, причем органическая часть упомянутого сульфонилхлорида является перфторированной по атому углерода, связанному с атомом серы, а количество основания, по меньшей мере, равно стехиометрически необходимому для нейтрализации выделяемой в процессе реакции хлористо-водородной кислоты или взято в избытке, равном самое большее количеству, стехиометрически необходимому для нейтрализации выделяющейся хлористоводородной кислоты. 13 2. Способ по п.1, отличающийся тем, что нуклеофильное соединение в нейтральной или анионной форме имеет в качестве ассоциированной кислоты кислоту, рKа которой самое большее равно приблизительно 7, преимущественно 6, предпочтительно 5. 3. Способ по пп.1 и 2, отличающийся тем,что азот нуклеофильного соединения связан с электроноакцепторной группой, преимущественно с сульфонильной, причем нуклеофильное соединение выбирают преимущественно из сульфамидов сульфоновых кислот, в которых сера связана с арилом, или из сульфамидов сульфоновых кислот, в которых сера связана с алифатическим радикалом, включая алкильные радикалы предпочтительно из сульфамидов сульфоновых кислот, в которых сера связана с алифатическим радикалом, перфторированных по атому углерода, находящемуся рядом с серой. 4. Способ по пп.1-3, отличающийся тем,что нуклеофильное соединение представляет собой соль сульфонамида (сульфамида) и неалкоилированного органического основания. 5. Способ по пп.1-4, отличающийся тем,что нуклеофильное соединение представляет собой сульфонамид (сульфамид) в форме жирорастворимой соли с упомянутым неалкоилированным и одновременно жирорастворимым органическим основанием. 6. Способ по пп.1-5, отличающийся тем,что упомянутое неалкоилированное органическое основание выбирают из пространственно затрудненных диалкоилфосфинов, триалкоилфосфинов, гидроксидов фосфония, пространственно затрудненных диалкоиламинов, триалкоиламинов, гидроксидов аммония. 7. Способ по пп.1-6, отличающийся тем,что упомянутое неалкоилированное и одновременно жирорастворимое основание имеет, по меньшей мере, значительную растворимость в бензоле (символ "s" согласно справочнику по химии и физике), преимущественно высокую растворимость в бензоле (символ "v" согласно справочнику по химии и физике). 8. Способ по пп.1-7, отличающийся тем,что упомянутое органическое основание имеет,по меньшей мере, значительную растворимость(символ "s" согласно справочнику по химии и физике), преимущественно высокую растворимость (символ "v" согласно справочнику по химии и физике). 9. Способ по пп.1-8, отличающийся тем,что рKа кислоты, ассоциированной с упомянутым органическим основанием, выше или равно рKа упомянутого сульфонамида. 10. Способ по пп.1-9, отличающийся тем,что рKа кислоты, ассоциированной с неалкоилированным и жирорастворимым основанием выше или равно рKа вышеупомянутого сульфонамида. 14 11. Способ по пп.1-10, отличающийся тем,что если нуклеофильным соединением является соль сульфонамида (сульфамида) и неалкоилированного органического основания, то указанное неалкоилированное органическое основание и указанное неалкоилированное и одновременно жирорастворимое основание являются идентичными. 12. Способ по пп.1-11, отличающийся тем,что контактирование осуществляют в органическом растворителе, преимущественно в слабополярном, предпочтительно мало смешивающемся с водой (не более 10 мас.%, преимущественно не более 5 мас.%, предпочтительно не более 2 мас.%). 13. Способ по пп.1-12, отличающийся тем,что контактирование осуществляют в органическом растворителе, который выбирают таким образом, чтобы упомянутая соль была растворима в нем преимущественно в концентрации по меньшей мере 0,05 М, предпочтительно по меньшей мере 0,2 М. 14. Способ по пп.1-13, отличающийся тем,что органическая часть сульфонилхлорида одинакова с органической частью сульфонамида. 15. Способ по пп.1-14, отличающийся тем,что органические части, одинаковые или разные, сульфонилхлорида и сульфонамида выбирают из радикалов формулы (Rf)-(CX2)p-GEA,где X, одинаковые или разные, обозначают фтор или радикал формулы CnF2n+1, где n - целое число, самое большее, равное 5, предпочтительно 2; р обозначает целое число, самое большее,равное 2;GEA обозначает электроноакцепторную группу, в которой возможные функциональные группы инертны в условиях реакции, преимущественно атом фтора или перфторированный радикал формулы CnF2n+1, где n - целое число,самое большее, равное 8, преимущественно 5,причем общее число атомов углерода в Rf составляет преимущественно от 1 до 15, предпочтительно от 1 до 10. 16. Способ по пп.1-15, отличающийся тем,что нуклеофильное соединение, нуклеофильным атомом которого является азот, представляет собой соль сульфонамида (сульфамида) и неалкоилированного органического основания, причем вышеупомянутый способ содержит после возможной стадии очистки и/или выделения стадию обработки гидроксидом или основной солью лития. 17. Реагент для осуществления способа по пп.1-16, характеризующийся тем, что он содержит вводимые одновременно или последовательно тяжелый сульфонилгалогенид (с атомным номером галогена, по меньшей мере равным атомному номеру хлора), преимущественно сульфонилхлорид, и неалкоилированное и одновременно жирорастворимое органическое основание, выбираемое из пространственно за 15 трудненных диалкоилфосфинов, триалкоилфосфинов, гидроксидов фосфония, пространственно затрудненных диалкоиламинов, триалкоиламинов, гидроксидов аммония, и слабополярный растворитель, причем органическая часть упомянутого сульфонилгалогенида является перфторированной по атому углерода, связанному с атомом серы. 18. Реагент по п.17, отличающийся тем,что слабополярный растворитель, включая смесь растворителей, выбирают среди растворителей, имеющих низкую растворимость в воде и не содержащих хлорированной алифатической цепочки. 19. Реагент по пп.17 и 18, отличающийся тем, что слабополярный растворитель выбирают(Еft, выраженная в ккал/моль) самое большее равна 40 (преимущественно две значащие цифры). 20. Реагент по пп.17-19, отличающийся тем, что слабополярный растворитель выбирают среди кислородсодержащих органических соединений (в частности, простых эфиров, сложных эфиров и даже кетонов), углеводородов(включая нефтяные фракции), ароматических углеводородов, галогенированных в ядре. 21. Реагент по пп.17-20, отличающийся тем, что слабополярный растворитель выбирают из замещенных бензолов и углеводородов, галогенированных в ядре.
МПК / Метки
МПК: C07C 303/38, C07B 45/00
Метки: также, способ, солей, перфторсульфонимидов, сульфонирования, синтеза, агент, перфторсульфонамидов
Код ссылки
<a href="https://eas.patents.su/9-4498-sposob-sinteza-perftorsulfonamidov-perftorsulfonimidov-i-ih-solejj-a-takzhe-agent-sulfonirovaniya.html" rel="bookmark" title="База патентов Евразийского Союза">Способ синтеза перфторсульфонамидов, перфторсульфонимидов и их солей, а также агент сульфонирования</a>
Предыдущий патент: Коровые антигенные частицы hbv с множественными иммуногенными компонентами, связанными посредством пептидных лигандов
Следующий патент: Замещенные гетероциклические соединения для лечения воспалительных процессов
Случайный патент: Функциональная разделительная промежуточная вставка для картриджей в многополюсном распределительном устройстве и прерывателе цепи