Способ получения 1-октена
Формула / Реферат
1. Двухстадийный способ получения 1-октена из бутадиена, включающий
первую стадию (а), в которой бис-гидродимеризацию бутадиена с образованием 1,7-октадиена выполняют в присутствии катализатора на основе комплекса палладия, содержащего один или более чем один трехзамещенный монодентатный фосфин, в апротонном полярном растворителе, возможно содержащем органическое основание; указанную первую стадию проводят в присутствии донора водорода;
вторую стадию (b), в которой выполняют частичное каталитическое гидрирование 1,7-октадиена, выделенного по окончании первой стадии; указанное гидрирование проводят в инертном растворителе, под давлением водорода или смеси водорода и азота, в присутствии катализатора,
при этом указанный способ отличается тем, что:
(i) на первой стадии апротонный полярный растворитель выбран из дизамещенных циклических мочевин, соответствующих общей формуле (I)
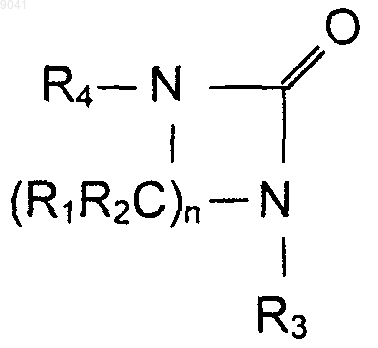
где n находится в диапазоне от 1 до 8;
R1 и R2 одинаковы или различны и выбраны из Н и C1-С6алкильного радикала;
R3 и R4 одинаковы или различны и выбраны из C1-C16алкильных радикалов;
(ii) на второй стадии катализатор выбран из комплексов рутения, не содержащих носителя и имеющих общую формулу (II)

где X выбран из группы, состоящей из Cl, Br, I, CH3COO, H, =C(H)Ph;
L выбран из монодентатных или бидентатных нейтральных лигандов;
m находится в диапазоне от 1 до 3;
n находится в диапазоне от 2 до 4.
2. Способ по п.1, в котором в соединении, имеющем общую формулу (I), n находится в диапазоне от 2 до 3; R1=R2=H, R3=R4=CH3.
3. Способ по п.1, в котором комплекс палладия, используемый на стадии (а), представляет собой заранее полученный комплекс, имеющий общую формулу
PdX2(PR3)2,
где X=Cl, Br, ацетат, а
R3 представляет собой С1-С16гидрокарбильный радикал.
4. Способ по п.1, в котором органическое основание, используемое на стадии (а), представляет собой триэтиламин.
5. Способ по п.1, в котором исходное массовое отношение бутадиена к растворителю находится в диапазоне от 1:10 до 10:1.
6. Способ по п.5, в котором исходное массовое отношение бутадиена к растворителю находится в диапазоне от 1:5 до 5:1.
7. Способ по п.1, в котором отношение донора водорода к бутадиену равно стехиометрическому молярному отношению 1:2.
8. Способ по п.1, в котором донор водорода представляет собой муравьиную кислоту.
9. Способ по п.1, в котором молярное отношение между органическим основанием и донором водорода находится в диапазоне от 0 до 1,5, более предпочтительно от 0,2 до 1,3, еще более предпочтительно от 0,4 до 0,8.
10. Способ по п.1, в котором стадию (а) проводят при температуре в диапазоне от 50 до 120шС, предпочтительно от 70 до 100шС.
11. Способ по п.1, в котором в комплексе рутения RuXmLn m находится в диапазоне от 2 до 3, n находится в диапазоне от 2 до 4; X выбран из Cl и =CHPh; L представляет собой фосфин.
12. Способ по п.11, в котором X=Cl, m=2, n=4, L=РРh3.
13. Способ по п.11, в котором m=3, n=2, L=РСу3.
14. Способ по п.1, в котором молярное отношение комплекса рутения, присутствующего на стадии (b) в реакционной среде, к 1,7-октадиену составляет от 1/100 до 1/500000, предпочтительно от 1/1000 до 1/150000, еще более предпочтительно от 1/5000 до 1/50000.
15. Способ по п.1, в котором содержание 1,7-октадиена в растворителе составляет от 5 до 90 мас.%, более предпочтительно от 10 до 80 мас.%.
16. Способ по п.1, в котором стадию (b) проводят при температуре в диапазоне от 0 до 150шС, предпочтительно от 5 до 60шС.
17. Способ по п.1, в котором стадию (b) проводят в присутствии смеси водорода с азотом, предпочтительно в присутствии только водорода, под давлением в диапазоне от 0,05 до 10 МПа, предпочтительно от 0,1 до 3 МПа.
Текст
009041 Настоящее изобретение относится к способу получения 1-октена из бутадиена в две стадии, более конкретно, первую стадию каталитической бис-гидродимеризации бутадиена с образованием 1,7 октадиена в присутствии донора водорода в апротонном полярном растворителе, выбранном из дизамещенных циклических мочевин, и вторую стадию частичного и селективного восстановления 1,7 октадиена водородом с образованием 1-октена в присутствии каталитической системы, включающей комплекс рутения, не содержащий носителя. 1-Октен широко используют в области техники, относящейся к производству линейного полиэтилена низкой плотности (ЛПЭНП), то есть сополимера, получаемого из этилена и 1-олефинов, поскольку он придает конечному продукту улучшенные механические характеристики и улучшенную свариваемость. 1-Октен также применяют в области техники, относящейся к изготовлению пластификаторов, после проведения операций гидроформилирования, восстановления до линейных спиртов и этерификации. В настоящей области техники известен способ синтеза 1-октена из бутадиена. В некоторых патентах описан синтез 1-октена из бутадиена посредством трехстадийного процесса. В US-A-5030792 на первой стадии проводят каталитическую теломеризацию бутадиена в присутствии уксусной кислоты, с получением 2,7-октадиенилацетата; полученное соединение на второй стадии гидрируют с образованием н-октилацетата, который, в свою очередь, на третьей стадии подвергают пиролизу с получением 1-октена. Такой способ неудобен тем, что включает большое количество стадий реакции, а также проблемами, связанными с коррозией обычных материалов под действием уксусной кислоты. В WO 92/10450 описана каталитическая теломеризация бутадиена со спиртом, таким как этанол или метанол, с образованием простого эфира 2,7-октадиенила. Полученное соединение на второй стадии подвергают гидрированию с образованием простого октилового эфира, который, в свою очередь, на третьей стадии подвергают пиролизу с получением 1-октена. Хотя в этом способе не используют коррозионные карбоновые кислоты, этот способ также неудобен тем, что включает большое количество стадий, а также имеет общую низкую селективность. Наконец, в WO 03/31378 описан синтез 1-октена из бутадиена, только в две стадии, в соответствии со схемой, включающей уравнения (1) и (2) На первой стадии описанного способа выполняют каталитическую бис-гидродимеризацию бутадиена с образованием 1,7-октадиена под действием восстанавливающего агента, такого как муравьиная кислота. На второй стадии проводят частичное каталитическое гидрирование 1,7-октадиена с получением 1-октена. Несмотря на то, что способ, описанный в WO 03/31378, имеет некоторые преимущества перед предыдущими способами, поскольку количество стадий, необходимых для получения 1-октена, уменьшено в указанном способе до двух, этот способ имеет большое количество недостатков, в частности, необходимость использования как на первой, так и на второй стадии больших количеств дорогостоящих благородных металлов, применяемых в качестве катализаторов. Первую стадию способа, описанного в WO 03/31378, проводят согласно реакции, известной в литературе, то есть бис-гидродимеризации бутадиена в присутствии муравьиной кислоты и катализаторов на основе палладия и фосфинов. Во всех случаях описанная реакция проходит практически не селективно, с образованием смесей 1,6-октадиена и 1,7-октадиена; кроме того, выходы и эффективность катализатора в указанной реакции низки. Кроме того, указанный способ требует применения больших количеств катализатора, что создает проблемы, связанные со стоимостью катализатора и его регенерацией. При снижении концентрации катализатора до более низких значений снижается селективность по отношению к 1,7-октадиену. Из вышеописанного можно заключить, что существует необходимость разработки более эффективного способа гидродимеризации бутадиена, который позволяет достичь большей степени превращения и селективности по 1,7-октадиену, а также позволит снизить концентрации используемых благородных металлов. Вторая стадия способа, описанного в WO 03/31378, состоит в частичном гидрировании 1,7 октадиена до 1-октена. При проведении этой реакцию так, как описано в WO 03/31378, то есть в гетерогенной фазе при использовании катализатора на основе рутения на носителе, активность катализатора оказывается чрезвычайно низкой. Действительно, для получения 70% степени конверсии 1,7-октадиена и 60% селективности по отношению к 1-октену требуется очень большое время реакции, порядка 24 ч, и кроме того, в реакции в любом случае образуются изомерные олефины. Кроме того, из-за низкой каталитической активности выбранного катализатора (т.е. рутения на носителе) его количество, используемое в этом случае, является значительно более высоким.-1 009041 Таким образом, необходим, в частности, для выполнения этой стадии более эффективный и более селективный способ проведения частичного восстановления 1,7-октадиена даже при работе с небольшими количествами катализатора. В настоящее время найден способ приготовления 1-октена из бутадиена, не имеющий указанных недостатков. В соответствии с этим настоящее изобретение относится к двухстадийному способу получения 1 октена из бутадиена, который включает первую стадию (а), на которой проводят бис-гидродимеризацию бутадиена с образованием 1,7 октадиена в присутствии катализатора на основе комплекса палладия, содержащего один или более чем один трехзамещенный монодентатный фосфин, в апротонном полярном растворителе, возможно содержащем органическое основание; причем вышеуказанную первую стадию проводят в присутствии донора водорода, предпочтительно муравьиной кислоты; вторую стадию (b), на которой проводят частичное каталитическое гидрирование 1,7-октадиена,выделенного в завершение первой стадии; причем указанное гидрирование проводят в инертном растворителе под давлением водорода или смеси водорода и азота в присутствии катализатора; при этом вышеуказанный способ отличается тем, что:(i) на первой стадии апротонный полярный растворитель выбирают из дизамещенных циклических мочевин, соответствующих общей формуле (I)R1 и R2 одинаковы или различны и выбраны из Н и C1-C6 алкильного радикала, предпочтительноR3 и R4 одинаковы или различны и выбраны из C1-C16, предпочтительно С 1-С 3 алкильных радикалов;(ii) на второй стадии катализатор выбирают из комплексов рутения, не содержащих носителя и соответствующих общей формуле (II) где X выбирают из Cl, Br, I, CH3COO, H, =C(H)Ph;L выбирают из монодентатных или бидентатных нейтральных лигандов;m находится в диапазоне от 1 до 3. Типичными примерами дизамещенных циклических мочевин, соответствующих общей формуле (I),являются диметилэтиленмочевина (n=2; R1=R2=H; R3=R4=CH3) и диметилпропиленмочевина (n=3;R1=R2=H; R3=R4=CH3). Использование на первой стадии особых растворителей, предлагаемых в настоящем изобретении,т.е. дизамещенных циклических мочевин, позволяет при прочих равных условиях увеличить степень превращения бутадиена и селективность по отношению к 1,7-октадиену. Это означает, что концентрация катализатора может быть снижена до чрезвычайно низких значений без ущерба для степени превращения бутадиена и селективности по отношению к 1,7-октадиену, которые остаются весьма высокими. Кроме того, на первой стадии (а), т.е. бис-гидродимеризации бутадиена с образованием 1,7 октадиена, катализатор на основе палладия может быть получен заранее или образован in situ. В последнем случае катализатор получают in situ из соли палладия и одного или более фосфинов. В предпочтительном варианте выполнения соль палладия выбирают из карбоксилатов палладия, еще более предпочтительно из Pd(Me3CCOO)2 и Pd(acetate)2. Что касается фосфинов, то типичными примерами фосфинов являются трифенилфосфин, три(о-толил)фосфин, (3-сульфонатфенил)дифенилфосфин, трициклогексилфосфин, триметилфосфин, триэтилфосфин, триизопропилфосфин, трибутилфосфин и смешанные фосфины метилдифенилфосфин, диметилфенилфосфин, по отдельности или в сочетании друг с другом. Предпочтительным является трифенилфосфин. В случае образования комплекса палладия in situ, молярное отношение между фосфинами и палладием находится в диапазоне от 1 до 100, предпочтительно от 2 до 40. В предпочтительном варианте выполнения палладиевый катализатор подвергают предварительному формированию, и он состоит из одного или более комплексов палладия, имеющих общую формулуPdX2(PR3)2, где X=Cl, Br, ацетат, a R3 представляет собой C1-C16 гидрокарбильный (углеводородный) радикал, предпочтительно выбранный из группы, содержащей фенил, о-толил, метил, трициклогексил,этил, изопропил, бутил и соответствующие смеси. Предпочтительными являются следующие комплексы:PdCl2(PEt3)2, PdCl2(PCy3)2, PdCl2(PBut3)2, PdCl2(PiPr3)2, где Et=этил, Су=циклогексил, iPr=изопропил,But=н-бутил. Что касается органического основания, которое факультативно может быть использовано на первой-2 009041 стадии, типичные примеры включают пиридины, N-алкилморфолины, триалкиламины. В предпочтительном варианте выполнения органическое основание представляет собой триэтиламин. Первую стадию проводят в присутствии донора водорода, предпочтительно в стехиометрическом молярном отношении 1:2 по отношению к бутадиену; см. уравнение (1), или это отношение может быть немного меньше. Предпочтительно донор водорода представляет собой муравьиную кислоту. Первоначальное массовое отношение бутадиена к растворителю находится в диапазоне от 1:10 до 10:1, более предпочтительно от 1:5 до 5:1. В предпочтительном варианте выполнения используют донор водорода, предпочтительно муравьиную кислоту, в стехиометрическом отношении (т.е. 1/2 мол.) к бутадиену или в несколько меньшем количестве, чем стехиометрическое. Молярное отношение между органическим основанием, например триэтиламином, и донором водорода, например муравьиной кислотой, может находиться в диапазоне от 0 до 1,5, более предпочтительно от 0,2 до 1,3, еще более предпочтительно от 0,4 до 0,8. Стадию (а) проводят при температуре в диапазоне от 50 до 120 С, предпочтительно от 70 до 100 С,предпочтительно под давлением азота в диапазоне 0,5-2 МПа, более предпочтительно от 0,8 до 1,5 МПа. Продолжительность реакции на стадии (а) примерно составляет от 10 до 180 мин, более предпочтительно от 15 до 120 мин. В соответствии с вышеуказанным способом на первой стадии можно улучшить селективность по 1,7-октадиену даже при использовании чрезвычайно малых количеств катализатора, например, таких,что начальное молярное соотношение бутадиен/палладий находится в диапазоне от 5000 до 1000000,предпочтительно от 20000 до 200000; при этом степень превращения бутадиена не снижается в значительной степени, оставаясь высокой. По окончании первой стадии реакционный продукт, 1,7-октадиен, может быть выделен традиционными способами. Более конкретно, в предпочтительном варианте выполнения настоящего изобретения реакционный продукт отделяют расслоением смеси, используя тот факт, что 1,7-октадиен не смешивается во всех соотношениях с дизамещенными циклическими мочевинами. Верхняя углеводородная фаза, преимущественно состоящая из 1,7-октадиена, может быть отмыта от неуглеводородных остатков водой; затем 1,7-октадиен очищают традиционными способами, например перегонкой. Вторую стадию способа, то есть частичное каталитическое гидрирование 1,7-октадиена с образованием 1-октена, проводят в присутствии катализатора, состоящего из комплекса рутения. Катализатор предпочтительно выбран из комплексов рутения, имеющих формулу RuXmLn, в которой m находится в диапазоне от 1 до 3, n находится в диапазоне от 2 до 4; X=Cl, Br, I, СН 3 СОО, Н, =C(H)Ph; L=монодентатный нейтральный лиганд, такой как РРh3 (трифенилфосфин), РСу 3 (трициклогексилфосфин), Р(оСН 3 С 6 Н 4)3 (триортотолилфосфин), СО (моноксид углерода); или L=бидентатный нейтральный лиганд,такой как дифенилфосфинэтан (ddpe), дипиридил (bipy), 1,10-фенантролин (Phen), 4,7-дифенил-1,10 фенантролин (bato), применяемые по отдельности или в сочетании друг с другом. Более конкретно, предпочтительными являются следующие комплексы рутения: RuCl2(PPh3)3,RuCl2(PPh3)4, RuCl2(CO)(PPh3)3, RuHCl(PPh3)3, RuHCl(CO)(PPh3)3, RuCl2(dppe)2, RuCl2(PCy3)3,RuCl2(CO2)(PPh3)2, (PCy3)2Cl2Ru=C(H)Ph, [Ru(CO)2Cl2]x. Наиболее предпочтительными используемыми катализаторами являются RuCl2(PPh3)x, где х=3 или 4. Молярное отношение комплекса рутения, добавляемого в реакционную среду, к 1,7-октадиену находится в диапазоне от 1/100 до 1/500000, предпочтительно от 1/1000 до 1/150000, еще более предпочтительно от 1/5000 до 1/50000. Стадия (b) может быть проведена как в растворителе, так и в чистом диене, предпочтительно в присутствии растворителя. Подходящие растворители представляют собой спирты общей формулы R-OH,где R представляет собой алкильный радикал, содержащий от 1 до 6 атомов углерода; простые эфиры RO-R', где R и R' имеют то же значение, что и вышеуказанный R; циклические простые эфиры, содержащие до 6 атомов углерода, линейные или разветвленные алифатические углеводороды, содержащие от 5 до 16 атомов углерода; частично или полностью галогенированные углеводороды, содержащие от 1 до 3 атомов углерода, ароматические или алкилароматические углеводороды, содержащие до 9 атомов углерода; кетоны, содержащие до 6 атомов углерода. Предпочтительно растворители выбирают из группы,состоящей из метанола, этанола, пропанола и их смесей. В качестве растворителей также могут быть использованы смеси растворителей, не смешиваемых полностью друг с другом, таких как метанол и C3-C16 алифатические углеводороды. Применение таких смесей растворителей облегчает отделение катализатора от реакционной смеси, благодаря большему сродству катализатора к спиртовой фазе. В еще более предпочтительном варианте выполнения вторую стадию проводят в метанольном растворе, и 1-октен (вместе с возможным количеством непрореагировавшего 1,7-октадиена и возможно октаном как побочным продуктом) может быть извлечен из реакционной смеси при помощи традиционной жидкость-жидкостной экстракции алифатическими углеводородами, содержащими от 8 до 16 атомов углерода, предпочтительно додеканом, при этом в метанольном растворе остается катализатор, который направляют рециклом в реакцию. Затем 1-октен извлекают из-3 009041 смеси углеводородов и очищают традиционными способами. Если используют растворитель, то содержание диена в растворителе находится в диапазоне от 5 до 90 мас.%, более предпочтительно от 10 до 80 мас.%. Реакцию стадии (b) обычно проводят при температуре в диапазоне от 0 до 150 С, предпочтительно от 5 до 60 С. Этот диапазон представляет собой температурный промежуток, в котором каталитическая система обладает наименьшей изомеризационной активностью по отношению к двойной связи, совместимой с хорошей скоростью гидрирования. В общем случае реакцию проводят под давлением водорода или смеси водорода с азотом, предпочтительно в присутствии только водорода, при давлении в диапазоне от 0,05 до 10 МПа, предпочтительно от 0,1 до 3 МПа. Приблизительная продолжительность реакции составляет от 2 до 200 мин, более предпочтительно от 5 до 60 мин. Для снижения протекания последующей реакции гидрирования 1-октена до октана реакцию предпочтительно проводят до степени превращения 1,7-октадиена, не превышающей 80%, предпочтительно составляющей от 40 до 60%. Если значение степени превращения находится в этом диапазоне, полученная селективность по отношению к 1-октену обычно находится в диапазоне от 75 до 90%. Кроме того, при работе в условиях,предлагаемых в изобретении, обычно не образуется других изомеров 1-октена и 1,7-октадиена. Для лучшего понимания настоящего изобретения ниже представлены следующие примеры. Примеры Синтез 1,7-октадиена Примеры с 1 по 14 (катализатор образован in situ). В автоклав из Hastelloy С емкостью 300 мл, снабженный механической перемешивающей системой и нагревательной системой, в указанном ниже порядке подают ингредиенты, тип и количество которых обозначены в табл. 1 или ниже в тексте: растворитель, органическое основание (если присутствует), 7 мл муравьиной кислоты (концентрацией 99 мас.%) в стехиометрическом отношении к бутадиену, трифенилфосфин, применяемый в качестве лиганда, и Pd(CH3COO)2, применяемый в качестве катализатора. Затем автоклав закрывали и добавляли 20 г бутадиена. В автоклаве создавали давление азота до величины 1,0 МПа и производили нагревание до температуры 90 С, выдерживая указанную температуру в течение времени, указанного в табл. 1. По окончании автоклав охлаждали, содержимое автоклава обрабатывали водой и бикарбонатом натрия, а затем экстрагировали циклогексаном. Количество полученных продуктов определяли при помощи газовой хроматографии с использованием метода внутреннего стандарта. Степень превращения (конверсия) бутадиена и селективности по отношению к прореагировавшему бутадиену указаны в табл. 1. Таблица 1NMП=N-метилпирролидон; ТГФ=тетрагидрофуран; ТММ=тетраметилмочевина; ДМЭМ=диметилэтиленмочевина; ДМПМ=диметилпропиленмочевина. Из табл. 1 ясно видно, что при прочих равных условиях, применение в качестве растворителей циклических мочевин повышает степень превращения бутадиена, в то время как селективность по 1,7 октадиену остается прежней или возрастает.-4 009041 Примеры с 15 по 20 (заранее приготовленный катализатор). В автоклав Hastelloy С емкостью 300 мл, снабженный механической перемешивающей системой и нагревательной системой, в указанном ниже порядке были помещены ингредиенты, тип и количество которых обозначены в табл. 2 или ниже в тексте: 45 мл растворителя, 15 мл триэтиламина, 7 мл муравьиной кислоты (концентрацией 99 мас.%) в стехиометрическом отношении к бутадиену, и катализатор в молярном отношении к бутадиену, как указано в табл. 2. Затем автоклав закрывали и добавляли 20 г бутадиена. В автоклаве создавали давление азота до 1 МПа, и производили нагревание до температуры 90 С, выдерживая указанную температуру в течение 120 мин. По окончании автоклав охлаждали, содержимое автоклава обрабатывали водой и бикарбонатом натрия, а затем экстрагировали циклогексаном. Количество полученных продуктов определяли при помощи газовой хроматографии с использованием метода внутреннего стандарта. Степень превращения (конверсия) бутадиена и селективности по отношению к прореагировавшему бутадиену указаны в табл. 2. Таблица 2PBu=три-н-бутилфосфин; PEt=триэтилфосфин; РСу=трициклогексилфосфин. Из табл. 2 ясно видно, что при прочих равных условиях, применение в качестве растворителей циклических мочевин и использование заранее приготовленного палладиевого катализатора повышает как степень превращения бутадиена, так и, в меньшей степени, селективность по 1,7-октадиену. Гидрирование 1,7-октадиена до 1-октена Примеры с 21 по 25. В стеклянную колбу емкостью 250 мл, находящуюся в атмосфере аргона, поместили в указанном порядке 100 мл метанола, такое количество 1,7-октадиена (1,7-ОД), чтобы отношение 1,7 ОД/катализатор имело значение, указанное в табл. 3, и 0,01 ммоля катализатора. Раствор хорошо перемешивали до полного растворения катализатора, а затем при помощи стальной иглы, используя разность давлений, переносили в автоклав из Hastelloy С емкостью 300 мл, снабженный механической перемешивающей системой и нагревательной системой, с заранее созданным вакуумом. Давление аргона в автоклаве повышали до значения, немного превышающего атмосферное давление. Автоклав нагревают (или охлаждают) до желаемой температуры и затем вводят водород, повышая давление в автоклаве до 2 МПа и соединяя автоклав с системой восполнения израсходованного водорода. Таким образом инициировали реакцию. Через определенные промежутки времени из автоклава отбирали образцы проб, которые анализировали при помощи газовой хроматографии с использованием метода внутреннего стандарта, определяя количество оставшегося 1,7-октадиена, количество образовавшихся 1-октена и октана, а также диеновых и моноеновых изомеров. Селективность определена по отношению к прореагировавшему 1,7 октадиену. Полученные результаты показаны в табл. 3.(а) проведено в растворе метанол/додекан (1/1 объемн.) Из табл. 3 видно, что при работе в условиях в соответствии с настоящим изобретением, в растворе метанола, реакция гидрирования 1,7-октадиена с образованием 1-октена проходит в течение нескольких минут в зависимости от концентрации катализатора, при отсутствии изомеризации 1,7-октадиена и 1 октена. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Двухстадийный способ получения 1-октена из бутадиена, включающий первую стадию (а), в которой бис-гидродимеризацию бутадиена с образованием 1,7-октадиена выполняют в присутствии катализатора на основе комплекса палладия, содержащего один или более чем один трехзамещенный монодентатный фосфин, в апротонном полярном растворителе, возможно содержащем органическое основание; указанную первую стадию проводят в присутствии донора водорода; вторую стадию (b), в которой выполняют частичное каталитическое гидрирование 1,7-октадиена,выделенного по окончании первой стадии; указанное гидрирование проводят в инертном растворителе,под давлением водорода или смеси водорода и азота, в присутствии катализатора,при этом указанный способ отличается тем, что:(i) на первой стадии апротонный полярный растворитель выбран из дизамещенных циклических мочевин, соответствующих общей формуле (I)R1 и R2 одинаковы или различны и выбраны из Н и C1-С 6 алкильного радикала;R3 и R4 одинаковы или различны и выбраны из C1-C16 алкильных радикалов;(ii) на второй стадии катализатор выбран из комплексов рутения, не содержащих носителя и имеющих общую формулу (II) где X выбран из группы, состоящей из Cl, Br, I, CH3COO, H, =C(H)Ph;L выбран из монодентатных или бидентатных нейтральных лигандов;-6 009041 2. Способ по п.1, в котором в соединении, имеющем общую формулу (I), n находится в диапазоне от 2 до 3; R1=R2=H, R3=R4=CH3. 3. Способ по п.1, в котором комплекс палладия, используемый на стадии (а), представляет собой заранее полученный комплекс, имеющий общую формулуR3 представляет собой С 1-С 16 гидрокарбильный радикал. 4. Способ по п.1, в котором органическое основание, используемое на стадии (а), представляет собой триэтиламин. 5. Способ по п.1, в котором исходное массовое отношение бутадиена к растворителю находится в диапазоне от 1:10 до 10:1. 6. Способ по п.5, в котором исходное массовое отношение бутадиена к растворителю находится в диапазоне от 1:5 до 5:1. 7. Способ по п.1, в котором отношение донора водорода к бутадиену равно стехиометрическому молярному отношению 1:2. 8. Способ по п.1, в котором донор водорода представляет собой муравьиную кислоту. 9. Способ по п.1, в котором молярное отношение между органическим основанием и донором водорода находится в диапазоне от 0 до 1,5, более предпочтительно от 0,2 до 1,3, еще более предпочтительно от 0,4 до 0,8. 10. Способ по п.1, в котором стадию (а) проводят при температуре в диапазоне от 50 до 120 С,предпочтительно от 70 до 100 С. 11. Способ по п.1, в котором в комплексе рутения RuXmLn m находится в диапазоне от 2 до 3, n находится в диапазоне от 2 до 4; X выбран из Cl и =CHPh; L представляет собой фосфин. 12. Способ по п.11, в котором X=Cl, m=2, n=4, L=РРh3. 13. Способ по п.11, в котором m=3, n=2, L=РСу 3. 14. Способ по п.1, в котором молярное отношение комплекса рутения, присутствующего на стадии(b) в реакционной среде, к 1,7-октадиену составляет от 1/100 до 1/500000, предпочтительно от 1/1000 до 1/150000, еще более предпочтительно от 1/5000 до 1/50000. 15. Способ по п.1, в котором содержание 1,7-октадиена в растворителе составляет от 5 до 90 мас.%,более предпочтительно от 10 до 80 мас.%. 16. Способ по п.1, в котором стадию (b) проводят при температуре в диапазоне от 0 до 150 С, предпочтительно от 5 до 60 С. 17. Способ по п.1, в котором стадию (b) проводят в присутствии смеси водорода с азотом, предпочтительно в присутствии только водорода, под давлением в диапазоне от 0,05 до 10 МПа, предпочтительно от 0,1 до 3 МПа.
МПК / Метки
Метки: 1-октена, способ, получения
Код ссылки
<a href="https://eas.patents.su/8-9041-sposob-polucheniya-1-oktena.html" rel="bookmark" title="База патентов Евразийского Союза">Способ получения 1-октена</a>
Предыдущий патент: Новые амидные соединения, обладающие антагонистическим в отношении мсн действием, и содержащие эти соединения лекарственные средства
Следующий патент: Соль фосфорной кислоты ингибитора дипептидилпептидазы-iv
Случайный патент: Усовершенствования в безопасных крышках или относящиеся к безопасным крышкам для электрических штепсельных розеток и аналогичных устройств