Карбапенемовый антибиотик, композиция и способ получения
Номер патента: 534
Опубликовано: 28.10.1999
Авторы: Димишель Лиза М., Кауфман Майкл Дж., Уильямс Джон М., Ханке Уильям Э., Сидлер Дэниел Р., Бергквист Пол Э., Циммерман Джеффри Э., Дюбост Дэвид К.
Формула / Реферат
1. Фармацевтическая композиция, которая содержит соединение, представленное формулой I:
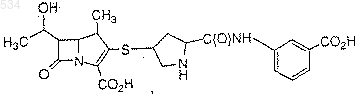
или его фармацевтически приемлемую соль, стабилизированную форму, пролекарство или гидрат в комбинации с источником диоксида углерода.
2. Фармацевтическая композиция по п.1, содержащая в качестве источника диоксида углерода карбонат натрия или бикарбонат натрия.
3. Фармацевтическая композиция по п.2, содержащая около 3-6 мас.ч. соединения I или его фармацевтически приемлемой соли, стабилизированной формы, пролекарства или гидрата и около 1 мас.ч. бикарбоната натрия.
4. Фармацевтическая композиция по п.3, содержащая около 4,5 частей соединения I или его фармацевтически приемлемой соли, стабилизированной формы, пролекарства или гидрата.
5. Фармацевтическая композиция по п.2, содержащая около 3-6 мас.ч. соединения I или его фармацевтически приемлемой соли, стабилизированной формы, пролекарства или гидрата и около 1 мас.ч. карбоната натрия.
6. Фармацевтическая композиция по п.5, содержащая около 4,5 частей соединения I или его фармацевтически приемлемой соли, стабилизированной формы, пролекарства или гидрата.
7. Фармацевтическая композиция по п.2, содержащая около 4-10 мас.ч. соединения I или его фармацевтически приемлемой соли, стабилизированной формы, пролекарства или гидрата и 1 мас.ч. карбоната натрия.
8. Фармацевтическая композиция по п.7, где около 6,7 мас.ч. соединения I или его фармацевтически приемлемой соли, стабилизированной формы, пролекарства или гидрата комбинируют с 1 мас.ч. карбоната натрия.
9. Фармацевтическая композиция по п 1, содержащая около 4-10 мас.ч. соединения формулы I или его фармацевтически приемлемой соли, стабилизированной формы, пролекарства или гидрата и 1 мас.ч. бикарбоната натрия.
10. Фармацевтическая композиция по п.8, где около 6,7 мас.ч. соединения формулы I или его фармацевтически приемлемой соли, стабилизированной формы, пролекарства или гидрата комбинируют с 1 мас.ч. бикарбоната натрия.
11. Фармацевтическая композиция по п.2, дополнительно содержащая ингибитор дегидропептидазы.
12. Фармацевтическая композиция по п.11, где ингибитором дегидропептидазы является циластатин.
13. Соединение, представленное формулой II
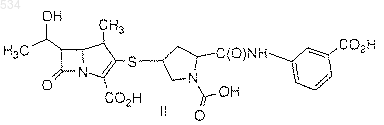
или его фармацевтически приемлемая соль, пролекарство или гидрат.
14. Фармацевтическая композиция, которая содержит соединение, представленное формулой II
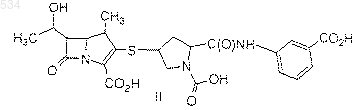
или его фармацевтически приемлемую соль, пролекарство или гидрат в комбинации с фармацевтически приемлемым носителем.
15. Соединение по п.13, где фармацевтически приемлемую соль выбирают из группы, включающей
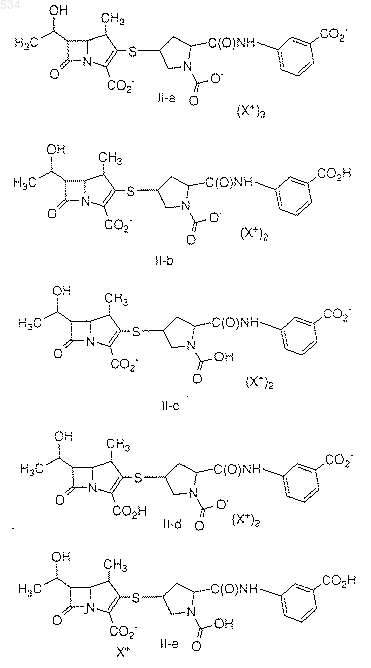

где X+ представляет фармацевтически приемлемую катионную группу.
16. Фармацевтическая композиция, которую получают комбинированием соединения формулы I:
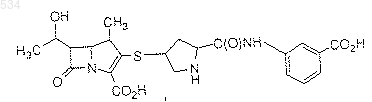
или его фармацевтически приемлемой соли, пролекарства или гидрата с источником диоксида углерода.
17. Фармацевтическая композиция по п.16, где источник диоксида углерода выбирают из диоксида углерода, карбоната натрия и бикарбоната натрия.
18. Фармацевтическая композиция по п.17, где источником диоксида углерода является карбонат натрия или бикарбонат натрия.
19. Способ стабилизации карбапенема формулы I
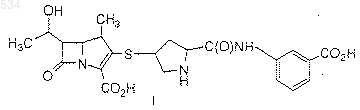
или его фармацевтически приемлемой соли, пролекарства или гидрата, заключающийся в добавлении к данному соединению достаточного количества источника диоксида углерода для образования соединения формулы II
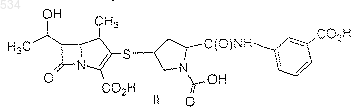
или его фармацевтически приемлемой соли, пролекарства или гидрата.
20. Способ по п.19, где источник диоксида углерода выбирают из диоксида углерода, карбоната натрия и бикарбоната натрия.
21. Способ по п.20, где источник диоксида углерода выбирают из карбоната натрия и бикарбоната натрия.
Текст
1 Настоящее изобретение относится к композиции карбапенемового антибиотика, стабилизированной форме антибиотика и способам его получения. Композицию можно использовать при лечении инфекционных болезней,включая вызванные грамположительными и-отрицательными, аэробными и анаэробными бактериями. Композиция обеспечивает хорошую стабильность против бета-лактамаз и подходящую продолжительность действия. Сущность изобретения Описана фармацевтическая композиция,которая содержит соединение формулы I: или его фармацевтически приемлемую соль,стабилизированную форму, пролекарство или гидрат в комбинации с источником диоксида углерода. Подробное описание изобретения Используемый здесь термин стабилизированная форма относится к соединениям, которые имеют карбаматную группу, образованную у атома азота пирролидина, как показано на соединениях формулы II. Этот карбамат получают смешиванием соединения формулы I или его соли, пролекарства или гидрата с источником диоксида углерода, таким как карбонат натрия или бикарбонат натрия. Примеры показаны на соединениях формулы II и формул от II-а доII-g. Термин пролекарство относится к соединениям с удаляемой группой, присоединенной к гидроксилу гидроксиэтильной боковой цепи (положение 6 кольца карбапенема), карбоновой кислотой в положении 3 кольца карбапенема или группой мета-карбоновой кислоты на кольце фенила боковой цепи. Группы, которые пригодны для образования пролекарств, должны быть очевидны специалисту медицинской химии из приведенных здесь данных. Примеры включают аллил, ацетил, бензилоксикарбонил,метоксиметил, трет-бутоксикарбонил, триметилсилил и тому подобное. Термин гидрат используют в общепринятом смысле для включения соединений формул I и II в физической ассоциации с водой. Настоящее изобретение относится к фармацевтическим композициям, которые содержат карбапенемовое антибиотическое соединение: а также его соли, стабилизированные формы,пролекарства и гидраты. Соединение формулы I является карбапенемовым антибиотиком, который особенно пригоден для внутривенного или внутримышечного введения. 2 В одном аспекте изобретения фармацевтическую композицию изготовляют с любым фармацевтически приемлемым буфером, который при растворении обеспечит рН от около 6,0 до около 9,0. Например, предпочтительным фармацевтически приемлемым буфером является бикарбонат натрия. Предпочтительное значение рН композиции при растворении от около 6,2 до около 8,5. В другом аспекте изобретения включается стабилизированная форма соединения, показанная ниже как формула II. Обычно для образования соединения формулы II с соединением формулы I можно использовать любое соединение,которое при растворении дает диоксид углерода. Композиции настоящего изобретения обычно изготовляют с использованием источника диоксида углерода. Предпочтительными источниками диоксида углерода являются диоксид углерода (газообразный, жидкий или твердый), карбонаты и бикарбонаты, более предпочтительны карбонат натрия и бикарбонат натрия,которые можно вводить в состав готовой препаративной формы, так чтобы при растворении получали подходящее значение рН, например около 6,2-8,5. Природное значение рН мононатриевой соли соединения I приблизительно 5,4. Соединения формулы I можно синтезировать в соответствии с патентом США 5 478 820, выданным Betts et al. 26 декабря, 1995, содержание которого вводится здесь в качестве ссылки. Соединение формулы I в лиофилизированной или нелиофилизированной форме, смешанное с соединением, которое образует диоксид углерода, таким как карбонат натрия или бикарбонат натрия, превращается в соединение формулы II. Обычно соединения формулы II можно синтезировать смешиванием соединения формулы I с источником диоксида углерода и затем растворением смеси в подходящем растворителе. Соединение формулы I можно смешать с источником диоксида углерода и смесь растворить, что обычно приводит к образованию соединения формулы II. Во многих случаях предпочтительно растворение соединения формулы I с соединением,образующим диоксид углерода, в водном растворителе с последующей лиофилизацией образуемой композиции, что обеспечивает образование смеси, содержащей соединения формулы II. При растворении соединение формулы II(II и от IIа до IIg) после определенного времени превращается в соединение формулы I (I, I-a, I-b и I-с). 3 Порошок соединения формулы I может быть смешан с соединением, образующим диоксид углерода так, чтобы при растворении или восстановлении образовалось соединение формулы II или его соль, пролекарство или гидрат. В соответствии с другим вариантом, соединение формулы I и соединение, образующее диоксид углерода, можно смешать в растворе для образования соединения II, после чего композицию лиофилизуют, чтобы обеспечить образование композиции, содержащей соединение формулы II или его соль, пролекарство или гидрат. Количество карбоната натрия или бикарбоната натрия, используемое в композиции, может изменяться в широких пределах. Например,количество карбоната натрия в готовой препаративной форме может изменяться от такого низкого значения, как около 0,025 г карбоната натрия/грамм лекарственного средства, до такого высокого значения, как около 0,25 г карбоната натрия/грамм лекарственного средства. Таким же образом, количество бикарбоната натрия в готовой препаративной форме может изменяться от такого низкого значения, как около 0,025 г/грамм лекарственного средства, до такого высокого значения, как около 0,7 г/грамм лекарственного средства. Для регулирования рН композиции при растворении или пересоздании можно включить другие соединения. Примеры их включают гидроксид калия, гидроксид натрия, N-метилглюкамин и тому подобное. Одна готовая препаративная форма, которая представляет особенный интерес, содержит около 3-6 мас.ч., предпочтительно около 4,5 мас.ч., соединения I или его фармацевтически приемлемой соли, стабилизированной формы,пролекарства или гидрата и 1 мас.ч. бикарбоната натрия. Предпочтителен карбапенем в форме мононатриевой соли. Значение рН, которое получают при растворении этой готовой препаративной формы, приблизительно 6,5. Изготовление данного лекарственного средства по этому способу может повысить стабильность продукта в растворе. Другая готовая препаративная форма, которая представляет особенный интерес, содержит около 4-10 мас.ч., предпочтительно около 6,7 мас.ч., соединения I или его фармацевтически приемлемой соли, стабилизированной формы, пролекарства или гидрата и 1 мас.ч. карбоната натрия. Предпочтителен карбапенем в форме мононатриевой соли. Значение рН, которое получают при растворении этой готовой препаративной формы, приблизительно 7,5. Изготовление данного лекарственного средства по этому способу может повысить стабильность продукта в растворе. Как упоминалось выше, соединение формулы I или II можно использовать в лиофилизированной или нелиофилизированной форме. 4 Лиофилизированную форму получают с использованием стандартных способов лиофилизации. В композицию по настоящему изобретению, кроме того, можно включить дополнительные компоненты. Поскольку композицию предпочтительно вводят инъекцией, в нее можно включить различные разбавители, буферы,консерванты, местно-анестезирующие средства,средства, регулирующие тоничность, и другие компоненты. Репрезентативные примеры разбавителей включают стерильную воду для инъекции, изотонический раствор, 5% раствор декстрозы(D5W), лактатированный раствор Рингера и тому подобное. Предпочтительным разбавителем является изотонический раствор или стерильная вода для инъекции. Репрезентативные примеры буферов включают фосфатный буфер, такой как однозамещенный фосфат натрия, цитратный буфер,такой как цитрат натрия, меглумин и три(гидроксиметил)аминометан. Репрезентативные примеры консервантов включают бутилгидроксиацетон (ВНА), бутилгидрокситолуол (ВНТ) и хлорид бензалкония. Репрезентативные примеры местноанестезирующих средств включают бензокаин,лидокаин, новокаин, понтокаин и тому подобное. Репрезентативные примеры агентов, модифицирующих тоничность, включают хлорид натрия, маннит, декстрозу, глюкозу, лактозу и сахарозу. Репрезентативные примеры фармацевтических наполнителей включают воду, маннит,сорбит, декстрозу, лактозу, глюкозу, декстран,сахарозу, мальтозу, желатин, альбумин бычьей сыворотки (BSA), глицин, маннозу, рибозу, поливинилпирролидон (PVP), производные целлюлозы, глутамин, инозит, глутамат калия,эритрит, серин и другие аминокислоты. Когда соединение формулы I приготовляют в виде фармацевтической композиции с подходящим количеством карбоната натрия или бикарбоната натрия, любой или все из разновидностей компонентов, описанных здесь, могут содержаться в готовой препаративной форме при разбавлении или восстановлении. Соединение I представляет нестабилизированную форму свободной кислоты. Поэтому здесь включены различные солевые формы соединения формулыI, такие как соли от формулы I-а до I-с. 6 ванного соединения. Соединения от II-а до II-g являются примерами солевых форм стабилизированного соединения. Значение X+ представляет уравновешивающий заряд катион, который присутствует в ассоциации с соединением, когда необходимо поддерживать нейтральность общего заряда. Типично заряженной разновидностью может быть образующий фармацевтически приемлемую соль ион, такой как ион натрия, калия, магния и тому подобное. В случаях, когда в соединении присутствуют два карбоксилатных аниона, как в формуле I-а, или когда присутствует полумолярное количество относительно соединения, такое как в формуле I-b или I-с, может также присутствовать двухвалентная разновидность, такая как Са 2+. Когда противоион включает бискатионную разновидность, например Са 2+, он обычно присутствует в подходящем количестве относительно остатка карбапенема,чтобы обеспечить нейтральность общего заряда. Таким образом, для поддержания общей нейтральности заряда с монокарбоксилатом может быть включено полумолярное количество Са 2+. Все такие примеры осуществления включены в настоящее изобретение. Многочисленные солеобразующие ионы перечисляются в статье Berge, S.M., et al. J.Pharm. Sci. 66(1): 1-16 (1977), содержание которой вводится здесь в качестве ссылки. Предпочтительной группой солеобразующих катионов, представленных X+, является ион, выбранный из группы, включающей натрий, калий, кальций и магний. Более предпочтительный Х+ представляет ион, выбранный из группы, состоящей из Na+,Ca+2 и К+. Путем включения подходящего количества соединения, образующего диоксид углерода,предпочтительно бикарбоната натрия или карбоната натрия, образуют одну или несколько следующих стабилизированных структур. Соединение II, приведенное выше, называют формой свободной кислоты стабилизиро Количество соединения, образующего диоксид углерода, например бикарбоната натрия или карбоната натрия, которое включают в композицию, такое, которое достаточно для образования соединений от формулы II до формулы IIg и которое необязательно обеспечивает желаемое рН композиции при растворении или пересоздании. Для обеспечения электронного баланса и нейтральности общего заряда присутствует от нуля до трех положительно заряженных противоионов. В композицию можно включить разные противоионы. Следовательно, в фармацевтическую композицию для обеспечения общей нейтральности заряда могут быть включе 7 ны вместе, например, кальций и натрий. Противоионы можно, таким образом, варьировать в широких пределах. Обычно противоион или противоионы являются фармацевтически приемлемыми катионными разновидностями. Карбапенемовое соединение по настоящему изобретению пригодно для лечения бактериальных инфекций у животных и людей. Термин фармацевтически приемлемая соль относится к тем солевым формам, которые будут очевидны специалисту фармацевтической химии, т.е. тем формам, которые фактически нетоксичны и которые обеспечивают желаемые фармакокинетические свойства, приятный вкус, абсорбцию,распределение, метаболизм или экскрецию. Другими факторами, более практическими по природе, которые также важны при выборе, являются цена исходных материалов, легкость кристаллизации, выход, стабильность, гигроскопичность и сыпучесть получаемой массы лекарственного средства. Фармацевтические композиции можно удобно получить из активных ингредиентов в комбинации с фармацевтически приемлемыми носителями. Таким образом, настоящее изобретение относится к фармацевтическим композициям и способам лечения бактериальных инфекций, использующим карбапенемовое соединение. Карбапенем можно использовать в различных фармацевтических препаратах. Композиции для инъекции, предпочтительного пути доставки, можно получить в унифицированной лекарственной форме или в контейнере со многими дозами. Композиции могут иметь такие формы,как суспензии, растворы или эмульсии, масляные или водные по природе, и могут содержать различные образующие формы агенты, такие как разбавители, буферы, консерванты и тому подобное. Следовательно, соединение присутствует в комбинации с этими фармацевтически приемлемыми носителями. Альтернативно активный ингредиент может быть в форме порошка, который можно пересоздать жидкостью, такой как стерильная вода, изотонический раствор и тому подобное, во время введения. Порошок может быть в лиофилизированной или нелиофилизированной форме. Репрезентативные пероральные композиции типично бывают в форме таблеток, капсул,растворов или суспензий. Такие композиции могут также быть упакованы в контейнеры с унифицированной дозой или множеством доз. В этих пероральных композициях фармацевтически приемлемые носители могут содержать разбавители, таблетирующие и гранулирующие добавки,смазочные средства,дезинтегрирующие агенты, буферы, подслащивающие вещества, консерванты и тому подобное. Композиции для местного применения могут быть изготовлены с фармацевтически приемлемыми носителями в форме гидрофобных 8 или гидрофильных мазей, кремов, лосьонов,растворов, красок или порошков. Доза, которая должна быть введена, зависит в значительной степени от состояния и размера млекопитающего-пациента, которого лечат, а также пути доставки и частоты введения. Парентеральный путь (инъекцией) предпочтителен. Композиции для доставки человеку, независимо от того, жидкие они или твердые, на унифицированную дозу могут содержать от около 0,01% до около 99% активного материала,причем предпочтительный диапазон составляет около 10-60%. Композиция обычно будет содержать от около 10 мг до около 3000 мг активного ингредиента, однако, вообще предпочтительно использование дозированного количества в диапазоне от около 100 мг до около 1000 мг. При парентеральном введении унифицированная доза обычно представляет собой соединение в стерильной воде или физиологическом растворе или соединение, находящееся в форме порошка, предназначенного для растворения или пересоздания. Предпочтительный способ введения соединения формулы I парентеральный путем внутривенной (в.в.) инфузии. Альтернативно,соединение можно ввести внутримышечной(в.м.) инъекцией. Для взрослого пациента дозу от около 5 до около 50 мг антибактериального соединения формулы I на кг массы тела вводят от 1 до 6 раз в день. Предпочтительная доза составляет от около 100 мг до около 1000 мг соединения, которую дают от одного до четырех раз в день,предпочтительно 1-2 раза в день, наиболее предпочтительно один раз ежедневно. Более конкретно, для слабых инфекций предпочтительна доза от около 100 мг до около 1000 мг для введения от одного до четырех раз ежедневно, наиболее предпочтительно один раз ежедневно. Для средних инфекций предпочтительна доза от около 500 мг до около 1000 мг для введения от одного до четырех раз ежедневно. Для сильных, опасных для жизни инфекций предпочтительна доза около 1000-2000 мг для введения от одного до шести раз ежедневно. Для детей предпочтительна доза 5-25 мг/кг массы тела, вводимая от 1 до 4 раз в день; наиболее предпочтительна доза 10 мг/кг, вводимая от одного до четырех раз ежедневно. Соединение формулы I относится к широкому классу соединений, известных как карбапенемы. Встречающиеся в природе карбапенемы восприимчивы к воздействию почечного фермента, известного как дегидропептидаза(DHP). Это воздействие или деградация может снизить эффективность карбапенемового антибактериального агента. Соединение, используемое в настоящем изобретении, значительно менее подвержено такому воздействию и, следовательно, использования ингибитора DHP может не требоваться. Однако использование ингибитора DHP необязательное, и рассматривается как включенное в настоящее изобретение. Ингибиторы DHP и их использование с карбапенемовыми антибактериальными агентами описывается в заявках на Европейские патенты 79102616.4, поданной 24 июля 1979 (патент 0 007 614) и 82107174.3, поданной 9 августа 1982 (публикация 0 072 014). Соединение по настоящему изобретению,когда ингибирование DHP желательно или необходимо, можно комбинировать или использовать с подходящим ингибитором DHP, как описано в указанных выше патентах и опубликованной заявке. Цитированная заявка на Европейский патент устанавливает способ определения восприимчивости настоящих карбапенемов к DHP и описывает подходящие ингибиторы,комбинированные композиции и способы лечения. Предпочтительное массовое отношение соединение формулы I: ингибитор DHP в комбинированных композициях составляет около 1:1. Предпочтительным ингибитором DHP является 7-(L-2-амино-2-карбоксиэтилтио)-2-(2,2 диметилциклопропанкарбоксамид)-2-гептеновая кислота или ее соль, известная как циластатин. Карбапенем активен против различных грамположительных и в меньшей степени грамотрицательных бактерий и поэтому находит применение в медицине и ветеринарии. Фармакокинетический профиль композиции, описанной здесь, неожиданно лучше, чем такие профили родственных соединений. 10 Репрезентативные примеры фармацевтических композиций, содержащих описанные здесь соединения, приводятся ниже. Композиция 1 Соединение I Бикарбонат натрия Порошок включает смесь указанных выше ингредиентов. Соединение I находится в форме мононатриевой соли. Получаемое значение рН водного раствора (225 мл) приблизительно 6,5. Композиция 2 Соединение I 6,7 г Карбонат натрия 1,0 г Порошок включает смесь указанных выше ингредиентов. Соединение I находится в форме мононатриевой соли. Получаемое значение рН водного раствора (335 мл) приблизительно 7,5. Пример Соединение I Бикарбонат натрия, USP Хлорид натрия, USP 45,4 мг/мл (эквивалентно 36 мг безводной свободной кислоты) Порошок включает смесь ингредиентов,указанных выше в композиции 1, и смешивается с водой (сколько надо до 1,0 мл). Конечные значения рН раствора приводятся ниже. Стабильность раствора этой готовой препаративной формы для внутривенного введения определяли при 25 С и получили следующие результаты. Несмотря на то, что некоторые предпочтительные примеры осуществления изобретения описаны здесь подробно, многочисленные альтернативные примеры осуществления рассматриваются как находящиеся в пределах объема прилагаемой формулы изобретения. Следовательно, изобретение этим не ограничивается. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Фармацевтическая композиция, которая содержит соединение, представленное формулой I: или его фармацевтически приемлемую соль,стабилизированную форму, пролекарство или гидрат в комбинации с источником диоксида углерода. 2. Фармацевтическая композиция по п.1,содержащая в качестве источника диоксида углерода карбонат натрия или бикарбонат натрия. 3. Фармацевтическая композиция по п.2,содержащая около 3-6 мас.ч. соединения I или его фармацевтически приемлемой соли, стабилизированной формы, пролекарства или гидрата и около 1 мас.ч. бикарбоната натрия. 4. Фармацевтическая композиция по п.3,содержащая около 4,5 частей соединения I или его фармацевтически приемлемой соли, стабилизированной формы, пролекарства или гидрата. 5. Фармацевтическая композиция по п.2,содержащая около 3-6 мас.ч. соединения I или его фармацевтически приемлемой соли, стаби 11 лизированной формы, пролекарства или гидрата и около 1 мас.ч. карбоната натрия. 6. Фармацевтическая композиция по п.5,содержащая около 4,5 частей соединения I или его фармацевтически приемлемой соли, стабилизированной формы, пролекарства или гидрата. 7. Фармацевтическая композиция по п.2,содержащая около 4-10 мас.ч. соединения I или его фармацевтически приемлемой соли, стабилизированной формы, пролекарства или гидрата и 1 мас.ч. карбоната натрия. 8. Фармацевтическая композиция по п.7,где около 6,7 мас.ч. соединения I или его фармацевтически приемлемой соли, стабилизированной формы, пролекарства или гидрата комбинируют с 1 мас.ч. карбоната натрия. 9. Фармацевтическая композиция по п 1,содержащая около 4-10 мас.ч. соединения формулы I или его фармацевтически приемлемой соли, стабилизированной формы, пролекарства или гидрата и 1 мас.ч. бикарбоната натрия. 10. Фармацевтическая композиция по п.8,где около 6,7 мас.ч. соединения формулы I или его фармацевтически приемлемой соли, стабилизированной формы, пролекарства или гидрата комбинируют с 1 мас.ч. бикарбоната натрия. 11. Фармацевтическая композиция по п.2,дополнительно содержащая ингибитор дегидропептидазы. 12. Фармацевтическая композиция по п.11,где ингибитором дегидропептидазы является циластатин. 13. Соединение, представленное формулой или его фармацевтически приемлемая соль,пролекарство или гидрат. 14. Фармацевтическая композиция, которая содержит соединение, представленное формулой II или его фармацевтически приемлемую соль,пролекарство или гидрат в комбинации с фармацевтически приемлемым носителем. 15. Соединение по п.13, где фармацевтически приемлемую соль выбирают из группы,включающей где X+ представляет фармацевтически приемлемую катионную группу. 16. Фармацевтическая композиция, которую получают комбинированием соединения формулы I: или его фармацевтически приемлемой соли,пролекарства или гидрата с источником диоксида углерода. 17. Фармацевтическая композиция по п.16,где источник диоксида углерода выбирают из диоксида углерода, карбоната натрия и бикарбоната натрия. 18. Фармацевтическая композиция по п.17,где источником диоксида углерода является карбонат натрия или бикарбонат натрия. 19. Способ стабилизации карбапенема формулы I или его фармацевтически приемлемой соли,пролекарства или гидрата, заключающийся в добавлении к данному соединению достаточного количества источника диоксида углерода для образования соединения формулы II или его фармацевтически приемлемой соли,пролекарства или гидрата. 20. Способ по п.19, где источник диоксида углерода выбирают из диоксида углерода, карбоната натрия и бикарбоната натрия. 21. Способ по п.20, где источник диоксида углерода выбирают из карбоната натрия и бикарбоната натрия.
МПК / Метки
МПК: A61K 31/40, C07D 477/20
Метки: получения, карбапенемовый, композиция, способ, антибиотик
Код ссылки
<a href="https://eas.patents.su/8-534-karbapenemovyjj-antibiotik-kompoziciya-i-sposob-polucheniya.html" rel="bookmark" title="База патентов Евразийского Союза">Карбапенемовый антибиотик, композиция и способ получения</a>
Предыдущий патент: Сульфонилалканоиламиногидроксиэтиламиносульфонамид в качестве ингибиторов ретровирусной протеазы
Следующий патент: Новые противосудорожные i-ar(алк)ил-имидазолин-2-оны, содержащие в 4-положении двузамещенный остаток амина, и способ их получения
Случайный патент: Композиция для лечения спида












