Получение замещенных ароматических аминов
Номер патента: 1708
Опубликовано: 25.06.2001
Авторы: Вилер Эдвард Л., Мальц Расселл Е.Мл., Саймон Марк В.
Формула / Реферат
1. Способ получения замещенных ароматических аминов формулы (I), включающий стадии:
(а) окисление раствора ароматического амина формулы (II) в присутствии окислителя и комплекса пентацианоферрата (II) металла с получением комплекса арилендиаминпентацианоферрата, причем указанный металл выбирают из группы, состоящей из калия и натрия; и
(б) каталитического восстановления указанного комплекса арилендиаминпентацианоферрата водородом с использованием гетерогенного металлического катализатора с получением соответствующих замещенных ароматических аминов формулы (I)
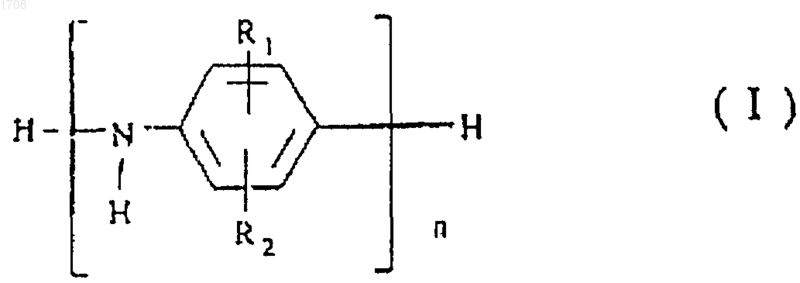
где n равно 2-5, и R1 и R2 определены ниже;
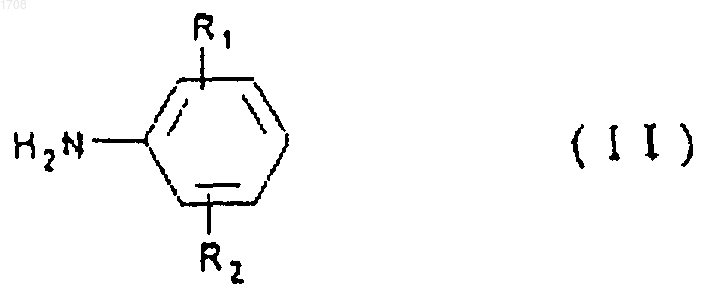
R1 и R2 могут быть одинаковыми или различными, должны быть в орто- или метаположении по отношению к аминогруппе, и могут быть водородом, С1-С4алкилом C1-С4алкокси, галогеном, циано, СОО- ионами, образующими соли и амиды или их смеси.
2. Способ по п.1, в котором окислителем являются кислород или перекись водорода.
3. Способ по п.2, в котором окислителем является кислород, и гетерогенный металлический катализатор присутствует в течение указанной стадии окисления.
4. Способ по п.2, в котором кислород используют под давлением в диапазоне от примерно 1 до 100 атмосфер.
5. Способ по п.2, в котором кислород на стадии окисления и водород на стадии восстановления используют под давлением, выбранным независимо и в диапазоне от примерно 2 до примерно 75 атмосфер.
6. Способ по п.1, в котором комплекс пентацианоферрата (II) металла является комплексом тринатрийпентацианоферрата (II), содержащий растворимые в воде лиганды, выбранные из группы, состоящей из аммиака, моноалкиламинов, диалкиламинов, триалкиламинов, N,N-диметиламиноэтанола, N,N,N',N'-тетраметилэтилендиамина и пиридина.
7. Способ по п.6, в котором, комплекс тринатрийпентацианоферрата (II) имеет структуру Na3 [Fe (CN)5NН3 х Н2О] или его димер.
8. Способ по п.1, в котором гетерогенный металлический катализатор является катализатором на носителе и выбирается из группы, состоящей из палладия, платины, рутения, родия или никеля.
9. Способ по п.8, в котором катализатором являются платина или палладий.
10. Способ получения N-фенил-п-фенилендиамина включающий следующие стадии:
а) окисление анилина в присутствии окислителя комплекса тринатрийпентацианоферрата (II) для образования комплекса N-фенил-п-фенилендиаминпентацианоферрата; и
б) каталитическое восстановление комплекса N-фенил-п-фенилендиаминпентацианоферрата с водородом, используя гетерогенный металлический катализатор с получением N-фенил-п-фенилендиамина.
11. Способ по п.10, в котором органический растворитель, смешиваемый с водой, дополнительно добавляют для растворения анилина и выбирают из группы, состоящей из этиленгликоля, пропиленгликоля, диэтиленгликоля, триэтиленгликоля или их смесей.
12. Способ по п.10, в котором комплекс N-фенил-п-фенилендиаминпентацианоферрата подвергается гидрированию в присутствии гетерогенного металлического катализатора и растворителя, не смешиваемого с водой, выбранного из группы, состоящей из бутилацетата, гексанола, 2-этил-1-бутанола, гексилацетата, этилбутилацетата, амилацетата и замещенного или незамещенного анилина.
13. Способ по п.1, в котором проводят дополнительные стадии: (с) выделения комплекса пентацианоферрата (II) металла, который был преобразован в процессе стадии восстановления; и (с) повторной переработки указанного комплекса за счет повторения стадии окисления (а) с применением комплекса пентацианоферрата (II) металла.
14. Способ по п.1, в котором указанную стадию окисления проводят в водной среде.
15. Способ по п.1, в котором указанную стадию окисления (а) проводят в диапазоне температур от 40 до 55шС, а указанная стадия восстановления (б) имеет диапазон температуры реакции примерно от 5 до 60шС для реакции с водородом.
16. Способ по п.1, в котором рН реакции равно от 10 до 12.
17. Способ по п.1, в котором рН реакции поддерживают в основном при величине, эквивалентной рН раствора комплекса пентацианоферрата (II) метала, растворенного в воде.
Текст
1 Предпосылки изобретения 1. Область изобретения Настоящее изобретение относится к способу получения фенил-п-фенилендиамина(PPDA) и высших аминов формулы (1), указанной ниже, на основе исходных материалов со структурной формулой (11). Более конкретно,оно относится к способу получения PPDA, по которому анилин окисляют в присутствии комплексов тринатрийпентацианоферрата (II), содержащих растворимые в воде лиганды, такие как аммиак, моноалкиламины, диалкиламины и триалкиламины, а кислород или перекись водорода используют в качестве окисляющих агентов. Комплекс затем восстанавливают за счет гидрирования с использованием подходящих гетерогенных металлических катализаторовR1 и R2 могут быть одинаковыми или различными, должны быть в орто или метаположении по отношению к аминогруппе, и могут быть водородом, C1 - С 4 алкилом, C1 - С 4 алкокси, галогеном, циано, карбоксилатными солями и амидами карбоновых кислот или их смесью. Изобретение относится к производствуPPDA с возможностью вторичной переработки комплексов переходных металлов, высокой избирательностью и выходом. Конверсия анилина в N-фенил-п-фенилендиамин находится в пределах 40-85%. Выход PPDA - от 91 до 97%. Способ данного изобретения является эффективным в стоимостном выражении и не дает побочных продуктов, вредных для окружающей среды. Уровень техники Производство п-фенилендиамина и его производных широко распространено, и его применение хорошо известно. В Патенте США 5.117,063, Стерна и др., раскрываются различные способы полученияN-фенил-пфенилендиамина, когда анилин и нитробензол вступают в реакцию при определенных условиях. В других публикациях раскрывается окислительная димеризация анилина с получениемN-фенил-п-фенилендиамина. В Британском патенте 1,400,767 и Европейском патенте 0261096 используют феррицианид щелочного металла, а в Европейском патенте 0-272-238 используют гипогалит в качестве окислителя. Ни один из этих процессов не является высокоизбирательным и не дает хорошей конверсии.J. Bacon и R.N.Adams в J. Am.Chem. Soc.,90 стр. 6596 (1968) сообщают об анодном окис 001708 2 лении анилина до N-фенил-п-хинондиимина, но не приводят ни показателей конверсии, ни уровня выхода. Е. Herrington в J. Chem. Soc. стр. 4683 (1958) сообщает об окислительной димеризации анилина с динатрийпентацианоаминоферратом (III) с образованием комплекса,содержащего N-фенил-п-фенилендиамин, который затем химически восстанавливают с помощью таких восстановителей как гидрат гидразина, дитионат натрия, кислый сульфит натрия,сероводород. Использование комплекса тринатрийпентацианоферрата (III) и каталитического восстановления водородом в соответствии с настоящим изобретением отличается от данной публикации, и эта разница приводит к существенному усовершенствованию процесса. Стехиометрия настоящего изобретения значительно усовершенствована по сравнению с работойHerrington, так как можно использовать более высокие отношения содержания анилина к комплексу в способе, описанном в данной заявке. Цель данного изобретения - обеспечить способ получения N-фенил-п-фенилендиамина и соответствующих соединений. Далее целью данного изобретения является раскрыть способ получения таких соединений с помощью водных процессов, что позволит легко удалять непрореагировавший анилин с последующим отделением перестроенного исходного комплекса от желаемого конечного продукта [формула (I)] после восстановления, обеспечивая при этом процесс коммерчески выгодный, как с точки зрения низкой стоимости, так и возможности вторичной переработки. Еще одной целью данного изобретения является обеспечение способа, который выявит преимущества такого продукта как пфенилендиамин как по высокому выходу, так и хорошей избирательности. Кроме того была цель разработать процесс, который давал бы меньше отходов в сточные воды. Можно добавить еще одно - получение производных фенилендиамина, которые могут быть использованы в промышленности как противостарители, изготовленные из продуктов высокой чистоты на основе способа данного изобретения. Сущность изобретения Настоящее изобретение направлено на усовершенствование способа получения замещенных ароматических аминов формулы (II),состоящего из следующих стадий: а) окисления ароматических аминов формулы (II) в присутствии комплекса пентацианоферрата металла (II) с образованием комплекса арилендиаминпентацианоферрата; причем указанный металл выбирают из группы, включающей калий и натрий; и б) каталитического восстановления указанного комплекса арилендиаминпентацианоферрата водородом с применением гетерогенного металлического катализатора с получением соответствующего замещенного ароматического амина формулы (I).R1 и R2 могут быть одинаковыми или разными,должны быть в орто или метаположении по отношению к аминогруппе, могут быть водородом, C1 - С 4 алкилом, C1 - С 4 алкокси, галогеном,циано, солями, карбоксилатными солями и амидами карбоновых кислот или их смесями. Наиболее предпочтительным осуществлением способа является окисление анилина в присутствии комплексов тринатрийпентацианоферрата (II), содержащих различные растворимые в воде лиганды, такие как аммиак, моноалкиламины, диалкиламины, триалкиламины и подобные вещества. Окислителями могут быть кислород или перекись водорода. Затем комплекс N-фенил-п-фенилендиамин пентацианоферрата восстанавливается водородом с применением гетерогенного металлического катализатора, который может иметь или не иметь носитель. Пригодными носителями могут быть известные вещества, такие как, например, углерод или оксид алюминия. Смесь анилина и Nфенил-п-фенилендиамина затем экстрагировалась соответствующим растворителем после фильтрации гетерогенного катализатора. Предпочтительными растворителями являются безопасные для окружающей среды, несмешиваемые с водой и легко рециркулируемые типы. Водный слой, содержащий комплекс пентацианоферрата (II) затем рециркулируетcя. Подробное описание изобретения Предпочтительный способ получения Nфенил-п-фенилендиамина (PPDA) настоящего изобретения включает стадии а) окисления анилина в присутствии комплексов тринатрийпентацианоферрата (II) с необязательным использованием гетерогенного металлического катализатора; с последующим б) восстановлением комплекса N-фенил-п-фенилендиаминпентацианоферрата водородом с применением гетерогенного металлического катализатора. В большинстве случаев обе стадии (а) и (б) используют один и тот же гетерогенный катализатор. На первой стадии любой подходящий оксидант, включая кислород или перекись водорода, могут использоваться в качестве окислителей. Наиболее предпочтительным окислителем является кислород. Еще более предпочтительным является применение кислорода под давлением и при повышенных температурах,что увеличивает скорость окисления и облегчает завершение стадии а). Комплексы пентацианоферрата металла(II), применяемые в данном изобретении, должны быть растворимы в воде как и лиганды, со 001708 4 ставляющие часть комплекса. Предпочтительными металлами являются щелочные металлы типа натрия или калия. Наиболее предпочтительный комплекс - тринатрийпентацианоферрат (II), содержащий различные растворимые в воде лиганды, является примером класса используемых комплексов. Этими лигандами могут быть аммиак, моноалкиламины, диалкиламины или триалкиламины. Предпочтительной структурой для этого комплекса является - Na3[Fe(CN)5NН 3 х Н 2 О], или ее димер. На второй стадии предпочтительной реакции комплекс N-фенил-п-фенилендиаминпентацианоферрата восстанавливается водородом при использовании гетерогенного металлического катализатора. Данный катализатор выбирается из гетерогенных металлов группы VIII, таких как палладий, платина, рутений, родий или никель. Катализатор может иметь или не иметь носитель. При наличии носителя им может быть углерод, оксид алюминия и подобные материалы, многие из которых известны тем, кто работает в данной области. Смесь анилина и PPDA, которая является продуктом реакции, экстрагируется соответствующим растворителем. Затем гетерогенный катализатор отфильтровывается. Подходящие растворители включают такие растворители,которые не смешиваются с водой и легко рециркулируются. Соединения по данному изобретению могут синтезироваться с рядом преимуществ при применении следующего способа. Предпочтительный способ получения PPDA содержится в примерах, следующих ниже. Первая стадия предпочтительного способа по данному изобретению включает растворение натрийпентацианоаминоферрата (II) в воде. Синтез натрийпентацианоферрата (II) известен. Его получают по методу Г. Брауера, описанному в книге "Handbook of Preparative InorganicChemistry" ("Справочник по неорганической химии"), 2-ое изд., т.II, Academic Press, NY,1965, стр. 1511 Новый способ получения тринатрийпентацианоамминоферрата (II) Альтернативный способ получения тринатрийпентацианоамминоферрата (II) - это одновременное добавление водного раствора тетрагидрата хлорида, железа стабилизированного фосфорноватистой кислотой, и цианида натрия в соотношении от 1 до 5 эквивалентов к водному раствору гидроксида аммония. Водный раствор гидроксида аммония может содержать от одного эквивалента в расчете на хлорид железа до избыточных количеств. Предпочтительный диапазон составляет от двух до десяти эквивалентов, и наиболее предпочтительный - от трех до шести эквивалентов гидроксида аммония. Одновременное добавление проводят в течение от одного до трех часов, а затем раствор 5 фильтруют, если необходимо удалить небольшие количества гидроксида железа, и комплекс осаждается при добавлении изопропанола или любого подходящего растворимого в воде органического растворителя. Комплекс может быть высушен или растворен в воде повторно без сушки и использован непосредственно. Избыточные количества аммония и изопропанола выделяют. При введении анилина, чтобы способствовать его растворению, может быть добавлен органический растворитель, смешиваемый с водой. По настоящему изобретению подобная реакция может происходить без органического растворителя. Примерами таких растворителей являются этиленгликоль, пропиленгликоль, диэтиленгликоль и триэтиленгликоль. Добавляются два эквивалента анилина, и смесь затем окисляется. Кислород и пероксид водорода - два возможных окислителя, которые могут быть использованы. До окисления может быть добавлен гетерогенный металлический катализатор. На второй стадии процесса по данному изобретению окисленный комплекс, содержащий N-фенил-п-фенилендиамино лиганд подвергается гидрированию в присутствии гетерогенного металлического катализатора. Это можно проводить без добавленного растворителя или в присутствии соответственного несмешиваемого с водой растворителя. Возможные растворители этой категории включают бутилацетат, гексанол, 2-этил-1-бутанол, гексилацетат, этилбутилацетат, амилацетат, метилизобутилкетон или анилин, а также им подобные. После гидрирования гетерогенный катализатор удаляется фильтрацией, и органический слой отделяется. Растворитель, анилин и N-фенил-пфенилендиамин регенерируются дистилляцией. Пентацианоамминоферрат натрия (II) затем перерабатывается вторично. Реакцию лучше всего проводить при рН,эквивалентном рН раствора, содержащего растворенный в воде комплекс. При необходимости рН регулируется после каждого повторного цикла комплекса добавлением аммония в раствор для сохранения рН, эквивалентным исходной величине рН раствора в начале процесса. Эта регулировка рН достигается добавлением соответствующего основания, например, гидроксида аммония или аммиака, лиганда, используемого в комплексе. Наиболее благоприятный диапазон рН от 10 до 12 рН - эквивалентен рН растворенного комплекса, который зависит от концентрации предпочитаемого раствора. Давление кислорода и водорода может быть в диапазоне от 1 до 100 атмосфер. Наилучший диапазон - от 2 до примерно 75 атмосфер. Более точно от 50 до 75 атмосфер или около 5,0 х 106 до примерно 7,5 х 106 Нм-2. Сходные диапазоны давления используются для реакции восстановления водородом. 6 Диапазон температуры может меняться до точки, при которой комплекс теряет свою стабильность, что обычно происходит в диапазоне от 5 С до примерно 65 С в закрытой системе. Хотя реакция может протекать и при более низких температурах, скорость реакции стадии окисления при такой температуре тоже значительно ниже. Предпочтительной для окислительной реакции является температура в пределах 30 - 55 С, а самой предпочтительной - между 45 и 55 С. Применяемая температура требует баланса ряда факторов для достижения максимальной скорости и выхода реакции. Температура выше указанной будет медленно разрушать комплекс. Низкие температуры снижают растворимость комплекса и скорость реакции. Целый ряд лигандов может быть использован вместо аммиака в комплексе пентацианоферрата натрия (11). Лиганды могут быть моноалкиламинами, такими как метил, этил, пропил, или бутиламины, диалкиламинами, такими как диметил или диэтиламины, и триалкиламинами, такими как триметиламин или триэтиламин. Могут использоваться и другие амины N,N-диметиламинэтанол, N, N, N', N'- тетраметилэтилендиамин, и замещенный и незамещенный пиридин. Еще может использоваться целый ряд других аминов, их применение ограничивается только их растворимостью и способностью замещаться анилином и их стабильностью. В данном изобретении натрийпентацианоферраты (II), содержащие лиганды другие, не аммиак, получают замещением комплекса аммиака избыточным количеством соответствующего лиганда. Среди гетерогенных металлических катализаторов, которые могут использоваться, палладий-на-углероде, платина-на-углероде, рутений-на-углероде, родий-на-углероде и никель Ренея. Другие носители кроме углерода, такие как двуоксид алюминия, кизельгур, двуоксид кремния и подобные им, могут также использоваться. Наиболее предпочтительными среди используемых катализаторов являются благородные металлы. Еще более предпочтительными катализаторами являются благородные металлы с носителями. Но самыми желательными катализаторами являются платина или палладий на углеродном носителе. Способность комплекса пентацианоамминоферрата к повторной переработке демонстрируется различными примерами, приведенными в описании данного изобретения. Процедура повторной переработки может проводиться при температуре от 25 до 60 С, но наилучшим является интервал от 45 до 55 С. Способность к повторной переработке полезна при использовании других лигандов кроме аммиака в комплексах пентацианоферрата(11), таких как пентацианотриметиламиноферрат (11) или пентацианоизопропиламиноферрат(11). Эксперименталь 7 ные данные вторичной переработки, включая конверсию и данные выхода, представлены в описанных примерах. Гидроалкилирование PPDA для получения противостарителей может проводиться одним из различных методов, известных работающим в этой области специалистам. Смотри, например,патент США 3,336,386, который включен для ссылок в данный документ. Желательно, чтобы реакция PPDA и подходящего кетона или альдегида протекала в присутствии водорода и катализатора, такого как сульфид платины с или без носителя. Подходящие кетоны включают метилизобутилкетон, ацетон, метилизоамилкетон и 2-октанон. Следующие примеры призваны проиллюстрировать данное изобретение более подробно,но никоим образом не ограничивают содержание данного изобретения. Примеры Пример 1. Окисление анилина с использованием перекиси водорода в качестве окислителя (стадия а) и водорода (с 5% палладий/углерод) в качестве восстановителя (стадия б) при получении PPDA. Реакция стадии а протекает при использовании 3,0 г анилина, 6,0 г натрийпентацианоамминоферрата (II), 300 мл дистиллированной воды и 0,1 г 5-ти % палладия на угле (Pd/C) (50% влажность) в трехгорлой колбе с механической мешалкой и дополнительной воронкой. Восемь мл 30% пероксида водорода (окислитель) было добавлено через 0,5 ч. Гетерогенный катализатор был удален фильтрацией, а реакционная смесь помещалась в автоклав с приводом Magne. Затем добавлялся 1,0 г свежего катализатора Pd/C (50% воды).Сосуд герметично закрывался и продувался сначала азотом, а затем водородом, и давление с водородом достигало 1000 фунтов на кв. дюйм (69 атмосфер или 6,9 х 106 Нм-2). Процесс перемешивания при комнатной температуре продолжался в течение 2 ч. После вентиляции и продувания азотом к реакционной смеси добавлялся изопропилацетат. Катализатор удалялся фильтрацией, и органический раствор анализировался методом газовой хроматографии с использованием прибора Вариан (Varian) 3400, снабженного капиллярной колонкой DB-I. Продукт N-фенил-р-фенилендиамин (PPDA) был обнаружен при конверсии 74,3%, а анилин был замерен на уровне 18,4 %. Выход на основе конверсии анилина составил 91%. Примеры 2-6. Окисление анилина с помощью кислорода в качестве окислителя (стадия а) и водорода с несколькими металлическими катализаторами в качестве восстановителей (стадия б) при приготовлении PPDA. Используя основную методику, описанную в примере 1, проводилось несколько реакций в однолитровом автоклаве с приводом Маgne с использованием 38,0 г натрийпентацианоамми 001708 8 ноферрата (II), 18,6 г анилина, 2,0 г металлического катализатора, 50,0 г этиленгликоля и 150 г дистиллированной воды. Металлические катализаторы, применяемые в примерах 2-6, это Pd,Ru, Pt, Rh и Ni с носителями, соответственно. В примерах 2-5 гетерогенные катализаторы присутствовали в количестве 5 мас.% на углероде, и они применялись при 4,0 г и 50% воды. В примере 6 никель использовался как 50%Ni/кизельгур в количестве 2,0 г сухим. Автоклав был герметично закрыт, продувался сначала кислородом, и давление подавалось до 400 фунтов на кв.дюйм (28 атм или 2,8 х 106 Нм-2). Перемешивание в автоклаве протекало при комнатной температуре в течение 2,5 ч. После этого перемешивания автоклав продувался азотом, а затем в автоклав насосом подавалось 100 мл бутилацетата. Автоклав продувался водородом, а затем создавалось давление с водородом до 400 фунтов на кв. дюйм (28 атм или 2,8 х 106 Нм-2). Затем вновь происходило перемешивание в течение 1 ч при комнатной температуре. Раствор эфира отделялся и анализировался методом высокоэффективной жидкостной хроматографии. Никель-катализатор на кизельгуре (пример 6) оказался неактивным. Результаты данных примеров представлены в таблице 1. Таблица 1 Катализатор, г Конверсия,%, (а) Выход,%, (б) 5%Pd/C 4,0 г 50%Н 2O 69 93 5%Ru/C 4,0 г 50%Н 2 О 30 87 5%Pt/C 4,0 г 50%Н 2O 72 95 5% Rh/C 4,0 г 50 Н 2 О 51 96 50 % Ni/ кизелгур 2,0 г 6 3 88 сухой Примечание к таблице 1. (а) Анализ N-фенил-пфенилендиамина методом высокоэффективной жидкостной хроматографии с обратной фазой и с использованием градиента вода-ацетонитрил с насосом Perkin-Elmer серии 410 LC,с диодным детектором LC 235 и колонкой 3 С 18, 3,3 пекосферы.(б) Выход N-фенил-р-фенилендиамина основан на анилине после конверсии. Пример 2 3 4 5 Пример 7. Окисление анилина с использованием кислорода и без металлического катализатора (стадия а) и восстановление с гидразином(II), 12,8 г анилина, 100 мл этиленгликоля и 300 мл дистиллированной воды. Сосуд был герметически закрыт, продут азотом, затем кислородом и с кислородом доведен до давления 400 фунтов на кв. дюйм (28 атм или 2,8 х 106 Нм-2). Перемешивание проходило в автоклаве в течение 6 ч при 15-20 С с охлаждением для контроля температуры. После окисления один мл пробы вынимался из автоклава. Затем к пробе был добавлен изопропилацетат, и синтез PPDA продолжался при восстановлении, стадия(б) с гидразином. 9 Оставшаяся в автоклаве смесь была продута азотом, затем водородом и с водородом доведена до давления 400 фунтов на кв. дюйм (28 атм или 2,8 х 106 Нм-2). Перемешивание продолжалось при комнатной температуре в течение 1 ч. Проводилась вентиляция, продув азотом и добавление изопропилацетата. После этого отделялся органический слой. Анализ проводился методом газовой хроматографии с использованием прибора Varian 3400G.C., снабженного колонкой DB-1. Степень конверсии в N-фенил-п-фенилендиамин (PPDA) при гидрировании была 6%. Конверсия при восстановлении гидразином - 66%. В результате этого примера было сделано заключение, что гидрогенолиз требует металлического катализатора, а окисление может происходить и без него. Однако нужно отметить,что может оказаться полезным добавление гетерогенного катализатора перед окислением. Обнаруженное небольшое количество N-фенил-пфенилендиамина могло стать результатом реакции переноса электронов в процессе окисления. Примеры 8-10. Проведение реакций окисления и восстановления (стадия а) для получения PPDA под давлением. Реакции в данных примерах осуществлялись сходно с указанной выше методикой. В автоклаве емкостью 1 л и приводом Маgnе комбинировались 76,0 г трех различных навесок натрийпентацианоферрата (II), 3, 2 г анилина,4,0 г 5% Pd/C катализатора, 100 г этиленгликоля и 300 г дистиллированной воды. Автоклав закрывался герметично, продувался сначала кислородом, а потом вместе с кислородом доводился до желаемого давления. Перемешивание проходило при комнатной температуре в течение 2,5 ч. После окисления автоклав продувался сначала азотом. С помощью насоса в автоклав подавалось 200 мл бутилацетата, затем автоклав продувался водородом и вместе с водородом доводился до желаемого давления. Перемешивание проходило при комнатной температуре в течение 1,0 ч. После отделения органического слоя обычным способом проводился анализ методом высокоэффективной жидкостной хроматографии, который дал следующие показатели конверсии, представленные в таблице 2. Таблица 2 Пример О 2 и Н 2 давление, psi.(атм.) Конверсия,% Выход (а), % 8 400 (28) 69 93 9 800 (56) 63 88 10 100 (8) 55 94 Примечание к таблице 2. Во втором столбце показано давление для кислорода и водорода (а) Выход основан на используемом анилине. Примеры 11 и 12. Демонстрация способности комплекса натрийпентацианоамминоферрата (II) к вторичной переработке. В соответствии с предыдущими примерами реакция протекала в 1 л-автоклаве с приво 001708 10 дом Маgnе. Использовались 76,0 г натрийпентацианоамминоферрата (II), 37,2 г анилина, 8,0 г 5% катализатора Pd/C, 100 г этиленгликоля и 300 г дистиллированной воды. Автоклав герметично закрывался, продувался сначала кислородом, и давление доводилось до 400 фунт/дюйм 2(28 атм или 2,8 х 106 Нм-2) с кислородом. Затем в течение 2,5 ч продолжалось перемешивание при комнатной температуре. Вслед за окислением автоклав продувался сначала азотом, а затем с помощью насоса в автоклав подавалось 200 мл бутилацетата. После этого в автоклаве создавали давление водородом до 400 ф/кв. дюйм (28 атм. или 2,8 х 106 Нм-2). Перемешивание в автоклаве при комнатной температуре продолжалось 1 ч. Автоклав открывался, раствор фильтровался для удаления металлического катализатора, и слои разделялись. Слой эфира анализировался методом газовой хроматографии, и водный слой возвращался в автоклав. В этот момент добавлялось 37,2 г анилина и 8,0 г 5-ти % катализатора Pd/C. Автоклав вновь герметично закрывался, продувался кислородом, и давление создавалось кислородом до 400 ф/кв. дюйм (28 атм. или 2,8 х 106 Нм-2). Смесь перемешивалась при комнатной температуре в течение 2,5 ч, а затем продувалась азотом. Потом 200 мл бутилацетата подавалось в автоклав с помощью насоса. Затем следовало продувание водородом и давление вместе с водородом доводилось до 400 ф/дюйм кв. (28 атм. или 2,8 х 106 Нм-2). Смесь перемешивалась при комнатной температуре в течение 1,0 ч. Раствор эфира анализировался методом газовой хроматографии. Результаты анализа по конверсии и по выходу как первичного (пример 11), так и вторично переработанного материала(а) ГХ анализ с использованием газового хроматографа модели Perkin Elmer 8310 с колонкой SP 2100, 1 м.(б) на основе анилина после конверсии.(11) и повторная переработка. В соответствии с предыдущими примерами реакция проходила в 1 л автоклаве с приводом Маgnе с использованием 42,8 г - натрийпентацианотриметиламиноферрата (II), или такого же количества натрийпентацианоизопропиламиноферрата (II), 18,6 г анилина, 4,0 г 5-ти% Pd/C катализатора и 200 г дистиллированной воды. Автоклав герметически закрывался и продувался сначала кислородом, затем создавалось давление кислородом до 250 ф/дюйм кв. (18 атм. или 1,8 х 106 Нм-2). Перемешивание в сосу 11 де затем проходило при комнатной температуре в течение 0,5 ч. Вслед за окислением автоклав продувался азотом, а затем в него насосом вводили 200 мл бутилацетата. Далее в автоклаве создавалось давление с водородом до 400 ф/дюйм кв. (28 атм или 2,8 х 106 Нм-2). Затем перемешивание продолжалось при комнатной температуре еще 1 ч. После завершения периода перемешивания автоклав открывали и его содержимое вынимали. Затем смесь фильтровалась, и водный и органический слой разделялись. Раствор эфира,находящийся в органическом слое, анализировался методом газовой хроматографии с использованием газового хроматографа Perkin-Elmer,модель 8310 с однометровой колонкой SP2100,после этого водный слой возвращали в автоклав. В этот момент добавляли 18,6 г анилина и 4,0 г 5-ти % Pd/C катализатора. Автоклав герметически закрывался, продувался кислородом, и создавалось давление кислородом до 250 ф/дюйм кв. (18 атм. или 1,8 х 106 Нм-2). Перемешивание в автоклаве продолжалось при комнатной температуре в течение 3,0 ч с последующим введением насосом в автоклав 100 мл бутилацетата. Автоклав сначала продувался азотом, а затем водородом, и давление с водородом доводилось до 250 ф/дюйм кв. (18 атм. или 1,8 х 106 Нм-2). Автоклав затем подвергался перемешиванию при комнатной температуре в течение 0,5 ч, после чего автоклав открывался и содержимое вынималось. Раствор эфира анализировался методом газовой хроматографии с использованием таких же приборов, которые указывались в предыдущих примерах. Результаты анализов представлены в таблице 4. Пример 13 Применяемый лиганд Конверсия,% Триметиламин 89,5 Триметиламин (1 цикл 14 63 втор. переработки) 15 Изопропиламин 55 Примечание к таблице 4. а) выход основан на используемом анилине Примеры 16-17. Применение катализатора на основе неблагородных металлов в процессе восстановления (стадия б) при приготовленииPPDA. В соответствии с предыдущими примерами реакция протекала в 1 л-автоклаве с приводом Маgnе с использованием 57 г натрийпентацианотриметиламиноферрата (II), 27,9 г анилина и 250 г дистиллированной воды. Автоклав закрывался герметично, продувался сначала кислородом, и давление кислородом доводилось до 250 ф/дюйм кв. (18 атм. или 1,8 х 106 Нм-2). Затем при комнатной температуре 3 ч продолжалось перемешивание. После окисления автоклав продувался сначала азотом, а затем открывался и в него добав 12 ляли катализатор. Затем добавляли бутил-ацетат(200 мл). Автоклав герметично закрывали и давление водородом поднимали до желаемой величины 400 ф./дюйм кв. (28 атм. или 2,8 х 106 Нм-2). Катализаторы, применяемые для восстановления, стадия б, представлены в таблице 5. Перемешивание в автоклаве продолжалось 1 ч при комнатной температуре. Анализ раствора эфира проводился методом газовой хроматографии с использованием того же оборудования, которое было указано в предыдущих примерах. Результаты этих анализов представлены в таблице 5. Таблица 5 Содержание Катализатор; Конверсия. Выход (а),Пример катализатора время(а) Выход основан на грамм-молекулах примененного анилина. Учитывая, что множество изменений и модификаций могут быть произведены без нарушения принципов, составляющих изобретение,необходимо делать ссылки на прилагаемую формулу изобретения для понимания объема защиты прав на изобретение. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ получения замещенных ароматических аминов формулы (I), включающий стадии:(а) окисление раствора ароматического амина формулы (II) в присутствии окислителя и комплекса пентацианоферрата (II) металла с получением комплекса арилендиаминпентацианоферрата, причем указанный металл выбирают из группы, состоящей из калия и натрия; и(б) каталитического восстановления указанного комплекса арилендиаминпентацианоферрата водородом с использованием гетерогенного металлического катализатора с получением соответствующих замещенных ароматических аминов формулы (I)R1 и R2 могут быть одинаковыми или различными, должны быть в орто- или метаположении по отношению к аминогруппе, и могут быть водородом, С 1 - С 4 алкилом C1 - С 4 алкокси, галогеном, циано, СООионами, образующими соли и амиды или их смеси. 2. Способ по п.1, в котором окислителем являются кислород или перекись водорода. 3. Способ по п.2, в котором окислителем является кислород, и гетерогенный металличе 13 ский катализатор присутствует в течение указанной стадии окисления. 4. Способ по п.2, в котором кислород используют под давлением в диапазоне от примерно 1 до 100 атмосфер. 5. Способ по п.2, в котором кислород на стадии окисления и водород на стадии восстановления используют под давлением, выбранным независимо и в диапазоне от примерно 2 до примерно 75 атмосфер. 6. Способ по п.1, в котором комплекс пентацианоферрата (II) металла является комплексом тринатрийпентацианоферрата (II), содержащий растворимые в воде лиганды, выбранные из группы, состоящей из аммиака, моноалкиламинов, диалкиламинов, триалкиламинов, N,Nдиметиламиноэтанола,N,N,N',N'-тетраметилэтилендиамина и пиридина. 7. Способ по п.6, в котором, комплекс тринатрийпентацианоферрата (II) имеет структуруNa3 [Fe (CN)5NН 3 х Н 2 О] или его димер. 8. Способ по п.1, в котором гетерогенный металлический катализатор является катализатором на носителе и выбирается из группы, состоящей из палладия, платины, рутения, родия или никеля. 9. Способ по п.8, в котором катализатором являются платина или палладий. 10. Способ получения N-фенил-п-фенилендиамина включающий следующие стадии: а) окисление анилина в присутствии окислителя комплекса тринатрийпентацианоферрата(II) для образования комплекса N-фенил-пфенилендиаминпентацианоферрата; и б) каталитическое восстановление комплекса N-фенил-п-фенилендиаминпентацианоферрата с водородом, используя гетерогенный металлический катализатор с получением Nфенил-п-фенилендиамина. 14 11. Способ по п.10, в котором органический растворитель, смешиваемый с водой, дополнительно добавляют для растворения анилина и выбирают из группы, состоящей из этиленгликоля, пропиленгликоля, диэтиленгликоля, триэтиленгликоля или их смесей. 12. Способ по п.10, в котором комплекс Nфенил-п-фенилендиаминпентацианоферрата подвергается гидрированию в присутствии гетерогенного металлического катализатора и растворителя, не смешиваемого с водой, выбранного из группы, состоящей из бутилацетата, гексанола, 2-этил-1-бутанола, гексилацетата, этилбутилацетата, амилацетата и замещенного или незамещенного анилина. 13. Способ по п.1, в котором проводят дополнительные стадии: (с) выделения комплекса пентацианоферрата (II) металла, который был преобразован в процессе стадии восстановления; и (с) повторной переработки указанного комплекса за счет повторения стадии окисления(а) с применением комплекса пентацианоферрата (II) металла. 14. Способ по п.1, в котором указанную стадию окисления проводят в водной среде. 15. Способ по п.1, в котором указанную стадию окисления (а) проводят в диапазоне температур от 40 до 55 С, а указанная стадия восстановления (б) имеет диапазон температуры реакции примерно от 5 до 60 С для реакции с водородом. 16. Способ по п.1, в котором рН реакции равно от 10 до 12. 17. Способ по п.1, в котором рН реакции поддерживают в основном при величине, эквивалентной рН раствора комплекса пентацианоферрата (II) метала, растворенного в воде.
МПК / Метки
МПК: C07C 209/60, C01C 3/12
Метки: получение, ароматических, замещенных, аминов
Код ссылки
<a href="https://eas.patents.su/8-1708-poluchenie-zameshhennyh-aromaticheskih-aminov.html" rel="bookmark" title="База патентов Евразийского Союза">Получение замещенных ароматических аминов</a>
Предыдущий патент: Способ обработки сейсмических данных
Следующий патент: Способ получения органосиланов реакцией перераспределения
Случайный патент: Инъекционное устройство












